Изобретение относится к химико-фармацевтической промышленности, а именно к производству биологически активных добавок к пище из растительного сырья, комплексного актопротекторного, адаптогенного и детоксикационного действия в отношении внутренних сред организма человека и животных.
Целью заявляемого изобретения является создание комплексного твердофазного (ультрадисперсного порошкового) биопрепарата из природного растительного сырья с повышенной комплексной актопротекторной, адаптогенной и детоксикационной активностью в отношении внутренних сред организма для людей, работающих и проживающих в экстремальных условиях среды, для спортивной медицины и ветеринарии.
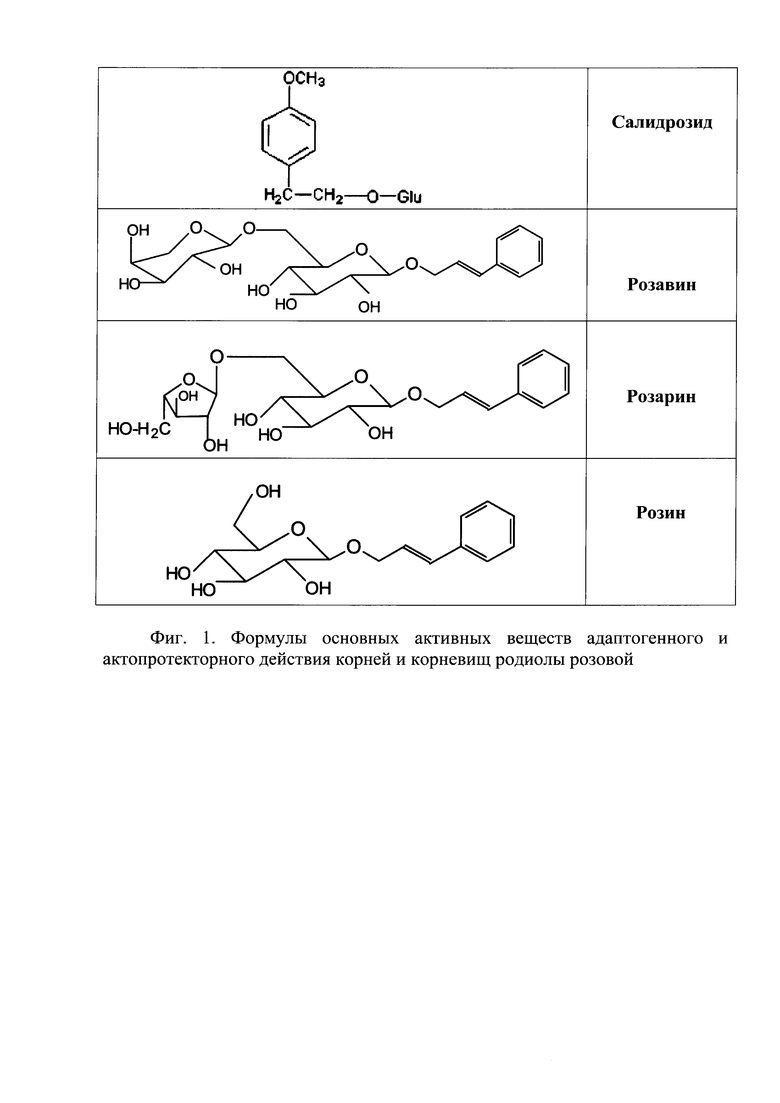
Известен препарат ФС.2.5.0036.15 «Родиолы розовой корневища и корни» Rhodiola rosea L., сем. толстянковых - Crassulaceae. [1]. Препарат в виде экстракта или таблетированной формы оказывает адаптогенное, антистрессорное действие, повышает неспецифическую резистентность организма, является иммуномодулятором. Он обладает стимулирующим действием на ЦНС, устраняет переутомление, раздражительность, симптомы неврастении и вегетососудистой дистонии; восстанавливает и повышает физическую и умственную работоспособность, защищает от неблагоприятных факторов внешней среды. Основные активные вещества адаптогенного и актопротекторного действия: салидрозид и гликозиды транс-коричного спирта: розавин, розарин, розин (фиг. 1). Суммарное содержание последних не менее 1 мас.% (в пересчете на розавин), салидрозида - не менее 0,8 мас.% [1].
Вместе с тем, известно, что при любом стрессогенном воздействии на организм, физическом и/или умственном переутомлении происходит накопление эндогенных токсинов, включая, молочную и мочевую кислоты, мочевину и аммиак, медиаторы воспаления - эндотоксины малой и средней молекулярной массы и др. [2, 3]. Поэтому весьма желательной компонентой комплекса мероприятий проводимого в целях повышения адаптационного и актопротекторного потенциала организма человека должна быть детоксикация не только желудочно-кишечного тракта, но и внутренних сред организма (кровь, лимфа, межклеточные жидкости). Известны медицинские приемы (гемодиализ) и биопрепараты (БАДы) для очистки крови: «Детокс+», «Куркумин» и др. К их недостаткам, относительно заявленной цели, относится, например, проведение только в клинических условиях (гемодиализ), а также отсутствие адаптогенного и актопротекторного действия.
Из растительного сырья перспективными в плане сорбционного действия являются средства на основе лишайников: БАД «Ягель» и «Ягель-Детокс» [4, 5].
Ранее было показано, что предэкстракционная биотехнологическая обработка слоевищ лишайника диоксидом углерода в состоянии сверхкритической жидкости [6, 7] либо их механохимическая активация [8, 9] приводят к частичному разрушению трехмерной β-полисахаридной матрицы с образованием β-олигосахаридов, которые обладают следующими отличительными свойствами:
- Не гидролизуются в желудочно-кишечном тракте (ЖКТ) и во внутренних средах организма, т.к. содержат прочные β-гликозидные связи, не расщепляемые в кислой среде желудка, а кишечная микрофлора и внутренние среды организма не содержат соответствующие β-гликозидазы.
- Содержат большое количество гидрофильных функциональных групп (-OH, -NH2, =CO и др.) и гидрофобных фрагментов, что обеспечивает образование супрамолекулярных комплексов (СМК) с контактирующими с ними низкомолекулярными соединениями как гидрофильной, так и гидрофобной природы, в которых β-олигосахариды выступают в качестве «активного носителя», а низкомолекулярные соединения - «фармаконов».
- СМК, благодаря бифильной природе лишайниковых β-олигосахаридов близких по строению к олигогликозидными фрагментами гликокаликса клеточных мембран и их небольшим размерам, хорошо всасываются из желудочно-кишечного тракта в кровь и легко транспортируются через клеточные мембраны. Например, в качестве «фармаконов» могут выступать активные вещества корней и корневищ родиолы розовой, что повысит их биоусвояемость.
- После распада СМК во внутренних средах организма (цитоплазма, межклеточные жидкости, кровь, лимфа) β-олигосахариды связывают конечные продукты метаболизма - эндотоксины (молочная и мочевая кислота, мочевина, медиаторы воспаления - эндотоксины малой и средней молекулярной массы и др.), а также экзотоксины (катионы тяжелых металлов, радионуклиды, оксиды углерода и серы, органические токсические соединения, включая фенолы, алкогольные токсины (ацетальдегид, ацетон), бактериальные и вирусные токсины и др.) и выводят их из организма.
Благодаря этим свойствам лишайниковых β-олигосахаридов, во-первых, обеспечивается проявление детоксикационной активности в отношении внутренних сред организма. Во-вторых, достигается повышенная усвояемость и биоактивность «фармакона» независимо от степени его гидрофобности/гидрофильности.
Детоксикационная активность лишайниковых β-олигосахаридов была установлена в экспериментах по связыванию in vitro тяжелых металлов и модельных органических веществ на примере метиленового синего [10], а также in vivo на примере алкогольных токсинов [6, 11].
Повышение биоусвояемости и биоактивности «фармакона» адаптогенного и актопротекторного действия при комплексообразовании с лишайниковыми β-олигосахаридами и проявление их детоксикационной активности в отношении эндотоксинов (молочной кислоты, мочевины) было установлено, например, при испытаниях биопрепарата «Кладород» состоящего из лишайниковых β-олигосахаридов и флавогликозидов, выделяемых из корней и корневищ родиолы розовой (салидрозида и др.) [12-17].
Наиболее близкой к заявляемому изобретению является композиция -биологически активная добавка актопротекторного, адаптогенного действия, получаемая путем механохимической активации смеси слоевищ лишайника рода Cladonia, корней и корневищ родиолы розовой (Rhodiola rosea L.), в соотношении 10:1, в отсутствие бикарбоната натрия [18] - прототип.
К недостаткам прототипа можно отнести недостаточно высокую детоксикационную и адаптогенную, актопротекторную активность по сравнению с заявляемой композицией. Это обусловлено меньшей степенью разрушения прочной трехмерной матрицы лишайниковых β-полисахаридов в отсутствие бикарбоната натрия в смеси, подвергаемой механохимической активации. Соответственно, лишайниковые β-олигосахариды и СМК лишайниковых β-олигосахаридов с активными вещества корней и корневищ родиолы розовой (салидрозид, розавин, розарин, розин и др.) образуются в более низкой концентрации. Это, в свою очередь, приводит к снижению как детоксикационного, так и адаптогенного, актопротекторного эффектов при использовании композиции in vivo.
Технический эффект (сущность) заявляемого изобретения заключается в повышении детоксикационной, адаптогенной и актопротекторной активности.
Технический эффект (сущность) заявляемого изобретения достигается благодаря тому, что механохимическая обработка смеси слоевищ лишайника рода Cladonia, корней и корневищ родиолы розовой происходит в присутствии 0,7-0,9 мас.% (от массы растительного сырья) бикарбоната натрия в одну технологическую стадию.
Изобретение может быть реализовано следующим образом.
(1) Слоевища лишайника рода Cladonia, а также корни и корневища родиолы розовой подвергаются предварительному грубому помолу на мельнице до размеров частиц 0,6–1,2 мм. (2) Порошки смешивают в массовом соотношении [слоевища лишайника] / [корни и корневища родиолы розовой] = 5:1, помещают в камеру шаровой мельницы (например, АГО-2, АГО-3 или ЦЭМ-7-80) и подвергают механохимической активации в присутствии 0,7-0,9 мас.% (от массы растительного сырья) бикарбоната натрия в течение 3 минут при 1500 об/мин. Образуется ультрадисперсный порошок с размером частиц 20-60 нм.
В этих условиях часть лишайниковых β-полисахаридов расщепляется до легко усваиваемых в организме человека и животных β-олигосахаридов. Свидетельством этого является увеличение концентрации «восстанавливающих концов» (свободных концевых альдегидных групп β-олигосахаридов) в 14,1 раза - с 4,6 (в порошке грубого помола) до 64,7 мг*экв глюкозы/г порошка (в прототипе - в 7,3 раза - с 4,6 до 33,5 мг*экв глюкозы/г порошка). Происходит также образование более высоких концентраций СМК между лишайниковыми β-полисахаридами и активными веществами корней и корневищ родиолы розовой (салидрозид и др.).
Состав получаемой композиции и композиции в соответствии с прототипом, отражен в таблице 1.
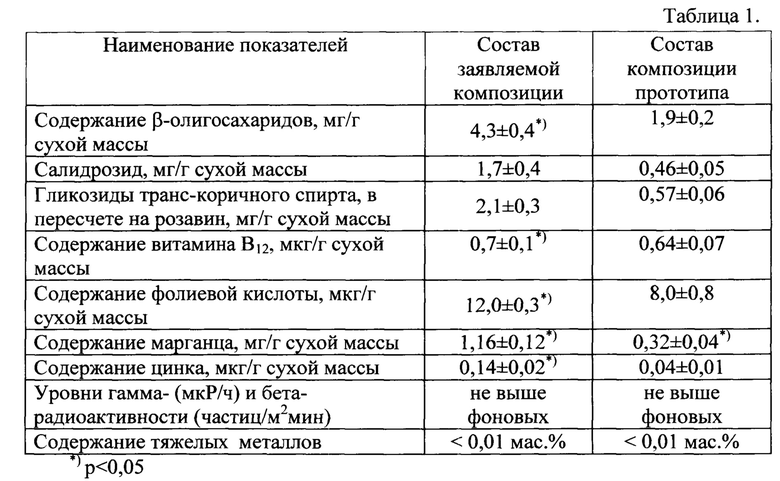
Полученная композиция обладает следующими основными повышенными, по сравнению с прототипом, свойствами:
(1) Актопротекторное и адаптогенное действие.
(1.1) Актопротекторная и адаптогенная эффективность заявляемой композиции, по сравнению с прототипом, изучалась in vivo в виварном эксперименте на белых лабораторных мышах линии CD-1, по методикам, приведенным в работах [8, 9, 12, 17, 19] и в прототипе [18].
Животные (самцы) с начальной массой тела 22-26 г получали заявляемую композицию (группа 1, n=20), прототип (группа 2, n=20), либо плацебо (глюконат кальция; группа 3, n=20) ежедневно в дозе 50 мг/кг путем перорального введения зондом в желудок в течение 45 дней.
На 30-е и 45-е сутки эксперимента проводили оценку выносливости и физической работоспособности животных (адаптивный и актопротектроный потенциалы) по плавательному тесту «Отчаяния» по Porsolt и «Вынужденное плавание» с нагрузкой (фиксировали время плавания животных от начала эксперимента до предельного истощения). А также по тесту «AutoTrack», в рамках которого оценивали «Двигательную активность» (пройденное расстояние при предельной нагрузке - «бег до отказа»), показателем которой являлась неспособность животного продолжать бег против движущейся ленты, несмотря на электростимуляцию.) и «Исследовательскую активность» (количество стоек). Тест характеризует изменения эмоционально-стрессорного состояния животных. Увеличение параметра указывает на повышение их социальной заинтересованности, поисковой активности, адаптивного потенциала. Снижение - на скованность, уменьшение адаптивного потенциала. Это согласуется с классическими представлениями, о том, что поисковая активность способствует успешному выходу из стрессовой ситуации. Результаты тестов приведены в таблице 2. Для всех данных применена описательная статистика: оценены среднее значение и стандартная ошибка среднего. Для определения достоверности межгрупповых различий результаты проанализированы тестом Mann-Whitney (U-test) для непараметрических данных. Их межгрупповое сравнение с нормальным распределением проводили с использованием t-критерия Стьюдента (t-test) для множественного сравнения. Статистический анализ проводили программой Statistica ver. 7.0 при р<0,05.
Установлено, что прием как заявляемой композиции, так и прототипа не вызывает ни патологических изменений при гистологическом анализе, ни клинических признаков, ни смертности животных. За время эксперимента отмечалось увеличение их массы тела во всех трех группах на 37-42%, что объясняется продолжающимся ростом и развитием животных.
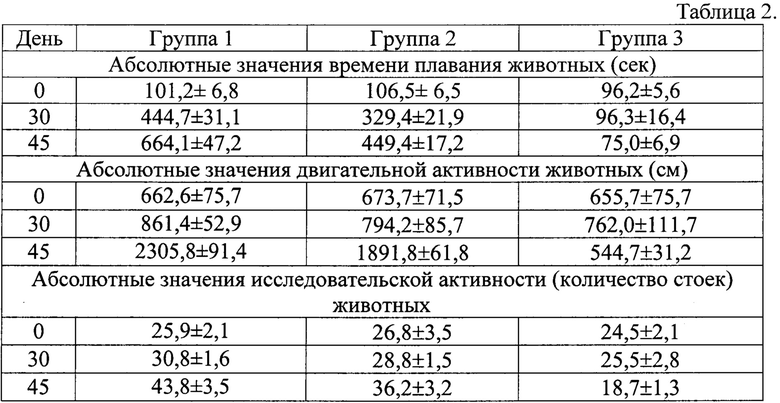
Результаты, приведенные в таблице 2, свидетельствуют о том, что прием заявляемой композиции в течение 45 дней вызывает на 24-56% более выраженное повышение адаптивного и актопротекторного потенциала у лабораторных животных, по сравнению с прототипом.
(1.2) На основании сравнительного анализа состава прототипа со списком компонентов запрещенных ВАДА, который не выявил в нем содержания допинговых компонентов, а также результатов антидопинговой экспертизы композиции прототипа, проведенной в Федеральном научном центре физической культуры и спорта» (ФГБУ ФНЦ ВНИИФК), была исследована адаптогенная и актопротекторная активность заявляемой композиции в спортивной медицине с участием спортсменов пяти скоростно-силовых и сложно-координационных видов спорта: бокс и бои без правил, борьба вольного стиля, а также массовых видов спорта: ушу и цигун [13, 15, 16, 20, 21].
(1.2.1)_Исследованы изменения морфологических и биохимических показателей спортсменов сборных команд России по единоборствам (боксеры и бойцы без правил) до и после приема заявляемой композиции (группа 1; n=15), прототипа (группа 2; n=15) и плацебо (глюконат кальция; группа №3; n=15), в период учебно-тренировочных сборов, с учетом вида спорта и этапа подготовки. Спортивная квалификация - от мастера спорта до мастера спорта международного класса. Средний возраст - 28±4 года, стаж занятий спортом 11±5 лет. Спортсмены всех трех групп находились в одинаковых условиях (питание, медицинский контроль, условия проживания и тренировочного процесса). Спортсмены группы №1 в течение 28 дней получали по одной желатиновой капсуле в день, содержащей 450 мг заявляемой композиции, per os между приемами пищи, группы №2 - прототипа, группы №3 - плацебо в капсулах такого же цвета. Все назначения и медицинский контроль в период проведения эксперимента проводились врачом команды. Установлено, что курсовой прием препаратов не сопровождался достоверным увеличением массы тела спортсменов всех трех групп, составляя 75,7±1,0 кг. При этом показатели массы жира достоверно снизились, а мышечной массы, динамики адаптивного потенциала организма к повышенным нагрузкам (оценивали по: интегральному гормональному показателю - соотношение уровней тестостерона и кортизола в периферической крови (Т/К)) и ряда показателей уровня скоростно-силовой подготовленности увеличились у спортсменов 1-й группы, по сравнению со спортсменами 2-й группы и, особенно по сравнению с группой №3 (таблица 3).
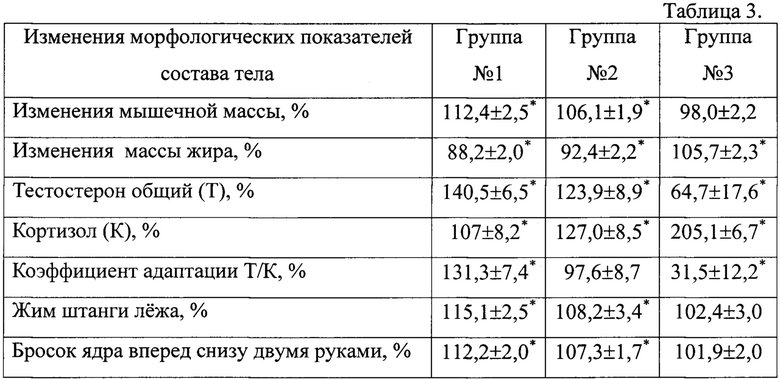
*) р>0,05
(1.2.2) С участием высококвалифицированных спортсменов (членов молодежной и взрослой сборных команд Республики Саха (Якутия) - борцов вольного стиля, применяя прибор «Омега-С», исследовали влияние заявляемой композиции и прототипа на психофизиологическое состояние организма спортсменов, включая количественную оценку параметров: «Адаптация к физическим нагрузкам», «Тренированность», «Энергообеспечение», «Психоэмоциональное состояние», «Спортивная форма». Исследование проводили в период 15-дневных летних сборов на спортивной базе ГБУ РС(Я) «Школа Высшего Спортивного Мастерства» «Манньыаттах» в Мегино-Кангаласском улусе. Все спортсмены, принимавшие участие в эксперименте, прошли углубленный медицинский осмотр и были признаны практически здоровыми. В исследовании участвовало 75 спортсменов в возрасте от 17 до 25 лет (средний возраст 21±4,0 года), одной спортивной квалификации - кандидаты и мастера спорта. Участники исследования были разделены на три репрезентативные по исходным физическим показателям группы. Спортсмены группы №1 (n=25) в течение 15 дней получали per os между приемами пищи по две желатиновые капсулы, содержащие 450 мг заявляемой композиции, в день; группы №2 (n=25) - прототипа, группы №3 (n=25) - плацебо (глюконат кальция) в капсулах такого де цвета. Контрольные измерения проводили два раза: в начале и в конце сборов, т.е. до и после приема заявляемой композиции, прототипа или плацебо. Предварительно, с помощью прибора «Омега-С», провели диагностику степени физической подготовки спортсменов и по результатам показателя «уровень адаптации к физическим нагрузкам» (в % от максимума) каждую группу спортсменов разделили на три подгруппы: (А) спортсмены с низким уровнем исходной физической подготовки (от 14 до 35% от максимального уровня); (Б) спортсмены со средним уровнем исходной физической подготовки (от 36 до 64%); (В) спортсмены с высоким уровнем исходной физической подготовки (от 64 до 100%). В таблице 4 приведены результаты по влиянию 15-дневного приема заявляемой композиции, прототипа или плацебо на психофизиологическое состояние организма спортсменов подгрупп «А» (с низким уровнем исходной физической подготовки), так как в этих подгруппах актопротекторные и адаптогенные свойства заявляемой композиции проявились наиболее ярко.
Параллельно с оценкой психофизиологического состояния спортсменов на приборе «Омега-С», провели комплексное измерение силовых качеств спортсменов подгрупп 1А, 2А и 3А, с помощью станового динамометра (сила тяги, взрывная сила). В этом эксперименте участвуют практически все основные мышцы тела (см. таблица 4).
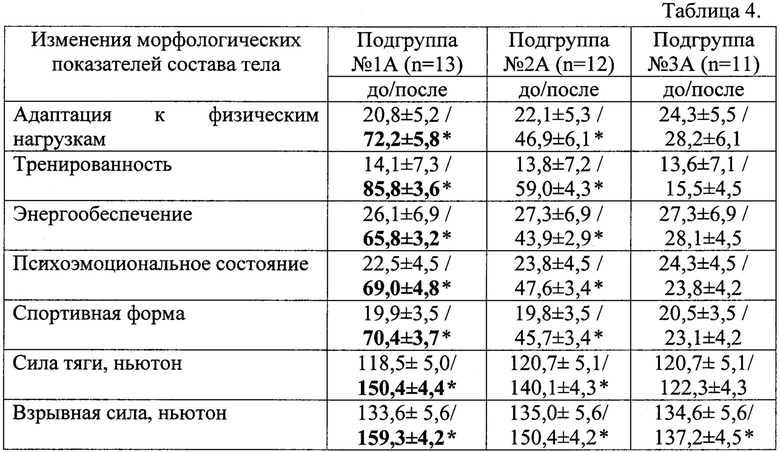
* р>0,05
Из результатов, приведенных в таблице 4, видно, что если 15-дневный прием композиции прототипа (2 капсулы в день) увеличивает основные показатели адаптивного потенциала испытуемых в 1,6-4,3 раза (измеряемые силовые качества при этом возрастают на 15,4-19,6 ньютон), то прием заявляемой композиции - в 2,5-6,1 раза, при повышении силовых качеств на 25,7-31,9 ньютон.
(1.2.3) Исследовано влияние заявляемой композиции и прототипа на адаптивный потенциал, физическую работоспособность и спортивный результат людей, занимающихся массовыми видами спорта, на примере ушу и цигун на базе центра изучения этих массовых видов спорта «Небесная река» PC (Я), разной спортивной квалификации, n=45, возраст - от 17 до 68 лет (средний возраст - 43±20 лет), время проведения - две недели в летний период. Все респонденты, принимавшие участие в эксперименте, прошли углубленный медицинский осмотр и были признаны практически здоровыми. Психофизиологическое состояние их организмов оценивали, также как и борцов вольного стиля, с помощью прибора «Омега-С» в первый и завершающий день эксперимента. Респонденты были разделены на три группы, репрезентативные по исходному значению критерия психофизиологического состояния организма «Адаптация к физическим нагрузкам». Участники первой группы принимали заявляемую композицию, по одной капсуле, содержащей 450 мг заявляемой композиции, per os три раза в день, за 20-30 минут до приема пищи, второй группы - композицию прототипа по такой же схеме, третьей - плацебо (капсулы с глюконатом кальция такого же цвета). Результаты приведены в таблице 5 в виде «результат измерения после эксперимента / результат до эксперимента, в %».
Параллельно оценивали фазу неспецифической адаптивной реакции (НАР) организма по лейкоцитарной формуле крови [2]. Выделяли группу людей, организм которых находится в «позитивных» НАР («устойчивая активация» и «устойчивая тренировка»). При их формировании активности катаболических и анаболических реакций в организме сбалансированы на высоком или среднем уровне интенсивности, соответственно. Группу людей, организм которых находится в «негативных» НАР («стресс» и «переактивация»), при которых активность катаболических реакций резко превалируют над активностью анаболических процессов. А также группу переходных НАР: «неустойчивая активация» и «неустойчивая тренировка».
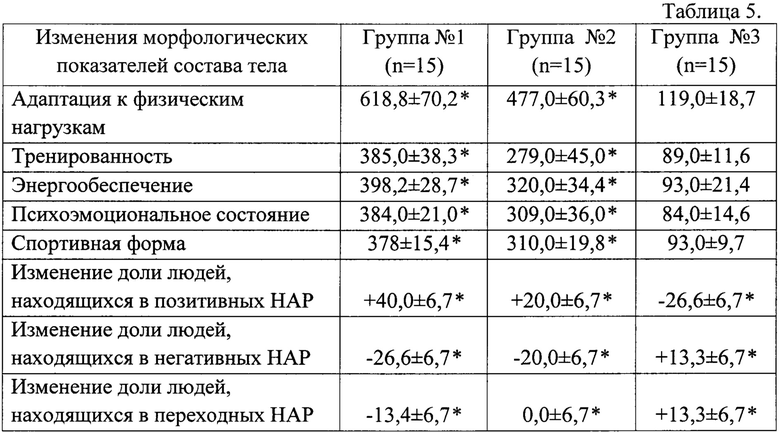
* р<0,05
Из результатов, приведенных в таблице 5, следует, что 2-недельный прием композиции прототипа увеличивает основные показатели адаптивного потенциала респондентов, занимающихся ушу и цигун в 3,1-4,0 раза, то прием заявляемой композиции - в 4,1-5,2 раза. При этом, в группе принимающих заявляемую композицию, доля лиц находящихся в «позитивных» НАР увеличивается на 40% (находящихся в «негативных» и «переходных» НАР уменьшается на 26,6 и 13,4%, соответственно). В группе принимающих композицию прототипа, доля лиц находящихся в «позитивных» НАР увеличивается на 20% (находящихся в «негативных» НАР уменьшается на 20%, находящихся в «переходных» НАР - не изменяется).
(2) Детоксикационное действие.
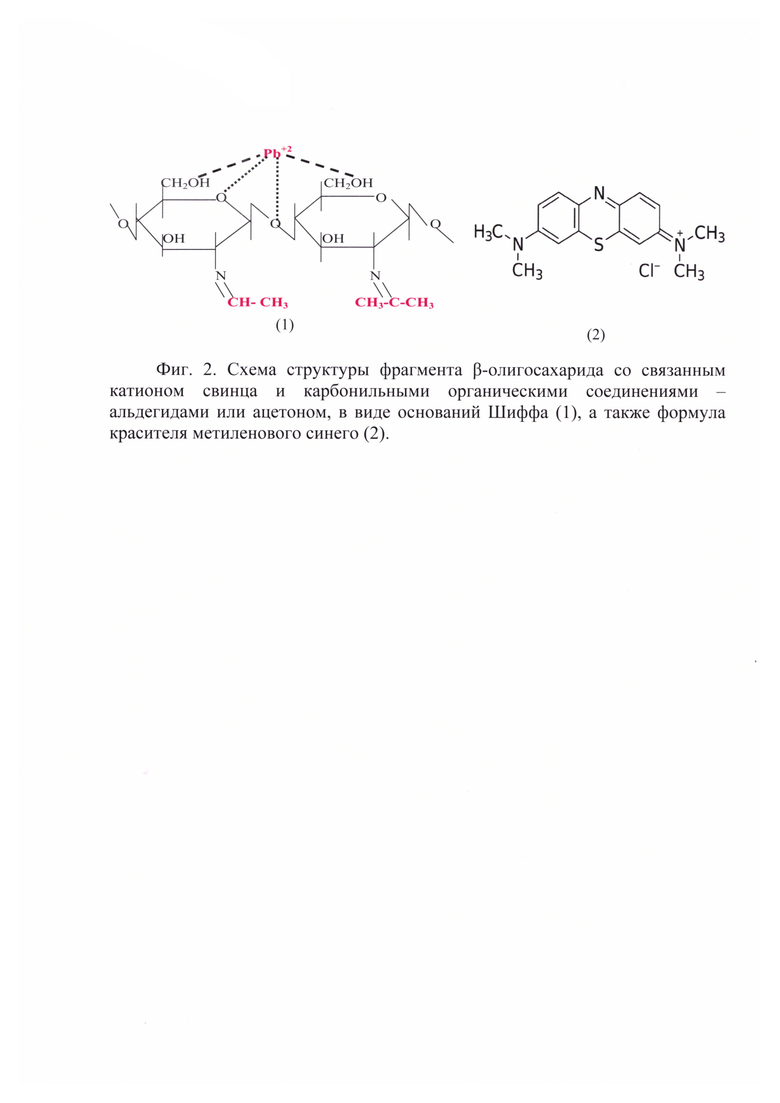
(2.1) Детоксикационные свойства заявляемой композиции определяли in vitro, изучая адсорбционную активность заявляемой композиции или прототипа по катионам тяжелых металлов (на примере ионов Pb2+, раствор соли ацетата свинца) и по метиленовому синему (как аналогу органических эндотоксинов малой и средней молекулярной массы - медиаторов воспалительного процесса; фиг. 2). В раствор адсорбируемого вещества добавляли ультрадисперсный порошок заявляемой композиции или прототипа, инкубировали 20 мин или 24 часа. Центрифугированием отделяли нерастворимую фракцию ультрадисперсных порошков с адсорбированным веществом, затем фильтрацией через нанофильтр с диаметром пор 10 нм фирмы «Amicon» (США) отделяли растворимые комплексы адсорбированного вещества с β-олигосахаридами (они остаются на нанофильтре), и определяли остаточную концентрацию адсорбируемого вещества в растворе. В таблице 6 приведены полученные результаты, расчет проводили в мкмолях адсорбированного вещества на г порошка ягеля грубого помола, исходно взятого для получения заявляемой композиции или прототипа.
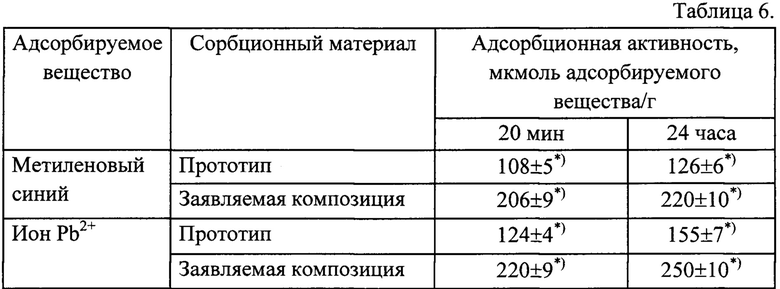
*) р<0,05
Следует отметить, что по метиленовому синему даже у прототипа - это очень высокая адсорбционная емкость по сравнению с такими известными адсорбентами, как полифепан или глина белая, у которых она составляет всего 31,3 и 35,6 мкмоль/г, соответственно. Заявляемая же композиция обладает адсорбционной емкостью в 1,7-1,9 раза большей, чем прототип. По катионам тяжелых металлов у заявляемой композиции также было отмечено повышение в 1,6-1,8 раза адсорбционной емкости in vitro по сравнению с прототипом. По-видимому, это объясняется более высокой концентрацией лишайниковых β-олигосахаридов в заявляемой композиции, по сравнению с прототипом за счет проведения процесса механохимической активации в присутствии 0,7-0,9 мас.% (от массы растительного сырья) бикарбоната натрия.
(2.2) Детоксикационная активность была зарегистрирована in vivo по изменению в крови концентрации «токсина усталости» (молочной кислоты) и мочевины крови в результате ежедневного введения в корм белым лабораторным мышам линии CD-1 заявленной композиции в дозе 50 мг/кг (в контроле - адекватной дозы прототипа), на фоне ежедневной повышенной нагрузки в виде 4-минутного плавания, в течение 10 дней. Показано, что при потреблении животными заявляемой композиции на фоне вышеуказанной физической нагрузки снижение уровня молочной кислоты достигало 46-60% (прототипа - 24-36%) по сравнению с контролем (отсутствие добавок); мочевины - 41% (прототип - 26%).
(2.3) Детоксикационная активность заявляемой композиции, по сравнению с прототипом была исследована в период 15-дневных летних сборов высококвалифицированных спортсменов - борцов вольного стиля (см. п. 1.2.2). Перед началом и в конце сборов в крови спортсменов определяли уровень молочной кислоты и мочевины на фоне интенсивной физической (стандартной дневной тренировочной) нагрузки (через 10-15 минут после окончания вечерней тренировки). В таблице 7 приведены полученные результаты в виде изменений содержания соответствующего конечного продукта обмена углеводного или белкового обмена в процессе 15-дневного приема заявляемой композиции, прототипа или плацебо, в %.

Таким образом, предложенная твердофазная композиция, получаемая механохимической активацией, в присутствии 0,7-0,9 мас.% (от массы растительного сырья) бикарбоната натрия, смеси слоевищ лишайников рода Cladonia, корней и корневищ родиолы розовой (Rhodiola rosea L.) в соотношении 5:1, и содержащая лишайниковые β-олигосахариды в концентрации 4,3±0,4 мг/г, салидрозид в концентрации 1,7±0,4 мг/г и гликозиды транс-коричного спирта в концентрации 2,1±0,3 мг/г (в пересчете на розавин) обладает повышенным на 24-56% (по сравнению с прототипом) адаптогенным и актопротекторным действием ив 1,5-1,9 раза повышенной детоксикационной активностью. Композиция может быть использована в целях повышения адаптивного потенциала, физической и умственной работоспособности, устойчивости к неблагоприятным факторам среды людей, работающих и проживающих в экстремальных условиях, а также в спортивной медицине, так как композиция не содержит компонентов из списка запрещенных ВАДА и прошла антидопинговую экспертизу.
Литература.
1. ФС.2.5.0036.15 от 29.10.2015 «Корни и корневища родиолы розовой»
2. Гаркави Л.Х., Квакина Е.Б., Кузьменко Т.С. Антистрессорные реакции и активационная терапия (Реакция активации как путь к здоровью через процессы самоорганизации). - М.: изд. ИМЕДИС.- 1998. - 656 с
3. Graham D. Lamb and D. George Stephenson Point: Counterpoint: Lactic acid accumulation is an advantage/disadvantage during muscle activity // Journal of Applied Physiology. - 2006. - V. 100. - №4. - P. 1410-1412.
4. Свидетельство о государственной регистрации, санитарно-эпидемиологическое заключение и ТУ на БАД «Ягель» / Свидетельство ЕВРАЗЭС о гос. регистрации Роспотребнадзора РФ № RU.77.99.11.003.E.051236.11.11 от 17.11.2011.
5. Свидетельство о государственной регистрации, санитарно-эпидемиологическое заключение и ТУ на БАД «Ягель-Детокс» / Свидетельство ЕВРАЗЭС о гос. регистрации Роспотребнадзора РФ № RU.77.99.11.003.Е.003704.05.13 от 20.05.2013.
6. Кершенгольц Б.М., Журавская А.Н., Ремигайло П.А., Филиппова Г.В., Шеин А.А., Шашурин М.М., Кершенгольц Е.Б. Способ получения водки, обладающей пониженным токсическим и наркотическим эффектом // Патент РФ №2318407 от 10.03.2008, приоритет от 10.01.2006.
7. Кершенгольц Б.М., Кершенгольц Е.Б., Шеин А.А. Комплекс биологически активных веществ, выделенных из лишайников методом СO2 флюидной сверхкритической экстракции, оценка его влияния на состояние крыс при их алкоголизации // Наука и образование. - №2. - 2005. - С. 74-80.
8. Аньшакова В.В. Биотехнологическая механохимическая переработка лишайников рода Cladonia // Рос. акад. естествознания. - Москва: Издательский дом Академии естествознания, 2013. - 115 с.
9. Кершенгольц Б.М. Лишайники: биотехнологии переработки, биопрепараты на их основе // Монография. - изд-во LAP LAMBERT Academic Publishing. - 2016. - 100 с. (6,3 п.л.)
10. Аньшакова В.В., Шарина А.С., Каратаева Е.В., Кершенгольц Б.М. Способ получения сорбционного материала из слоевищ лишайников // Патент РФ №2464997 от 27.10.2012, приоритет от 20.07.2011.
11. Кершенгольц Б.М., Кунгурцев С.В., Шашурин М.М. Способ профилактики и купирования похмелья с помощью питьевой воды // Патент РФ №2608657 от 23.01.2017, приоритет от 05.06.2015.
12. Аньшакова В.В., Степанова А.В., Уваров Д.М., Смагулова А.Ш., Наумова К.Н., Васильев П.П., Кершенгольц Б.М. Актопротекторная активность комплексного битопрепарата на основе таллома лишайников и родиолы розовой // Экология человека. 2015. №5. С. 46-51.
13. K.N. Naumova, V.V. Anshakova, B.M. Kershengolts Nonspecific adaptive reactions of athletes: evaluation and correction // Journal of Biopharmaceuticals. - 2015. - №4. P. 238-239.
14. Аньшакова B.B. Повышение активности действующего вещества лишайниковыми β-олигосахаридами // Биофармацевтический журнал. - 2012. - Т. 4. №4. - С. 42-46.
15. Аньшакова В.В., Наумова К.Н., Васильев П.П., Степанова А.В., Платонова Р.И. Комплексные БАД на основе северного биосырья в медикло-биологическом совершенствовании физкультурно-спортивной деятельности // Вестник Башкирского университета. - 2013. - Т. 18, №4. - С. 1069-1072.
16. Аньшакова В.В., Степанова А.В., Уваров Д.М. Комплексные пищевые добавки из возобновляемого сырья для специализированного питания спортсменов // Технология пищевых производств. - 2017. - Т. 44, №1. - С. 5-10.
17. Аньшакова В.В., Кершенгольц Б.М. Адаптогенный механохимический биокомплекс на основе растительного сырья // Вопросы биологической, медицинской и фармацевтической химии. 2013. - №10. - С. 29-33.
18. Аньшакова В.В., Кершенгольц Б.М. Биологически активная добавка актопротекторного, адаптогенного действия из растительного сырья и способ ее получения // Патент РФ №2477143 от 10.03.2013, приоритет от 26.10.2011.
19. Аньшакова, В.В. Оценка адаптогенной эффективности механохимического биокомплекса на основе растительных субстанций // Нанотехнологии и охрана здоровья. - 2012. - №1 (Т. 4). - С. 16-22.
20. Наумова К.Н., Аньшакова В.В., Кершенгольц Б.М., Платонова Р.И., Халыев С.Д. Способ повышения общей физической работоспособности спортсменов скоростно-силовых видов спорта // Патент РФ №2568836, приоритет от 24.07.2014, зарегистрирован в реестре 20.11.2015, бюллетень №32.
21. Наумова К.Н., Аньшакова В.В., Кершенгольц Б.М. Способ повышения психофизиологического состояния организма спортсменов массовых видов спорта // Патент РФ №2604126 (приоритет от 15.06.2015). зарегистр. в госреестре 14.11.2016.
| название | год | авторы | номер документа |
|---|---|---|---|
| Жидкофазная композиция, обладающая антибактериальным и детоксикационным действием | 2017 |
|
RU2652347C1 |
| Твердофазная композиция, обладающая антибактериальным и детоксикационным действием | 2017 |
|
RU2657782C1 |
| Твердофазная композиция природных биоактивных ингредиентов для коррекции метаболических нарушений при сахарном диабете второго типа | 2017 |
|
RU2661622C1 |
| Композиция на основе бетулина и слоевищ лишайников, обладающая антибактериальным, противовирусным и детоксикационным действием | 2019 |
|
RU2710236C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА АКТОПРОТЕКТОРНОГО, АДАПТОГЕННОГО ДЕЙСТВИЯ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2477143C1 |
| СПОСОБ ПОВЫШЕНИЯ ПСИХОФИЗИОЛОГИЧЕСКОГО СОСТОЯНИЯ ОРГАНИЗМА СПОРТСМЕНОВ МАССОВЫХ ВИДОВ СПОРТА | 2015 |
|
RU2604126C1 |
| СПОСОБ ПОВЫШЕНИЯ ОБЩЕЙ ФИЗИЧЕСКОЙ РАБОТОСПОСОБНОСТИ СПОРТСМЕНОВ СКОРОСТНО-СИЛОВЫХ ВИДОВ СПОРТА | 2014 |
|
RU2568836C1 |
| Способ и состав для производства водки | 2020 |
|
RU2745450C1 |
| Твердофазная композиция для коррекции метаболических нарушений при сахарном диабете второго типа | 2020 |
|
RU2747985C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЦИОННОГО МАТЕРИАЛА ИЗ СЛОЕВИЩ ЛИШАЙНИКОВ | 2011 |
|
RU2464997C1 |
Изобретение относится к фармацевтической промышленности, а именно к твердофазной композиции, обладающей комплексным актопротекторным, адаптогенным и детоксикационным действием. Твердофазная композиция, обладающая комплексным актопротекторным, адаптогенным и детоксикационным действием, представляет собой ультрадисперсный порошок, механохимически активированных в присутствии 0,7-0,9 мас.% от массы растительного сырья бикарбоната натрия, смеси слоевищ лишайников рода Cladonia и корней и корневищ родиолы розовой (Rhodiola rosea L.) в массовом соотношении 5:1, которая содержит лишайниковые β-олигосахариды, салидрозид и гликозиды транс-коричного спирта в определенной концентрации. Вышеописанная композиция обладает повышенным актопротекторным, адаптогенным и детоксикационным действием. 2 ил., 7 табл.
Твердофазная композиция, обладающая комплексным актопротекторным, адаптогенным и детоксикационным действием, представляющая собой ультрадисперсный порошок, механохимически активированных в присутствии 0,7-0,9 мас.% от массы растительного сырья бикарбоната натрия, смеси слоевищ лишайников рода Cladonia и корней и корневищ родиолы розовой (Rhodiola rosea L.) в массовом соотношении 5:1, характеризующаяся тем, что содержит лишайниковые β-олигосахариды в концентрации 4,3±0,4 мг/г, салидрозид в концентрации 1,7±0,4 мг/г и гликозиды транс-коричного спирта в концентрации 2,1±0,3 мг/г в пересчете на розавин.
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА АКТОПРОТЕКТОРНОГО, АДАПТОГЕННОГО ДЕЙСТВИЯ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2477143C1 |
| В.В.АНЬШАКОВА и др | |||
| Влияние механоактивации биокомплексов на основе слоевищ лишайников на экстрагируемость эссенциальных микроэлементов в модельных средах //Химия в интересах устойчивого развития, 19, 2011, 433-436 | |||
| RU 26004126 С1, 10.12.2016 | |||
| ANSHAKOVA VV | |||
| et al | |||
| Adaptogenic activity of a complex biomedication based on a northern renew raw material //Wiad Lek., 2016, 69:55-60. | |||
Авторы
Даты
2018-07-17—Публикация
2017-08-28—Подача