Изобретение относится к области медицины и фармакологии, в частности к эндокринологии, и может быть использовано в целях коррекции метаболических нарушений при сахарном диабете второго типа (СД2). Сахарный диабет (СД) - метаболическое заболевание, связанное с нарушением метаболизма глюкозы из-за абсолютной или относительной недостаточности инсулина, а также нарушения передачи инсулинового сигнального каскада в тканях-мишенях инсулина. Вместе с тем, ключевым в патогенезе СД2, особенно на ранних его стадиях, является не нарушение синтеза инсулина в β-клетках островков Лангерганса поджелудочной железы, а ингибирование его секреции в результате нарушений биоэнергетических процессов в этих клетках и изменений структуры и свойств клеточных мембран, приводящих к формированию ряда дефектов, связанных с «искажениями» процесса «узнавания» глюкозы или чувствительности к глюкозе рецепторов на мембране β-клеток поджелудочной железы, либо нарушения транспортной функции ионных каналов. В результате снижения уровня инсулина в крови или нарушения передачи инсулинового сигнального каскада в клетках-мишенях нарушается транспорт глюкозы в клетки-мишени инсулина, формируется состояние гипергликемии и глюкозурии, в то время как сами клетки-мишени испытывают дефицит глюкозы; в результате нарушается весь комплекс биоэнергетических процессов в соответствующих тканях [1-3]. Наиболее часто встречаются сердечно-сосудистые осложнения СД: артериальная гипертензия, диабетические ангио- и ретинопатия, ишемическая болезнь сердца и ряд других осложнений. Эти же осложнения принято считать причиной преждевременной инвалидизации и высокой смертности от СД.
Традиционная сахароснижающая терапия включает гипогликемические и антигипергликемические средства. При этом гипогликемические средства (производные сульфонилмочевины, меглитиниды и др.) стимулируют секрецию эндогенного инсулина (это сопровождается прибавкой массы тела) и способны вызывать гипогликемические состояния, а антигипергликемические средства (блокаторы альфа-глюкозидазы, бигуаниды (метформин), тиазолидиндионы (глитазоны)) улучшают периферическую утилизацию глюкозы, но не оказывают стимулирующего действия на β-клетки поджелудочной железы. Поэтому они не повышают уровень инсулина в крови и не вызывают гипогликемических состояний. Использование выше указанных способов глюкозонормализующей медикаментозной терапии не позволяет достигнуть точности регуляции гликемии, имеет ряд побочных эффектов и противопоказаний при сопутствующих заболеваниях, поэтому новые разработки в этой области направлены на изучение принципиально нового механизма регуляции гомеостаза глюкозы посредством инкретинов -пептидных гормонов желудочно-кишечного тракта, вырабатываемых в ответ на прием пищи и вызывающих глюкозозависимую стимуляцию секреции инсулина, а также на создание препаратов, восстанавливающих интактность мембран β-клеток панкреаса, биоэнергетический гомеостаз и функциональную активность ионных каналов, участвующих в глюкозостимулированной секреции инсулина.
Для лечения пациентов с СД2 используется широкий спектр фармакологических препаратов с различными механизмами действия, направленными на нормализацию гомеостаза глюкозы. В течение многих лет эти препараты, мишенью воздействия которых являются β-клетки и периферические ткани, доминируют на фармацевтическом рынке [4]. Вместе с тем, установлено, что, несмотря на большой ассортимент различных групп пероральных сахароснижающих препаратов, редко удается добиться и поддерживать длительное время целевые показатели гликированного гемоглобина. Кроме того длительный прием per os сахароснижающих фармацевтических препаратов часто приводит к побочным эффектам и имеет строгие противопоказания при обострениях осложнений [4].
Фитопрепаратам, обладающим способностью снижать концентрацию глюкозы в крови и моче, эти недостатки не свойственны. Они включают различные лекарственные растения, обладающие гипогликемическим (антидиабетическим) действием, в первую очередь за счет повышения уровня секреции инсулина β-клетками поджелудочной железы, в качестве основного или дополнительного лечения, а также благодаря купированию дефицита биоэнергетических моносахаридов в клетках. Растения, обладающие гипогликемическими свойствами, длительное время используются в народной медицине. И именно они являются источником активных веществ целого ряда противодиабетических фармацевтических средств. Например, козлятник лекарственный (лат. Galega officinalis), содержащий алкалоид галегин с антигипергликемическими свойствами. Галегин является структурным аналогом метформина - препарата широко применяемого при лечении СД2. В настоящее время становится актуальным поиск новых, ранее неиспользовавшихся природных соединений или их смесей в профилактике СД2, сводящийся к созданию композиций биоактивных веществ гипогликемического назначения и использующихся совместно или в комбинации со стандартной сахароснижающей терапией.
Известен жидкофазный биопрепарат «Ягель», получаемый водно-спиртовой экстракцией слоевищ лишайников рода Cladonia, предварительно обработанных диоксидом углерода в состоянии суперкритической жидкости (одно из основных активных веществ - лишайниковые β-олигосахариды) [5], который оказывает эффект стимуляции секреции инсулина клетками инсулиномы в 1,8-2,0 раза при добавлении в среду их инкубации в течение 3-4 недель за счет восстановления инсулин-секреторной способности, благодаря модификации клеточных и митохондриальных мембран β-клеток лишайниковыми β-олигосахаридами [6]. Далее, повышается уровень трансмембранного переноса глюкозы в клетку, увеличивается интенсивность клеточного дыхания и митохондриальная активность в мышечных клетках [6]. Клинические исследования эффективности БАД «Ягель», проведенные в целях профилактики СД2 показали, что после 3-х недельного приема препарата доля лиц с повышенными содержанием глюкозы снизилась в 3,0 раза (до 14,3%), холестерина - в 1,6 раза (до 33,3%), коэффициента атерогенности - в 2,6 раза, а с сочетанным повышенными уровнями глюкозы и холестерина - более чем в 5 раз [7]. В итоге БАД «Ягель» был рекомендован для профилактики развития сердечно-сосудистых заболеваний и метаболических нарушений, вызванных гипергликемией.
Клинические исследования эффективности другого биопрепарата, активным веществом которого также являются лишайниковые β-олигосахариды - БАД «Ягель-Детокс» [8], получаемого путем механохимической активации грубо измельченных слоевищ лишайника рода Cladonia, в целях коррекции метаболических нарушений у больных СД2, показали, что его прием в течение 3 месяцев приводит к стойкому снижению уровня глюкозы крови на 20%, гликированного гемоглобина - на 12%, общего холестерина - на 7%, при повышении содержания липопротеидов высокой плотности на 18%, в итоге коэффициент атерогенности снизился на 24% [9, 10].
Лишайниковые β-олигосахариды обладают и другими важными свойствами, значимыми для достижения цели - коррекции метаболических нарушений при СД2. Они:
- не гидролизуются в желудочно-кишечном тракте (ЖКТ), т.к. содержат прочные β-гликозидные связи и в кишечнике человека не вырабатываются целлюлазы, способные их ферментативно гидролизовать;
- содержат большое количество гидрофильных функциональных групп (-ОН, -NH2, =СО и др.) и гидрофобных фрагментов, обеспечивающих образование супрамолекулярных комплексов (СМК) с контактирующими с ними низкомолекулярными и/или олигомерными соединениями как гидрофильной, так и гидрофобной природы, в котором β-олигосахариды выступают в качестве «активного носителя», а содержащиеся в композиции (или вводимые в нее) низкомолекулярные соединения - «фармаконы»;
- СМК хорошо всасывается из ЖКТ в кровь, благодаря бифильному строению и размерам «активного носителя», легко транспортируется через клеточные мембраны за счет небольших размеров и бифильной природы лишайниковых β-олигосахаридов, близких к олигогликозидными фрагментами гликокаликса клеточных мембран, обеспечивая повышенную биодоступность «фармакона»;
- во внутренних средах организма, после распада супрамолекулярного комплекса, лишайниковые β-олигосахариды связывают во внутренних средах (цитоплазма, межклеточные жидкости, кровь, лимфа) конечные продукты метаболизма - эндотоксины (молочная и мочевая кислота, мочевина, медиаторы воспаления - эндотоксины малой и средней молекулярной массы и др.), а также экзотоксины (катионы тяжелых металлов, радионуклиды, оксиды углерода и серы, органические токсические соединения, включая фенолы, алкогольные токсины: ацетальдегид, ацетон, бактериальные и вирусные токсины и др.) и выводят их из организма.
Благодаря этим свойствам лишайниковых β-олигосахаридов достигается, во-первых, повышенная усвояемость и биоактивность «фармакона» независимо от степени его гидрофобности/гидрофильности. Во-вторых, обеспечивается проявление детоксикационной активности в отношении внутренних сред организма.
Повышение биодоступности и биоактивности «фармакона» актопротекторного действия при комплексообразовании с лишайниковыми β-олигосахаридами и проявление их детоксикационной активности в отношении эндотоксинов: молочной кислоты, мочевины, было установлено, например, при испытаниях биопрепарата «Кладород», состоящего из лишайниковых β-олигосахаридов и флавогликозидов, выделяемых из корней и корневищ родиолы розовой (салидрозида и др.) [11-13].
Использование лишайников рода Cladonia и Cetraria в противодиабетической практике подтверждает рецепт лишайникового хлеба, в котором в качестве добавки используется первичный лишайниковый метаболит - β-полисахарид лихенин. Лишайниковый хлеб может служить заменой стандартному диабетическому хлебу, при выпечке которого в муку добавлялся измельченный порошок лишайника [14, 15]. Известно употребление в китайской медицине кладонии оленьей (Cladina rangiferina (L.) Nyl.) и супа из дерматокарпона матово-красного (Dermatocarpon miniatum (L.) при высоком артериальном давлении, а также как диуретического средства [16]. Стереокаулон голый (Stereocaulon paschale (L.) Hoffm.) использовался для лечения воспаления, связанного с диабетом. В модельных экспериментах in vivo с мышами с аллоксан-индуцированным диабетом выявлены гипогликемические свойства экстрактов лишайника Cladonia humilis, заключающееся в повышении уровня секреции инсулина и синтеза гликогена (р<0,05 и р<0,01 соответственно), в снижении уровня глюкозы крови (р<0,05), а также выявлена способность этого экстракта ингибировать процесс глюконеогенеза (р<0.01) и повышать уровень толерантности к углеводам [17].
Из других фитокомпозиций и фитоисточников биоактивных веществ, эффективных в отношении коррекции метаболических нарушений при СД2, известен сбор «Детский», обладающий гипогликемической активностью и применяющийся при комбинированной профилактике и лечении СД2 на фоне стандартной сахароснижающей терапии. Он включает плоды шиповника коричного, створки фасоли обыкновенной, листья шелковицы белой, ореха грецкого, смородины черной, шалфея лекарственного, крапивы двудомной, траву галеги лекарственной, тимьяна ползучего, плоды лимонника китайского и соломку овса посевного [18].
Известна фитокомпозиция «Прасковья» предназначенная для пероральной и фитопаротерапии сахарного диабета [19], содержащая (1) лист: брусники, толокнянки обыкновенной, смородины черной лесной, черники обыкновенной; (2) плоды и корень: боярышника кроваво-красного, шиповника иглистого; (3) траву: вероники беловойлочной, горца птичьего, грушанки крупнолистной, донника лекарственного, крапивы двудомной жгучей, манжетки обыкновенной, мяты перечной, подмаренника настоящего, полыни обыкновенной, термопсиса ланцетного, хвоща полевого, череды трехраздельной, ярутки полевой; (4) соцветия зверобоя продырявленного; (5) лист и кору ивы плакучей; (6) цветы: клевера лугового, лабазника вязолистного; (7) корень: лопуха большого, левзеи сафлоровидной, цикория обыкновенного, пырея ползучего; (8) плоды: можжевельника обыкновенного, рябины сибирской; (9) колос молочной спелости овса посевного; (10) корень и траву: одуванчика лекарственного, подорожника большого; (11) соцветия:первоцвета крупночашечного, тысячелистника обыкновенного; (12) клубни топинамбура; (13) мох уснеи сибирской.
Известна также антидиабетическая фитокомпозиция, содержащая по 11,8 мас. %: траву козлятника лекарственного (галеги), корни одуванчика лекарственного, листья шелковицы белой, корни девясила высокого, листья брусники обыкновенной, створки плодов фасоли обыкновенной, листья лавра благородного, траву череды поникшей, а также 5,6 мас. % цветки липы сердцевидной [20] и др.
Вместе с тем, получение известных фитопрепаратов, основное действие которых направлено на повышение толерантности к углеводам, снижение уровня гликированного гемоглобина, отличается такими технологическими стадиями, при которых происходит неполный выход всего комплекса физиологически активных веществ. Терапевтический эффект от использования таких композиций недостаточно высок, т.к. биопрепараты на основе фитосмесей, получаемые простым механическим смешиванием, характеризуются низкой биодоступностью и слабой биоактивностью. Прием данных препаратов может вызывать побочные эффекты, такие как изжога, аллергические реакции, повышение артериального давления, кетоацидоз.
Более выраженным противодиабетическим действием, из известных фитокомпозиций, обладает комплекс биоактивных веществ, выделяемых из клубней топинамбура (лат. 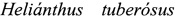 ), основным активным веществом в котором является инулин - до 60% содержания в сухом веществе. Инулин - полифруктозан D-фруктозы, единственный природный полисахарид, состоящий на 95% из фруктозы. Инулин не переваривается пищеварительными ферментами желудочно-кишечного тракта человека. Часть его в кислой среде желудочного сока гидролизуется до коротких фруктозных цепочек - фруктозоолигосахаридов (ФОС), выполняющих функции детоксикации в кишечнике, и отдельных молекул фруктозы, которые проникают в кровеносное русло. Всосавшиеся в кишечнике ФОС и в крови продолжают выполнять детоксикационную функцию, связывая, обезвреживая и облегчая выведение из организма эндо- и экзотоксинов [21, 22]. ФОС утилизируются большинством штаммов бифидобактерий, а также некоторыми культурами лактобактерий. При их употреблении в кишечнике происходит нормализация микробной флоры с увеличением абсорбции из кишечника ионов кальция и магния. Они обладают низкой калорийностью и поэтому могут быть рекомендованы пациентам с сахарным диабетом и ожирением.
), основным активным веществом в котором является инулин - до 60% содержания в сухом веществе. Инулин - полифруктозан D-фруктозы, единственный природный полисахарид, состоящий на 95% из фруктозы. Инулин не переваривается пищеварительными ферментами желудочно-кишечного тракта человека. Часть его в кислой среде желудочного сока гидролизуется до коротких фруктозных цепочек - фруктозоолигосахаридов (ФОС), выполняющих функции детоксикации в кишечнике, и отдельных молекул фруктозы, которые проникают в кровеносное русло. Всосавшиеся в кишечнике ФОС и в крови продолжают выполнять детоксикационную функцию, связывая, обезвреживая и облегчая выведение из организма эндо- и экзотоксинов [21, 22]. ФОС утилизируются большинством штаммов бифидобактерий, а также некоторыми культурами лактобактерий. При их употреблении в кишечнике происходит нормализация микробной флоры с увеличением абсорбции из кишечника ионов кальция и магния. Они обладают низкой калорийностью и поэтому могут быть рекомендованы пациентам с сахарным диабетом и ожирением.
Природная фруктоза, из которой состоит инулин, - уникальный моносахарид, диетический сахар, который способен участвовать в тех же обменных процессах, что и глюкоза, и полноценно замещать ее в ситуациях, когда глюкоза клетками не усваивается, т.е. в случаях относительной или абсолютной нехватки инсулина. Еще и поэтому диетическая и лечебная ценность инулина очень велика.
Известно, что топинамбур уникален по сбалансированности, входящих в его состав микроэлементов. Отмечено высокое содержание (в мг/г): железа - до 0,12, калия - до 2,0, кальция - до 0,4, кремния - до 0,08, магния - до 0,3, марганца - до 0,45, фосфора и цинка - до 5,0. Такое оптимальное соотношение микроэлементов значительно усиливает функциональную активность иммунной, эндокринной, нервной систем организма, а также улучшает клинические показатели крови. Отмечено высокое содержание витаминов группы В (В1 В2 и В6), С, РР, каротиноидов, каротина (до 0,06-0,07 мг/г), органических поликислот: лимонной, яблочной, малеиновой, янтарной, фумаровой. В комплексе с витамином С они обладают ярко выраженными антиоксидантными свойствами. Отмечено также относительно высокое содержание белка (3,2% на сухое вещество), представленного 16 аминокислотами, в том числе незаменимыми: валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин, гистидин, аргинин (для детей). По данным Новосибирского НИИ клинической иммунологии СО РАН белки топинамбура близки по своей структуре белкам тимуса и обладают свойствами регуляторов созревания и протекции функциональной активности клеток иммунной системы. Пектиновые вещества (до 110 мг/г массы сухого вещества) обладают абсорбирующими, вяжущими и желирующими свойствами, снижают уровень холестерина в организме, способствуют улучшению обменных процессов, нормализуют перистальтику кишечника, улучшают периферическое кровообращение, способны сорбировать и выводить из организма эндо- и экзотоксины. Поэтому клубни топинамбура не накапливают тяжелые металлы (даже при выращивании на участках с искусственно повышенным их содержанием в 10-15 раз), радиоактивные элементы (даже при искусственном заражении опытных делянок изотопами стронция и цезия выше фонового содержания в 10-20 раз содержание этих элементов в клубнях увеличивается только на 10-30%). Это объясняет тот факт, что у топинамбура совершенно отсутствует токсичное и аллергизирующее действие.
Главным, применительно к цели предлагаемого изобретения, является то, что длительное употребление топинамбура снижает уровень глюкозы в крови, и является эффективным средством профилактики и купирования метаболических нарушений при СД2. Механизмы этого следующие: (1) нерасщепленные соляной кислотой в желудке молекулы инулина и клетчатка способны выводить значительное количество пищевой глюкозы и препятствовать ее всасыванию в кровь, что способствует снижению уровня глюкозы в крови после еды; (2) ФОС связывают и выводят из организма токсические продукты нарушенного обмена веществ: ацетон и другие кетоновые тела; (3) в крови ФОС и органические полиоксикислоты (яблочная, фумаровая, малеиновая, лимонная, янтарная и др.) также выполняют антиоксидантные и антитоксические функции, уменьшая тяжесть течения заболевания; (4) ФОС способны встраиваться в клеточную стенку, облегчая прохождение внутрь клетки глюкозы, хотя и в относительно небольших, по сравнению с нормой, количествах; (5) фруктоза, проникая в клетки всех органов без участия инсулина, способна полноценно замещать глюкозу в обменных процессах, значительно уменьшая внутриклеточный дефицит глюкозы в биоэнергетических процессах. Все это ведет к существенному и стойкому снижению концентрации глюкозы в крови, которое не сопровождается резкими колебаниями этого показателя в течение суток. Стабильное снижение уровня глюкозы в крови приводит к повышению выработки собственного инсулина β-клетками поджелудочной железы. Этому же способствует и высокое содержание в топинамбуре цинка, кремния, калия, необходимых для синтеза инсулина. При этом уменьшается суточная потребность больного во вводимом в виде инъекций инсулине. При регулярном употреблении топинамбура отмечается замедление или отсутствие развития диабетической нефропатии, грозящей почечной недостаточностью; диабетической ретинопатии, приводящей к слепоте; поражения сосудов конечностей, заканчивающегося гангреной и т.д.
Вместе с тем, противодиабетическая активность комплекса биоактивных веществ топинамбура может быть усилена путем образования совместных механохимически активированных композиций с активными веществами ягелевых биопрепаратов, прежде всего с лишайниковыми β-олигосахаридами, благодаря способности последних, во-первых, повышать уровень секреции инсулина β-клетками поджелудочной железы. Во-вторых, увеличивать биоусвояемость ФОС, образующихся из инулина в кислой среде желудка. В-третьих, при механоактивации грубоизмельченных клубней топинамбура увеличивается концентрация ФОС.
Наиболее близкой к заявляемому изобретению в отношении эффективности коррекций метаболических нарушений при СД2 является композиция, состоящая из биоактивных веществ слоевищ лишайников рода Cladonia, листьев брусники  и толокнянки
и толокнянки 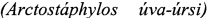 , образующаяся в процессе их совместной механохимической активации в соотношении 18:1:1 [23] - прототип.
, образующаяся в процессе их совместной механохимической активации в соотношении 18:1:1 [23] - прототип.
Технический эффект (сущность) заявляемого изобретения заключается в коррекции метаболических нарушений при СД2 при приеме заявляемой композиции, а именно в снижении уровня глюкозы и гликированного гемоглобина (HbA1c) крови, а также в нормализации показателей липидного обмена, включая коэффициент атерогенности, вплоть до стабилизации этих показателей в верхней границе нормы.
Технический эффект (сущность) заявляемого изобретения достигается благодаря тому, что проводят совместную механохимическую активацию высушенных и предварительно грубо измельченных слоевищ лишайника рода Cladonia и клубней топинамбура в массовом соотношении 9:1, в присутствии 0,7-0,9 мас. % (от массы растительного сырья) бикарбоната натрия. Это приводит в отсутствие растворителей к: (1) расщеплению части β-гликозидных связей в лишайниковых β-полисахаридах с образованием β-олигосахаридов (активного наполнителя); (2) расщеплению части 1-2 гликозидных связей в инулине с образованием ФОС и фруктозы; (3) образованию супрамолекулярных комплексов «активного наполнителя» с ФОС, благодаря чему в 2,0-2,5 раза повышается их биодоступность; (4) лишайниковые β-олигосахариды и ФОС во внутренних средах организма выполняют роль их детоксиканта; (5) фруктоза, проникая в клетки всех органов без участия инсулина, полноценно замещает глюкозу в обменных процессах, значительно уменьшая энергетический клеточный голод, а ФОС, встраиваясь в клеточную стенку, облегчают инсулин-независимое прохождение внутрь клетки и самой глюкозы.
Изобретение может быть реализовано следующим образом.
Смесь порошков измельченных до размера частиц 1-3 мм слоевищ лишайников рода Cladonia и клубней топинамбура в массовом соотношении 9:1 подвергают совместной механохимической активации в присутствии 0,7-0,9 мас. % (от массы растительного сырья) бикарбоната натрия на центробежных планетарных мельницах-активаторах непрерывного промышленного типа (например, ЦЭМ 7-80) или дискретного, лабораторного типа (АГО-2) при следующих условиях: частота вращения >1000 об/мин и ускорении мелющих тел g>30. Полученный ультрадисперсный порошок (размер частиц 20-60 нм) капсулируют в твердые желатиновые капсулы с дозировкой по 400±20 мг в одной капсуле для приема per os.
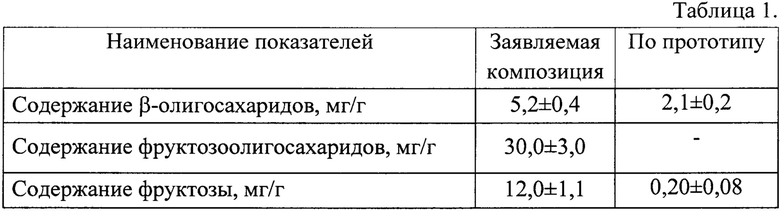
Полученная композиция характеризуется следующим составом основных активных веществ (табл. 1).
Подтверждение биологической активности
Показанием для назначения препарата был верифицированный диагноз «сахарный диабет 2-го типа» с метаболическими нарушениями на фоне таблетированной сахароснижающей терапии. Коррекции, предшествующей сахароснижающей терапии, не проводилось. При обследовании больных характерными инструментально-лабораторными критериями, свидетельствующими о метаболических нарушениях были: (1) гипергликемия (глюкоза венозной плазмы натощак > 6,1 ммоль/л, НвА1с>6,5%); (2) дислипидемия (OXC>4,5 ммоль/л, ЛПНП>2,6 ммоль/л, ЛПВП<1,0 ммоль/л (муж) ЛПВП<1,2 ммоль/л (жен), ТГ>1,7 ммоль/л); (3) артериальная гипертензия (АД>130/80 мм.рт.ст.); (4) избыточная масса тела и ожирение (ИМТ>25 кг/м2).
Программа исследования предусматривала комплексное лечение и обследование выборки из 150 пациентов: группа №1 (контроль) - 50 пациентов, получавших плацебо; группа №2 (сравнения) - 50 пациентов, получавших биопрепарат прототипа; группа №3 - 50 пациентов, получавших заявляемую композицию. Соответствующий препарат назначался дополнительно к стандартной таблетированной сахароснижающей терапии и принимался per os по 1 капсуле 3 раза в день, курс приема составлял 3 и 6 месяцев.
Клинико-лабораторный контроль для оценки эффективности заявляемой композиции, по сравнению с прототипом, проводили через 3 и 6 месяцев. Он включал: общее клинико-инструментальное обследование, биохимический и клинический анализы крови, определение содержания НвА1с (гликированного гемоглобина). У всех пациентов, участвовавших в исследовании, взято информированное согласие. Для обработки результатов использовались статистические пакеты - Stat Soft Statistica v.6.0, SPSS 9.0.
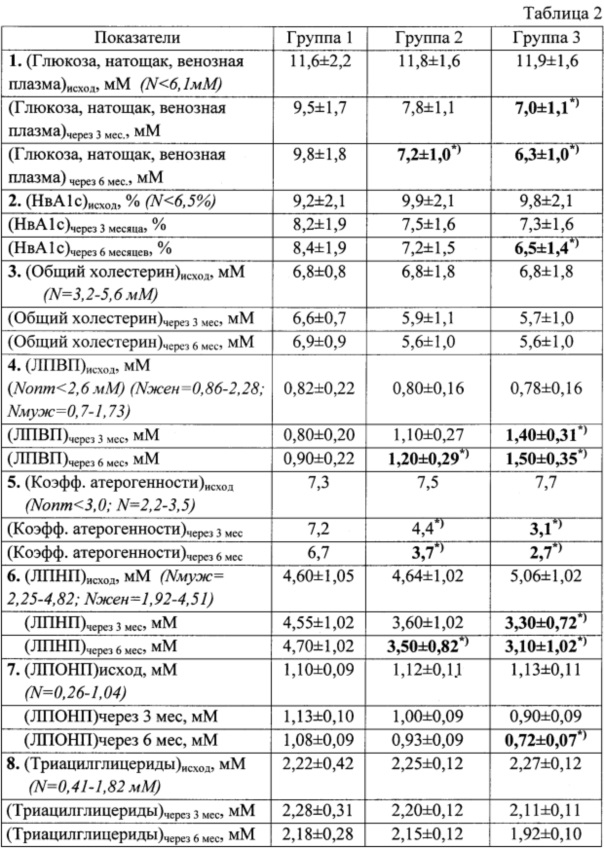
Динамическое наблюдение показало, что биопрепараты заявляемой композиции и прототипа, а также плацебо, больные переносили хорошо, нежелательных явлений, побочных эффектов не наблюдалось. Полученные результаты приведены в таблице 2.
*)р<0,05
Контроль уровня гликированного гемоглобина показал снижение уровня во всех группах исследования. Вместе с тем, статистически значимое снижение отмечено только в группе №3, принимавших препарат в течение 6 месяцев. Показатели глюкозы венозной крови натощак также демонстрировали статистически значимое снижение в группе №3 уже на 3 месяце исследования, а к 6-му месяцу в группах №№2 и 3. Некоторое улучшение показателей в группе сравнения, получавшей плацебо можно объяснить более частым самоконтролем пациентов, модификацией образа жизни. Выявлено значительное достоверное улучшение показателей липидного обмена в группе №2 и особенно в группе №3, которое выражалось в уменьшении коэффициента атерогенности прежде всего за счет повышения уровня липопротеидов высокой плотности (ЛПВП). Отмечено также снижение содержания липопротеидов низкой плотности (ЛПНП), а в группе №3 к 6 месяцу эксперимента и липопротеидов очень низкой плотности (ЛПОНП).
Контроль динамики артериального давления и индекса массы тела не выявил достоверно значимых изменений во всех трех группах за период исследования.
Таким образом, заявляемая композиция оказывает достоверно на 11-23% более значимый эффект в отношении коррекции углеводно-липидных метаболических нарушений при СД2, по сравнению с прототипом, проявляющийся в снижении уровня гликированного гемоглобина (HbA1c) и глюкозы в крови больных СД2, повышении коэффициента атерогенности за счет прежде всего увеличения содержания ЛПВП, а также в снижении уровня ЛПНП и ЛПОНП в режиме устойчивого терапевтического эффекта.
Литература
1. Muoio D.M., Newgard С.В. (2006) Obesity-related derangements in metabolic regulation. Annu Rev Biochem. 75, 367-401.
2. Ahren, B. (2005) Type 2 diabetes, insulin secretion and beta-cell mass. Curr Mol Med. 5, 275-286.
3. Шаройко В.В. Метаболические и сигнальные пути, контролирующие секрецию инсулина бета-клетками островков Лангерганса поджелудочной железы, и их роль в норме и при сахарном диабете. Диссертация на соискание ученой степени доктора биологических наук / Санкт-Петербургский государственный университет. Санкт-Петербург, 2011. - 340 с.
4. Аметов А.С. Современные методы терапии сахарного диабета 2-го типа // Регулярные выпуски «РМЖ». - №4. - 2008. - С. 170-177.
5. Свидетельство о государственной регистрации, санитарно-эпидемиологическое заключение и ТУ на БАД «Ягель» / Свидетельство ЕВРАЗЭС о гос. регистрации Роспотребнадзора РФ № RU.77.99.11.003.E.051236.11.11 от 17.11.2011.
6. Чуркина Е.В., Кершенгольц Б.М., Шаройко В.В. Эффект препарата «Ягель» из слоевищ лишайника рода Cladonia на секрецию инсулина // Дальневосточный медицинский журнал. - №2. - 2011. - С. 67-70.
7. Гольдерова А.С., Кривошапкина З.Н., Миронова Г.Е., Яковлева А.И., Олесова Л.Д., Кершенгольц Б.М. Влияние БАД «Ягель» на биохимические показатели крови // Якутский медицинский журнал. - 2010. - №4. С. 73-76.
8. Свидетельство о государственной регистрации, санитарно-эпидемиологическое заключение и ТУ на БАД «Ягель-Детокс» / Свидетельство ЕВРАЗЭС о гос. регистрации Роспотребнадзора РФ № RU.77.99.11.003.E.003704.05.13 от 20.05.2013.
9. Кершенгольц Б.М., Сыдыкова Л.А., Шаройко В.В. Лишайниковые β-олигосахариды в коррекции метаболических нарушений при сахарном диабете 2-го типа // Наука и образование. 2014. №2 (74). С. 81-86.
10. Kershengolts В.М., Sydykova L.A., Sharoyko V.V., Anshakova V.V., Stepanova A.V., Varfolomeeva N.A. Lichens' β-oligosaccharidesin thecorrection of metabolic-disordersin type2 diabetesmellitus // Wiadomosci Lekarskie. - Tom LXVIII, 2015, Nr 4  (1928). - P. 480-483.
(1928). - P. 480-483.
11. Аньшакова B.B., Степанова A.B., Уваров Д.М., Смагулова А.Ш., Наумова К.Н., Васильев П.П., Кершенгольц Б.М. Актопротекторная активность комплексного биопрепарата на основе таллома лишайников и родиолы розовой // Экология человека. - 2015. - №5. - С. 46-51.
12. K.N. Naumova, V.V. Anshakova, B.M. Kershengolts Nonspecific adaptive reactions of athletes: evaluation and correction // Journal of Biopharmaceuticals. - 2015. - №4. - P. 238-239.
13. Аньшакова В.В. Повышение активности действующего вещества лишайниковыми β-олигосахаридами // Биофармацевтический журнал. - 2012. - Т.4. №4. - С. 42-46.
14. Isaac Burney Yeo. Food in health and disease. London. 1901. 592 p. (P.425).
15. Аньшакова B.B., Каратаева E.B., Кершенгольц Б.М. Способ повышения качества хлебобулочных изделий и сохранения их свежести с помощью твердофазной пищевой добавки «ЯГЕЛЬ-Т» // Патент RU №2466542 С1 от 20.11.2012, приоритет от 15.04.2011.
16. S.Y. Hwang, D.J. Son, I.W. Kim et al. Korean red ginseng attenuates hypercholesterole-mia-enhanced platelet aggregation through suppression of diacylglycerol liberation in high-cholesterol-diet-fed rabbits // Phytotherapy Research, V.22, n.6, pp. 778-783, 2008.
17. Yibing Zhang, Jinli Shi, Yong Zhao, Haifeng Cui, Chunyu Cao, Sha Liu An investigation of the anti-diabetic effects of an extract from Cladonia humilis // Pak. J. Pharm. Sci., Vol. 25, No.3, July 2012, pp. 509-512.
18. Блинов B.A. Противодиабетический сбор «Детский». - патент RU 2131740 от 20.06.1999, приоритет от 03.06.1997.
19. Лосевская П.Я., Лосевской В.П. Патент RU 2238753 Сбор «Прасковья» и способ лечения сахарного диабета и заболеваний осложненных сахарным диабетом при фитопаротерапии, 27.10.2004, приоритет от 21.05.2003.
20. Насухова Н.М., Коновалов Д.А., Козлова В.В., Насухова A.M., Пшукова И.В. Патент RU 2611353. Композиция, обладающая антидиабетическим действием.
21. Шендеров, Б.А., Манвелова М.А. Функциональное питание и пробиотики: микроэкологические аспекты / [2-е изд., перераб.]. - М.: Агар, 1997. - 230 с.
22. Ладнова О.Л., Меркулова Е.Г. Применение инулина и стевии при разработке рецептур продуктов нового поколения, научный журнал «Успехи современного естествознания». - №2. - 2008. - С. 46-47.
23. Уваров Д.М., Сыдыкова Л.А., Аньшакова В.В., Соловьева М.И., Степанова А.В., Кершенгольц Б.М. Способ коррекции метаболических нарушений при сахарном диабете второго типа // Патент РФ 2613271, приоритет от 24.12.2015, зарегистрировано в реестре 15.03.2017.
| название | год | авторы | номер документа |
|---|---|---|---|
| Твердофазная композиция для коррекции метаболических нарушений при сахарном диабете второго типа | 2020 |
|
RU2747985C1 |
| Способ коррекции метаболических нарушений при сахарном диабете второго типа | 2015 |
|
RU2613271C1 |
| Твердофазная композиция, обладающая антибактериальным и детоксикационным действием | 2017 |
|
RU2657782C1 |
| Жидкофазная композиция, обладающая антибактериальным и детоксикационным действием | 2017 |
|
RU2652347C1 |
| Твердофазная композиция, обладающая актопротекторным, адаптогенным и детоксикационным действием | 2017 |
|
RU2661623C1 |
| СПОСОБ ПРОФИЛАКТИКИ И КУПИРОВАНИЯ ПОХМЕЛЬЯ С ПОМОЩЬЮ ПИТЬЕВОЙ ВОДЫ | 2015 |
|
RU2608657C2 |
| Композиция на основе бетулина и слоевищ лишайников, обладающая антибактериальным, противовирусным и детоксикационным действием | 2019 |
|
RU2710236C1 |
| Жидкофазная композиция с повышенным содержанием природных устойчивых к окислению омега-3 полинепредельных жирных кислот | 2017 |
|
RU2662316C1 |
| Способ и состав для производства водки | 2020 |
|
RU2745450C1 |
| Способ консервирования молока и жидких молочных продуктов | 2017 |
|
RU2662982C1 |
Изобретение относится к фармацевтической промышленности, а именно к твердофазной композиции, обладающей свойством коррекции метаболических нарушений при сахарном диабете второго типа. Твердофазная композиция, обладающая свойством коррекции метаболических нарушений при сахарном диабете второго типа, представляет собой ультрадисперсный порошок механохимически активированной в присутствии 0,7-0,9 мас. % от массы растительного сырья бикарбоната натрия смеси слоевищ лишайников рода Cladonia и клубней топинамбура (Helidnthus tuberosus) в массовом соотношении 9:1, которая содержит лишайниковые β-олигосахариды, фруктозоолигосахариды, фруктозу в определенной концентрации. Вышеописанная композиция эффективно корректирует метаболические нарушения при сахарном диабете второго типа. 2 табл.
Твердофазная композиция, обладающая свойством коррекции метаболических нарушений при сахарном диабете второго типа, представляющая собой ультрадисперсный порошок механохимически активированной в присутствии 0,7-0,9 мас. % от массы растительного сырья бикарбоната натрия смеси слоевищ лишайников рода Cladonia и клубней топинамбура (Helidnthus tuberosus) в массовом соотношении 9:1 и характеризующаяся тем, что содержит лишайниковые β-олигосахариды в концентрации 5,2±0,4 мг/г, фруктозоолигосахариды - 30,0±3,0 мг/г, фруктозу - 12,0±1,1 мг/г.
| Способ коррекции метаболических нарушений при сахарном диабете второго типа | 2015 |
|
RU2613271C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОАКТИВНОГО ТВЕРДОФАЗНОГО БИОПРЕПАРАТА АНТИБИОТИЧЕСКОГО ДЕЙСТВИЯ ЯГЕЛЬ ИЗ СЛОЕВИЩ ЛИШАЙНИКОВ | 2011 |
|
RU2467063C1 |
| ЧУРКИНА Е.В и др | |||
| Эффект препарата "Ягель" из слоевищ лишайника рода Cladonia на секрецию инулина //Дальневосточный медицинский журнал, 2010, стр.67-70. | |||
Авторы
Даты
2018-07-17—Публикация
2017-08-28—Подача