Изобретение относится к фармацевтической промышленности и может быть использовано в качестве средства для лечения заболеваний верхних дыхательных путей.
Бронхиальная астма - хроническое, воспалительное заболевание верхних дыхательных путей. Главное проявление бронхиальной астмы -обратимая (самостоятельно или после воздействия лекарственных препаратов) обструкция бронхов, проявляющаяся удушьем.
Распространенность аллергической бронхиальной астмы - около 6%. Большую тревогу вызывает огромное число не выявленных форм заболевания. Как правило, это легкие формы бронхиальной астмы, которые могут прятаться под диагнозами «обструктивный бронхит» или просто «хронический бронхит». Заболеваемость среди детей еще выше и в некоторых регионах достигает 20%. Среди детей, число пациентов с не выставленным диагнозом - еще выше.
В основе развития аллергической бронхиальной астмы лежит патогенетический механизм гиперчувствительности немедленного типа (IgE-зависимый иммунный ответ). Один из самых частых механизмов развития аллергических заболеваний. Для него характерно то, что от момента поступления аллергена до развития симптомов заболевания проходят считанные минуты. Безусловно, это относиться только к тем, у кого уже есть сенсибилизация (аллергическая настроенность) к данному веществу.
Атопическая бронхиальная астма - аллергическое заболевание, в обострении которого ведущую роль играет контакт с аллергенами. Чаще всего, заболевание вызывают аллергены, поступающие ингаляционным путем: бытовые (различные разновидности клещей домашней пыли, домашняя пыль, библиотечная пыль, перо подушек), пыльцевые, эпидермальные (шерсть и перхоть животных, перья птиц, корм для рыб и т.д.), грибковые.
Характерным симптомом бронхиальной астмы является хороший эффект от приема антигистаминных препаратов (цетрин, зиртек, эриус и т.д.) и особенно после ингаляции бронхорасширяющих препаратов (сальбутамол, беродуал и т.д.).
Эффективных мер первичной профилактики, то есть направленных на предотвращение заболевания, к сожалению, не разработано. При уже существующей проблеме необходимо адекватное лечение и устранение аллергенов, что позволяет стабилизировать течение заболевания.
При лечении бронхиальной астмы используют ингаляции. Растворы для ингаляций при бронхиальной астме следующие.
Альбутерол (2,5 мг/мл) или метапротеренол (50 мг/мл) выпускают в растворе для ингаляций; 0,25-0,5 мл одного из них растворяют в 3 мл физиологического раствора.
При бронхиальной астме ингаляцию проводят с помощью специальных ингаляторов в течение 5-15 мин. Обычно минимальный интервал между ингаляциями - не менее 4 ч. В начале приступа это лечение проводят более активно.
Для профилактики частых приступов бронхиальной астмы применяют беклометазон, триамцинолон или флунизолид в виде дозированных аэрозолей. Они уменьшают или полностью устраняют потребность в системном назначении стероидов. Обычная разовая доза - 2 вдоха 4 раза в сутки (флунизолид - 2 раза в сутки) через 5-10 мин после ингаляции бронходилататора. Для уменьшения риска кандидоза после ингаляции полость рта и глотку необходимо прополоскать водой. Некоторые больные нуждаются в больших дозах препаратов (в 4 раза превышающих начальную дозу).
Ингаляционные формы кортикостероидов не дают серьезных системных побочных эффектов.
Известны составы ингаляционных растворов эфирных масел в спирте этиловом 70%-ном, а также состав, содержащий мятное масло 0,71 г, настойку эвкалипта 35,7 г, глицерин 35,7 г, спирт этиловый 96%-ный - до 100 мл, предназначенные для лечения заболеваний носа, гортани, легких, бронхов и астматических состояний [Применение эфирных масел для ингаляций. https://medn.ru/statyi/Primenenieefirnvxmaseldlv.htmll.
Недостаток этих составов заключается в низкой эффективности при лечении аллергических симптомов и хронических патологий верхних дыхательных путей. Кроме того, активные вещества, содержащиеся в этих препаратах, не действуют на основные патогенетические механизмы заболеваний.
Наиболее близким к предложенной ингаляционной форме является ингаляционный аэрозоль Бекотид®, состав которого включает действующее вещество беклометазона дипропионат и вспомогательные вещества глицерин, этанол и пропеллент норфлуран [Энциклопедия РЛС https://www.rlsnet.ru/tn_index_id_506.htm].
Недостатком известной ингаляционной формы является развитие серьезных осложнений гормонального характера и выраженная устойчивость, которая развивается при продолжительном приеме препарата.
Техническая проблема, решаемая изобретением, заключается в расширении арсенала ингаляционных лекарственных средств для лечения заболеваний верхних дыхательных путей.
Технический результат изобретения заключается в создании ингаляционной лекарственной формы дииндолилметана, который воздействует на большинство патогенетических звеньев заболеваний верхних дыхательных путей.
Технический результат достигается ингаляционным препаратом для лечения заболеваний верхних дыхательных путей, включающим действующее вещество, этанол и глицерин, который характеризуется тем, что в качестве действующего вещества включает 3,3'-дииндолилметан, который содержится в количестве 0,85-17,0 мг/мл, а этанол и глицерин в массовом соотношении 2:1 - остальное до 1 мл.
3,3'-Дииндолилметан (ДИМ), соединение растительного происхождения, обладающее широким спектром биологической активности. На основе ДИМ разработаны лекарственные средства перорального применения для лечения воспалительных заболеваний вирусного генеза и предраковых патологий человека. Дииндолилметан обладает ингибирующей активностью в отношении гистондеацетилазы, то есть его с полным основанием можно отнести к веществам с эпигенетической активностью. При воздействии на клетки ДИМ может восстанавливать активную экспрессию генов, замолчавших в результате изменений в конформации хроматина. Он также снижает содержание ДНК метилтранфераз и меняет спектр синтеза микроРНК, что приводит к восстановлению измененной генетической программы клеток-мишеней [Carmen P. Wong, AnnaHsu, AlexBuchanan, Zoraya Palomera-Sanchez, Laura M. Beaver, E. Andres Houseman, David E. Williams, Roderick H. Dashwood, Emily Ho. Effects of Sulforaphane and 3,3'-Diindolylmethane on Genome-Wide Promoter Methylation in Normal Prostate Epithelial Cells and Prostate Cancer Cells. PLOS ONE 2014, 9(1), e86787; Yiwei Li, Dejuan Kong, Zhiwei Wang, Fazlul H. Sarkar. Regulation of microRNAs by Natural Agents: An Emerging Field in Chemoprevention and Chemotherapy Research. Pharm Res 2010, 27:1027-1041; Yongming Li, Xia Li, Bin Guo. Chemopreventive Agent 3,3'-Diindolylmethane Selectively Induces Proteasomal Degradation of Class I Histone Deacetylases. Cancer Res 2010; 70(2):646-654; Han Jin Cho, Mi Ra Seon, Yeo Myeong Lee, Jaebong Kim, Jin-Kyung Kim, Sang Geon Kim, Jung Han Yoon Park. 3,3'-Diindolylmethane Suppresses the Inflammatory Response to Lipopolysaccharidein Murine Macrophages. J. Biochemical, Molecular, and Genetic Mechanisms 2007, 12: 17-23].
Другое важное свойство ДИМ - это его ингибирующая активность в отношении ядерного фактора транскрипции - ведущего драйвера воспалительных реакций, ответственного за транскрипцию многих генов, вовлеченных в воспалительную реакцию [KM. Wahidur Rahman, Fazlul HSarkar. Inhibition of Nuclear Translocation of Nuclear Factor - KB Contributes to 3,3'-Diindolylmethane-Induced Apoptosis in Breast Cancer Cells. Cancer Res 2005; 65(1): 364-371].
ДИМ является природным агонистом арилкарбоновых рецепторов, которые вовлечены в формирование приобретенного иммунитета и в развитие аллергических и воспалительных реакций. [Gabrielle N. Winston-McPherson, Dongxu Shu, Weiping Tang. Synthesis and Biological Evaluation of 2,3'-Diindolylmethanes as Agonists of Aryl Hydrocarbon Receptor. Bioorg Med Chem Lett. 2014, 24(16): 4023-4025; Ichen Chen, Andrew McDougal, Fan Wang, Stephen Safe. Aryl hydrocarbon receptor-mediated antiestrogenic and antitumorigenic activity of diindolylmethane. Carcinogenesis 1998, 19 (9): 1631-1639; Nancy I. Kerkvliet. AHR-Mediated Immunomodulation: The Role of Altered Gene Transcription. BiochemPharmacol. 2009, 15/77(4): 746-760].
Для ДИМ также описана удивительная способность снижать аутоиммунную агрессию, влияя на дифференцировку Т-лимфоцитов [Michael Rouse, Roshni Rao, Mitzi Nagarkatti, Prakash S. Nagarkatti. 3,3'-Diindolylmethane Ameliorates Experimental Autoimmune Encephalomyelitis by Promoting Cell Cycle Arrest and Apoptosis in Activated T Cells through MicroRNA Signaling Pathways. J Pharmacol Exp Ther 2014, 350:341-352] и подавлять аллергические реакции [Peter Ettmayer, Peter Mayer, Frank Kalthojf, Wolfgang Neruda, Nathalie Harrer, Gabriella Hartmann, Michelle M. Epstein, Volker Brinkmann, Christoph Heusser, Maximilian Woisetschlager. A Novel Low Molecular Weight Inhibitor of Dendritic Cells and В Cells Blocks Allergic Inflammation. Am J Respir Crit Care Med 2006, 173:599-606]. [Zhi Chen, Arian Laurence, John J. О'Shea. Signal transduction pathways and transcriptional regulation in the control of Thl7 differentiation. Seminlmmunol. 2007, 19(6): 400-408]. Таким образом, ДИМ представляет собой весьма перспективную молекулу для терапии и профилактики аллергической астмы. Большим недостатком ДИМ с точки зрения разработки лекарственных средств является его низкая биодоступность. В литературе описаны различные подходы к решению данной проблемы [RU 2409363 С1, опубл. 20.01.2011; RU 2419426 С1, опубл. 27.05.2011].
Особо следует отметить, что обострение приступов бронхиальной астмы часто происходит на фоне гриппозной инфекции. Острая воспалительная реакция, которая сопровождает инфекционный процесс, обусловлена активацией синтеза провоспалительных цитокинов, которые и провоцируют обострение бронхиальной астмы. Эффективность ДИМ при лечении гриппозной инфекции продемонстрирована в патенте RU 2537025. Как показали исследования, ДИМ в биодоступной форме существенно снижает смертность экспериментальных животных, инфицированных вирусом гриппа. Однако в клинических исследованиях было показано, что для достижения значимого лечебного эффекта необходимо принимать довольно большие дозы препарата. Из этих наблюдений можно предположить, что прием препарата на основе ДИМ в ингаляционной форме может быть более эффективным.
Другая патология, в которой за последние годы не наблюдается существенный прогресс в создании эффективных лекарственных средств, это респираторный папилломатоз гортани.
Рецидивирующий респираторный папилломатоз (РРП) - наиболее часто встречающаяся доброкачественная опухоль дыхательных путей в детском возрасте. Установлено, что этиологическим фактором заболевания является вирус папилломы человека (ВПЧ). Идентифицировано более 100 типов ВПЧ; в биопсийном материале у подавляющего большинства больных РРП определяются два генотипа вируса - ВПЧ-6 и ВПЧ-11 типа. Отечественная статистика не располагает достоверными сведениями о распространенности РРП среди детского и взрослого населения, однако известно, что в США отмечается 4,3 новых случая папилломатоза гортани на 100000 детского населения в год, причем 75% больных составляют дети первых 5 лет жизни.
На основании экспериментальных и клинических данных удалось показать, что индольные соединения являются перспективными молекулами, обладающие высокой избирательной ингибирующей активностью в отношении эпителиальных клеток, инфицированных вирусами папилломы человека. Очевидным недостатком такой терапии является невозможность создания необходимых концентраций активного вещества в патологических очагах, что обусловлено низкой биодоступностью индол-3-карбинола при пероральном приеме и непредсказуемостью его превращения в желудке в дииндолилметан.
Таким образом, как и в случае с бронхиальной астмой, так и в случае респираторного папилломатоза, необходима новая ингаляционная лекарственная форма дииндолилметана, которая, по нашему мнению, должна будет решить эту проблему [Nkechi Ichite, Mahavir Chougule, Apurva R. Patel, Tanise Jackson, Stephen Safe, MandipSingh. Inhalation Delivery of a Novel Diindolylmethane Derivative for the Treatment of Lung Cancer. MolCancerTher. 2010, 9(11): 3003-3014].
В связи с изложенным, предметом настоящего изобретения явилась разработка ингаляционной жидкой формы дииндолилметана и ее клиническая апробация у больных с аллергической бронхиальной астмой и рецидивирующим респираторным паппиломатозом.
Очевидно, что местное применение препаратов на основе ДИМ позволяет достичь максимальной биодоступности и, следовательно, максимального терапевтического эффекта. Это подтверждается проведенными клиническими исследованиями при лечении дисплазий шейки матки, ассоциированных с вирусами папилломы человека [Levon Ashrafian, Gennady Sukhikh, Vsevolod Kiselev, Mikhail Paltsev, Vadim Drukh, Igor Kuznetsov, Ekaterina Muyzhnek, Inna Apolikhina, Evgeniya Andrianova. Double-blind randomized placebocontrolled multicenter clinical trial (phase IIa) on diindolylmethane's efficacy and safety in the treatment of СЕЧ: implications for cervical cancer prevention. The EPMA Journal (2015) 6:25].
Известна попытка лечения респираторного папилломатоза пероральным назначением препаратов на основе дииндолилметана [Zeligs М.А. US 7,348,352 В2 Diindolylmethane for the treatment of HPV infection]. Эти исследования доказали свою обоснованность, однако не позволяли достичь выраженного клинического эффекта. Представленные ниже результаты клинических исследований убедительно свидетельствуют, что разработанное лекарственное средство в виде ингаляций на основе дииндолилметана имеет высокую терапевтическую эффективность при лечении гриппозной инфекции, бронхиальной астмы и рецидивирующего папилломатоза гортани.
Изобретение поясняется графическими материалами.
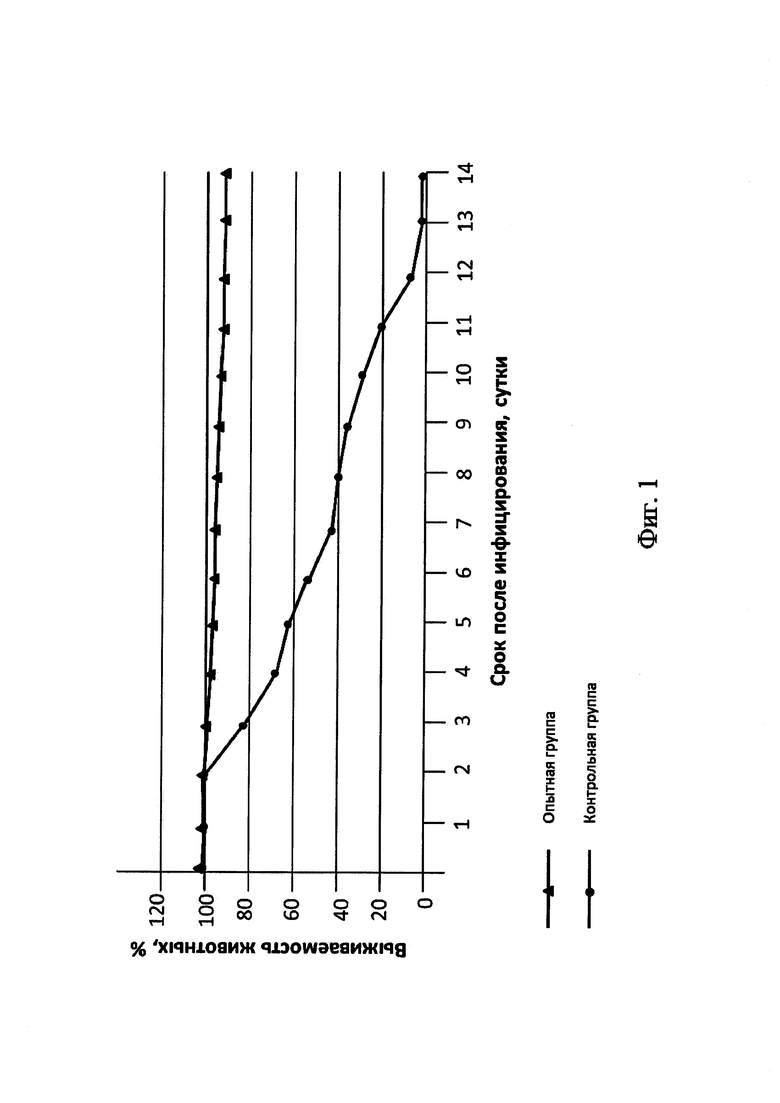
На фиг. 1 показано протективное действие предложенного ингаляционного препарата при летальной гриппозной пневмонии у белых мышей. Доза вируса 10 LD50.
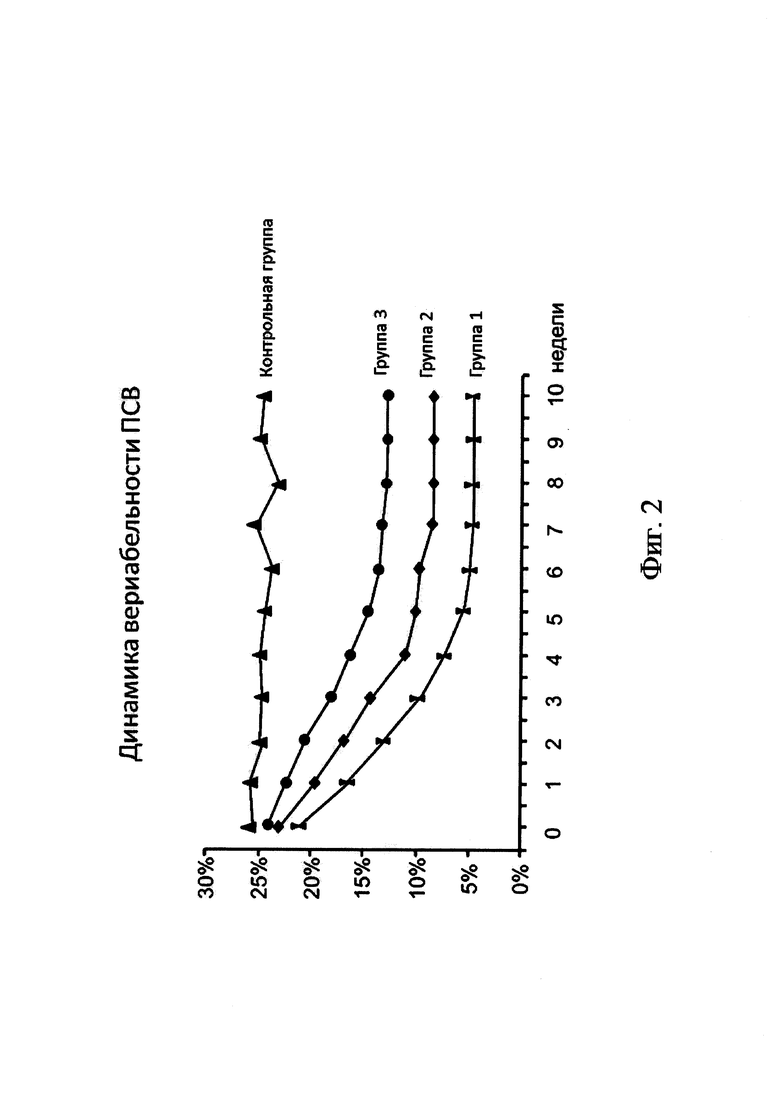
На фиг. 2 представлена динамика клинической симптоматики у больных бронхиальной астмой при лечении предложенным ингаляционным препаратом.
Пример 1
Рецептура для ингаляционного введения ДИМ.
Лекарственный препарат для ингаляционного введения готовился на основе раствора активного вещества 3,3'-дииндолилметана (ДИМ) в смеси этанола и глицерина. Данный раствор готовился по следующей рецептуре.
Смешивали 36 г этанола и 18 г глицерина. В этой смеси растворяли 1,0 г ДИМ. В одном впрыске/одной дозе (170 мкл) такого раствора содержится 2,5 мг ДИМ. Вторая и третья дозировки готовились путем растворения соответственно 0,35 г и 0,05 г ДИМ в таком же объеме смеси этанола и глицерина при других их соотношениях в смеси.
С учетом значений плотностей спирта и глицерина были рассчитаны концентрации ДИМ в исходной (первой), а также последующих второй и третьей дозировках в размерности % w/v (weight/volume), то есть количество граммов вещества (ДИМ) в 100 мл раствора, а также в размерности мг/мл. Данные величины составили:

Пример 2
Исследование терапевтической эффективности ингаляционного препарата на модели летальной гриппозной инфекции.
Протективное действие разработанного препарата исследовалось при летальной гриппозной пневмонии у белых мышей. Доза вируса 10 LD50.
При анализе динамики показателей патологического процесса в условиях применения разработанного препарата было показано, что он также влияет на продление срока жизни животных и снижению специфической смертности в группах. Так, ингаляционное введение максимальной дозы разработанного препарата приводит к 100%-ной защите животных от летальной гриппозной пневмонии.
Формуляцию ДИМ в концентрации 2 мг/мл использовали для приготовления аэрозоля путем распыления с помощью струйного небулайзера PARILCSTAR, используя сухой сжатый воздух (скорость потока 4 л/мин).
Самки мышей (20±2 г) были обездвижены в клетках с помощью специальных держателей и помещены в аэрозольную камеру так, чтобы с аэрозольным облаком контактировал только нос каждой мыши. Небулайзер был соединен с верхней частью ингаляционной камеры, из которой образуемый аэрозоль поступал к животным. Продолжительность контакта аэрозоля с животными составляла 10 минут.
На 2-й день после введения соответствующей дозы вируса гриппа животные 2-раза в день получали аэрозоль в течение всего срока наблюдений (14 дней). Для наглядности протективное действие препарата при наибольшей из использованных доз вируса (10 LD50) представлено на фиг. 1. Как следует из графика, летальность в опытной группе мышей была существенно меньше, по сравнению с контрольной группой, получавших аэрозоль в виде физиологического раствора.
Пример 3
Изучение терапевтической эффективности разработанного лекарственного средства у больных с бронхиальной астмой.
Для исследования были отобраны три группы пациентов (по 10 в каждой группе) в возрасте 10-30 лет с диагнозом Бронхиальная астма, персистирующее течение легкой или средней тяжести. Критериями включения были: персистирующие симптомы астмы, от 1 раза в неделю до 1 раза в день, ночные пробуждения от симптомов астмы. Вариабельность показателей ПСВ (пиковая скорость выдоха) в диапазоне 20-30%. У всех пациентов, включенных в исследование, отмечались симптомы бронхиальной астмы к дерматофагоидному клещу (40%), пыльце растений (50%) и со смешанной сенсибилизацией (10%).
Пациентам назначали препарат в виде ингаляций два раза в день в течение 10 недель. Пациенты 1-й группы получали препарат в дозе 3 мг за одну ингаляцию, 2-я группа - 1 мг и 3-я группа - 0,2 мг. В течение этого времени проводили оценку симптомов болезни и оценивали динамику вариабельности ПСВ. Контрольной группе пациентов проводили стандартную терапию.
Во всех исследуемых группах наблюдалось улучшение клинической симптоматики. Измерение ПСВ показало, что максимальное улучшение показателей наблюдалось в группах 1 и 2 (фиг. 2)
Во всех исследуемых группах пациентов уже через 3 недели наблюдалась тенденция к нормализации параметров содержания эозинофилов в мокроте и существенное снижение концентрации иммуноглобулинов Е, что свидетельствовало о выраженном противоаллергическом действии назначаемого препарата.
Пример 4
Исследование эффективности препарата у больных с диагнозом рецидивирующий папилломатоз гортани.
Препарат назначали в виде двух ингаляций (утром и вечером) в дозировке номер 3 (0,05 г ДИМ + 36 г этанола + 18 г глицерина). Длительность лечения составляла не менее 12 недель. Терапию начинали после очередного удаления папиллом.
Анализировали длительность межрецидивного периода до и после назначения препарата. Эффективность лечения оценивали по увеличению межрецидивного периода (увеличение временного интервала между операциями по удалению папиллом в 1,5 раза и более от исходного);
Результаты: Выраженный положительный эффект противорецидивной терапии препаратом получен у 78,2% больных. Ни в одном случае не наблюдали каких-либо побочных эффектов от проводимой терапии.
В зависимости от клинической формы РРП, положительный эффект противорецидивной терапии отмечен: у 14 из 16 детей с локализованной формой и у 19 из 23 - с распространенной формой.
Разработанное лекарственное средство может применяться в виде ингаляций для лечения заболеваний верхних дыхательных путей, в частности бронхиальной астмы, гриппозной инфекции и респираторного папилломатоза гортани в течение всего периода заболевания до достижения устойчивого терапевтического эффекта.
Изобретение относится к фармацевтической промышленности и может быть использовано в качестве средства для лечения заболеваний верхних дыхательных путей. Ингаляционный препарат для лечения заболеваний верхних дыхательных путей содержит действующее вещество, этанол и глицерин, в качестве действующего вещества препарат включает 3,3'-дииндолилметан в количестве 0,85-17,0 мг/мл, этанол и глицерин в массовом соотношении 2:1 - остальное до 1 мл. Разработанное лекарственное средство может применяться в виде ингаляций для лечения заболеваний верхних дыхательных путей, в частности бронхиальной астмы, гриппозной инфекции и респираторного папилломатоза гортани в течение всего периода заболевания до достижения устойчивого терапевтического эффекта. 4 пр., 2 ил.
Ингаляционный препарат для лечения заболеваний верхних дыхательных путей, включающий действующее вещество, этанол и глицерин, отличающийся тем, что в качестве действующего вещества включает 3,3'-дииндолилметан, который содержится в количестве 0,85-17,0 мг/мл, а этанол и глицерин в массовом соотношении 2:1 - остальное до 1 мл.
| Qian X | |||
| et al | |||
| Chemoprevention of lung tumorigenesis by intranasally administered diindolylmethane in A/J mice / Cancirogenesis, 34 (4), 841-849, 2013 | |||
| МАКСИМАЛЬНЫЙ ТЕПЛОВОЙ РАСЦЕПИТЕЛЬ ТОКА | 2009 |
|
RU2464665C2 |
| Ichite N | |||
| et al | |||
| Inhalation delivery of a novel diindolylmethane derivative for the treatment of lung cancer/ Mol Cancer Ther, 9 (11), 3003-3014, 2010 | |||
| US 8580843 B2, 12.11.2013 | |||
| RU 2013124416 A, 10.12.2014. | |||
Авторы
Даты
2018-09-05—Публикация
2017-08-18—Подача