Изобретение относится к способам получения продуктов для регенерации воздуха на основе надпероксида калия, используемых для защиты органов дыхания человека от поражающих факторов химической и биологической природы в индивидуальных дыхательных аппаратах (ИДА).
Известен способ получения продукта для регенерации воздуха [патент РФ №2596770 МПК A62D 9/00, 2016 г.], осуществляемый следующим образом. В раствор пероксида водорода с концентрацией от 50 до 85% массовых при интенсивном перемешивании вводят сульфат магния. После его полного растворения (примерно 1-3 минуты) в жидкую фазу вводят тетрабораты щелочных металлов, в качестве которых используют тетрабораты лития, натрия, калия или их смесь, затем гидроксид лития и гидроксид калия. Гидроксид калия вводят в систему через 10÷15 минут после введения гидроксида лития. Мольное соотношение исходных компонентов должно составлять следующие величины: пероксид водорода/сульфат магния (H2O2/MgSO4)=450÷800; пероксид водорода/тетраборат щелочного металла (H2O2/Me2B4O7)=400÷700; пероксид водорода/гидроксид лития (H2O2/LiOH)=3,0÷15,0; пероксид водорода/гидроксид калия (Н2О2/КОН)=1,60÷2,00. Для снижения кинетики процесса распада пероксида водорода добавление гидроксидов лития и калия проводят таким образом, чтобы температура жидкой фазы тройной системы МеОН - H2O2 - H2O (щелочной раствор пероксида водорода) не превышала 25°С. Полученный щелочной раствор пероксида водорода диспергируют форсункой в сушильную камеру в прямотоке сушильного агента, где происходит его дегидратация. Используется типовая сушильная камера с форсункой. В качестве сушильного агента используют воздух или любой инертный газ, например азот. Температуру сушильного агента варьируют в пределах от 120 до 300°С (предпочтительно 180÷220°С). По окончании дегидратации твердый продукт отделяют от газовой смеси с помощью обычного батарейного циклона и рукавного фильтра и собирают в специальный контейнер. Далее полученный продукт формуют различными способами для придания определенной геометрической формы (гранулы, блоки, таблетки и др.).
Однако продукт для регенерации воздуха, полученный известным способом, характеризуется недостаточно высокой степенью отработки по диоксиду углерода, что приводит к увеличению массогабаритных параметров индивидуальных дыхательных аппаратов. Последнее крайне неудобно при эксплуатации ИДА пользователями, вынужденными в силу специфики условий труда постоянно носить их (например, шахтеры). Кроме того, данный способ недостаточно экономичен и безопасен.
Задачей изобретения является разработка способа получения продукта для регенерации воздуха, имеющего улучшенные эксплуатационные характеристик при его работе в составе индивидуальных дыхательных аппаратов.
Технический результат заключается в получении продукта для регенерации воздуха, имеющего высокую степень отработки по диоксиду углерода при его эксплуатации в индивидуальных дыхательных аппаратах, обеспечивающую снижение массогабаритных параметров изделия.
Дополнительным техническим результатом является повышение экономичности и безопасности процесса.
Технический результат достигается тем, что в способе получения продукта для регенерации воздуха путем смешения раствора пероксида водорода с сульфатом магния и гидроксидами лития и калия с последующей дегидратацией полученного щелочного раствора пероксида водорода распылением его в токе сушильного агента, в раствор пероксида водорода после его смешения с сульфатом магния вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота (H2O2/Н3ВО3)=285÷800.
При этом гидроксиды лития и калия вводят в жидкую фазу одновременно двумя порциями с интервалом 7-10 минут таким образом, чтобы температура в зоне синтеза не превышала 40°С.
Изобретение позволяет достигнуть заявленный технический результат по следующим обстоятельствам. Как хорошо известно специалистам, работающим в технике процессов хемосорбции, поглощение из газообразной фазы сорбата (CO2) происходит в тонком слое жидкой фазы, образующейся на поверхности хемосорбентов. Часто лимитирующей стадией процессов хемосорбции является внутренняя диффузия молекул сорбата в объем жидкой фазы и образование в ней ионизированных молекул, вступающих в химические реакции. При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3-, поскольку ортобораты практически полностью гидролизуются вследствие слишком малой константы образования [В(ОН)4]-. В растворе образуются тетрабораты, метабораты и соли других полиборных кислот (nB2O2⋅mH2O), не существующие в свободном состоянии (и которые по этой причине невозможно ввести в жидкую фазу в виде исходных соединений), что хорошо известно из курса неорганической химии [Карапетьянц М.X. Дракин С.И. Общая и неорганическая химия. М.: Химия 1994]. Присутствие в жидкой фазе в указанном количестве солей щелочных металлов полиборных кислот приводит к снижению вязкости поверхностной пленки водного раствора, образующейся на поверхности продукта для регенерации воздуха, что приводит к усилению диффузионных процессов на границах раздела фаз, в жидкой фазе и повышению растворимости и ионизации диоксида углерода в водном растворе поверхностной пленки. В результате за счет интенсификации массообменных процессов на границах газ - жидкость и жидкость - твердая фаза повышается степень отработки продукта для регенерации воздуха по диоксиду углерода.
Необходимо отметить, что взаимодействие пероксида водорода и гидроксидов щелочных металлов при нормальных условиях - ярко выраженный экзотермический процесс, сопровождающийся каталитическим разложением пероксидных продуктов под воздействием гидроксид - анионов [У. Шамб, Ч. Сеттерфилд, Р. Вентворс. Перекись водорода, - М.: Иностранная литература, - 1958. - 578 с.] и выделением атомарного кислорода. Это не только приводит к снижению содержания пероксидных соединений в продукте синтеза, но и создает дополнительную угрозу возникновения «кислородного» пожара, локализовать который практически невозможно. Поэтому следует отметить, что полученный щелочной раствор пероксида водорода при температуре 40°С за 8 часов (продолжительность технологического цикла) теряет не более 0,28% активного кислорода, т.е. меньше, чем щелочной раствор пероксида водорода, приготовленный с использованием технологических приемов и соотношения компонентов, описанных в патенте РФ №2596770, где щелочной раствор пероксида водорода при температуре 25°С за 8 часов (продолжительность технологического цикла) теряет 0,35% активного кислорода. Таким образом, здесь абсолютно уместно говорить об увеличении стабилизирующего влияния присутствующих в щелочном растворе пероксида водорода ионов на химическую устойчивость жидкой фазы тройной системы МеОН-H2O2-H2O и повышении безопасности процесса получения продукта для регенерации воздуха. Механизм стабилизации различных растворов пероксида водорода неизвестен [Г.А. Серышев. Химия и технология перекиси водорода, - Л.: Химия, -1984. - С. 182.]. Поэтому сложно однозначно оценить влияние того или иного иона или их ассоциатов, содержащихся в многокомпонентном растворе, на стабильность системы в целом. Нахождение стабилизатора для конкретной цели - задача, которая решается только эмпирическим путем. Но было отмечено, что в раствор пероксида водорода в первую очередь следует вводить сульфат магния, а после его растворения вводить в полученный раствор ортоборную кислоту, а гидроксиды щелочных металлов следует вводить двумя порциями с интервалом 7-10 минут.
Кроме того, использование ортоборной кислоты позволяет ускорить процесс приготовления щелочного раствора пероксида водорода и осуществлять его приготовление и хранение в течение производственного цикла при более низкой температуре, что положительно отражается на экономичности способа получения продукта для регенерации воздуха.
Способ получения продукта для регенерации воздуха осуществляют следующим образом. В раствор пероксида водорода с концентрацией от 50 до 85% массовых при интенсивном перемешивании вводят сульфат магния. После его полного растворения (примерно 1-3 минуты) в жидкую фазу вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота (H2O2/H3BO3)=285÷800, гидроксид лития и гидроксид калия. Гидроксиды лития и калия вводят в систему одновременно двумя порциями с интервалом 7÷10 минут таким образом, чтобы температура в зоне реакции не превышала 40°С. Такой режим позволяет максимально нивелировать влияние температурного фактора на разложение пероксидных продуктов. Полученный щелочной раствор пероксида водорода диспергируют форсункой в сушильную камеру в прямотоке предварительно декарбонизированного сушильного агента, где происходит его дегидратация. Используется типовая сушильная камера с форсункой. В качестве сушильного агента используют воздух или любой инертный газ, например азот. Декарбонизация сушильного агента проводится с помощью любого поглотителя диоксида углерода. Для уменьшения расхода сушильного агента его предварительно можно обезвоживать, пропуская через регенерируемые поглотители воды типа цеолита, силикате ля и др. Температуру сушильного агента варьируют в пределах от 120 до 300°С (предпочтительно 180÷220°С). По окончании дегидратации твердый продукт отделяют от газовой смеси с помощью обычного батарейного циклона и рукавного фильтра и собирают в специальный контейнер. Далее полученный продукт формуют различными способами для придания определенной геометрической формы (гранулы, блоки, таблетки и др.) и размещают в патроне ИДА.
В примерах 1-5 приведены данные о получении заявляемым способом продукта для регенерации воздуха.
Пример 1.
К 56,82 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 150 г сульфата магния (H2O2/MgSO4=800). После растворения MgSO4 примерно через 1 минуту в жидкую фазу вводят 77,5 г ортоборной кислоты (H2O2/H3BO3=800), затем одновременно 0,8 кг гидроксида лития и 3,1 кг твердого 90% гидроксида калия. Примерно через 7 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 7,2 кг гидроксида лития (H2O2/LiOH=3) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=2,0). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 40°С. После этого раствор диспергируют через форсунку в сушильную камеру, в которую подают декарбонизованный осушенный воздух, нагретый до температуры 220°С. Расход раствора через форсунку составляет 155 мл/мин. Расход сушильного агента 970 кг/час. Получают 39,8 кг продукта, содержащего 67,9% KO2, 7,5% КОН, 15,5% Li2O2, 3,8% LiOH, 4,3% H2O, 0,65% полиборатов лития и калия и 0,35% MgSO4.
Пример 2.
К 51,7 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 210 г сульфата магния (H2O2/MgSO4=520). После растворения MgSO4 примерно через 1,5 минуты в жидкую фазу вводят 94,0 г ортоборной кислоты (H2O2/H3BO3=600), затем одновременно 0,44 кг гидроксида лития и 3,1 кг твердого 90% гидроксида калия. Примерно через 8 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 3,93 кг гидроксида лития (H2O2/LiOH=5) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,82). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 40°С. Далее как в примере 1. Получают 38,5 кг продукта, содержащего 74,3% KO2, 9,4% КОН, 9,2% Li2O2, 2,6% LiOH, 3,8% H2O, 0,45% полиборатов лития и калия и 0,25% MgSO4.
Пример 3.
К 45,45 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 160 г сульфата магния (H2O2/MgSO4=600). После растворения MgSO4 примерно через 1,5 минуты в жидкую фазу вводят 99,2 г ортоборной кислоты (H2O2/H3BO3=500), затем одновременно 0,13 кг гидроксида лития и 3,1 кг твердого 90% гидроксида калия. Примерно через 8 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 1,15 кг гидроксида лития (H2O2/LiOH=15) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,6). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 40°С. Далее как в примере 1. Получают 36,2 кг продукта, содержащего 78,9% KO2, 13,2% КОН, 2,9% Li2O2, 0,5% LiOH, 3,6% H2O, 0,54% полиборатов лития и калия и 0,36% MgSO4.
Пример 4.
К 27,23 л водного 85% раствора пероксида водорода при непрерывном перемешивании добавляют 167 г сульфата магния (H2O2/MgSO4=670). После растворения MgSO4 примерно через 2 минуты в жидкую фазу вводят 165,2 г ортоборной кислоты (H2O2/H3BO3=350), затем одновременно 0,32 кг гидроксида лития и 3,1 кг твердого 90% гидроксида калия. Примерно через 9 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 2,87 кг гидроксида лития (H2O2/LiOH=7) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,86). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 40°С. Далее как в примере 1. Получают 37,6 кг продукта, содержащего 76,3% KO2, 12,2% КОН, 6,2% Li2O2, 1,5% LiOH, 3,2% H2O, 0,3% полиборатов лития и калия и 0,3% MgSO4.
Пример 5.
К 48,9 л водного 50% раствора пероксида водорода при непрерывном перемешивании добавляют 230 г сульфата магния (H2O2/MgSO4=450). После растворения MgSO4 примерно через 3 минуты в жидкую фазу вводят 187,2 г ортоборной кислоты (H2O2/Н3ВО3=285), затем одновременно 0,2 кг гидроксида лития и 3,1 кг твердого 90% гидроксида калия. Примерно через 10 минут после прохождения реакции нейтрализации и равномерного распределения всех введенных компонентов по объему жидкой фазы одновременно добавляют 1,86 кг гидроксида лития (H2O2/LiOH=10) и 28,0 кг твердого 90% гидроксида калия (H2O2/КОН=1,72). Добавление второй порции щелочей производят таким образом, чтобы температура жидкой фазы не превышала 40°С. Далее как в примере 1. Получают 36,4 кг продукта, содержащего 74,6% KO2, 13,2% КОН, 6,0% Li2O2, 0,9% LiOH, 4,3% H2O, 0,43% полиборатов лития и калия и 0,57% MgSO4.
Продукт для регенерации воздуха, полученный заявляемым способом, испытан в патроне серийного индивидуального дыхательного аппарата ШСС-Т (ТУ ВТ 8.154.000), используемого шахтерами и горноспасателями, на установке "Искусственные легкие".
Испытания на установке "Искусственные легкие" проводили при следующих условиях:
Объемы кислорода и диоксида углерода указаны при 10°С и 101,3 кПа,
легочная вентиляция - при 37°С и 101,3 кПа.
Для сравнения в тех же условиях испытывался продукт для регенерации воздуха, специально изготовленный по способу, описанному в патенте РФ №2596770 (пример 5). Все продукты для регенерации воздуха имели форму гранул одинакового размера и плотности. Время защитного действия ИДА определяли как время от начала его работы до того момента, когда концентрация CO2 в потоке газо-воздушной смеси на линии "вдоха" установки «Искусственные легкие» достигала 3%. Результаты испытаний представлены в таблице.
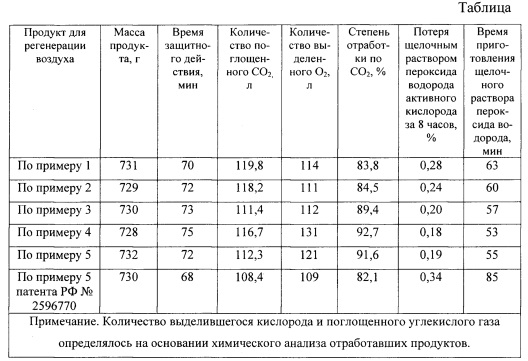
Как видно из представленных в таблице данных, продукт для регенерации воздуха, полученный по изобретению, по таким важным эксплуатационным характеристикам, как время защитного действия и степень отработки по диоксиду углерода, превосходит аналогичные показатели продукта для регенерации воздуха, полученного по патенту РФ №2596770.
Перечисленные выше позитивные аспекты, связанные с процессом регенерации воздуха в патроне ИДА, обусловлены наличием в продукте для регенерации воздуха в указанном количестве солей щелочных металлов полиборных кислот и способом их введения в продукт, что приводит к снижению вязкости поверхностной пленки водного раствора, образующейся на поверхности продукта. Это, в свою очередь, приводит к усилению диффузионных процессов на границах раздела фаз, в жидкой фазе и повышению растворимости и ионизации реагирующих веществ в водном растворе поверхностной пленки. В результате за счет интенсификации массообменных процессов на границах газ - жидкость и жидкость - твердая фаза повышается степень отработки по диоксиду углерода продукта для регенерации воздуха при его эксплуатации в индивидуальных дыхательных аппаратах, что позволяет снизить массогабаритные параметры изделия.
Это особенно актуально при эксплуатации продукта для регенерации воздуха в ИДА постоянного ношения пользователями, обусловленной спецификой условий труда.
Кроме того, присутствие в щелочном растворе пероксида водорода в указанном количестве солей щелочных металлов полиборных кислот и последовательность введения в жидкую фазу исходных компонентов позволяют сократить время приготовления щелочного раствора пероксида водорода и снизить в течение производственного цикла выделение атомарного кислорода, т.е. повысить безопасность и экономичность процесса.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2012 |
|
RU2518610C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2008 |
|
RU2367492C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2015 |
|
RU2596770C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2019 |
|
RU2703878C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2014 |
|
RU2575025C2 |
| СПОСОБ ПОЛУЧЕНИЯ СТРУКТУРИРОВАННОГО РЕГЕНЕРАТИВНОГО ПРОДУКТА | 2015 |
|
RU2599664C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2013 |
|
RU2538898C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ ХИМИЧЕСКОЙ РЕГЕНЕРАЦИИ ВОЗДУХА В СИСТЕМАХ ЖИЗНЕОБЕСПЕЧЕНИЯ ПИЛОТИРУЕМЫХ ЛЕТАТЕЛЬНЫХ АППАРАТОВ | 2022 |
|
RU2810279C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2014 |
|
RU2561412C1 |
| Способ стабилизации щелочного раствора пероксида водорода | 2017 |
|
RU2642571C1 |
Изобретение относится к способам получения продуктов для регенерации воздуха для систем жизнеобеспечения человека. Для получения продукта для регенерации воздуха осуществляют смешение раствора пероксида водорода с сульфатом магния и гидроксидами лития и калия с последующей дегидратацией полученного щелочного раствора пероксида водорода распылением его в токе сушильного агента. При этом в раствор пероксида водорода после добавления сульфата магния вводят ортоборную кислоту при мольном соотношении пероксид водорода/ортоборная кислота (Н2O2/Н3ВО3)=285-800. Гидроксиды лития и калия вводят одновременно двумя порциями с интервалом 7-10 мин таким образом, чтобы температура в зоне синтеза не превышала 40°С. За счет интенсификации массообменных процессов на границах газ - жидкость и жидкость - твердая фаза повышается степень отработки по диоксиду углерода продукта для регенерации воздуха при его эксплуатации в индивидуальных дыхательных аппаратах, обеспечивающая снижение массогабаритных параметров изделия. 5 пр., 1 табл.
Способ получения продукта для регенерации воздуха путем смешения раствора пероксида водорода с сульфатом магния и гидроксидами лития и калия с последующей дегидратацией полученного щелочного раствора пероксида водорода распылением его в токе сушильного агента, отличающийся тем, что в раствор пероксида водорода после его смешения с сульфатом магния вводят ортоборную кислоту при мольном соотношении пероксид водорода / ортоборная кислота (Н2O2/Н3ВО3)=285-800, при этом гидроксиды лития и калия вводят в жидкую фазу одновременно двумя порциями с интервалом 7-10 мин. таким образом, чтобы температура в зоне синтеза не превышала 40°C.
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2015 |
|
RU2596770C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТРУКТУРИРОВАННОГО РЕГЕНЕРАТИВНОГО ПРОДУКТА | 2015 |
|
RU2599664C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2010 |
|
RU2456046C1 |
| JP 2003306315 A, 28.10.2003 | |||
| US 4508700 A, 02.04.1985 | |||
| Устройство поэлементного фазирования приемников дискретных сигналов | 1972 |
|
SU450377A2 |
Авторы
Даты
2018-10-16—Публикация
2017-12-13—Подача