Тадалафил ((6R-транс)-6-(1,3-бензодиоксол-5-ил)-2,3,6,7,12,12a-гексагидро-2-метил-пиразино[1, 2':1,6]пиридо[3,4-b]индол-1,4-дион) формулы (1)
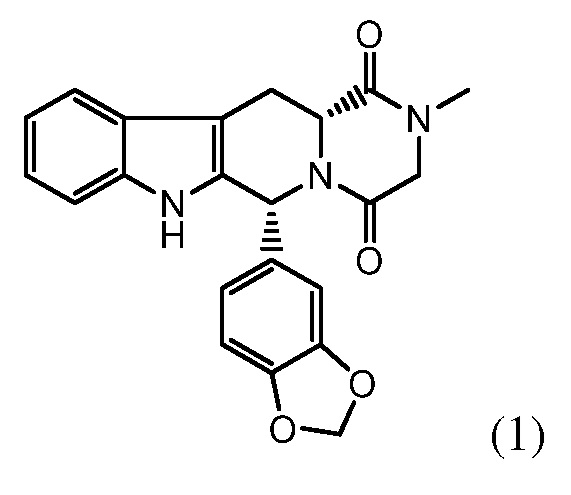
является фармацевтически активным соединением, применяемым для лечения эректильной дисфункции (ED) и доброкачественной гиперплазии простаты (BHP), которое поступает на рынок под наименованием Cialis® в форме таблеток 2,5, 5, 10 и 20 мг и под наименованием Adcirca® в форме таблеток 20 мг для лечения легочной артериальной гипертензии. Это соединение было обнаружено корпорацией ICOS и впервые описано в WO 9519978. Тадалафил плохо растворим в воде; поэтому необходимо включать это соединение в такие лекарственные составы, которые обеспечивают улучшение растворимости и биодоступности.
В заявке WO 9638131 раскрыты твердые дисперсии в форме продуктов совместного осаждения (копреципитатов) тадалафила и фталата гидроксипропилметилцеллюлозы. Однако при измерении растворимости составов, полученных с применением этих копреципитатов, авторы обнаружили, что эта растворимость является слишком низкой, чтобы ожидать хорошей биодоступности. Таким образом, совместное осаждение с фталатом гидроксипропилметилцеллюлозы не является подходящим способом для повышения биодоступности тадалафила.
В заявке WO 0108688 раскрыт состав, включающий тадалафил, измельченный до частиц с размером d90 менее 10 микронов и обладающий улучшенной биодоступностью. Однако измельчение до частиц столь малого размера может приводить к уменьшению сыпучести, потере действующего вещества и может влиять на химическую и полиморфную стабильность активного ингредиента.
В заявке WO 2008005039 раскрыты композиции тадалафила и водорастворимых полимеров, полученные растворением тадалафила и гидрофильного полимера в этаноле и последующей распылительной сушкой раствора с получением порошка, который можно применять для получения фармацевтического состава (примеры фармацевтических составов не приведены). Во всех имеющихся в заявке примерах применяются значительные количества этанола, составляющие примерно 1000 мл на грамм тадалафила, что делает способ неприменимым в промышленных масштабах.
В заявке WO 2011012217 раскрыты составы, включающие копреципитат тадалафила и акрилатного полимера катионного характера. Этот копреципитат смешивают с другими эксципиентами и прессуют в таблетки. Способ получения указанного копреципитата является трудоемким; требуется высушивание копреципитата при относительно высокой температуре в течение продолжительного времени (20 часов), что может приводить к разрушению действующего ингредиента.
В заявке WO 2012095151 раскрыты составы, которые получают гранулированием горячей жидкости в кипящем слое, используя раствор тадалафила и распыляя полученный продукт на нерастворимый в воде полимер, смешанный с разбавителем. Гранулирование в кипящем слое необходимо осуществлять при высоких температурах, что может повысить содержание примесей. Полученный гранулят смешивают с другими эксципиентами и прессуют в таблетки. В примерах упоминается применение этилцеллюлозы в качестве нерастворимого в воде полимера, который часто используется в составах с продолжительным высвобождением и может оказывать отрицательное влияние на растворение и, следовательно, биодоступность.
В свете описанного выше известного уровня техники, существует потребность в композициях, включающих тадалафил, демонстрирующих хорошую растворимость и биодоступность, а также в способе получения этих композиций, который не обладает упомянутыми выше недостатками.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении обнаружено, что твердая дисперсия тадалафила, стабилизирующая тадалафил в аморфной форме в по меньшей мере двух различных типах полимеров: по меньшей мере одном полимере, растворимом в водной среде при pH не выше 5,0 и по меньшей мере одном полимере с pH-зависимой растворимостью, растворимом при pH выше 5,0, обеспечивает оптимальный уровень биодоступности тадалафила, так что указанная фармацевтическая композиция является биологическим эквивалентом, как после еды, так и натощак, имеющегося на рынке продукта Cialis®.
В одном из вариантов осуществления настоящее изобретение относится к фармацевтической композиции, включающей твердую дисперсию тадалафила в по меньшей мере двух различных типах полимеров, где по меньшей мере один из этих полимеров растворим в водной среде при pH не выше 5,0 и по меньшей мере один полимер обладает pH-зависимой растворимостью и растворим при pH выше 5,0, демонстрирующей скорость растворения по меньшей мере примерно 85 масс.% в течение 20 мин при тестировании в 1000 мл фосфатного буфера (pH 6,8) +0,35 масс.% SDS в аппарате II USP (емкости с пиком на дне) при 50 об/мин.
Во втором варианте осуществления настоящее изобретение относится к способу получения указанной фармацевтической композиции, включающий стадии:
a. Получение двух растворов в растворителе или смеси растворителей:
i. тадалафила и по меньшей мере одного полимера, растворимого в водной среде при pH не выше 5,0;
ii. тадалафила и по меньшей мере одного полимера с pH-зависимой растворимостью, растворимого при pH выше 5,0;
b. Последовательного распыления растворов, полученных на стадии a, над наполнителем;
c. Гранулирования смеси, полученной на стадии b;
d. Высушивания полученного гранулята.
В третьем варианте осуществления фармацевтическая композиция по настоящему изобретению отличается тем, что эта композиция стабилизирована влагозащитным слоем с WVTR (скоростью проникновения водяных паров) менее 0,35 г/м2/сутки при 38°C/90% отн. вл. (относительной влажности).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
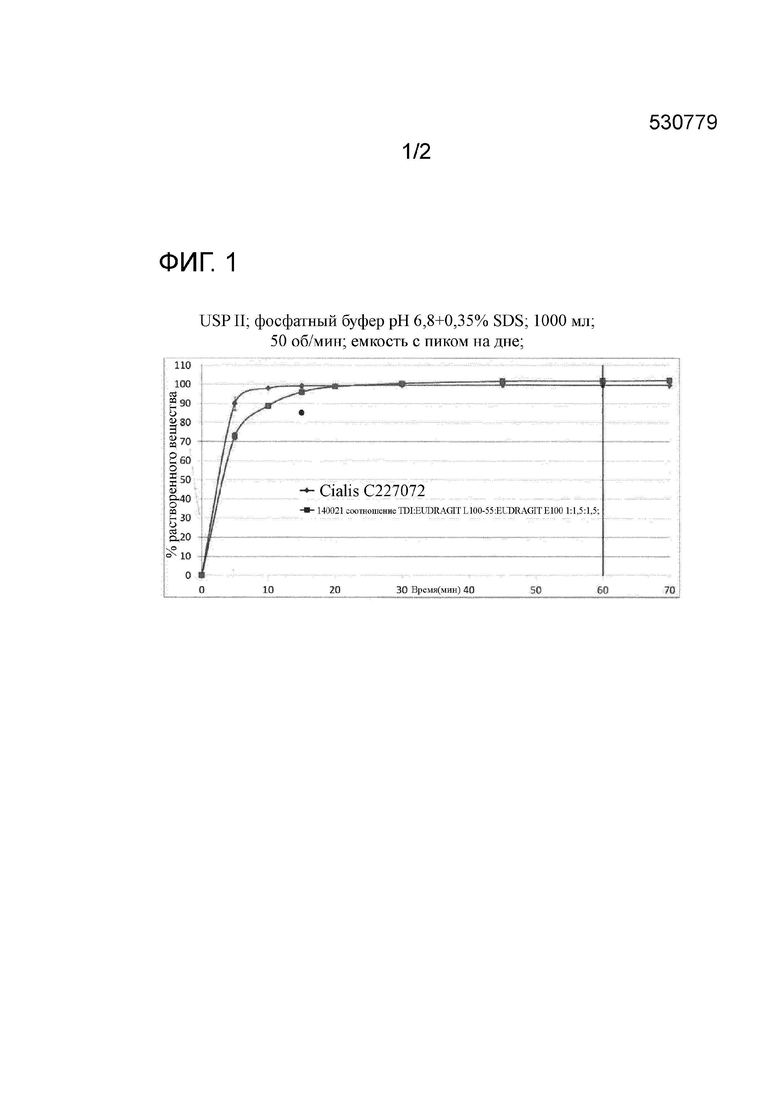
Фиг.1 представляет собой профиль растворения фармацевтического состава, полученного в примере 1, включающего твердую дисперсию аморфного тадалафила, по сравнению с профилем растворения таблеток Cialis® 20 мг IR в 1000 мл фосфатного буфера (pH 6,8) +0,35 масс. % SDS в аппарате II USP (емкости с пиком на дне) при 50 об/мин.
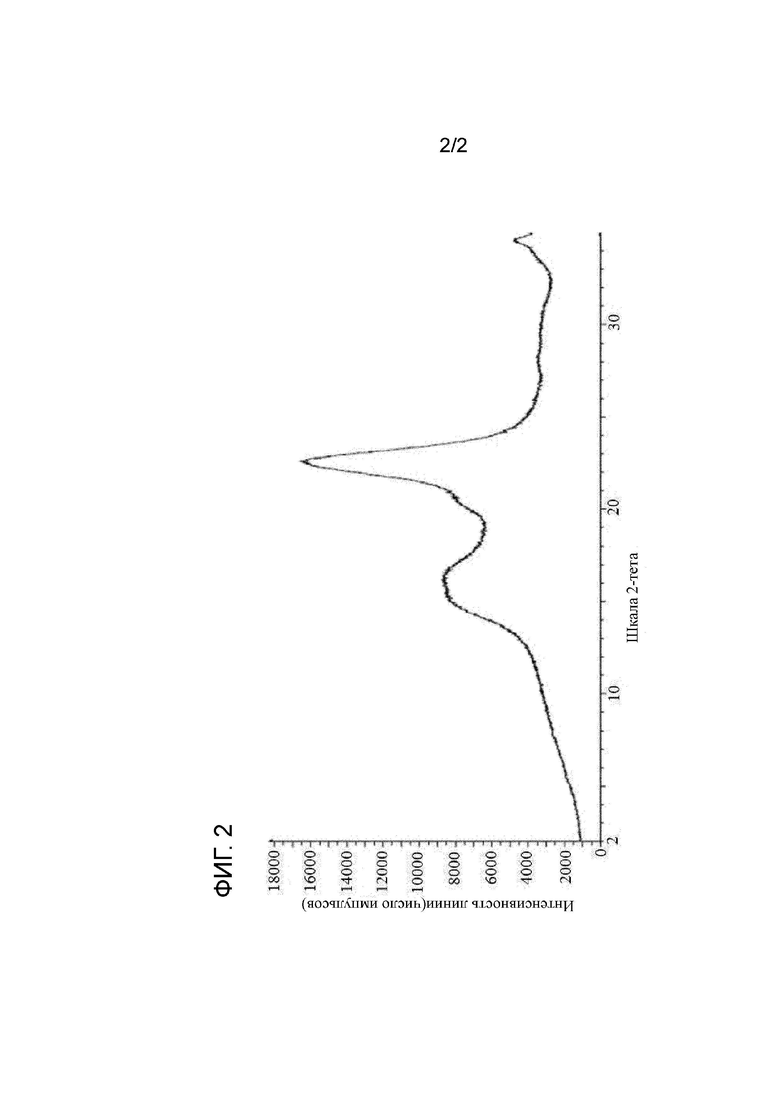
Фиг.2 представляет собой картину порошковой рентгеновской дифракции (XRPD) гранулята твердой дисперсии тадалафила, полученного в примере 1.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к фармацевтической композиции, включающей твердую дисперсию тадалафила в по меньшей мере двух различных типах полимеров, где по меньшей мере один из этих полимеров растворим в водной среде при pH не выше 5,0 и по меньшей мере один полимер обладает pH-зависимой растворимостью и растворим при pH выше 5,0, демонстрирующей скорость растворения по меньшей мере примерно 85 масс. % в течение 20 мин при тестировании в 1000 мл фосфатного буфера (pH 6,8) +0,35 масс. % SDS в аппарате II USP (емкости с пиком на дне) при 50 об/мин.
Подходящими полимерами, растворимыми в водной среде при pH не выше 5,0, являются, например, катионные метакрилатные сополимеры, повидон, гипромеллоза, полоксамер, полиэтиленгликоль, поливинилкапролактам, поливинилацетат, привитые сополимеры полиэтиленгликоля.
Предпочтительно, полимер, растворимый в водной среде при pH не выше 5,0 представляет собой катионный метакрилатный сополимер. Более предпочтительно, он является сополимером на основе диметиламиноэтилметакрилата - бутилметакрилата - метилметакрилата в соотношении 2:1:1.
Подходящие сополимеры на основе диметиламиноэтилметакрилата - бутилметакрилата - метилметакрилата в соотношении 2:1:1 поставляются на рынок компанией Evonik под торговыми наименованиями Eudragit® E100, E PO и E 12,5.
Подходящими полимерами с pH-зависимой растворимостью, растворимыми при pH выше 5,0, являются анионные сополимеры метакриловой кислоты, ацетат сукцинат гипромеллозы и фталат гипромеллозы.
Предпочтительно, полимер с pH-зависимой растворимостью, растворимый выше pH 5,0, является анионным сополимером метакриловой кислоты. Наиболее предпочтительно, он является сополимером, на основе сополимера метакриловая кислота-этилакрилат (1:1).
Подходящие сополимеры на основе сополимера метакриловая кислота-этилакрилат (1:1) поставляются на рынок компанией Evonik под торговыми наименованиями Eudragit® L 100-55 и L30 D-55.
Термин "соотношение 2:1:1" в тексте настоящего описания относится к (мольному) соотношению присутствующих в сополимере диметиламиноэтилметакрилатных групп к бутилметакрилатным группам и к метилметакрилатным группам.
Термин "соотношение 1:1" в тексте настоящего описания относится к (мольному) соотношению присутствующих в сополимере остатков метакриловой кислоты к этилакрилатным группам.
В соответствии с настоящим изобретением, под термином "твердая дисперсия" подразумевается твердый продукт, состоящий из гидрофобного лекарственного средства, т.е. тадалафила, и матрицы, т.е. сополимеров метакрилатов или метакриловой кислоты, в котором тадалафил молекулярно диспергирован в указанных сополимерах. В указанных твердых дисперсиях тадалафил находится в аморфной форме.
Массовое соотношение тадалафил:общее количество полимеров в композиции по настоящему изобретению находится в пределах от 1:1 до 1:8, предпочтительно 1:3.
Массовое соотношение полимера(ов), растворимого в водной среде при pH не выше 5,0 и полимера(ов) с pH-зависимой растворимостью, растворимого при pH выше 5,0, находится в пределах от 1:1 до 1:4.
Предпочтительно, композиция по настоящему изобретению дополнительно включает наполнитель. Наполнитель, который следует применять согласно настоящему изобретению, может быть любым наполнителем, известным рядовому специалисту в данной области техники. Конкретно, наполнитель, который следует применять согласно настоящему изобретению, представляет собой неорганический наполнитель, полисахарид, моно- или дисахарид или сахарный спирт. Преимущественно, наполнитель, применяемый согласно настоящему изобретению, выбран из группы, состоящей из микрокристаллической целлюлозы, алюминометасиликата магния и крахмала. Микрокристаллическая целлюлоза является особенно предпочтительным наполнителем.
Предпочтительно, композиция по настоящему изобретению дополнительно включает другие эксципиенты.
Более предпочтительно, композиция по настоящему изобретению дополнительно включает дезинтегрирующее средство. Дезинтегрирующее средство, которое предполагается применять согласно настоящему изобретению, может быть любым дезинтегрирующим средством, известным рядовому специалисту в данной области техники. Подходящие дезинтегрирующие средства для применения согласно настоящему изобретению, выбирают из группы, состоящей из кроскармеллозы, кросповидона и натрия крахмал гликолята. Особенно предпочтительным дезинтегрирующим средством является кроскармеллоза.
Предпочтительно, композиция по настоящему изобретению дополнительно включает смазывающее средство. Смазывающее средство, которое должно применяться согласно настоящему изобретению, может являться любым смазывающим средством, известным рядовому специалисту в данной области техники. Особенно предпочтительным смазывающим средством является стеарат магния.
Предпочтительно, доза тадалафила в фармацевтической композиции по настоящему изобретению составляет 2,5, 5, 10, 20 или 40 мг.
Эксперименты по XRPD-анализу композиции по настоящему изобретению не демонстрируют пиков кристаллического вещества, что указывает на отсутствие свободного (кристаллического) тадалафила и показывает наличие аморфной твердой дисперсии (см., например, фиг.2).
Фармацевтическая композиция по настоящему изобретению демонстрирует характер растворимости, типичный для составов с немедленным высвобождением (см., например, фиг. 1) без необходимости применения тонкоизмельченного тадалафила в качестве действующего фармацевтического ингредиента. В композициях по настоящему изобретению, тадалафил не присутствует в форме частиц, но он молекулярно диспергирован в матрице, которая образована полимером(ами), растворимым в водной среде при pH не выше 5,0 и полимером(ами) с pH-зависимой растворимостью, растворимым при pH выше 5,0, где взаимодействие с полимерами способствует повышению растворимости тадалафила, улучшая его биодоступность, в результате чего фармацевтическая композиция по настоящему изобретению биологически эквивалентна имеющемуся на рынке продукту Cialis® после еды и натощак.
При исследовании стабильности фармацевтических композиций с различными твердыми дисперсиями тадалафила, наблюдалось небольшое, но статистически значимое уменьшение скорости растворения. В настоящем изобретении было обнаружено, что источник этой проблемы лежит в постоянном проникновении достаточного количества паров воды через поры упаковочного материала. Скорость проникновения паров воды (WVTR), именуемая также скоростью проникновения паров влаги (MVTR), является показателем прохождения паров воды через вещество. Для измерения WVTR имеются различные методики, начиная от гравиметрических методик, которые измеряют набор или потерю влаги по изменению массы, до сложных инструментальных методик, которые в ряде случаев способны измерять исключительно низкие скорости переноса влаги. Для определения WVTR доступны коммерческие приборы, в которых используется либо модулированный по давлению инфракрасный детектор, либо механически модулированный инфракрасный детектор. Многочисленные стандартные методики описаны в таких источниках, как в ISO, ASTM, BS и DIN, например, ASTM F1249 и DIN53122. Условия, в которых проводятся измерения, оказывают значительное влияние на результат. Вместе с результатом необходимо измерять, контролировать и регистрировать как температуру, так и градиент влажности в объеме образца. Авторы обнаружили, что скорость растворения фармацевтических композиций по настоящему изобретению можно сохранить с помощью влагозащитного слоя с WVTR менее 0,35 г/м2/день при 38°C/90% отн. вл. (относительной влажности). Предпочтительно, WVTR влагозащитного слоя поддерживают на уровне менее 0,2 г/м2/день при 38°C/90% отн. вл. Более предпочтительно, WVTR влагозащитного слоя поддерживают на уровне менее 0,1 г/м2/день при 38°C/90% отн. вл., и наиболее предпочтительно, WVTR влагозащитного слоя поддерживают на уровне менее 0,01 г/м2/день при 38°C/90% отн. вл.
Блистерные упаковки относятся к группе основных упаковочных материалов в фармацевтической промышленности. Они применяются для защиты фармацевтических композиций от таких внешних факторов, как влажность и загрязнения в течение продолжительных периодов времени. Тип применяемого блистерного упаковочного материала и толщина его пленки определяют величину WVTR. Типовые значения WVTR 250 мкм блистерной пленки из PVC (ПВХ) и двухслойной блистерной пленки 250 мкм PVC/90 г/м2 PVDC составляют >3 г/м2/день и 0,35 г/м2/день при 38°C/90% отн. вл., соответственно. Пленка холодной формовки, известная также как альфоль, имеет значение WVTR, равное 0,005 г/м2/день при 38°C/90% отн. вл.
В другом варианте осуществления настоящего изобретения, описанную выше фармацевтическую композицию стабилизируют с помощью влагозащитного слоя с WVTR менее 0,35 г/м2/день при 38°C/90% отн. вл. Предпочтительно, этот слой создают путем упаковки фармацевтической композиции в блистерный упаковочный материал с WVTR менее 0,35 г/м2/день при 38°C/90% отн. вл. Наиболее предпочтительно, путем упаковки фармацевтической композиции в пленку холодной формовки.
Далее, настоящее изобретение относится к способу получения указанной фармацевтической композиции, включающей твердую дисперсию тадалафила в по меньшей мере двух различных типах полимеров, как описано выше, включающему стадии:
a. Получения двух растворов в растворителе или смеси растворителей:
i. тадалафила и по меньшей мере одного полимера, растворимого в водной среде при pH не более 5,0;
ii. тадалафила и по меньшей мере одного полимера с pH-зависимой растворимостью, растворимого при pH выше 5,0;
b. Последовательного распыления растворов, полученных на стадии a, над наполнителем;
c. Гранулирования смеси, полученной на стадии b;
d. Высушивания полученного гранулята.
Растворитель или смесь растворителей, которые следует применять в соответствии с настоящим изобретением, может представлять собой любой растворитель или смесь растворителей, известные рядовому специалисту в данной области техники. Важно, чтобы тадалафил и полимер(ы) были растворены полностью.
Преимущественно, растворитель, применяемый согласно настоящему изобретению, может являться полярным органическим растворителем, в то время как смесь растворителей может являться смесью полярных органических растворителей или смесью полярного органического растворителя с водой. Подходящие для применения в настоящем изобретении полярные органические растворители включают апротонные полярные органические растворители, выбранные из группы, состоящей из этилацетата, тетрагидрофурана, диоксана, дихлорметана, ацетонитрила, диметилформамида, диметилсульфоксида и ацетона. Особенно предпочтительными полярными органическими растворителями являются тетрагидрофуран и ацетон. Особенно предпочтительной смесью апротонного полярного органического растворителя с водой является смесь ацетона и воды.
Особенно предпочтительной является смесь ацетона и воды в массовом соотношении от примерно 8:2 до примерно 9:1, более предпочтительно в массовом соотношении от 8,5:1,5 до 9:1.
Стадии способа по настоящему изобретению, как правило, проводят при температуре от примерно 25°C до примерно 50°C. В предпочтительном варианте способа по настоящему изобретению, стадии проводят при температуре от примерно 40°C до примерно 50°C. Во время стадии b оба раствора последовательно распыляют над наполнителем. Предпочтительно, порядок распыления на стадии b является следующим:
1. Распыление над наполнителем раствора тадалафила и по меньшей мере одного полимера, растворимого в водной среде при pH не выше 5,0;
2. Распыление над наполнителем раствора тадалафила и по меньшей мере одного полимера с pH-зависимой растворимостью, растворимого при pH выше 5,0.
Предпочтительно, способ по настоящему изобретению реализуют в грануляторе с кипящим слоем или в грануляторе с высоким усилием сдвига, более предпочтительно в грануляторе с кипящим слоем.
Предпочтительно, способ по настоящему изобретению дополнительно включает стадии смешивания высушенного и необязательно просеянного гранулята с дезинтегрирующим средством, смазывающим компонентом и, необязательно, одним или несколькими дополнительными фармацевтически приемлемыми эксципиентами, и прессования этой смеси в таблетки с применением методик и оборудования, хорошо известных специалисту в данной области техники.
Способ по настоящему изобретению является предпочтительным, поскольку он позволяет избежать применения больших количеств растворителей и трудоемких процедур измельчения. Кроме того, в способе по настоящему изобретению требуется короткое время гранулирования. По указанным причинам, способ по настоящему изобретению легко реализовать в промышленных масштабах.
Приведенные ниже примеры предназначены для иллюстрации объема настоящего изобретения, но не для ограничения объема изобретения этими примерами.
ПРИМЕРЫ
Пример 1
**Подвергается выпариванию на стадии гранулирования
Способ получения
135 г ацетона и 15 г воды смешивали и нагревали до 45-50°C. Добавляли 12,5 г Eudragit L100-55 и полностью растворяли в растворителе. Затем добавляли и растворяли 4,17 г тадалафила. Взвешивали внутригранулярную порцию микрокристаллической целлюлозы (MCC) (127,7 г) и добавляли в кипящий слой. Раствор распыляли над MCC и гранулировали в кипящем слое при скорости распыления примерно 6-7 г/мин. После окончания первого распыления, в другой емкости смешивали 135 г ацетона и 15 г воды и нагревали до 45-50°C. Добавляли 12,5 г Eudragit E100 и полностью растворяли в растворителе. Затем добавляли и растворяли 4,17 г тадалафила. Второй раствор распыляли над порошком, полученным в результате предыдущего распыления, и гранулировали в кипящем слое при той же скорости потока. После добавления второго раствора продолжали высушивание до LOD<3% и просеивали через сито 0,8 мм (XRPD гранул на фиг.2 показывает наличие аморфного тадалафила без пиков, соответствующих кристаллической структуре). Оставшуюся часть MCC (31,93 г) и натрий кроскармеллозу (6 г) взвешивали, просеивали и смешивали с просеянными гранулами в течение 15 мин. 1 г стеарата магния просеивали через сито 0,500 мм и смешивали с полученной ранее смесью в течение 5 мин. Полученную гомогенную порошковую смесь прессовали в условиях контролируемой влажности на роторной таблетирующей машине, получая таблетки 480 мг с твердостью 150N.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЖЕЛУДОЧНО-РЕЗИСТЕНТНАЯ ФАРМАЦЕВТИЧЕСКАЯ ИЛИ НУТРИЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С УСТОЙЧИВОСТЬЮ К ВОЗДЕЙСТВИЮ ЭТАНОЛА | 2012 |
|
RU2649806C2 |
| КОМПОЗИЦИИ СТАБИЛЬНЫХ ТИАКУМИЦИНОВ | 2008 |
|
RU2484829C2 |
| ПРЕССОВАННЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 2016 |
|
RU2744270C2 |
| ПОКРЫВАЮЩАЯ КОМПОЗИЦИЯ, ПОДХОДЯЩАЯ ДЛЯ ФАРМАЦЕВТИЧЕСКИХ ИЛИ НУТРИЦЕВТИЧЕСКИХ ЛЕКАРСТВЕННЫХ ФОРМ | 2011 |
|
RU2599023C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА И СПОСОБ ДЛЯ ДОСТАВКИ ВЫЗЫВАЮЩИХ ЗАВИСИМОСТЬ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ | 2007 |
|
RU2433817C2 |
| СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ВКЛЮЧАЮЩИЕ В СЕБЯ ТВЕРДЫЕ РАСТВОРЫ СЛАБООСНОВНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2007 |
|
RU2434630C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА В ТОЛСТУЮ КИШКУ | 2007 |
|
RU2646825C2 |
| КОМПОЗИЦИЯ ПОКРЫТИЯ, ПОДХОДЯЩАЯ ДЛЯ ФАРМАЦЕВТИЧЕСКИХ ИЛИ НУТРИЦЕВТИЧЕСКИХ ДОЗИРОВАННЫХ ФОРМ | 2011 |
|
RU2606588C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ИЛИ НУТРИЦЕВТИЧЕСКИЙ СОСТАВ | 2010 |
|
RU2604861C2 |
| СПОСОБ СТАБИЛИЗАЦИИ ЛЕКАРСТВЕННОГО СРЕДСТВА ПРОТИВ ДЕМЕНЦИИ | 2005 |
|
RU2401125C2 |
Настоящее изобретение относится к фармацевтической композиции, включающей твердую дисперсию тадалафила и по меньшей мере два различных типа полимеров: по меньшей мере один катионный метакрилатный сополимер и по меньшей мере один анионный сополимер метакриловой кислоты. Катионный метакрилатный сополимер получен на основе диметиламиноэтилметакрилата-бутил метакрилата-метилметакрилата в соотношении 2:1:1. Анионный сополимер метакриловой кислоты получен на основе сополимера метакриловая кислота-этилакрилат в соотношении 1:1. Также описан способ получения композиции методом мокрого гранулирования. Композиция по изобретению демонстрирует скорость растворения тадалафила по меньшей мере 85 мас.% в течение 20 мин при тестировании в 1000 мл фосфатного буфера (pH 6,8)+0,35 мас.% додецилсульфата натрия (SDS) в аппарате II USP (емкости с пиком на дне) при 50 об/мин. 2 н. и 18 з.п. ф-лы, 2 ил., 1 табл., 1 пр.
1. Фармацевтическая композиция, включающая твердую дисперсию тадалафила и по меньшей мере два различных типа полимеров:
a. По меньшей мере один катионный метакрилатный сополимер;
b. По меньшей мере один анионный сополимер метакриловой кислоты;
где катионный метакрилатный сополимер получен на основе диметиламиноэтилметакрилата-бутилметакрилата-метилметакрилата в соотношении 2:1:1, и анионный сополимер метакриловой кислоты получен на основе сополимера метакриловая кислота-этилакрилат в соотношении 1:1,
демонстрирующая скорость растворения по меньшей мере 85 масс. % в течение 20 мин при тестировании в 1000 мл фосфатного буфера (pH 6,8) +0,35 масс. % додецилсульфата натрия (SDS) в аппарате II USP (емкости с пиком на дне) при 50 об/мин.
2. Композиция по п.1, где массовое соотношение тадалафил:суммарное количество полимеров в композиции находится в диапазоне от 1:1 до 1:8.
3. Композиция по п.1, где массовое соотношение тадалафил:суммарное количество полимеров в композиции составляет 1:3.
4. Композиция по п.2, где массовое соотношение катионного метакрилатного сополимера(ов) и анионного сополимера(ов) метакриловой кислоты находится в диапазоне от 1:1 до 1:4.
5. Композиция по п.4, дополнительно включающая наполнитель.
6. Композиция по п.5, где наполнитель представляет собой микрокристаллическую целлюлозу.
7. Композиция по п.5, дополнительно включающая другие фармацевтические эксципиенты.
8. Композиция по п.7, дополнительно прессованная в таблетки.
9. Композиция по п.7, где доза тадалафила в композиции выбрана из группы, включающей 2,5, 5, 10, 20 или 40 мг.
10. Композиция по любому из пп.1-9, отличающаяся тем, что эта композиция стабилизирована влагозащитным слоем со скоростью проникновения паров воды (WVTR) менее 0,35 г/м2/сутки при 38°C/90% отн. вл.
11. Композиция по п.10, где влагозащитный слой создан путем упаковки таблеток в блистерный упаковочный материал.
12. Композиция по п.10, где блистерный упаковочный материал представляет собой блистерную упаковку холодного формования.
13. Способ получения композиции по любому из пп.1-9, включающий стадии:
a. Получения двух растворов в растворителе или смеси растворителей:
i. тадалафила и по меньшей мере одного катионного метакрилатного сополимера;
ii. тадалафила и по меньшей мере одного анионного сополимера метакриловой кислоты;
b. Последовательного распыления растворов, полученных на стадии a, над наполнителем;
c. Гранулирования смеси, полученной на стадии b;
d. Высушивания полученного гранулята.
14. Способ по п.13, где растворитель выбран из группы, состоящей из этилацетата, тетрагидрофурана, диоксана, дихлорметана, ацетонитрила, диметилформамида, диметилсульфоксида, ацетона и смеси ацетона с водой.
15. Способ по п.14, где растворитель представляет собой смесь ацетона с водой.
16. Способ по п.15, где массовое соотношение ацетона и воды в смеси составляет от 8:2 до 9:1.
17. Способ по п.13, где стадию a осуществляют при температуре от 25°C до 50°C.
18. Способ по п.13, где стадию a осуществляют при температуре от 45°C до 50°C.
19. Способ по п.13, где последовательность осуществления стадии b является следующей:
1. распыление над наполнителем раствора тадалафила и по меньшей мере одного катионного метакрилатного сополимера;
2. распыление над наполнителем раствора тадалафила и по меньшей мере одного анионного сополимера метакриловой кислоты.
20. Способ по п.13, дополнительно включающий стадии:
a. смешивания высушенного и необязательно просеянного гранулята с дезинтегрирующим средством, смазывающим компонентом и, необязательно, одним или несколькими дополнительными фармацевтически приемлемыми эксципиентами; и
b. прессования полученной смеси в таблетки.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Прибор для печатания карт местности с выраженным рельефом по парным аэрофотоснимкам | 1926 |
|
SU10971A1 |
Авторы
Даты
2018-11-23—Публикация
2014-07-04—Подача