РОДСТВЕННАЯ ЗАЯВКА
В данной заявке заявляется приоритет по предварительной заявке на выдачу патента США с серийным номером 61/558775, поданной 11 ноября 2011 года, описание которой включено в настоящий документ в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к новым производным 4-прегенен-11β-17-21-триол-3,20-диона, способам их получения, фармацевтическим композициям, содержащим их, и к их применению в качестве фармацевтических средств как модуляторов глюкокортикоидных или минералокортикоидных рецепторов. Настоящее изобретение относится, в частности, к применению этих соединений и их фармацевтических композиций для лечения расстройств, связанных с модулированием глюкокортикоидного или минералокортикоидного рецептора.
УРОВЕНЬ ТЕХНИКИ
Агонисты глюкокортикоида (GC) представляют собой класс противовоспалительных соединений, пригодных для лечения многочисленных глазных болезней, включая повышенное внутриглазное давление, глаукому, увеит, окклюзию вены сетчатки, дегенерацию желтого пятна, диабетическую ретинопатию, различные формы макулярного отека, послеоперационное воспаление, воспалительные состояния конъюнктивы век и конъюнктивы глазного яблока, роговицы и переднего сегмента глазного яблока, такие как аллергические конъюнктивиты, розовые угри на глазах, сухость глаз, блефариты, отслоение сетчатки, дисфункцию мейбомиевой железы (MGD), точечный поверхностный кератит, кератит с опоясывающим герпесом, ирит, циклит, некоторые инфекционные конъюнктивиты, травму роговицы из-за химического, радиационного или термического ожога, проникновение инородных тел, аллергию или их комбинации.
Ограничение потенциального применения и побочный эффект угрозы потери зрения для традиционных терапий GC агонистами (например, флуоцинолона ацетонидом) представляет собой глазная гипертензия, которая, вероятно, создается за счет повышенного сопротивления потока водянистой влаги глаз через трабекулярную сеть. Механизм сопротивления истечению, вызванного GC агонистом, и последующей глазной гипертензии понятен не до конца.
Таким образом, в данной области существует необходимость модулирования GC за счет действия агониста или антагониста GC рецепторов, которое не приводит к повышению внутриглазного давления или другим побочным эффектам, и она описана в настоящем документе.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым производным 4-прегенен-11β-17-21-триол-3,20-диона, пригодным для лечения одного или более глазных заболеваний. Описаны также способы лечения одного или более глазных заболеваний. Глазные заболевания, подлежащие лечению с помощью соединений и/или композиций, описанных в настоящем документе, включают, но не ограничиваясь этим, повышенное внутриглазное давление, глаукому, увеит, окклюзию вены сетчатки, дегенерацию желтого пятна, диабетическую ретинопатию, различные формы макулярного отека, послеоперационное воспаление, воспалительные состояния конъюнктивы век и конъюнктивы глазного яблока, роговицы и заднего сегмента глазного яблока, такие как аллергические конъюнктивиты, розовые угри на глазах, сухость глаз, блефариты, отслоение сетчатки, дисфункцию мейбомиевой железы (MGD), точечный поверхностный кератит, кератит с опоясывающим герпесом, ирит, циклит, некоторые инфекционные конъюнктивиты, травму роговицы из-за химического, радиационного или термического ожога, проникновение инородных тел, аллергию или их комбинации.
Таким образом, в одном аспекте настоящего изобретения представлено соединение Формулы I, его энантиомеры, диастереоизомеры, гидраты, сольваты, кристаллические формы и отдельные изомеры, таутомеры или фармацевтически приемлемые соли,
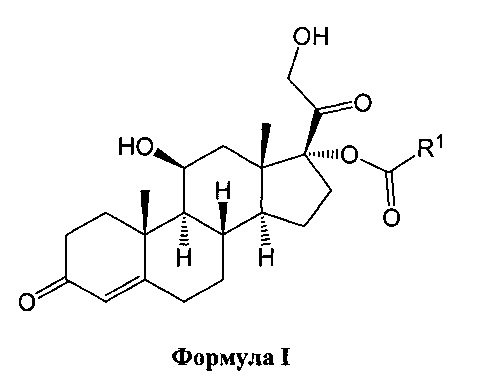
где:
R1 представляет собой необязательно замещенный C7-C11 алкил, необязательно замещенный С2-С8 алкенил, необязательно замещенный С2-С8 алкинил, необязательно замещенный С4 или С6-8 циклоалкил, необязательно замещенный арил, замещенный бензил, необязательно замещенный гетероцикл, необязательно замещенный С3-С10 циклоалкенил, необязательно замещенный С5-С10 циклодиен, необязательно замещенный О(C3-C6) алкил, аминогруппы, сульфонамидные группы, амидные группы, кроме фенила.
В другом варианте реализации настоящего изобретения представлено соединение Формулы I, где R1 выбран из:
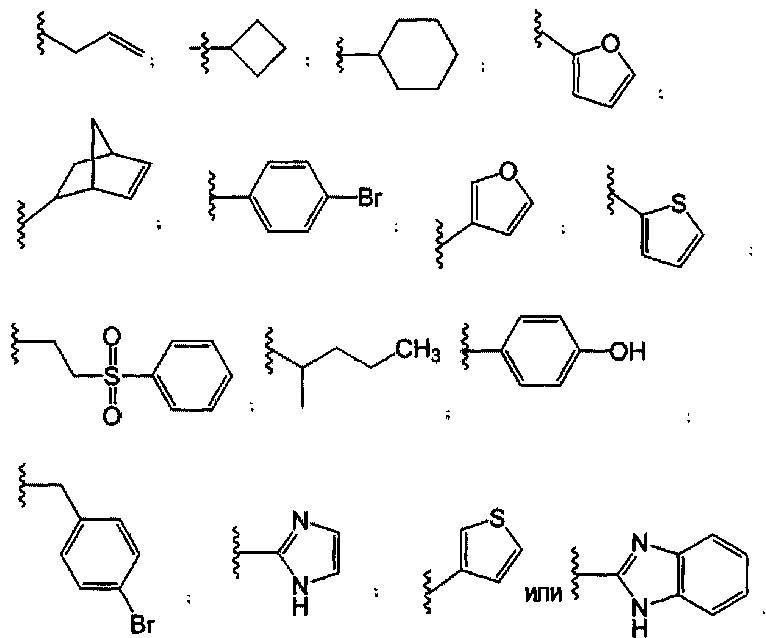
Термин «аклил», используемый в настоящем документе, относится к насыщенным одновалентным или двухвалентным углеводородным фрагментам, имеющим линейные или разветвленные фрагменты или их комбинации, и содержащим от 7 до 11 углеродных атомов. Одна метиленовая (-CH2-) группа алкильной группы может быть заменена кислородом, серой, сульфоксидом, азотом, карбонилом, карбоксилом, сульфонилом, сульфатом, сульфонатом, амидом, сульфонамидом, двухвалентным С3-8 циклоалкилом, двухвалентным гетероциклом или двухвалентной арильной группой. Алкильные группы могут быть независимо замещены атомами галогена, гидроксильными группами, циклоалкильными группами, аминогруппами, гетероциклическими группами, арильными группами, группами карбоновых кислот, сложноэфирными группами, кетоновыми группами, группами фосфоновых кислот, группами сульфоновых кислот, группами фосфорных кислот, нитрогруппами, амидными группами, сульфонамидными группами.
Термин «циклоалкил», используемый в настоящем документе, относится к одновалентной или двухвалентной группе из 4 и 6-8 углеродных атомов, полученной из насыщенного циклического углеводорода. Циклоалкильные группы могут быть моноциклическими или полициклическими. Циклоалкил может быть независимо замещен атомами галогена, сульфонил C1-8 алкильными группами, сульфоксид C1-8 алкильными группами, сульфонамидными группами, нитрогруппами, циано-группами, -ОС1-8 алкильными группами, -SC1-8 алкильными группами, -C1-8 алкильными группами, -С2-6 алкенильными группами, -С2-6 алкинильными группами, кетоновыми группами, алкиламино-группами, аминогруппами, арильными группами, С3-8 циклоалкильными группами или гидроксильными группами.
Термин «циклоалкенил», используемый в настоящем документе, относится к одновалентной или двухвалентной группе из 3-10 углеродных атомов, полученной из насыщенного циклоалкила, имеющей одну двойную связь. Циклоалкенильные группы могут быть моноциклическими или полициклическими. Циклоалкенильные группы могут быть независимо замещены атомами галогена, сульфонильными группами, сульфоксидными группами, нитрогруппами, циано-группами, -ОС1-6 алкильными группами, -SC1-6 алкильными группами, -C1-6 алкильными группами, -С2-6 алкенильными группами, -С2-6 алкинильными группами, кетоновыми группами, алкиламиногруппами, арильными группами, С3-8 циклоалкильными группами или гидроксильными группами.
Термин «циклодиен», используемый в настоящем документе, относится к одновалентной или двухвалентной группе из 5-10 углеродных атомов, полученной из насыщенного циклоалкила, имеющей две двойные связи. Циклодиеновые группы могут быть моноциклическими или полициклическими. Циклодиеновые группы могут быть независимо замещены атомами галогена, сульфонильными группами, сульфоксидными группами, нитрогруппами циано-группами, -ОС1-6 алкильными группами, -SC1-6 алкильными группами, -C1-6 алкильными группами, -C2-6 алкенильными группами, - С2-6 алкинильными группами, кетоновыми группами, алкиламино-группами, арильными группами, C3-8 циклоалкильными группами или гидроксильными группами.
Термин «галоген», используемый в настоящем документе, относится к атому хлора, брома, фтора, йода.
Термин «алкенил», используемый в настоящем документе, относится к одновалентному или двухвалентному углеводородному радикалу, имеющему от 2 до 8 углеродных атомов, полученному из насыщенного алкила, имеющему по меньшей мере одну двойную связь. Одна метиленовая (-СН2-) группа алкенильной группы может быть заменена кислородом, серой, сульфоксидом, азотом, карбонилом, карбоксилом, сульфонилом, сульфатом, сульфонатом, амидом, сульфонамидом, двухвалентным С3-8 циклоалкилом, двухвалентным гетероциклом или двухвалентной арильной группой. С2-8 алкенил может быть в конфигурации Ε или Ζ. Алкенильные группы могут быть замещены алкильными группами, описанными выше, или атомами галогена.
Термин «алкинил», используемый в настоящем документе, относится к одновалентному или двухвалентному углеводородному радикалу, имеющему от 2 до 8 углеродных атомов, полученному из насыщенного алкила, имеющему, по меньшей мере, одну тройную связь. Одна метиленовая (-СН2-) группа алкинильной группы может быть заменена кислородом, серой, сульфоксидом, азотом, карбонилом, карбоксилом, сульфонилом, сульфатом, сульфонатом, амидом, сульфонамидом, двухвалентным С3-8 циклоалкилом, двухвалентным гетероциклом или двухвалентной арильной группой. Алкинильные группы могут быть замещены алкильными группами, описанными выше, или атомами галогена.
Термин «гетероцикл», используемый в настоящем документе, относится к 3-10-членному кольцу, которое может быть ароматическим или неароматическим, насыщенным или ненасыщенным, содержащему по меньшей мере один гетероатом, выбранный из кислорода, азота, серы или комбинации по меньшей мере двух из них, которые прерывают карбоциклическую кольцевую структуру. Гетероциклическое кольцо может прерываться фрагментом С=O; гетероатомы S и N могут быть окислены. Гетероциклы могут быть моноциклическими или полициклическими. Гетероциклические кольцевые фрагменты могут быть замещены атомами галогена, сульфонильными группами, сульфоксидными группами, нитрогруппами, циано-группами, -OC1-6 алкильными группами, -SC1-6 алкильными группами, -С1-8 алкильными группами, -С2-6 алкенильными группами, -С2-6 алкинильными группами, кетоновыми группами, алкиламино-группами, арильными группами, С3-8 циклоалкильными группами или гидроксильными группами.
Термин «арил», используемый в настоящем документе, относится к органическому фрагменту, полученному из ароматического углеводорода, состоящего из кольца, содержащего от 6 до 10 углеродных атомов, путем удаления одного атома водорода. Арил может быть замещен атомами галогена, сульфонил C1-6 алкильными группами, сульфоксид С1-6 алкильными группами, сульфонамидными группами, группами карбоновых кислот, C1-6 алкилкарбоксилатными (сложноэфирными) группами, амидными группами, нитрогруппами, циано-группами, -OC1-6 алкильными группами, -SC1-6 алкильными группами, -C1-6 алкильными группами, -С2-6 алкенильными группами, -C2-6 алкинильными группами, кетоновыми группами, альдегидами, алкиламино-группами, аминогруппами, арильными группами, С3-8 циклоалкильными группами или гидроксильными группами. Арилы могут быть моноциклическими или полициклическими.
Термин «гидроксил», используемый в настоящем документе, представляет группу формулы «-ОН».
Термин «карбонил», используемый в настоящем документе, представляет группу формулы «-С(О)-».
Термин «кетон», используемый в настоящем документе, представляет органическое соединение, имеющее карбонильную группу, связанную с атомом углерода, такую как -(CO)Rx, где Rx может быть алкилом, арилом, циклоалкилом, циклоалкенилом, гетероциклом, как описано выше.
Термин «амин», используемый в настоящем документе, представляет группу формулы «-NRxRy», где Rx и Ry могут быть одинаковыми или независимо представлять собой водород, алкил, арил, циклоалкил, циклоалкенил, гетероцикл, как описано выше.
Термин «карбоксил», используемый в настоящем документе, представляет группу формулы «-C(O)O-».
Термин «сульфонил», используемый в настоящем документе, представляет группу формулы «-SO2-».
Термин «сульфат», используемый в настоящем документе, представляет группу формулы «-O-S(O)2-O-».
Термин «сульфонат», используемый в настоящем документе, представляет группу формулы «-S(O)2-O-».
Термин «карбоновая кислота», используемый в настоящем документе, представляет группу формулы «-С(O)ОН».
Термин «нитро», используемый в настоящем документе, представляет группу формулы «-NO2».
Термин «циано», используемый в настоящем документе, представляет группу формулы «-CN».
Термин «амид», используемый в настоящем документе, представляет группу формулы «-C(O)NRxRy», где Rx и Ry могут быть одинаковыми или независимо представлять собой водород, алкил, арил, циклоалкил, циклоалкенил, гетероцикл, как описано выше.
Термин «сложный эфир», используемый в настоящем документе, представляет группу формулы «-C(O)ORx», где Rx представляет собой алкил, арил, циклоалкил, циклоалкенил, гетероцикл, как описано выше.
Термин «сульфонамид», используемый в настоящем документе, представляет группу формулы «-S(O)2NRxRy», где Rx и Ry могут быть одинаковыми или независимо представлять собой водород, алкил, арил, циклоалкил, циклоалкенил, гетероцикл, как описано выше.
Термин «сульфоксид», используемый в настоящем документе, представляет группу формулы «-S(O)-».
Термин «фосфоновая кислота», используемый в настоящем документе, представляет группу формулы «-Р(O)(ОН)2».
Термин «фосфорная кислота», используемый в настоящем документе, представляет группу формулы «-ОР(O)(ОН)2».
Термин «сульфоновая кислота», используемый в настоящем документе, представляет группу формулы «-S(O)2OH».
Формула «Н», используемая в настоящем документе, представляет атом водорода.
Формула «О», используемая в настоящем документе, представляет атом кислорода.
Формула «N», используемая в настоящем документе, представляет атом азота.
Формула «S», используемая в настоящем документе, представляет атом серы.
Соединения настоящего изобретения представляют собой:
(8S,9S,10R,11S,13S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1H-циклопента[а]фенантрен-17-ил (4-бромфенил)ацетат;
(8S,9S,10R,11S,13S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1H-циклопента[а]фенантрен-17-ил 3-(фенилсульфонил)пропаноат;
(8S,9S,10R,11S,13S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1H-циклопента[а]фенантрен-17-ил 2-фуроат.
Некоторые соединения Формулы I и некоторые из их промежуточных соединений имеют в своей структуре по меньшей мере один стереогенный центр. Этот стереогенный центр может присутствовать в конфигурации R или S, упомянутое обозначение R и S используется в соответствии с правилами, описанными в публикации Pure Appli. Chem. (1976), 45, 11-13.
Термин «фармацевтически приемлемые соли» относится к солям или комплексам, которые сохраняют заданную биологическую активность описанных выше соединений и обладают минимальными нежелательными токсикологическими эффектами или не обладают ими. «Фармацевтически приемлемые соли», согласно настоящему изобретению, включают терапевтически активные нетоксичные солевые формы оснований или кислот, которые могут образовывать соединения Формулы I.
Солевая форма присоединения кислоты для соединения Формулы I, которое встречается в свободной форме в виде основания, может быть получена обработкой указанного свободного основания соответствующей кислотой, такой как неорганическая кислота, такая как, например, хлороводородная кислота, бромоводородная кислота, серная кислота, фосфорная кислота, азотная кислота и тому подобные; или органическая кислота, такая как, например, уксусная, гидроксиуксусная, пропановая, молочная, пировиноградная, малоновая, фумаровая кислота, малеиновая кислота, щавелевая кислота, винная кислота, янтарная кислота, яблочная кислота, аскорбиновая кислота, бензойная кислота, дубильная кислота, памоевая кислота, лимонная, метилсульфоновая, этансульфоновая, бензолсульфоновая, муравьиная и тому подобные (Handbook of Pharmaceutical Salts, P. Heinrich Stahal&Camille G. Wermuth (ред.), Verlag Helvetica Chemica Acta-Zürich, 2002, 329-345). Солевая форма присоединения основания соединения Формулы I, которое находится в своей кислотной форме, может быть получена обработкой этой кислоты соответствующим основанием, таким как неорганическое основание, например, гидроксид натрия, гидроксид магния, гидроксид калия, гидроксид кальция, аммиак и тому подобными; или органическим основанием, таким как, например, L-аргинин, этаноламин, бетаин, бензатин, морфолин и тому подобными. (Handbook of Pharmaceutical Salts, P. Heinrich Stahal&Camille G. Wermuth (ред.), Verlag Helvetica Chemica Acta-Zürich, 2002, 329-345).
Соединения Формулы I и их соли могут быть в форме сольвата, которая включена в рамки настоящего изобретения. Такие сольваты включают, например, гидраты, алкоголяты и тому подобные.
В отношении настоящего изобретения, ссылка на соединение или соединения охватывает это соединение в каждой из его возможных изомерных форм и их смесей, если специально не указана конкретная изомерная форма.
Соединения по настоящему изобретению могут существовать в различных полиморфных формах. Хотя это однозначно не указано в представленной выше формуле, такие формы входят в рамки настоящего изобретения.
Соединения, описанные в настоящем документе, пригодная для лечения различных глазных заболеваний, включая, но не ограничиваясь этим, повышенное внутриглазное давление, глаукому, увеит, окклюзию вены сетчатки, дегенерацию желтого пятна, диабетическую ретинопатию, различные формы макулярного отека, послеоперационное воспаление, воспалительные состояния конъюнктивы век и конъюнктивы глазного яблока, роговицы и переднего сегмента глазного яблока, такие как аллергические конъюнктивиты, розовые угри на глазах, сухость глаз, блефариты, отслоение сетчатки, дисфункцию мейбомиевой железы (MGD), точечный поверхностный кератит, кератит с опоясывающим герпесом, ирит, циклит, некоторые инфекционные конъюнктивиты, травму роговицы из-за химического, радиационного или термического ожога, проникновение инородных тел, аллергию или их комбинации.
В других вариантах реализации настоящего изобретения представлены способы лечения расстройств, связанных с модулированием глюкокортикоидных рецепторов (GR) и/или минералокортикоидных рецепторов (MR). Такие способы могут быть осуществлены, например, введением субъекту, нуждающемуся в этом, терапевтически эффективного количества, по меньшей мере, одного соединения настоящего изобретения или любой его комбинации, или его фармацевтически приемлемых солей, гидратов, сольватов, кристаллических форм и отдельных изомеров, энантиомеров и диастереомеров.
В другом варианте реализации представлены фармацевтические композиции, содержащие по меньшей мере одно соединение настоящего изобретения в фармацевтически приемлемом носителе.
Соединения, описанные в настоящем документе, могут быть введены в фармацевтически эффективных дозах. Такие дозы обычно представляют собой минимальную дозу, необходимую для достижения заданного терапевтического эффекта. Как правило, такие дозы находятся в диапазоне от около 1 мг/день до около 1000 мг/день; более предпочтительно, в диапазоне от около 10 мг/день до около 500 мг/день. В другом иллюстративном варианте реализации соединение или соединения могут присутствовать в композиции или рецептуре в диапазоне от около 0,5 мг/кг/день до около 100 мг/кг/день или от около 1 мг/кг/день до около 100 мг/кг/день. Однако фактическое количество соединения, подлежащего введению, в любом конкретном случае определяет лечащий врач, принимающий во внимание релевантные обстоятельства, такие как возраст и вес пациента, общее физическое состояние пациента, тяжесть глазного заболевания и способ введения. В некоторых случаях дозу повышают в индивидуальном порядке.
В другом иллюстративном варианте реализации представлены фармацевтические композиции, содержащие по меньшей мере одно соединение в фармацевтически приемлемом носителе. Фармацевтические композиции могут быть использованы в форме твердого вещества, раствора, эмульсии, дисперсии, мицеллы, липосомы и тому подобного, где полученная композиция содержит одно или более соединений, описанных в настоящем документе, в качестве активного компонента, в смеси с органическим или неорганическим носителем или вспомогательным веществом, пригодным для энтерального или парентерального применения. Одно или более соединений могут быть смешаны, например, с обычными нетоксичными, фармацевтически приемлемыми носителями для таблеток, гранул, капсул, суппозиториев, растворов, эмульсий, суспензий и любых других форм, пригодных для применения. Носители, которые могут быть использованы, включают глюкозу, лактозу, гуммиарабик, желатин, маннит, крахмальный клейстер, трисиликат магния, тальк, кукурузный крахмал, кератин, коллоидный диоксид кремния, картофельный крахмал, мочевину, триглицериды средней длины цепи, декстраны и другие носители, пригодные для использования в производстве препаратов в твердой, полутвердой, или жидкой форме. Кроме того, могут быть использованы вспомогательные вещества, стабилизирующие, загущающие и подкрашивающие средства и отдушки. Соединения, описанные в настоящем документе, включают в фармацевтические композиции в количествах, достаточных для получения заданного эффекта в процессе или состоянии заболевания.
В другом варианте реализации соединения, описанные в настоящем документе, могут быть введены перорально в любой приемлемой форме, такой как таблетки, жидкость, капсулы, порошок и тому подобные. Однако могут быть желательны или необходимы другие способы, в частности, если пациент страдает тошнотой. Такие другие пути могут включать, без исключения, трансдермальный, парентеральный, подкожный, интраназальный, интратекальный, внутримышечный, внутривенный и внутриректальный способы доставки. Дополнительно, могут быть разработаны композиции для замедленного высвобождения активного соединения в течение заданного периода времени, или для тщательного контроля количества высвобожденного лекарства в заданное время в течение курса терапии.
Фармацевтические композиции в форме, пригодной для перорального применения, например, вводят в виде таблеток, пастилок, лепешек, водных или масляных суспензий, диспергируемых порошков или гранул, эмульсий, твердых или мягких капсул, или сиропов, или эликсиров. Композиции, предназначенные для перорального применения, могут быть получены в соответствии с любым способом, известным в данной области для производства фармацевтических композиций, и такие композиции могут содержать один или более агентов, выбранных из группы, состоящей из подсластителей, таких как сахароза, лактоза или сахарин, вкусовых добавок, таких как перечная мята, масло гаультерии или вишни, красители и консервирующие агенты, с целью получения фармацевтически простых и приятных на вкус композиций. Таблетки, содержащие соединения, описанные в настоящем документе, в смеси с нетоксичными фармацевтически приемлемыми вспомогательными веществами также могут быть произведены известными способами.
Фармацевтические композиции могут быть в форме стерильной суспензии для инъекций. Эта суспензия может быть составлена в композицию в соответствии с известными способами, с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих средств. Стерильные препараты для инъекций могут также быть стерильным раствором или суспензией в нетоксичном, приемлемом для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В качестве растворителя или суспендирующей среды обычно используют стерильные нелетучие масла. С этой целью может быть использовано любое безвкусное нелетучее масло, включая синтетические моно- или диглицериды, жирные кислоты (включая олеиновую кислоту), растительные масла природного происхождения, такие как кунжутное масло, кокосовое масло, арахисовое масло, хлопковое масло и так далее, или синтетический жирный наполнитель, такой как этилолеат или тому подобные. При необходимости могут быть включены буферные растворы, консерванты, антиоксиданты и тому подобные.
Соединения изобретения можно также вводить в форме суппозиториев для ректального введения лекарственного средства. Эти композиции могут быть получены посредством смешивания соединений изобретения с подходящим не раздражающим наполнителем, таким как масло какао, синтетические глицеридные эфиры полиэтиленгликолей, которые являются твердыми при обычных температурах, но разжижаются и/или растворяются в ректальной полости с высвобождением лекарственного средства. Фактическое количество соединения, подлежащего введению, в любом конкретном случае определяет лечащий врач, принимающего во внимание релевантные обстоятельства, такие как тяжесть состояния, возраст и вес пациента, общее физическое состояние пациента, причина состояния и способ введения.
В настоящем документе описаны соединения, способные модулировать глюкокортикоидные рецепторы (GR) и/или минералокортикоидные рецепторы (MR). Соединения, описанные в настоящем документе, могут обладать более высокой активацией GR и/или связывающей силой, по сравнению с таким соединением как кортизол. Следовательно, эти соединения могут эффективно лечить глазные показания. Эти соединения могут быть дополнительно метаболизированы ферментами эстеразы в глазах с образованием природного агониста кортизола, уменьшая посредством этого риск глазной гипертензии. Кортизол, оставшийся в глазах и в организме, далее метаболизируется до неактивных соединений природными дегидроксилазами и другими ферментами, обеспечивая безопасный терапевтический подход.
У пациентов природный эндогенный агонист GC кортизол (гидрокортизон) обладает минимальным действием на внутриглазное давление при локальном нанесении в виде глазных капель, по сравнению с синтетическими GC, такими как дексаметазон, преднизолон и флуорометолон (Cantrill et al., 1975). Дополнительное подкрепление общей превосходной безопасности кортизола в качестве терапевтического средства представляет собой тот факт, что различные местные гидрокортизоновые композиции в настоящее время продаются непосредственно потребителям, без рецепта.
Не ограничиваясь какой-либо конкретной теорией, было неожиданно обнаружено, что описанные в настоящем документе соединения могут обладать более высоким модулированием глюкокортикоидного рецептора, чем кортизол, благодаря модификации в 17-положении молекулы кортизола.
При использовании в настоящем документе, термин «терапевтически эффективное количество» означает количество фармацевтической композиции, которое вызывает биологическую или медицинскую реакцию у пациента, нуждающегося в этом, видимую для исследователя, ветеринара, врача или другого клинициста. В некоторых вариантах реализации субъект, нуждающийся в этом, представляет собой млекопитающее. В некоторых вариантах реализации млекопитающее представляет собой человека.
Вспомогательные вещества могут быть, например, (1) инертными разбавителями, такими как карбонат кальция, лактоза, фосфат кальция или фосфат натрия; (2) гранулирующими средствами и средствами для улучшения распадаемости таблеток, такими как кукурузный крахмал, картофельный крахмал или альгиновая кислота; (3) связывающими агентами, такими как трагакантовая камедь, кукурузный крахмал, желатин или гуммиарабик, и (4) смазывающими агентами, такими как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без оболочки или они могут быть покрыты посредством известных методов, чтобы замедлить дезинтеграцию и абсорбцию в желудочно-кишечном тракте и, тем самым, обеспечить пролонгированное действие в течение более длительного периода. Например, для временной задержки может быть использован такой материал как глицерилмоностеарат или глицерилдистеарат.
В некоторых случаях композиции для перорального применения могут быть в форме твердых желатиновых капсул, где соединения смешаны с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином. Они могут быть также в форме мягких желатиновых капсул, где соединения смешаны с водной или масляной средой, например, арахисовым маслом, жидким парафином или оливковым маслом.
Соединения, описанные в настоящем документе, также могут быть введены в виде офтальмически приемлемых рецептур или композиций. Офтальмически приемлемую жидкость смешивают таким образом, чтобы ее можно было наносить локально на глаза. Следует по возможности максимизировать комфорт, несмотря на то, что иногда по соображениям состава композиции (например, стабильности) может потребоваться более низкий уровень комфорта, чем оптимальный. Если комфорт нельзя максимизировать, то жидкую композицию следует составлять так, чтобы жидкость была приемлемой для пациента для местного офтальмического применения. Дополнительно, офтальмически приемлемая жидкость должна быть упакована для разового использования или содержать консервант для предотвращения загрязнения при многократном применении.
Для офтальмических применений, растворы или лекарственные средства часто выпускают с использованием физиологического солевого раствора в качестве основного носителя. pH офтальмических растворов должен предпочтительно поддерживаться на удобном уровне с помощью соответствующей буферной системы. Композиции могут также содержать обычные фармацевтически приемлемые консерванты, стабилизаторы и поверхностно-активные вещества.
Консерванты, которые могут быть использованы в офтальмических композициях, описанных в настоящем документе, включают, но не ограничиваясь этим, бензалкония хлорид, хлорбутанол, тимерозал, фенилртути ацетат и фенилртути нитрат. Подходящее поверхностно-активное вещество включает, например, Tween 80. Точно так же, в офтальмических препаратах, описанных в настоящем документе, могут быть использованы различные пригодные жидкие носители. Эти носители включают, но не ограничиваясь этим, поливиниловый спирт, повидон, гидроксипропилметилцеллюлозу, полоксамеры, карбоксиметилцеллюлозу, гидроксиэтилцеллюлозу и очищенную воду.
Регуляторы тоничности могут быть добавлены по необходимости или для удобства. Они включают, но не ограничиваясь этим, соли, в частности, хлорид натрия, хлорид калия, маннит и глицерин, или другие пригодные офтальмически приемлемые регуляторы тоничности.
Различные буферы и среды для регулирования pH могут быть использованы в тех пределах, в каких полученная композиция остается офтальмически приемлемой. Соответственно, буферы включают ацетатные буферы, цитратные буферы, фосфатные буферы и боратные буферы. Для регулирования pH этих композиции при необходимости могут быть использованы кислоты или основания.
В одном из иллюстративных вариантов реализации офтальмическая композиция, описанная в настоящем документе, может содержать компоненты, используемые в следующих количествах, которые перечислены в Таблице 1.
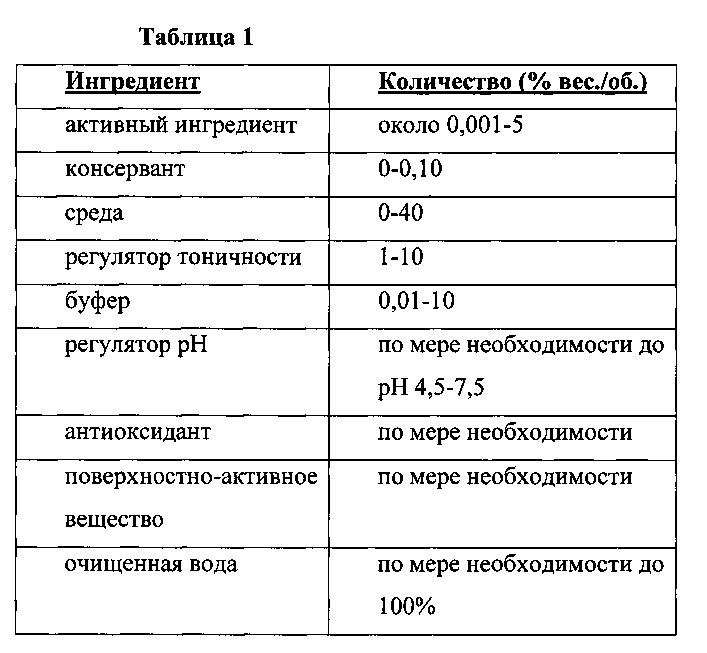
В других вариантах реализации офтальмически приемлемая жидкость может быть составлена в композицию для внутриглазной инъекции. Соединения, описанные в настоящем документе, могут быть составлены в композиции в виде жидкости, гелеобразной пасты или подобных форм для внутриглазной инъекции. Дополнительно, эти соединения могут быть составлены в композиции с устойчивым высвобождением или контролируемым высвобождением внутриглазных имплантатов, содержащих биоразлагаемые полимеры, такие как полимолочная кислота, полигликолевая кислота, их комбинации и тому подобные.
Некоторые иллюстративные композиции могут содержать комбинацию двух или более соединений, описанных в настоящем документе. В зависимости от конкретного глазного заболевания или набора заболеваний, подлежащих лечению, могут быть составлены композиции с различными соотношениями соединений.
Поскольку индивидуальные пациенты могут находиться в широком диапазоне тяжести симптомов, и каждая композиция обладает собственными уникальными терапевтическими характеристиками, то точный способ введения и используемая дозировка для каждого пациента остается на усмотрение лечащего врача.
Настоящее изобретение относится также к способам получения соединений Формулы I. Соединения Формулы I по настоящему изобретению могут быть получены аналогично стандартным способам, понятным специалистам в области синтетической органической химии. Схема синтеза, представленная ниже, иллюстрирует способ получения соединений по настоящему изобретению.
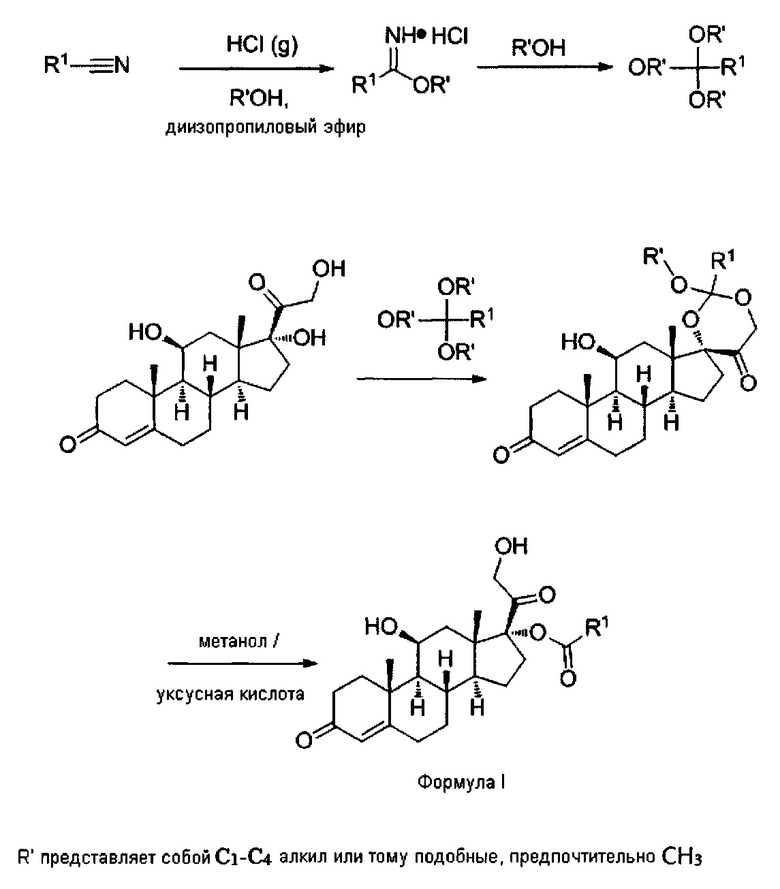
ПОДРОБНОЕ ОПИСАНИЕ
Следует понимать, что изложенное выше общее описание и следующее подробное описание являются лишь примерными и пояснительными, и не ограничивают заявленное изобретение. При использовании в настоящем документе, применение единственного числа включает множественное число, если специально не оговорено иное.
Специалистам в данной области очевидно, что некоторые из соединений по настоящему изобретению могут содержать один или несколько асимметричных центров, так что эти соединения могут существовать в энантиомерных, а также в диастереомерных формах. Если специально не указано иное, то в рамки настоящего изобретения входят все энантиомеры, диастереомеры и рацемические смеси. Некоторые из соединений по настоящему изобретению могут образовывать соли с фармацевтически приемлемыми кислотами или основаниями, и такие фармацевтически приемлемые соли соединений, описанных в настоящем документе, также входят в рамки настоящего изобретения.
Настоящее изобретение включает все фармацевтически приемлемые соединения, обогащенные изотопами. Любое соединение настоящего изобретения может содержать один или более изотопных атомов, обогащенных или отличающихся от природного соотношения, таких как дейтерий 2H (или D) вместо протия 1H (или Н), или использовать 13C-обогащенный материал вместо 12С, и тому подобные. Аналогичное замещение может быть использовано для Ν, О и S. Применение изотопов может способствовать аналитическим, а также терапевтическим аспектам настоящего изобретения. Например, применение дейтерия может повышать период полувыведения in vivo за счет изменения метаболизма (скорости) соединений настоящего изобретения. Эти соединения могут быть получены по описанным способам получения с использованием реагентов, обогащенных изотопами.
Следующие примеры представлены лишь для иллюстративных целей и не предназначены и не должны толковаться как ограничивающие настоящее изобретение каким-либо образом. Специалистам в данной области понятно, что могут быть сделаны различные изменения и модификации следующих примеров, не выходя за пределы общей идеи или рамок настоящего изобретения.
Специалистам в данной области очевидно, что индивидуальные изомерные формы могут быть получены разделением их смесей обычным образом. Например, в случае диастереоизомерных изомеров может быть использовано хроматографическое разделение.
Названия соединений были получены при помощи программы ACD версии 12.0; а названия Промежуточных соединений и реагентов, используемых в примерах, были получены при помощи таких программ как Chem Bio Draw Ultra версии 12.0 или Auto Nom 2000 из MDL ISIS Draw 2.5 SP1.
В общем, описание соединений выполнили по следующим способам:
Спектры ЯМР были записаны на приборе Varian 300 и/или 600 МГц и получены при комнатной температуре. Химические сдвиги даны в миллионных долях по отношению к внутреннему сигналу тетраметилсилана или к сигналу растворителя.
Все реагенты, растворители, катализаторы, для которых не описан синтез, были закуплены у поставщиков химических реактивов, таких как Sigma Aldrich, Fluka, Bio-Blocks, Combi-blocks, TCI, VWR, Lancaster, Oakwood, Trans World Chemical, Alfa, Fisher, AK Scientific, AmFine Com, Carbocore, Maybridge, Frontier, Matrix, Ukrorgsynth, Toronto, Ryan Scientific, SiliCycle, Anaspec, Syn Chem, Chem-Impex, MIC-scientific, Ltd; хотя некоторые известные промежуточные соединения были получены по опубликованным методикам.
Как правило, соединения по настоящему изобретению были очищены колоночной хроматографией (автоматическая жидкостная флэш-хроматография) на Teledyne-ISCO CombiFlash с колонкой из диоксида кремния, если не указано иное.
Пример 1
Промежуточное соединение 1
2-(Триметоксиметил)фуран
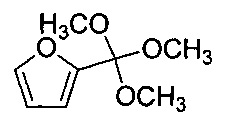
Безводный раствор HCl в метаноле приготовили медленным добавлением ацетилхлорида (10,5 мл) к метанолу (20 мл) при комнатной температуре. Раствор перемешивали в течение 2 часов. После охлаждения на ледяной бане под азотом, через шприц добавили 2-фуронитрил (12 мл, 137 мМ). Реакционную смесь перемешивали в сухой атмосфере при 0°C в течение ночи. После нагревания до комнатной температуры промежуточное соединение осадили добавлением сухого эфира (50 мл).
Его отфильтровали через сухую стеклянную фильтровальную воронку в сухую емкость и промыли сухим эфиром. После выпаривания эфира твердое вещество обработали сухим метанолом и перемешивали при 50°C в течение 70 часов. Смесь обработали сухим эфиром (60 мл), а хлорид аммония удалили фильтрацией через сухую стеклянную фильтровальную воронку. В результате концентрирования фильтрата получили указанное в заголовке соединения (6 г) в виде бесцветного маслянистого вещества.
Пример 2
Промежуточное соединение 2
(8S,9S,10R,11S,13S,14S,17R)-2'-(2-фурил)-11-гидрокси-2'-метокси-10,13-диметил-1,6,7,8,9,10,11,12,13,14,15,16-додекагидро-5'H-спиро[циклопента[а]фенантрен-17,4'-[1,3]диоксан]-3,5'(2Н)-дион
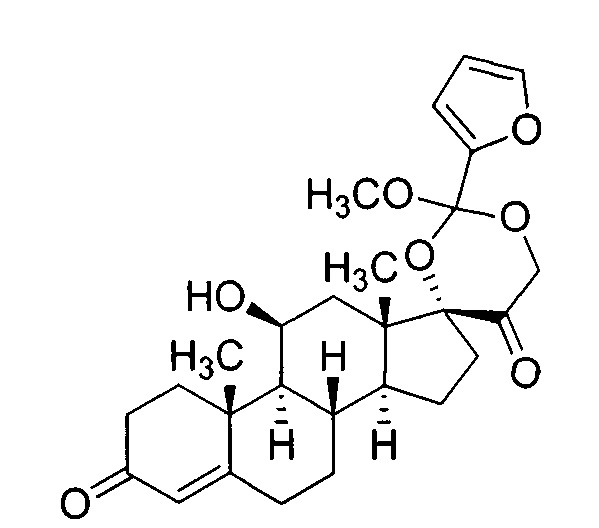
Раствор кортизола (10,4 г, приблизительно 28 мМ), высушенный выпариванием из этанола-бутанола) в сухом тетрагидрофуране (40 мл) обработали неочищенным Промежуточным соединением 1 (5,4 г, 32 мМ) и 0,5 мл раствора безводной п-толуолсульфоновой кислоты в толуоле (приблизительно 0,7 М). Реакционную смесь перемешивали при комнатной температуре в течение 48 часов. Добавили дополнительное количество сухого ТГФ (100 мл) и безводного раствора p-TSA (2 мл) и перемешивали реакционную смесь в течение 48 часов. Реакционную смесь частично концентрировали и перемешивали еще одну ночь. Реакционную смесь разделили между этилацетатом и водным раствором двухосновного фосфата натрия. Органический слой промыли насыщенным солевым раствором, высушили и выпарили. Остаток очистили хроматографией (силикагель, 30-70 этилацетата в дихлорметане) и получили Промежуточное соединение 2 (0,9 г).
Пример 3
Соединение 1
(8S,9S,10R,11S,113S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Н-циклопента[а]фенантрен-17-ил 2-фуроат
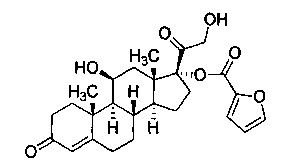
Промежуточное соединение 1 растворили в тетрагидрофуране (20 мл) и охладили на бане изо льда и соленой воды под инертной атмосферой. Раствор обработали 0,37 мл 1 M водного раствора серной кислоты. Реакционную смесь перемешивали на холоду в течение 2 часов. Реакционную смесь обработали раствором двухосновного фосфата натрия и этилацетатом. Этилацетатный раствор промыли насыщенным солевым раствором, высушили и выпарили. Продукт очистили хроматографией (силикагель 60, 50-50 этилацетата-дихлорметана) и концентрировали. Остаток кристаллизовали из дихлорметана - гексана с получением Соединения 1 (1,9 г, 82%).
ЯМР (CDCl3, ТМС): δ 1.00 (s, 3Н), 1.13 (m, 3Н), 1.47 (s, 3Н), 1.51 (m, 1H), 2.54-1.74 (m's, 13H), 2.90 (m, 1H), 3.08 (m, 1H), 4.37 (m, 2H), 4.56 (m, 1H), 5.71 (s, 1H), 6.54 (m, 1H), 7.20 (m, 1H), 7.61 (m, 1H).
Пример 4
Промежуточное соединение 3
Метил 2-(4-бромфенил)ацетимидата гидрохлорид

Таким же образом, как описано в Примере 1, 2-(4-бромфенил)ацетонитрил преобразовали в Промежуточное соединение 3. Полученный остаток не обрабатывали метанолом, а выделили с получением Промежуточного соединения 3.
Пример 5
Промежуточное соединение 4
(8S,9S,10R,11S,13S,14S,17R)-2'-(4-бромбензил)-11-гидрокси-2'-метокси-10,13-диметил-1,6,7,8,9,10,11,12,13,14,15,16-додекагидро-5'H-спиро[циклопента[а]фенантрен-17,4'-[1,3]диоксан]-3,5'(2H)-дион
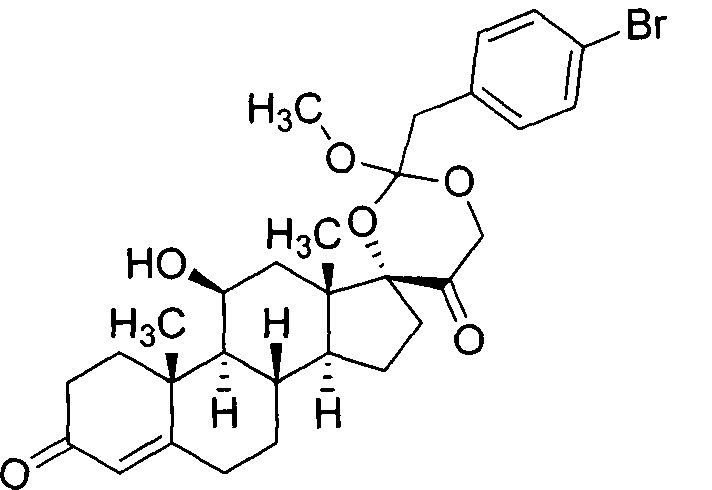
Таким же образом, как описано в Примере 2, кортизол и Промежуточное соединение 3 преобразовали в Промежуточное соединение 4. В результате очистки силикагелевой флэш-хроматографией (элюирование 20% этилацетата в CH2CI2) получили 24,8 мг Промежуточного соединения 4: ICMS-ESI (m/z): рассчитано для C30H37BrO6, 572, 574,; [М+Н]+ найдено 573, 575.
Пример 6
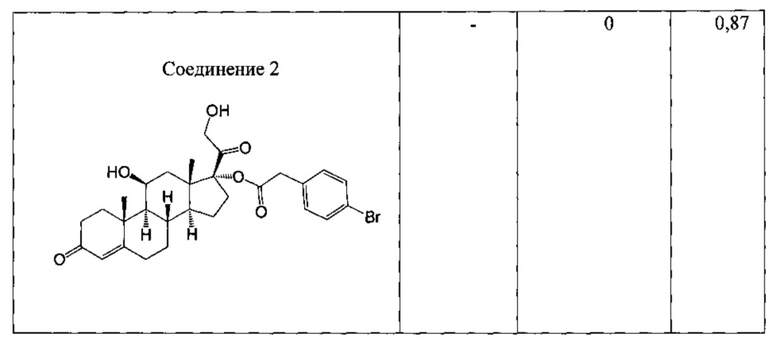
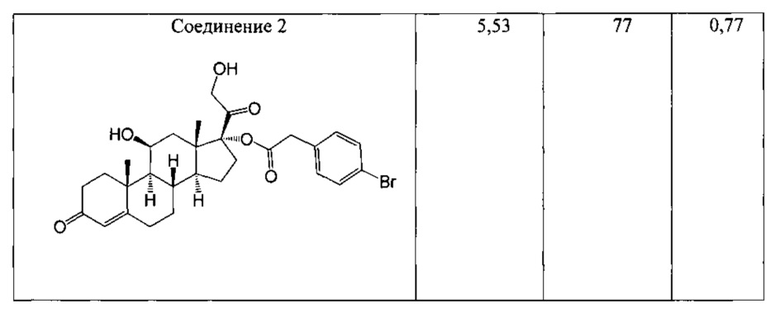
Соединение 2
(8S,9S,10R,11S,13S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Н-циклопента[а]фенантрен-17-ил(4-бромфенил)ацетат
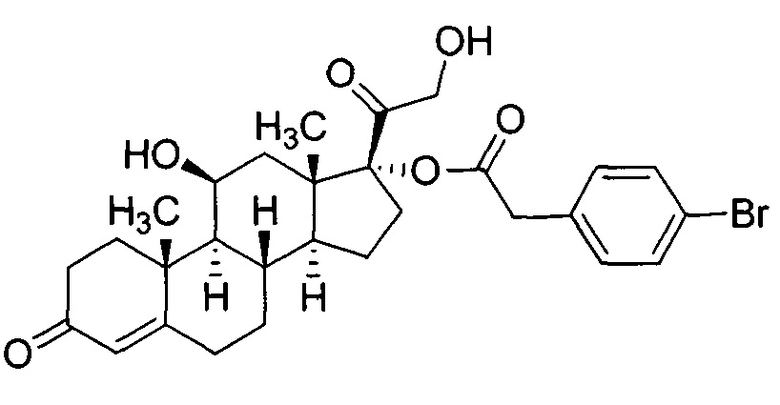
Таким же образом, как описано в Примере 3, Промежуточное соединение 4 преобразовали в Соединение 2. В результате очистки неочищенной реакционной смеси силикагелевой хроматографией (20% этилацетата, метиленхлорид) получили 57,7 мг Соединения 2.ICMS-ESI (m/z): рассчитано для C29H35BrO6, 558, 560; [М+Н]+ найдено 559, 561.
Пример 7
Промежуточное соединение 5
(8S,9S,10R,11S,13S,14S,17R)-2'-этокси-11-гидрокси-10,13-диметил-2'-[2-(фенилсульфонил)этил]-1,6,7,8,9,10,11,12,13,14,15,16-додекагидро-5'H-спиро[циклопента[а]фенантрен-17,4'-[1,3]диоксан]-3,5'(2Н)-дион
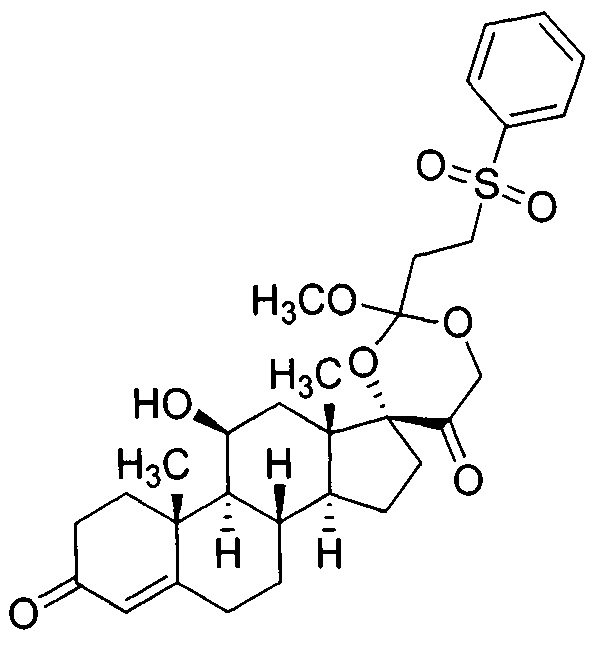
Таким же образом, как описано в Примере 2, кортизол и ((3,3,3-триметоксипропил)сульфонил)бензол преобразовали в Промежуточное соединение 5. В результате очистки неочищенной реакционной смеси силикагелевой хроматографией
(20% этилацетата, метиленхлорид) получили 13,1 мг Промежуточного соединения 5. LCMS-ESI (m/z): рассчитано для C32H42O8S, 586; [М+Н]+ найдено 587.
Пример 8
Соединение 3
(8S,9S,10R,11S,13S,14S,17R)-17-гликолоил-11-гидрокси-10,13-диметил-3-оксо-2,3,6,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Н-циклопента[а]фенантрен-17-ил 3-(фенилсульфонил)пропаноат
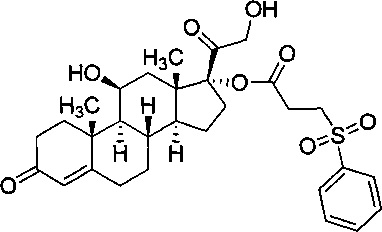
Таким же образом, как описано в эксперименте в Примере 3, Промежуточное соединение 5 преобразовали в указанное в заголовке соединение. В результате очистки неочищенной реакционной смеси силикагелевой хроматографией (20% этилацетата, метиленхлорид) получили 96,9 мг Соединения 3. LCMS-ESI (m/z): рассчитано для C30H38O6S, 558; [М+Н]+ найдено 559.
Пример 9
Активность трансактивации глюкокортикоидного рецептора для кортизола и 17-эфирных производных
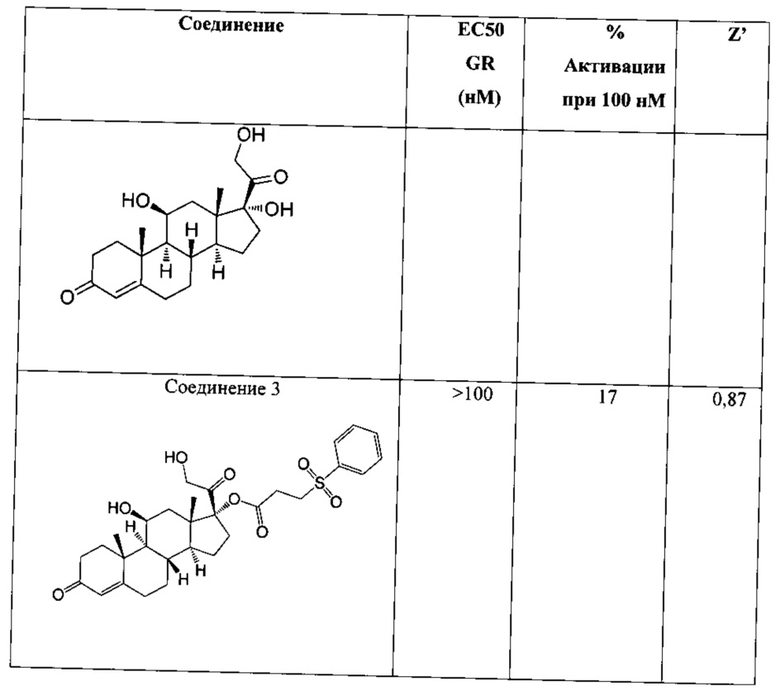
Активирующую активность в отношении глюкокортикоидного рецептора (GR) оценили с помощью клеточной линии HeLa, содержащей MMTV-bla репортер (MMTV-bla HeLa CELLSENSOR®, Invitrogen Corp., Карлсбад, штат Калифорния). Клеточную линию устойчиво трансфицировали экспрессионным конструктом, содержащим кДНК β-лактамазы, управляемым чувствительным элементом, ранее идентифицированным как чувствительный элемент глюкокортикоидного рецептора. Результаты одного из экспериментов, выполненного в двух экземплярах для исследуемых соединений и контрольного соединения, дексаметазона, представлены в Таблице 2. Все анализы выполнили в 10-точечных дозозависимых эффектах, используя серии полулогарифмических разбавлений, начиная с максимальной концентрации соединения 100 нМ. Соединения инкубировали в течение 5 часов. Активация эндогенного GR приводит к экспрессии репортерной β-лактамазы, которую обнаруживают превращением субстрата FRET в формате логометрического анализа. Этот функциональный анализ позволяет измерять рецепторный агонизм соединений и может быть использован для определения активности и селективности соединения. Воспроизводимость анализа определили расчетом значений Z' для необработанных образцов по сравнению с максимальным стимулированием. Значение Z' было более 0,6, указывая на хорошую воспроизводимость данного аналитического формата.
Несколько соединений продемонстрировали дозозависимое стимулирование сигнального пути GR (Таблица 2). Два соединения, кортизол 17-циклопентаноат и кортизол 17-бензоат, продемонстрировали примерно в 30 раз более высокую активность, по сравнению с исходной молекулой кортизола.

Пример 10
Активность трансактивации минералокортикоидного рецептора для кортизола и 17-эфирных производных
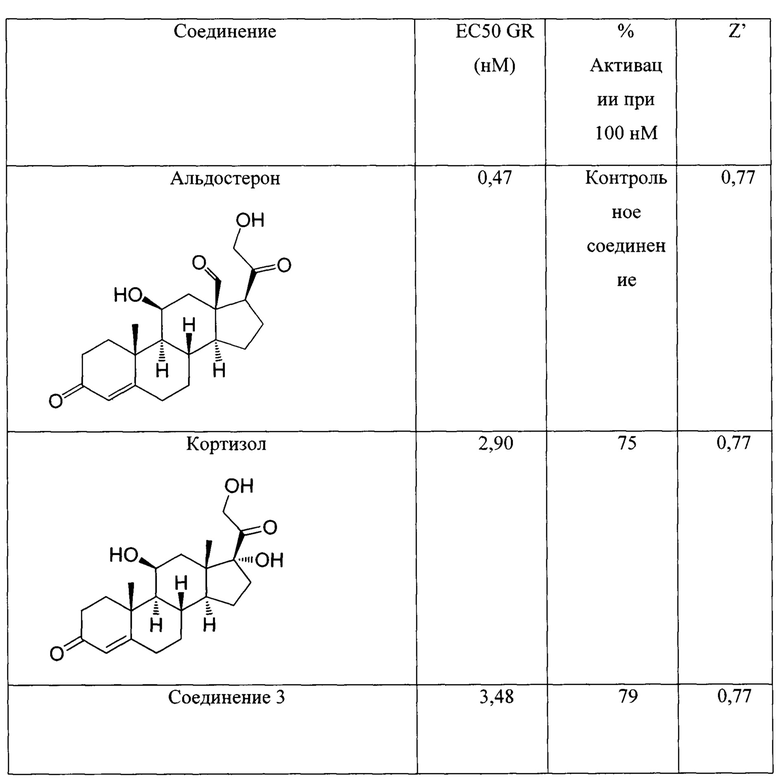
Активирующую активность в отношении минералокортикоидного рецептора (MR) оценили с помощью клеточной линии HEK 293Т, содержащей UAS-bla репортер (UAS-bla HEK 293Т CELLSENSOR®). Эту клеточную линию устойчиво котрансифицировали с экспрессионным конструктом, содержащим кДНК β-лактамазы под управлением активирующей последовательности (UAS) и другого экспрессионного конструкта, кодирующего для гибридного белка GAL4(DBD)-MR(LBD). Результаты одного из экспериментов, выполненного в двух экземплярах для новых соединений и контрольного соединения, альдостерона, в режиме агонистов, представлены в Таблице 2. Все анализы выполнили в 10-точечных дозозависимых эффектах, используя серии полулогарифмических разбавлений, начиная с максимальной концентрации соединения 100 нМ. Соединения инкубировали в течение 16 часов. Активация гибридного белка GAL4(DBD)-MR(LBD) приводит к экспрессии репортерной β-лактамазы, которую обнаруживают превращением субстрата FRET в формате логометрического анализа. Этот функциональный анализ позволяет измерять рецепторный агонизм соединений и может быть использован для определения активности и селективности соединения. Воспроизводимость анализа определили расчетом значений Z' для необработанных образцов по сравнению с максимальным стимулированием. Значение Z' было более 0,6, указывая на хорошую воспроизводимость данного аналитического формата. Несколько соединений продемонстрировали дозозависимое стимулирование сигнального пути MR (Таблица 3).
Таблица 3. Активность минералокортикоидного рецептора. Представлены значения ЕС50 (нМ) и Z' для контрольного соединения, альдостерона, и соединений, испытанных в режиме агонистов.
I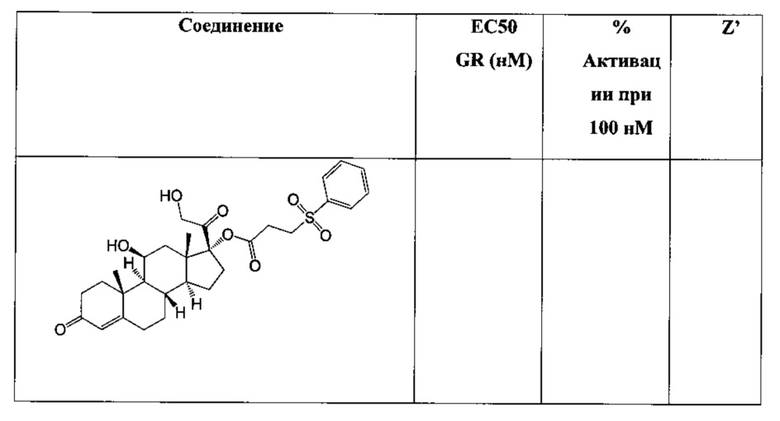
Пример 11
Лечение повышенного внутриглазного давления
58-Летний мужчина пришел к офтальмологу для обычного осмотра. Врач обнаружил, что у пациента наблюдается повышенное внутриглазное давление и существует высокий риск дальнейших осложнений. Пациенту прописали применение местной жидкой композиции, содержащей одно из соединений в Таблице 1, один раз в день в каждый глаз.
Пациент вернулся для следующего осмотра через три месяца. При измерении внутриглазного давления было отмечено, что у пациента наблюдается сниженное внутриглазное давление.
Пример 12
Лечение глазного раздражения
38-Летний мужчина пришел к офтальмологу с жалобой на раздражение в правом глазу. Врач обнаружил, что правый глаз пациента воспален и покраснел. Пациенту прописали применение местной жидкой композиции, содержащей одно из соединений в Таблице 1, дважды в день в правый глаз.
Пациент вернулся для следующего осмотра через неделю. При осмотре правого глаза было отмечено, что покраснение исчезло, а пациент указал, что раздражение прошло.
Если не указано иное, все числа, выражающие количества компонентов, свойства, такие как молекулярный вес, условия реакции и так далее, используемые в описании и формуле изобретения, следует понимать как измененные во всех случаях термином «около». Соответственно, если не указано иное, числовые параметры, представленные в описании и приложенной формуле изобретения, представляют собой приближения, которые могут варьироваться в зависимости от заданных свойств, которые могут быть получены с помощью настоящего изобретения. По крайней мере, но не в качестве попытки ограничить применение принципа эквивалентов до рамок формулы изобретения, каждый числовой параметр должен толковаться по меньшей мере в свете числа представленных значащих цифр и путем применения обычных стандартных методик. Несмотря на то, что числовые диапазоны и параметры, представленные выше в широком описании настоящего изобретения, являются приближениями, числовые значения, представленные выше в конкретных примерах, записаны максимально точно. Однако любое числовое значение, по сути, содержит определенные ошибки, неизбежно возникающие из стандартных отклонений, содержащихся в их соответствующих испытательных измерениях.
Термины в единственном числе, используемые в контексте описания настоящего изобретения (особенно в контексте следующей формулы изобретения) следует толковать как включающие единственное и множественное число, если в настоящем документе не указано иное, или очевидно не опровергается контекстом. Перечисление диапазонов значений в настоящем документе служит только в качестве сокращенного способа индивидуального упоминания каждого отдельного значения, входящего в этот диапазон. Если в настоящем документе не указано иное, то каждое отдельное значение является включенным в настоящее описание так, как если бы оно было упомянуто индивидуально. Все способы, описанные в настоящем документе, могут быть выполнены любым подходящим образом, если в настоящем документе не указано иное, или если очевидно не опровергается контекстом. Применение любого или всех примеров, или иллюстративной формулировки (например, «такой как»), представленных в настоящем документе, предназначено только для лучшего освещения настоящего изобретения и не предназначено для ограничения рамок настоящего изобретения, заявленных другим образом. Никакие формулировки настоящего описания не следует толковать как указывающие на не заявленный элемент, существенный для практического осуществления настоящего изобретения.
Группировку альтернативных элементов или вариантов воплощения настоящего изобретения, описанных в настоящем документе, не следует толковать как ограничения. Каждый член группы может быть упомянут и заявлен индивидуально или в любой комбинации с другими членами этой группы или другими элементами, представленными в настоящем документе. Предусматривается, что один или более членов группы могут быть включены или исключены из группы по соображениям удобства и/или патентоспособности. При возникновении любого такого включения или исключения, подразумевается, что настоящее описание содержит эту группу в модифицированном виде, осуществляя, таким образом, письменное описание всех групп Маркуша, используемых в приложенной формуле изобретения.
В настоящем документе описаны некоторые варианты реализации настоящего изобретения, включая наилучший способ, известный авторам изобретения для осуществления настоящего изобретения. Конечно, при прочтении вышеизложенного описания специалистам в данной области станут очевидны варианты этих описанных вариантов реализации. Авторы изобретения ожидают, что опытные специалисты осуществят такие варианты надлежащим образом, и авторы изобретения полагают, что настоящее изобретение может быть осуществлено на практике другим способом, чем конкретно описано в настоящем документе. Соответственно, настоящее изобретение включает все модификации и эквиваленты предмета обсуждения, изложенного в формуле изобретения, приложенной к этому документу, насколько допускается применимыми правовыми нормами. Более того, любые комбинации описанных выше элементов во всех возможных вариациях являются включенными в настоящее изобретение, если в настоящем документе не указано иное, или если это очевидно не опровергается контекстом.
[0001] В завершение, следует понимать, что варианты реализации настоящего изобретения, описанные в настоящем документе, являются иллюстрациями принципов настоящего изобретения. Другие модификации, которые могут быть использованы, входят в рамки настоящего изобретения. Так, в качестве примера, но не ограничения, альтернативные конфигурации настоящего изобретения могут быть использованы в соответствии с указаниями, представленными в настоящем документе. Соответственно, настоящее изобретение не ограничивается в точности тем, что показано и описано в настоящем документе.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ ПРОИЗВОДНЫХ 4-ПРЕГЕНЕН-11β-17-21-ТРИОЛ-3,20-ДИОНА | 2012 |
|
RU2683775C2 |
| ЛЕЧЕНИЕ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ ГЛЮКОКОРТИКОИДНЫХ И МИНЕРАЛОКОРТИКОИДНЫХ РЕЦЕПТОРОВ | 2015 |
|
RU2718921C2 |
| САМОЭМУЛЬГИРУЮЩИЕСЯ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВ (SEDDS) ДЛЯ ДОСТАВКИ ОФТАЛЬМОЛОГИЧЕСКОГО ЛЕКАРСТВА | 2016 |
|
RU2746083C2 |
| ПИРИМИДИНЦИКЛОГЕКСИЛЬНЫЕ МОДУЛЯТОРЫ ГЛЮКОКОРТИКОИДНЫХ РЕЦЕПТОРОВ | 2012 |
|
RU2599253C2 |
| ПРОИЗВОДНЫЕ ТРИЦИКЛИЧЕСКОГО ЛАКТАМА В КАЧЕСТВЕ ИНГИБИТОРОВ 11-β-ГИДРОКСИСТЕРОИДНОЙ ДЕГИДРОГЕНАЗЫ | 2005 |
|
RU2386617C2 |
| ЦИКЛИЧЕСКИЕ ПУРИНОВЫЕ ДИНУКЛЕОТИДЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ STING | 2016 |
|
RU2722019C2 |
| ПРОИЗВОДНЫЕ АРИЛМОЧЕВИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ N-ФОРМИЛПЕПТИДНОГО-1 РЕЦЕПТОРА (FPRL-1) | 2012 |
|
RU2627271C2 |
| ПРОИЗВОДНЫЕ N-МОЧЕВИНОЗАМЕЩЕННЫХ АМИНОКИСЛОТ КАК МОДУЛЯТОРЫ ФОРМИЛ-ПЕПТИДНОГО РЕЦЕПТОРА | 2014 |
|
RU2696581C2 |
| АГОНИСТ ГЛЮКОКОРТИКОИДНОГО РЕЦЕПТОРА И ЕГО ИММУНОКОНЪЮГАТЫ | 2017 |
|
RU2745748C2 |
| НЕСТЕРОИДНЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРОВ ГЛЮКОКОРТИКОИДОВ | 2006 |
|
RU2420528C2 |
Изобретение относится к новым производным Формулы I, а также к фармацевтическим композициям на их основе. Технический результат: получены новые соединения, обладающие агонистической активностью в отношении глюкокортикоидных или минералокортикоидных рецепторов, которые могут быть использованы для лечения расстройств, связанных с модулированием глюкокортикоидного или минералокортикоидного рецептора, например сухости глаз. 4 н. и 6 з.п. ф-лы, 3 табл., 12 пр.
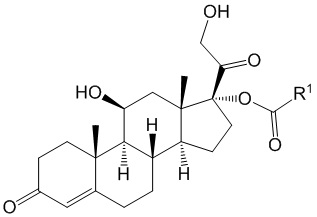 I
I
1. Соединение, имеющее Формулу I, его энантиомеры, диастереоизомеры или фармацевтически приемлемые соли,
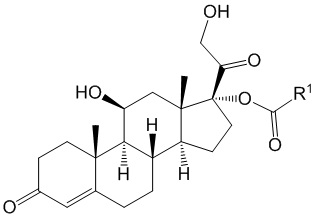 ,
,
Формула I
где R1 представляет собой:
 ,
,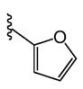 или
или 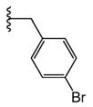 .
.
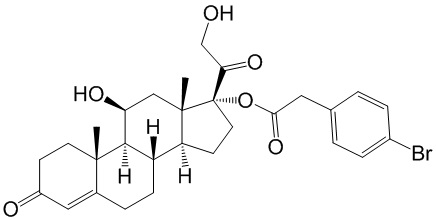
2. Соединение по п. 1, имеющее структуру
 .
.
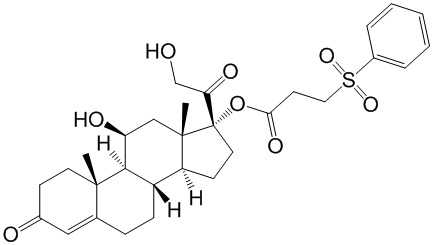
3. Соединение по п. 1, имеющее структуру
 .
.
4. Соединение по п. 1, имеющее структуру
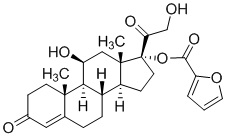 .
.
5. Фармацевтическая композиция для лечения расстройства, связанного с модулированием глюкокортикоидного или минералокортикоидного рецептора, содержащая в качестве активного ингредиента терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый адъювант, разбавитель или носитель.
6. Фармацевтическая композиция по п. 5, отличающаяся тем, что соединение выбрано из:
 ,
,  и
и  .
.
7. Способ лечения расстройства, связанного с модулированием глюкокортикоидного рецептора, который включает введение пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одного соединения Формулы I

Формула I
где R1 представляет собой:
 или
или  .
.
8. Способ лечения расстройства, связанного с модулированием минералокортикоидного рецептора, который включает введение пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одного соединения Формулы I

Формула I
где R1 представляет собой:
 или
или  .
.
9. Способ по п. 7, отличающийся тем, что указанное расстройство представляет собой сухость глаз.
10. Способ по п. 8, отличающийся тем, что указанное расстройство представляет собой сухость глаз.
| US4242334 A, 30.12.1980 | |||
| ЗАМЕЩЕННЫЕ КОРТИКОИД-17-АЛКИЛКАРБОНАТЫ, СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ КОРТИКОИД-17-АЛКИЛКАРБОНАТОВ | 1991 |
|
RU2060997C1 |
| US3984544 A, 05.10.1976 | |||
| US3484436 A, 16.12.1969 | |||
| US3557162 A, 19.01.1971 | |||
| WO2005099715 A2, 27.10.2005 | |||
| ПРОИЗВОДНЫЕ ФУЗИДОВОЙ КИСЛОТЫ, СТЕРЕОИЗОМЕР, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОЕДИНЕНИЯ | 2000 |
|
RU2257391C2 |
Авторы
Даты
2019-05-20—Публикация
2012-11-09—Подача