Изобретение относится к медицине, а именно к экспериментальным исследованиям в онкологии, а также к фармации и может быть использовано в доклинических испытаниях противоопухолевых лекарственных средств посредством оценки их влияния на процесс образования аутофагосом опухолевых клеток в культуре.
Поиск и разработка новых способов оценки эффективности противоопухолевых лекарственных средств в медицине и фармации обусловлены необходимостью их всестороннего испытания, направленного на определение механизмов, за счет которых реализуется противоопухолевый эффект.
После Нобелевской премии 2016 г., полученной Ёсинори Осуми, исследовавшим аутофагию в дрожжевых клетках с помощью генетического подхода, и выяснения молекулярных механизмов индукции, протекания и регуляции аутофагии, стало очевидно, что индукцию аутофагии можно генетически контролировать, что, в свою очередь, открыло другой подход к созданию эффективных противоопухолевых средств, а именно: разработке лекарственных средств, ингибирующих цитопротекторную аутофагию.
Как известно, аутофагия (как один из возможных путей программируемой клеточной гибели) - это процесс, при котором внутренние компоненты клетки доставляются внутрь ее лизосом или вакуолей и подвергаются в них деградации. В неопухолевых клетках аутофагия инициируется, например, токсическим стрессом или в условиях обеднения среды питательными веществами и направлена на избавление клеток от ненужных органелл, а также и организма от ненужных клеток (Farrugia G, Balzan R. Oxidative stress and programmed cell death in yeast (Front Oncol.). - 2012. - T. 2, вып. 64. - DOI: 10.3389/fonc. 2012.00064). В то время, как в опухолевых клетках на определенном этапе аутофагия может стать цитопротекторной и способствовать формированию их резистентности к химиотерапии за счет деградации поврежденных в результате воздействия органелл и других компонентов клетки, что приводит к быстрой прогрессии заболевания. Следовательно, при лечении онкологических заболеваний важна разработка лекарственных средств, ингибирующих цитопротекторную аутофагию. Такой способностью могут обладать и уже известные противоопухолевые средства.
Так, например, нами установлено, что экстракт аврана лекарственного, обладающий противоопухолевым действием (Патент на изобретение RUS 2519769 21.03.2013. Средство, обладающее противоопухолевым и иммуномодулирующим действием. Полуконова Н.В., Наволокин Н.А., Дурнова Н.А., Маслякова Г.Н., Бучарская А.Б.) относится также и к средствам, обладающим избирательным действием на опухолевые клетки, активирующим их апоптоз и препятствующим формированию их резистентности за счет ингибирования цитопротекторной аутофагии (направлена заявка на изобретение. Средство, обладающее избирательным действием на опухолевые клетки, активирующее их апоптоз и препятствующее формированию их резистентности. Полуконова Н.В., Наволокин Н.А., Мудрак Д.А., Полуконова А.В., Бучарская А.Б., Маслякова Г.Н.). Так, на фиг. 1А видно, что под действием экстракта аврана количество клеток с аутофагосомами, выраженное в процентах, находится в обратной корреляции как с количеством мертвых клеток, также выраженным в процентах, так и с концентрацией экстракта.
В то время, как другой противоопухолевый экстракт - бессмертника песчаного {Наволокин К.А., Полуконова Н.В., Маслякова Г.Н., Скворцова В.В., Байтман Т.П., Бучарская А.Б., Дурнова НА. Противоопухолевая активность растительных экстрактов, содержащих биофлавоноиды // Российский биотерапевтический журнал. 2013. Т. 12. №2. С. 59-59; Наволокин Н.А., Мудрак Д.А., Матвеева О.В., Тычина С.А., Бучарская А.Б., Полуконова К.В., Маслякова Г.Н. Влияние растительных экстрактов, содержащих флавоноиды, на лейкоцитарную формулу и красный костный мозг лабораторных крыс с перевитой саркомой 45 // Успехи современного естествознания. 2015. №4. С. 134-140; Наволокин Н.А., Мудрак Д.А., Полуконова К.В., Тычина С.А., Канаева Т.В., Бучарская А.Б., Маслякова Г.Н. Антикахексическая и противоопухолевая активность флавоноидсодержащего экстракта бессмертника песчаного (Helichnysum arenarium) при пероралъном введении крысам с перевитой саркомой-45 // Злокачественные опухоли. 2016. №4-S1 (20). С. 329-330) не формирует резистентность опухолевых клеток за счет ингибирования цитопротекторной аутофагии. На фиг. 1Б при действии экстракта бессмертника не было выявлено корреляции как между количеством клеток с аутофагосомами и количеством мертвых клеток, так и количеством клеток с аутофагосомами и концентрацией экстракта, что связано с отсутствием у этого экстракта свойства ингибировать аутофагию.
Необходима разработка способа оценки, позволяющего определить минимально эффективную концентрацию противоопухолевого средства в преодолении формирования резистентности опухолевых клеток за счет ингибирования цитопротекторной аутофагии.
Модели in vitro с использованием культур клеток и биохимических показателей на клеточном уровне в последнее время находят все более широкое применение в различных областях биомедицинских исследований и получают постепенное признание регулирующих организаций в качестве замены тестов на животных. Тестирование в экспериментах in vitro позволяет провести отбор из множества препаратов и служит важным этапом, целью которого является получение первичной информации о противоопухолевом действии лекарственных средств, и составляет основу правильного выбора схем применения химиопрепаратов при проведении как адъювантной, так и неоадъювантной химиотерапии.
Известен способ оценки цитотоксической активности противоопухолевых средств по выживаемости клеток с помощью стандартного МТТ-теста (колориметрический тест для оценки метаболической активности клеток) с использованием МТТ-реагента (3, 4, 5-диметилтиазол-2-ил-2,5-дифенилтетразолиум бромид). Метод основан на способности дегидрогеназ живых, метаболически активных клеток восстанавливать МТТ- реагент до голубых нерастворимых кристаллов формазана (Mosmann, Tim (December 1983). «Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays». Journal of Immunological Methods 65 (1-2): 55-63). Восстановление МТТ и других тетразолиевых красителей зависит от клеточной метаболической активности из-за тока НАДФ-Н. Быстро делящиеся клетки, к которым могут относиться не только опухолевые клетки, показывают высокую степень восстановления МТТ.
Недостатком способа является то, что он неспецифичен и может использоваться для определения цитотоксичности не только противоопухолевых средств, полученные с помощью этого теста результаты не позволяют определить эффективные концентрации противоопухолевого лекарственного средства в преодолении формирования резистентности опухолевых клеток, кроме того из-за того, что способ отражает только состояние дыхания клеток, он не всегда адекватно говорит о цитотоксичности.
Известен способ оценки противоопухолевых средств (Патент РФ «Способ скрининга противоопухолевых препаратов- ингибиторов PARP1 на основе биохимических методов анализа» опубликовано в Бюл. 14.06.17 г.; Lili Zhai, ShuaiLi, HuilanLi, Yi Zheng, Ronggang Lang, Yu Fan, Feng Gu, Xiaojing Guo, Xinmin Zhang, Li Fu. Polymorphism sinpoly (ADP-ribose) polymerase-1 (PARP1) promoterand 3' untranslated region and their association with PARP1 expression in breast cancer patients // IntJ Clin Exp Pathol. 2015; 8(6): 7059-7071; Патент РФ «Тест- система для скрининга химических соединений на наличие ингибирующей активности в отношении PARP1» №2 016148005 решение о выдаче 19.12.17 г.) на стадии первичного скрининга и стадии химической оптимизации соединения. В основе данного способа лежат исследования транскрипционного белкового фактора PARP1, являющегося мишенью действия противоопухолевых препаратов. Создана база данных, содержащая информацию об ингибиторах PARP1 (http: //parp1inhibitors.ru/). Получены две системы: одна на базе мононуклеосомной матрицы, но с двухлинкерными участками, в которые размещены флуорофорные метки; вторая система - динуклеосомная, собрана из двух рядом расположенных нуклеосом, что позволяет оценивать влияние нескольких нуклеосом в системе.
Недостатком данного способа является то, что он не выявляет такого свойства противоопухолевого средства, как преодоление формирования резистентности опухолевых клеток за счет ингибирования цитопротекторной аутофагии.
Наиболее близким к заявленному способу является способ оценки потенциальной противоопухолевой активности и цитотоксичности противоопухолевых препаратов в экспериментах in vitro. Для этого опухолевые клетки подвергаются воздействию растворами потенциальных противоопухолевых средств в разных концентрациях в течение различного времени, при этом получают зависимость доли выживших (погибших) клеток в результате такого воздействия. Оценка количества выживших клеток производится косвенными методами: как колориметрическим методом с использованием МТТ (J. Carmichael, W.G. DeGraff, A.F. Gazdar, J.D. Minna, J.B. Mitchell. Evaluation of a tetrazolium-based semiautomated colorimetric assay: assessment of chemosensitivity testing. Cancer Res. 1987, Vol. 47, 4, p. 936-942), так и флуоресцентным методом с использованием флуоресцеиндиацетата (ФДА) (J.R. Sellers, S. Cook, V.C. Goldmacher. A cytotxicity assay utilizing a fluorescent dye that determines accurate surviving fractions of cells. J. Immunol. Meth. 1994. V. 172, p. 255-264) или с использованием радиоактивных меток (М Korbelik, GKrosl. Enhanced macrophage cytotoxicity against tumor cells treated with photodynamic therapy. Photochem Photobiol. 1994, Vol. 60, 5, p. 497-502). При всех перечисленных способах клетки после воздействия дополнительно инкубируют с растворами веществ, которые, в зависимости от жизнедеятельности клеток, изменяют уровень поглощения, флуоресценции или радиоактивный сигнал, что позволяет, измеряя количественно уровень поглощения, флуоресценции или радиоактивный сигнал, количественно оценить долю выживших или погибших клеток.
Недостатком данного способа является получение данных только о доли выживших или погибших клеток, что недостаточно ни для установления способности противоопухолевого средства к преодолению формирования резистентности опухолевых клеток в результате химиотерапии, ни для определения его минимальных эффективных концентраций. Кроме того, при расчете эффективной концентрации цитотоксичности противоопухолевого средства выбирают концентрацию, вызывающую максимальную гибель опухолевых клеток. Обычно такая концентрация достаточно высока и может оказывать негативное воздействие и на здоровые, неопухолевые клетки.
Нами впервые для определения минимально эффективных концентраций противоопухолевого лекарственного средства, обладающего свойством, препятствующим формированию резистентности опухолевых клеток за счет ингибирования в них цитопротекторных аутофагосом, предложено использование количества клеток с аутофагосомами, выраженное в процентах от числа живых клеток. Подтверждением наличия у лекарственного противоопухолевого средства способности подавлять формирование аутофагосом в опухолевых клетках является наличие обратной корреляции между процентом клеток с аутофагосомами и концентрацией лекарственного средства при условии наличия прямой корреляции между процентом мертвых клеток и значением концентрации лекарственного средства, как видно на фиг 1А. Значение концентрации такого лекарственного средства, при которой процент клеток с аутофагосомами будет равен нулю и будет минимально эффективной для преодоления резистентности опухолевых клеток за счет ингибирования цитопротекторной аутофагии.
Технической задачей заявленного способа является разработка алгоритма выявления минимально эффективных концентраций противоопухолевых лекарственных средств, ингибирующих цитопротекторную аутофагию в опухолевых клетках, что позволит повысить эффективность методов лечения злокачественных новообразований за счет снижения значений эффективных концентраций лекарственного средства.
СПОСОБ СОСТОИТ В СЛЕДУЮЩЕМ: используются клеточные культуры опухолей человека, которые подвергаются воздействию растворами в разных концентрациях противоопухолевого средства, препятствующим формированию резистентности опухолевых клеток за счет ингибирования в них цитопротекторных аутофагосом в течение 24 ч. Затем после воздействия лекарственным средством клетки инкубируют с двумя флуоресцентными красителями в тесте «живые и мертвые», например, акридиновый оранжевый (окрашивающий в зеленый цвет только живые клетки) и йодистый пропидий (интеркалирующий через разрушенную мембрану ядра погибающих или уже погибших клеток и окрашивающий их в красно-оранжевый цвет). Применение одновременно двух флуоресцентных красителей позволяет выявлять общее количество погибших клеток (окрашивание в красный цвет), и общее количество живых клеток (окрашивание в зеленый цвет), в том числе клеток с аутофагосомами.
После окрашивания красителями подсчитывают: среднее количество клеток (СКК) в поле зрения, среднее количество живых клеток, количество клеток с аутофагосомами и определяют процент клеток с аутофагосомами от количества живых клеток. Концентрация, при которой процентом клеток с аутофагосомами будет равен нулю и будет минимально эффективной для преодоления резистентности опухолевых клеток. На фиг. 1А видно, что минимально эффективной концентрацией экстракта аврана является концентрация 0,75 мг/мл, при которой процент клеток с аутофагосомами равен нулю.
Для анализа выбрана культура клеток рака шейки матки Hela и противоопухолевый растительный экстракт аврана лекарственного (Патент на изобретение RUS 2519769 21.03.2013. Средство, обладающее противоопухолевым и иммуномодулирующим действием. Полуконова К.В., Наволокин Н.А., Дурнова Н.А., Маслякова Г.К, Бучарская А.Б.). Экстракт получен определенным способом (Патент на изобретение RUS 2482863 15.02.2012. Способ получения сухого экстракта из растительного сырья, обладающего биологической активностью Полуконова К.В., Наволокин НА., Дурнова НА., Маслякова Г.Н, Бучарская А.Б.), направленный на снижение токсичности экстрактивных веществ и повышение выхода флавоноидов. В качестве флуоресцентных красителей использованы акридиновый оранжевый и йодистый пропидий.
На фиг. 2А представлены клетки Hela при флюоресцентной микроскопии и окраске акридиновым оранжевым и йодистым пропидием через 24 ч после инкубации только в среде в контроле, стрелкой указаны единичные аутофагосомы. Появление мертвых клеток единично.
На фиг. 2Б представлены клетки Hela при флюоресцентной микроскопии и окраске акридиновым оранжевым и йодистым пропидием через 24 ч после инкубации с экстрактом аврана в концентрации 0,1875 мг/мл, стрелкой указаны многочисленные аутофагосомы. СКК в поле зрения по сравнению с контролем в диапазоне концентраций от 0,0937 до 3 мг/мл сократилось в два раза (таб. 1), а при концентрации 6 мг/мл - в три раза, что свидетельствовало о высокой цитостатической активности экстракта.
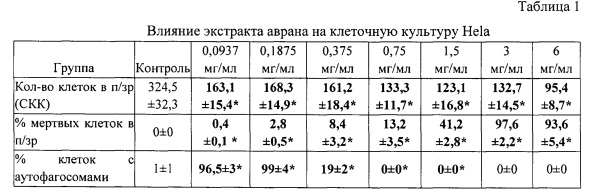
Примечание: *указаны достоверные отличия с контролем при T>1.96 и p<0.05
Процент мертвых клеток прямо пропорционально увеличивался, начиная от концентрации 0,1875 мг/мл, т.е. экстракт обладал и значительной цитотоксической активностью.
Максимальная аутофагическая активность экстракта наблюдалась при концентрациях 0,0937 и 0,1875 мг/мл (табл. 1), что свидетельствовало об активном действии экстракта на опухолевые клетки. Выявлена достаточно четкая тенденция - при резком падении количества клеток с аутофагосомами, резко увеличивается количество мертвых клеток (табл. 1), что подтверждает роль цитопротекторной аутофагии при выживании опухолевых клеток в условиях противоопухолевой терапии.
Начиная с концентрации экстракта 0,375 мг/мл число клеток с аутофагосомами резко сократилось.
На фиг. 3 видно, что, начиная с концентрации экстракта 0,75 мг/мл, в опухолевых клетках Hela аутофагосомы не образовывались.
На фигуре 1А представлена зависимость между процентом клеток с аутофагосомами и концентраций экстракта. Для выявления взаимосвязи был проведен корреляционный анализ методом Спирмана; для оценки взаимосвязи показателей был использован непараметрический критерий Спирмана. В результате анализа выявлена обратная двусторонняя взаимосвязь средней силы (r=-0.56) высокой статистической значимости (р=0.004) уже в первые 24 ч эксперимента. На фиг. 1А видно, что при концентрации 0,75 мг/мл экстракт ингибирует процесс образования аутофагосом и начинается резкая гибель опухолевых клеток, следовательно, эта концентрация минимально эффективная в преодолении формирования резистентности опухолевых клеток.
В результате минимально эффективной концентрацией экстракта аврана, полученной описанным способом, оказалась концентрация 0,75 мг/мл, в то время, как концентрация, которая бы была получена наиболее близким к заявленному способу, при которой погибает наибольшее количество опухолевых клеток - 3 мг/мл. Следовательно, заявленный нами способ позволил снизить значение минимально эффективной концентрации, что позволяет существенно снизить и токсический эффект, оказываемый и на здоровые клетки.
Таким образом, учитывая полученные результаты, мы считаем целессообразным для определения минимально эффективной концентрации противоопухолевого лекарственного средства, препятствующего формированию резистентности опухолевых клеток за счет ингибирования цитопротекторной аутофагии, использование процента клеток с аутофагосомами от количества живых клеток. Значение концентрации, при которой процент клеток с аутофагосомами будет равен нулю и будет минимально эффективной для преодоления резистентности опухолевых клеток.
Пример
Брали культуру клеток рака шейки матки Hela и противоопухолевый растительный экстракт аврана лекарственного (экстракт получали способом, указанным в Патенте на изобретение RUS 2482863 15.02.2012. Способ получения сухого экстракта из растительного сырья, обладающего биологической активностью Полуконова К.В., Наволокин Н.А., Дурнова Н.А., Маслякова Г.Н, Бучарская А.Б.).
Опухолевые клетки рака шейки матки Hela были получены из криобанка коллекции клеточных культур лаборатории вирусологии (г. Саратов) научно-исследовательской ветеринарной станции РАСХН. Культивирование проводилось в пластиковых флаконах в среде RPMI 4 (10% эмбриональной сыворотки, гентамицин, ампициллин, амфотерицин).
Эксперименты проводили в 96 луночных культуральных планшетах - одна контрольная и пять экспериментальных. Контролем служили клетки в питательной среде без добавления экстракта, выросших в течение суток. В 21 лунку внесли водный раствор экстракта аврана по три лунки каждой концентрации и три лунки были контрольными. Анализировались следующие концентрации: 0,0937, 0,1875, 0,375, 0,75, 1,5, 3, 6 мг/мл.
Клетки культивировали в СO2-инкубаторе при 37°С в течение 24 часов, после чего окрашивали. В качестве красителя использовали йодистый пропидий, проникающий в нежизнеспособные клетки за счет разрушения их мембраны.
Для визуализации клеток использовали режим регистрации флюоресценции. Световой микроскоп LeicaDM 2500 с дополнительным галогеновым осветителем Leica CLS 150, позволяющим освещать объект с двух сторон сбоку, для реализации режима темного поля. Захват и анализ изображений проводили с помощью цифровой видеокамеры LeicaDFC 420 С и программного обеспечения LeicaApplicationSuite V 3.1. Конфокальный микроскоп Leica LSM SP-5 (LeicaMicrosistems, Германия) в режиме регистрации флюоресценции со спектральным сдвигом соответствующим используемым флюорофорам. Для обсчета клеток использовали программное обеспечение ImageJ.
Для анализа клеток в контрольной и экспериментальной культурах были использованы следующие показатели: среднее количество клеток (СКК) в поле зрения, среднее количество мертвых клеток, среднее количество живых клеток, количество клеток с аутофагосомами и зависимость процента клеток с аутофагосомами от концентрации.
На фиг. 2А представлены клетки Hela при флюоресцентной микроскопии и окраске акридиновым оранжевым и йодистым пропидием через 24 ч после инкубации только в среде в контроле, стрелкой указаны единичные аутофагосомы. Появление мертвых клеток единично.
На фиг. 2Б представлены клетки Hela при флюоресцентной микроскопии и окраске акридиновым оранжевым и йодистым пропидием через 24 ч после инкубации с экстрактом аврана в концентрации 0,1875 мг/мл, стрелкой указаны многочисленные аутофагосомы. СКК в поле зрения по сравнению с контролем в диапазоне концентраций от 0,0937 до 3 мг/мл сократилось в два раза (таб. 1), а при концентрации 6 мг/мл - в три раза, что свидетельствовало о высокой цитостатической активности экстракта.
Процент мертвых клеток прямо пропорционально увеличивался, начиная от концентрации 0,1875 мг/мл, т.е. экстракт обладал и значительной цитотоксической активностью.
Максимальная аутофагическая активность экстракта наблюдалась при концентрациях 0,0937 и 0,1875 мг/мл (табл. 1), что свидетельствовало об активном действии экстракта на опухолевые клетки. Выявлена достаточно четкая тенденция - при резком падении количества клеток с аутофагосомами, резко увеличивается количество мертвых клеток (табл. 1), что подтверждает роль цитопротекторной аутофагии при выживании опухолевых клеток в условиях противоопухолевой терапии.
Начиная с концентрации экстракта 0,375 мг/мл число клеток с аутофагосомами резко сократилось.
На фиг. 3 видно, что, начиная с концентрации экстракта 0,75 мг/мл, в опухолевых клетках Hela аутофагосомы не образовывались.
На фигуре 1А представлена зависимость между процентом клеток с аутофагосомами и концентраций экстракта. Для выявления взаимосвязи был проведен корреляционный анализ методом Спирмана; для оценки взаимосвязи показателей был использован непараметрический критерий Спирмана. В результате анализа выявлена обратная двусторонняя взаимосвязь средней силы (r=-0.56) высокой статистической значимости (р=0.004) уже в первые 24 ч эксперимента. На фиг. 1А видно, что при концентрации 0,75 мг/мл экстракт ингибирует процесс образования аутофагосом и начинается резкая гибель опухолевых клеток, следовательно, эта концентрация минимально эффективная в преодолении формирования резистентности опухолевых клеток.
В результате минимально эффективной концентрацией экстракта аврана, полученной описанным способом, оказалась концентрация 0,75 мг/мл, в то время, как концентрация, которая бы была получена наиболее близким к заявленному способу, при которой погибает наибольшее количество опухолевых клеток - 3 мг/мл. Следовательно, заявленный нами способ позволил снизить значение минимально эффективной концентрации, что позволяет существенно снизить и токсический эффект, оказываемый и на здоровые клетки.
Таким образом, для определения минимально эффективной концентрации противоопухолевого лекарственного средства, препятствующего формированию резистентности опухолевых клеток за счет ингибирования цитопротекторной аутофагии, использование процента клеток с аутофагосомами от количества живых клеток целесообразно. Значение концентрации, при которой процент клеток с аутофагосомами будет равен нулю и будет минимально эффективной для преодоления резистентности опухолевых клеток.
В отличие от наиболее близкого к заявленному способу оценки эффективной концентрации противоопухолевых препаратов в экспериментах in vitro в предлагаемом нами способе эффективная концентрация будет существенно ниже и поэтому будет оказывать меньшее негативное влияние на здоровые клетки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИЗБИРАТЕЛЬНЫМ ДЕЙСТВИЕМ НА ОПУХОЛЕВЫЕ КЛЕТКИ, АКТИВИРУЮЩЕЕ ИХ АПОПТОЗ И ПРЕПЯТСТВУЮЩЕЕ ФОРМИРОВАНИЮ ИХ РЕЗИСТЕНТНОСТИ | 2018 |
|
RU2694547C1 |
| СРЕДСТВО, ВЫЗЫВАЮЩЕЕ В ЭКСПЕРИМЕНТАХ IN VIVO ЗАМЕЩЕНИЕ ОПУХОЛЕВОЙ ТКАНИ СОЕДИНИТЕЛЬНОЙ И ПЕРЕВОДЯЩЕЕ КЛЕТКИ ОПУХОЛИ ИЗ ФАЗЫ G1 КЛЕТОЧНОГО ЦИКЛА В СОСТОЯНИЕ ПОКОЯ G0 | 2018 |
|
RU2731105C2 |
| Способ комбинированной терапии рака печени РС-1 в эксперименте | 2020 |
|
RU2734143C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 2018 |
|
RU2714930C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2017 |
|
RU2657423C1 |
| Средство, обладающее противогрибковым действием в отношении грибов рода Candida | 2017 |
|
RU2657779C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2013 |
|
RU2519769C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2549477C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕВОЙ КАХЕКСИИ | 2015 |
|
RU2578440C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ СОЕДИНЕНИЙ ДЛЯ ЛЕЧЕНИЯ РАКА | 2010 |
|
RU2575828C2 |


Изобретение относится к медицине, а именно к онкологии и фармации, и может быть использовано для определения минимальной эффективной концентрации противоопухолевого лекарственного средства, ингибирующего цитопротекторную аутофагию. Для этого осуществляют воздействие лекарственного средства на опухолевые клетки человека в культуре в течение 24 ч. Затем окрашивают клетки одновременно двумя флуоресцентными красителями акридиновым оранжевым и йодистым пропидием. Проводят подсчет процентного содержания живых клеток с аутофагосомами по отношению ко всем живым клеткам. Определяют минимально эффективную концентрацию лекарственного средства, при которой процентное содержание живых клеток с аутофагосомами по отношению ко всем живым клеткам будет равно нулю. Изобретение позволяет повысить эффективность лечения злокачественных новообразований за счет определения минимально эффективных концентраций противоопухолевых лекарственных средств. 3 ил., 1 табл., 1 пр.
Способ определения минимальной эффективной концентрации противоопухолевого лекарственного средства, ингибирующего цитопротекторную аутофагию, включающий воздействие лекарственного средства на опухолевые клетки человека в культуре в течение 24 ч, окраску клеток одновременно двумя флуоресцентными красителями акридиновым оранжевым и йодистым пропидием, подсчет процентного содержания живых клеток с аутофагосомами по отношению ко всем живым клеткам и определение минимально эффективной концентрации лекарственного средства, при которой процентное содержание живых клеток с аутофагосомами по отношению ко всем живым клеткам будет равно нулю.
| СПОСОБ СКРИНИНГА ПРОТИВООПУХОЛЕВЫХ ПРЕПАРАТОВ - ИНГИБИТОРОВ PARP1 НА ОСНОВЕ БИОХИМИЧЕСКИХ МЕТОДОВ АНАЛИЗА | 2015 |
|
RU2639535C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУХОГО ЭКСТРАКТА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ, ОБЛАДАЮЩЕГО БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2482863C1 |
| LIN CJ et al., Resveratrol enhances the therapeutic effect of temozolomide against malignant glioma in vitro and in vivo by inhibiting autophagy, Free Radic Biol Med | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| SELLERS J.R | |||
| et al., A cytotoxicity assay utilizing a fluorescent dye that determines accurate surviving fractions of cells | |||
| J | |||
| Immunol | |||
| Meth | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| V | |||
| Приспособление для воспроизведения изображения на светочувствительной фильме при посредстве промежуточного клише в способе фотоэлектрической передачи изображений на расстояние | 1920 |
|
SU172A1 |
| Гудок | 1921 |
|
SU255A1 |
Авторы
Даты
2019-07-05—Публикация
2018-02-13—Подача