Изобретение относится к области медицинского приборостроения, а именно в неинвазивной оценке функционального состояния поверхностных сосудов и уровня оксигенации участка биологической ткани оптическими методами.
Известно устройство для измерения медико-биологических параметров кожи и слизистых оболочек in vivo (см. патент РФ №2337608 по кл. МПК А61В5/00, опуб. 10.11.2008), содержащее блок источников первичного оптического излучения с разными длинами волн излучения, систему транспортировки первичного и вторичного излучения к биологической ткани и обратно, выполненную в виде жгута оптических волокон с разветвленной приборной и единой рабочей частью, оптико-электронную систему регистрации вторичного оптического излучения, содержащую фотоприемники с оптическими фильтрами, полихроматор с дифракционной решеткой и устройство сбора и трансляции данных в блок обработки результатов диагностики. Устройство позволяет определять содержание в крови фракции оксигемоглобина, а также наличие в тканях липофусцина, меланина, общее объемное кровенаполнение тканей.
Недостатком данного аналога является локализованный и интегральный характер измерений функционального состояния сосудов и уровня оксигенации участка биологической ткани, что делает трудоемким процесс измерения сравнительно больших поверхностей и требует наличия системы сканирования. Кроме этого, работа с прибором требует особой осторожности из-за наличия волоконного зонда, который может быть поврежден, например, перегибом или деформацией торца волокна, что приведет к полной потере работоспособности прибора.
Известно также устройство для получения распределения показателя кровотока и уровня оксигенации по широкому полю зрения без сканирования [Reif R. et al. Monitoring hypoxia induced changes in cochlear blood flow and hemoglobin concentration using a combined dual-wavelength laser speckle contrast imaging and Doppler optical microangiography system //PloS one. – 2012. – Т. 7. – №. 12. – С. e52041], содержащее два светодиодных лазера, зеркало, два дихроичных зеркала, два матричных фотоприёмника, подключённых к компьютеру для синхронной работы.
Лазерные пучки двух диодов с помощью зеркала и дихроичного зеркала сводятся соосно, расширяются посредством двух линз и одновременно направляются на объект исследования. Фотообъектив формирует изображение объекта. Дихроичное зеркало делит изображение объекта на две спектральные компоненты и направляет их на два матричных фотоприемника.
К недостаткам данного прибора стоит отнести существенную дороговизну изделия из-за наличия двух матричных фотоприемников и двух дихроичных зеркал. Кроме этого, использование источников излучения с высокой степенью когерентности существенно снижает пространственное разрешение системы при расчете уровня оксигенации.
Наиболее близким к заявляемому является устройство регистрации цифровых голографических и спектральных изображений микрообъектов (см. патент РФ № 2574791 по кл. МПК G02B27/22, опуб. 10.02.2016), содержащее оптически связанные и расположенные последовательно по центральной оси источник светового излучения, коллиматор, светоделительный элемент, референтный канал с первым зеркалом, а также объектный канал для формирования отражённого объектного пучка, имеющий микрообъектив и плоскость для объекта исследований. В приемном канале установлен акустооптический монохроматор изображений; в референтный канал помещен подвижный двухпозиционный элемент, выполненный с возможностью в первом положении блокировать свет в канале с помощью оптического поглотителя, а во втором - ослабляющий свет в канале с помощью сменного нейтрального светофильтра; причем элементы референтного канала - микрообъектив и зеркало - выполнены как единое целое в виде подвижного модуля и имеют единый механизм осевого перемещения.
К недостаткам данного технического решения следует отнести существенную дороговизну прибора из-за присутствия перестраиваемого акустооптического монохроматора, медлительность работы из-за необходимости механической блокировки пучка в референтном канале для получения спектральных изображений объекта. Кроме того, необходима калибровка прибора на нулевую разность хода и постоянный контроль положения опорного плеча, что делает настройку и работу с прибором трудоемкими. Наряду с этим, не продемонстрирована возможность восстановления уровня оксигенации и индекса кровотока по данным, полученным с помощью данного устройства.
К общему недостатку вышеперечисленных известных устройств стоит отнести невозможность перефокусировки системы пост-фактум, что делает необходимым точную настройку фокуса перед регистрацией сигнала. Фокусировка особенно важна при использовании объективов с малой глубиной резко-изображаемого пространства.
Технической проблемой заявляемого изобретения является осуществление неинвазивной оптической диагностики функционального состояния поверхностных сосудов и уровня оксигенации биообъектов in vivo.
Техническим результатом изобретения является возможность одновременного, неинвазивного измерения индекса кровотока и уровня оксигенации биологической ткани по полному полю с высоким пространственным и временным разрешениями и возможностью численной фокусировки оптической системы после записи изображения оптическими методами.
Технический результат достигается тем, что устройство регистрации цифровых голографических и спектральных изображений микрообъектов, содержащее оптически связанные и расположенные последовательно по центральной оси источник светового излучения, коллиматор, светоделительный элемент, референтный канал с первым зеркалом, а также объектный канал для формирования отражённого объектного пучка, имеющий микрообъектив и плоскость для объекта исследований, приёмный канал с матричным фотоприёмником, согласно изобретению, дополнительно содержит соединённые между собой блок управления и блок синхронизации, который подключён к источнику светового излучения и матричному фотоприёмнику, референтный канал снабжён дополнительным зеркалом для формирования отражённого референтного пучка, расположенным под углом по отношению к центральной оси, объектный канал снабжён осветительным блоком, подключённым к блоку синхронизации и выполненным в виде светодиодов, осветительный блок расположен между микрообъективом и плоскостью для объекта исследований, между объектным каналом и светоделительным элементом введена апертурная диафрагма, при этом первое зеркало расположено под углом 45о по отношению к центральной оси, а дополнительное зеркало – под углом 45о – α, где α – угол между направлениями отражённых объектного и референтного пучков в приёмном канале.
Устройство может содержать два поляризатора, один из которых расположен по центральной оси после светоделительного элемента, а второй – перпендикулярно центральной оси перед матричным фотоприёмником.
Источник светового излучения, осветительный блок и приемный канал связаны между собой блоком синхронизации для обеспечения синхронной смены длин волн освещения. В результате получают серию спектральных и голографических изображений, позволяющих оценить функциональное состояние поверхностных сосудов и уровня оксигенации участка объекта исследования.
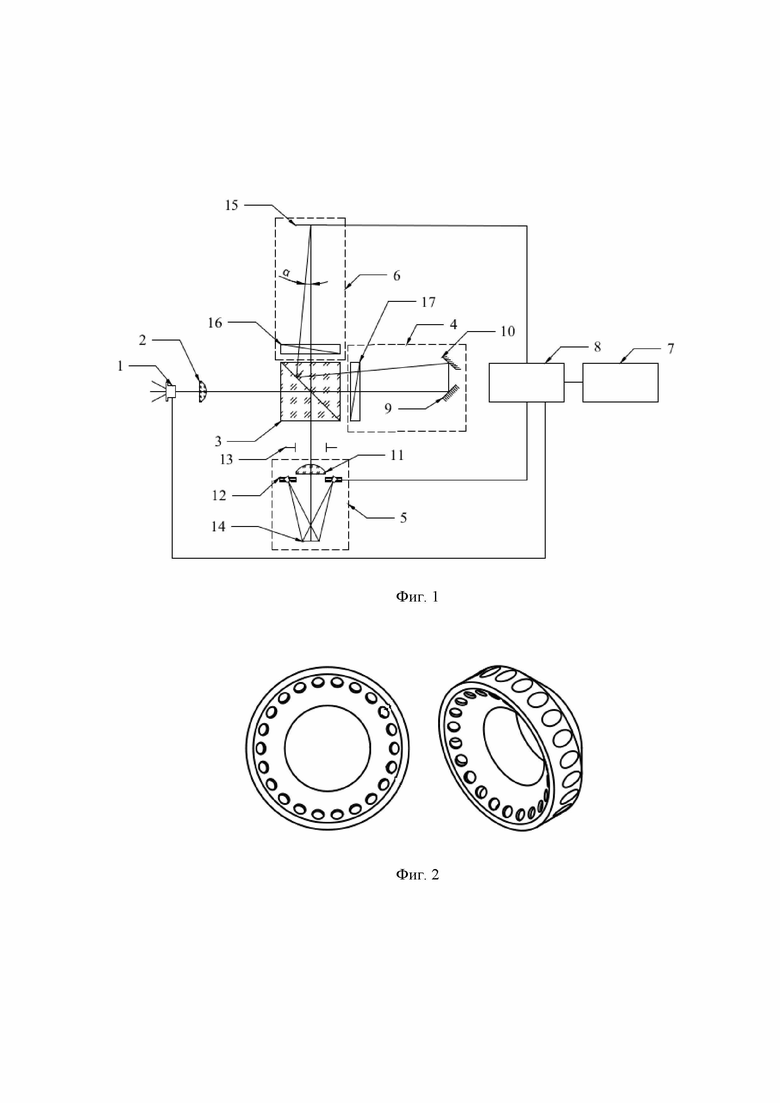
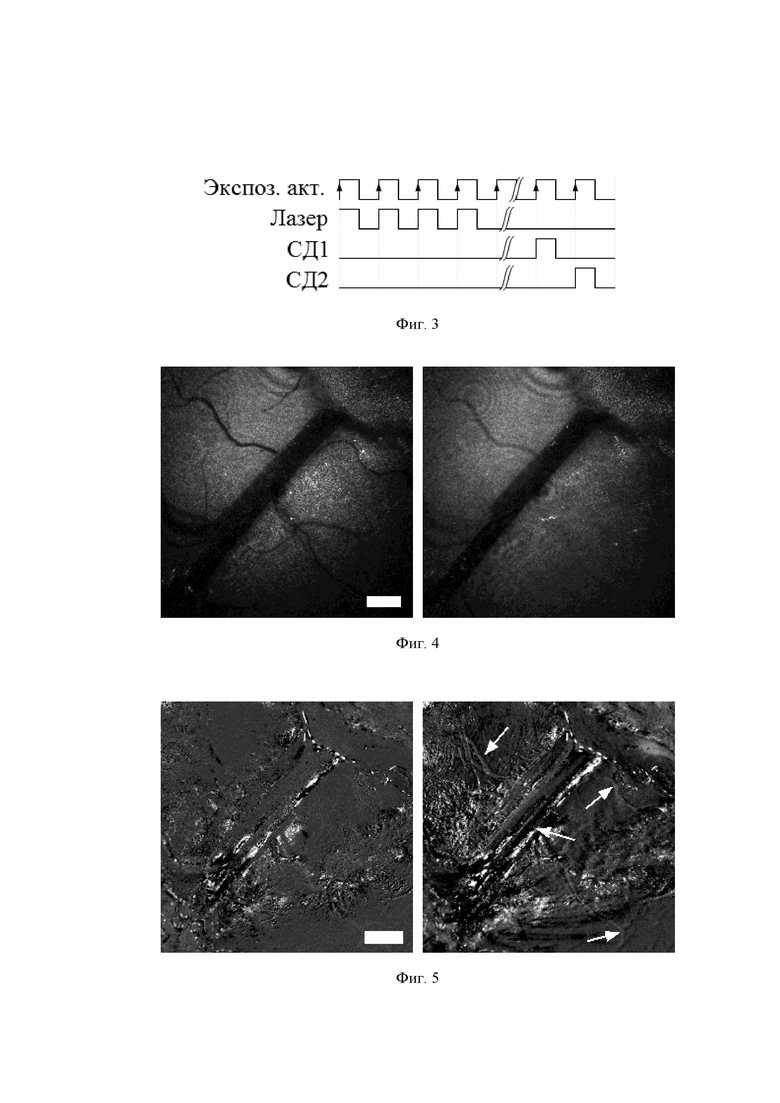
Изобретение поясняется иллюстрациями, где на фиг. 1 представлена схема устройства регистрации цифровых голографических и спектральных изображений микрообъектов, на фиг. 2 – осветительный блок, на фиг. 3 – временная диаграмма работы устройства, где обозначено «Экспоз. акт» – время экспонирования матричного фотоприемника, «Лазер» – источник светового излучения, «СД1» и «СД2» – красные и зеленые светодиоды в осветительном блоке, на фиг. 4 – картина распределения индекса кровотока до окклюзионной пробы (слева) и после (справа), на фиг. 5 – картина распределения уровня оксигенации участка биологической ткани по полному полю до окклюзионной пробы (слева) и после (справа).
На фиг. 1 позициями обозначено:
1 – источник светового излучения,
2 – коллиматор,
3 – светоделительный элемент,
4 – референтный канал,
5 – объектный канал,
6 – приёмный канал,
7 – блок управления,
8 – блок синхронизации,
9, 10 – первое и дополнительное зеркала референтного канала 4,
11 – микрообъектив объектного канала 5,
12 – осветительный блок
13 – апертурная диафрагма,
14 – плоскость для объекта исследований,
15 – матричный фотоприёмник приёмного канала 6,
16, 17 – поляризаторы.
Устройство содержит расположенные последовательно по центральной оптической оси источник светового излучения 1, коллиматор 2, светоделительный элемент 3, референтный канал 4. Устройство содержит также объектный канал 5 для формирования отражённого объектного пучка, приёмный канал 6 с матричным фотоприёмником 15, блок управления 7, соединённый с блоком синхронизации 8, подключённым к источнику светового излучения 1 и матричному фотоприёмнику 15. Объектный канал 5 содержит микрообъектив 11 и плоскость 14 для объекта исследований. Референтный канал 4 содержит два зеркала: первое 9 расположено под углом 45о по отношению к центральной оси, а дополнительное зеркало – под углом 45о – α, где α – угол между направлениями отражённых объектного и референтного пучков в приёмном канале 6. Объектный канал 5 снабжён осветительным блоком 12, подключённым к блоку синхронизации 8 и расположенным между микрообъективом 11 и плоскостью 14 для объекта исследования. Между объектным каналом 5 и светоделительным элементом 3 введена апертурная диафрагма13. Осветительный блок 12 представляет собой деталь в форме усеченного конуса, выполненную из пластика по технологии 3Д печати. В середине осветительного блока расположено отверстие для крепления микрообъектива, по краям осветительного блока расположены отверстия для крепления светодиодов.
Устройство также может содержать два поляризатора, один из которых 16 расположен перпендикулярно центральной оптической оси в приёмном канале 6 перед матричным фотоприёмником 15, а второй 17 – по центральной оптической оси после светоделительного элемента 3
Устройство работает следующим образом.
От источника светового излучения 1, выполненного в виде светодиодного лазера, посредством коллиматора 2, выполненного в виде линзы, излучение коллимируется и направляется на светоделительный элемент 3, который разделяет падающую на него световую волну на предметный пучок, направленный на объект исследования, расположенный на плоскости 14, и референтный пучок, направленный на зеркала 9 и 10 Апертурная диафрагма 13 помещенная в плоскость выходного зрачка микрообъектива 11 регулирует размер субъективных спеклов. Поляризатор 16 служит для устранения переотражений от внутренних границ в светоделительном элементе 3, а так же прямого отражения от задней поверхности микрообъектива 11. Поляризатор 17 регулирует интенсивность референтного пучка. Микрообъектив 11 формирует изображение объекта в плоскости матричного приёмника 15.
Комплекс зеркал 9 и 10 имеет возможность смещения в плоскости, перпендикулярной оптической оси системы, для достижения желаемого сдвига лазерного пучка относительно оптической оси. Данная конфигурация позволяет избежать расхождения полей в плоскости приёмника 15 при необходимом угле наклона зеркала 10. Осветительный блок 12, состоящий из 11 светодиодов красного цвета свечения и 11 диодов зеленого цвета свечения, крепится на тело микрообъектива 11. Данный осветительный блок позволяет производить измерения оксигенации участка биологической ткани. Осветительный блок 12, матричный фотоприемник 15 и источник светового излучения 1 в виде лазерного диода соединены с блоком синхронизации 8, подключённым к блоку управления 7 для синхронного переключения длин волн освещения.
В процессе работы устройства триггерные импульсы с матричного фотоприемника 15, (см. позицию "Экспоз. акт" на фиг.3) подаются на блок синхронизации 8, который, в свою очередь, последовательно переключает источник светового излучения 1 (см. «Лазер» фиг.3), а также красные (см. "СД1" фиг. 3) и зеленые (см. "СД2"фиг. 3) светодиоды в осветительным блоке 12 для записи голограммы и спектральных изображений микрообъектов соответственно.
Производится запись внеосевых голограмм, состоящая из коллимации лазерного излучения, деления лазерного пучка на две примерно равные части —референтный пучок и объектный пучок. После отражения эти пучки сводятся в плоскости регистрации матричного фотоприемника 15 под небольшим углом для получения интерференционной картины (голограммы). После регистрации голограммы производится ее фильтрация в области спектра пространственных частот для восстановления комплексной амплитуды отраженной объектом волны (изображение объекта). Знание комплексной амплитуды волны позволяет осуществлять численную фокусировку изображения после его записи путем моделирования распространения волнового фронта вдоль оптической оси системы согласно теории углового спектра [Goodman J. W. Introduction to Fourier optics. – Roberts and Company Publishers, 2005.].
В результате когерентного сложения отражённых референтного и предметного пучков в плоскости матричного фотоприемника формируются интерференционные полосы с периодом 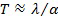 , где
, где 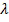 - длина волны лазерного излучения. Математически такое сложение описывается формулой 1
- длина волны лазерного излучения. Математически такое сложение описывается формулой 1
где 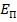 и
и 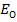 - предметное и опорное поле соответственно. * - означает комплексное сопряжение.
- предметное и опорное поле соответственно. * - означает комплексное сопряжение.
Результирующая интерференционная картина или, как ее принято называть, голограмма регистрируется при помощи современной КМОП-матрицы с физическим размером пикселя ρ, причем, 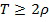 для удовлетворения критерия Найквиста.
для удовлетворения критерия Найквиста.
Интерес представляет последнее слагаемое в формуле 1. Для его сегментации от остальных производится цифровая фильтрация пространственного спектра голограммы. Данная фильтрация возможна только при полном разделении всех трех слагаемых в пространственном спектре голограммы. Вышеуказанное условие достигается путем регулирования диаметра отверстия апертурной диафрагмы и угла наклона между интерферирующими полями.
После пространственной фильтрации сегментированное слагаемое 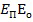 подвергается обратному преобразованию Фурье для получения распределения комплексной амплитуды света на поверхности объекта в виде
подвергается обратному преобразованию Фурье для получения распределения комплексной амплитуды света на поверхности объекта в виде 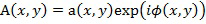 , где
, где 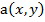 и
и 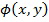 - амплитуда и фаза волны соответственно. Знание амплитуды и фазы волны, отраженной от объекта, позволяет применить алгоритм численной фокусировки. Его суть заключается в восстановлении волнового фронта в некоторой плоскости, отличной от плоскости регистрации голограммы. Данный метод находит свое полезное применение при визуализации слабо-рассеивающих или прозрачных объектов. Требуется запись лишь одной голограммы для получения изображений на разных глубинах объекта, без необходимости механической фокусировки оптической системы, что позволяет восстанавливать 3Д изображения объекта исследования.
- амплитуда и фаза волны соответственно. Знание амплитуды и фазы волны, отраженной от объекта, позволяет применить алгоритм численной фокусировки. Его суть заключается в восстановлении волнового фронта в некоторой плоскости, отличной от плоскости регистрации голограммы. Данный метод находит свое полезное применение при визуализации слабо-рассеивающих или прозрачных объектов. Требуется запись лишь одной голограммы для получения изображений на разных глубинах объекта, без необходимости механической фокусировки оптической системы, что позволяет восстанавливать 3Д изображения объекта исследования.
Восстановленное изображение объекта, в силу своей микроструктуры и высокой когерентности излучения, имеет зернистую структуру — спеклы. Анализ временной динамики спекл-структур путем применения известного алгоритма анализа спекл-изображений (Fercher, A. F. Flow visualization by means of single-exposure speckle photography / A. F. Fercher, J. D. Briers // Optics Communications. 1981. Т. 37, №. 5. С. 326-330) позволяет контрастировать кровеносные сосуды от статичных участков ткани. Наличие в структуре объекта движущихся с произвольной скоростью частиц, например эритроцитов в кровяном русле, приводит к локальному изменению рассеивающих свойств объекта во времени, что, в свою очередь, приводит к локальным флуктуациям интенсивности спекл-поля. Если период регистрации изображения много больше периода флуктуаций, то результатом будет снижение контраста или локальное «размытие» спеклов. Спекл-контраст определялся как отношение среднеквадратичного отклонения флуктуаций интенсивности σ к среднему значению этих флуктуаций <I> в некоторой локальной области изображения объекта 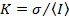 .
.
Данное устройство было опробовано на лабораторных животных – белых мышах in vivo. Белая мышь находилась под общим наркозом, ее голова была зафиксирована в специализированном зажиме, часть черепа была трепанирована для непосредственного доступа к коре головного мозга. После трепанации мышь была помещена в плоскость для объекта исследований. Для проверки работоспособности устройства были проведены контрольные замеры индекса кровотока и уровня оксигенации коры головного мозга ( фиг. 4 и фиг. 5 соответственно слева). После окончания контрольной записи была произведена оклюзионная проба – пережатие сонной артерии, что существенно ограничило доступ крови к коре головного мозга. Результаты замеров индекса кровотока и уровня оксигенации коры головного мозга мыши также представлены на фиг. 4 и фиг. 5 соответственно справа.
На фиг. 4 отчетливо видно снижение и полное перекрытие кровотока в большом количестве сосудов вокруг центральной вены. Масштаб — 500 мкм. Каждый пиксель изображения кодирует скорость кровотока в относительных единицах.
На фиг. 5 отчетливо видно падение среднего уровня оксигенации образца, наряду с характерными провалами общей оксигенации в местах залегания кровеносных сосудов (отмечены стрелочками). Масштаб — 500 мкм. Каждый пиксель изображения кодирует изменение общего уровня оксигенации относительного базового значения в относительных единицах.
Использование светодиодов в красном и зеленом спектральных диапазонах, закрепленных в специальной оправке на микрообъектив, позволяет получать данные об уровне оксигенации.
Простейшим алгоритмом оцени уровня оксигенации является анализ отраженного объектом света на двух длинах волн (см., например, патент WO2016015009). В данном комплексе использовались общедоступные светодиоды диаметром 3 мм, излучающие свет на длинах волн ~635 и ~560 нм соответственно. Изменение концентрации окси- и деокси- гемоглобина рассчитывалось по обще известному закону Бугера — Ламберта — Бера:
где 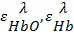 - коэффициент экстинкции окси- и деокси- гемоглобина на соответствующих длинах волн,
- коэффициент экстинкции окси- и деокси- гемоглобина на соответствующих длинах волн, 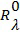 ,
, 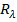 - интенсивность света, отраженного объектом в начальный и текущий момент времени соответственно на данной длине волны,
- интенсивность света, отраженного объектом в начальный и текущий момент времени соответственно на данной длине волны, 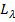 - глубина проникновения излучения данной длины волны в образец,
- глубина проникновения излучения данной длины волны в образец, 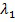 - длина волны красных светодиодов (~650 нм),
- длина волны красных светодиодов (~650 нм), 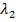 - длина волны зеленых светодиодов (~535 нм).
- длина волны зеленых светодиодов (~535 нм).
На основании представленных результатов заявляемое устройство позволяет отслеживать функциональное изменение состояния сосудов и уровня оксигенации биооъектов in-vivo без использования сканирующих элементов. Пространственное разрешение системы составляет 20 мкм, временное - 100 Гц, что является высоким показателем для устройств такого рода.
Численная фокусировка осуществляется после записи голограммы для коррекции возможной расфокусировки системы из-за механических движений объекта или иных причин.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИХ ТРЕХМЕРНЫХ И СПЕКТРАЛЬНЫХ ИЗОБРАЖЕНИЙ МИКРООБЪЕКТОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2574791C2 |
| МЕТОД И УСТРОЙСТВО ДЛЯ РЕГИСТРАЦИИ СПЕКТРАЛЬНЫХ ЦИФРОВЫХ ГОЛОГРАФИЧЕСКИХ ИЗОБРАЖЕНИЙ ОПТИЧЕСКИ ПРОЗРАЧНЫХ МИКРООБЪЕКТОВ | 2015 |
|
RU2601729C1 |
| Установка для измерения микрорельефа поверхности с использованием метода фазовых шагов | 2018 |
|
RU2677239C1 |
| МИКРОСКОП ПРОХОДЯЩЕГО И ОТРАЖЕННОГО СВЕТА | 2009 |
|
RU2419114C2 |
| ДВУХКАНАЛЬНЫЙ ДИФРАКЦИОННЫЙ ФАЗОВЫЙ МИКРОСКОП | 2015 |
|
RU2608012C2 |
| СПОСОБ ИНТЕРФЕРЕНЦИОННОЙ МИКРОСКОПИИ | 2013 |
|
RU2536764C1 |
| МЕТОД И УСТРОЙСТВО ДЛЯ РЕГИСТРАЦИИ ИЗОБРАЖЕНИЙ ФАЗОВЫХ МИКРООБЪЕКТОВ В ПРОИЗВОЛЬНЫХ УЗКИХ СПЕКТРАЛЬНЫХ ИНТЕРВАЛАХ | 2016 |
|
RU2626061C1 |
| УСТРОЙСТВО ДЛЯ ИЗМЕРЕНИЯ ДЕФОРМАЦИИ | 2020 |
|
RU2769885C1 |
| ИНТЕРФЕРЕНЦИОННЫЙ МИКРОСКОП | 2013 |
|
RU2527316C1 |
| СТЕНД ДЛЯ ПРОИЗВОДСТВА РАДУЖНЫХ МУЛЬТИПЛЕКСНЫХ ГОЛОГРАММ | 2001 |
|
RU2216759C2 |
Изобретение может использоваться при неинвазивной оценке функционального состояния поверхностных сосудов и уровня оксигенации участка биологической ткани. Устройство содержит коллиматор, светоделительный элемент, референтный канал с первым зеркалом, объектный канал, имеющий микрообъектив и плоскость для объекта исследований, приёмный канал с матричным фотоприёмником. Введены соединённые между собой блок управления и блок синхронизации. В референтном канале первое зеркало расположено под углом 45° к центральной оси и введено дополнительное зеркало под углом к центральной оси 45° – α, где α – угол между отражёнными объектным и референтным пучками в приёмном канале. В объектном канале между микрообъективом и плоскостью для объекта исследований введен осветительный блок, подключённый к блоку синхронизации и выполненный в виде светодиодов. Между объектным каналом и светоделительным элементом введена апертурная диафрагма. Технический результат - возможность одновременного неинвазивного измерения индекса кровотока и уровня оксигенации биологической ткани по полному полю с высоким пространственным и временным разрешениями и возможностью численной фокусировки после записи изображения оптическими методами. 1 з.п. ф-лы, 5 ил.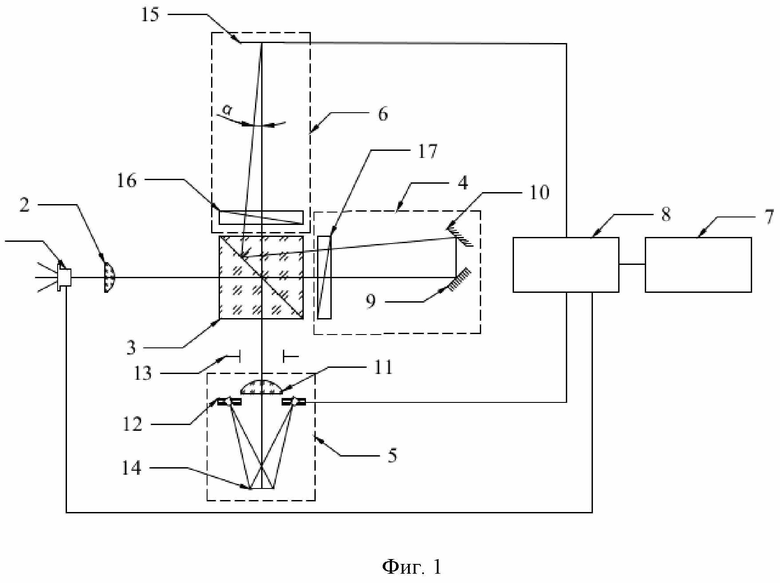
1 Устройство регистрации цифровых голографических и спектральных изображений микрообъектов, содержащее оптически связанные и расположенные последовательно по центральной оси источник светового излучения, коллиматор, светоделительный элемент, референтный канал с первым зеркалом, объектный канал для формирования отражённого объектного пучка, имеющий микрообъектив и плоскость для объекта исследований, приёмный канал с матричным фотоприёмником, отличающееся тем, что оно дополнительно содержит соединённые между собой блок управления и блок синхронизации, подключённый к источнику светового излучения и матричному фотоприёмнику, референтный канал снабжён дополнительным зеркалом для формирования отражённого референтного пучка, расположенным под углом по отношению к центральной оси, объектный канал снабжён осветительным блоком, подключённым к блоку синхронизации и выполненным в виде светодиодов, осветительный блок расположен между микрообъективом и плоскостью для объекта исследований, между объектным каналом и светоделительным элементом введена апертурная диафрагма, при этом первое зеркало расположено под углом 45о по отношению к центральной оси, а дополнительное зеркало – под углом 45о – α, где α – угол между направлениями отражённых объектного и референтного пучков в приёмном канале.
2 Устройство по п.1, отличающееся тем, что оно содержит два поляризатора, один из которых расположен по центральной оси после светоделительного элемента, а второй – перпендикулярно центральной оси перед матричным фотоприёмником.
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИХ ТРЕХМЕРНЫХ И СПЕКТРАЛЬНЫХ ИЗОБРАЖЕНИЙ МИКРООБЪЕКТОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2574791C2 |
| Arkady Abdurashitov, Olga Bragina, Olga Sindeeva, Sergey Sindeev, Oxana V | |||
| Semyachkina-Glushkovskaya, Valery V | |||
| Tuchin, Off-axis holographic laser speckle contrast imaging of blood vessels in tissues, Optics J | |||
| of Biomedical, 25.04.2017, https://www.spiedigitallibrary.org/journals/journal-of-biomedical-optics/volume-22/issue-09/091514/Off-axis-holographic-laser-speckle-contrast-imaging-of-blood-vessels/10.1117/1.JBO.22.9.091514.full | |||
| US 2016305761 A1, 20.10.2016 | |||
| МЕТОД И УСТРОЙСТВО ДЛЯ РЕГИСТРАЦИИ СПЕКТРАЛЬНЫХ ЦИФРОВЫХ ГОЛОГРАФИЧЕСКИХ ИЗОБРАЖЕНИЙ ОПТИЧЕСКИ ПРОЗРАЧНЫХ МИКРООБЪЕКТОВ | 2015 |
|
RU2601729C1 |
| Сушилка для винных дрожжей | 1950 |
|
SU89690A1 |
Авторы
Даты
2019-10-17—Публикация
2019-01-17—Подача