Релевантные заявки
Настоящая заявка заявляет приоритет заявки на патент США 61/075640, поданной 25 июня 2008 г., и заявки на патент США 61/075956, поданной 26 июня 2008 г.
Уровень техники
Фактор некроза опухолей альфа (TNFα, также известный как кахетин) представляет собой природный цитокин млекопитающих, продуцируемый клетками многочисленных типов, включая моноциты и макрофаги, в ответ на эндотоксин или другие стимулы. TNFα является основным медиатором воспалительных, иммунологических и патофизиологических реакций (Grell M. et al., 1995, Cell, 83:793-802).
Растворимый TNFα образуется при расщеплении трансмембранного белка-предшественника (Kriegler et al., 1988, Cell, 53:45-53), и секретируемые полипептиды массой 17 кДа подвергаются сборке в растворимые гомотримерные комплексы (Smith et al., 1987, J. Biol. Chem., 262:6951-6954; обзоры по TNFα смотри у Butler et al., 1986, Nature, 320:584; Old, 1986, Science, 230:630). Затем данные комплексы связываются с рецепторами, обнаруживаемыми на поверхности различных клеток. В результате подобного связывания генерируется ряд провоспалительных эффектов, которые включают: (i) высвобождение других провоспалительных цитокинов, таких как интерлейкин IL-6, IL-8 и IL-1; (ii) высвобождение матричных металлопротеиназ и (iii) положительную регуляцию экспрессии эндотелиальных адгезивных молекул, которые дополнительно усиливают воспалительный и иммунный каскад привлечением лейкоцитов во внесосудистые ткани.
Большое количество заболеваний ассоциировано с повышенными уровнями TNFα, многие их которых имеют большое значение в клинике. Было показано, что при ряде заболеваний человека имеется положительная регуляция, включая хронические заболевания, такие как ревматоидный артрит (RA), воспалительные заболевания кишечника, в том числе, болезнь Крона и язвенный колит, сепсис, застойную сердечную недостаточность, астму, бронхиальную астму и рассеянный склероз. У мышей, трансгенных по человеческому TNFα, конститутивно продуцируется большое количество TNFα, и у этих животных развивается спонтанный деструктивный полиартрит, напоминающий RA (Keffer et al., 1991, EMBO J., 10:4025-4031). Следовательно, TNFα относится к провоспалительным цитокинам.
В настоящее время хорошо установлено, что TNFα является ключевым соединением в патогенезе RA, который, в свою очередь, является хроническим, прогрессирующим и приводящим к истощению заболеванием, характеризующимся воспалением и разрушением многочисленных суставов, и также проявлением системных симптомов, таких как лихорадка, недомогание и хроническая усталость. Также RA приводит к развитию хронического синовиального воспаления с частым прогрессированием вплоть до разрушения хрящевой и костной ткани. Повышенные концентрации TNFα обнаружены в синовиальной жидкости и периферической крови пациентов, страдающих RA. В том случае, когда пациентам с RA вводят блокирующие TNFα лекарственные средства, то у них уменьшается воспаление, купируются симптомы заболевания и замедляется повреждение суставов (McKown et al., 1999, Arthritis Rheum., 42:1204-1208).
В физиологическом отношении TNFα также ассоциирован с защитой от определенных инфекций (Cerami et al., 1988, Immunol. Today, 9:28). TNFα продуцируется макрофагами, которые были активированы липополисахаридами грамотрицательных бактерий. С учетом этого обстоятельства полагают, что TNFα является эндогенным медиатором центрального значения, который принимает участие в развитии и патогенезе эндотоксического шока в результате бактериального сепсиса (Michie et al., 1989, Br. J. Surg., 76:670-671; Debets et al., 1989, Second Vienna Shock Forum, p. 463-466; Simpson et al., 1989, Crit. Care Clin., 5:27-47; Waage et al., 1987, Lancet, 1:355-357; Hammerle et al., 1989, Second Vienna Shock Forum, p. 715-718; Debets et al., 1989, Crit. Care Med., 17:489-497; Calandra et al., 1990, J. Infect. Dis., 161:982-987; Revhaug et al., 1988, Arch. Surg., 123:162-170).
Также было показано, что как и в других системах органов, TNFα играет ключевую роль в центральной нервной системе, в частности, при воспалительных и аутоиммунных заболеваниях нервной системы, включая рассеянный склероз, синдром Гуллиана-Барре и тяжелую миастению, и при дегенеративных расстройствах нервной системы, включая болезнь Альцгеймера, болезнь Паркинсона и болезнь Хантингтона. TNFα также принимает участие в развитии расстройства связанных систем сетчатки и мышц, включая неврит зрительного нерва, макулярную дегенерацию, диабетическую ретинопатию, дерматомиозит, амиотрофический латеральный склероз и мышечную дистрофию, а также травмы нервной системы, в том числе, травматическое повреждение головного мозга, острое повреждение спинного мозга и инсульт.
Гепатит представляет собой другое связанное с TNFα воспалительное заболевание, которое среди других причин, может быть вызвано вирусными инфекциями, включая, вирус Эпштейна-Барра, цитомегаловирус и вирусы гепатита А-Е. Гепатит вызывает острое воспаление печени в портальной и лобулярной области с последующим развитием фиброза и опухолей. Также TNFα может опосредовать кахексию при злокачественном заболевании, которая в большинстве случаев приводит к прогрессированию заболевания и летальному исходу (Tisdale M.J., 2004, Langenbecks Arch. Surg., 389:299-305).
Ключевая роль, которую играет TNFα в развитии воспаления, в клеточных иммунных ответах и патологии многих заболеваний, привела к поиску антагонистов TNFα. Одной группой антагонистов TNFα, разработанных для лечения заболеваний, опосредованных TNFα, являются антитела или фрагменты антител, которые специфически связываются с TNFα и тем самым блокируют его функцию. При применении анти-TNFα-антител было показано, что блокада TNFα может изменить направленность эффектов TNFα, включая снижение уровня IL-1, GM-CSF, IL-6, IL-8, адгезивных молекул и разрушение тканей (Feldmann et al., 1997, Adv. Immunol., 1997:283-350). Специфические ингибиторы TNFα, которые недавно стали промышленно доступными, включают моноклональные, химерные мышиные-человеческие антитела против TNFα (инфликсимаб, ремикадТМ; Centocor Corporation/Johnson&Johnson), которые показали клиническую эффективность при лечении RA и болезни Крона. Все имеющиеся на рынке ингибиторы TNFα вводят внутривенно или подкожно с интервалом одну неделю или более в виде болюс-инъекций, что обеспечивает высокие начальные концентрации, которые постепенно снижаются к моменту следующей инъекции. Объем распределения ограничен.
Несмотря на описанные достижения, остается потребность в новых и эффективных формах антител или других иммуносвязывающих соединений для лечения TNFα-ассоциированных заболеваний, таких как RA. В частности, имеется насущная необходимость в иммуносвязывающих соединениях с оптимальными функциональными свойствами для эффективного и продолжительного лечения артрита и других TNFα-ассоциированных заболеваний, которые обеспечат более гибкое введение и формуляцию и которые обладают повышенным проникновением в ткани и тем самым обеспечат высокий объем распределения.
Сущность изобретения
Следовательно, основной целью изобретения является обеспечение стабильных и растворимых антител или других иммуносвязывающих соединений, которые специфически связываются с TNFα в условиях in vitro и in vivo. В предпочтительном варианте осуществления указанное иммуносвязывающее соединение представляет собой scFv-антитело или Fab-фрагмент.
Настоящее изобретение относится к стабильным scFv-антителам или Fab-фрагментам, специфическим к TNFα, которые содержат определенные последовательности легкой цепи и тяжелой цепи, оптимизированные в отношении стабильности, растворимости и связывания с TNFα в условиях in vitro и in vivo и низкой иммуногенности. Указанные антитела предназначены для диагностики и/или лечения TNFα-опосредованных заболеваний. Также раскрываются нуклеиновые кислоты, векторы и клетки-хозяева для экспрессии рекомбинантных антител по изобретению, способы их выделения и применение указанных антител в медицине.
Краткое описание фигур
На фигуре 1 показана относительная способность 44 супернатантов гибридом с антителами RabMab против TNFα к связыванию TNFα (тест Biacore) и нейтрализации активности последнего (тест на клетках L929).
На фигуре 2 показана способность 20 одноцепочечных антител RabMab против TNFα и 7 гуманизированных одноцепочечных антител против TNFα к избирательному связыванию с TNFα (тест секреторной ELISA, пожалуйста, обратите внимание, что для данного теста использовали супернатант бактериальной культуры, который не нормализовали по содержанию одноцепочечных антител).
На фигуре 3 показана кинетика связывания антитела EP43max (фигура 3А) и кинетика связывания антитела EP34max (фигура 3В) с человеческим TNFα.
На фигуре 4 показана активность антител EP43max (пустые квадраты) и эффективность антител ESBA105 (закрашенные кружки). EC50 EP43max составляет 1 нг/мл и EC50 ESBA105 составляет 6,5 нг/мл.
На фигуре 5 показана функциональная активность антител EP43max, EP6max и EP19max в тесте термического развертывания молекулы белка (FTIR).
На фигуре 6 приведены кривые тепловой денатурации антитела EP43max и его производных при сравнении FTIR анализом.
На фигуре 7 показано сравнение антитела EP43max (фигура 7А) и его варианта EP43minmax (фигура 7В) в тесте теплового стресса.
На фигуре 8 показано определение CDR H1, использованного в данном документе для трансплантации антигенсвязывающих сайтов из кроличьих моноклональных антител в каркасные области человеческого антитела с высокой растворимостью и стабильностью.
На фигуре 9а показана активность антитела Epi34max и адалимумаба в блокировании цитотоксической активности рекомбинантного человеческого TNFalpha в концентрации 1000 пг/мл (мышиные клетки L929). Было установлено, что IC50 Ep34max и адалимумаба составили соответственно 1,03 нг/мл и 8,46 нг/мл. На фигуре 9b показана активность адалимумаба и антитела Ep34max в блокировании цитотоксической активности рекомбинантного человеческого TNFalpha в концентрации 10 пг/мл (человеческие клетки Kym-1). Было установлено, что значения IC50 инфликсимаба и Ep34max (791) равнялись соответственно 66,2 нг/мл и 0,69 нг/мл.
На фигуре 10а показана активность антитела Epi34max и инфликсимаба в блокировании цитотоксической активности рекомбинантного человеческого TNFalpha в концентрации 1000 пг/мл (мышиные клетки L929). Было установлено, что IC50 Ep34max и инфликсимаба равнялись соответственно 1,04 нг/мл и 13,9 нг/мл. На фигуре 10b показана эффективность инфликсимаба и антитела Ep34max (791) в блокировании цитотоксической активности рекомбинантного человеческого TNFalpha в концентрации 10 пг/мл (человеческие клетки Kym-1). Было установлено, что значения IC50 инфликсимаба и Ep34max составили соответственно 14,8 нг/мл и 0,63 нг/мл.
На фигуре 11 показан график тепловой денатурации BioATR FT-IR по данным трансформированного инфракрасного спектра Fourier в области амидной полосы I антитела Ep34max по сравнению с антителом ESBA903. V50 для ESBA903 составляла 71,12 и для Ep34max 71,50; крутизна ESBA903 2,481 и для Ep34max 2,540.
На фигуре 12 приведены кривые термического развертывания DSC scFv-антител Ep34max и ESBA903. Тпл. антитела Ep34max составляет 78,11°С и Тпл. антитела ESBA903 равняется 76,19°С.
Подробное описание изобретения
Основной целью изобретения является обеспечение стабильного и растворимого иммуносвязывающего соединения, которое специфически связывается с TNFα в условиях in vitro и in vivo. В предпочтительном варианте осуществления указанным производным антитела является scFv-антитело или Fab-фрагмент. Иммуносвязывающие соединения по изобретению предпочтительно содержат легкую и/или тяжелую цепь.
Определения
Для облегчения понимания настоящего изобретения приводятся определения некоторых терминов. Дополнительные определения приводятся по тексту подробного описания.
В том смысле, в котором термин «антитело» используется в данном документе, он является синонимом «иммуноглобулина». Антитела по настоящему изобретению могут представлять собой целые иммуноглобулины или их фрагменты, содержащие, по меньшей мере, одну вариабельную область иммуноглобулина, такую как одноцепочечная вариабельная область, Fv (Skerra A. and Pluckthun A., 1988, Science, 240:1038-1041), scFv (Bird R.E. et al., 1988, Science, 242:423-426; Huston J.S. et al., 1988, Proc. Natl. Acad. Sci. USA, 85:5879-5883), Fab, (Fab’)2 или другие фрагменты, хорошо известные специалистам в данной области.
Термин «CDR» относится к одному из шести гипервариабельных участков внутри вариабельных областей антитела, которые в основном отвечают за связывание с антигеном. Одно из наиболее часто используемых определений шести CDR приводится Kabat E.A. et al., 1991, Sequences of proteins of immunological interest. NIH Publication 91-3242).
В том смысле, в котором в данном документе используется термин CDR, он относится только к CDR1, CDR2 и CDR3 вариабельной области легкой цепи (CDR L1, CDR L2, CDR L3 или L1, L2, L3), а также к CDR2 и CDR3 вариабельной области тяжелой цепи (CDR Н2, CDR Н3 или Н2, Н3). Однако в том смысле, в котором в данном документе определяется CDR1 вариабельной области тяжелой цепи (CDR Н1 или Н1), то он определяется по следующим остаткам (система нумерация Kabat): начинается с положения 26 и заканчивается перед положением 36. По существу это слитая конструкция CDR Н1, как иначе определяется по Kabat и Chotia (также для иллюстрации смотри фигуру 8).
В том смысле, в котором в данном документе используется термин «каркасная область», он относится к участку вариабельной области, VL или VH, который служит в качестве каркаса для антигенсвязывающих петель (CDR) данной вариабельной области. По существу это вариабельная область без CDR.
Термины «одноцепочечное антитело», «одноцепочечный фрагмент Fv» или «scFv» относятся к молекуле, содержащей вариабельную область тяжелой цепи антитела (или область VH) и вариабельную область легкой цепи антитела (или область VL), соединенные через линкер. Такие молекулы scFv имеют общее строение: NH2-VL-линкер-VH-СООН или NH2-VН-линкер-VL-СООН.
Термин «иммуносвязывающее соединение» относится к молекуле, которая содержит весь или часть антигенсвязывающего участка антитела, например, всю или часть вариабельной области тяжелой и/или легкой цепи, так, что иммуносвязывающее соединение специфически распознает антиген-мишень. Не ограничивающие примеры иммуносвязывающих соединений включают полноразмерные молекулы иммуноглобулинов и scFv, а также фрагменты антител, включая, не ограничиваясь этим, (i) Fab-фрагмент, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) F(ab’)2-фрагмент, бивалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком, в шарнирной области; (iii) Fab’-фрагмент, состоящий из доменов VH и CH1; (v) Fv-фрагмент, состоящий из областей VL и VH одного плеча антитела; (vi) однодоменное антитело, такое как Dab-фрагмент, который состоит из доменов VL и VH, антитело Camelid или Shark (например, shark Ig-NAR нанотела®); и (vii) нанотело, область тяжелой цепи, содержащее вариабельную область и две константных области.
Система нумерации, используемая в данном документе для идентификации положений аминокислотных остатков в вариабельных областях тяжелой и легкой цепи антитела, представляет систему, описанную A.Honegger, J. Mol. Biol., 309, 2001, 657-670 (система AHo). Таблицы перевода между таблицами системы AHo и наиболее часто используемой системой, описанной Kabat et al. (Kabat E.A. et al., 1991, Sequences of Proteins of Immunological Interest, Fifth Edition, US Department Health and Human Services, NIH Publication No. 91-3242), приведены A. Honegger, J. Mol. Biol., 309, 2001, 657-670.
Термин «эпитоп» или «антигенная детерминанта» относится к участку на антигене, с которым специфически связывается иммуноглобулин или антитело (например, TNF). Как правило, эпитоп содержит, по меньшей мере, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислот в уникальной пространственной конформации. Смотри, например, Epitope Mapping Protocols in Methods in Molecular Biology, Vol. 66, G.E. Morris, Ed. (1996).
Термины «специфическое связывание», «избирательное связывание», «избирательно связывается» и «специфически связывается» относятся к антителу, которое связывается с эпитопом на заранее определенном антигене. Как правило, антитело связывается с аффинностью (KD), составляющей менее чем 10-7 М, например, примерно менее чем 10-8 М, 10-9 М или 10-10 М, или даже ниже.
Термин KD относится к константе равновесия диссоциации конкретного взаимодействия антитело-антиген. Как правило, антитела по изобретению связываются с TNF с константой равновесия диссоциации (KD) примерно менее чем 10-7 М, например, примерно менее чем 10-8 М, 10-9 М или 10-10 М, или даже ниже, по данным технологии поверхностного плазмонного резонанса (SPR) на аппарате BIACORE.
В том смысле, в котором в данном документе используется термин «идентичность», он относится к совпадению последовательностей двух полипептидов, молекул или двух нуклеиновых кислот. В том случае, когда положение в обеих из двух сравниваемых последовательностях занято одинаковым основанием или аминокислотным мономером (например, если положение в каждой из двух молекул ДНК занято аденином или положение в каждом из полипептидов занято лизином), то тогда соответствующие молекулы являются идентичными по данному положению. «Процентная идентичность» между двумя последовательностями представляет собой функцию числа совпадающих положений в двух последовательностях, деленное на число сравниваемых положений, ×100. Например, если совпадают 6 из 10 положений в двух последовательностях, то тогда две последовательности обладают 60% идентичностью. В качестве примера: ДНК-последовательности CTGACT и CGGTT обладают 50% идентичностью (в целом совпадают 3 из 6 положений). Как правило, сравнение проводят, когда две последовательности выравнивают с получением максимальной идентичности. Такое выравнивание можно проводить с использованием, например, метода Needleman et al., 1970, J. Mol. Biol., 48:443-453, применяя соответственно такие компьютерные программы, как Align program (DNAstar, Inc.). Также можно определить процентную идентичность для двух аминокислотных последовательностей с использованием алгоритма E. Meyers and Miller (Comput. Appl. Biosci., 4:11-17, 1988), который включен в программу ALIGN (версия 2.0), с помощью таблицы весов остатков PAM120, штрафа за пропуск длиной 12 и штрафа за пропуск длиной 4. Кроме того, можно определить процентную идентичность между двумя аминокислотными последовательностями с использованием алгоритма Needleman и Wunsch (J. Mol. Biol., 48:444-453, 1970), который включен в программу GAP в программном пакете GCG (доступен на сайте www.gcg.com), с матрицей Blossum 62 или с матрицей PAM250 и весом пропуска 16, 14, 12, 10, 8, 6 или 4 и весом длины 1, 2, 3, 4, 5 или 6.
«Сходными» последовательностями являются последовательности, которые при выравнивании имеют идентичные или сходные аминокислотные остатки, где сходные остатки представляют консервативные замены на соответствующие аминокислотные остатки в подвергшейся выравниванию референс-последовательности. В этом отношении «консервативная замена» остатка в референс-последовательности представляет замену на остаток, который в физическом или функциональном отношении аналогичен соответствующему референс-остатку, например, имеет аналогичный размер, форму, электрический заряд, химические свойства, в том числе, способность к образованию ковалентных или водородных связей или тому подобное. Таким образом, «модифицированная консервативной заменой» последовательность представляет последовательность, которая отличается от референс-последовательности или последовательности дикого типа по одной или более консервативным заменам. «Процентная сходность» между двумя последовательностями представляет собой функцию числа положений, которые содержат совпадающие остатки или консервативные замены в двух последовательностях, деленное на число сравниваемых положений, ×100. Например, если совпадают 6 из 10 положений в двух последовательностях и 2 из 10 положений содержат консервативные замены, то тогда две последовательности обладают 80% положительной сходностью.
В том смысле, в котором в данном документе используется термин «консервативные модификации последовательности», он относится к аминокислотным модификациям, которые не оказывают отрицательного влияния или не изменяют связывающие характеристики антитела, содержащего аминокислотную последовательность. Такие консервативные модификации последовательности включают нуклеотидные или аминокислотные замены, добавления и делеции. Например, модификации можно вводить стандартными в данной области методами, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены включают замены, в которых аминокислотный остаток замещен аминокислотным остатком с такой же боковой цепью. В данной области известны группы аминокислотных остатков с аналогичными боковыми цепями. Данные группы включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, предполагаемый остаток заменимой аминокислоты в человеческом анти-VEGF-антителе предпочтительно замещен на другой аминокислотный остаток из группы с той же боковой цепью. Способы идентификации нуклеотидных и аминокислотных консервативных замен, которые не приводят к элиминации связывания с антигеном, являются хорошо известными в данной области (смотри, например, Brummell et al., Biochem, 32:1180-1187, 1993; Kobayashi et al., Protein Eng., 12(10):879-884, 1999 и Burks et al., Proc. Natl. Acad. Sci. USA, 94:412-417, 1997).
В том смысле, в котором в данном документе используется термин «аминокислотная консенсусная последовательность», он относится к аминокислотной последовательности, которую можно получить с использованием матрицы, по меньшей мере, из двух и предпочтительно более подвергшихся выравниванию аминокислотных последовательностей, с пропусками при выравнивании, так что становится возможным определить наиболее часто встречаемый аминокислотный остаток в каждом положении. Консенсусная последовательность представляет такую последовательность, которая содержит аминокислоты, которые наиболее часто присутствуют в каждом положении. В том случае, когда две или более аминокислот в равной степени находятся в одном положении, то консенсусная последовательность включает обе или все такие аминокислоты.
Аминокислотную последовательность белка можно анализировать на различных уровнях. Например, консерватизм или вариабельность могут проявляться на уровне одного остатка, на уровне многочисленных остатков, многочисленных остатков с пропусками и т.п. Остатки могут проявлять консерватизм идентичного остатка или они могут быть консервативными на уровне группы. Примеры групп аминокислот включают полярные, но незаряженные R-группы (серин, треонин, аспарагин и глутамин); положительно заряженные R-группы (лизин, аргинин и глутамин); отрицательно заряженные R-группы (глутаминовая кислота и аспарагиновая кислота); гидрофобные R-группы (аланин, изолейцин, лейцин, метионин, фенилаланин, триптофан, валин и тирозин); и особые аминокислоты (цистеин, глицин и пролин). Специалистам в данной области известны другие группы аминокислот, и их можно определить с использованием структурных определений или других данных для оценки замещаемости. В этом смысле заменяемую аминокислоту можно отнести к любой аминокислоте, которую можно заместить и при этом сохранить функциональный консерватизм в этом положении.
Очевидно, понятно аминокислоты одной и той же группы могут различаться по степени проявления их биофизических свойств. Например, известно, что некоторые гидрофобные R-группы (например, аланин, серин или треонин) являются более гидрофильными (т.е. обладают более высокой гидрофильностью или более низкой гидрофобностью) по сравнению с другими гидрофобными R-группами (например, валином или лейцином). Относительную гидрофильность или гидрофобность можно определить с использованием общепринятых в данной области способов (смотри, например, Rose et al., Science, 229:834-838, 1985 и Cornette et al., J. Mol. Biol., 195:659-685, 1987).
В том смысле, в котором в данном документе одну аминокислотную последовательность (например, первую последовательность VH или VL) выравнивают с одной или более дополнительными аминокислотными последовательностями (например, одной или более последовательностями VH или VL, имеющихся в базе данных), то аминокислотное положение в последовательности (например, в первой последовательности VH или VL) можно сравнить с «соответствующим положением» в одной или более дополнительных аминокислотных последовательностях. В том смысле, в котором в данном документе используется термин «соответствующее положение», то он представляет равноценное положение в сравниваемой последовательности(ях), когда последовательности оптимально выровнены, т.е. когда последовательности выравниваются для достижения наиболее высокой процентной идентичности или процентной сходности.
В том смысле, в котором в данном документе используется термин «химерные» иммуносвязывающие соединения, он относится к антителам, которые содержат участок тяжелой и/или легкой цепи, идентичный или гомологичный соответствующим последовательностям в антителах, полученных из конкретного вида или принадлежащих к конкретной группе или подгруппе антител, в то время как остальная часть цепи(ей) идентична или гомологична соответствующим последовательностям в антителах, полученных из другого вида или принадлежащих к другой группе или подгруппе антител, а также фрагментам таких антител.
В том смысле, в котором в данном документе используется термин «гуманизированные антитела», он относится к иммуносвязывающим соединениям, которые синтезированы с использованием технологии рекомбинантной ДНК, для элиминации иммунного ответа на чужеродные антигены. Получение гуманизированных антител является хорошо известным методом, применяемым для снижения иммуногенности моноклональных антител из чужеродных источников. Гуманизированное антитело состоит из гуманизированной вариабельной области тяжелой цепи, гуманизированной вариабельной области легкой цепи и полностью человеческих константных областей. Гуманизация вариабельной области включает выбор каркасной области-акцептора, как правило, человеческой каркасной области-акцептора, числа CDR из иммуносвязывающего соединения-донора для вставки в каркасную область-акцептор вариабельной области и замену остатков из каркасной области-донора в каркасной области-акцепторе. Общий способ трансплантации CDR в человеческие акцепторные каркасные области раскрыт Winter в патенте США № 5225539, который в полном объеме включен в данный документ для сведения. В патенте США № 6407312 приведены наставления, которые в полном объеме включены в данный документ для сведения, раскрывается ряд аминокислотных положений каркасной области, для которых предпочтительной является замена из донорного иммуносвязывающего соединения.
В том смысле, в котором в данном документе используется термин «функциональное свойство», он представляет свойство полипептида (например, иммуносвязывающего соединения), которое желательно улучшить (например, по сравнению с обычным полипептидом) и/или которое является преимущественным для специалиста в данной области, например, в целях улучшения производственных характеристик или терапевтической эффективности полипептида. В одном варианте осуществления функциональное свойство представляет собой повышенную стабильность (например, стабильность к нагреванию). В другом варианте осуществления функциональное свойство представляет собой повышенную растворимость (например, в условиях клетки). В еще одном варианте осуществления функциональное свойство представляет собой отсутствие агрегации. В еще одном варианте осуществления функциональное свойство представляет собой повышение экспрессии (например, в прокариотической клетке). В еще одном варианте осуществления функциональное свойство представляет повышение выхода белка после рефолдинга при выделении из телец включений. В некоторых вариантах осуществления функциональное свойство не представляет собой повышение аффинности связывания антигена.
Термин «нуклеиновокислотная молекула» относится к молекулам ДНК и молекулам РНК. Нуклеиновокислотная молекула представляет одноцепочечную или двухцепочечную, но предпочтительно двухцепочечную ДНК. Нуклеиновая кислота «операбельно связана», когда она имеет функциональную связь с другой нуклеиновокислотной последовательностью. Например, промотор или энхансер операбельно связан с кодирующей последовательностью, если он оказывает влияние на транскрипцию последовательности.
Термин «вектор» относится к нуклеиновокислотной молекуле, способной транспортировать другую нуклеиновую кислоту, с которой она связана. Одним типом вектора является «плазмида», которая представляет собой циклическую двухцепочечную ДНК-петлю, в которую могут быть лигированы дополнительные сегменты ДНК. Другой тип вектора представляет вирусный вектор, с которым можно лигировать дополнительные сегменты в вирусный геном. Некоторые векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, содержащие бактериальный ориджин репликации, и эписомальные векторы млекопитающих). Другие векторы (например, неэписомальные векторы млекопитающих) можно интегрировать в геном клетки-хозяина при введении в клетку-хозяин и обеспечив тем самым репликацию вместе с геномом хозяина.
Термин «клетка-хозяин» относится к клетке, в которую введен экспрессирующий вектор. Клетки-хозяева могут включать бактериальные, микробные, растительные клетки и клетки животных. Бактерии, чувствительные к трансформации, включают члены семейства энтеробактерий, такие как штаммы Escherichia coli или Salmonella; Bacillaceae, такие как Bacillus subtilis; Pneumococcus; Streptococcus и Haemophilus influenzae. Подходящие микроорганизмы включают Saccharomyces cerevisiae и Pichia pastoris. Подходящие клетки-хозяева животных включают клетки CHO (линии клеток яичника китайского хомячка) и клетки NSO.
Термины «лечить», «лечение» и «терапия» относятся к лечебным или профилактическим мероприятиям, описанным в данном документе. В способах «лечения» используется введение субъекту, нуждающемуся в таком лечении, антитела по настоящему изобретению, например, субъекту с уже имеющимся TNFα-опосредованным нарушением или субъекту, у которого имеется риск развития такого нарушения, в целях профилактики, лечения, замедления, снижения тяжести заболевания или ослабления одного или более симптомов заболевания, или предупреждения рецидивирования заболевания для пролонгации выживаемости субъекта по сравнению с отсутствием такого лечения.
Термин «TNFα-опосредованное нарушение» или «TNFα-опосредованное заболевание» относится к заболеванию, для начала развития, прогрессирования или устойчивого проявления симптомов или его болезненных состояний необходимо участие TNF. Приведенные в качестве примера TNFα-опосредованные нарушения включают, не ограничиваясь этим, хронические и/или аутоиммунные воспалительные заболевания в целом, опосредованные иммунной системой воспалительные заболевания в целом, воспалительное заболевание ЦНС, воспалительные заболевания, поражающие глаза, суставы, кожу, слизистые, центральную нервную систему, желудочно-кишечный тракт, мочевые пути или легкие, увеиты в целом, ретинит, HLA-B27+увеит, болезнь Бехчета, синдром сухого глаза, глаукому, синдром Шегрена, сахарный диабет (включая диабетическую нейропатию), резистентность к инсулину, артриты в целом, ревматоидный артрит, остеоартрит, реактивный артрит и синдром Рейтера, юношеский артрит, анкилозирующий спондилит, рассеянный склероз, синдром Гуллиана-Барре, тяжелую миастению, амиотрофический латеральный склероз, саркоидоз, гломерулонефрит, хроническое заболевание почек, цистит, псориаз (включая псориатический артрит), гидраденит гнойный, панникулит, гангренозную пиодермию, синдром SAPHO (синовит, акне, пустулез, гиперстоз и остеит), акне, синдром Свита, пемфигус, болезнь Крона (включая некишечные проявления заболевания), язвенный колит, бронхиальную астму, гиперчувствительность при пневмонии, общие аллергии, аллергический ринит, аллергический синусит, хроническое обструктивное заболевание легких (COPD), фиброз легких, гранулематоз Вегенера, синдром Кавасаки, гигантоклеточный артерит, васкулит Чарга-Стросса, нодозный полиартрит, ожоги, синдром трансплантат против хозяина, реакции хозяин против трансплантата, эпизоды отторжения после трансплантации органа или костного мозга, системные и местные проявления васкулита в целом, системную и дискоидную красную волчанку, полимиозит и дерматомиозит, склеродермию, преэклампсию, острый и хронический панкреатит, вирусный гепатит, гепатит в результате злоупотребления алкоголем, послеоперационное воспаление, такое как воспаление после операции на глазах (например, по поводу катаракты (замена хрусталика) или операции по поводу глаукомы), после операции на суставах (включая артроскопическую операцию), после операции на структурах, связанных с суставами (например, связках), после операции в ротовой полости и/или стоматологических операций, после минимально инвазивных вмешательств на сердце и сосудах (например, PTCA, атеректомии, размещения стента), после лапароскопических и/или эндоскопических внутрибрюшинных и гинекологических процедур, после эндоскопических урологических вмешательств (например, операции на предстательной железе, уретероскопии, цистоскопии, интерстициальный цистит), или воспаление в периоперативный период (профилактика) в целом, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, паралич Белла, болезнь Крейцфельда-Якоба; связанный со злокачественным заболеванием остеолизис, связанное со злокачественным заболеванием воспаление, связанная со злокачественным заболеванием боль, связанная со злокачественным заболеванием кахексия, метастазы в кости, острые и хронические формы боли, независимо от того, вызваны они центральными или периферическими эффектами TNFα, и независимо от того, классифицируются они как воспалительная, ноцицептивная или неройпатическая формы боли, ишиас, боль в нижней области спины, синдром запястного канала, комплексный регионарный болевой синдром (CRPS), подагру, невралгию после герпеса, фибромиалгию, местные болевые состояния, синдромы хронической боли в результате метастазирующей опухоли, дисменорею; бактериальный, вирусный или грибковый сепсис, туберкулез, СПИД, атеросклероз, заболевание коронарных артерий, гипертензию, дислипидемию, сердечную недостаточность и хроническую сердечную недостаточность. Термин «эффективная доза» или «эффективная дозировка» относится к количеству, достаточному для достижения или, по меньшей мере, для частичного достижения желаемого эффекта. Термин «терапевтически эффективная доза» определяется, как количество, достаточное для излечения или, по меньшей мере, для частичного купирования заболевания и его осложнений у пациента, уже страдающего заболеванием. Количества, эффективные для данного применения, будут зависеть от тяжести заболевания, которое подвергается лечению, и общего состояния собственной иммунной системы пациента.
Термин «субъект» относится к человеку или животному, отличному от человека. Например, способы и композиции по настоящему изобретению можно использовать для лечения субъекта с TNF-опосредованным нарушением.
Термин «зайцеобразные» относится к членам таксономического отряда Зайцеобразные, состоящего из семейств Зайцы (например, зайцы и кролики) и Пищуховые (пищухи). В наиболее предпочтительном варианте осуществления представителем зайцеобразных является кролик. В том смысле, в котором в данном документе используется термин «кролик», он относится к животному, принадлежащему к семейству Зайцы.
Различные номенклатуры использовали для полученных иммуносвязывающих соединений. Как правило, их идентифицируют по номеру (например, #34). В тех случаях, когда используют префикс, такой как EP или Epi (например, EP 34, который идентичен Epi 34 или #34), то указывается одно и то же иммуносвязывающее соединение.
Если не указано иначе, то все технические и научные термины, использованные в данном документе, имеют то же значение, которое обычно понимается специалистами в данной области, к которой относится данное изобретение. Несмотря на то, что на практике или при тестировании настоящего изобретения можно использовать методы и вещества, аналогичные или эквивалентные описанным в данном документе, подходящие способы и вещества описаны ниже. В случае конфликта настоящая заявка, включая определения, будет контролировать. Кроме того, вещества, способы и примеры являются только иллюстративными и не предназначаются для ограничения.
Ниже различные аспекты изобретения будут подробно описаны в последующих подразделах. Очевидно, понятно, что различные варианты осуществления, преимущества и ограничения по желанию можно комбинировать. Кроме того, в зависимости от конкретного варианта осуществления можно не использовать выбранные определения, варианты осуществления или ограничения.
Анти-TNFα-антитела
В одном аспекте настоящее изобретение относится к иммуносвязывающим соединениям, которые связываются с TNFα и, таким образом, являются подходящими для блокирования функции TNFα в условиях in vivo. CDR данных иммуносвязывающих соединений получены из кроличьих моноклональных анти-TNFα-антител, как описано в патенте США № 7431927. Известно, что кроличьи антитела обладают особенно высокой аффинностью. Кроме того, последовательности CDR, раскрытые в данном документе, являются природными последовательностями, означая, что не требуется проводить созревания аффинности полученных иммуносвязывающих соединений. В предпочтительном варианте осуществления иммуносвязывающее соединение нейтрализует TNFα в условиях in vivo.
В некоторых вариантах осуществления изобретение относится к иммуносвязывающему соединению, которое специфически связывается с TNFα, содержащему, по меньшей мере, одну из аминокислотных последовательностей CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 или CDRL3. Приведенные в качестве примера аминокислотные последовательности CDR для применения в иммуносвязывающих соединениях по изобретению приведены как SEQ ID No:3-50 (таблица 1). CDR с последовательностями SEQ ID No:3-50 можно трансплантировать на любой подходящий связывающий каркас с использованием принятых в данной области способов (смотри, например, Reichmann L. et al., 1998, Nature, 332:323-327; Jones P. et al., 1986, Nature, 321:522-525; Queen C. et al., 1989, Proc. Natl. Acad. Sci. USA, 86:10029-10033; патент США № 5225539, Winter и патенты США № 5530101; 5585089; 5693762 и 6180370, Queen et al.). В одном антителе можно объединить CDR из других исходных антител с получением дополнительных видов антител. Однако предпочтительно, чтобы иммуносвязывающие соединения, раскрытые в данном документе, были гуманизированными, и таким образом, подходящими для терапевтических применений.
Таким образом, в одном варианте осуществления изобретение относится к иммуносвязывающему соединению, которое специфически связывается с человеческим TNFα, где иммуносвязывающее соединение содержит:
(i) гуманизированную вариабельную область тяжелой цепи (VH), где вариабельная область тяжелой цепи содержит последовательность человеческой вариабельной каркасной области тяжелой цепи и последовательности CDR H1, CDR H2 или CDR H3, происходящие из кроличьего иммуносвязывающего соединения; и/или
(ii) гуманизированную вариабельную область легкой цепи (VL), где вариабельная область легкой цепи содержит последовательность человеческой вариабельной каркасной области легкой цепи и последовательности CDR L1, CDR L2 или CDR L3, происходящие из кроличьего иммуносвязывающего соединения.
Как это известно в данной области, многие VH кроличьих цепей содержат дополнительные парные цистеины по сравнению с мышиными и человеческими аналогами. В дополнение к консервативным дисульфидным мостикам, образованным cys22 и cys92, также имеется мостик cys21-cys79, а также мостик S-S между CDR, образованный между последним остатком CDRH1 и первым остатком CDRH2 в некоторых кроличьих цепях. Кроме того, пары цистеиновых остатков часто обнаруживают в CDR-L3. Дополнительно многие CDR кроличьих антител не относятся к какой-либо ранее известной канонической структуре. В частности, CDR-L3 часто имеет большую длину по сравнению с CDR-L3 человеческого или мышиного аналога.
В дополнение к кроликам в изобретении также можно использовать для трансплантации CDR любого представителя Зайцеобразных.
В случае антител кроличьи CDR с последовательностями SEQ ID No:3-50 могут быть «пересажены» в каркасные области любого антитела из любого вида. Однако ранее было установлено, что антитела или производные антител, содержащие каркасные области, идентифицированные в так называемом скрининге «контроля качества» (международная заявка WO0148017), обычно характеризуются высокой стабильностью и/или растворимостью и, таким образом, также могут быть пригодными в контексте внеклеточных применений, таких как нейтрализация человеческого TNFα. Кроме того, также было установлено, что одна конкретная комбинация данных растворимых и стабильных каркасных областей VL (вариабельной области легкой цепи) и VH (вариабельной области тяжелой цепи) является особенно пригодной для «принятия» кроличьих CDR. Неожиданно было установлено, что при трансплантации в указанную каркасную область или ее производные может быть полностью сохранена петлевая конформация большого разнообразия кроличьих CDR, в основном независимо от последовательности донорной каркасной области. Кроме того, указанная каркасная область или ее производные, содержащие различные кроличьи CDR, хорошо экспрессируются и хорошо продуцируются в противоположность кроличьим единичным цепям дикого типа и почти полностью сохраняют аффинность исходных кроличьих антител-доноров. Следовательно, в одном варианте осуществления CDR с последовательностями SEQ ID No:3-50 трансплантируют в каркасные области человеческого антитела, полученные в результате скрининга «контроля качества», раскрытого в EP1479694. Аминокислотные последовательности приведенных в качестве примера каркасных областей для применения в изобретении представлены как SEQ ID No:1 и 2 ниже.
SEQ ID No:1
Вариабельная область легкой цепи FW1.4
EIVMTQSPSTLSASVGDRVIITC(X)n=3-50WYQQKPGKAPKLLIY(X)n=3-50
VPSRFSGSGGSGAEFTLTISSLQPDDFATYYC(X)n=3-50FGQGTKLTVLG
SEQ ID No:2
Вариабельная область тяжелой цепи FW1.4
EVQLVESGGGLVQPGGSLRLSCAAS(X)n=3-50WVRQAPGKGLEWVS(X)n=3-50
RFTISRDNSKNTLYLQMNSLRAEDTAVYYCAK(X)n=3-50WGQGTLVTVSS
Х может представлять любую природную аминокислоту. Может присутствовать, по меньшей мере, от 3 до 50 аминокислот. Как правило, CDR вводят в сайты, в которых присутствует Х.
В других вариантах осуществления изобретение относится к иммуносвязывающему соединению, которое специфически связывается с TNFα, содержащему, по меньшей мере, одну аминокислотную последовательность VH или VL. Приведенные в качестве примера аминокислотные последовательности VH или VL для применения в иммуносвязывающих соединениях по изобретению представляют последовательности SEQ ID No:51-111.
В некоторых вариантах осуществления изобретение также относится к иммуносвязывающему соединению, которое специфически связывается с TNFα, содержащему аминокислотную последовательность с существенной сходностью с аминокислотной последовательностью SEQ ID No:51-111, и где иммуносвязывающее соединение сохраняет или имеет улучшенные желаемые функциональные свойства иммуносвязывающего соединения против TNFα по изобретению. Приведенные в качестве примера процентные сходности включают, не ограничиваясь этим, примерно 50%, 60%, 70%, 75%, 80%, 85%, 90% или 95% идентичность.
В некоторых вариантах осуществления изобретение также относится к иммуносвязывающему соединению, которое специфически связывается с TNFα, содержащему аминокислотную последовательность с существенной идентичностью с аминокислотной последовательностью SEQ ID No:51-111, и где иммуносвязывающее соединение сохраняет или имеет улучшенные желаемые функциональные свойства иммуносвязывающего соединения против TNFα по изобретению. Приведенные в качестве примера процентные идентичности включают, не ограничиваясь этим, примерно 50%, 60%, 70%, 75%, 80%, 85%, 90% или 95% идентичность.
В некоторых вариантах осуществления изобретение также относится к иммуносвязывающему соединению, которое специфически связывается с TNFα, содержащему аминокислотную последовательность с консервативными заменами относительно аминокислотной последовательности SEQ ID No:51-111, и где иммуносвязывающее соединение сохраняет или имеет улучшенные желаемые функциональные свойства иммуносвязывающего соединения против TNFα по изобретению.
В наиболее предпочтительном варианте осуществления иммуносвязывающее соединение по изобретению содержит, по меньшей мере, одну последовательность CDR, которая, по меньшей мере, на 80%, более предпочтительно, по меньшей мере, на 85%, 90%, 95% или 100% идентична любой из последовательностей SEQ ID No:3-50.
В предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:3-8.
В другом предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:9-14.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:15-20.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:21-26.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:27-32.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:33-38.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:39-44.
В еще одном предпочтительном варианте осуществления изобретения обеспечивается иммуносвязывающее соединение, содержащее, по меньшей мере, один, предпочтительно два, три, четыре, пять или наиболее предпочтительно шесть CDR из группы, состоящей из последовательностей SEQ ID No:45-50.
Последовательности CDR SEQ ID No:3-50, приведенные в данном документе, могут дополнительно содержать замены. Предпочтительно последовательности содержат 3, более предпочтительно 2 и наиболее предпочтительно только одну замену(ы). Указанные замены предпочтительно представляют замены, которые не оказывают отрицательного влияния на избирательную связывающую способность иммуносвязывающего соединения, но аффинность иммуносвязывающего соединения изменяется, предпочтительно, повышается.
Rabmab-доноры CDR
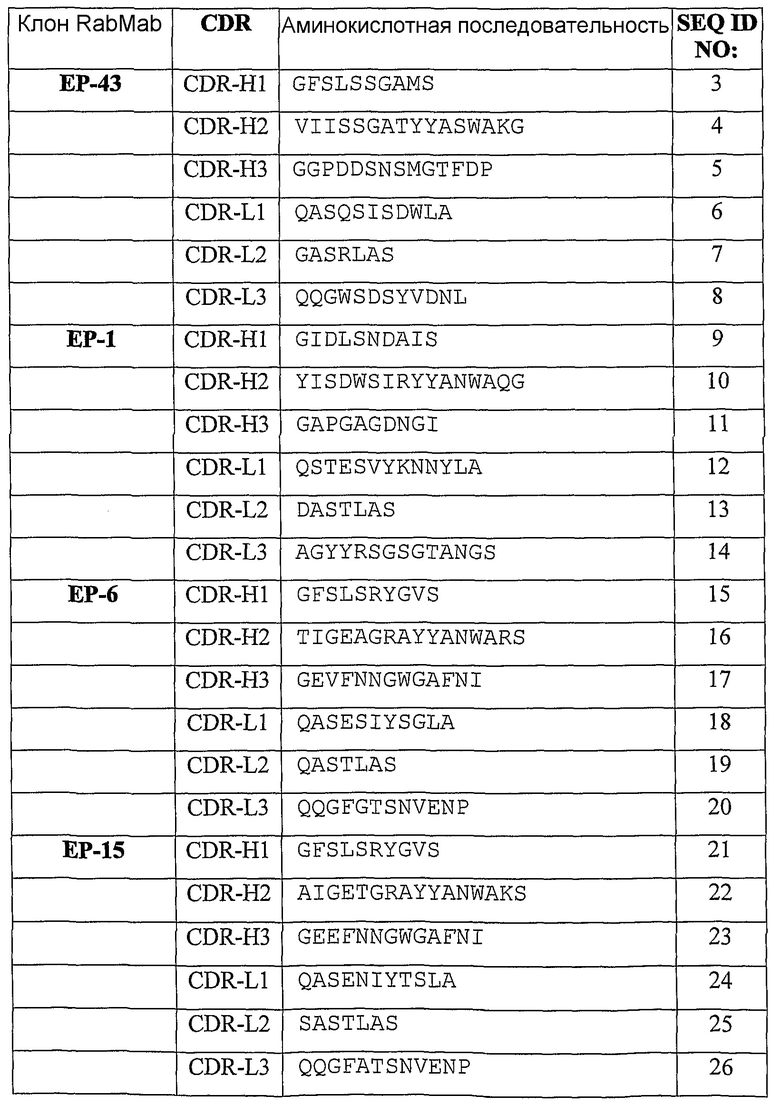
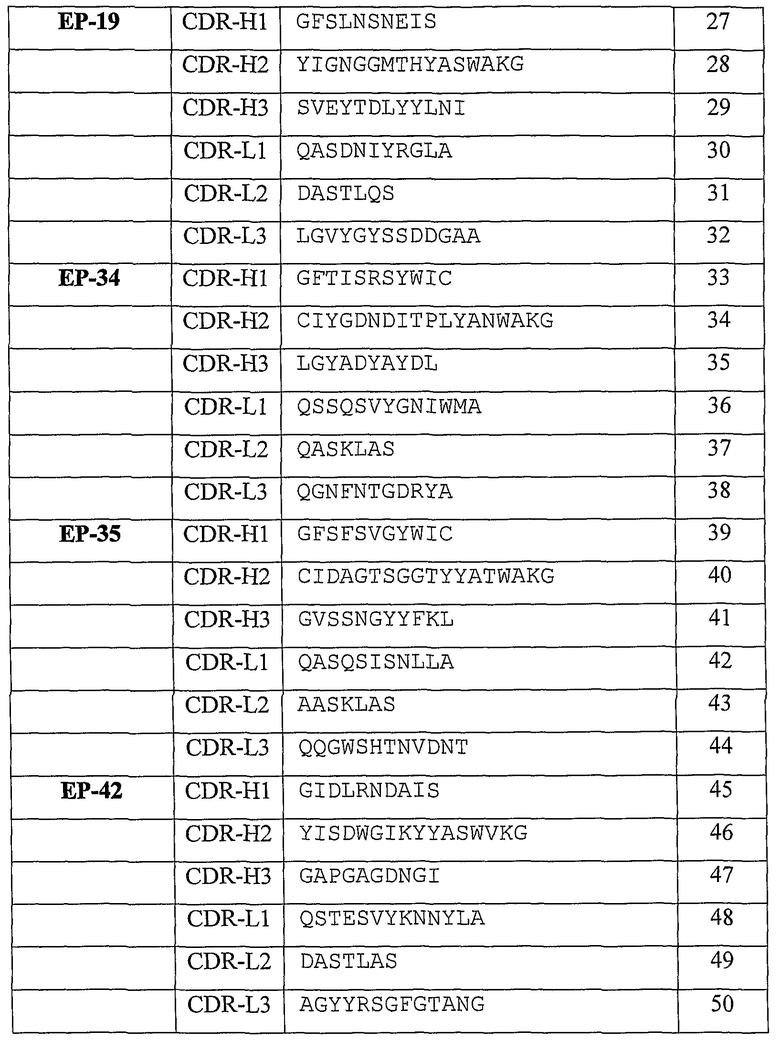
В другом варианте осуществления изобретение относится к антителам, которые связываются с эпитопом на человеческом TNFα, который распознается моноклональным антителом, содержащим ряд CDR (H1-H3, L1-L3; относящимся к клону Rabmab), как приведено в таблице 1. Такие антитела можно идентифицировать, основываясь на их способности перекрестно конкурировать с антителом из таблицы 1 в обычном тесте связывания с TNF. Способность тестируемого антитела ингибировать связывание антитела из таблицы 1 с человеческим TNFα свидетельствует о том, что тестируемое антитело может конкурировать с антителом из таблицы 1 за связывание с человеческим TNFα и, таким образом, оно взаимодействует с одним и тем же эпитопом на человеческом TNFα, что и антитело из таблицы 1. В предпочтительном варианте осуществления антитело, которое связывается с одним и тем же эпитопом на человеческом TNFα, что и антитела, приведенные в таблице 1, представляет человеческое моноклональное антитело. Такие человеческие моноклональные антитела можно получить и выделить, как описано в данном документе.
В одном варианте осуществления антитела или фрагменты антител по настоящему изобретению представляют собой одноцепочечные антитела (scFv) или Fab-фрагменты. В случае scFv-антител выбранная VL-область может быть связана с выбранной VH-областью в любой ориентации посредством гибкого линкера. Подходящая структура линкера, известного в данной области, представляет собой аминокислотную последовательность GGGGS или ее варианты. В предпочтительном варианте осуществления настоящего изобретения используют линкер (GGGGS)4 (SEQ ID No:72) или его производные, но также возможны варианты из 1-3 повторов (Holliger et al., 1993, Proc. Natl. Acad. Sci. USA, 90:6444-6448). Другие линкеры, которые можно использовать для настоящего изобретения, описаны Alfthan et al., 1995, Protein Eng., 8:725-731; Choi et al., 2001, Eur. J. Immunol., 31:94-106; Hu et al., 1996, Cancer Res., 56:3055-3061; Kipriyanov et al., 1999, J. Mol. Biol., 293:41-56 и Roovers et al., 2001, Cancer Immunol. Immunother., 50:51-59. Расположение может представлять следующее: NH2-VL-линкер-VH-COOH или NH2-VH-линкер-VL-COOH, при том, что первая ориентация является предпочтительной. В случае Fab-фрагментов выбранные вариабельные области легкой цепи VL слиты с константной областью цепи каппа человеческого Ig, в то время как подходящие вариабельные области тяжелой цепи VH слиты с первым (N-концевым) СН1 константной области человеческого IgG. В С-конце образуется межцепочечный дисульфидный мостик между двумя константными областями.
Антитела или производные антител по настоящему изобретению могут иметь аффинности к человеческому TNF, которые можно охарактеризовать значениями констант диссоциации Kd в пределах 1 фМ до 10 мкМ. В предпочтительном варианте осуществления настоящего изобретения Kd составляет ≤1 нМ. Аффинность антитела для антигена можно определить экспериментально с использованием подходящего метода (Berzofsky et al. «Antibody-Antigen Interactions» в «Fundamental Immunology», Paul W.E., Ed., Raven Press: New York, NY, 1992; Kuby J., Immunology W.H., Freeman and Company: New York, NY) и методов, описанных в указанных источниках.
Предпочтительные антитела включают антитела, содержащие вариабельную область тяжелой (VH) и/или вариабельную область легкой (VL) цепи, со следующими последовательностями VH и VL (последовательности CDR подчеркнуты):


















Получение анти-TNF-антител
Настоящее изобретение основано, по меньшей мере, частично на установлении того, что каркасные области человеческих антител с высокой растворимостью и стабильностью, идентифицированные в тесте контроля качества (QC), являются особенно подходящими каркасными областями для «приема» CDR от других видов животных, отличных от человека, например, кроличьих CDR. В частности, изобретение основано на установлении того факта, что вариабельные области легкой и тяжелой цепи конкретного человеческого антитела (так называемого антитела «FW 1.4») являются особенно пригодными в качестве акцепторов для CDR из различных кроличьих антител с различной специфичностью связывания. Несмотря на то что каркасная область человеческого одноцепочечного антитела FW 1.4 ESBA Tech’s явно не «проявила себя» в тесте контроля качества и при экспрессии в клетках HeLa при использовании с ее исходными CDR (как описано в международной заявке WO03097697), неожиданно было установлено, что при объединении с другими CDR, такими как кроличьи CDR, образуются очень стабильные, растворимые и хорошо продуцируемые одноцепочечные антитела. Кроме того, гуманизированные иммуносвязывающие соединения, полученные трансплантацией кроличьих CDR в данные хорошо совместимые каркасные области легкой и тяжелой цепей устойчиво и воспроизводимо сохраняют связывающую способность кроличьих антител, из которых получены донорные CDR. Кроме того, иммуносвязывающие соединения, полученные способами по изобретению, воспроизводимо проявляют высокие функциональные свойства, такие как растворимость и стабильность. Следовательно, основной целью изобретения является обеспечение способов трансплантации кроличьих и других «нечеловеческих» CDR в каркасные области легкой цепи и/или тяжелой цепи растворимых и стабильных человеческих антител соответственно с последовательностями SEQ ID No:1 (K127) и SEQ ID No:2 (a43) с получением тем самым гуманизированных антител с улучшенными биофизическими свойствами.
В предпочтительном варианте осуществления каркасная область содержит одну или более замен в каркасной области тяжелой цепи (VH) в положении из группы, состоящей из Н24, Н25, Н56, Н82, Н84, Н89 и Н108 (система нумерации AHo). Дополнительно или альтернативно каркасная область может содержать замену в каркасной области легкой цепи (VH) в положении L87 по системе нумерации AHo. Было показано, что наличие указанных замен обеспечивает каркасную область-акцептор, которая почти полностью сохраняет аффинность исходных антител-доноров. В более предпочтительном варианте осуществления в последовательности каркасной области присутствует одна или более замен, выбранных из группы, состоящей из треонина (Т) в положении Н24, валина (V) в положении Н25, глицина (G) или аланина (А) в положении Н56, лизина (K) в положении Н82, треонина (T) в положении Н84, валина (V) в положении Н89 и аргинина (R) в положении Н108, и треонина (Т) в положении L87 согласно системе нумерации AHo.
Таким образом, в еще более предпочтительном варианте осуществления каркасная область-акцептор представляет:



Х может представлять любую природную аминокислоту; может присутствовать, по меньшей мере, от 3 до 50 аминокислот. Как правило, CDR вводят в сайты, в которых присутствует Х.
Антитела или производные антител по настоящему изобретению можно получить с использованием обычных методов, известных в области рекомбинантной генетики. Имея информацию о последовательности полипептидов, можно получить кДНК, кодирующие их, синтезом генов с использованием способов, хорошо известных в данной области. Данные кДНК можно клонировать в подходящие плазмиды-векторы. После обеспечения ДНК, кодирующей области VL и/или VH, можно провести сайт-направленный мутагенез, например, ПЦР с использованием мутагенных праймеров для получения различных производных. Можно выбрать наилучшую «исходную» последовательность с учетом числа желаемых изменений в последовательностях VL и/или VH. Предпочтительными последовательностями являются последовательности ТВ-А и их производные, например, последовательности scFv или гибридные пептидные последовательности Fab, их можно выбрать в качестве матриц для ПЦР-опосредованного мутагенеза и/или клонирования.
Способы включения или трансплантации CDR в каркасные области включают протоколы, описанные, например, Riechmann L. et al., 1998, Nature, 332:323-327; Jones P. et al., 1986, Nature, 321:522-525; Queen et al., 1989, Proc. Natl. Acad. Sci. USA, 86:10029-10033; патент США № 5225539, Winter и патенты США № 5530101; 5585089; 5693762 и 6180370, Queen et al., а также способы, раскрытые в предварительных заявках на патент США № 61/075697 и 61/155041 под названием «Humanization of Rabbit Antibodies Using Universal Antibody Frameworks», поданными соответственно 25 июня 2008 и 4 февраля 2009.
Для присоединения линкеров, переставленных доменов или слитых конструкций при получении Fab-фрагментов можно использовать обычные методы клонирования и мутагенеза, хорошо известные специалистам в данной области. Основные протоколы, раскрывающие общие способы по данному изобретению, описаны в «Molecular Cloning, A Laboratory Manual» (Sambrook&Russel, 3th ed., 2001) и в «Current Protocols in Molecular Biology» (Ausubel et al., 1999).
Последовательность ДНК, несущая ген, кодирующий полипептид scFv, или в случае Fab-фрагментов, кодирующая каждый из двух отдельных генов или би-цистронный оперон, содержащий два гена для слитых конструкций VL-Cκ и VH-CH1, клонируют в подходящий экспрессирующий вектор, предпочтительно вектор с индуцибельным промотором. Следует соблюдать осторожность в том отношении, чтобы впереди каждого гена имел место соответствующий сайт связывания рибосомы для гарантии трансляции. Очевидно, понятно, что антитела по настоящему изобретению содержат раскрытые последовательности в большей степени, чем полностью состоят из них. Например, для стратегий клонирования может потребоваться, чтобы была получена конструкция антитела с наличием одного или более дополнительных остатков в N-конце. В частности, метионин из старт-кодона может присутствовать в конечном белке в тех случаях, когда он не отщепляется после трансляции. Большинство конструкций scFv-антител имеет дополнительный аланин в N-конце. В предпочтительном варианте осуществления настоящего изобретения выбирается экспрессирующий вектор для экспрессии в периплазматическое пространство в E. coli (Krebber, 1997). Указанный вектор содержит промотор впереди отщепляемой сигнальной последовательности. Затем кодирующую последовательность пептида антитела сливают в рамке считывания с отщепляемой сигнальной последовательностью. Это позволяет направить экспрессированный полипептид в периплазму бактерий, где сигнальная последовательность отщепляется. Затем антитело подвергается укладке. В случае Fab-фрагментов оба гибридных пептида VL-Cκ и VH-CH1 должны быть связаны с секретируемым сигналом. С-концевые цистеины образуют ковалентную S-S-связь после того, как пептиды достигают периплазмы. Если предпочтительной является цитоплазматическая экспрессия антител, то указанные антитела обычно можно получить с высоким выходом из телец включений, которые можно легко отделить от других клеточных фрагментов и белка. В данном случае тельца включений солюбилизируют в денатурирующем агенте, таком как гуанидин гидрохлорид (GndHCl), и затем подвергают рефолдингу посредством ренатурации, хорошо известной специалистам в данной области.
Плазмиды, экспрессирующие полипептиды scFv или Fab, вводят в подходящий хозяин, предпочтительно в бактериальную, дрожжевую клетку или клетку млекопитающих, наиболее предпочтительно в подходящий штамм E. coli, например, JM83, для экспрессии в периплазматическое пространство или в BL21 для экспрессии в тельца включений. Полипептиды можно выделить из периплазмы или из телец включений и очистить с использованием обычных методов, таких как ионообменная хроматография, обратнофазовая хроматография, аффинная хроматография и/или гель-фильтрация, хорошо известных специалистам в данной области.
Антитела или производные антител по настоящему изобретению можно охарактеризовать в отношении выхода, растворимости и стабильности в условиях in vitro. Способность к связыванию с TNF, предпочтительно с человеческим TNFα, можно тестировать в условиях in vitro с помощью ELISA или поверхностного плазмонного резонанса (BIACore) с использованием рекомбинантного человеческого TNF, как описано в международной заявке WO9729131, последний метод позволяет также определить константу скорости диссоциации koff, которая предпочтительно должна составлять менее 10-3 сек-1. Предпочтительные значения Kd составляют ≤10 нМ.
Помимо антител с высокой аффинностью связывания для человеческого TNF также желательно получить анти-TNF-антитела, которые обладают положительными свойствами с точки зрения перспективы их применения в терапии. Например, антитело может представлять антитело, проявляющее нейтрализующую активность в тесте оценки TNF-опосредованной цитотоксичности на клетках L929. В данном тесте оценки токсичности мышиные фибробласты L929, обработанные актиномицином, подвергают стимуляции рекомбинатным человеческим TNF (hTNF). Было установлено, что 90% максимальная индуцированная hTNF цитотоксичность имела место при концентрации TNF, равной 1000 пг/мл.
Все клетки L929 культивировали в среде RPMI 1640, содержащей феноловый красный, в среде с L-глутамином с добавлением эмбриональной телячьей сыворотки (10% об./об.). Нейтрализующую активность связывающих TNF соединений оценивали в среде RPMI 1640 без фенолового красного и с 5% эмбриональной телячьей сывороткой. К клеткам L929 добавляли связывающие TNF соединения в различных концентрациях (0-374 нг/мл) в присутствии 1000 пг/мл hTNF для определения концентрации, при которой антагонистическое действие первых достигает половины от максимального ингибирования (ЕС50%). Строили кривую концентрация-эффект с помощью нелинейной сигмоидальной регрессии с различной крутизной и рассчитывали значение ЕС50.
Оптимизированные мутантные варианты
Антитела по настоящему изобретению можно дополнительно оптимизировать в отношении улучшенных функциональных свойств, например, повышенной растворимости и/или стабильности.
В некоторых вариантах осуществления антитела по изобретению оптимизируют согласно методологии «функционального консенсуса», описанной в публикации заявки РСТ № РСТ/ЕР2008/001958 под названием «Sequence Based Engineering and Optimization of Single Chain Antibodies», поданной 12 марта 2008, которая включена в данный документ для сведения.
Например, иммуносвязывающие TNF соединения по изобретению можно сравнить с базой данных функционально выбранных scFv для идентификации аминокислотных положений, которые являются более или менее толерантными по вариабельности по сравнению с соответствующим положением(ями) в иммуносвязывающем VEGF соединении, указывая на то, что такое идентифицированное положение(я) может быть подходящим для конструирования повышенной функциональной способности, такой как стабильность и/или растворимость.
Примерные положения в каркасной области для замещения описаны в публикации заявки РСТ № РСТ/СН2008/000285 под названием «Methods of Modifying Antibodies and Modified Antibodies with Improved Functional Properties», поданной 25 июня 2008, и в публикации заявки РСТ № РСТ/СН2008/000284 под названием «Sequence Based Engineering and Optimization of Single Chain Antibodies», поданной 25 июня 2008. Например, можно ввести одну или более следующих замен в аминокислотное положение (система нумерация по AHo указана для каждого аминокислотного положения, приведенного ниже) в вариабельной области тяжелой цепи иммуносвязывающего соединения по изобретению:
(a) Q или E в аминокислотном положении 1;
(b) Q или E в аминокислотном положении 6;
(с) T, S или A в аминокислотном положении 7, более предпочтительно, Т или А, еще более предпочтительно, Т;
(d) A, T, P, V или D, более предпочтительно, Т, P, V или D в аминокислотном положении 10;
(e) L или V, более предпочтительно, L в аминокислотном положении 12;
(f) V, R, Q, M или K, более предпочтительно, V, R, Q или M в аминокислотном положении 13;
(g) R, M, E, Q или K, более предпочтительно, R, M, E или Q, еще более предпочтительно, R или E в аминокислотном положении 14;
(h) L или V, более предпочтительно, L в аминокислотном положении 19;
(i) R, T, K или N, более предпочтительно, R, T или N, еще более предпочтительно, N в аминокислотном положении 20;
(j) I, F, L или V, более предпочтительно, I, F или L, еще более предпочтительно, I или L в аминокислотном положении 21;
(k) R или K, более предпочтительно, K в аминокислотном положении 45;
(l) T, P, V, А или R, более предпочтительно, T, P, V или R, еще более предпочтительно, R в аминокислотном положении 47;
(m) K, Q, H или E, более предпочтительно, K, H или E, еще более предпочтительно, K в аминокислотном положении 50;
(n) M или I, более предпочтительно, I в аминокислотном положении 55;
(o) K или R, более предпочтительно, K в аминокислотном положении 77;
(p) A, V, L или I, более предпочтительно, A, L или I, еще более предпочтительно, А в аминокислотном положении 78;
(q) E, R, T или A, более предпочтительно, E, T или A, еще более предпочтительно, E в аминокислотном положении 82;
(r) T, S, I или L, более предпочтительно, T, S или L, еще более предпочтительно, T в аминокислотном положении 86;
(s) D, S, N или G, более предпочтительно, D, N или G, еще более предпочтительно, N в аминокислотном положении 87;
(t) A, V, L или F, более предпочтительно, A, V или F, еще более предпочтительно, V в аминокислотном положении 89;
(u) F, S, H, D или Y, более предпочтительно, F, S, H или D в аминокислотном положении 90;
(v) D, Q или E, более предпочтительно, D или Q, еще более предпочтительно, D в аминокислотном положении 92;
(w) G, N, T или S, более предпочтительно, G, N или T, еще более предпочтительно, G в аминокислотном положении 95;
(x) T, A, P, F или S, более предпочтительно, T, A, P или F, еще более предпочтительно, F в аминокислотном положении 98;
(y) R, Q, V, I, M, F или L, более предпочтительно, R, Q, I, M, F или L, еще более предпочтительно, Y, еще более предпочтительно, L в аминокислотном положении 103; и
(z) N, S или A, более предпочтительно, N или S, еще более предпочтительно, N в аминокислотном положении 107.
Дополнительно или альтернативно одну или более следующих замен можно ввести в вариабельную область легкой цепи иммуносвязывающего соединения по изобретению:
(aa) Q, D, L, E, S или I, более предпочтительно, L, E, S или I, еще более предпочтительно, L или E в аминокислотном положении 1;
(bb) S, A, Y, I, P или T, более предпочтительно, A, Y, I, P или T, еще более предпочтительно, P или T в аминокислотном положении 2;
(cc) Q, V, T или I, более предпочтительно, V, T или I, еще более предпочтительно, V или T в аминокислотном положении 3;
(dd) V, L, I или M, более предпочтительно, V или L в аминокислотном положении 4;
(ee) S, E или P, более предпочтительно, S или E, еще более предпочтительно, S в аминокислотном положении 7;
(ff) T или I, более предпочтительно, I в аминокислотном положении 10;
(gg) A или V, более предпочтительно, A в аминокислотном положении 11;
(hh) S или Y, более предпочтительно, Y в аминокислотном положении 12;
(ii) T, S или A, более предпочтительно, T или S, еще более предпочтительно, T в аминокислотном положении 14;
(jj) S или R, более предпочтительно, S в аминокислотном положении 18;
(kk) T или R, более предпочтительно, R в аминокислотном положении 20;
(ll) R или Q, более предпочтительно, Q в аминокислотном положении 24;
(mm) H или Q, более предпочтительно, H в аминокислотном положении 46;
(nn) K, R или I, более предпочтительно, R или I, еще более предпочтительно, R в аминокислотном положении 47;
(oo) R, Q, K, E, T или M, более предпочтительно, Q, K, E, T или M в аминокислотном положении 50;
(pp) K, T, S, N, Q или P, более предпочтительно, T, S, N, Q или P в аминокислотном положении 53;
(qq) I или M, более предпочтительно, М в аминокислотном положении 56;
(rr) H, S, F или Y, более предпочтительно, H, S или F в аминокислотном положении 57;
(ss) I, V или T, более предпочтительно, V или T, R, еще более предпочтительно, T в аминокислотном положении 74;
(tt) R, Q или K, более предпочтительно, R или Q, еще более предпочтительно, R в аминокислотном положении 82;
(uu) L или F, более предпочтительно, F в аминокислотном положении 91;
(vv) G, D, T или A, более предпочтительно, G, D или T, еще более предпочтительно, T в аминокислотном положении 92;
(xx) S или N, более предпочтительно, N в аминокислотном положении 94;
(yy) F, Y или S, более предпочтительно, Y или S, еще более предпочтительно, S в аминокислотном положении 101; и
(zz) D, F, H, E, L, A, T, V, S, G или I, более предпочтительно, H, E, L, A, T, V, S, G или I, еще более предпочтительно, A или V в аминокислотном положении 103.
В других вариантах осуществления иммуносвязывающие соединения по изобретению содержат одну или более мутаций, приводящих к повышению растворимости и/или стабильности, описанных в предварительной заявке на патент США № 61/075692 под названием «Solubility Optimization of Immunobinders», поданной 25 июня 2008 г. В некоторых предпочтительных вариантах осуществления иммуносвязывающие соединения содержат мутацию, повышающую растворимость, в аминокислотном положении, выбранном из группы аминокислотных положений тяжелой цепи, состоящей из 12, 103 и 144 (по нумерации AHo). В одном предпочтительном варианте осуществления иммуносвязывающее соединение содержит одну или более замен, выбранных из группы, состоящей из: (а) серина (S) в аминокислотном положении 12 тяжелой цепи; (b) серина (S) или треонина (Т) в аминокислотном положении 103 тяжелой цепи; и (с) серина (S) или треонина (Т) в аминокислотном положении 144 тяжелой цепи. В другом предпочтительном варианте осуществления иммуносвязывающее соединение содержит следующие замены: (а) серин (S) в аминокислотном положении 12 тяжелой цепи; (b) серин (S) или треонин (Т) в аминокислотном положении 103 тяжелой цепи; и (с) серин (S) или треонин (Т) в аминокислотном положении 144 тяжелой цепи.
Как уже указывалось выше, комбинации последовательностей VL и VH, в частности, имеющие такой же или по существу такой же набор последовательностей CDR, но различающиеся по последовательностям каркасных областей, например, за счет присутствия замен, указанных выше, можно переставить или объединить с использованием линкерной последовательности. Приведенные в качестве примера комбинации, не ограничиваясь этим, включают:




























В предпочтительном варианте осуществления последовательность имеет, по меньшей мере, 90% идентичность, более предпочтительно, по меньшей мере, 95% идентичность и, наиболее предпочтительно, 100% идентичность с любой из последовательностей SEQ ID No:94-121.
Применения анти-TNF-антител
Для терапевтических применений анти-TNF-антитела по изобретению вводят млекопитающему, предпочтительно человеку, в фармацевтически приемлемой лекарственной форме, такой как обсуждались выше, включая лекарственные формы, которые можно вводить человеку внутривенно в виде болюса или продолжительной инфузией в течение определенного периода времени, а также внутримышечным, внутрибрюшинным, интрацереброспинальным, подкожным, внутриартикулярным, интрасиновиальным, интратекальным, пероральным, местным или ингаляционным путями. Также антитела соответственно вводят интратуморально, перитуморально, в очаг поражения или около очага поражения, для проявления местных, а также системных терапевтических эффектов.
Для профилактики или лечения заболевания соответствующая дозировка антитела будет зависеть от типа заболевания, которое подвергается лечению, как определено выше, тяжести и характера течения заболевания, цели введения антитела: для профилактики или лечения, предшествующей терапии, истории болезни пациента и его «ответа» на введение антитела, а также мнения лечащего врача. Антитело соответственно вводят пациенту однократно или многократно.
Анти-TNF-антитела являются пригодными для лечения TNF-опосредованных заболеваний. В зависимости от типа и тяжести заболевания доза антитела в пределах от 1 мкг/кг до 50 мг/кг (например, 0,1-20 мг/кг) является начальной возможной дозой для введения пациенту, например, однократно или многократно, или с помощью продолжительной инфузии. Типичная суточная или недельная доза может находиться в пределах примерно от 1 мкг/кг до примерно 20 мг/кг или выше в зависимости от факторов, упомянутых выше. Для повторных введений в течение нескольких суток или более, в зависимости от состояния пациента, лечение повторяют до достижения желаемого купирования симптомов заболевания. Однако можно использовать другие схемы введения. Эффективность данной терапии легко проследить с использованием обычных методов и тестов, включающих, например, радиографическое исследование опухолей.
Согласно другому варианту осуществления изобретения эффективность антитела для профилактики или лечения заболевания можно повысить введением антитела курсами или в комбинации с другим лекарственным препаратом, который является эффективным для данных целей, например, таким как васкулярный эндотелиальный ростовой фактор (VEGF), антитело, способное ингибировать или нейтрализовать ангиогенную активность кислого или основного фибробластного ростового фактора (FGF), или ростовой фактор гепатоцитов (HGF), антитело, способное ингибировать или нейтрализовать коагулянтную активность тканевого фактора, протеин С или протеин S (смотри Esmon et al., публикация заявки РСТ № WO 91/01753, опубликованная 21 февраля 1991 г.), антитело, способное связываться с рецептором HER2 (смотри Hudziak et al., публикация заявки РСТ № WO 89/06692, опубликованная 27 июля 1989 г.), или одним или более широко применяемыми лекарственными средствами, например, такими как алкилирующие агенты, антагонисты фолиевой кислоты, антиметаболиты обмена нуклеиновых кислот, антибиотики, аналоги пиримидинов, 5-фторурацил, цисплатин, пуриновые нуклеозиды, амины, аминокислоты, триазоловые нуклеозиды или кортикостероиды. Подобные другие средства могут находиться в одной композиции, предназначенной для введения, или их можно вводить по отдельности. Также антитело подходит для введения курсами или в комбинации с лучевой терапией, включающей облучение или введение радиоактивных веществ.
Антитела по изобретению можно использовать в качестве агентов для аффинной хроматографии. В данном способе антитела иммобилизуют на твердой фазе, такой как смола Сефадекс или фильтровальная бумага, с использованием методов, хорошо известных в данной области. Иммобилизованное антитело контактирует с пробой, содержащей белок TNF (или его фрагмент), предназначенной для очистки, и затем подложку промывают подходящим растворителем, который будет удалять по существу весь материал из пробы за исключением белка TNF, который связывается с иммобилизованным антителом. Наконец, подложку промывают другим подходящим растворителем, таким как глициновый буфер, рН 5,0, который будет высвобождать белок TNF от антитела.
Также анти-TNF-антитела могут быть пригодными для диагностических тестов на обнаружение белка TNF, например, детектирования его экспрессии в определенных клетках, тканях или сыворотке крови. Такие диагностические тесты можно применять для диагностики рака.
Для диагностических применений антитело, как правило, метят детектируемой меткой. Имеются многочисленные метки, которые можно подразделить на следующие группы:
(a) радиоизотопы, такие как 111In, 99Tc, 14C, 131I, 125I, 3H, 32P или 35S. Антитело можно метить радиоактивным изотопом с использованием методов, например, описанных в «Current protocols in Immunology», Volumes 1 and 2, Colligen et al., Ed. Wiley-Interscience, New York, N.Y., Pubs. (1991), и радиоактивность можно определить с использованием сцинтилляционного счетчика;
(b) флуоресцентные метки, такие как хелаты редких щелочноземельных металлов (хелаты европия), или флуоресцеин и его производные, родамин и его производные, дансил, лиссамин, фикоэритрин и техасский красный. Флуоресцентные метки можно конъюгировать с антителом с использованием методов, раскрытых, например, в «Current protocols in Immunology», смотри выше. Флуоресценцию можно количественно определить с использованием флуориметра;
(с) различные метки фермент-субстрат, и в патенте США № 4275149 приводится обзор некоторых из них. Как правило, фермент катализирует химическое превращение хромогенного субстрата, которое можно детектировать с использованием различных методов. Например, фермент может катализировать изменение цвета субстрата, которое определяют спектрофотометрически. Альтернативно фермент может изменить флуоресценцию или хемилюминесценцию субстрата. Методы количественного определения изменения флуоресценции описаны выше. Хемилюминесцентный субстрат становится электронно-возбужденным в результате химической реакции и затем может испускать свет, который можно детектировать (например, с использованием хемилюминометра), или отдавать энергию на флуоресцентный акцептор. Примеры ферментативных меток включают люциферазу (например, люциферазу светлячков и бактериальную люциферазу; патент США № 4737456), люциферин, 2,3-дигидрофталазиндионы, малатдегидрогеназу, уреазу, пероксидазу, такую как пероксидаза хрена (HRPO), щелочную фосфатазу, бета-галактозидазу, глюкоамилазу, лисозим, оксидазы сахаридов (например, глюкозоксидаза, галактозоксидаза и глюкоза-6-фосфатдегидрогеназа), гетероциклические оксидазы (такие как уриказа и ксантиноксидаза), лактопероксидазу, микропероксидазу и тому подобное. Методы конъюгирования ферментов с антителами описаны O’Sullivan et al., «Methods for Preparation of Enzyme-Antibody Conjugates for use in Enzyme Immunoassay», в «Methods in Enzym.» (ed. J. Langone & H. Van Vunakis), Academic Press, New York, 73:147-166 (1981). Примеры комбинаций фермент-субстрат включают, например:
(i) пероксидазу хрена (HRPO) с перекисью водорода в качестве субстрата, где перекись водорода окисляет предшественник красителя (например, ортофенилендиамин (OPD) или 3,3’,5,5’-тетраметилбензидин гидрохлорид (TMB));
(ii) щелочную фосфатазу (АР) с пара-нитрофенилфосфатом в качестве хромогенного субстрата; и
(iii) бета-D-галактозидазу (бета-D-Gal) с хромогенным субстратом (например, Р-нитрофенил-бета-D-галактозидазу) или флуорогенным субстратом (например, 4-метилумбеллиферил-бета-D-галактозидаза).
Специалистам в данной области известны многочисленные другие комбинации фермент-субстрат. Общий обзор по ним смотри в патентах США №№ 4275149 и 4318980. В некоторых случаях метку непосредственно конъюгируют с антителом. Специалистам в данной области знакомы различные методы достижения этой цели. Например, антитело можно конъюгировать с биотином или любую метку из трех больших групп, упомянутых выше, можно конъюгировать с авидином или тому подобное. Биотин избирательно связывается с авидином и, таким образом, метку можно конъюгировать с антителом данным опосредованным методом. Альтернативно для проведения опосредованного конъюгирования метки с антителом его конъюгируют с гаптеном с небольшой молекулой (например, дигоксином) и одну из различных типов меток, упомянутых выше, конъюгируют с антителом к гаптену (например, антителом к дигоксину). Таким образом, можно провести опосредованное конъюгирование метки с антителом.
В другом варианте осуществления изобретения не требуется вводить метку в анти-TNF-антитело, и его присутствие можно детектировать с использованием меченого антитела, которое связывается с антителом к TNF.
Антитела по настоящему изобретению можно использовать в любом известном в данной области методе, таком как конкурентное связывание, прямые или опосредованные сэндвич-методы и тесты, основанные на иммунопреципитации. Zola, Monoclonal Antibodies: A Manual of Techniques, pp. 147-158 (CRC Press, Inc. 1987).
Тесты конкурентного связывания основаны на способности меченого стандарта конкурировать с анализируемым веществом в тестируемой пробе за связывание с ограниченным количеством антитела. Количество белка TNF в тестируемой пробе обратно пропорционально количеству стандарта, который связывается с антителами. Для облегчения определения количества стандарта, который становится связанным, обычно антитела не солюбилизируют до и после конкуренции, таким образом, что стандарт и анализируемое соединение, которые связаны с антителами, можно соответственно отделить от стандарта и анализируемого соединения, которые остаются несвязанными.
Сэндвич-методы включают применение двух антител, каждое из которых способно связываться с различным иммуногенным фрагментом, или эпитопом, белка, который детектируется. В сэндвич-методе анализируемое соединение в тестируемой пробе связывается с первым антителом, которое иммобилизовано на твердой подложке, и затем второе антитело связывается с анализируемым веществом, образуя при этом нерастворимый трехкомпонентный комплекс. Смотри, например, патент США № 4376110. Второе антитело само по себе может включать детектируемую метку (прямые сэндвич-методы), или его можно анализировать с использованием антитела к иммуноглобулинам, которое мечено детектируемой меткой (опосредованные сэндвич-методы). Например, одним типом сэндвич-метода является ELISA, где в данном случае детектируемая метка представляет фермент.
Для проведения иммуногистохимии образец опухоли может быть свежеотобранным или замороженным, или его можно залить в парафин и зафиксировать в консерванте, например, таком как формалин.
Также антитела можно использовать для диагностических тестов в условиях in vivo. Обычно антитело метят радионуклидом (например, 111In, 99Tc, 14C, 131I, 125I, 3H, 32P или 35S) таким образом, что становится возможным определить локализацию опухоли с использованием иммуносцинтиографии.
Антитело по настоящему изобретению можно обеспечить в наборе, упакованной комбинации реагентов в заранее определенных количествах, с инструкциями по постановке диагностического теста. В том случае, когда антитело мечено ферментом, то набор будет включать субстраты и кофакторы, необходимые для фермента (например, предшественник-субстрат, который обеспечивает детектируемый хромофор или флуорофор). В дополнение можно включить другие добавки, такие как стабилизаторы, буферы (например, блокирующий буфер или лизирующий буфер) и тому подобное. Относительные количества различных реагентов могут варьировать в широких пределах для обеспечения концентраций реагентов в растворе, которые оптимизируют чувствительность теста. В частности, реагенты могут находиться в виде сухих порошков, обычно лиофилизованных, включая эксципиенты, которые при растворении будут обеспечивать раствор реагента с соответствующей концентрацией.
Фармацевтические препараты
В одном аспекте изобретение относится к фармацевтическим композициям, содержащим анти-TNF-антитела для лечения опосредованных TNF заболеваний. Термин «фармацевтическая композиция» относится к препаратам, которые находятся в такой форме, которая надежно обеспечивает высокую биологическую активность антитела или производного антитела, и которая не содержит дополнительных компонентов, которые являются токсичными для субъектов, которым вводят композицию. «Фармацевтически приемлемые» эксципиенты (носители, добавки) представляют вещества, которые разумно вводить субъекту-млекопитающему для обеспечения эффективной дозы используемого активного ингредиента.
«Стабильная композиция» представляет композицию, в которой антитело или производное антитело в основном сохраняет его физическую стабильность и/или химическую стабильность, и/или биологическую стабильность при хранении. В данной области имеются различные аналитические методы определения стабильности белка, и их обзор представлен, например, в «Peptide and Protein Drug Delivery», 247-301, Vincent Lee Ed., Marcel Dekker, Inc., New York, N.Y., Pubs., 1991 и Jones A. Adv. Drug Delivery Rev., 10:29-90, 1993. Стабильность можно определить при выбранной температуре в течение выбранного периода времени. Предпочтительно, композиция является стабильной при комнатной температуре (примерно при 30°С) или при 40°С, по меньшей мере, в течение 1 месяца и/или является стабильной примерно при 2-8°С, по меньшей мере, в течение 1 года или, по меньшей мере, в течение 2 лет. Кроме того, композиция предпочтительно является стабильной после ее замораживания (например, до -70°С) и оттаивания.
Антитело или производное антитела «сохраняет его физическую стабильность» в фармацевтической композиции, если не демонстрирует признаков агрегации, преципитации и/или денатурации при визуальном исследовании цвета и/или прозрачности, или по данным рассеивания УФ-света или гель-хроматографии.
Антитело или производное антитела «сохраняет его химическую стабильность» в фармацевтической композиции, если химическая стабильность в данный период времени является таковой, что белок по-прежнему сохраняет свою биологическую активность, как определено ниже. Химическую стабильность можно оценить детектированием или количественным определением химически измененных форм белка. Химическое изменение может включать модификацию размера (например, укорочение), что можно оценить, например, с использованием гель-хроматографии, электрофореза в SDS-PAGE и/или матрично-активированной лазерной десорбции/иониизации/времяпролетной масс-спектрометрии (MALDI/TOF MS). Другие типы химического изменения включают изменение заряда (например, в результате деамидирования), которое можно обнаружить, например, ионообменной хроматографией.
Антитело или производное антитела «сохраняет его биологическую стабильность» в фармацевтической композиции, если биологическая активность антитела в данный период времени не отличается более чем на 10% (в пределах ошибки метода) от его биологической активности на время приготовления фармацевтической композиции, например, по данным теста связывания антигена. Другие тесты оценки «биологической активности» антител приведены в данном документе ниже.
Под термином «изотоническая» понимается, что интересующая композиция имеет по существу одинаковое с кровью человека осмотическое давление. Как правило, изотонические композиции будут иметь осмотическое давление в пределах примерно от 250 до 350 мосм. Изотоничность можно определить, например, с использованием осмометра давления пара или осмометра-криоскопа.
«Полиол» представляет собой соединение с многочисленными гидроксильными группами, и оно включает сахара (редуцирующие и нередуцирующие сахара), сахарные спирты и сахарные кислоты. Предпочтительные полиолы в данном документе имеют молекулярную массу, которая составляет менее чем примерно 600 кДа (например, в пределах примерно от 120 до 400 кДа). «Редуцирующий сахар» представляет сахар, содержащий гемиацетальную группу, которая может восстанавливать ионы металлов или ковалентно взаимодействовать с лизином или другими аминогруппами в белках, в то время как «нередуцирующий сахар» является сахаром, который не обладает подобными свойствами. Примерами редуцирующих сахаров являются фруктоза, манноза, мальтоза, лактоза, арабиноза, ксилоза, рибоза, рамноза, галактоза и глюкоза. Нередуцирующие сахара включают сахарозу, трегалозу, сорбозу, мелезитозу и раффинозу. Маннит, ксилит, эритрит, треитол, сорбит и глицерин представляют примеры сахарных спиртов сахаров. В отношении сахарных кислот, то эти соединения включают L-глюконат и его соли металлов. В тех случаях, когда желательно, чтобы композиция оставалась стабильной при замораживании-оттаивании, то полиол предпочтительно представляет полиол, который не кристаллизуется при температуре замораживания (например, -20°С), что иначе приводит к дестабилизации антитела в композиции. Нередуцирующие сахара, такие как сахароза и трегалоза, представляют собой предпочтительные полиолы в данном документе, при этом трегалоза является более предпочтительной по сравнению с сахарозой за счет более высокой стабильности растворов трегалозы.
В том смысле, в котором термин «буфер» используется в данном документе, он относится к забуференному раствору, который выдерживает изменения рН под действием его кислых-основных компонентов. Буфер по данному изобретению имеет рН в пределах примерно от 4,5 до примерно 6,0; предпочтительно, примерно от 4,8 до примерно 5,5; и, наиболее предпочтительно, имеет рН примерно 5,0. Примеры буферов, которые контролируют рН в данных пределах, включают ацетатный (например, ацетат натрия), сукцинатный (например, сукцинат натрия), глюконатный, гистидиновый, цитратный и другие органические кислые буферы. В тех случаях, когда желательно, чтобы композиция была стабильной при замораживании-оттаивании, то предпочтительно, чтобы буфер не был фосфатным.
С точки зрения фармакологии в контексте настоящего изобретения «терапевтически эффективное количество» антитела или производного антитела относится к количеству, эффективному для профилактики или лечения нарушения, которое подвергается лечению, против которого антитело или производное антитела является эффективным. Термин «заболевание/нарушение» представляет любое состояние, на которое будет оказывать положительное влияние антитело или производное антитела. Оно включает хронические и острые нарушения или заболевания, в том числе, патологические состояния, которые предрасполагают млекопитающего к развитию данного заболевания.
«Консервант» представляет собой соединение, которое можно включить в композицию для значительного снижения действия бактерий в ней, облегчая тем самым, например, получение композиции многоразового использования. Примеры потенциальных консервантов включают октадецилдиметилбензиламмония хлорид, гексаметония хорид, бензалкония хлорид (смесь алкилбензилдиметиламмония хлоридов, в которых алкильные группы представляют собой длинноцепочечные соединения) и бензетония хлорид. Другие типы консервантов включают ароматические спирты, такие как фенол, бутиловый и бензиловый спирт, алкилпарабены, такие как метил- или пропилпарабен, катехол, резорцин, циклогексанол, 3-пентанол и м-крезол. Наиболее предпочтительным консервантом в данном изобретении является бензиловый спирт.
Также настоящее изобретение относится к фармацевтическим композициям, содержащим одно или более антител или производных антител, вместе, по меньшей мере, с одним физиологически приемлемым носителем или эксципиентом. Фармацевтические композиции могут содержать, например, одно или более веществ, выбранных из воды, буферов (например, нейтрального забуференного физиологического раствора или забуференного фосфатом физиологического раствора), этанола, минерального масла, растительного масла, диметилсульфоксида, углеводов (например, глюкозы, маннозы, сахарозы или декстранов), маннита, белков, адъювантов, полипептидов или аминокислот, таких как глицин, антиоксидантов, комплексообразующих соединений, таких как ЭДТА или глютатион, и/или консервантов. Как уже указывалось выше, в фармацевтические композиции, описанные в данном документе, можно включить другие активные ингредиенты (но необязательно).
Носитель представляет собой соединение, которое может быть связано с антителом или производным антитела перед введением пациенту, часто в целях контроля стабильности или биодоступности соединения. Обычно носители для применения в таких композициях являются биосовместимыми и также могут быть биодеградируемыми. Носители включают, например, моновалентные или поливалентные молекулы, такие как сывороточный альбумин (например, человеческий или бычий), яичный альбумин, пептиды, полилизин и полисахариды, такие как аминодекстран и полиамидоамины. Также носители включают твердые вещества для основы, такой как шарики и микрочастицы, например, из полилактата-полигликолята, поли(лактид-со-гликолида), полиакрилата, латекса, крахмала, целлюлозы или декстрана. Носитель может быть связан с соединениями различными путями, включая ковалентное связывание (прямое или через линкер), нековалентное взаимодействие или смешивание.
Фармацевтические композиции можно готовить в форме для любого подходящего пути введения, включая, например, местное, пероральное, интраназальное, ректальное или парентеральное введение. В некоторых вариантах осуществления предпочтительными являются композиции, находящиеся в лекарственной форме, подходящей для перорального применения. Такие формы включают, например, пилюли, таблетки, пастилки, сосательные таблетки, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсию, твердые или мягкие капсулы, сиропы или эликсиры. В других вариантах осуществления композиции, описанные в данном документе, можно формулировать в виде лиофилизата. В том смысле, в котором в данном документе используется термин «парентеральный», он включает подкожное, внутрикожное, внутрисосудистое (например, внутривенное), внутримышечное, интраспинальное, интракраниальное, интратекальное и внутрибрюшинное инъекционное введение, а также любой другой метод инъекционного или инфузионного введения.
Композиции, предназначенные для перорального введения, можно приготовить с использованием любого метода, известного в данной области для получения фармацевтических композиций, и они могут содержать один или более агентов, таких как подсластители, вкусовые вещества, краситель и консерванты, для обеспечения привлекательных внешне и приятных на вкус препаратов. Таблетки содержат активный ингредиент в смеси с физиологически приемлемыми эксципиентами, которые являются подходящими для производства таблеток. Такие эксципиенты включают, например, инертные разбавители (например, карбонат кальция, карбонат натрия, лактозу, фосфат кальция или фосфат натрия), средства для грануляции и разрыхления (например, кукурузный крахмал или альгиновую кислоту), связующие вещества (например, крахмал, желатин или аравийскую камедь) и скользящие вещества (например, стеарат магния, стеариновую кислоту или тальк). Таблетки могут быть без оболочки или их можно покрыть оболочками с использованием известных методов, в целях замедления разрыхления и всасывания в желудочно-кишечном тракте и, тем самым, обеспечения замедленного действия в течение более длительного периода времени. Например, можно использовать вещества, задерживающие всасывание во времени, такие как глицерилмоностеарат или глицерилдистеарат.
Также композиции для перорального введения могут находиться в виде твердых желатиновых капсул, в которых активный ингредиент смешан с инертным твердым разбавителем (например, карбонатом кальция, фосфатом кальция или каолином) или в виде мягких желатиновых капсул, в которых активный ингредиент находится в смеси с водой или масляной средой (например, арахисовым маслом, жидким парафином или оливковым маслом). Водные суспензии содержат антитело или производное антитела в смеси с эксципиентами, подходящими для получения водных суспензий. Такие эксципиенты включают суспендирующие вещества (например, натриевую соль карбоксиметилцеллюлозы, метилцеллюлозу, гидроксипропилметилцеллюлозу, альгинат натрия, поливинилпирролидон, трагакантовую камедь и аравийскую камедь); и диспергирующие или смачивающие вещества (например, природные фосфатиды, такие как лецитин, продукты конденсации алкиленоксида с жирными кислотами, такие как полиоксиэтиленстеарат, продукты конденсации этиленоксида с длинноцепочечными алифатическими спиртами, такие как гептадекаэтиленоксицетанол, продукты конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и гекситола, такие как полиоксиэтиленсорбит моноолеат, или продукты конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и ангидридов гекситола, такие как полиоксиэтиленсорбитан моноолеат). Водные суспензии также могут содержать один или более консервантов, например, этил- или н-пропил-п-гидроксибензоат, один или более красителей, одно или более вкусовых веществ, и один или более подсластителей, таких сахароза или сахарин. Сиропы и эликсиры можно готовить с подсластителями, такими как глицерин, пропиленгликоль, сорбит или сахараза. Такие композиции также могут содержать одно или более успокаивающих веществ, консервантов, вкусовых веществ и/или красителей.
Масляные суспензии можно готовить суспендированием активных ингредиентов в растительном масле (например, арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле) или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, такой как пчелиный воск, твердый парафин или цетиловый спирт. Можно добавить подсластители, такие как были приведены выше, и/или вкусовые вещества для обеспечения приятных на вкус препаратов для приема внутрь. Такие суспензии можно консервировать при добавлении антиоксиданта, такого как аскорбиновая кислота.
Диспергируемые порошки и гранулы, подходящие для получения водной суспензии при добавлении воды, обеспечивают активный ингредиент в смеси с диспергируемым или смачивающим веществом, суспендирующим веществом и одним или более консервантами. Примерами подходящих диспергирущих или смачивающих веществ и суспендирующих веществ являются агенты, уже приведенные в качестве примера выше. Могут также присутствовать дополнительные эксципиенты, например, подсластители, вкусовые вещества и красители.
Фармацевтические композиции также могут находиться в виде эмульсий масло-в-воде. Масляная фаза может представлять собой растительное масло (например, оливковое масло или арахисовое масло), минеральное масло (жидкий парафин) или их смеси. Подходящие эмульгаторы включают природные камеди (например, аравийскую камедь или траганкантовую камедь), природные фосфатиды (например, соевые бобы, лецитин и сложные эфиры или неполные сложные эфиры жирных кислот и гекситола), ангидриды (например, сорбитан моноолеат) и продукты конденсации неполных эфиров, полученных из жирных кислот и гекситола, с этиленоксидом (например, полиоксиэтиленсорбитан моноолеат). Эмульсия также может содержать один или более подсластителей и/или вкусовых веществ.
Фармацевтическую композицию можно приготовить в виде стерильной водной или масляной суспензии для инъекций, в которой модулятор, в зависимости от используемого носителя и концентрации, суспендирован или растворен в носителе. Такую композицию можно формулировать, следуя методам, известным в данной области, с использованием диспергирующих, смачивающих и/или суспендирующих веществ, приведенных выше. Среди приемлемых носителей и растворителей, которые можно использовать, находится вода, 1,3-бутандиол, раствор Рингера и изотонический раствор хлорида натрия. В дополнение: в качестве растворителя или суспендирующей среды можно использовать стерильные жирные масла. Для данной цели можно использовать любое мягкое жирное масло, включая синтетические моно- и диглицериды. Кроме того, при приготовлении инъекционных композиций можно использовать жирные кислоты, такие как олеиновая кислота, и адъюванты, такие как местные анестетики, консерванты и/или буферы, которые можно растворить в носителе.
Фармацевтические композиции можно готовить в виде композиций с замедленным высвобождением (например, такой композиции, как капсула, которая обеспечивает медленное высвобождение модулятора после введения). Обычно такие композиции можно приготовить с использованием хорошо известной технологии и вводить, например, с помощью пероральной, ректальной или подкожной имплантации или имплантации в желаемом месте-мишени. Носители, которые применяются в таких композициях, являются биосовместимыми и также они могут быть биодеградируемыми; предпочтительно, композиция обеспечивает относительно постоянную скорость высвобождения модулятора. Количество антитела или производного антитела, содержащееся в композиции с замедленным высвобождением, зависит, например, от места имплантации, скорости и предполагаемой продолжительности высвобождения, а также природы заболевания/нарушения, которое подвергается лечению или профилактике.
Антитело или производные антитела, описанные в данном документе, обычно вводят в количестве, обеспечивающем определенную концентрацию в жидкости организма (например, крови, плазме крови, сыворотке крови, спинномозговой жидкости, синовиальной жидкости, лимфе, целлюлярной интерстициальной жидкости, слезах или моче), которая является достаточной для детектируемого связывания с TNF и профилактики или купирования TNF-опосредованных заболеваний/нарушений. Доза считается эффективной, если она оказывает заметное лечебное действие для пациента, как описано в данном документе. Предпочтительные дозы для системного введения находятся в пределах примерно от 0,1 мг до примерно 140 мг на кг массы тела в сутки (примерно от 0,5 мг до примерно 7 г на пациента в сутки) при том, что обычно дозы для приема внутрь примерно в 5-20 раз выше по сравнению с дозами, которые используются для внутривенного введения. Количество антитела или производного антитела, которое можно объединить с носителями для получения единичной лекарственной формы, будет варьировать в зависимости от хозяина, который подвергается лечению, и конкретного пути введения. Как правило, единичные лекарственные формы содержат примерно от 1 мг до примерно 500 мг активного ингредиента.
Фармацевтические композиции можно упаковать для лечения состояний, «отвечающих» на антитело или производное антитела к TNF. Упакованные фармацевтические композиции могут включать контейнер, содержащий эффективное количество, по меньшей мере, одного антитела или производного антитела, описанного в данном документе, и инструкции (например, на этикетке), указывающие, что содержащаяся композиция предназначена для применения в лечении заболевания/нарушения, «отвечающего» на антитело или производное антитела после введения пациенту.
Антитела или производные антител по настоящему изобретению также можно химически модифицировать. Предпочтительными модифицирующими группами являются полимеры, например, необязательно замещенные полиалкен, полиалкинилен или полиоксиалкилен с прямой или разветвленной цепью или разветвленные или неразветвленные полисахариды. Такая эффекторная группа может повысить период полураспада антитела в условиях in vivo. Конкретные примеры синтетических полимеров включают необязательно замещенные поли(этиленгликоль) (ПЭГ), поли(пропиленгликоль), поли(виниловый спирт) с прямой или разветвленной цепью или их производные. Конкретные природные полимеры включают лактозу, амилозу, декстран, гликоген или их производные. Размер полимера может варьировать, как это желательно, но обычно средняя молекулярная масса находится в пределах примерно от 500 Да до 50000 Да. Для местного применения, когда антитело предназначено для проникновения в ткани, предпочтительная молекулярная масса полимера составляет примерно 5000 Да. Молекулу полимера можно присоединить к антителу, в частности, к С-концу Fab-фрагмента тяжелой цепи через ковалентно связанный шарнирный пептид, как описано в международной заявке WO0194585. В отношении присоединения ПЭГа можно обратиться к следующим источникам «Poly(ethylenglycol) Chemistry, Biotechnological and Biomedical Applications», 1992, J. Milton Harris (ed), Plenum Press, New York и «Bioconjugation Protein Coupling Techniques for the Biomedical Sciences», 1998, M. Aslam и A. Dent, Grove Publishers, New York.
После получения интересующего антитела и производного антитела, как описано выше, готовят фармацевтическую композицию, содержащую его. Антитело, предназначенное для использования в композиции, не подвергают предварительной лиофилизации, и интересующая композиция представляет водную композицию. Предпочтительно, антитело или производное антитела в композиции представляет фрагмент антитела, такой как scFv. Терапевтически эффективное количество антитела, находящееся в композиции, определяют, например, с учетом желаемых объемов и способа(в) введения. Приводимые в качестве примера концентрации антитела в композиции находятся в пределах от 0,1 мг/мл до примерно 50 мг/мл, предпочтительно, примерно от 0,5 мг/мл до примерно 25 мг/мл и наиболее предпочтительно, примерно от 2 мг/мл до примерно 10 мг/мл.
Готовят водную композицию, содержащую антитело или производное антитела в растворе с забуференным рН. Буфер по данному изобретению имеет значение рН в пределах примерно от 4,5 до примерно 6,0, предпочтительно, примерно от 4,8 до примерно 5,5 и, наиболее предпочтительно, имеет рН, равный примерно 5,0. Примеры буферов, которые контролируют рН в данных пределах, включают ацетатный (например, ацетат натрия), сукцинатный (например, сукцинат натрия), глюконатный, гистидиновый, цитратный и другие органические кислые буферы. Концентрация буфера может оставлять примерно от 1 мМ до примерно 50 мМ, предпочтительно, примерно от 5 мМ до примерно 30 мМ в зависимости, например, от конкретного буфера и желаемой изотоничности композиции. Предпочтительным буфером является ацетатный натриевый (примерно 10 мМ) буфер, рН 5,0.
Полиол, который является повышающим тоничность соединением, и может стабилизировать антитело, включается в состав композиции. В предпочтительных вариантах осуществления композиции не содержат повышающего тоничность количества соли, такой как хлорид натрия, поскольку это может вызвать осаждение антитела или производного антитела и/или может привести к окислению при низком значении рН. В предпочтительных вариантах осуществления полиол представляет нередуцирующий сахар, такой как сахароза или трегалоза. Полиол добавляют в композицию в количестве, которое может варьировать в зависимости от желаемой изотоничности композиции. Предпочтительно, водная композиция является изотоничной, в этом случае подходящие концентрации полиолов в композиции в пределах примерно от 1% до примерно 15% мас./об., предпочтительно, в пределах примерно от 2% до примерно 10% мас./об. Однако также могут быть подходящими гипертонические или гипотонические композиции. Количество добавляемого в композицию полиола также может меняться в зависимости от молекулярной массы полиола. Например, можно внести меньшее количество моносахарида (например, маннита) по сравнению с дисахаридом (таким как трегалоза).
В композицию антитела или производного антитела также добавляют поверхностно-активное вещество. Приведенные в качестве примера поверхностно-активные вещества включают неионогенные поверхностно-активные вещества, такие как полисорбаты (например, полисорбаты 20, 80 и т.д.) или полоксамеры (например, полоксамер 188). Количество добавляемого поверхностно-активного вещества представляет такое количество, которое приводит к снижению агрегации формулированного антитела/производного антитела и/или сводит до минимума образование частиц в композиции, и/или снижает адсорбцию. Например, поверхностно-активное вещество может находиться в композиции в количестве примерно от 0,001% до примерно 0,5%, предпочтительно, примерно от 0,005% до примерно 0,2% и наиболее предпочтительно, примерно от 0,01% до примерно 0,1%.
В одном варианте осуществления композиция содержит указанные выше вещества (т.е. антитело или производное антитела, буфер, полиол и поверхностно-активное вещество) и по существу не содержит одного или более консервантов, таких как бензиловый спирт, фенол, крезол, хлорбутанол и бензетоний Cl. В другом варианте осуществления в композицию можно включить консервант, в частности, когда композиция является мультидозовой композицией. Концентрация консерванта может находиться в пределах примерно от 0,1% до примерно 2%, наиболее предпочтительно, примерно от 0,5% до примерно 1%. В состав композиции можно включить один или более других фармацевтически приемлемых носителей, эксципиентов или стабилизаторов, описанных в Remington’s Pharmaceutical Sciences 21st edition, Osol, A. Ed., 2006), при условии, что они не оказывают отрицательного влияния на желаемые характеристики композиции. Приемлемые носители, эксципиенты или стабилизаторы являются нетоксичными для реципиентов в используемых дозах и концентрациях, и они включают: дополнительные буферы; сорастворители; антиоксиданты, в том числе, аскорбиновую кислоту и метионин; комплексообразующие вещества, такие как ЭДТА; комплексы металлов (например, комплексы Zn-протеин); биодеградируемые полимеры, такие как полиэфиры; и/или солеобразующие противоионы, такие как натрий.
Композиции, предназначенные для введения в условиях in vivo, должны быть стерильными. Это можно легко осуществить фильтрованием через стерильные мембранные фильтры до или после приготовления композиции.
Композицию вводят млекопитающему, нуждающемуся в лечении антителом, предпочтительно человеку, с использованием известных способов, таких как внутривенное введение в виде болюса или продолжительной инфузии в течение определенного периода времени, внутримышечным, внутрибрюшинным, интрацереброспинальным, подкожным, интраартикулярным, интрасиновиальным, интратекальным, пероральным, местным или ингаляционным путями. В предпочтительных вариантах осуществления композицию вводят млекопитающему внутривенным путем. Для таких целей композицию можно вводить, например, с использованием шприца или системы для внутривенных инъекций.
Соответствующая доза («терапевтически эффективное количество») антитела будет зависеть, например, от заболевания, которое подвергается лечению, тяжести и характера течения заболевания, от цели введения антитела – профилактической или терапевтической, предшествующей терапии, истории болезни пациента и «ответа» на лечение антителом, типа используемого антитела и мнения лечащего врача. Антитело или производное антитела соответственно вводят пациенту однократно или многократно, и его можно вводить пациенту в любое время с момента постановки диагноза. Антитело или производное антитела можно вводить в виде самостоятельного средства лечения или в комбинации с другими лекарственными препаратами, пригодными для лечения данного заболевания.
В качестве общего предложения: терапевтически эффективное количество антитела или производного антитела для введения находится в пределах примерно от 0,1 до примерно 50 мг/кг массы тела пациента однократно или многократно, с типичными пределами используемого антитела примерно от 0,3 до примерно 20 мг/кг, более предпочтительно, примерно от 0,3 до примерно 15 мг/кг ежедневно. Эффективность данной терапии легко проследить с использованием обычных методов.
Промышленные изделия
В другом варианте осуществления изобретения обеспечивается промышленное изделие, содержащее контейнер, в котором находится фармацевтическая композиция по настоящему изобретению, предпочтительно, водная фармацевтическая композиция, и необязательно обеспечиваются инструкции по ее применению. Подходящие контейнеры включают, например, бутыли, флаконы и шприцы. Контейнер может быть изготовлен из различных материалов, таких как стекло или пластик. Приведенный в качестве примера контейнер представляет собой отдельный стеклянный флакон емкостью 3-20 см3. Альтернативно для мультидозовой композиции контейнер может представлять собой отдельный стеклянный флакон емкостью 3-100 см3. Контейнер содержит композицию и этикетку на нем или связанную с ним, также могут быть вложены инструкции по применению. Предмет производства может дополнительно содержать другие материалы, желательные с коммерческой точки зрения или с позиций потребителя, в том числе буферы, разбавители, фильтры, иглы, шприцы и вкладыши в упаковки с инструкциями по применению композиции.
Пояснение изобретения примерами
Далее настоящее изобретение иллюстрируется следующими примерами, которые не следует рассматривать в качестве ограничивающих его. Содержание всех фигур и всех источников литературы, патентов и опубликованных заявок на патент, цитированных в данном документе, точно в полном объеме включено в данный документ для сведения.
В примерах использованы следующие материалы и методы, если не указано иначе.
Общие материалы и методы
В целом в практике настоящего изобретения используются, если не указано иначе, обычные методы химии, молекулярной биологии, технологии рекомбинантной ДНК, иммунологии (в частности, например, технологии антител) и стандартные методы получения полипептидов. Смотри, например, Sambrook, Fritsch and Maniatis, Molecular Cloning: Cold Spring Harbor Laboratory Press, 1989; Antibody Engineering Protocols (Methods in Molecular Biology), 510, Paul, S., Humana Pr, 1996; Antibody Engineering: A Practical Approach (Practical Approach Series, 169), McCafferty, Ed., Irl Pr, 1996; Antibodies: A Laboratory Manual, Harlow et al., C.S.H.L. Press, Pub., 1999 и Current Protocols in Molecular Biology, eds. Ausubel et al., John Wiley & Sons, 1992.
Оценка термостабильности
Полные ИК-спектры диффузного отражения Фурье (FTIR-ATR) получали для различных единичных цепей и молекул с использованием кюветы FT-IR Bio-ATR в спектрофотометре Tensor Bruker. Молекулы концентрировали до 3 мг/мл и диализовали в течение ночи при 4°С против PBS, рН 6,5, и протекающий буфер собирали в качестве контроля. Получали профили денатурации при термической обработке молекул в широком диапазоне значений температуры с приращением температуры на 5°С (в пределах от 25°С до 95°С). Все манипуляции со спектрами проводили с использованием программного обеспечения OPUS. Основной буфер и временный атмосферный (CO2 и Н2О) фон вычитали из спектра белка. Затем полученный белковый спектр корректировали с учетом базовой линии и белковый спектр амида I определяли по ширине самого широкого разрешаемого пика в предполагаемой области. Спектры второго производного получали для спектров полосы амида I с использованием полиномиальной функции третьей степени с выравнивающей функцией. Изменения в структуре белка устанавливали по анализу второго амидного производного I с использованием линейной калибровочной кривой для первоначального построения кривой, полагая, что имеет место 0% денатурации при 3 нижних определениях и имеет место 100% денатурация при 3 верхних определениях. Профили денатурации использовали для приближения средних точек переходов термического развертывания (ТМ) для каждого варианта с использованием сигмоидальной модели Boltzmann.
Определение растворимости
Относительную растворимость различных молекул scFv после усиления агрегации белка и осаждения в присутствии сульфата аммония. Сульфат аммония добавляли к водным растворам белка с приращением насыщения на 5% в конечной смеси соль-белок. Осаждение в динамических пределах определяли эмпирически и интервалы насыщения снижали в этих пределах до значений 2,5% насыщения в конечной смеси. После добавления сульфата аммония образцы осторожно смешивали и центрифугировали в течение 30 мин при 6000 об/мин. Определяли оставшийся в супернатанте белок для каждого процента насыщения сульфатом аммония. Строили кривые растворимости по определению концентрации белка в супернатанте с использованием спектрофотометра NanoDropTM 1000. Данные по оставшемуся в супернатанте растворимому белку нормализовали и использовали для установления средних точек относительной растворимости для каждого варианта с использованием сигмоидальной модели Boltzmann.
Анализ краткосрочной стабильности
Белок исследовали через 2 недели инкубации при 40°С на наличие растворимых агрегатов и продуктов деградации. Белки в концентрации 10 мг/мл диализовали в течение ночи при 4°С против PBS в широком диапазоне значений рН (3,5; 4,5; 5,5; 6,5; 7,0; 7,5 и 8,5). Контрольный белок в той же концентрации в стандартном буфере PBS (рН 6,5) хранили при -80°С в течение 2 недель. Определение полос деградации проводили электрофорезом в SDS-PAGE на временные точки t=0 и t=14 суток, и растворимые агрегаты оценивали с использованием SEC-HPLC. Определение оставшейся активности проводили через 2 недели выдерживания при 40°С с использованием Biacore.
Тест оценки активности антител
Нейтрализующую активность связывающих TNF соединений оценивали в TNFα-опосредованном тесте цитотоксичности. Токсичность для мышиных фибробластов L929, обработанных актиномицином, индуцировали рекомбинантным человеческим TNF (hTNF). Было установлено, что 90% максимальная hTNF-индуцированная цитотоксичность имела место в концентрации 1000 пг/мл. Все клетки L929 культивировали в среде RPMI 1640, содержащей феноловый красный, с добавлением L-глутамина и эмбриональной телячьей сыворотки (10% об./об.). Нейтрализующую активность связывающих TNF соединений оценивали в среде RPMI 1640 без фенолового красного и с 5% эмбриональной телячьей сыворотки. Различные концентрации связывающего TNF соединения (0-374 нг/мл) добавляли к клеткам L929 в присутствии 1000 пг/мл hTNF для определения концентрации, при которой антагонистическое действие достигает половины максимального ингибирования (EC50). Кривую зависимости «концентрация-эффект» строили с использованием нелинейной сигмоидальной регрессии с различной крутизной и рассчитывали EC50.
Анализ связывания scFv-антител против TNF с использованием BIAcore
Для определения аффинности связывания при рН 5,0 и рН 7,4 (данные не приводятся) использовали поверхностный плазмонный резонанс на BIAcoreTM-T100 с сенсорным чипом NTA и His-меченым TNF (производства ESBATech). Поверхность сенсорного чипа NTA представляет собой карбоксиметилированный декстрановый матрикс, предварительно иммобилизованный с нитрилоуксусной кислотой (NTA), для захвата молекул с гистидиновой меткой посредством хелатирования Ni2+NTA. Триммеры человеческого TNF N-his (5 нМ) захватывались никелем через их N-концевые his-метки и ESBA105 (анализируемое соединение) вводили в нескольких концентрациях в пределах от 30 нМ до 0,014 нМ в трехкратных серийных разведениях. На стадии регенерации комплекс, состоящий из никеля, лиганда и анализируемого соединения, вымывали. Это позволяет использовать одинаковые условия регенерации для различных образцов. Ответный сигнал генерировали с использованием технологии поверхностного плазмонного резонанса (SPR) и определяли в резонансных единицах (RU). Все анализы проводили при температуре 25°С. Сенсограммы получали для каждого образца scFv-антитела против TNF после поправки на ячейку со стандартом с последующим вычитанием показания для буфера. Кажущуюся константу скорости диссоциации (kd), кажущуюся константу скорости ассоциации (ka) и кажущуюся константу равновесия диссоциации (KD) рассчитывали с использованием модели связывания взаимнозначного соответствия Langmuir с программным обеспечением BIAcore Т100 evaluation версия 1.1.
Пример 1:
Трансплантация CDR и функциональная гуманизация кроличьих моноклональных антител против TNF
Трансплантация кроличьих CDR
В отличие от обычных способов гуманизации, в которых используют человеческую каркасную область антитела-акцептора, которая обладает наибольшей гомологией с антителом-донором, отличным от человеческого, кроличьи CDR трансплантировали в каркасную область FW1.4 (последовательности SEQ ID No:1 и 2, связанные линкером (GGGGS)4) с получением min-трансплантата или в «превращенную в кроличью» каркасную область rFW1.4 (последовательность SEQ ID No:92) или ее вариант rFW1.4 (v2) (последовательность SEQ ID No:93) с получением max-трансплантата. Обе каркасные области выбирали в основном с учетом их функциональных свойств (растворимости и стабильности), структурного соответствия для «принятия» самых разнообразных кроличьих CDR и разумной гомологии с кроличьей консенсусной последовательностью вариабельной области. Каркасная область rFW1.4 представляет собой производное каркасной области FW1.4, которая дополнительно сконструирована с целью обеспечения универсальной каркасной области-акцептора практически для любого набора кроличьих CDR. Несмотря на то, что стабильная и растворимая каркасная последовательность FW1.4 демонстрирует высокую гомологию к кроличьим антителам, она не является наиболее гомологичной последовательностью из доступных последовательностей.
Идентификация остатков, потенциально принимающих участие в связывании
Для каждой последовательности кроличьей вариабельной области идентифицирован наиболее близкий кроличий аналог зародышевой линии. В том случае, когда наиболее близкая последовательность зародышевой линии не была установлена, то последовательность сравнивали с подгруппой консенсусных или консенсусом кроличьих последовательностей с высокой процентной сходностью. Редкие остатки каркасной области рассматривались в качестве возможного результата соматической гипермутации и, следовательно, в качестве остатков, принимающих участие в связывании антигена. Следовательно, такие остатки считались возможными для трансплантации на акцепторные каркасные области rFW1.4 или rFW1.4 (v2) для получения max-трансплантатов. В частности, трансплантировали остатки, потенциально принимающие участие в непосредственном взаимодействии с антигеном или оказывающие влияние на расположение VL и VH. Дополнительные остатки, которые предположительно оказывали влияние на структуру CDR, при необходимости замещали. Когда CDR трансплантировали на FW1.4 (min-трансплантаты), то замены в каркасной области не проводили. Можно идентифицировать положения в каркасной области, которые «пересаживали» для получения max-трансплантатов, раскрытых в данном документе, посредством выравнивания последовательностей каркасных областей rFW1.4, rFW1.4 (v2) и интересующих последовательностей scFv, приведенных в данном документе. Для данной цели можно использовать, например, Webtools, известные в данной области (например, Clusta1W в качестве доступного от 23 июня 2009 г. на htt://www.ebi.ac.uk/Tools/clustalw2/index.html. или MultiAlin в качестве доступного от 23 июня 2009 г. на http:/bioinfo.genotoul.fr/multalin). Все положения в каркасной области, в которых rFW1.4 и rFW1.4 (v2) содержат одинаковые остатки и в которых интересующее scFv-антитело имеет другой остаток, представляют собой положения в каркасной области, которые трансплантированы для получения max-трансплантатов.
Перестановка доменов
Вариабельные области легкой цепи min-трансплантатов комбинировали с вариабельными областями тяжелой цепи max-трансплантатов для установления оптимальных комбинаций в отношении биофизических свойств (растворимости и стабильности) и активности.
Клонирование и экспрессия scFv
scFv, описанные и охарактеризованные в данном документе, получали следующим образом. Гуманизированные последовательности VL и гуманизированные последовательности VH (SEQ ID No:51-88, без последовательности SEQ ID No:72) соединяли через линкер с последовательностью SEQ ID No:72 с получением scFv в следующей ориентации: NH2-VL-линкер-VH-COOH (смотри, например, последовательности SEQ ID No:94-121). Во многих случаях последовательности ДНК, кодирующих различные scFv, синтезировали de novo в сервис-провайдере Entelechon GmbH (www.entelechon.com). Полученные вставки ДНК клонировали в бактериальный экспрессирующий вектор pGMP002 через сайты рестрикции NcoI и HindIII, введенные соответственно в 5’- и 3’-концы последовательности ДНК scFv. Между последовательностью ДНК области VL и области VH расположен сайт рестрикции BamHI. В некоторых случаях ДНК, кодирующую scFv, не синтезировали de novo, но экспрессирующие scFv конструкции клонировали перестановкой доменов. Следовательно, области VL вырезали и вводили в новые конструкции через сайты рестрикции NcoI и HindIII, области VH - через сайты рестрикции BamHI и HindIII. В других случаях вводили точечные мутации в область VH и/или VL с использованием методов сборки на основе ПЦР, известных в данной области. Клонирование GMP002 описано в примере 1 в международной заявке WO2008006235. Получение scFv проводили аналогично получению антитела ESBA105, как описано в примере 1 в международной заявке WO2008006235.
Пример 2: анализ профиля и отбор кроличьих антител-доноров CDR
Общая экспериментальная схема, которой следовали для отбора кроличьих антител («RabMab») с ингибирующей TNF активностью, была следующей: кроличьи антитела использовали в качестве антител-доноров CDR при получении иммуносвязывающих TNF соединений с высокой растворимостью. Кроликов иммунизировали TNFα перед спленэктомией. Выделяли спленоциты у кроликов для получения гибридом. В целом было выделено 44 гибридомы и проводили анализ профиля супернатантов данных гибридом в отношении аффинности связывания, биологической активности и специфичности связывания.
На фигуре 1 приведены данные по относительной активности супернатантов 44 гибридом, содержащих RabMab против TNF, в тесте нейтрализации TNFα в условиях in vivo. Нейтрализацию оценивали по определению ингибирования цитотоксичности TNFα в культивированных мышиных фибробластах L929. Супернатанты проявляли различную эффективность в тесте на клетках L929. Определяли значения EC50 (эффективная концентрация, при которой достигается 50% ингибирование) в первичном (синие столбцы) и вторичном скрининге (красные столбцы), и данные нормализовали по отношению к наилучшему результату в каждом тесте. Аффинность связывания с TNFα определяли анализом BIACore для каждого RabMab (зеленые столбцы).
RabMab, кодированные каждой гибридомой, также секвенировали и последовательности подвергали филогенетическому анализу, основанному на прогнозе кластеров эпитопов. Было отобрано четыре типичных RabMab (EPI-6, EPI-19, EPI-34 и EPI-43) с высокой связывающей активностью и высокой нейтрализующей активностью из различных филогенетических семейств в качестве антител-доноров для трансплантации CDR. Кроме того, было отобрано четыре (4) дополнительных RabMab (EPI-1, EPI-15, EPI-35 и EPI-42) для трансплантации CDR, основываясь на их детектированной высокой активности в секреторной ELISA (смотри фигуру 2).
Пример 3: трансплантация CDR и функциональная гуманизация кроличьих антител-доноров
В отличие от обычных методов гуманизации антител, в которых используется человеческая каркасная область антитела-акцептора, обладающая высокой гомологией последовательности с антителом-донором, отличным от человеческого, кроличьи CDR трансплантировали в человеческую каркасную область (FW 1.4), которую заранее отбирали для обеспечения желаемых функциональных свойств (растворимости и стабильности) с использованием теста контроля качества. Несмотря на то что последовательность стабильной и растворимой каркасной области демонстрирует высокую гомологию с RabMab, выбранное антитело-акцептор не является наиболее гомологичной последовательностью из доступных последовательностей.
Для каждого антитела RabMab был получен ряд трансплантатов CDR. В том смысле, в котором в данном документе используется термин «min-трансплантат» или «min», он относится к гуманизированной вариабельной области, которую получали трансплантацией кроличьих CDR из кроличьей вариабельной области в нативную человеческую каркасную область-акцептор (FW 1.4, SEQ ID No:172). В каркасных областях не делали никаких изменений. Саму каркасную область предварительно выбирали с учетом желаемых функциональных свойств (растворимости и стабильности). В том смысле, в котором в данном документе используется термин «max-трансплантат» или «max», он относится к гуманизированной вариабельной области, которую получали трансплантацией кроличьих CDR из кроличьей вариабельной области в «превращенную в кроличью», человеческую каркасную область-акцептор «RabTor» (rFW 1.4, SEQ ID No:173) или в ее производное, обозначенное в данном документе как rFW 1.4 (v2) (SEQ ID No:174). Каркасную область «RabTor» получали включением консервативных кроличьих остатков (которые являются в большей степени вариабельными у других видов) в положения каркасной области, которые обычно принимают участие в образовании структуры кроличьей вариабельной области и обеспечении ее стабильности, с целью получения универсальной применимой каркасной области, которая «принимала» бы практически любой набор кроличьих CDR без необходимости в трансплантации остатков каркасной области-донора, иных чем в положениях, которые различаются по их вероятной исходной последовательности, например, которые изменяются во время соматической гипермутации и, таким образом, возможно, принимают участие в связывании антигена. Вероятная исходная последовательность определяется, как наиболее близкий кроличий аналог зародышевой линии и в том случае, когда наиболее близкая последовательность зародышевой линии не установлена, то последовательность сравнивают с подгруппой консенсусных или консенсусом кроличьих последовательностей с высокой процентной сходностью. Термины «min-max» или «minmax» относятся к гуманизированной вариабельной области, состоящей из «min-трансплантата» вариабельной области легкой цепи в комбинации с «max-трансплантатом» вариабельной области тяжелой цепи, в то время как «max-min» или «maxmin» относятся к гуманизированной вариабельной области, состоящей из «max-трансплантата» вариабельной области легкой цепи в комбинации с «min-трансплантатом» вариабельной области тяжелой цепи.
В таблице 2 приведены обобщенные данные по детальной характеристике гуманизированных одноцепочечных антител, происходящих из восьми различных моноклональных кроличьих антител или rabmab (EP1, EP6, EP15, EP19, EP34, EP35, EP42 и EP43). Так называемые «min» трансплантаты (например, ЕР1 min) относятся к конструкциям, в которые трансплантировали только кроличьи CDR, в то время как в так называемые «max» трансплантаты трансплантировали не только CDR, но и также некоторые аминокислотные положения в каркасной области-доноре. Дополнительно в таблице 2 приведены данные для двух His-меченых одноцепочечных антител (EP34min_C-His и EP19max_C-His), а также для референсного одноцепочечного антитела ESBA105, описанного в международной заявке 2006/131013. Третья колонка, обозначенная как «L929» указывает относительную активность различных одноцепочечных антител по данным теста на клетках L929 в сравнении с активностью антитела ESBA105. Приведены значения kon, koff и Kd соответственно в единицах М-1сек-1, сек-1 и М. В седьмой колонке приведена средняя точка термического развертывания белка антитела по данным FT-IR. В последней колонке показан относительный выход правильно уложенного белка, полученного из солюбилизированных телец включений после рефолдинга.
Некоторые данные BIACore, которые вошли в таблицу 2, представлены также на фигуре 3: приведена кинетика связывания для антитела ESBA105 (фигура 3а), EP43max (фигура 3b) и EP43max (фигура 3с) с человеческим TNFα. Данные по активности антител в клеточных тестах приведены на фигуре 4, на которой представлен сравнительный анализ антитела ESBA105 (закрашенные кружки) с антителом EP43max (пустые квадраты) в тесте на клетках L929. На фигурах 9 и 10 приведены дополнительные данные по активности антитела EP43max в сравнении с промышленно доступными антителами инфликсимабом и адалимумабом в клеточных тестах.
Обобщенные данные по детальной характеристике четырех кроличьих моноклональных антител (ЕР6, ЕР19, ЕР34 и ЕР43) и их вариантов с трансплантированными CDR.
*клетки L929 [ЕС50-Е105/ЕС50-Х] в массовых единицах [нг/мл] по сравнению с функциональной активностью антитела ESBA105 (международная заявка WO06/131013)
** (мг/л раствора для рефолдинга);
*** не определяли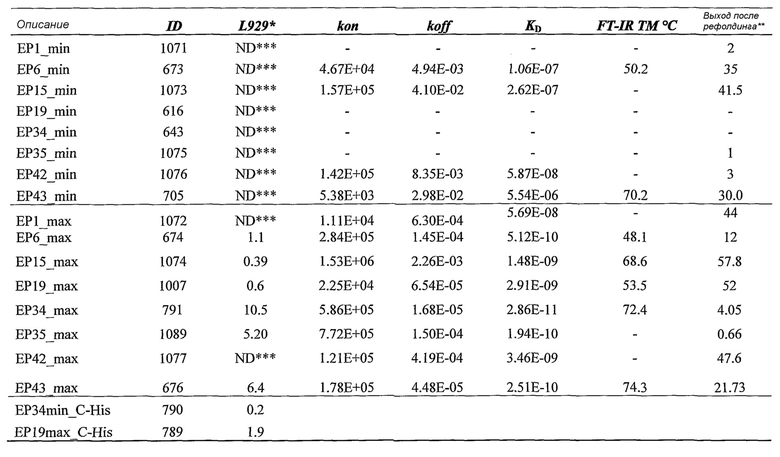
Пример 4: оптимизация растворимости и стабильности ЕР43max, эффективного связывающего TNFα соединения
Антитело EP43max выбрали для дальнейшей оптимизации, основываясь на его способности связываться с TNF. В результате биофизической характеристики данного иммуносвязывающего соединения было установлено, что оно имеет высокую среднюю точку денатурации (Tm>70°С) в тесте термического развертывания белка (FTIR) (смотри фигуру 5). Тем не менее антитело ЕР43max подвергали оптимизации в отношении растворимости в целях сужения его широкой фазы перехода при термическом развертывании. Для повышения растворимости нативного антитела ЕР43max три аминокислотных положения 12, 103 или 144 в области VH замещали на аминокислоты с более высокой гидрофильностью. Было показано, что данная комбинация приводит к повышению растворимости нативного белка, не оказывая влияния на стабильность или связывающую активность антитела. Вводили замены (V→S в положении 12 согласно нумерации AHo, V→T в положении 103 согласно нумерации AHo и L→T в положении 144 согласно нумерации AHo) для замещения гидрофобных остатков на границе областей V-C вариабельной области тяжелой цепи (VH) в антителе ЕР43max. В дополнение к мутациям, приводящим к повышению растворимости, идентифицировали девять стабилизирующих структуру антитела мутаций (T10S, K47R, Y57S, L91F и T103V в VL и E1Q, E6Q, S7T и V103L I в VH) в антителе ЕР43max (смотри таблицу 3). Данные стабилизирующие остатки идентифицировали по результатам функционального консенсусного анализа каркасных областей в тесте контроля качества (QC) ESBATech’s. Стабилизирующие остатки в положениях 1 и 3 в VL и в положении 89 в VH уже присутствовали в молекуле ЕР43max. Идентифицировали дополнительную стабилизирующую мутацию (M→L) в положении 4 области VL, но их не учитывали с учетом предполагаемой роли в связывании антигена.
Стабилизирующие мутации в антителе EP43max
Пример 5: оптимизированные мутантные варианты ЕР43max, эффективного связывающего TNFα соединения
В таблицах 4 и 5 приведены данные, характеризующие три оптимизированных варианта антитела ЕР43max. ЕР43_maxDHP представляет собой мутантный вариант ЕР43max с повышенной растворимостью и он содержит три мутации, приводящие к повышению растворимости, указанные выше (V→S в положении 12 по системе нумерации AHo, V→T в положении 103 по системе нумерации AHo и L→T в положении 144 по системе нумерации AHo). Варианты EP43_maxmin и EP43_minmax получали перестановкой доменов между трансплантатами «min» и «max». Например, вариант «minmax» содержит минимальный вариант трансплантата (только CDR-трансплантат) легкой цепи и максимальный трансплантат тяжелой цепи (т.е. трансплантированные кроличьи CDR плюс остатки кроличьей каркасной области, принимающие участие в связывании антигена), в то время как вариант «maxmin» содержит максимальный вариант трансплантата легкой цепи и минимальный вариант трансплантата тяжелой цепи.
Данные характеристики антитела EP43max и его мутантных вариантов
TM ºC
Данные характеристики антитела EP43max и его мутантных вариантов
Кривые термической денатурации антитела ЕР43max и его оптимизированных мутантных вариантов сравнивали анализом FTIR (смотри фигуру 6 и таблицу 6). Было установлено, что антитело EP43minmax имеет более низкую среднюю точку развертывания белковой молекулы по сравнению с антителом ЕР43max.
Сравнение кривых термической денатурации антитела EP43max и его оптимизированных мутантных вариантов анализом FTIR
Кроме того, мутантный вариант minmax демонстрировал одностадийный переход при развертывании, указывая на то, что обе области развертывались при очень близких температурах. Антитело ЕР43max (фигура 7А) и его вариант EP43minmax (фигура 7В) дополнительно сравнивали в тесте термического стресса. Содержание β-листа и концентрацию растворимого белка оценивали после термического концентрирования при возрастающей температуре (50°С, 60°С и 70°С). Мутантный вариант EP43minmax был достоверно более стабильным по сравнению с антителом ЕР43max при средней температуре, равной 60°С.
Пример 6: сравнение антитела ЕР43max с промышленно доступными связывающими TNFα соединениями
Сравнивали способность ЕР43max, адалимумаба и инфликсимаба блокировать цитотоксическую активность рекомбинантного человеческого TNFα в концентрации 1000 пг/мл, как подробно описано выше, в тесте на клетках L929. Оценивали способность ЕР43max, адалимумаба и инфликсимаба блокировать цитотоксическую активность рекомбинантного человеческого TNFα в концентрации 10 пг/мл в тесте на клетках Kym-1. Результаты приведены соответственно на фигурах 9а, 9b и фигурах 10а, 10b.
На фигуре 9а показана активность антитела ЕР43max и адалимумаба в блокировании цитотоксической активности рекомбинантного человеческого TNFα в концентрации 1000 пг/мл (мышиные клетки L929). Установили, что значения IC50 ЕР43max и адалимумаба составляли соответственно 1,03 нг/мл и 8,45 нг/мл. На фигуре 9b показана способность адалимумаба и ЕР43max блокировать цитотоксическую активность рекомбинантного человеческого TNFα в концентрации 10 пг/мл (тест на человеческих клетках Kym-1). Было установлено, что значения IC50 адалимумаба и ЕР43max (791) составляли соответственно 66,2 нг/мл и 0,69 нг/мл.
На фигуре 10а показана эффективность антитела ЕР43max и инфликсимаба блокировать цитотоксическую активность рекомбинантного человеческого TNFα в концентрации 1000 пг/мл (мышиные клетки L929). Установили, что значения IC50 ЕР43max и инфликсимаба составляли соответственно 1,04 нг/мл и 13,9 нг/мл. На фигуре 10b показана способность инфликсимаба и ЕР43max (791) блокировать цитотоксическую активность рекомбинантного человеческого TNFα в концентрации 10 пг/мл (тест на клетках Kym-1). Было установлено, что значения IC50 инфликсимаба и ЕР43max составляли соответственно 14,98 нг/мл и 0,63 нг/мл. Таким образом, в обоих случаях антитело ЕР43max показало лучшую функциональную активность по сравнению с инфликсимабом.
Другие варианты осуществления
Очевидно, понятно, что изобретение также включает любую из методологий, источников литературы и/или композиций, приведенных в приложениях А-Е.
Эквивалентные варианты осуществления
Многочисленные модификации и альтернативные варианты осуществления настоящего изобретения очевидны специалистам в данной области в свете приведенного выше описания. Следовательно, данное описание следует рассматривать только в качестве иллюстративного и приведенного для специалистов в данной области в целях описания наилучшего способа осуществления настоящего изобретения. Детали структуры могут существенно варьировать, не отступая от сущности изобретения, и сохраняется исключающее применение всех модификаций, которые находятся в объеме прилагаемой формулы изобретения. Полагается, что настоящее изобретение будет ограничиваться только до той степени, которая требуется прилагаемой формулой изобретения и применимыми правилами закона.
Все литературные источники и аналогичный материал, цитированные в данной заявке, включая патенты, заявки на патент, статьи, книги, научные труды, диссертации, веб-страницы, фигуры и/или приложения, независимо от формата такой литературы и аналогичных материалов, экспрессно в полном объеме включены в данный документ для сведения. В случае, если один или более включенных источников литературы и аналогичных материалов отличается от или противоречит данной заявке, включая определенные термины, применение терминов, описанные методики или тому подобное, то данная заявка контролирует это.
Заголовки разделов, использованные в данном документе, приведены только в целях систематизации приводимого материала и не предназначены для ограничения сущности, описанной любым путем.
Несмотря на то, что настоящее изобретение описано в сочетании с различными вариантами осуществления и примерами, не полагается, чтобы настоящие наставления будут ограничиваться такими вариантами осуществления или примерами. Напротив, очевидно специалисты в данной области понимают, что настоящее изобретение включает различные альтернативы, модификации и эквивалентные варианты.
Формулу изобретения не следует рассматривать в качестве ограничивающейся описанной последовательностью или элементами, если не заявлено иначе. Очевидно, понятно, что можно сделать различные изменения в форме и деталях, не отступая от объема прилагаемой формулы изобретения. Следовательно, заявляются все варианты осуществления, которые находятся в объеме и не отступают от сущности последующей формулы изобретения, и эквивалентные им варианты.

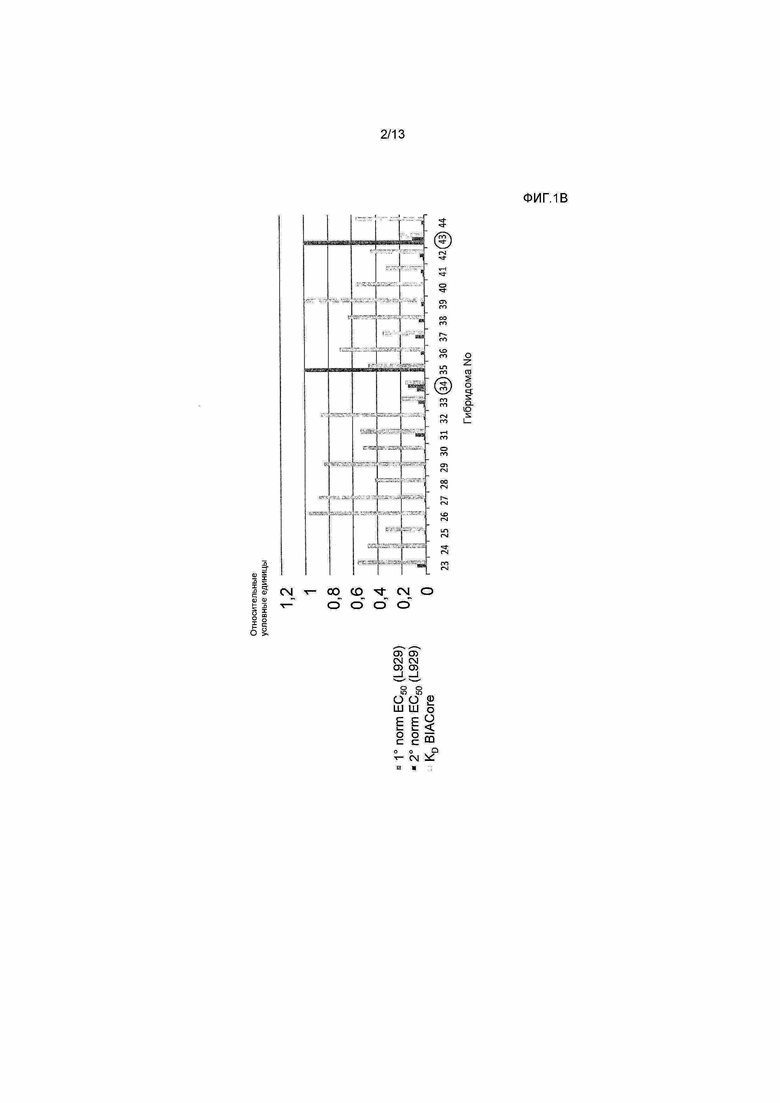



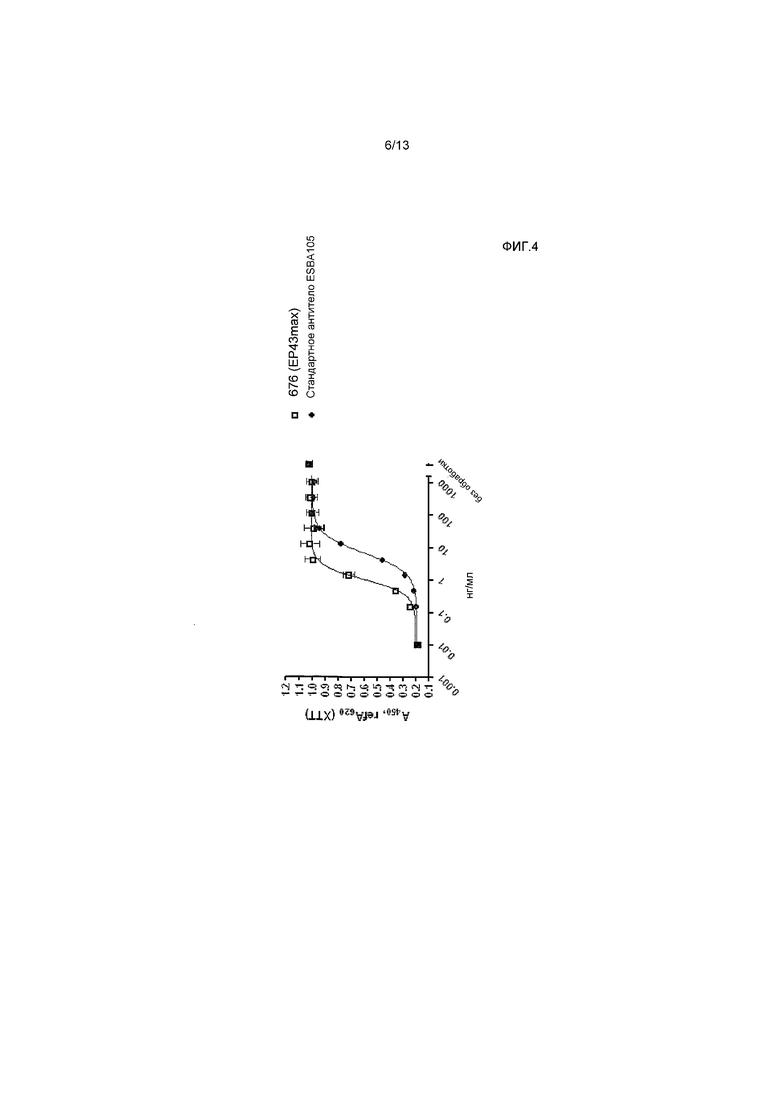
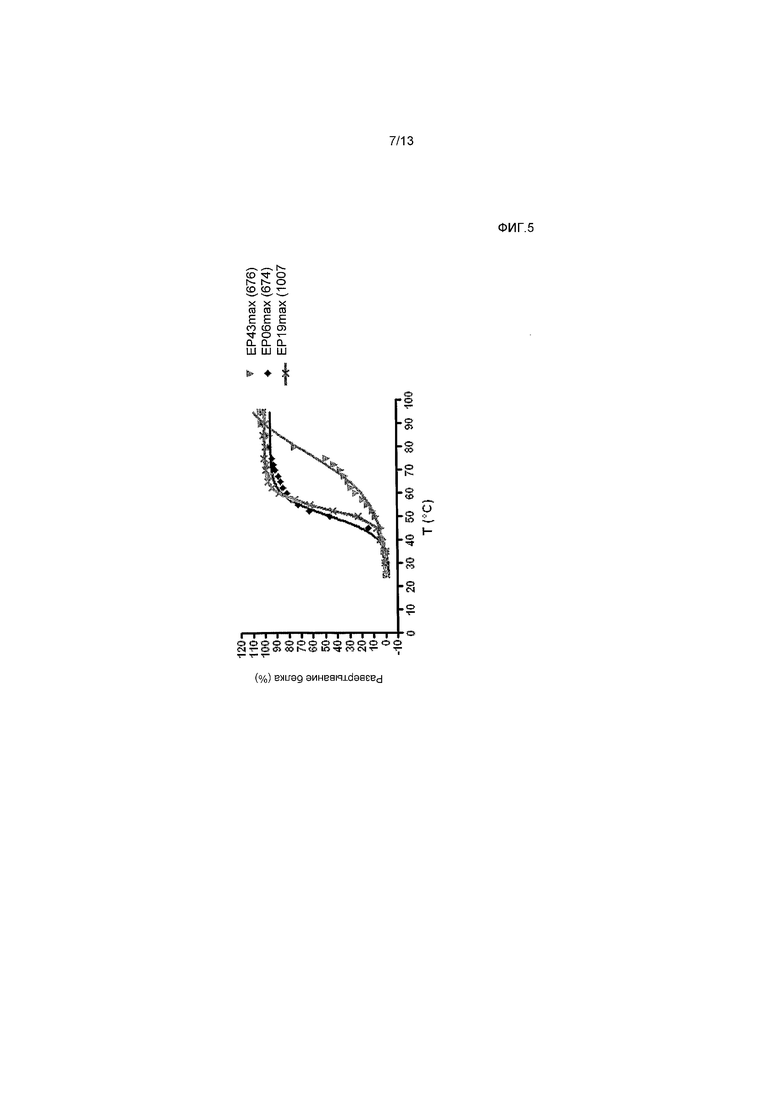
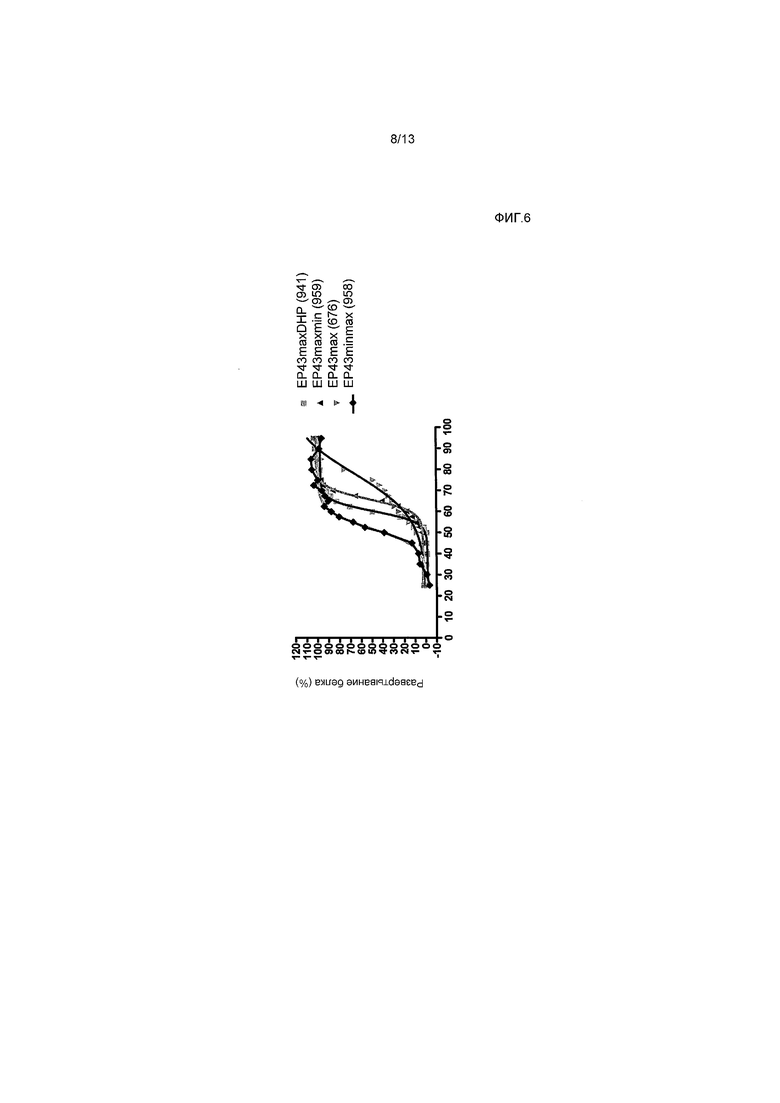





Изобретение относится к биотехнологии, в частности к фармацевтической композиции для лечения TNF альфа–ассоциированных заболеваний у млекопитающего, которая включает антитело, которое содержит специфические последовательности легкой цепи и тяжелой цепи, которые оптимизированы в отношении стабильности, растворимости, связывания с TNF в условиях in vitro и in vivo и низкой иммуногенности. Изобретение позволяет расширить ассортимент препаратов для лечения TNF альфа–ассоциированных заболеваний у млекопитающего. 15 з.п. ф-лы, 12 ил., 6 табл., 6 пр.
1. Фармацевтическая композиция для лечения TNFα-ассоциированного заболевания у млекопитающего, включающая эффективное количество антитела или его антигенсвязывающего фрагмента, который специфически связывается с человеческим TNFα, где антитело или его антигенсвязывающий фрагмент содержит:
(a) последовательность человеческой вариабельной каркасной области тяжелой цепи и последовательности CDR H1, CDR H2 и CDR H3, происходящие из кроличьего антитела, которое специфически связывается с человеческим TNFα, где человеческая вариабельная каркасная область тяжелой цепи обладает по меньшей мере 90% идентичностью с SEQ ID NO:2; и
(b) последовательность человеческой вариабельной каркасной области легкой цепи и последовательности CDR L1, CDR L2 и CDR L3, происходящие из кроличьего антитела, которое специфически связывается с человеческим TNFα, где человеческая вариабельная каркасная область легкой цепи обладает по меньшей мере 90% идентичностью с SEQ ID NO:1,
и, где человеческая вариабельная каркасная область тяжелой цепи имеет по меньшей мере одну из следующих аминокислот: треонин (Т) в положении 24, валин (V) в положении 25, аланин (А) или глицин (G) в положении 56, лизин (K) в положении 82, треонин (T) в положении 84, валин (V) в положении 89 и аргинин (R) в положении 108 (нумерация AHo),
где концентрация антитела или фрагмента антитела в композиции составляет от примерно 0,1 мг/мл до примерно 50 мг/мл, и
где TNFα-ассоциированное заболевание выбрано из группы, состоящей из хронических и/или аутоиммунных воспалительных заболеваний в целом, опосредованных иммунной системой воспалительных заболеваний в целом, воспалительного заболевания ЦНС, воспалительных заболеваний, поражающих глаза, суставы, кожу, слизистые, центральную нервную систему, желудочно-кишечный тракт, мочевые пути или легкие, увеитов в целом, ретинита, HLA-B27+увеита, болезни Бехчета, синдрома сухого глаза, глаукомы, синдрома Шегрена, сахарного диабета (включая диабетическую нейропатию), резистентности к инсулину, артрита в целом, ревматоидного артрита, остеоартрита, реактивного артрита и синдрома Рейтера, юношеского артрита, анкилозирующего спондилита, рассеянного склероза, синдрома Гуллиана-Барре, тяжелой миастении, амиотрофического латерального склероза, саркоидоза, гломерулонефрита, хронического заболевания почек, цистита, псориаза (включая псориатический артрит), гидраденита гнойного, панникулита, гангренозной пиодермии, синдрома SAPHO (синовит, акне, пустулез, гиперстоз и остеит), акне, синдрома Свита, пемфигуса, болезни Крона (включая некишечные проявления заболевания), язвенного колита, бронхиальной астмы, гиперчувствительности при пневмонии, общих аллергий, аллергического ринита, аллергического синусита, хронического обструктивного заболевания легких (COPD), фиброза легких, гранулематоза Вегенера, синдрома Кавасаки, гигантоклеточного артериита, васкулита Чарга-Стросса, нодозного полиартрита, ожогов, синдрома трансплантат против хозяина, реакции хозяин против трансплантата, эпизодов отторжения после трансплантации органа или костного мозга, системных и местных проявлений васкулита в целом, системной и дискоидной красной волчанки, полимиозита и дерматомиозита, склеродермии, преэклампсии, острого и хронического панкреатита, вирусного гепатита, гепатита в результате злоупотребления алкоголем, послеоперационного воспаления, такого как воспаление после операции на глазах (например, по поводу катаракты (замена хрусталика) или операции по поводу глаукомы), после операции на суставах (включая артроскопическую операцию), после операции на структурах, связанных с суставами (например, связках), после операции в ротовой полости и/или стоматологических операций, после минимально инвазивных вмешательств на сердце и сосудах (например, PTCA, атеректомии, размещения стента), после лапароскопических и/или эндоскопических внутрибрюшинных и гинекологических процедур, после эндоскопических урологических вмешательств (например, операции на предстательной железе, уретероскопии, цистоскопии, интерстициальный цистит), или воспаления в периоперативный период (профилактика) в целом, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, паралича Белла, болезни Крейцфельда-Якоба; связанного со злокачественным заболеванием остеолизиса, связанного со злокачественным заболеванием воспаления, связанной со злокачественным заболеванием боли, связанной со злокачественным заболеванием кахексии, метастаз в кости, острых и хронических форм боли, независимо от того, вызваны они центральными или периферическими эффектами TNFα, и независимо от того, классифицируются они как воспалительная, ноцицептивная или неройпатическая формы боли, ишиас, боли в нижней области спины, синдрома запястного канала, комплексного регионарного болевого синдрома (CRPS), подагры, невралгии после герпеса, фибромиалгии, местных болевых состояний, синдрома хронической боли в результате метастазирующей опухоли, дисменореи; бактериального, вирусного или грибкового сепсиса, туберкулеза, СПИДа, атеросклероза, заболевания коронарных артерий, гипертензии, дислипидемии, сердечной недостаточности и хронической сердечной недостаточности.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что концентрация антитела или фрагмента антитела в композиции составляет от примерно 0,5 мг/мл до примерно 25 мг/мл.
3. Фармацевтическая композиция по п.1, отличающаяся тем, что концентрация антитела или фрагмента антитела в композиции составляет от примерно 2 мг/мл до примерно 10 мг/мл.
4. Фармацевтическая композиция по п.1, отличающаяся тем, что последовательность человеческой вариабельной каркасной области тяжелой цепи представляет собой или включает SEQ ID NO:89 или SEQ ID NO:90, и последовательность человеческой вариабельной каркасной области легкой цепи представляет собой или включает SEQ ID NO:91.
5. Фармацевтическая композиция по п.1, отличающаяся тем, что антитело содержит повышающую растворимость замену по меньшей мере в одном из аминокислотных положений тяжелой цепи 12, 103 и 144 (нумерация AHo).
6. Фармацевтическая композиция по п.5, отличающаяся тем, что повышающая растворимость замена выбрана из группы, состоящей из: (а) серина (S) в положении 12; (b) треонина (Т) в положении 103; и (с) треонина (Т) в положении 144.
7. Фармацевтическая композиция по п.1, отличающаяся тем, что антитело или его антигенсвязывающий фрагмент содержит:
(a) последовательности CDR SEQ ID NO:3; SEQ ID NO:4; SEQ ID NO:5; SEQ ID NO:6; SEQ ID NO:7 и SEQ ID NO:8;
(b) последовательности CDR SEQ ID NO:9; SEQ ID NO:10; SEQ ID NO:11; SEQ ID NO:12; SEQ ID NO:13 и SEQ ID NO:14;
(c) последовательности CDR SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19 и SEQ ID NO: 20;
(d) последовательности CDR SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 25 и SEQ ID NO: 26;
(e) последовательности CDR SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31 и SEQ ID NO: 32;
(f) последовательности CDR SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37 и SEQ ID NO: 38;
(g) последовательности CDR SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41, SEQ ID NO: 42, SEQ ID NO: 43 и SEQ ID NO: 44; или
(h) последовательности CDR SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 48, SEQ ID NO: 49 и SEQ ID NO: 50.
8. Фармацевтическая композиция по п.7, отличающаяся тем, что каркасная область тяжелой цепи антитела, содержащего последовательности CDR из d), e), f), g) или h), имеет делеции в положениях каркасной области 85 и 88.
9. Фармацевтическая композиция по п.7, отличающаяся тем, что последовательности CDR из группы a) имеют замену по меньшей мере в одном из положений 22, 74, 95, 97 и 99 вариабельной области легкой цепи (VL) согласно системе нумерации AHo.
10. Фармацевтическая композиция по п.7, отличающаяся тем, что последовательности CDR из группы c) имеют замену по меньшей мере в одном из положений 87, 89 и 92 вариабельной области легкой цепи (VL) согласно системе нумерации AHo.
11. Фармацевтическая композиция по п.7, отличающаяся тем, что последовательности CDR из группы f) имеют замену по меньшей мере в одном из положений 15, 48, 90 вариабельной области легкой цепи (VL) согласно системе нумерации AHo.
12. Фармацевтическая композиция по п.7, отличающаяся тем, что последовательности CDR из группы g) имеют замену по меньшей мере в одном из положений 57 и 87 вариабельной области легкой цепи (VL) согласно системе нумерации AHo, предпочтительно на валин (V) в положении L57 и треонин (T) в положении L87.
13. Фармацевтическая композиция по п.7, отличающаяся тем, что последовательности CDR из группы g) или h) имеют замену по меньшей мере в одном из положений 1, 3, 4, 10, 47, 57, 91 и 103 вариабельной области легкой цепи (VL) согласно системе нумерации AHo, предпочтительно, замену, приводящую к повышению стабильности, выбранную из группы, состоящей из
(a) глутаминовой кислоты (E) в положении 1,
(b) валина (V) в положении 3,
(c) лейцина (L) в положении 4;
(d) серина (S) в положении 10;
(e) аргинина (R) в положении 47;
(f) серина (S) в положении 57;
(g) фенилаланина (F) в положении 91; и
(h) валина (V) в положении 103.
14. Фармацевтическая композиция по п.7, отличающаяся тем, что:
(a) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:51; SEQ ID NO:53 и SEQ ID NO:55, и вариабельную область легкой цепи (VL), обладающую, по меньшей мере, 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:52; SEQ ID NO:54; SEQ ID NO:56; SEQ ID NO:57; SEQ ID NO:58 и SEQ ID NO:59;
(b) вариабельную область тяжелой цепи (VH), обладающую, по меньшей мере, 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:60 и SEQ ID NO:62, и/или вариабельную область легкой цепи (VL), обладающую, по меньшей мере, 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:61 и SEQ ID NO:63;
(c) вариабельную область тяжелой цепи (VH), обладающую, по меньшей мере, 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:64 и SEQ ID NO:66, и/или вариабельную область легкой цепи (VL), обладающую, по меньшей мере, 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:65 и SEQ ID NO:67;
(d) вариабельную область тяжелой цепи (VH), обладающую, по меньшей мере, 90% идентичностью с последовательностью, выбранной из группы, состоящей из SEQ ID NO:64 и SEQ ID NO:66, и/или вариабельную область легкой цепи (VL), обладающую, по меньшей мере, 90% идентичностью с последовательностью, выбранной из группы, состоящей из SEQ ID NO:65 и SEQ ID NO:67;
(e) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:68 и SEQ ID NO:70, и/или вариабельную область легкой цепи (VL), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:69 и SEQ ID NO:71;
(f) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:73 и SEQ ID NO:75, и/или вариабельную область легкой цепи (VL), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:74 и SEQ ID NO:76;
(g) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:77 и SEQ ID NO:79, и/или вариабельную область легкой цепи (VL), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:78 и SEQ ID NO:80;
(h) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:81 и SEQ ID NO:83, и/или вариабельную область легкой цепи (VL), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:82 и SEQ ID NO:84; или
(i) вариабельную область тяжелой цепи (VH), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:85 и SEQ ID NO:87, и/или вариабельную область легкой цепи (VL), обладающую по меньшей мере 90% идентичностью последовательности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:86 и SEQ ID NO:88.
15. Фармацевтическая композиция по п.14, отличающаяся тем, что комбинация последовательностей VL и VH обладает по меньшей мере 90% идентичностью последовательности, предпочтительно, 100% идентичностью с любой из SEQ ID NO:94 - SEQ ID NO:121.
16. Фармацевтическая композиция по п.1, отличающаяся тем, что фрагментом антитела является scFv, Fab или Dab.
| WO2006131013 A2, 14.12.2006 US2006216293 A1, 28.09.2006 RU 2303604 C2, 27.07.2007. |
Авторы
Даты
2019-10-31—Публикация
2018-12-27—Подача