Настоящее изобретение относится к композиции для применения в качестве терапевтического средства, вспомогательного к противоопухолевому химиотерапевтическому лечению, лечению синдрома приобретенного иммунодефицита и лечению лейкозов. Композиция состоит из смеси, содержащей или, предпочтительно, состоящей из штамма бактерий Lactobacillus reuteri LRE 03 DSM 23879, который способен сильно стимулировать продукцию провоспалительных цитокинов Th1 (Т-хелперов 1) интерферона INF-гамма, причем указанные цитокины проявляют выраженную противовирусную и/или противобактериальную активность, и/или штамма бактерий Lactobacillus salivarius LS06 DSM 26037, который способен сильно стимулировать продукцию дендритных клеток, причем указанные дендритные клетки проявляют выраженную противовирусную и/или противобактериальную активность. Дополнительно указанная композиция может содержать один или более чем один из следующих компонентов: бактериальный штамм, обладающий способностью при его употреблении продуцировать бактериальные экзополисахариды EPS; и/или растительный полисахарид, такой как камедь тары; и/или гель Aloe arborescens; и/или желатинизирующий агент, такой как альгинат натрия, и/или цинк с высокой биодоступностью, интернализованный в тиндализованную бактериальную клетку.
В области онкологии известно, что современная медицинская терапия включает химиотерапию, эндокринную терапию, лечение иммуномодуляторами и лечение молекулярно-направленными лекарственными средствами. Главная цель противоопухолевой химиотерапии заключается в том, чтобы уничтожить опухолевые клетки в любой фазе клеточного цикла и таким образом уменьшить массы как первичной опухоли, так и метастаз.
Известно, что противоопухолевое химиотерапевтическое лечение уменьшает активность иммунной системы и что ослабленная иммунная система не способна защитить организм от вирусных и бактериальных инфекций.
Кроме того, известно, что химиотерапия («химия») воздействует главным образом на опухоль, но к сожалению она также оказывает побочные эффекты в отношении здоровых тканей, особенно тканей с быстрой пролиферацией и обновлением, таких как слизистые пищевода, желудка и кишечника, приводя к воспалению слизистой оболочки, тошноте, рвоте, диарее, нарушению всасывания питательных веществ и, следовательно, нарушению питания.
Следовательно, общим свойством всех химиотерапевтических препаратов является: токсичность в отношении костного мозга, что в свою очередь ведет к иммуносупрессии и последующим инфекциям, вызываемым главным образом грамотрицательными бактериями и грибами, такими как Candida, токсичность для эпителия желудочно-кишечного тракта и токсичность для кишечной микрофлоры (химиотерапевтические антибиотики).
Введение эффективных химиотерапевтических доз без сопутствующей терапии, способной противодействовать, конечно, в определенных пределах, неблагоприятным эффектам "химии" путем проведения вспомогательной терапии, было бы невозможно.
Соответственно, было бы желательно иметь натуральное и хорошо переносимое средство, способное уменьшить неблагоприятные эффекты, типичные для химиотерапевтического лечения.
По этой причине по-прежнему сохраняется потребность в вспомогательной терапии для предупреждения и/или уменьшения как симптомов, так и побочных эффектов химиотерапии, применяемой для лечения опухолей, особенно повреждений слизистых пищевода, желудка и кишечника, которые обычно поражаются при химиотерапевтическом лечении. Поэтому необходимо иметь подходящее предохранение и защиту слизистых, таких как, например, слизистая пищевода, слизистая желудка и слизистая кишечника.
Кроме того, по-прежнему сохраняется потребность в вспомогательном к химиотерапии лечении, способном воздействовать на иммунную систему путем ее стимуляции (иммуностимуляции), для восстановления ее эффективности, поскольку химиотерапия влечет за собой снижение эффективности иммунной системы, что приводит к восприимчивости организма к бактериям и вирусам, вызывая возникновение бактериальных и вирусных инфекций.
После долгой и интенсивной научно-исследовательской и поисковой деятельности в отношении обширной группы бактериальных штаммов, принадлежащих к различным видам, авторы настоящего изобретения идентифицировали и выбрали определенные бактериальные штаммы, которые подходящим образом соответствуют вышеизложенным потребностям.
Объектом настоящего изобретения является:
- штамм бактерий, принадлежащих к виду Lactobacillus reuteri, идентифицированный как Lactobacillus reuteri LRE03, с депозитарным номером DSM 23879, депонированный 05.08.2010 Probiotical SpA в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH) в соответствии с Будапештским Договором, и/или
- штамм бактерий, принадлежащих виду Lactobacillus salivarius, идентифицированный как Lactobacillus salivarius LS06, с депозитарным номером DSM 26037, депонированный 06.06.2012 Probiotical SpA в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH) в соответствии с Будапештским Договором.
Авторы изобретения обнаружили, что штамм бактерий Lactobacillus reuteri LRE03 DSM 23879 проявляет выраженную противовирусную и/или противобактериальную активность благодаря его подтвержденной и неожиданной способности (см. экспериментальную часть) стимулировать продукцию провоспалительных цитокинов (Th1) интерферона INF-гамма. Штамм бактерий Lactobacillus reuteri LRE03 DSM 23879 демонстрирует неожиданную иммуностимулирующую активность в отношении эндогенной продукции интерферона гамма INF-гамма. Штамм бактерий Lactobacillus reuteri LRE03 DSM 23879, отобранный авторами изобретения, проявляет неожиданную иммуномодулирующую активность благодаря активации, на уровне слизистых, иммунной системы, оказывая противомикробное и провоспалительное действие через стимуляцию провоспалительных цитокинов (ТЫ) интерферона INF-гамма. Продукция эндогенных цитокинов не оказывает токсического действия в отличие от инфузионного введения указанных цитокинов, как в случае экзогенных цитокинов.
Также авторы изобретения обнаружили, что штамм бактерий Lactobacillus salivarius LS06 DSM 26037 проявляет выраженную противовирусную и/или противобактериальную активность благодаря его подтвержденной и неожиданной способности (см. экспериментальную часть) стимулировать продукцию дендритных клеток. Дендритные клетки помогают иммунной системе в защите организмов от внешних атак опасных микроорганизмов, таких как вирусы и бактерии.
Наконец, авторы изобретения обнаружили, что штамм бактерий, принадлежащих виду Lactobacillus fermentum, идентифицированный как Lactobacillus fermentum LF11, с депозитарным номером DSM 19188, депонированный 20.03.2007 Anidral S.r.l. Company (сейчас Probiotical S.p.A) в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH) в соответствии с Будапештским Договором, обладает способностью создавать и поддерживать в кишечнике среду, неблагоприятную для возникновения, персистенции или распространения инфекции Candida, в частности против видов Candida albicans, Candida krusei, Candida glabrata и Candida parapsilosis, часто возникающей у пациентов, которых лечили химиотерапевтическими лекарственными средствами, вследствие возникающего в результате состояния хронического дисбиоза. Данные по ингибированию in vitro четко подтверждают, что механизм действия штамма L. fermentum LF11 DSM19188 по меньшей мере частично основан на определенных молекулах, отличных от органических кислот, таких как бактериоцины, внеклеточные белки или перекись водорода.
Объектом настоящего изобретения является (1) смесь бактерий, содержащая или, альтернативно, состоящая из штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, и/или штамма бактерий Lactobacillus salivarius LS06 DSM 26037, и/или штамма бактерий Lactobacillus fermentum LF11 DSM 19188.
В одном воплощении указанная смесь (1) содержит или, альтернативно, состоит из:
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, или
- штамма бактерий Lactobacillus salivarius LS06 DSM 26037, или
- штамма бактерий Lactobacillus fermentum LF11 DSM 19188, для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
В другом воплощении смесь (1) бактерий содержит или, альтернативно, состоит из:
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus salivarius LS06 DSM 26037 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
В еще одном воплощении смесь (1) бактерий содержит или, альтернативно, состоит из штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении 3:2:1, 3:1:1, 2:1:1, 2:2:1 или 1:1:1, для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
Смесь (1) бактерий имеет концентрацию бактериальных клеток от 1×108 колониеобразующих единиц (КОЕ)/г смеси до 1×1012 КОЕ/г смеси, предпочтительно от 1×109 КОЕ/г смеси до 1×1011 КОЕ/г смеси. В контексте настоящего изобретения все вышеописанные смеси для краткости изложения называют "смесь бактерий или смеси бактерий по настоящему изобретению".
Другим объектом настоящего изобретения является фармацевтическая композиция, или пищевая композиция, или композиция в виде пищевой добавки, или композиция для медицинского устройства, под которой подразумевается вещество в соответствии с директивным определением 93/42/ЕЕС, именуемое в дальнейшем для краткости изложения "композиция или композиции по настоящему изобретению", где указанная композиция содержит или, альтернативно, состоит из:
(1) смеси бактерий по настоящему изобретению, как описано выше, и/или
(2) смеси бактерий Streptococcus thermophilus ST10 DSM 25246 и камеди тары (растительный полисахарид), где указанный штамм обладает способностью при его употреблении продуцировать экзополисахариды (EPS) in situ, которые в присутствии камеди тары образуют так называемый "мукоадгезивный желатинизирующий комплекс", и/или
(3) смеси, содержащей или, альтернативно, состоящей из камеди, предпочтительно альгината или его производного, и/или геля, предпочтительно геля Aloe или его производного, и/или
(4) источника легкоусвояемого цинка, и/или
(5) одного или более чем одного эксципиента, и/или добавки, и/или вспомогательного компонента препаратов, соответствующих критериям пищевой чистоты или фармакологической чистоты, приемлемых для организма.
В одном воплощении, которое составляет объект настоящего изобретения, композиция по настоящему изобретению содержит или, альтернативно, состоит из: (1) смеси бактерий по настоящему изобретению и (5) одного или более чем одного эксципиента, и/или добавки, и/или вспомогательного компонента препаратов, соответствующих критериям пищевой чистоты или фармакологической чистоты, приемлемых для организма, где указанная композиция предназначена для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
В другом воплощении, которое составляет объект настоящего изобретения, композиция по настоящему изобретению содержит или, альтернативно, состоит из: (1) смеси бактерий по настоящему изобретению, (2) штамма бактерий Streptococcus thermophilus ST10 DSM 25246 и камеди тары (растительный полисахарид), где указанный штамм обладает способностью при его употреблении продуцировать экзополисахариды (EPS) in situ, которые в присутствии камеди тары образуют так называемый "мукоадгезивный желатинизирующий комплекс", и/или (5) одного или более чем одного эксципиента, и/или добавки, и/или вспомогательного компонента препаратов, соответствующих критериям пищевой чистоты или фармакологической чистоты, приемлемых для организма, где указанная композиция предназначена для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
Указанный мукоадгезивный желатинизирующий комплекс способен обеспечивать механический барьерный эффект по всему желудочно-кишечному тракту. Бактериальные экзополисахариды (EPS) представляют собой экзополисахариды, продуцируемые in situ штаммом бактерий Streptococcus thermophilus ST10 DSM 25246. Штамм бактерий Streptococcus thermophilus ST10 DSM 25246 был депонирован 19.09.2011 в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH) в соответствии с Будапештским Договором Probiotical S.p.A. Композиция по настоящему изобретению содержит от 1×108 до 1×1012 жизнеспособных клеток Streptococcus thermophilus ST10 DSM 25246/г композиции, предпочтительно от 1×109 до 1×1011 жизнеспособных клеток Streptococcus thermophilus ST10 DSM 25246/г композиции.
В другом воплощении, которое составляет объект настоящего изобретения, композиция по настоящему изобретению содержит или, альтернативно, состоит из: (1) смеси бактерий по настоящему изобретению, (2) штамма бактерий Streptococcus thermophilus ST10 DSM 25246 и камеди тары (растительный полисахарид), где указанный штамм обладает способностью при его употреблении продуцировать экзополисахариды (EPS) in situ, которые в присутствии камеди тары образуют так называемый "мукоадгезивный желатинизирующий комплекс", (3) смеси, содержащей или, альтернативно, состоящей из камеди, предпочтительно альгината или его производного, и/или геля, предпочтительно геля Aloe или его производного, и (5) одного или более чем одного эксципиента, и/или добавки, и/или вспомогательного компонента препаратов, соответствующих критериям пищевой чистоты или фармакологической чистоты, приемлемых для организма, где указанная композиция предназначена для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов. Указанная смесь (3) содержит, или, альтернативно, состоит из камеди, предпочтительно альгината или его производного и/или геля, предпочтительно геля Aloe или его производного. Альгинат или его производное предпочтительно представляет собой альгинат натрия. Продукт Aloe или его производное предпочтительно представляет собой Aloe arborescens, предпочтительно в лиофилизированной форме. Aloe arborescens предпочтительно находится в лиофилизированной форме. В одном воплощении композиция по настоящему изобретению содержит альгинат натрия и лиофилизированный Aloe arborescens в массовом соотношении от 1:50 (альгинат : Aloe) до 50:1, предпочтительно от 1:30 (альгинат : Aloe) до 30:1.
Дополнительно авторы изобретения обнаружили, что активация иммунной системы (IS) также может быть достигнута с помощью цинка с очень высокой биодоступностью в дополнение к действию, вызванному штаммом бактерий Lactobacillus reuteri LRE03 DSM 23879 и/или штаммом бактерий Lactobacillus salivarius LS06 DSM 26037. Очень высокая биодоступность цинка является следствием того факта, что он находится в форме цинка, интернализованного внутри тиндализованной бактериальной клетки штамма бактерий, принадлежащего виду Bifidobacterium lactis, где предпочтительно штамм, выбранный авторами изобретения, представляет собой штамм бактерий Bifidobacterium lactis Bb 1 DSM 17850, депонированный в DSMZ 23.12.2005, являющийся объектом европейской заявки на патент No. 08789404, включенной в данное описание посредством ссылки.
По существу авторы изобретения обнаружили, что цинк с высокой биодоступностью, интернализованный в тиндализованную клетку (инактивированную клетку), способен активировать иммунную систему (IS), особенно тимус, отвечающий за продукцию Т-лимфоцитов, которые продуцируют нетоксичные эндогенные цитокины, такие как гамма-интерферон.
В другом воплощении, которое составляет объект настоящего изобретения, композиция по настоящему изобретению содержит или, альтернативно, состоит из: (1) смеси по настоящему изобретению, (2) штамма бактерий Streptococcus thermophilus ST10 DSM 25246 и камеди тары (растительный полисахарид), где указанный штамм обладает способностью при его употреблении продуцировать экзополисахариды (EPS) in situ, которые в присутствии камеди тары образуют так называемый "мукоадгезивный желатинизирующий комплекс", (3) смеси, содержащей или, альтернативно, состоящей из камеди, предпочтительно альгината или его производного, и/или геля, предпочтительно геля Aloe или его производного, (4) источника цинка с высокой усвояемостью и биодоступностью в форме цинка, интернализованного внутри тиндализованной бактериальной клетки штамма бактерий, принадлежащих виду Bifidobacterium lactis, где предпочтительно указанный штамм представляет собой штамм бактерий Bifidobacterium lactis Bb 1 DSM 17850, и (5) одного или более чем одного эксципиента, и/или добавки, и/или вспомогательного компонента препаратов, соответствующих критериям пищевой чистоты или фармакологической чистоты, приемлемых для организма, где указанная композиция предназначена для применения в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов, или альтернативно, для применения в защите слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов. Указанный источник (4) цинка с высокой усвояемостью и биодоступностью присутствует как органический цинк в форме бактериального тиндализованного продукта штамма Bifidobacterium lactis ВЫ DSM 17850 (ProbioZinc®, депонированного 23.12.2005 в DSMZ - Немецкой коллекции микроорганизмов и клеточных культур GmbH BioMan S.r.l. Company (Italy). Бактериальный тиндализованный продукт штамма Bifidobacterium animalis ssp. lactis Вb1 DSM 17850 присутствует в количестве от 10 до 50 мг/г композиции, предпочтительно 20 мг/г композиции.
Все вышеупомянутые композиции по настоящему изобретению эффективно применимы для использования в качестве вспомогательной терапии при противоопухолевом химиотерапевтическом лечении, лечении синдрома приобретенного иммунодефицита и лечении лейкозов. Дополнительно композиции по настоящему изобретению эффективно применимы для использования в качестве вспомогательного терапевтического средства для предупреждения и/или уменьшения симптомов и побочных эффектов, типичных для химиотерапии, применяемой для лечения опухолей, особенно повреждений, вызываемых на слизистых пищевода, желудка и кишечника, которые обычно повреждаются во время химиотерапевтического лечения. Наконец, композиции по настоящему изобретению эффективно применимы для использования в качестве вспомогательного терапевтического средства для иммунной системы, поскольку химиотерапия влечет за собой снижение эффективности иммунной системы, которое приводит к восприимчивости организма к бактериям и вирусам, вызывая возникновение бактериальных и вирусных инфекций.
Наконец, композиция по настоящему изобретению содержит эксципиент, и/или добавку, и/или вспомогательный компонент препаратов, соответствующие критериям пищевой чистоты или фармакологической чистоты, которые обеспечивают возможность изготовления таких фармацевтических форм как порошки, гранулы, таблетки или капсулы.
Композиция по настоящему изобретению содержит от 1×108 до 1×1012 жизнеспособных бактериальных клеток КОЕ/г композиции, предпочтительно от 1×109 до 1×1011 жизнеспособных бактериальных клеток КОЕ/г композиции. Композиция по настоящему изобретению рекомендована предпочтительно для введения 1-2 раза в сутки в течение 4-12 недель.
Композиция по настоящему изобретению состоит из подходящего количества камеди тары, которая вследствие ее желатинизирующих и мукоадгезивных свойств способна образовывать гидрогель в течение нескольких минут после ее употребления благодаря ее тиксотропным свойствам, тем самым создавая прежде всего в желудочно-кишечном тракте действие механического барьера против адгезии патогенных микроорганизмов к слизистой органа, таким образом уменьшая их транслокацию через стенку кишечника и последующий риск инфицирования соседних органов, что является основным, когда происходит нарушение функций иммунной системы. Такой барьерный эффект осуществляется и распространяется по всему желудочно-кишечному тракту путем одновременного присутствия экзополисахаридов (EPS), продуцируемых in situ микроорганизмом Streptococcus thermophilus ST10, тем самым увеличивая вязкость окружающей среды путем саморегулируемого, исключительно механического механизма. Употребление указанной бактерии доставляет в кишечник человека источник желатинизирующих молекул, тем самым выполняя действие, полностью взаимодополняющее действие камеди тары.
Вышеописанный мукоадгезивный желатинизирующий комплекс имеет инновационное свойство, которое следует принять во внимание: растительная камедь тары постепенно разлагается резидентной микробиотой во время ее продвижения по кишечнику, что тем самым постепенно снижает ее желатинизирующую способность механического барьера. Постепенное уменьшение действия растительной камеди эффективно уравновешивается постепенным увеличением высвобождения в полость кишечника экзополисахаридов (EPS), которые продуцирует in situ бактериальный штамм Streptococcus thermophilus ST10 DSM 25246, который действует главным образом в подвздошной кишке и толстой кишке.
Таким образом, синергическая комбинация камеди тары и экзополисахаридов (EPS), продуцируемых in situ, обеспечивает присутствие желатинизирующих молекул на протяжении всего желудочно-кишечного тракта, максимально увеличивая и оптимизируя действие механического барьера продукта. Следовательно, присутствие, образование и сохранение гидрофильного геля в просвете органа можно впервые считать действительно абсолютными, с первой областью, где действие растительной камеди является максимальным, и второй областью, где действие экзополисахаридов (EPS), продуцируемых in situ, является максимальным.
Благодаря присутствию лиофилизированного Aloe arborescens (Alagel™) (например 1,5 грамм/доза) и альгината натрия (например 50 мг/доза), двух компонентов с желатинизирующей активностью, композиция по настоящему изобретению способна обеспечивать механический барьерный эффект для защиты слизистых пищевода, желудка и кишечника. Более того, альгинат натрия проявляет механическое препятствующее действие против гастроэзофагеального рефлюкса, а также физическое защитное действие против воспаления пищевода и гастрита. Таким образом, комбинация Aloe arborescens и альгината натрия способна делать побочные эффекты химиотерапевтического лечения более переносимыми у индивидуумов с опухолевым заболеванием. Более того, продукт Aloe arborescens, кроме действия по физической защите слизистых пищевода, желудка и кишечника, способен уменьшать адгезивные способности патогенных штаммов посредством физико-механического препятствия, со специальным упоминанием жгутиковых микроорганизмов, как на уровне пищевода, так и на уровне желудка и кишечника. Продукт Aloe также способен снижать проницаемость желудка и кишечника, тем самым делая вклад в восстановление физиологического барьерного эффекта такого органа, и действовать синергически с камедью тары и экзополисахаридами (EPS) для снижения риска транслокации бактерий из кишечника. Более того, Aloe arborescens обладает противовоспалительной активностью, тем самым оказывая дополнительную защиту на уровне слизистых.
В свете ее общего механизма действия, композиция по настоящему изобретению способна делать побочные эффекты химиотерапевтического лечения, особенно бактериальные инфекции, более переносимыми для индивидуумов с опухолевым заболеванием.
Дополнительно, присутствие в композиции по настоящему изобретению смеси (1) по настоящему изобретению (имеющей концентрацию бактериальных клеток от 1×108 КОЕ/г смеси до 1×1012 КОЕ/г смеси, предпочтительно от 1×109 КОЕ/г смеси до 1×1011 КОЕ/г смеси), содержащей или, альтернативно, состоящей из:
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, или
- штамма бактерий Lactobacillus salivarius LS06 DSM 26037, или
- штамма бактерий Lactobacillus fermentum LF11 DSM 19188, или
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus salivarius LS06 DSM 26037 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении 3:2:1, 3:1:1, 2:1:1, 2:2:1 или 1:1:1;
обеспечивает усиление вышеописанного барьерного эффекта посредством механизма, являющегося дополнительным к механизму мукоадгезивного желатинизирующего комплекса, Aloe arborescens и альгината натрия.
Действительно, штамм L. reuteri LRE03 DSM 23879 способен значительно стимулировать эндогенную продукцию гамма-интерферона (IFN-γ). Способность штамма L. reuteri LRE03 DSM 23879 индуцировать высвобождение цитокинов, в частности гамма-интерферона IFN-гамма, первичными клетками иммунной системы количественно оценивали путем его совместного инкубирования с РВМС (мононуклеарные клетки периферической крови), выделенными из периферической крови здоровых взрослых индивидуумов. Результаты показали стимуляцию секреции IFN-гамма с концентрацией 480 пг/мл, а именно в 47 раз больше, чем в контроле. Продукцию IFN-гамма оценивали в культуральном супернатанте через 5 суток после стимуляции относительно условий без стимуляции (базовый уровень).
Гамма-интерферон (IFN-γ) обладает свойствами, препятствующими вирусным и бактериальным инфекциям подобно другим интерферонам и нефизиологической пролиферации клеток, что опосредовано изменениями цитоскелета и клеточной мембраны, модуляциями экспрессии продукта онкогена и регуляцией процесса дифференцировки клеток (задержка почти всех фаз митоза как у нормальных, так и у опухолевых клеток). IFN-γ также демонстрирует основное и характерное иммуномодулирующее действие путем стимуляции активности как клеток, специализированных для иммунного ответа организма, таких как макрофаги, моноциты, нейтрофилы, так и неспециализированных клеток, таких как тромбоциты, эндотелиальные и эпителиальные клетки, фибробласты и клетки паренхимы.
Дополнительное усиление барьерного эффекта, получаемого от композиции по настоящему изобретению и опосредованного Aloe и альгинатом натрия, обеспечивается присутствием подходящего количества цинка с высокой биодоступностью (2 мг/доза), интернализованного микроорганизмом Bifidobacterium lactis Вb1. Цинк с высокой биодоступностью (интернализованный) находится в форме тиндализованной (инактивированной) клетки. Эта форма цинка обладает очень высокой биодоступностью и, следовательно, способностью легче усваиваться организмом. Ион цинка, будучи биодоступным и легкоусвояемым организмом, играет центральную роль и оказывает прямое действие в отношении тимуса, который отвечает за образование/продукцию лимфоцитов.
Штамм бактерий Bifidobacterium lactis Bb 1 DSM 17850 был депонирован в DSMZ 23.12.2005 BioMan S.r.l. Company (Italy). Действительно, штамм бактерий Bifidobacterium lactis Bb 1 DSM 17850 обладает способностью аккумулировать цинк внутри клетки во время своего роста в жидкой культуральной среде. Цинк из рациона, накопленный внутри клетки (ProbioZinc®), обладает усвояемостью в 17 выше чем глюконат цинка и в 31,5 раз выше чем сульфат цинка, как показано в исследовании in vitro, проведенном на клетках Сасо-2 в системе Transwell. Высокая усвояемость микроэлемента цинка позволяет эффективно компенсировать условия недостаточности даже при очень низких дозировках. Более того, известно, что цинк играет важную роль в отношении иммунной системы, особенно для тимуса, представляющего собой орган, где происходит образование Т-лимфоцитов, которые, когда дифференцируются в CD4+ Т-лимфоциты (Т-лимфоциты-хелперы), секретируют ряд цитокинов, таких как IL(интерлейкин)-12 и IFN-γ. Указанный механизм действия цинка является синергическим с таковым у штамма L. reuteri LRE03 DSM 23879.
В дополнение к вышеизложенному, штаммы L reuteri LRE03 DSM 23879 и L. fermentum LF11 DSM 19188 опосредуют усиление барьерного эффекта для защиты слизистых желудочно-кишечного тракта, опосредуемого желатинизирующим комплексом, Aloe и альгинатом натрия, путем препятствующего действия против грамотрицательных бактерий, главным образом штамм L. fermentum LF11 DSM 19188 действует непосредственно против колиформных бактерий, E.coli и грибов рода Candida. Были выбраны микроорганизмы с выраженным барьерным действием против потенциальных грамотрицательных патогенов, со специальным упоминанием видов Escherichia coli, Enterobacter cloacae и Klebsiella pneumoniae, которые представляют собой колиформные бактерии, которые могут вызывать даже тяжелые инфекции желудочно-кишечного тракта у индивидуумов, проходящих химиотерапию. В результате этой научно-исследовательской деятельности был успешно выбран штамм L fermentum LF11 DSM 19188.
Дополнительно, штамм L fermentum LF11 DSM 19188 также обладает способностью устанавливать и сохранять барьерный эффект против дрожжей рода Candida, как продемонстрировано, в частности, в отношении видов Candida albicans, Candida krusei, Candida glabrata и Candida parapsilosis. Особенно штамм L fermentum LF11 DSM 19188 способен создавать и поддерживать в кишечнике среду, неблагоприятную для возникновения, персистенции или распространения инфекции Candida, часто возникающей у пациентов, которых лечили химиотерапевтическими лекарственными средствами, как следствие и проявление возникающего в результате состояния хронического дисбиоза.
Данные по ингибированию in vitro четко подтверждают, что механизм действия штамма L. fermentum LF11 DSM19188 по меньшей мере частично основан на определенных молекулах, отличных от органических кислот, таких как бактериоцины, внеклеточные белки или перекись водорода.
Интересно, что компоненты композиции, которая представляет собой объект настоящего изобретения, обладающие механическим действием, прежде всего действуют путем уменьшения адгезивных свойств патогенных штаммов посредством физико-механического препятствия, со специальным упоминанием жгутиковых микроорганизмов, тогда как штаммы бактерий L reuteri LRE03 DSM 23879, Lactobacillus salivarius LS06 DSM 26037 и L. fermentum LF11 DSM 19188 проявляют дополнительный эффект к вышеописанному препятствию против патогенов (вирусов, бактерий и дрожжей), которые становятся неспособными прикрепляться к поверхности слизистой, таким образом оставаясь в просвете желудочно-кишечного тракта.
В свете вышеизложенного, механизм действия композиции, представляющей собой объект настоящего изобретения, состоит в установлении и поддержании механического барьерного эффекта для физической защиты слизистых пищевода, желудка и кишечника, также уменьшая способность патогенных штаммов, со специальным упоминанием жгутиковых штаммов, к адгезии. Более того, механический барьерный эффект продукта способен восстанавливать физиологическую проницаемость слизистой кишечника, обычно повышенную во время химиотерапевтического лечения.
Эффекты, усиливающие первичный барьерный эффект, представляют собой стимуляцию эндогенной секреции цитокинов, способных противодействовать вирусным инфекциям и нефизиологической пролиферации клеток, а также синтез специфических молекул с противобактериальной активностью и активностью против Candida, тем самым обеспечивая дополнительную защиту индивидуумов, которых лечат противоопухолевыми химиотерапевтическими лекарственными средствами.
В свете ее общего механизма действия, композицию, представляющую собой объект настоящего изобретения, эффективно используют для применения в качестве вспомогательного терапевтического средства у индивидуумов с опухолевыми заболеваниями и подлежащих химиотерапии, а также антиретровирусном лечении у индивидуумов с синдромом приобретенного иммунодефицита (СПИД) и лечении лейкозов.
Экспериментальная часть
Авторы изобретения протестировали иммуномодулирующие свойства штамма бактерий Lactobacillus reuteri LRE 03 (ID1777) DSM 23879, как описано ниже.
Конкретно, исследование проводили после различных периодов времени стимуляции, для того, чтобы проанализировать как цитокины, вовлеченные в врожденный иммунитет, так и те, которые ответственны за приобретенный иммунитет.
а) Бактериальные культуры и условия роста
Во-первых, бактериальные культуры штамма бактерий Lactobacillus reuteri LRE 03 DSM 23879 получали в определенных условиях роста. Штамм культивировали в среде Man Rogosa Sharpe (MRS) на термостатируемой бане при 37°С. Что касается экспериментов по иммуномодулированию после периода роста в течение приблизительно 16 часов, бактерии субкультивировали в течение 6 часов в условиях, описанных выше, для достижения фазы экспоненциального роста. Затем их дважды промывали стерильным фосфатно-солевым буфером (PBS, рН 7,2), физиологический статус и число клеток определяли цитофлуориметрическим методом с использованием набора "Cell Viability Kit with liquid beads", доступного в продаже от Becton Dickinson Company, в соответствии с инструкциями производителя. Соответственно, концентрацию клеток доводили до оптимальной концентрации, установленной в предварительных экспериментах, и использовали в последующих тестах.
б) Отделение мононуклеарных клеток периферической крови
Затем отделяли мононуклеарные клетки периферической крови.
Мононуклеарные клетки периферической крови (РВМС) отделяли путем центрифугирования в градиенте плотности. Для этой цели 20 мл "лейкоцитарной пленки" здоровых доноров из Службы переливания крови (Immuno-transfusion Service) Ospedale di Borgomanero (Italy) использовали в каждом эксперименте, таким образом получая средний выход 200×106 РВМС/лейкоцитарная пленка. Количество отделенных клеток определяли путем подсчета клеток в камере Бюркера с использованием раствора Тюрка, который позволяет различить мононуклеарные клетки и полиморфоядерные клетки. Концентрацию клеток доводили до 2×106 клеток/мл в ростовой среде RPMI-1640 (Invitrogen), дополненной 10% инактивированной нагреванием эмбриональной сыворотки крупного рогатого скота (FCS, Gibco), 1% глутамина и 25 мМ Hepes (N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота).
в) Стимуляция РВМС
Далее мононуклеарные клетки периферической крови (РВМС) стимулировали бактериальным штаммом. После отделения РВМС стимулировали бактериальным штаммом в течение 1 и 5 суток. Внутренние контроли в каждом эксперименте представляли собой следующее:
Отрицательный контроль: только РВМС
1-суточный контроль: РВМС, стимулированные 1 мкг/мл липополисахарида (LPS; Escherichia coli, серотип 055:В5, Sigma Chemicals Co., St. Louis, MO).
5-суточный контроль: РВМС, стимулированные 1 мкг/мл фитогемагглютинина (PHA-P; Sigma Chemicals Co., St. Louis, MO).
В различные периоды анализа культуры центрифугировали при 1500 об/мин в течение 10 минут. Супернатанты отбирали и хранили при -20°С до анализа. Клетки использовали для последующих тестов.
г) Анализ пролиферации клеток
Затем выполняли анализ пролиферации клеток. Пролиферацию клеток оценивали цитофлуориметрическим методом с использованием протокола мечения ядер бромдезоксиуридином (BrdU). Этот метод был разработан как альтернатива более традиционной системе радиоактивного мечения тимидином, меченным тритием. В частности, к культурам клеток добавляли смесь 5-бром-2'-дезоксиуридина (BrdU) и 2'-дезоксицитидина (dC), каждый в конечной концентрации 20 мкМ. После 16-часового инкубирования при 37°С в увлажненной атмосфере, 5% СО2, анализировали пролиферацию клеток цитофлуориметрическим методом. Культуральные супернатанты собирали и хранили при -20°С до анализа. После фиксирования и пермеабилизации клеточной стенки клеточную ДНК метили анти-BrdU моноклональными антителами (mAb), коньюгированными с FITC (флуоресцеинизотиоцианат) (Becton Dickinson). Клетки анализировали в течение 24 часов от их получения с использованием цитофлуориметра FACScalibur от Becton Dikinson Company и программы анализа CellQuest.
Результаты выражали как индекс пролиферации клеток (P.I.), который рассчитывали как соотношение процента пролиферирующих клеток в присутствии стимулирующего воздействия и процента таких же клеток в отсутствие стимуляции. Величину P.I. больше 2 считали приемлемой (пороговая величина). Во всех экспериментах стимуляция митогеном (РНА) в качестве контроля всегда приводила к величине больше пороговой величины, подтверждая, что РВМС были жизнеспособными и способными к пролиферации.
д) Анализ молекул, характеризующих индивидуальные субпопуляции клеток
Далее проводили анализ молекул, характеризующих индивидуальные субпопуляции клеток. В отношении иммунофенотипической характеристики, клетки инкубировали в течение 30 минут в темноте с различными комбинациями следующих моноклональных антител (mAb), конъюгированных с флуоресцеинизотиоцианатом (FITC), фикоэритрином (РЕ) или перидинин-хлорофилл-протеином (PerCP): CD3, CD4, CD8, CD14, CD16, CD19, CD20, CD56, HLA-DR. После инкубирования образцы промывали, фиксировали раствором, содержащим 1% параформальдегида и хранили при 4°С. В пределах 24 часов после получения образцы анализировали с помощью цитофлуориметра FACScalibur, при этом клетки выбирали так, чтобы исключить из анализа примеси остатков разрушенных клеток.
е) Дозирование цитокинов
Далее выполняли дозирование цитокинов. Концентрацию цитокинов в культуральных супернатантах определяли путем анализа E.L.I.S.A. (твердофазный иммуноферментный анализ). Более конкретно, для дозирования цитокинов (IL-4, IL-10, IFN-γ и IL-12р70) использовали наборы "Human ELISA Ready-SET-Go" от eBioscence Company, San Diego CA.
ж) Статистический анализ
Статистический анализ выполняли с использованием двустороннего парного t-критерия Стьюдента. Величину р менее 0,05 считали существенной.
РЕЗУЛЬТАТЫ
1) Определяли пролиферативный ответ, индуцированный штаммом бактерий Lactobacillus reuteri LRE 03 DSM 23879. Анализ клеточной пролиферации in vitro представляет собой чрезвычайно полезный биологический параметр для исследования функционирования иммунной системы. Для того чтобы проанализировать, может ли тестируемый бактериальный штамм воздействовать на индукцию пролиферации лимфоцитов, мононуклеарные клетки периферической крови (РВМС) стимулировали бактериальным штаммом Lactobacillus reuteri LRE 03 DSM 23879. Фитогемагглютинин (PHA), который представляет собой митогенный стимул, способный индуцировать поликлональную пролиферацию Т-лимфоцитов, использовали в качестве положительного контроля. РВМС выделяли из образцов периферической венозной крови 4 здоровых доноров-мужчин возраста 40 лет в среднем (диапазон 21-52 года), из Службы переливания крови (Transfusion Service) Ospedale S.S.  , Borgomanero (Novara).
, Borgomanero (Novara).
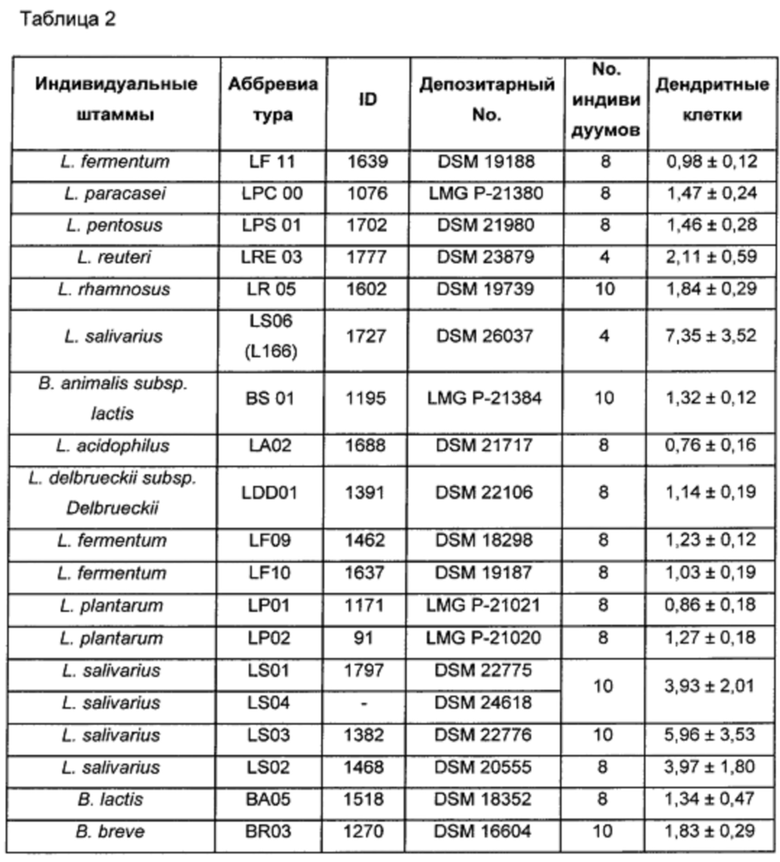
Как показано на Фиг. 1, где показан индекс пролиферации клеток (P.I., см. описанные выше способы), пролиферативный ответ РВМС во всех условиях стимуляции был значительно выше, чем в отсутствие стимуляции (базовый уровень).
На фиг. 1 показано среднее ± стандартная ошибка среднего (S.E.M.) по результатам 4 независимых экспериментов. Статистическую значимость рассчитывали с использованием t-критерия Стьюдента. Величины р менее 0,05 следует считать статистически значимыми по сравнению с базовым уровнем (нестимулированные РВМС).
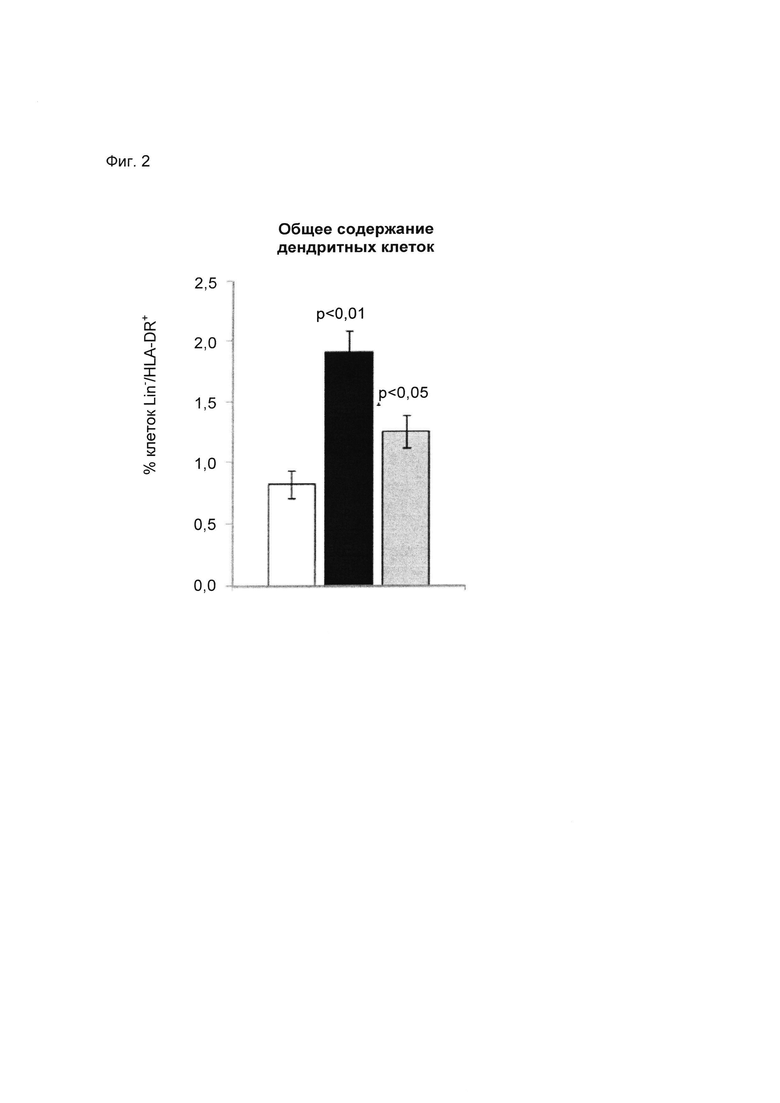
2) Оценивали действие бактериального штамма Lactobacillus reuteri LRE 03 DSM 23879 на различные субпопуляции клеток. Для определения, пролиферация каких субпопуляций клеток была индуцирована после стимуляции тестируемым пробиотическим штаммом, был выполнен многопараметрический анализ проточной цитометрии. На следующих фигурах (Фиг. 2 и Фиг. 3) показано процентное содержание основных субпопуляций клеток, вовлеченных как в врожденный, так и в приобретенный иммунный ответ.
2а) Врожденный иммунитет. Через одни сутки стимуляция бактериальном штаммом Lactobacillus reuteri LRE 03 (DSM 23879) вызывала изменение в общем процентном содержании дендритных клеток (Линия-/HLA-DR+).
На Фиг. 2 показан пролиферативный ответ, среднее ± S.E.M. по результатам 4 независимых экспериментов. Статистическую значимость рассчитывали с использованием t-критерия Стьюдента. Величины р менее 0,05 следует считать статистически значимыми по сравнению с базовым уровнем (нестимулированные РВМС).
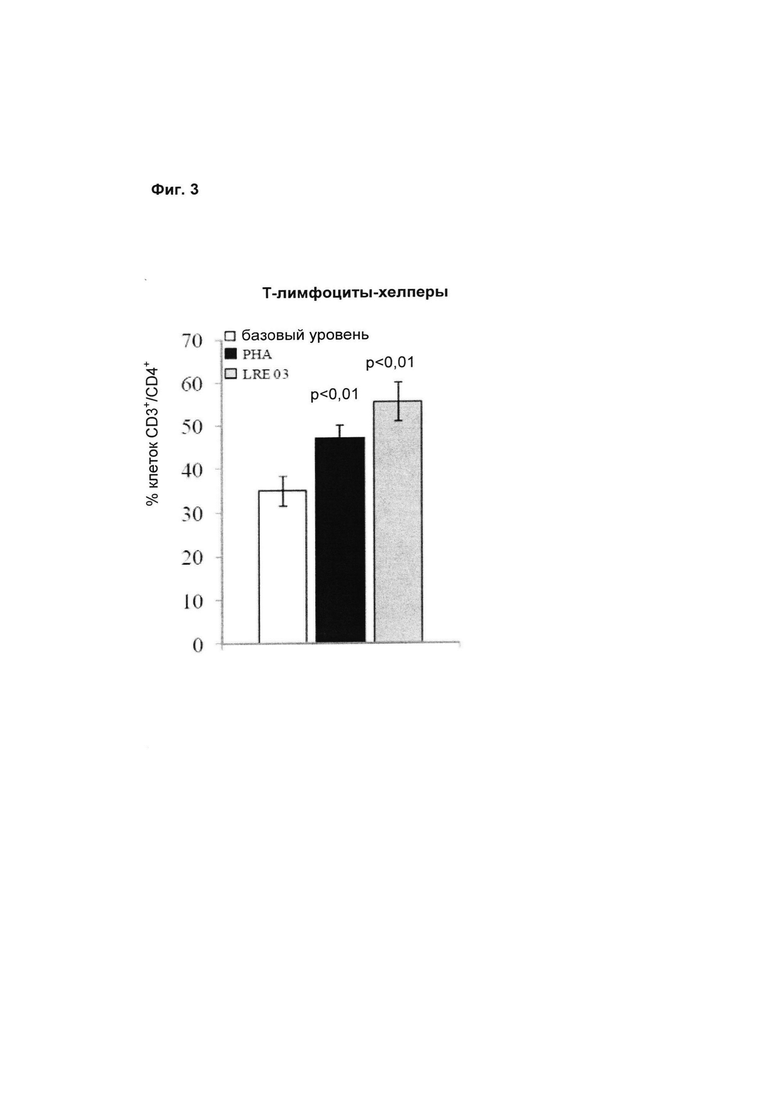
2б) Приобретенный иммунитет. Через пять суток стимуляция бактериальным штаммом Lactobacillus reuteri LRE 03 DSM 23879 вызывала значительное увеличение процентного содержания Т-лимфоцитов-хелперов (CD3+/CD4).
На Фиг. 3 показано среднее ± S.E.M. по результатам 12 независимых экспериментов. Статистическую значимость рассчитывали с использованием t-критерия Стьюдента. Величины р менее 0,05 следует рассматривать как статистически значимые по сравнению с базовыми условиями (нестимулированные РВМС).
3) Секреция цитокинов. Различный спектр цитокинов, секретируемых субпопуляциями клеток, вовлеченных в иммунные ответы, играет основную роль в выборе эффекторной системы для использования в ответ на специфический антигенный стимул. Т-лимфоциты представляют собой главные эффекторные и регуляторные клетки клеточного иммунитета. В ответ на антиген или патогенный агент Т-клетки синтезируют и секретируют разнообразные цитокины, требуемые для роста и дифференцировки и в качестве активирующих факторов для других иммунокомпетентных клеток. Для исследования, будет ли тестируемый бактериальный штамм индуцировать секрецию РВМС различных цитокинов, указанные клетки активировали в течение 1 и 5 суток. Количество цитокинов (IL-12р70, IFN-γ и IL-4), высвобождаемых в культуральные супернатанты, измеряли путем анализа E.LI.S.A.
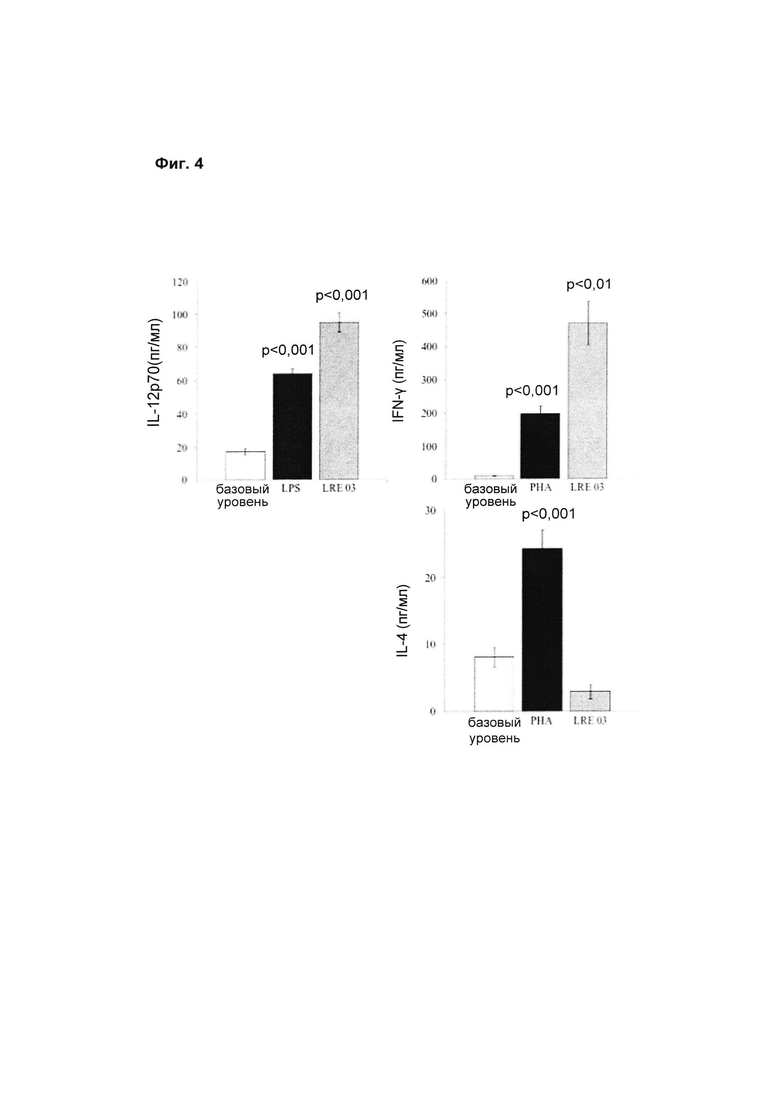
4) Цитокины с преимущественно провоспалительным действием. Оценивали индукцию цитокинов IL-12p70 и IFN-γ как основных представителей цитокинов с преимущественно провоспалительным действием. Как показано на Фиг. 4, бактериальный штамм Lactobacillus reuteri LRE 03 (DSM 23879) способен индуцировать значительное увеличение уровня обоих тестируемых цитокинов относительно базовых условий.
5) Цитокины с преимущественно иммунорегуляторным действием. Оценивали индукцию цитокинов IL-4 как основных представителей цитокинов с преимущественно иммунорегуляторным действием. Как показано на Фиг. 4, тестируемый бактериальный штамм Lactobacillus reuteri LRE 03 (DSM 23879) продемонстрировал способность вызывать снижение секреции цитокина IL-4 относительно базовых условий.
На Фиг. 4 показано среднее ± S.E.M. по результатам 4 независимых экспериментов. Статистическую значимость рассчитывали с помощью t-критерия Стьюдента. Величины р менее 0,05 следует рассматривать как статистически значимые по сравнению с базовым уровнем (нестимулированные РВМС). Продукцию цитокинов IL-12p70 оценивали в культуральных супернатантах через 1 сутки стимуляции. Продукцию IFN-γ и IL-4 оценивали в культуральных супернатантах через 5 суток стимуляции.
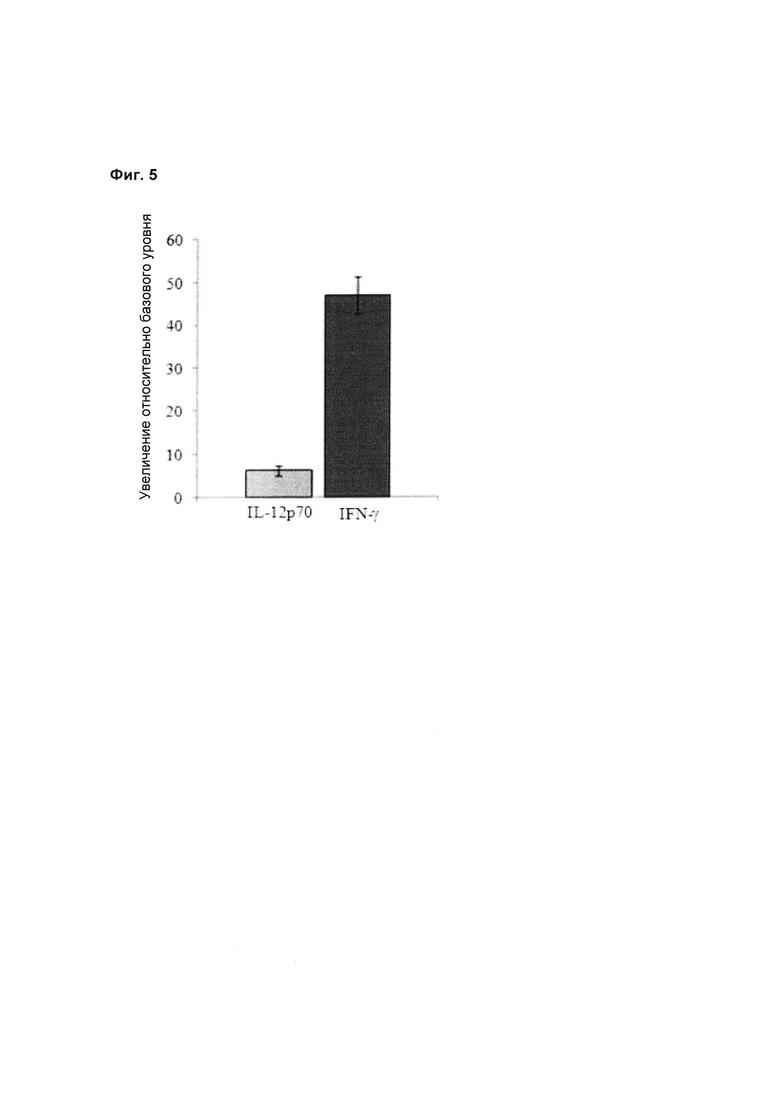
Данные относительно дозировки цитокинов, секретируемых РВМС в результате стимуляции бактериальным штаммом Lactobacillus reuteri LRE 03 DSM 23879, подтвердили способность самого штамма существенно увеличивать уровень провоспалительных цитокинов. Более конкретно, бактериальный штамм Lactobacillus reuteri LRE 03 DSM 23879 увеличивал секрецию цитокина IL-12p70 и цитокина IFN-γ в 6 раз и в 47 раз, соответственно, относительно условий без стимуляции (базовый уровень, Фиг. 5).
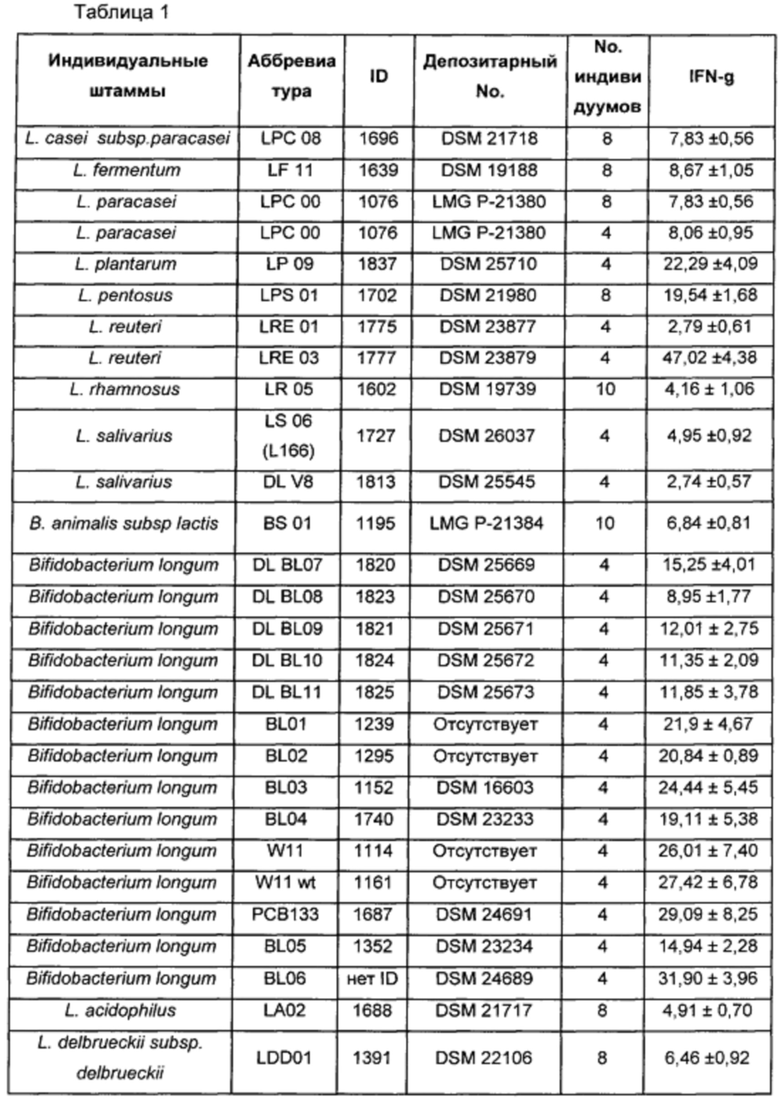
В отношении выраженной способности бактериального штамма Lactobacillus reuteri LRE 03 DSM 23879 стимулировать секрецию цитокина IFN-γ, результаты настоящего изобретения сравнивали с таковыми, полученными в экспериментах на других бактериальных штаммах, которые все принадлежат коллекции Probiotical S.p.A. Более конкретно, сравнивали повышение относительно базового уровня, а именно кратность изменения количества IFN-γ относительно условий без стимуляции (базовый уровень).
Как показано в таблице 1, бактериальный штамм Lactobacillus reuteri LRE 03 (DSM 23879) в результате показал себя наилучшим IFN-γ-индуцирующим агентом по сравнению с обоими штаммами того же самого вида и штаммов различных видов, все из которых принадлежат роду Lactobacillus.
В таблице 1 показано повышение уровня цитокина IFN-γ, индуцированного стимуляцией различными лактобациллами и бифидобактериями по сравнению с базовым уровнем.
Экспериментальная часть
Авторы изобретения протестировали иммуномодулирующие свойства бактериального штамма Lactobacillus salivarius LS 06 DSM 26037 как описано ниже.
Более конкретно, оценивали иммуномодулирующие свойства пробиотического штамма Lactobacillus salivarius LS 06 DSM 26037, ранее охарактеризованного с микробиологической и молекулярной точек зрения, в отношении общего количества циркулирующих дендритных клеток. В частности, после 24 часов стимуляции был проведен многопараметрический анализ проточной цитометрии путем отбора DC (дендритных клеток) из мононуклеарных клеток периферической крови здоровых взрослых доноров.
а) Бактериальные культуры и условия роста
Штамм культивировали в среде Ман-Рогоза-Шарпе (MRS) на термостатируемой бане при 37°С. В отношении экспериментов по иммуномодулированию, после периода роста приблизительно 16 часов бактерии субкультивировали в течение 6 часов в условиях, описанных выше, до достижения экспоненциальной фазы роста. Так, их дважды промывали стерильным фосфатно-солевым буфером (PBS, рН 7,2), физиологический статус и число клеток определяли цитофлуориметрическим методом с использованием набора "Cell Viability Kit with liquid beads", доступного в продаже от Becton Dickinson Company, в соответствии с инструкциями производителя. Затем концентрацию клеток доводили до оптимальной концентрации, установленной в предварительных экспериментах, и использовали в последующих тестах.
б) Отделение мононуклеарных клеток периферической крови
Мононуклеарные клетки периферической крови (РВМС) отделяли путем центрифугирования в градиенте плотности. Для этой цели 20 мл "лейкоцитарной пленки" здоровых доноров из Службы переливания крови (Immuno-transfusion Service) Ospedale di Borgomanero (Italy) использовали в каждом эксперименте, таким образом получая средний выход 200×106 РВМС/лейкоцитарная пленка. Количество отделенных клеток определяли путем подсчета клеток в камере Бюркера с использованием раствора Тюрка, который позволяет различить мононуклеарные клетки и полиморфоядерные клетки. Концентрацию клеток доводили до 2×106 клеток/мл в ростовой среде RPMI-1640 (Invitrogen), дополненной 10% инактивированной нагреванием эмбриональной сыворотки крупного рогатого скота (FCS, Gibco), 1% глутамина и 25 мМ Hepes.
в) Стимуляция РВМС
После отделения РВМС стимулировали бактериальным штаммом в течение 24 часов. Внутренние контроли в каждом эксперименте представляли собой следующее: Отрицательный контроль: только РВМС; 1-суточный контроль: РВМС, стимулированные 1 мкг/мл липополисахарида (LPS; Escherichia coli, серотип 055:В5, Sigma Chemicals Co., St. Louis, MO).
После стимуляции культуры центрифугировали при 1500 об/мин в течение 10 минут. Затем супернатант отбрасывали и клетки использовали в последующих тестах.
г) Общий анализ дендритных клеток
В отношении иммунофенотипической характеристики, клетки инкубировали в течение 30 минут в темноте с различными комбинациями следующих моноклональных антител (mAb), коньюгированных с флуоресцеинизотиоцианатом (FITC) или перидинин-хлорофилл протеином (PerCP): CD3, CD14, CD16, CD19, CD20, CD56 и HLA-DR. После инкубирования образцы промывали, фиксировали раствором, содержащим 1% параформальдегида, и хранили при 4°С. В пределах 24 часов после получения образцы анализировали с помощью цитофлуориметра FACScalibur, при этом клетки выбирали так, чтобы исключить из анализа примеси остатков разрушенных клеток.
д) Статистический анализ
Статистический анализ выполняли с использованием двустороннего парного t-критерия Стьюдента. Величину р менее 0,05 считали значимой.
Результаты: Действие бактериального штамма на дендритные клетки
Для определения действия тестируемого пробиотического штамма на модулирование дендритных клеток проводили многопараметрический анализ проточной цитометрии.
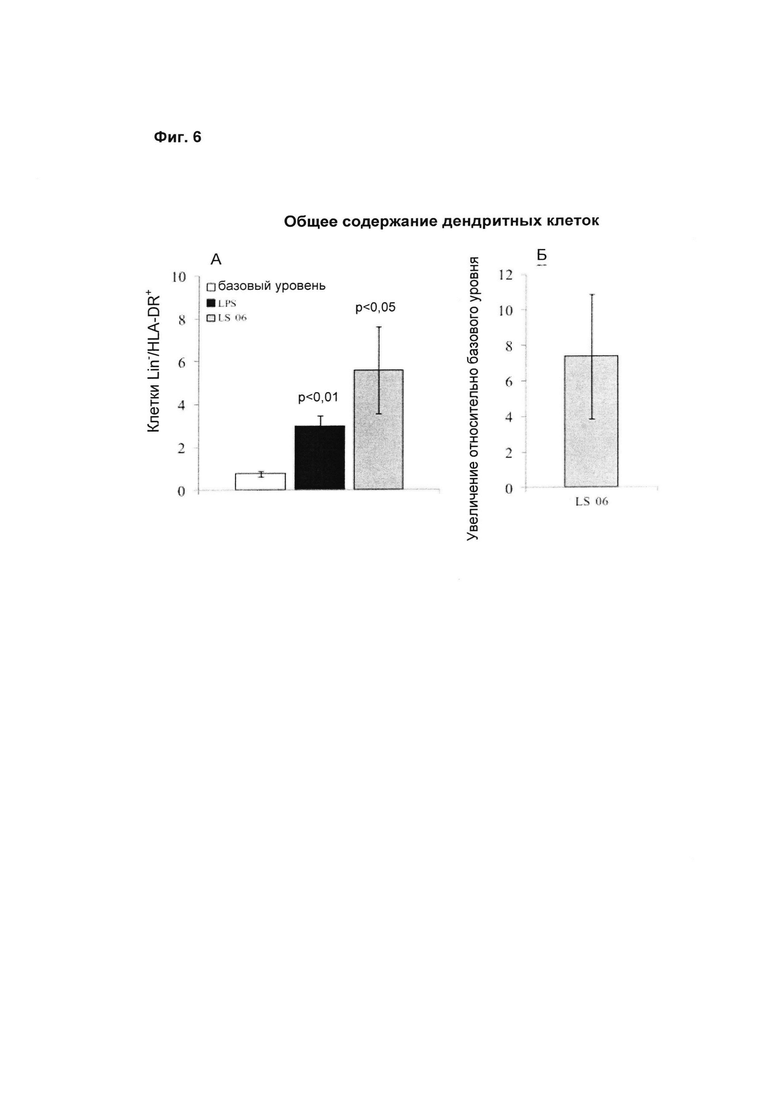
Как показано на Фиг. 6А, через 24 часа стимуляция штаммом LS 06 индуцировала значительное увеличение общего процентного содержания дендритных клеток (Линия-/HLA-DR+).
Более конкретно, бактериальный штамм L salivarius LS 06 (DSM 26037) увеличивал общее процентное содержание дендритных клеток в 7 раз относительно условий без стимуляции (базовый уровень, Фиг. 6Б).
На Фиг. 6Б показано среднее ± S.E.M. по результатам 12 независимых экспериментов. Статистическую значимость рассчитывали с использованием t-критерия Стьюдента. Величины р менее 0,05 следует рассматривать как статистически значимые по сравнению с базовым уровнем (нестимулированные РВМС).
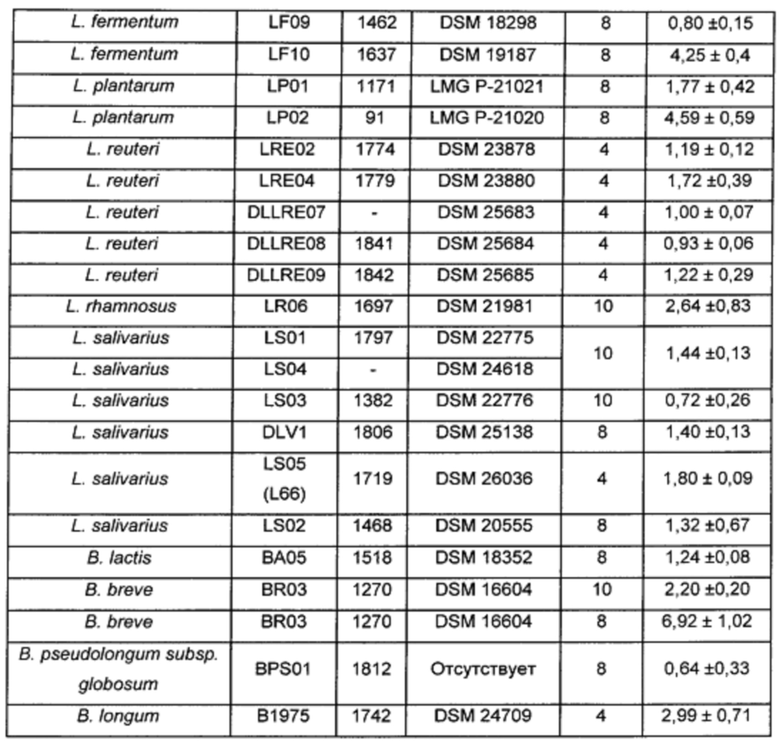
В таблице 2 показано увеличение количества дендритных клеток, индуцированное стимуляцией различными лактобациллами и бифидобактериями, относительно базового уровня.
Заключение
Данные продемонстрировали, что бактериальный штамм L. salivarius LS 06 индуцировал значительное повышение общего процентного содержания DC относительно стандартных базовых условий. В частности, бактерия LS 06 увеличивала в 7 раз общее процентное содержание DC.
Колонизация кишечника бактериями, способными модулировать дендритные клетки, такими как штамм L. salivarius LS 06, охарактеризованный в настоящем исследовании, представляет собой очень важный фактор при заболеваниях, характеризуемых иммунологическим дисбалансом.
Изобретение относится к фармацевтической промышленности, а именно к применению композиции в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов. Применение композиции, содержащей смесь, состоящую из: штамма бактерий, принадлежащих виду Lactobacillus reuteri, идентифицированного как Lactobacillus reuteri LRE03, с депозитарным номером DSM 23879 и/или штамма бактерий, принадлежащих виду Lactobacillus salivarius, идентифицированного как Lactobacillus salivarius LS06, в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов. Вышеописанная композиция стимулирует продукцию провоспалительных цитокинов (Тh1) интерферона INF-гамма, причем указанные цитокины проявляют выраженную противовирусную и/или противобактериальную активность, стимулировать продукцию дендритных клеток, причем указанные дендритные клетки также проявляют выраженную противовирусную и/или противобактериальную активность. 9 з.п. ф-лы, 2 табл., 6 ил.
1. Применение композиции, содержащей смесь, состоящую из:
- штамма бактерий, принадлежащих виду Lactobacillus reuteri, идентифицированного как Lactobacillus reuteri LRE03, с депозитарным номером DSM 23879, депонированного 05.08.2010 Probiotical SpA в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH), и/или
- штамма бактерий, принадлежащих виду Lactobacillus salivarius, идентифицированного как Lactobacillus salivarius LS06, с депозитарным номером DSM 26037, депонированного 06.06.2012 Probiotical SpA в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH),
в качестве противовирусного и/или противобактериального агента у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
2. Применение по п. 1, где указанная композиция состоит из смеси, дополнительно содержащей:
- штамм бактерий, принадлежащих виду Lactobacillus fermentum, идентифицированный как Lactobacillus fermentum LF11, с депозитарным номером DSM 19188, депонированный 20.03.2007 Anidral S.r.l. Company (в настоящее время Probiotical S.p.A) в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ GmbH).
3. Применение по п. 1 или 2, где указанная композиция содержит смесь с концентрацией бактерий от 1×108 колониеобразующих единиц (КОЕ)/г смеси до 1×1012 КОЕ/г смеси, предпочтительно от 1×109 КОЕ/г смеси до 1×1011 КОЕ/г смеси.
4. Применение по п. 3, где указанная смесь содержит или, альтернативно, состоит из:
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus salivarius LS06 DSM 26037 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1, или - штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188 в массовом соотношении от 1:5 до 5:1, предпочтительно от 1:3 до 3:1, еще более предпочтительно от 1:2 до 2:1 или 1:1.
5. Применение по п. 3, где указанная смесь содержит или, альтернативно, состоит из:
- штамма бактерий Lactobacillus reuteri LRE03 DSM 23879, штамма бактерий Lactobacillus salivarius LS06 DSM 26037 и штамма бактерий Lactobacillus fermentum LF11 DSM 19188, в массовом соотношении, выбранном из 3:2:1, 3:1:1, 2:1:1, 2:2:1 и 1:1:1.
6. Применение по любому из пп. 1-5, где указанная композиция дополнительно содержит штамм бактерий, принадлежащих виду Streptococcus thermophilus, идентифицированный как Streptococcus thermophilus ST10 DSM 25246, и камедь тары, где указанный штамм при введении способен продуцировать экзополисахариды in situ.
7. Применение по любому из пп. 1-6, где указанная композиция дополнительно содержит камедь, предпочтительно альгинат или его производное, еще более предпочтительно альгинат натрия.
8. Применение по любому из пп. 1-7, где указанная композиция дополнительно содержит гель Aloe или его производное, предпочтительно гель Aloe arborescens, причем еще более предпочтительно гель представляет собой лиофилизированный гель Aloe arborescens.
9. Применение по любому из пп. 1-8, где указанная композиция дополнительно содержит штамм бактерий, принадлежащих виду Bifidobacterium lactic, идентифицированный как Bifidobacterium lactic Bb 1, с депозитарным номером DSM 17850, депонированный в DSMZ 23.12.2005 BioMan S.r.l. Company, где указанный штамм обладает способностью аккумулировать цинк внутри клетки во время его роста в жидкой культуральной среде.
10. Применение по любому из пп. 1-9 для защиты слизистых желудка, пищевода и кишечника у индивидуумов, проходящих противоопухолевое химиотерапевтическое лечение, лечение синдрома приобретенного иммунодефицита и лечение лейкозов.
| WO2013084052 A1, 13.06.2013 | |||
| US2010143305 A1, 10.06.2010 | |||
| US6103227 A, 15.08.2000 | |||
| KR20100049827 A, 13.05.2010. |
Авторы
Даты
2020-02-05—Публикация
2015-04-30—Подача