ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Для настоящей заявки испрашивается приоритет на основании предварительной заявки на патент США № 62/022,392, поданной 9 июля 2014 г., которая полностью включена в настоящий документ путем ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам замораживания клеток (таких как клетки млекопитающего) для хранения в банке, и к среде для замораживания для применения в замораживании клеток.
УРОВЕНЬ ТЕХНИКИ
Банки клеток получают следующим образом: сначала нарабатывают клетки в периодических/перфузионных культурах клеток, а затем собирают клетки для хранения в банке. Способ включает три стадии: наработку клеток, сбор и концентрирование клеток и хранение клеток в банке. Этап сбора в этом процессе служит для концентрирования конечной жидкой культуры клеток с использованием центрифугирования. Последующий процесс объединения в пула и заполнения служит для получения ампул банка клеток для длительного хранения.
Эти традиционные способы могут давать нестабильную или низкую жизнеспособность клеток для некоторых клеточных линий после размораживания. Для хранения клеток в банке обязательна высокая жизнеспособность клеток после размораживания замороженных клеток. Соответственно, существует потребность в улучшенных способах замораживания клеток для хранения клеток в банке. Была бы полезна среда для культур клеток для замораживания клеток, которая обеспечивает повышенную жизнеспособность клеток после хранения в банке.
Все публикации, патенты и заявки на патенты, цитируемые в настоящем документе, включены в него посредством ссылки полностью и для любых целей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте настоящего документа предложен способ улучшения размораживания банков клеток, включающий замораживание эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения в банке в среде для замораживания, причем среда для замораживания содержит буферный раствор и криопротектор, и при этом рН среды для замораживания равен от приблизительно 6,7 до приблизительно 8,5 перед замораживанием или откорректирован до pH от приблизительно 6,7 до приблизительно 8,5 перед замораживанием.
В другом аспекте предложен способ замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения, включающий замораживание клеток в среде для замораживания, причем среда для замораживания содержит буферный раствор и криопротектор, и при этом рН среды для замораживания равен от приблизительно 6,7 до приблизительно 8,5 перед замораживанием или откорректирован до pH от приблизительно 6,7 до приблизительно 8,5 перед замораживанием.
В некоторых вариантах реализации способов, описанных выше или здесь, рН среды для замораживания равен от приблизительно 6,7 до приблизительно 8,3, от приблизительно 6,8 до приблизительно 8,3, от приблизительно 6,9 до приблизительно 8,3, от приблизительно 7.0 до приблизительно 8,3, от приблизительно 7,1 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8,3, от приблизительно 7,3 до приблизительно 8,3, от приблизительно 7,4 до приблизительно 8,3, от приблизительно 7,5 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8.0, от приблизительно 7,2 до приблизительно 7,8 или приблизительно 7,5 перед замораживанием.
В некоторых вариантах реализации способов, описанных выше или здесь, pH среды для замораживания откорректирован до значения pH от приблизительно 6,7 до приблизительно 8,5, от приблизительно 6,7 до приблизительно 8,3, от приблизительно 6,8 до приблизительно 8,3, от приблизительно 6,9 до приблизительно 8,3, от приблизительно 7.0 до приблизительно 8,3, от приблизительно 7,1 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8,3, от приблизительно 7,3 до приблизительно 8,3, от приблизительно 7,4 до приблизительно 8,3, от приблизительно 7,5 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8.0, от приблизительно 7,2 до приблизительно 7,8, или приблизительно равного 7,5. В некоторых вариантах реализации способов, описанных выше или здесь, клетки (например, клетки млекопитающего или клетки насекомого) объединяют со средой для замораживания перед и/или после корректировки pH. В некоторых вариантах реализации откорректированный pH представляет собой целевой pH или измеренный pH. В некоторых вариантах реализации целевой pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации измеренный pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации способов, описанных выше или здесь, способ дополнительно включает этап измерения исходного pH среды для замораживания, содержащей клетки (например, клетки млекопитающего или клетки насекомого), перед корректировкой pH среды для замораживания. В некоторых вариантах реализации способов, описанных выше или здесь, способ дополнительно включает этап измерения откорректированного pH среды для замораживания. В некоторых вариантах реализации способов, описанных выше или здесь, если измеренный pH среды для замораживания ниже целевого pH, способ включает повторение этапа корректировки и этапа измерения до достижения откорректированного pH среды для замораживания, равного от приблизительно 6,7 до приблизительно 8,5, или равного любому значению pH, описанному в настоящем тексте, или значению в любом диапазоне pH, описанном в настоящем тексте.
В некоторых вариантах реализации способов, описанных в настоящем документе или выше, pH корректируют путем добавления основания. В некоторых вариантах реализации основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновой кислоты), гидроксида натрия и гидроксида калия. В некоторых вариантах реализации pH среды для замораживания корректируют путем добавления основания в среду для замораживания в соответствии со следующей формулой Vbase=Cbase*Vp (pHt - pHi), где Cbase представляет собой коэффициент, значение которого зависит от основания, Vbase представляет собой объем основания, добавляемый в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации pH среды для замораживания корректируют путем добавления карбоната натрия в среду для замораживания в соответствии со следующей формулой 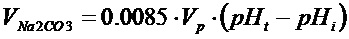 , где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации целевой pH представляет собой pH от приблизительно 6,7 до приблизительно 8,5, приблизительно 7,2 до приблизительно 8,3, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации целевой pH составляет 7,5.
, где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации целевой pH представляет собой pH от приблизительно 6,7 до приблизительно 8,5, приблизительно 7,2 до приблизительно 8,3, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации целевой pH составляет 7,5.
В некоторых вариантах реализации способов, описанных выше или здесь, клетки (например, клетки млекопитающего или клетки насекомого) находятся в среде, pH которой равен приблизительно 6,2 до приблизительно 6,6 перед объединением клеток со средой для замораживания.
В некоторых вариантах реализации способов, описанных выше или здесь, криопротектор представляет собой ДМСО(диметилсульфоксид), глицерин, пропандиол, этиленгликоль, макромолекулу, сахар или их комбинацию. В некоторых вариантах реализации концентрация ДМСО или глицерина в среде для замораживания перед замораживанием составляет приблизительно 5% до приблизительно 12,5% по объему. В некоторых вариантах реализации концентрация ДМСО или глицерина в среде для замораживания перед замораживанием клеток (например, клеток млекопитающего или клеток насекомого) составляет от приблизительно 5% до приблизительно 10% по объему.
В некоторых вариантах реализации способов, описанных выше или здесь, среда для замораживания, содержащая клетки (например, клетки млекопитающего или клетки насекомого), имеет плотность клеток, определенную как объем осажденных клеток (ООК), равную от приблизительно 8% до приблизительно 28% перед замораживанием.
В некоторых вариантах реализации способа, описанного выше или здесь, способ дополнительно включает этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток (например, клеток млекопитающего или клеток насекомого) со средой для замораживания. В некоторых вариантах реализации жидкую культуру клеток охлаждают до температуры, равной или более низкой чем приблизительно 20oC. В некоторых вариантах реализации жидкую культуру клеток охлаждают до температуры, равной или более низкой чем приблизительно 10oC.
В другом аспекте настоящего описания предложен способ замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения или улучшения размораживания банков клеток, включающий (a) корректировку pH среды для замораживания, содержащей клетки, до pH от приблизительно 6,7 до приблизительно 8,5, причем среда для замораживания содержит буферный раствор и криопротектор, и (b) замораживание клеток.
В некоторых вариантах реализации pH корректируют до значения pH от приблизительно 6,7 до приблизительно 8,3, от приблизительно 6,8 до приблизительно 8,3, от приблизительно 6,9 до приблизительно 8,3, от приблизительно 7.0 до приблизительно 8,3, от приблизительно 7,1 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8,3, от приблизительно 7,3 до приблизительно 8,3, от приблизительно 7,4 до приблизительно 8,3, от приблизительно 7,5 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8.0, от приблизительно 7,2 до приблизительно 7,8 или до значения, приблизительно равного 7,5. В некоторых вариантах реализации откорректированный pH представляет собой целевой pH или измеренный pH. В некоторых вариантах реализации целевой pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации целевой pH равен приблизительно 7,5. В некоторых вариантах реализации измеренный pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте.
В некоторых вариантах реализации способов, описанных выше или здесь, способ дополнительно включает этап измерения исходного pH среды для замораживания, содержащей клетки, (например, клетки млекопитающего или клетки насекомого) перед корректировкой pH среды для замораживания. В некоторых вариантах реализации способ дополнительно включает этап измерения откорректированного pH среды для замораживания. В некоторых вариантах реализации, если измеренный pH среды для замораживания ниже целевого pH, способ включает повторение этапа корректировки и этапа измерения до достижения откорректированного pH среды для замораживания, равного от приблизительно 6,7 до приблизительно 8,5, от приблизительно 7,2 до приблизительно 8,3, или любому значению pH, описанному в настоящем тексте, или значению в любом диапазоне pH, описанном в настоящем тексте.
В некоторых вариантах реализации способов, описанных выше или здесь, pH корректируют путем добавления основания. В некоторых вариантах реализации основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксида натрия и гидроксида калия. В некоторых вариантах реализации pH среды для замораживания корректируют путем добавления основания в среду для замораживания в соответствии со следующей формулой Vbase=Cbase*Vp (pHt - pHi), где Cbase представляет собой коэффициент, значение которого зависит от основания, Vbase представляет собой объем основания, добавляемый в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации pH среды для замораживания корректируют путем добавления карбоната натрия в среду для замораживания в соответствии со следующей формулой 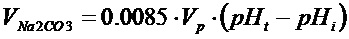 , где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации целевой pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации целевой pH приблизительно равен 7,5.
, где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В некоторых вариантах реализации целевой pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации целевой pH приблизительно равен 7,5.
В некоторых вариантах реализации клетки (например, клетки млекопитающего или клетки насекомого) находятся в среде с pH от приблизительно 6,2 до приблизительно 6,6 перед объединением клеток со средой для замораживания.
В некоторых вариантах реализации криопротектор в среде для замораживания представляет собой ДМСО, глицерин, пропандиол, этиленгликоль, макромолекулу, сахар или их комбинацию. В некоторых вариантах реализации концентрация ДМСО или глицерина в среде для замораживания, содержащей клетки (например, клетки млекопитающего или клетки насекомого), перед замораживанием составляет приблизительно 5% до приблизительно 12,5% по объему. В некоторых вариантах реализации концентрация ДМСО или глицерина в среде для замораживания, содержащей клетки (например, клетки млекопитающего или клетки насекомого), перед замораживанием клетки равна от приблизительно 5% до приблизительно 10% по объему.
В некоторых вариантах реализации среда для замораживания, содержащая клетки (например, клетки млекопитающего или клетки насекомого), имеет плотность клеток, определенную как объем осажденных клеток (ООК), от приблизительно 8% до приблизительно 28% перед замораживанием.
В некоторых вариантах реализации способ дополнительно включает этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток (например, клеток млекопитающего ил клеток насекомого) со средой для замораживания. В некоторых вариантах реализации жидкую культуру клеток охлаждают до температуры, равной или более низкой чем приблизительно 20oC, или равной или более низкой чем приблизительно 10oC.
В другом аспекте предложен способ замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения или улучшения размораживания банков клеток, включающий (a) корректировку pH среды для замораживания до pH от приблизительно 6,7 до приблизительно 8,5, причем среда для замораживания содержит буферный раствор и криопротектор; (b) объединение клеток со средой для замораживания с получением пула клеток; и (c) замораживание клеток в пуле клеток.
В некоторых вариантах реализации pH корректируют до значения pH от приблизительно 6,7 до приблизительно 8,3, от приблизительно 6,8 до приблизительно 8,3, приблизительно 6,9 до приблизительно 8,3, от приблизительно 7.0 до приблизительно 8,3, приблизительно 7,1 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8,3, приблизительно 7,3 до приблизительно 8,3, от приблизительно 7,4 до приблизительно 8,3, приблизительно 7,5 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8.0, от приблизительно 7,2 до приблизительно 7,8, или приблизительно 7,5. В некоторых вариантах реализации откорректированный pH представляет собой целевой pH или измеренный pH. В некоторых вариантах реализации целевой pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте. В некоторых вариантах реализации измеренный pH равен от приблизительно 6,7 до приблизительно 8,5, или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте.
В некоторых вариантах реализации способ дополнительно включает этап измерения откорректированного pH среды для замораживания. В некоторых вариантах реализации если измеренный pH среды для замораживания ниже целевого pH, способ дополнительно включает повторение этапа корректировки и этапа измерения до достижения откорректированного pH среды для замораживания, равного от приблизительно 6,7 до приблизительно 8,5, или любому значению pH, описанному в настоящем тексте, или в любом диапазоне pH, описанном в настоящем тексте.
В некоторых вариантах реализации способов, описанных выше или здесь, pH корректируют путем добавления основания. В некоторых вариантах реализации основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксида натрия и гидроксида калия.
В некоторых вариантах реализации способов, описанных выше или здесь, клетки (например, клетки млекопитающего или клетки насекомого) находятся в среде с pH, равным от приблизительно 6,2 до приблизительно 6,6, перед объединением клеток со средой для замораживания.
В некоторых вариантов реализации способов, описанных выше или в настоящем документе, криопротектор в среде для замораживания представляет собой ДМСО, глицерин, пропандиол, этиленгликоль, макромолекулу, сахар или их комбинацию. В некоторых вариантах реализации концентрация ДМСО или глицерина в пуле клеток составляет от приблизительно 5% до приблизительно 12,5% по объему, или от приблизительно 5% до приблизительно 10% по объему.
В некоторых вариантах реализации способов, описанных выше или здесь, пул клеток содержит клетки (например, клетки млекопитающего или клетки насекомого) при плотности клеток, определенную как объем осажденных клеток, от приблизительно 8% до приблизительно 28% (ООК).
В некоторых вариантах реализации способов, описанных выше или здесь, способ дополнительно включает этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток (например, клеток млекопитающего или клеток насекомого) со средой для замораживания. В некоторых вариантах реализации жидкую культуру клеток охлаждают до температуры, равной или более низкой чем приблизительно 20oC. В некоторых вариантах реализации жидкую культуру клеток охлаждают до температуры, равной или более низкой чем приблизительно 10oC.
В некоторых вариантах реализации способов, описанных выше или здесь, клетки представляют собой клетки млекопитающего, такие как клетки яичника китайского хомячка (CHO), клетки миеломы мыши NS0, клетки человека PER.C6® или гибридомы. В некоторых вариантах реализации клетки представляют собой клетки насекомого, такие как High FiveTM, S2 (Schneider 2), Sf9 и Sf21. В некоторых вариантах реализации способов, описанных выше или здесь, клетки (например, клетки млекопитающего или клетки насекомого) содержат нуклеиновую кислоту, кодирующую полипептид. В некоторых вариантах реализации полипептид представляет собой терапевтический белок. В некоторых вариантах реализации терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
В другом аспекте предложен пул эукариотических клеток (например, пул клеток млекопитающего или пул клеток насекомого) для замораживания клеток, содержащий буферный раствор, криопротектор и эукариотические клетки, содержащие нуклеиновую кислоту, кодирующую полипептид, причем pH среды равен от приблизительно 6,7 до приблизительно 8,5 или от приблизительно 7,2 до приблизительно 8,3 (или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте) перед замораживанием клеток. В некоторых вариантах реализации клетки представляют собой клетки млекопитающего, такие как клетки яичника китайского хомячка (CHO), клетки миеломы мыши NS0, клетки человека PER.C6® или гибридомы. В некоторых вариантах реализации клетки представляют собой клетки насекомого, такие как High FiveTM, S2 (Schneider 2), Sf9 и Sf21. В некоторых вариантах реализации клетки (например, клетки млекопитающего или клетки насекомого) содержат нуклеиновую кислоту, кодирующую полипептид. В некоторых вариантах реализации полипептид представляет собой терапевтический белок. В некоторых вариантах реализации терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
В другом аспекте предложен банк клеток, содержащий множество контейнеров, причем каждый контейнер содержит (a) среду для замораживания, содержащую буфер и криопротектор, и (b) эукариотические клетки (например, клетки млекопитающего или клетки насекомого), содержащие нуклеиновую кислоту, кодирующую полипептид, причем рН среды для замораживания равен от приблизительно 6,7 до приблизительно 8,5 или от приблизительно 7,2 до приблизительно 8,3 (или равен любому значению pH, описанному в настоящем тексте, или лежит в любом диапазоне pH, описанном в настоящем тексте) перед замораживанием клеток. В некоторых вариантах реализации контейнеры представляют собой ампулы. В некоторых вариантах реализации клетки представляют собой клетки млекопитающего, такие как клетки яичника китайского хомячка (CHO), клетки миеломы мыши NS0, клетки человека PER.C6® или гибридомы. В некоторых вариантах реализации клетки представляют собой клетки насекомого, такие как High FiveTM, S2 (Schneider 2), Sf9 и Sf21. В некоторых вариантах реализации клетки (например, клетки млекопитающего или клетки насекомого) содержат нуклеиновую кислоту, кодирующую полипептид. В некоторых вариантах реализации полипептид представляет собой терапевтический белок. В некоторых вариантах реализации терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
Следует понимать, что одно, несколько или все свойства различных вариантов изобретения, описанных в настоящем документе, могут быть объединены с получением других вариантов изобретения согласно настоящему изобретению. Эти и другие аспекты настоящего изобретения будут ясны специалисту в данной области.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 показан пример схемы технологического процесса создания банка клеток.
На Фигурах 2A-2B показаны результаты определения жизнеспособности клеток в пассаже после размораживания в день 1 (ФИГ. 2A) и роста день 4 (ООК) (ФИГ. 2B) для банков клеток, полученных из пулов с откорректированным pH при начальном pH, равном 6,6 или 6,3.
На Фигурах 3A-3F показаны результаты определения жизнеспособности клеток в пассаже после размораживания в день 1 (ФИГ. 3A, 3C и 3E) и общая скорость роста клеток, определенная по ООК (ФИГ. 3B, 3D и 3F), в зависимости от pH в банке и влияние корректировки pH до целевого pH в определенном диапазоне на девяти линиях клеток CHO, продуцирующих разные антитела (антитела 1-9).
На Фигурах 4A-4B показана динамика плотности жизнеспособных клеток (ПЖК) или числа жизнеспособных клеток (ЧЖК) в пассаже после размораживания (ФИГ. 4A) и их жизнеспособность (%) (ФИГ. 4B), которые демонстрируют влияние корректировки pH до 7,5 от начального значения в пуле pH, равного 6,3, в сравнении с корректировкой pH.
На ФИГ. 5 показано отношение объема осажденных жизнеспособных клеток (ООЖК) к числу жизнеспособных клеток (ЧЖК), которое представляет собой средство непрямой оценки размера клеток, в процессе объединения клеток в пул. Эти данные демонстрирую влияние добавления среды для замораживания (FM) и корректировки pH до pH 7,3, 7,6 или 8.0 на объем клеток. Более высокое отношение указывает на больший объем клеток.
На Фигурах. 6A-6B показан общий рост клеток в пассаже после размораживания, определенный по ООК, для банков клеток, полученных из пула с откорректированным pH, при начальном значении pH 6,4 (целевое 6,2) или 6,6 (целевое 6,7) в момент времени t0 (ФИГ. 6A) и t2 (2 ч) (ФИГ. 6B).
ПОДРОБНОЕ ОПИСАНИЕ
Предложены способы улучшения размораживания банков клеток, включающие замораживание эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения в банке в среде для замораживания, причем среда для замораживания содержит буферный раствор и криопротектор, и при этом рН среды для замораживания равен приблизительно 6,7 до приблизительно 8,5 перед замораживанием.
Также предложены способы замораживания эукариотических клеток (например, клетки млекопитающего, клетки насекомого и т.д.) для хранения, включающие замораживание клеток в среде для замораживания, причем среда для замораживания содержит буферный раствор и криопротектор, и при этом рН среды для замораживания равен приблизительно 6,7 до приблизительно 8,5 перед замораживанием.
Также предложены способы замораживания эукариотических клеток (например, клетки млекопитающего, клетки насекомого и т.д.) для хранения или улучшения размораживания банков клеток, включающий (a) корректировку pH среды для замораживания, содержащей клетки, до pH от приблизительно 6,7 до приблизительно 8,5, причем среда для замораживания содержит буферный раствор и криопротектор; и (b) замораживание клеток.
Также предложены способы замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.) для хранения или улучшения размораживания банков клеток, включающие (a) корректировку pH среды для замораживания до pH от приблизительно 6,7 до приблизительно 8,5, причем среда для замораживания содержит буферный раствор и криопротектор; (b) объединение клеток со средой для замораживания с получением пула клеток; и (c) замораживание клеток в пуле клеток.
Также в настоящем документе предложены пулы эукариотических клеток для замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.), содержащие буферный раствор, криопротектор и эукариотические клетки, содержащие нуклеиновую кислоту, кодирующую полипептид, причем pH среды равен от приблизительно 6,7 до приблизительно 8,5 перед замораживанием клеток.
Также в настоящем документе предложены балки клеток, содержащие множество контейнеров, причем каждый контейнер содержит (a) среду для замораживания, содержащую буфер и криопротектор, и (b) эукариотические клетки (например, клетки млекопитающего, клетки насекомого и т.д.), содержащие нуклеиновую кислоту, кодирующую полипептид, причем рН среды для замораживания равен от приблизительно 6,7 до приблизительно 8,5 перед замораживанием клеток.
I. Определения
Термины «среда» и «среда для культивирования клеток» относятся к раствору, применяемому для поддержания клеток. Среда может дополнительно содержать источник питательных веществ, применяемый для выращивания клеток. Специалисту в данной области понятно, что источник питательных веществ может содержать компоненты, необходимые клеткам для роста и/или выживания, или может содержать компоненты, которые способствуют росту и/или выживанию клеток. Витамины, незаменимые аминокислоты или аминокислоты, не относящиеся к незаменимым, и микроэлементы являются примерами компонентов среды.
«Основная питательная среда» относится к среде, содержащей основные питательные вещества, необходимые для роста и выживания клеток. Примеры основной питательной среды включают минимальную поддерживающую среду Игла (EMEM) и минимальную поддерживающую среду, модифицированную методом Дульбекко(DMEM).
«Химически определенная среда для культивирования клеток» или «CDM» (СОС) представляет собой среду с определенным составом, не содержащую продуктов растительного или животного происхождения, таких как, например, сыворотка крови животного или растительный пептон. Как это понятно для специалиста в данной области, среда определенного состава может применяться в способе получения белка, в котором клетка находится в контакте с СОС и секретирует в нее белок. Соответственно, предполагается, что композиция может содержать СОС и полипептидный продукт, и что присутствие полипептида не делает СОС химически неопределенной.
«Химически неопределенная среда для культивирования клеток» относится к среде, химический состав которой не может быть определен, и которая может содержать один или больше продуктов животного или растительного происхождения, например, сыворотку крови животного или растительный пептон. Как это понятно специалисту в данной области, химически неопределенная среда для культивирования клеток может содержать продукт растительного или животного происхождения в качестве источника питательных веществ.
«Среда для замораживания», «среда для замораживания клеток» «среда для культивирования клеток для замораживания» (клеточная культуральная среда для замораживания) относится к буферному раствору, содержащему криопротектор. Среду для замораживания можно применять для замораживания клеток (например, клеток млекопитающего или клеток насекомого), содержащихся в среде для замораживания. «Буферный раствор» в настоящем тексте относится к изотоническому водному pH-буферному солевому раствору, который обеспечивает поддержание целостности клеточной мембраны и служит носителем для одного или более криопротекторов. Среда для замораживания может также содержать дополнительные компоненты, присутствующие в среде для культивирования клеток. Примеры буферов могут включать бикарбонатный буфер, ФБР (фосфатный буферный раствор), HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновую кислоту), MOPS (3-(N-морфолинo)пропансульфоновую кислоту), TES (N-[трис(гидроксиметил)метил]-2-аминоэтансульфоновую кислоту), TRIS (трис(гидроксиметил)аминометан), TEST (комбинация TES/TRIS) и их комбинации. Примеры среды могут включать минимальную поддерживающую среду Игла (EMEM) и минимальную поддерживающую среду, модифицированную методом Дульбекко (DMEM). Криопротекторы защищают клетки от повреждения при замораживании и могут быть разделены на «проникающие», т.к. способные пересекать плазматическую мембрану (например, глицерин, диметилсульфоксид (ДМСО), пропандиол, этиленгликоль и т.д.) и «непроникающие» (например, макромолекулы, сахара и т.д.).
«Культивирование» клетки относится к приведению клетки в контакт с культуральной средой в условиях, подходящих для выживания, и/или роста и/или пролиферации клеток.
«Периодическая культура» относится к культуре, в которой все компоненты для культивирования клеток (включая клетки и все питательные вещества для культивирования) помещают в культуральный сосуд в начале процесса культивирования.
Фраза «периодическая культура клеток с подпиткой» в настоящем документе относится к периодической культуре, в которой клетки и культуральную среду (среду для культивирования) первоначально помещают в культуральный сосуд, и в процессе культивирования в культуру добавляют дополнительные питательные вещества непрерывно или с интервалами с периодическим сбором клеток и/или продукта или без него до прекращения культивирования.
«Перфузионная культура» представляет собой способ культивирования, в котором клетки удерживаются в культуре путем, например, фильтрации, инкапсуляции, удерживания на микроносителях и т.д., а культуральный среду непрерывно или периодически добавляют в реакционный сосуд или удаляют из него.
«Хранение клеток в банке» или «хранение в банке» представляет собой процесс, в котором клетки замораживают до температур ниже нуля (подвергают криоконсервации) для остановки ферментативных/химических реакций, что позволяет сохранять клетки в жизнеспособном состоянии для последующего использования. Замороженные клетки можно хранить при температуре равной или более низкой, чем приблизительно 0°C (например, при -20°C, -70°C, -80°C или ниже) для последующего использования. Например, клетки могут храниться в ампулах, размещенных в паровой фазе в криогенном аппарате на базе жидкого азота при -196 °C.
«Культуральный сосуд» относится к контейнеру, применяемому для культивирования клеток. Культуральный сосуд может быть любого размера, допускающего его применение для культивирования клеток.
Термин «титр» в настоящем документе относится к общему количеству экспрессируемого рекомбинантным способом полипептида, продуцируемого культурой клеток, разделенному на заданное значение объема среды. Титр обычно выражают в миллиграммах полипептида на миллилитр среды.
Термин «нуклеиновая кислота» в настоящем описании относится к полимеру любой длины из нуклеотидов и включает ДНК и РНК. Нуклеотиды могут представлять собой дезоксирибонуклеотиды, рибонуклеотиды, модифицированные нуклеотиды и основания и/или их аналоги или любой субстрат, который может быть встроен в полимер ДНКполимеразой или РНКполимеразой или в результате реакции синтеза. Полинуклеотид включать модифицированные нуклеотиды, такие как метилированные нуклеотиды. Модификация структуры нуклеотида, если таковая присутствует, может быть осуществлена до или после сборки полимера.
«Изолированная нуклеиновая кислота» обозначает и включает не встречающуюся в природных условиях, рекомбинантную или природную последовательность вне ее обычного окружения или выделенную из ее обычного окружения. Изолированная молекула нуклеиновой кислоты находится в форме или условиях, отличных от встречающихся в природе. Соответственно, изолированные молекулы отличаются от нуклеиновой кислоты в таком виде, в котором она существует в природных клетках. Однако, изолированная молекула нуклеиновой кислоты включает молекулу нуклеиновой кислоты, содержащуюся в клетке, которая обычно экспрессирует белок, в случае когда, например, молекула нуклеиновой кислоты находится в локусе хромосомы, отличном от того, в котором она находится в природных клетках.
«Изолированный» (выделенный) белок (например, изолированное антитело) это белок, который был идентифицирован и отделен от и/или выделен из компонента его природного окружения. Примеси, являющиеся компонентами его природного окружения, представляют собой материалы, которые препятствовали бы применению этого белка в исследованиях, диагностике или терапии, они могут включать ферменты, гормоны и другие белковые и небелковые растворимые веществ. Изолированный белок включает белок in situ в рекомбинантной клетке, поскольку в этом случае отсутствует по меньшей мере один компонент природного окружения белка. Однако обычно получение изолированных белков включает по меньшей мере один этап очистки.
«Очищенный» полипептид обозначает, что степень чистоты полипептида была повышена, в результате чего он существует в более чистой форме, чем в его природном окружении и/или при первоначальном получении и/или синтезе и/или амплификации в лабораторных условиях. Чистота представляет собой относительное понятие не необязательно обозначает абсолютную чистоту.
«Примеси» относятся к материалам, которые отличаются от целевого полипептидного продукта. Примеси включают: материалы клетки-хозяина, такие как белки клетки-хозяина, нуклеиновая кислота, вариант, фрагмент или производное целевого полипептида, другой полипептид, эндотоксин, примесь вирусного происхождения, компоненты среды для культивирования клеток и т.д., но не ограничиваются перечисленным. Примеси могут также включать материалы, привносимые в процессе очистки, такие как отработанный белок A.
Термины «полипептид» и «белок» используются в настоящем документе взаимозаменяемо для обозначения полимеров любой длины из аминокислот. Полимер может быть линейным или разветвленным, он может включать модифицированные аминокислоты, и может содержать не-аминокислоты. Эти термины охватывают также полимеры из аминокислот, модифицированные естественным путем или в результате вмешательства; например, в результате образования дисульфидных связей, гликозилирования, липидизации, ацетилирования, фосфорилирования или любых других манипуляций или модификаций, таких как конъюгация с меткой. Это определение также включает, например, полипептиды, содержащие один или больше аналогов аминокислот (включая, например, неприродные аминокислоты и т.д.), а также другие модификации, известные в данной области. Примеры полипептидов, входящие в приведенное в настоящем документе определение, включают белки млекопитающих, такие как, например, ренин; гормон роста, включая человеческий гормон роста и бычий гормон роста; релизинг-фактор гормона роста, паратиреоидный гормон, тиреотропный гормон, липопротеины, антитрипсин альфа-1, A-цепь инсулина, В-цепь инсулина, проинсулин, фолликулостимулирующий гормон, кальцитонин, лютеинизирующий гормон, глюкагон, факторы свертывания, такие как фактор VIIIC, фактор IX, тканевой фактор и фактор фон Виллебранда, противосвертывающие факторы, такие как белок C, предсердный натрийуретический фактор, легочный сурфактант, активаторы плазминогена, такие как урокиназа или человеческий активатор плазминогена мочи или тканевой активатор плазминогена (t-PA), бомбезин, тромбин, гемопоэтический фактор роста, фактор некроза опухоли альфа и бета, энкефалиназа, цитокин RANTES (регулируемый при активации, экспрессируемый и секретируемый нормальными Т-клетками), воспалительный белок макрофагов человека (MIP-1-альфа), сывороточные альбумины, такие как человеческий сывороточный альбумин, Мюллерова ингибирующая субстанция, A-цепь релаксина, B-цепь релаксина, прорелаксин, мышиный гонадотропин-ассоциированный пептид; микробные белки, такие как бета-лактамаза, ДНКаза, IgE, антиген цитотоксических Т-лимфоцитов (CTLA), такие как CTLA-4, ингибин, активин, фактор роста эндотелия сосудов(VEGF), рецепторы гормонов или факторов роста, белок A или D, ревматоидные факторы, нейтротрофические факторы, такие как костный нейротрофический фактор (BDNF), нейтротрофин-3, -4, -5 или -6 (NT-3, NT-4, NT-5 или NT-6) или факторы роста нервов, такие как NGF-b, тромбоцитраный фактор роста (PDGF), факторы роста фибробластов, такие как aFGF и bFGF, эпидермальные факторы роста (EGF), трансформирующие факторы роста (TGF), такие как TGF-альфа и TGF-бета, включая TGF-β1, TGF-β2, TGF-β3, TGF-β4 или TGF-β5, инсулинподобные факторы роста -I и -II (ИФР-I и ИФР-II), дес(1-3)-ИФР-I (мозговой ИФР-I), белки, связывающие инсулинопобобные факторы роста (IGFBPs), белки CD, такие как CD3, CD4, CD8, CD19 и CD20, эритропоэтин, остеоиндуктивные факторы, иммунотоксины, белки морфогенеза костей (BMP), интерфероны, такие как интерферон-альфа, -бета и -гамма, колониестимулирующие факторы (CSF), например, M-CSF, GM-CSF и G-CSF, интерлейкины (ILs), например, IL-1 - IL-10, супероксиддисмутаза, T-клеточные рецепторы, поверхностные мембранные белки, стимулятор гемолиза, вирусный антиген, такой как, например, часть оболочки вируса СПИДа, транспортные белки, «хоминг»-рецепторы, адрессины, регуляторные белки, интегрины, такие как CD11a, CD11b, CD11c, CD18, молекулы адгезии ICAM, VLA-4 и VCAM, опухолевые антигены, такие как CA125 (антиген рак яичников) или рецептор HER2, HER3 или HER4, иммуноадгезины, и фрагменты и/или варианты любого из вышеупомянутых белков, а также антитела, включая фрагменты антител, связывающиеся с белками, включая, например, любой из вышеуказанных белков.
Термин «антитело» используется в настоящем документе в самом широком смысле и, в частности, включает антитела (включая полноразмерные моноклональные антитела), поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител длины достаточной для того чтобы они могли демонстрировать необходимую биологическую активность. Антитело может быть человеческим, гуманизированным и/или подвергнутым процедуре созревания аффинности.
Термин «моноклональное антитело» в настоящем документе относится к антителу, полученного из пулы по существу гомогенных антител, т.е., отдельные антитела, составляющие эту популяцию, идентичны за исключением возможных природных мутаций, которые могут присутствовать в небольших количествах. Моноклональные антитела высоко специфичны, поскольку они нацелены на единственный антигенный сайт. Кроме того, в отличие от препаратов поликлональных антител, которые включают различные антитела, нацеленные на различные детерминанты (эпитопы), каждое моноклональное антитело нацелено против единственной детерминанте на антигене. В дополнение к их специфичности, моноклональные антитела обладают тем преимуществом, что их можно синтезировать без примесей других антител. Определение «моноклональное» не подразумевает, что антитело должно быть обязательно получено каким-либо конкретным способом. Например, моноклональные антитела для применения в соответствии с настоящим изобретением могут быть получены с использованием различных методик, включая, например, метод гибридом (например, Kohler и Milstein, Nature, 256:495-97 (1975), Hongo с соавт., Hybridoma, 14 (3): 253-260 (1995), Harlow с соавт., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2е изд. 1988); Hammerling с соавт., в: Monoclonal Antibodies and T-Cell Hybridomas 563-681 (Elsevier, N.Y., 1981)), методы рекомбинации ДНК в бактериальных клетках, эукариотических клетках животных или растений (см., например, патент США № 4,816,567), методики фагового дисплея (см., например, Clackson с соавт., Nature, 352: 624-628 (1991), Marks с соавт., J. Mol. Biol. 222: 581-597 (1992), Sidhu с соавт., J. Mol. Biol. 338(2): 299-310 (2004), Lee с соавт., J. Mol. Biol. 340(5): 1073-1093 (2004), Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004) и Lee с соавт., J. Immunol. Methods 284(1-2): 119-132 (2004), и методики получения человеческих или антител, сходных с антителами человека, в организме животных, которые содержат части или все гены или локусы человеческих иммуноглобулинов, кодирующие последовательности иммуноглобулинов человека (см., например, WO 1998/24893, WO 1996/34096; WO 1996/33735; WO 1991/10741, Jakobovits с соавт., Proc. Natl. Acad. Sci. USA 90: 2551 (1993), Jakobovits с соавт., Nature 362: 255-258 (1993), Bruggemann с соавт., Year in Immunol. 7:33 (1993), патенты США №№: 5,545,807; 5,545,806, 5,569,825; 5,625,126, 5,633,425 и 5,661,016, Marks с соавт., Bio/Technology 10: 779-783 (1992), Lonberg с соавт., Nature 368: 856-859 (1994), Morrison, Nature 368: 812-813 (1994), Fishwild с соавт., Nature Biotechnol. 14: 845-851 (1996), Neuberger, Nature Biotechnol. 14: 826 (1996) и Lonberg and Huszar, Intern. Rev. Immunol. 13: 65-93 (1995).
Термин «фармацевтическая композиция» относится к препарату, который имеет форму, обеспечивающую возможность реализации биологической активности активного ингредиента, и который не содержит дополнительных компонентов, неприемлемо токсичных для субъекта, которому предполагается вводить указанную композицию. Такие композиции являются стерильными.
«Фармацевтически приемлемые» носители, вспомогательные вещества или стабилизаторы - это носители, вспомогательные вещества или стабилизаторы, которые нетоксичны для клетки или млекопитающего, подвергающихся из воздействию в применяемых дозировках и концентрациях (Remington's Pharmaceutical Sciences (20е издание), ред. A. Gennaro, 2000, Lippincott, Williams & Wilkins, Philadelphia, PA). Часто физиологически приемлемый носитель представляет собой водный pH-буферный раствор. Примеры физиологически приемлемых носителей включают буферы, такие как буферы на основе фосфата, цитрата и других органических кислот, антиоксиданты, включая аскорбиновую кислоту, низкомолекулярные (содержащие менее приблизительно 10 остатков) полипептиды, белки, такие как сывороточный альбумин, желатин или иммуноглобулины, гидрофильные полимеры, такие как поливинилпирролидон, аминокислоты, такие как глицин, глютамин, аспарагин, аргинин или лизин, моносахариды, дисахариды и другие углеводороды, включая глюкозу, маннозу или декстрины, хелатирующие агенты, такие как ЭДТА, сахарные спирты, такие как маннитол или сорбит, солеобразующие противоионы, такие как натрий, и/или неионные поверхностно-активные вещества, такие как Tween™, полиэтиленгликоль (PEG, ПЭГ) и Pluronics™.
В настоящем описании и прилагаемой формуле изобретения любые формы единственного числа включают указание на множественное число, если контекст явно не диктует обратное. Таким образом, например, признак «соединение» необязательно включает комбинацию двух или более таких соединений и т.п.
Понятно, что аспекты и варианты реализации изобретения, описанного в настоящем документе, включают варианты «содержащие», «состоящие» и «состоящие по существу из» аспектов и варианты реализации.
Указание на «приблизительное» значение или параметр в настоящем документе включает (и описывает) варианты реализации, которые относятся к этому значению или параметру как таковому. Например, описание, относящееся к «приблизительно X» включает описание «X». Численные диапазоны включают числа, определяющие этот диапазон.
В тех случаях, когда аспекты и варианты реализации изобретения описаны в терминах групп Маркуша или с использованием других классификаций или альтернатив, настоящее изобретение охватывает не только всю группу, описанную как целое, но и каждый член этой группы отдельно, а также все возможные подгруппы основной группы, а также основную группу без одного или более членов группы. Настоящее изобретение также предусматривает явное исключения одного или более любых членов групп согласно заявленному изобретению.
II. Способы и применения согласно настоящему изобретению
Предложены способы замораживания клеток для хранения в банке или хранения в среде для замораживания клеток. Также предложены способы улучшения размораживания банков клеток. Способы включают этап замораживания клеток в среде для замораживания, причем среда для замораживания содержит буферный раствор и криопротектор, и при этом pH среды для замораживания, содержащей клетки, равен от приблизительно 6,7 до приблизительно 8,5 или от приблизительно 6,7 до приблизительно 8,3 перед замораживанием. Способы могут дополнительно включать этап корректировки pH среды для замораживания до значения от приблизительно 6,7 до приблизительно 8,5 или до от приблизительно 6,7 до приблизительно 8,3. Предложенные способы можно применять для создания главных банков клеток (ГБК,ГБК) и рабочих банков клеток (РБК, РБК). В некоторых вариантах реализации способы, описанные в настоящем документе, улучшают жизнеспособность клеток и/или рост клеток после размораживания.
Эукариотические клетки (например, клетки млекопитающего, клетки насекомого и т.д.) для применения в процессе замораживания и хранения в банке могут быть получены способом, включающим протоколы культивирования клеток и концентрирования, известные в данной области. Способ может включать наработку, сбор и концентрирование клеток перед закладкой на хранение в банк. Наработку клеток можно осуществлять различными способами. В одном из примеров для наработки клеток может применяться автоматический биореактор; однако также возможно применение других способов/культуральных сосудов (например, T-колб, колб для встряхивания, роллерных флаконов, сосудов для культивирования с постоянным перемешиванием т.д.). Сбор и концентрирование клеток можно осуществлять путем центрифугирования с последующим ресуспендированием осажденных клеток в среде для замораживания. В другом примере клетки можно собрать и концентрировать за один этап при помощи половолоконного фильтра (HFF). Концентрирование клеток также можно осуществить при помощи других перфузионных мембран/устройств для удаления среды из культуральной жидкости/(например, поверхностных перфузионных мембран, осадителей клеток, центрифуг с непрерывной циркуляцией и т.д.). В некоторых вариантах реализации описанного в настоящем документе способа процесс сбора и концентрирования клеток или культуральную жидкость с собранными клетками охлаждают до температуры, равной или ниже приблизительно 20°C (например, равной или более низкой, чем любое из следующих значение: 19°C, 18°C, 17°C, 16°C, 15°C, 14°C, 13°C, 12°C, 11°C и 10°C).
Осажденные или концентрированные клетки можно затем объединить со средой для замораживания, перед замораживанием клеток. В некоторых вариантах реализации осажденные клетки могут быть ресуспендированы в среде для замораживания. В некоторых вариантах реализации среда для замораживания, содержащая концентрированный криопротектор, может быть добавлена в собранные и концентрированные клетки или собранные и концентрированные клетки могут быть добавлены в среду для замораживания, содержащую криопротектор, для хранения клеток в банке. Среда для замораживания может включать буферный раствор и криопротектор. В некоторых вариантах реализации буфер в среде может включать цвиттерионный буфер. В некоторых вариантах реализации буфер в среде может включать буфер, выбранный их бикарбонатного буфера, ФБР (фосфатного буферного раствора), HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновой кислоты), MOPS (3-(N-морфолинo)пропансульфоновой кислоты), TES (N-[трис(гидроксиметил)метил]-2-аминоэтансульфоновой кислоты), TRIS (трис(гидроксиметил)аминометана), TEST (комбинация TES/TRIS) и их комбинаций. В некоторых вариантах реализации концентрация буфера в среде для замораживания перед замораживанием клеток равна от приблизительно 10 мМ до приблизительно 50 мМ. В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит от приблизительно 10 мМ до приблизительно 35 мМ бикарбоната натрия (например, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ, приблизительно 30 мМ или приблизительно 35 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит от приблизительно 10 мМ до приблизительно 50 мМ HEPES (например, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ, приблизительно 30 мМ, приблизительно 35 мМ, приблизительно 40 мМ, приблизительно 45 мМ, или приблизительно 50 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит приблизительно 10 мМ до приблизительно 12 мМ ФБР (например, приблизительно 10 мМ, приблизительно 11 мМ или приблизительно 12 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит приблизительно 10 мМ до приблизительно 20 мМ MOPS (например, приблизительно 10 мМ, приблизительно 12 мМ, приблизительно 15 мМ, приблизительно 18 мМ или приблизительно 20 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит приблизительно 10 мМ до приблизительно 30 мМ TES (например, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ, или приблизительно 30 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит приблизительно 10 мМ до приблизительно 30 мМ TRIS (например, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ или приблизительно 30 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации среда для замораживания перед замораживанием клеток содержит приблизительно 10 мМ до приблизительно 30 мМ TEST (например, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ или приблизительно 30 мМ, включая любые концентрации в интервалах между этими значениями). В некоторых вариантах реализации криопротектор представляет собой вещество, проникающее внутрь клетки, или вещество, не проникающее внутрь клетки. В некоторых вариантах реализации криопротектор представляет собой вещество, выбранное из группы, состоящей из глицерина, диметилсульфоксида (ДМСО), пропандиола, этиленгликоля и сахаров. В некоторых вариантах реализации среда для замораживания, добавляемая в собранные и концентрированные клетки, представляет собой концентрированную среду для замораживания. В некоторых вариантах реализации среда для замораживания, содержащая концентрированный криопротектор, может содержать 20-30% (об./об.) диметилсульфоксида (ДМСО) или глицерина. В некоторых вариантах реализации концентрированную среду для замораживания вливают (например, 1 объемную часть среды для замораживания (содержащей защитный криопротектор): 3 части жидкой клеточной культуры) в собранные и концентрированные клетки. В некоторых вариантах реализации среда для замораживания, содержащая клетки, перед замораживанием клеток содержит приблизительно 5% до приблизительно 12,5% ДМСО или глицерина.
В некоторых вариантах реализации среда для замораживания может дополнительно содержать дополнительные компоненты, присутствующие в среде для культивирования клеток. В некоторых вариантах реализации среда для замораживания может содержать минимальную поддерживающую среду Игла (EMEM) или среду Игла, модифицированную по способу Дульбекко (DMEM).
В некоторых вариантах реализации способ подготовки клеток (таких как клетки млекопитающего или клетки насекомого) для замораживания может дополнительно включать этап корректировки pH среды для замораживания или среды для замораживания, содержащей концентрированный криопротектор, причем pH корректируют до значения от приблизительно 6,7 до приблизительно 8,5 перед объединением осажденных клеток или концентрированных клеток со средой для замораживания или средой для замораживания, содержащей концентрированный криопротектор. В некоторых вариантах реализации способ подготовки клеток (таких как клетки млекопитающего или клетки насекомого) для замораживания дополнительно включает этап корректировки pH среды для замораживания, содержащей клетки, причем pH среды для замораживания корректируют до значения от приблизительно 6,7 до приблизительно 8,5. В некоторых вариантах реализации откорректированный pH представляет собой целевой pH или измеренный pH.
В некоторых вариантах реализации плотность клеток перед замораживанием измеряют по объему осажденных клеток (ООК). В некоторых вариантах реализации среда для замораживания, содержащая клетки для хранения в банке, имеет плотность клеток, измеренную как объем осажденных клеток (ООК), от 8% до 28% (например, приблизительно, любое значение из 8%, 10%, 15%, 20%, 25% и 28%) перед замораживанием. В некоторых вариантах реализации плотность клеток в среде для замораживания перед замораживанием может составлять приблизительно 21% по ООК.
В некоторых вариантах реализации клетки в среде для замораживания помещают в ампулы или одноразовые пакеты перед замораживанием. В одном из примеров реализации способ включает: помещение суспензии клеток в стерилизованные в автоклаве стеклянные ампулы, которые помещают на влажный лед при помощи стерилизованного в автоклаве автоматического шприца, запечатывание ампул, проведение теста на целостность и замораживание ампул в программируемом замораживателе с последующим переносом ампул в криогенный аппарат на базе жидкого азота для длительного хранения.
В некоторых вариантах реализации жизнеспособность клеток после размораживания улучшается за счет применения способов, описанных в настоящем документе. В некоторых вариантах реализации жизнеспособность клеток повышается по меньшей мере на приблизительно любое значение из 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75% или 85% по сравнению с жизнеспособностью клеток после замораживания в среде для замораживания с рH 6,7 или ниже и/или без охлаждения собранной культуры клеток в процессе сбора и размораживания.
Корректировка pH
В соответствии со способами согласно настоящему описанию pH среды для замораживания (содержащей или не содержащей клетки) можно корректировать, например, путем добавления основания в среду. В некоторых вариантах реализации pH среды для замораживания корректируют до значения pH выше приблизительно 6,7. В некоторых вариантах реализации pH среды для замораживания корректируют до значения pH (целевого pH или измеренного pH) от приблизительно 6,7 до приблизительно 8,5. В некоторых вариантах реализации pH среды для замораживания корректируют до значения pH от приблизительно 6,8 до приблизительно 8,3, от приблизительно 6,9 до приблизительно 8,3, от приблизительно 7.0 до приблизительно 8,3, от приблизительно 7,1 до приблизительно 8,3, от приблизительно 7,2 до приблизительно 8,3, от приблизительно 7,3 до приблизительно 8,3, от приблизительно 7,4 до приблизительно 8,3, от приблизительно 7,5 до приблизительно 8,3, от приблизительно 7,6 до приблизительно 8,3, от приблизительно 7,7 до приблизительно 8,3, или от приблизительно 7,8 до приблизительно 8,3 В некоторых вариантах реализации pH среды для замораживания корректируют до значения pH (целевого pH или измеренного pH) от приблизительно 7,2 до приблизительно 7,8. В некоторых вариантах реализации целевой pH или измеренный pH равен от приблизительно 7,2 до приблизительно 8,3. В некоторых вариантах реализации целевой pH или измеренный pH равен от приблизительно 7,2 до приблизительно 7,8 (например, pH составляет приблизительно 7,5). В некоторых вариантах реализации, если первая корректировка pH не обеспечивает повышения pH до диапазона целевых значений pH (например, pH от приблизительно 7,3 до приблизительно 7,7), осуществляют вторую корректировку pH. В некоторых вариантах реализации возможно проведение более, чем одной корректировки pH.
Основание, добавляемое для корректировки pH, может представлять собой любое основание, которое хорошо известно в данной области, но в примерах реализации основание представляет собой карбонат натрия, бикарбонат натрия, натриевую соль N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксид натрия или гидроксид калия.
pH среды для замораживания может быть измерен в любой момент перед замораживанием, и pH может быть откорректирован в любое время перед замораживанием. В некоторых вариантах реализации pH среды для замораживания измеряют и/или корректируют перед объединением с клетками для хранения в банке. В других вариантах реализации pH среды для замораживания измеряют и/или корректируют после объединения с клетки для хранения в банке. В некоторых вариантах реализации pH среды для замораживания измеряют и/или корректируют больше одного раза. В некоторых вариантах реализации pH среды для замораживания измеряют и/или корректируют два, три раза или больше перед замораживанием. В других вариантах реализации pH среды для замораживания измеряют и/или корректируют перед и после объединения с клетками для хранения в банке. В некоторых вариантах реализации pH корректируют в соответствии со следующим уравнением: Vbase=Cbase*Vp (pHt - pHi), где Cbase представляет собой коэффициент, значение которого зависит от основания, Vbase представляет собой объем основания, добавляемый в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. В настоящем тексте исходный pH представляет собой pH среды для замораживания, содержащей клетки, (т.е., после ее объединения с клетками), но до корректировки pH для замораживания. Cbase представляет специальный коэффициент, который зависит от типа основания, выбранного для корректировки pH. Коэффициент Cbase может быть получен в зависимости от выбора основания. В одном из примеров реализации, в котором основание представляет собой 1M карбонат натрия, корректировку pH осуществляют в соответствии с приведенным ниже уравнением 1:
Уравнение 1: Расчет объема основания для добавления для корректировки pH
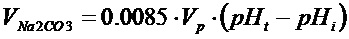 ,
,
где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH, и pHi представляет собой исходный pH. Исходный pH - это pH среды для замораживания, содержащей клетки (т.е., после ее объединения с клетками), но до корректировки pH для замораживания. Целевой pH среды для замораживания может представлять собой значение pH выше физиологического pH, такое как pH выше 7,2. В некоторых вариантах реализации целевой pH среды для замораживания лежит в диапазоне от 7,2 до 8,3. В некоторых вариантах реализации целевой pH среды для замораживания лежит в диапазоне от 7,2 до 7,8. В некоторых вариантах реализации целевой pH среды для замораживания представляет собой любое значение из 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8.0, 8,1, 8,2 и 8,3.
pH среды для замораживания может быть измерен методами, известными в данной области. Например, pH среды может быть измерен на анализаторах BioProfile® 400 (Nova Biomedical) или BioProfile® FLEX (Nova Biomedical). В настоящем тексте все упоминания pH в этой заявке, включая измеренный pH, целевой pH, откорректированный pH и исходный pH относятся к значению pH, измеренному при температуре образца, откорректированной до приблизительно 37°C (например, от 36°C до 38°C или от 35°C до 39°C).
III. Среды для замораживания
Среды для замораживания клеток, описанные в настоящем документе, могут найти применение в способах (например, способе замораживания эукариотических клеток (например, клеток млекопитающего, клеток насекомого и т.д.); и/или способе улучшения размораживания банков клеток, содержащих эукариотические клетки (например, клетки млекопитающего или клетки насекомого)), и в композициях (например, пуле клеток, содержащем буферный раствор, криопротектор и эукариотические клетки (например, клетки млекопитающего или клетки насекомого)).
В некоторых вариантах реализации среда для замораживания, описанная в настоящем документе, содержит буферный раствор и криопротектор. В некоторых вариантах реализации буфер содержит цвиттерионный буфер. В некоторых вариантах реализации буфер включает ФБР, HEPES, TES, TRIS и TEST.
Среда для замораживания могут включать любой криопротектор известный в данной области и описанный здесь, такой как ДМСО, глицерин, этиленгликоль, непроникающие в клетку макромолекулы, сахара и т.д. В некоторых вариантах реализации концентрация ДМСО мом глицерина в среде для замораживания клеток составляет 5%-12,5% по объему (об./об.) после объединения с клетками для хранения в банке. В некоторых вариантах реализации среда для замораживания может быть получена путем добавления среды для замораживания, содержащей концентрированные буферы и/или криопротектор, в концентрированные клетки. В некоторых вариантах реализации среда для замораживания концентрированный криопротектор могут содержать приблизительно 20% до приблизительно 30% (об./об.) ДМСО или глицерина.
В некоторых вариантах реализации среда для замораживания может включать дополнительные компоненты, присутствующие в среде для культивирования клеток. В некоторых вариантах реализации среда Ham's F10 (Sigma), минимальная поддерживающая среды ([MEM], Sigma), RPMI-1640 (Sigma) и минимальная поддерживающая среда, модифицированная методом Дульбекко([DMEM], Sigma), которые подходят для культивирования клеток млекопитающего, могут быть добавлены в среду для замораживания, описанную в настоящем документе, для замораживания клеток млекопитающих. Дополнительно любая из сред, описанных в работах Ham и Wallace, Meth. Enz., 58:44 (1979), Barnes и Sato, Anal. Biochem., 102:255 (1980), Vijayasankaran с соавт., Biomacromolecules., 6:605:611 (2005), Patkar с соавт., J Biotechnology, 93:217-229 (2002), патентах США №№: 4,767,704; 4,657,866; 4,927,762, или 4,560,655, WO 90/03430; WO 87/00195, патенте США № Re. 30,985 или патенте США № 5,122,469 (тексты каждого из указанных источников включены в настоящий документ посредством ссылки полностью) могут быть дополнены или модифицированы как подробно описано в настоящем документе.
Для специалиста в данной области понятно, что среда для замораживания клеток, подробно описанная в настоящем документе, может включать другие компоненты, полезные для культивирования или замораживания клеток. Например, понятно, что среды могут включать дополнительные компоненты, такие как аминокислоты (например, глютамин, аргинин или аспарагин), витамины (включая витамины группы B, такие как любые один или больше из витамина B1, витамина B2, витамина B3, витамина B6, витамина B7, витамина B9 или витамина B12, но не ограничиваясь перечисленными), переходные металлы (включая никель, железо (например, трехвалентное железо или двухвалентное железо) или цинк, но не ограничиваясь ими) и другие компоненты среды. Любая среда, описанная в настоящем документе, может быть при необходимости дополнены гормонами и/или другими факторами роста (такими как инсулин, трансферрин или эпидермальный фактор роста), ионами (такими как натрий, хлор, кальций, магний и фосфат-ионы), буферами (такими как HEPES), нуклеозидами (такими как аденозин и тимидин), микроэлементами (определяемыми как неорганические соединения, конечные концентрации которых обычно лежат в микромолярном диапазоне) и глюкозой или эквивелентными источниками энергии. В некоторых аспектах описанная в данном документе среда для замораживания содержит белки растительного или животного происхождения. В некоторых вариантах реализации описанная в данном документе среда для замораживания не содержит белков растительного или животного происхождения. Также могут быть включены любые другие необходимые добавки в соответствующих концентрациях, которые будут известны специалисту в данной области.
Среда для замораживания клеток (пула клеток) согласно настоящему описанию может дополнительно содержать одну или больше клеток для хранения в банке. В одном из примеров реализации эти клетки представляют собой клетки млекопитающего, такие как клетки CHO. Примеры типов клеток, которые могут найти применение в способах, описанных в настоящем документе, включают клетки яичника китайского хомячка (CHO), клетки миеломы мыши NS0, клетки человека PER.C6® и гибридомы. В другом примере реализации эти клетки представляют собой клетки насекомого, такие как High FiveTM, S2 (Schneider 2), Sf9 и Sf21. В некоторых вариантах реализации клетки представляют собой рекомбинантные клетки, содержащие гетерологичную нуклеиновую кислоту, кодирующую полипептид (например, терапевтический белок). Специалисту в данной области понятно, что эти клетки могут дополнительно содержать рекомбинантные плазмиды и другие полезные биологические соединения. В некоторых вариантах реализации клетки для хранения в банке могут применяться для получения терапевтических белков и биологических продуктов, таких как антитела, фрагменты антител, ферменты, рецепторные белки слияния или их фрагменты.
IV. Эукариотические клетки и банки клеток
Также в настоящем документе предложен банк клеток, содержащий множество контейнеров, причем каждый контейнер содержит среду для замораживания, содержащую эукариотическую клетку(например, клетку млекопитающего, клетку насекомого и т.д.), содержащую нуклеиновую кислоту (например, гетерологичную), кодирующую полипептид, причем pH среды равен от приблизительно 6,7 до приблизительно 8,5 перед замораживанием клеток. Банк клеток может представлять собой предварительный банк, главный банк клеток (MCB, ГБК) или рабочий банк клеток (WCB, РБК). Предварительный банк может включать замороженные (например, хранящиеся в холодильнике с жидким азотом) контейнеры (например, ампулы), содержащие клетки, продуцирующие определенный пептид полипептид, из которого получают ГБК. ГБК может включать замороженные (например, хранящиеся в холодильнике с жидким азотом) контейнеры (например, ампулы), содержащие культуру клеток, полученную из субкультуры из предварительного банка, и из которой получают все последующие клетки для производства. Главные банки клеток создают и хранят в соответствии с действующими правилами организации производства и контроля качества, они могут применяться для получения полипептидного продукта. Рабочий банк клеток может включать замороженные (например, хранящиеся в холодильнике с жидким азотом) контейнеры (например, ампулы), содержащие культуру клеток, полученную из субкультуры из ГБК. Рабочие банки клеток создают и хранят в соответствии с действующими правилами организации производства и контроля качества, они могут применяться для получения полипептидного продукта. В некоторых вариантах реализации контейнеры представляют собой ампулы.
Эукариотические клетки (например, клетки млекопитающего, клетки насекомого и т.д.), которые можно замораживать в среде для замораживания и хранить как описано в настоящем документе, включают любые эукариотические клетки, которые можно культивировать и/или применять для продуцирования полипептида. В некоторых вариантах реализации клетки представляет собой клетку млекопитающего, такую как клетка яичника китайского хомячка (CHO). Клетки CHO могут включать DHFR- клетки CHO (дефицитные по рецептору дегидрофолатредуктазы, Urlaub с соавт., Proc. Natl. Acad. Sci. USA 77:4216 (1980)), например, ATCC® CRL-9096TM, и CHO-K1 (ATCC® CRL-61TM), но не ограничиваются перечисленными.
Другие примеры клеток млекопитающего включают следующие, но не ограничиваются ими: линия CV1 клеток почек обезьяны, трансформированная SV40 (COS-7, Американская коллекция типовых культур:CRL 1651), линию клеток почки эмбриона человека (клетки 293 или клетки 293, субклонированные для выращивания в суспензионной культуре, Graham с соавт., J. Gen Virol. 36:59 (1977)), клетки почки хомячка (BHK, Американская коллекция типовых культур: CCL 10), мышиные клетки Сертоли (TM4, Mather, Biol. Reprod. 23:243-251 (1980)), клетки почки обезьяны (CV1, Американская коллекция типовых культур: CCL 70), клетки почки африканской зеленой мартышки (VERO-76, Американская коллекция типовых культур: CRL-1587); клетки карциномы шейки матки человека (HELA, Американская коллекция типовых культур: CCL 2), клетки почки собаки (MDCK, Американская коллекция типовых культур: CCL 34), клетки крыс Buffalo (BRL 3A, Американская коллекция типовых культур: CRL 1442), клетки легкого человека (W138, Американская коллекция типовых культур: CCL 75), клетки печени человека (Hep G2, HB 8065), клетки опухоли молочной железы мыши (MMT 060562, Американская коллекция типовых культур: CCL51), клетки TRI (Mather с соавт., Annals N.Y. Acad. Sci. 383:44-68 (1982)), клетки MRC 5, клетки FS4 и линия гепатомы человека (Hep G2). Другие полезные линии клеток-хозяев включают линии клеток миеломы, такие как NS0 и Sp2/0. Обзор некоторых линий клеток-хозяев млекопитающих, подходящих для получения антител, можно найти, например, в работе Yazaki и Wu, Methods in Molecular Biology, Vol. 248 (B. K. C. Lo, ed., Humana Press, Totowa, N.J., 2003), стр. 255-268.
В некоторых вариантах реализации клетка представляет собой линию клеток насекомого, такую как High FiveTM, S2 (Schneider 2), Sf9, и Sf21.
В некоторых вариантах реализации описанные в настоящем документе клетки (например, клетка млекопитающего или клетки насекомого) содержат нуклеиновую кислоту (например, гетерологичную нуклеиновую кислоту), кодирующую полипептид, и эти клетки можно применять для продуцирования полипептида. В некоторых вариантах реализации нуклеиновая кислота введена в клетки. Для введения нуклеиновой кислоты в клетки могут применяться любые способы, известные в данной области. Например, клетки можно трансформировать векторами (например, вектором экспрессии), содержащими одну или больше нуклеиновых кислот, кодирующих полипептид. В некоторых вариантах реализации клетка представляет собой стабильную линию клеток. В некоторых вариантах реализации полипептид выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
Примеры полипептидов включают белки млекопитающих, такие как, например, ренин, гормон роста, включая человеческий гормон роста и бычий гормон роста, релизинг-фактор гормона роста, паратиреоидный гормон, тиреотропный гормон, липопротеины, антитрипсин альфа-1, A-цепь инсулина, В-цепь инсулина, проинсулин; фолликулостимулирующий гормон, кальцитонин, лютеинизирующий гормон, глюкагон; факторы свертывания, такие как фактор VIIIC, фактор IX, тканевой фактор и фактор фон Виллебранда, противосвертывающие факторы, такие как белок C, предсердный натрийуретический фактор, легочный сурфактант, активатор плазминогена, такой как урокиназа или человеческий активатор плазминогена мочи или тканевой активатор плазминогена (t-PA), бомбезин, тромбин, гемопоэтический фактор роста, фактор некроза опухоли альфа и бета, энкефалиназа, цитокин RANTES (регулируемый при активации, экспрессируемый и секретируемый нормальными Т-клетками), воспалительный белок макрофагов человека (MIP-1-альфа), сывороточные альбумины, такие как человеческий сывороточный альбумин, Мюллерова ингибирующая субстанция, A-цепь релаксина, B-цепь релаксина, прорелаксин, мышиный гонадотропин-ассоциированный пептид, микробные белки, такие как бета-лактамаза, ДНКаза, IgE, антигены цитотоксических Т-лимфоцитов (CTLA), такие как CTLA-4, ингибин, активин, фактор роста эндотелия сосудов(VEGF), рецепторы гормонов или факторов роста, белок A или D, ревматоидные факторы, нейтротрофические факторы, такие как костный нейротрофический фактор (BDNF), нейтротрофин-3, -4, -5 или -6 (NT-3, NT-4, NT-5 или NT-6) или факторы роста нервов, такие как NGF-b, тромбоцитраный фактор роста (PDGF), факторы роста фибробластов, такие как aFGF и bFGF, эпидермальные факторы роста (EGF), трансформирующие факторы роста (TGF), такие как TGF-альфа и TGF-бета, включая TGF-β1, TGF-β2, TGF-β3, TGF-β4 или TGF-β5, инсулинподобные факторы роста -I и -II (ИФР-I и ИФР-II); дес(1-3)-ИФР-I (мозговой ИФР-I), белки, связывающие инсулинопобобные факторы роста (IGFBPs), белки CD, такие как CD3, CD4, CD8, CD19 и CD20, эритропоэтин, остеоиндуктивные факторы, иммунотоксины, белки морфогенеза костей (BMP), интерфероны, такие как интерферон-альфа, -бета и -гамма, колониестимулирующие факторы (CSFs, например, M-CSF, GM-CSF и G-CSF, интерлейкины (ИЛ), например, ИЛ-1 - ИЛ-10, супероксиддисмутаза, T-клеточные рецепторы, поверхностные мембранные белки, стимулятор гемолиза, вирусный антиген, такой как, например,часть оболочки вируса СПИДа, транспортные белки, «хоминг»-рецепторы, адрессины, регуляторные белки, интегрины, такие как CD11a, CD11b, CD11c, CD18, молекулы адгезии ICAM, VLA-4 и VCAM, опухолевый антиген, такие как CA125 (антиген рак яичников) или рецептор HER2, HER3 или HER4, иммуноадгезины и фрагменты и/или варианты любого из вышеупомянутых белков, а также антитела, включая фрагменты антител, связывающиеся с белками, включая, например, любой из вышеуказанных белков.
В некоторых вариантах реализации описанные в настоящем документе клетки (например, клетки млекопитающего или клетки насекомого) содержат нуклеиновую кислоту, кодирующую антитело. В некоторых вариантах реализации антитело представляет собой моноклональное антитело. Определение «моноклональное» указывает на то, что антитело получено из по существу гомогенной пулы антител, при этом не требуется чтобы антитело было получено каким-либо определенным способом. Например, моноклональные антитела для применения в соответствии с настоящим изобретением могут быть получены с использованием различных методик, включая, например, метод гибридом (например, Kohler & Milstein, Nature, 256:495-97 (1975), Hongo с соавт., Hybridoma, 14 (3): 253-260 (1995), Harlow с соавт., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2е изд. 1988); Hammerling с соавт., в: Monoclonal Antibodies and T-Cell Hybridomas 563-681 (Elsevier, N.Y., 1981)), рекомбинантные способы (см., например, патент США № 4,816,567), методики фагового дисплея (см., например, Clackson с соавт., Nature, 352: 624-628 (1991), Marks с соавт., J. Mol. Biol. 222: 581-597 (1992), Sidhu с соавт., J. Mol. Biol. 338(2): 299-310 (2004), Lee с соавт., J. Mol. Biol. 340(5): 1073-1093 (2004), Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004) и Lee с соавт., J. Immunol. Methods 284(1-2): 119-132 (2004), и методики получения человеческих антител или антител, сходных с антителами человека, в организме животных, которые содержат части или все гены или локусы человеческих иммуноглобулинов, кодирующие последовательности иммуноглобулинов человека (см., например, WO 1998/24893, WO 1996/34096; WO 1996/33735; WO 1991/10741, Jakobovits с соавт., Proc. Natl. Acad. Sci. USA 90: 2551 (1993), Jakobovits с соавт., Nature 362: 255-258 (1993), Bruggemann с соавт., Year in Immunol. 7:33 (1993), патенты США №№: 5,545,807; 5,545,806, 5,569,825; 5,625,126, 5,633,425 и 5,661,016, Marks с соавт., Bio/Technology 10: 779-783 (1992), Lonberg с соавт., Nature 368: 856-859 (1994), Morrison, Nature 368: 812-813 (1994), Fishwild с соавт., Nature Biotechnol. 14: 845-851 (1996), Neuberger, Nature Biotechnol. 14: 826 (1996) и Lonberg and Huszar, Intern. Rev. Immunol. 13: 65-93 (1995). В некоторых вариантах реализации антитело представляет собой гуманизированное антитело, химерное антитело, человеческое антитело, антитело из библиотеки или мультиспецифическое антитело. В некоторых вариантах реализации антитело представляет собой антигенсвязывающий фрагмент антитела. Примеры антигенсвязывающих фрагментов включают фрагменты Fab, Fab', F(ab')2 и Fv, диатела; линейные антитела, одноцепочечные молекулы антител, и мультиспецифические антитела, образованные из фрагментов антител. Fab-фрагмент содержит вариабельные домены тяжелой и легкой цепи, а также содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Fab'-фрагменты отличаются от Fab-фрагментов добавлением нескольких остатков на карбокси-конце домена CH1 тяжелой цепи, включая один или больше цистеинов из шарнирного участка антитела. Fab'-SH в настоящем документе обозначает Fab', в котором остаток (остатки) цистеина константных доменов несут свободную тиольную группу. F(ab')2-фрагменты антитела первоначально получали как пары фрагментов Fab' с шарнирными цистеинами между ними. Также известны другие химические соединения фрагментов антител. «Fv» представляет собой минимальный фрагмент антитела, который содержит полный антигенсвязывающий сайт. «одноцепочесный Fv-фрагменты» или «scFv»-фрагменты антител содержат домены VH и VL антитела, причем эти домены содержатся в одной полипептидной цепи. Обычно полипептид scFv дополнительно содержит полипептидный линкер между доменами VH и VL, который позволяет scFv образовывать структуру, необходимую для связывания антитела. Обзор scFv можно найти, например, в работе Pluckthün в The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York, 1994), стр. 269-315. Многие способы очистки антител, описанные выше, можно легко адаптировать для очистки антигенсвязывающего фрагмента.
В некоторых вариантах реализации антитела, кодируемые нуклеиновой кислотой в клетках (например, клетках млекопитающего или клетках насекомого), включают терапевтические и диагностические антитела. Антитела, входящие в объем настоящего изобретения, включают следующие, но не ограничиваются имм: анти-HER2 антитела, включая трастузумаб (HERCEPTIN®) (Carter с соавт., Proc. Natl. Acad. Sci. USA, 89:4285-4289 (1992), патент США № 5,725,856); анти-CD20 антитела, такие как химерное анти-CD20 «C2B8», описанное в патенте США № 5,736,137 (RITUXAN®), химерный или гуманизированный вариант антитела 2H7, описанный в патенте США № 5,721,108B1, или тозитомумаб (BEXXAR®), анти-IL-8 антитело (St John с соавт., Chest, 103:932 (1993), и международная публикация № WO 95/23865); анти-VEGF антитела геманизированные анти-VEGF антитела и/или анти-VEGF антитела, подвергнутые созреванию аффинности, такие как гуманизированное анти-VEGF антитело huA4,6,1 AVASTIN® (Kim с соавт., Growth Factors, 7:53-64 (1992), международная публикация № WO 96/30046 и WO 98/45331, опубликованная 15 октября 1998г.); антитела к антигену карциномы предстательной железы (PSCA) (WO01/40309); анти-CD40 антитела, включая S2C6 и его гуманизированные варианты (WO00/75348), анти-CD11a (патент США № 5,622,700, WO 98/23761, Steppe с соавт., Transplant Intl. 4:3-7 (1991), и Hourmant с соавт., Transplantation 58:377-380 (1994)); анти-IgE антитела (Presta с соавт., J. Immunol. 151:2623-2632 (1993), и международная публикация № WO 95/19181), анти-CD18 (патент США № 5,622,700, выпущенный 22 апреля 1997 г, или в соответствии с публикацией WO 97/26912 от 31 июля 1997г), анти-IgE антитела (включая E25, E26 и E27, патент США № 5,714,338, выпущенный 3 февраля 1998г./ или патент США № 5,091,313, выпущенный 25 февраля 1992 г., WO 93/04173, опубликованная 4 марта 1993г., или международная заявка № PCT/US98/13410, поданная 30 июня 1998г., патент США № 5,714,338), антитело к рецептору Apo-2 (WO 98/51793, опубликованная 19 ноября 1998г.), анти-ФНО-α антитела, включая cA2 (REMICADE®), CDP571 и MAK-195 (см., патент США № 5,672,347, выпущенный 30 сентября 1997г., Lorenz с соавт., J. Immunol. 156(4):1646-1653 (1996), и Dhainaut с соавт., Crit. Care Med. 23(9):1461-1469 (1995)); антитела к тканевому фактору (TF) (европейский патент № 0 420 937 B1, выдан 9,11,1994), антитела к человеческому интегрину α4β7 (WO 98/06248, опубликована 19.02,1998), антитела к рецептору эпидермального фактора роста (EGFR) (химерное или гуманизированное антитело 225, как описано в WO 96/40210, опубликованной 19,12,1996), анти-CD3 антитела, такие как OKT3 (патент США № 4,515,893, выдан 7,5,1985), анти-CD25 или анти-tac антитела, такие как CHI-621 (SIMULECT®) и (ZENAPAX®) (см. патент США № 5,693,762, выдан 2,12,1997), анти-CD4 антитела, такие как антитело cM-7412 (Choy с соавт., Артрит Rheum 39(1):52-56 (1996)), анти-CD52 антитела, такие как CAMPATH-1H (Riechmann с соавт., Nature 332:323-337 (1988)), антитела к рецептору Fc, такие как антитело M22 против Fc.γ.RI, описанное в Graziano с соавт., J. Immunol. 155(10):4996-5002 (1995), антитела к эмбриональному опухолевому антигену (CEA), такие как hMN-14 (Sharkey с соавт., Cancer Res. 55(23 Suppl): 5935s-5945s (1995); антитела, направленные против эпителиальных клеток молочной железы, включая huBrE-3, hu-Mc 3 и CHL6 (Ceriani с соавт., Cancer Res. 55(23): 5852s-5856s (1995) и Richman с соавт., Cancer Res. 55(23 Supp): 5916s-5920s (1995)), антитела, которые связываются с клетками карциномы толстой кишки, такие как C242 (Litton с соавт., Eur J. Immunol. 26(1): 1-9 (1996)), анти-CD38 антитела, например, AT13/5 (Ellis с соавт., J. Immunol. 155(2):925-937 (1995)): анти-CD33 антитела, такие как Hu M195 (Jurcic с соавт., Cancer Res 55(23 Suppl):5908s-5910s (1995) и CMA-676 или CDP771, анти-CD22 антитела, такие как LL2 или LymphoCide (Juweid с соавт., Cancer Res 55(23 Suppl):5899s-5907s (1995)), анти-EpCAM антитела, такие как 17-1A (PANOREX®), анти-GpIIb/IIIa антитела, такие как абциксимаб или c7E3 Fab (REOPRO®), антитела против респираторного синцитиального вируса, такие как MEDI-493 (SYNAGIS®), антитела к цитомегаловирусу, такие как PROTOVIR®, антитела к ВИЧ, такие как PRO542, антитела к вирусу гепатита, такие как антитело к вирусу гепатита B OSTAVIR®, анти-CA125 антитело OvaRex; антитело GD3 к идиопатическому эпитопу BEC2, анти-αvβ3 антитело VITAXIN®., антитела к почечноклеточной карциноме человека, такие как ch-G250; ING-1, антитело к 17-1A человека (3622W94), антитело к колоректальной опухоли человека (A33), антитело R24 к к меланоме человека, направленное против ганглиозида GD3, антитело против плоскоклеточной карциномы (SF-25), и антитела против человеческого лейкоцитарного антигена (HLA), такие как Smart ID10 и анти-HLA DR антитело Oncolym (Lym-1). Предпочтительными антигенами - -мишенями для антител являются: рецептор HER2, фактор роста эпителия сосудов VEGF, IgE, CD20, CD11a и CD40.
Примеры ниже приведены с целью иллюстрации, но не ограничения изобретения.
ПРИМЕРЫ
Пример 1: Влияние pH пулы клеток, температуры хранения и времени хранения на выживаемость размороженных клеток
Способ добавления основания для контроля pH при хранении (Исследование на уменьшенной модели №1)
Исследование выполняли для оценки возможности осуществимости выполнения корректировки pH в наихудшем случае и в условиях обычного пула (целевые начальные значения pH 6,2 и 6,7, соответственно) для улучшения выхода при размораживании. Изучали корректировку до нескольких целевых рН для определения оптимального pH при хранении. pH измеряли с использованием прибора BioProfile® 400 (Nova Biomedical) с заданной температурой 37°C. Аналогично, расчеты pH с использованием Уравнения 1 основаны на температуре образца 37°C.
Клетки осаждали посредством центрифугирования. Пулы клеток получали для каждого набора исследуемых условий посредством ресуспендирования клеток до концентрации 100×106 клеток/мл в истощенной среде. Указанные пулы клеток взбалтывали при 37°C с газопроницаемыми мембранами для обмена CO2/O2 или без них для приведения pH к начальным условиям pH (6,2 или 6,7). При достижении целевых начальных значений pH пулы клеток быстро охлаждали <10°C и 20% (об./об.) и добавляли среду для замораживания с ДМСО (1:3 частям жидкости культуры клеток). Корректировку рН осуществляли с использованием Уравнения 1 для расчета объемов добавляемого 1M карбоната натрия, необходимых для достижения целевых значений pH 6,9, 7,1 и 7,3, и осуществляли окончательное автономное измерение pH для подтверждения подходящего увеличения значения pH перед получением контрольных клеток для хранения (действительное значение pH при хранении было 6,9, 7,1/7,2 и 7,5).
Результаты размораживания продемонстрировали существенное улучшение жизнеспособности через 1 день до 68% (от 24% до 92% для корректировки с pH 6,2 до 7,5) (Фиг. 2A), и улучшение через 4 дня до 0,64% (от 0,17% до 0,81% для корректировки с pH 6,2 до 7,5) (Фиг. 2B).
Уравнение 1: Расчет объема добавляемого раствора основания для корректировки pH
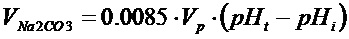 ,
,
где VNa2CO3=Объем добавляемого 1M карбоната натрия, Vp=Объем пулы клеток,
pHt=целевое значение pH, pHi=начальное значение pH,
Способ добавления основания для контроля pH при хранении (Дополнительные исследования pH на уменьшенной модели)
В соответствии со сходными процедурами, описанными выше, проводили несколько исследований для изучения влияния корректировки рН на дополнительные линии клеток.
В общей сложности отобрали девять линий клеток CHO, относящихся к различным типам клеток (DP12, CHO-K1). В течение нескольких дней перед помещением на длительное хранение, клетки поддерживали в соответствии со стандартными протоколами. Клетки осаждали посредством центрифугирования и получали приблизительно 60-90 мл контрольных популяций клеток для каждого из исследуемых условий посредством ресуспендирования в истощенной среде до достижения объема осажденных клеток 28% (packed cell volume, PCV, ООК). Указанные пулы клеток встряхивали при 37° с газопроницаемыми мембранами для обмена CO2/O2 или без них для приведения pH к начальным условиям pH (6,2 или 6,7). Эти два начальные значения pH были выбраны для имитации наихудшего возможного случая и обычных условий, наблюдаемых при концентрирования с пользованием половолоконного фильтра и после него. При достижении начальных целевых значений pH, пулы клеток быстро охлаждали до <10°C и добавляли 20% (об./об.) среды для замораживания с ДМСО (1:3 частям жидкости культуры клеток)для достижения окончательного объема консервируемых клеток 21%. Корректировку значений рН осуществляли после использования Уравнения 1 для расчета требуемого объема добавки 1M карбоната натрия для корректировки pH до 7,0, 7,3, 7,6 или 8,0. осуществляли окончательное автономное измерение pH для подтверждения подходящего увеличения значения pH перед получением клеток для хранения.
Во всех случаях образцы размораживали в двух повторах, где в каждый сосуд размораживали одну ампулу. Результаты продемонстрировали, что клетки всех типов, ранее подвергавшихся воздействию низких pH, способны восстанавливаться при корректировке рН до значений выше 7,3 перед помещением на хранение. Каждая линия клеток продемонстрировала различную чувствительность к рН при хранении. Корректировка pH до значения приблизительно 7,5 в большинстве случаев обеспечивала жизнеспособность выше 80% в день 1 после размораживания (Фиг. 3A-3F и Фиг. 4A-4B). На скорость роста после размораживания влияли только самые низкие из исследованных значения pH. Что интересно, самые высокие из исследованных значения pH (около 8,0-8,2) не оказывали негативное влияние на восстановление после размораживания, несмотря на то, что они был значительно выше нормального физиологического значения pH.
Указанные исследования (изучение клеток типа CHO-K1) продолжили чтобы получить больше информации о длительном воздействии высоких значений pH. В этих исследованиях изучали исследовали имитацию банка клеток, замороженного сразу (t0) после корректировки рН (аналогично всем ранее описанным исследованиям на уменьшенной модели) и, во второй момент времени, через 2 ч (t2). В ходе указанного выдерживания в течение 2 ч, небольшие пулы клеток (приблизительно 10 мл в каждом случае) выдерживали в пробирках Falcon®, погруженных во влажный лед. На стадии выдерживания наблюдался небольшой сдвиг значения pH, приведший к изменению до 0,2 единиц pH. Результаты этих исследований продемонстрировали, что выдерживание в течение 2 ч в этом диапазоне значений pH, изученных в ходе исследования, не оказывает какого-либо влияния (пример приведен на Фиг. 6A-6B).
Способы охлаждения жидкости культуры клеток в ходе сбора клеток
Способ «медленного сбора клеток с помощью насоса» в комбинации с охлаждающим теплообменником адаптировали для добавления возможности охлаждения в традиционных процессах помещения клеток на хранение. В частности, указанный процесс «медленного сбора клеток с помощью насоса» требовал снижения обычной скорости потока при сборе клеток с приблизительно 4 л/мин до 600 мл/мин для соответствия скоростям сбора, используемым для традиционных процедур получения клеток для хранения. Трубопровод охлаждающего теплообменника, представляющий собой силиконовую трубку 15 размера длиной 15 футов, покрытую осажденной платиной, погруженную во влажный лед, был размещен в канале для сбора клеток. Измерение температуры, полученной в ходе контрольного пропускания воды, продемонстрировало, что указанный «способ сбора клеток с охлаждением» позволяет добиться снижения температуры культуры до приблизительно 12°C в течение первых 30 минут перед концентрированием при использовании половолоконного фильтра. Основываясь на данных, полученных при 10°C, эта возможность охлаждения с большой вероятностью приведет к приостановке клеточного метаболизма и предотвратит смещение значения pH в кислую область.
Процесс подтверждения результатов исследования
Процесс хранения клеток в банке. Образцы клеток для хранения получали сначала путем наработки адаптированных к суспензии клеток CHO путем культивирования вв периодической культуре с подкормкой/перфузионной культуре с последующим сбором клеток для хранения в банке. Исходный источник клеток был из ГБК (из потомства РБК). Указанный способ включал три стадии: наработку клеток, сбор и концентрирование клеток, и хранение клеток в банке. Целью стадии накопления клеток было получение количества клеток, требующегося для получения полноразмерного ГБК или РБК (420×1 мл или 10 мл ампулы, соответственно) в одной партии. Клетки выращивали в селективной среде для системы посевных ферментеров в ходе начального процесса масштабирования и в ходе процесса с качающимся биореактором. Стадия сбора клеток служит для концентрирования конечной культуры клеток с помощью половолоконного фильтра (HFF) для обеспечения плотности клеток, необходимой для хранения в банке. Последующий процесс объединения в пул и заполнения служит для приготовления ампул с клетками для хранения в банке в течение длительного времени. Процесс объединения в пул осуществляли во влажном льду для поддержания температуры в определенном диапазоне (около 5-10°C). Последовательность операций указанного способа показана на Фиг. 1.
Процессы сбора и концентрирования клеток осуществляли с использованием картриджа с половолоконным фильтром. Измерение изменения значений pH продемонстрировало, что указанный «способ сбора клеток с охлаждением» обеспечивал эффективное снижение сдвига значения pH в ходе концентрирования клеток приблизительно на 0,35 единицы pH (с ~6,30 до 6,66 для исходного процесса и процесса «с охлаждением», соответственно). После корректировки значения рН получали пулы охлажденных клеток, предназначенных для хранения, в начальный (0 мин) и более поздний (120 мин) моменты времени для проверки промежуточного влияния поддержания значения рН пулы клеток.
Полученные после хранения пулы клеток оценивали по их активности в первичной культуре. Ампулы с клетками после хранения оттаивали в колбах для культивирования, а не в биореакторах с использованием серийного разведения 1:250 (1:10, затем 1:25). Результаты размораживания успешно продемонстрировали, что указанный способ (сбор с охлаждением и корректировка рН) пригоден для получения популяций клеток для хранения в банке с приемлемым качеством после размораживания. При том, что пулы клеток для хранения в банке, полученные в ходе исходного обычного способа, демонстрировали снижение жизнеспособности, эти новые пулы клеток для хранения в банке были стабильными и уровень их жизнеспособности через 1 день составлял 79,1-85,3% (приблизительно 65% улучшение). Не наблюдалось никакого неблагоприятного влияния выдерживания клеток при повышенных значениях pH в течение времени.
Исследование продемонстрировало, что клетки из пулы клеток, подвергнутых корректировке до более высоких значений pH, были меньшего размера (Фиг. 5). Это наблюдаемое изменение в размере может указывать на то, что более высокие значения pH вызывают обезвоживание клеток (вероятно ввиду повышенного осмотического давления или повышенной эластичности клеточной мембраны, приводящей к сжатию клеток, или ввиду обоих факторов).
Выводы
Оказалось, что pH при хранении в банке является крайне важным для результатов размораживания, и могут изменять значения жизнеспособности клеток в день 1 после размораживания на величину до 65%. Соответственно, были разработаны технологические улучшения процедур сбора и хранения в банке для уменьшения воздействия на клетки низких pH улучшения контроля pH в процессе хранения в банке. По сути, предложены два улучшения процесса, включая: 1) охлаждение культуральной жидкости клеточной культуры в ходе при помощи силиконового трубчатого теплообменника; и 2) применение корректировки pH для повышения pH при хранении в банке до 7,5.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ СОЗДАНИЯ БАНКОВ КЛЕТОК СО СВЕРХВЫСОКОЙ ПЛОТНОСТЬЮ | 2015 |
|
RU2826038C2 |
| СПОСОБЫ СОЗДАНИЯ БАНКОВ КЛЕТОК СО СВЕРХВЫСОКОЙ ПЛОТНОСТЬЮ | 2015 |
|
RU2723129C2 |
| СПОСОБЫ ФОРМИРОВАНИЯ БАНКА КЛЕТОК ВЫСОКОЙ ПЛОТНОСТИ (ВАРИАНТЫ) | 2014 |
|
RU2668796C2 |
| СПОСОБЫ ПРИГОТОВЛЕНИЯ ПОЛОКСАМЕРА ДЛЯ ПРИМЕНЕНИЯ В КЛЕТОЧНОЙ КУЛЬТУРАЛЬНОЙ СРЕДЕ | 2015 |
|
RU2710551C2 |
| КОМПОЗИЦИИ КЛЕТОЧНЫХ КУЛЬТУР С АНТИОКСИДАНТАМИ И СПОСОБЫ ПОЛУЧЕНИЯ ПОЛИПЕПТИДОВ | 2014 |
|
RU2718986C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ КЛЕТОК МЛЕКОПИТАЮЩИХ И ПОЛУЧЕНИЕ ПОЛИПЕПТИДОВ С ИСПОЛЬЗОВАНИЕМ КОМПОЗИЦИИ КЛЕТОЧНОЙ КУЛЬТУРЫ | 2013 |
|
RU2678142C2 |
| СПОСОБЫ ОЧИСТКИ ПОЛИПЕПТИДОВ | 2011 |
|
RU2594163C2 |
| УЛУЧШЕННАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ КЛЕТОК | 2011 |
|
RU2798069C2 |
| СПОСОБЫ ИНАКТИВАЦИИ ВИРУСА С ИСПОЛЬЗОВАНИЕМ ЭКОЛОГИЧНЫХ ДЕТЕРГЕНТОВ | 2014 |
|
RU2707951C1 |
| СПОСОБЫ ИНАКТИВАЦИИ ВИРУСОВ И БАКТЕРИЙ В КЛЕТОЧНОЙ КУЛЬТУРАЛЬНОЙ СРЕДЕ | 2013 |
|
RU2685203C2 |
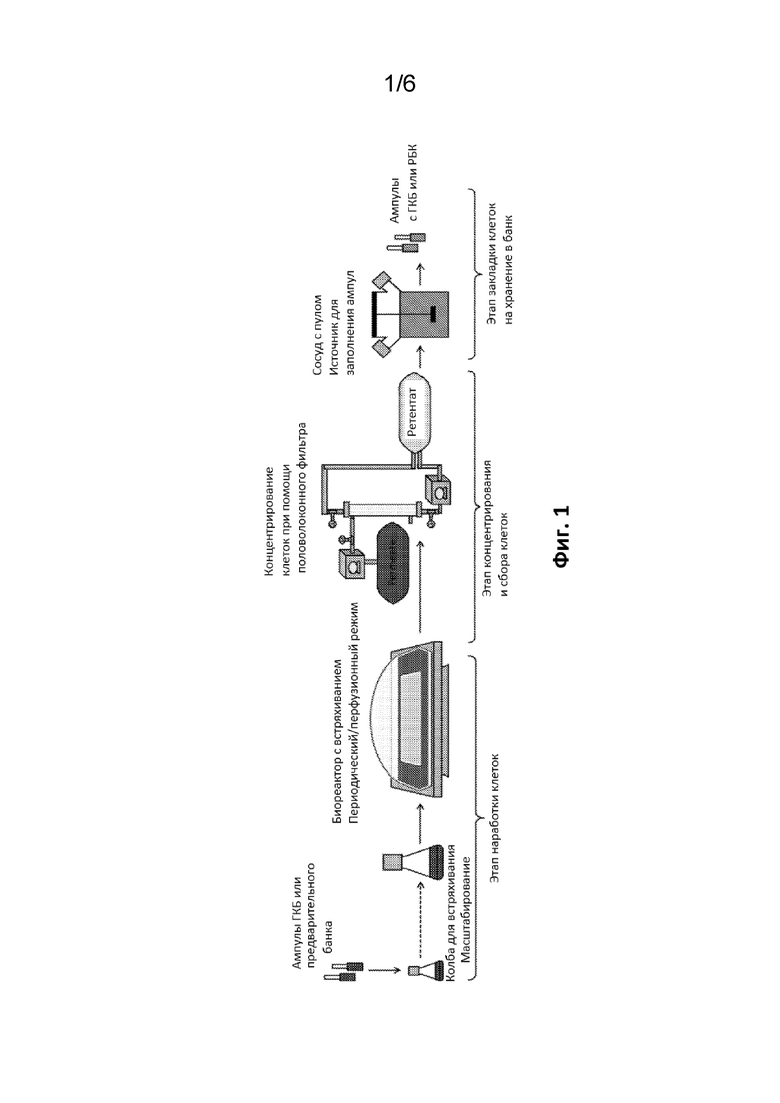

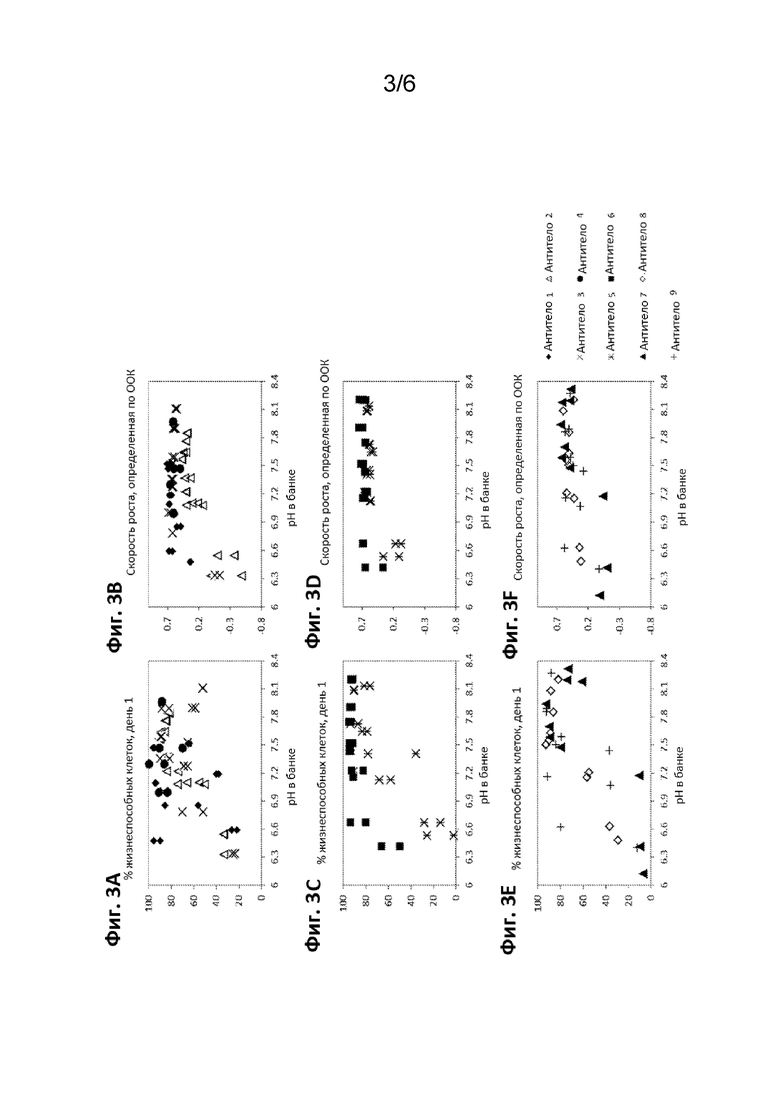
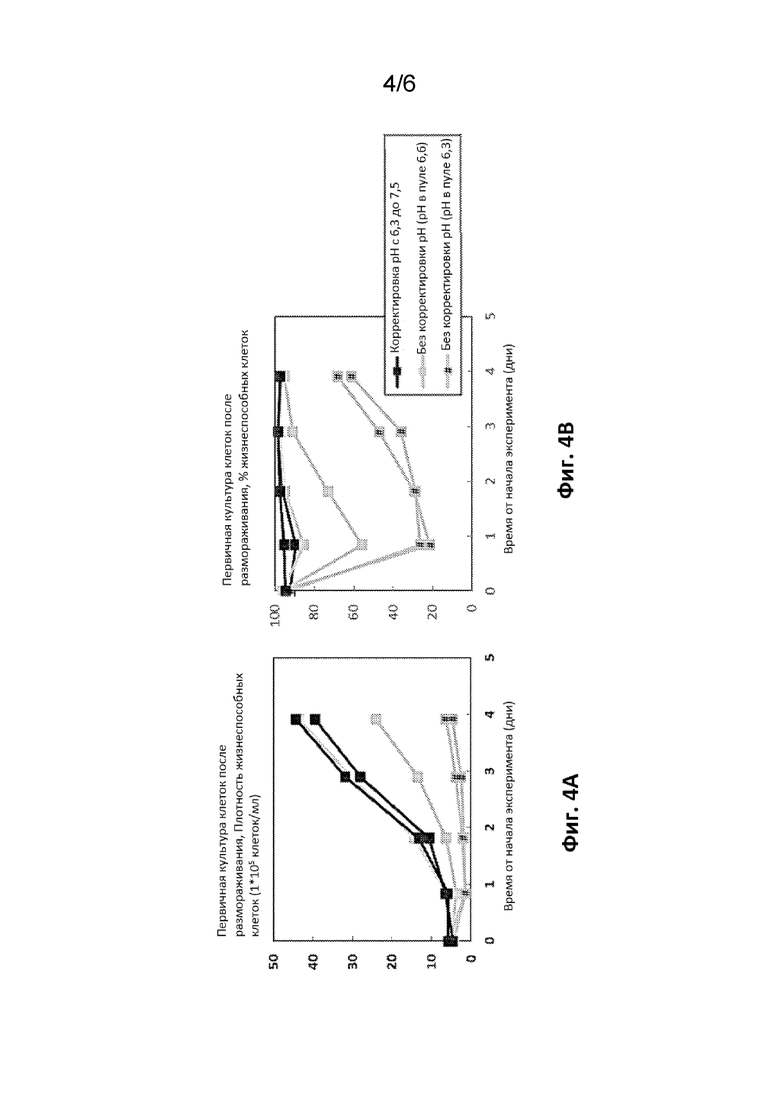
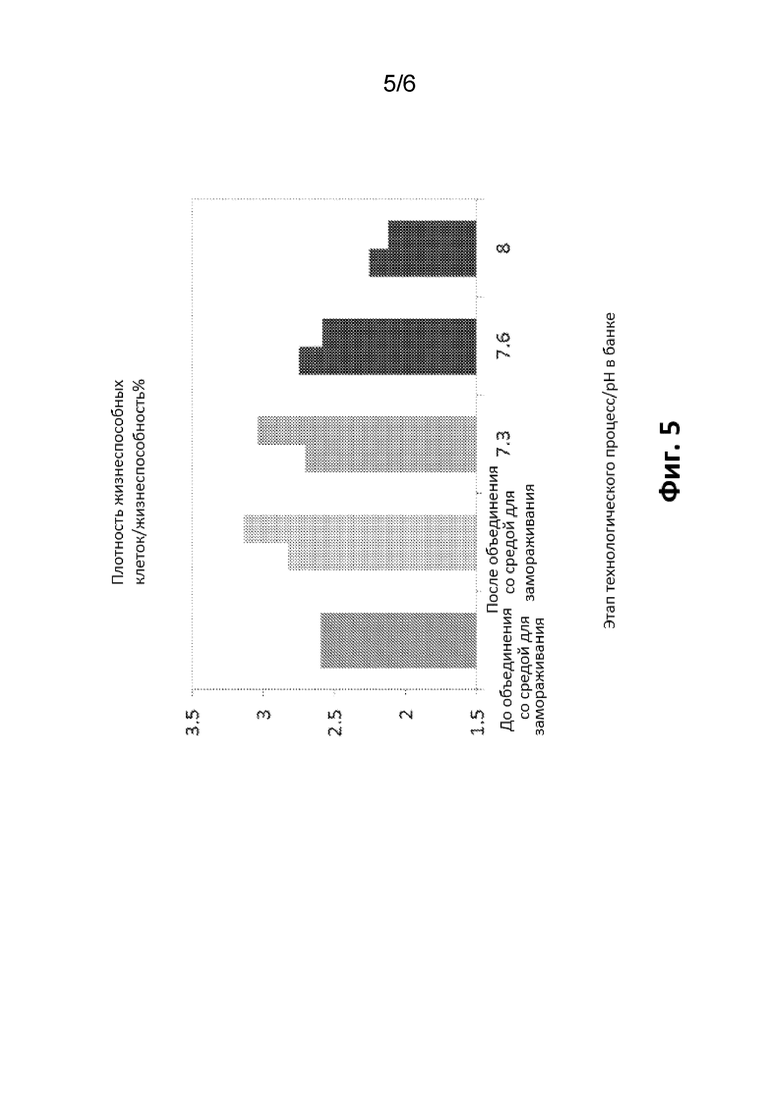
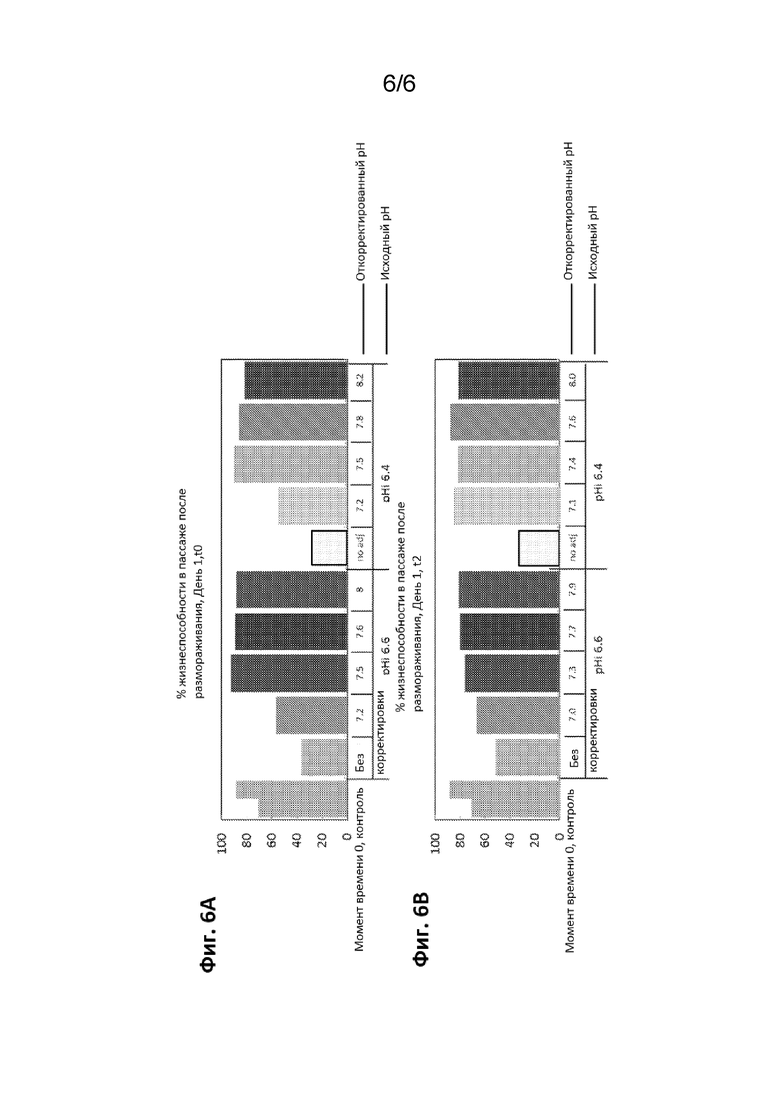
Изобретение относится к области биотехнологии, а именно к улучшению размораживания банков клеток, замораживанию клеток яичника китайского хомячка (СНО), композиции для замораживания клеток СНО и банку клеток. Способ включает замораживание клеток CHO в среде для замораживания, которая содержит буферный раствор и DMSO, при рН среды для замораживания, доведенном до от 7,5 до 8,5 перед замораживанием. Изобретение позволяет повысить жизнеспособность и скорость роста клеток при оттаивании. 6 н. и 63 з.п. ф-лы, 6 ил., 1 пр.
1. Способ улучшения размораживания банков клеток, включающий замораживание клеток яичника китайского хомячка (CHO) для хранения в банке в среде для замораживания, отличающийся тем, что среда для замораживания содержит буферный раствор и DMSO, и при этом рН среды для замораживания был доведен до от 7,5 до 8,5 перед замораживанием.
2. Способ замораживания клеток CHO для хранения, включающий замораживание клеток CHO в среде для замораживания, отличающийся тем, что среда для замораживания содержит буферный раствор и DMSO, и при этом рН среды для замораживания был доведен до от 7,5 до 8,5 перед замораживанием.
3. Способ по п. 1 или 2, отличающийся тем, что pH среды для замораживания откорректирован до значения pH, равного 7,5.
4. Способ по п. 1 или 2, отличающийся тем, что клетки объединяют со средой для замораживания до и/или после корректировки pH.
5. Способ по п. 1 или 2, отличающийся тем, что откорректированный pH представляет собой целевой pH или измеренный pH.
6. Способ по п. 5, отличающийся тем, что целевой pH равен от 7,5 до 8,3.
7. Способ по п. 5, отличающийся тем, что измеренный pH равен от 7,5 до 8,3.
8. Способ по п. 1 или 2, дополнительно включающий этап измерения исходного pH среды для замораживания, содержащей клетки, перед корректировкой pH среды для замораживания.
9. Способ по п. 1 или 2, дополнительно включающий этап измерения откорректированного pH среды для замораживания.
10. Способ по п. 9, отличающийся тем, что если измеренный pH среды для замораживания ниже целевого pH, повторяют этап корректировки и этап измерения до достижения откорректированного pH среды для замораживания от 7,5 до 8,3.
11. Способ по п. 1 или 2, отличающийся тем, что pH корректируют путем добавления основания.
12. Способ по п. 11, отличающийся тем, что основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксида натрия и гидроксида калия.
13. Способ по п. 1, отличающийся тем, что pH среды для замораживания корректируют путем добавления основания в среду для замораживания в соответствии со следующей формулой: Vbase=Cbase*Vp (pHt-pHi), где Cbase представляет собой коэффициент, значение которого зависит от основания, Vbase представляет собой объем основания, добавляемый в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
14. Способ по п. 13, отличающийся тем, что pH среды для замораживания корректируют путем добавления карбонат натрия в среду для замораживания в соответствии со следующей формулой: 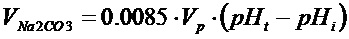 , где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
, где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
15. Способ по п. 13, отличающийся тем, что целевой pH составляет от 7,5 до 8,3.
16. Способ по п. 1 или 2, отличающийся тем, что клетки CHO находятся в среде с pH от 6,2 до 6,6 перед объединением клеток CHO со средой для замораживания.
17. Способ по п. 1 или 2, отличающийся тем, что концентрация DMSO в среде для замораживания перед замораживанием составляет от 5% до 12,5% по объему.
18. Способ по п. 17, отличающийся тем, что концентрация DMSO в среде для замораживания перед замораживанием составляет от 5% до 10% по объему.
19. Способ по п. 1 или 2, отличающийся тем, что среда для замораживания, содержащая клетки CHO, имеет плотность клеток, определенную как объем осажденных клеток (PCV), от 8% до 28% перед замораживанием.
20. Способ по п. 1 или 2, дополнительно включающий этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток CHO со средой для замораживания.
21. Способ по п. 20, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 20°C.
22. Способ по п. 20, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 10°C.
23. Способ замораживания клеток CHO для хранения, включающий (a) корректировку pH среды для замораживания, содержащей клетки CHO, до pH от 7,5 до 8,5, причем среда для замораживания содержит буферный раствор и DMSO; и (b) замораживание клеток CHO.
24. Способ по п. 23, отличающийся тем, что pH корректируют до от 7,5 до 8,3.
25. Способ по п. 23, отличающийся тем, что pH корректируют до pH 7,5.
26. Способ по п. 23, отличающийся тем, что откорректированный pH представляет собой целевой pH или измеренный pH.
27. Способ по п. 26, отличающийся тем, что целевой pH равен от 7,5 до 8,3.
28. Способ по п. 26, отличающийся тем, что измеренный pH равен от 7,5 до 8,3.
29. Способ по п. 23, дополнительно включающий этап измерения исходного pH среды для замораживания, содержащей клетки, перед корректировкой pH среды для замораживания.
30. Способ по п. 23, дополнительно включающий этап измерения откорректированного pH среды для замораживания.
31. Способ по п. 30, отличающийся тем, что если измеренный pH среды для замораживания ниже целевого pH, повторяют этап корректировки и этап измерения до достижения откорректированного pH среды для замораживания от 7,5 до 8,5.
32. Способ по п. 23, отличающийся тем, что pH корректируют путем добавления основания.
33. Способ по п. 32, отличающийся тем, что основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксида натрия и гидроксида калия.
34. Способ по п. 32, отличающийся тем, что pH среды для замораживания корректируют путем добавления основания в среду для замораживания в соответствии со следующей формулой: Vbase=Cbase*Vp (pHt-pHi), где Cbase представляет собой коэффициент, значение которого зависит от основания, Vbase представляет собой объем основания, добавляемый в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
35. Способ по п. 32, отличающийся тем, что pH среды для замораживания корректируют путем добавления карбоната натрия в среду для замораживания в соответствии со следующей формулой: 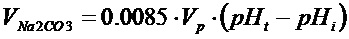 , где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
, где VNa2CO3 представляет собой объем 1M карбоната натрия для добавления в среду для замораживания, Vp представляет собой объем среды для замораживания, pHt представляет собой целевой pH и pHi представляет собой исходный pH.
36. Способ по п. 34, отличающийся тем, что целевой pH составляет от 7,5 до 8,3.
37. Способ по п. 23, отличающийся тем, что клетки CHO находятся в среде с pH от 6,2 до 6,6 перед объединением клеток CHO со средой для замораживания.
38. Способ по п. 23, отличающийся тем, что концентрация DMSO в среде для замораживания, содержащей клетки CHO, перед замораживанием составляет от 5% до 12,5% по объему.
39. Способ по п. 38, отличающийся тем, что концентрация DMSO в среде для замораживания, содержащей клетки CHO, перед замораживанием составляет от 5% до 10% по объему.
40. Способ по п. 23, отличающийся тем, что среда для замораживания, содержащая клетки CHO, имеет плотность клеток, определенную как объем осажденных клеток (PCV), от 8% до 28% перед замораживанием.
41. Способ по п. 23, дополнительно включающий этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток CHO со средой для замораживания.
42. Способ по п. 41, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 20°C.
43. Способ по п. 41, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 10°C.
44. Способ замораживания клеток CHO для хранения, включающий (a) корректировку pH среды для замораживания до pH от 7,5 до 8,5, причем среда для замораживания содержит буферный раствор и DMSO; (b) объединение клеток CHO со средой для замораживания с получением пула клеток и (c) замораживание клеток CHO в пуле клеток.
45. Способ по п. 44, отличающийся тем, что pH корректируют до значения pH 7,5.
46. Способ по п. 44, отличающийся тем, что откорректированный pH представляет собой целевой pH или измеренный pH.
47. Способ по п. 46, отличающийся тем, что целевой pH равен от 7,5 до 8,3.
48. Способ по п. 46, отличающийся тем, что измеренный pH равен от 7,5 до 8,3.
49. Способ по п. 44, дополнительно включающий этап измерения откорректированного pH среды для замораживания.
50. Способ по п. 44, отличающийся тем, что если измеренный pH среды для замораживания ниже целевого pH, этап корректировки и этап измерения повторяют до достижения откорректированного pH среды для замораживания от 7,5 до 8,5.
51. Способ по п. 44, отличающийся тем, что pH корректируют путем добавления основания.
52. Способ по п. 51, отличающийся тем, что основание выбирают из группы, состоящей из карбоната натрия, бикарбоната натрия, натриевой соли N-2-гидроксиэтилпиперазин-N-2-этансульфоновой кислоты, гидроксида натрия и гидроксида калия.
53. Способ по п. 44, отличающийся тем, что клетки CHO находятся в среде с pH от 6,2 до 6,6 перед объединением клеток CHO со средой для замораживания.
54. Способ по п. 44, отличающийся тем, что концентрация DMSO в пуле клеток составляет от 5% до 12,5% по объему.
55. Способ по п. 54, отличающийся тем, что концентрация DMSO в пуле клеток составляет от 5% до 10% по объему.
56. Способ по п. 44, отличающийся тем, что пул клеток содержит клетки CHO при плотности клеток, определенной как объем осажденных клеток (PCV), от 8% до 28%.
57. Способ по п. 44, дополнительно включающий этап охлаждения жидкой культуры клеток в процессе сбора и концентрирования клеток перед объединением клеток CHO со средой для замораживания.
58. Способ по п. 57, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 20oC.
59. Способ по п. 57, отличающийся тем, что жидкую культуру клеток охлаждают до температуры, равной или более низкой чем 10oC.
60. Способ по любому из пп. 1, 2, 23 или 44, отличающийся тем, что клетки CHO содержат нуклеиновую кислоту, кодирующую полипептид.
61. Способ по п. 60, отличающийся тем, что полипептид представляет собой терапевтический белок.
62. Способ по п. 61, отличающийся тем, что терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
63. Композиция для замораживания клеток CHO, где композиция содержит буферный раствор, DMSO и клетки CHO, содержащие нуклеиновую кислоту, кодирующую полипептид, отличающаяся тем, что pH среды равен от 7,5 до 8,5 перед замораживанием клеток.
64. Композиция по п. 63, отличающаяся тем, что полипептид представляет собой терапевтический белок.
65. Композиция по п. 64, отличающаяся тем, что терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
66. Банк клеток, содержащий множество контейнеров, причем каждый контейнер содержит (a) среду для замораживания, содержащую буферный раствор и DMSO, и (b) клетки CHO, содержащие нуклеиновую кислоту, кодирующую полипептид, причем рН среды для замораживания равен от 7,5 до 8,5 перед замораживанием клеток.
67. Банк клеток по п. 66, отличающийся тем, что контейнеры представляют собой ампулы.
68. Банк клеток по п. 66, отличающийся тем, что полипептид представляет собой терапевтический белок.
69. Банк клеток по п. 68, отличающийся тем, что терапевтический белок выбран из группы, состоящей из антитела, фрагмента антитела, фермента и рецепторного белка слияния.
| WO 1993014191 A1, 22.07.1993 | |||
| СПОСОБ КРИОКОНСЕРВАЦИИ КЛЕТОК ФОТОТРОФНЫХ МИКРООРГАНИЗМОВ | 2012 |
|
RU2508397C1 |
| US 2009029340 A1, 29.01.2009. | |||
Авторы
Даты
2020-02-19—Публикация
2015-07-09—Подача