Синдром системной воспалительной реакции (SIRS) представляет собой воспалительное состояние всего организма без конкретного источника инфекции. Его могут вызывать многие факторы, включая, но, не ограничиваясь ими, травму, операцию, недостаточность надпочечников, эмболию легких, инфаркт миокарда, кровотечение, анафилаксию, передозировку лекарственным средством, иммунодефицит и ожоги. Существует четыре основных диагностических симптома SIRS, как указано ниже, но наличие любых двух таких симптомов является достаточным для диагноза (см., например, Nystrom (1998) Journal of Antimicrobial Chemotherapy, 41, Suppl. A, 1-7).
i) частота сердечных сокращения более 90 ударов в минуту;
ii) температура тела ниже 36°C или выше 38°C;
iii) частота дыхания более 20 вдохов в минуту (тахипноэ) и
vi) число лейкоцитов менее 4000 клеток/мм3 или более 12000 клеток/мм3 или наличие более 10% незрелых нейтрофилов.
SIRS вызывает обширную активацию иммуногенных белков острой фазы, нарушающих систему комплемента и пути свертывания, что в свою очередь вызывает повреждения сосудистой системы, а также внутренних органов. Затем активируются различные нейроэндокринные контррегуляторные системы, которые часто усугубляют проблему.
Сепсис является конкретной формой SIRS, и наиболее распространенной причиной смерти в отделениях интенсивной терапии. Он вызывается подозреваемой или установленной инфекцией. Сепсис характеризуется гиперактивной и несбалансированной сети эндогенных провоспалительных цитокинов и часто приводит к обширному воспалению и тромбообразованию, которое может приводить к покраснению, жару, отеку, боли, дисфункции органа или органной недостаточности. Тромбообразование вовремя сепсиса также может вызывать сниженный приток крови к конечностям и жизненно важным органам и может приводить к органной недостаточности или началу гангрены.
Аналогично SIRS, сепсис, как правило, приводит к острому воспалению, присутствующему во всем организме, и, таким образом, обычно ассоциирован с лихорадкой и лейкоцитозом (повышенное количество лейкоцитов в крови). Современная теория сепсиса сводится к тому, что иммунный ответ хозяина на инфекцию запускает SIRS, который в свою очередь вызывает симптомы, описанные выше. Вслед за инфекцией и сепсисом кровоснабжение ткани и доставка кислорода могут восстанавливаться, приводя к септическому шоку. Для постановки диагноза септический шок у пациента должны присутствовать инфекция и стойкая артериальная гипотензия.
SIRS, сепсис и септический шок представляют собой тяжелые медицинские состояния. Даже при срочном и интенсивном лечении эти заболевания с большой вероятностью прогрессирую в синдром полиорганной недостаточности и могут даже приводить к гибели.
Большинство терапевтических стратегий в настоящее время направлены на провоспалительные медиаторы, но при исследовании в больших многоцентровых клинических испытаниях не было выявлено, что они улучшают выживаемость пациентов. Для видов терапии, предназначенных блокировать один единственный цитокин, такой как TNFα и IL-1β, демонстрировали ограниченную эффективность вследствие ранней и переходной кинетики этих воспалительных цитокинов. Недавно международные эксперты в области интенсивно терапии и инфекционных заболеваний разработали руководство по ведению больных для улучшения лечения, проводимого у пациентов, страдающих SIRS, сепсисом или септическим шоком. Эти руководства направлены на изменение комплексной диагностики и выборов способа лечения в простые "особо важные" задачи и в числе других видов лечения предполагают введение антибиотиков широкого спектра действия, стероидов и дротрекогина альфа (активированного).
Однако уровень смертности, связанной с сепсисом, остается от 30% до 50%, при этом опубликовано уровень смертности от септического шока является даже выше от 50% до 60%. Опубликовано приблизительно 750000 новых случаев сепсиса каждый год, где по меньшей мере 210000 из них приводит к летальному исходу. Вследствие того, что виды медицинского лечения становятся все более агрессивными, частота возникновения SIRS, сепсиса и септического шока, вероятно, возрастет, и, таким образом, необходимым является новое надежное лечение этих состояний.
Сущность изобретения
Было выявлено, что введение мезенхимальных стромальных клеток (MSC), в частности стромальных клеток жировой ткани человека (hASC) является пригодным для лечения SIRS, сепсиса, тяжелого сепсиса и септического шока. Например, было выявлено MSC, в частности hASC, защищают от смертности при пневмонии, связанной с сепсисом, что обеспечивает доказательство того, что MSC могут являться пригодными для лечения SIRS, сепсиса и септического шока. Было выявлено, что MSC функционируют на нескольких уровнях, регулируя критические аспекты SIRS, сепсиса, тяжелого сепсиса и септического шока, включая путем снижения общих уровней различных воспалительных цитокинов и хемокинов и путем ингибирования инфильтрации лейкоцитов в различные органы-мишени.
Таким образом, в одном из аспектов изобретение относится композиции, содержащей мезенхимальные стромальные клетки (MSC), для применения в лечении сепсиса у индивидуума, страдающего пневмонией или после пневмонии, например, для применения в способе лечения сепсиса у индивидуума, страдающего пневмонией или после пневмонии.
Изобретение также относится к применению мезенхимальных стромальных клеток (MSC) в производстве лекарственного средства для лечения сепсиса у индивидуума, страдающего пневмонией или после пневмонии.
Изобретение также относится к способу лечения сепсиса у индивидуума, страдающего пневмонией или после пневмонии, включающему введение мезенхимальных стромальных клеток (MSC) индивидууму.
Эти и другие аспекты изобретения более подробно описаны ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры 1-4: бактериальная нагрузка в различных тканях через 48 часов после инфекции. На A и B представлены результаты двух независимых экспериментов. Плацебо=обработка лактатом Рингера; ASC=обработка ASC; КОЕ=колониеобразующие единицы. Фигура 1: кровь; фигура 2: гомогенат легких; фигура 3: гомогенат печени и фигура 4: гомогенат селезенки.
Фигуры 5-8: уровни цитокинов и хемокинов в гомогенатах легких через 48 часов после инфекции. На A и B представлены результаты двух независимых экспериментов. Плацебо=обработка лактатом Рингера; ASC=обработка ASC. Фигура 5: TNFα; фигура 6: IL1β; фигура 7: IL6 и фигура 8: Mip-2.
Фигуры 9-12: бактериальная нагрузка в различных тканях после инфекции. Плацебо=обработка лактатом Рингера; ASC=обработка ASC; КОЕ=колониеобразующие единицы. Фигура 9: кровь; фигура 10: гомогенат легких; фигура 11: гомогенат печени и фигура 12: гомогенат селезенки.
ОПРЕДЕЛЕНИЯ
Как используют в настоящем описании, следующие ниже термины и фразы имеют значения, указанные ниже. Если не определено иное, все технические и научные термины, используемые в настоящем описании, имеют то же значение, как и общепринято понимаемые специалистом в данной области, к которой принадлежит данное изобретение.
Формы единственного числа относятся к одному или более чем одному (т.е. по меньшей мере к одному) объекту. В качестве примера, "элемент" означает один элемент или более одного элемента.
Термин "приблизительно", когда его используют по отношению к значению, относится к значению ±10%.
Под "жировой тканью" подразумевают любую жировую ткань. Жировая ткань может представлять собой бурую или белую жировую ткань, получаемую, например, из подкожного, сальникового/висцерального, грудного, относящегося к половым железам или другого участка жировой ткани. Предпочтительно жировая ткань представляет собой подкожную белую жировую ткань. Жировая ткань может содержать первичную культуру клеток или иммортализованную линию клеток. Жировая ткань может быть сформирована любым организмом, содержащим жировую ткань. В некоторых вариантах осуществления жировая ткань представляет собой жировую ткань млекопитающего и в дополнительных вариантах осуществления жировую ткань человека. Подходящим источником жировой ткани является хирургическая липосакция. Однако следует понимать, что ни источник жировой ткани, ни способ выделения жировой ткани не является критичным для изобретения. Если клетки, как описано в настоящем описании, желательно аутологично трансплантировать индивидууму, жировую ткань можно выделять у такого индивидуума.
"Стромальные клетки жировой ткани (ASC)" относятся к MSC, которые происходят из жировой ткани, как правило, из жировой ткани человека (hASC).
Следует понимать, что термин "биологический лекарственный препарат" означает фармацевтическое вещество на основе белка или нуклеиновой кислоты для терапевтического использования, которое, как правило, получают способами, отличными от прямой экстракции из нативного (неконструированного) биологического источника.
Как используют в настоящем описании, следует понимать, что термин "клетки/кг" означает количество клеток (например, MSC), вводимых на килограмм массы тела пациента.
Подразумевают, что термин "конститутивно" означает экспрессию гена без какой-либо специальной индукции.
Термин "культура" относится к росту клеток, организмов, многоклеточных организмов или ткани в среде. Термин "культивирование" относится к любому способу получения такого роста и может включать многие этапы. Термин "дальнейшее культивирование" относится к культивированию клетки, организма, многоклеточного организма или ткани до определенной стадии роста, затем использованию другого способа культивирования с приведением указанной клетки, организма, многоклеточного организма или ткани к другой стадии роста. "Культура клеток" относится к росту клеток in vitro. В такой культуре клетки пролиферируют, оно они не организуют ткань саму по себе. "Тканевая культура" относится к поддержанию или росту ткани, например, эксплантаты зародышевого органа или взрослого органа in vitro, так чтобы сохранять его архитектуру и функцию. "Монослойная культура" относится к культуре, в которой клетки размножаются в подходящей среде, при этом в основном прикреплены друг к другу и к субстрату. Кроме того, "суспензионная культура" относится к культуре, в которой клетки размножаются в суспендированном состоянии в подходящей среде. Аналогично, "проточная культура" относится к культивированию клеток или эксплантаты в постоянном потоке свежей среды для поддержания клеточного роста, например, жизнеспособности. Термин "кондиционированные среды" относится к супернатанту, например, не содержащему культивируемые клетки/ткань, получаемому после определенного периода времени контактирования с культивируемыми клетками, таким образом, что среду изменяют таким образом, чтобы она содержала определенные паракринные и/или аутокринные факторы, продуцируемые клетками и секретируемые в культуру. "Конфлюэнтная культура" представляет собой культуру клеток, в которой все клетки находятся в контакте, таким образом, вся поверхность сосуда для культивирования является покрытой, и подразумевает, что клетки также достигли своей максимальной плотности, хотя конфлюэнтность не обязательно означает, что деление прекращается или что популяция не увеличивается в размере.
Термин "среда для культивирования" или "среда" является общепризнанным в данной области и, как правило, относится к любому веществу или препарату, используемому для культивирования живых клеток. Термин "среда", как используют по отношению к культуре клеток, включает компоненты среды, окружающей клетки. Среды могут являться твердыми, жидкими, газообразными или представлять собой смесь фаз и веществ. Среды включают жидкие среды для выращивания, а также жидкие среды, которые не поддерживают рост клеток. Среды также включают желатиновые среды, такие как матриксы на основе агара, агарозы, желатина и коллагена. Иллюстративные газообразные среды включают газообразную фазу, действию которой подвергаются клетки, растущие на on a чашке Петри или другой твердой или полутвердой подложке. Термин "среда" также относится к веществу, которое предназначен для применения в культуре клеток, даже если оно еще не контактировало с клетками. Другими словами, богатая питательными веществами жидкость, подготавливаемая для бактериальной культуры, представляет собой среду. Аналогично, смесь порошков, которая при смешивании с водой или другой жидкостью становится подходящей для культуры клеток, можно называть "порошковая среда". "Среда определенного состава" относится к средам, которые состоят из химически определенных (как правило, очищенных) компонентов. "Среды определенного состава" не содержат плохо охарактеризованных биологических экстрактов, таких как экстракт дрожжей и мясной бульон. "Богатая среда" включает среды, которые конструируют для поддержания роста большей части или всех жизнеспособных форм конкретного вида. Богатые среды часто содержат сложные биологические экстракты. "Среда, подходящая для роста культуры высокой плотности" представляет собой любую среду, которая позволяет культуре клеток достигать OD600 3 или выше, когда другие условия (такие как температура и скорость передачи кислорода) обеспечивают такой рост. Термин "минимальная среда" относится к среде, которая способствует росту многих типов микроорганизмов, которые не требуют какие-либо специальные питательные добавки. Многие основные среды, как правило, содержат четыре основных химических группы: аминокислоты, углеводы, неорганические соли и витамины. Минимальная среда, как правило, служит в качестве основы для более сложных сред, к которой добавляют добавки, такие как сыворотка, буферы, факторы роста, липиды и т.п. Примеры основных сред включают, но не ограничиваются ими, минимальную среду Игла, минимальную поддерживающую среду, модифицированную Дульбекко среду Игла, среду 199, смеси питательных веществ Хама F-10 и Хама F-12, Мак-Коя 5A, Дульбекко MEM/F-I 2, RPMI 1640 и модифицированную Исков среду Дульбекко (IMDM).
Термины "содержит" и "содержащий" используют в широком открытом смысле, означающем, что могут содержаться дополнительные элементы.
Как используют в настоящем описании, подразумевают, что термин "размноженные", когда относится к клеткам имеет свое обычное значение в данной области, а именно клетки, которые пролиферировали in vitro. MSC можно размножать с получением популяции клеток, которые сохраняют по меньшей мере одну биологическую функцию MSC, как правило, способность прикрепляться к пластиковой поверхности в стандартных условиях культивирования. Размноженная популяция клеток может сохранять способность дифференцироваться в один или более типов клеток.
Термин "включая" используют в настоящем описании для обозначения "включая, но, не ограничиваясь". "Включая" и "включая, но, не ограничиваясь" используют взаимозаменяемо.
"Маркер" относится к биологической молекуле, наличие, концентрацию, активность или фосфорилирование состояние которой можно детектировать и использовать для идентификации фенотипа клетки.
"Мезенхимальные стромальные клетки (в настоящем описании также обозначаемые как "MSC") представляют собой мультипотентные стромальные клетки, например, они представляют собой клетки, которые способны приводить к образованию многим различных типов клеток.
"Пациент", "индивидуум" или "хозяин", подлежащий лечению способом по изобретению, может означать человека или не являющего человеком животное.
Термин "фармацевтическая композиция" относится к композиции, предназначенной для применения в терапии. Композиции по изобретению представляют собой фармацевтические композиции, предназначенные для применения для лечения SIRS, сепсиса, тяжелого сепсиса, септического шока и подобных сепсису состояний. Композиции по изобретению могут содержать в дополнение к MSC, неклеточные компоненты. Примеры таких неклеточных компонентов включают, но не ограничиваются ими, среды для культивирования клеток, которые могут содержать один или более белков, аминокислот, нуклеиновых кислот, нуклеотидов, коферментов, антиоксидантов и металлов.
Фразу "фармацевтически приемлемые" применяют в настоящем описании по отношению к таким соединениям, веществам, композициям и/или лекарственным формам, которые в объеме медицинской точки зрения являются пригодными для использования в контакте с тканями человека и животных без избыточной токсичности, раздражения, аллергического ответа или другой проблемы или осложнения в соответствии с разумным соотношением польза/риск.
Как используют в настоящем описании, фраза "фармацевтически приемлемый носитель" означает фармацевтически приемлемое вещество, композицию или носитель, такой как жидкий или твердый наполнитель, разбавитель, эксципиент или инкапсулирующий растворитель материал, участвующий в переносе или транспорте соединения по изобретению из одного органа или части организма в другой орган или часть организма. Каждый носитель должен являться "приемлемым" в том смысле, что являться совместимым с другими ингредиентами состава и не опасными для пациента.
Термин "фенотип" относится к наблюдаемым характеристикам клеток, таким как размер, морфология, экспрессия белка и т.д.
"Пролиферация" относится к увеличению числа клеток. "Пролиферирующий" и "пролиферация" относится к клеткам, претерпевающим митоз.
Подразумевают, что "рефрактерный" означает не имеющий существенного клинического преимущества при использовании для лечения заболеваний, например, отсутствует значительное улучшение состояния или ослабление симптомов или последующего рецидива заболевания.
Как используют в настоящем описании, термин "раствор" включает фармацевтически приемлемый носитель или разбавитель, в котором MSC, используемые в изобретении, остаются жизнеспособными.
Термин "по существу чистый" в отношении популяций MSC относится к популяции клеток, в которой по меньшей мере приблизительно 75%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90% или по меньшей мере приблизительно 95% по количеству клеток представляют собой MSC. Другими словами, термин "по существу чистый" в отношении популяций MSC относится к популяциям клеток, которые содержат менее приблизительно 20%, менее приблизительно 10% или менее приблизительно 5% по количеству линейно-коммитированные клетки.
Как используют в настоящем описании, "подложка" относится к любому устройству или веществу, которое может служить в качестве основы или матрицы для роста стромальных стволовых клеток жировой ткани.
"Терапевтическое средство" или "терапевтический" относится к средству, способному оказывать желаемое биологическое действие на хозяина. Химиотерапевтические и генотоксичные средства представляют собой примеры терапевтических средств, которые, как правило, как известно, являются химического происхождения, в отличие от биологических или вызывают терапевтический эффект в результате конкретного механизма действия, соответственно. Примеры терапевтических средств биологического происхождения включают факторы роста, гормоны и цитокины. Различные терапевтических средств известны в данной области, и их можно идентифицировать по их эффектам. Определенные терапевтические средства способны регулировать клеточную пролиферацию и дифференцировку. Примеры включают химиотерапевтические нуклеотиды, лекарственные средства, гормоны, неспецифические (не являющиеся антителом) белки, олигонуклеотиды (например, антисмысловые олигонуклеотиды, которые связываются с последовательностью-мишенью нуклеиновой кислоты (например, последовательность иРНК)), пептиды и пептидомиметики.
ПОДРОБНОЕ ОПИСАНИЕ
Изобретение относится к композиции, содержащей мезенхимальные стромальные клетки (MSC), для применения для лечения сепсиса у индивидуума. В дополнительном варианте осуществления изобретение также относится к применению мезенхимальных стромальных клеток (MSC) в производстве лекарственного средства для лечения сепсиса у индивидуума. В другом варианте осуществления изобретение также относится к способу лечения сепсиса у индивидуума, включающему введение мезенхимальных стромальных клеток (MSC) индивидууму. Следует понимать, что "индивидуум" в контексте настоящего изобретения, как правило, представляет собой индивидуума, нуждающегося в лечении. Таким образом, изобретение также относится к способу лечения сепсиса у нуждающегося в этом индивидуума, страдающего пневмонией или после пневмонии, включающему введение мезенхимальных стромальных клеток (MSC) индивидууму.
Предпочтительно указанный сепсис связан, вызван или возникает после состояния воспалительного состояния легких, как правило, пневмонии. В одном из вариантов осуществления сепсис является вторичным по отношению к пневмонии. Предпочтительно указанный сепсис представляет собой тяжелый сепсис и связан, вызван или возникает после воспалительного состояния легких, как правило, пневмонии. В одном из вариантов осуществления сепсис представляет собой тяжелый сепсис, который является вторичным по отношению к пневмонии. Указанная пневмония может быть вызвана грибами, бактериями или вирусами. В одном из вариантов осуществления пневмония вызывается бактериями, например, грамотрицательными бактериями (грамотрицательная пневмония). Грамотрицательные бактерии могут включать род Klebsiella, например, вид Klebsiella pneumoniae, такую как серотип 2 Klebsiella pneumoniae. В других вариантах осуществления пневмония вызывается Streptococcus pneumonia, в альтернативных вариантах осуществления пневмония может вызываться Haemophilus influenzae, Chlamydophila pneumonia, Legionella pneumophila или грибом Pneumocystis jiroveci. Пневмония может представлять собой быть внебольничную, связанную с оказанием медицинской помощи, внутрибольничную или вентилятор-ассоциированную пневмонию. Пневмония может представлять собой лобарную пневмонию, бронхиальную пневмонию или острую интерстициальную пневмонию.
Было выявлено, что MSC обеспечивает иммуномодулирующий эффект, в частности на участке воспаления. Выявлено, что экзогенно вводимые MSC, как правило, локализуются в легких. Таким образом, MSC являются особенно эффективными для лечения сепсиса, который является вторичным по отношению к воспалительному состоянию легких, такому как пневмония.
Примеры демонстрирую, что внутривенное введение ASC снижает тяжесть ассоциированного с пневмонией сепсиса, например, в результате снижения бактериальных нагрузок на различные органы, включая кровь и легкие, и снижения уровней цитокинов и хемокинов в легких.
Таким образом, в одном из вариантов осуществления изобретение относится к MSC, например, ASC для применения в способе лечения ассоциированного с пневмонией сепсиса у являющегося человеком индивидуума, где введение, например, посредством внутривенной инъекции MSC снижает системную (например, в крови) общую бактериальную нагрузку (КОЕ/мл) до статистически значимых уровней, например, в 10 раз или более, например, в 50 раз или более или в 100 раз или более, по сравнению с характерными системными общими бактериальными нагрузками у не получающих лечение индивидуумов. Общие бактериальные нагрузки можно определять способами, хорошо известными специалисту в данной области, например, полуколичественной бактериальной культурой или количественной ПЦР.
КЛЕТКИ ПО ИЗОБРЕТЕНИЮ
MSC представляют собой недифференцированные стромальные клетки, обладающие способностью дифференцироваться в другие клетки, и, как правило, происходящие из соединительной ткани, и, таким образом, они не являются гемопоэтическими клетками. Термин "соединительная ткань" относится к ткани, происходящей из мезодермы, и включает несколько тканей, которые характеризуется тем, что их клетки входят в состав внеклеточного матрикса. К числу различных типов соединительных тканей относят адипозные и хрящевые ткани. В одном из вариантов осуществления MSC являются из стромальной фракции жировой ткани. В другом варианте осуществления MSC получают из хондроцитов, например, из гиалинового хряща. В другом варианте осуществления MSC получают из кожи. Кроме того, в другом варианте осуществления MSC получают из костного мозга. Альтернативные источники MSC включают, но не ограничиваются ими, надкостницу, пульпу зуба, селезенку, поджелудочную железу, связку, сухожилия, скелетную мышцу, пупочный канатик и плаценту.
MSC можно получать из любого подходящего источника и от любого подходящего животного, включая людей. Как правило, указанные клетки получают из постнатальной соединительной ткани млекопитающих. В предпочтительном варианте осуществления MSC получают из источника соединительной ткани, такого как стромальная фракция жировой ткани, гиалиновый хрящ, костный мозг, кожу и т.д. Также в конкретном варианте осуществления MSC принадлежат млекопитающему, например, грызуну, примату и т.д., предпочтительно, человеку. Как правило, MSC получают из стромальной фракции жировой ткани человека, т.е. они представляют собой стромальные клетки жировой ткани (ASC).
MSC прикрепляются к пластику в стандартных условиях культивирования.
MSC представляют собой недифференцированные мультипотентные клетки, обладающие способностью дифференцироваться в соматические клетки или в их направлении, такие как мезодермальные клетки (например, адипозные, хондроциты, остеобласты) и необязательно в или в направлении эндодермальных и/или эктодермальных типов или линий клеток. Как правило, клетки обладают способностью дифференцироваться в или в направлении по меньшей мере двух или всех типов клеток, выбранных из группы, состоящей из линий адипоцитов, хондробластов и остеобластов.
В одном из вариантов осуществления MSC могут представлять собой стволовые клетки, как правило, стволовые клетки жировой ткани. Как правило, MSC (i) не экспрессируют маркеры, специфичные для APC; (ii) не экспрессируют конститутивно IDO; (iii) значительно не экспрессируют конститутивно MHC II. Как правило, экспрессия IDO или MHC II можно индуцировать стимуляцией IFN-γ.
Как правило, MSC могут экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более (например, до 13)) маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105. Например, MSC могут экспрессировать один или более (например, два, три или все) маркеров CD29, CD59, CD90 и CD105, например, CD59 и/или CD90.
Как правило, MSC могут не экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более, или десять или более (например, до 15)) маркеров фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133, например, MSC не экспрессируют один или более (например, два, три или все) из маркеров CD34, CD45, CD31 и CD14, например, CD31 и/или CD34.
Размноженные MSC
В одном из вариантов осуществления MSC представляют собой культуру in vitro размноженных MSC или культуру in vitro их размноженного потомства (далее в настоящем описании их обозначают как размноженные MSC или "eMSC"). Способы получения eMSC являются известными в данной области, например, как описано в WO2007039150. eMSC сохраняют некоторые фенотипические характеристики MSC, например, eMSC прикрепляются к пластику в стандартных условиях культивирования и сохраняют недифференцированный фенотип.
eMSC представляют собой недифференцированные мультипотентные клетки, обладающие способностью дифференцироваться в соматические клетки, такие как мезодермальные клетки. При этом MSC обладают способностью дифференцироваться по меньшей мере в направлении одной или более линий специализированных клеток, таких как, но не ограничено ими, линии адипоцитов, хондробластов и остеобластов; как правило, в eMSC такая способность дифференцироваться является сниженной или даже может отсутствовать, например, при этом MSC могут дифференцироваться в направлении по меньшей мере в остеогенных и адипоцитарных линий, получаемые из них eMSC могут дифференцироваться только в направлении линии адипоцитов. Это может являться предпочтительным для терапевтических применений клеток, где клетки можно вводить пациентам, т.к. обоснованно ожидают, что с очень маленькой вероятностью может происходить неожиданная и потенциально опасная дифференцировка eMSC.
В одном из вариантов осуществления eMSC могут представлять собой потомство стволовых клеток. Как правило, eMSC (i) не экспрессируют маркеры, специфичные для APC; (ii) не экспрессируют конститутивно IDO; (iii) значительно не экспрессируют конститутивно MHC II. Как правило, экспрессию IDO или MHC II можно индуцировать стимуляцией IFN-γ.
Как правило, eMSC могут экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более (например, до 13)) маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105, например, MSC могут экспрессировать один или более (например, два, три или все) маркеров CD29, CD59, CD90 и CD105, например, CD59 и/или CD90.
Как правило, eMSC могут не экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более, или десять или более (например, до 15)) маркеров фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133, например, MSC не экспрессируют один или более (например, два, три или все) маркеров CD34, CD45, CD31 и CD14, например, CD31 и/или CD34. Кроме того MSC могут необязательно не экспрессировать маркер STRO-1.
ПОПУЛЯЦИИ КЛЕТОК
В одном из аспектов настоящее изобретение относится к популяциям MSC и/или eMSC для терапевтических применений, как описано в настоящем описании, такие популяции могут далее в настоящем описании обозначаться как "популяции клеток по изобретению". Как правило, MSC представляет собой размноженные ASC человека, как правило, аллогенные размноженные ASC человека. Как правило, популяции клеток по изобретению являются гомогенной или по существу гомогенной популяцией MSC и/или eMSC. Популяции клеток по изобретению содержат или по существу содержат MSC и/или eMSC, однако популяции клеток по изобретению также могут содержать другие типы клеток. Таким образом, в одном из вариантов осуществления изобретение относится к популяции клеток по изобретению, в которой по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99% клеток представляют собой MSC и/или eMSC.
Как правило, популяции клеток по изобретению представляют собой популяцию размноженной культуры MSC, состоящую или по существу состоящую из eMSC, однако популяции клеток по изобретению также могут содержать другие типы клеток. Таким образом, в одном из вариантов осуществления изобретение относится к популяции клеток по изобретению, в которой по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99% клеток представляют собой eMSC. В одном из вариантов осуществления eMSC представляют собой eASCs, например, eASC человека. В конкретном варианте осуществления клетки являются аллогенными в отношении индивидуума, подлежащего лечению.
Как правило, популяция клеток по изобретению может обладать способностью дифференцироваться в направлении по меньшей мере одной или более специализированных линий клеток, таких как, но не ограничиваясь ими, линии адипоцитов, хондробластов и остеобластов. В одном из вариантов осуществления популяция клеток по изобретению может обладать способностью дифференцироваться в или в направлении по меньшей мере двух или всех типов клеток, выбранных из группы, состоящей из линии адипоцитов, хондробластов и остеобластов. Однако в альтернативном варианте осуществления такая способность дифференцироваться является сниженной или даже может отсутствовать, например, при этом MSC могут дифференцироваться в направлении по меньшей мере остеогенных и адипоцитарных линий, получаемая из них популяция eMSC может дифференцироваться только в направлении линии адипоцитов. Это может являться предпочтительным для терапевтических применений клеток, где клетки можно вводить пациентам, т.к. обоснованно ожидают, что с очень маленькой вероятностью может происходить неожиданная и потенциально опасная дифференцировка eMSC.
Как правило, популяция клеток по изобретению может экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более (например, до 13)) маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105, например, MSC могут экспрессировать один или более (например, два, три или все) маркеров CD29, CD59, CD90 и CD105, например, CD59 и/или CD90. Таким образом, в одном из вариантов осуществления изобретение относится к популяции клеток по изобретению, в которой по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99% клеток экспрессируют один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более (например, до 13)) маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105, например, MSC могут экспрессировать один или более (например, два, три или все) маркеров CD29, CD59, CD90 и CD105, например, CD59 и/или CD90. В альтернативном варианте осуществления изобретение относится к популяции клеток по изобретению, в которой уровень экспрессии одного или более (например, двух или более, трех или более, четырех или более, пяти или более, шести или более, семи или более, восьми или более, девяти или более или десяти или более (например, до 13)) маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105 составляет по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99%, например, популяция клеток по изобретению может экспрессировать один или более (например, два, три или все) маркеров CD29, CD59, CD90 и CD105, например, CD59 и/или CD90 на указанном выше уровне.
Как правило, популяция клеток по изобретению может не экспрессировать один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более (например, до 15)) маркеров фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133, например, MSC не экспрессируют один или более (например, два, три или все) маркеров CD34, CD45; CD31; CD14 например, CD31 и/или CD34. Кроме того MSC могут необязательно не экспрессировать маркер STRO-1.
Таким образом, в одном из вариантов осуществления изобретение относится к популяция клеток по изобретению, в которой по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99% клеток не экспрессируют один или более (например, два или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более, или десять или более (например, до 15)) маркеров фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133, например, MSC могут экспрессировать один или более (например, два, три или все) маркеров CD34, CD45, CD31 и CD14, например, CD31 и/или CD34. В альтернативном варианте осуществления изобретение относится к популяции клеток по изобретению, в которой уровень экспрессии одного или более (например, двух или более, трех или более, четырех или более, пяти или более, шести или более, семи или более, восьми или более, девяти или более или десяти или более (например, до 15)) маркеров фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133 является ниже по меньшей мере приблизительно на 35%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 25%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 25%, по меньшей мере приблизительно на 5%, по меньшей мере приблизительно на 1%, например, популяции клеток по изобретению могут экспрессировать один или более (например, два, три или все) маркеров CD34, CD45, CD31 и CD14, например, CD31 и/или CD34 на указанных выше уровнях.
В некоторых вариантах осуществления MSC или eMSC предварительно стимулируют для повышения одной или более из их пролиферативной способности, миграционной способности, выживаемости, терапевтического эффекта и иммунорегуляторных свойств. Как правило, по меньшей мере приблизительно 40% (например, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95% по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99%) популяций клеток по изобретению предварительно стимулируют для повышений один или более из их пролиферативной способности, миграционной способности, выживаемости, терапевтического эффекта и иммунорегуляторных свойств. В некоторых вариантах осуществления предварительную стимуляцию можно получать приведением MSC в контакт с цитокином. В некоторых вариантах осуществления изобретения предварительную стимуляцию можно получать приведением MSC в контакт с IFN-γ.
КОМПОЗИЦИИ ПО ИЗОБРЕТЕНИЮ
В одном из вариантов осуществления настоящее изобретение относится к композициям, содержащим популяции клеток по изобретению для применения в способах лечения по настоящему изобретению. Предпочтительно, чтобы указанная композиция являлась фармацевтической композицией. Композиция по изобретению может содержать по существу чистую популяцию MSC или eMSC, например, по существу чистую популяцию ASC или eASC, например, eASC человека. MSC, eMSC, ASC или eASC могут представлять собой стволовые клетки. Композиция по настоящему изобретению также может содержать компоненты культуры клеток, например, среды для культивирования, содержащие одну или более из аминокислот, металлов и факторов кофермента. Композиция может содержать небольшие популяции других стромальных клеток. Композиция также может содержать другие неклеточные компоненты, которые могут поддерживать рост и выживаемость MSC при конкретных обстоятельствах, например, имплантации, росте в непрерывной культуре или использованию в качестве биологического материла или композиции.
Концентрация MSC и/или eMSC в композиции по изобретению может составлять по меньшей мере приблизительно 1×104 клеток/мл, по меньшей мере приблизительно 1×105 клеток/мл, по меньшей мере приблизительно 1×106 клеток/мл, по меньшей мере приблизительно 10×106 клеток/мл или по меньшей мере приблизительно 40×106 клеток/мл. Как правило, концентрация составляет приблизительно от 1×106 клеток/мл до 1×107 клеток/мл, например, приблизительно от 5×106 клеток/мл до 1×107 клеток/мл.
Композиции по изобретению, как правило, содержат фармацевтически приемлемый носитель и/или разбавитель. Примеры таких носителей и разбавителей хорошо известны в данной области и могут включать: сахара, таке как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные средства, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический физиологический раствор; раствор Рингера; этиловый спирт; растворы с забуференным pH; сложные полиэфиры, поликарбонаты и/или полиангидриды и другие нетоксичные совместимые вещества, применяемые в фармацевтических составах. Как правило, композиции по изобретению содержат DMEM в качестве носителя, который можно необязательно дополнять сывороткой (например, HSA) в концентрации, например, приблизительно до 5%, приблизительно до 10%, приблизительно до 15%, приблизительно до 20%, приблизительно до 25%, приблизительно до 30%.
Композиция по изобретению может являться стерильной и/или жидкой в тех случаях, когда существует простая возможность введения через шприц. Кроме того, композиция может являться стабильной в условиях производства и хранения и защищенной от загрязняющего действия микроорганизмов, таких как бактерии и грибы в результате использования, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты и тимеросала.
СПОСОБЫ ПОЛУЧЕНИЯ
Способы выделения и культивирования MSC для получения eMSC и популяции клеток по изобретению и композиции, содержащих популяции клеток по изобретению, известны в данной области. Как правило, способы получения композиций, содержащих популяции клеток, включают следующие этапы:
(i) выделения MSC из ткани и отбор по адгезии к подходящей поверхности, например, пластику,
(ii) размножение MSC с получением популяции клеток по изобретению, содержащей eMSC.
Необязательно популяции клеток по изобретению можно криоконсервировать во время этапа размножения (ii) и/или после него. Необязательно фенотип популяций клеток по изобретению можно оценивать во время этапа размножения (ii) и/или после него. Необязательно популяции клеток по изобретению можно выделять после этапа размножения (ii) и ресуспендировать в фармацевтически приемлемом носителе и/или разбавителях.
MSC для применения в изобретение можно выделять из любой подходящей ткани, такой как, но не ограничиваясь ими, периферическая кровь, костный мозг, плацента, жировая ткань, надкостница, пульпа зуба, селезенка, поджелудочная железа, связка, кожа, сухожилия, скелетная мышца, пупочный канатик и плацента. В предпочтительном варианте осуществления MSC получают из источника соединительной ткани, такого как стромальная фракция жировой ткани, гиалиновый хрящ, костный мозг, кожа и т.д.
В одном из вариантов осуществления MSC получают из стромальной фракции жировой ткани. В другом варианте осуществления MSC получают из хондроцитов, например, из гиалинового хряща. В другом варианте осуществления MSC получают из кожи. Также, в другом варианте осуществления MSC получают из костного мозга.
MSC можно получать из любого подходящего источника и от любого подходящего животного, включая людей. Как правило, указанные клетки получают из постнатальных соединительных тканей млекопитающих.
MSC также можно выделять из любого организма того же вида что и индивидуум или отличного вида. Любой организм с MSC может являться потенциальным кандидатом. В одном из вариантов осуществления организм может представлять собой млекопитающее, а в другом варианте осуществления организм представляет собой человека.
MSC жировой ткани можно получать любыми средствами, стандартными в данной области. Как правило, указанные клетки получают путем диссоциации клеток из ткани источника (например, липоаспирата или жировой ткани), как правило, посредство обработки ткани расщепляющим ферментом, таким как коллагеназа. Затем, расщепленное вещество ткани, как правило, фильтруют через фильтр приблизительно от 20 микрон до 1 мм. Затем выделяют клетки (как правило, посредством центрифугирования) и культивируют на адгезивной поверхности (как правило, планшетах или колбах для культивирования тканей). Такие способы известны в данной области и являются, например, такими как описано в патенте США № 6777231. Согласно этой методологии липоаспираты получают из жировой ткани и выделяемых из них клеток. В этой методологии клетки можно промывать для удаления загрязняющего дебриса и эритроцитов предпочтительно в PBS. Клетки расщепляли коллагеназой (например, при 37°C в течение 30 минут, 0,075% коллагеназы I типа, Invitrogen, Carlsbad, CA) в PBS. Для устранения оставшихся эритроцитов расщепленный образец можно промывать (например, 10% эмбриональной телячьей сывороткой), обрабатывать 160 ммоль/л ClNH4 и в заключении суспендировать в полной среде DMEM (DMEM, содержащей 10% FBS, 2 ммоль/л глутамина и 1% пенициллина/стрептомицина). Клетки можно фильтровать через 40 мкм нейлоновый фильтр.
Клетки культивируют в подходящем сосуде для культивирования тканей, содержащем поверхность, подходящую для прикрепления MSC, например, пластик. Неприкрепившиеся клетки удаляют, например, промыванием в подходящем буфере с получением выделенной популяции прикрепленных стромальных клеток (например, MSC). Выделяемые таким образом клетки можно высевать (предпочтительно 2-3×104 клеток/см2) на флаконы для тканевых культур и размножать при 37°C и 5% CO2, заменяя среду для культивирования каждые 3-4 суток. Клетки предпочтительно пересевают в новый флакон для культивирования (1000 клеток/см2), когда культуры достигают 90% конфлюэнтности.
Выделение клеток предпочтительно проводят в стерильных условиях или в соответствии с GMP.
В определенных вариантах осуществления клетки можно культивировать в течение по меньшей мере приблизительно 15 суток, по меньшей мере приблизительно 20 суток, по меньшей мере приблизительно 25 суток или по меньшей мере приблизительно 30 суток. Как правило, размножение клеток в культуре улучшает гомогенность фенотипа клеток в популяции клеток, таким образом, что получают по существу чистую или гомогенную популяцию.
Клетки предпочтительно открепляют от адгезивной поверхности (например, посредством трипсина) и переносят в новый сосуд для культивирования (пересевают), когда культуры достигают приблизительно 75%, 80%, 85%, 90% или 95% конфлюэнтности.
В определенных вариантах осуществления клетки размножают в культуре в течение по меньшей мере трех пересеваний культур или "пересевают по меньшей мере три раза". В других вариантах осуществления клетки пересевают по меньшей мере четыре раза, по меньшей мере пять раз, по меньшей мере шесть раз, по меньшей мере семь раз, по меньшей мере восемь раз, по меньшей мере девять раз или по меньшей мере десять раз.
В определенных вариантах осуществления клетки размножают в культуре в течение по меньшей мере трех удвоений популяции. В определенных вариантах осуществления клетки размножают в культуре в течение по меньшей мере четырех, пяти, шести, семи, восьми, девяти, десяти или 15 удвоений популяций. В определенных вариантах осуществления клетки размножают в культуре в течение менее чем семи, восьми, девяти, десяти или 15 удвоений популяций. В определенных вариантах осуществления клетки размножают в культуре в течение приблизительно от 5 до 10 удвоений популяций.
Клетки можно культивировать любым способом, известным в данной области для культивирования стромальных стволовых клеток. Обсуждение различных способов культивирования, а также их увеличение масштаба, можно найти у Freshney R.I., Culture of Animal Cells: A Manual of Basic Technique, 4th Edition, Wiley-Liss 2000. Клетки можно размножать с использованием флаконов для культивирования или биореакторов, подходящих для крупномасштабного размножения. Биореакторы, подходящие для крупномасштабного размножения мезенхимальных стромальных клеток, являются коммерчески доступными и могут включать биореакторы 2D (т.е. по существу плоские) и 3D. Примеры таких биореакторов включают, но не ограничиваются ими, поршневой проточный биореактор, перфузионный биореактор, непрерывный биореактор с механическим перемешиванием, биореактор с неподвижным слоем.
В определенных вариантах осуществления клетки культивируют как монослойную культуру. Можно использовать любую среду, способную поддерживать MSC в тканевой культуре. Составы сред, которые поддерживают рост MSC, включают, но не ограничиваются ими, модифицированную Дульбекко среду Игла (DMEM), альфа-модифицированную минимальную питательную среду (αMEM) и среды Roswell Park Memorial Institute 1640 (среды RPMI 1640). Как правило, к указанным выше средам добавляют от 0 до 20% эмбриональной телячьей сыворотки (FBS) для поддержания роста стромальных клеток. Однако можно использовать среду определенного состава, если идентифицируют необходимые факторы роста, цитокины и гормоны в FBS для стромальных клеток и хондроцитов и предоставляют в подходящих концентрациях в средах для выращивания. Среды, пригодные в способах по изобретению, могут содержать одно или более представляющих интерес соединений, включая, но, не ограничиваясь ими, антибиотики, митогенные или вызывающие дифференцировку соединения для стромальных клеток. Клетки по изобретению можно выращивать при температурах от 31°C до 37°C в увлажненном инкубаторе. Содержание диоксида углерода можно поддерживать от 2% до 10% и содержание кислорода можно поддерживать от 1% до 22%.
Антибиотики, которые можно добавлять к среде, включают, но не ограничиваются ими, пенициллин и стрептомицин. Концентрация пенициллина в химически определенной среде для культивирования может составлять приблизительно от 10 приблизительно до 200 единиц на мл. Концентрация стрептомицина в химически определенной среде для культивирования может составлять приблизительно от 10 приблизительно до 200 мкг/мл.
Как правило, MSC, как исползают в способах по настоящему изобретению, представляют собой размножившиеся популяции клеток, предпочтительно указанные клетки размножают с получением по существу чистой или гомогенной популяции.
В одном из вариантов осуществления указанные популяции клеток размножают до тех пор, пока экспрессия маркера CD34 не снижается по сравнению со свежевыделенными, неразмноживщимися клетками. Например, популяцию клеток размножают до тех пор, пока экспрессия маркера CD34 не сживается до уровня менее 50%, менее 35%, менее 30%, или менее 5%, например, 35-5% или 20-10% клеток в популяции. Как правило, популяцию клеток размножают до тех пор, пока экспрессия маркера CD34 не снижается до уровня менее 5% клеток в популяции. Таким образом, популяция eMSC по изобретению содержит менее 50%, менее 35%, менее 30% или менее 5%, например, 35-5% или 20-10% клеток, экспрессирующих CD34.
В одном из вариантов осуществления указанные популяции клеток размножают до тех пор, пока экспрессия маркера STRO-1 не снижается по сравнению с со свежевыделенными, неразмноживщимися клетками. Например, популяцию клеток размножают до тех пор, пока экспрессия маркера STRO-1 не снижается до уровня менее 50%, менее 35%, менее 30%, или менее 5%, например, 35-5% или 20-10% клеток в популяции. Как правило, популяцию клеток размножают до тех пор, пока экспрессия маркера STRO-1 не снижается до уровня менее 5% клеток в популяции. Таким образом, популяция eMSC по изобретению содержит менее 50%, менее 35%, менее 30% или менее 5%, например, 35-5% или 20-10% клеток, экспрессирующих STRO-1.
Как правило, популяции клеток размножают до тех пор, пока экспрессия маркеров CD34 и STRO-1 не снижается по сравнению со свежевыделенными, неразмножившимися клетками. Например, популяцию клеток размножают до тех пор, пока экспрессия маркеров CD34 и STRO-1 не снижается до уровня менее 50%, менее 35%, менее 30% или менее 5%, например, 35-5% или 20-10% клеток в популяции. Как правило, популяция клеток размножают до тех пор, пока экспрессия CD34 и STRO-1 не снижается до уровня менее 5% клеток в популяции. Таким образом, популяция eMSC по изобретению содержит менее 50%, менее 35%, менее 30% или менее 5%, например, 35-5% или 20-10% клеток, экспрессирующих CD34 и STRO-1.
Размножившиеся популяции MSC (например, популяции, экспрессирующие 5% или менее CD34 и/или STRO-1) являются предпочтительными, т.к. они характеризуются меньшей мультипотентностью по сравнению со свежевыделенными клетки, т.е. они могут обладать более низкой, сниженной или не обладать способностью дифференцироваться в другие фенотипы клеток по сравнению с природными не подвергавшимися размножению MSC.
Специалисту в данной области очевидно, что такой способ получения композиции по изобретению не является ограниченным, и что композиции по изобретению, получаемые любым способом, входят в объем изобретения. В одном из вариантов осуществления изобретение относится к способу получения композиции по изобретению, который включает: (a) сбор ткани от донора; (b) получение клеточной суспензии посредством ферментативной обработки; (c) осаждение клеточной суспензии и повторное суспендирование клеток в среда для культивирования; (d) культивирование клеток в течение по меньшей мере приблизительно 5 суток или 5 удвоений популяций.
В одном из вариантов осуществления клетки можно криоконсервировать до введения, например, во время и/или после размножения. Таким образом, изобретение также относится к криоконсервированным клеткам по изобретению. Способы криоконсервации клетки известны в данной области, и, как правило, для них необходимым является использование подходящих криозащитных средств (например, DMSO). Клетки можно криоконсервировать в любой момент времени во время стадий выделения и/или размножения и размораживать перед введением. Как правило, клетки можно криоконсервировать при 3, 4, 5, 6, 7, 8, 9, 10, 12, 15 или более пересеваниях, например, клетки можно криоконсервировать при 3-10 или 5-10 пересеваниях. Необязательно клетки можно повторно высевать и культивировать перед введением.
В одном из вариантов осуществления клетки можно выделять из криоконсервации и/или среды для культивирования и ресуспендировать в фармацевтически приемлемом носителе и/или разбавителях до введения (например, DMEM, необязательно дополненной сывороткой).
В некоторых вариантах осуществления популяции клеток по изобретению в композиции по изобретению можно предварительно стимулировать для повышения одной или более из их пролиферативной способности, миграционной способности, выживаемости, терапевтического эффекта и иммунорегуляторных свойств. В некоторых вариантах осуществления предварительную стимуляцию можно путем приведения MSC в контакт с цитокином. В некоторых вариантах осуществления изобретения предварительную стимуляцию можно проводить путем приведения MSC в контакт с IFN-γ.
В определенных вариантах осуществления MSC можно предварительно стимулировать с использованием концентрации IFN-γ от 0,1 до 100 нг/мл. В дополнительных вариантах осуществления MSC можно предварительно стимулировать с использованием концентрации IFN-γ от 0,5 до 85 нг/мл, от 1 до 70 нг/мл, от 1,5 до 50 нг/мл, от 2,5 до 40 нг/мл или от 3 до 30 нг/мл. Предварительная стимуляция может происходить при продолжительности стимуляции более приблизительно 12 часов. Предварительная стимуляция может происходить при продолжительности стимуляции более приблизительно 13 часов, более приблизительно 18 часов, при продолжительности стимуляции более приблизительно 24 часов, при продолжительности стимуляции более приблизительно 48 часов или при продолжительности стимуляции более приблизительно 72 часов.
В одном из вариантов осуществления MSC по изобретению можно стабильно или транзиторно трансфицировать или трансдуцировать представляющей интерес нуклеиновой кислотой с использованием стратегии на основе плазмиды, вирусного или альтернативного вектора. Представляющие интерес нуклеиновые кислоты включают, но не ограничиваются ими, нуклеиновые кислоты, кодирующие продукты генов, которые повышают продукцию компонентов внеклеточного матрикса, встречающихся в типе ткани, которую необходимо восстанавливать, например, стенке кишечника или вагинальной стенки.
Трансдукцию вирусных векторов, несущих регуляторные гены, в стромальные клетки можно проводить с использованием вирусных векторов, включая, но, не ограничиваясь ими, аденовирус, ретровирус или аденоассоциированный вирус, очищенный (например, связыванием с хлоридом цезия) при множественности заражения (вирусные единицы:клетка) приблизительно от 10:1 до 2000:1. Клетки можно подвергать воздействию вируса в не содержащей сыворотку или содержащей сыворотку среде при отсутствии или в присутствии катионного детергента, такого как полиэтиленимин или Lipofectamine™ в течение периода приблизительно от 1 часа приблизительно до 24 часов (Byk T. et al., (1998) Human Gene Therapy 9:2493-2502; Sommer B. et al. (1999) Calcif. Tissue Int. 64:45-49).
Другие подходящие способы переноса векторов или плазмид в стромальные клетки включают комплексы липид/ДНК, такие как комплексы, описанные в патентах США № 5578475, 5627175, 5705308, 5744335, 5976567, 6020202 и 6051429. Подходящие реагенты включают липофектамин, липосомальный состав 3:1 (масс./масс.) поликатионного липида 2,3-диолеилокси-N-[2(сперминкарбоксамидо)этил]-N,N-диметил-1-пропанамаминийтрифторацетат (DOSPA) (Chemical Abstracts Registry name: N-[2-(2,5-бис[(3-аминопропил)амино]-1-окспентил}амино)этил]-N,N-диметил-2,3-бис(9-октадеценилокси)-1-пропанаминийтрифторацетат) и нейтральный липид диолеилфосфатидилэтаноламин (DOPE) в фильтрованной через мембрану воде. Иллюстративным является состав Lipofectamine 2000TM (доступный от Gibco/Life Technologies № 11668019). Другие реагенты включают: трансфицирующий реагент FuGENETM 6 (смесь липидов в нелипосомальной форме и другие соединения в 80% этаноле, получаемом от Roche Diagnostics Corp. № 1814443) и трансфицирующий реагент LipoTAXITM (липидный состав от Invitrogen Corp., №204110). Трансфекцию стромальных клеток можно проводить электропорацией, например, как описано у M.L. Roach and J.D. McNeish, (2002) Methods in Mol. Biol. 185:1. Подходящие вирусные векторные системы для получения стромальных клеток со стабильными генетическими изменениями могут быть основаны на аденовирусах и ретровирусах, и их можно получать с использованием коммерчески доступных вирусных компонентов.
Трансфекцию плазмидных векторов, несущих регуляторные гены, в MSC, можно получать в монослойных культурах в результате использования осаждения ДНК фосфатом кальция или способов на основе катионного детергента (Lipofectamine™, DOTAP) или в трехмерных культурах путем введения плазмидных ДНК-векторов непосредственно в биосовместимый полимер (Bonadio J. et al., (1999) Nat. Med. 5:753-759).
Для отслеживания и детекции функциональных белков, кодируемых этими генами, вирусные или плазмидные ДНК-векторы могут содержать легко детектируемый маркерный ген, такой как зеленый флуоресцентный белок или фермент бета-галактозидазу, каждый из которых можно отслеживать гистохимическими способами.
После размножения предпочтительно, чтобы популяции клеток по изобретению оценивали для определения экспрессии характерных маркеров для подтверждения их фенотипа, которое можно проводить общепринятыми способами.
Термин "экспрессируемый" используют для описания наличия маркера в клетке. Для того чтобы считаться экспрессируемым маркер должен присутствовать на детектируемом уровне. Под "детектируемым уровнем" подразумевают то, что маркер можно детектировать с использованием одной из стандартных лабораторных методологий, таких как ПЦР, блоттинг или анализ FACS. Характеристику поверхностного маркера фенотипа популяции MSC можно проводить любым известным в данной области способом. В качестве примера, а не ограничения, такую фенотипическую характеристику можно проводить путем окрашивания индивидуальных клеток. Такое окрашивание можно получать с использованием антител. Это может представлять собой прямое окрашивание с использованием меченого антитела или непрямое окрашивание с использованием второго меченого антитела против первичного антител, специфического к маркеру клетки. Связывание антитела можно детектировать любым известным в данной области способом. Связывание антитела также можно детектировать проточной цитометрией, иммунофлуоресцентной микроскопией или рентгенографией.
Альтернативно или дополнительно, считают, что ген экспрессируется клеткой популяции по изобретению, если экспрессию можно в достаточной степени детектировать после 30 циклов ПЦР, которые соответствуют уровню экспрессии в клетке по меньшей мере приблизительно 100 копиям на клетку. Термины "экспрессируют" и "экспрессия" имеют соответствующие значения. На уровне экспрессии ниже такого порога считают, что маркер не экспрессируется. Сравнение между уровнем экспрессии маркера во взрослой стромальной клетке по изобретению и уровнем экспрессии того же маркера в другой клетке, такой как, например, эмбриональная стволовая клетка, можно предпочтительно проводить путем сравнения двух типов клеток, которые выделяли у того же вида. Предпочтительно этот вид представляет собой млекопитающее, и более предпочтительно этот вид представляет собой человека. Такое сравнение можно проводить подходящим способом с использованием эксперимента полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР).
Маркеры клеточной поверхности можно идентифицировать любым подходящим общепринятым способом, как правило, на основе положительной/отрицательной селекции; например, можно использовать моноклональные антитела против маркеров клеточной поверхности, присутствие/отсутствие в клетках которых необходимо подтверждать; хотя также можно использовать другие способы. Таким образом, в конкретном варианте осуществления используют моноклональные антитела против одного, двух, трех, четырех, пяти, шести, семи или всех CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105 для подтверждения отсутствия указанных маркеров в отобранных клетках; и моноклональные антитела против одного, двух, трех, четырех или всех из фактора VIII, альфа-актина, десмина, S-100, кератина, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133 используют для подтверждения их присутствия или детектируемых уровней экспрессии, по меньшей мере одного и предпочтительно всех из указанных маркеров.
В дополнительном варианте осуществления используют моноклональные антитела против по меньшей мере одного, двух, трех или всех из CD34, CD45, CD31, CD14, например, CD31 и/или CD34 для подтверждения присутствия или детектируемых уровней экспрессий указанных маркеров. В дополнительном варианте осуществления моноклональные антитела против CD34 используют для подтверждения отсутствия указанного маркера в отобранных клетках. В дополнительном варианте осуществления моноклональные антитела против STRO-1 используют для подтверждения отсутствия указанного маркера в отобранных клетках. В дополнительном варианте осуществления моноклональные антитела против по меньшей мере одного, двух, трех или всех из CD29, CD59, CD90, CD105, например, CD59 и/или CD90 используют для подтверждения их присутствия или детектируемых уровней экспрессий.
Указанные моноклональные антитела являются известными, коммерчески доступными, или специалист в данной области можно их получать общепринятыми способами.
Индуцированную IFN-γ активность IDO в отобранных клетках можно определять любым подходящим общепринятым анализом. Например, отобранные клетки можно стимулировать IFN-γ и анализировать на экспрессию IDO; затем можно проводить общепринятый анализ вестерн-блоттинга на экспрессию белка IDO и можно измерять ферментную активность IDO после стимуляции IFN-γ отобранных клеток посредством преобразования триптофана в кинуренин, например, анализом высокоэффективной жидкостной хроматографии (ВЭЖХ) и фотометрическим определением концентрации кинуренина в супернатанте в качестве информации считывания. Вследствие того, что клетки по изобретению экспрессируют IDO в определенных условиях, для отбора клеток по изобретению можно использовать любой подходящий способ, который обеспечивает возможность детекции активности IDO после стимуляции IFN-γ. Подходящий анализ для определения индуцируемой IFN-γ активности IDO в отобранных клетках описан в WO2007039150. Количество продуцируемого IDO зависит от числа клеток на квадратный сантиметр, которое предпочтительно находится на уровне 5000 клеток/см2 или более, но не ограничено этой концентрацией и концентрацией IFN-γ, которая в идеале составляет 3 нг/мл или более, но не ограничено этой концентрацией. Активность продуцируемо IDO в описанных условиях приводит к детектируемой продукции кинуренина в мМ диапазоне после 24 часов или более.
ВВЕДЕНИЕ
В одном из вариантов осуществления композицию по изобретению можно получать для системного введения (например, ректально, назально, буккально, влагалищно, через имплантированный резервуар или посредством ингаляции). В другом варианте осуществления композицию по изобретению можно получать для местного введения. Композицию по изобретению можно вводить парентеральным путем. Композиция можно вводить подкожным, внутрикожным, внутривенным, внутримышечным, внутрисуставным, интрасиновиальным, внутригрудинным, интратекальным, внутриочаговым, внутрилимфатическим и интракраниальным путями. Предпочтительный путь введения является внутривенным. Предпочтительные MSC представляют собой ASC.
Таким образом, изобретение относится к MSC, таким как ASC, для применения в лечении сепсиса, вторичного по отношению к пневмонии, у пациента, где MSC необходимо вводить внутривенным путем. Как правило, пациент представляет собой человека.
В одном из вариантов осуществления изобретение относится к ASC для применения для лечения сепсиса, вторичного по отношению к пневмонии, у пациента, например, являющегося человеком пациента, где ASC вводят системно, например, внутривенным путем, например, внутривенной инъекцией, например, внутрилимфатической инъекцией в лимфатические органы, такие как периферический лимфатический орган, включая, но, не ограничиваясь ими, лимфоузлы, наиболее предпочтительно подмышечный или паховый лимфоузел. В каждом из этих вариантов осуществления MSC могут представлять собой ASC, например, eASC. Как используют в настоящем описании, термин "лимфатическая система" приведен в своем общепринятом в данной области значении и относится к лимфоидной ткани, такой как лимфатический орган, соединенный проводящей системой лимфатических сосудов и лимфатических капилляров. Термин "лимфатический орган" относится к лимфоузлам, наиболее предпочтительно к подмышечному или паховому лимфоузлу. В одном из вариантов осуществления ASC вводят не прямо в легкое или вводят внутритрахеальным путем. В одном из вариантов осуществления MSC, используемые в изобретении, могут являться аутологичными по отношению к индивидууму, подлежащему лечению. В дополнительном варианте осуществления MSC, используемые в изобретении, могут являться аллогенными или ксеногенными по отношению к индивидууму, подлежащему лечению. Аллогенные стромальные клетки жировой ткани, получаемые от донора, можно теоретически использовать для лечения любого пациента, независимо от несовместимости MHC.
В одном из вариантов осуществления композицию по изобретению можно вводить посредством инъекции или имплантации композиции в один или более целевых участков у индивидуума, подлежащего лечению. В дополнительном варианте осуществления композицию по изобретению можно вводить в средство доставки, которое облегчает введение композиции индивидууму посредством инъекции или имплантации. В одном из вариантов осуществления средство доставки может содержать катетер. В дополнительном варианте осуществления средство доставки может содержать шприц.
ДОЗИРОВАНИЕ
Дозирование MSC и любого дополнительного терапевтического средства изменяется в зависимости от симптомов, возраста и массы тела пациента, природы и тяжести нарушения, подлежащего лечению или профилактике, пути введения и формы дополнительного терапевтического средства. Композиции по изобретению можно вводить в однократной дозе или в дробных дозах. Подходящие дозы для MSC и любого дополнительного терапевтического средства(в) можно определять известными способами.
Как правило, указанная доза составляет приблизительно 10×106 клеток/кг массы индивидуума или менее, составляет приблизительно 9×106 клеток/кг или менее, составляет приблизительно 8×106 клеток/кг или менее, составляет приблизительно 7×106 клеток/кг или менее, составляет приблизительно 6×106 клеток/кг или менее, составляет приблизительно 5×106 клеток/кг или менее. В альтернативном варианте осуществления указанная доза может составлять приблизительно от 0,25×106 клеток/кг приблизительно до 5×106 клеток/кг или более предпочтительно приблизительно от 1×106 клеток/кг приблизительно до 5×106 клеток/кг. Таким образом, в дополнительных альтернативных вариантах осуществления доза может составлять приблизительно 0,25×106 клеток/кг, 0,5×106 клеток/кг, 0,6×106 клеток/кг, 0,7×106 клеток/кг; 0,8×106 клеток/кг; 0,9×106 клеток/кг; 1,1×106 клеток/кг; 1,2×106 клеток/кг; 1,3×106 клеток/кг; 1,4×106 клеток/кг; 1,5×106 клеток/кг; 1,6×106 клеток/кг; 1,7×106 клеток/кг; 1,8×106 клеток/кг; 1,9×106 клеток/кг или 2×106 клеток/кг. В других вариантах осуществления доза может составлять от 0,1 до 1 миллиона клеток/кг или от 1 до 2 миллионов клеток/кг или от 2 до 3 миллионов клеток/кг, или от 3 до 4 миллионов клеток/кг; или от 4 до 5 миллионов клеток/кг, или от 5 до 6 миллионов клеток/кг, или от 6 до 7 миллионов клеток/кг, или от 7 до 8 миллионов клеток/кг, или от 8 до 9 миллионов клеток/кг, или от 9 до 10 миллионов клеток/кг.
В альтернативном варианте осуществления клетки можно вводить пациенту в виде фиксированной дозы, независимо от массы пациента. Как правило, указанная доза составляет приблизительно от 10 миллиона клеток до 500 миллионов клеток, например, указанная доза составляет приблизительно 10×106 клеток, 50×106 клеток, 10×107 клеток, 50×107 клеток.
Таким образом, в одном из вариантов осуществления изобретение относится к MSC, таким как ASC для применения в лечении сепсиса, вторичного по отношению к пневмонии, такого как тяжелый сепсис, вторичный по отношению к пневмонии, у являющегося человеком индивидуума, где MSC вводят внутривенным путем, например, посредством внутривенной инъекции в дозе приблизительно от 0,25×106 клеток/кг приблизительно до 5×106 клеток/кг массы индивидуума. Характерная доза составляет 4×106 клеток/кг массы индивидуума. Сепсис может являться вторичным по отношению к бактериальной пневмонии (например, грамотрицательной пневмонии).
В другом варианте осуществления, который можно необязательно объединять с указанным выше вариантом осуществления, изобретение относится к MSC, таким как ASC, для применения для лечения сепсиса, вторичного по отношению к пневмонии, такого как тяжелый сепсис, вторичный по отношению к пневмонии, у являющегося человеком индивидуума, где MSC вводят повторно, например, вводят две или более доз, например, по меньшей мере 3 дозы, по меньшей мере 4, 5, 6, 7, 8, 9 или 10 доз. В одном из вариантов осуществления вводят две дозы. В другом варианте осуществления вводят три дозы. В дополнительном варианте осуществления вводят четыре дозы. Интервал между дозами может составлять одни сутки, одну неделю или один месяц. Как правило, интервал составляет одни сутки. MSC можно вводить в течение периода не более 1 недели (например, с суточными интервалами, такими как 1 и 3 суток или 1, 3 и 5 суток, или 1, 3, 5 и 7 суток). В одном из вариантов осуществления две дозы MSC вводят с интервалом одни сутки, например, на сутки 1 и сутки 3 (сутки 1 означают первую дозу MSC).
Точное время введения и количество конкретного средства, которое приведет к наиболее эффективному лечению у данного пациента, зависит от активности, фармакокинетики и биодоступность средства, физиологического состояния пациента (включая возраст, пол, тип и стадию заболевания, общее физическое состояние, ответную реакцию на данную дозу и тип лекарственной терапии), пути введения и т.д. Информацию, представленную в настоящем описании, можно использовать для оптимизации лечения, например, определения оптимального времени и/или количества введения, для которого требуется не более чем общепринятое экспериментирование, такое как мониторинг индивидуума и подбор дозы и/или времени дозирования. В то время как индивидуум получает лечение, за здоровьем индивидуума можно проводить мониторинг путем оценки одного или более соответствующих показателей в определенный момент времени в течение периода продолжительностью 24 часа. Схемы лечения, включая дозы, время введения и составы можно оптимизировать в соответствии с результатами такого мониторинга.
Лечение можно начинать с меньших доз, которые являются меньше оптимальной дозы. В дальнейшем дозу можно повышать небольшими шагами до тех пор, пока не получают оптимальный терапевтический эффект.
Комбинированное использование нескольких терапевтически средств может снижать необходимую дозу для любого отдельного компонента, т.к. начало и продолжительность эффекта различных компонентов может являться комплементарным. В такой комбинированной терапии различные активные средства можно доставлять совместно или раздельно и одномоментно или в различные моменты времени в течение суток.
ВИДЫ АДЪЮВАНТНОЙ ТЕРАПИИ
В одном из вариантов осуществления фармацевтическая композиция по изобретению может содержать одно или более (или два или более, или три или более, например, 1, 2, 3, 4 или 5) дополнительных терапевтических средств, или альтернативно ее можно вводить в сочетании с одним или более (или двумя или более, или тремя или более, например, 1, 2, 3, 4 или 5) дополнительными терапевтическими средствами.
В некоторых вариантах осуществления MSC и одно или более дополнительных терапевтических средств можно вводить индивидууму одновременно. В других вариантах осуществления MSC и одно или более дополнительных терапевтических средств можно вводить индивидууму последовательно. Одно или более дополнительных терапевтических средств можно вводить до или после введения MSC.
Указанное в качестве терапевтического средства можно выбирать из следующего ниже: анальгетика, такого как нестероидное противовоспалительное лекарственное средство, агониста или салицилата опиата; противоинфекционного средства, такого как антигельминтик, противоанаэробный препарат, антибиотик, аминогликозидный антибиотик, противогрибковый антибиотик, антибиотик широкого спектра действия, цефалоспоринный антибиотик, макролидный антибиотик, β-лактамный антибиотик, пенициллиновый антибиотик, хинолоновый антибиотик, сульфонамидный антибиотик, тетрациклиновый антибиотик, противомикобактериального препарата, противотуберкулезного противомикобактериального препарата, противопротозойного средства, противомалярийного антипротозойного средства, противовирусного средства, антиретровирусного средства, противочесоточного средства, противовоспалительного средства, кортикостероидного противовоспалительного средства, противозудного средства/местного анестетика, местного противоинфекционного средства, противогрибкового местного противоинфекционного средства, противовирусного местного противоинфекционного средства; электролитическое и почечное средство, такие как повышающее кислотность средство, подщелачивающее средство, диуретик, диуретик ингибитор карбоангидразы, петлевой диуретик, осмотический диуретик, калийсберегающий диуретик, тиазадный диуретик, восполняющее электролиты средство и средство, способствующее выведению мочевой кислоты; фермента, такого как панкреатический фермент и тромболитический фермент; желудочно-кишечного средства, такого как противодиарейное средство, противорвотное средство, желудочно-кишечное противовоспалительное средство, салицилатное желудочно-кишечное противовоспалительное средство, антацидное противоязвенное средство, противоязвенное средство на основе ингибитора протонного насоса образования желудочного сока, противоязвенное средство, направленное на для слизистую желудка, противоязвенное средство на основе H2-блокатора, холелитолитическое средство, способствующее пищеварению средство, рвотное средство, слабительное средство и размягчающее стул средство и прокинетическое средсто; общего анестетика, такого как ингаляционный анестетик, галогенированный ингаляционный анестетик, внутривенный анестетик, барбитуратный внутривенный анестетик, бензодиазепиновый внутривенный анестетик и an внутривенный анестетик на основе опиатного агониста; гормона или гормонального модификатора, такого как абортивное средство, средство, действующее на надпочечники, кортикостероидное средство, действующее на надпочечники, андроген, антиандроген, иммунобиологическое средство, такое как иммуноглобулин, иммуносупрессорное средство, анатоксин и вакцина; местного анестетика, такого как амидный местный анестетик и местный анестетик на основе сложного эфира; средства, действующего на скелетные мышцы, такого как противоподагрическое противовоспалительное средство, кортикостероидное противовоспалительное средство, противовоспалительное средство на основе соединений золота, иммуноподавляющее противовоспалительное средство, нестероидное противовоспалительное лекарственное средство (NSAID), салицилатное противовоспалительное средство, минерала, и витаминов, таких как витамин A, витамин B, витамин C, витамин D, витамин E и витамин K.
В другом варианте осуществления дополнительное терапевтическое средство может представлять собой фактор роста или другую молекулу, которая влияет на клеточную пролиферацию или активацию. В дополнительном варианте осуществления такой фактор роста может индуцировать конечную дифференцировку. В другом варианте осуществления фактор роста может представлять собой вариант или фрагмент природного фактора роста. Способы получения таких вариантов хорошо известны в данной области и могут включать, например, создание консервативных аминокислотных замен или посредством мутагенеза и оценку получаемого варианта в отношении необходимой функциональности.
Ниже изобретение дополнительно проиллюстрировано следующими ниже примерами. Эти примеры приведены только в качестве иллюстрации и не предназначены являться ограничивающими.
ПРИМЕР 1
Эффект лечения ASC на ассоциированный с пневмонией сепсис
Задача: определить эффект ASC, вводимых через 6 часов после инфекции, на прогрессирование и распространение бактерий и на уровни провоспалительных цитокинов в легком.
Мыши:
- В возрасте от восьми до двенадцати недель беспатогенные самки мышей C57BL/6.
- Мышей случайным образом распределяли и содержали в течение 7 суток до эксперимента для акклиматизации.
- Животных в эксперименте наблюдали дважды в сутки. В случае очень тяжелого заболевания необходимым является более частое (6×) наблюдение и по существу в соответствии с комитет по этике обращения с животными.
Пневмония
Грамотрицательную пневмонию индуцировали интраназальной инстилляцией живых Klebsiella pneumoniae 2 серотипа (1×104 КОЕ; ATCC 43816; American Type Culture Collection). Бактерии культивировали в среде трипсиновой соевый бульон (TSB) и планшетах с кровяным агаром (BA).
Сутки -1: начало культивирования
Один слой исходного раствора Klebsiella pneumoniae -80°C помещали в 50 мл среды TSB и растили в течение ночи (16 часов) при 37°C.
Сутки 0: получение инокулята
1 мл культуры (сутки -1) ресуспендировали в 100 мл (теплой) среды TSB и растили до OD=1,0 (±2,5-3 часов). 10 мл культуры промывали холодным стерильным 0,9% NaCl (Baxter) при центрифугировании при 4000 об/мин в течение 10 минут при 4°C. Супернатант удаляли и промывали еще 2 раза, как описано выше. Осадок ресуспендировали в 10 мл NaCl, концентрация бактерий составляла приблизительно 0,4×109 КОЕ/мл. Получаемый раствор разбавляли в 2000 раза приблизительно до 20×104 КОЕ/мл. Концентрацию инокулята проверяли путем высевания 50 мкл инокулята в разведениях 102-104 на три планшета BA. КОЕ подчитывали после культивирования в течение ночи при 37°C (сутки 1). Мышей инокулировали.
Инокулят: 50 мкл/мышь при 1×104 КОЕ
Стволовые клетки
ASC (1×106 размноженные стволовые клетки, жировой ткани человека) или плацебо (лактат Рингера) вводили внутривенно через 6 часов после интраназальной инокуляции мышей.
План исследования
T=0 часов
- Анестетик изофлуран
- Все мыши: интраназальная инстилляция живых Klebsiella pneumoniae 2 серотипа (50 мкл, 1×104 КОЕ)
T=6 часов
- Группа I: (n=8) 1× внутривенная (в/в) инъекция 200 мкл плацебо (лактат Рингера)
- Группа II: (n=8) 1× в/в инъекция 1×106 ASC (в 200 мкл лактата Рингера)
T=48 часов: умерщвление мышей
Конечные точки исследования
- Бактериальные нагрузки в легких, селезенка, печени и крови (полуколичественные культуры)
- Воспаление: цитокин (TNF-α, IL-1β, IL-6) и хемокин (MIP-2) в гомогенатах легких
Результаты
На фигурах 1-8 представлены результаты двух независимых экспериментов (отмеченных A и B, соответственно). Как представлено на фигурах 1-4 по сравнению с плацебо, лечение ASC после 6 часов инфекции снижало бактериальную нагрузку в крови (фигура 1) и легких (фигура 2), а также снижало бактериальные нагрузки в печени (фигура 3) или селезенке (фигура 4). Кроме того, как представлено на фигурах 5-8, уровни провоспалительных цитокинов и хемокинов снижались в гомогенатах легких после лечения ASC по сравнению с плацебо. Эти результаты демонстрируют, что лечение ASC снижает тяжесть ассоциированного с пневмонией сепсиса. Бактериальные нагрузки и уровни провоспалительных цитокинов/хемокинов снижались в различных выделениях, включая органы-мишени, релевантные для пневмонии, такие как кровь и легкие. Таким образом, MSC, такие как ASC, неожиданно является пригодными для лечения ассоциированного с пневмонией сепсиса.
Результаты дополнительного исследования приведены на фигурах 9-12, вновь демонстрирующих, что внутривенное введение ASC при ассоциированном с пневмонией сепсисом снижает бактериальную нагрузку в различных органах, таких как кровь.
ПРИМЕР 2
Клиническое испытание проводят на пациентах с тяжелой пневмонией, тяжелым сепсисом или септическим шоком. Пациентов включают в исследование в течение 24 часов после диагностики сепсиса.
Приблизительно половина пациентов, включенных в исследование, получают лечение лекарственным препаратом, содержащим суспензию размноженных получаемых от донора (аллогенных) стромальных клеток жировой ткани (eASC) в растворе лактата Рингера. Другая половина получат плацебо, состоящее из суспензии лактата раствора Рингера. Пациенты в группе лечения получают однократную дозу 4 миллионов клеток/кг массы тела пациента лекарственного препарата. Пациенты в группе плацебо получают однократную дозу плацебо. В обоих случаях введение проводят посредством внутривенной инфузии.
Лекарственный препарат представляет собой клеточную суспензию в стерильном растворе буфера, содержащем стромальные клетки жировой ткани (eASC) аллогенного происхождения в одноразовых флаконах, получаемые в результате липоаспирации у здоровых индивидуумов и размноженные in vitro. Лекарственный препарат поставляют в виде стерильной, прозрачной, бесцветной суспензии для внутриочагового введения, предоставляемой в 6 мл флаконах (суспензия 10 миллионов eASC на мл модифицированной Дульбекко среде Игла [DMEM] с сывороточным альбумином человека). Лекарственный препарат вводят как суспензию в лактате раствора Рингера при скорости инфузии 4 мл/мин.
Исследуемое плацебо представляет собой лактат раствора Рингера для внутриочагового введения при скорости инфузии 4 мл/мин. Соответствующий объем плацебо (лактат раствора Рингера) вводят каждому индивидууму из групп плацебо. Объем плацебо рассчитывают в соответствии с массой индивидуума.
Получение лекарственного препарата
Лекарственный препарат на основе аллогенных eASC состоит из клеточной суспензии живых взрослых стромальных клеток, экстрагированных из подкожной жировой ткани здоровых доноров. Подкожную жировую ткань удаляли липосакцией у здорового донора и транспортировали на производственное предприятие GMP. Донорство, заготовку и тестирование проводят в соответствии с требованиями Директивы 2004/23/EC и, таким образом, в соответствии с директивами 2006/17/EC и 2006/83/EC. ASC выделяют посредством расщепления коллагеназой I типа жировой ткани с последующим центрифугированием. Получаемый клеточный осадок ресуспендируют и лизируют в лизирующим эритроциты растворе, и центрифугируют. Стромальную сосудистую фракцию, получаемую из клеточного осадка, помещают в контейнеры для культивирования клеток в среду для культивирования и антибиотики и инкубируют при 37°C и 5% CO2 и в увлаженной атмосфере. Через 24-48 часов после высевания среду для культивирования удаляют для устранения фракций неприкрепившихся клеток. ASC, прикрепившиеся к пластиковым планшетам для культивирования размножают в условиях in vitro. Каждые 3-4 суток среду для культивирования заменяют после достижения 90-95% конфлюэнтности и открепляют клетки трипсином/EDTA, собирают, центрифугируют и размножают без антибиотиков до необходимого удвоения. Затем их собирают и криоконсервируют до использования. Перед назначенной датой введения размораживают достаточное количество криоконсервированных флаконов для обеспечения необходимой дозы для введения. ASC восстанавливают из их криоконсервированного состояния путем высевания и культивирования (для подтверждения жизнеспособности). На сутки, когда флаконы заполняют и упаковывают, культуры промывали раствором фосфатного буфера и трипсином/EDTA. ASC сразу же ресуспендировали в отобранных эксципиентах (модифицированная Дульбекко среда Игла и сыворотка с альбумином человека) для формулирования лекарственного продукта.
eASC характеризуют в отношении идентичности (фенотипического профиля), чистоты, активности, морфологии, жизнеспособности и кинетики клеточного роста в соответствии с Руководством по лекарственным препаратам на основе клеток (EMEA/CHMP/410869/2006) и Аналитического доклада по стволовым клеткам (EMA/CAT/ 571134/2009).
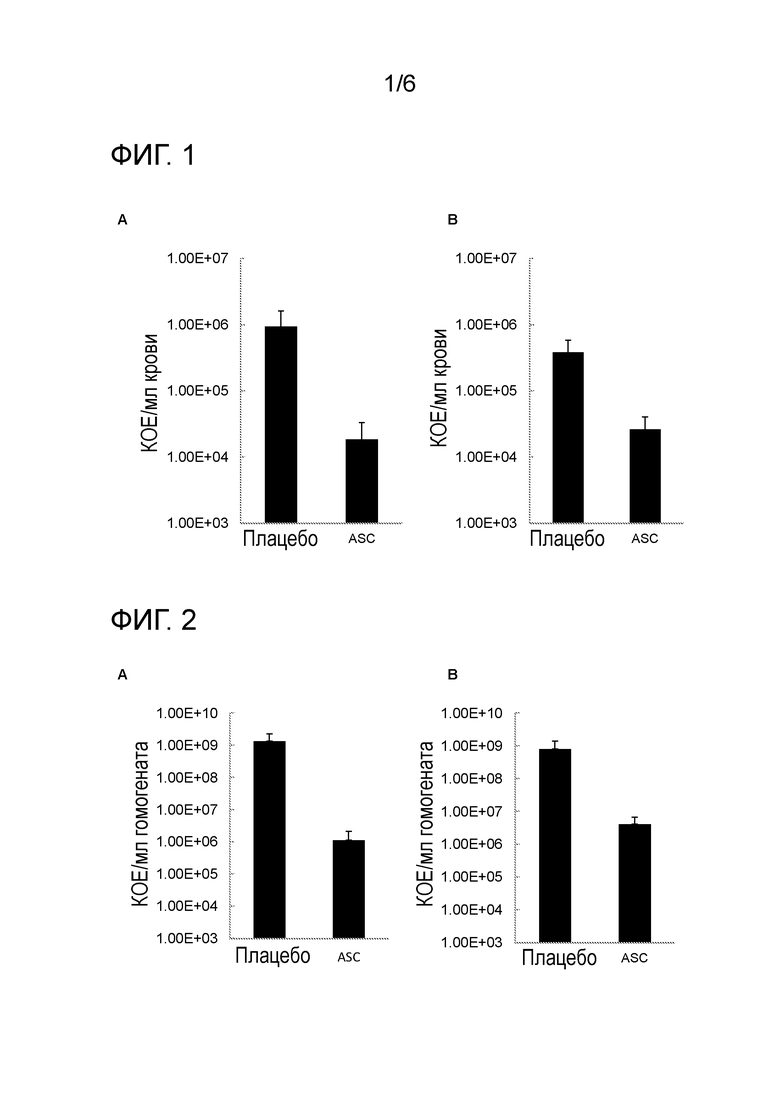





Изобретение относится к области биотехнологии, а именно к применению композиции, применению мультипотентных мезенхимальных стромальных клеток и способу лечения сепсиса у индивидуума. Способ включает введение композиции, содержащей мультипотентные мезенхимальные стромальные клетки жировой ткани в подходящей дозе, для лечения сепсиса, являющегося вторичным по отношению к пневмонии, у индивидуума, являющегося человеком, путем внутривенного введения композиции. Также предложено применение мультипотентных мезенхимальных стромальных клеток в подходящей дозе в производстве лекарственного средства для лечения сепсиса у индивидуума, являющегося человеком. Изобретение позволяет расширить арсенал технических средств. 3 н. и 20 з.п. ф-лы, 12 ил., 2 пр.
1. Применение композиции, содержащей мультипотентные мезенхимальные стромальные клетки в подходящей дозе, для лечения сепсиса у индивидуума, являющегося человеком, где мультипотентные мезенхимальные стромальные клетки представляют собой стромальные клетки жировой ткани (ASC), где сепсис является вторичным по отношению к воспалительному состоянию легких, где воспалительным состоянием легких является пневмония, и, где композицию вводят внутривенным путем.
2. Применение мультипотентных мезенхимальных стромальных клеток в подходящей дозе в производстве лекарственного средства для лечения сепсиса у индивидуума, являющегося человеком, где мультипотентные мезенхимальные стромальные клетки представляют собой стромальные клетки жировой ткани (ASC), где сепсис является вторичным по отношению к воспалительному состоянию легких, где воспалительным состоянием легких является пневмония, и, где лекарственное средство вводят внутривенным путем.
3. Применение по п. 1 или 2, где сепсис представляет собой тяжелый сепсис.
4. Применение по любому из предшествующих пунктов, где пневмония вызвана бактериями.
5. Применение по любому из предшествующих пунктов, где клетки представляют собой размноженные стромальные клетки жировой ткани.
6. Применение по любому из предшествующих пунктов, где ASC являются аллогенными.
7. Применение по любому из предшествующих пунктов, где композиция или лекарственное средство содержит от приблизительно 0,25×106 клеток/кг до приблизительно 5×106 клеток/кг массы индивидуума.
8. Применение по любому из предшествующих пунктов, где мультипотентные мезенхимальные стромальные клетки вводят индивидууму несколько раз, например, на сутки 1 и сутки 3.
9. Применение по любому из предшествующих пунктов, где по меньшей мере приблизительно 50% ASC экспрессируют один или более из маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105.
10. Применение по любому из предшествующих пунктов, где по меньшей мере приблизительно 50% ASC не экспрессируют маркеры фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133.
11. Применение по любому из предшествующих пунктов, где ASC вводят в фармацевтически приемлемом носителе и/или разбавителе.
12. Применение по любому из предшествующих пунктов, где ASC вводят в сочетании с одним или более дополнительных терапевтических средств.
13. Способ лечения сепсиса у индивидуума, являющегося человеком, включающий введение композиции, содержащей мультипотентные мезенхимальные стромальные клетки в подходящей дозе, индивидууму, где мультипотентные мезенхимальные стромальные клетки представляют собой стромальные клетки жировой ткани (ASC), где сепсис является вторичным по отношению к воспалительному состоянию легких, где воспалительным состоянием легких является пневмония, и, где композицию вводят внутривенным путем.
14. Способ по п. 13, где сепсис представляет собой тяжелый сепсис.
15. Способ по п. 13 или 14, где пневмония вызвана бактериями.
16. Способ по любому из пп. 13-15, где клетки представляют собой размноженные стромальные клетки жировой ткани.
17. Способ по любому из пп. 13-16, где ASC являются аллогенными.
18. Способ по любому из пп. 13-17, где композиция содержит от приблизительно 0,25×106 клеток/кг до приблизительно 5×106 клеток/кг массы индивидуума.
19. Способ по любому из пп. 13-18, где мультипотентные мезенхимальные стромальные клетки вводят индивидууму несколько раз, например на сутки 1 и сутки 3.
20. Способ по любому из пп. 13-19, где по меньшей мере приблизительно 50% ASC экспрессируют один или более из маркеров CD9, CD10, CD13, CD29, CD44, CD49A, CD51, CD54, CD55, CD58, CD59, CD90 и CD105.
21. Способ по любому из пп. 13-20, где по меньшей мере приблизительно 50% ASC не экспрессируют маркеры фактор VIII, альфа-актин, десмин, S-100, кератин, CD11b, CD11c, CD14, CD45, HLAII, CD31, CD34, CD45, STRO-1 и CD133.
22. Способ по любому из пп. 13-21, где ASC вводят в фармацевтически приемлемом носителе и/или разбавителе.
23. Способ по любому из пп. 13-22, где ASC вводят в сочетании с одним или более дополнительных терапевтических средств.
| HALL S.R.R., et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| WO 2010015929 A2 (CELLERIX SACONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS), 11.02.2010 | |||
| WO 2005093044 A1 (OSIRIS THERAPEUTICS, INC | |||
| ), | |||
Авторы
Даты
2020-03-03—Публикация
2015-06-30—Подача