Область техники, к которой относится изобретение
Настоящее изобретение относится к применению антоцианидинов из семейства флавоинидов, в частности, 3-дезоксиантоцианидинов для лечения, профилактики и/или стабилизации глазных болезней, в частности для лечения, профилактики и/или стабилизации возрастной макулодистрофии (ВМД), болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
Предшествующий уровень техники
Накопление липофусцинов в клетках сетчатки, таких как клетки ретинального пигментного эпителия (РПЭ), сопутствует различным глазным болезням и происходит в процессе старения. Липофусцины клеток РПЭ содержат липиды, белки и гетерогенную смесь флуорофоров, в частности, А2Е (N-ретинил-N-ретинилиденэтаноламина).
А2Е является побочным продуктом цикла превращений родопсина (фиг. 1), который генерируется во внешнем сегменте фоторецепторов в форме предшественника, связанного с фосфолипидом. В ходе цикла превращений родопсина под действием света в фоторецепторах происходит изомеризация 11-цис-ретиналя в полный транс-ретиналь. Клетки РПЭ позволяют восстанавливать 11-цис-ретиналь из полного транс-ретиналя. Кроме того, клетки РПЭ ежедневно поглощают и разлагают часть мембран внешних сегментов фоторецепторов, чтобы на их основе могли появляться новые диски. Тем не менее, полный транс-ретиналь целиком не восстанавливается в 11-цис-ретиналь, и его часть преобразуется в А2Е за счет конденсации двух молекул полного транс-ретиналя с этаноламином. С возрастом происходит постепенное накопление А2Е в клетках РПЭ.
Продемонстрировано, что накопление липофусцинов в клетках РПЭ, в частности, накопление А2Е вызывает увеличение гибели клеток РПЭ. В действительно, под действием синего света и в присутствии кислорода А2Е генерирует активные частицы, которые вызывают повреждение белков, липидов и ДНК, и, соответственно, существенный окислительный стресс в стареющих клетках РПЭ (Sparrow JR and Cai В., Invest Ophthalmol Vis Sci, 2001, 42, 1356-1362; Sparrow JR и др., J Biol Chem, 2003, 278 (20), 18207-18213). Образующиеся при этом выделения накапливаются и в конечном итоге вызывают в различных местах гибель клеток РПЭ с последующей гибелью фоторецепторов, с которыми они были связаны.
С накоплением липофусцинов в клетках РПЭ связаны различные глазные болезни, такие как, например, ВМД или болезнь Штаргардта.
ВМД является прогрессирующим и истощающим хроническим дегенеративным заболеванием сетчатки, которое поражает субъектов пожилого возраста и которое имеет многофакторное происхождение. Оно является причиной необратимой слепоты среди пожилого населения, в частности, в Европе и Северной Америке.
ВМД поражает центральную часть сетчатки, называемую желтым пятном, что приводит к тяжелому нарушению зрения и необратимой потере центрального зрения. Патофизиологические механизмы ВМД по-прежнему малопонятны, но установлено, что в них может быть вовлечено прогрессирующее накопление липофусцинов и физиологическое старение РПЭ.
Для ранней стадии ВМД характерны отложения, называемые друзами, которые лишь минимально влияют на зрение. Более поздние стадии ВМД включают две ее тяжелые формы: сухую, также называемую географической атрофией, и влажную, также известную как экссудативная или неоваскулярная форма. Сухая форма встречается чаще, чем влажная, но только влажная форма поддается лечению в настоящее время.
В основе существующей профилактики или лечения лежит применение пищевых добавок, содержащих антиоксиданты общего типа, такие как, например, цинк, витамины А, С и Е, терапевтическая эффективность которых ограничена.
Соответственно, существует потребность в новых активных соединениях для лечения, профилактики и/или стабилизации ВМД, в частности, сухой ВМД, но также для лечения, профилактики и/или стабилизации глазных болезней, связанных с накоплением липофусцинов в клетках сетчатки, таких как болезнь Штаргардта.
Сообщалось об использовании в этих целях антоцианинов, получаемых из натуральных экстрактов (Liu и др., British J. Nutr., 2012, 108, 16-27; Wang и др., J. Sci. Food Agric, 2015, 95, 936-944).
Антоцианины относятся к классу полифенолов и входят в состав пигментов, которые от природы присутствуют в плодах и цветах. В структуру этих соединений входит катион флавилия, связывающий гликозид (Схема 1). Основу природных антоцианинов составляют 6 различных агликонов, связывающих различные сахара, наиболее распространенными из которых являются глюкоза, галактоза и арабиноза. Агликоновая часть антоцианинов называется антоцианидином.
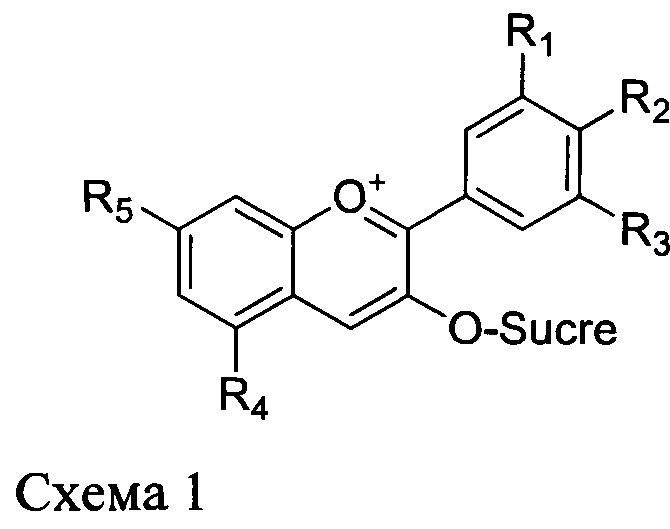
Общая структура природных антоцианинов, в которой R1-R5 предпочтительно означают Н или ОН.
У Sparrow и др. (WO 2005/077176) также описано применение антоцианинов для лечения или профилактики глазных болезней, связанных с накоплением А2Е в клетках РПЭ. Было осуществлено сравнение активности некоторых антоцианинов и эквивалентных им антоцианидинов. В частности, были оценены цианидин, петунидин и мальвидин (Таблица 1), которые продемонстрировали фотопротекторную активность, эквивалентную активности, полученной у соответствующих антоцианинов, при этом выживаемость клеток РПЭ под действием синего света составляла 30-70% после инкубации со 100 мкМ соединений.

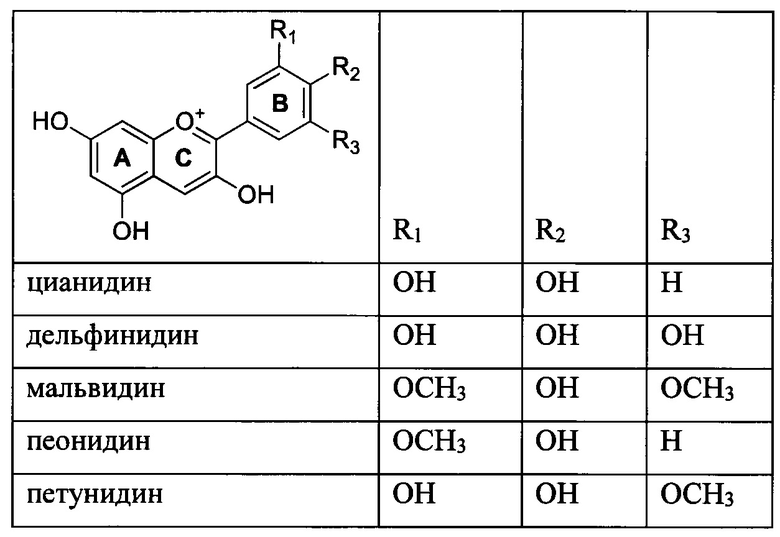
Другие исследования также продемонстрировали, что природные антоцианидины могут оказывать фотопротекторное действие на клетки РПЭ (Tanaka и др., J. Agric. Food Chem., 2011, 59, 528-536; Tanaka и др., Life Sciences, 2013, 92, 17-25; FR 2996773). В частности, в этих исследованиях оценивались цианидин, дельфинидин, пеонидин и мальвидин. Цианидин и дельфинидин, по-видимому, обладают фотопротекторным действием в отличие от мальвидин. Результаты, полученные в отношении пеонидина, являются противоречивыми.
Тем не менее, в других исследованиях делался вывод о неэффективности антоцианидинов, в частности, цианидина, дельфинидина, пеонидина, петунидина и мальвидина с точки зрения выживаемости клеток РПЭ (Hanneken и др., Invest. Ophthal. Visual Sci., 2006; 47 (7), 3164-3177; Majumdaar and Srirangam, J. Pharm. Pharmacol., 2010, 62, 951-965).
Таким образом, из техники известны противоречивые сведения об эффективности антоцианидинов в отношении фотопротекции клеток РПЭ.
Несмотря на существующие предубеждения, заявитель глубоко изучил активность природных и неприродных антоцианидинов в отношении фотопротекции клеток РПЭ.
Заявитель неожиданно обнаружил, что 3-дезоксиантоцианидины, содержащие, по меньшей мере, одну гидроксильную группу в цикле А и в цикле В, обладают отличной фотопротекторной активностью. В частности, настоящее изобретение относится к применению 3-дезоксиантоцианидинов Формулы I:
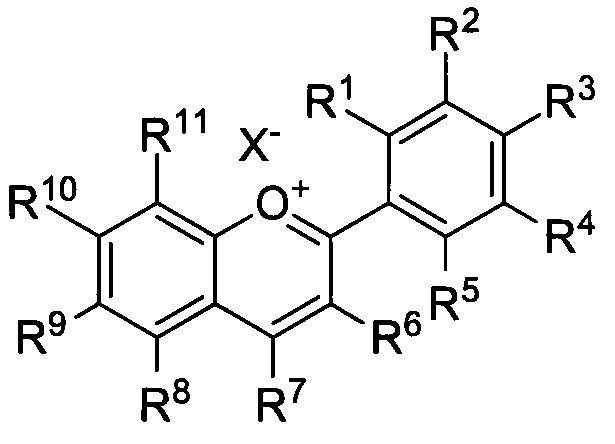
в которой R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и X- имеют следующие значения, в частности, R6 отличается от гидроксила, по меньшей мере, один из R1, R2, R3, R4 или R5 означает гидроксил, и, по меньшей мере, один из R8, R9, R10 или R11 означает гидроксил; для лечения, профилактики и/или стабилизации ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
Настоящее изобретение продемонстрировало эффективность этих соединений с использованием клеточной модели фототоксичности, индуцированной взаимосвязью между лечением с помощью А2Е и облучением синим светом, на первичных культурах РПЭ. Заявитель также продемонстрировал, что эти соединения обеспечивают фотопротекцию на модели in vivo.
Краткое изложение сущности изобретения
Таким образом, изобретение относится к соединению Формулы I

в которой
R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил;
R6 означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино;
R7 означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино;
R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино, при условии, что один из R8, R9, R10 или R11 означает гидроксил;
X- означает анион, выбранный из: аниона, полученного из минеральной кислоты, такого как, например, анион бромида, хлорида, боротетрафторида или перхлорида; аниона, полученного из органической кислоты, такого как, например, анион ацетата, бората, цитрата, тартрата, бисульфтата, сульфата или фосфата; или аниона, полученного из сульфатной или сульфонатной группы;
для применения при лечении, профилактики и/или стабилизации ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
В одном из вариантов осуществления R6 в соединении Формулы I означает атом водорода.
В одном из вариантов осуществления соединением Формулы I является соединение Формулы Ia

в которой R1, R2, R3, R4, R5, R8, R10 и X- имеют оговоренные выше значения.
В одном из вариантов осуществления в соединении согласно изобретению
R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила и алкокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил; и
R8 и R10 каждый независимо означает группу, выбранную из водорода, гидроксила и алкокси, при условии, что один из R8 или R10 означает гидроксил.
В одном из вариантов осуществления соединением Формулы I является соединение Формулы Ib

в которой R1, R2, R3, R8 и X- имеют оговоренные выше значения.
В одном из вариантов осуществления R8 в соединении согласно изобретению означает атом водорода.
В одном из вариантов осуществления соединение для применения согласно изобретению выбрано из:
2',7-дигидрокси-4'-метокси-флавилийхлорида;
2',3',7-тригидрокси-4'-метокси-флавилийхлорида;
3',7-дигидрокси-4'-метокси-флавилийхлорида;
4',5,7-тригидрокси-флавилийхлорида;
3',5,7-тригидрокси-4'-метокси-флавилийхлорида;
3',4',5',5,7-пентадрокси-флавилийхлорида;
3',4',5,7-тетрагидрокси-флавилийхлорида.
Изобретение также относится к соединению, выбранному из:
2',7-дигидрокси-4'-метокси-флавилийхлорида;
2',3',7-тригидрокси-4'-метокси-флавилийхлорида.
Изобретение также относится к фармацевтической композиции, содержащей соединение, выбранное из 2',7-дигидрокси-4'-метокси-флавилийхлорида и 2',3',7- тригидрокси-4'-метокси-флавилийхлорида, в сочетании с фармацевтически приемлемым носителем.
Изобретение также относится к лекарству, содержащему соединение, выбранное из 2',7-дигидрокси-4'-метокси-флавилийхлорида и 2',3',7-тригидрокси-4'-метокси-флавилийхлорида.
Определения
Приведенные далее термины имеют следующее значение в настоящем изобретении:
- "ацилокси" означает алкильную группу -(С=O)-O;
- "алкенил" означает любую линейную или разветвленную, необязательно замещенную углеводородную цепь, содержащую, по меньшей мере, одну двойную связь из 2-12 атомов углерода, предпочтительно 2-6 атомов углерода; такой как, например, винил или аллил;
- "алкиларил" означает алкиларильную группу;
- "алкил" означает насыщенную линейную или разветвленную углеводородную цепь из 1-12 атомов углерода, предпочтительно от 1-6 атомов углерода, более предпочтительно метил, этил, пропил, изопропил, n-бутил, втор-бутил, изобутил, трет-бутил;
- "алкокси" означает алкильную группу -О;
- "амино" означает группу -NH2 или любую группу, полученную из -NH2 путем замещения одного или нескольких атомов водорода замещенной или незамещенной, алифатической, или ароматической органической группой. Группами, полученными из -NH2, предпочтительно являются алкиламиногруппы, т.е. N-алкильные группы, содержащие моноалкиламино- и диалкиламиногруппы;
- "аралкил" означает арилалкильную группу;
- "арил" означает моно- или полициклическую систему из 5-20, предпочтительно 6-12 атомов углерода, которые имеют одно или несколько ароматических колец, из числа которых можно упомянуть фенильную группу, бифенильную группу, 1-нафтильную группу, 2-нафтильную группу, тетрагидронафтильную группу, инданильную группу и бинафтильную группу. Арильная группа может быть замещена 1-3 заместителями, выбранными независимо друг от друга из гидроксильной группы, линейной или разветвленной алкильной группы, содержащей 1, 2, 3 4, 5 или 6 атомов углерода, в частности, метила, этила, пропила, бутила, алкоксильной группы или атома галогена, в частности, брома, хлора и йода;
- "арилокси" означает арильную группу -О;
- "гало" означает фтор, хлор, бром или йод;
- "гетероарил" означает моно- или полициклическую группу из 5-20, предпочтительно 5-12 атомов углерода, которые имеют одно или несколько ароматических колец, при этом один или несколько атомов углерода замещены гетероатомом, предпочтительно N, О или S, гетероатомы азота и серы необязательно способны к окислению, а гетероатомы азота необязательно способны к образованию четвертичного основания. Такие циклы могут быть сжаты до арильной, циклоалкильной, гетероарильной или гетероциклильной группы. Неограничивающими примерами такой гетероарильной группы являются пирролил, фуранил, тиофенил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, оксатриазолил, тиатриазолил, пиридинил, пиримидил, пиразинил, пиридизинил, оксазинил, диоксинил, тиазинил, триазинил, имидазо [2,1-b] [1,3] тиазолил, тиено [3,2-b] фуранил, тиено [3,2-b] тиофенил, тиено [2,3-d] [1,3] тиазолил, тиено [2,3-d] имидазолил, тетразоло [1,5-а] пиридинил, индолил, индолизинил, изоиндолил, бензофуранил, изобензофуранил, бензотиофенил, изобензотиофенил, индазолил, бензимидазолил, 1,3-бензоксазолил, 1,2-бензизоксазолил, 2,1-бензизоксазолил, 1,3-бензотиазолил, 1,2-бензоизотиазолил, 2,1-бензоизотиазолил, бензотриазолил, 1,2,3-бензохадиазолил, 2,1,3-бензохадиазолил, 1,2,3-бензотиадиазолил, 2,1,3-бензотиадиазолил, тиенопиридинил, пуринил, имидазо [1,2-а] пиридинил, 6-оксо-пиридизин-1(6Н)-ил, 2-оксо-пиридин-1(2Н)-ил, 6-оксо-пирудазин-1(6Н)-ил, 2-оксо- пиридин-1(2Н)-ил, 1,3-бензодиоксолил, хинолинил, изохинолинил, циннолинил, хиназолинил, хиноксалинил;
- "гетероарилокси" означает гетероарильную группу -О;
- "субъект" означает животное, включая человека. В контексте настоящего изобретения субъектом может являться "пациент", а именно, лицо, получающее медицинскую помощь, проходящее или прошедшее лечение или наблюдаемое на предмет развития болезни;
- "лечение" означает профилактику, ослабление или смягчение, по меньшей мере, одного нежелательного эффекта или симптома болезни.
- "профилактика болезни" означает предотвращение возникновения, по меньшей мере, одного нежелательного эффекта или симптома болезни. Термин "профилактика" в настоящем изобретении может означать вторичную профилактику, а именно, предотвращение повторного появления симптома или рецидива болезни;
- "стабилизация болезни" означает прекращение или замедление обострения, по меньшей мере, одного нежелательного эффекта или симптома болезни. Это также может означать ослабление последствий заболевания после его установления;
- "эффективное количество" означает количество действующего вещества, которое требуется и является достаточным для замедления или прекращения развития, обострения или ухудшения одного или нескольких симптомов болезни или нарушения; или для достижения симптомов облегчения болезни или состояния; или для лечения болезни или нарушения;
- "фармацевтически приемлемый носитель" означает носитель, которые не вызывает какой-либо нежелательной, аллергической или иной реакции при его введении животному, предпочтительно человеку. Он включает все растворители, дисперсные среды, покрытия, антибактериальные и противогрибковые средства, изотонические средства, замедлители всасывания и сходные соединения. В случае введения человеку препараты должны соответствовать стандартам стерильности, общей безопасности и чистоты согласно требованиям регулирующих органов, таких как, например, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) или Европейское агентство лекарственных средств (ЕМА);
- "применение" означает введение действующего вещества отдельно или в составе фармацевтически приемлемой композиции субъекту, которому требуется лечение или профилактика симптома или болезни.
Подробное описание изобретения
Соединения
Настоящее изобретение относится к 3-дезоксиантоцианидинам Формулы I
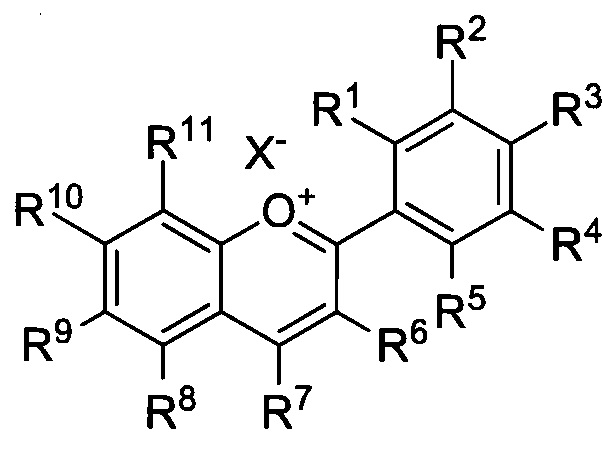
в которой
R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил;
R6 означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино;
R7 означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино;
R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода, гало, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, алкила, арила, аралкила, алкиларила, алкенила, нитро, нитрила, амино, при условии, что один из R8, R9, R10 или R11 означает гидроксил;
X- означает анион, выбранный из: аниона, полученного из минеральной кислоты, такого как, например, анион бромида, хлорида, боротетрафторида или перхлорида; аниона, полученного из органической кислоты, такого как, например, анион ацетата, бората, цитрата, тартрата, бисульфтата, сульфата или фосфата; или аниона, полученного из сульфатной или сульфонатной группы.
В одном из вариантов осуществления R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил, предпочтительно при условии, что один из R1, R2 или R3 означает гидроксил.
В одном из вариантов осуществления R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила, алкокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил, предпочтительно при условии, что один из R1, R2 или R3 означает гидроксил. Алкоксильной группой предпочтительно является метоксильная группа.
В одном из вариантов осуществления R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила, метокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил, предпочтительно при условии, что один из R1, R2 или R3 означает гидроксил.
В одном из вариантов осуществления R1 означает водород или гидроксил, предпочтительно R1 означает водород.
В одном из вариантов осуществления R1 означает водород или гидроксил.
В одном из вариантов осуществления R3 означает гидроксил или алкокси. В одном из частных вариантов осуществления R3 означает гидроксил. В одном из частных вариантов осуществления R3 означает алкокси, предпочтительно метокси.
В одном из вариантов осуществления R4 означает водород. В одном из частных вариантов осуществления R5 означает водород. В одном из частных вариантов осуществления R4 и R5 означают водород.
В одном из вариантов осуществления R6 означает водород, алкил, алкокси или арил. В одном из вариантов осуществления R6 означает водород.
В одном из вариантов осуществления R7 означает водород, гидроксил или алкокси, предпочтительно R7 означает водород.
В одном из вариантов осуществления R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода, гидроксила, алкокси, арилокси, гетероарилокси, ацилокси, при условии, что один из R8, R9, R10 или R11 означает гидроксил, предпочтительно при условии, что один из R8 или R10 означает гидроксил.
В одном из вариантов осуществления R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода, гидроксила, алкокси, при условии, что один из R8, R9, R10 или R11 означает гидроксил, предпочтительно при условии, что один из R8 или R10 означает гидроксил. Алкоксильной группой предпочтительно является метоксильная группа.
В одном из вариантов осуществления R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода, гидроксила, при условии, что один из R8, R9, R10 или R11 означает гидроксил, предпочтительно при условии, что один из R8 или R10 означает гидроксил.
В одном из вариантов осуществления R8 означает водород, гидроксил или алкокси. В одном из вариантов осуществления R8 означает водород. В одном из вариантов осуществления R8 означает гидроксил. В одном из вариантов осуществления R6 и R8 означают водород.
В одном из вариантов осуществления R9 означает водород, гидроксил или алкокси. В одном из частных вариантов осуществления R9 означает водород.
В одном из вариантов осуществления R10 означает водород, гидроксил или алкокси. В одном из вариантов осуществления R10 означает гидроксил.
В одном из вариантов осуществления R11 означает водород, гидроксил или алкокси. В одном из вариантов осуществления R11 означает водород.
В одном из вариантов осуществления R9 и R11 означают водород. В одном из частных вариантов осуществления R8, R9 и R11 означают водород.
В одном из вариантов осуществления R8 и R10 означают гидроксилы.
В одном из вариантов осуществления R8, R9 и R11 означают водород, a R10 означает гидроксил. В одном из вариантов осуществления R9 и R11 означают водород, a R8 и R10 означают гидроксилы.
В одном из вариантов осуществления X- означает анион, полученный из минеральной кислоты, такой как, например, анион бромида, хлорида, боротетрафторида или перхлорида; предпочтительно X- означает хлорид или бромид; более предпочтительно X- означает хлорид.
В одном из вариантов осуществления X- означает анион, полученный из органической кислоты, такой как, например, анион ацетата, бората, цитрата, тартрата, бисульфтата, сульфата или фосфата.
В одном из вариантов осуществления X- означает, анион, полученный из сульфатной или сульфонатной группы.
В одном из вариантов осуществления соединением Формулы I является соединение Формулы I'

в которой R1, R2, R3, R4, R5, R7, R8, R9, R10, R11 и X- имеют значения, оговоренные в Формуле I.
В одном из вариантов осуществления соединением Формулы I является соединение Формулы Ia

в которой R1, R2, R3, R4, R5, R8, R10 и X- имеют оговоренные выше значения.
В одном из вариантов осуществления в Формуле Ia:
R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила и алкокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил;
R8 и R10 каждый независимо означает группу, выбранную из водорода, гидроксила и алкокси, при условии, что один из R8 или R10 означает гидроксил.
В одном из вариантов осуществления соединением Формулы I является соединение Формулы Ib

в которой R1, R2, R3, R4, R8 и X- имеют оговоренные выше значения.
В одном из вариантов осуществления в Формуле Ib:
R1, R2, R3 и R4 каждый независимо означает группу, выбранную из водорода, гидроксила и алкокси, при условии, что один из R1, R2, R3 или R4 означает гидроксил;
R8 означает группу, выбранную из водорода, гидроксила и алкокси.
В одном из вариантов осуществления в Формуле Ib:
R1, R2, R3 и R4 каждый независимо означает группу, выбранную из водорода, гидроксила и метокси, при условии, что один из R1, R2, R3 или R4 означает гидроксил;
R8 означает водород или гидроксил.
В одном из вариантов осуществления соединениями Формулы I являются соединения, приведенные далее в таблице:


В одном из вариантов осуществления соединениями Формулы I являются соединения 1 и 2.
В одном из вариантов осуществления соединением Формулы I является соединение природного происхождения, такое как, например апигенинидин, диосметинидин, трицетинидин или лютеолинидин. Соединения природного происхождения могут быть получены из природных продуктов, в частности, из растений и/или плодов или могут быть путем полного или частичного химического синтеза с использованием природных соединений, таких как, например, соответствующие антоцианины.
В другом варианте осуществления соединением Формулы I является соединение неприродного происхождения. Соединения неприродного происхождения могут быть получены путем полного или частичного химического синтеза.
Соединения Формулы I может быть получено посредством реакций, известных специалистам в данной области техники.
Применение
Изобретение относится к композиции, содержащей соединение Формулы I и физиологически приемлемый носитель. В одном из вариантов осуществления композицией согласно изобретению является фармацевтическая композиция, содержащая соединение Формулы I в сочетании с фармацевтическим приемлемым носителем.
Изобретение относится к лекарству, содержащему соединение Формулы I.
Описанное далее применение относится к применению соединения Формулы I, фармацевтической композиции или лекарства согласно настоящему изобретению.
Изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации глазных болезней. В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации глазных болезней, связанных с накоплением липофусцинов в клетках сетчатки, в частности, для лечения, профилактики и/или стабилизации ВМД или болезни Штаргардта.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации ВМД. В одном из частных вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации промежуточных форм ВМД. Термин "промежуточная форма" означает раннюю стадию ВМД, для которой характерны отложения, называемые друзами, которые лишь минимально влияют на зрение. В одном из частных вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации тяжелых форм ВМД, в частности, сухой формы и/или влажной формы ВМД. В одном из частных вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации сухой ВМД. В одном из частных вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации влажной ВМД.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации болезни Штаргардта.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации пигментной ретинопатии.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для лечения, профилактики и/или стабилизации диабетической ретинопатии.
Изобретение также относится к применению соединений Формулы I для профилактики поражений, которые могут быть вызваны воздействием синего излучения. Термин "синее излучение" означает излучение в синем диапазоне спектра видимого, т.е. с длиной волны от 435 до 490 нм.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для уменьшения гибели клеток ретинального пигментного эпителия (РПЭ).
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для уменьшения или предотвращения накопление липофусцина в клетках РПЭ. В одном из вариантов осуществления липофусцин содержит А2Е и/или изомерные или окисленные формы А2Е.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для стабилизации клеточных мембран РПЭ. В одном из вариантов осуществления клеточными мембранами могут являться плазматические, лизосомальные, ядерные или митохондриальные мембраны.
В одном из вариантов осуществления упомянутые выше применения относятся к соединению или смеси соединений Формулы I.
В одном из вариантов осуществления упомянутые выше применения относятся к одному или нескольким соединениям Формулы I в сочетании с другим действующим веществом. В частности, действующим веществом может являться антиоксидант, такой как, например, цинк или витамины А, С или Е.
Изобретение также относится к способу лечения или профилактики глазной болезни, включающему введение субъекту эффективного количества соединения Формулы I согласно изобретению для достижения положительной динамики и/или профилактики упомянутой глазной болезни. В одном из вариантов осуществления изобретение относится к способу лечения, профилактики и/или стабилизации глазной болезни, связанной с накоплением липофусцинов в клетках сетчатки, более точно, лечения, профилактики и/или стабилизации ВМД или болезни Штаргардта, включающему введение субъекту эффективного количества соединения Формулы I согласно изобретению для достижения положительной динамики и/или профилактики упомянутой глазной болезни.
В одном из вариантов осуществления изобретение относится к способу лечения или профилактики ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
Изобретение также относится к применению соединений Формулы I для получения лекарства для лечения, профилактики и/или стабилизации глазной болезни. В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для получения лекарства для лечения, профилактики и/или стабилизации глазной болезни, связанной с накоплением липофусцинов в клетках сетчатки, более точно, для лечения, профилактики и/или стабилизации ВМД или болезни Штаргардта.
В одном из вариантов осуществления изобретение относится к применению соединений Формулы I для получения лекарства для лечения, профилактики и/или стабилизации ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
В одном из вариантов осуществления субъектом является животное, предпочтительно млекопитающее, более предпочтительно человек.
В одном из вариантов осуществления у пациента диагностирована ВМД, болезнь Штаргардта, пигментная ретинопатия и/или диабетическая ретинопатия. В другом варианте осуществления у субъекта существует опасность развития ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии. В одном из вариантов осуществления субъект имеет генетическую предрасположенность к развитию ВМД, болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
В одном из вариантов осуществления соединения Формулы I согласно изобретению вводятся внутриглазным путем. Термин "внутриглазной путь" означает введение соединения непосредственно внутрь глаза. "Внутрь глаза" включает, в частности, переднюю камеру, заднюю камеру, стекловидное тело, сосудистую оболочку, желтое пятно, сетчатку, кровеносные сосуды и нервы, которые обеспечивают васкуляризацию или иннервацию задней области глаза. В одном из вариантов осуществления соединения Формулы I вводятся внутриглазным путем в задний сегмент глаза. В одном из вариантов осуществления соединения Формулы I вводятся интравитреально. В другом варианте осуществления соединения Формулы I вводятся в субретинальное отделение глаза. В другом варианте осуществления соединения Формулы I вводятся субконъюнктивально.
В одном из вариантов осуществления соединения Формулы I вводятся местно. Могут использоваться капли или ванночки. Также могут применяться методы ионтофореза, известные специалистам в данной области техники, чтобы способствовать местному всасыванию в глаз соединений согласно изобретению.
В одном из вариантов осуществления соединения Формулы I не вводятся перорально.
В одном из вариантов осуществления соединения Формулы I имеют форму, применимую для инъекции. В одном из вариантов осуществления соединения Формулы I имеют форму раствора, такого как, например, стерильный водный раствор, дисперсия, эмульсия, суспензия; или твердую форму, применимую для приготовления раствора или суспензии путем добавления жидкости.
В одном из вариантов осуществления соединения Формулы I имеют форму, которая может обеспечивать замедленное и/или регулируемое высвобождение. В частности, соединения Формулы I могут иметь форму имплантата или саморассасывающейся биоматрицы. Саморассасывающаяся биоматрица может содержать карбомер или полимер. Полимером может являться биоразлагаемая микросфера. В качестве альтернативы, соединения Формулы I могут иметь форму липосом. Может использоваться любой известный специалистам глазной препарат, который позволяет обеспечивать замедленное и/или регулируемое высвобождение действующего вещества.
В одном из вариантов осуществления соединения Формулы I вводятся с частотой не более одного раза в месяц, предпочтительно один раз в 2 месяца, более предпочтительно один раз в 4 месяца, еще более предпочтительно один раз в 6 месяцев.
В одном из вариантов осуществления соединения Формулы I вводятся интравитреально в форме, которая обеспечивает ежесуточное высвобождение дозы от 0,01 мг до 1 мг в каждый глаз, предпочтительно от 0,1 мг до 0,5 мг в каждый глаз.
Краткое описание чертежей
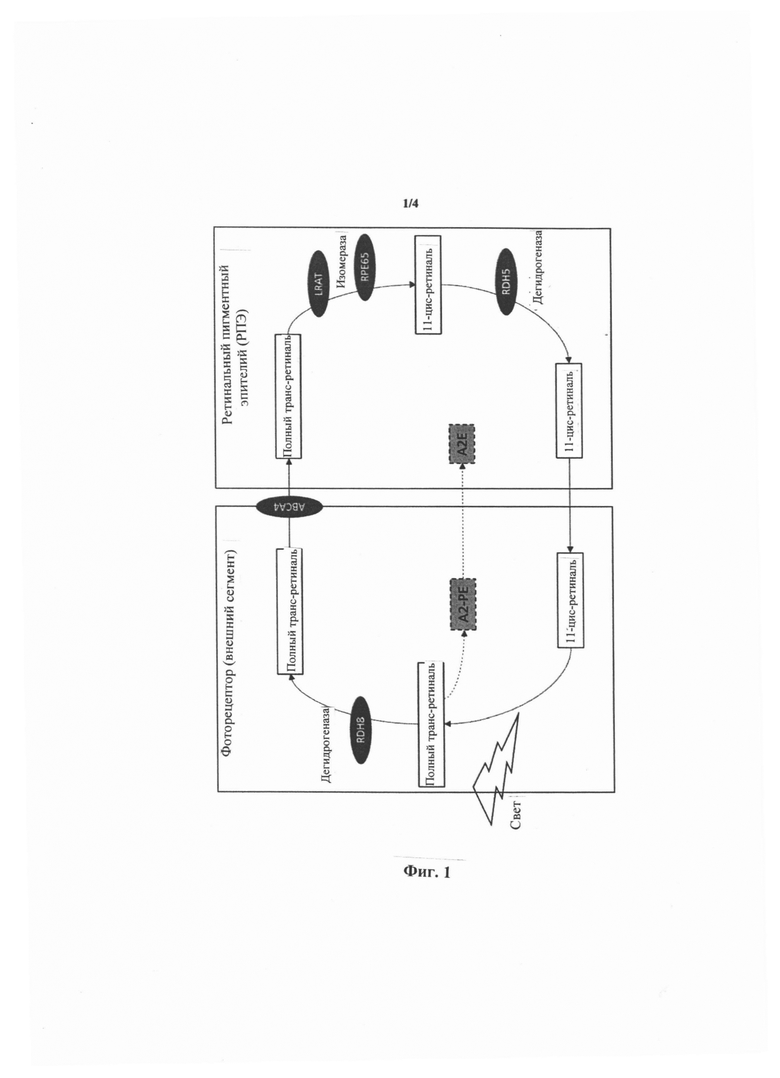
На фиг. 1 показана схема, на которой в обобщенном виде представлены основные стадии цикла превращений родопсина.
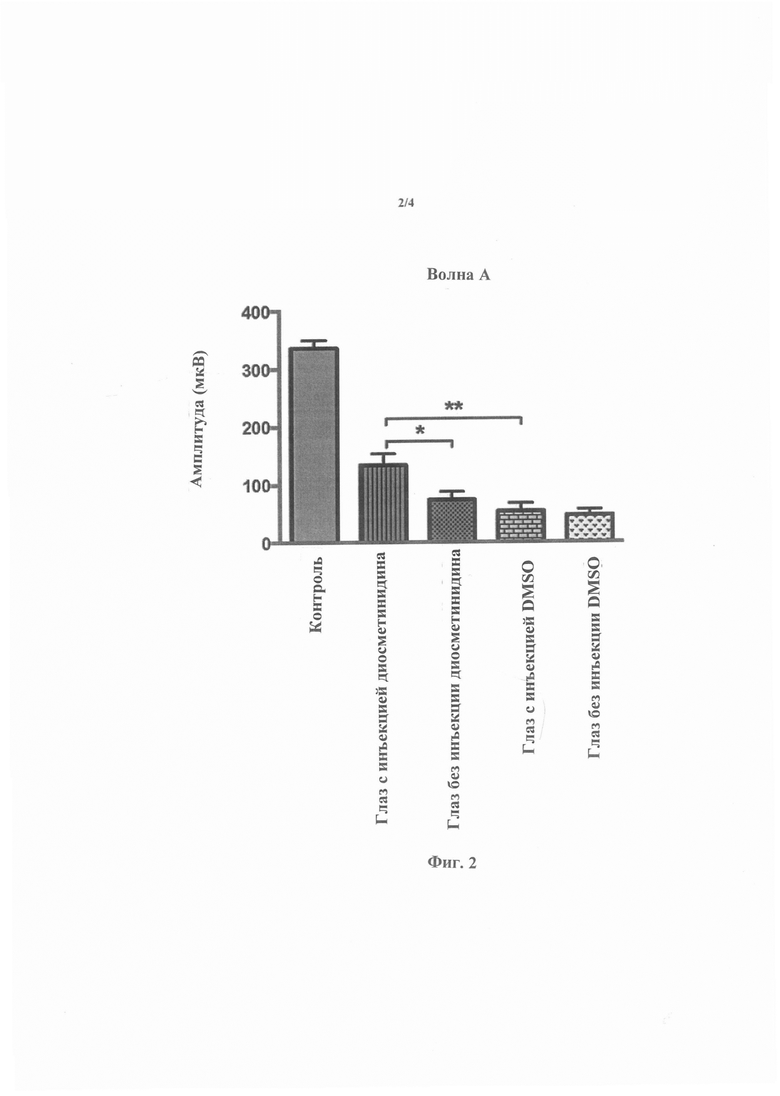
На фиг. 2 и 3 показаны графики, иллюстрирующие электроретинограммы мышей через одну неделю после индуцированной фототоксичности. Волна А (фиг. 2) иллюстрирует электрическую активность фоторецепторов, а волна В (фиг. 3) иллюстрирует электрическую активность клеток внутренней сетчатки. Данные были подвергнуты статистическому анализу дисперсионным методом с последующим применением критерия Даннетта (*р<0,05, **р<0,01, ***р<0,001).
На фиг. 4 показан график, иллюстрирующий число слоев фоторецепторов в зависимости от расстояния до зрительного нерва после интравитреальной инъекции диосметинидина.
Примеры
Настоящее изобретение иллюструруется следующими примерами.
Пример 1. Синтез соединений согласно изобретению
Соединение 1
Растворили 2,4-дигидроксибензальдегид (69 мг) и 2'-гидрокси-4'-метокси-ацетофенон (83 мг - 1 эквивалент) в 500 мкл этанола. Добавили 40 мкл тионилхлорида непосредственно в реакционную среду, которая быстро окрасилась. Через один час перемешивания испарили реакционную среду, осадили остаток в этилацетат, профильтровали и высушили, чтобы получить конечное соединение (77 мг - выход 50%).
Соединение 2
Растворили 2,4-дигидроксибензальдегид (276 мг) и 2',3'-дигидрокси-4'-метокси-ацетофенон (364 мг - 1 эквивалент) в 2 мл этанола и 2 мл этилацетата. Добавили 500 мкл тионилхлорида непосредственно в реакционную среду, которая быстро окрасилась. Через один час перемешивания испарили реакционную среду, осадили остаток в этилацетат, профильтровали и высушили. Растворили твердое вещество в минимальном количестве метанола и осадили путем добавления эквивалентного объема простого метил-трет-бутилового эфира (ТВМЕ). Профильтровали и высушили твердое вещество. Повторяли процедуру до достижения чистоты. Конечный выход составил 60%.
Полученные соединения имели чистоту >95% (по данным ЖХВР), а их подлинность была подтверждена путем МС и ЯМР спектроскопии. Осуществили масс-спектрометрию высокого разрешения на спектрометре LTQ Orbitrap-XL (ThermoFisher Scientific), оснащенном источником NSI (нано-ESI). Осуществили анализ протонных (1Н) ядерных магнитно-резонансных (ЯМР) спектров в DMSO-d6+1% CF3COOD на устройстве Bruker Avance DPX300 (300,16 МГц).
Масс-спектрометр высокого разрешения (Orbitrap)
Соединение 1: m/z 269,0809 (М)+, расчетная величина 269,0808 для С16Н13О4, Δ=0,054 частей на миллион.
Соединение 2: m/z 285.0757 (М)+, расчетная величина 285,0757 для С16Н13О5, Δ=-0,105 частей на миллион.
1Н-ЯМР спектры (δ частей на миллион)

Пример 2. Анализ in vitro фотопротекторной активности
Метод
Использовали клеточную модель фототоксичности, индуцированной взаимосвязью между лечением с помощью А2Е и облучением синим светом, на первичных культурах РПЭ, выживаемость клеток которых была измерена. В этой модели использовались первичные культуры ретинального пигментного эпителия взрослых свиней.
Эта модель позволяет, в частности, проводить отбор молекул с целью обнаружения новых кандидатов для лечения сухой формы ВМД. Эта модель ближе к "физиологической" ситуации, чем линии клеток, обычно описанные в литературе, поскольку используемые клетки содержат защитные вещества, обеспечиваемые рационом животного, и, соответственно, не находятся в ситуации "дефицита", и их нарушение вызвано добавлением А2Е в культуральную среду.
В течение 48 часов обработали клетки, культивированные на 96-луночных планшетах, испытываемыми соединениями (в 5 мМ растворе в DMSO) таким образом, чтобы получить конечные концентрации 5 или 20 мкМ, из них последние 19 часов в присутствии А2Е (конечная концентрация 30 мкМ). Затем в течение 50 минут освещали предварительно обработанные клетки синим светом (470 нм) посредством 96 LED W7113PBC/Н (Kingbright) с углом раствора пучка 16° и силой света 1440 милликандел при токе 8,6 мА. Измерили выживаемость клеток через 24 часа.
Определили выживаемость и гибель клеток через 24 часа после индуцированной фототоксичности по окрашиванию клеток хехстом (ядерным маркером) и этидием (маркером ядер мертвых клеток). Получили изображения каждой лунки с помощью флуоресцентного микроскопа, оснащенного моторизованным приводом под управлением программного обеспечения Metamorph, и с помощью специализированной программы представили выживаемость клеток в количественной форме. Осуществили эксперименты с 96-луночными микропланшетами в четырех экземплярах, и воспроизвели каждый эксперимент, по меньшей мере, четыре раза.
Представили результаты в форме соотношения, отображающего число живых клеток в лунках, обработанных испытываемыми молекулами, деленное на число живых клеток в контрольных лунках (обработанных средой для разбавления без А2Е) и умноженное на 100. Величина у контрольных лунок, обработанных А2Е, но без молекул, составляла 39,7±3,7.
Результаты
Соединения согласно изобретению позволяют достигать очень высоких процентных показателей выживаемости клеток при концентрации 20 мкМ, а также 5 мкМ (Таблица 2).

НД: нет данных
Для сравнения подвергли испытанию 3-гидрокси-антоцианидины (Таблица 3).
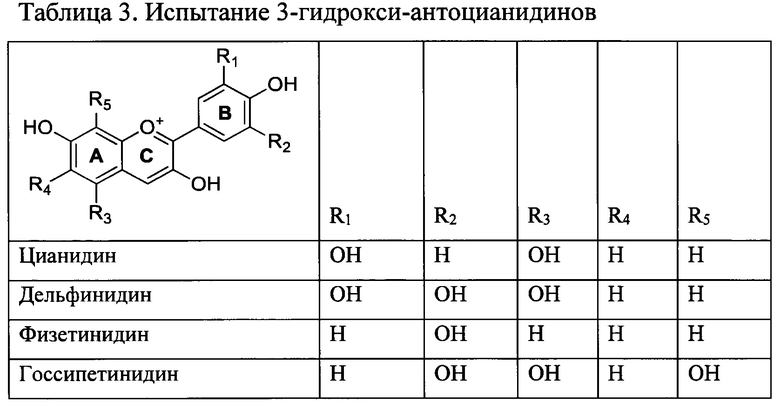

Данные выживаемости клеток в присутствии 3-гидрокси-антоцианидинов представлены в Таблице 4.
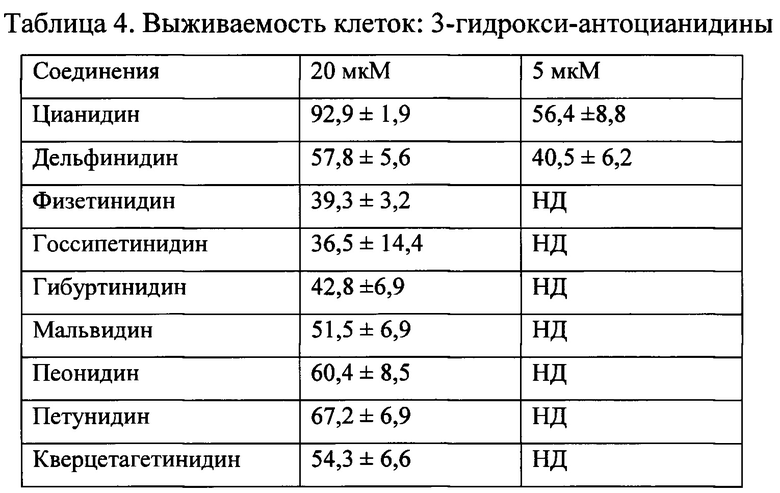
Эти результаты демонстрируют, что эффективность фотопротекции существенно снижается из-за присутствия гидроксильной группы в положении 3 антоцианидинов. Только цианидин обладает существенным фотопротекторным действием при концентрации 20 мкМ. Тем менее, при более низкой концентрации его эффективность снижается в отличие от соединений согласно изобретению.
Для сравнения также подвергли испытанию 3-дезокси-антоцианидины, которые не содержат, по меньшей мере, один свободный гидроксил в цикле А и цикле В (Таблица 5).
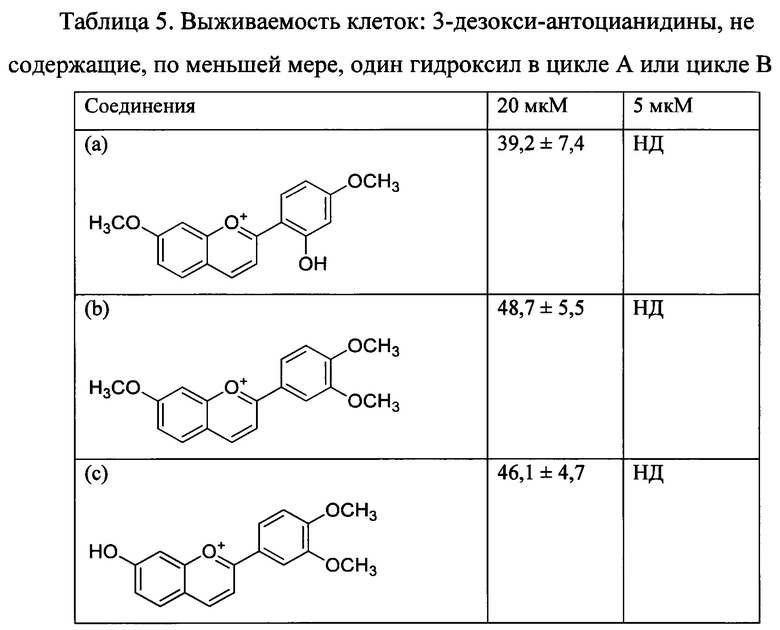
Процент выживаемости клеток при концентрации 20 мкМ составляет менее 50%; соответственно, концентрация 5 мкМ не испытывалась.
Полученные результаты ясно демонстрируют, что при отсутствии, по меньшей мере, одной гидроксильной группы в каждом из циклов А и В эффективность фотопротекции является значительно меньшей, чем у соединений согласно изобретению.
Пример 3. Анализ in vivo фотопротекторной активности у мышей
Использовали модель генетически модифицированных мышей, разработанную Maeda и др. (Invest Ophthalmol. Vis. Sci., 2009, 50, 4917-4925), чтобы испытать фотопротекторную активность соединений согласно изобретению.
В этой модели у мышей инактивированы два гена, участвующих в цикле превращений зрительного пигмента (АВСА4 и Rdh8, смотри фиг. 1), что приводит к раннему накоплению А2Е в глазах. Соответственно, эта животная модель типична для патологии человека.
Использовали мышей в возрасте 7 недель, которым интравитреально ввели диосметинидин (50 мкМ), солюбилизированный в DMSO и разбавленный с помощью PBS (1,2:100) до получения концентрации 100-130 мкМ в стекловидном теле. Ввели контрольным животным DMSO, разбавленный с помощью PBS. После 24 часов нахождения в темноте, подвергли мышей облучению синим светом (4000 люкс, 1 час).
Электроретинограммы, полученные через 7 дней, продемонстрировали защитный эффект диосметинидина, присутствие которого позволило сохранять значительную электрическую активность (фиг. 2 и 3) и хорошую выживаемость фоторецепторов (фиг. 4).


Изобретение относится к применению соединения Формулы I, где R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила, C1-6-алкокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил; R6 означает водород; R7 означает водород; R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода и гидроксила, при условии, что один из R8, R9, R10 или R11 означает гидроксил; X- означает анион, выбранный из: аниона, полученного из минеральной кислоты, такого как, например, анион бромида, хлорида, боротетрафторида или перхлорида; для лечения, профилактики и/или стабилизации возрастной макулодистрофии (ВМД), болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии. Также изобретение относится к новым конкретным производным флавилийхлорида, фармацевтической композиции и лекарственному средству на их основе. Технический результат: выявлены соединения, обладающие фотопротекторной активностью, что полезно при лечении некоторых заболеваний глаза. 4 н. и 5 з.п. ф-лы, 4 ил., 7 табл., 3 пр.

1. Применение соединения Формулы I

в которой
R1, R2, R3, R4 и R5 каждый независимо означает группу, выбранную из водорода, гидроксила, C1-6-алкокси, при условии, что один из R1, R2, R3, R4 или R5 означает гидроксил;
R6 означает водород;
R7 означает водород;
R8, R9, R10 и R11 каждый независимо означает группу, выбранную из водорода и гидроксила, при условии, что один из R8, R9, R10 или R11 означает гидроксил;
X- означает анион, выбранный из: аниона, полученного из минеральной кислоты, такого как, например, анион бромида, хлорида, боротетрафторида или перхлорида;
для лечения, профилактики и/или стабилизации возрастной макулодистрофии (ВМД), болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
2. Применение соединения по п. 1 Формулы Ia

в которой R1, R2, R3, R4, R5, R8, R10 и X- имеют значения, как определено в п. 1.
3. Применение соединения по п. 1, в котором
R8 и R10 каждый независимо означает группу, выбранную из водорода и гидроксила, при условии, что один из R8 или R10 означает гидроксил.
4. Применение соединения по п. 1 Формулы Ib
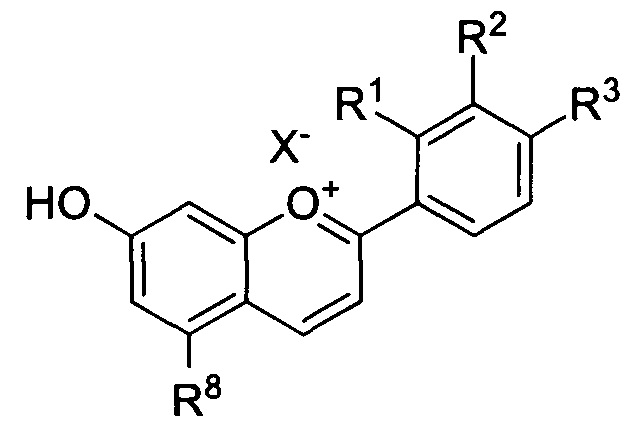
в которой R1, R2, R3, R8 и X- имеют значения, как определено в п. 1.
5. Применение соединения по п. 1, в котором R8 означает атом водорода.
6. Применение соединения по любому из пп. 1-5, выбранного из:
2',7-дигидрокси-4'-метокси-флавилийхлорида;
2',3',7-тригидрокси-4'-метокси-флавилийхлорида;
3',7-дигидрокси-4'-метокси-флавилийхлорида;
4',5,7-тригидрокси-флавилийхлорида;
3',5,7-тригидрокси-4'-метокси-флавилийхлорида;
3',4',5',5,7-пентадрокси-флавилийхлорида;
3',4',5,7-тетрагидрокси-флавилийхлорида.
7. Соединение, выбранное из:
2',7-дигидрокси-4'-метокси-флавилийхлорида;
2',3',7-тригидрокси-4'-метокси-флавилийхлорида.
8. Фармацевтическая композиция, содержащая соединение по п. 7 в сочетании с фармацевтическим приемлемым носителем, для лечения, профилактики и/или стабилизации возрастной макулодистрофии (ВМД), болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
9. Лекарственное средство, содержащее соединение по п. 7, для лечения, профилактики и/или стабилизации возрастной макулодистрофии (ВМД), болезни Штаргардта, пигментной ретинопатии и/или диабетической ретинопатии.
| M | |||
| WOLNIAC, I.WAVER "13C CPMAS NMR and DFT calculations of anthocyanidines", Solid State Nuclear Magnetic Resonance, 2008, 34, pages 44-51 | |||
| RU 97107548 A, 7.05.1999 | |||
| US 20140322371 A1, 30.10.2014 | |||
| JUNJI TANACA ET AL "Purple Rice Extract and Anthocyanidins of the Constituents Protect against Light-induced Retinal Damage in Vitro and in Vivo", |
Авторы
Даты
2020-08-26—Публикация
2016-05-27—Подача