Изобретение относится к области медицины, конкретно к онкологии, и может быть использовано для определения риска развития гематогенного метастазирования у больных немелкоклеточным раком легкого после проведения радикального оперативного лечения.
Рак легкого является одной из часто встречающихся злокачественных опухолей и наиболее распространенной причиной смертности от онкологической патологии в России [1]. Основным гистологическим вариантом рака легкого является немелкоклеточный рак (НМРЛ). Пятилетняя выживаемость больных НМРЛ не превышает 55%, а наиболее частой причиной смерти оперированных больных являются гематогенные метастазы (60-70%). На практике для контроля лечения и выявления прогрессии данного заболевания применяют неспецифичные опухолевые маркеры, которые не эффективны для ранней оценки метастазирования: СЕА - раково-эмбриональный антиген, NSE - нейрон-специфическая энолаза, TPA - тканевой полипептидный антиген [2]. В связи с этим, необходим поиск новых информативных дополнительных маркеров раннего выявления прогрессирования НМРЛ.
Наиболее близким к заявляемому, является способ диагностики и прогноза метастазов при раке легкого на основе определения амплификации гена c-MAF в ткани первичной опухоли, взятой до лечения, который также презентируется как мишень для лечения метастазов (МХ2014014802 (А)). Авторы изобретения определили, что усиление амплификации гена MAF, расположенного в участке длинного плеча 16-ой хромосомы (16q22-24), играет важную роль в появлении метастазов в кости. Уровень экспрессии мРНК данного гена оценивали методом количественного ПЦР в группах пациентов с гематогенными метастазами и без. Было исследовано 74 больных раком легкого, клиническое наблюдение составляло 5 лет. Было показано, что экспрессия мРНК и содержание белка гена c-MAF в опухолевых клетках положительно коррелирует с различными клиническими параметрами, включая рецидив и метастазирование, в частности, метастазирование в кости у больных с раком легких. Также, c-MAF был предложен авторами как мишень для лечения метастазов в кости. Недостатками данного способа являются:
- ограниченная область его применения: прогнозирование и диагностика метастазирования рака легкого осуществляется в отношении только костных метастазов.
- низкая точность предлагаемого метода: нижняя граница доверительного интервала 50%.
- усложнение методики, увеличение времени, трудозатрат и себестоимости анализа, а также необходимость большого количества исходного материала: метод включает обязательную оценку содержания белкового продукта гена c-MAF, т.к. он имеет несколько изоформ.
Новый технический результат - повышение точности, информативности и сокращение времени исследования в способах прогноза метастазирования у больных НМРЛ.
Для достижения нового технического результата в способе прогнозирования риска развития гематогенных метастазов у больных немелкоклеточным раком легкого после операции, путем определения уровня экспрессии генов в ткани опухоли с помощью полимеразной цепной реакции (ПЦР) в режиме реального времени, уровень экспрессии дополнительно определяют в гистологически неизмененной ткани легкого, при этом используют специфичные праймеры к мРНК пяти актин-связывающих белков (АСБ): аденилат циклаза-ассоциированного протеина 1, кофилина 1, профилина 1, фасцина 1 и эзрина, проводят сравнительный анализа уровня экспрессии мРНК, кодирующих гены пяти перечисленных актин-связывающих белков в опухолевой ткани относительно гистологически неизмененной ткани легкого, увеличение уровня экспрессии мРНК каждого АСБ в опухолевой ткани по сравнению с неизмененной оценивают в 1 балл и при сумме баллов от 3 до 5 прогнозируют повышенный риск развития гематогенных метастазов у паципента.
Способ осуществляют следующим образом.
Во время радикальной операции от пациента НМРЛ получают образцы ткани первичной опухоли и прилегающей гистологически неизмененной («условно-нормальной») ткани легкого, взятой на расстоянии не менее 1 см от границы опухоли. Образцы тканей замораживают в растворе RNAlater и хранят при -80°С.
Выделяют РНК из образцов. При этом RIN выделенных образцов должен быть больше или равен 4, а концентрация РНК не менее 80 нг/мкл.
Проводят синтез кДНК на матрице РНК с использованием случайных гексаолигонуклеотидов. Условия реакции: реакция проводится в течение 30 мин при 42°С, затем проводят инактивацию обратной транскриптазы при 95°С в течение 2 мин.
Проводят полимеразную цепную реакцию в режиме реального времени (RT-PCR) с использованием специфичных праймеров к мРНК пяти актин-связывающих белков (АСБ) (аденилат циклаза-ассоциированный протеин 1 (САР1), кофилин 1, профилин 1, фасцин 1, эзрин) (таблица 1). Протокол реакции ПЦР: предварительный прогрев при 95°С - 6 мин, 40 основных циклов: денатурация при 95°С - 10 сек, отжиг и элонгация: 52°С - 35 сек. В качестве референсного гена используют GAPDH (glyceraldehyde 3-phosphate dehydrogenase) (таблица 1).
Сравнивают количество амплифицированных фрагментов (мРНК) 5 АСБ в ткани первичной опухоли с количеством соответствующих амплифицированных фрагментов (мРНК) пяти АСБ в гистологически неизмененной ткани легкого. Уровень экспрессии мРНК рассчитывают по методу 2-ΔΔCt. При увеличении уровня экспрессии мРНК каждого АСБ в опухолевой ткани по сравнению с неизмененной пациенту присваевается 1 балл. При присвоении пациенту в 3, 4 или 5 баллов прогнозируют повышенный риск развития гематогенных метастазов. В частности, при увеличении в опухолевой ткани относительно неизмененной уровня экспрессии мРНК трех из пяти АСБ прогнозируют увеличение риска развития гематогенных метастазов в 2,4 раза; при увеличении четырех из пяти АСБ
- в 4,8 раз; при увеличении пяти АСБ - в 7,2 раза.
Предлагаемый подход к оценке прогноза в отношении риска возникновения гематогенных метастазов при НМРЛ обусловлен рядом предпосылок.
На развитие и прогрессирование НМРЛ, помимо клинико-морфологических параметров заболевания, влияют индивидуальные молекулярно-генетические характеристики опухоли. Значимыми процессами, происходящими на клеточном уровне и определяющими метастатический потенциал опухолевых клеток, являются нарушение адгезивных свойств и приобретение способности к активному перемещению в экстраклеточном матриксе, важную роль в которых играет реорганизация актинового цитоскелета. Эти процессы опосредуются функционированием различных белков, в том числе АСБ, в связи с чем, изучение уровня экспрессии генов АСБ является актуальным. Семейство актин-связывающих белков насчитывает около 100 представителей, и список этот продолжает пополняться. АСБ группируют в соответствии с функциями, которые они выполняют в отношении актина. Выделяют группу актин-деполимеризующих белков, представителями которой являются аденилат циклаза-ассоциированный протеин 1 (САР1) и кофилин. Эти белки могут работать как в паре, так и самостоятельно [3]. К группе мономер-связывающих белков относится профилин, который обеспечивает рециркуляцию G-актина при ремоделировании цитоскелета [4]. Фасцин - представитель группы поперечносвязывающих белков, которые облегчают формирование пучков и ветвление нитей актина [5]. Эзрин относится к белкам, обеспечивающим прикрепление актина к клеточной мембране [6]. Поэтому изучение роли функционально разных АСБ в патологических процессах представляет собой важную задачу в понимании процессов, связанных с ремоделированием актинового цитоскелета, в частности - метастазирования и инвазии опухолевых клеток.
Работы, связанные с изучением вовлеченности САР1 в опухолевую прогрессию, ведутся достаточно недавно и за последние 10 лет было показано участие САР1 в патогенезе рака нескольких локализаций. Так, на клеточных линиях неинвазивного (95-С) и инвазивного (95-D) рака легкого, было показано, что значение белка САР1 возрастает в ткани немелкоклеточного рака легкого по сравнению с неизмененной тканью, а экспрессия САР1 в ткани метастазирующих опухолей значительно превышает таковую в ткани неметастазирующих опухолей. В этой же работе отмечена взаимосвязь экспрессии белка САР1 со стадией аденокарциномы легкого [7]. Позже другими исследователями на тканях немелкоклеточного рака легкого была построена модель с использованием САР1 для предсказания появления метастазов в головном мозге с чувствительностью и специфичностью 79.5 и 67.1%, соответственно. Авторы предположили, что САР1 включен в патогенез возникновения метастазов в головной мозг, и что высокие уровни экспрессии этого белка могут предсказывать неблагоприятный прогноз для пациентов с немелкоклеточным раком легкого [8]. Повышение экспрессии САР1 в опухоли и сыворотке крови и его достоверная корреляция с наличием лимфогенных метастазов отмечена и в опухолях других локализаций: при раке поджелудочной железы, молочной железы, плоскоклеточном раке пищевода, плоскоклеточном раке области головы и шеи [9-12]. САР1 может участвовать в деполимеризации актина как самостоятельно, так и совместно с другим актин-связывающим белком - кофилином [3]. Локальная активация кофилина инициирует формирование ламеллоподий и активирует клеточную миграцию [13]. Кофилин является одним из ключевых факторов в регуляции клеточного цикла и играет важную роль в патогенезе опухолей. Чрезмерная экспрессия кофилина была обнаружена при раке разных локализаций [14-16]. Роль в канцерогенезе профилина до сих пор не определена. Показано, что высокий уровень профилина может быть связан как с ингибированием роста и метастазирования при раке поджелудочной железы и печени [17; 18], так и с опухолевой прогрессией при почечно-клеточной карциноме и плоскоклеточном раке гортани [19; 20]. Эзрин способствует метастазированию опухоли, однако молекулярные механизмы этого до сих пор до конца не изучены. Так, в ткани рака языка повышается экспрессия данного белка, и в связи с этим, может быть терапевтической мишенью при плоскоклеточных карциномах языка [21]. На клеточных культурах рака прямой кишки показано участие эзрина в сигнальных каскадах [22; 23]. Фасцин способствуют нарушению межклеточных контактов и способствует выходу опухолевых клеток во внеклеточный матрикс [5]. Повышенный уровень фасцина зарегистрирован в опухолях легких [24], желудка [25], яичников [26]. Повышенный уровень фасцина в ткани рака молочной железы рассматривается как возможный диагностический маркер трипл-негативного рака [27]. В эксперименте на мышах показано, что, ингибируя физиологическую функцию фасцина, можно снизить миграцию опухолевых клеток и метастазирование [28]. Информативность отобранных АСБ также подтверждена наличием значимых различий экспрессии их мРНК в ткани плоскоклеточного рака головы и шеи по сравнению с диспластически измененным эпителием гортани и гортаноглотки и в ткани первичной опухоли при лимфогенном метастазировании [29].
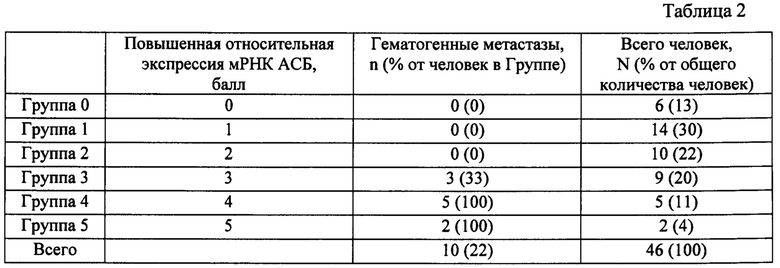
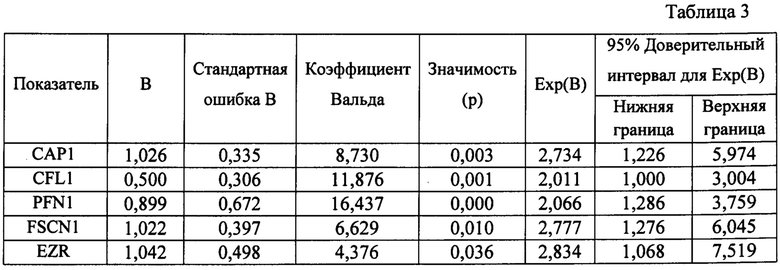
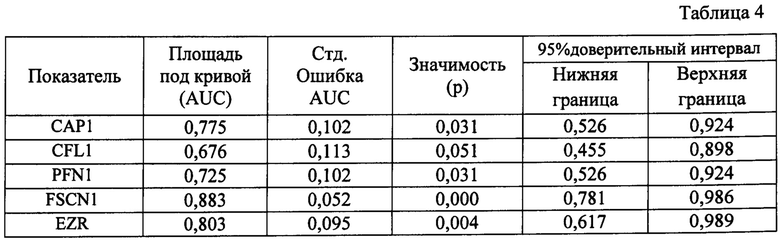
Способ основан на анализе данных клинических исследований. Определяли значимости показателей экспрессии мРНК АСБ (САР1, кофилина 1, профилина 1, фасцина 1 и эзрина) для оценки прогноза риска метастазирования больных НМРЛ в 2х-летней безметастатической выживаемости. Общее количество пациентов, включенных в анализ, составило 46 человек. Пациенты были разделены на 6 групп в зависимости от присвоенных баллов (таблица 2). Т.е. у нулевой группы экспрессия мРНК АСБ в опухоли была ниже или такая же как в нормальной ткани, у первой группы увеличивалась экспрессия мРНК одного из пяти изучаемых АСБ, им присваивался 1 балл, у второй группы - 2, и т.д. до пяти баллов. Прогностическая значимость признаков в отношении 2-летней безметастатической выживаемости оценена с использованием регрессионной модели Кокса (таблица 3) и ROC-анализа (таблица 4). В группах 0,1 и 2 наблюдалась 100%-ная выживаемость. При увеличении мРНК трех из пяти белков метастазы развивались в трети случаев, а при увеличении мРНК четырех и пяти белков метастазы развивались в 100% случаев. Чувствительность метода составляет 67%, специфичность - 96%, значимость - 84,5%.
Способ иллюстрируется следующими примерами:
Клинический пример 1. Больной Т., 60 лет. Центральный рак средне-нижнедолевого бронха левого легкого. Стадия IIA, T2N0M0. Гистология Умереннодифференцированный неороговевающий плоскоклеточный рак. Выполнена операция - Левосторонняя нижняя билобэктомия, медиастинальная лимфодиссекция D3.
Было выполнено исследование согласно предлагаемому способу, по результатам молекулярно-генетического исследования в ткани первичной опухоли выявлено увеличение уровня экспрессии мРНК профилина и эзрина - 2 балла. Прогноз - отсутствие метастазирования.
Адъювантная терапия не проводилась в связи ранней стадией опухолевого процесса, низкими функциональными резервами пациента. При динамическом наблюдении за больным в течение 40 месяцев признаков прогрессирования заболевания не найдено.
Клинический пример 2. Больной М., 63 года. Периферический рак верхней доли правого легкого. Стадия IB, T2N0M0. Гистология - Низкодифференцированный неороговевающий плоскоклеточный рак. Выполнена Верхняя лобэктомия справа.
Было выполнено исследование согласно предлагаемому способу: при молекулярно-генетическом исследовании выявлено повышение уровня относительной экспрессии мРНК кофилина, фасцина и эзрина в опухолевой ткани - 3 балла. Прогноз -повышенный риск развития метастазов.
В послеоперационном периоде проведено 4 курса химиотерапии гемцитабин/цисплатин. При контрольном обследовании через 33 месяца - прогрессирование: метастатическое поражение левого легкого.
Клинический пример 3. Больной К., 58 лет. Центральный рак нижнедолевого бронха левого легкого с переходом на главный бронх. Стадия IIIA, T3N2M0. Гистология - умереннодифференцированный неороговевающий плоскоклеточный рак с метастазами в 6 медиастинальных лимфоузлов. Выполнена операция - Расширенно-комбинированная левосторонняя пневмонэктомия с интраперикардиальной обработкой сосудов, резекцией перикарда, адвентиции пищевода, медиастинальной лимфодиссекцией D3.
Было выполнено исследование согласно предлагаемому способу. По результатам молекулярно-генетического исследования выявлено увеличение уровня экспрессии САР1, кофилина, фасцина и эзрина в опухолевой ткани по сравнению с неизмененной - 4 балла. Прогноз - высокий риск метастазирования.
Проведено 5 курсов адъювантной химиотерапии по схеме Цисплатин/Этопозод. При динамическом наблюдении за больным, спустя 21 месяц после операции на контрольном обследовании выявлено метастатическое поражение печени, забрюшинных лимфатических узлов, обоих надпочечников.
Предлагаемый способ позволяет повысить точность, информативность прогнозирования риска метастазирования, сократить время исследования и использовать его результаты для обоснования тактики ведения пациентов.
Источники информации, принятые во внимание при составлении описания:
1. Злокачественные новообразования в России в 2016 году (заболеваемость и смертность) / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИРЦ» Минздрава Россию. - 2018. - 250 с.
2. Wang R., Wang G., Zhang N. et al. Clinical evaluation and cost-effectiveness analysis of serum tumor markers in lung cancer // Biomed. Res. Int. - 2013. - Vol.2013. - P. 195692.
3. Zhou G.L., Zhang H., Wu H. et al. Phosphorylation of the cytoskeletal protein CAP1 controls its association with cofilin and actin // J. Cell Sci. - 2014. - Vol.127(23). - P. 5052-5065.
4. Gunning P.W., Ghoshdastider U., Whitaker S. et al. The evolution of compositionally and functionally distinct actin filaments // J. Cell Sci. - 2015. - Vol.128(11). - P. 2009-2019.
5. Karasavvidou F., Barbanis S., Pappa D. et al. Fascin determination in urothelial carcinomas of the urinary bladder: a marker of invasiveness // Arch. Pathol. Lab. Med. - 2008. - Vol.132(12). - P. 1912-1915.
6. Коржевский Д.Э., Карпенко M.H., Кирик O.B. Белки, ассоциированные с микротрубочками, как показатели дифференцировки и функционального состояния нервных клеток // Морфология. - 2011. - Т. 139, №1. - С. 13-21.
7. Tan М., Song X., Zhang G. et al. Overexpression of adenylate cyclase-associated protein 1 is associated with metastasis of lung cancer // Oncol. Rep. - 2013. - Vol. 30(4). - P. 1639-1644.
8. Xie S.S., Tan M., Lin H.Y. et al. Overexpression of adenylate cyclase-associated protein 1 may predict brain metastasis in non-small cell lung cancer // Oncol. Rep. - 2015. - Vol. 33(1). - P. 363-371.
9. Какурина Г.В., Кондакова И.В., Чойнзонов Е.Л. и др. Особенности протеома сыворотки крови больных плоскоклеточными карциномами головы и шеи // Сибирский онкологический журнал. - 2013. - №2. - С. 62-66.
10. Yamazaki К., Takamura М., Masugi Y. et al. Adenylate cyclase-associated protein 1 overexpressed in pancreatic cancers is involved in cancer cell motility // Lab. Invest. - 2009. - Vol. 89. - P. 425-432.
11. Liu X., Yao N., Qian J. et al. High expression and prognostic role of CAP1 and CtBP2 in breast carcinoma: associated with E-cadherin and cell proliferation // Med. Oncol. - 2014. - Vol. 31(3). - P. 878.
12. Li M., Yang X., Shi H. et al. Downregulated expression of the cyclase-associated protein 1 (CAP1) reduces migration in esophageal squamous cell carcinoma // Jpn. J. Clin. Oncol. - 2013. - Vol. 43(9). - P. 856-864.
13. Zhang H., Ghai P., Wu H. et al. Mammalian adenylyl cyclase-associated protein 1 (CAP1) regulates cofilin function, the actin cytoskeleton, and cell adhesion // J. of Boil. Chemistry. - 2013. - Vol. 288(29). - P. 20966-20977.
14. Wang F., Wu D., Fu H. et al. Cofilin 1 promotes bladder cancer and is regulated by TCF7L2 // Oncotarget. - 2017. - Vol. 8(54). - P. 92043-92054.
15. Satoh M., Takano S., Sogawa K. et al. Immune-complex level of cofilin-1 in sera is associated with cancer progression and poor prognosis in pancreatic cancer // Cancer Sci. -2017. - Vol.108(4). - P. 795-803.
16. Su J., Zhou Y., Pan Z. et al. Downregulation of LIMK1-ADF/cofilin by DADS inhibits the migration and invasion of colon cancer // Sci Rep.- 2017. - Vol. 7. - P. 45624.
17. Shen K., Xi Z., Xie J. et al. Guttiferone K suppresses cell motility and metastasis of hepatocellular carcinoma by restoring aberrantly reduced profilin 1 // Oncotarget. - 2016. - Vol. 7(35). - P. 56650-56663.
18. Schoppmeyer R., Zhao R., Cheng H. et al. Human profilin 1 is a negative regulator of CTL mediated cell-killing and migration // Eur. J. Immunol. - 2017. - Vol. 47(9). - P. 1562-1572.
19. Karamchandani J.R., Gabril M.Y., Ibrahim R. et al. Profilin-1 expression is associated with high grade and stage and decreased disease-free survival in renal cell carcinoma // Hum. Pathol. - 2015. - Vol.46(5). - P. 673-680.
20. Li L., Zhang Z., Wang C. et al. Quantitative proteomics approach to screening of potential diagnostic and therapeutic targets for laryngeal carcinoma // PLoS One. - 2014. - Vol. 9(2). - P. e90181.
21. Saito S., Yamamoto H., Mukaisho K. et al. Mechanisms underlying cancer progression caused by ezrin overexpression in tongue squamous cell carcinoma // PLoS One. - 2013. -Vol. 8(1). - P. e54881.
22. Iessi E., Zischler L., Etringer A. et al. Death receptor-induced apoptosis signalling regulation by ezrin is cell type dependent and occurs in a DISC-independent manner in colon cancer cells // PLoS One. - 2015. - Vol. 10(5). - P. e0126526.
23. Haase G., Gavert N., Brabletz T. et al. The WNT target gene 11 in colon cancer invasion and metastasis // Cancers (Basel). - 2016. - Vol. 8(5). - P. E48.
24. Zhao W., Gao J., Wu J. et al. Expression of Fascin-1 on human lung cancer and paracarcinoma tissue and its relation to clinicopathological characteristics in patients with lung cancer // Onco Targets Ther. - 2015. - Vol.8. - P. 2571-2576.
25. Hashimoto Y., Shimada Y., Kawamura J. et al. The prognostic relevance of fascin expression in human gastric carcinoma // Oncology. - 2004. - Vol. 67(3-4). - P. 262-270.
26. El-Balat A., Arsenic R.,  N. et al. Fascin-1 expression as stratification marker in borderline epithelial tumours of the ovary // J. Clin. Pathol. - 2016. - Vol. 69(2). - P. 142-148.
N. et al. Fascin-1 expression as stratification marker in borderline epithelial tumours of the ovary // J. Clin. Pathol. - 2016. - Vol. 69(2). - P. 142-148.
27. Wang C.Q., Tang C.H., Chang H.T. et al. Fascin-1 as a novel diagnostic marker of triple-negative breast cancer // Cancer Med. - 2016. - Vol. 5(8). - P. 1983-1988.
28. Han S., Huang J., Liu B. et al. Improving fascin inhibitors to block tumor cell migration and metastasis // Mol. Oncol. - 2016. - Vol. 10(7). - P. 966-980.
29. Какурина Г.В. Кондакова И.В., Спирина Л.В. и др. Экспрессия генов, кодирующих белки клеточной подвижности, в развитии плоскоклеточного рака головы и шеи // Бюллетень экспериментальной биологии и медицины. - 2018. - Т. 166, №8. - С. 209-212.
Приложение
Таблица 1 - Последовательность праймеров, используемых в полимеразной цепной реакции
Примечание - F (от англ. forward) - прямой праймер, R (от англ. reverse) - обратный праймер; САР - аденилат циклаза-ассоциированный протеин; CFL - кофилин; PFN - профилин; FSCN - фасцин; EZR - эзрин; GAPDH- глицеральдегид-3-фосфат-дегидрогеназа.
Таблица 2 - Распределение больных немелкоклеточным раком легкого в зависимости от увеличения относительной экспрессии мРНК актин-связывающих белков в опухолевой ткани.
Таблица 3 - Значимость относительной экспрессии мРНК актин-связывающих белков в опухолевой ткани в регрессионной модели Кокса
Примечание - САР - аденилат циклаза-ассоциированный протеин; CFL - кофилин; PFN -профилин; FSCN - фасцин; EZR - эзрин.
Таблица 4 - Значимость относительной экспрессии мРНК актин-связывающих белков в опухолевой ткани в регрессионной модели Кокса
Примечание - САР - аденилат циклаза-ассоциированный протеин; CFL - кофилин; PFN -профилин; FSCN - фасцин; EZR - эзрин.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПРОГРЕССИИ В ОТДАЛЕННОМ ПЕРИОДЕ У БОЛЬНЫХ ПЛОСКОКЛЕТОЧНЫМ РАКОМ ГОЛОВЫ И ШЕИ | 2021 |
|
RU2765013C1 |
| Способ прогнозирования риска развития отдаленных метастазов у больных операбельными формами рака молочной железы с метастазами в регионарные лимфоузлы | 2020 |
|
RU2733697C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РИСКА НЕБЛАГОПРИЯТНОГО ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ РАКОМ ЖЕЛУДКА | 2016 |
|
RU2662085C1 |
| Способ прогнозирования пятилетней безметастатической выживаемости у больных раком молочной железы на основе экспрессии генов белков YKL-39 и CCL18 | 2017 |
|
RU2659676C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ГЕМАТОГЕННЫХ МЕТАСТАЗОВ ПРИ ПЛОСКОКЛЕТОЧНОМ РАКЕ ЛЕГКОГО | 2012 |
|
RU2489718C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ ЛЮМИНАЛЬНЫМ В И ТРИЖДЫ НЕГАТИВНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ У ПАЦИЕНТОК, НЕ ПОЛУЧАВШИХ В НЕОАДЪЮВАНТНОМ РЕЖИМЕ ХИМИО- ИЛИ ГОРМОНОТЕРАПИЮ | 2017 |
|
RU2648523C1 |
| Способ прогнозирования безрецидивной выживаемости у больных раком молочной железы | 2016 |
|
RU2623869C1 |
| Способ прогнозирования степени риска развития гематогенных метастазов при инвазивной карциноме неспецифического типа молочной железы на основе оценки экспрессии белка LIMCH1 | 2020 |
|
RU2755242C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ГЕМАТОГЕННЫХ МЕТАСТАЗОВ ПОСЛЕ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ РАКА ПОЧКИ | 2013 |
|
RU2528100C1 |
| Способ прогнозирования риска лимфогенного метастазирования при раке молочной железы на основе экспрессии гена белка YKL-39 | 2016 |
|
RU2632115C1 |
Изобретение относится к области медицины, конкретно к онкологии и может быть использовано для определения риска развития гематогенного метастазирования у больных немелкоклеточным раком легкого (НМРЛ) после проведения радикального оперативного лечения. Способ включает определение уровня экспрессии генов в ткани опухоли и гистологически не изменной ткани легкого с использованием специфичных праймеров к мРНК пяти актин-связывающих белков (АСБ): аденилат циклаза-ассоциированного протеина 1, кофилина 1, профилина 1,фасцина 1 и эзрина, затем проводят сравнительный анализа уровня экспрессии мРНК, кодирующих гены пяти перечисленных актин-связывающих белков в опухолевой ткани относительно гистологически неизмененной ткани легкого, при этом увеличение уровня экспрессии мРНК каждого АСБ в опухолевой ткани по сравнению с неизмененной пациента оценивают в 1 балл и при сумме баллов от 3 до 5 прогнозируют повышенный риск развития гематогенных метастазов. Использование изобретения позволяет повысить точность, информативность прогнозирования риска метастазирования, сократить время исследования. 4 табл., 3 пр.
Способ прогнозирования риска развития гематогенных метастазов у больных немелкоклеточным раком легкого после операции путем определения уровня экспрессии генов в ткани опухоли с помощью полимеразной цепной реакции (ПЦР) в режиме реального времени, отличающийся тем, что уровень экспрессии дополнительно определяют в гистологически неизмененной ткани легкого, при этом используют специфичные праймеры к мРНК пяти актин-связывающих белков (АСБ): аденилат циклаза-ассоциированного протеина 1, кофилина 1, профилина 1, фасцина 1 и эзрина, проводят сравнительный анализа уровня экспрессии мРНК, кодирующих гены пяти перечисленных актин-связывающих белков в опухолевой ткани относительно гистологически неизмененной ткани легкого, увеличение уровня экспрессии мРНК каждого АСБ в опухолевой ткани по сравнению с неизмененной оценивают в 1 балл и при сумме баллов от 3 до 5 прогнозируют повышенный риск развития гематогенных метастазов у пациента.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ГЕМАТОГЕННЫХ МЕТАСТАЗОВ ПРИ ПЛОСКОКЛЕТОЧНОМ РАКЕ ЛЕГКОГО | 2012 |
|
RU2489718C1 |
| Способ мониторинга эффективности противоопухолевой терапии немелкоклеточного рака легкого | 2015 |
|
RU2611340C2 |
| СПОСОБ ОЦЕНКИ РИСКА ПРОГРЕССИРОВАНИЯ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО ПОСЛЕ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ | 2011 |
|
RU2472161C1 |
| ПОНОМАРЕВА А.А | |||
| и др | |||
| Сравнительный анализ эпигенетических и белковых маркеров в крови больных немелкоклеточным раком легкого // Сибирский онкологический журнал | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| С | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| WANG R | |||
| et al | |||
| Clinical evaluation and cost-effectiveness analysis of serum | |||
Авторы
Даты
2020-09-29—Публикация
2019-04-09—Подача