Изобретение относится к химии высокомолекулярных соединений, конкретно к способу получения люминесцирующих биосовместимых регулярно привитых полифлуореновых молекулярных щеток с высокой степенью прививки с использованием метода «прививки через» для поликонденсации.
Изобретение может быть использовано в биотехнологии и медицинской диагностике.
Уровень техники
В последние десятилетия в полимерной химии активно развивается направление, связанное с синтезом и исследованием свойств разветвленных полимерных систем, как правило, из привитых сополимеров, с достаточно хорошо определяемой структурой, так называемых «молекулярных щеток» («molecular brushes»). Молекулярные щетки состоят из «хребта» (основной полимерной цепи) и ковалентно присоединенных к нему боковых полимерных цепей. Молекулярные щетки способны к формированию различных пространственно-регулярных наноструктур и, благодаря особой топологии и химической функциональности, обладают уникальными свойствами. Понятие «молекулярные щетки» входит в более широкое понятие «полимерные щетки» («polymer brushes»). В полимерных щетках прививка закрепляется, как правило, на жесткой полимерной поверхности, частный случай - на основной полимерной цепи (полимерном «хребте»).
Молекулярные щетки благодаря своей уникальной макромолекулярной архитектуре являются перспективным объектом для разработки новых материалов. Компактная архитектура молекулярных щеток, в которых основная цепь принимает вытянутую конформацию из-за стерического отталкивания боковых цепей, в совокупности с возможностью управлять природой, молекулярными параметрами основной и боковых цепей, т.е. управлять размерами и формой макромолекул, открывает обширные возможности применения этих объектов в биотехнологии, например, в области направленной доставки лекарств, диагностики и исследования процессов, протекающих в клетках. Следует подчеркнуть, что необходимым условием для этого является также наличие таких важных свойств, как биосовместимость и способность к люминесценции [С.Yang, Н. Liu, Y. Zhang, Zh. Xu, X. Wang, В. Cao, M. Wang. Hydrophobic-Sheath Segregated Macromolecular Fluorophores: Colloidal Nanoparticles of Polycaprolactone-Grafted Conjugated Polymers with Bright Far-Red/Near-Infrared Emission for Biological Imaging // Biomacromolecules. 2016. №17. P. 1673-1683].
Известны попытки получения нетоксичных молекулярных щеток - привитых сополимеров на основе полиэфиров с боковыми цепями полиалкилоксазолинов [М. П. Курлыкин, А. Э. Бурсиана, О. В. Голуб, А. П. Филиппов, А. В. Теньковцев. Мультицентровые полиэфирные инициаторы для получения привитых сополимеров с олиго(2-этил-2-оксазолиновыми) боковыми цепями // Высокомолекулярные соединения. Серия Б. 2016. том 58. №4. С. 306-313] и на основе виниловых полимеров с аналогичными боковыми цепями [N. Zhang, R. Luxenhofer, R. Jordan Thermoresponsive Poly(2-oxazoline) Molecular Brushes by Living Ionic Polymerization: Kinetic Investigations of Pendant Chain Grafting and Cloud Point Modulation by Backbone and Side Chain Length Variation // Macromol. Chem. Phys. 2012. V. 213. P. 973-981]. Основным недостатком известных полимерных систем с точки зрения практического применения является отсутствие люминесценции, что затрудняет их идентификацию при различных био-медицинских приложениях.
Известны люминесцирующие молекулярные щетки на основе сополимера флуорена с боковыми цепями поли(ε-капролактона) [С.Yang, Н. Liu, Y. Zhang, Zh. Xu, X. Wang, В. Cao, M. Wang. Hydrophobic-Sheath Segregated Macromolecular Fluorophores: Colloidal Nanoparticles of Polycaprolactone-Grafted Conjugated Polymers with Bright Far-Red/Near-Infrared Emission for Biological Imaging // Biomacromolecules. 2016. №17. P. 1673-1683] и поли(ε-капролактон)-блок-поли(олигоэтиленгликольметакрилата) [С.Yang, S. Huang, X. Wang, M. Wang. Theranostic Unimolecular Micelles of Highly Fluorescent Conjugated Polymer Bottlebrushes for Far Red/Near Infrared Bioimaging and Efficient Anticancer Drug Delivery // Polymer Chemistry. 2016. №3. P. 1-15], которые флуоресцируют красным светом. Известные сополимеры были использованы для формирования наноконтейнеров для доставки гидрофобных агентов фотодинамической терапии. С этой же целью в работе [Н. Zhao, W. Ни, Н. Ma, R. Jiang, Y. Tang, Y. Ji, X. Lu, В. Hou, W. Deng, W. Huang, Q. Fan. Photo-Induced Charge-Variable Conjugated Polyelectrolyte Brushes Encapsulating Upconversion Nanoparticles for Promoted siRNA Release and Collaborative Photodynamic Therapy under NIR Light Irradiation // Adv. Funct. Mater. 2017. V.27. P. 1-14] были получены молекулярные щетки с боковыми цепями поли(2-(диметиламино)-этилметакрилата) и поли(изопропилакриламида). Для синтеза молекулярных щеток использовался наиболее распространенный метод полимеризации - «прививка от». Согласно методу сначала получают основную цепь - мультицентровый макроинициатор, затем прививают на него боковые цепи путем полимеризации. Плотность прививки в известных молекулярных щетках имеет объективные, обусловленные природой процесса ограничения, прежде всего, стерические затруднения, и не превышает 50%, ее трудно контролировать. Существенным недостатком перечисленных известных молекулярных щеток также является высокая токсичность для организма.
Проблемы контроля регулярности и плотности прививки в молекулярных щетках, то есть качества щеток, при использовании метода «прививка от» в настоящее время не решены, актуальной остается и проблема создания биосовместимых и в то же время люминесцирующих молекулярных щеток, т.к. это препятствует дальнейшему использованию молекулярных щеток в медицине.
Раскрытие изобретения
Задачей заявляемого изобретения является создание технологии получения люминесцирующих нетоксичных регулярно привитых полифлуореновых молекулярных щеток с высокой контролируемой степенью прививки.
Эта задача решается заявляемым изобретением - способом получения люминесцирующих регулярно привитых полифлуореновых молекулярных щеток с боковыми цепями водорастворимых термочувствительных биосовместимьгх полимеров.
Заявляемый способ характеризуется следующей совокупностью существенных признаков:
Способ получения люминесцирующих регулярно привитых полифлуореновых молекулярных щеток с боковыми цепями водорастворимых термочувствительных биосовместимых полимеров путем использования метода «прививки через» для поликонденсации, заключающийся в том, что проводят поликонденсацию флуоренового макромономера(ов) (4-6 мас. %), включающего(их) боковые полимерные цепи будущей молекулярной щетки из водорастворимых термочувствительных биосовместимых полимеров, представляющего(их) собой 2,7-дибромфлуорен с присоединенными к нему в положении 9,9 цепями полиалкилоксазолина или олигоэтиленгликоля, и второго мономера (0,5-3 мас. %) - 2,7-пинаколинового эфира дибороновой кислоты-9,9-дигексил-флуорена или 2,7-пинаколинового эфира дибороновой кислоты-9,9-диоктил-флуорена, при соотношении макромономер(ы) : второй мономер = 1:1 в растворе N,N-диметилформамида в атмосфере инертного газа в присутствии катализатора - 1,1'-бис(дифенилфосфино)ферроцена палладий (II) хлорида (0,25-0,35 мас. %), и 0,2 М раствора углекислого калия (30-35 об. %) в микроволновом реакторе при 95-100°С и мощности 100 W в течение 1-1.5 ч, по окончании реакции раствор очищают дробным осаждением с последующим центрифугированием, проводят очистку от остатков низкомолекулярных и олигомерных примесей с помощью диализа в течение 2 суток и центрифугирования раствора в пробирке с мембраной из пористой регенерированной целлюлозы, замораживают раствор и лиофильно сушат 2 суток, получают гигроскопичный сохраняемый в эксикаторе целевой продукт - люминесцирующую молекулярную щетку с формулой звена:
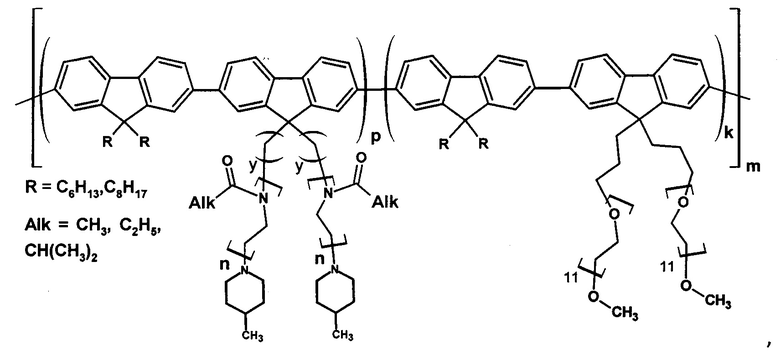
где p, k - мольная доля: p+k=1, p=0-1, k=0-1;
y=3, 6;
Mw=120-380 кДа.
В заявляемом изобретении разработан способ получения молекулярных щеток, где в качестве основной цепи выбран нетоксичный полисопряженный полимер - полифлуорен, излучающий синий свет с высоким квантовым выходом флуоресценции порядка 60-80% [Polyfluorenes / ed. by U. Scherf, D. Neher. Berlin: Springer, 2008. 322 р.]. В качестве боковых цепей выбраны биосовместимые термочувствительные водорастворимые полимеры - полиалкилоксазолины [В. Verbraeken, В. D. Monnery, К. Lava, R. Hoogenboom. The chemistry of poly(2-oxazoline)s // Europ.Polym. J. 2017. V. 88. P. 451-469], олигоэтиленгликоль [С.Yang, S. Huang, X. Wang, M. Wang. Theranostic Unimolecular Micelles of Highly Fluorescent Conjugated Polymer Bottlebrushes for Far Red/Near Infrared Bioimaging and Efficient Anticancer Drug Delivery // Polymer Chemistry. 2016. №3. P. 1-15]. Указанные полимеры обладают нижней критической температурой растворения (НКТР), которая варьируется от природы, например, алкильного заместителя и архитектуры макромолекул. НКТР для поли(изопропилоксазолина) лежит в области 37°С, что может быть потенциально использовано для образования полимерных сеток in situ в организме. Возможна визуализация исследуемых объектов с помощью люминесценции, которой обладают получаемые в результате реализации заявляемого способа молекулярные щетки.
В заявляемом изобретении разработан оригинальный метод «прививка через» для поликонденсации, где основную роль играют не макроинициаторы, как в «прививке от», а макромономеры с потенциальными боковыми цепями для будущей щетки. Ранее этот метод использовался только для радикальной полимеризации [H.-il Lee, J. Pietrasik, S. S. Sheiko, K. Matyjaszewski. Stimuli-responsive molecular brushes // Progr. Polym. Sci. 2010. V. 35. P. 24-44]. Для синтеза целевых молекулярных щеток в заявляемом изобретении проводят поликонденсацию макромономеров с получением регулярно привитых полимерных щеток с высокой плотностью прививки и возможностью варьировать природу боковых цепей в одной макромолекуле для придания полимеру различных свойств, имея возможность, что очень важно для увеличения спектра щеток, использовать разные макромономеры в одном синтезе.
Совокупность существенных признаков заявляемого способа обеспечивает получение технического результата - разработки технологии получения люминесцирующих нетоксичных молекулярных щеток с гарантированными регулярностью и высокой плотностью прививки, которая изначально вводится в макромономер, что обеспечивает указанный эффект.
Заявляемый способ отличается от известных использованием метода «прививка через» для поликонденсации, полимерным составом «хребта» и боковых цепей, макромономера, второго мономера, исходя из этого - и конкретными условиями способа.
Анализ известного уровня техники не позволил обнаружить решение, полностью совпадающее по совокупности существенных признаков с заявляемым, что может указывать на его новизну.
Только совокупность существенных признаков заявляемого способа позволяет достичь указанного технического результата. Известность нетоксичности и люминесцентных свойств полифлуорена, биосовместимости полимеров, использованных для боковых цепей, изначально открывали перспективы для их применения в биотехнологии, но не гарантировали априори получения из них качественных молекулярных щеток для применения в медицинской диагностике. Традиционный для аналогичных известных из литературы полимерных систем метод «прививка от» и полимеризация оказались непригодны по указанным выше причинам, прежде всего невозможности контроля за регулярностью и плотностью прививки. В то же время известный метод «прививка через» применялся только для радикальной полимеризации, что не подходило для макромономеров из заявляемого изобретения. Только совокупность операций и условий заявляемого способа позволил реализовать этот метод для поликонденсации с хорошими выходом и результатами по свойствам молекулярных щеток, что, в свою очередь, было неочевидно. Это позволяет утверждать о соответствии заявляемого способа условию охраноспособности «изобретательский уровень» («неочевидность»).
Графические материалы:
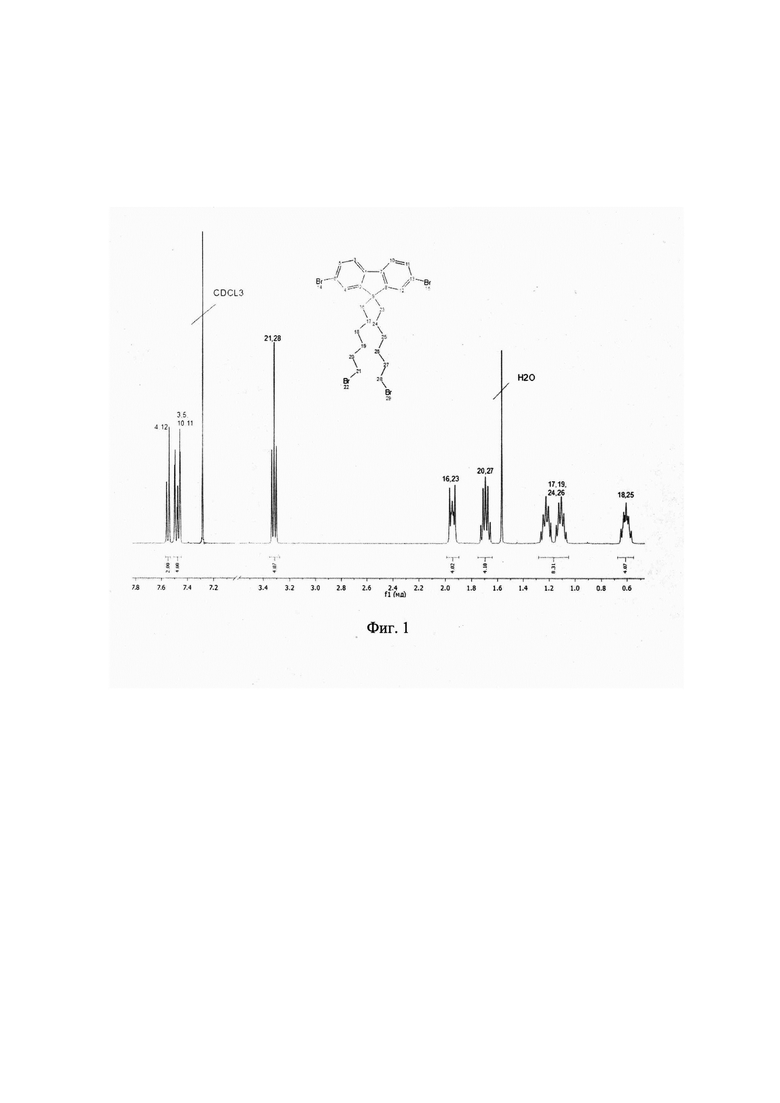
Фиг. 1. 1Н ЯМР спектр инициатора - 2,7-дибром-9,9-бис-(6-бромгексил)флуорена (пример 1), снят на приборе Bruker АС-400, 400 МГц.
Фиг. 2. 1Н ЯМР спектр смеси мономеров (пример 1), соответствующей эквимольному соотношению реагентов.
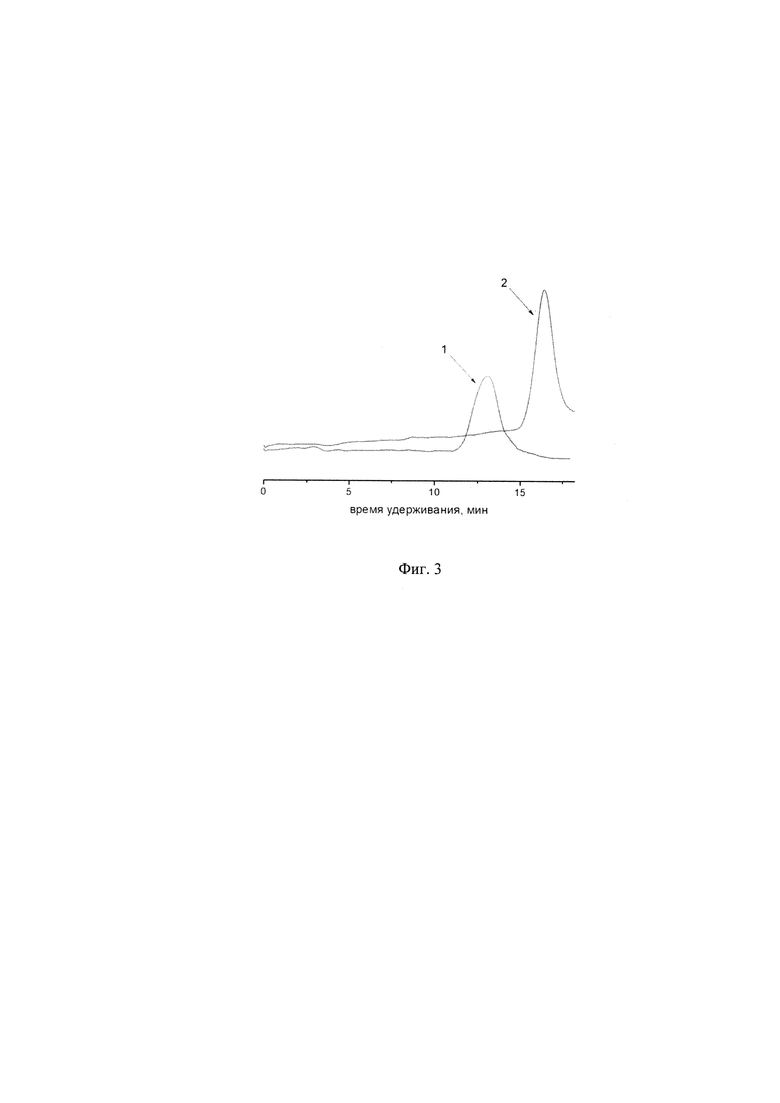
Фиг. 3. Хроматограммы: 1 - молекулярной щетки, 2 - макромономера (пример 1). Прибор: Agilent-1260 Infinity. Растворитель - ДМФА, 50°С.
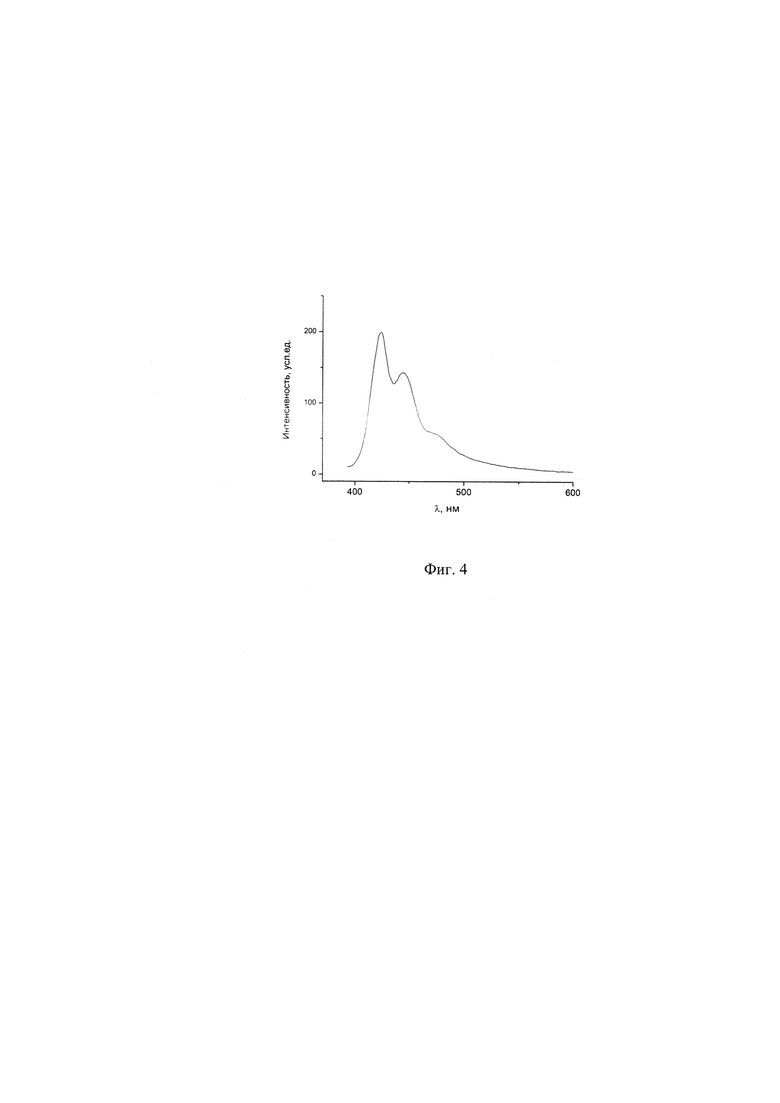
Фиг. 4. Спектр флуоресценции молекулярной щетки, полученной согласно примеру 1, в водном растворе на приборе спектрофотометре LS-100 (PTI®, Canada).
Для подтверждения соответствия заявляемого изобретения требованию «промышленная применимость» приводим примеры конкретной реализации.
Использованы коммерческие реактивы: мономеры водорастворимых термочувствительных биосовместимых полимеров - алкилоксазолины (метил-, этил-, изопропил-) и олигоэтиленгликоль монометиловый эфир (Mn=500), 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорена, 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктил-флуорена; растворитель N,N-диметилформамид (ДМФА), катализатор 1,1'-бис(дифенилфосфино)ферроцена палладий (II) хлорид (PdCl2[dppf] (Aldrich)), 4-метилпиперидин, хлорбензол, K2CO3, 1,6-дибромгексан, 3-бромпропанол, тозилхлорид, 2,7-дибромфлуорен, тетрабутиламмоний бромид, диметилсульфоксид.
Макромономер - 2,7-дибромфлуорен с присоединенными к нему в положении 9,9 цепями олигоэтиленгликоля (2,7-дибром-9,9-ди(2,5,8,11,14,17,23,26,29,32,35-додекаоксаоктатриаконтан-38-ил)флуорен синтезирован по методике, описанной в WO 2010/151807 А1.
Примеры с одним макромономером:
Пример 1. Синтез полифлуореновой молекулярной щетки с боковыми полиэтилоксазолиновыми цепями (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорен), p=1, k=0, y=6.
Получение макромономера осуществлено в 2 стадии: а) Синтез инициатора - 2,7-дибром-9,9-бис-(6-бромгексил)флуорена путем алкилирования 2,7-дибромфлуорена 1,6-дибромгексаном в 50%-ном растворе КОН с добавлением тетрабутиламмоний бромида по следующей схеме:
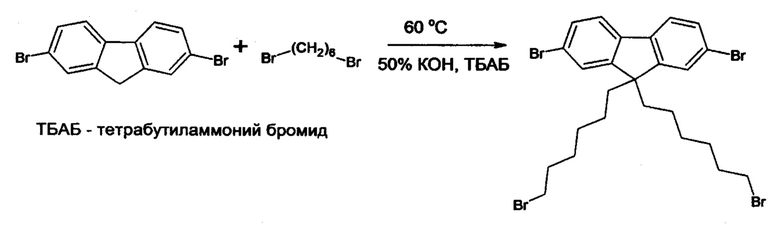
В круглодонную колбу объемом 250 мл с механической мешалкой вносят 8,3 г (9,5 мас. %) 2,7-дибромфлуорена, 50 мл (73 г, 90,3 мас. %) 1,6-дибромгексана, 0,166 г (0,2 мас. %) тетрабутиламмоний бромида, 50 мл 50%-ного раствора гидроксида калия. Реакцию ведут в атмосфере аргона при постоянном перемешивании 4 ч при 60°С. Затем реакционную смесь выливают в воду и экстрагируют хлористым метиленом, органический слой промывают водой 3 раза. Хлористый метилен удаляют на роторном испарителе. Примесь 1,6-дибромгексана отгоняют под вакуумом. Продукт очищают на колонке с силикагелем в смеси хлористый метилен/петролейный эфир в соотношении 1:10 (1,6-дибромгексан) и 1:1 (основное вещество). Все фракции около 50 мл. Растворители удаляют на роторном испарителе. Полученный белый порошок сушат в вакууме при 50°С. Выход: 13,49 г, 81%. Тпл=71-72°С.
б) Получение макромономера, содержащего боковые цепи будущей молекулярной щетки, путем катионной полимеризации с раскрытием цикла этилоксазолина, инициируемой 2,7-дибром-9,9-(6-бромгексил) флуореном по следующей схеме:
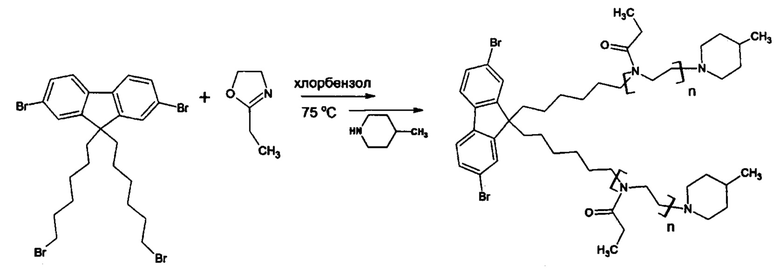
Для удаления влаги нагретую до 120°С стеклянную ампулу остужают в атмосфере аргона. Вносят в нее 0,5 г 2,7-дибром-9,9-бис-(6-бромгексил)флуорена и растворяют в 3,1 мл хлорбензола. Затем добавляют 3,1 мл 2-этил-2-оксазолина. Запаивают ампулу и оставляют в термостате на 72 ч при температуре 75°С. По окончании реакции ампулу вскрывают, добавляют 1 мл 4-метилпиперидина, перемешивают и оставляют на сутки при комнатной температуре. Затем хлорбензол отгоняют под вакуумом, растворяют полимер в воде и очищают диализом (мешки из регенерированной целлюлозы, поры 3.5 кДа) в течение 2 суток, периодически меняя воду. Полученный раствор замораживают и лиофильно сушат 2 суток. Полученный макромономер хранят в эксикаторе. Выход: 3,08 г, 87%. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=11 кДа, Mw/Mn=1,3).
Полученный макромономер содержит боковые цепи молекулярной щетки, описание получения которой приведено ниже.
Структуры полученного инициатора и макромономера были подтверждены спектральными методами, молекулярно-массовые характеристики полимеров исследованы методом гель-проникающей хроматографии (ГПХ). Полученные спектральные характеристики и хроматограммы подтверждены фигурами 1-3.
Синтез молекулярной щетки путем поликонденсации полученного макромономера и 2,7-пинаколинового эфира дибороновой кислоты-9,9-дигексил-флуорена по следующей схеме:
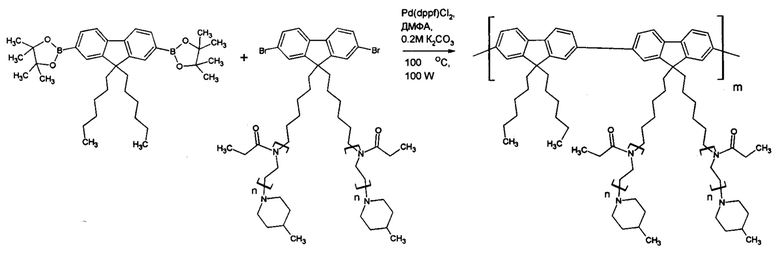
В стеклянную круглодонную колбу объемом 65 мл взвешивают навески 0,05 г (5 мас. %) макромономера и 0,0094 г (1 мас. %) 2,7-пинаколинового эфира дибороновой кислоты-9,9-дигексил-флуорена (соотношение мономеров 1:1, определено методом 1Н ЯМР, см. фиг. 2). Закрывают колбу холодильником и адаптером с отводом для ввода проб и вакуумным краном (Aldrich z530255). Затем систему вакуумируют и заполняют аргоном 3 раза. В перчаточном боксе в атмосфере аргона в колбу добавляют 0,003 г (0,3 мас. %) катализатора PdCl2[dppf] (Aldrich). Затем систему трижды вакуумируют и заполняют аргоном. Вносят в систему с помощью шприца через септу в адаптере 1 мл ДМФА, 0,5 мл (33 об. %) 0,2М раствора K2СО3 (раствор в бидистилированной воде), которые предварительно были продуты аргоном в течение 1 ч. Реакцию проводят в микроволновом реакторе СЕМ Discover SP при температуре 95-100°С и мощности 100 W (Режим: SPS mode, Т=5°С) в течение 1 ч. По окончании реакции раствор очищают дробным осаждением с последующим центрифугированием и проводят диализ (мешок из регенерированной целлюлозы с размером пор 12-14 кДа,) в течение 2 суток, очищают от остатков олигомерных примесей с помощью центрифугирования раствора в пробирке Amicon Ulta 4, Millipore, Sigma-Aldrich Z740192, с мембраной с размером пор 30 кДа; замораживают раствор и лиофильно сушат 2 суток. Выход полимера: 0,037 г, 70%. Полученный гигроскопичный полимер хранят в эксикаторе.
Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=250 кДа, Mw/Mn=1,7).
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Доказательства люминесценции полученной молекулярной щетки:
- Излучает синий свет с квантовым выходом флуоресценции 30-40%.
- Спектр флуоресценции (фиг. 4) доказывает наличие люминесценции (максимумы = 420, 445, 475 нм).
Доказательство нетоксичности полученной молекулярной щетки: Молекулярная щетка включает полимерную основную цепь из нетоксичного полифлуорена и боковые цепи из водорастворимых термочувствительных биосовместимых полимеров. Основываясь на литературных данных [С.Yang, S. Huang, X. Wang, М. Wang. Theranostic Unimolecular Micelles of Highly Fluorescent Conjugated Polymer Bottlebrushes for Far Red/Near Infrared Bioimaging and Efficient Anticancer Drug Delivery // Polymer Chemistry. 2016. №3. P. 1-15], которые свидетельствуют о том, что щетки, состоящие из нетоксичных основных полимерных цепей и биосовместимых боковых полимерных цепей (например, полифлуореновые молекулярные щетки с поли(олигоэтиленгликольметакрилатными) боковыми цепями), в целом нетоксичны, можно утверждать, что указанная молекулярная щетка также нетоксична.
Доказательство нетоксичности справедливо и для всех приведенных ниже примеров №№2-12.
Пример 2. Синтез люминесцирующей полифлуореновой молекулярной щетки с боковыми полиизопропилоксазолиновыми цепями (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорен). p=1, k=0, y=6.
Проведен в условиях примера 1. Исходное соединение при синтезе макромономера заменено на изопропилоксазолин. Концентрации реагентов: макромономер - 4 мас. %, второй мономер - 0,5 мас. %, катализатор - 0,25 мас. %, углекислый калий - 30 об. %. Получена молекулярная щетка со следующей формулой звена:
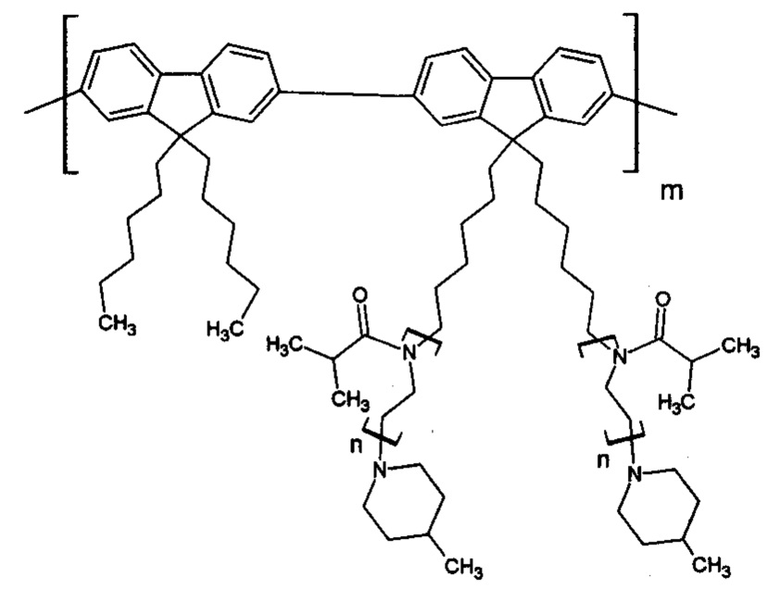
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=300 кДа, Mw/Mn=1,8). Выход полимера: 73%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 3. Синтез люминесцирующей полифлуореновой молекулярной щетки с боковыми полиметилоксазолиновыми цепями (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорен). p=1, k=0, y=6.
Проведен в условиях примера 1. Исходное соединение при синтезе макромономера заменено на метилоксазолин. Концентрации реагентов: макромономер - 6 мас. %, второй мономер - 3 мас. %, катализатор - 0,35 мас. %, углекислый калий - 35 об. %. Получена молекулярная щетка со следующей формулой звена:
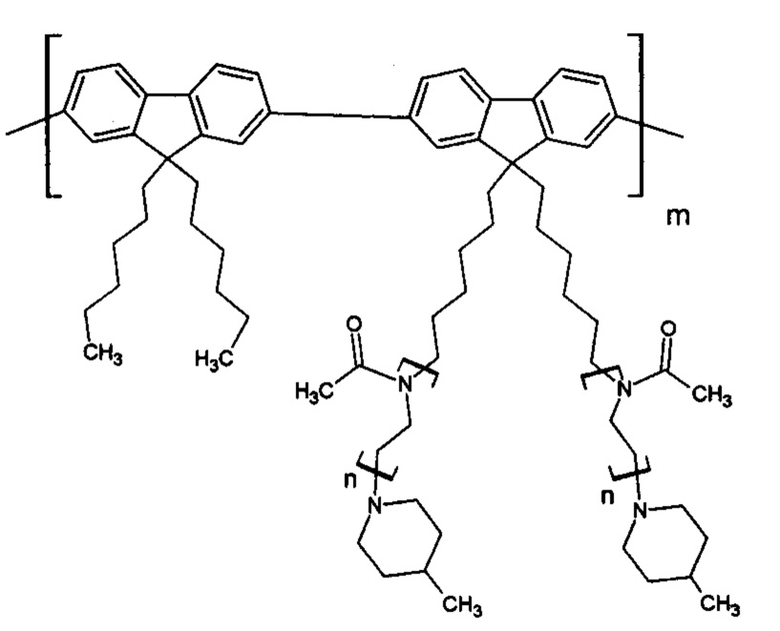
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=280 кДа, Mw/Mn=1,7). Выход полимера: 72%
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие.
Пример 4. Синтез люминесцирующей полифлуореновой молекулярной щетки с боковыми цепями олигоэтиленгликоля (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорен). p=0, k=1.
Проведен в условиях примера 1. Макромономер получен по методике, описанной в WO 2010/ 151807 А1, реакцией 2,7-дибром-9,9-ди(3-метилбензолсульфонатопропенил) флуорена с монометиловым эфиром олигоэтиленгликоля. Концентрации реагентов: макромономер - 4 мас. %, второй мономер - 2 мас. %, катализатор - 0,25 мас. %, углекислый калий - 30 об. %.
В результате поликонденсации получена молекулярная щетка со следующей формулой звена:
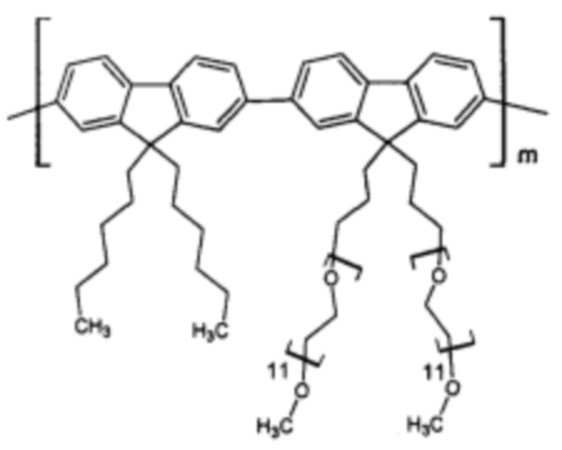
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=120 кДа, Mw/Mn=1,8). Выход полимера: 80%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 5. Синтез люминесцирующей полифлуореновой молекулярной щетки с боковыми полиэтилоксазолиновыми цепями (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктилфлуорен). p=1, k=0, y=6.
Проведен в условиях примера 1. Второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктилфлуорен. Получена молекулярная щетка со следующей формулой звена:
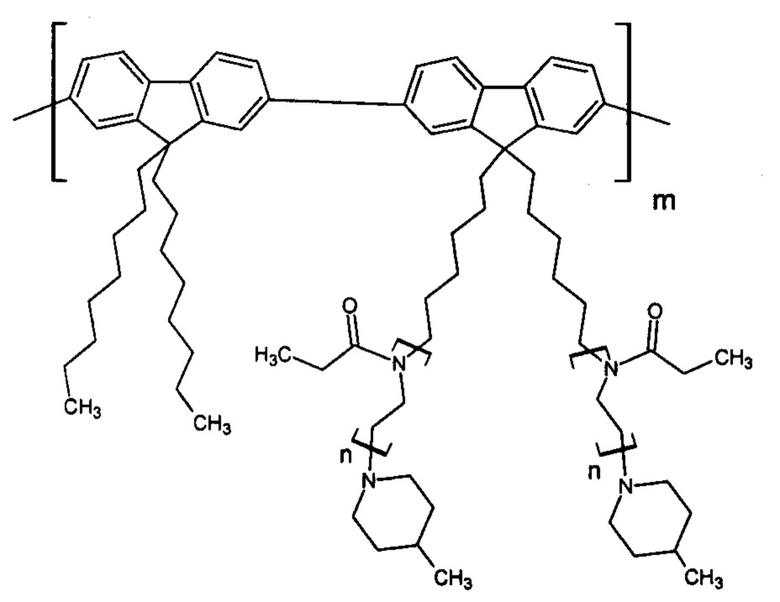
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=310 кДа, Mw/Mn=2). Выход полимера: 75%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Примеры с двумя разными макромономерами:
Пример 6. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями разных полиалкилоксазолинов: этил - и изопропил. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Суммарная концентрация двух макромономеров равна 5 мас. %. Исходные соединения при синтезе макромономера: этилоксазолин и изопропилоксазолин. Получена молекулярная щетка со следующей формулой звена:
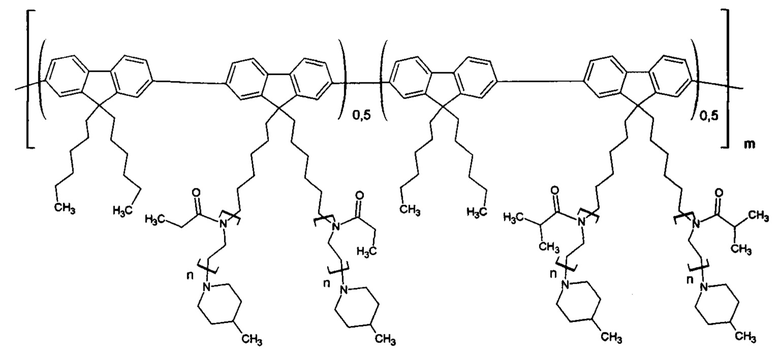
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=210 кДа, Mw/Mn=1,7). Выход полимера: 65%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 7. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями разных полиалкилоксазолинов: метил - и изопропил. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Исходные соединения при синтезе макромономеров: метилоксазолин и изопропилоксазолин. Суммарная концентрация двух макромономеров равна 5 мас. %. Получена молекулярная щетка со следующей формулой звена: 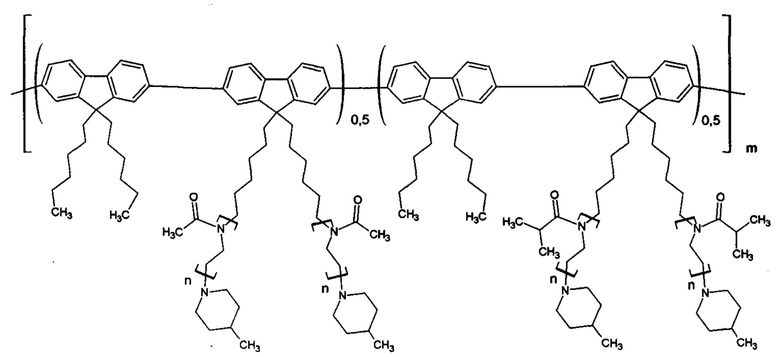
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=230 кДа, Mw/Mn=1,8). Выход полимера: 68%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 8. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями разных полиалкилоксазолинов: этил - и метил. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-дигексил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Исходные соединения при синтезе макромономера: этилоксазолин и метилоксазолин. Суммарная концентрация двух макромономеров равна 5 мас. %. Получена молекулярная щетка со следующей формулой звена:
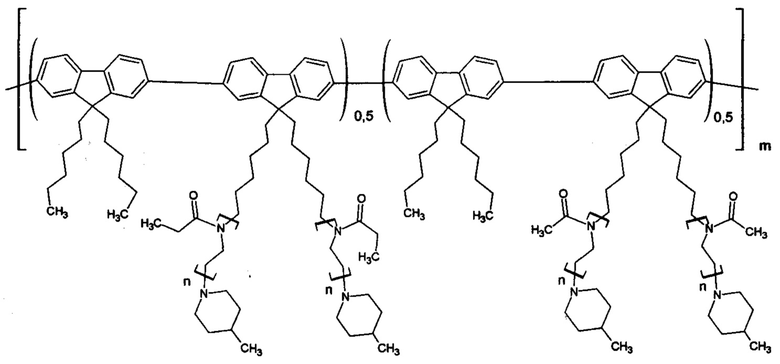
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=220 кДа, Mw/Mn=1,7). Выход полимера: 63%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие.
Пример 9. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями из полиэтилоксазолина и олигоэтиленгликоля. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Исходные соединения при синтезе макромономеров: этилоксазолин и олигоэтиленгликоль. Суммарная концентрация двух макромономеров равна 4 мас. %. Получена молекулярная щетка со следующей формулой звена:
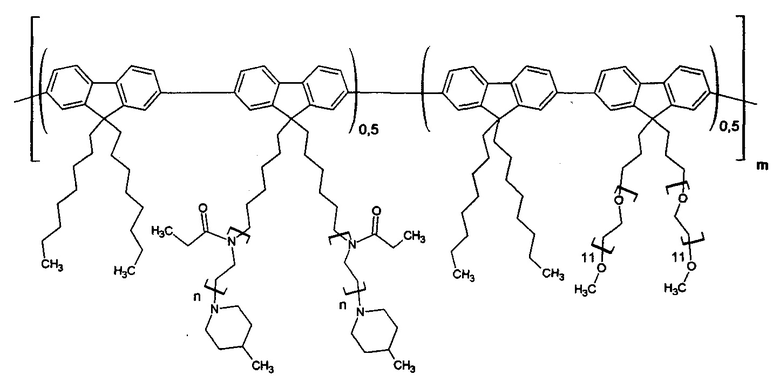
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=210 кДа, Mw/Mn=1,7). Выход полимера: 61%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 10. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями из полиметилоксазолина и олигоэтиленгликоля. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Исходные соединения при синтезе макромономеров: метилоксазолин и олигоэтиленгликоль. Суммарная концентрация двух макромономеров равна 4 мас. %. Получена молекулярная щетка со следующей формулой звена:
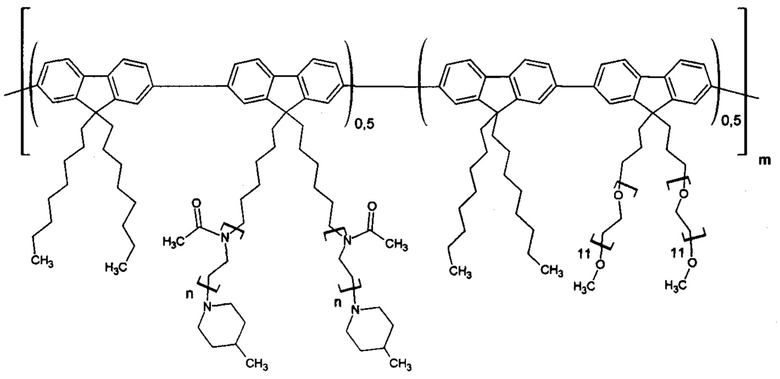
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=260 кДа, Mw/Mn=1,8). Выход полимера: 65%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 11. Синтез люминесцирующей полифлуореновой молекулярной щетки из двух макромономеров с боковыми цепями из полиизопропилоксазолина и олигоэтиленгликоля. В соотношении (50:50) (второй мономер - 2,7-пинаколиновый эфир дибороновой кислоты-9,9-диоктил-флуорена). p=0,5, k=0,5, y=6.
Проведен в условиях примера 1. Исходные соединения при синтезе макромономеров: изопропилоксазолин и олигоэтиленгликоль. Суммарная концентрация двух макромономеров равна 4 мас. %. Получена молекулярная щетка со следующей формулой звена:
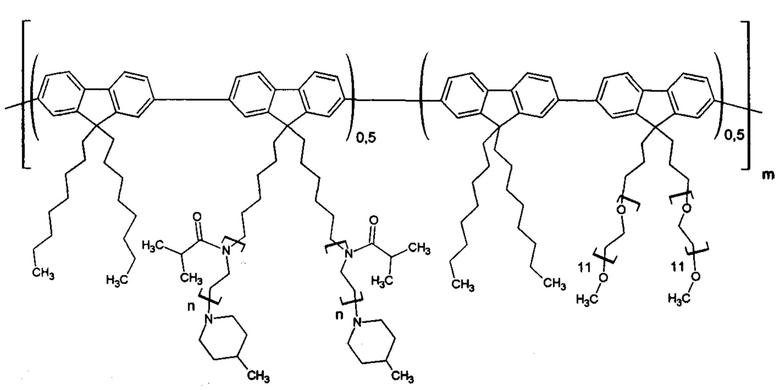
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=280 кДа, Mw/Mn=1,9). Выход полимера: 70%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как нетоксичны ее составляющие. Пример 12. Синтез полифлуореновой молекулярной щетки с боковыми полиэтилоксазолиновыми цепями. p=1, k=0, y=3.
Проведен в условиях примера 1.
а) Синтез инициатора - 2,7-дибром-9,9-ди(3-метилбензолсульфонатопропенил)флуорен получили в две стадии по методике, описанной в патентном документе WO 2010/ 151807 А1:
1. синтез 2,7-дибром-9,9-ди(3-гидроксипропил)флуорена реакцией 2,7-дибромфлуорена с 3 -бромпропанолом;
2. реакция 2,7-дибром-9,9-ди(3-гидроксипропил)флуорена с п-толуол сульфонилхлоридом.
б) Получение макромономера, содержащего боковые цепи будущей молекулярной щетки, путем катионной полимеризации с раскрытием цикла этилоксазолина, инициируемой 2,7-дибром-9,9-ди(3-метилбензолсульфонатопропенил)флуореном по следующей схеме:
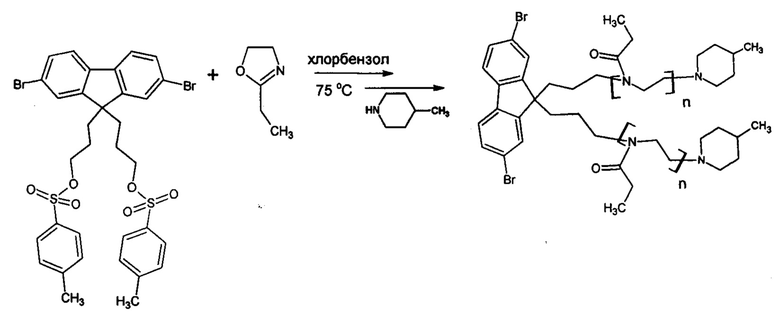
Получена молекулярная щетка со следующей формулой звена:
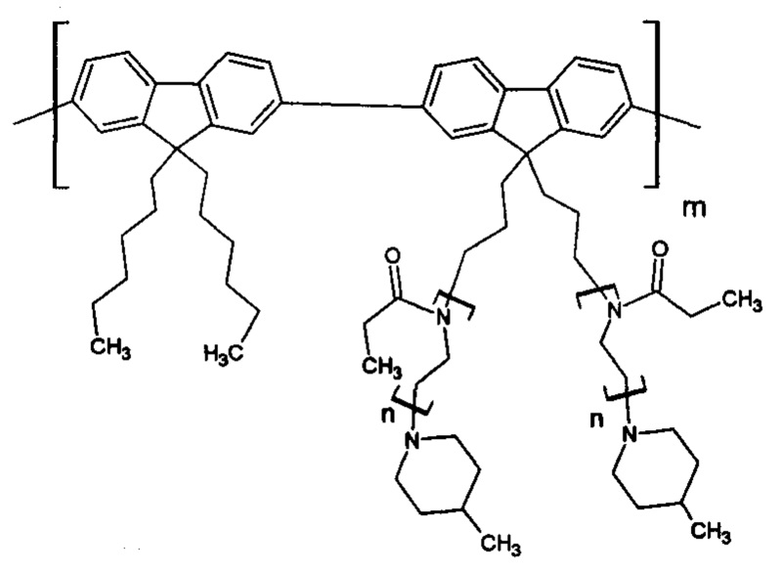
Полученный гигроскопичный продукт хранят в эксикаторе. Молекулярно-массовые характеристики определили методом ГПХ в растворе ДМФА при 50°С (Mw=380 кДа, Mw/Mn=1,8). Выход полимера: 74%.
Регулярность молекулярной щетки обусловлена процессом поликонденсации, определяющей четкую последовательность соединения мономеров. Высокая плотность прививки - наличием заранее заданных и входящих в макромономер боковых цепей.
Получена люминесцирующая молекулярная щетка, излучающая синий свет с квантовым выходом флуоресценции 30-40%.
Полученная молекулярная щетка не токсична, так как не токсичны ее составляющие.
Реализация заявляемого изобретения не исчерпывается приведенными примерами.
Выход за рамки заявленных интервальных параметров приводит к невозможности реализации заявляемого изобретения.
В результате реализации заявляемого изобретения разработана технология получения люминесцирующих нетоксичных полифлуореновых молекулярных щеток с гарантированными регулярностью и высокой плотностью прививки путем использования метода «прививки через» в поликонденсации с высоким выходом целевого продукта и воспроизводимостью результатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВОДОРАСТВОРИМЫЕ МОЛЕКУЛЯРНЫЕ ПОЛИФЛУОРЕНОВЫЕ ЩЕТКИ, ИЗЛУЧАЮЩИЕ БЕЛЫЙ СВЕТ | 2022 |
|
RU2800291C1 |
| Молекулярные полифлуореновые щетки с боковыми цепями полиметакриловой кислоты | 2021 |
|
RU2777171C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОРГАНОСИЛОКСАНОВЫХ МОЛЕКУЛЯРНЫХ ЩЕТОК | 2021 |
|
RU2783679C1 |
| ДЕНДРОНИЗОВАННЫЕ ПОЛИАРИЛСИЛАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2466156C2 |
| ГРЕБНЕОБРАЗНЫЕ ПОЛИМЕТИЛСИЛОКСАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2440382C1 |
| ТЕРМОСТАБИЛЬНЫЕ ЗАЩИТНЫЕ ПОКРЫТИЯ ИЗ ПОЛИИМИДОВ НА ОСНОВЕ 3,5-ДИАМИНОБЕНЗОЙНОЙ КИСЛОТЫ | 2021 |
|
RU2791384C1 |
| Сопряженный полимер на основе замещенного флуорена, бензотиадиазола и тиофена и его применение в перовскитных солнечных батареях | 2021 |
|
RU2789133C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРА ЭТИЛЕН-α-ОЛЕФИНДИЕНА | 2012 |
|
RU2599626C2 |
| НОВОЕ ЦИКЛОПЕНТА[b]ФЛУОРЕНИЛЬНОЕ СОЕДИНЕНИЕ ПЕРЕХОДНОГО МЕТАЛЛА, КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЕГО, И СПОСОБ ПОЛУЧЕНИЯ ГОМОПОЛИМЕРА ЭТИЛЕНА ИЛИ СОПОЛИМЕРА ЭТИЛЕНА И альфа-ОЛЕФИНА ПРИ ЕЕ ИСПОЛЬЗОВАНИИ | 2012 |
|
RU2632895C2 |
| БИОДЕГРАДИРУЕМЫЕ АРГИНИНСОДЕРЖАЩИЕ ПОЛИМЕРЫ | 2014 |
|
RU2549908C1 |

Изобретение относится к области химии высокомолекулярных соединений, а именно к способу получения люминесцирующих регулярно привитых полифлуореновых молекулярных щеток с боковыми цепями водорастворимых термочувствительных биосовместимых полимеров путем использования метода «прививки через» для поликонденсации, заключающийся в том, что проводят поликонденсацию флуоренового макромономера(ов) (4-6 мас.%), включающего(их) боковые полимерные цепи будущей молекулярной щетки из водорастворимых термочувствительных биосовместимых полимеров, представляющего(их) собой 2,7-дибромфлуорен с присоединенными к нему в положении 9,9 цепями полиалкилоксазолина или олигоэтиленгликоля, и второго мономера (0,5-3 мас.%) - 2,7-пинаколинового эфира дибороновой кислоты-9,9-дигексил-флуорена или 2,7-пинаколинового эфира дибороновой кислоты-9,9-диоктил-флуорена, при соотношении макромономер(ы) : второй мономер = 1:1 в растворе N,N-диметилформамида в атмосфере инертного газа в присутствии катализатора - 1,1'-бис(дифенилфосфино)ферроцена палладий (II) хлорида (0,25-0,35 мас.%), и 0,2 М раствора углекислого калия (30-35 об.%) в микроволновом реакторе при 95-100°С и мощности 100 W в течение 1-1,5 ч, по окончании реакции раствор очищают дробным осаждением с последующим центрифугированием, проводят очистку от остатков низкомолекулярных и олигомерных примесей с помощью диализа в течение 2 суток и центрифугирования раствора в пробирке с мембраной из пористой регенерированной целлюлозы, замораживают раствор и лиофильно сушат 2 суток, получают гигроскопичный сохраняемый в эксикаторе целевой продукт - люминесцирующую молекулярную щетку с формулой звена:
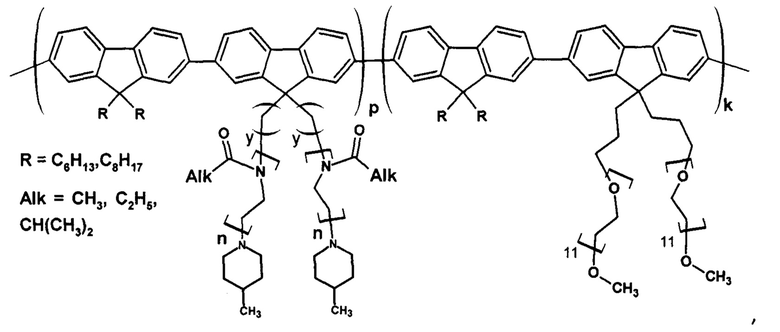
где р, k - мольная доля: р+k=1, р=0-1, k=0-1; y=3, 6; Mw=120-380 кДа. Технический результат: разработан способ получения молекулярных щеток методом «прививки через», отличающийся высоким выходом целевого продукта и высокой плотностью прививок. 12 пр., 4 ил.
Способ получения люминесцирующих регулярно привитых полифлуореновых молекулярных щеток с боковыми цепями водорастворимых термочувствительных биосовместимых полимеров путем использования метода «прививки через» для поликонденсации, заключающийся в том, что проводят поликонденсацию флуоренового макромономера(ов) (4-6 мас.%), включающего(их) боковые полимерные цепи будущей молекулярной щетки из водорастворимых термочувствительных биосовместимых полимеров, представляющего(их) собой 2,7-дибромфлуорен с присоединенными к нему в положении 9,9 цепями полиалкилоксазолина или олигоэтиленгликоля, и второго мономера (0,5-3 мас.%) - 2,7-пинаколинового эфира дибороновой кислоты-9,9-дигексил-флуорена или 2,7-пинаколинового эфира дибороновой кислоты-9,9-диоктил-флуорена, при соотношении макромономер(ы) : второй мономер = 1:1 в растворе N,N-диметилформамида в атмосфере инертного газа в присутствии катализатора - 1,1'-бис(дифенилфосфино)ферроцена палладий (II) хлорида (0,25-0,35 мас.%), и 0,2 М раствора углекислого калия (30-35 об.%) в микроволновом реакторе при 95-100°С и мощности 100 W в течение 1-1,5 ч, по окончании реакции раствор очищают дробным осаждением с последующим центрифугированием, проводят очистку от остатков низкомолекулярных и олигомерных примесей с помощью диализа в течение 2 суток и центрифугирования раствора в пробирке с мембраной из пористой регенерированной целлюлозы, замораживают раствор и лиофильно сушат 2 суток, получают гигроскопичный сохраняемый в эксикаторе целевой продукт - люминесцирующую молекулярную щетку с формулой звена:
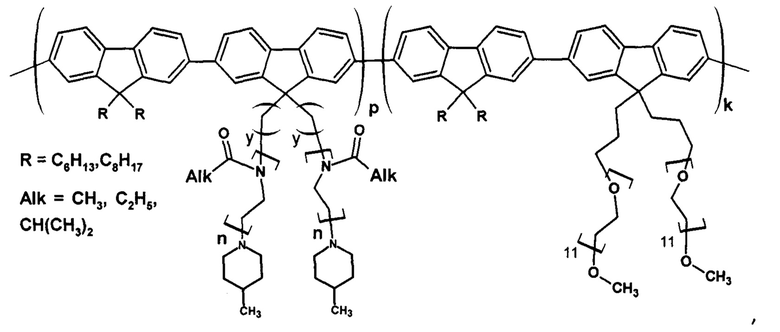
где р, k - мольная доля: р+k=1, р=0-1, k=0-1;
y=3, 6;
Mw=120-380 кДа.
| ИЛЬГАЧ Д.М | |||
| и др.: "ИСПОЛЬЗОВАНИЕ МЕТОДОВ КОНТРОЛИРУЕМОЙ РАДИКАЛЬНОЙ ПОЛИМЕРИЗАЦИИ ДЛЯ СИНТЕЗА ПОЛИМЕРНЫХ ЩЕТОК", ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ, СЕРИЯ С, 2015, 57(1), с.6-24 | |||
| Cangjie Yang и др.: "Hydrophobic-Sheath Segregated Macromolecular Fluorophores: Colloidal Nanoparticles of Polycaprolactone-Grafted Conjugated Polymers with Bright |
Авторы
Даты
2020-11-17—Публикация
2019-11-27—Подача