Изобретение относится к области нанотехнологии, медицины и пищевой промышленности.
Известны следующие способы получения микрокапсул.
Известен способ получения кремнийорганолипидных микрокапсул с использованием роторно-кавитационной установки, обладающей высокими сдвиговыми усилиями и мощными гидроакустическими явлениями звукового и ультразвукового диапазона для диспергирования (патент RU №2173140, опубликован 10.09.2001).
Недостатком данного способа является применение специального оборудования – роторно-кавитационной установки, которая обладает ультразвуковым действием, что оказывает влияние на образование микрокапсул и при этом может вызывать побочные реакции в связи с тем, что ультразвук разрушающе действует на полимеры белковой природы, поэтому предложенный способ применим при работе с полимерами синтетического происхождения.
Известен способ получения микрокапсул хлорида натрия с использованием распылительного охлаждения в распылительной градирне Niro (патент RU №2359662, опубликован 27.06.2009), в котором охлаждение происходит при следующих условиях: температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 об/мин. Микрокапсулы по изобретению обладают улучшенной стабильностью и обеспечивают регулируемое и/или пролонгированное высвобождение активного ингредиента.
Недостатками предложенного способа являются длительность процесса и применение специального оборудования, комплекс определенных условий (температура воздуха на входе 10°С, температура воздуха на выходе 28°С, скорость вращения распыляющего барабана 10000 об/мин).
Наиболее близким является способ получения микрокапсулированных препаратов, содержащих пиретроидные инсектициды (патент RU №2134967, опубликован 27.08.1999). Согласно описанию, в воде диспергируют раствор смеси природных липидов и пиретроидного инсектицида в весовом отношении 2-4 : 1 в органическом растворителе, что приводит к упрощению способа микрокапсулирования.
Недостатком способа является диспергирование в водной среде, что делает предложенный способ неприменимым для получения микрокапсул водорастворимых препаратов в водорастворимых полимерах.
Техническая задача – упрощение и ускорение процесса получения нанокапсул, уменьшение потерь при получении нанокапсул (увеличение выхода по массе).
Решение технической задачи достигается способом получения нанокапсул антоцианов краснокочанной капусты, отличающимся тем, что в качестве оболочки нанокапсул используется альгинат натрия, а в качестве ядра – антоцианы краснокочанной капусты при получении нанокапсул методом осаждения нерастворителем с применением бутилхлорида в качестве осадителя.
Отличительной особенностью предлагаемого метода является получение нанокапсул методом осаждения нерастворителем с использованием бутилхлорида в качестве осадителя, а также использование альгината натрия в качестве оболочки наночастиц и антоцианов краснокочанной капусты – в качестве ядра.
Результатом предлагаемого метода являются получение нанокапсул антоцианов краснокочанной капусты.
Предполагаемое изобретение охарактеризовано на следующих графических изображениях:
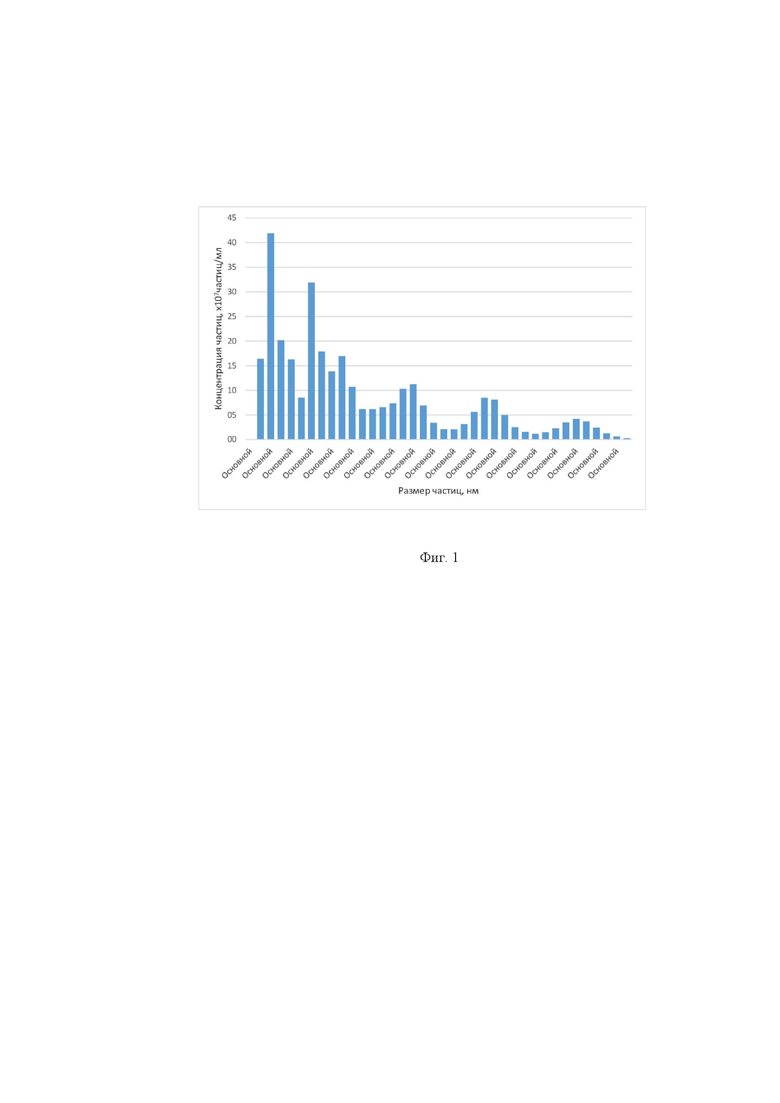
Фиг. 1. Распределение частиц по размерам в образце нанокапсул антоцианов краснокочанной капусты в альгинате натрия (соотношение ядро : оболочка 1 : 3).
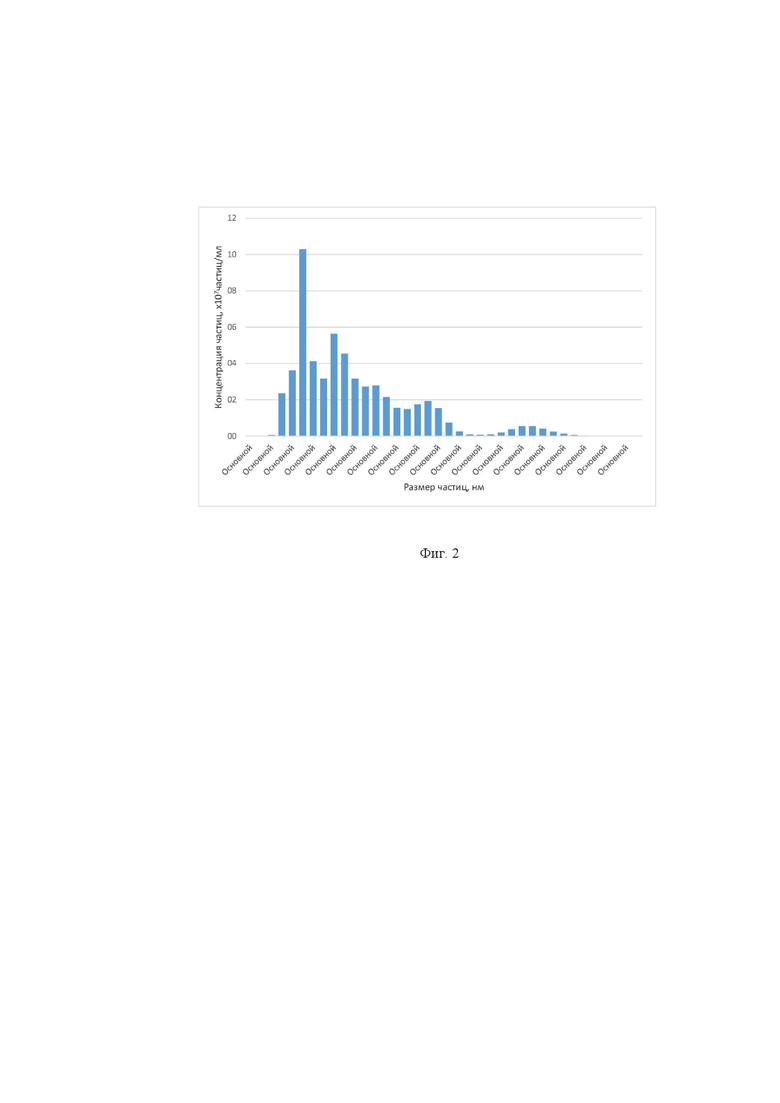
Фиг. 2. Распределение частиц по размерам в образце нанокапсул антоцианов краснокочанной капусты в альгинате натрия (соотношение ядро : оболочка 1 : 2).
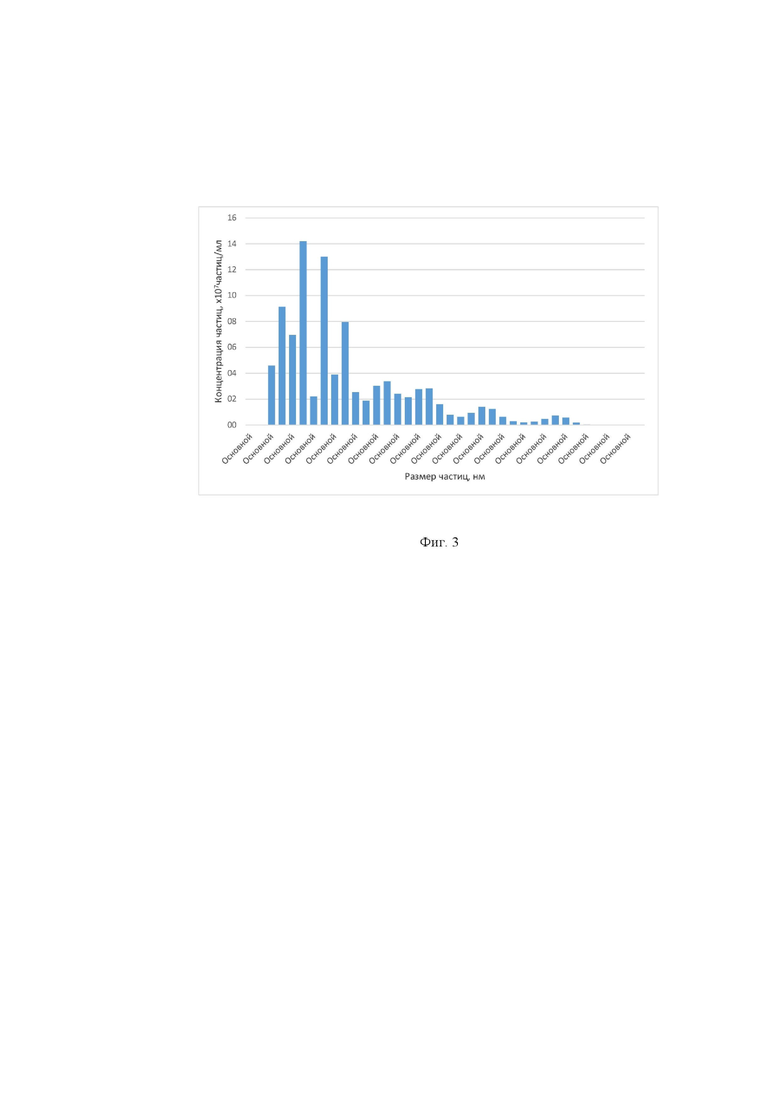
Фиг. 3. Распределение частиц по размерам в образце нанокапсул антоцианов краснокочанной капусты в альгинате натрия (соотношение ядро : оболочка 1 : 1).
Примеры осуществления способа
Пример 1
Получение нанокапсул антоцианов краснокачанной капусты, соотношение ядро : оболочка 1 : 3.
5 мл спиртового раствора, содержащего 0,5 г антоцианов краснокачанной капусты добавляют в суспензию 1,5 г альгината натрия в циклогексане, в присутствии 0,01 г препарата Е472с (сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота – другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием) в качестве поверхностно-активного вещества при перемешивании со скоростью 700 об/мин. Далее приливают 5 мл бутилхлорида. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 2,0 г порошка нанокапсул. Выход составил 100%.
Статистические характеристики распределения представлены
в таблице 1.
Таблица 1

Пример 2
Получение нанокапсул антоцианов краснокачанной капусты, соотношение ядро : оболочка 1 : 2.
5 мл спиртового раствора, содержащего 0,5 г антоцианов краснокочанной капусты добавляют в суспензию 1 г альгината натрия в циклогексане, в присутствии 0,01г препарата Е472с (сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота – другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием) в качестве поверхностно-активного вещества при перемешивании со скоростью 700 об/мин. Далее приливают 5 мл бутилхлорида. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 1,5 г порошка нанокапсул. Выход составил 100%.
Статистические характеристики распределения представлены
в таблице 2.
Таблица 2

Пример 3
Получение нанокапсул антоцианов краснокачанной капусты, соотношение ядро : оболочка 1 : 1.
5 мл спиртового раствора, содержащего 0,5 г антоцианов краснокочанной капусты добавляют в суспензию 0,5 г альгината натрия в циклогексане, в присутствии 0,01 г препарата Е472с (сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота – другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием) в качестве поверхностно-активного вещества при перемешивании со скоростью 700 об/мин. Далее приливают 5 мл бутилхлорида. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 1,0 г порошка нанокапсул. Выход составил 100%.
Статистические характеристики распределения представлены
в таблице 3.
Таблица 3

Пример 4
Определение размеров нанокапсул методом NTA.
Измерения проводили на мультипараметрическом анализаторе наночастиц Nanosight LM0 производства Nanosight Ltd (Великобритания) в конфигурации HS-BF (высокочувствительная видеокамера Andor Luca, полупроводниковый лазер с длиной волны 405 нм и мощностью 45 мВт). Работа прибора основана на методе анализа траекторий наночастиц (Nanoparticle Tracking Analysis, NTA), описанном в ASTM E2834.
Оптимальным разведением для разведения было выбрано 1 : 100. Для измерения были выбраны параметры прибора: Camera Level = 16, Detection Threshold = 10 (multi), Min Track Length:Auto, Min Expected Size: Auto, длительность единичного измерения 215s, использование шприцевого насоса. Результаты измерений размеров нанокапсул по примерам 1-3 представлены на фигурах 1-3 и в таблицах №1,2,3 соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения нанокапсул антоцианов краснокочанной капусты в натрий карбоксиметилцеллюлозе | 2020 |
|
RU2726830C1 |
| Способ получения нанокапсул антоцианов краснокочанной капусты в хитозане | 2020 |
|
RU2726791C1 |
| Способ получения нанокапсул сухого экстракта дикого ямса в каппа-каррагинане | 2018 |
|
RU2691393C1 |
| Способ получения нанокапсул тимола | 2019 |
|
RU2725614C1 |
| Способ получения нанокапсул сухого экстракта заманихи | 2017 |
|
RU2670437C1 |
| Способ получения нанокапсул сухого экстракта барбариса | 2017 |
|
RU2671191C1 |
| Способ получения нанокапсул сухого экстракта прополиса | 2018 |
|
RU2713422C2 |
| Способ получения нанокапсул сухого экстракта одуванчика | 2017 |
|
RU2674663C1 |
| Способ получения нанокапсул витамина РР (николинамида) | 2018 |
|
RU2696771C1 |
| Способ получения нанокапсул аспирина в альгинате натрия | 2014 |
|
RU2619329C2 |
Изобретение относится к области капсулирования активного вещества. Способ получения нанокапсул антоцианов краснокочанной капусты в альгинате натрия осуществляют, добавляя к спиртовому раствору, содержащему антоцианы краснокачанной капусты, суспензию альгината натрия в циклогексане в присутствии препарата Е472с, представляющего собой сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты в качестве поверхностно-активного вещества, при скорости перемешивания 700 об/мин. Далее приливают бутилхлорид для осаждения нанокапсул. Полученную суспензию нанокапсул отфильтровывают и сушат при комнатной температуре. Массовое соотношение ядро/оболочка в полученных нанокапсулах составляет 1:3, 1:2 или 1:1. Предлагаемый способ получения нанокапсул антоцианов краснокочанной капусты упрощает технологию получения нанокапсул, ускоряет процесс осаждения получаемых нанокапсул и увеличивает выход по массе нанокапсул. 3 табл., 4 пр., 3 ил.
Способ получения нанокапсул антоцианов краснокочанной капусты в альгинате натрия, характеризующийся тем, что антоцианы в спиртовом растворе добавляют в суспензию альгината натрия в циклогексане в присутствии сложного эфира глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты в качестве поверхностно-активного вещества при скорости перемешивания 700 об/мин, далее приливают бутилхлорид, полученную суспензию нанокапсул отфильтровывают и сушат при комнатной температуре, при этом массовое соотношение ядро/оболочка в нанокапсулах составляет 1:3, 1:2 или 1:1.
| Способ получения нанокапсул витамина РР (николинамида) | 2018 |
|
RU2696771C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННЫХ ПРЕПАРАТОВ, СОДЕРЖАЩИХ ПИРЕТРОИДНЫЕ ИНСЕКТИЦИДЫ | 1997 |
|
RU2134967C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНОЛИПИДНЫХ МИКРОКАПСУЛ ДЛЯ СОЗДАНИЯ МЕДИЦИНСКИХ, КОСМЕТИЧЕСКИХ ПРЕПАРАТОВ | 2000 |
|
RU2173140C1 |
| Способ получения нанокапсул L-метионина в альгинате натрия | 2018 |
|
RU2688153C1 |
| Способ получения нанокапсул сухого экстракта дикого ямса в каппа-каррагинане | 2018 |
|
RU2691393C1 |
| WO 2016049456 A1, 31.03.2016. | |||
Авторы
Даты
2020-11-19—Публикация
2020-06-01—Подача