Область техники
Настоящее изобретение относится к питательной композиции для младенцев и детей младшего возраста (приблизительно от 12 до 36 месяцев), в которой сумма триацилглицеринов (ТАГ) sn-1(3) пальмитиновой кислоты (ПК), миристиновой кислоты (МК) и стеариновой кислоты (СК) составляет менее 13% от ТАГ. Настоящая композиция постоянно способствует всасыванию жиров и кальция в кишечнике, улучшает кишечный комфорт, уменьшает боли в животе, вызванные образованием твердого стула, способствует регулярной дефекации и снижает частоту и тяжесть запоров.
Предпосылки создания изобретения
Грудное вскармливание считается идеальным источником питательных веществ и является предпочтительным выбором для кормления младенцев в возрасте до по меньшей мере 6 месяцев. Таким образом, грудное молоко (ГМ) в течение длительного времени считалось моделью для разработки детских смесей (ДС). Хотя за последние десятилетия в питательных композиция ДС наблюдаются заметные улучшения, все еще остаются значительные различия по сравнению с составом и функциональными преимуществами, которыми обладает ГМ. В частности, все еще наблюдаются различия во всасывании жиров и кальция, а также в желудочно-кишечной переносимости, между младенцами на грудном вскармливании (ВГ) и на вскармливании детской смесью (ВС). Всасывание и жиров, и Ca у младенцев ВС ниже, чем у младенцев ВГ. Кроме того, у младенцев ВГ происходит частая дефекация жидким или мягким стулом, тогда как у младенцев ВС дефекация происходит реже, наблюдается твердый, труднее проходящий стул, и, следовательно, они могут ощущать дискомфорт с болью, а в некоторых случаях наблюдается запор. Эти нарушения или особенности характера дефекации воспринимаются родителями как ненормальные и являются обычной причиной для беспокойства родителей и частым поводом к обращению за консультацией в лечебное учреждение.
Различия в частоте расстройств пищеварения у младенцев ВГ и ВС можно приписать отличиям в составе липидов ГМ, по сравнению с ДС, в частности, отличиям в составе триглицеридов (триацилглицерин, ТАГ).
Более 98% жиров грудного молока представлено в форме ТАГ, который содержит насыщенные и ненасыщенные жирные кислоты (ЖК), этерифицированные в положениях sn-1, -2, -3 молекулы sn-глицерина. Грудное молоко богато насыщенными жирными кислотами (НЖК), пальмитиновой кислотой (ПК) (составляющей ~20–25% от всех ЖК), из которой от 50 до 70% этерифицировано в положении sn-2 цепи глицерина. Такая конфигурация сопровождается размещением ненасыщенных ЖК, олеиновой и линолевой кислот в положении sn-1(3) в ТАГ. Коровье молоко, как и ГМ, содержит большое количество ПК (приблизительно 23–32,3% от всех ЖК), но лишь приблизительно 45% ПК этерифицировано в положении sn-2 в ТАГ, при 47% ПК в положении sn-1 и 7,5% ПК в положении sn-3. Растительные масла в составе ДС, такие как пальмовое масло, хотя они имеют общее количество ПК, близкое к таковому в ГМ, содержат высокий процент, как правило, 80–85% или более, пальмитиновой кислоты, находящейся в положении sn-1 или sn-3 в ТАГ.
Эфиры пальмитиновой кислоты (и других жирных кислот) в положениях sn-1 и sn-3 в ТАГ будут вероятнее всего расщеплены во время переваривания и образуют свободные жирные кислоты. Свободная пальмитиновая кислота может связывать кальций и образовывать нерастворимые мыла пальмитиновой кислоты в кишечнике. Экскреция этих мыл с калом может частично отвечать за более твердый стул, наблюдаемый у младенцев ВС при кормлении некоторыми детскими смесями.
Кроме того, в результате таких отклонений в характере дефекации и во всасывании жиров и кальция младенцы, которых вскармливают обычными ДС, также могут страдать от недоедания (замедленный рост), расстройств пищеварения, например, колик, сниженного аппетита, отрыгивания, и даже непереносимости пищевых компонентов. Пищеварительные расстройства, включая колики, могут проявляться как диарея, обильные газы, кишечный дискомфорт и боль, которые могут вызывать частые крики и беспокойство у младенцев или детей младшего возраста.
Твердый стул может вызывать запоры, беспокойство и крики, плохую переносимость пищи, желудочный дискомфорт и боли в животе. С возрастом стул становится еще тверже. Это может быть связано с изменениями рациона или изменениями кишечной моторики. Например, по мере введения младенцу ВГ дополнительного питания помимо грудного молока, особенно других источников белка, частота запоров возрастает. Аналогично, когда младенец ВС начинает потреблять источники белка помимо молока, частота запоров может возрастать. Поскольку тенденция к повышению твердости стула с возрастом, у детей младшего возраста запоры могут случаться чаще, чем у младенцев.
Таким образом, в соответствии с одним вариантом осуществления изобретения композиции настоящего изобретения снижают частоту и тяжесть запоров у младенцев и детей младшего возраста.
Образование в кишечнике нерастворимого мыла из жирных кислот также приводит к низкой биодоступности жиров и кальция.
Кроме того, у популяции, такой как младенцы, потеря кальция может повысить риск недостаточной минерализации костной ткани.
Слабое всасывание жиров может приводить к недоеданию и слабому развитию, поскольку жиры служат компактным источником энергии (обеспечивая 40–50% потребности в калориях).
Для улучшения биодоступности жиров и кальция для младенцев ВС были разработаны ДС с относительно низким общим содержанием ПК, чтобы количество ПК sn-1(3) в жировой смеси не превышало количества ПК sn-1(3) в жирах грудного молока. Кроме того, путем применения структурных ТАГ повышали пропорцию ПК в положении sn-2, тем самым снижая количества ПК sn-1(3). Известно, что снижение количества ПК в положении sn-1(3) путем применения структурных ТАГ улучшает всасывание ПК благодаря снижению образования мыла пальмитиновой кислоты в стуле, по сравнению со смесью на основе растительного масла, богатого пальмитиновой кислотой sn-1(3).
Однако исследованиями не удалось однозначно доказать преимущества ДС для смягчения стула и для всасывания жиров и Са.
Например, в публикации Carnielli et al. [Structural position and amount of palmitic acid in infant formulas: effects on fat, fatty acid, and mineral balance. J. Pediatr. Gastroenterol. Nutr. 1996 Dec; 23 (5): 553–60] показано, что у младенцев, которые потребляли смесь со структурными ТАГ, содержащую 8,5% от всех ЖК в виде ПК sn-1(3), всасывание ПК было лучше, чем у младенцев, которых вскармливали обычной ДС с 18,2% от всех ЖК в виде ПК sn-1(3). Интересно, что снижение ПК sn-1(3) было связано с улучшением всасывания насыщенных ЖК (т.е. лауриновой, миристиновой, пальмитиновой, стеариновой кислот), помимо пальмитиновой кислоты. Не наблюдалось значительных отличий для моно- и полиненасыщенных ЖК. Эти результаты согласуются с таковыми в других исследованиях, где младенцев кормили ДС, содержащей структурные ТАГ с количеством ПК sn-1(3) от 10,1 до 14,6% от всех ЖК, и в их стуле было значительно меньшее количество насыщенных ЖК, экскретированных большей частью в виде мыла, чем у младенцев, которых кормили обычной смесью. Остается неясным, как мыла пальмитиновой кислоты могут влиять на всасывание других насыщенных ЖК [Lopez-Lopez A, et al. The influence of dietary palmitic acid triacylglyceride position on the fatty acid, calcium and magnesium contents of at term newborn faeces. Early Hum. Dev. 2001 Nov; 65 Suppl: S83–S94, и Bar-Yoseph et al., SN2-Palmitate Reduces Fatty Acid Excretion in Chinese Formula-fed Infants. J. Pediatr. Gastroenterol. Nutr. 2016 Feb; 62 (2): 341–7].
В патенте EP1237419B2 от Nutricia представлены композиции ДС, в которых липидный компонент содержит ТАГ жирных кислот, где остатки ПК составляют более 10%, предпочтительно от 16 до 24%, от всех содержащихся в ТАГ эфиров ЖК, и при этом по меньшей мере в 30% триглицеридов они находятся в положении sn-2. ДС по EP 1237419, известные способностью смягчать стул, также включают пребиотик. Известно, что пре- и пробиотики стимулируют рост здоровой микробиоты у младенцев и детей младшего возраста, чтобы их кишечная флора по составу больше приближалась к таковой у детей на грудном вскармливании. Композиции по EP1237419 также содержат гидролизованный белок. Гидролизованный белок улучшает усвояемость, в частности, в отношении снижения риска аллергической реакции на белки коровьего молока.
В WO2013/068879 описаны композиции ДС, применяемые для улучшения консистенции стула. Эти ДС содержат олигофруктозу (по меньшей мере 0,45 г/100 ккал), чтобы увеличить количество bifidobacteria в толстом кишечнике, и 7,5–12% липидного компонента состоит из 7,5–12% ПК в положении sn-2 (для снижения кальциевого мыла).
Существует потребность в питательных композициях, применяемых в смесях для младенцев или детей младшего возраста для улучшения консистенции стула и снижения экскреции кальция со стулом (в форме мыла), особенно так, чтобы характер дефекации и всасывание Са и липидов приближалось к таковым у младенцев, вскармливаемых грудным молоком.
Существует потребность в питательных композициях, применяемых в смесях для младенцев или детей младшего возраста, которые диетически сбалансированы (по жирным кислотам) и которые могут улучшать пищеварительный комфорт и могут уменьшать или устранять боли в животе у младенцев и детей младшего возраста.
Существует потребность в питательных композициях, применяемых в смесях для младенцев или детей младшего возраста, которые облегчают регулярную дефекацию, предотвращают или снижают частоту и/или тяжесть запоров у младенцев или детей младшего возраста.
Существует потребность в обеспечении питательных композиций, которые способствуют всасыванию как жиров, так и кальция у младенцев или детей младшего возраста.
Существует потребность в обеспечении питательных композиций, которые увеличивают минерализацию костей, увеличивают прочность костей и/или увеличивают минеральную плотность костей у младенцев или детей младшего возраста.
Существует потребность в обеспечении питательных композиций, которые гарантируют здоровый рост у младенцев или детей младшего возраста.
До сих пор влияние других длинноцепочечных насыщенных жирных кислот (ДЦ-НЖК) в положении sn-1(3), помимо ПК, а именно миристиновой (14 : 0) и стеариновой (18 : 0) кислот, не рассматривали как важный фактор снижения доступности жиров и Ca, а также твердости стула у младенцев ВС. В ряде исследований заявитель определил, что суммарное (общее) количество этих трех ДЦ-НЖК (т.е. миристиновой, пальмитиновой и стеариновой кислот) в положении sn-1(3) в ТАГ важно для поддержания всасывания жирных кислот и кальция (Ca) и в приближении характера дефекации к таковому у младенцев ВГ.
Заявитель определил для липидных компонентов питательных композиций профили ТАГ, которые являются благоприятными для уменьшения пищеварительного дискомфорта, и/или уменьшения болей в животе, и/или уменьшения риска запора у младенцев и/или детей младшего возраста.
Таким образом, заявитель определил, что питательные композиции, имеющие сумму миристиновой, пальмитиновой и стеариновой кислот в положении sn-1(3), по существу, менее 13% (мас.%/мас.%) от ТАГ, могут улучшать желудочно-кишечную переносимость, биодоступность жиров и Ca у младенцев и детей младшего возраста. Конкретно, заявитель определил, что сумма МК, ПК и СК sn-1(3) менее 13% от ТАГ постоянно способствует всасыванию жиров и Ca путем снижения образования кальциевого мыла жирных кислот. Заявитель также определил, что питательные композиции, содержащие липиды, в которых сумма МК, ПК и СК sn-1(3) составляет менее 13% от ТАГ, постоянно улучшают консистенцию стула и приближают характер дефекации к таковому у младенцев ВГ.
Результаты исследований расщепления in vitro, проведенных заявителем, доказывают эффективность композиций с липидами, которые имеют указанные выше ограниченные количества ПК, СК и МК sn-1(3).
Изложение сущности изобретения
В первом аспекте настоящее изобретение относится к композиции для младенцев или детей младшего возраста, содержащей белки, углеводы и липиды, причем указанные липиды содержат триацилглицерины (ТАГ) жирных кислот (ЖК), причем указанные ТАГ жирных кислот содержат стеариновые, пальмитиновые и миристиновые эфиры, при этом суммарное количество стеариновых, пальмитиновых и миристиновых эфиров в положении sn-1(3) в ТАГ составляет менее 13,0% (мас.%/мас.%) от ТАГ, а миристиновая кислота составляет до 3,6% от всех ЖК, пальмитиновая кислота составляет до 11,1% от всех ЖК, миристиновая кислота составляет до 4,6% от всех ЖК (мас.%/мас.%).
В одном варианте осуществления изобретения общая сумма пальмитиновых, миристиновых и стеариновых эфиров в ТАГ составляет менее 19,3% (мас.%/мас.%) от общего содержания ТАГ жирных кислот.
В одном варианте осуществления изобретения углеводы в композиции на 99–100% состоят из лактозы.
В одном варианте осуществления изобретения количество белка в композиции менее или равно 3,0 или 2,1 г белка/100 ккал композиции, предпочтительно менее или равно 1,9 г белка/100 ккал, более предпочтительно менее или равно 1,8 г белка/100 ккал, а наиболее предпочтительно менее или равно 1,7 г белка/100 ккал.
В одном варианте осуществления изобретения белки представляют собой смесь сывороточного белка и казеина, причем пропорция сывороточного белка и казеина составляет от 50 : 50 до 80 : 20.
В одном варианте осуществления изобретения белок частично гидролизован.
В одном варианте осуществления изобретения композиция также содержит по меньшей мере один пребиотик, предпочтительно выбранный из 2’-фукозиллактозы, лактодифукотетрозы, 3’-фукозиллактозы, лакто-N-фукопентозы I, лакто-N-фукопентозы II, лакто-N-фукопентозы III, лакто-N-неотетрозы, лакто-N-тетрозы, 3’-сиалиллактозы, 6’-сиалиллактозы, 3’-сиалиллакто-N-тетрозы, 6’-сиалиллакто-N-неотетрозы, инулина, фруктоолигосахарида (FOS), короткоцепочечного фруктоолигосахарида (короткоцепочечный FOS), галактоолигосахарида (GOS), ксилоолигосахарида (XOS), ганглиозида, частично гидролизованной камеди гуара, гуммиарабика, камеди соевых бобов или их смесей.
В одном варианте осуществления изобретения композиция также содержит пробиотики, предпочтительно выбранные из Lactobacillus paracasei, Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium lactis и Bifidobacterium breve, Bifidobacterium animalis, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus reuteri, Lactobacillus johnsonii, Lactobacillus plantarum, Lactococcus lactis, Streptococcus thermophilus, Enterococcusfaecium, Saccharomyces cerevisiae, Saccharomyces boulardii и E. Coli Nissle. В частности, пробиотики и пробиотики, содержащие неразмножающийся штамм, такие как род Lactobacillus, Bifidobacterium или их комбинацию, например, Lactobacillus johnsonii, Lactobacillus paracasei, Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium breve или их комбинацию и/или нежизнеспособные фракции этих бактерий.
В одном варианте осуществления изобретения липиды композиции содержат докозагексаеновую кислоту (DHA), и/или арахидоновую кислоту (ARA), и/или эйкозапентаеновую кислоту (EPA).
В одном варианте осуществления изобретения композицию применяют для уменьшения пищеварительного дискомфорта, и/или уменьшения болей в животе, и/или уменьшения частоты и/или тяжести колик, и/или уменьшения частоты и/или тяжести запора у младенцев или детей младшего возраста.
Указанное уменьшение пищеварительного дискомфорта, и/или уменьшение болей в животе, и/или уменьшение частоты и/или тяжести колик, и/или уменьшение частоты и/или тяжести запора может содержать уменьшение твердости стула, предпочтительно до приближения консистенции стула к таковой у младенцев на грудном вскармливании или у детей младшего возраста с нормальным характером дефекации.
В одном варианте осуществления изобретения композицию применяют для улучшения гомеостаза кальция и всасывания кальция и липидов, повышения удерживания кальция и липидов, и/или уменьшения образования мыла с пальмитиновой кислотой, или стеариновой кислотой, или миристиновой кислотой у младенцев или детей младшего возраста.
В одном варианте осуществления изобретения композицию применяют для увеличения минерализации костей, увеличения прочности костей и/или увеличения минеральной плотности костей у младенцев или детей младшего возраста.
Описание графических материалов
На фиг. 1 представлены результаты растворимости кальция in vitro из образцов переваренной детской смеси, содержащих разные количества ДЦ-НЖК sn-1,3 (пример 4).
Подробное описание
Любую ссылку на документы предшествующего уровня техники в данном описании не следует рассматривать как признание того, что такой предшествующий уровень техники является широко известным или составляет часть общеизвестных знаний в данной области.
В данном описании слова «содержит», «содержащий» и аналогичные слова не следует интерпретировать в исключительном или исчерпывающем смысле. Иными словами, предполагается, что они означают «включая, без ограничений».
Все используемые в настоящем документе технические и научные термины, если не дано их иное определение, имеют общепринятое значение, понятное среднему специалисту в данной области.
Термин «младенец» в контексте настоящего изобретения будет означать ребенка в возрасте до 12 месяцев.
Термины «ребенок младшего возраста» или «дети младшего возраста» относится к ребенку в возрасте от 12 месяцев до 3 лет.
В контексте настоящего изобретения младенец может представлять собой любого доношенного младенца или недоношенного младенца. В одном варианте осуществления изобретения младенца выбирают из группы недоношенных младенцев и доношенных младенцев.
Термин «детская смесь» (или ДС) в контексте настоящего изобретения относится к питательной композиции, предназначенной для младенцев в первые месяцы жизни, в соответствии с определением в Codex Alimentarius (Кодекс STAN 72-1981), и к специальным продуктам для младенцев (включая продукты питания для специальных медицинских целей) в соответствии с определением в Codex Alimentarius (Кодекс STAN 72-1981).
Термином «смесь для прикармливаемых детей» обозначаются смеси, предназначенные для применения у детей в возрасте от 6 до 12 месяцев.
Термином «молочная смесь для детей от 1 до 3 лет» обозначаются смеси, предназначенные для применения у детей, начиная с одного года, по существу, до возраста трех лет. По существу, это напиток на молочной основе, адаптированный для специфических потребностей в питании у детей младшего возраста.
«Обогатитель» можно определить как композицию для недоношенных младенцев и/или для доношенных младенцев, которые являются «маленькими для своего гестационного возраста» и нуждаются в дополнительном питании, которое поддерживает рост.
В контексте настоящего изобретения термин «композиция для применения в смесях для младенцев или детей младшего возраста» также относится к самой смеси, например детской смеси (ДС), которая содержит все питательные вещества, необходимые для соответствия стандартам для детской смеси, определенным в Codex Alimentarius. Кроме того, «композиция для применения в смесях для младенцев или детей младшего возраста» может представлять собой композицию, содержащую питательные вещества, которую можно смешивать вместе с другими питательными веществами для получения смеси, т.е. такую «композицию для применения в составе для младенцев» можно добавлять в смесь, предназначенную для применения в качестве детской смеси. Кроме того, «композиция для применения в смесях» может представлять собой добавку или обогатитель для детской смеси, смеси для прикармливаемых детей, молочной смеси для детей от 1 до 3 лет или грудного молока.
Пальмитиновая кислота (ПК), миристиновая кислота (МК) и стеариновая кислота (СК)
В контексте настоящего изобретения термин «пальмитиновая кислота» (ПК) относится к насыщенной жирной кислоте, 16 : 0. Для обозначения «пальмитиновой кислоты», этерифицированной с глицерином, например в триацилглицеринах (ТАГ), также можно употреблять термины «пальмитат» или «эфир пальмитиновой кислоты». Представленные ниже термины используются для описания пространственного распределения ПК в ТАГ. Если ПК этерифицирована во внешнем (альфа), первом или третьем положении в ТАГ, то ПК находится в положении sn-1 или sn-3 в ТАГ. Такую ПК в контексте настоящего изобретения называют пальмитатом sn-1(3), или ПК sn-1(3), или эфиром ПК sn-1(3), или пальмитиновой кислотой sn-1(3), или эфиром пальмитиновой кислоты sn-1(3). Если ПК этерифицирована во внутреннем (бета) положении в ТАГ, известном как положение sn-2 или бета, то в контексте настоящего изобретения ее называют пальмитатом sn-2, или ПК sn-2, или эфиром ПК sn-2, или пальмитиновой кислотой sn-2, или эфиром пальмитиновой кислоты sn-2. Питательные композиции настоящего изобретения содержат липидный компонент, содержащий ТАГ.
В контексте настоящего изобретения термин «миристиновая кислота» (МК) относится к насыщенной жирной кислоте, 14 : 0. Вместо «миристиновой кислоты» также можно употреблять термины «миристат», или «остаток миристиновой кислоты», или «эфир МК», когда она этерифицирована в ТАГ.
Если МК этерифицирована во внешнем (альфа), первом или третьем положении в ТАГ, то ПК находится в положении sn-1 или sn-3 в ТАГ. Такую МК в контексте настоящего изобретения называют миристатом sn-1(3), или МК sn-1(3), или эфиром МК sn-1(3), или миристиновой кислотой sn-1(3), или эфиром миристиновой кислоты sn-1(3). Если МК этерифицирована во внутреннем (бета) положении в ТАГ, известном как положение sn-2 или бета, то в контексте настоящего изобретения ее называют миристатом sn-2, или МК sn-2, или эфиром МК sn-2, или миристиновой кислотой sn-2, или эфиром миристиновой кислоты sn-2.
В контексте настоящего изобретения термин «стеариновая кислота» (СК) относится к насыщенной жирной кислоте, 18 : 0. Вместо «стеариновой кислоты» также можно употреблять термины «стеарат» или «эфир стеариновой кислоты», когда она этерифицирована в ТАГ.
Если СК этерифицирована во внешнем (альфа), первом или третьем положении в ТАГ, то СК находится в положении sn-1 или sn-3 в ТАГ. Такую СК в контексте настоящего изобретения называют стеаратом sn-1(3), или СК sn-1(3), или эфиром СК sn-1(3), или стеариновой кислотой sn-1(3), или эфиром стеариновой кислоты sn-1(3). Если СК этерифицирована во внутреннем (бета) положении в ТАГ, известном как положение sn-2 или бета, то в контексте настоящего изобретения ее называют стеаратом sn-2, или СК sn-2, или эфиром СК sn-2, или стеариновой кислотой sn-2, или эфиром стеариновой кислоты sn-2.
В контексте настоящего изобретения процентные содержания (%) показаны как отношение массы к массе (мас.%/мас%.).
В контексте настоящего изобретения термины «сумма эфиров пальмитиновой кислоты и стеариновой кислоты и миристиновой кислоты, расположенных в положении sn-1(3) ТАГ» или «ДЦ-НЖК sn-1(3)» относятся к количеству пальмитиновой кислоты sn-1(3) плюс количество sn-1(3) миристиновой кислоты плюс количество sn-1(3) стеариновой кислоты, на основании количества пальмитиновой кислоты плюс миристиновой кислоты плюс стеариновой кислоты, представленных в форме ТАГ.
Аналогичным образом термин «количество sn-1(3)-пальмитиновой кислоты» относится к количеству альфа-пальмитиновой кислоты, рассчитанному на основе общего количества пальмитиновой кислоты в ТАГ.
Настоящее изобретение относится к питательным композициям и их применению в случае питательных композиций для младенцев и детей младшего возраста. Питательные композиции содержат белки, углеводы и липиды.
Заявитель проводил исследование на основании набора опубликованных клинических испытаний, сообщавших о всасывании жиров и Са и/или о консистенции стула у младенцев. Заявитель анализировал состав и пространственное распределение ТАГ в масляных смесях ТАГ для ДС, которые применяли в испытаниях для определения благоприятного состава ЖК и профиля ТАГ (т.е. пространственного распределения ЖК в ТАГ).
Это исследование проводили с использованием базы данных, которая содержит состав ЖК и их распределение в ТАГ из 450 промышленно производимых жиров и масел. Состав ЖК и соответственное пространственное распределение в ТАГ из этих жиров и масел выполняли методом газовой хроматографии [Beggio M, Giuffrida F, Golay P, Nagy K, Destaillats F. Robotized method for the quantification of fatty acids by gas-liquid chromatography. Eur. J. Lipid. Sci. Technol. 2013; 115: 825–30] и методом неводной обращенно-фазовой жидкостной хроматографии с гибридной масс-спектрометрией [Nagy K, Sandoz L, Destaillats F, Schafer O. Mapping the regioisomeric distribution of fatty acids in triacylglycerols by hybrid mass spectrometry. J. Lipid Res. 2013 Jan; 54 (1): 290–305] соответственно. Состав ЖК и пространственное распределение ЖК в положениях sn-1(3) и sn-2 в каждом типе масел из этой базы данных представляли собой средний состав от 1 до 21 отдельного образца из разных мест в мире. В каждом масле и жире рассчитывали сумму ДЦ-НЖК в положении sn-1(3) в ТАГ. Результаты приведены ниже в таблицах 1 и 2.
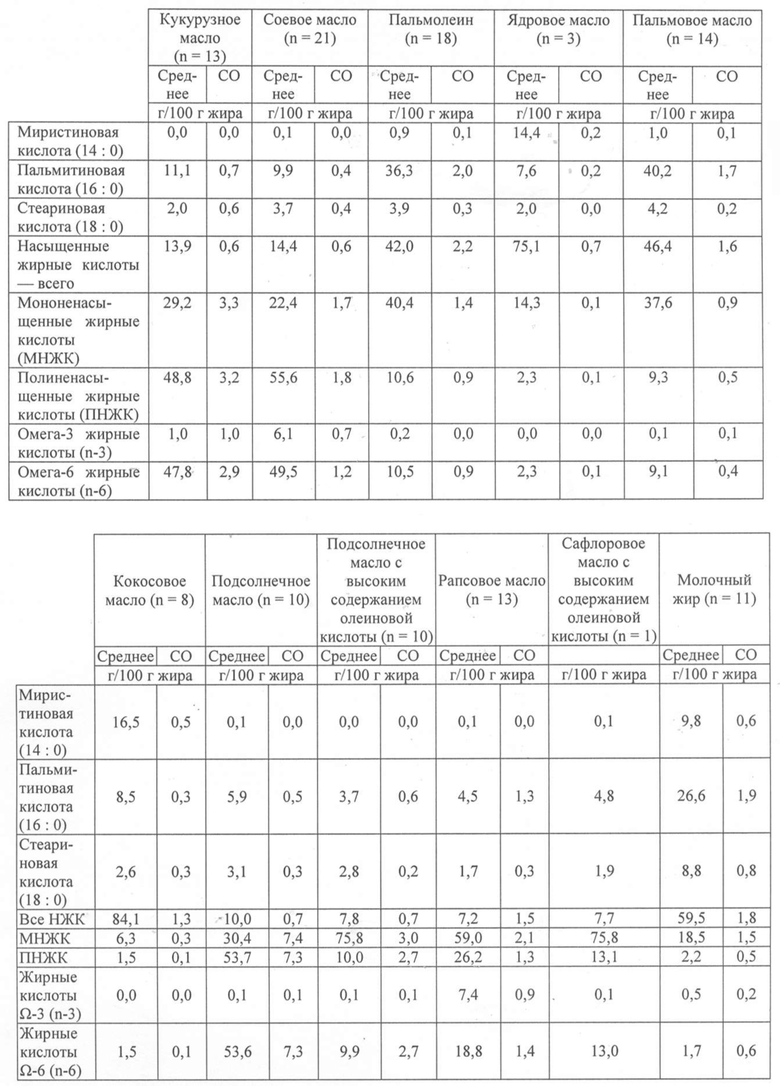
Таблица 1. Содержание миристиновой, пальмитиновой и стеариновой кислот в различных растительных маслах и молочном жире
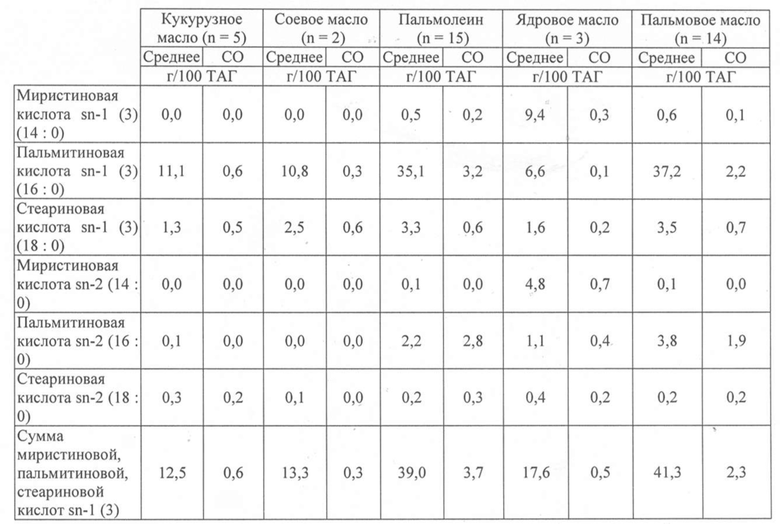
Таблица 2. Пространственное распределение миристиновой кислоты, пальмитиновой кислоты и стеариновой кислоты в различных растительных маслах и молочном жире
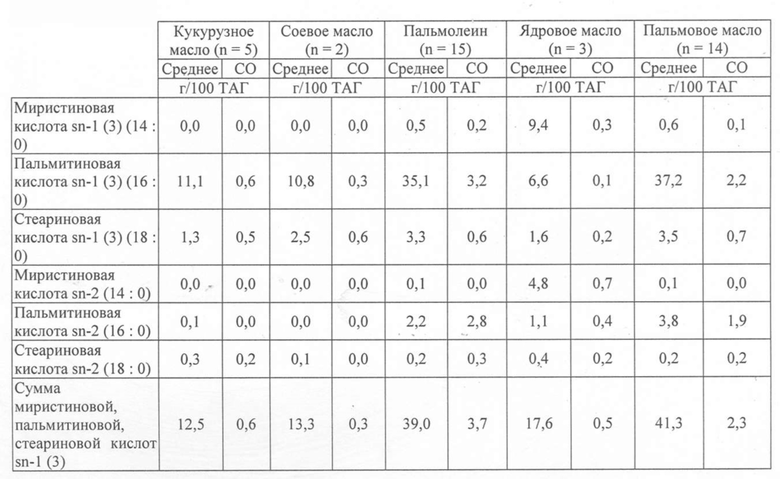
На модели переваривания in vitro заявитель дополнительно исследовал влияние состава ЖК и пространственного распределения остатков ЖК на биодоступность жиров и кальция. На основании результатов этих анализов заявитель определил благоприятный интервал для суммы МК, ПК и СК в положениях sn-1(3) в ТАГ для включения в композиции для младенцев и детей младшего возраста, которые уменьшают пищеварительный дискомфорт и/или боль, и/или уменьшают боли в животе, и/или уменьшают риск запора у младенцев и детей младшего возраста.
Липиды
В соответствии с одним аспектом изобретения липиды в питательной композиции содержат ТАГ, которые содержат эфиры стеариновой кислоты, пальмитиновой кислоты и миристиновой кислоты. Суммарное количество остатков пальмитиновой кислоты, миристиновой кислоты и стеариновой кислоты в положении sn-1(3) в ТАГ, по существу, составляет менее 13% (мас.%/мас.%) от ТАГ. Липиды могут содержать другие ЖК. Суточные дозы липидов и всех остальных вводимых соединений должны в любом случае соответствовать опубликованным руководящим указаниям по безопасности и нормативным требованиям. Это особенно важно при введении новорожденным детям, в частности детям с низким весом при рождении, очень низким или чрезвычайно низким весом при рождении. Таким образом, смесь липидов отвечает действующим диетическим требованиям для включения в детскую смесь.
Специалист может получить сведения о составе ЖК и пространственном структурном составе ТАГ в нескольких маслах из таблиц 1 и 2, чтобы определить количество данных масел, которые он может включать в композицию. Специалисту известно, как определять содержание и пространственное распределение ЖК в источнике липидов, которым он хочет использовать, согласно стандартным методам, включая приведенные выше (Beggio et al.; Nagy K., et al.), которые заявитель применял при определении величин, приведенных в таблицах 1 и 2.
Липиды в питательной композиции в соответствии с определенными вариантами осуществления изобретения могут быть в форме смеси масел, к которой относятся смесь растительных жиров и масел, и/или молочных жиров и/или животных жиров, содержащих ТАГ. Эти ТАГ содержат эфиры стеариновой кислоты (СК), пальмитиновой кислоты (ПК) и миристиновой кислоты (МК). Смесь масел может представлять собой смесь из одного или более растительных масел и жиров, например, рапсового масла, подсолнечного масла, подсолнечного масла с высоким содержанием олеиновой кислоты, кокосового масла, соевого масла, масла канолы, сафлорового масла, сафлорового масла с высоким содержанием олеиновой кислоты, кукурузного масла и масла, содержащего длинноцепочечные полиненасыщенные жирные кислоты (ДЦ-ПНЖК), такие как масла из определенных микроводорослей и грибков, включая Mortierella alpina, рыбий жир, молочный жир, животный жир и фракции животного жира. Смесь масел также может содержать другие растительные масла и жиры, подходящие для питания для младенцев.
Таблица 3. Интервалы содержания типичных растительных масел и молочного жира, пригодные для питательных композиций в соответствии с изобретением
на 100 ккал
на 100 ккал
на 100 ккал
Подсолнечное масло с высоким содержанием
олеиновой кислоты*
41,9–51,3%
42,1–51,5%
39,2–48%
Масло, содержащее ДЦ-ПНЖК (например,
масло Mortierella Alpina)*
0,45–0,55%
0,99–1,2%
* % от суммарной массы липидов
В таблице 3 выше показано несколько примеров интервалов содержания различных растительных масел, которые можно применять при составлении смеси масел в питательных композициях в соответствии с вариантами осуществления изобретения. Эти величины основаны на средних значениях составов масел, приведенных в таблицах 1 и 2. В композициях настоящего изобретения в качестве липидных компонентов можно применять другие растительные масла и/или молочные жиры и/или животные жиры, в дополнение к или вместо источников липидов, приведенных в таблице 3. Содержание ПК, СК и МК sn-1(3) в таких других источниках липидов должно быть известным. Если оно неизвестно, то его можно определить в соответствии со способами, известными специалисту в данной области и описанными выше. Сумма ПК, СК и МК sn-1(3), по существу, составляет менее 13% (мас. %/мас.%) от ТАГ.
Отдельные значения из таблицы 3 в каждом из масел могут независимо варьироваться, если сумма эфиров ПК, МК и СК sn-1(3) составляет менее 13% (мас.%/мас.%) от ТАГ.
В соответствии с одним вариантом осуществления изобретения липиды в питательных композициях могут содержать от 17,3 до 21,1%, предпочтительно от 18,0 до 20,0%, например 19,2% рапсового масла, от 11,5 до 14,1%, предпочтительно от 12,0 до 13,5%, например 12,8% подсолнечного масла, от 41,9 до 51,3%, предпочтительно от 43,0 до 48,0%, например 46,6% подсолнечного масла с высоким содержанием олеиновой кислоты, и от 18,0 до 22,0%, предпочтительно от 19,0 до 21,0%, например 20,0% кокосового масла.
В соответствии с еще одним вариантом осуществления изобретения липиды в питательных композициях могут содержать от 16,9 до 20,7%, предпочтительно от 17,5 до 19,0%, например 18,8% рапсового масла, от 11,3 до 13,9%, предпочтительно от 12,0 до 13,5%, например 12,6% подсолнечного масла, от 42,1 до 51,5%, предпочтительно от 45,0 до 49,0%, например 46,6% подсолнечного масла с высоким содержанием олеиновой кислоты, и от 17,5 до 21,5%, предпочтительно от 18,0 до 20,0%, например 19,5% кокосового масла.
В соответствии с еще одним вариантом осуществления изобретения липиды в питательных композициях могут содержать от 23,9 до 29,3%, предпочтительно от 25,0 до 28,0%, например 26,6% молочного жира, от 15,8 до 19,4%, предпочтительно от 16,5 до 18,0%, например 17,6% рапсового масла, от 8,2 до 10,0%, предпочтительно от 8,8 до 9,5%, например 9,1% подсолнечного масла, и от 39,2 до 48,0%, предпочтительно от 42,0 до 46,0%, например 43,6% подсолнечного масла с высоким содержанием олеиновой кислоты.
В отношении этих вариантов осуществления или любых других вариантов осуществления изобретения в смесь липидов, например, содержащую докозагексаеновую кислоту (22 : 6 n-3, DHA), и/или арахидоновую кислоту, (20 : 4 n-6, ARA), и/или эйкозапентаеновую кислоту (20 : 5 n-3, EPA), также можно включать ДЦ-ПНЖК. ARA, по существу, можно добавлять в количестве до 2,0% от общего содержания жиров. DHA, по существу, можно добавлять в количестве до 1,0% от общего содержания жиров. Если в жировую смесь включена EPA, то она, по существу, не превышает количества DHA.
В отношении описанных выше вариантов осуществления изобретения специалисту понятно, что липиды в питательной композиции предпочтительно не включают дополнительного источника ТАГ sn-1(3). В противном случае количества дополнительной ПК, СК или МК sn-1(3) в ТАГ таковы, что общая сумма ПК, СК или МК sn-1(3) в питательной композиции составляет менее 13,0% от ТАГ.
По предварительным результатам исследования переваривания in vitro (способ описан в примере 1) заявитель определил, что ДС, содержащие липиды с суммой МК, ПК и СК sn-1(3) ниже 13,0% (мас.%/мас.%), значительно повышают биодоступность Ca и жирных кислот по сравнению с ДС, содержащими бóльшие количества этих ДЦ-НЖК sn-1(3). Начальные результаты свидетельствуют о том, что после переваривания в системе in vitro в водной фазе продукта переваривания обнаруживается значительно больше кальция, если переваренная ДС содержит смесь липидов в соответствии с изобретением, по сравнению со стандартной детской смесью, в которой сумма остатков ПК, МК и СК sn-1(3) превышает 13,0% (мас.%/мас.%) от ТАГ (т.е. 23,6 мас.%/мас.%).
Следовательно, количество образованного кальциевого мыла уменьшается относительно такового, образованного с бóльшими количествами этих НЖК sn-1(3). Питательные композиции, содержащие липиды, в которых сумма МК, ПК и СК sn-1(3) составляет менее 13,0% (мас.%/мас.%), могут уменьшать пищеварительный дискомфорт и/или боли, и/или уменьшать боли в животе, и/или уменьшать риск запора у младенцев или детей младшего возраста.
В одном варианте осуществления изобретения питательная композиция содержит липиды, в которых ПК, СК и МК представлены в форме ТАГ, причем сумма (общее количество) остатков ПК, МК и СК sn-1(3) составляет менее 13,0% (мас.%/мас.%) от ТАГ. Эти питательные композиции особенно эффективны для уменьшения твердости стула у младенцев или детей младшего возраста. В частности, в соответствии с одним вариантом осуществления изобретения у младенцев в возрасте до приблизительно 6 месяцев композиции обеспечивают смягчение консистенции стула и приближают ее к таковой у младенцев ВГ. В соответствии с одним вариантом осуществления изобретения при употреблении композиций в соответствии с вариантами осуществления изобретения у младенцев, в частности, младенцев старше 6 месяцев, а также у детей младшего возраста достигается снижение частоты и тяжести запоров.
Таким образом, один аспект изобретения относится к питательной композиции для младенцев или детей младшего возраста, содержащей белки, углеводы и липиды, причем липиды содержат ПК, СК и МК в виде ТАГ, при этом сумма ПК, МК и СК sn-1(3) составляет менее 13,0% (мас.%/мас.%) от ТАГ, для применения с целью уменьшения пищеварительного дискомфорта и/или болей, и/или уменьшения болей в животе, и/или уменьшения риска запора у младенцев или детей младшего возраста. Конкретно, указанное уменьшение пищеварительного дискомфорта и/или болей, и/или уменьшение болей в животе, и/или уменьшение риска запора у младенцев или детей младшего возраста содержит уменьшение твердости стула, предпочтительно так, чтобы консистенция стула приближалась к таковой у младенцев ВГ или детей младшего возраста с нормальным характером дефекации. Липиды могут содержать растительные масла, и/или животные жиры, и/или молоко животного.
Твердость стула можно измерять с помощью параметров, которые известны специалисту в данной области. Пищеварительный дискомфорт и боли в животе можно измерять путем измерения, например, интенсивности и частоты криков и беспокойства младенца, измерения снижения аппетита, пальпацией живота и другими стандартными методами. Дети младшего возраста способны сообщать об уровнях пищеварительного дискомфорта и боли в животе.
Уменьшение риска запора можно измерять путем наблюдения за частотой дефекации у младенца или ребенка младшего возраста.
В исследованиях пищеварения in vitro заявитель доказал, что при введении детских смесей в соответствии с изобретением повышается биодоступность кальция.
Таким образом, эти питательные композиции особенно эффективны для увеличения всасывания кальция, минерализации костей и/или увеличения минеральной плотности костей у младенцев или детей младшего возраста.
В дополнительном аспекте настоящее изобретение относится к питательной композиции для младенцев или детей младшего возраста, содержащей белки, углеводы и липиды, причем липиды содержат ПК, СК и МК в виде ТАГ, а сумма эфиров ПК, МК и СК sn-1(3) составляет менее 13,0% (мас.%/мас.%) от ТАГ, для применения с целью увеличения минерализации костей, увеличения прочности костей и/или увеличения минеральной плотности костей.
Питательные композиции в соответствии с вариантами осуществления изобретения особенно эффективны для повышения всасывания жирных кислот у младенцев и детей младшего возраста. Эти жирные кислоты представляют собой МК, СК и ПК, но также могут включать другие ЖК.
В дополнительном аспекте настоящее изобретение относится к питательной композиции для младенцев или детей младшего возраста, содержащей белки, углеводы и липиды, причем липиды содержат ПК, СК и МК в форме триацилглицерина, а сумма остатков ПК, МК и СК sn-1(3) составляет менее 13,0% (мас.%/мас.) от ТАГ, для применения с целью обеспечения нормального роста младенцев или детей младшего возраста.
ДЦ-ПНЖК
В липидную смесь композиции можно включать одну или более незаменимых длинноцепочечных полиненасыщенных жирных кислот (ДЦ-ПНЖК). Примерами ДЦ-ПНЖК, которые можно добавлять, служат докозагексаеновая кислота (DHA), арахидоновая кислота (ARA) и эйкозапентаеновая кислота (EPA). ДЦ-ПНЖК можно добавлять в таких концентрациях, которые составляют более 0,01% общего количества ЖК, присутствующих в композиции. Таким образом, содержащие ДЦ-ПНЖК масла можно добавлять в количестве приблизительно 0,2–2% от общего количества липидов в композиции.
Белки
Питательные композиции настоящего изобретения могут содержать источник белка в количестве не более 4,0, 3,0 или 2,1 г/100 ккал, предпочтительно от 1,6 до 3 г/100 ккал, наиболее предпочтительно от 1,8 до 2,1 г/100 ккал. В одном варианте осуществления источник белка в питательной композиции представлен в количестве от 3,0 до 4,0 г/100 ккал или менее 3,0 г/100 ккал. В одном варианте осуществления источник белка в питательной композиции представлен в количестве по меньшей мере 1,6 г/100 ккал или по меньшей мере 1,8 г/100 ккал. Предпочтительно верхний предел количества составляет менее 2,1 г/100 ккал. Верхний предел 2,1 г/100 килокалорий служит для поддержания желаемого влияния питательной композиции на твердость стула путем модуляции кишечной микробиоты. Минимальное количество — это количество, необходимое для достаточного обеспечения организма белками для роста и развития, например, по меньшей мере 1,6 г/100 ккал, по меньшей мере 1,8 г/100 ккал или по меньшей мере 2 г/100 ккал. Тип белка не считается критическим для настоящего изобретения, при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечивается удовлетворительной рост. Предпочтительно, чтобы молочная сыворотка составляла более 50% от массы источника белка. В одном варианте осуществления содержание белка составляет от 30 до 80% сывороточных белков. Таким образом, можно применять источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается сывороточных белков, источник белка может быть основан на кислой сыворотке или сладкой молочной сыворотке или на их смесях и может включать альфа-лактальбумин и бета-лактоглобулин в любых желаемых соотношениях.
В одном варианте осуществления изобретения питательная композиция содержит белки, которые представляют собой смесь сывороточного белка и казеина, причем пропорция сывороточного белка и казеина составляет от 50 : 50 до 80 : 20, предпочтительно 60 : 40.
В одном варианте осуществления изобретения питательная композиция содержит белки, которые представляют собой смесь сывороточного белка и казеина, причем пропорция сывороточного белка и казеина составляет от 20 : 80 до 40 : 60, предпочтительно 35 : 65.
В одном варианте осуществления изобретения питательная композиция содержит белок в форме 100% сывороточного белка. Этот вариант осуществления преимущественно подходит для гидролизованных белков.
По существу, белки могут быть интактными или гидролизованными или могут представлять собой смесь интактных и гидролизованных белков. Может быть желательно вводить частично гидролизованные белки (степень гидролиза от 2 до 20%), например, младенцам, предположительно подверженным риску развития аллергии на коровье молоко. Если используются гидролизованные белки, то процесс гидролиза можно проводить по желанию и так, как известно в данной области. Например, гидролизат сывороточного белка можно получать ферментативным гидролизом фракции молочной сыворотки на одной или более стадий. Если фракция молочной сыворотки, применяемая в качестве исходного материала, по существу, не содержит лактозы, то установлено, что в процессе гидролиза блокировка лизина белка проявляется в гораздо меньшей степени. Это позволяет снизить степень блокировки лизина с приблизительно 15 мас.% общего лизина до менее приблизительно 10 мас.% лизина; например приблизительно 7 мас.% лизина, что значительно улучшает питательное качество источника белка.
В одном предпочтительном варианте осуществления в питательные композиции настоящего изобретения можно включать пробиотики. Примеры известных композиций пробиотиков представляют собой Bacillus, Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Saccharomyces, Kluyveromyces, Candida, Streptococcus, in particular selected from the group consisting of Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacilluslactis, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactococcus lactis, Streptococcus thermophilus, Enterococcusfaecium, Saccharomyces cerevisiae, Saccharomyces boulardii, E. Coli Nissle. В частности, пробиотики и пробиотики, содержащие неразмножающийся штамм, такие как род Lactobacillus, Bifidobacterium или их комбинация, например Lactobacillus johnsonii, Lactobacillus paracasei, Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium breve или их комбинация, и применения этих бактерий.
Углеводы
Лактоза может составлять, по существу, 100% от содержания углеводов. Можно также добавлять и другие углеводы, такие как сахароза, мальтодекстрин и крахмал. Однако в одном предпочтительном варианте осуществления в питательную композицию изобретения можно включать углеводы, которые предпочтительно действуют как пребиотики. Например, пребиотики предпочтительно выбраны из 2’-фукозиллактозы, лактодифукотетрозы, 3’-фукозиллактозы, лакто-N-фукопентозы I, лакто-N-фукопентозы II, лакто-N-фукопентозы III, лакто-N-неотетрозы, лакто-N-тетрозы, 3’-сиалиллактозы, 6’-сиалиллактозы, 3’-сиалиллакто-N-тетрозы, 6’-сиалиллакто-N-неотетрозы, инулина, фруктоолигосахаридов (FOS), короткоцепочечного фруктоолигосахарида (короткоцепочечного FOS), галактоолигосахаридов (GOS), ксилоолигосахаридов (XOS), ганглиозидов, частично гидролизованной камеди гуара, гуммиарабика, камеди соевых бобов, рожкового дерева (камеди рожкового дерева) или их смесей.
Углевод или углеводы могут присутствовать в суточных дозах композиции в количестве от приблизительно 1 до 20 г, или от 1 до 80%, или от 20 до 60%. Альтернативно углеводы составляют от 10 до 80% сухой композиции, например, в количестве от 9 до 14 г/100 ккал.
В предпочтительных вариантах осуществления лактоза составляет более 90%, более 95% или, в самых предпочтительных вариантах осуществления, более 98% или более 99% от содержания углеводов в композиции.
В одном варианте осуществления питательная композиция содержит смесь олигосахаридов в соответствии с публикацией WO2007/090894 (общие положения и особенно пример 1). В частности, ее можно применять в комбинации с GOS. Базовая смесь может обеспечивать смесь олигосахаридов, содержащую 5–70 мас.% по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; 20–90 мас.% по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc; и 5–50 мас.% по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, состоящей из NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc.
К питательной композиции можно добавлять другие компоненты, такие как витамины и минеральные вещества.
При необходимости композиция настоящего изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т.п.
Композиция может также содержать другие вещества, которые могут оказывать благоприятное воздействие, такие как лактоферрин, нуклеотиды, нуклеозиды, ганглиозиды, полиамины и т.п.
Формы питательных композиций для младенцев и детей младшего возраста
В соответствии с одним вариантом осуществления изобретения питательная композиция представляет собой детскую смесь.
Детская смесь в соответствии с настоящим изобретением может представлять собой начальную смесь для младенцев от рождения до 4–6 месяцев и обеспечивает полноценное питание для этой возрастной группы (как для доношенных, так и для недоношенных младенцев). Кроме того, детская смесь может представлять собой смесь для прикармливаемых младенцев в возрасте в диапазоне от четырех до шести месяцев и двенадцати месяцев, которую дают младенцу в сочетании с возрастающими количествами продуктов, таких как детские каши и пюре из фруктов, овощей и других продуктов питания по мере отлучения младенца от груди.
В соответствии с одним вариантом осуществления изобретения питательная композиция представляет собой молочную смесь для детей от 1 до 3 лет.
Детская смесь может также содержать все витамины и минеральные вещества, которые считаются обязательными в ежедневной диете, в значимых с точки зрения питания количествах. Для некоторых витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, присутствующих в питательной композиции, включают в себя витамин А, витамин В1, витамин В2, витамин В6, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозитол, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлорид, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме соли.
В соответствии с еще одним вариантом осуществления изобретения питательная композиция представляет собой обогатитель или добавку к человеческому грудному молоку или к детской смеси, либо композиция представляет собой композицию для применения в составлении детской смеси.
Питательные композиции изобретения могут быть в текучей (жидкой) форме. Они могут продаваться готовыми к употреблению (без дополнительного разбавления).
Продукты изобретения могут быть в форме дегидратированных порошков, которые готовят к употреблению растворением в воде или молоке.
Приготовление питательных композиций
Питательные композиции в соответствии с настоящим изобретением можно приготовить любым известным или другим подходящим способом. Например, детскую смесь можно получать путем смешивания источника белков, источника углеводов и источника липидов в соответствующих пропорциях. На данной стадии можно добавлять эмульгаторы, если они используются. Витамины и минеральные вещества можно добавлять на этой стадии, но также можно добавлять и позднее, чтобы избежать термического разложения. Затем можно добавлять и примешивать воду, предпочтительно воду, очищенную обратным осмосом, или деионизированную воду для образования жидкой смеси. Температура смешивания предпочтительно должна быть комнатной, но также может быть выше. Затем жидкую смесь можно подвергать термической обработке для снижения бактериальных нагрузок. Затем смесь можно гомогенизировать.
Для получения порошковой композиции гомогенизированную смесь высушивают в подходящем сушильном аппарате, таком как распылительная сушилка или сублимационная сушилка, и превращают в порошок.
Способы, применяемые в производстве смесей для младенцев и детей младшего возраста, основаны на представлении о том, что продукты должны иметь необходимые питательные характеристики и быть микробиологически безопасными для употребления. Таким образом, ключевое значение в способах производства имеют стадии, которые устраняют или ограничивают рост микроорганизмов. Технология производства каждой конкретной смеси патентуется производителем, но в общем случае она включает консервирование эмульсии типа «масло в воде» путем дегидратации в случае порошковых продуктов или путем стерилизации в случае готовых к употреблению или концентрированных жидких продуктов. Порошковую детскую смесь можно производить с применением различных способов, таких как сухое смешивание дегидратированных ингредиентов для получения однородной смеси или гидратация и мокрое смешивание смеси макроингредиентов, таких как жировые, белковые и углеводные ингредиенты, с последующим выпариванием и распылительной сушкой полученной смеси. Можно применять комбинацию двух описанных выше способов, когда сначала получают основу порошка путем мокрого смешивания и распылительной сушки всех или некоторых из макроингредиентов, а затем путем сухого смешивания добавляют остальные ингредиенты, включая углеводы, минеральные вещества, витамины и другие питательные микроэлементы, для создания готовой смеси. Жидкие смеси доступны в готовом к употреблению формате или в виде жидкого концентрата, который необходимо разбавлять водой, обычно в соотношении 1: 1. Для производства этих продуктов применяются такие же способы, как и для производства рекомбинированного молока.
Если необходимо получить жидкую детскую смесь, гомогенизированную смесь разливают в подходящие контейнеры, предпочтительно асептическим способом. Однако жидкую композицию можно также стерилизовать в контейнере, подходящий аппарат для разливания и стерилизации такого типа доступен в продаже.
Изобретение дополнительно описано со ссылкой на следующие примеры. Следует понимать, что изобретение в заявленном виде не будет каким-либо образом ограничено этими примерами.
Пример 1
Анализ переваривания in vitro
Анализом переваривания детских смесей (ДС) in vitro измеряли биодоступность кальция в смесях. Данный метод основан на методе, описанном в Perales et al., Bioavailability of Calcium from Milk-Based Formulas and Fruit Juices Containing Milk and Cereals Estimated by in Vitro Methods (Solubility, Dialyzability, and Uptake and Transport by Caco-2 Cells), J. Agric. Food Chem. 2005, 53, 3721–3726 3721) с некоторыми адаптациями.
Данный анализ моделирует две стадии пищеварения у младенцев, которые включают фазы пищеварения в желудке и кишечнике в микросреде, сходной с таковой у младенцев. После переваривания пепсином, желудочной липазой, панкреатином и экстрактом желчи в анализе на растворимость определяли растворимость/нерастворимость кальция в детских смесях. В методе, который применял заявитель, на желудочной и кишечной фазах устанавливали pH 5,5 и 6,5 соответственно. Применяли следующие концентрации ферментов: желудочная липаза (18 Ед/мл), пепсин (450 Ед/мл), панкреатин (30,9 мг/мл), экстракт желчи (2 мМ). Диализ не проводили.
Центрифугировали кишечные гидролизаты с получением жировой фазы, водной фазы и осадка. Содержание кальция оценивали в каждой из этих фаз. Определяли общее содержание кальция в ДС и растворимого кальция (находящегося в водной и жировой фазах). По этим данным определяли растворимость/нерастворимость кальция из детских смесей.
Результаты показали, что количество кальция в осадке (т.е. кальция в форме нерастворимого мыла) было значительно ниже в смесях, содержащих меньшие количества насыщенных жирных кислот ПК, МК и СК sn-1(3), по сравнению со смесями, содержащими бóльшие количества ПК, МК и СК sn-1(3). Эти исследования доказывают, что при переваривании ДС, содержащих ПК, МК и СК sn-1(3) в предписанных интервалах в соответствии с настоящим изобретением меньше кальция осаждается в виде мыла и, следовательно, больше кальция растворяется и доступно для всасывания по сравнению со стандартными детскими смесями, содержащими бóльшие количества ПК, МК и СК sn-1(3).
Ниже представлен стандартный состав стандартной ДС.
Таблица 1. Состав растительного масла в стандартной ДС
Подсолнечное масло*
10,7%
Масло, содержащее ДЦ-ПНЖК (например, масло Mortierella Alpina)*
0,5%
* % от суммарной массы липидов
Пример 2. Жировые смеси в питательных композициях для младенцев и детей младшего возраста
Таблица 1. Три примера смесей липидов, иллюстрирующие изобретение
на 100 ккал
на 100 ккал
на 100 ккал
18,8%
12,6%
46,8%
19,5%
2,3%
-
17,6%
9,1%
43,6%
-
2%
1,1%
Подсолнечное масло с высоким содержанием
олеиновой кислоты*
46,6%
Масло, содержащее ДЦ-ПНЖК (например,
масло Mortierella Alpina)*
0,5%
* % от суммарной массы липидов
Таблица 2. Состав жирных кислот (ПК, МК и СК) в смесях 1–3. Состав жирных кислот и сумму НЖК sn-1(3) в каждой смеси рассчитывали на основании среднего состава от 1 до 21 образца жира из разных мест в мире
глицеринов)
Пример 3
Составы детских смесей
Пример 4
Материалы и методы
Применяемая модель липолиза in vitro предназначена для имитации биохимии здоровых, доношенных младенцев. Вкратце, модель in vitro состояла из двух стадий липолиза с желудочным и кишечным перевариванием. На желудочной стадии детскую смесь переваривали в среде, содержащей NaCl, трис, малеиновую кислоту и фосфолипиды яйца при pH 5,5 в течение 15 мин при 37°C. Затем к желудочной среде добавляли липазу желудка кролика (18 Ед/мл) и пепсин (450 Ед/мл), инкубировали в течение 60 мин при 37°C. Перед стадией кишечного переваривания pH желудочного гидролизата поднимали до pH 6,5, а затем добавляли кишечную среду, содержащую смесь желчной соли (2 мМ), фосфолипиды яйца, NaCl, трис и малеиновую кислоту, инкубировали при 37°C в течение 15 мин. Затем к кишечной среде добавляли панкреатин (30,9 мг/мл) и инкубировали в течение 90 мин при 37°C. Для остановки кишечного переваривания пробы помещали на лед по меньшей мере на 10 мин, чтобы остановить процесс переваривания (активность ферментов). Пробы гидролизатов затем центрифугировали при 13 500 g в течение 30 мин при 4°C. Собирали жировую фазу, супернатант (водную фазу) и осадок и определяли содержание кальция методом пламенной атомно-абсорбционной спектрометрии в каждой фазе, а также в детской смеси перед перевариванием. Содержание кальция в жировой фазе и в жидкой фазе соответствует растворимому кальцию, тогда как содержание кальция в фазе осадка соответствует нерастворимому кальцию, осажденному как нерастворимые мыла жирных кислот.
Результаты
На фиг. 1 представлено перераспределение нерастворимого и растворимого кальция в разных детских смесях после двух стадий липолиза детских смесей в условиях, имитирующих биохимию здоровых, доношенных младенцев. Нерастворимость/растворимость кальция во всех детских смесях испытывали в тройной повторности. Нерастворимый кальций — это кальций, определяемый во фракции осадка в форме мыла, тогда как растворимый кальций — это кальций, который определяется как в водной, так и жировой фракциях после 2 стадий переваривания (желудочной и кишечной). Результаты выражены в % от общего кальция и представляют средние значения по 3 пробам каждой детской смеси. Извлечение кальция из переваренных детских смесей составляет 99–100%.
Результаты показывают, что нерастворимость/растворимость кальция различается в разных детских смесях, содержащих разные количества ДЦ-НЖК sn-1,3 (которые также ниже показаны в таблице 3). В контрольной детской смеси, содержащей 24,7% ДЦ-НЖК sn-1,3 в виде ТАГ, после переваривания 44,3% кальция находилось в нерастворимой форме, тогда как 56,6% от общего кальция находилось в растворимой форме. Напротив, в детской смеси в соответствии с изобретением (содержащей жировую смесь 2, как описано в примере 2) с количеством ДЦ-НЖК sn-1,3 ≈ 9% от ТАГ растворимость кальция была самой высокой, при всего 16% от общего содержания кальция, извлеченного из осадка (нерастворимый кальций), по сравнению с контрольной детской смесью (ДЦ-НЖК sn-1,3 ≈ 25% от ТАГ) (83% по сравнению с 56,6% от общего кальция). Аналогично растворимость кальция была самой высокой в детской смеси в соответствии с изобретением (содержащей жировую смесь 3, как описано в примере 2), содержащей ≈ 11% ДЦ-НЖК sn-1,3 (% от ТАГ), по сравнению с контрольной детской смесью (84% по сравнению с 56,6% от общего кальция). Из осадка извлекалось только 16,5% от общего кальция.
Таблица 3
глицеринов)
В совокупности результаты изобретения показывают, что растворимость кальция была самой высокой в детской смеси, содержащей небольшое количество ДЦ-НЖК sn-1,3 по сравнению с контрольной детской смесью. Результаты растворимости изобретения хорошо согласуются с концепцией, представленной в настоящем документе.

Изобретение относится к питательной композиции для младенцев и детей младшего возраста. Питательная композиция для младенцев или детей младшего возраста содержит белки, углеводы и липиды, причем указанные липиды содержат триацилглицерины (ТАГ) жирных кислот (ЖК), причем указанные ТАГ жирных кислот содержат стеариновые, пальмитиновые и миристиновые эфиры. При этом суммарное количество стеариновых, пальмитиновых и миристиновых эфиров в положении sn-1(3) в ТАГ составляет менее 13,0% (мас.%/мас.%) от ТАГ, а миристиновая кислота составляет до 3,6% от всех ЖК, пальмитиновая кислота составляет до 11,1% от всех ЖК, стеариновая кислота составляет до 4,6% от всех ЖК (мас.%/мас.%). Причем липиды содержат смесь масел, выбранную из: а) от 17,3 до 21,1 % рапсового масла, от 11,5 до 14,1 % подсолнечного масла, от 41,9 до 51,3 % подсолнечного масла с высоким содержанием олеиновой кислоты и от 18,0 до 22,0 % кокосового масла; b) от 16,9 до 20,7 % рапсового масла, от 11,3 до 13,9 % подсолнечного масла, от 42,1 до 51,5 % подсолнечного масла с высоким содержанием олеиновой кислоты и от 17,5 до 21,5 % кокосового масла или с) от 23,9 до 29,3 % молочного жира, от 15,8 до 19,4 % рапсового масла, от 8,2 до 10,0 % подсолнечного масла, от 39,2 до 48,0 % подсолнечного масла с высоким содержанием олеиновой кислоты. Изобретение позволяет получить композицию для улучшения гомеостаза кальция и всасывания кальция и липидов, увеличения удерживания кальция и липидов и/или уменьшения образования мыла с пальмитиновой кислотой, или стеариновой кислотой, или миристиновой кислотой у младенцев или детей младшего возраста. Композиция также используется для увеличения минерализации костей, увеличения прочности костей и/или увеличения минеральной плотности костей у младенцев или детей младшего возраста. 2 н. и 10 з.п. ф-лы, 1 ил., 7 табл., 4 пр.
1. Питательная композиция для младенцев или детей младшего возраста, содержащая белки, углеводы и липиды, причем указанные липиды содержат триацилглицерины (ТАГ) жирных кислот (ЖК), причем указанные ТАГ жирных кислот содержат стеариновые, пальмитиновые и миристиновые эфиры, при этом суммарное количество стеариновых, пальмитиновых и миристиновых эфиров в положении sn-1(3) в ТАГ составляет менее 13,0% (мас.%/мас.%) от ТАГ, а миристиновая кислота составляет до 3,6% от всех ЖК, пальмитиновая кислота составляет до 11,1% от всех ЖК, стеариновая кислота составляет до 4,6% от всех ЖК (мас.%/мас.%), причем липиды содержат смесь масел, выбранную из:
а) от 17,3 до 21,1 % рапсового масла, от 11,5 до 14,1 % подсолнечного масла, от 41,9 до 51,3 % подсолнечного масла с высоким содержанием олеиновой кислоты и от 18,0 до 22,0 % кокосового масла;
b) от 16,9 до 20,7 % рапсового масла, от 11,3 до 13,9 % подсолнечного масла, от 42,1 до 51,5 % подсолнечного масла с высоким содержанием олеиновой кислоты и от 17,5 до 21,5 % кокосового масла или
с) от 23,9 до 29,3 % молочного жира, от 15,8 до 19,4 % рапсового масла, от 8,2 до 10,0 % подсолнечного масла, от 39,2 до 48,0 % подсолнечного масла с высоким содержанием олеиновой кислоты,
и при этом младенец является ребенком в возрасте до 12 месяцев, а ребенок младшего возраста является ребенком в возрасте от 12 месяцев до 3 лет.
2. Композиция по п. 1, в которой общая сумма пальмитиновых, миристиновых и стеариновых эфиров в ТАГ составляет менее 19,3% (мас.%/мас.%) от общего содержания ТАГ жирных кислот.
3. Композиция по п. 1 или 2, в которой указанные углеводы состоят из лактозы на от 99 до 100%.
4. Композиция по любому из пп. 1–3, в которой количество указанного белка менее или равно 3,0 или 2,1 г белка/100 ккал композиции, предпочтительно менее или равно 1,9 г белка/100 ккал, более предпочтительно менее или равно 1,8 г белка/100 ккал, а наиболее предпочтительно менее или равно 1,7 г белка/100 ккал.
5. Композиция по любому из пп. 1–3, в которой количество указанного белка менее или равно 2,1 г белка/100 ккал композиции, предпочтительно менее или равно 1,9 г белка/100 ккал, более предпочтительно менее или равно 1,8 г белка/100 ккал, а наиболее предпочтительно менее или равно 1,7 г белка/100 ккал.
6. Композиция по п. 4 или 5, в которой белок представляет собой смесь сывороточного белка и казеина, причем пропорция сывороточного белка и казеина составляет от 50:50 до 80:20.
7. Композиция по п. 4, 5 или 6, в которой белок частично гидролизован.
8. Композиция по любому из пп. 1–7, которая также содержит по меньшей мере один пребиотик, предпочтительно выбранный из 2’-фукозиллактозы, лактодифукотетрозы, 3’-фукозиллактозы, лакто-N-фукопентозы I, лакто-N-фукопентозы II, лакто-N-фукопентозы III, лакто-N-неотетрозы, лакто-N-тетрозы, 3’-сиалиллактозы, 6’-сиалиллактозы, 3’-сиалиллакто-N-тетрозы, 6’-сиалиллакто-N-неотетрозы, инулина, фруктоолигосахарида (FOS), короткоцепочечного фруктоолигосахарида (короткоцепочечного FOS), галактоолигосахарида (GOS), ксилоолигосахарида (XOS), ганглиозида, частично гидролизованной камеди гуара, гуммиарабика, камеди соевых бобов или их смесей.
9. Композиция по любому из пп. 1–8, которая также содержит пробиотики, предпочтительно выбранные из Lactobacillus paracasei, Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium lactis и Bifidobacterium breve, Bifidobacterium animalis, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus reuteri, Lactobacillus johnsonii, Lactobacillus plantarum, Lactococcus lactis, Streptococcus thermophilus, Enterococcusfaecium, Saccharomyces cerevisiae, Saccharomyces boulardii и E. Coli Nissle, в частности, пробиотики и пробиотики, содержащие неразмножающийся штамм, такие как род Lactobacillus, Bifidobacterium или их комбинацию, например, Lactobacillus johnsonii, Lactobacillus paracasei, Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium breve или их комбинацию и/или нежизнеспособные фракции этих бактерий.
10. Композиция по любому из пп. 1–9, в которой липиды содержат докозагексаеновую кислоту (DHA), и/или арахидоновую кислоту (ARA), и/или эйкозапентаеновую кислоту (EPA).
11. Композиция по любому из пп. 1–10 для применения в уменьшении пищеварительного дискомфорта, и/или уменьшении болей в животе, и/или уменьшении частоты и/или тяжести колик, и/или уменьшении частоты и/или тяжести запора у младенцев или детей младшего возраста, причем указанное уменьшение пищеварительного дискомфорта, и/или уменьшение болей в животе, и/или уменьшение частоты и/или тяжести колик, и/или уменьшение частоты и/или тяжести запора содержит уменьшение твердости стула предпочтительно до приближения консистенции стула к таковой у младенцев на грудном вскармливании или у детей младшего возраста с нормальным характером дефекации, при этом младенец является ребенком в возрасте до 12 месяцев, а ребенок младшего возраста является ребенком в возрасте от 12 месяцев до 3 лет.
12. Применение композиции по любому из пп. 1–10 для улучшения гомеостаза кальция и всасывания кальция и липидов, увеличения удерживания кальция и липидов и/или уменьшения образования мыла с пальмитиновой кислотой, или стеариновой кислотой, или миристиновой кислотой у младенцев или детей младшего возраста, причем указанная композиция используется для увеличения минерализации костей, увеличения прочности костей и/или увеличения минеральной плотности костей у младенцев или детей младшего возраста, при этом младенец является ребенком в возрасте до 12 месяцев, а ребенок младшего возраста является ребенком в возрасте от 12 месяцев до 3 лет.
| US 5601860 A1, 11.02.1997 | |||
| WO 2016050754 A1, 07.04.2016 | |||
| YU ZHANG-BIN ET AL: "Effects of infant formula containing palm oil on the nutrient absorption and defecation in infants: a meta-analysis", ZHONGHUA ER KE ZA ZHI (CHINESE JOURNAL OF PEDIATRICS), vol | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| РУССКАЯ ПЕЧЬ С ПЛИТОЙ И ДЫМООБОРОТАМИ | 1923 |
|
SU904A1 |
| US 20030026860 A1, 06.02.2003 | |||
| US | |||
Авторы
Даты
2021-06-16—Публикация
2017-07-28—Подача