Предпосылки создания изобретения
Настоящее изобретение, по существу, относится к области здоровья нервной системы, защиты нервной системы и развития нервной системы. В частности, изобретение относится к композиции для применения в поддержании нейронального развития, в частности улучшения, усиления, стимуляции или модуляции функции, относящейся к нейромедиатору – гамма-аминомасляной кислоте (ГАМК) – или влияющей на него в центральной нервной системе (ЦНС) и к другим сопутствующим когнитивным преимуществам, в частности у младенцев и детей младшего возраста, предпочтительно в целевой группе (недоношенных или доношенных) младенцев или детей младшего возраста с рождения до 7 лет.
Более конкретно изобретение относится к введению олигосахаридов грудного молока (ОГМ), необязательно в комбинации с дополнительными олигосахаридами-пребиотиками, в частности фруктоолигосахаридами (FOS), или олигофруктозой (OF) и/или олигосахаридами коровьего молока (BMO) для улучшения, усиления, стимуляции или модуляции ГАМКергической функции в ЦНС, в частности фильтрации информации или способности фокусироваться или концентрироваться на умственной или физической активности.
ЦНС, и, в частности, головной мозг, управляет когнитивными функциями. Кора головного мозга, которая представляет собой самый внешний пласт нервной ткани головного мозга млекопитающего, играет ключевую роль во внимании, перцептивном восприятии, высшей когнитивной функции (исполнительной функции) и интеграции информации с афферентных входов.
Развитие и созревание ЦНС представляет собой чрезвычайно сложный биологический феномен, в который вовлечено множество физиологических процессов, включая, например, рост и дифференцировку нейронов и глиальных клеток, нейрональное наведение и ветвление, а также формирование межнейронных взаимодействий (нервных сигналов) посредством роста аксонов и синаптогенеза.
Нейрональная пластичность, определяемая как способность головного мозга к постоянной адаптации функций и структурной организации к изменяющимся требованиям, важна для созревания нервной системы и зрелых функций. Она обязательна для правильного функционирования головного мозга и необходима для процессов познания, обучения и запоминания. В литературе были выявлены и исследованы некоторые из нейрональных маркеров, включая белки и нейротрофические факторы, такие как нейротрофический фактор мозга (BDNF), необходимые для протекания этих физиологических процессов или по меньшей мере участвующие в них [Huang, E. J., Reichardt, L. F. (2001); Neurotrophins: Roles in Neuronal Development and Function, Annu. Rev. Neurosci., 24: 677-736]; [Musumeci, G., Minichiello, L. (2011); BDNF-TrkB signalling in fear learning: from genetics to neural networks, Rev. Neurosci., 22(3):303-15]; [Xiao, J. et al. (2009); The role of neurotrophins in the regulation of myelin development, Neurosignals, 17: 265-276] и [Von Bohlen, Halbach, O. (2011); Immunohistological markers for proliferative events, gliogenesis, and neurogenesis within the adult hippocampus, Cell Tissue Res., 345(1):1-19].
ЦНС начинает развиваться сразу после зачатия, затем во время беременности и продолжает развиваться до раннего взросления. В частности, структурное созревание преимущественно происходит до рождения, в то время как созревание функциональной сети преимущественно происходит после рождения. У эмбрионов человека кора головного мозга развивается достаточно поздно и в течение длительного периода времени.
Во внутриутробном периоде у человека происходит пик созревания и роста нейронов / головного мозга с 30-й недели беременности.
Развитие ГАМКергических функций, включая способность фильтровать информацию, в частности сенсорную информацию, такую как визуальные сигналы, является очень важным этапом в развитии когнитивных функций у млекопитающих, в частности у младенцев и детей младшего возраста. Хотя такое развитие и улучшение ГАМКергических функций имеет особое значение в течение первых месяцев/лет жизни (когда нейрональная пластичность является самой высокой), оно также может влиять на субъектов более старшего возраста, подростков и взрослых, а также пожилых людей или субъектов с заболеваниями.
Преждевременно родившиеся дети по определению появляются на свет с еще недоразвитым мозгом, и они действительно демонстрируют только базовую электрическую активность в первичных сенсорных областях коры головного мозга, то есть в тех зонах, которые отвечают за осязание, зрение и слух, а также в первичных двигательных областях коры головного мозга. У этих детей постнатальное постепенное созревание головного мозга необходимо для компенсации состояния недозрелости головного мозга при рождении, и такое компенсаторное созревание особенно важно для более сложной части головного мозга, которая опосредует большую часть эмоционального, социального и когнитивного созревания в первые несколько лет жизни [Lubsen, J. et al. (2011); Microstructural and functional connectivity in the developing preterm brain, Seminars in Perinatology, 35, 34-43].
Недоношенные дети рождаются в период, очень важный для структурного и функционального развития и созревания головного мозга, и, таким образом, они пропускают стадию внутриутробного развития головного мозга. После рождения они подвержены риску патологических состояний, включая геморрагические и гипокси-ишемические поражения головного мозга, а также риску проблем развития в дальнейшей жизни, включая когнитивные расстройства. Данный риск по всей видимости тем выше, чем более недоношенными рождаются дети и чем меньше их вес при рождении. Когнитивные расстройства, связанные с более низким IQ, пониженным вниманием и кратковременной памятью, а также проблемы с исполнительными функциями могут сохраняться в школьном и подростковом возрасте [Talge, N. et al. (2010). Late-Preterm Birth and its Association with Cognitive and Socioemotional Outcomes at 6 Years of Age. Pediatrics, 126, 1124-1131; van Baar, A., et al. (2009). Functioning at school age of moderately preterm children born at 32 to 36 weeks' gestational age. Pediatrics, 124, 251-257; Farooqi, A et al. (2011). Impact at age 11 years of major neonatal morbidities in children born extremely preterm. Pediatrics, 127, e1247-1257; Nosarti, C. et al. (2010). Neurodevelopmental outcomes of preterm birth. Cambridge: Cambridge University Press].
В целом незрелость ЦНС или замедленное созревание ЦНС может наблюдаться у таких младенцев, как:
недоношенные младенцы, младенцы с низким весом при рождении (<2500 г), с очень низким и крайне низким весом при рождении (<1500 г), с чрезвычайно низким весом при рождении (<1000 г) и младенцы, маленькие для своего гестационного возраста [Allen, M.C. (2008); Neurodevelopmental outcomes of preterm infants, Curr. Opin Neurol., 21(2): 123-8].
Преждевременно родившиеся или доношенные младенцы с задержкой внутриутробного развития (ЗВУР), которая произошла в результате каких-либо неблагоприятных явлений во время беременности (курение матери, прием лекарств матерью, низкое качество плаценты, неправильное расположение плаценты, неправильное питание матери и плода, чрезмерный стресс/тревожность матери и т.д.); [Gregory, A. et al. (2008); Intrauterine Growth Restriction Affects the Preterm Infant’s Hippocampus, Pediatric Research, 63(4): 438–443].
Любой новорожденный ребенок и младенец с задержкой роста нервной системы в результате, например, гипоксемии (ишемии) при родах, постнатальных осложнений, постнатального лечения стероидами или любого другого неблагоприятного явления (см., например, Barrett, R.D. et al. (2007); Destruction and reconstruction: hypoxia and the developing brain, Birth Defects Res. C. Embryo Today, 81: 163-76).
У таких младенцев отмечаются когнитивные дисфункции, а также дисфункция роста и развития, что указывает на недостаточную «компенсацию» процесса развития нервной системы. Незрелость или замедленное созревание коры головного мозга может привести к замедлению и/или нарушению способности к обучению, обобщению информации, обработке афферентных импульсов, потере или недостаточному развитию высших функций мышления, исполнительных функций, концентрации, внимания, моторных навыков и языка. Это может привести к поведенческим проблемам, патологическому снижению интеллекта и, следовательно, патологическому снижению умственной деятельности.
Как правило, отмечали, что грудное вскармливание недоношенных младенцев может приводить к улучшению нейронального развития по сравнению с кормлением смесями. (См., например: Rozé et al. The apparent breastfeeding paradox in very preterm infants: relationship between breast feeding, early weight gain and neurodevelopment based on results from two cohorts, EPIPAGE and LIFT. BMJ Open 2012;2:e000834.)
Было отмечено, что в здоровой популяции грудное вскармливание младенцев может приводить к улучшению когнитивной функции и повышению образовательных способностей во взрослом возрасте по сравнению со вскармливанием смесями. (См., например: Victoria et al. Association between breastfeeding and intelligence, educational attainment, and income at 30 years of age: a prospective birth cohort study from Brazil. Lancet 2015.)
По мнению авторов изобретения, это, как правило, указывает на возможное отсутствие некоторых питательных веществ, присутствующих в человеческом грудном молоке, в традиционной/стандартной искусственной смеси или их доставку в субоптимальном количестве. Существует потребность в выявлении ключевых различий между традиционной смесью и человеческим грудным молоком и в соответствующей адаптации искусственной смеси.
Расстройства поведения и нейронального развития, связанные с замедленным созреванием коры головного мозга, в частности патологические ГАМКергические функции, включают в себя такие расстройства, как синдром дефицита внимания и гиперактивности, расстройства аутического спектра, а также шизофрению.
Когнитивную функцию человека можно измерять с помощью клинических тестов, которые зависят от возраста; педиатрам и специалистам в области развития детей известно множество таких тестов. Для младенцев и детей грудного возраста существуют скрининг-тесты и тесты на развитие нервной системы, такие как, например, шкала развития младенцев Бейли (BSID), шкала оценки поведения новорожденных Бразелтона, оценка нейропсихологического развития (NEPSY) и шкала психического развития Гриффитса. Для детей дошкольного и/или школьного возраста тесты на когнитивные способности включают словарный тест в картинках Пибоди (PPVT), тест на невербальный интеллект 2 (TONI-2), Векслеровскую шкалу интеллекта для дошкольников и младших школьников (WPPSI) и цветные прогрессивные матрицы Равена (CPM).
Известно, что питание играет важную роль в созревании нейронов в головном мозге (обзор Huppi, P.S. (2008); Nutrition for the Brain, Pediatric Research, 63(3): 229-231 и Cusik and Georgieff (2016); The Role of Nutrition in Brain Development: The Golden Opportunity of the “First 1000 Days”, Journal of Pediatrics, 175:16-21).
Последствия неправильного питания могут быть необратимыми и могут включать в себя снижение когнитивного развития, ухудшение памяти и способности к обучению и, следовательно, экономической продуктивности в будущем (см., например, Horton, R; (2008) The Lancet, Vol. 371, Issue 9608, page 179; Laus, M.F. et al. (2011); Early postnatal protein-calorie malnutrition and cognition: a review of human and animal studies, Int. J. Environ. Res. Public Health., 8(2): 590-612).
Хотя известно, что материнское грудное молоко обеспечивает наилучшую питательную поддержку развивающемуся мозгу, если грудное вскармливание невозможно, существует необходимость в обеспечении искусственных питательных композиций (таких как детская смесь или смесь для прикармливаемых детей), которые индуцируют улучшение или активируют развитие оптимальных когнитивных функций.
Таким образом, пероральное введение представляет собой подходящий способ положительного воздействия на развитие нервной системы для обеспечения оптимального развития когнитивной функции, памяти и умственных способностей у недоношенных или доношенных новорожденных детей, младенцев, детей, начинающих ходить, детей старшего или юношеского возраста или молодых животных.
Однако мало известных и достоверных данных о способности питательных диет или питательных композиций влиять на развитие или стимуляцию ГАМКергических функций, и, в частности, у младенцев и детей младшего возраста.
Таким образом, существует потребность в стимулировании и поддержке здорового формирования когнитивной функции в целом и в улучшении, усилении, стимулировании или модулировании ГАМКергической функции в ЦНС, в частности фильтрации информации или способности фокусироваться или концентрироваться на умственной или физической активности.
Существует потребность в предотвращении, профилактике или компенсации синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении, особенно у нуждающихся в этом субъектов, и в особенности путем активации или модуляции ГАМКергических функций в ЦНС.
Существует потребность в стимуляции развития или улучшении таких функций у субъектов младшего возраста, в частности у младенцев и детей младшего возраста, таких как младенец или дети младшего возраста, недоношенные или нет, от рождения до 7 лет.
Существует потребность в обеспечении такого вмешательства в питание и/или профилактического вмешательства в питание в форме, которая является приемлемой для популяции субъектов, в частности для тех лиц в этой популяции, которые являются наиболее уязвимыми или больше всего нуждаются в этом. Кроме того, существует потребность в отсутствии индуцирования неблагоприятных явлений, побочных или негативных воздействий в такой популяции.
Существует потребность в обеспечении нуждающейся популяции субъектов такими решениями самым простым и наиболее экономичным способом, предпочтительно не за счет применения конкретных ингредиентов, считающихся лекарственными средствами или медикаментами, а предпочтительно как часть рациона питания.
Настоящее изобретение относится ко всем млекопитающим, включая животных и людей, и, в частности, к младенцам и детям младшего возраста или домашним животным младшего возраста, у которых пластичность мозга наиболее высока. Предпочтительной целевой группой являются человеческие (недоношенные или доношенные) младенцы или дети младшего возраста / домашние животные в возрасте от рождения до 7 лет.
Изложение сущности изобретения
Авторы настоящего изобретения неожиданно обнаружили, что введение конкретного олигосахарида или смеси конкретных олигосахаридов, содержащих ОГМ, отдельно или в комбинации с OF и/или BMO, является особенно эффективным для улучшения, усиления, стимулирования или модулирования ГАМКергической функции в ЦНС или фильтрования информации или способности фокусироваться или концентрироваться на умственной или физической активности. Введение указанных олигосахаридов можно осуществлять в рамках вмешательства в питание или в рамках терапевтического вмешательства у нуждающихся в этом субъектов.
Краткое описание графических материалов
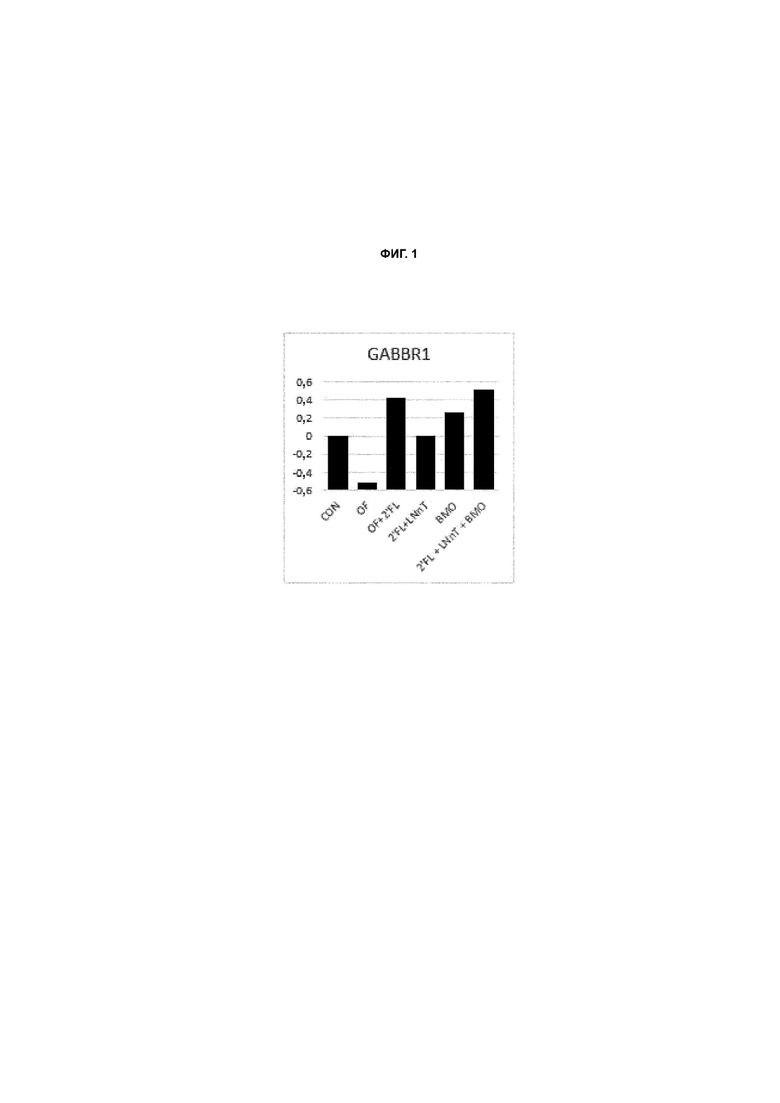
Фиг. 1. Показано влияние различных рационов питания (ОГМ, BMO, ОГМ + BMO, OF, OF + ОГМ) у поросят на экспрессию в гиппокампе ГАМКергического рецептора GABBR1. ОГМ, OF и BMO описаны в примерах.
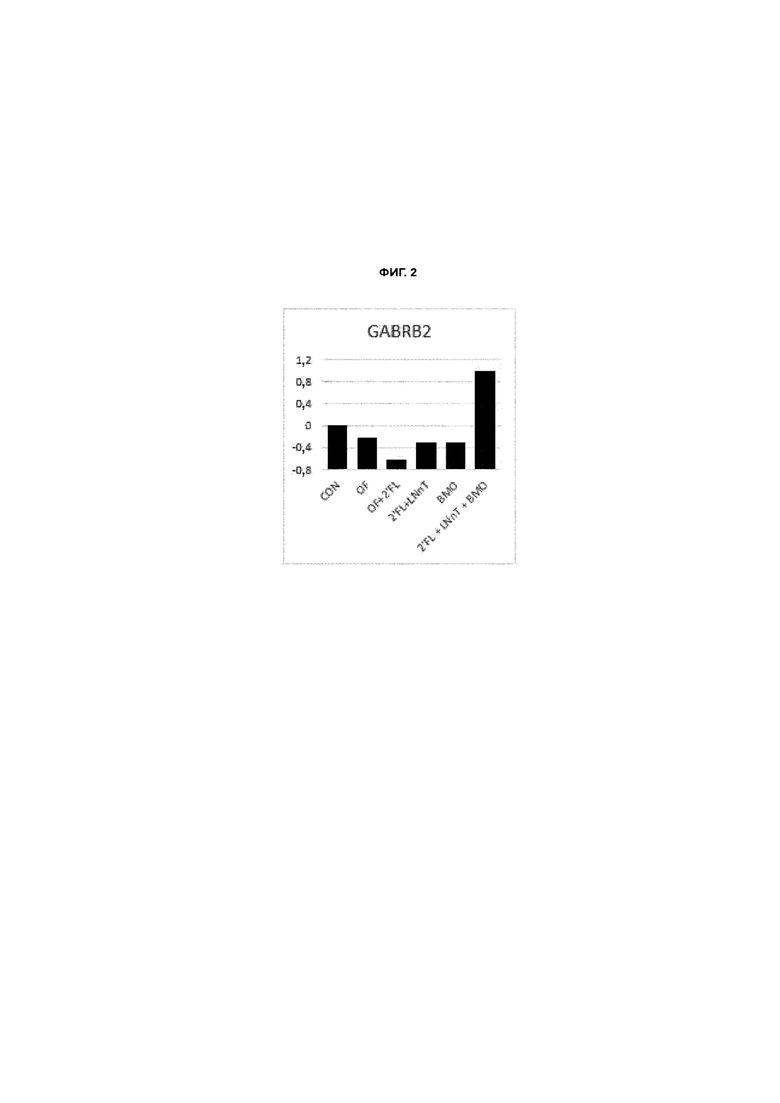
Фиг. 2. Показано влияние различных рационов питания (ОГМ, BMO, ОГМ + BMO, OF, OF + ОГМ) у поросят на экспрессию в гиппокампе ГАМКергического рецептора GABRB2. ОГМ, OF и BMO описаны в примерах.
Подробное описание примеров осуществления
Определения
В настоящем документе следующие термины имеют приведенные ниже значения.
Термин «младенец» означает ребёнка в возрасте до 12 месяцев.
Термин «ребенок младшего возраста» означает ребенка в возрасте от одного до семи лет.
Употребление форм единственного числа при описании элемента или компонента изобретения не должно иметь ограничительного характера в отношении количества экземпляров (т.е. вхождений) элемента или компонента. Следовательно, элемент или компонент в единственном числе включает «один или по меньшей мере один», и употребление элемента или компонента в единственном числе также включает множественное число, за исключением случаев, когда число явным образом обозначено как единственное.
Термин «олигосахарид грудного молока» применяется в виде сокращения ОГМ, в совокупности относится к олигосахаридам, присутствующим в грудном молоке, и подпадает под стандартное определение, принятое любым специалистом в данной области. ОГМ включают, без ограничений, фукозилированные олигосахариды (такие как 2’-фукозиллактоза, 3’фукозиллактоза, дифукозиллактоза, лакто-N-фукопентаоза I, лакто-N-фукопентаоза II, лакто-N-фукопентаоза III, лакто-N-фукопентаоза V, лакто-N-фукогексаоза, лакто-N-дифукогексаоза I, фукозиллакто-N-гексаоза, фукозиллакто-N-неогексаоза I, фукозиллакто-N-неогексаоза II, дифукозиллакто-N-гексаоза I, дифукозиллакто-N-неогексаоза I, дифукозиллакто-N-неогексаоза II, фукозил-пара-лакто-N-гексаоза и любая их комбинация), N-5 ацетилированные олигосахариды (такие как лакто-N-тетраоза (LNT), N-неотетраоза (LNnT) и любая их комбинация) и сиалилированные олигосахариды.
Термин «олигосахарид коровьего молока» (сокращенно BMO) относится к олигосахаридам, присутствующим в коровьем молоке, и подпадает под стандартное определение, принятое любым специалистом в данной области. Смесь BMO, применяемая в контексте настоящего изобретения, может быть, например, получена из молочной сыворотки коровьего молока. Вкратце, ультрафильтрат коровьей сыворотки, включая олигосахариды, такие как 3′- и 6′-сиалиллактоза и GOS, могут быть деминерализованы комбинацией электродиализа и ионного обмена, как описано в данной области. BMO могут включать, без ограничений, фукозилированные олигосахариды (такие как 2’-фукозиллактоза, 3’фукозиллактоза, дифукозиллактоза, лакто-N-фукопентаоза I, лакто-N-фукопентаоза II, лакто-N-фукопентаоза III, лакто-N-фукопентаоза V, лакто-N-фукогексаоза, лакто-N-дифукогексаоза I, фукозиллакто-N-гексаоза, фукозиллакто-N-неогексаоза I, фукозиллакто-N-неогексаоза II, дифукозиллакто-N-гексаоза I, дифукозиллакто-N-неогексаоза I, дифукозиллакто-N-неогексаоза II, фукозил-пара-лакто-N-гексаоза и любая их комбинация), N-5 ацетилированные олигосахариды (такие как лакто-N-тетраоза (LNT), N-неотетраоза (LNnT) и любая их комбинация) и сиалилированные олигосахариды.
Применяемый в настоящем документе термин «олигофруктоза» (сокращенно OF) относится к олигомеру фруктозы (т.е. фруктозному олигосахариду), имеющему степень полимеризации от 2 до 10, например степень полимеризации от 2 до 8. OF могут быть также названы фруктозными олигосахаридами, или фруктоолигосахаридами (сокращенно FOS), или короткоцепочечными фруктоолигосахаридами (сокращенно scFOS). В настоящем описании термины OF, FOS и scFOS имеют одинаковое значение и могут применяться взаимозаменяемо.
Инулин, содержащий длинноцепочечные полимеры, специально исключен из настоящего определения OF. OF отличают от инулина по степени полимеризации (инулин имеет гораздо более длинные цепочки).
FOS/scFOS/OF, как правило, доступны в продаже, например под торговым наименованием олигофруктоза ORAFTI производства Beneo GmbH (г. Мангейм, Германия) (например, ингредиент Orafti® P95).
Термин «сиалилированный олигосахарид» означает олигосахарид, содержащий один или более остатков сиаловой кислоты.
Термин «фукозилированный олигосахарид» означает олигосахарид, содержащий один или более остатков фукозы.
В настоящем документе термин «sn-2-пальмитат» относится к пальмитиновой кислоте в положении sn-2 триглицерида, с которым она связана.
Гамма-аминомасляная кислота, или «ГАМК», является общеизвестным ингибирующим нейротрансмиттером в ЦНС и благодаря своей функции ингибирования нейронной активности участвует, например, в синхронизации сети нейронов в гиппокампе. Термин «ГАМКергический» означает «относящийся к нейромедиатору ГАМК или влияющий на него». Например, синапс является ГАМКергическим, если в качестве нейромедиатора в нем применяется ГАМК. В другом примере ГАМКергический нейрон может продуцировать ГАМК. В другом примере вещество является ГАМКергическим, если оно способно вызывать эффекты посредством взаимодействий с ГАМК-системой, например путем стимуляции или блокирования передачи нервных импульсов. В другом примере ГАМКергическое вещество или ГАМКергический агент представляет собой любое химическое вещество, способное модифицировать эффекты ГАМК в организме или головном мозге. Классы ГАМКергических лекарственных средств включают, без ограничений, агонисты рецептора ГАМК, антагонисты рецептора ГАМК и ингибиторы обратного захвата ГАМК. Конкретным примером рецептора ГАМК является рецептор ГАМК типа B (GABBR).
Термин «ГАМКергическая функция в центральной нервной системе (ЦНС)» в настоящем документе относится к любой ГАМКергической функции, оказываемой посредством или в отношении любой клетки, части клетки, клеточного рецептора, системы или цепи клеток, содержащихся в ЦНС, включая, без ограничений, нейроны и нейроглию, такую как астроциты, олигодендроциты, микроглию и эпендимальные клетки, например применяющие ГАМКергическую нейротрансмиссию, транспорт ГАМК или захват ГАМК. ГАМКергическая нейротрансмиссия является основой для фильтрации поступающей информации в ЦНС, поскольку она ограничивает, уменьшает или удаляет нежелательную или ненужную информацию. Таким образом, конкретная ГАМКергическая функция в ЦНС предусматривает функции фильтрации информации или способности фокусироваться или концентрироваться на умственной или физической активности. В данной области продемонстрировано множество примеров ГАМКергической модуляции фильтрации информации. Например, содержание ГАМК в гиппокампе коррелировало со способностью подавлять извлечение нежелательной памяти, запускаемого у человека посредством напоминаний (Schmitz et al. Nat Commun. 2017, 8(1):1311). В зрительной крыше у рыбы данио-рерио ГАМКергические интернейроны необходимы для фильтрации пространственной информации, что позволяет рыбам должным образом охотиться на мелкую добычу (Del Bene et al. Science 2010, 330(6004):669-673). Кроме того, было показано, что изменение уровня ГАМК в стриатуме посредством захвата астроцитами модулирует свойства фильтрации информации нейронами (Goubard et al. J Physiol 2011, 589(9):2301-2319). Улучшение, усиление, стимулирование или модулирование ГАМКергических функций в ЦНС можно оценить, например, измеряя уровни экспрессии известных генов, входящих в ГАМКергическую систему, например генов ГАМКергических рецепторов или переносчиков. Например, экспрессия гена в гиппокампе может указывать на улучшенную, усиленную, стимулированную или модулированную ГАМКергическую функцию.
Термин «питательная композиция» означает композицию, которой питается субъект. Данная питательная композиция обычно предназначена для перорального или внутривенного применения и обычно включает источник липидов или жира и источник белка. Питательная композиция предпочтительно представляет собой полноценную питательную смесь, которая удовлетворяет всем или большинству потребностей субъекта в питании (например, детскую смесь). Питательные композиции содержат продукты питания.
Термин «детская смесь» означает продукт питания, специально предназначенный для применения в пищу младенцами в течение первых четырех–шести месяцев жизни и сам по себе удовлетворяющий потребности в питании этой категории лиц (статья 1.2 Директивы Европейской комиссии 91/321/EEC от 14 мая 1991 г. о детских смесях и смесях для прикармливаемых детей).
Термин «смесь для прикармливаемых детей» означает продукт питания, специально предназначенный для употребления в пищу младенцами старше четырех месяцев и составляющий основной жидкий компонент в рационе питания этой категории лиц, который предполагает постепенно увеличиваемое разнообразие.
Термин «начальная детская смесь» означает продукт питания, специально предназначенный для употребления в пищу младенцами в течение первых четырех месяцев жизни.
Детская смесь, смесь для прикармливаемых детей и начальная детская смесь могут иметь либо форму жидкости, готовой к употреблению или концентрированной, либо форму сухого порошка, который может быть разведен с образованием смеси после добавления воды. Такие смеси хорошо известны в данной области.
Термин «детское питание» означает продукт питания, специально предназначенный для употребления в пищу младенцами в течение первых лет жизни.
Термин «детская композиция на зерновой основе» означает продукт питания, специально предназначенный для применения в пищу младенцами в течение первых лет жизни.
Термин «молочная смесь для детей от 1 до 3 лет» означает напиток на основе молока, адаптированный для конкретных потребностей в питании детей младшего возраста.
Термин «период отлучения от груди» означает период, в течение которого в рационе питания младенца материнское молоко замещают другой пищей.
Термин «искусственная смесь» означает смесь, полученную с помощью химических и/или биологических средств, которая может быть химически идентична смеси природного происхождения, присутствующей в молоке млекопитающих.
Термин «пребиотик» означает неперевариваемые углеводы, которые благоприятно влияют на организм-хозяина, избирательно стимулируя рост и/или активность полезных для здоровья бактерий, например бифидобактерий в толстом кишечнике человека (Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr. 1995;125:1401-12).
Термин «пробиотик» означает препараты клеток микроорганизмов или компонентов клеток микроорганизмов, которые оказывают благоприятное воздействие на здоровье или самочувствие организма-хозяина (Salminen S, Ouwehand A. Benno Y. et al. Probiotics: how should they be defined. Trends Food Sci. Technol. 1999:10 107-10).
Если не указано иное, все процентные содержания даны по массе.
Если количества ингредиентов указаны как масса ингредиента / масса порошковой питательной композиции, предполагается, что настоящее изобретение также относится к соответствующему количеству на литр, с учетом коэффициента разбавления сухой порошковой питательной композиции 130 г/л (или указанного в инструкциях по разведению иным образом).
Олигосахариды грудного молока
ОГМ являются в совокупности третьим по величине компонентом сухих веществ грудного молока после лактозы и жира. ОГМ обычно состоит из лактозы на восстанавливающем конце с углеводным ядром, которое часто содержит фукозу или сиаловую кислоту на невосстанавливающем конце. Было выделено и охарактеризовано более сотни олигосахаридов молока, однако они представляют собой лишь очень малую часть от общего числа, которое еще предстоит охарактеризовать.
Для различных целей могут быть разработаны детские смеси с применением ингредиентов ОГМ, таких как фукозилированные олигосахариды, в частности 2FL, лакто-N-тетраоза, лакто-N-неотетраоза или сиалилированные олигосахариды.
В публикации EP0975235B1 Abbott Laboratories описана искусственная питательная композиция, содержащая один или более олигосахаридов грудного молока, причем ОГМ в композиции выбраны из группы, состоящей из восьми ОГМ (3-фукозиллактозы, лакто-N-фукопентаозы III, лакто-N-фукопентаозы II, дифукозиллактозы, 2’-фукозиллактозы, лакто-N-фукопентаозы I, лакто-N-неотетраозы и лакто-N-фукопентаозы V), причем упомянутая композиция предназначена нормальных, здоровых младенцев, детей, взрослых или индивидуумов, имеющих особые нужды, например связанные с определенными патологическими состояниями. В публикации EP0975235B1 утверждается, что, как правило, олигосахариды защищают младенцев от вирусных и бактериальных инфекций дыхательных, желудочно-кишечных и мочеполовых путей.
В одном варианте осуществления композиция настоящего изобретения содержит ОГМ, выбранный из группы, состоящей из фукозилированных олигосахаридов, таких как 2’-фукозиллактоза (2FL), сиалилированных олигосахаридов и/или N-ацетиллактозамина, такого как лакто-N-неотетраоза (LNnT) или лакто-N-тетраоза (LNT), или их комбинации. В настоящем документе представлены экспериментальные примеры композиций, содержащих 2FL.
N-ацетиллактозамин
В некоторых вариантах осуществления композиция изобретения содержит по меньшей мере один N-ацетиллактозамин. Иными словами, композиция в соответствии с изобретением содержит N-ацетиллактозамин и/или олигосахарид, содержащий N-ацетиллактозамин. К подходящим олигосахаридам, содержащим N-ацетиллактозамин, относятся лакто-N-тетраоза (LNT) и лакто-N-неотетраоза (LNnT).
Таким образом, в предпочтительном варианте осуществления N-ацетиллактозамин предпочтительно выбран из группы, содержащей лакто-N-тетраозу (LNT) и лакто-N-неотетраозу (LNnT).
LNT и LNnT можно синтезировать химическим путем с помощью ферментативного переноса сахаридных звеньев с донорных фрагментов на акцепторные фрагменты с применением гликозилтрансфераз, как описано, например, в патентах США № 5,288,637 и WO 96/10086. В альтернативном варианте осуществления LNT и LNnT можно получать путем химического превращения кетогексоз (например, фруктозы), либо свободных, либо связанных с олигосахаридом (например, лактулозой), в N-ацетилгексозамин или N-ацетилгексозамин-содержащий олигосахарид, как описано в Wrodnigg, T.M.; Stutz, A.E. (1999) Angew. Chem. Int. Ed. 38:827-828. Полученный таким образом N-ацетиллактозамин можно затем переносить на лактозу в качестве акцепторного фрагмента.
Композиция в соответствии с изобретением предпочтительно содержит от 0,1 до 3 г N-ацетиллактозамина на 100 г композиции в расчете на массу сухого вещества. Она предпочтительно содержит от 0,1 до 3 г LNnT на 100 г композиции в расчете на массу сухого вещества.
В одном варианте осуществления питательная композиция в соответствии с изобретением содержит N-ацетиллактозамин, предпочтительно выбранный из группы, содержащей лакто-N-тетраозу (LNT) и лакто-N-неотетраозу (LNnT).
Сиалилированные олигосахариды
Композиция в соответствии с изобретением в некоторых вариантах осуществления может содержать один или более сиалилированных олигосахаридов.
Сиалилированные олигосахариды включают все сиалилированные ОГМ, включая 3’-сиалиллактозу и 6’-сиалиллактозу. В указанной композиции предпочтительно присутствуют как 3'-сиалиллактоза, так и 6'-сиалиллактоза. В этом варианте осуществления соотношение 3'-сиалиллактозы и 6'-сиалиллактозы предпочтительно находится в диапазоне от 100 : 1 до 1 : 100, более предпочтительно от 10 : 1 до 1 : 10, еще более предпочтительно от 5 : 1 до 1 : 2.
3’- и 6’-формы сиалиллактозы могут быть выделены из природного источника, такого как молоко животных, методом хроматографии или фильтрации. В альтернативном варианте осуществления их можно получать с помощью биотехнологических средств с применением специфических сиалилтрансфераз или сиалидаз, нейраминидаз либо методом ферментации на основе ферментов (рекомбинантных или природных ферментов), путем химического синтеза, либо методом микробиологической ферментации. В последнем случае микроорганизмы могут экспрессировать свои природные ферменты и субстраты, или возможно создание микроорганизмов, вырабатывающих соответствующие субстраты и ферменты. Можно применять культуры из микроорганизмов одного вида или смешанные культуры. Образование сиалилолигосахаридов можно инициировать акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления сиалиллактозы можно получать путем химического синтеза из лактозы и свободной N’-ацетилнейраминовой кислоты (сиаловой кислоты). Сиалиллактозы также доступны в продаже, например производства Kyowa Hakko Kogyo, Япония.
Композиция в соответствии с изобретением предпочтительно содержит от 0,05 до 10 г, более предпочтительно от 0,1 до 5 г, еще более предпочтительно от 0,1 до 2 г сиалилированного(-ых) олигосахарида(-ов) на 100 г композиции в расчете на массу сухого вещества.
В одном варианте осуществления питательная композиция в соответствии с изобретением содержит сиалилированный олигосахарид, предпочтительно выбранный из группы, содержащей 3'-сиалиллактозу и 6'-сиалиллактозу. Более предпочтительно указанная композиция содержит как 3’-сиалиллактозу, так и 6’-сиалиллактозу, причем соотношение 3'-сиалиллактозы и 6'-сиалиллактозы предпочтительно находится в диапазоне от 100 : 1 до 1 : 100, более предпочтительно от 10 : 1 до 1 : 10, еще более предпочтительно от 5 : 1 до 1 : 2.
Фукозилированный олигосахарид
Композиция согласно настоящему изобретению может содержать один или более фукозилированных олигосахаридов. Фукозилированные олигосахариды предпочтительно состоят из 2’-фукозиллактозы (2-FL) или содержат ее.
Фукозилированный олигосахарид может быть выбран из группы, содержащей 2'-фукозиллактозу, 3-фукозиллактозу, дифукозиллактозу (DiFL), лакто-N-фукопентаозы (т.е. лакто-N-фукопентаозу I, лакто-N-фукопентаозу II, лакто-N-фукопентаозу III и лакто-N-фукопентаозу V), лакто-N-дифукогексаозу I, фукозиллакто-N-гексаозу, дифукозиллакто-N-гексаозу I и дифукозиллакто-N-неогексаозу II. Особенно предпочтительным фукозилированным олигосахаридом является 2'-фукозиллактоза (2-FL) или DiFL.
Фукозилированный олигосахарид может быть выделен из природного источника, такого как молоко животных, методами хроматографии или фильтрации. В альтернативном варианте осуществления его можно получать с помощью биотехнологических средств с применением специфических фукозилтрансфераз и/или фукозидазы либо посредством применения метода ферментации на основе ферментов (рекомбинантных или природных ферментов), либо методом микробиологической ферментации. В последнем случае или микроорганизмы могут экспрессировать свои природные ферменты и субстраты, или возможно создание микроорганизмов, вырабатывающих соответствующие субстраты и ферменты. Можно применять культуры из микроорганизмов одного вида и/или смешанные культуры. Образование фукозилированного олигосахарида может быть инициировано акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления фукозилированные олигосахариды можно получать из лактозы и свободной фукозы с помощью химического синтеза. Фукозилированные олигосахариды также имеются в продаже, например производства Kyowa Hakko Kogyo, Япония.
Композиция в соответствии с изобретением предпочтительно содержит от 0,1 до 3 г фукозилированного(-ых) олигосахарида(-ов) на 100 г композиции в расчете на массу сухого вещества, наиболее предпочтительно 2FL.
В одном варианте осуществления питательная композиция по изобретению содержит фукозилированный олигосахарид, предпочтительно выбранный из группы, содержащей 2'-фукозиллактозу, 3-фукозиллактозу, дифукозиллактозу, лакто-N-фукопентаозы (т.е. лакто-N-фукопентаозу I, лакто-N-фукопентаозу II, лакто-N-фукопентаозу III и лакто-N-фукопентаозу V), лакто-N-дифукогексаозу I, фукозиллакто-N-гексаозу, дифукозиллакто-N-гексаозу I и дифукозиллакто-N-неогексаозу II, и предпочтительно фукозилированный олигосахарид представляет собой 2’-фукозиллактозу (2-FL).
Дополнительные пребиотики
Помимо основных олигосахаридов, составляющих предмет настоящего патента, композиция изобретения может дополнительно содержать по меньшей мере один или один дополнительный пребиотик, обычно в количестве от 0,3 до 10% массы композиции.
Пребиотики, как правило, неперевариваемы в том смысле, что они не расщепляются и не всасываются в желудке или тонком кишечнике и, таким образом, остаются в нативном виде при переходе в толстый кишечник, в котором их селективно ферментируют полезные бактерии.
Композиция в соответствии с изобретением может содержать в некоторых вариантах осуществления олигофруктозу (OF). В качестве примера такой OF можно привести коммерческий ингредиент ORAFTI® производства Beneo GmbH (г. Мангейм, Германия).
В некоторых вариантах осуществления пребиотики из композиции изобретения содержат другие фруктоолигосахариды (FOS) и/или галактоолигосахариды (GOS). Можно применять комбинацию пребиотиков, такую как 90% ГОС и 10% короткоцепочечных фруктоолигосахаридов, например в виде продукта, продаваемого BENEO-Orafti под торговой маркой Orafti® oligofructose (см. http://www.beneo-orafti.com/Our-Products/Oligofructose) (ранее Raftilose®), или 10% инулина, например в виде продукта, продаваемого BENEO-Orafti под торговой маркой Orafti® inulin (см. http://www.beneo-orafti.com/Our-Products/Inulin) (ранее Raftiline®). Другой комбинацией пребиотиков является 70% короткоцепочечных фруктоолигосахаридов и 30% инулина, что представляет собой продукт, продаваемый BENEO-Orafti® под торговой маркой Prebio 1.
В одном варианте осуществления питательная композиция в соответствии с изобретением содержит пребиотик, выбранный из перечня олигосахаридов коровьего молока, инулина, ксилоолигосахаридов, полидекстрозы или любой их комбинации.
В одном варианте осуществления питательная композиция изобретения содержит олигосахарид коровьего молока (BMO). BMO может содержать олигосахариды, которые представляют собой N-ацетилированный олигосахарид, галактоолигосахарид, сиалилированный олигосахарид, фукозилированный олигосахарид или их комбинацию.
Пробиотики
Композиция изобретения может дополнительно содержать по меньшей мере один пробиотик. Не имеющие ограничительного характера примеры пробиотиков включают: Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Streptococcus, Kluyveromyces, Saccharoymces, Candida, в частности выбранные из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactococcus lactis, Enterococcus faecium, Saccharomyces cerevisiae, Saccharomyces boulardii или их смесей, предпочтительно выбранные из группы, состоящей из Bifidobacterium longum NCC3001 (ATCC BAA-999), Bifidobacterium longum NCC2705 (CNCM I-2618), Bifidobacterium longum NCC490 (CNCM I-2170), Bifidobacterium lactis NCC2818 (CNCM I-3446), Bifidobacterium breve штамм A, Lactobacillus paracasei NCC2461 (CNCM I-2116), Lactobacillus johnsonii NCC533 (CNCM I-1225), Lactobacillus rhamnosus GG (ATCC53103), Lactobacillus rhamnosus NCC4007 (CGMCC 1.3724), Enterococcus faecium SF 68 (NCC2768; NCIMB10415) и их комбинаций.
В одном варианте осуществления указанный пробиотик представляет собой пробиотический бактериальный штамм, предпочтительно бифидобактерии и/или лактобациллы. Подходящие пробиотические бактериальные штаммы включают Lactobacillus rhamnosus ATCC 53103, производства Valio Oy, Финляндия, под товарным знаком LGG; Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus paracasei CNCM I-2116, Lactobacillus johnsonii CNCM I-1225, Streptococcus salivarius DSM 13084, продаваемые BLIS Technologies Limited, Новая Зеландия, под названием KI2; Bifidobacterium lactis CNCM 1-3446, продаваемый в числе прочих Christian Hansen, Дания, под товарным знаком Bb 12; Bifidobacterium longum ATCC BAA-999, продаваемый компанией Morinaga Milk Industry Co. Ltd., Япония, под товарным знаком BB536; Bifidobacterium breve, продаваемый Danisco под товарным знаком Bb-03; Bifidobacterium breve, продаваемый Morinaga под товарным знаком M-16V; Bifidobacterium infantis, продаваемый Procter & GambIe Co. под товарным знаком Bifantis; и Bifidobacterium breve, продаваемый Institut Rosell (Lallemand) под товарным знаком R0070.
Композиция в соответствии с изобретением предпочтительно содержит от 10e3 до 10e12 КОЕ пробиотического бактериального штамма, более предпочтительно от 10e7 до 10e12 КОЕ на грамм композиции в расчете на массу сухого вещества.
В одном варианте осуществления питательная композиция содержит пробиотический бактериальный штамм, выбранный из перечня, состоящего из Lactobacillus acidophilus, Lactobacillus salivarius, Lactobacillus rhamnosus, Lactobacillus paracasei, Lactobacillus casei, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus fermentum, Lactobacillus lactis, Lactobacillus delbrueckii, Lactobacillus helveticus, Lactobacillus bulgari, Lactococcus lactis, Lactococcus diacetylactis, Lactococcus cremoris, Streptococcus salivarius, Streptococcus thermophilus, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium longum, Bifidobacterium breve, Bifidobacterium infantis или Bifidobacterium adolescentis или любой их смеси.
Целевая популяция
В одном варианте осуществления настоящее изобретение направлено на / предназначено для млекопитающих. Млекопитающие предпочтительно представляют собой человека или домашних животных, таких как собака или кошка.
В более предпочтительном варианте осуществления настоящее изобретение предназначено для молодых млекопитающих, таких как молодые люди, например младенцы (например, от 0 до 6 месяцев или от 0 до 12 месяцев) или дети младшего возраста (например, от 1 до 3 лет или от 1 до 7 лет) или для молодых собак (например, щенков) или молодых кошек. В одном еще более предпочтительном варианте осуществления млекопитающее представляет собой младенца или ребёнка младшего возраста. Без связи с какой-либо теорией молодые млекопитающие имеют высокую пластичность головного мозга и развития головного мозга (или формирования связей в головном мозге) и получают наибольшую пользу от настоящего изобретения. Кроме того, предполагается, что настоящее изобретение может ориентироваться на конкретные окна вмешательства в питание (например, на детей в возрасте от 6 месяцев до 3 лет, от 3 месяцев до 18 месяцев), на субпопуляции, имеющие особые нужды (уязвимые молодые млекопитающие; сенильные и полусенильные млекопитающие) или находящиеся в фазе восстановления. В одном варианте осуществления настоящее изобретение, по существу, направлено на субъектов, нуждающихся в предотвращении, профилактике или компенсации синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении (например, млекопитающих, родившихся недоношенными или с субоптимальным ростом или развитием). В одном варианте осуществления настоящее изобретение, по существу, направлено на субъектов, страдающих от состояния или заболевания, связанного с ГАМКергическими функциями, в частности психическими или неврологическими расстройствами, связанными с ГАМКергическими функциями, такими как фильтрация информации или способность фокусироваться или концентрироваться на умственной или физической активности. Такое заболевание может предусматривать психические или неврологические расстройства, такие как синдром дефицита внимания и гиперактивности, расстройства аутического спектра, а также шизофрению.
В соответствии с предпочтительным вариантом осуществления композиция в соответствии с изобретением предназначена для применения у здоровых младенцев и/или здоровых детей младшего возраста. В одном варианте осуществления изобретение имеет особое значение для слабых младенцев, недоношенных младенцев, и/или младенцев, рожденных с аномально низким весом при рождении, и/или для младенцев, страдавших внутриутробным замедлением роста. Предпочтительным периодом применения является (-ются) период (-ы) наиболее быстрого развития памяти и/или развития связей головного мозга.
Композиция изобретения предназначена для младенцев и/или детей младшего возраста в возрасте 7 лет или менее, предпочтительно в возрасте 3 лет или менее, наиболее предпочтительно в возрасте 1 года или менее. В одном варианте осуществления композиция предназначена для младенцев в возрасте 6 месяцев или менее. В вариантах осуществления изобретения композицию применяют в течение первых 6 месяцев жизни, первого 1 года жизни, первых 3 лет жизни, первых 7 лет жизни и/или в течение периода восстановления после болезни или недостатка развития.
Питательная композиция
Питательная композиция в соответствии с изобретением предпочтительно представляет собой искусственную питательную композицию. Композиция изобретения может представлять собой, например, начальную детскую смесь, детскую смесь, детское питание, детскую композицию на зерновой основе, смесь для прикармливаемых детей или молочную смесь для детей от 1 до 3 лет, и указанная композиция предпочтительно представляет собой начальную детскую смесь. Композиция в соответствии с изобретением также может быть предназначена для применения до и/или во время периода отлучения от груди. В одном варианте осуществления питательная композиция может представлять собой полноценную питательную композицию или добавку для возрастных, пожилых или уязвимых лиц.
Композиция в соответствии с изобретением может представлять собой полноценную композицию, обеспечивающую 100% или большую часть потребностей в питании целевой популяции (например, с точки зрения потребности в калориях; или с точки зрения потребностей в витаминах или минеральных веществах, или с точки зрения потребностей в белках, липидах или углеводах). В альтернативном варианте осуществления композиция изобретения может представлять собой добавку, которая является дополнением к обычному рациону питания потребителя. Однако в этом случае дозировка и общее потребление композиции подобраны с возможностью обеспечения заявленного преимущества в отношении фильтрации информации (например, пропорционально калорийной нагрузке и потребностям субъекта в калориях).
Применение композиции изобретения может включать случаи, когда композиция представляет собой добавку, предпочтительно предлагаемую в форме единичных доз. В одном варианте осуществления композиция представляет собой добавку к человеческому грудному вскармливанию.
Композиция может быть в форме порошковой композиции, например, предназначенной для разбавления водой, или смешивания с молоком (например, человеческим грудным молоком), или потребления в виде порошка. В одном варианте осуществления композиция изобретения представлена в жидком виде; либо готовой к употреблению, либо предназначенной для разведения в воде или смешивания с молоком (например, человеческим грудным молоком).
Композиция в соответствии с настоящим изобретением может также содержать источник белка, предпочтительно в количестве менее 2,5 г на 100 ккал или менее 2,0 г на 100 ккал, еще более предпочтительно в количестве менее 1,8 г на 100 ккал. В одном варианте осуществления содержание белка составляет менее 1,6 г/100 ккал. Тип белка не считается критическим для настоящего изобретения при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечен удовлетворительный рост. Таким образом, можно применять источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается сывороточных белков, источник белка может быть основан на кислой молочной сыворотке или сладкой молочной сыворотке или их смесях и может включать альфа-лактальбумин и бета-лактоглобулин в любых желаемых пропорциях.
Композиция в соответствии с настоящим изобретением, по существу, содержит источник углеводов. Это особенно предпочтительно в том случае, когда питательная композиция изобретения представляет собой детскую смесь. В этом случае можно применять любой источник углеводов, обычно встречающийся в детских смесях, такой как лактоза, сахароза, мальтодекстрин, крахмал и их смеси, хотя предпочтительным источником углеводов является лактоза.
Композиция в соответствии с настоящим изобретением, по существу, содержит источник липидов. Это особенно важно, если питательная композиция настоящего изобретения представляет собой детскую смесь. В этом случае источником липидов может быть любой липид или жир, который подходит для применения в детских смесях. Предпочтительные источники жиров включают пальмовый олеин, подсолнечное масло с высоким содержанием олеиновой кислоты и сафлоровое масло с высоким содержанием олеиновой кислоты. Кроме того, можно добавлять незаменимые жирные кислоты линоленовую кислоту и α-линоленовую кислоту, а также небольшие количества масел, содержащих большие количества арахидоновой кислоты и докозагексаеновой кислоты в готовом виде, таких как рыбьи жиры или микробные масла. Источник жиров предпочтительно имеет соотношение жирных кислот n-6 и n-3 от около 5 : 1 до около 15 : 1; например, от около 8 : 1 до около 10 : 1.
Композиция изобретения также содержит предпочтительно все витамины и минеральные вещества, которые, как известно, являются незаменимыми в ежедневном рационе в значимых с точки зрения питания количествах. Для некоторых витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, которые необязательно присутствуют в композиции изобретения, включают витамин А, витамин В1, витамин В2, витамин В6, витамин В12, витамин Е, витамин K, витамин С, витамин D, фолиевую кислоту, инозит, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлор, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме солей. Присутствие и количества конкретных минеральных веществ и других витаминов могут варьироваться в зависимости от предполагаемой популяции.
При необходимости композиция изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т.п.
Композиция изобретения может также содержать другие вещества, которые могут оказывать благоприятное воздействие, такие как лактоферрин, нуклеотиды, нуклеозиды и т.п.
В одном варианте осуществления композиция изобретения, в особенности в форме детской смеси, содержит от около 1,8 до около 2,2 г общего количества белка на 100 ккал, например от около 1,8 до около 2,1 г или от около 1,9 до около 2,1 г белка на 100 ккал, причем необязательно от около 0,3 до около 0,4 г/100 ккал белка составляет альфа-лактальбумин. Детская смесь и смесь для прикармливаемых детей по настоящему изобретению могут иметь форму готовой к употреблению жидкости, или могут представлять собой жидкий концентрат или порошковую смесь, которая может быть разведена в готовую к употреблению жидкость путем добавления некоторого количества воды с получением результата, а смесь для прикармливаемых детей, составляющая предмет настоящего изобретения, включает все ингредиенты, требуемые по закону США или ЕС, включая, без ограничений, определенные витамины, минеральные вещества и незаменимые аминокислоты. Она может также включать нуклеотиды, такие как ЦМФ, УМФ, АМФ, ГМФ и ИМФ, лютеин, зеаксантин и другие ингредиенты, известные в данной области.
В одном варианте осуществления изобретения питательная композиция представляет собой корм для домашних животных (например, для собак или кошек или молодых собак или молодых кошек).
Эффект(-ы) и применение композиции изобретения
Настоящее изобретение относится к улучшению, усилению, стимуляции или модулированию ГАМКергической функции в ЦНС субъекта. Это может включать улучшение, усиление, стимулирование или модулирование фильтрации информации или способности фокусироваться или концентрироваться на умственной или физической активности.
Без связи с какой-либо теорией считается, что в одном аспекте изобретения такое усовершенствование, улучшение и/или активация связаны с влиянием олигосахарида изобретения на кишечную микробиоту. Олигосахариды, такие как ОГМ (например, 2FL или LNnT), BMO или OF, лишь в небольшой степени расщепляются в тонком кишечнике, таким образом, большая их часть становится доступной для ферментации микробиотой в толстой кишке. Действительно, было показано, что ОГМ (например, 2FL или LNnT), BMO или OF активируют рост кишечных бифидобактерий, что отражается в увеличении содержания бактерий этого семейства в стуле у младенцев, получающих смеси с добавлением олигосахаридов, содержащих ОГМ (например, 2FL или LNnT), BMO или OF. По-видимому, как олигосахариды, так и пробиотики связаны с благоприятным изменением экспрессии ГАМК-рецептора в головном мозге. Без ограничений, накладываемых какой-либо теорией, вследствие высокого присутствия ГАМК у некоторых видов бактерий (например, Lactobacillus и Bifidobacterium) такие пробиотические виды могут выступать в качестве несущей среды для доставки ГАМК, и их потребление может оказывать локальное воздействие на желудочно-кишечную систему, которое в конечном итоге модулирует нейрофизиологию хозяина (Lyte, BioEssays 2011, 33, 574–581). Данная связь выглядит еще сильнее, если учесть, что как прокариоты, так и эукариоты синтезируют ГАМК посредством декарбоксилирования глутамата глутамат-декарбоксилазой (GAD), и анализы в рамках проекта «Микробиом человека» позволяют предположить, что гены, кодирующие GAD, присутствуют в микробиоме человека (Mazzoli, R., Pessione, E. (2016). Front. Microbiol. 7, 1934; Pokusaeva et al., Neurogastroenterol. Motil. 2017, 29(1) doi:10.1111/nmo.12904).
Если коротко, настоящую питательную композицию можно применять для улучшения, усиления, стимулирования или модулирования ГАМКергической функции благодаря влиянию на кишечную микробиоту и ось кишечник – головной мозг, которая, как показано, влияет на многие аспекты функционирования головного мозга. Кроме того, может быть предусмотрено, что улучшение, усиление, стимулирование или модулирование ГАМКергической функции может быть связано с увеличением концентрации сиаловой кислоты (Neu5Ac) в головном мозге указанного индивидуума, опосредуемым различными метаболическими путями, на которые оказывает воздействие кишечная микробиота. Без ограничений, накладываемых какой-либо теорией, в одном варианте осуществления изобретения ОГМ действует синергетически с пробиотиком и эндогенной микробиотой, оказывая наилучшее влияние на такие метаболические пути.
В другом аспекте эффект, лежащий в основе настоящего изобретения, может быть связан с измененной экспрессией ГАМКергических генов в ЦНС субъекта, в частности ГАМК-рецепторов или ГАМК-переносчиков. В одном варианте осуществления изменение относится к измеренным повышенным или сниженным уровням экспрессии генов на уровне мРНК или на уровне белка по сравнению с контролем. В одном варианте осуществления экспрессия гена относится к экспрессии гена в гиппокампе у субъекта.
В другом аспекте эффект, лежащий в основе изобретения, может быть связан с улучшением нейрональной пластичности в головном мозге субъекта и/или с улучшением нейронального развития, нейрогенеза, прорастанием аксонов, миелинизацией и/или созреванием головного мозга указанного субъекта (без ограничений, накладываемых какой-либо теорией).
ГАМКергические функции, и, в частности, способность фильтровать информацию или фокусироваться на психической или физической активности, представляют собой важные аспекты функционирования и развития головного мозга и имеют решающее значение для общего когнитивного развития субъекта. Они оказывают влияние, в частности, на обработку, классификацию внешних сигналов и управление ими, на возможность обучения, а также на пространственную ориентацию.
В одном варианте осуществления настоящего изобретения ГАМКергическая функция представляет собой способность фильтровать информацию, например поступающую сенсорную информацию. Фильтрация информации имеет крайне важное значение для социального и когнитивного развития, особенно у молодых субъектов. В одном варианте осуществления настоящего изобретения ГАМКергическая функция заключается в способности фокусироваться или концентрироваться на психической или физической активности.
Таким образом, в одном аспекте настоящее изобретение относится к применению (или определяется применением) питательной композиции, содержащей ОГМ, для улучшения, усиления, стимуляции или модуляции ГАМКергической функции в ЦНС, в частности способности фильтровать информацию или фокусироваться или концентрироваться на умственной или физической активности у млекопитающего.
В одном аспекте настоящее изобретение относится к применению (или определяется применением) описанной в настоящем документе питательной композиции, содержащей ОГМ, для предотвращения, профилактики или компенсации синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении, особенно у нуждающихся в этом субъектов, и в особенности путем стимуляции или модуляции ГАМКергических функций в ЦНС.
В одном аспекте настоящее изобретение относится к применению (или определяется применением) описанной в настоящем документе питательной композиции, содержащей ОГМ, для улучшения, усиления или модуляции синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении, и в особенности путем стимуляции или модуляции ГАМКергических функций в ЦНС.
В одном аспекте настоящее изобретение относится к применению (или определяется применением) описанной в настоящем документе питательной композиции, содержащей ОГМ, для улучшения, усиления или модуляции ГАМКергической функции в ЦНС, в частности фильтрации информации или способности фокусироваться или концентрироваться на умственной или физической активности.
В одном варианте осуществления настоящее изобретение относится к применению (или определяется применением) описанной в настоящем документе питательной композиции, причем указанная композиция представляет собой детскую смесь, смесь для прикармливаемых детей, обогатитель грудного молока, молочную смесь для детей от 1 до 3 лет или корм для домашних животных.
В другом аспекте изобретение относится к ОГМ (или определяется ОГМ) для применения в улучшении, усилении, стимуляции или модуляции ГАМКергической функции в ЦНС, в частности способности фильтровать информацию или фокусироваться или концентрироваться на умственной или физической активности, у нуждающегося в этом субъекта. В конкретном варианте осуществления субъектом является млекопитающее, причем указанное млекопитающее предпочтительно представляет собой человека, кошку или собаку, и при этом указанный человек предпочтительно представляет собой младенца или ребёнка младшего возраста.
В другом аспекте изобретение относится к (или определяется) питательной композицией, содержащей ОГМ, для применения в улучшении, усилении, стимуляции или модуляции ГАМКергической функции в ЦНС, в частности способности фильтровать информацию или фокусироваться или концентрироваться на умственной или физической активности у нуждающегося в этом субъекта. В конкретном варианте осуществления субъект представляет собой млекопитающее, причем указанное млекопитающее предпочтительно представляет собой молодое млекопитающее, человека, собаку или кошку, более предпочтительно молодого человека, собаку или кошку, наиболее предпочтительно младенца или ребёнка младшего возраста. Питательная композиция может также содержать один или более необязательных ингредиентов, описанных в настоящем документе.
В другом аспекте настоящее изобретение относится к применению (или определяется применением) ОГМ в производстве питательной композиции для улучшения, усиления, стимуляции или модуляции ГАМКергической функции в ЦНС, в частности способности фильтровать информацию или фокусироваться или концентрироваться на умственной или физической активности у нуждающегося в этом субъекта. В конкретном варианте осуществления субъект представляет собой млекопитающее, причем указанное млекопитающее предпочтительно представляет собой молодое млекопитающее, человека, собаку или кошку, более предпочтительно молодого человека, собаку или кошку, наиболее предпочтительно младенца или ребёнка младшего возраста.
Дозировка
ОГМ. В одном варианте осуществления общее количество ОГМ составляет от 0,01 до 50 г/л, от 0,1 до 10 г/л, от 0,3 до 5 г/л, или от 0,5 до 1 г/л, или 0,25, или 0,5, или 1, или 1,5, или 2 г/л.
BMO. В одном варианте осуществления общее количество BMO составляет от 0,01 до 50 г/л, от 0,1 до 10 г/л, от 0,3 до 5 г/л, или от 0,5 до 1 г/л, или 0,25, или 0,5, или 1, или 1,5, или 2 г/л.
Фруктоолигосахарид/FOS/OF. При наличии питательная композиция настоящего изобретения может содержать от 0,1 до 20 г олигофруктозы (OF) на 100 г композиции в расчете на массу сухого вещества, например от 1 до 6 г или от 3 до 5 г олигофруктозы (OF) на 100 г композиции в расчете на массу сухого вещества.
Один вариант осуществления изобретения питательной композиции содержит количество фруктозного олигосахарида в следующих диапазонах или величине:
от 0,1 до 20 г/л, или от 0,5 до 10 г/л, или от 1 до 8 г/л, или от 2 до 6 г/л, или 1,5 г/л, или 3 г/л, или 5 г/л питательной композиции, когда композиция находится в готовой к употреблению жидкой форме, или
от 0,1 до 20 г/л, или от 0,5 до 10 г/л, или от 1 до 8 г/л, или от 2 до 6 г/л, или 1,5 г/л, или 3 г/л, или 5 г/л (жидкой разведенной формы), когда композиция находится в порошковой форме и предназначена для разведения с получением разведенной жидкой формы, или
то же, что и выше, умноженное на 2, 5, 10, 20, 50 или 100, когда питательная композиция находится в форме концентрированной композиции, предназначенной для разбавления (соответственно в 2, 5, 10, 20, 50 или 100 раз) в воде или человеческом грудном молоке или предназначена для непосредственного применения в концентрированной форме, или
от 0,4 г до 15 г/100 г порошковой питательной композиции, или от 0,8 до 10 г/100 г, или от 1 до 6 г/100 г, или от 2 до 5 г/100 г, или от 2,1 до 4 г/100 г или 1,2 г/100 г, или 2,3 г/100 г, или 3,8 г/100 г, или 4 г/100 г, или 6 г/100 г порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
В одном варианте осуществления содержание OF может составлять от 0,07 г до 3 г/100 ккал порошковой питательной композиции, или от 0,1 до 2 г/100 ккал, или от 0,4 до 1,5 г/100 ккал, или от 0,45 до 1 г/100 ккал, или от 0,45 до 0,75 г/100 ккал, или 0,3 г/100 ккал, или 0,4 г/100 ккал, или 0,5 г/100 ккал, или 0,75 г/100 ккал, или 1 г/100 ккал порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
2FL. Питательная композиция настоящего изобретения может содержать от 0,02 до 10 г 2FL на 100 г композиции в расчете на массу сухого вещества, например от 0,2 до 0,5 г или от 0,3 до 5 г 2FL на 100 г композиции в расчете на массу сухого вещества.
В одном варианте осуществления питательная композиция содержит 2FL в следующих диапазонах или количествах:
от 0,05 до 20 г/л, или от 0,1 до 5 г/л, или от 0,2 до 3 г/л, или от 0,1 до 2 г/л, или от 0,25 г/л до 1 г/л, или 0,25 г/л, или 1 г/л питательной композиции, когда композиция находится в готовой к употреблению жидкой форме, или
от 0,05 до 20 г/л, или от 0,1 до 5 г/л, или от 0,2 до 3 г/л, или от 0,1 до 2 г/л, или от 0,25 г/л до 1 г/л, или 0,25 г/л, или 1 г/л (жидкой разведенной формы), когда композиция находится в порошковой форме и предназначена для разведения с получением разведенной жидкой формы, или
то же, что и выше, умноженное на 2, 5, 10, 20, 50 или 100, когда питательная композиция находится в форме концентрированной композиции, предназначенной для разбавления (соответственно в 2, 5, 10, 20, 50 или 100 раз) в воде или человеческом грудном молоке или предназначена для непосредственного применения в концентрированной форме, или
от 0,04 г до 1,5 г/100 г порошковой питательной композиции, или от 0,08 до 1,2 г/100 г, или от 0,1 до 1 г/100 г, или от 0,2 до 0,8 г/100 г, или 0,2 г/100 г, или 0,4 г/100 г, или 0,8 г/100 г, или 1 г/100 г, или 1 г/100 г порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
В одном варианте осуществления содержание 2FL может составлять от 0,01 г до 0,3 г/100 ккал порошковой питательной композиции, или от 0,02 до 0,2 г/100 ккал, или от 0,04 до 0,15 г/100 ккал, или 0,02 г/100 ккал, или 0,04 г/100 ккал, или 0,07 г/100 ккал, или 0,15 г/100 ккал, или 0,3 г/100 ккал порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
LNnT. В одном варианте осуществления питательная композиция может содержать от 0,01 до 1 г LNnT на 100 г композиции в расчете на массу сухого вещества, например от 0,1 до 0,25 г или от 0,15 до 0,5 г LNnT на 100 г композиции в расчете на массу сухого вещества.
В одном варианте осуществления изобретения питательная композиция содержит количество LNnT в следующих диапазонах или величинах:
от 0,02 до 10 г/л, или от 0,05 до 2,5 г/л, или от 0,1 до 1,5 г/л, или от 0,05 до 1 г/л, или от 0,12 г/л до 0,5 г/л, или 0,12 г/л, или 0,5 г/л, или 1 г/л питательной композиции, когда композиция находится в готовой к употреблению жидкой форме, или
от 0,02 до 10 г/л, или от 0,05 до 2,5 г/л, или от 0,1 до 1,5 г/л, или от 0,05 до 1 г/л, или от 0,12 г/л до 0,5 г/л, или 0,12 г/л, или 0,5 г/л, или 1 г/л (жидкой разведенной формы), когда композиция находится в порошковой форме и предназначена для разведения с получением разведенной жидкой формы, или
то же, что и выше, умноженное на 2, 5, 10, 20, 50 или 100, когда питательная композиция находится в форме концентрированной композиции, предназначенной для разбавления (соответственно в 2, 5, 10, 20, 50 или 100 раз) в воде или человеческом грудном молоке или предназначена для непосредственного применения в концентрированной форме, или
от 0,02 г до 0,75 г/100 г порошковой питательной композиции, или от 0,04 до 0,6 г/100 г, или от 0,05 до 0,5 г/100 г, или от 0,1 до 0,4 г/100 г, или 0,1 г/100 г, или 0,2 г/100 г, или 0,25 г/100 г, или 0,5 г/100 г, или 1 г/100 г, или 3 г/100 г порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
В одном варианте осуществления содержание LNnT может составлять от 0,01 г до 0,3 г/100 ккал порошковой питательной композиции, или от 0,02 до 0,2 г/100 ккал, или от 0,04 до 0,15 г/100 ккал, или 0,02 г/100 ккал, или 0,04 г/100 ккал, или 0,07 г/100 ккал, или 0,15 г/100 ккал, или 0,3 г/100 ккал порошковой питательной композиции, если питательная композиция имеет форму сухого порошка.
Композиция изобретения, в частности в форме детской смеси, может содержать по меньшей мере около 0,4 г олигофруктозы на 100 ккал. В некоторых вариантах осуществления она содержит от около 0,4 до около 0,9 г, от около 0,4 до около 0,7 г, от около 0,4 до около 0,5 г, от около 0,7 до около 0,8 г или от около 0,7 до около 0,9 г олигофруктозы на 100 ккал. Олигофруктоза имеет степень полимеризации от 2 до 10. В одном варианте осуществления по меньшей мере 90% олигофруктозы имеет степень полимеризации от 2 до 8.
В одном варианте осуществления питательная композиция содержит 2 FL и LNnT, предпочтительно в количестве 1 г/л 2FL и 0,5 г/л LNnT, или 0,5 г/л 2FL и 0,25 г/л LNnT, или от 0,25 г/л до 2 г/л 2FL и от 0,1 до 1 г/л LNnT.
Способ изготовления питательной композиции
Питательную композицию можно готовить любым подходящим способом, известным в данной области. Например, коммерческая детская смесь или смесь для прикармливаемых детей, может выступать в качестве основной композиции, к которой добавляют необходимое количество олигосахаридов (например, ОГМ, такие как 2FL, LNnT или другие, OF, BMO), предпочтительно в сухой форме. В альтернативном варианте осуществления олигосахарид можно добавлять в виде сухого ингредиента или жидкого ингредиента в жидкий премикс, который будет служить основой для производства питательной композиции изобретения. Затем жидкую смесь можно высушивать с помощью любого традиционного средства.
Например, ее можно готовить посредством перемешивания вместе источника белка, источника углеводов (отличного от комбинации олигосахаридов настоящего изобретения) и источника жира в соответствующих пропорциях. На данном этапе можно включать эмульгаторы в случае их применения. На данной стадии можно добавлять витамины и минеральные вещества, но обычно их добавляют позднее во избежание термического разложения. Перед смешиванием в источнике жира можно растворять любые липофильные витамины, эмульгаторы и т.п. Затем можно добавлять воду, предпочтительно очищенную обратным осмосом, с образованием жидкой смеси. Температура воды для удобства находится в диапазоне от около 50°С до около 80°С для облегчения диспергирования ингредиентов. Для образования жидкой смеси можно применять доступные в продаже разжижители. 3’-сиалиллактозу (3’-SL) и 6’-сиалиллактозу (6’-SL) добавляют на этой стадии, если готовый продукт должен иметь жидкую форму. Если конечный продукт должен представлять собой порошок, на этой стадии при необходимости также можно добавлять 3’-сиалиллактозу (3’-SL) и 6’-сиалиллактозу (6’-SL). Затем жидкую смесь гомогенизируют, например, в две стадии.
Затем жидкую смесь можно термически обрабатывать для снижения бактериальной нагрузки путем быстрого нагрева жидкой смеси, например до температуры в диапазоне от около 80°C до около 150°C, в течение периода времени от около 5 секунд до около 5 минут. Нагревание можно осуществлять путем нагнетания пара с помощью автоклава или теплообменника, например пластинчатого теплообменника. Затем жидкую смесь можно охлаждать до температуры от около 60°C до около 85°C, например путем мгновенного охлаждения. Затем жидкую смесь можно снова гомогенизировать, например, в две стадии: под давлением в диапазоне от около 10 МПа до около 30 МПа на первой стадии и от около 2 МПа до около 10 МПа на второй стадии. Затем гомогенизированную смесь можно дополнительно охлаждать для добавления любых термочувствительных компонентов, таких как витамины и минеральные вещества. На данной стадии удобно регулировать рН и содержание твердых веществ в гомогенизированной смеси. Гомогенизированную смесь переносят в подходящий сушильный аппарат, такой как распылительная сушилка или сублимационная сушилка, и превращают в порошок. Влагосодержание порошка должно составлять менее около 5 мас.%.
Если предпочтительной является жидкая композиция, гомогенизированную смесь можно стерилизовать, а затем асептически разливать в подходящие контейнеры или можно сначала разливать в контейнеры, а затем автоклавировать.
Конкретные липиды
Композиция изобретения может содержать выбранные липиды, оказывающие определенные эффекты.
К таким липидам могут, в частности, относиться DHA, ARA, линолевая кислота или сфингомиелин, предпочтительно в количестве, приемлемом для обеспечения реальных преимуществ для здоровья головного мозга и в пределах общих нормативных требований для данного типа продуктов (например, рекомендаций ВОЗ по детской смеси; CODEX или Европейских директив по детской смеси).
В некоторых вариантах осуществления композиция изобретения содержит относительно высокий уровень sn-2-пальмитата или сфингомиелина. Они были связаны с оптимальными показателями характеристик и развития головного мозга и могут давать синергетический эффект с обязательными соединениями композиции изобретения.
Хотя вскармливание младенца смесью, содержащей высокий процент sn-2-пальмитата (в отсутствие OF), помогает активировать рост бифидобактерий в толстой кишке, считается, что комбинация высокого содержания sn-2-пальмитата с олигофруктозой обеспечивает существенно более высокий рост бифидобактерий в толстой кишке у младенцев, находящихся на вскармливании смесью. Кроме того, может быть достигнуто значимое снижение количества потенциально патогенных бактерий. Было обнаружено, что вскармливание младенца детской смесью, имеющей высокий уровень содержания sn-2-пальмитата и от около 3 до около 5 г/л, или от около 0,4 до около 0,7 г/100 ккал олигофруктозы, более полезно по сравнению со вскармливанием младенца той же смесью без олигофруктозы. Без ограничения какой-либо теорией, такой синергетический эффект между OF и sn-2-пальмитатом может также активировать кратковременную память, в частности, (но скорее всего, не только) через влияние на микробиом субъекта и популяцию бифидобактерий. Термин «высокий уровень содержания sn-2-пальмитата» следует понимать как ингредиенты, имеющие высокую процентную долю жирных кислот (предпочтительно более 33% жирных кислот) в виде пальмитата в sn-2-положении триглицеридов. Такие ингредиенты доступны в продаже под торговым наименованием BETAPOL® (Loders Croklaan, г. Вормервер, Нидерланды) или INFAT® (Advanced Lipids AB, г. Карлсхамн, Швеция, совместное предприятие AAK B.V. (г. Заандейк, Нидерланды) и Enzymotec Inc, г. Морристаун, США).
Недавние клинические исследования с участием младенцев показали, что питательные смеси, содержащие по меньшей мере одну жирную кислоту омега-6 и по меньшей мере одну жирную кислоту омега-3 в соотношении от около 6 до около 1, повышают накопление DHA в эритроцитах и плазме крови. Сбалансированное соотношение около 6 : 1 омега-6 жирных кислот и омега-3 жирных кислот также может обеспечивать долговременные полезные для здоровья эффекты, включая оптимальное развитие мозга и нервной системы. Такой баланс будет достигнут путем составления композиций настоящего изобретения с источниками жира из растительных масел, которые в своем составе имеют жирные кислоты омега-6, такие как, например, соевое масло и подсолнечное масло, и которые в своем составе имеют жирные кислоты омега-3, например рапс, канола, льняное семя, чиа, перла или грецкие орехи. Для обеспечения модифицированной жировой смеси будет применена уникальная жировая смесь с 5 разными маслами.
Следующие примеры представлены для иллюстрации определенных вариантов осуществления и признаков настоящего изобретения, но их не следует толковать как ограничивающие объем настоящего изобретения.
Примеры
Пример 1. Питательная композиция, содержащая ОГМ (2FL и/или LNnT)
Питательная композиция изобретения, содержащая ОГМ 2FL и/или LNnT и OF, представлена в таблице 1 ниже. Эта композиция приведена исключительно в качестве иллюстрации. Композиция по таблице 1 может представлять собой детскую смесь. В альтернативном варианте осуществления она может быть подобрана с возможностью применения в качестве смеси для прикармливаемых детей.
Таблица 1
0,01 или 0,07
0,1 или 0,5
Пример 2. Детская смесь, содержащая ОГМ (2 FL и/или LNnT), необязательные BMO и/или олигофруктозу (OF)
Питательная композиция изобретения, содержащая ОГМ (2FL и/или LNnT) и необязательно OF и/или BMO, представлена в таблице 2 ниже. Эта композиция приведена исключительно в качестве иллюстрации. Композиция, показанная в таблице 2, представляет собой детскую смесь. В альтернативном варианте осуществления она может быть подобрана с возможностью применения в качестве смеси для прикармливаемых детей.
Другой пример основан на коммерческих детских смесях NAN и/или лактогенных детских смесях (производства Nestlé, Швейцария), к которым добавляют специфические олигосахариды изобретения в количестве, указанном ниже.
Таблица 2
Beneo-Orafti® P95 и Inulin Beneo-Orafti®) (необязательно)
30
200
Экспериментальные данные
В исследовании на поросятах исследовали влияние различных олигосахаридов, содержащих ОГМ (например, 2FL) с добавлением OF и/или BMO или без такового, на экспрессию гена в гиппокампе. Тридцать шесть поросят-самцов (по 12 на экспериментальную группу) от момента через 48 ч после опороса до возраста 33 дня получали контрольное вещество (CON, заменитель молока для домашнего скота Purina ProNurse), ОГМ (CON + 1,5 г/л ОГМ (состояли из 1,0 г/л 2’FL + 0,5 г/л LNnT), OF [CON + 5 г/л OF], OF + ОГМ [CON + 5 г/л OF + 1,0 г/л ОГМ (2’FL), BMO (6,5 г/л BMO) или ОГМ + BMO (1,0 г/л 2’FL + 0,5 г/л LNnT + 6,5 г/л BMO). Все рационы питания содержали запас для изменения состава 8,0 г/л, которое было зарезервировано для добавления испытуемых компонентов рациона. Поросят вскармливали, давая 285 мл и 325 мл разведенного рациона на кг массы тела на 2–6-е сутки после рождения (PND 2–6) и 7–33-и сутки после рождения (PND 7–33) соответственно. Поросят умерщвляли на 32-й или 33-й день и отбирали ткань гиппокампа для анализа экспрессии мРНК.
Смесь BMO, примененная в молочных смесях, была получена из сыворотки коровьего молока. Вкратце, ультрафильтрат коровьей сыворотки, включая олигосахариды, такие как 3′- и 6′-сиалиллактоза и GOS, деминерализовали комбинацией электродиализа и ионного обмена, как описано в данной области техники.
Экспрессия гена в гиппокампе
Приблизительно 20 мг ткани гиппокампа вводили в пробирку Lysing Matrix D (MP Biomedicals, г. Санта-Ана, штат Калифорния, США), помещали на лед и добавляли 650 мкл лизирующего буфера (Agencourt RNAdvance Tissue Kit, Beckman Coulter, г. Индианаполис, штат Индиана, США). Пробирки встряхивали 2 x 1 минуту на скорости 6 на FastPrep®-24 (MP Biomedicals, г. Санта-Ана, штат Калифорния, США), а затем 400 мкл лизата экстрагировали с применением Agencourt RNAdvance Tissue Kit (Beckman Coulter, г. Индианаполис, штат Индиана, США) в соответствии с рекомендациями производителя. РНК количественно определяли с применением Quant-iT™ RiboGreen™ RNA Assay Kit (Invitrogen, г. Карлсбад, штат Калифорния, США) на Spectramax M2 (Molecular Devices, г. Саннивейл, штат Калифорния, США). Оценку качества РНК проводили с помощью Fragment Analyzer 96 с применением Standard Sensitivity RNA Analysis Kit (15 nt) (Advanced Analytical Technologies, Inc., г. Анкени, штат Айова, США). Относительное число копий мРНК для 93 генов количественно определяли с применением системы NanoString nCounter™ (NanoString Technologies Inc., г. Сиэтл, штат Вашингтон, США) в соответствии с инструкциями производителя, с применением 100 нг РНК в качестве исходного количества.
Результаты
Рационы ОГМ, BMO, BMO + ОГМ и OF + ОГМ продемонстрировали различное влияние на экспрессию генов по сравнению с контрольной группой CON. Экспрессия в гиппокампе мРНК нескольких ключевых генов, участвующих в ГАМКергический системе, показана на фиг. 1 для субъединицы 1 ГАМК-рецептора типа В (GABBR1) и на фиг. 2 для субъединицы Beta2 ГАМК-рецептора типа А (GABRB2). Введение ОГМ, предпочтительно в комбинации с пребиотиком, таким как OF и/или BMO, имеет удивительную способность модулировать ГАМКергическую систему на уровне экспрессии.
На фиг. 1 показано, что экспрессия мРНК гена рецептора GABBR1 либо сохраняется, либо даже значительно возрастает по сравнению с контрольным рационом (CON), если в тестовом рационе также присутствует ОГМ, отдельно (2'FL + LNnt), либо в комбинации с OF или BMO.
На фиг. 2 показано, что экспрессия мРНК гена рецептора GABRB2 особенно повышается по сравнению с контрольным рационом при введении ОГМ в комбинации с BMO.
Следует понимать, что один или более примеров в описании не имеют ограничительного характера и что настоящее описание должно охватывать варианты и эквиваленты этих примеров.
Изобретение относится к питательной композиции, содержащей олигосахарид грудного молока (ОГМ). Питательная композиция, содержащая олигосахарид грудного молока (ОГМ) применяется для улучшения, усиления, стимуляции или модуляции ГАМКергической функции в центральной нервной системе (ЦНС) у млекопитающего, предпочтительно у человеческого младенца или ребёнка младшего возраста с рождения до 7 лет. Питательная композиция, содержащая олигосахарид грудного молока (ОГМ), применяется также для предотвращения, профилактики или компенсации синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении у нуждающихся в этом субъектов. 3 н. и 11 з.п. ф-лы, 2 ил., 2 табл., 1 пр.
1. Применение питательной композиции, содержащей олигосахарид грудного молока (ОГМ), у млекопитающего, предпочтительно у человеческого младенца или ребёнка младшего возраста с рождения до 7 лет, для улучшения, усиления, стимуляции или модуляции ГАМКергической функции в центральной нервной системе (ЦНС).
2. Применение питательной композиции, содержащей олигосахарид грудного молока (ОГМ), у млекопитающего, предпочтительно человеческого младенца или ребёнка младшего возраста с рождения до 7 лет, для предотвращения, профилактики или компенсации синдрома дефицита внимания и гиперактивности, расстройств аутического спектра, а также шизофрении у нуждающихся в этом субъектов, предпочтительно путем стимуляции или модуляции ГАМКергических функций в ЦНС.
3. Применение питательной композиции по п. 1 или 2, причем указанная ГАМКергическая функция в ЦНС предусматривает фильтрацию информации или способность фокусироваться или концентрироваться на умственной или физической активности.
4. Применение питательной композиции по любому из пп. 1-3, причем указанный ОГМ выбран из группы, состоящей из N-ацетиллактозамина, сиалилированных олигосахаридов, фукозилированных олигосахаридов или их комбинации.
5. Применение питательной композиции по п. 4, причем ОГМ представляет собой фукозилированный олигосахарид, выбранный из группы, состоящей из фукозилированных олигосахаридов, 2’-фукозиллактозы, 3’фукозиллактозы, дифукозиллактозы, лакто-N-фукопентаозы I, лакто-N-фукопентаозы II, лакто-N-фукопентаозы III, лакто-N-фукопентаозы V, лакто-N-фукогексаозы, лакто-N-дифукогексаозы I, фукозиллакто-N-гексаозы, фукозиллакто-N-неогексаозы I, фукозиллакто-N-неогексаозы II, дифукозиллакто-N-гексаозы I, дифукозиллакто-N-неогексаозы I, дифукозиллакто-N-неогексаозы II, фукозил-пара-лакто-N-гексаозы и любой их комбинации, N-5 ацетилированных олигосахаридов, таких как лакто-N-тетраоза (LNT), N-неотетраоза (LNnT) и любая их комбинация, и предпочтительно фукозилированный олигосахарид выбран из 2’-фукозиллактозы (2-FL), diFL, LNnT, LNT и любой их комбинации.
6. Применение питательной композиции по п. 4, причем ОГМ представляет собой N-ацетиллактозамин, выбранный из группы, состоящей из лакто-N-тетраозы (LNT) и лакто-N-неотетраозы (LNnT).
7. Применение питательной композиции по п. 4, причем ОГМ представляет собой сиалилированный олигосахарид, предпочтительно выбранный из группы, состоящей из 3’-сиалиллактозы и 6’-сиалиллактозы, и более предпочтительно указанная композиция содержит как 3’-сиалиллактозу, так и 6’-сиалиллактозу, причем соотношение 3’-сиалиллактозы и 6’-сиалиллактозы предпочтительно находится в диапазоне от 100 : 1 до 1 : 100, более предпочтительно от 10 : 1 до 1 : 10, еще более предпочтительно от 5 : 1 до 1 : 2.
8. Применение питательной композиции по любому из предшествующих пунктов, причем количество ОГМ составляет от 0,01 до 50 г/л, от 0,1 до 10 г/л, от 0,3 до 5 г/л, или от 0,5 до 1 г/л, или 0,25, или 0,5, или 1, или 1,5, или 2 г/л.
9. Применение питательной композиции по любому из предшествующих пунктов, которая дополнительно содержит пребиотик, причем указанный пребиотик предпочтительно выбран из перечня, состоящего из олигосахарида коровьего молока (BMO), инулина, ксилоолигосахаридов, полидекстрозы, фруктозного олигосахарида (FOS) или олигофруктозы (OF) или любой их комбинации.
10. Применение питательной композиции по п. 9, причем указанный BMO предусматривает N-ацетилированный олигосахарид, галактоолигосахарид, сиалилированный олигосахарид, фукозилированный олигосахарид или их комбинацию.
11. Применение питательной композиции по любому из предшествующих пунктов, которая дополнительно содержит пробиотик, причем пробиотик предпочтительно выбран из перечня, состоящего из Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Streptococcus, Kluyveromyces, Saccharomyces, Candida, в частности выбран из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactococcus lactis, Enterococcus faecium, Saccharomyces cerevisiae, Saccharomyces boulardii или их смесей, предпочтительно выбран из группы, состоящей из Bifidobacterium longum NCC3001 (ATCC BAA-999), Bifidobacterium longum NCC2705 (CNCM I-2618), Bifidobacterium longum NCC490 (CNCM I-2170), Bifidobacterium lactis NCC2818 (CNCM I-3446), Bifidobacterium breve штамм A, Lactobacillus paracasei NCC2461 (CNCM I-2116), Lactobacillus johnsonii NCC533 (CNCM I-1225), Lactobacillus rhamnosus GG (ATCC53103), Lactobacillus rhamnosus NCC4007 (CGMCC 1.3724), Enterococcus faecium SF 68 (NCC2768; NCIMB10415) и их комбинаций.
12. Применение питательной композиции по любому из предшествующих пунктов, причем млекопитающее представляет собой человека, домашнее животное, кошку или собаку, причем предпочтительно млекопитающее представляет собой молодое млекопитающее, более предпочтительно младенца или ребёнка младшего возраста.
13. Применение питательной композиции по любому из предшествующих пунктов, причем указанная композиция представляет собой детскую смесь, смесь для прикармливаемых детей, обогатитель грудного молока, молочную смесь для детей от 1 до 3 лет или корм или добавку для домашних животных.
14. Применение олигосахарида грудного молока (ОГМ) для получения питательной композиции для улучшения, усиления, стимуляции или модулирования ГАМКергической функции в ЦНС у нуждающегося в этом субъекта, предпочтительно у человеческого младенца или ребёнка младшего возраста с рождения до 7 лет.
| US 20180103675 A1, 19.04.2018 | |||
| WO 2016146789 A1, 22.09.2016 | |||
| WO 2016066735 A1, 06.05.2016 | |||
| WO 2015086789 A1, 18.06.2015 | |||
| КОМПОЗИЦИЯ ПРЕБИОТИКОВ ДЛЯ НОРМАЛИЗАЦИИ МИКРОФЛОРЫ ОРГАНИЗМА | 2011 |
|
RU2473347C1 |
Авторы
Даты
2023-12-25—Публикация
2019-05-21—Подача