Изобретение относится к области химии полимеров, биохимии и медицины, а именно к способу получения инсулинсодержащей композиции, которую используют для лечения сахарного диабета путем перорального введения инсулина.
В настоящее время, по данным ВОЗ, в мире около 300 миллионов человек страдают сахарным диабетом, названным «неинфекционной эпидемией XX и XXI вв.», а по прогнозам к 2025 году количество больных диабетом вырастет до 435 миллионов. Лечение сахарного диабета сейчас, в основном, сводится к периодическим (несколько раз в сутки) инъекциям инсулина. И хотя такой способ лечения позволяет сохранить жизни большинству больным, введение инсулина непосредственно в кровоток имеет принципиальный недостаток.
Обычно (в норме) инсулин из поджелудочной железы сначала попадает в печень через кровеносные сосуды, соединенные с портальной печеночной веной. Через ту же вену в печень транспортируются продукты пищеварения. Поскольку основной функцией инсулина является регулирование последующих трансформаций продуктов пищеварения, то в естественных условиях оба эти компонента попадают в печень одновременно. Печень, в свою очередь, контролирует количество инсулина, достигающего других органов и тканей. При инъекционном же введении инсулина, а это практически единственный способ лечения сахарного диабета, такой контроль отсутствует, что и является причиной таких осложнений при сахарном диабете, как сердечно-сосудистые заболевания, расстройство функций головного мозга и т.д.
Единственной возможностью подключения печени к распределению инсулина является пероральное введение гормона, моделирующее естественный путь секреции инсулина [Saffran М., Pansky В., Colin Budd G., Williams F.E. // Insulin and gastrointestinal tract / Journal of Controlled release. 1997, V. 46. №1. Р. 89-98].
Известен способ получения инсулинсодержащей композиции иммобилизацией инсулина в гидрогеле на основе карбоксиметилцеллюлозы и полиакриловой кислоты [Gao X., Cao Y., Song X., Zhang Z., Zhuang X., He С., Chen X. Biodegradable, pH-responsive carboxymethyl cellulose/poly(acrylic.acid) hydrogels for oral insulin delivery // Macromolecular Bioscience. 2014. V. 14. №4. P. 565-575].
Недостатком этого способа является невысокая эффективность действия композиции при пероральном введении по сравнению с инъекцией раствора инсулина. Снижение концентрации глюкозы в крови наблюдалось в течение шести часов после введения композиции.
Известен способ получения инсулинсодержащей композиции иммобилизацией инсулина в гидрогеле на основе альгинат-декстран сульфата, связанного в комплекс с хитозан-полиэтиленгликоль-альбумином [Reis С.Р., Veiga F.J.., Ribeiro A.J., Neufeld R.J., Christiane  C. Affiliation Nanoparticulate biopolymers deliver insulin orally eliciting pharmacological response // Journal of Pharmaceutical Science. 2008. V. 97. №12. Р. 5290-5305].
C. Affiliation Nanoparticulate biopolymers deliver insulin orally eliciting pharmacological response // Journal of Pharmaceutical Science. 2008. V. 97. №12. Р. 5290-5305].
Недостатком этого способа является невысокая эффективность действия композиции при пероральном введении по сравнению с инъекцией раствора инсулина. Максимальное снижение концентрации глюкозы в крови наблюдалось через 14 часов после перорального введении композиции.
Наиболее близким по технической сущности и достигаемым результатам является способ получения инсулинсодержащей композиции иммобилизацией инсулина в объеме сшитого полиакриламида, модифицированного овомукоидом из белка утиных яиц [Патент РФ №2066551, А61K 38/28, А61K 38/55, опубл. 20.09.1996, Бюл. №26].
Недостатком известного способа является невысокая эффективность действия инсулинсодержащей композиции при пероральном введении. Так, если при инъекции раствора инсулина животным максимальное снижение уровня глюкозы в крови достигается через 30-45 минут, то при пероральном введении инсулинсодержащей композиции максимальное снижение уровня глюкозы достигается через 80-90 минут.
Задачей изобретения является повышение эффективности действия инсулинсодержащей композиции при пероральном введении, что выражается в ускорении снижения уровня глюкозы в крови.
Решение поставленной задачи достигается тем, что в способе получения инсулинсодержащей композиции иммобилизацией инсулина в объеме сшитого полиакриламида, модифицированного овомукоидом из белка утиных яиц, сшитый полиакриламид дополнительно модифицирован меркаптоуксусной кислотой путем радикальной полимеризации при комнатной температуре под действием окислительно-восстановительного катализатора полимеризации водного раствора, содержащего, г/ 100 мл: акриламид - 7,0-10,0, N,N'-метиленбисакриламид - 0,8-1,0, овомукоид из белка утиных яиц, ацилированный хлорангидридом акриловой кислоты - 0,4-0,8, меркаптоуксусная кислота - 0,01-0,12, с последующим измельчением образующегося гидрогеля, промыванием его бикарбонатным буфером и высушиванием.
Известен сшитый полиакриламид, модифицированный овомукоидом из белка утиных яиц и меркаптоуксусной кислотой, получаемый путем радикальной полимеризации при комнатной температуре под действием окислительно-восстановительного катализатора полимеризации водного раствора, с последующим измельчением образующегося гидрогеля и промыванием его бикарбонатным буфером до полного удаления непрореагировавших соединений [Патент РФ №2484475 C1, G01N 33/53, C12N 11/0, опубл. 10.06.2013, Бюл. №16].
Однако применение полиакриламида, модифицированного овомукоидом из белка утиных яиц и меркаптоуксусной кислотой, в инсулинсодержащей композиции для перорального введения не известно из уровня техники и приводит к неожиданному техническому результату - повышение эффективности действия инсулинсодержащей композициия за счет уменьшения времени максимального снижения концентрации глюкозы в крови при пероральном введении до 30-45 минут (времени, близкого ко времени максимального снижения концентрации глюкозы в крови при инъекции раствора инсулина).
В таблице 1 приведены составы конкретных смесей при получении модифицированного сшитого полиакриламида и свойства получаемого гидрогеля.
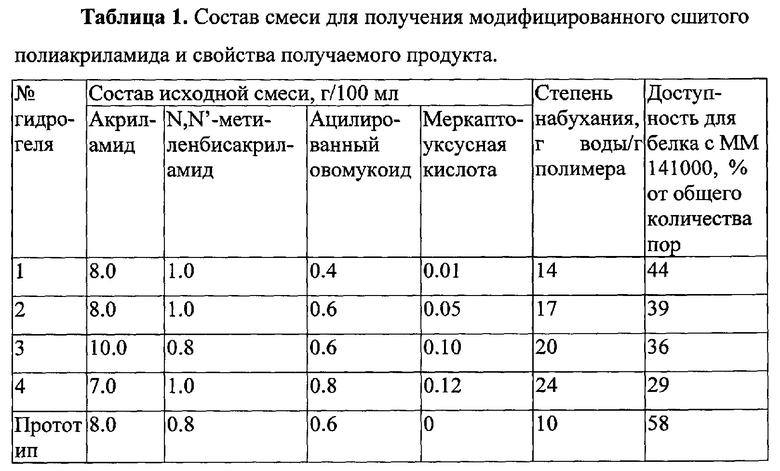
Модифицированный сшитый полиакриламид получают путем радикальной полимеризации при комнатной температуре под действием окислительно-восстановительного катализатора полимеризации: N,N,N,N-тетраметилэтилендиамин-персульфат аммония.
Степень набухания гидрогелей оценивают гравиметрически и рассчитывают по формуле: Sr=m1/m2-1, где m1 и m2 - массы равновесно набухшего и лиофильно высушенного гидрогеля, соответственно.
Для изучения проницаемости к 2 мл геля, набухшего в 0.5 М бикарбонате аммония, рН 8.0, добавляют 4 мл раствора белка в том же буфере. Смесь оставляют при 4°C до установления постоянного значения оптической плотности раствора белка при 280 нм (обычно не более 48 ч). Концентрацию белка в исходном растворе и после его инкубации с гелем оценивают с использованием калибровочной зависимости. Учитывая соотношения объемов используемых фаз, рассчитывают количество пор, доступных для белка, принимая за 100% их количество, доступных для воды.
По сравнению с прототипом модифицированный полиакриламидный гидрогель имеет повышенную степень набухания и пониженное содержание пор большого размера.
Пример 1
0.5 г лиофильно высушенного полиакриламидного гидрогеля №1, модифицированного овомукоидом и меркаптоуксусной кислотой, помещают в 15.0 мл водного раствора инсулина (активность инсулина равна 25 Ед/мг) с концентрацией 0.5 мг/мл на 1 час при комнатной температуре. В течение этого времени полимер полностью набухает в растворе и готов к употреблению.
Синтезированный гидрогель отделяют от раствора инсулина и вводят перорально с помощью катетера кроликам-самцам Шиншилла, массой 2.0-3.1 кг в количестве, соответствующем 5 Ед. инсулина на кг массы животного. Образцы крови забирают через 30, 45, 65, 80 и 90 минут. Концентрацию глюкозы в крови определяют с помощью глюкометра One Touch («Johnson & Johnson», США). Результаты представлены в таблице 2.
Примеры 2-4
Процесс проводят по примеру 1, используя модифицированные полиакриламидные гидрогели №2-4. Результаты приведены в таблице 2.
Пример 5 (контрольный).
Процесс проводят по примеру 1, используя модифицированную инсулинсодержащую композицию, полученную по способу-прототипу. Результаты приведены в таблице 2.
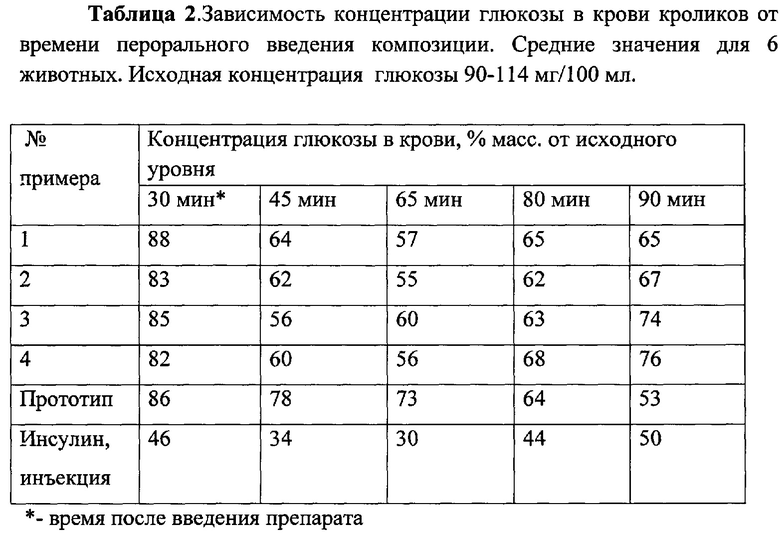
Из табл. 2 видно, что использование предложенного способа позволяет получать инсулинсодержащую композицию с повышенной эффективностью при его пероральном применении. Так, если при использовании композиции, полученной по способу-прототипу, время максимального снижения концентрации глюкозы в крови составляет 80-90 мин, то при использовании гидрогеля, полученного по предложенному способу, это время равно 30-35 мин, что сопоставимо с обычно наблюдаемым временем при инъекционном введении раствора инсулина. Однако при этом, как и для всех перорально вводимых препаратов инсулина, сохраняется физиологический путь поступления инсулина в кровоток (табл. 3).
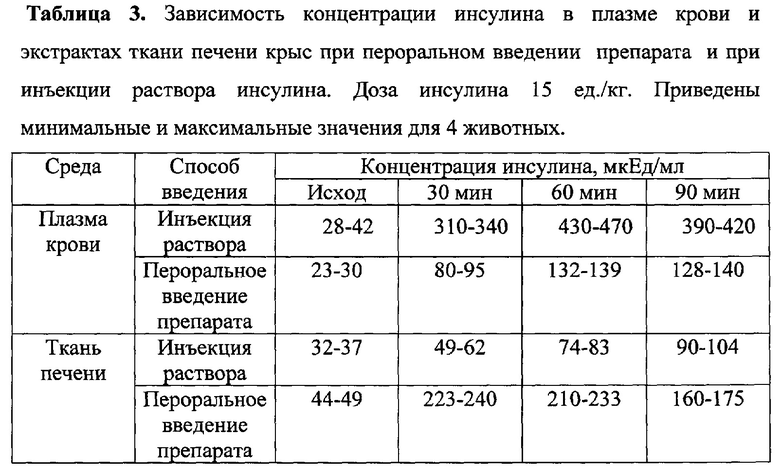
Видно, что если при инъекционном введении инсулин сразу проникает в кровоток, то при пероральном введении инсулин первоначально попадает в печень, подключая ее к распределению инсулина в организме и снижая тем самым риски часто наблюдаемых осложнений при лечении сахарного диабета.
Возможность перорального введения инсулина не только создает большие удобства для больных сахарным диабетом, но и позволяет усовершенствовать стратегию лечения этого заболевания.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНСОДЕРЖАЩИХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1994 |
|
RU2066551C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ, СОДЕРЖАЩИХ ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА | 2007 |
|
RU2342147C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГИДРОГЕЛЕВОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2014 |
|
RU2567623C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГИДРОГЕЛЕВОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2012 |
|
RU2484475C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИНСУЛИНА | 1994 |
|
RU2076733C1 |
| ТВЕРДОЕ ИНСУЛИНСОДЕРЖАЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1997 |
|
RU2117488C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЛЮКОЗОЧУВСТВИТЕЛЬНЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 2017 |
|
RU2652126C1 |
| ПОЛИПЕПТИДНАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2171687C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГЕМОСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2018 |
|
RU2681883C1 |
| ИНСУЛИНСОДЕРЖАЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2155602C1 |
Изобретение относится к фармацевтической промышленности, а именно к способу получения инсулинсодержащей композиции. Способ получения инсулинсодержащей композиции, включающий иммобилизацию инсулина в объеме сшитого полиакриламида, модифицированного овомукоидом из белка утиных яиц, при чем сшитый полиакриламид дополнительно модифицирован меркаптоуксусной кислотой путем радикальной полимеризации при комнатной температуре под действием окислительно-восстановительного катализатора полимеризации водного раствора с последующим измельчением образующегося гидрогеля, промыванием его бикарбонатным буфером и высушиванием, при этом водный раствор содержит: акриламид; N,N'-метиленбисакриламид; овомукоид из белка утиных яиц, ацилированный хлорангидридом акриловой кислоты; меркаптоуксусная кислота, взятые в определенном соотношении. Вышеописанный способ позволяет повысить эффективность действия инсулинсодержащей композиции за счет уменьшения времени максимального снижения концентрации глюкозы в крови при пероральном введении до 30-45 минут. 3 табл., 5 пр.
Способ получения инсулинсодержащей композиции иммобилизацией инсулина в объеме сшитого полиакриламида, модифицированного овомукоидом из белка утиных яиц, отличающийся тем, что сшитый полиакриламид дополнительно модифицирован меркаптоуксусной кислотой путем радикальной полимеризации при комнатной температуре под действием окислительно-восстановительного катализатора полимеризации водного раствора, содержащего, г/100 мл: акриламид - 7,0-10,0, N,N'-метиленбисакриламид - 0,8-1,0, овомукоид из белка утиных яиц, ацилированный хлорангидридом акриловой кислоты - 0,4-0,8, меркаптоуксусная кислота - 0,01-0,12, с последующим измельчением образующегося гидрогеля, промыванием его бикарбонатным буфером и высушиванием.
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНСОДЕРЖАЩИХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1994 |
|
RU2066551C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГЕМОСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2018 |
|
RU2681883C1 |
| РАСТВОР ИНСУЛИНА ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2005 |
|
RU2288000C1 |
| Creenley R.Z., Brown J.M, Garbow I., Vogt C.E., Zia H., Rodgers R.L., Christie M., Luzzi L.A., Polymer Matrices for orol delivery// Polymer Preprits 1990, V.31, N 2, р | |||
| Затвор для дверей холодильных камер | 1920 |
|
SU182A1 |
Авторы
Даты
2021-07-28—Публикация
2020-10-21—Подача