Изобретение относится к медицинскому диагностическому оборудованию, в частности к системам скрининга состояния сердечно-сосудистой системы человека в режиме реального времени с автоматической диагностикой патологических изменений на электрокардиограмме для раннего выявления, предупреждения и диагностики заболеваний сердечно-сосудистой системы человека.
Известен способ предварительной обработки электрокардиосигнала для персональных носимых кардиомониторов (RU 2624809 C1), заключающийся в том, что с датчиков ЭКГ снимают электрокардиосигналы, усиливают их, проводят первичную аналоговую обработку, характеризующийся тем, что аналоговый сигнал дискретизируют по амплитуде и по времени для перевода в цифровой сигнал, корректируют дрейф изолинии путем определения скользящего среднего на прямоугольном временном окне длительностью N1 в 30 дискретных отсчетов с последующим его вычитанием из входного сигнала, затем проводят адаптивную нормализацию сигналов R-пиков, для чего на каждом шаге дискретизации определяют скользящий максимум Amax(i) на прямоугольном окне N2 в 300 дискретных отсчетов и умножают значения каждого текущего отсчета окна N2 на коэффициент Gi=1/Amax(i), далее устраняют шумовые и высокочастотные наводки путем оценки для каждого текущего отсчета i разности ΔSi между площадью сигналов SN3 в рамках скользящего прямоугольного окна N3 в 15 дискретных отсчетов симметрично по семь отсчетов вправо и влево относительно текущего отсчета и ее средним значением SN1 ср. на скользящем окне N1, при этом, если разность ΔSi составляет величину более двух, оставляют исходную форму сигнала, а менее двух - заменяют на среднее значение сигнала в скользящем окне N1, затем осуществляют локализацию положения R-пиков пороговым детектированием по уровню 0,5, выбором максимума пиков из каждых пяти рядом расположенных отсчетов и определением временного расположения максимума, после этого удаляют нетипичные кардиоциклы и далее проводят извлечение информации, относящейся к сердечным сокращениям пользователя.
Основным недостатком известного способа является диагностика только по двум отведениям.
Известен переносной прибор «РИТМЕР» (https://ritmer.ru), позволяющий, в том числе, анализировать сердечную активность и определять случаи нестандартной активности сердца (в том числе бессимптомной).
Прибор «РИТМЕР» имеет ряд недостатков, в частности:
- количество распознаваемых патологий ограничено, что связано с диагностикой только по одному-трем отведениям ЭКГ (например, ограничена оценка ишемии миокарда)
- время непрерывной записи сигнала ЭКГ менее 15 часов;
- пользователь не имеет доступа к нативному сигналу ЭКГ в мобильном приложении, кроме короткого 5 минутного отрезка электрокардиосигнала, а видит только уже сформированное заключение и рекомендации;
- нет варианта передачи данных с мобильного кардиорегистратора на базовую микрокомпьютерную станцию вместо смартфона.
Известен прибор «Доктор «Спайдер» («Doctor Spyder», см., например: http://spyder-ecg.ru/#about), представляющий собой онлайн регистратор ЭКГ для длительного амбулаторного ЭКГ мониторирования и сбора полноценной информации о состоянии сердечно-сосудистой системы пациента. Прибор позволяет своевременно выявлять нарушения ритма и проводимости сердца, например, такие как:
- преходящая/постоянная форма фибрилляции предсердий;
- пароксизмальные тахикардии;
- преходящая блокада сердца;
- дисфункция синусового узла;
- диагностика аритмогенных синкопальных состояний.
К недостаткам данного прибора следует отнести:
- отсутствие возможности снятия ЭКГ в 12 отведениях;
- отсутствие возможности оценки ишемии миокарда по ЭКГ;
- отсутствие возможности записи сигнала ЭКГ на внутреннюю память прибора (если пациент удаляется от принимающего смартфона на расстояние более 5 метров запись ЭКГ теряется);
- нет варианта передачи данных с мобильного кардиорегистратора на базовую микрокомпьютерную станцию вместо смартфона.
В качестве прототипа выбрано носимое электронное устройство для получения электрокардиографических (ЭКГ) измерений (RU 197114 U1), содержащее корпус, закрепляемый на запястье пользователя, в котором установлены:
дисплей, обеспечивающий отображение информации;
микроконтроллер, выполняющий управление электронным устройством;
АЦП, обеспечивающий преобразование в цифровой вид сигналов, поступающих с электродов;
средство хранения данных, выполненное с возможностью хранения данных ЭКГ;
модуль беспроводной связи, обеспечивающий передачу данных из средства памяти на внешнее вычислительное устройство;
первый электрод, совмещенный с емкостной кнопкой, обеспечивающей активацию функции снятия ЭКГ и управление устройством;
второй и третий электроды, расположенные на тыльной стороне корпуса и обеспечивающие совместно с первым электродом регистрацию ЭКГ;
аккумулятор;
разъем для подключения внешних электродов, обеспечивающих регистрацию ЭКГ.
По существу, известное решение-прототип представляет собой аппаратно-программный комплекс, позволяющий принимать сигналы датчиков ЭКГ, обрабатывать их и передавать на удаленные (внешние) устройства: смартфон, планшет, или персональный компьютер.
Устройство, описанное в патенте RU 197114 U1 имеет следующие заявленные технические характеристики: «полоса частот амплитудно-частотных характеристик для обоих каналов аналоговых интерфейсов (109)-(110) составляет 0,67-320 Гц, с допустимыми отклонениями амплитуд 0.67 Гц-1 Гц +/-10%, 1 Гц -320 Гц - +/-1%. Частота дискретизации сигнала 1000 Гц.». Такие характеристики не позволяют реализовать алгоритмы диагностики сложных нарушений ритма, основанные на анализе ЭКГ высокого разрешения.
Задачей изобретения являлось создание прибора (аппаратно-программного комплекса), позволяющего реализовать технологию анализа данных ЭКГ высокого разрешения; в автоматическом режиме без участия врача-эксперта выявлять предикторы внезапной сердечной смерти, выявлять поздние потенциалы возбуждения желудочков, повысить уровень детектирования патологических наджелудочковых ритмов до 98,7% в автоматическом режиме диагностики.
Кроме того, стояла задача передачи большого массива данных в режиме реального времени без потери или искажения исходного сигнала ЭКГ (при передаче длительных записей (более 24 часов) через беспроводные каналы связи, возможны разрывы соединения и как следствие потеря времени на восстановление соединения и повторную передачу данных).
Кроме того, существует необходимость создание интеллектуального электрокардиографа, т.е. автоматизированной системы расшифровки сигналов электрокардиограммы (ЭКГ) с получением заключения, максимально приближенного к врачебному.
Указанная задача решается аппаратно-программным комплексом электрокардиографических (ЭКГ) измерений, содержащим корпус, закрепляемый на пользователе, в котором установлены: микроконтроллер, выполняющий управление электронным устройством; аналого-цифровой преобразователь, обеспечивающий преобразование в цифровой вид сигналов, поступающих с электродов; средство хранения данных, выполненное с возможностью хранения данных ЭКГ; модуль беспроводной связи, обеспечивающий передачу данных из средства памяти на внешнее вычислительное устройство; первый электрод, совмещенный с емкостной кнопкой, обеспечивающей активацию функции снятия ЭКГ устройством; второй и третий электроды, расположенные на тыльной стороне корпуса и обеспечивающие совместно с первым электродом регистрацию ЭКГ; аккумулятор; разъем для подключения внешних электродов, обеспечивающих регистрацию ЭКГ, в котором, полоса частот амплитудно-частотных характеристик для всех каналов аналоговых интерфейсов составляет 0-4000 Гц, с допустимыми отклонениями амплитуд от 0 до 2000 Гц ±10%,частота дискретизации сигнала 8000 Гц. При этом микроконтроллер и средство хранения данных выполнены с возможностью записи, чтения и передачи данных ЭКГ в параллельных потоках с приоритетом у процесса записи. Микроконтроллер также выполнен с возможностью реализации прямых алгоритмов диагностики, основанных на правилах и деревьях решений. Микроконтроллер также выполнен с возможностью подключения к блокам диагностики, реализующим методы машинного обучения.
К разъему для подключения внешних электродов возможно подключение кабеля с 7 контактами, позволяющими регистрировать 12 стандартных отведений ЭКГ.
Известно (теорема Котельникова-Шеннона), что при увеличении частоты дискретизации спектр шума квантования расширяется, и во столько же раз его спектральная плотность мощности уменьшается. При увеличении частоты дискретизации в 2 раза величина спектральной мощности шума уменьшается на 3 дБ или в 1,41 раза. В предлагаемом аппаратно-программном комплексе при увеличении частоты дискретизации со стандартных 1000 Гц до 8000 Гц величина спектральной мощности шума уменьшается на 12 дБ или в 3,98 раза.
Увеличении частоты дискретизации достигается применением интегрального аналого-цифрового преобразователя ADS1298IPAGR, содержащего в себе помимо самого модуля преобразователя еще аналоговою усилительную часть с возможностью гибкой настройки коэффициентов усиления, модуль коммутации (аналогового сложения и вычитания сигналов) для получения виртуальных потенциальных точек для снятия униполярных отведений электрокардиограммы и источник точного опорного напряжения. В сочетании с микроконтроллером STM32WB55C, имеющего ядро ARM CORTEX-M4, позволяющего достичь низкого энергопотребления при высокой производительности и встроенного в кристалл радиочастотного приемопередатчика ISM (Industrial, Scientific, Medical) диапазона, позволяющего осуществлять цифровую связь по стандартным протоколам Bluetooth, ZigBee, Thread. Сокращение шумов в сочетании с увеличением спектра обрабатываемого сигнала дает более точные результаты во многих методах автоматического исследования электрокардиограмм.
Наличие высоких частот дискретизации (более 4000 Гц) позволяет реализовать алгоритмы диагностики сложных нарушений ритма, основанные на анализе ЭКГ высокого разрешения. Среди методов повышения диагностической информативности электрокардиография высокого разрешения ЭКГ (ЭКГ ВР) заняла прочное место в медицинской деятельности и позволяет получить важную для диагностики информацию о больных. Усиленная электрокардиография требует регистрации ЭКГ сигналов с чувствительностью 50…100 мм/мВ. Такое усиление требуется для выявления низкоамплитудных элементов ЭКГ. Этим можно получить дополнительную информацию об электрической активности миокарда и выработать новые диагностические критерии, способствующие более точной интерпретации изменений ЭКГ.
В клинической электрокардиографии стала классической запись кривых при чувствительности электрокардиографа 10 мм/мВ. Выбор такого усиления не обусловлен какими-либо специальными техническими или медицинскими требованиями. Однако при подобной чувствительности некоторые элементы ЭКГ остаются невыраженными, что приводит к определенным трудностям при их оценке. В серийных приборах максимальная чувствительность ограничена требованиями 20 мм/мВ.
Для приборов ЭКГ ВР высокого класса требования к характеристикам таковы:
- подавление синфазных помех канала - от 80 до 120 дБ;
- уровень собственных шумов - от 10 до 1 мкВ;
Частотные характеристики усилителя соответствуют требованиям:
- полоса пропускания частот может регулироваться, в том числе расширяться в сторону снижения частот до 0 (с ручной компенсацией разностной инфранизкочастотной помехи) и в сторону верхних частот до 2000 Гц;
- максимальная чувствительность - 100 мм/мВ;
- минимальная - 10 мм/мВ;
- погрешность измерения амплитуды сигнала не более 10-50 мкВ;
- ошибки измерения интервалов времени, скорости движения носителя, эффективная ширина записи определяются характеристикой регистратора и могут быть не хуже, чем требуется по стандартам для кардиографов 1-го класса точности.
Технология анализа данных ЭКГ высокого разрешения позволяет в автоматическом режиме без участия врача эксперта выявлять предикторы внезапной сердечной смерти, выявлять поздние потенциалы возбуждения желудочков, повысить уровень детектирования патологических наджелудочковых ритмов до 98,7% в автоматическом режиме диагностики, а также прогнозировать риск развития пароксизмов наджелудочковых аритмий.
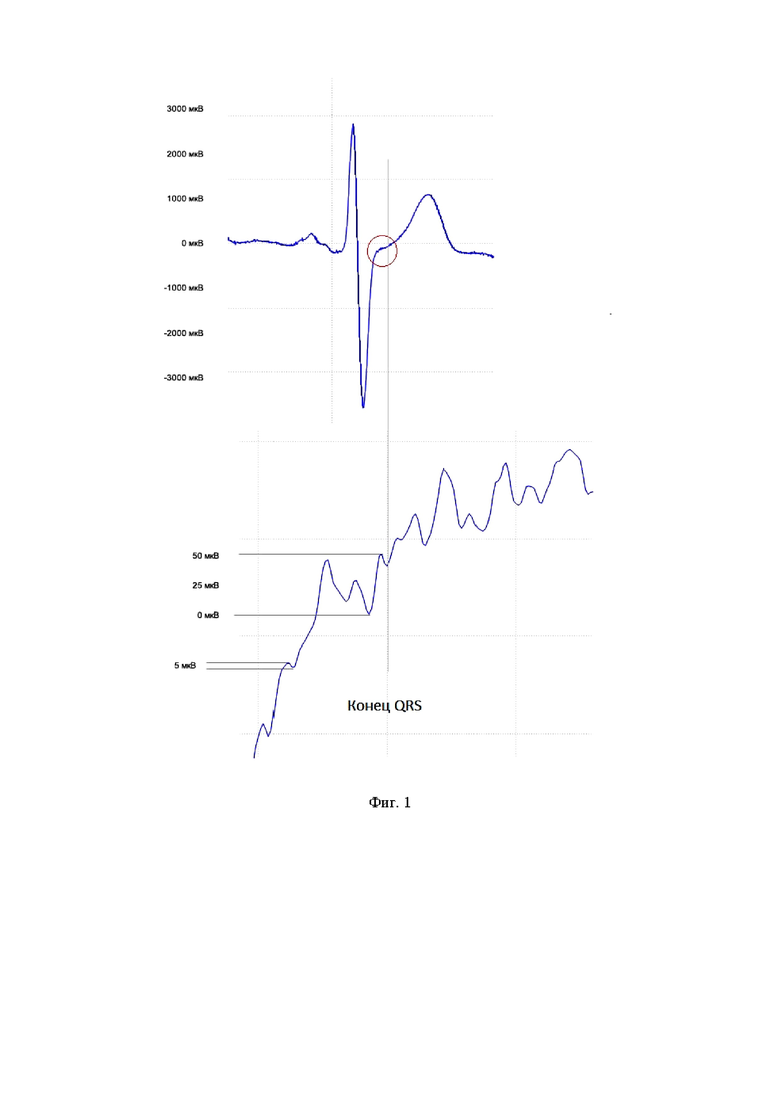
В настоящее время установлено, что субстратом возникновения и регистрации поздних потенциалов желудочков (ППЖ) служат электрофизиологическая и анатомическая неоднородность миокарда, когда здоровые кардиомиоциты перемежаются с ишемизированными или участками некроза и фиброза. Замедленная фрагментированная активность желудочков возникает при нарушении естественной параллельной ориентации миокардиальных волокон и разделении участков жизнеспособного миокарда соединительной тканью [De Chillou C., Sadoul N., Brianson S. et al. Factors determining the occurrence of late potentials on the signalaveraged electrocardiogram after a first myocardial infarction: a multivariate analysis // J. Amer. Coll. Cardiol. - 1991. - Vol. 18. - P. 1638-1642]. Появление ППЖ в отсутствии очаговых изменений миокарда можно объяснить негомогенностью электрофизиологических свойств миокарда вследствие неравномерных функциональных изменений кардиомиоцитов в условиях острой или хронической ишемии [Kondo N., Ikeda T., Kawase A. et al. Clinical usefulness of the combination of T-wave alternans and late potentials for identifying high-risk patients with moderately or severely impaired left ventricular function // Jpn. Circ. J. - 2001 Jul. - 65(7). - Р. 649-653.]. Кроме того, патогенетическим субстратом появления ППЖ могут быть микроочаги некроза и фиброза, возникающие в сердечной мышце на фоне повторных обострений длительно текущей ИБС. Подобные условия приводят к задержке и фрагментации электрических сигналов, замедлению распространения деполяризации, появлению поздней или следовой активности желудочков. Наличие зон задержанной желудочковой деполяризации способствует возникновению феномена “re-entry”, являющегося основной причиной злокачественных желудочковых нарушений ритма. Таким образом, ППЖ можно рассматривать в качестве неинвазивного маркера аритмогенеза. Для замедленных (фрагментированных) электрических сигналов характерны их малая продолжительность (40-180 мс), малая амплитуда (5-20 мкВ) и высокая частота (25-50 Гц). На обычной электрокардиограмме сигналы с подобными параметрами для анализа недоступны, необходимы усиление и фильтрация высокочастотного сигнала ЭКГ, т.е. ЭКГ высокого разрешения - ЭКГ ВР. Для выявления ППЖ при мониторинге ЭКГ используются показатели: длительность фильтрованного комплекса QRS(totQRS)>114 мс, длительность фильтрованного комплекса QRS на уровне 40 мкВ (LAS40)>38 мс, среднеквадратичная амплитуда последних 40 мс фильтрованного комплекса QRS(RMS40)<20 мкВ. О наличии ППЖ свидетельствует соблюдение двух из этих критериев. (см. фиг. 1)
Далее используются методы спектрального анализа ЭКГ и вейвлет-преобразования сигнала для автоматической диагностики ППЖ, и ППП (поздних потенциалов предсердий).
Спектральный анализ кардиосигналов - преобразование Фурье с разложением сигнала ЭКГ на составные синусоиды с различной частотой и амплитудой, что позволяет оценить спектральную плотность мощности составляющих кардиосигнала, высокочастотные компоненты, характерные для ППЖ. Выявление высокочастотного содержания спектра свидетельствует о существовании условий для фрагментирования электрической активности желудочков и развития нарушений ритма.
Методика спектрального анализа ППЖ - вейвлет-преобразование для составления частотно-временной карты сигнала, что позволяет по большому количеству кардиоциклов получать регистрацию ППЖ и анализировать. Метод предполагает точное исследование колебательных процессов различной периодичности, обеспечивает развертку исследуемого сигнала, при этом частота и координата рассматриваются как независимые переменные.
Наличие ППЖ позволяет прогнозировать риск развития желудочковых тахикардий. ППЖ могут использоваться в качестве диагностического критерия аритмогенной кардиомиопатии правого желудочка.
Проблема передачи массива данных в режиме реального времени без потерь решается следующим образом. Данные в первую очередь записываются в средство хранения данных (энергонезависимую память). При необходимости одновременной записи и чтения данных, например, при проведении исследования, включая данные, записанные произвольное время назад, запись и чтение производятся в параллельных потоках с приоритетом у процесса записи.
Данные при записи структурируются в виде отдельных файлов, содержащих короткие интервалы, что позволяет считывать произвольный момент записанного ЭКГ с высокой скоростью доступа. Запись осуществляется в единичных интервалах в размере кратном объему страницы энергонезависимой памяти.
Известно, что микросхемы энергонезависимой памяти больших объемов позволяют производить запись только большими блоками и при дополнительной записи в уже частично записанную страницу необходимо считать ранее записанные данные в оперативную память дополнить их новыми данными, произвести стирание страницы (стирание требует временных и энергетических затрат). При использовании высокой глубины дискретизации сигнала ЭКГ - 24 бита - требуется хранить и передавать большие объемы информации.
Для снижения объема можно использовать различные алгоритмы сжатия сигнала, что потребует много процессорного времени и повлечет высокие энергозатраты. Также, сжатие сигнала вносит нелинейные искажения в сжимаемый сигнал.
Задача решается вычислением максимальной скорости изменения сигнала (первой производной функции по времени) и восстановлением сигнала путем вычисления первообразной функции по времени. Абсолютным значением сигнала в данном случае можно пренебречь т.к. ни в одном диагностическом алгоритме он не задействован.
f(t) - исходный сигнал ЭКГ
f'(t) - первая производная функции по времени
F(f'(t))=f(t)+C; C - принимаем равным нулю.
В случае дискретного сигнала имеем:
f(t)=(a1), (a2), (a3)…(an) - дискретные отсчеты полученные от АЦП
f'(t)=(a2-a1), (a3-a2), (a4-a3)…(an-an-1) - разность между отсчетами АЦП
F(f'(t))⇒an=Σ a1, a2, a3…an - При декодировании любой произвольный дискретный отсчет равен сумме всех предыдущих данных.
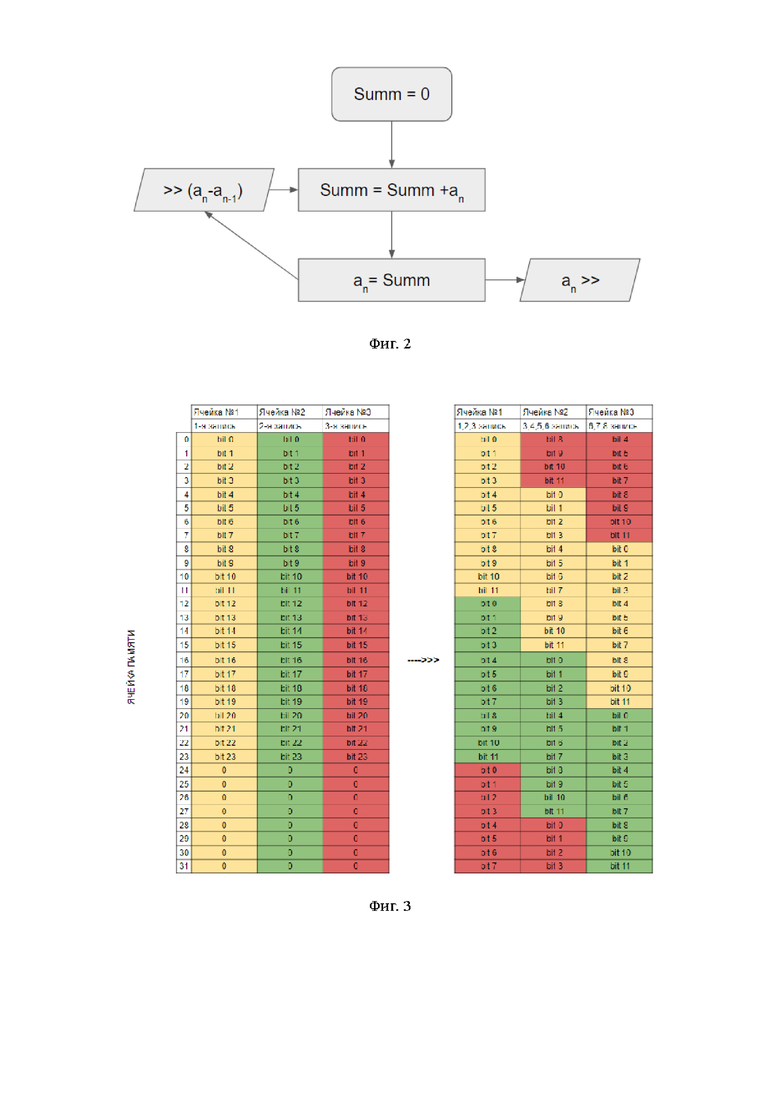
На фиг. 2 приведен алгоритм не требующий суммирования длинных рядов данных, использующий единственный регистр Summ для последовательного восстановления данных сигнала. Не требующий запоминания и вычисления суммы всех предыдущих данных.
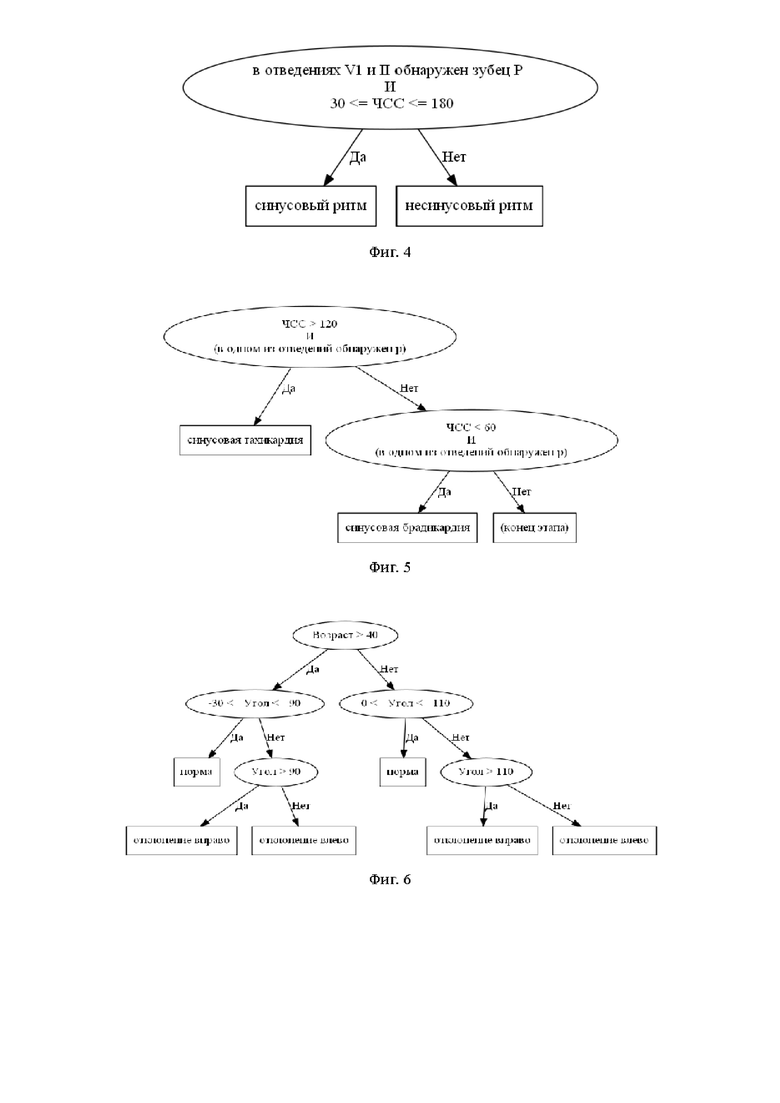
Данный алгоритм позволяет снизить разрядность кодирования каждого сэмпла сигнала с 24 бит (диапазон -2147483648…2147483647, соответствующий размеру машинного слова типа "long") до 10-12 бит (диапазон -2048…2047) , что позволяет сократить объем записываемых и передаваемых данных в 2,6 раза, путем "упаковывания" или регистрового смещения данных по стандартным ячейкам памяти (Фиг. 3). Данный алгоритм легко реализуется на микроконтроллерах с RISC вычислительным ядром (с сокращенным набором команд арифметико-логического устройства), в которых все вышеописанные операции выполняются за один машинный цикл и не требуют выполнения длительных алгоритмических процедур, что позволяет реализовать высокую энергоэффективность и длительную автономную работоспособность. Также это позволяет хранить и передавать данные с высокой дискретизацией по времени (с частотой до 8000 Гц).
Развитие методов автоматизированной обработки данных в сочетании с прогрессом в области телемедицинских технологий и использованием портативной медицинской аппаратуры открывает новые возможности для совершенствования методов ранней диагностики болезней системы кровообращения и дистанционного контроля состояния здоровья пациентов. Одним из перспективных направлений является создание интеллектуального электрокардиографа, т.е. автоматизированной системы расшифровки сигналов электрокардиограммы (ЭКГ) с получением заключения, максимально приближенного к врачебному. Для достижения этой цели в известных нам прототипах кардиорегистраторов используются прямые алгоритмы диагностики, основанные на правилах и деревьях решений. В целях повышения точности диагностики авторами была разработана система двух уровневой автоматической диагностики сигнала ЭКГ. Первым этапом использовались стандартные прямые методы диагностики. Примеры таких методов приведены на фиг. 4, 5, 6. На фиг. 4 показан пример дерева принятия решений для определения, является ли ритм синусовым. На фиг. 5 показан пример дерева принятия решений для определения синусовой тахикардии и брадикардии. На фиг. 6 показан пример дерева принятия решений для определения отклонения электрической оси сердца.
Вторым этапом - методы машинного обучения, включающий обучение и тестирование программного обеспечения на больших массивах базы данных ЭКГ и на структурированных врачебных заключениях.
Использовались методы машинного обучения - алгоритмы, автоматически строящиеся по большой выборке «размеченных данных», т.е. базе ЭКГ с известными заключениями. При этом в методах машинного обучения алгоритм постановки диагноза (решающая функция) не закладывался явным образом. Происходила «настройка» модели по данным обучающей выборки - набору характеристик и атрибутов ЭКГ пациента с известным заключением.
Был разработан базовый вариант программы анализа ЭКГ "Диагностика», позволяющий далее проводить ее обучение. Интерфейсная часть программы «Диагностика» написана на языке C#, математические методы - на языке Python с использованием библиотеки матричных вычисления NumPy (www.numpy.org), библиотеки вейвлет-анализа PyWavelets (github.com/PyWavelets) и библиотеки методов машинного обучения Scikit-learn (scikit-learn.org/stable).
Была создана база данных «Кардиобаза», включающая 36652 записей стандартной 12-канальной ЭКГ покоя в цифровом формате EDF. ЭКГ были получены от взрослых пациентов в возрасте 17-80 лет, Записи ЭКГ были независимо описаны врачами-экспертами (кардиологами и врачами функциональной диагностики) с формированием структурированного врачебного заключения.
Далее все записи ЭКГ были подвергнуты автоматическому анализу с использованием метода детектирования ключевых точек (ДКТ), сегментированы и автоматически описаны в том же формате доврачебного заключения разработанной авторами программой по классическим критериям анализа ЭКГ.
Алгоритм применения метода ДКТ включал следующие этапы:
- предварительная обработка сигнала ЭКГ: фильтрация (подавление шума), выделение изолинии);
- ДКТ сигнала - детектирование начала, пика и конца комплекса QRS, P- и T-волн и определение их морфологии;
- автоматическая генерация заключения.
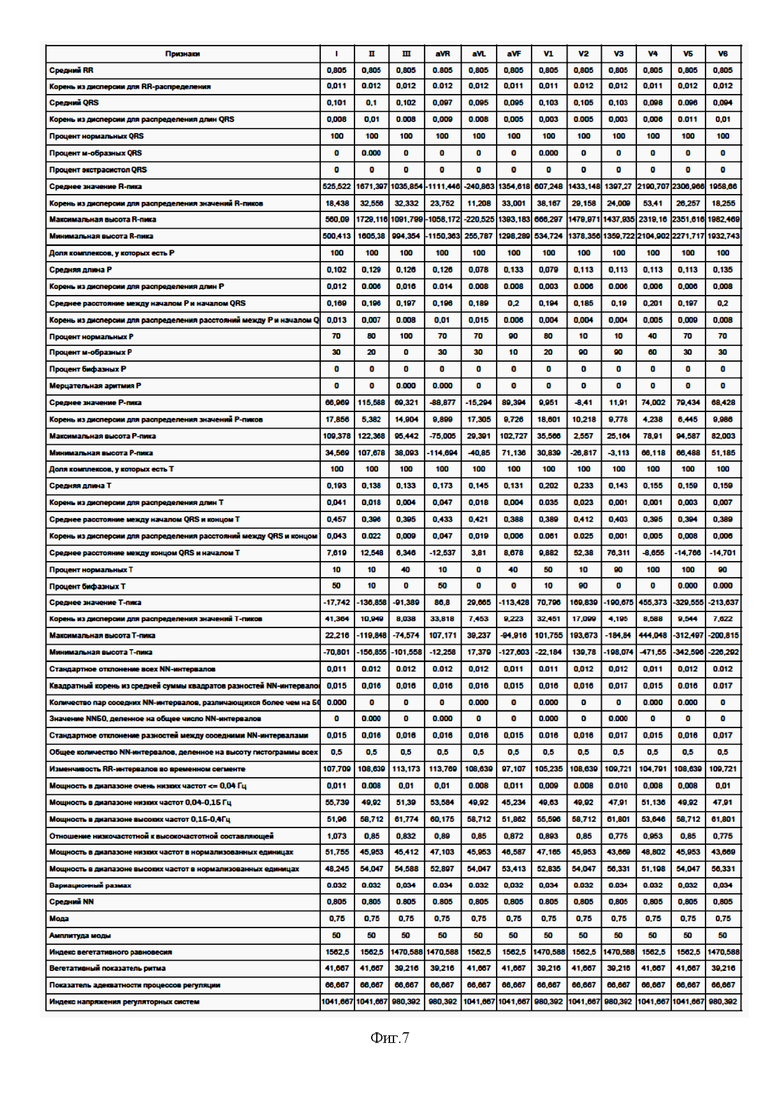
Использовались стандартные функции для вычисления числовых характеристик (средняя продолжительность и высота комплексов сигнала ЭКГ, их стандартные отклонения и т.д.). В итоге для описания каждого отведения ЭКГ были получены признаки (см. фиг. 7).
Было проведено обучение программы «Диагностика» с использованием ЭКГ, имеющихся в «Кардиобазе», с формализованными заключениями врачей. Были использованы методы машинного обучения: метод опорных векторов (SVM), дерево решений, методы квадратичного и линейного дискриминантного анализа, метод случайных подпространств, AdaBoost, случайный лес, логистическая регрессия (модель нейрона МакКаллока-Питтса) с предварительной предобработкой признаков с помощью слоя BatchNormalization, графовый метод.
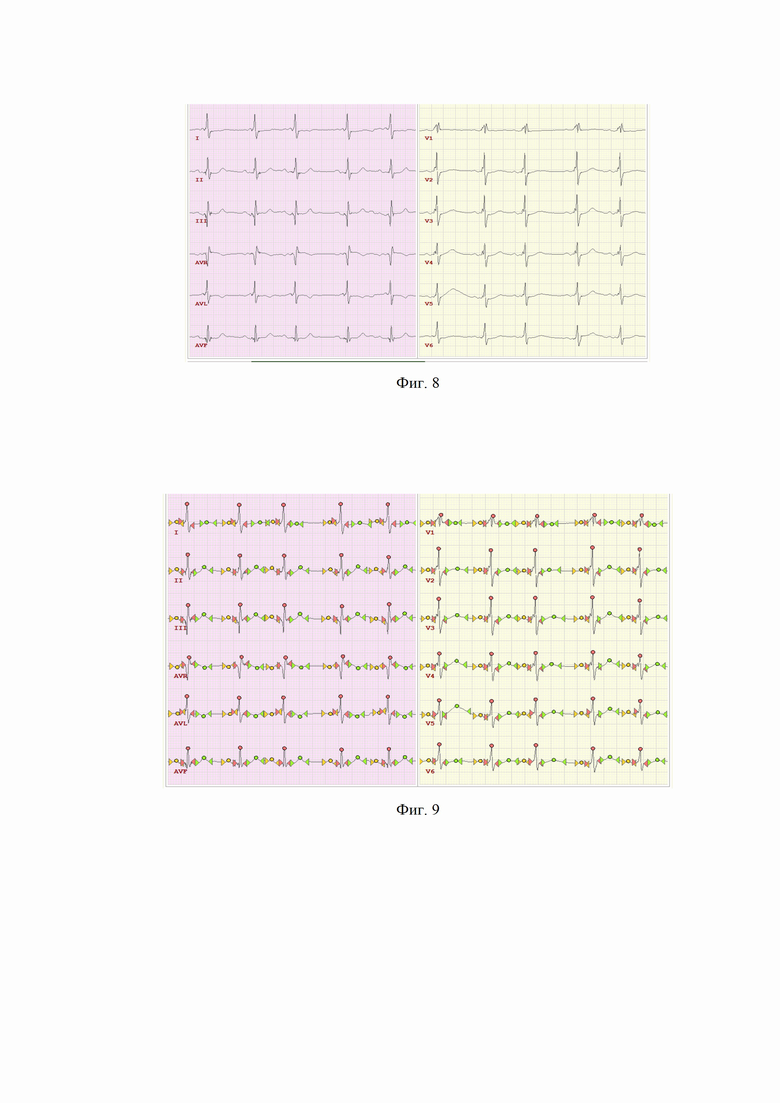
Программа автоматического анализа ЭКГ обучалась с применением методов машинного обучения на признаках, полученных с помощью ДКТ (см. фиг. 8 (Исходная ЭКГ (12 отведений) пациентки У., 69 лет) и фиг. 9 (ЭКГ с сегментацией пациентки У., 69 лет)).
Для тестирования программы «Диагностика» была проведена апробация методов машинного обучения к задаче анализа ЭКГ, которая была выполнена с использованием наиболее крупных и обработанных с участием медицинских экспертов открытых баз данных ЭКГ: ArrhythmiaDataSet (http://archive.ics.uci.edu/ml/datasets/arrhythmia), PhysioNetPTBDB(https://www.physionet.org/physiobank/database/ptbdb), PhysioNetCompetition 2017 (https://physionet.org/challenge/2017). При анализе результатов учитывалась точность диагностики относительно основных признаков и классов ЭКГ.
Проводилась комплексная оценка с сопоставлением результатов. Оценка качества происходила с помощью пятикратного перекрестного контроля по метрике ROC-AUC с помощью методов машинного обучения на доступных международных базах данных: Arryhthmia, PTBDB, PhysioNetCompetition 2017.
Чувствительность заключений, выполненных программой «Диагностика», оказалась равной 85,8%-100,0% по различным классам в сравнении с заключениями врачей-диагностов. Специфичность метода составила 90,2-99,0%, точность - 86,9-95,1%.
При анализе результатов автоматической расшифровки ЭКГ по разработанному алгоритму в соответствующих классах признаков точность диагностики составила 86,9-95,1%.
Результаты проведенного исследования показывают, что методы машинного обучения могут успешно применяться в задачах автоматического анализа ЭКГ, при этом наиболее перспективными является сочетание методов логистической регрессии и случайного леса.
Достигается технический результат, заключающийся в реализации автоматической доврачебной нозологической посиндромальной высокоточной диагностики патологических отклонений ЭКГ различной длительности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ И СИСТЕМА АВТОМАТИЧЕСКОГО АНАЛИЗА ЭКГ | 2020 |
|
RU2767157C2 |
| АППАРАТНО-ПРОГРАММНЫЙ КОМПЛЕКС ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2663626C1 |
| Способ обработки и анализа данных электрокардиограммы (ЭКГ) | 2023 |
|
RU2823433C1 |
| СПОСОБ ДИАГНОСТИКИ ЭЛЕКТРИЧЕСКОЙ НЕСТАБИЛЬНОСТИ МИОКАРДА | 1998 |
|
RU2178983C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2008 |
|
RU2391044C2 |
| СПОСОБ И СИСТЕМА НЕИНВАЗИВНОЙ СКРИНИНГОВОЙ ОЦЕНКИ ФИЗИОЛОГИЧЕСКИХ ПАРАМЕТРОВ И ПАТОЛОГИЙ | 2016 |
|
RU2657384C2 |
| ЭЛЕКТРОКАРДИОГРАФ ДЛЯ НЕИНВАЗИВНОЙ РЕГИСТРАЦИИ МИКРОПОТЕНЦИАЛОВ НА ЭЛЕКТРОКАРДИОГРАММЕ В РЕАЛЬНОМ МАСШТАБЕ ВРЕМЕНИ | 2013 |
|
RU2552876C2 |
| СПОСОБ ФОРМИРОВАНИЯ ФАЙЛА ДАННЫХ ДЛЯ АНАЛИЗА ЭКГ | 2023 |
|
RU2822304C1 |
| СПОСОБ ОБРАБОТКИ ЭЛЕКТРОКАРДИОСИГНАЛА ДЛЯ ДИАГНОСТИКИ ИНФАРКТА МИОКАРДА | 2008 |
|
RU2383295C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ДИАГНОСТИКИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2020 |
|
RU2759069C1 |
Изобретение относится к медицинской технике. Аппаратно-программный комплекс электрокардиографических (ЭКГ) измерений содержит закрепляемый на пользователе корпус, в котором установлены микроконтроллер, аналого-цифровой преобразователь, средство хранения данных, выполненное с возможностью хранения данных ЭКГ, модуль беспроводной связи, обеспечивающий передачу данных из средства памяти на внешнее вычислительное устройство, первый, второй и третий электроды, аккумулятор и разъем для подключения внешних электродов, обеспечивающих регистрацию ЭКГ. Первый электрод совмещен с емкостной кнопкой, обеспечивающей активацию функции снятия ЭКГ устройством. Второй и третий электроды расположены на тыльной стороне корпуса и обеспечивают совместно с первым электродом регистрацию ЭКГ. Полоса частот амплитудно-частотных характеристик для всех каналов аналоговых интерфейсов составляет 0-4000 Гц с допустимыми отклонениями амплитуд от 0 до 2000 Гц ±10% и частотой дискретизации сигнала 8000 Гц. Микроконтроллер и средство хранения данных выполнены с возможностью записи, чтения и передачи данных ЭКГ в параллельных потоках с приоритетом у процесса записи и с осуществлением записи в энергонезависимую память в единичных интервалах в размере кратном объёму страницы энергонезависимой памяти. Микроконтроллер реализует прямые алгоритмы диагностики, основанные на правилах и деревьях решений и выполнен с возможностью подключения к блокам диагностики, реализующим методы машинного обучения. Обеспечивается реализация алгоритмов диагностики сложных нарушений ритма, основанных на анализе ЭКГ высокого разрешения, с одновременной записью и чтением данных, например, при проведении исследования, включая данные, записанные произвольное время назад. Достигается автоматическая доврачебная нозологическая посиндромальная высокоточная диагностика патологических отклонений ЭКГ различной длительности без участия врача-эксперта. 1 з.п. ф-лы, 9 ил.
1. Аппаратно-программный комплекс электрокардиографических (ЭКГ) измерений, содержащий корпус, закрепляемый на пользователе, в котором установлены:
микроконтроллер, выполняющий управление электронным устройством;
аналого-цифровой преобразователь, обеспечивающий преобразование в цифровой вид сигналов, поступающих с электродов;
средство хранения данных, выполненное с возможностью хранения данных ЭКГ;
модуль беспроводной связи, обеспечивающий передачу данных из средства памяти на внешнее вычислительное устройство;
первый электрод, совмещенный с емкостной кнопкой, обеспечивающей активацию функции снятия ЭКГ устройством;
второй и третий электроды, расположенные на тыльной стороне корпуса и обеспечивающие совместно с первым электродом регистрацию ЭКГ;
аккумулятор;
разъем для подключения внешних электродов, обеспечивающих регистрацию ЭКГ,
отличающийся тем, что
полоса частот амплитудно-частотных характеристик для всех каналов аналоговых интерфейсов составляет 0-4000 Гц, с допустимыми отклонениями амплитуд от 0 до 2000 Гц ±10%, частота дискретизации сигнала 8000 Гц;
при этом микроконтроллер и средство хранения данных выполнены с возможностью записи, чтения и передачи данных ЭКГ в параллельных потоках с приоритетом у процесса записи, с осуществлением записи в энергонезависимую память в единичных интервалах в размере, кратном объёму страницы энергонезависимой памяти;
микроконтроллер также выполнен с возможностью реализации прямых алгоритмов диагностики, основанных на правилах и деревьях решений;
микроконтроллер также выполнен с возможностью подключения к блокам диагностики, реализующим методы машинного обучения.
2. Аппаратно-программный комплекс по п. 1, отличающийся тем, что выполнен с возможностью подключения к разъему для подключения внешних электродов кабеля с 7 контактами, позволяющими регистрировать 12 стандартных отведений ЭКГ.
| RU 197114 U1, 01.04.2020 | |||
| US 2015313489 A1, 05.11.2015 | |||
| US 2011092834 A1, 21.04.2011 | |||
| US 2005004481 A1, 06.01.2005 | |||
| US 2001039385 A1, 08.11.2001 | |||
| WO 2016207862 A1, 29.12.2016 | |||
| Способ изготовления цилиндрических спиральных пружин и устройство для его осуществления | 1985 |
|
SU1284645A1 |
| СПОСОБ ДИАГНОСТИРОВАНИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ | 2010 |
|
RU2442529C1 |
| СПОСОБ ДИАГНОСТИКИ РИСКА РАЗВИТИЯ ПАРОКСИЗМАЛЬНОЙ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2005 |
|
RU2283024C1 |
| КАРПЛЮК Е.С | |||
| "Оптимизация тракта ЭКГ на основе сигма-дельта АЦП" | |||
| Электроника и связь | |||
Авторы
Даты
2021-11-12—Публикация
2020-11-26—Подача