Изобретение относится к медицине, к офтальмологии и непосредственно к ее разделу ретинологии. На основе десятилетнего клинического опыта выработан комбинированный способ лечения хориоидальной неоваскуляризация (ХНВ). Данный способ сочетает в себе применение двух наиболее эффективных методов лечения ХНВ. В сочетании данных методов максимально использованы их эффективная составляющая, благодаря которой и достигается клинический эффект в лечении ХНВ и лимитированы, на сколько это возможно, недостатки данных методов.
Научная новизна
Проведено наблюдение и анализ развития ХНВ, неподдающейся антиангиогенной терапии или фокальной лазерной коагуляции или любому другому известному изолированному способу лечения, предложено ее название.
Предложена комбинированная схема лечения данного течения ХНВ при различных причинах ее появления, также схема лечения клинически обоснована. На клинических примерах показана эффективность такой комбинации.
Данный способ лечения является универсальным. Подходит для лечения ХНВ всех видов, форм и причин появления, возможен к применению при всех известных глазных патологиях, осложненных ХНВ. Возможен у пациентов практически с любым общим состоянием здоровья, отсутствует системные осложнения.
Предложен оригинальный способ коагуляции ХНВ, сочетающий безопасность и эффективность.
Намечены дальнейшие пути совершенствования методов борьбы с ХНВ. Это является научным потенциалом данного изобретения.
Показана актуальность данной схемы диагностики выраженных ХНВ с использованием ангио ОСТ и почти недоступности классической ФАГ.
Хориоидальная неоваскуляризация (ХНВ) - патологический механизм, являющийся общим грозным осложнением для многих глазных заболеваний. На первом месте из глазных нозологий, осложняющихся ХНВ, стоит возрастная макулярная дегенерация, далее дегенеративная миопия, хроническая центральная серозная ретинопатия, диабетическая пролиферативная и постромботическая ретинопатия, различные генетические заболевания сетчатки, травма. Можно сказать, что любое заболевание сетчатки (даже ее отслойка), может быть осложнено ХНВ.
В зависимости от локализации новообразованных сосудов относительно ретинального пигментного эпителия (РПЭ) принято выделять несколько типов ХНВ. При I типе ХНВ неоваскуляризация располагается под РПЭ (скрытая или оккультная ХНВ). Для II типа ХНВ характерно прорастание патологических сосудов в субретинальное пространство (классическая ХНВ). При развитии патологического процесса неоваскуляризации ХНВ может иметь смешанный тип с расположением новообразованных сосудов над и под пигментным эпителием сетчатки. В последнее время ученые выделяют редкий III тип ХНВ - ретинальную ангиоматозную пролиферацию и полипоидную хориоидальную васкулопатию (ПХВ).
Выход на первичную инвалидность вследствие хориоидальной неоваскуляризации (ХНВ) наблюдается у лиц работоспособного возраста в 11% случаев, а среди лиц старше 60 лет - в 28% случаев [1].
Лечение ХНВ путем интравитреального применения ингибиторов ангиогенеза
Международные рандомизированные многоцентровые исследования Radiance и Repair (2012 г.) убедительно доказывают патогенетически верный способ лечения ХНВ путем интравитреального введения различных ингибиторов ангиогенеза (ИВВИАГ, интравитреальное введение Anti-VEGF препарата), которые действуют на различные звенья, в данном случае патологического процесса неоваскуляризации. Интравитреальное применение ингибиторов ангиогенеза, то есть антиангиогенная терапия (ИВВИАГ) Луцентис (Ranibizumab) и Эйлеа (Aflibercept) не только стабилизирует, но часто повышает МКОЗ (Максимально коррегируемая острота зрения), уменьшает отек сетчатки и подавляет активность ХНВ. Введение препарата является малоинвазивной процедурой, но все же риск эндофтальмита и гемофтальма остается. В современных, доказанных схемах применения ингибиторов ангиогенеза всегда требуются кратные инъекции препарата. Инъекция препарата является относительно дорогостоящей процедурой. В загрузочной дозе инъекции препарата проводятся в количестве от трех до пяти с интервалом 1 месяц (в зависимости от конкретного препарата), далее инъекции проводятся при активизации процесса неоваскуляризации в процессе динамического наблюдения пациента. Данный способ лечения не предполагает полной остановки процесса неоваскуляризации, хотя эффективно подавляет этот процесс иногда на несколько лет. Пациент, даже при благоприятном воздействии препарата на очаг ХНВ, в среднем получает пять - семь инъекций препарата в течение года и остается на постоянном наблюдении у офтальмолога. Динамическое наблюдение проходит с применением высокотехнологичных и относительно дорогостоящих (особенно учитывая их частоту проведения) исследований. Это оптическая когерентная ангиография (ОКТ), ОКТ в ангиорежиме, флюоресцентная ангиография, а иногда ангиография с индоцианид зеленым красителем, часто требуете исследование на ретинальной камере в режиме аутофлюоресценции. Кратность приемов офтальмолога, кратность инъекций, необходимость лабораторного исследования основных параметров крови, мочи и общего состояния пациента перед каждой инъекцией, цена на препарат и динамическое наблюдение или сторонние процессы со здоровьем пациента которые нарушают график инъекций крайне отрицательно влияют на эффективность (комплаентность) данного способа лечения ХНВ. Появляются пациенты с формами ХНВ далее неподдающиеся даже кратным инъекциям антиангиогенных препаратов. Например, последняя пандемия короновирусной инфекции, когда профильные ЛПУ были переквалифицированы в инфекционные стационары или просто закрыты, нарушила графики такого лечения у большинства пациентов, которые до этого получали стандартную антионгиогенную терапию против ХНВ. Все это вызвало резкое повышение случаев хронизации процесса ХНВ или переход его в форму неподдающуюся лечению применением изолированной антиангиогенной терапии. В этой работе данный тип ХНВ предложено называть - пернициозным. Длительное существование ХНВ, даже при конечной эффективности антиангиогенной терапии, приводит к необратимым деструктивным процессам в центральной сетчатке. А если учитывать то, что ХНВ выявляется в уже развитом состоянии с уже определенными дистрофическими изменениями, то временной фактор в лечении играет важную роль [2, 3, 4, 5, 6].
Лазерная коагуляция ХНВ (ЛК ХНВ)
Лазерная коагуляция фокуса или зоны патолгической хориоидальной неоваскуляризации (ЛК ХНВ) - может полностью уничтожить ХНВ в зоне коагуляции, а следовательно, полностью решить проблему. Стабилизируется, иногда повышается, острота зрения, уходит отек, стремится к норме архитектоника сетчатки в фовеа. Но данный метод лечения подходит далеко не для всех видов ХНВ, его применение резко ограничено локализацией зоны ХНВ. При этом имеются данные о временном функциональном эффекте, рецидивировании ХНВ, расширении атрофии ПЭС за границы фотокоагуляционного рубца. При изолированной коагуляция ХНВ предпочтительна коагуляция всего фокуса патологического ангиогенеза, так как даже небольшая оставшаяся часть неоваскуляризации, может ответить на коагуляцию бурным ростом и дальнейшей пролиферацией. Наилучшие результаты достигаются при коагуляции экстрафовеолярных субретинальных неоваскулярных мембран (СНМ), тогда как суб- и юкстафовеолярные требуют применения специальных щадящих или сберегающих точку фиксации взора техник [2, 6, 7, 8, 9, 10, 11, 12, 13, 14].
Другие известные способы лечения ХНВ
Фотодинамическая терапия (ФДТ). На сегодняшний день является наиболее селективным методом. Суть данной методики заключается в том, что пациенту внутривенно вводят фотосенсибилизатор, который под воздействием лазерного излучения с длиной волны 660-670 нм, селективно разрушает эндотелий новообразованных сосудов (ХНВ), при этом не воздействуя на нормальные сосуды и окружающие ткани. Эффективность ФДТ зависит от характеристик фотосенсибилизатора, дозы препарата и времени, прошедшего от момента введения препарата до воздействия светом [15].
Данная методика имеет недостатки. Прежде всего необходимо специальное дорогостоящее оборудование и высококвалифицированный специалист, который понимает какой фотосенсибилизатор в какой дозировке применить в конкретном случае, сколько требуется сеансов данного лечения. Есть сложность расчета фотосенсибилизатора. Требуются несколько курсов. ХНВ может вновь активизироваться. Кроме того, есть ряд противопоказаний и побочные действия от введения любого фотосенсибилизатора, отмечается определенное отрицательное системное действие. На конечный результат лечения существенное воздействие может оказать общее соматическое состояние пациента. Известен, например, способ лечения субретинальной неоваскулярной мембраны (СНМ), заключающийся в проведении фотодинамической терапии путем введения фотосенсибилизатора с последующим транспупиллярным лазерным облучением СНМ. В качестве фотосенсибилизатора используется Фотосенс в дозе 0,05-0,3 мг/кг веса, а облучение проводят на третьи сутки после введения Фотосенса по достижении терапевтической дозы фотосенсибилизатора в мембране при длине волны 675 нм и плотности мощности 80-200 мВт/см2. Облучение повторяют каждые 3-5 дней. Количество сеансов варьируют от 2 до 5 [16].
Однако данный способ обладает существенными недостатками: он не позволяет проводить лечение скрытых форм неоваскулярных мембран, длительный срок выведения из организма фотосенсибилизатора Фотосенса требует соблюдения строгого режима по защите кожных покровов и сетчатки от солнечного и других видов излучений в течение 1-2 месяцев.
Другой селективный способ заключается в применении лазерного излучения в микроимпульсном режиме. Суть данного метода заключается в воздействии лазерным излучением на область вокруг патологического очага. От данного очага отступают на 450 - 500 мкм, на интактную зону сетчатки наносят аппликаты плотным слоем методом «закрашивания» с расстоянием между ними, равным одному диаметру аппликата, в горизонтальном или вертикальном направлении при следующих параметрах лазерного воздействия: длина волны 577 нм, мощность 100-270 мВт, экспозиция 20 не, период между пакетами импульсов 0,1-0,15 с, скважность 5%. Диаметр пятна 100 мкм, количество аппликатов 600-1200 шт. Способ обеспечивает снижение травматичности и трудоемкости, уменьшение повреждения сетчатки, стабилизацию процесса неоваскуляризации, повышение зрительных функций [17, 18].
Основной недостаток данного метода заключается в подборе параметров лазерного воздействия, то ест создания тестового коагулята, на основе которого настраивается скважность лазерного излучения. Сила пигментации в пределах макулярной зоны может сильно отличаться, а следовательно, и тропность ткани к лазерному излучению, в любом режиме, и особенно в режиме микроимпульса. Если при этом учесть, изменения в сетчатке вызванные наличием ХНВ, то воздействие лазерного излучения в таком режиме может стать слабо неконтролируемым и отрицательно повлиять на конечный результат лечения. Прозрачность оптических сред влияет на конечный результат лечения, из-за требуемой прецизионности параметров микроимпульсного воздействия на всей области сетчатки, где оно проводится.
Один из комбинированных способов лечения ХНВ при влажной формы возрастной макулярной дегенерации сетчатки, заключающийся в том, что вначале осуществляют введение ингибитора ангиогенеза в виде инъекции в стекловидное тело в дозе 0,5 мг 1 раз в месяц. Затем парабульбарно на 1,5 мл изотонического раствора вводят альфафетопротеин в дозе 0,0075 мг вечером и глутатион-Б-трансферазу в дозе 0,0000005 г утром. Введение проводят в каждый глаз ежедневно до визуализации сетчатки с новообразованными сосудами вокруг макулы. Далее проводят лазерную коагуляцию сосудов, без повреждения макулы. Затем парабульбарно и ретробульбарно, ближе к области макулы, трансплантируют суспензию аутологичных мононуклеаров костного мозга. Число мононуклеаров составляет 5-40 млн. При этом суспензию вводят на 1,5 мл «NCTF-135». Введение осуществляют 2-4 раза с интервалом в 2 месяца. Способ позволяет остановить неоангиогенез, ослабить аутоиммунный процесс в области тканей глаза, т.е. привести к блокаде патогенетических механизмов развития ВМД, что исключает рецидив заболевания при создании условий для органотипической регенерации сетчатки и выраженного улучшения зрительной функции [19].
Недостатками данного способа являются неоптимальность данной комбинации, так как ингибиторы ангиогенеза вуалируют точки активности ХНВ, на которые в дальнейшем проводится лазерная коагуляция. Эффективность применения и безопасность мононуклеаров не доказана в долгосрочном периоде. И данная комбинация технически сложна и очень дорогостоящая.
Известен способ лечения субретинальной неоваскулярной мембраны, заключающийся в том, что первоначально в задний отдел стекловидного тела вводят ингибитор ангиогенеза ранибизумаб в дозе 0,3-0,5 мг, через 5-7 дней после уменьшения отека определяют границы неоваскулярной мембраны методом флуоресцентной ангиографии, проводят фотодинамическую терапию посредством введения фотосенсибилизатора вертепорфина в дозе 0,08-0,1 мг/кг, через 15 минут проводят лазерное облучение новообразованных сосудов в пределах границ неоваскулярной мембраны, длиной волны 689 нм, при плотности мощности 500-600 мВт/см2 в течение 83-100 сек, облучение проводят однократно. Общая доза составляет до 50 Дж/см2 [20].
Недостатками известного способа являются инвазивность данной методики, риск послеоперационных осложнений, таких как гемофтальм, эндофтальмит. А также высокий риск неадекватности подобранных лазерных параметров при фотодинамической терапии, и как следствие, рубцовые осложнения.
Известен способ профилактики возможной неоваскуляризации при сахарном диабете, включающий введение ингибитора ангиогенеза в витреальную полость глаза с последующей лазеркоагуляцией ишемизированных зон сетчатки. При этом в качестве ингибитора ангиогенеза используют ранибизумаб (луцентис), который в дозе 0,4 мг вводят в лентико-макулярный канал стекловидного тела. Лазеркоагуляцию проводят при мощности лазерного излучения 100-200 мВт, экспозиции 0,1-0,2 секунды, диаметре пятна 200-300 мкм. Количество коагулятов при этом составляет от 250 до 300 [21].
Данный способ подходит для пациентов только с сахарным диабетом и по сути является модификацией классической панретинальной лазерной коагуляции сетчатки. Нет прицельного воздействия на фокусы ХНВ. Еще недостатками данного способа являются риск послеоперационного гемофтальма и эндофтальмита, риск развитий рубцовых изменений в отдаленном периоде в зоне ЛКС
Комбинированный способ лечения пернициозных ХНВ
Для создания данного способа лечения ХНВ, было проведено клиническое исследование. По дизайну исследование носило характер нерандомизированного проспективного клинического исследования в пределах одной основной группы пациентов и двух контрольных групп.
В исследование включены 36 пациентов, 38 глаз с различной причиной формирования хориоидальной неоваскулярной мембраны (ХНВ), из них с экстрафовеолярной и парафовеолярной - 24 глаза, субфовеолярной ХНВ - 14 глаз.
Все пациентам проводилась кратная антиангиогенная терапия без значительной конечной положительной динамики. Данное течение ХНВ мы предлагаем называть – пернициозным.
С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции. Далее этим пациентам проводилась коагуляция ХНВ с дифференцированным параметрами, руководствуясь проведенными методами диагностики. Во всех случаях останавливалось развитие ХНВ, а самое главное других пролиферативных процессов, вызванных ей, повышалась острота зрения и процесс стабилизировался минимум на 2 года. Кроме того, у 60% данных пациентов исчезали или резко снижались метаморфопсии. Жалобы на метаморфопсии часто беспокоили пациентов больше, чем снижение остроты зрения, во время развития заболевания, осложненного ХНВ. Снижение выраженности метаморфопсий и их исчезновение всеми пациентами отмечалось как положительная динамика состояния их зрения, даже если МКОЗ менялась незначительно. 28 пациентам после лазерной коагуляции фокуса ХНВ проводилось дополнительная ИВВИАГ в сроки от 2-3 недель до 3 месяцев от момента лазерной коагуляции.
Было две контрольные группы.
Первая контрольная группа из 43 человек (47 глаз), где проводилась только ИВВИАГ в кратном количестве. У 21 человека (22 глаза) из этой группы в течение нескольких лет неоваскуляризация заканчивалась центральным ретинофиброзом и значительным, стойким снижением центрального зрения. У 22 человек происходила стабилизация процесса, но первоначальной остроты зрения достигнуто не было, почти у всех пациентов были рецидивы ХНВ, требующие повторных инъекций препарата в течение трех лет с момента стабилизации.
Вторая контрольная группа: 22 человека (23 глаза). Данным пациентам проводилась изолированная коагуляция ХНВ. В данной группе были пациенты только с парафовеальной и парамакулярной локализацией ХНВ, которая встречается реже классической ХНВ субфовеолярной локализации. После лазерной коагуляции эффект наступал практически сразу. В течение пяти лет у 3 пациентов возникла географическая атрофия ПЭС с вовлечением фовеолы и снижением центрального зрения. У 15 пациентов наступила стойкая ремиссия более пяти - семи лет. У 4 пациентов неоваскуляризация рецидивировала и все они перешли на антиангиогенную терапию У 2 из них в итоге процесс патологическокго ангиогенеза закончился ретинофиброзом и потерей центрального зрения
Этапы исследования включали скрининговое обследование пациентов, дообследование с использованием высокотехнологичных методов исследования, проведение антиангиогенной терапии в сочетании с лазеркоагуляцией, контрольные обследования с использованием высокотехнологичных методов исследования, сбор и статистическую обработку результатов.
Материалы и методы
Всем пациентам проводилось полное офтальмологическое обследование включающее определение остроты зрения, тонометрию по Маклакову, биомикроскопию, офтальмобиомикроскопию с использованием асферической линзы 78 D (Volk), компьютерную периметрию на периметре OCULUS Centerfield, флуоресцентную ангиографию (ФАГ до 2019 г.) с использованием фундус камеры CARL ZEISS FF 450 IR и фундус камеры (Canon СХ-1). Исследование глазного дна в режиме аутофлюоресценции с использованием фундус камеры (Canon СХ-1), оптическую когерентную томографию (ОКТ), как классическую так и с применением ангиомодуля (OPTOPOL COST Copernicus REVO NX). Лазеркоагуляция ХНВ производилась с учетом данных ОСТ и ФАГ на диодных лазерах с длиной волны 532 нм (мощность индивидуальна Вт, экспозиция индивидуально сек). Срок наблюдения составил от 6 мес до 10 лет.
Статистическая обработка результатов осуществлялась при помощи программ Microsoft Excel 2003-2019, Statistica 6.0.-13.3.
В нашем исследовании основными диагностическими критериями мы считали снижение активности ХНВ в виде уменьшение отека сетчатки в фовеа, восстановление нормальной архитектоники макулы, уменьшение и исчезновение отслойки нейроэпителия сетчатки (НЭС) и пигментного эпителия сетчатки (ПЭС), снижение субретинального геморража. Эти данные были получены при помощи ОКТ, ангио ОКТ, ФАГ сетчатки, исследовании глазного дна в режиме аутофлуоресценции, биомикроскопии с фоторегистацией макулы. Важным критерием было повышение МКОЗ и субъективное ощущение состояния зрения каждым конкретным пациентом, особенно снижение жалоб на метоморфопсии.
Всем пациентам была проведена Флуоресцентная ангиография (ФАГ) (до 2019 г) до начала антиангиогенной терапии и после кратных инъекций. После 2019 года ввиду отсутствия флуоресцеина натрия мы проводили Ангио ОКТ в сочетании с ОКТ и аутофлуоресценцией. Данная комбинация инструментальных методов исследования давала аналогичные данные течения процесса как и ФАГ (см. фиг. 18, 19, 20). Также по ОКТ осуществлялось текущее наблюдение за процессом до и после каждой инъекции, после ЛК ХНВ и далее динамически в зависимости от каждого конкретного клинического случая.
При проведении данных исследований, в процессе ведения пациентов было установлено, снижение активности общей ХНВ после фокальной лазерной коагуляции ХНВ на фоне интавитреальных введений ингибиторов ангиогенеза. При лазерной коагуляции фокусов ХНВ снижался общий объем патологической хориоидальной неоваскуляризации и ингибиторы ангиогенеза более эффективно воздействовали на ХНВ в фовеа, а именно в той зоне макулы, где лазерная коагуляция невозможна. Так как лазерная коагуляция проводилась на фоне интравитреального введения антиангиогенного препарата, ХНВ теряла свою активность и не могла ответить на лазерную травму своей пролиферацией. В этом и заключается основной положительный эффект данной комбинации. Значительно снижалась активность ХНВ субфовеолярной, юкстафовеолярной, экстрафовеолярной локализаций, это мы объясняем цитоархитектоникой сетчатки в этой области, а именно ее малой толщиной и наличием аваскулярной зоны. Данное строение сетчатки позволяет антиангиогенному препарату глубже проникать к патологической неоваскуляризации, особенно на фоне снижения общего пула ХНВ после ее лазерной коагуляции и следовательно, более эффективно воздействовать на нее, даже при наличии отека, депозитов и других «экранирующих» образований и процессов. Этим мы объясняем «очищение» фовеа от данного патологического процесса и «отступление» ХНВ за аваскулярную зону, где уже классическая лазеркоагуляция может быть более эффективна и главное безопасно применена. Сохранение интактных зон ХНВ для ИВВИАГ за аваскулярной зоной объясняется появлением там значительного количества полиморфных эксудатов, которые появляются из-за декомпенсации микроциркуляции в данных зонах сетчатки. При нашем наблюдении, прежде всего из-за сопутствующей патологии, которая, в свою очередь, отрицательно влияла на сосудистую стенку, адекватность ее проницаемость и перициты, что и вызывало данные депозиты. Полное излечение пациентов только при антиангиогенной терапии не наступало в связи с индивидуальными особенностями пациентов, которые заключались в выраженной ангиогенной реакцией на гипоксию вследствие различных патологических процессов, высоким пулом ХНВ. Кроме того, на положительный эффект при ИВВИАГ сильное влияние оказывало нарушение комплаентности в виде больших чем месяц перерывов между инъекциями, по различным причинам.
У всех пациентов была антиангиогенная терапия от трех до тридцати восьми инъекций, без значительной конечной положительной динамики. Антиангиогенные препараты применялись путем интравитреальной инъекции в условиях стерильной операционной по стандартной технологии в дозе 0,5 мг (0,05 мл). Повторные инъекции, при необходимости, выполнялись с интервалом в 1-3 мес. Критерием для продолжения лечения было сохранение активности ХНВ. Лазеркоагуляция проводилась в широких пределах, но дифференцировано, в зависимости от места расположения ХНВ, ее вида и сопутствующих изменений сетчатки, депозитов и других экранирующих очаг ХНВ образований. Некоторые зоны сетчатки подвергались многократной ЛКС, другие коагулировались единожды. Коагуляция фокуса ХНВ проводилась по следующей методике. Использовалась лазерная установка IRIDEX IQ 532 (IRIDEX Corp.США) и Supra 532 (Quantel Medical, Франция), коагуляция проводилась в непрерывном режиме на фокус ХНВ, до границ фовеа. Коагуляция проводилась со следующими параметрами: Длина волны лазерного излучения 532 нм, мощность 200-350 мВт, длительность (экспозиция импульса) 0.05-0.07 с, период между импульсами 0,2-0,3 с, диаметр пятна 300 мкм, количество аппликатов 150-1300 шт. Для коагуляции использовалась линза REICHEL-MAINSTER IX (Ocular Instruments США). Коагуляция проводилась от внешнего края фокуса ХНВ к его центру. Коагуляция проводилась черепицеобразно или методом сплошного «закрашивания» каждый следующий коагулят примыкал к предыдущему. Обычно фокус подвергался трехкратной коагуляции с постепенным повышением энергии на четверть. Первый проход лазером начинался с применением лазеркоагулятов II степени по L'Esperance. Данный способ лазерной коагуляции позволял безопасно эффективно воздействовать на фокус ХНВ. Постепенное повышение энергии, дифференцированность ЛКС и направление коагуляции от края к центру, позволяла избежать осложнений в виде неконтролируемого распада ткани с повышенным выбросом протеинов теплового шока, эксудации, геморража, отека сетчатки и других осложнений, особенно отдаленных. При этом происходит надежная коагуляция фокуса ХНВ с потерей ей структурной целостности, полным распадом и отсутствием рецидивирования из этой зоны в будущем. Коагуляция фокуса или фокусов ХНВ проводилась в течение третьей недели от последнего ИВВИАГ. Далее необходимо динамическое наблюдение с тремя визитами раз в неделю, потом наблюдение раз в месяц. Дальнейшая тактика по результатам динамического наблюдения. В 85% такого комбинированного лечения наступал стойкий регресс процесса патологической ХНВ, повышения МКОЗ, и субъективного улучшения зрения пациентов. В процессе данной работы было уделено внимание субъективному ощущению качества зрения каждым конкретным пациентом. Многие пациенты жаловались, прежде всего, на метаморфопсии и они их беспокоили больше, чем снижение остроты зрения. И когда жалобы на метоморфопсии значительно снижались или исчезали совсем, после данного комбинированного лечения, пациенты отмечали это как явную положительную динамику в субъективном ощущении своих зрительных функций, даже если МКОЗ повышалась незначительно.
В настоящее время можно выделить 2 основных способа лечения ХНВ: фармакологическая терапия, а именно интравитреальное введение различных ингибиторов ангиогенеза и фокальное световое энергетическое воздействие, прежде всего классическая лазеркоагуляция сетчатки, субпороговая микроимпульсная лазеркоагуляция, фотодинамическая терапия. Все они имеют недостатки и не позволяют в отдельности достичь высокого и стойкого результата в лечении ХНВ.
Техническим результатом предлагаемого изобретения является надежное и безопасное ограничение и даже полное прекращение процесса патологического хориоидального ангиогенеза, со стойким временным эффектом.
Поставленный технический результат достигается тем, что в комбинированном способе лечения хориоидальной неоваскуляризации всех типов, включающий воздействие на хориоидальную неоваскуляризацию интравитреального введения ингибиторов ангиогенеза и непосредственно лазерную коагуляцию фокусов патологической хориоидальной неоваскуляризации, дополнительно с помощью диагностических инструментальных методов офтальмологического исследования определяется тип, размер, активность ХНВ и на основе этих данных производится индивидуальное комбинированное воздействие интравитреального введения ингибиторов ангиогенеза в сочетании с лазерной коагуляцией ХНВ.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1
Пациент М., 1961 г.р.
Ds. ЦСХРП, осложненная ХНВ OD. Начальная катаракта OU, Оперированная миопия средней степени, состояние после кератотомии OU, Состояние после интравитреального введения Anti-VEGF препарата OD.
Четырехкратное интравитреальное введение Anti-VEGF препарата в правый глаз по поводу ХНВ на фоне хронической ЦСХРП. С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены несколько фокусов ХНВ. 09 10 2020 ФЖС трех фокусов ХНВ. Зрение на момент ФЛКС Vis OD=0.2 sph+1.25 D,=0.6, метаморфопсии, через три недели отмечает значительное улучшение, жалобы на метоморфопсии исчезли Vis OD=0.5 sph+1.0 D,=0.9, по ОКТ сохраняется минимальная активность одного из фокусов ХНВ, дополнительное введение Anti-VEGF 10 11 2020.
22 03 2021 Vis OD=0.5 sph+1.0 D,=1.0
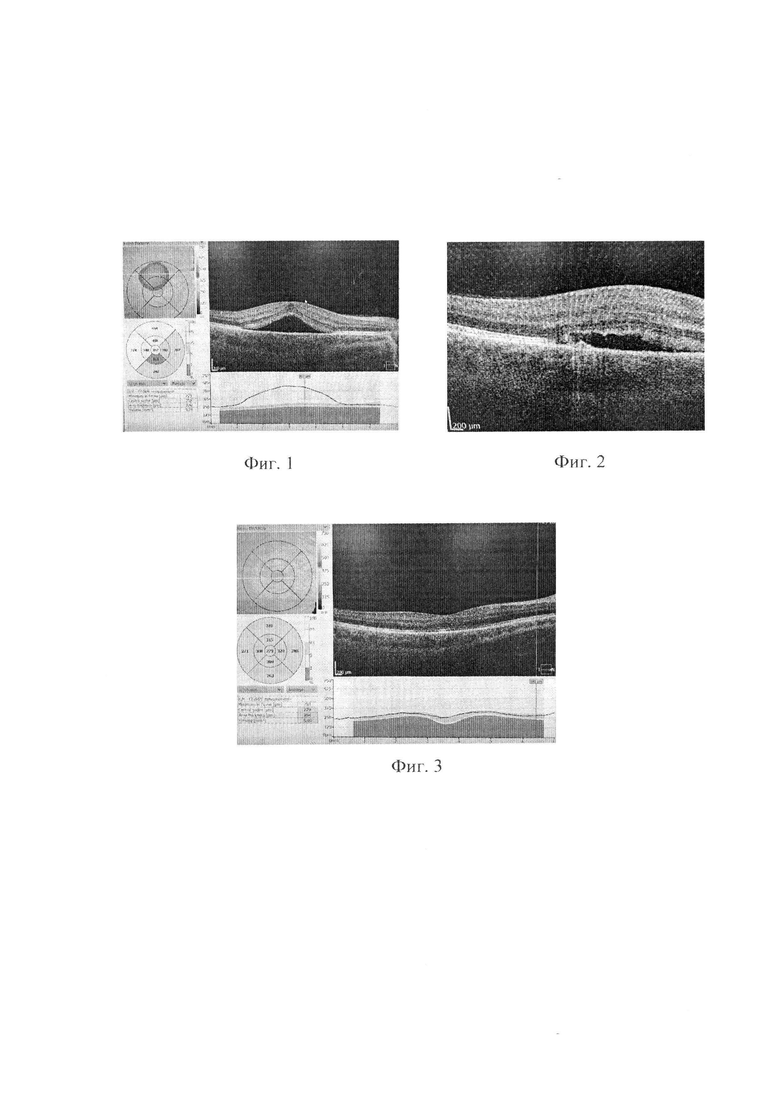
На фиг. 1 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 2 показан фокус наиболее активной минимально классической ХНВ, на фиг. 3 - после лечения.
Пример 2
Пациент Б., 1936 г.р.
Ds. Н35.3 ВМД влажная форма, Н31.8 ХНВ, состояние после интравитреального введения Anti-VEGF препарата пятикратно, ФЛКС ХНВ OS. Z96.1 Артифакия, состояние после ЗЛКТ OS. Н25.8 Зрелая катаракта OD. Старая тотальная отслойка OD, Н40.1 ОУ II А глаукома OU.
Интравитреальное введение Anti-VEGF препарата в левый глаз пятикратно по поводу ХНВ как осложнения ВМД и высокой миопии в 2020 г.: 13.05, 09.07, 12.08, 15.09, 14.10, без особой положительной динамики, ХНВ сохраняет активность 24.11.2020. С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены активные фокусы ХНВ. ФЛКС фокусов ХНВ 19 01 2020, Зрение на момент ФЛКС Vis OS=0.08 sph -2.5 D=0.09, через 2 недели, отмечает положительную динамику, снижение затуманенное™ Vis OS=0.09 sph - 2.5 D=0.1
29.01.2021 Vis OS=0.1 sph-2.5 D=0.2
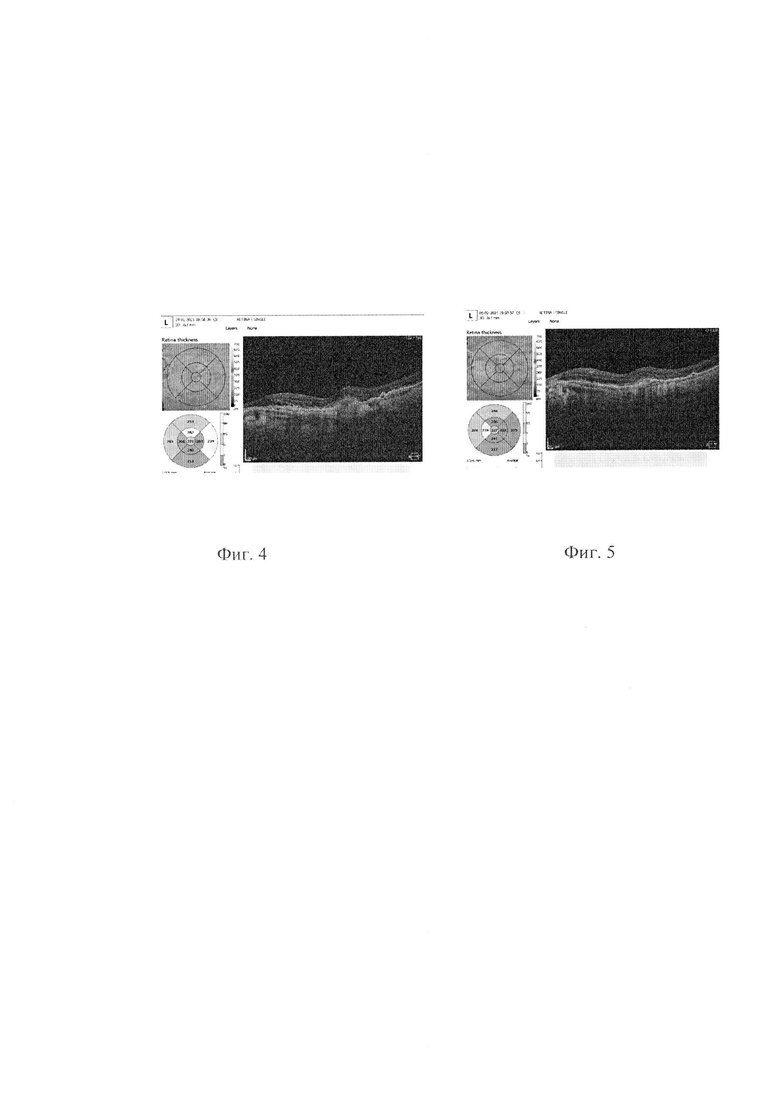
На фиг. 4 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 5 после лечения на 29. 01. 2021.
Пример 3
Пациентка Б., 1974 г.р.
Ds. Н36.0 Оперированная пролиферативная диабетическая ретинопатия. Н31.8 ХНВ, состояние после интравитреального введения Anti-VEGF препарата четырехкратно, состояние после ФЛКС зон ХНВ, состояние после четырех этапов ПрЛКС OS. Z96.1 Артифакия, состояние после ЗЛКТ OS. Субатрофия правого глаза.
До 03.2013 левый глаз не беспокоил, получала терапию от диабета, в июне 2013 зрение на левый глаз снизилось с 0.8 до 0.1, диагностирован высокий отек в МЗ и признаки ХНВ в проекции папиломакулярного пучка. Интравитреальное введение Anti-VEGF препарата в левый глаз поводу ХНВ на фоне пролифреативной ДР четырехкратно 09.2013, 10.2013, 11.2013, 12.2013, высота отека снижалась, но активность ХНВ не уменьшалась, за 1 -1.5 мес высота отека приходила на прежний уровень, появлялись свежие геморрагии. С помощью биомикроскопии, классической ОКТ, флуоресцентной ангиографии, был выявлен фокус активной ХНВ. Зрение на момент ФЛКС Vis OS=0.1 sph+2.0 D=0.2. 14 02 2014, ПрЛКС ФЛКС фокуса ХНВ, п/о период без особенностей, ХНВ неактивна. Динамическое наблюдение 2-3 раза в год с ОКТ, в течение 7 лет, активности ХНВ нет.
29.01.2020 Vis OS=0.4 sph+1.25 D=0.5
На фиг. 6 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 7 после лечения на 29.01.2020.
Пример 4
Пациент Т., 1942 г.р.
Ds. Н35.3 ВМД влажная форма, ХНВ, КМО, состояние после интравитреального введения Anti-VEGF препарата пятикратно, состояние после ФЛКС ХНВ, барраж МЗ OD, Н35.3 ВМД переходная форма OS, Н25.0 Начальная катаракта OU, Н40.1 ОУ II А глаукома OU.
ЖС на OS. Глаукома OU. В OU закапывает Дорзопт-плюс 2 р/д постоянно, Интравитреальное введение Anti-VEGF препарата в правый глаз 14.01.2019, 14.01.2020, 25.02.2020, 14.04.2020, проведена ФЛКС зон активной ХНВ и барраж МЗ на правый глаз 28.05.2020 зрение на момент ФЛКС 0.02 эксц. н\к, далее ИВВИАГ 04.08.2020, п/о период без особенностей, отмечает значительное снижение искажений предметов и «просветление темного пятна». Динамическое наблюдение, активности ХНВ нет.
Vis OD=0.04 н\к 15.04.2021
На фиг. 8 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 9 после лечения 15.04.2021.
Пример 5
Пациентка Д., 1951 г.р.
Ds. Н35.3 ВМД влажная форма, ХНВ, состояние после интравитреального введения Anti-VEGF препарата шестикратно, ФЛКС ХНВ OS. Н40.1 ОУ III а (опер, ПГ, ББ, ИКА) глаукома, артифакия OD. ОУ II А (опер, ПГ, ББ, ИКА) глаукома, периферический ретиношизис OS. Z96.1 Артифакия, минимальный фиброз задней капсулы хрусталика OS, Н31.8 Неву с хориоидеи OS.
Глаукома с 2010. OD ГСЭ 2012, OS ГСЭ 2014. В 2013 ЭК ИОЛ на правый глаз. Капает дорзопт плюс х 2, трилактан х 2. Интравитреальная инъекция Афлиберцепта в OS по поводу ХНВ как осложнения ВМД шестикратно, УЗ ФЭК ИОЛ OS с одновременным ИВВИАГ от 15.10.2019 крайняя ИВВИАГ 07.04.2020, в конце 2020 года жалобы на снижение зрения, искажения предметов пред левым глазом.
С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены 5 активных фокусов ХНВ. ФЛКС фокусов ХНВ. 26.01.2020, зрение на момент проведения ФЛКС левого глаза 0.4 sph - 2.0 D=0.6, п/о период без особенностей, отмечает отсутствие искажений предметов и повышение остроты зрения. Динамическое наблюдение, активности ХНВ нет.
Vis OS=0.8 sph-2.0 D=0.9 12.03.2021
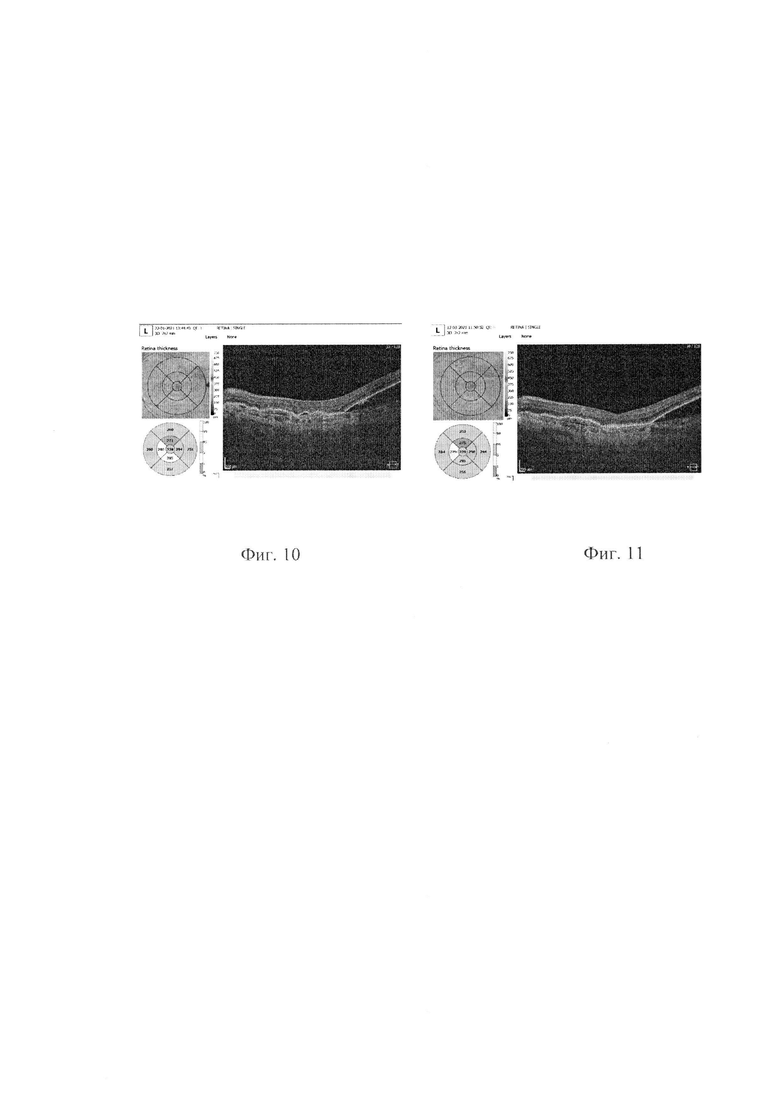
На фиг. 10 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 11 после лечения 12.03.2021.
Пример 6
Пациентка Я., 1938 г.р.
Ds. Н35.3 ВМД влажная форма, ХНВ, КМО, состояние после интравитреального введения Anti-VEGF препарата, ФЛКС ХНВ OS. ВМД влажная форма, исход, ретинофиброз, состояние после интравитреального введения Anti-VEGF препарата OD почти зрелая катаракта OD; Артифакия, состояние после ЗЛКТ OS; Миопический астигматизм OU; Ангиопатия смешанного генеза OU.
Интравитреальное введение Anti-VEGF препарата трехкратно в правый глаз по поводу ХНВ, УЗ ФЭК ИОЛ OS 2013, ЗЛКТ 04.16.2015. Интравитреальное введение Anti-VEGF препарата в левый глаз 10 раз, крайний 07.10.2021. При динамическом наблюдении отмечается активность ХНВ. С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены несколько активных фокусов ХНВ. ФЛКС фокусов ХНВ. 11 01 2021, зрение на момент проведения ФЛКС левого глаза 0.1 н.к. П/о период без особенностей, отмечает отсутствие искажений предметов и повышение остроты зрения дополнительное введение Anti-VEGF 26.01.2021. Динамическое наблюдение, активности ХНВ нет.
VOS=0.2н\к 29.01.2020
На фиг. 12 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 13 после лечения
Пример 7
Пациентка Б., 1947 г.р.
Ds. Н35.3 ВМД влажная форма, смешанная форма ХНВ, состояние после ИВВИА, состояние после ЛКС OD. ВМД сухая форма OS. Начальная осложненная катаракта, псевдоэксфоллиативный синдром, ангиосклероз сетчатки OU.
Интравитреальное введение Anti-VEGF препарата в правый глаз пятикратно, без особой положительной динамики, ХНВ сохраняет активность. Жалобы на низкое зрение и умеренные метаморфопсии. С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены 2 обширных активных фокуса смешанной ХНВ. ФЛКС фокусов ХНВ. 05.03.2021, зрение на момент проведения ФЛКС левого глаза Vis OS=0.2sph+1.0 D=0.3, п/о период без особенностей, через 2 недели отмечает отсутствие искажений предметов и повышение остроты зрения. Динамическое наблюдение, активности ХНВ нет.
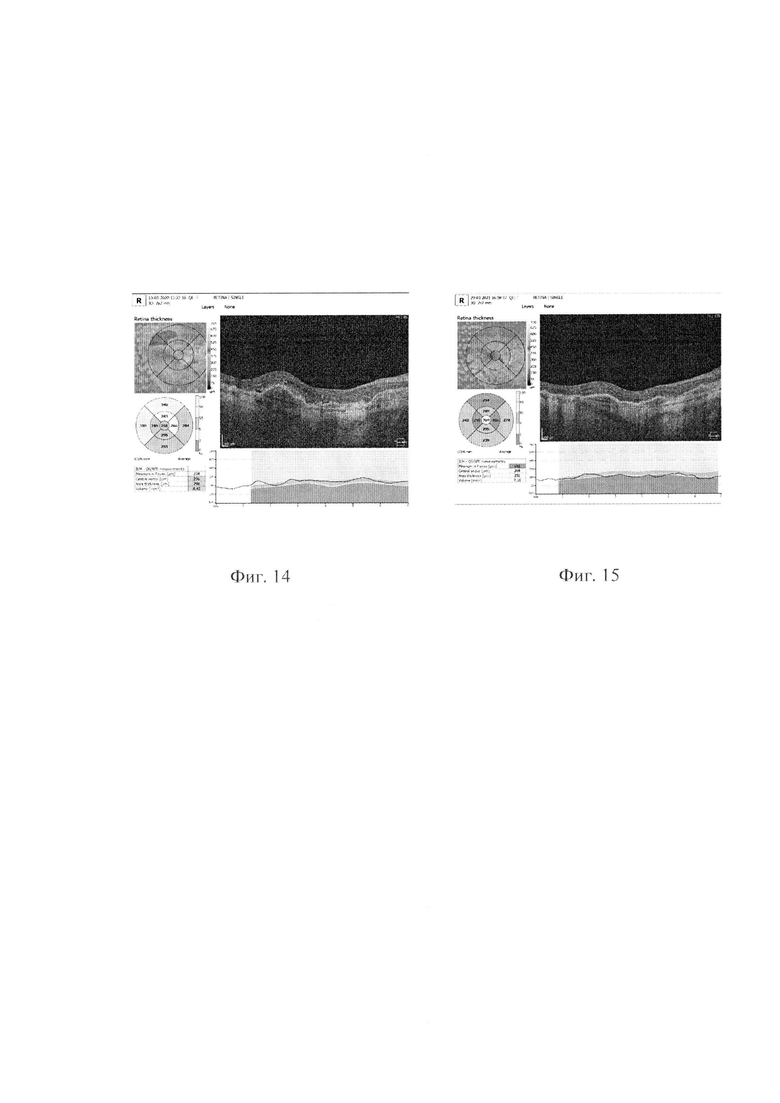
На фиг. 14 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 15 после лечения 29.03.2021.
Vis OS=0.2sph+1.0 D=0.3 29.03.2021
Пример 8
Пациентка Л., 1965 г.р.
Ds. Н 35.9 ЦСХРП, осложненная ХНВ OD., Артифакия, состояние после ЗЗВЭ OD Состояние после многократного интравитреального введения Anti-VEGF препарата, ФЛКС ХНВ OD.
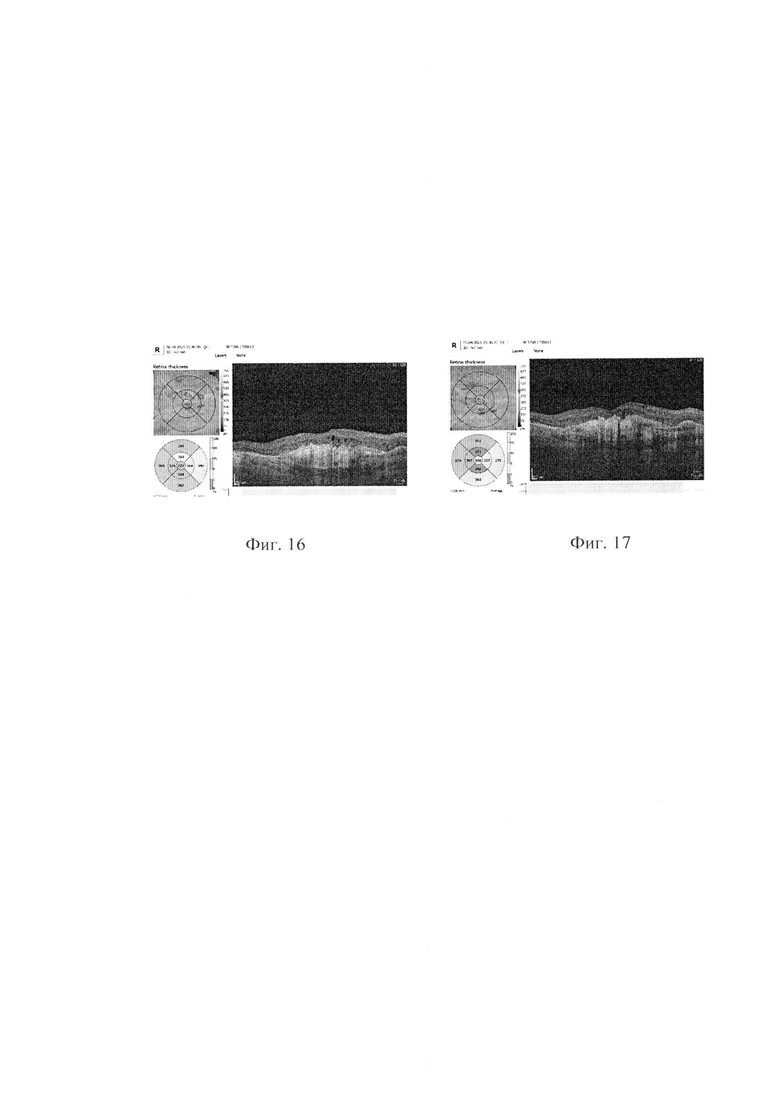
Жалобы на снижение зрение, «затуманенность» появились 09.2010 диагностирована ЦСХРП, дефекты ПЭС (два фокуса) выявлены с помощью ДФАГ, проведена ФЛКС, по период без особенностей. 10.2014 Обширное субретинальное кровоизлияние, обширная активная ХНВ OD, многочисленные ИВВИАГ, в 10.2014. Гемофтальм. 33 В. 29.03.2016 ФЭК ИОЛ OD. В 06.2017 повторная ДФАГ - обширная ХНВ с выходом за аркады, было продолжено ИВВИАГ, всего 38 инъекций, последние 26.03.2021. Высота отека снижалась, но активность ХНВ не уменьшалась, за 2-3 мес высота отека приходила на прежний уровень снижалось зрение, усиливались искажения и «пелена». С помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлены обширные активные зоны смешанной ХНВ. ФЛКС ХНВ. 01.04.2021, зрение на момент проведения ФЛКС правого глаза VisOD=0.16 н/к, п/о период без особенностей, активность ХНВ снижена,. Уменьшилась отечность внутренних слоев сетчатки, пациента отмечает улучшение, продолжено динамическое наблюдение.
VisOD=0.2 н/к 15.04.2021
На фиг. 16 представлены данные ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 17 после лечения на 15.04.2021.
Пример 9
Пациентка Р., 1961 г.р.
Н34.9 Постромботическая ретинопатия, осложненная ХНВ, КМО, состояние после пятикратного интравитреального введения Anti-VEGF препарата, состояние после витрэктомии, ПТРП, артифакия, OD. ФЛКС ХНВ OD Синдром сухого глаза OU.
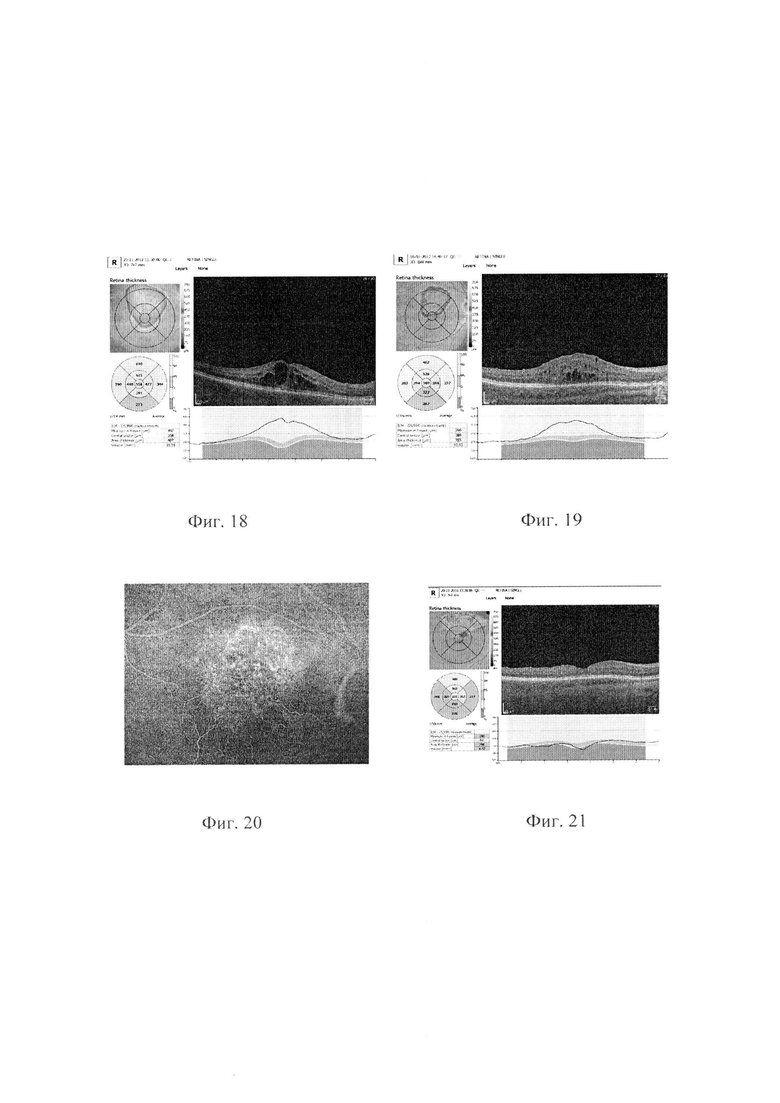
В 2010 г. тромбоз ветви ЦВС OD. Пятикратно ИВИ анти VEGF. 01.03.2016 33 В, удаление ЭРМ OD. 11.10.2016 ФЭК ИОЛ. В начале 2017 жалобы на искажения предметов, снижение зрения. С помощью биомикроскопии, классической ОКТ, флуоресцентной ангиографии, был выявлен фокус активной ХНВ, 06.02.2017 проведена ФЛКС фокуса, зрение на момент проведения ФЛКС правого глаза. 0.4 н/к, п/о период без особенностей, через 2 недели отмечает отсутствие искажений предметов и повышение остроты зрения. Динамическое наблюдение, активности ХНВ нет. 25.05.2017 дополнительное введение Anti-VEGF. Сейчас пациентка живет в другом городе по телефонной связи сообщает, что эффект от лечения держится, субъективно и по ОКТ изменений нет.
VisOD=0.9 н/к 20.11.2018
На фиг. 18 представлены данные ОКТ и толщина сетчатки в макулярной зоне в ближайший месяц после тромбоза ветви ЦВС, на фиг. 19 представлены данные ОКТ и толщина сетчатки в макулярной зоне в момент развития ХНВ, на фиг. 20 представлена картина ХНВ при флуоресцентной ангиографии, на фиг. 21 представлены данные ОКТ и толщина сетчатки в макулярной зоне после лечения.
Пример 10
Пациент Ш., 1960 г.р.
Ds. Н35.3 ВМД влажная форма, ХНВ, состояние после интравитреального введения Anti-VEGF препарата многократно, состояние после ФЛКС ХНВ OS, Н35.3 ВМД переходная форма OS, Н25.0. Начальная катаракта OU.
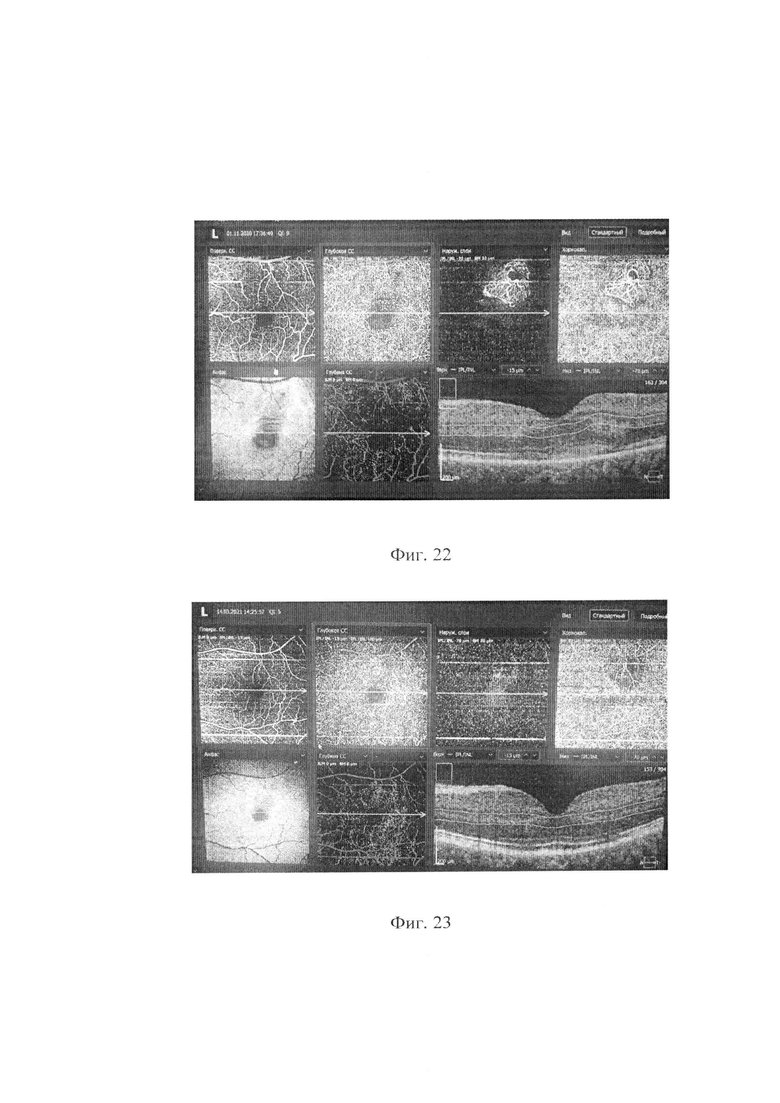
Интравитреальное введение Anti-VEGF препарата девять раз в правый глаз по поводу ХНВ. В 2019-20 с помощью биомикроскопии, классической ОКТ, ангио ОКТ, аутофлуоресценции были выявлен фокус активной смешанной ХНВ. ФЛКС фокусов ХНВ 05.11.2020. Зрение на момент ФЛКС Vis OS=0.4 н/к, через 2 недели отмечает положительную динамику, снижение затуманенности.
Vis OS=0.95 14.03.2021
На фиг. 22 представлены данные ангио ОКТ и толщина сетчатки в макулярной зоне до лечения, на фиг. 23 после лечения. При демонстрации данных фигур следует обратить внимание на то, что размеры и визуализация фокуса ХНВ при флуоресцентной ангиографии фиг. 20 соответствует данным ангио ОКТ на фиг 22 и фиг. 23.
ВЫВОДЫ
1. Выработана наиболее эффективная и безопасная схема лечения большинства ХНВ различной этиологии. Схема лечения является комбинацией двух самых эффективных методов лечения ХНВ в настоящее время.
2. Пернициозная хориоидальная неоваскуляризация обладает рядом характерных признаков, выявляемых клиническими методами диагностики, и не поддается даже многократным инъекциям антиангиогенных препаратов.
3. Интравитреальное применение ингибитора ангиогенеза при таком типе ХНВ приводит к клинически значимому снижению патологического процесса в аваскулярной зоне по данным ОКТ и ФАГ, но не устраняет процесс патологического ангиогенеза полностью.
4. ЛК ХНВ приводит к ее полному исчезновению в месте коагуляции, но ее применение сильно ограничено локализацией ХНВ относительно фовеа, а также возможной географической атрофией. Невозможно безопасно коагулировать ХНВ, если даже ее часть подходит парафовеолярно.
5. ИВВИАГ в сочетании с коагуляцией ХНВ позволяет воздействовать на любой тип ХНВ с любой локализацией ХНВ. Под прикрытием ИВВИАГ возможна частичная лазерная коагуляция ХНВ в пределах безопасности для фовеолы, прежде всего из-за возможной географической атрофии ПЭС. Под прикрытием ИВВИАГ, ХНВ при лазерной коагуляции не в полном объеме не может активироваться и дальше пролиферировать. В свою очередь, лазерная коагуляция ХНВ в месте ее применения приводит к полному исчезновению ХНВ как биологической структуры.
6. Интравитреальное применение, введение ингибиторов ангиогенеза, подходит для любого места локализации ХНВ. Но процедура является инвазивной, в 99% случаев требуются кратные инъекции, важен временной интервал, ХНВ часто рецидивирует, важно постоянное динамическое наблюдение. Длительно существующие ХНВ становятся резистентыми к антиангиогенной терапии и также вызывают атрофию ПЭС
7. Оценки данных ОКТ, ангио ОКТ и ФАГ после кратных инъекций антиангиогенных препаратов позволяет адекватно провести классическую лазеркоагуляцию оставшихся зон патологического процесса.
8. Показания к выполнению ФАГ в ходе динамического наблюдения за пациентами с ХНВ зависят от типа реакции на антиангиогенную терапию в сочетании с ЛК ХНВ.
9. Комбинация ИВВИАГ с коагуляцией ХНВ позволяет надежно и длительно остановить процесс патологического ангиогенеза в центральной зоне сетчатки. Эффект после такого лечения может сохраняться более 5 лет.
10. Требуется индивидуальный подход к каждому пациенту, в зависимости от типа, локализации, активности и площади ХНВ. Все эти данные получают при обследовании с использованием ангио ОКТ, аутофлуоресценции, флуоресцентной ангиографии, биомикроскопии. И других необходимых методов исследования в каждом конкретном случае.
11. Необходимо проводить анализ и исследование изменения архитектоники сетчатки и прежде всего ангиоархитектоники хориоидеи, все это в будущем позволит еще усовершенствовать метод.
12. Необходимо изучение вопроса о возможном выделении медиатора антиангиогенеза при таких обширных коагуляциях, что дает свой положительный лечебный эффект.
Источники информации:
1. Libman E.S. [Blindness and disability due to pathology of the vision in Russia]. Slepota i invalidnosb vsledstvie patologii organa zrenija v Rossii. Ophthalmology. National manual. Ed. by SJe. Avetisov, E.A. Egorov, L.K. Moshetova, V.V. Neroev. M., 2008:38-41 (in Russ.).
2. MPS (Macular Photocoagulation Study Research Group) 1991.
3. WolfS., Balciuniene V.J., Laganovska G., Menchini U., Ohno-Matsui K., Sharma Т., Wong T.Y., Silva R., Pilz S., Gekkieva M. RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology. 2014.
4. Tufail A., Narendran N., Patel P.J. et al. Ranibizumab in myopic choroidal neovascularisation: the 12-month results from the REPAIR study. Ophthalmology. 2013.
5. Bojko Je.V., Sosnovskij S.V., Berezin R.D., Kacherovich P.A., Tavtilova D.A. [Intraviteral injections: theory and practice] Intraviterabnye in#ekcii: teorija i praktika. [Ophthalmic journal]. Oftabmologicheskie vedomosti. 2010;2:28-35 (in Russ.).
6. Izmajlov A.S., Balashevich L.I. Choroidal neovascularization, diagnostics and treatment. SPb. 2001; 7. Ivanishko Yu. A., 2004; 8. Mazunin I. Yu., 2009; 9. Jalkh A.E., 1987; 10. Oshima Y., 1998; 11. Pece A., 1994; 12. Ruiz-Moreno J.M., 2002; 13. Secretan M., 1997;
14. Virgili G., Menchini F. Laser photocoagulation for choroidal neovascularisation in pathologic myopia. Cochrane Database Syst. Rev. 2005; 19(4): CD 004765.
15.Medvedev I.B., Belikova E.I., Sjamichev M.P. Photodynamic therapy with Vizudin in treatment of choroidal neovascularization at complicated myopia. Annals of ophthalmology. Вестник офтальмологии, 2007; 6: 23-25.
16. Патент RU 2290973 C1, опубл. 12.07.2005
17. патент RU 2676075 опубл 27.12.2018
18. Акопян B.C. и др., Морфологические и иммуногистохимические особенности субпорогового лазерного воздействия на сетчатку. Современные технологии в офтальмологии. №1, 2015, с. 15-16.
19. Патент RU 2467727 С2, опубл. 27.11.2012
20. Патент RU 2395318 С1, опубл. 27.07.2010
21. Патент RU 2452443 С1, опубл. 10.06.2012
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования ответа на повторную анти-VEGF терапию хориоидальной неоваскуляризации при ВМД | 2022 |
|
RU2788971C1 |
| Способ лечения хориоидальной неоваскуляризации | 2018 |
|
RU2676075C1 |
| Способ дифференциальной диагностики миопической хориоидальной неоваскуляризации и неоваскулярной возрастной макулярной дегенерации на миопических глазах | 2020 |
|
RU2749120C1 |
| Способ прогнозирования анатомических результатов anti-VEGF терапии васкулярной отслойки пигментного эпителия сетчатки | 2024 |
|
RU2836567C1 |
| Способ топографически-ориентированного лазерного лечения субактивных хориоидальных неоваскулярных мембран экстрафовеальной локализации на навигационной лазерной установке | 2022 |
|
RU2777740C1 |
| Способ лечения активных хориоидальных неоваскулярных мембран экстрафовеальной локализации | 2022 |
|
RU2777739C1 |
| Способ комбинированного лечения пациентов с хориоидальной неоваскуляризацией I типа на фоне хронической центральной серозной хориоретинопатии | 2021 |
|
RU2762769C1 |
| Способ определения показаний к антиангиогенной терапии при подозрении на влажную форму возрастной макулярной дегенерации | 2021 |
|
RU2758662C1 |
| Способ прогнозирования эффективности лечения неоваскулярной формы ВМД | 2022 |
|
RU2788103C1 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ХОРИОИДАЛЬНОЙ НЕОВАСКУЛЯРИЗАЦИИ | 2008 |
|
RU2375023C1 |



Изобретение относится к медицине, а именно к офтальмологии. Осуществляют интравитреальное введение ингибиторов ангиогенеза и лазерную коагуляцию фокусов хориоидальной неоваскуляризации (XHB). При выявлении активных фокусов XHB после интравитреальных инъекций ингибитора ангиогенеза, проводят лазерную коагуляцию фокуса XHB, от внешнего края фокуса к его центру. При этом используют длину волны лазерного излучения 532 нм, мощность 200-350 м Вт, длительностью импульса 0,05-0,07 с, периодом между импульсами 0,2-0,3 с, диаметром пятна лазерного аппликата 300 мкм, в количестве лазерных аппликатов 150-1300 шт, где каждый следующий коагулят примыкает к предыдущему. При этом первый проход лазера начинают с применением лазерных коагулятов II степени по шкале L’Esperance, фокус подвергают трёхкратной коагуляции с постепенным повышением на четверть энергии лазерного излучения от первоначальных параметров. В частном случае при сохранении активности XHB проводят дополнительные интравитреальные инъекции ингибитора ангиогенеза. Способ позволяет надежно и безопасно ограничить и даже полностью прекратить процесс патологического хориоидального ангиогенеза, со стойким эффектом. 1 з.п. ф-лы, 10 пр., 23 ил.
1. Комбинированный способ лечения хориоидальной неоваскуляризации, включающий интравитреальное введение ингибиторов ангиогенеза и лазерную коагуляцию фокусов хориоидальной неоваскуляризации (XHB), отличающийся тем, что при выявлении активных фокусов XHB после интравитреальных инъекций ингибитора ангиогенеза, проводят лазерную коагуляцию фокуса XHB, от внешнего края фокуса к его центру, при этом используют длину волны лазерного излучения 532 нм, мощность 200-350 м Вт, длительностью импульса 0,05-0,07 с, периодом между импульсами 0,2-0,3 с, диаметром пятна лазерного аппликата 300 мкм, в количестве лазерных аппликатов 150-1300 шт, где каждый следующий коагулят примыкает к предыдущему, при этом первый проход лазера начинают с применением лазерных коагулятов II степени по шкале L’Esperance, фокус подвергают трёхкратной коагуляции с постепенным повышением на четверть энергии лазерного излучения от первоначальных параметров.
2. Способ по п. 1, отличающийся тем, что при сохранении активности XHB проводят дополнительные интравитреальные инъекции ингибитора ангиогенеза.
| Майорова А.М | |||
| Полипоидная хориоидальная васкулопатия как подтип возрастной макулярной дегенерации: диагностика и лечение, М., 2018, С | |||
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| Ranson N.T | |||
| et al | |||
| Intravitreal triamcinolone in subfoveal recurrence of choroidal neovascularisation after laser treatment in macular degeneration | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Gisele Soubrane, Neil M | |||
Авторы
Даты
2022-04-21—Публикация
2021-04-21—Подача