ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет относительно заявки на патент США № 62/598 267, поданной 13 декабря 2017 года, содержание которой полностью включено в настоящий документ посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Заявка содержит перечень последовательностей, который представлен в электронном формате ASCII и полностью включен в данный документ посредством ссылки. Указанная копия ASCII, созданная 13 декабря 2018 года, названа 104409_000448_sequence_listing.txt и составляет 8 797 байтов по размеру.
ОБЛАСТЬ ТЕХНИКИ
[0003] Настоящее изобретение относится к Сурвивин-антигенам и молекулам нуклеиновой кислоты, кодирующим их. Настоящее изобретение также относится к вакцинам, содержащим такие Сурвивин-антигены и/или молекулы нуклеиновых кислот. Настоящее изобретение дополнительно относится к способам использования вакцин для индукции иммунных ответов и предотвращения и/или лечения субъектов, имеющих раковые клетки и/или опухоли, которые экспрессируют сурвивин.
УРОВЕНЬ ТЕХНИКИ
[0004] Рак является одной из основных причин смерти во всем мире. В Соединенных Штатах рак является второй наиболее распространенной причиной смерти, на которую приходится приблизительно 1 из каждых 4 смертей. Рак возникает из одной клетки, которая трансформировалась из нормальной клетки в раковую клетку. Такая трансформация часто является многостадийным процессом, переходящим от предракового поражения к злокачественному новообразованию. Множество факторов способствуют прогрессированию этого, включая старение, генетический вклад и воздействие внешних факторов, таких как физические канцерогены (например, ультрафиолетовое и ионизирующее излучение), химические канцерогены (например, асбест, компоненты табачного дыма и т.д.) и биологические канцерогены (например, некоторые вирусы, бактерии и паразиты).
[0005] Профилактика, диагностика и лечение рака могут принимать различные формы. Профилактика может включать скрининг на предрасполагающие факторы (например, конкретные генетические варианты), изменение поведения (например, курение, диета и уровень физической активности) и вакцинацию против вирусов (например, от вируса гепатита В, вируса папилломы человека). Лечение может включать химиотерапию, лучевую терапию и хирургическое удаление опухоли или раковой ткани. Несмотря на наличие многочисленных способов профилактики и лечения, такие способы часто имеют ограниченный успех в эффективной профилактике и/или лечении рака.
[0006] Сурвивин, также известный как бакуловирусный ингибитор апоптоза, содержащий повтор 5 (BIRC5), является ингибитором апоптоза, который блокирует функцию каспазы и тем самым предотвращает запрограммированную смерть клеток. В дополнение к своей роли в апоптозе Сурвивин однозначно играет существенную эволюционно консервативную роль в митозе. (Li, F. et al. Control of apoptosis and mitotic spindle checkpoint by Survivin. Nature 396, 580-584, doi:10.1038/25141 (1998).) Сверхэкспрессия Сурвивина связана с пролиферацией опухолевых клеток, прогрессированием, ангиогенезом, терапевтической устойчивостью и неблагоприятным прогнозом. В здоровых клетках и тканях экспрессия Сурвивина либо отсутствует, либо присутствует на низких уровнях. Однако Сурвивин является членом семейства ингибиторов белка апоптоза (IAP), и гены IAP высоко экспрессируются в различных раковых клетках и первичных биопсиях опухоли. Среди IAP Сурвивин демонстрирует наиболее отчетливую сверхэкспрессию в опухолях и эмбриональных тканях. В многочисленных исследованиях рака яичников число образцов пациентов с положительным результатом на экспрессию Сурвивина составляло от 74 до 92%. (См. Cohen, C., Lohmann, C. M., Cotsonis, G., Lawson, D. & Santoianni, R. Survivin expression in ovarian carcinoma: correlation with apoptotic markers and prognosis. Modern pathology : an official journal of the United States and Canadian Academy of Pathology, Inc 16, 574-583, doi:10.1097/01.MP.0000073868.31297.B0 (2003); Felisiak-Golabek, A. et al. Nuclear Survivin expression is a positive prognostic factor in taxane-platinum-treated ovarian cancer patients. Journal of ovarian research 4, 20, doi:10.1186/1757-2215-4-20 (2011).) Вклад сурвивина в онкогенез в сочетании с его ограниченным паттерном экспрессии и сверхэкспрессии в различных опухолях делает его привлекательной мишенью для иммунотерапии рака.
[0007] Сурвивин представляет собой наименьший член семейства IAP. Это белок весом 16,3 кДа, состоящий из 142 аминокислот и характеризующийся наличием одного BIR-повтора. Он также не имеет карбоксильного концевого пальцевого домена RING в своей белковой структуре. (Chen, X., Duan, N., Zhang, C. & Zhang, W. Survivin and Tumorigenesis: Molecular Mechanisms and Therapeutic Strategies. Journal of Cancer 7, 314-323, doi:10.7150/jca.13332 (2016).) Было идентифицировано несколько изоформ Сурвивина, а изоформа Сурвивина 1 является доминирующим транскриптом. Сурвивин экспрессируется во время развития плода, но не экспрессируется в полностью дифференцированных тканях. Однако он на высоком уровне экспрессируется во многих раковых клетках. Таким образом, Сурвивин является потенциальным антигеном-мишенью для лечения рака.
[0008] Представляют интерес вакцины для лечения и профилактики рака, в частности эпителиального рака яичников (ЭКЯ). Однако существующие вакцины, нацеленные на антигены опухолевых клеток, ограничены плохой экспрессией антигена in vivo. Соответственно, в данной области техники сохраняется потребность в безопасных и эффективных вакцинах и способах их применения для профилактики и/или лечения рака и снижения смертности у субъектов, страдающих от рака.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
[0009] В данном документе предложены:
[0010] Молекулы нуклеиновых кислот, содержащие одну или более последовательностей нуклеиновых кислот, выбранных из группы, состоящей из: (a) последовательности нуклеиновой кислоты, которая кодирует аминокислоты 19-159 SEQ ID NO:2; (б) последовательности нуклеиновой кислоты, которая кодирует аминокислоты 19-210 SEQ ID NO:4; (в) последовательности нуклеиновой кислоты, которая кодирует аминокислоты 19-232 SEQ ID NO:8; (г) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины аминокислот 19-159 SEQ ID NO:2; (д) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины аминокислот 19-210 SEQ ID NO:4; (е) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины аминокислот 19-232 SEQ ID NO:8; (ж) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен аминокислотам 19-159 SEQ ID NO:2; (з) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен аминокислотам 19-210 SEQ ID NO:4; (и) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен аминокислотам 19-232 SEQ ID NO:8; (к) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен аминокислотам 19-159 SEQ ID NO:2; (л) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен аминокислотам 19-210 SEQ ID NO:4; и (м) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен аминокислотам 19-232 SEQ ID NO:8.
[0011] Молекулы нуклеиновых кислот, содержащие одну или более последовательностей нуклеиновых кислот, выбранных из группы, состоящей из: (a) нуклеотидов 55-423 SEQ ID NO:1; (б) нуклеотидов 55-636 SEQ ID NO:3; (в) фрагмента, содержащего по меньшей мере 90% всей длины нуклеотидов 55-423 SEQ ID NO:1; (г) фрагмента, содержащего по меньшей мере 90% всей длины нуклеотидов 55-636 SEQ ID NO:3; (д) фрагмента, который по меньшей мере на 95% идентичен нуклеотидам 55-423 SEQ ID NO:1; (е) фрагмента, который по меньшей мере на 95% идентичен нуклеотидам 55-636 SEQ ID NO:3; (ж) фрагмента, содержащего по меньшей мере 90% последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична нуклеотидам 55-423 SEQ ID NO:1; и (з) фрагмента, содержащего по меньшей мере 90% последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична нуклеотидам 55-636 SEQ ID NO:3.
[0012] Молекулы нуклеиновых кислот, содержащие одну или более последовательностей нуклеиновых кислот, выбранных из группы, состоящей из: (a) последовательности нуклеиновой кислоты, которая кодирует SEQ ID NO:2; (б) последовательности нуклеиновой кислоты, которая кодирует SEQ ID NO:4; (в) последовательности нуклеиновой кислоты, которая кодирует SEQ ID NO:8; (г) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины SEQ ID NO:2; (д) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины SEQ ID NO:4; (е) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины SEQ ID NO:8; (ж) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен SEQ ID NO:2; (з) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен SEQ ID NO:4; (и) последовательности нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен SEQ ID NO:8; (к) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:2; (л) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:4; и (м) последовательности нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:8.
[0013] Молекулы нуклеиновых кислот, содержащие одну или более последовательностей нуклеиновых кислот, выбранных из группы, состоящей из: (a) SEQ ID NO:1; (б) SEQ ID NO:3; (в) фрагмента, содержащего по меньшей мере 90% всей длины SEQ ID NO:1; (г) фрагмента, содержащего по меньшей мере 90% всей длины SEQ ID NO:3; (д) фрагмента, который по меньшей мере на 95% идентичен SEQ ID NO:1; (е) фрагмента, который по меньшей мере на 95% идентичен SEQ ID NO:3; (ж) фрагмента, содержащего по меньшей мере 90% всей длины последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична SEQ ID NO:1; и (з) фрагмента, содержащего по меньшей мере 90% всей длины последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична SEQ ID NO:3.
[0014] Молекулы нуклеиновой кислоты, содержащие последовательность нуклеиновой кислоты, приведенную в SEQ ID NO:1.
[0015] Молекулы нуклеиновой кислоты, содержащие последовательность нуклеиновой кислоты, приведенную в SEQ ID NO:3.
[0016] Молекулы нуклеиновой кислоты, согласно настоящему описанию, для применения в качестве лекарственного средства.
[0017] Молекулы нуклеиновой кислоты, согласно настоящему описанию, для применения в качестве лекарственного средства при лечении рака.
[0018] Молекулы нуклеиновой кислоты, согласно настоящему описанию, для использования при получении лекарственного средства.
[0019] Молекулы нуклеиновой кислоты, согласно настоящему описанию, для применения в получении лекарственного средства для лечения рака.
[0020] Векторы, содержащие молекулу нуклеиновой кислоты, согласно настоящему описанию.
[0021] Векторы, содержащие плазмиду или вирусный вектор.
[0022] Композиции, содержащие одну или более молекул нуклеиновой кислоты, согласно настоящему описанию.
[0023] Композиции, согласно настоящему описанию, содержащие фармацевтически приемлемый носитель.
[0024] Композиции, согласно настоящему описанию, содержащие один или более векторов, согласно настоящему описанию.
[0025] Белки, содержащие аминокислотную последовательность, выбранную из группы, состоящей из: (a) аминокислот 19-159 SEQ ID NO:2; (б) аминокислот 19-210 SEQ ID NO:4; (в) аминокислот 19-232 SEQ ID NO:8; (г) фрагмента, содержащего по меньшей мере 90% всей длины аминокислот 19-159 SEQ ID NO:2; (д) фрагмента, содержащего по меньшей мере 90% всей длины аминокислот 19-210 SEQ ID NO:4; (е) фрагмента, содержащего по меньшей мере 90% всей длины аминокислот 19-232 SEQ ID NO:8; (ж) аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-159 SEQ ID NO:2; (з) аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-210 SEQ ID NO:4; (и) аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-232 SEQ ID NO:8; (к) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-159 SEQ ID NO:2; (л) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-210 SEQ ID NO:4; и (м) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична аминокислотам 19-232 SEQ ID NO:8.
[0026] Белки, содержащие аминокислотную последовательность, выбранную из группы, состоящей из: (a) SEQ ID NO:2; (б) SEQ ID NO:4; (в) SEQ ID NO:8; (г) фрагмента, содержащего по меньшей мере 90% всей длины SEQ ID NO:2; (д) фрагмента, содержащего по меньшей мере 90% всей длины SEQ ID NO:4; (е) фрагмента, содержащего по меньшей мере 90% всей длины SEQ ID NO:8; (ж) аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:2; (з) аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:4; (и) аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:8; (к) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:2; (л) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:4; и (м) фрагмента, содержащего по меньшей мере 90% всей длины аминокислотной последовательности, которая по меньшей мере на 95% идентична SEQ ID NO:8.
[0027] Белки, содержащие аминокислотную последовательность, приведенную в SEQ ID NO:2.
[0028] Белки, содержащие аминокислотную последовательность, приведенную в SEQ ID NO:4.
[0029] Белки, содержащие аминокислотную последовательность, приведенную в SEQ ID NO:8.
[0030] Вакцины, содержащие молекулы нуклеиновой кислоты, согласно настоящему описанию.
[0031] Вакцины, содержащие вектор, согласно настоящему описанию.
[0032] Вакцины, согласно настоящему описанию, дополнительно содержащие фармацевтически приемлемый наполнитель.
[0033] Вакцины, согласно настоящему описанию, дополнительно содержащие адъювант.
[0034] Вакцины, согласно настоящему описанию, где адъювант представляет собой IL-12, IL-15, IL-28 или RANTES.
[0035] Способы лечения субъекта с сурвивин-экспрессирующей раковой клеткой, включающий введение терапевтически эффективного количества вакцины согласно настоящему описанию.
[0036] Способы, согласно настоящему описанию, в которых введение включает стадию электропорации.
[0037] Способы, согласно настоящему описанию, в которых введение осуществляется в одно или более мест субъекта.
[0038] Способы вакцинации субъекта против сурвивин-экспрессирующей раковой клетки, включающие введение количества вакцины, согласно настоящему описанию, эффективного для индукции гуморального или клеточного иммунного ответа.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0039] Краткое описание, а также нижеследующее подробное описание более понятны при прочтении вместе с прилагаемыми графическими материалами. В целях иллюстрации изобретения на графических материалах показаны примеры вариантов воплощения изобретения; однако изобретение не ограничено конкретными раскрытыми способами, композициями и устройствами. В графических материалах:
[0040] На фиг. 1 показано схематическое представление изофомы 1 синтетического консенсусного антигена Сурвивин. Звездочки обозначают мутации, необходимые для устранения антиапоптотической активности.
[0041] На фиг.2 показана общая структура мономера A (слева) и мономера B (справа) изоформы 1 синтетического консенсусного антигена Сурвивина. Изменения относительно нативного Сурвивина обозначены сферами.
[0042] На фиг. 3 показано схематическое представление изофомы 1T3 синтетического консенсусного антигена Сурвивин. Звездочки обозначают мутации, необходимые для устранения антиапоптотической активности. Темно-серая область справа (3’) представляет укороченную область изоформы Сурвивина 3 (T3).
[0043] На фиг.4 показана конструкция pGX1428, содержащая изоформу 1 синтетического консенсусного антигена Сурвивин.
[0044] На фиг.5 показана конструкция pGX1429, содержащая изоформу 1T3 синтетического консенсусного антигена Сурвивин.
[0045] На фиг.6 показана экспрессия белков синтетического консенсусного антигена Сурвивина 1 и синтетического консенсусного антигена Сурвивина 1Т3 в клетках рабдомиосаркомы человека (RD), трансфецированных pGX1428 и pGX1429, соответственно, с помощью иммуноблоттинга. Белковые полосы ожидаемой молекулярной массы были обнаружены для pGX1428 (17,5 кДа) и pGX1429 (25,3 кДа). β-Актин использовали в качестве контроля для нанесения.
[0046] На фиг. 7A-7H показана иммуногенность синтетического консенсусного антигена Сурвивина 1 и синтетического консенсусного антигена Сурвивина 1T3. Самки CB6F1 были иммунизированы 3 раза с интервалом в 3 недели указанными дозами Сурвивина 1 (pGX1428) (фиг. 7A-7D), Сурвивина 1T3 pGX1429 (E-H) (n=8/группа) или pGX0001 (пустой вектор) (n=4). На фиг. 7A: Сурвивин 1-специфичные ответы IFNγ с помощью ELISpot при указанных количествах дозы pGX1428. На фиг. 7B: Ответы Сурвивин 1-специфических CD4+Т-клеток. На фиг. 7C: Ответы Сурвивин 1-специфических CD8+Т-клеток. На фиг. 7D: Сурвивин 1T3-специфичные ответы IFNγ с помощью ELISpot при указанных количествах дозы pGX1429. На фиг. 7E: Ответы Сурвивин 1T3-специфических CD4+Т-клеток. На фиг. 7F: Ответы Сурвивин 1T3-специфических CD8+Т-клеток. На фиг. 7G: Цитокиновый профиль ответов Сурвивин 1-специфичных CD4+Т-клеток и CD8+Т-клеток. На фиг. 7H: Цитокиновый профиль ответов Сурвивин 1T3-специфичных CD4+Т-клеток и CD8+Т-клеток.
[0047] На фиг. 8 показана стратегия гейтирования проточной цитометрии.
[0048] На фиг. 9 показана относительная частота CD4+и CD8+Т-клеток. Клеточные иммунные ответы, индуцированные pGX1428 и pGX1429, были преимущественно в компартменте CD4+T-клеток относительно компартмента CD8+T-клеток.
[0049] На фиг. 10A-10F показан цитолитический потенциал Сурвивин-специфических Т-клеток. Цитолитический потенциал антигенспецифических Т-клеток, индуцированных Сурвивином 1 и Сурвивином 1T3. На фиг. 10A: Частота Сурвивин 1-специфических CD4+CD107a+Т-клеток. На фиг. 10B: Частота Сурвивин 1T3-специфических CD4+CD107a+Т-клеток. На фиг. 10C: Цитокиновый профиль CD4+CD107a+ T-клеток. На фиг. 10D: Частота Сурвивин 1-специфических CD8+CD107a+Т-клеток. На фиг. 10E: Частота Сурвивин 1T3-специфических CD8+CD107a+Т-клеток. На фиг. 10F: Цитокиновый профиль CD4+CD107a+ T-клеток.
[0050] На фиг. 11A-11D показано картирование эпитопа ответов IFN-гамма на Сурвивин. Ширина ответов IFNγ, индуцированных Сурвивином 1 и Сурвивином 1T3. На фиг. 11A: Пулы пептидов Сурвивина 1 после обработки 50 мкг pGX1428, pGX1429 или pGX0001. На фиг. 11B: Пулы пептидов Сурвивина T3 после обработки 50 мкг pGX1429 или pGX0001. Сравнение последовательностей pGX1428 и pGX1429 с положением пулов матриц, обозначенных пунктирными линиями. На фиг. 11C: Сравнение последовательностей pGX1428 и pGX1429. Аминокислоты, обозначенные красным текстом, указывают на эпитопы, идентифицированные с помощью матричного картирования. Подчеркнутый текст представляет части последовательности, которые добавляются к синтетическому консенсусному антигену Сурвивин: N-конец указывает на сайт расщепления фуринами IgELS и RGRKRRS. На фиг. 11D: Дизайн матрицы Сурвивина 1 и Сурвивина Т3. Пептиды, которые вызвали ответ, обозначены пунктирными линиями.
[0051] На фиг. 12 показаны Сурвивин-специфичные IFNγ SFU/106 PBMC от отдельных приматов, не являющихся людьми, иммунизированных с использованием варианта воплощения изобретения, содержащего синтетический консенсус Сурвивин 1T3.
[0052] На фиг. 13 показаны Сурвивин-специфичные IFNγ SFU/106 PBMC от отдельных приматов, не являющихся людьми, иммунизированных с использованием варианта воплощения изобретения, содержащего синтетический консенсус Сурвивин 1T3 с низкой дозой IL-12 (0,04 мг).
[0053] На фиг. 14 показаны Сурвивин-специфичные IFNγ SFU/106 PBMC от отдельных приматов, не являющихся людьми, иммунизированных с использованием варианта воплощения изобретения, содержащего синтетический консенсус Сурвивин 1T3 с высокой дозой IL-12 (0,20 мг).
[0054] На фиг. 15A-15C показаны результаты отдельных исследований на животных NHP, а также сравнение между иммунизацией синтетической консенсусной конструкцией Сурвивин 1 и синтетической консенсусной конструкцией Сурвивин 1T3. На фиг. 15A показаны результаты для животных группы 1; На фиг.15В показаны результаты для животных группы 2; и на фиг. 15C показаны результаты для животных группы 3.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0055] Настоящее изобретение относится к вакцинам, содержащим синтетический консенсусный антиген Сурвивин. Сурвивин экспрессируется во многих опухолях. Соответственно, вакцина обеспечивает лечение рака или раковых опухолей, экспрессирующих Сурвивин.
[0056] Синтетический консенсусный антиген Сурвивин может представлять собой консенсусный антиген Сурвивин, полученный из последовательностей Сурвивина из разных видов или из разных изоформ в пределах вида, и, таким образом, синтетический консенсусный антиген Сурвивин не является нативным. Консенсусный антиген Сурвивин может быть дополнительно модифицирован путем введения одной или более мутаций в последовательность консенсуса для создания последовательности синтетического консенсуса. Мутации могут разрушать или модифицировать конкретные функциональные домены нативной последовательности Сурвивина, тем самым нарушая или усиливая структуру или функцию функциональных доменов. В некоторых вариантах воплощения дополнительные последовательности добавляют к последовательности синтетического консенсусного антигена Сурвивина для введения новых структур или функций. Например, последовательность синтетического консенсусного антигена Сурвивина может иметь сайт расщепления фурином. Последовательность синтетического консенсусного антигена Сурвивина может включать дополнительный сигнал локализации для усиления внеклеточного транспорта конечного белкового продукта. Дополнительный сигнал локализации может представлять собой IgELS или другую последовательность клеточного транспорта.
[0057] Синтетический консенсусный антиген Сурвивин может индуцировать ответы антиген-специфических Т-клеток и/или высокий титр антител, тем самым индуцируя или вызывая иммунный ответ, который направлен или реагирует на рак или опухоль, экспрессирующую антиген. В некоторых вариантах воплощения индуцированный или вызванный иммунный ответ может представлять собой клеточный, гуморальный или как клеточный, так и гуморальный иммунные ответы. В некоторых вариантах воплощения индуцированный или вызванный клеточный иммунный ответ может включать индукцию или секрецию интерферона-гамма (IFN-γ) и/или фактора некроза опухоли альфа (TNF-α) и/или интерлейкина 2 (IL-2). В других вариантах воплощения индуцированный или вызванный иммунный ответ может снижать или ингибировать один или более факторов иммуносупрессии, которые способствуют росту опухоли или рака, экспрессирующего антиген, например, но не ограничиваясь ими, факторы, которые подавляют презентацию МНС, факторы, которые стимулируют антиген-специфические регуляторные Т-клетки (Treg), PD-L1, FasL, цитокины, такие как IL-10 и TFG-β, опухоль-ассоциированные макрофаги, ассоциированные с опухолью фибробласты, растворимые факторы, продуцируемые иммуносупрессорными клетками, CTLA-4, PD-1, MDSC, MCP-1 и молекулу иммунной контрольной точки.
[0058] Вакцина, согласно изобретению, может обеспечить любую комбинацию конкретных раковых антигенов для конкретной профилактики или лечения рака у субъекта, который нуждается в лечении.
[0059] Одним из способов конструирования нуклеиновой кислоты и ее кодируемой аминокислотной последовательности рекомбинантного ракового антигена является введение мутаций, которые изменяют конкретные аминокислоты в общей аминокислотной последовательности нативного ракового антигена. Введение мутаций не настолько изменяет раковый антиген, что его нельзя универсально применять у субъекта-млекопитающего и предпочтительно субъекта-человека или собаки, но изменяет его настолько, что полученная аминокислотная последовательность нарушает толерантность или считается чужеродным антигеном в организме для того, чтобы генерировать иммунный ответ. Другим способом может быть создание консенсусного рекомбинантного ракового антигена, который имеет идентичность аминокислотной последовательности по меньшей мере от 85% до 99% по сравнению с его соответствующим нативным раковым антигеном; предпочтительно по меньшей мере 90% и до 98% идентичности последовательности; более предпочтительно по меньшей мере 93% и до 98% идентичности последовательности; или даже более предпочтительно по меньшей мере 95% и до 98% идентичности последовательности. В некоторых случаях рекомбинантный раковый антиген имеет идентичность аминокислотной последовательности на 95, 96, 97, 98% или 99% по сравнению с его соответствующим нативным раковым антигеном. Нативный раковый антиген является антигеном, обычно ассоциированным с конкретным раком или раковой опухолью. В зависимости от ракового антигена консенсусная последовательность ракового антигена может встречаться у разных видов млекопитающих или внутри подтипов вида, или среди вирусных штаммов или серотипов. Некоторые раковые антигены не сильно отличаются от аминокислотной последовательности дикого типа ракового антигена. Некоторые раковые антигены имеют последовательности нуклеиновых кислот/аминокислот, которые настолько различаются между видами, что консенсусная последовательность не может быть получена. В этих случаях рекомбинантный раковый антиген, который будет нарушать толерантность и генерировать иммунный ответ, создается таким образом, что имеет идентичность аминокислотной последовательности по меньшей мере от 85% до 99% по сравнению с его соответствующим нативным раковым антигеном; предпочтительно по меньшей мере 90% и до 98% идентичности последовательности; более предпочтительно по меньшей мере 93% и до 98% идентичности последовательности; или даже более предпочтительно по меньшей мере 95% и до 98% идентичности последовательности. В некоторых случаях рекомбинантный раковый антиген имеет идентичность аминокислотной последовательности на 95, 96, 97, 98% или 99% по сравнению с его соответствующим нативным раковым антигеном. Вышеупомянутые подходы могут быть объединены так, что конечный рекомбинантный раковый антиген имеет процентное сходство с аминокислотной последовательностью нативного ракового антигена, как обсуждалось выше.
[0060] Вакцина может быть дополнительно комбинирована с антителами к ингибиторам контрольных точек, таким как PD-1 и PDL-1, для усиления стимуляции как клеточного, так и гуморального иммунного ответа. Использование антител против PD-1 или против PDL-1 не позволяет PD-1 или PDL-1 подавлять ответы Т-клеток и/или В-клеток. В целом, разработка раковых антигенов, распознаваемых иммунной системой, помогает преодолеть другие формы иммуносупрессии опухолевыми клетками, и эти вакцины можно использовать в сочетании с терапией подавления или ингибирования (например, терапия анти-PD-1 и анти-PDL-1 антителами) для дальнейшего усиления Т-клеточных и/или В-клеточных ответов.
[0061] Вакцина может увеличить выживаемость без опухолей на 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44% и 45%. Вакцина может уменьшить массу опухоли на 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59% и 60% после иммунизации. Вакцина может предотвращать и блокировать повышение белка 1 хемоаттрактанта моноцитов (МСР-1), цитокина, секретируемого клетками-супрессорами миелоидного происхождения. Вакцина может увеличить выживаемость без опухолей на 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59% и 60%.
[0062] Вакцина может усиливать клеточный иммунный ответ у субъекта, которому вводят вакцину, от приблизительно в 50 раз до приблизительно в 6000 раз, от приблизительно в 50 раз до приблизительно в 5500 раз, от приблизительно в 50 раз до приблизительно в 5000 раз, от приблизительно в 50 раз до приблизительно в 4500 раз, от приблизительно в 100 до приблизительно в 6000 раз, от приблизительно в 150 раз до приблизительно в 6000 раз, от приблизительно в 200 раз до приблизительно в 6000 раз, от приблизительно в 250 раз до приблизительно в 6000 раз или от приблизительно в 300 раз до приблизительно в 6000 раз по сравнению с клеточным иммунным ответом у субъекта, которому не вводили вакцину. В некоторых вариантах воплощения вакцина может усиливать клеточный иммунный ответ у субъекта, которому вводят вакцину, приблизительно в 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1100, 1200, 1300, 1400, 1500, 1600, 1700, 1800, 1900, 2000, 2100, 2200, 2300, 2400, 2500, 2600, 2700, 2800, 2900, 3000, 3100, 3200, 3300, 3400, 3500, 3600, 3700, 3800, 3900, 4000, 4100, 4200, 4300, 4400, 4500, 4600, 4700, 4800, 4900, 5000, 5100, 5200, 5300, 5400, 5500, 5600, 5700, 5800, 5900 раз или в 6000 раз по сравнению с клеточным иммунным ответом у субъекта, которому не вводили вакцину.
[0063] Вакцина может повышать уровни интерферона гамма (IFN-γ) у субъекта, которому вводят вакцину, от приблизительно в 50 раз до приблизительно в 6000 раз, от приблизительно в 50 раз до приблизительно в 5500 раз, от приблизительно в 50 раз до приблизительно в 5000 раз, от приблизительно в 50 раз до приблизительно в 4500 раз, от приблизительно в 100 до приблизительно в 6000 раз, от приблизительно в 150 раз до приблизительно в 6000 раз, от приблизительно в 200 раз до приблизительно в 6000 раз, от приблизительно в 250 раз до приблизительно в 6000 раз или от приблизительно в 300 раз приблизительно в 6000 раз по сравнению с уровнями IFN-γ у субъекта, которому не вводили вакцину. В некоторых вариантах воплощения вакцина может повышать уровни IFN-γ у субъекта, которому вводят вакцину, приблизительно в 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1100, 1200, 1300, 1400, 1500, 1600, 1700, 1800, 1900, 2000, 2100, 2200, 2300, 2400, 2500, 2600, 2700, 2800, 2900, 3000, 3100, 3200, 3300, 3400, 3500, 3600, 3700, 3800, 3900, 4000, 4100, 4200, 4300, 4400, 4500, 4600, 4700, 4800, 4900, 5000, 5100, 5200, 5300, 5400, 5500, 5600, 5700, 5800, 5900 раз или в 6000 раз по сравнению с уровнями IFN-γ у субъекта, которому не вводили вакцину.
[0064] Как более подробно описано ниже, вакцина может дополнительно содержать один или более ингибиторов одной или более молекул иммунной контрольной точки (то есть ингибитора иммунной контрольной точки). Молекулы иммунной контрольной точки описаны ниже более подробно. Ингибитором иммунной контрольной точки является любая нуклеиновая кислота или белок, которые предотвращают подавление любого компонента в иммунной системе, такого как презентация класса MHC, презентация и/или дифференцировка Т-клеток, презентация и/или дифференцировка В-клеток, любой цитокин, хемокин или передача сигналов пролиферации и/или дифференцировки иммунных клеток. Как также более подробно описано ниже, вакцина может быть дополнительно комбинирована с антителами к ингибиторам контрольных точек, таким как PD-1 и PDL-1, для усиления стимуляции как клеточного, так и гуморального иммунного ответа. Использование антител против PD-1 или против PDL-1 не позволяет PD-1 или PDL-1 подавлять ответы Т-клеток и/или В-клеток.
Определения
[0065] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют такое же значение, как общедоступное обычному специалисту в данной области техники. В случае конфликта настоящий документ, включая определения, будет иметь преимущественную силу. Предпочтительные способы и материалы описаны ниже, хотя способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, могут быть использованы на практике или при тестировании настоящего изобретения. Все публикации, заявки на патенты, патенты и другие ссылки, упомянутые в данном документе, включены в качестве ссылки во всей их полноте. Материалы, способы и примеры, раскрытые в данном документе, являются только иллюстративными и не предназначены для ограничения. Используемая в данном документе терминология предназначена только для описания конкретных вариантов воплощения и не предназначена для ограничения.
[0066] Термины «состоят(состоит)», «включают(включает)», «имеющий», «имеет», «может», «содержат(содержит)» и их варианты, в контексте данного документа, предполагаются неограничивающими переводимыми фразами, терминами или словами, которые не исключают возможности дополнительных действий или структур. Формы существительного единственного числа и «и» включают формы множественного числа, если контекст четко не определяет иное. В настоящем раскрытии также рассматриваются другие варианты осуществления, «содержащие», «состоящие из» и «состоящие по существу из», представленные в данном документе варианты воплощения или элементы, независимо от того, изложены они явно или нет.
[0067] Для перечисления числовых диапазонов в настоящем документе каждое промежуточное значение, имеющее ту же степень точности, что и минимум и максимум приведенного диапазона, четко предусмотрено. Например, для диапазона 6-9 числа 7 и 8 предусмотрены в дополнение к 6 и 9, а для диапазона 6,0-7,0 - числа 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9 и 7,0 предусмотрены явно.
[0068] Термин «адъювант», в контексте данного документа, означает любую молекулу, добавленную к вакцинам, описанным в настоящем документе, для усиления иммуногенности антигена.
[0069] «Антитело», в контексте данного документа, означает антитело класса IgG, IgM, IgA, IgD или IgE или его фрагмент или производное, включая Fab, F(ab')2, Fd и одноцепочечные антитела, диатела, биспецифичные антитела, бифункциональные антитела и их производные. Антитело может представлять собой антитело, выделенное из образца сыворотки млекопитающего, поликлонального антитела, аффинно-очищенного антитела или любой их смеси, которое проявляет достаточную специфичность связывания с желаемым эпитопом или последовательностью, полученной из него.
[0070] «Антиген» относится к белкам, имеющим аминокислотные последовательности синтетического консенсусного антигена Сурвивин, включая: (a) аминокислоты 19-159 SEQ ID NO:2; (б) аминокислоты 19-210 SEQ ID NO:4; (в) аминокислоты 19-232 SEQ ID NO:8; (г) фрагменты, содержащие по меньшей мере 90% аминокислот 19-159 SEQ ID NO:2; (д) фрагменты, содержащие по меньшей мере 90% аминокислот 19-210 SEQ ID NO:4; (е) фрагменты, содержащие по меньшей мере 90% аминокислот 19-232 SEQ ID NO:8; (ж) белки, которые по меньшей мере на 95% идентичны аминокислотам 19-159 SEQ ID NO:2; (з) белки, которые по меньшей мере на 95% идентичны аминокислотам 19-210 SEQ ID NO:4; (и) белки, которые по меньшей мере на 95% идентичны аминокислотам 19-232 SEQ ID NO:8; (к) фрагменты, содержащие по меньшей мере 90% белка, который по меньшей мере на 95% идентичен аминокислотам 19-159 SEQ ID NO:2; (л) фрагменты, содержащие по меньшей мере 90% белка, который по меньшей мере на 95% идентичен аминокислотам 19-210 SEQ ID NO:4; и (м) фрагменты, содержащие по меньшей мере 90% белка, который по меньшей мере на 95% идентичен аминокислотам 19-232 SEQ ID NO:8. «Антиген» также относится к белкам, имеющим аминокислотные последовательности синтетического консенсусного антигена Сурвивин, включая: (a) SEQ ID NO:2; (б) SEQ ID NO:4; (в) SEQ ID NO:8; (г) фрагменты, содержащие по меньшей мере 90% всей длины SEQ ID NO:2; (д) фрагменты, содержащие по меньшей мере 90% всей длины SEQ ID NO:4; (е) фрагменты, содержащие по меньшей мере 90% всей длины SEQ ID NO:8; (ж) белки, которые по меньшей мере на 95% идентичны SEQ ID NO:2; (з) белки, которые по меньшей мере на 95% идентичны SEQ ID NO:4; (и) белки, которые по меньшей мере на 95% идентичны SEQ ID NO:8; (к) фрагменты, содержащие по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:2; (л) фрагменты, содержащие по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:4; и (м) фрагменты, содержащие по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO:8. Антигены могут необязательно включать сигнальные пептиды, такие как пептиды из других белков.
[0071] Термины «кодирующая последовательность» или «кодирующая нуклеиновая кислота», в контексте данного документа, означают нуклеиновые кислоты (молекулы РНК или ДНК), которые содержат нуклеотидную последовательность, кодирующую белок. Кодирующая последовательность может дополнительно включать сигналы инициации и терминации, функционально связанные с регуляторными элементами, включая промотор и полиаденилирования, способные управлять экспрессией в клетках субъекта или млекопитающего, которым вводят нуклеиновую кислоту.
[0072] Термины «комплемент» или «комплементарность», используемые в данном документе в отношении нуклеиновой кислоты, может означать спаривание оснований Уотсона-Крика (например, A-T/U и C-G) или Хугстина между нуклеотидами или аналогами нуклеотидов молекул нуклеиновой кислоты.
[0073] Термины «консенсус» или «консенсусная последовательность», в контексте данного документа, означают полипептидную последовательность, основанную на анализе выравнивания множества последовательностей для одного и того же гена из разных организмов или из разных изоформ в организме. Могут быть получены последовательности нуклеиновых кислот, которые кодируют консенсусную полипептидную последовательность.
[0074] Термин «постоянный ток», в контексте данного документа, означает ток, который воспринимается или испытывается тканью или клетками, определяющими указанную ткань, во время воздействия электрического импульса, доставляемого в ту же ткань. Электрический импульс подается от устройств электропорации, описанных в данном документе. Плотность тока остается постоянной в указанной ткани в течение всего времени воздействия электрического импульса, поскольку устройство электропорации, предложенное в настоящем документе, имеет элемент обратной связи, предпочтительно обладающий мгновенной обратной связью. Элемент обратной связи позволяет измерять сопротивление ткани (или клеток) на протяжении всего времени воздействия импульса и заставлять устройство электропорации изменять выходную электрическую мощность (например, увеличивать напряжение) таким образом, чтобы плотность тока в одной и той же ткани оставалась постоянной в течение всего времени воздействия электрического импульса (порядка микросекунд) и от импульса к импульсу. В некоторых вариантах воплощения элемент обратной связи содержит контроллер.
[0075] Термины «обратная связь по току» или «обратная связь», в контексте данного документа, могут использоваться взаимозаменяемо и могут означать активную реакцию предоставленных устройств электропорации, которая включает измерение тока в ткани между электродами и соответствующее изменение выходной энергии, передаваемой устройством EP, для поддержания плотности тока на постоянном уровне. Этот постоянный уровень задается пользователем перед началом инициации импульсной последовательности или электротерапии. Обратная связь может быть обеспечена компонентом электропорации, например, контроллером устройства электропорации, поскольку электрическая цепь в нем способна непрерывно контролировать ток в ткани между электродами и сравнивать этот контролируемый ток (или ток в ткани) с заданным током и непрерывно производить регулировку выходной мощности для поддержания контролируемого тока на заданных уровнях. Цикл обратной связи может быть мгновенным, поскольку он является аналоговой замкнутой обратной связью.
[0076] Термин «децентрализованный ток», в контексте данного документа, может означать структуру электрических токов, подаваемых из различных наборов игольчатых электродов устройств электропорации, описанных в данном документе, при этом схемы минимизируют или предпочтительно устраняют возникновение теплового напряжения, связанного с электропорацией, в любой области ткани, являющейся электропорированной.
[0077] Термины «электропорация», «электропермеабилизация» или «электрокинетическое усиление» («EP»), используемые в данном документе взаимозаменяемо, означают воздействие импульса трансмембранного электрического поля для индукции микроскопических путей (пор) в биомембране; их присутствие позволяет биомолекулам, таким как плазмиды, олигонуклеотиды, миРНК, лекарственные препараты, ионы и вода, проходить с одной стороны клеточной мембраны на другую.
[0078] В контексте данного документа, термин «фрагмент», в отношении последовательностей нуклеиновой кислоты, означает последовательность нуклеиновой кислоты или ее часть, которая кодирует полипептид, способный вызывать иммунный ответ у млекопитающего, который перекрестно реагирует с антигеном, раскрытым в данном документе. Фрагменты могут быть фрагментами ДНК, выбранными по меньшей мере из одной из различных нуклеотидных последовательностей, которые кодируют фрагменты белка, изложенные ниже. Фрагменты могут содержать по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% одной или более последовательностей нуклеиновых кислот, указанных ниже, за исключением добавления гетерологичного сигнального пептида. Фрагмент может содержать по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или, по меньшей мере 99% одной или более последовательностей нуклеиновых кислот, указанных ниже, и дополнительно необязательно включать последовательность, кодирующую гетерологичный сигнальный пептид, который не нужно включать при расчете процента идентичности. Фрагменты могут дополнительно содержать кодирующие последовательности для сигнального пептида, такого как сигнальный пептид иммуноглобулина, например сигнальный пептид IgE или IgG. Кодирующая последовательность, кодирующая N-концевой метионин и/или сигнальный пептид, может быть связана с фрагментом кодирующей последовательности.
[0079] В некоторых вариантах воплощения фрагменты могут содержать по меньшей мере 20 нуклеотидов или более, по меньшей мере 30 нуклеотидов или более, по меньшей мере 40 нуклеотидов или более, по меньшей мере 50 нуклеотидов или более, по меньшей мере 60 нуклеотидов или более, по меньшей мере 70 нуклеотидов или более, по меньшей мере 80 нуклеотидов или более, по меньшей мере 90 нуклеотидов или более, по меньшей мере 100 нуклеотидов или более, по меньшей мере 150 нуклеотидов или более, по меньшей мере 200 нуклеотидов или более, по меньшей мере 250 нуклеотидов или более, по меньшей мере 300 нуклеотидов или более, по меньшей мере 350 нуклеотидов или более, по меньшей мере 400 нуклеотидов или более, по меньшей мере 450 нуклеотидов или более, по меньшей мере 500 нуклеотидов или более, по меньшей мере 550 нуклеотидов или более, по меньшей мере 600 нуклеотидов или более, по меньшей мере 650 нуклеотидов или более по меньшей мере одной из последовательностей нуклеиновых кислот, указанных ниже.
[0080] Термины «фрагмент» или «иммуногенный фрагмент», в отношении полипептидных последовательностей, означают полипептид, способный вызывать иммунный ответ у млекопитающего, который перекрестно реагирует с антигеном, раскрытым в данном документе. Фрагменты могут быть полипептидными фрагментами, выбранными из по меньшей мере одной из различных аминокислотных последовательностей, приведенных ниже. Фрагменты консенсусных белков могут составлять по меньшей мере 10%, по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% консенсусного белка, исключая добавление любого гетерологичного сигнального пептида. Фрагмент может содержать по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% одной или более аминокислотных последовательностей, указанных ниже, и дополнительно необязательно включать гетерологичный сигнальный пептид, который не нужно включать при расчете процента идентичности. Фрагменты могут дополнительно содержать сигнальный пептид, такой как сигнальный пептид иммуноглобулина, например сигнальный пептид IgE или IgG.
[0081] В некоторых вариантах воплощения фрагменты консенсусных белков могут содержать по меньшей мере 20 аминокислот или более, по меньшей мере 30 аминокислот или более, по меньшей мере 40 аминокислот или более, по меньшей мере 50 аминокислот или более, по меньшей мере 60 аминокислот или более, по меньшей мере 70 аминокислот или более, по меньшей мере 80 аминокислот или более, по меньшей мере 90 аминокислот или более, по меньшей мере 100 аминокислот или более, по меньшей мере 110 аминокислот или более, по меньшей мере 120 аминокислот или более, по меньшей мере 130 аминокислот или более, по меньшей мере 140 аминокислот или более, по меньшей мере 150 аминокислот или более, по меньшей мере 160 аминокислот или более, по меньшей мере 170 аминокислот или более, по меньшей мере 180 аминокислот или более, по меньшей мере 200 аминокислот или более, по меньшей мере 220 аминокислот или более последовательности белка, раскрытого в данном документе.
[0082] В контексте данного документа, термин «генетическая конструкция» относится к молекулам ДНК или РНК, которые содержат нуклеотидную последовательность, кодирующую белок. Кодирующая последовательность включает сигналы инициации и терминации, функционально связанные с регуляторными элементами, включая промотор и сигнал полиаденилирования, способные управлять экспрессией в клетках субъекта, которому вводят нуклеиновую кислоту. В контексте данного документа, термин «экспрессируемая форма» относится к генной конструкции, которая содержит необходимые регуляторные элементы, функционально связанные с кодирующей последовательностью, которая кодирует белок, таким образом, что при наличии в клетке субъекта будет экспрессироваться кодирующая последовательность.
[0083] В контексте данного документа, термин «гомология» относится к степени комплементарности. Может быть частичная гомология или полная гомология (то есть идентичность). Частично комплементарная последовательность, которая по меньшей мере частично ингибирует гибридизацию полностью комплементарной последовательности с нуклеиновой кислотой-мишенью, называется функциональным термином «по существу гомологичная». При использовании в отношении двухцепочечной последовательности нуклеиновой кислоты, такой как кДНК или геномный клон, термин «по существу гомологичный», в контексте данного документа, относится к зонду, который может гибридизоваться с цепью двухцепочечной последовательности нуклеиновой кислоты в условиях низкой жесткости. При использовании в отношении последовательности одноцепочечной нуклеиновой кислоты термин «по существу гомологичный», в контексте данного документа, относится к зонду, который может гибридизоваться (т.е. является комплементом) с одноцепочечной матрицей последовательности нуклеиновой кислоты в условиях низкой жесткости.
[0084] Термины «идентичный» или «идентичность», в контексте данного документа, относительно двух или более последовательностей нуклеиновых кислот или полипептидов, означает, что последовательности имеют определенный процент остатков, которые являются одинаковыми в указанной области. Процент может быть рассчитан путем оптимального выравнивания двух последовательностей, сравнения двух последовательностей в указанной области, определения количества позиций, в которых одинаковый остаток встречается в обеих последовательностях, для получения количества совпадающих позиций, деления количества совпавших позиций на общее количество позиций в указанной области и умножение результата на 100, чтобы получить процент идентичности последовательности. В тех случаях, когда две последовательности имеют разную длину или выравнивание приводит к одному или более ступенчатым концам и указанная область сравнения включает только одну последовательность, остатки одной последовательности включаются в знаменатель, но не в числитель вычисления. При сравнении ДНК и РНК тимин (T) и урацил (U) можно считать эквивалентными. Идентификация может быть выполнена вручную или с помощью компьютерного алгоритма последовательностей, такого как BLAST или BLAST 2.0.
[0085] Термин «импеданс», в контексте данного документа, может использоваться при рассмотрении в деталях механизма обратной связи и может быть преобразован в текущее значение в соответствии с законом Ома, что позволяет проводить сравнение с заданным током.
[0086] Термин «иммунный ответ», в контексте данного документа, означает активацию иммунной системы хозяина, например, млекопитающего, в ответ на введение антигена. Иммунный ответ может быть в форме клеточного или гуморального ответа, или обоих.
[0087] Термины «нуклеиновая кислота», или «олигонуклеотид», или «полинуклеотид», в контексте данного документа, означают по меньшей мере два нуклеотида, ковалентно связанных друг с другом. Описание одной цепи также определяет последовательность дополнительной цепи. Таким образом, нуклеиновая кислота также охватывает комплементарную цепь описанной одной цепи. Многие варианты нуклеиновой кислоты могут быть использованы для той же цели, что и данная нуклеиновая кислота. Таким образом, нуклеиновая кислота также включает по существу идентичные нуклеиновые кислоты и их комплементы. Одна цепь обеспечивает зонд, который может гибридизоваться с последовательностью-мишенью в жестких условиях гибридизации. Таким образом, нуклеиновая кислота также включает зонд, который гибридизуется в жестких условиях гибридизации.
[0088] Нуклеиновые кислоты могут быть одноцепочечными или двухцепочечными или могут содержать части как двухцепочечной, так и одноцепочечной последовательности. Нуклеиновая кислота может представлять собой ДНК, как геномную, так и кДНК, РНК или гибридную, где нуклеиновая кислота может содержать комбинации дезоксирибо- и рибонуклеотидов и комбинации оснований, включая урацил, аденин, тимин, цитозин, гуанин, инозин, ксантин, гипоксантин, изоцитозин и изогуанин. Нуклеиновые кислоты могут быть получены способами химического синтеза или рекомбинантными способами.
[0089] «Функционально связанный», в контексте данного документа, означает, что экспрессия гена находится под контролем промотора, с которым он пространственно связан. Промотор может быть расположен на 5’ (слева) или 3' (справа) от гена под его контролем. Расстояние между промотором и геном может быть приблизительно таким же, как расстояние между этим промотором и геном, который он контролирует, в гене, из которого происходит промотор. Как известно в данной области техники, изменение этого расстояния может быть осуществлено без потери функции промотора.
[0090] В контексте данного документа, термины «пептид», «белок» или «полипептид» могут означать связанную последовательность аминокислот и могут быть природным, синтетическим или быть модификацией или комбинацией природного и синтетического.
[0091] Термин «промотор», в контексте данного документа, означает синтетическую молекулу или молекулу природного происхождения, которая способна предоставлять, активировать или усиливать экспрессию нуклеиновой кислоты в клетке. Промотор может содержать одну или более специфических последовательностей, регулирующих транскрипцию, для дополнительного усиления экспрессии и/или изменения пространственной экспрессии и/или временной экспрессии нуклеиновой кислоты в клетке. Промотор также может содержать дистальные энхансерные или репрессорные элементы, которые могут находиться на расстоянии до нескольких тысяч пар оснований от стартового сайта транскрипции. Промотор может быть получен из источников, включая вирусные, бактериальные, грибковые, растительные, насекомых и животных. Промотор может регулировать экспрессию генного компонента конститутивно или дифференциально по отношению к клетке, ткани или органу, в котором происходит экспрессия, или относительно стадии развития, на которой происходит экспрессия, или в ответ на внешние раздражители, такие как физиологические стрессы, патогены, ионы металлов или возбуждающие агенты. Типичные примеры промоторов включают промотор бактериофага Т7, промотор бактериофага Т3, промотор SP6, промотор lac оператора, промотор tac, поздний промотор SV40, ранний промотор SV40, промотор RSV-LTR, промотор CMV IE, ранний промотор SV40 или поздний промотор SV40 и промотор CMV IE.
[0092] Термины «сигнальный пептид» и «лидерная последовательность» используются в данном документе взаимозаменяемо и относятся к аминокислотной последовательности, которая может быть связана на аминоконце белка, указанного в данном документе. Сигнальные пептиды/лидерные последовательности обычно направляют локализацию белка. Используемые в данном документе сигнальные пептиды/лидерные последовательности предпочтительно облегчают секрецию белка из клетки, в которой он продуцируется. Сигнальные пептиды/лидерные последовательности часто отщепляются от остатка белка, часто называемого зрелым белком, при секреции из клетки. Сигнальные пептиды/лидерные последовательности связаны на амино-конце (то есть на N-конце) белка.
[0093] «Жесткие условия гибридизации», в контексте данного документа, означают условия, при которых первая последовательность нуклеиновой кислоты (например, зонд) будет гибридизоваться со второй последовательностью нуклеиновой кислоты (например, мишенью), таких как в сложной смеси нуклеиновых кислот. Жесткие условия зависят от последовательности и будут разными в разных обстоятельствах. Жесткие условия могут быть выбраны так, чтобы они были приблизительно на 5-10°C ниже, чем температура плавления (Tm) для конкретной последовательности при pH определенной ионной силы. Tm может быть температурой (при определенной ионной силе, pH и нуклеиновой концентрации), при которой 50% зондов, комплементарных мишени, гибридизуются с последовательностью-мишенью в равновесии (так как последовательности-мишени присутствуют в избытке, при Tm, 50% зондов заняты в равновесии). Жесткие условия могут быть такими, в которых концентрация соли составляет менее чем приблизительно 1,0 М иона натрия, например, концентрация иона натрия приблизительно 0,01-1,0 М (или других солей) при рН 7,0-8,3, а температура составляет по меньшей мере приблизительно 30°С для коротких зондов (например, приблизительно 10-50 нуклеотидов) и по меньшей мере приблизительно 60°С для длинных зондов (например, больше, чем приблизительно 50 нуклеотидов). Жесткие условия также могут быть достигнуты с добавлением дестабилизирующих агентов, таких как формамид. Для селективной или специфической гибридизации положительный сигнал может по меньшей мере в 2-10 раз превышать фоновую гибридизацию. Примерные строгие условия гибридизации включают следующее: 50% формамид, 5x SSC и 1% SDS, инкубирование при 42°C или 5x SSC, 1% SDS, инкубирование при 65°C, с промывкой в 0,2x SSC и 0,1% SDS при 65°C.
[0094] Термин «субъект», в контексте данного документа, может означать млекопитающее, которому необходима или требуется иммунизация, представленными в данном документе вакцинами. Млекопитающим может быть человек, шимпанзе, собака, кошка, лошадь, корова, мышь или крыса.
[0095] Термин «практически комплементарный», в контексте данного документа, означает, что первая последовательность по меньшей мере на 60, 65, 70, 75, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98% или 99% идентичны комплементу второй последовательности в области 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 180, 270, 360, 450, 540 или более нуклеотидов или аминокислот, или что две последовательности гибридизуются в жестких условиях гибридизации.
[0096] Термин «практически идентичный», в контексте данного документа, означает, что первая и вторая последовательность по меньшей мере на 60, 65, 70, 75, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98% или 99% идентичны в области 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 180, 270, 360, 450, 540 или более нуклеотидов или аминокислот, или что две последовательности гибридизуются в жестких условиях гибридизации.
[0097] Термины «лечить», «лечение» или «лечащий», в контексте данного документа, могут означать защиту животного от заболевания посредством средств предотвращения, супрессии, подавления или полного устранения заболевания. Профилактика заболевания включает введение вакцины по настоящему изобретению животному до начала заболевания. Супрессия заболевания включает введение вакцины по настоящему изобретению животному после индукции заболевания, но до его клинического проявления. Подавление заболевания включает введение вакцины по настоящему изобретению животному после клинического проявления заболевания.
[0098] В контексте данного документа, термин «вариант», в отношении нуклеиновой кислоты, означает (и) часть или фрагмент эталонной нуклеотидной последовательности; (ii) комплемент эталонной нуклеотидной последовательности или ее часть; (iii) нуклеиновую кислоту, которая по существу идентична эталонной нуклеиновой кислоте или ее комплементу; или (iv) нуклеиновую кислоту, которая гибридизуется в жестких условиях с эталонной нуклеиновой кислотой, ее комплементом или последовательностью, по существу идентичной ей.
[0099] В контексте данного документа, термин «вариант», в отношении пептида или полипептида, означает пептид или полипептид, который отличается по аминокислотной последовательности вставкой, делецией или консервативной заменой аминокислот, но сохраняет по меньшей мере одну биологическую активность. Вариант также может означать белок с аминокислотной последовательностью, которая по существу идентична эталонному белку с аминокислотной последовательностью, которая сохраняет по меньшей мере одну биологическую активность. Консервативная замена аминокислоты, то есть замена аминокислоты другой аминокислотой со схожими свойствами (например, гидрофильностью, степенью и распределением заряженных областей), как известно, в данной области техники обычно включает незначительные изменения. Эти незначительные изменения могут быть идентифицированы, частично, с учетом индекса гидрофобности аминокислот, как понимается в данной области техники. Kyte et al., J. Mol. Biol. 157:105-132 (1982). Индекс гидрофобности аминокислоты основан на оценке ее гидрофобности и заряда. В данной области техники известно, что аминокислоты с подобными индексами гидрофобности могут быть замещены и при этом сохранять функцию белка. В одном аспекте аминокислоты с индексами гидрофобности ± 2, являются замещенными. Гидрофильность аминокислот также может быть использована для выявления замен, которые приводят к тому, что белки сохраняют биологическую функцию. Оценка гидрофильности аминокислот в контексте пептида позволяет рассчитать наибольшую локальную среднюю гидрофильность этого пептида, что является полезным измерением, которое, как сообщалось, хорошо коррелирует с антигенностью и иммуногенностью. Патент США № 4554101, полностью включен в данный документ в качестве ссылки. Замена аминокислот, имеющих сходные значения гидрофильности, может привести к тому, что пептиды сохраняют биологическую активность, например иммуногенность, как понимается в данной области техники. Замены могут быть выполнены с аминокислотами, имеющими значения гидрофильности у друг друга в пределах ± 2. Как на индекс гидрофобности, так и на значение гидрофильности аминокислот влияет конкретная боковая цепь этой аминокислоты. В соответствии с этим наблюдением считается, что аминокислотные замены, которые совместимы с биологической функцией, зависят от относительного сходства аминокислот и, в частности, от боковых цепей этих аминокислот, что проявляется в гидрофобности, гидрофильности, заряде, размере и других свойствах.
[00100] Вариант может представлять собой последовательность нуклеиновой кислоты, которая по существу идентична по всей длине полной последовательности гена или ее фрагмента. Последовательность нуклеиновой кислоты может быть на 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99% или 100% идентична по всей длине генной последовательности или ее фрагмента. Вариант может представлять собой аминокислотную последовательность, которая по существу идентична по всей длине аминокислотной последовательности или ее фрагмента. Аминокислотная последовательность может быть на 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99% или 100% идентична по всей длине аминокислотной последовательности или ее фрагмента.
[00101] Термин «вектор», в контексте данного документа, означает последовательность нуклеиновой кислоты, содержащую источник репликации. Вектор может представлять собой вирусный вектор, бактериофаг, бактериальную искусственную хромосому или дрожжевую искусственную хромосому. Вектор может быть вектором ДНК или РНК. Вектор может быть самореплицирующимся внехромосомным вектором и предпочтительно представляет собой ДНК-плазмиду. Вектор может содержать или включать одну или более гетерологичных последовательностей нуклеиновых кислот.
Вакцины
[00102] В данном документе представлены вакцины, содержащие синтетический консенсусный антиген Сурвивин, согласно настоящему описанию, молекулу нуклеиновой кислоты, кодирующую антиген, молекулу нуклеиновой кислоты, кодирующую фрагмент антигена, молекулу нуклеиновой кислоты, кодирующую вариант антигена или их комбинации. Вакцины могут быть способны вызывать у субъекта иммунный ответ против антигена. Иммунный ответ может представлять собой терапевтический или профилактический иммунный ответ. Вакцины могут содержать вектор или множество векторов, как более подробно описано ниже.
[00103] В некоторых вариантах воплощения вакцина содержит молекулу нуклеиновой кислоты. В некоторых вариантах воплощения молекула нуклеиновой кислоты кодирует синтетический консенсусный антиген Сурвивин. В некоторых вариантах воплощения молекула нуклеиновой кислоты содержит последовательность нуклеиновой кислоты, которая кодирует SEQ ID NO: 3; последовательность нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% длины SEQ ID NO 3; последовательность нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен SEQ ID NO: 3; или последовательность нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO: 3. В некоторых вариантах воплощения молекула нуклеиновой кислоты содержит SEQ ID NO: 1; фрагмент, содержащий по меньшей мере 90% всей длины SEQ ID NO: 1; фрагмент, который по меньшей мере на 95% идентичен SEQ ID NO: 1; или фрагмент, содержащий по меньшей мере 90% всей длины последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична SEQ ID NO: 1.
[00104] В некоторых вариантах воплощения молекула нуклеиновой кислоты содержит последовательность нуклеиновой кислоты, которая кодирует SEQ ID NO: 4; последовательность нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% длины SEQ ID NO 4; последовательность нуклеиновой кислоты, которая кодирует белок, который по меньшей мере на 95% идентичен SEQ ID NO: 4; или последовательность нуклеиновой кислоты, которая кодирует фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO: 4. В некоторых вариантах воплощения молекула нуклеиновой кислоты содержит SEQ ID NO: 2; фрагмент, содержащий по меньшей мере 90% всей длины SEQ ID NO: 2; фрагмент, который по меньшей мере на 95% идентичен SEQ ID NO: 2; или фрагмент, содержащий по меньшей мере 90% всей длины последовательности нуклеиновой кислоты, которая по меньшей мере на 95% идентична SEQ ID NO: 2.
[00105] В некоторых вариантах воплощения вакцина содержит синтетический консенсусный антиген Сурвивин, где антиген содержит SEQ ID NO: 3; фрагмент, содержащий по меньшей мере 90% длины SEQ ID NO 3; аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 3; или фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO: 3.
[00106] В некоторых вариантах воплощения вакцина содержит синтетический консенсусный антиген Сурвивин, где антиген содержит SEQ ID NO: 4; фрагмент, содержащий по меньшей мере 90% длины SEQ ID NO 4; аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 4; или фрагмент, содержащий по меньшей мере 90% всей длины белка, который по меньшей мере на 95% идентичен SEQ ID NO: 4.
[00107] Вакцины могут быть использованы для защиты от рака, например, рака или опухоли, экспрессирующей Сурвивин. Вакцины могут быть использованы для профилактики и/или лечения опухоли, экспрессирующей Сурвивин, у субъекта, нуждающегося в этом. Вакцины могут индуцировать клеточные ответы и/или ответы антител против Сурвивин и против опухолей, экспрессирующих Сурвивин.
[00108] В одном варианте воплощения вакцины могут быть использованы для защиты, предотвращения и/или лечения, или для индукции клеточного ответа и/или ответа антител против клеток рака яичника, экспрессирующих Сурвивин, в частности клеток эпителия яичника, экспрессирующих Сурвивин, более конкретно клеток серозного рака яичника, экспрессирующих Сурвивин.
[00109] Разработка противораковой вакцины, согласно настоящему описанию, включает идентификацию ракового антигена, например, Сурвивин, который не распознается иммунной системой и является антигеном, ассоциированным с опухолью («рак/яичко», «C/T»). Идентифицированный раковый антиген изменяется от аутоантигена к чужеродному антигену для распознавания иммунной системой. Перестройка нуклеиновой кислоты и аминокислотной последовательности рекомбинантного ракового антигена от ауто- к чужеродному антигену нарушает толерантность антигена иммунной системой. Чтобы нарушить толерантность, к антигену рака могут быть применены более мер редизайна, как описано ниже.
[00110] Рекомбинантный раковый антиген вакцины не распознается как аутоантиген, тем самым нарушая толерантность. Нарушение толерантности может индуцировать ответы антиген-специфических Т-клеток и/или высокий титр антител, тем самым индуцируя или вызывая иммунный ответ, который направлен или реагирует на рак или опухоль, экспрессирующую антиген. В некоторых вариантах воплощения индуцированный или вызванный иммунный ответ может представлять собой клеточный, гуморальный или как клеточный, так и гуморальный иммунные ответы. В некоторых вариантах воплощения индуцированный или вызванный клеточный иммунный ответ может включать индукцию или секрецию интерферона-гамма (IFN-γ) и/или фактора некроза опухоли альфа (TNF-α) и/или интерлейкина 2 (IL-2). В других вариантах воплощения индуцированный или вызванный иммунный ответ может снижать или ингибировать один или более факторов иммуносупрессии, которые способствуют росту опухоли или рака, экспрессирующего антиген, например, но не ограничиваясь ими, факторы, которые подавляют презентацию МНС, факторы, которые стимулируют антиген-специфические регуляторные Т-клетки (Treg), PD-L1, FasL, цитокины, такие как IL-10 и TFG-β, опухоль-ассоциированные макрофаги, ассоциированные с опухолью фибробласты, растворимые факторы, продуцируемые иммуносупрессорными клетками, CTLA-4, PD-1, MDSC, MCP-1 и молекулу иммунной контрольной точки.
[00111] В конкретном варианте воплощения вакцина может обеспечивать клиренс или предотвращать рост опухолевых клеток путем (1) увеличения цитотоксических Т-лимфоцитов, таких как CD8+ и/или CD107a+ (CTL), для атаки и уничтожения опухолевых клеток; (2) увеличения ответов Т-хелперов; и/или (3) усиления воспалительных реакций посредством IFN-γ, IL-2 и TFN-α или предпочтительно всего вышеупомянутого.
[00112] Вакцина может быть ДНК-вакциной. ДНК-вакцины описаны в патентах США № 5593972, 5739118, 5817637, 5830876, 5962428, 5981505, 5580859, 5303055 и 5676594, которые полностью включены в данный документ посредством ссылки. ДНК-вакцина может дополнительно содержать элементы или реагенты, которые препятствуют ее интеграции в хромосому.
[00113] Вакцина может содержать РНК, кодирующую раковый антиген. РНК-вакцина может быть введена в клетку.
[00114] Вакцина может представлять собой аттенуированную живую вакцину, вакцину с использованием рекомбинантных векторов для доставки антигена, субъединичные вакцины и гликопротеиновые вакцины, например, но не ограничиваясь этим, вакцины, описанные в патентах США №№: 4510245; 4797368; 4722848; 4790987; 4920209; 5017487; 5077044; 5110587; 5112749; 5174993; 5223424; 5225336; 5240703; 5242829; 5294441; 5294548; 5310668; 5387744; 5389368; 5424065; 5451499; 5,453,364; 5462734; 5470734; 5474935; 5482713; 5591439; 5643579; 5650309; 5698202; 5955088; 6034298; 6042836; 6156319 и 6589529, каждый из которых включен в данный документ посредством ссылки.
[00115] В некоторых вариантах воплощения вакцина из нуклеиновой кислоты может дополнительно содержать кодирующую последовательность для молекулярного адъюванта, в некоторых случаях молекулярным адъювантом может быть IL-12, IL-15, IL-28, IL-31, IL-33 и/или RANTES, а в некоторых случаях молекулярный адъювант представляет собой ингибитор контрольной точки, включая против цитотоксического антигена Т-лимфоцитов 4 (CTLA-4), против рецептора запрограммированной смерти-1 (PD-1) и против гена активации лимфоцитов (LAG-3). Кодирующая последовательность для IL-12, IL-15, IL-28, IL-31, IL-33 и/или RANTES может быть включена в одну или более молекул нуклеиновой кислоты, которые содержат кодирующую последовательность для одного или более антигенов. Кодирующая последовательность для IL-12, IL-15, IL-28, IL-31, IL-33 и/или RANTES может быть включена в одну или более отдельных молекул нуклеиновой кислоты, таких как одна или более отдельных плазмид или векторов, и вводиться в комбинации с вакциной нуклеиновой кислоты.
[00116] Вакцины по настоящему изобретению могут иметь свойства, требуемые для эффективных вакцин, такие как безопасность, таким образом, что сама вакцина не вызывает заболевания или смерти; защита от болезней; индукция нейтрализующего антитела; индукция защитных Т-клеточных ответов; и обеспечение простоты введения, небольшое количество побочных эффектов, биологическую стабильность и низкую стоимость на дозу. Вакцина может достигать некоторых или всех из этих свойств путем содержания молекулы(молекул) нуклеиновой кислоты, кодирующей раковый антиген, как рассмотрено ниже.
Вакцина в комбинации с ингибитором иммунной контрольной точки
[00117] Вакцина может дополнительно содержать один или более ингибиторов одной или более молекул иммунной контрольной точки (то есть ингибитора иммунной контрольной точки). Молекулы иммунной контрольной точки описаны ниже более подробно. Ингибитором иммунной контрольной точки является любая нуклеиновая кислота или белок, которые предотвращают подавление любого компонента в иммунной системе, такого как презентация класса MHC, презентация и/или дифференцировка Т-клеток, презентация и/или дифференцировка В-клеток, любой цитокин, хемокин или передача сигналов пролиферации и/или дифференцировки иммунных клеток.
[00118] Такой ингибитор может быть последовательностью нуклеиновой кислоты, аминокислотной последовательностью, небольшой молекулой или их комбинацией. Последовательность нуклеиновой кислоты может представлять собой ДНК, РНК, кДНК, их вариант, их фрагмент или их комбинацию. Нуклеиновая кислота также может включать дополнительные последовательности, которые кодируют последовательности линкера или метки, которые связаны с ингибитором иммунной контрольной точки пептидной связью. Малая молекула может представлять собой низкомолекулярное, например, менее 800 Дальтон, органическое или неорганическое соединение, которое может служить в качестве субстрата фермента, лиганда (или его аналога), связанного с белком или нуклеиновой кислотой, или регулятора биологического процесса. Аминокислотная последовательность может быть белком, пептидом, его вариантом, его фрагментом или их комбинацией.
[00119] В некоторых вариантах воплощения ингибитор иммунной контрольной точки может представлять собой одну или более последовательностей нуклеиновых кислот, кодирующих антитело, его вариант, его фрагмент или их комбинацию. В других вариантах воплощения ингибитор иммунной контрольной точки может представлять собой антитело, его вариант, его фрагмент или их комбинацию.
Молекула иммунной контрольной точки
[00120] Молекула иммунной контрольной точки может быть последовательностью нуклеиновой кислоты, аминокислотной последовательностью, небольшой молекулой или их комбинацией. Последовательность нуклеиновой кислоты может представлять собой ДНК, РНК, кДНК, их вариант, их фрагмент или их комбинацию. Нуклеиновая кислота также может включать дополнительные последовательности, которые кодируют последовательности линкера или метки, которые связаны с ингибитором иммунной контрольной точки пептидной связью. Малая молекула может представлять собой низкомолекулярное, например, менее 800 Дальтон, органическое или неорганическое соединение, которое может служить в качестве субстрата фермента, лиганда (или его аналога), связанного с белком или нуклеиновой кислотой, или регулятора биологического процесса. Аминокислотная последовательность может быть белком, пептидом, его вариантом, его фрагментом или их комбинацией.
PD-1 и PD-L1
[00121] Молекулой иммунной контрольной точки может быть белок запрограммированной клеточной смерти 1 (PD-1), лиганд запрограммированной клеточной смерти 1 (PD-L1), его фрагмент, его вариант или их комбинация. PD-1 представляет собой белок клеточной поверхности, кодируемый геном PDCD1. PD-1 является членом суперсемейства иммуноглобулинов и экспрессируется на Т-клетках и про-В-клетках и, таким образом, способствует участию и/или дифференцировке этих клеток. В частности, PD-1 является мембранным белком типа 1 семейства регуляторов Т-клеток CD28/CTLA-4 и отрицательно регулирует сигналы рецептора Т-клеток (TCR), тем самым отрицательно регулируя иммунные ответы. PD-1 может отрицательно регулировать ответы CD8+ T-клеток и, таким образом, ингибировать, цитотоксичность опосредованную CD8, и усиливать рост опухоли.
[00122] PD-1 имеет два лиганда, PD-L1 и PD-L2, которые являются членами семейства B7. PD-L1 активируется на макрофагах и дендритных клетках (DC) в ответ на обработку LPS и GM-CSF и на T-клетках и B-клетках при передаче сигналов TCR и B-клеточных рецепторов. PD-L1 экспрессируется многими линиями опухолевых клеток, включая миеломы, мастоцитомы и меланомы.
Антитело против молекулы иммунной контрольной точки
[00123] Как описано выше, ингибитор иммунной контрольной точки может представлять собой антитело. Антитело может связываться или реагировать с антигеном (т.е. молекулой иммунной контрольной точки, описанной выше). Соответственно, антитело может считаться антителом против иммунной контрольной точки или антителом иммунной контрольной точки. Антитело может кодироваться последовательностью нуклеиновой кислоты, содержащейся в данном документе.
[00124] Антитело может включать полипептид тяжелой цепи и полипептид легкой цепи. Полипептид тяжелой цепи может включать вариабельную область тяжелой цепи (VH) и/или по меньшей мере одну константную область тяжелой цепи (CH). По меньшей мере одна константная область тяжелой цепи может включать константную область тяжелой цепи 1 (СН1), константную область тяжелой цепи 2 (СН2) и константную область тяжелой цепи 3 (СН3) и/или шарнирную область.
[00125] В некоторых вариантах воплощения полипептид тяжелой цепи может включать область VH и область CH1. В других вариантах воплощения полипептид тяжелой цепи может включать область VH, область CH1, шарнирную область, область CH2 и область CH3.
[00126] Полипептид тяжелой цепи может включать набор областей, определяющих комплементарность («CDR»). Набор CDR может содержать три гипервариабельные области области VH. Начиная с N-конца полипептида тяжелой цепи, эти CDR обозначены как «CDR1», «CDR2» и «CDR3» соответственно. CDR1, CDR2 и CDR3 полипептида тяжелой цепи могут способствовать связыванию или распознаванию антигена.
[00127] Полипептид легкой цепи может включать область вариабельной легкой цепи (VL) и/или область константной легкой цепи (CL). Полипептид легкой цепи может включать набор областей, определяющих комплементарность («CDR»). Набор CDR может содержать три гипервариабельные области области VL. Начиная с N-конца полипептида легкой цепи, эти CDR обозначены как «CDR1», «CDR2» и «CDR3» соответственно. CDR1, CDR2 и CDR3 полипептида легкой цепи могут способствовать связыванию или распознаванию антигена.
[00128] Антитело может содержать набор областей, определяющих комплементарность («CDR») тяжелой цепи и легкой цепи, и, соответственно, помещаться между набором каркасной тяжелой цепи и легкой цепи («FR»), которые обеспечивают поддержку CDR и определяют пространственную взаимосвязь CDR относительно друг друга. Набор CDR может содержать три гипервариабельных участка V-области тяжелой или легкой цепи. Начиная с N-конца тяжелой или легкой цепи, эти области обозначены как «CDR1», «CDR2» и «CDR3» соответственно. Следовательно, антигенсвязывающий сайт может включать шесть CDR, содержащих набор CDR из каждой V-области тяжелой и легкой цепи.
[00129] Антитело может представлять собой иммуноглобулин (Ig). Ig может быть, например, IgA, IgM, IgD, IgE и IgG. Иммуноглобулин может включать полипептид тяжелой цепи и полипептид легкой цепи. Полипептид тяжелой цепи иммуноглобулина может включать область VH, область CH1, шарнирную область, область CH2 и область CH3. Полипептид легкой цепи иммуноглобулина может включать область VL и область CL.
[00130] Кроме того, протеолитический фермент папаин предпочтительно расщепляет молекулы IgG с образованием нескольких фрагментов, два из которых (фрагменты F(ab)) содержат ковалентный гетеродимер, который включает интактный антигенсвязывающий сайт. Фермент пепсин способен расщеплять молекулы IgG с образованием нескольких фрагментов, включая фрагмент F(ab')2, который содержит оба антигенсвязывающих сайта. Соответственно, антитело может представлять собой Fab или F(ab')2. Fab может включать полипептид тяжелой цепи и полипептид легкой цепи. Полипептид тяжелой цепи Fab может включать область VH и область CH1. Легкая цепь Fab может включать область VL и область CL.
[00131] Антитело может представлять собой поликлональное или моноклональное антитело. Антитело может представлять собой химерное антитело, одноцепочечное антитело, аффинно-зрелое антитело, человеческое антитело, гуманизированное антитело или полностью человеческое антитело. Гуманизированное антитело может представлять собой антитело от видов, не являющихся человеком, которое связывает желаемый антиген, имея одну или более областей, определяющих комплементарность (CDR), от видов, не являющихся человеком, и каркасные области от молекулы иммуноглобулина человека.
Антитело к PD-1
[00132] Антитело против иммунной контрольной точки может представлять собой антитело против PD-1 (также обозначаемое в данном документе как «антитело к PD-1»), его вариант, его фрагмент или их комбинацию. Антитело к PD-1 может представлять собой ниволумаб. Антитело против PD-1 может ингибировать активность PD-1, таким образом индуцируя, вызывая или усиливая иммунный ответ против опухоли или рака и уменьшая рост опухоли.
Антитело к PD-L1
[00133] Антитело против иммунной контрольной точки может представлять собой антитело против PD-L1 (также обозначаемое в данном документе как «антитело к PD-L1»), его вариант, его фрагмент или их комбинацию. Антитело против PD-L1 может ингибировать активность PD-L1, таким образом индуцируя, вызывая или усиливая иммунный ответ против опухоли или рака и уменьшая рост опухоли.
Анитигены
[00134] Как описано выше, вакцина может содержать антиген или нуклеиновую кислоту, кодирующую антиген. Антигеном может быть Сурвивин, его фрагмент, его вариант или комбинация его фрагмента и варианта.
[00135] Соответственно, вакцина может быть использована для лечения субъектов, страдающих от рака или опухолей, которые экспрессируют Сурвивин. В некоторых вариантах воплощения рак представляет собой рак яичника. В некоторых вариантах воплощения рак яичников представляет собой эпителиальный рак яичников. Рак яичников может быть серозным эпителиальным раком яичников. Вакцина может также использоваться для лечения субъектов с раком или опухолями, которые экспрессируют Сурвивин, для предотвращения развития таких опухолей у субъектов. Синтетический консенсусный антиген Сурвивин может отличаться от нативного гена Сурвивина и, таким образом, обеспечивать терапию или профилактику против опухоли, экспрессирующей синтетический консенсусный антиген Сурвивин. Соответственно, в данном документе предоставлены синтетические консенсусные последовательности антигена Сурвивина, которые отличаются от нативного гена Сурвивина (то есть мутированные или синтетические гены или последовательности Сурвивин).
[00136] Транскрипты нативного гена Сурвивина процессируются во множество мРНК. Конкретные изоформы мРНК Сурвивина могут быть выбраны на основании, например, их экспрессии в раковых клетках. В конкретных вариантах воплощения изоформа Сурвивина выбрана на основании ее экспрессии в раковых клетках яичников. Описанные в данном документе синтетические консенсусные последовательности антигена Сурвивина избегают альтернативного процессинга, продуцируя один полноразмерный транскрипт, что приводит к более сильной индукции эффекторных T- и B-клеточных ответов.
[00137] Предложены выделенные молекулы нуклеиновой кислоты, содержащие описанные выше гетерологичные последовательности. Предложены выделенные молекулы нуклеиновой кислоты, состоящие из описанных выше гетерологичных последовательностей. Выделенные молекулы нуклеиновой кислоты, содержащие вышеописанные гетерологичные последовательности, могут быть встроены в векторы, такие как плазмиды, вирусные векторы и другие формы молекул нуклеиновой кислоты, как описано ниже. В данном документе предложены последовательности нуклеиновых кислот, которые кодируют синтетические консенсусные антигены Сурвивин. Кодирующие последовательности, кодирующие синтетические консенсусные антигены Сурвивина, имеют последовательности, как описанные выше.
[00138] Предложены молекулы белка, содержащие описанные выше гетерологичные аминокислотные последовательности. Предложены молекулы белка, состоящие из описанных выше гетерологичных аминокислотных последовательностей. В данном документе предложены белки и полипептиды, имеющие описанные выше последовательности. Белки и полипептид могут называться синтетическими консенсусными антигенами Сурвивин и иммуногенами Сурвивин. Консенсусные синтетические антигены Сурвивин способны вызывать иммунный ответ против опухолей, экспрессирующих Сурвивин.
[00139] В одном аспекте желательно, чтобы синтетический консенсусный антиген Сурвивин обеспечивал улучшенную транскрипцию и трансляцию, включая наличие одного или более из следующего: лидерной последовательности с низким содержанием GC для увеличения транскрипции; стабильность мРНК и оптимизацию кодонов; и, насколько это возможно, устранения мотивов цис-действующей последовательности (то есть внутренних TATA-боксов).
[00140] Синтетический консенсусный антиген Сурвивин может быть последовательностью консенсусного антигена (или иммуногена), полученной из двух или более видов, изоформ или вариантов. В одном варианте воплощения консенсусная последовательность создана из изоформ Сурвивина разных видов. Консенсусная последовательность получена из последовательностей Сурвивина, собранных из GenBank или другой подобной базы данных последовательностей ДНК или белков. В некоторых вариантах воплощения консенсусный антиген может содержать часть первой изоформы, объединенную с частью второй изоформы, причем часть второй изоформы, например, является негомологичной по отношению к любой части первой изоформы. Синтетический консенсусный антиген Сурвивин может содержать консенсусную последовательность и/или модификацию(модификации) для улучшения экспрессии. Модификация может включать оптимизацию кодонов, оптимизацию РНК, добавление последовательности Kozak (например, GCC ACC) для усиления инициации трансляции и/или добавление лидерной последовательности иммуноглобулина для повышения иммуногенности синтетического консенсусного антигена Сурвивин. Синтетический консенсусный антиген Сурвивин может содержать сигнальный пептид, такой как сигнальный пептид иммуноглобулина, например, но не ограничиваясь этим, сигнальный пептид иммуноглобулина E (IgE) или иммуноглобулина G (IgG). В некоторых вариантах воплощения синтетический консенсусный антиген Сурвивина может включать мутации или делеции в последовательностях сигнала локализации, например, сигнала ядерной локализации, например, чтобы нарушить ядерную локализацию при трансляции. В некоторых вариантах воплощения консенсусный антиген Сурвивин может содержать метку гемагглютинина (HA). Консенсусный антиген Сурвивин может быть сконструирован так, чтобы вызывать более сильные и более широкие клеточные и/или гуморальные иммунные ответы, чем соответствующий не оптимизированный по кодонам антиген Сурвивин.
[00141] Консенсусная последовательность Сурвивина может быть мутирована для разрушения и/или усиления определенных структур и/или функций нативного Сурвивина для получения синтетической консенсусной последовательности антигена Сурвивина. В одном варианте воплощения мутации вводятся для устранения антиапоптотической активности Сурвивина. В конкретном варианте воплощения мутации T34A, T48A и C84A вводят в последовательность изоформы 1 консенсуса Сурвивина для отмены антиапоптотической функции. (См. Muchmore, S. W. et al. Crystal structure and mutagenic analysis of the inhibitor-of-apoptosis protein Survivin. Molecular cell 6, 173-182 (2000); O'Connor, D. S. et al. Regulation of apoptosis at cell division by p34cdc2 phosphorylation of Survivin. Proceedings of the National Academy of Sciences of the United States of America 97, 13103-13107, doi:10.1073/pnas.240390697 (2000); Barrett, R. M., Colnaghi, R. & Wheatley, S. P. Threonine 48 in the BIR domain of Survivin is critical to its mitotic and anti-apoptotic activities and can be phosphorylated by CK2 in vitro. Cell cycle (Georgetown, Tex.) 10, 538-548 (2011).)
[00142] В некоторых вариантах воплощения последовательность синтетического консенсусного антигена Сурвивина может быть сгенерирована из одной изоформы, например, доминантной изоформы Сурвивина, или последовательность консенсуса может содержать комбинацию части первой изоформы и части второй изоформы или укороченную часть второй изоформы. В одном варианте воплощения последовательность синтетического консенсуса происходит от изоформы 1 Сувивина (Сурвивин 1). В другом варианте воплощения последовательность синтетического консенсуса происходит от изоформы 3 Сувивина (Сурвивин 3). В одном варианте воплощения последовательность синтетического консенсусного антигена Сурвивина 3 представляет собой укороченную часть Сурвивина 3 (Сурвивин 3T). В одном варианте воплощения последовательность синтетического консенсуса представляет собой комбинацию Сурвивина 1 и Сурвивина T3 или Сурвивина 1T3.
[00143] В предпочтительном варианте воплощения последовательность синтетического консенсусного антигена Сурвивин имеет 95,0% или более идентичности с SEQ ID NO:1 или SEQ ID NO:3. В этом варианте воплощения последовательность нуклеиновой кислоты SEQ ID NO:1 или SEQ ID NO:3 кодирует аминокислотную последовательность SEQ ID NO:2 или SEQ ID NO:8, соответственно. В других вариантах воплощения последовательность синтетического консенсусного антигена Сурвивин имеет 95,0% или более идентичности, 95,2% или более идентичности, 95,4% или более идентичности, 95,6% или более идентичности, 95,8% или более идентичности, 96,0% или более идентичности, 96,2% или более идентичности, 96,4% или более идентичности, 96,6% или более идентичности, 96,8% или более идентичности, 97,0% или более идентичности, 97,2% или более идентичности, 97,4% или более идентичности, 97,6% или более идентичности, 97,8% или более идентичности , 98,0% или более идентичности, 98,2% или более идентичности, 98,4% или более идентичности, или 98,6% или более идентичности, 98,8% или более идентичности, 99,0% или более идентичности, 99,2% или более идентичности, 99,4% или более идентичности, 99,6% или более идентичности, 99,8% или более идентичности или 100% идентичности с SEQ ID NO:1 или SEQ ID NO:3.
Векторы
[00144] Вакцина может содержать один или более векторов, которые включают гетерологичную нуклеиновую кислоту, кодирующую синтетический консенсусный антиген Сурвивин. Один или более векторов могут быть способны экспрессировать антиген в количестве, эффективном, для того, чтобы вызвать иммунный ответ у млекопитающего. Вектор может содержать гетерологичную нуклеиновую кислоту, кодирующую антиген. Вектор может иметь последовательность нуклеиновой кислоты, содержащую источник репликации. Вектор может представлять собой плазмиду, бактериофаг, бактериальную искусственную хромосому или дрожжевую искусственную хромосому. Вектор может быть либо самовоспроизводящимся внехромосомным вектором, либо вектором, который интегрируется в геном хозяина.
[00145] Один или более векторов могут быть экспрессионной конструкцией, которая представляет собой плазмиду, которая обычно используется для введения специфического гена в целевую клетку. Как только экспрессирующий вектор оказывается внутри клетки, белок, который кодируется геном, продуцируется рибосомальными комплексами клеточно-транскрипционной и трансляционной машинерии. Плазмиду часто конструируют так, чтобы она содержала регуляторные последовательности, которые действуют как энхансерные и промоторные области и приводили к эффективной транскрипции гена, переносимого на векторе экспрессии. Векторы по настоящему изобретению экспрессируют большие количества стабильной матричной РНК и, следовательно, белков.
[00146] Векторы могут иметь сигналы экспрессии, такие как сильный промотор, сильный кодон терминации, регулирование расстояния между промотором и клонированным геном и вставка последовательности терминации транскрипции и PTIS (переносимая последовательность инициации трансляции).
[00147] Вектор может представлять собой кольцевую плазмиду или линейную нуклеиновую кислоту. Кольцевая плазмида и линейная нуклеиновая кислота способны направлять экспрессию конкретной нуклеотидной последовательности в соответствующей клетке субъекта. Вектор может иметь промотор, функционально связанный с антиген-кодирующей нуклеотидной последовательностью, который может быть функционально связан с сигналами терминации. Вектор также может содержать последовательности, необходимые для правильной трансляции нуклеотидной последовательности, а также последовательности для клонирования и субклонирования вектора и его фрагментов. Вектор, содержащий интересующую нуклеотидную последовательность, может быть химерным, что означает, что по меньшей мере один из его компонентов является гетерологичным по отношению по меньшей мере к одному из его других компонентов. Экспрессия нуклеотидной последовательности в экспрессионной кассете может находиться под контролем конститутивного промотора или индуцибельного промотора, который инициирует транскрипцию только тогда, когда на клетку-хозяина воздействует какой-то конкретный внешний стимул. В случае многоклеточного организма промотор также может быть специфичным для конкретной ткани или органа или стадии развития. В предпочтительном варианте воплощения плазмидный вектор представляет собой pGX1428, описанный в данном документе, дополнительно содержащий последовательность нуклеиновой кислоты SEQ ID NO: 1; или pGX1429, описанный в данном документе, дополнительно содержащий последовательность нуклеиновой кислоты SEQ ID NO: 3.
[00148] Вектор может представлять собой плазмиду. Плазмида может использоваться для трансфекции клеток нуклеиновой кислотой, кодирующей антиген. Трансформированные клетки-хозяева могут культивироваться и поддерживаться в условиях, когда имеет место экспрессия антигена.
[00149] Плазмида может содержать последовательность нуклеиновой кислоты, которая кодирует один или более различных антигенов, раскрытых выше, включая кодирующие последовательности, которые кодируют синтетический консенсусный антиген, способный вызывать иммунный ответ против антигена, фрагменты таких белков, варианты таких белков, фрагменты вариантов или слитые белки, которые состоят из комбинаций консенсусных белков и/или фрагментов консенсусного белка и/или вариантов консенсусного белка и/или фрагментов вариантов консенсусных белков.
[00150] Одна плазмида может содержать кодирующую последовательность для одного антигена, кодирующую последовательность для двух антигенов, кодирующую последовательность для трех антигенов или кодирующую последовательность для четырех антигенов.
[00151] В некоторых вариантах воплощения плазмида может дополнительно содержать кодирующую последовательность, которая кодирует CCR20 отдельно или как часть одной из этих плазмид. Аналогично, плазмиды могут дополнительно содержать кодирующие последовательности для IL-12, IL-15 и/или IL-28.
[00152] Плазмида может дополнительно содержать кодон инициации, который может быть слева от кодирующей последовательности, и стоп-кодон, который может быть справа от кодирующей последовательности. Кодон инициации и терминации может находиться внутри рамки с кодирующей последовательностью.
[00153] Плазмида также может содержать промотор, который функционально связан с кодирующей последовательностью. Промотор, функционально связанный с кодирующей последовательностью, может быть промотором из вируса обезьяны 40 (SV40), промотор вируса опухоли молочной железы мыши (MMTV), промотором вируса иммунодефицита человека (ВИЧ), таким как промотор длинного концевого повтора (LTR) бычьего вируса иммунодефицита (BIV), промотором вируса Молони, промотором вируса птичьего лейкоза (ALV), промотором цитомегаловируса (CMV), таким как немедленно-ранний промотор CMV, промотором вируса Эпштейна-Барра (EBV) или промотором вируса саркомы Рауса (RSV). Промотор также может быть промотором человеческого гена, такого как человеческий актин, человеческий миозин, человеческий гемоглобин, человеческий мышечный креатин или человеческий металлотионеин. Промотором также может быть тканеспецифичный промотор, такой как мышечный или кожный специфический промотор, природный или синтетический. Примеры таких промоторов описаны в публикации заявки на патент США №. 20040175727, содержание которого полностью включено в настоящий документ.
[00154] Плазмида также может содержать сигнал полиаденилирования, который может быть справа от кодирующей последовательности. Сигналом полиаденилирования может быть сигнал полиаденилирования SV40, сигнал полиаденилирования LTR, сигнал полиаденилирования бычьего гормона роста (bGH), сигнал полиаденилирования гормона роста человека (hGH) или сигнал полиаденилирования β-глобина человека. Сигнал полиаденилирования SV40 может быть сигналом полиаденилирования от плазмиды pCEP4 (Invitrogen, Сан-Диего, Калифорния).
[00155] Плазмида также может содержать энхансер слева от кодирующей последовательностью. Энхансером может быть энхансер человеческого актина, человеческого миозина, человеческого гемоглобина, человеческого мышечного креатина или вирусный энхансер, такой как энхансер CMV, FMDV, RSV или EBV. Энхансеры полинуклеотидной функции описаны в патентах США № 5593972, 5962248 и WO 94/016737, содержание каждого из которых полностью включено в качестве ссылки.
[00156] Плазмида также может содержать точку начала репликации млекопитающего для поддержания внехромосомной плазмиды и получения множества копий плазмиды в клетке. Плазмидой может быть pVAXI, pCEP4 или pREP4 от Invitrogen (Сан-Диего, Калифорния), которая может включать точку начала репликации вируса Эпштейна-Барра и кодирующую область ядерного антигена EBNA-1, что может приводить к высококопийной эписомной репликации без интеграции. Основой плазмиды может быть pA V0242. Плазмида может быть плазмидой дефектного по репликации аденовируса типа 5 (Ad5).
[00157] Плазмида также может содержать регуляторную последовательность, которая может хорошо подходить для экспрессии генов в клетке, в которую вводится плазмида. Кодирующая последовательность может содержать кодон, который может обеспечить более эффективную транскрипцию кодирующей последовательности в клетке-хозяине.
[00158] Кодирующая последовательность также может содержать лидерную последовательность Ig. Лидерная последовательность может быть 5’ кодирующей последовательностью. Консенсусные антигены, кодируемые этой последовательностью, могут содержать N-концевой лидер Ig, за которым следует консенсусный белок антигена. Лидером N-концевого Ig может быть IgE или IgG.
[00159] Плазмидой может быть pSE420 (Invitrogen, Сан-Диего, Калифорния), которая может быть использована для продуцирования белка в Escherichia coli (E.coli). Плазмида также может быть p YES2 (Invitrogen, Сан-Диего, Калифорния), которая может быть использована для продуцирования белка в штаммах дрожжей Saccharomyces cerevisiae. Плазмида также может быть полной системой экспрессии бакуловируса MAXBAC™ (Invitrogen, Сан-Диего, Калифорния), которая может быть использована для продуцирования белка в клетках насекомых. Плазмида также может быть pcDNA I или pcDNA3 (Invitrogen, Сан-Диего, Калифорния), которые могут быть использованы для продуцирования белка в клетках млекопитающих, таких как клетки яичника китайского хомячка (CHO).
[00160] Вектор может быть кольцевой плазмидой, которая может трансформировать клетку-мишень путем интеграции в клеточный геном или существовать внехромосомно (например, автономная реплицирующаяся плазмида с точкой начала репликации).
[00161] Вектором может быть pVAX, pcDNA3.0 или provax или любой другой вектор экспрессии, способный экспрессировать ДНК, кодирующую антиген и позволяющий клетке выполнять трансляцию последовательности в антиген, который распознается иммунной системой.
[00162] Также в данном документе предоставлена линейная вакцина на основе нуклеиновых кислот или кассета с линейной экспрессией («LEC»), которая способна эффективно доставляться субъекту посредством электропорации и экспрессии одного или более желаемых антигенов. LEC может представлять собой любую линейную ДНК, лишенную какого-либо фосфатного остова. ДНК может кодировать один или более антигенов. LEC может содержать промотор, интрон, стоп-кодон и/или сигнал полиаденилирования. Экспрессия антигена может контролироваться промотором. LEC может не содержать генов устойчивости к антибиотикам и/или фосфатного остова. LEC может не содержать других последовательностей нуклеиновых кислот, не связанных с желаемой экспрессией гена антигена.
[00163] LEC может быть получена из любой плазмиды, способной к линеаризации. Плазмида может быть способной экспрессировать антиген. Плазмида может быть pNP (Пуэрто-Рико/34) или pM2 (Новая Каледония/99). Плазмидой может быть WLV009 , pVAX, pcDNA3.0 или provax или любой другой вектор экспрессии, способный экспрессировать ДНК, кодирующую антиген и позволяющий клетке выполнять трансляцию последовательности в антиген, который распознается иммунной системой.
[00164] LEC может быть pcrM2. LEC может быть pcrNP. pcrNP и pcrMR могут быть получены из pNP (Пуэрто-Рико/34) и pM2 (Новая Каледония/99) соответственно.
[00165] Вектор может иметь промотор. Промотор может быть любым промотором, который способен управлять экспрессией гена и регулировать экспрессию выделенной нуклеиновой кислоты. Такой промотор представляет собой цис-действующий элемент последовательности, необходимый для транскрипции через ДНК-зависимую РНК-полимеразу, которая транскрибирует последовательность антигена, описанную в настоящем документе. Выбор промотора, используемого для прямой экспрессии гетерологичной нуклеиновой кислоты, зависит от конкретного применения. Промотор может быть расположен приблизительно на том же расстоянии от начала транскрипции в векторе, что и от начального сайта транскрипции в его естественных условиях. Тем не менее, изменение этого расстояния может быть обеспечено без потери функции промотора.
[00166] Промотор может быть функционально связан с последовательностью нуклеиновой кислоты, кодирующей антиген и сигналы, необходимые для эффективного полиаденилирования транскрипта, сайтов связывания рибосом и терминации трансляции.
[00167] Промотором может быть промотор CMV, ранний промотор SV40, поздний промотор SV40, металлотионеиновый промотор, промотор вируса опухоли молочной железы мыши, промотор вируса саркомы Рауса, промотор полиэдрина или другой промотор, показанный эффективным для экспрессии в эукариотических клетках.
[00168] Вектор может включать энхансер и интрон с функциональными донорными и акцепторными сайтами сплайсинга. Вектор может содержать область терминации транскрипции справа от структурного гена для обеспечения эффективной терминации. Область терминации может быть получена из того же гена, что и последовательность промотора, или может быть получена из разных генов.
Способы получения вектора
[00169] В данном документе предложены способы получения вектора, которые содержит молекулы нуклеиновой кислоты, кодирующие синтетический консенсусный антиген Сурвивин, обсуждаемый в данном документе. Вектор после заключительного этапа субклонирования может быть использован для инокуляции культуры клеток в крупномасштабном ферментационном резервуаре с использованием способов, известных в данной области техники.
[00170] Вектор для использования с устройствами EP, которые более подробно описаны ниже, может быть приготовлен или изготовлен с использованием комбинации известных устройств и технологий, но предпочтительно они изготавливаются с использованием оптимизированной технологии изготовления плазмиды, которая описана в предварительной заявке США с серийным № 60/939792, которая была подана 23 мая 2007 года (см. Пат. США публикация № 20090004716). В некоторых примерах векторы ДНК, используемые в этих исследованиях, могут быть приготовлены в концентрациях, превышающих или равных 10 мг/мл. Технологии изготовления также включают или объединяют различные устройства и протоколы, которые обычно известны специалистам в данной области техники, в дополнение к тем, которые описаны в заявке США с серийном номером 60/939792, включая те, которые описаны в патенте США № 7238522, который выдан 3 июля 2007 года. Вышеупомянутая заявка и патент, серийный номер США 60/939792, и патент США № 7238522, соответственно, включены в данный документ полностью.
Наполнители и другие компоненты вакцины
[00171] Вакцина может дополнительно содержать фармацевтически приемлемый наполнитель. Фармацевтически приемлемый наполнитель может представлять собой функциональную молекулу, такую как наполнитель, переносчик или разбавитель. Фармацевтически приемлемый наполнитель может представлять собой агент, облегчающий трансфекцию, который может включать поверхностно-активные вещества, такие как иммуностимулирующие комплексы (ISCOMS), неполный адъювант Фрейнда, аналог LPS, включая монофосфориллипид A, мурамилпептиды, аналоги хинона, везикулы, такие как сквален и сквален, гиалуроновая кислота, липиды, липосомы, ионы кальция, вирусные белки, полианионы, поликатионы или наночастицы или другие известные средства, облегчающие трансфекцию.
[00172] Средство, облегчающее трансфекцию, представляет собой полианион, поликатион, включая поли-L-глутамат (LGS) или липид. Средство, облегчающее трансфекцию, представляет собой поли-L-глутамат, а поли-L-глутамат может присутствовать в вакцине в концентрации менее 6 мг/мл. Средство, облегчающее трансфекцию, может также включать поверхностно-активные вещества, такие как иммуностимулирующие комплексы (ISCOMS), неполный адъювант Фрейнда, аналог LPS, включая монофосфориллипид А, мурамилпептиды, аналоги хинона и везикулы, такие как сквален и сквален, и гиалуроновую кислоту также могут быть использованы в сочетании с генетической конструкцией. ДНК-векторные вакцины могут также включать средство, облегчающее трансфекцию, такое как липиды, липосомы, включая лецитиновые липосомы или другие липосомы, известные в данной области техники, в виде смеси ДНК-липосом (см., например, W09324640), ионы кальция, вирусные белки, полианионы, поликатионы или наночастицы, или другие известные средства, облегчающие трансфекцию. Средство, облегчающее трансфекцию, представляет собой полианион, поликатион, включая поли-L-глутамат (LGS) или липид. Концентрация трансфекционного средства в вакцине составляет менее 4 мг/мл, менее 2 мг/мл, менее 1 мг/мл, менее 0,750 мг/мл, менее 0,500 мг/мл, менее 0,250 мг/мл. менее 0,100 мг/мл, менее 0,050 мг/мл или менее 0,010 мг/мл.
[00173] Фармацевтически приемлемый наполнитель может представлять собой один или более адъювантов. Адъювант может представлять собой другие гены, которые экспрессируются в альтернативном векторе или доставляются в виде белков в комбинации с указанным выше вектором в вакцине. Один или более адъювантов могут быть выбраны из группы, состоящей из: CCL20, α-интерферона (IFN- α), β-интерферона (IFN-β), γ-интерферона, фактора роста тромбоцитов (PDGF), TNFα, TNFβ, GM-CSF, эпидермальный фактор роста (EGF), хемокина, привлекающего Т-клетки кожи (CTACK), эпителиального тимус-экспрессированного хемокина (TECK), эпителиального хемокина, связанного со слизистой оболочкой (MEC), IL-12, IL-15, IL-28, MHC, CD80, CD86, IL-l, IL-2, IL-4, IL-5, IL-6, IL-10, IL-18, IL-33, MCP-1, MIP-la, MIP-1~, IL-8, L-селектина, P-селектина, E-селектина, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50.95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, мутантных форм IL-18, CD40, CD40L, фактора роста сосудов, фактора роста фибробластов, IL-7, фактора роста нервов, фактор роста сосудистого эндотелия, Fas, рецептора TNF, Flt, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DRS, KILLER, TRAIL-R2, TRICK2, DR6, каспазы ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IkB, неактивного NIK, SAP K, SAP-I, JNK, генов ответа интерферона, NFkB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK LIGAND, Ox40, Ox40 LIGAND, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAPI, TAP2, IL-15, имеющих сигнальную последовательность или кодирующую последовательность, которая кодирует удаленную сигнальную последовательность, и необязательно включает другой сигнальный пептид, такой как из IgE, или кодирующую последовательность, которая кодирует другой сигнальный пептид, такой как из IgE, и его функциональные фрагменты или их комбинацию. Адъювантом может быть IL-12, IL-15, IL-28, CTACK, TECK, тромбоцитарный фактор роста (PDGF), TNFα, TNFβ, GM-CSF, эпидермальный фактор роста (EGF), IL-1, IL-2 , IL-4, IL-5, IL-6, IL-10, IL-12, IL-18 или их комбинация.
[00174] В некоторых вариантах воплощения адъювант может представлять собой одну или более молекул нуклеиновой кислоты, которые кодируют белки, выбранные из группы, состоящей из: CCL-20, IL-12, IL-15, IL-28, CTACK, TECK, MEC или RANTES. Примеры конструкций и последовательностей IL-12 раскрыты в заявке PCT № PCT/US1997/019502 и соответствующей серийной заявке США № 08/956,865 и предварительной заявке США № 61/569600, поданной 12 декабря 2011 г., каждая из которых включена в данный документ посредством ссылки. Примеры конструкций и последовательностей IL-15 раскрыты в заявке PCT № PCT/US04/18962 и соответствующей заявке США, серийный номер 10/560650, и в заявке PCT № PCT/US07/00886 и соответствующей заявке США, серийный № 12/160766, и в заявке PCT № PCT/USI0/048827, каждая из которых включена в данный документ посредством ссылки. Примеры конструкций и последовательностей IL-28 раскрыты в заявке PCT № PCT/US09/039648 и соответствующей заявке США, серийный номер 12/936192, каждая из которых включена в данный документ посредством ссылки. Примеры RANTES и других конструкций и последовательностей раскрыты в заявке PCT № PCT/US1999/004332 и соответствующей заявке США, серийный номер 09/622452, каждая из которых включена в данный документ посредством ссылки. Другие примеры конструкций и последовательностей RANTES раскрыты в заявке PCT № PCT/US11/024098, которая включена в данный документ посредством ссылки. Примеры RANTES и других конструкций и последовательностей раскрыты в заявке PCT № PCT/US1999/004332 и соответствующей заявке США, серийный номер 09/622452, каждая из которых включена в данный документ посредством ссылки. Другие примеры конструкций и последовательностей RANTES раскрыты в заявке PCT № PCT/US11/024098, которая включена в данный документ посредством ссылки. Примеры хемокинов CTACK, TECK и MEC конструкций и последовательностей раскрыты в заявке PCT № PCT/US2005/042231 и соответствующей заявке США, серийный номер 11/719646, каждая из которых включена в данный документ посредством ссылки. Примеры ОХ40 и других иммуномодуляторов раскрыты в заявке США № 10/560653, которая включена в данный документ посредством ссылки. Примеры DR5 и других иммуномодуляторов раскрыты в заявке США № 09/622452, которая включена в данный документ посредством ссылки.
[00175] Другие гены, которые могут быть использованы в качестве адъювантов, включают те, которые кодируют: MCP-1, MIP-la, MIP-1p, IL-8, RANTES, L-селектин, P-селектин, E-селектин, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50.95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, IL-4, мутантные формы IL-18, CD40, CD40L, фактор роста сосудов, фактор роста фибробластов, IL-7, IL-22, фактора роста нервов, фактор роста сосудистого эндотелия, Fas, рецептор TNF, Flt, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DR5, KILLER, TRAIL-R2, TRICK2, DR6, каспазу ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IkB, неактивный NIK, SAP K, SAP-1, JNK, гены ответа интерферона, NFkB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK LIGAND, Ox40, Ox40 LIGAND, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAP1, TAP2 и их функциональные фрагменты.
[00176] Вакцина может дополнительно содержать средство, способствующее генетической вакцине, как описано в заявке с серийным номером США 021579, поданной 1 апреля 1994 года, которая полностью включена в данный документ посредством ссылки.
[00177] Вакцина может содержать плазмиды в количестве от приблизительно 1 нанограмма до 100 миллиграмм; от приблизительно 1 микрограмма до приблизительно 10 миллиграмм; или предпочтительно от приблизительно 0,1 микрограмма до приблизительно 10 миллиграмм; или более предпочтительно от приблизительно 1 до приблизительно 2 мг. В некоторых предпочтительных вариантах воплощения вакцина по настоящему изобретению содержит от приблизительно 5 нанограмм до приблизительно 1000 микрограмм ДНК. В некоторых предпочтительных вариантах воплощения вакцина может содержать от приблизительно 10 нанограмм до приблизительно 800 микрограмм ДНК. В некоторых предпочтительных вариантах воплощения вакцина может содержать от приблизительно 0,1 до приблизительно 500 микрограмм ДНК. В некоторых предпочтительных вариантах воплощения вакцина может содержать от приблизительно 1 до приблизительно 350 микрограмм ДНК. В некоторых предпочтительных вариантах воплощения вакцина может содержать от приблизительно 25 до приблизительно 250 микрограмм, от приблизительно 100 до приблизительно 200 микрограмм, от приблизительно 1 нанограмма до 100 миллиграмм; от приблизительно 1 микрограмма до приблизительно 10 миллиграмм; от приблизительно 0,1 микрограмма до приблизительно 10 миллиграмм; от приблизительно 1 до приблизительно 2 мг, от приблизительно 5 до приблизительно 1000 микрограмм, от приблизительно 10 до приблизительно 800 микрограмм, от приблизительно 0,1 до приблизительно 500 микрограмм, от приблизительно 1 до приблизительно 350 микрограмм, от приблизительно 25 до приблизительно 250 микрограмм от приблизительно 100 до приблизительно 200 мкг антигена или плазмиды, кодирующей его.
[00178] Вакцина может быть составлена в соответствии с применяемым способом введения. Фармацевтическая композиция для инъекционных вакцин может быть стерильной, апирогенной и не содержат твердых частиц. Можно использовать изотонический состав или раствор. Добавки для изотоничности могут включать хлорид натрия, декстрозу, маннит, сорбит и лактозу. Вакцина может содержать вазоконстриктор. Изотонические растворы могут включать забуференный фосфатом физиологический раствор. Вакцина может дополнительно содержать стабилизаторы, включая желатин и альбумин. Стабилизаторы могут обеспечивать стабильность состава при комнатной температуре или температуре окружающей среды в течение продолжительных периодов времени, включая LGS или поликатионы или полианионы.
Фармацевтические композиции вакцины
[00179] Вакцина может быть в форме фармацевтической композиции. Фармацевтическая композиция может содержать вакцину. Фармацевтические композиции могут содержать от приблизительно 5 нанограмм (нг) до приблизительно 10 миллиграмм (мг) молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции согласно настоящему изобретению содержат от приблизительно 25 нг до приблизительно 5 мг молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 50 нг до приблизительно 1 мг молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 0,1 до приблизительно 500 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 1 до приблизительно 350 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 5 до приблизительно 250 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 10 до приблизительно 200 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 15 до приблизительно 150 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 20 до приблизительно 100 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 25 до приблизительно 75 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 30 до приблизительно 50 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 35 до приблизительно 40 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 100 до приблизительно 200 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 10 до приблизительно 100 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 20 до приблизительно 80 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 25 до приблизительно 60 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 30 нг до приблизительно 50 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции содержат от приблизительно 35 нг до приблизительно 45 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых предпочтительных вариантах воплощения фармацевтические композиции содержат от приблизительно 0,1 до приблизительно 500 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых предпочтительных вариантах воплощения фармацевтические композиции содержат от приблизительно 1 до приблизительно 350 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых предпочтительных вариантах воплощения фармацевтические композиции содержат от приблизительно 25 до приблизительно 250 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых предпочтительных вариантах воплощения фармацевтические композиции содержат от приблизительно 100 до приблизительно 200 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины.
[00180] В некоторых вариантах воплощения фармацевтические композиции согласно настоящему изобретению содержат по меньшей мере 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100 нг молекулы нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции могут содержать по меньшей мере 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95,100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 245, 250, 255, 260, 265, 270, 275, 280, 285, 290, 295, 300, 305, 310, 315, 320, 325, 330, 335, 340, 345, 350, 355, 360, 365, 370, 375, 380, 385, 390, 395, 400, 405, 410, 415, 420, 425, 430, 435, 440, 445, 450, 455, 460, 465, 470, 475, 480, 485, 490, 495, 500, 605, 610, 615, 620, 625, 630, 635, 640, 645, 650, 655, 660, 665, 670, 675, 680, 685, 690, 695, 700, 705, 710, 715, 720, 725, 730, 735, 740, 745, 750, 755, 760, 765, 770, 775, 780, 785, 790, 795, 800, 805, 810, 815, 820, 825, 830, 835, 840, 845, 850, 855, 860, 865, 870, 875, 880, 885, 890, 895, 900, 905, 910, 915, 920, 925, 930, 935, 940, 945, 950, 955, 960, 965, 970, 975, 980, 985, 990, 995 или 1000 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции могут содержать по меньшей мере 1,5; 2; 2,5; 3; 3,5; 4; 4,5; 5; 5,5; 6; 6,5; 7; 7,5; 8; 8,5; 9; 9,5 или 10 мг или более молекулы(молекул) нуклеиновой кислоты вакцины.
[00181] В других вариантах воплощения фармацевтические композиции могут содержать до и включая 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100 нг молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции могут содержать до и включая 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95,100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 245, 250, 255, 260, 265, 270, 275, 280, 285, 290, 295, 300, 305, 310, 315, 320, 325, 330, 335, 340, 345, 350, 355, 360, 365, 370, 375, 380, 385, 390, 395, 400, 405, 410, 415, 420, 425, 430, 435, 440, 445, 450, 455, 460, 465, 470, 475, 480, 485, 490, 495, 500, 605, 610, 615, 620, 625, 630, 635, 640, 645, 650, 655, 660, 665, 670, 675, 680, 685, 690, 695, 700, 705, 710, 715, 720, 725, 730, 735, 740, 745, 750, 755, 760, 765, 770, 775, 780, 785, 790, 795, 800, 805, 810, 815, 820, 825, 830, 835, 840, 845, 850, 855, 860, 865, 870, 875, 880, 885, 890, 895, 900, 905, 910, 915, 920, 925, 930, 935, 940, 945, 950, 955, 960, 965, 970, 975, 980, 985, 990, 995 или 1000 микрограмм молекулы(молекул) нуклеиновой кислоты вакцины. В некоторых вариантах воплощения фармацевтические композиции могут содержать до и включая 1,5; 2; 2,5; 3; 3,5; 4; 4,5; 5; 5,5; 6; 6,5; 7; 7,5; 8; 8,5; 9; 9,5 или 10 мг молекулы(молекул) нуклеиновой кислоты вакцины.
[00182] Фармацевтическая композиция может дополнительно содержать другие средства для целей составления в соответствии с используемым способом введения. В тех случаях, когда фармацевтические композиции представляют собой фармацевтические композиции для инъекций, они являются стерильными, апирогенными и не содержат твердых частиц. Предпочтительно использовать изотонический состав. Как правило, добавки для изотоничности могут включать хлорид натрия, декстрозу, маннит, сорбит и лактозу. В некоторых случаях предпочтительными являются изотонические растворы, такие как забуференный фосфатом физиологический раствор. Стабилизаторы включают желатин и альбумин. В некоторых вариантах воплощения вазоконстрикторный агент добавляют к препарату.
[00183] Фармацевтическая композиция может дополнительно содержать фармацевтически приемлемый наполнитель, как указано выше в Разделе 2. Например, фармацевтически приемлемый наполнитель может включать функциональные молекулы, носители, адъюванты, носители, разбавители или средства, облегчающие трансфекцию, как предложено в Разделе 2.
Показания к применению
[00184] Вакцины и фармацевтические композиции, содержащие вакцины, представленные в настоящем документе, можно использовать для лечения или профилактики раковых клеток и раковых опухолей, экспрессирующих Сурвивин. В частности, вакцины и фармацевтические композиции, содержащие вакцины, представленные в настоящем документе, можно использовать для лечения или профилактики рака яичников, более конкретно эпителиального рака яичников, наиболее конкретно серозного рака яичников.
Способы вакцинации
[00185] В данном документе представлены способы лечения и/или профилактики рака с использованием фармацевтических составов, описанных выше. Также в данном документе описаны способы применения фармацевтических составов, описанных выше, для лечения и/или профилактики рака у субъекта. В данном документе также описаны способы вакцинации субъекта. Также в данном документе описаны способы введения фармацевтических составов, описанных в данном документе, субъекту, нуждающемуся в этом. Способы, описанные в данном документе, в совокупности называемые способами лечения с использованием фармацевтических составов, описанных в данном документе, могут включать введение одной или более вакцин, согласно настоящему описанию, субъекту, нуждающемуся в этом, для индукции терапевтического и/или профилактического иммунного ответа. Вакцина может быть введена субъекту для модуляции активности иммунной системы субъекта и усиления иммунного ответа. Введение вакцины может быть трансфекцией раковых антигенов, согласно настоящему описанию, в виде молекулы нуклеиновой кислоты, которая экспрессируется в клетке и доставляется на поверхность клетки, после чего иммунная система распознает и индуцирует клеточный, гуморальный или клеточный и гуморальный ответ. Введение вакцины может быть использовано для того, чтобы индуцировать или вызвать иммунный ответ у субъектов против одного или более раковых антигенов, как описано в настоящем документе, путем введения субъекту вакцины, как описано в настоящем документе.
[00186] Вакцина может быть введена субъекту для модуляции активности иммунной системы субъекта и, таким образом, усиления иммунного ответа. В некоторых вариантах субъектом является млекопитающее. При введении вакцины млекопитающему и тем самым введении вектора в клетки млекопитающего трансфицированные клетки будут экспрессировать и секретировать один или более раковых антигенов, согласно настоящему описанию. Эти секретируемые белки или синтетические антигены будут распознаваться иммунной системой как чужеродные, что приведет к возникновению иммунного ответа, который может включать: антитела, созданные против одного или более раковых антигенов, и ответ Т-клеток, конкретно против одного или более раковых антигенов. В некоторых примерах млекопитающее, вакцинированное вакцинами, обсуждаемыми в данном документе, будет иметь примированную иммунную систему, и при заражении одним или более антигенами рака, согласно настоящему описанию, примированная иммунная система позволит быстро избавиться от последующих антигенов рака, согласно настоящему описанию, независимо от того, через гуморальный, клеточный или как клеточный, так и гуморальный иммунные ответы.
[00187] Способы введения ДНК вакцины описаны в патентах США №№ 4945050 и 5036006, оба из которых полностью включены в настоящее описание посредством ссылки.
[00188] Вакцина может быть введена млекопитающему, чтобы вызвать иммунный ответ у млекопитающего. Млекопитающее может быть человеком, приматом, не являющимся человеком, коровой, свиньей, овцой, козой, антилопой, бизоном, водяным буйволом, быками, оленем, ежами, слонами, ламой, альпакой, мышами, крысами и предпочтительно человеком, коровой или свиньей Вакцина также может быть введена субъекту, не являющемуся млекопитающим, например курице, чтобы вызвать иммунный ответ.
[00189] Доза вакцины может составлять от 1 микрограмм до 10 мг активного компонента на килограмм (кг) массы тела во времени (компонент/кг массы тела/время) и может составлять от 20 микрограмм до 10 мг компонента/кг массы тела/время. Вакцину можно вводить каждые 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или 31 день. Количество доз вакцины для эффективного лечения может составлять 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более доз.
Способы генерации иммунного ответа с помощью вакцины
[00190] Вакцина может быть использована для генерирования иммунного ответа у млекопитающего или немлекопитающего субъекта, включая терапевтический или профилактический иммунный ответ. Иммунный ответ может генерировать антитела и/или Т-клетки-киллеры, направленные на один или более раковых антигенов, согласно настоящему описанию. Такие антитела и Т-клетки могут быть выделены.
[00191] Некоторые варианты воплощения предоставляют способы генерирования иммунных ответов против одного или более раковых антигенов, согласно настоящему описанию, причем эти варианты воплощения включают введение вакцины субъекту. Некоторые варианты воплощения обеспечивают способы профилактической вакцинации субъекта против рака или опухоли, экспрессирующих один или более раковых антигенов, как описано выше, причем эти варианты воплощения включают введение вакцины. Некоторые варианты воплощения предоставляют способы терапевтической вакцинации субъекта, который страдает от рака или опухоли, экспрессирующих один или более раковых антигенов, причем эти варианты воплощения включают введение вакцины. Диагностика рака или опухоли, экспрессирующих один или более раковых антигенов, согласно настоящему описанию, до введения вакцины может проводиться в обычном режиме.
Способы лечения рака с помощью вакцины
[00192] Вакцина может быть использована для генерирования или индукции иммунного ответа у млекопитающего, который реактивен или направлен на Сурвивин-экспрессирующий рак или опухоль (например, рак яичника) млекопитающего или субъекта, нуждающегося в этом. Вызванный иммунный ответ может предотвратить рак или рост опухоли.
[00193] Вызванный иммунный ответ может предотвращать и/или уменьшать метастазирование раковых или опухолевых клеток. Соответственно, вакцина может быть использована при способе, который лечит и/или предотвращает рак или опухоли у млекопитающего или субъекта, которому вводят вакцину.
Пути введения
[00194] Вакцина или фармацевтическая композиция может вводиться различными путями, включая пероральный, парентеральный, сублингвальный, трансдермальный, ректальный, трансмукозальный, местный, посредством ингаляции, посредством буккального введения, внутриплеврально, внутривенно, внутриартериально, внутрибрюшинно, подкожно, внутримышечно, интраназально, интратекально и/или внутрисуставно, или их комбинациями. Для ветеринарного применения композицию можно вводить в виде подходящей приемлемой композиции в соответствии с обычной ветеринарной практикой. Ветеринар может легко определить режим дозирования и путь введения, который наиболее подходит для конкретного животного. Вакцину можно вводить с помощью традиционных шприцев, безыгольных инъекционных устройств, «генных пушек с бомбардировкой микрочастицами» или других физических способов, таких как электропорация («EP»), «гидродинамический способ» или ультразвук.
[00195] Вектор вакцины может быть введен млекопитающему с помощью нескольких хорошо известных технологий, включая инъекцию ДНК (также называемую ДНК-вакцинацией) с in vivo электропорацией и без нее, трансфекцию, опосредованную липосомами, трансфекцию, обеспеченную наночастицами, и использование рекомбинантных векторов, таких как рекомбинантный аденовирус, рекомбинантный аденовирус-ассоциированный вирус и рекомбинантная вакцинация. Один или более раковых антигенов вакцины можно вводить путем инъекции ДНК вместе с in vivo электропорацией.
[00196] Вакцина или фармацевтическая композиция, содержащая вакцину, может быть введена путем электропорации. Введение вакцины посредством электропорации может быть выполнено с использованием устройств электропорации, которые могут быть сконфигурированы для доставки в желаемую ткань млекопитающего импульса энергии, эффективного для образования обратимых пор в клеточных мембранах, и предпочтительно импульс энергии представляет собой постоянный ток. соответствующий входящему току, заданному пользователем. Устройство электропорации может содержать компонент электропорации и электродную установку или ручную установку. Компонент электропорации может включать и объединять один или более различных элементов устройств электропорации, в том числе: контроллер, генератор сигналов тока, измеритель импеданса, регистратор сигналов, элемент ввода, элемент сообщения о состоянии, порт связи, компонент памяти, источник питания и выключатель. Электропорацию можно проводить с использованием устройства электропорации in vivo, например системы CELLECTRA® EP (Inovio Pharmaceuticals, Inc., Блу Белл, Пенсильвания) или электропоратора Elgen (Inovio Pharmaceuticals, Inc.), чтобы облегчить трансфекцию клеток вектором.
[00197] Примеры устройств электропорации и способов электропорации, которые могут облегчать введение ДНК-вакцин по настоящему изобретению, включают те, которые описаны в патенте США № 7245963, Draghia-Akli и др., патентной публикация США. 2005/0052630, представленный Smith et al., содержание которого полностью включено в данный документ посредством ссылки. Другие устройства электропорации и способы электропорации, которые можно использовать для обеспечения введения ДНК-вакцин, включают устройства, представленные в одновременно находящейся на рассмотрении и находящейся в совместном владении заявке на патент США, серийный № 11/874072, поданной 17 октября 2007 г., которая претендует на преимущество в соответствии с 35 USC 119 (д) к предварительным заявкам США Сер. № 60/852149, поданной 17 октября 2006 года, и 60/978982, поданной 10 октября 2007 года, и все они включены в настоящий документ в полном объеме.
[00198] Патент США № 7245963, Draghia-Akli, et al. описывает модульные электродные системы и их использование для обеспечения введения биомолекулы в клетки выбранной ткани организма или растения. Модульные электродные системы могут содержать множество игольчатых электродов; иглу для подкожных инъекций; электрический разъем, который обеспечивает проводящую связь от программируемого импульсного контроллера постоянного тока к множеству игольчатых электродов; и источник питания. Оператор может обхватить множество игольчатых электродов, которые установлены на опорной конструкции и плотно вставить их в выбранную ткань в теле или растения. Затем биомолекулы вводят через подкожную иглу в выбранную ткань. Программируемый контроллер импульсов постоянного тока активируется, и электрический импульс постоянного тока подается на множество игольчатых электродов. Применяемый электрический импульс постоянного тока облегчает введение биомолекулы в клетку между совокупностью электродов. Все содержание патента США № 7245963 полностью включено в настоящее описание посредством ссылки.
[00199] Публикация патента США 2005/0052630, представленная Smith et al. описывает устройство электропорации, которое можно использовать для эффективного обеспечения введения биомолекулы в клетки выбранной ткани организма или растения. Устройство электропорации содержит электрокинетическое устройство («устройство EKD»), работа которого задается внешним программным обеспечением или встроенным программным обеспечением. Устройство EKD генерирует серию программируемых паттернов импульсов постоянного тока между электродами в массиве на основе пользовательского управления и ввода параметров импульсов, а также позволяет хранить и получать данные о форме сигнала тока. Устройство электропорации также содержит сменный электродный диск, имеющий ряд игольчатых электродов, центральный канал для инъекционной иглы и съемный направляющий диск. Все содержание публикации патента США. 2005/0052630 полностью включена в данный документ в качестве ссылки.
[00200] Электродные массивы и способы, описанные в патенте США № 7245963 и публикации патента США 2005/0052630, можно адаптировать для глубокого проникновения не только в такие ткани, как мышцы, но и в другие ткани или органы. Из-за конфигурации массива электродов инъекционная игла также полностью вставляется в орган-мишень, и инъекция вводится перпендикулярно целевому проблемному участку в места, которые изначально заданы электродами. Электроды, описанные в патенте США № 7245963 и публикации патента США 2005/005263, предпочтительно имеют длину 20 мм и 21 калибр игл.
[00201] Кроме того, в некоторых вариантах осуществления, которые включают устройства электропорации и их применение, существуют устройства электропорации, которые описаны в следующих патентах: патент США 5 273 525, выданный 28 декабря 1993 г., патенты США 6 110 161, выданные 29 августа 2000 г., 6 261 281, выданный 17 июля 2001 г., и 6 958 060, выданный 25 октября 2005 г., и патент США 6 939 862, выданный 6 сентября 2005 г. Кроме того, в настоящем документе рассматриваются патенты, охватывающие объект изобретения, предложенный в патенте США 6 697 669, выданном 24 февраля 2004 г., который касается введения ДНК с использованием любого из множества устройств, и патент США 7 328 064, выданный 5 февраля 2008 г., который относится к способу введения ДНК. Вышеуказанные патенты включены посредством ссылки во всей их полноте.
[00202] В данном документе предложены способы получения векторов, которые содержат молекулу(ы) нуклеиновой кислоты, кодирующую синтетический консенсусный антиген Сурвивин, обсуждаемый в данном документе. После заключительной стадии субклонирования в плазмиду для экспрессии в млекопитающих векторы могут быть использованы для инокуляции культуры клеток в крупномасштабном ферментационном резервуаре с использованием известных способов в данной области.
[00203] Векторы ДНК для использования с EP-устройствами по настоящему изобретению могут быть составлены или изготовлены с использованием комбинации известных устройств и технологий, но предпочтительно они изготавливаются с использованием оптимизированной технологии изготовления, которая описана в опубликованной заявке США № 20090004716, поданной 23 мая 2007 года. В некоторых примерах векторы ДНК, используемые в этих исследованиях, могут быть приготовлены в концентрациях, превышающих или равных 10 мг/мл. Технологии изготовления также включают или объединяют различные устройства и протоколы, которые широко известны специалистам в данной области техники, в дополнение к тем, которые описаны в заявке США с серийном номером 60/939792, включая те, которые описаны в патенте США № 7238522, который выдан 3 июля 2007 года. Вышеупомянутая заявка и патент, серийный номер США 60/939792, и патент США № 7238522, соответственно, включены в данный документ полностью.
Примеры
[00204] Настоящее изобретение дополнительно проиллюстрировано в следующих примерах. Следует понимать, что эти примеры, хотя и отображают предпочтительные варианты воплощения изобретения, приведены только в качестве иллюстрации. Из приведенного выше обсуждения и этих примеров специалист в данной области техники может определить основные характеристики этого изобретения и, не отступая от его сущности и объема, может внести различные изменения и модификации изобретения, чтобы адаптировать его к различным применениям и условиям. Таким образом, различные модификации изобретения в дополнение к тем, которые показаны и описаны в данном документе, будут очевидны для специалистов в данной области техники из предшествующего описания. Такие модификации также должны попадать в объем прилагаемой формулы изобретения.
Пример 1 - Получение изоформы 1 консенсуса Сурвивина
[00205] Двадцать девять последовательностей изоформы 1 Сурвивина были получены из GenBank (www.ncbi.nlm.nih.gov/genbank/). Номера доступа GenBank для выбранных последовательностей изоформы 1 Сурвивина представляют собой: NP_001125727.1, 3UIG, 1F3H, BAC22748.2, NP_001159.2, CAG46540.1, BAD97148.1, XP_002748841.1, XP_003818322.1, NP_001253110.1, XP_011810718.1, XP_011832690.1, XP_001083183.1, XP_003786134.1, XP_012516801.1, XP_007957800.1, XP_001915435.1, XP_008523102.1, AAT37504.1, XP_004432883.1, XP_003417277.1, XP_004374167.1, NP_999306.1, XP_002918421.1, NP_001003348.1, NP_001009280.1, XP_004748859.1, NP_001001855.2 и AAU89275.1.
[00206] Консенсусная последовательность была получена с помощью программного пакета DNASTAR® Lasergene (версия 13.0.0.357). Двадцать девять последовательностей, перечисленных выше, были импортированы в MegAlign и выровнены с использованием программы выравнивания множественных последовательностей ClustalW. Полученная последовательность изоформы 1 консенсуса Сурвивина имеет гомологию 97,2-97,9% с нативной изоформой 1 Сурвивина человека. Чтобы устранить потенциальную биологическую функцию полученного белка изоформы 1 консенсуса Сурвивина, были введены три мутации, чтобы устранить антиапоптотическую активность Сурвивина. Три мутации представляют собой Т34А, Т48А и С84А. Дополнительно, для того, чтобы иметь более высокий уровень экспрессии, к N-концу добавляли левую последовательность Козака и лидерную последовательность IgE. Кроме того, использование кодонов этого гена было адаптировано к смещению кодонов генов Homo Sapiens. (Andre, S. et al. Increased immune response elicited by DNA vaccination with a synthetic gp120 sequence with optimized codon usage. Journal of virology 72, 1497-1503 (1998); Deml, L. et al. Multiple effects of codon usage optimization on expression and immunogenicity of DNA candidate vaccines encoding the human immunodeficiency virus type 1 Gag protein. Journal of virology 75, 10991-11001, doi:10.1128/JVI.75.22.10991-11001.2001 (2001)).
Кроме того, была также проведена оптимизация РНК: избегали областей с очень высоким (> 80%) или очень низким (<30%) содержанием GC и мотивами цис-действующей последовательности, такими как внутренние боксы TATA, chi-сайты и сайты рибосомного входа. В результате белок изоформы 1 синтетического консенсусного антигена Сурвивина обладает 95,1-95,8% идентичностью с нативным белком изоформы 1 Сурвивина человека. Нуклеотидная последовательность изоформы 1 синтетического консенсусного антигена Сурвивина представлена в SEQ ID NO: 1. Аминокислотная последовательность изоформы 1T3 синтетического консенсусного антигена Сурвивина представлена в SEQ ID NO: 2.
[00207] Изоформа 1 синтетического консенсусного антигена Сурвивина была расщеплена с помощью BamHI и XhoI и клонирована в запатентованный вектор экспрессии pGX0001 с кассетой экспрессии, помещенной под контроль транскрипции немедленно-раннего промотора цитомегаловируса. Полученная плазмида была обозначена pGX1428. Было выполнено секвенирование полной длины, а затем проанализировано и подтверждено, что оно является правильным. Схематическое представление конструкции изоформы 1 синтетического консенсусного антигена Сурвивина показано на фиг.1. Общая структура изоформы 1 синтетического консенсусного антигена Сурвивина показана на фиг. 2.
Таблица 1.
T65A
C101A
T65A
C101A
Таблица 2. Характеристики изоформы 1 синтетического консенсусного антигена Сурвивин
Пример 2 - Получение изоформы 1T3 консенсуса Сурвивина
[00208] Для создания изоформы 3 человеческого консенсуса Сурвивина было получено 8 последовательностей изоформы 3 Сурвивина из GenBank (www.ncbi.nlm.nih.gov/genbank/). Номера доступа GenBank для выбранных последовательностей изоформы 3 Сурвивина представляют собой: NP_001012270.1, XP_008969790.1, XP_008011275.1, XP_009189614.1, XP_011897653.1, XP_011810642.1, XP_011844315.1 и XP_011718355.1.
[00209] Консенсусная последовательность была получена с помощью программного пакета DNASTAR® Lasergene (версия 13.0.0.357). Восемь последовательностей, перечисленных выше, были импортированы в MegAlign и выровнены с использованием программы выравнивания множественных последовательностей ClustalW. Шесть из этих последовательностей от низших животных содержали дополнительные 11 аминокислотных остатков на их C-терминальном конце, которых нет в человеческих последовательностях. Эти дополнительные остатки не учитывались при создании изоформы 3 консенсусного человеческого Сурвивина, чтобы избежать возникновения нецелевого иммунного ответа у людей. После создания изоформы 3 человеческого консенсусного Сурвивина идентичная аминокислотная последовательность между изоформой 1 и 3 Сурвивина была удалена из изоформы 3 консенсуса Сурвивина. Укороченная последовательность изоформы 3 консенсуса Сурвивина (антиген Сурвивина Т3) имеет 96,8% гомологии последовательности с нативной последовательностью изоформы Т3 человеческого Сурвивина. Иммуноген изоформы 1Т3 антигена Сурвивин получали путем добавления сайта расщепления фурином между антигеном 1 Сурвивина (описанным выше) и антигеном Т3 Сурвивина.
[00210] Как только была получена последовательность ДНК изоформы 1T3 синтетического консенсусного антигена Сурвивина, для того чтобы иметь более высокий уровень экспрессии, к N-концу добавляли левую последовательность Kozak и лидерную последовательность IgE. (Yang, J. S. et al. Induction of potent Th1-type immune responses from a novel DNA vaccine for West Nile virus New York isolate (WNV-NY1999). The Journal of infectious diseases 184, 809-816, doi:10.1086/323395 (2001)). Кроме того, использование кодонов этого гена было адаптировано к смещению кодонов генов Homo Sapiens (Andre, S. et al. Increased immune response elicited by DNA vaccination with a synthetic gp120 sequence with optimized codon usage. Journal of virology 72, 1497-1503 (1998); Deml, L. et al. Multiple effects of codon usage optimization on expression and immunogenicity of DNA candidate vaccines encoding the human immunodeficiency virus type 1 Gag protein. Journal of virology 75, 10991-11001, doi:10.1128/JVI.75.22.10991-11001.2001 (2001)). Кроме того, была также проведена оптимизация РНК: избегали областей с очень высоким (> 80%) или очень низким (<30%) содержанием GC и мотивами цис-действующей последовательности, такими как внутренние TATA-боксы, chi-сайты и сайты рибосомного входа 11,12. Изоформа 1T3 синтетического консенсусного антигена Сурвивина была расщеплена с помощью BamHI и XhoI и клонирована в вектор экспрессии pGX0001 с кассетой экспрессии, помещенной под контроль транскрипции немедленно-раннего промотора цитомегаловируса. Полученная плазмида была обозначена pGX1429. Было выполнено секвенирование полной длины, а затем проанализировано и подтверждено, что оно является правильным. Нуклеотидная последовательность изоформы 1T3 синтетического консенсусного антигена Сурвивина представлена в SEQ ID NO:3, как показано в таблице 1. Аминокислотная последовательность изоформы 1T3 синтетического консенсусного антигена Сурвивина представлена в SEQ ID NO:8, как показано в таблице 1. Схематическое представление конструкции изоформы 1T3 синтетического консенсусного антигена Сурвивина показано на фиг.3. Характеристики конструкции изоформы 1T3 синтетического консенсусного антигена Сурвивина приведены в таблице 3.
Таблица 3. Характеристики изоформы 1T3 синтетического консенсусного антигена Сурвивин
Пример 3. - Конструирование Сурвивин-экспрессирующих векторов pGX
[00211] pGX0001 (модифицированный вектор экспрессии pVAX1) под контролем немедленно-раннего промотора цитомегаловируса человека (промотор hCMV) использовали в качестве каркасного вектора. Оригинальный pVAX1 был получен от Thermo Fisher Scientific.
[00212] Модификации были введены в pVAX1 для создания pGX0001 и идентифицированы на основе описанной последовательности pVAX1, доступной от Thermo Fisher Scientific. Эти модификации перечислены ниже, и не было обнаружено никаких проблем, касающихся амплификации плазмиды и транскрипции и трансляции антигена. Никаких дополнительных изменений в последовательности pGX0001 до настоящего времени не наблюдалось ни в одном из плазмидных продуктов на платформе, использующей pGX0001 в качестве основной цепи.
Модификация Пара оснований Описание
C>G 241 в CMV промоторе
C>T 1158 основная цепь, справа от сигнала полиаденилирования (bGH polyA) бычьего гормона роста
A> - 2092 основная цепь, справа от гена устойчивости к канамицину
gene
C>T 2493 в точке начала репликации pUC (pUC ori)
G>C 2969 в самом конце Ori pUC слева от сайта RNASeH
Пары оснований 2, 3 и 4 изменяются с ACT на CTG в основной цепи слева от промотора CMV.
[00213] pGX1428 представляет собой ДНК-плазмиду, кодирующую белок изоформы 1 синтетического консенсусного антигена Сурвивин (антигена Сурвивин 1). Связанное продуцирование мРНК управляется человеческим промотором CMV (промотором hCMV) и прекращается сигналом полиаденилирования 3'-конца бычьего гормона роста (bGH polyA). Основная цепь pGX0001 включает ген устойчивости к канамицину (KanR) и плазмидную точку начала репликации (pUC ori) для производственных целей. Эти элементы не функционируют в эукариотических клетках. pGX1428 получали путем клонирования последовательности ДНК изоформы 1 синтетического консенсусного антигена Сурвивин (антигена Сурвивин 1) в pGX0001 в сайтах BamHI и XhoI, как показано на фиг. 4.
[00214] pGX1429 представляет собой ДНК-плазмиду, кодирующую белок 1T3 синтетического консенсусного антигена Сурвивин (антигена Сурвивин 1T3). Связанное продуцирование мРНК управляется человеческим промотором CMV (промотором hCMV) и прекращается сигналом полиаденилирования 3'-конца бычьего гормона роста (bGH polyA). Основная цепь pGX0001 включает ген устойчивости к канамицину (KanR) и плазмидную точку начала репликации (pUC ori) для производственных целей. Эти элементы не функционируют в эукариотических клетках. pGX1429 получали путем клонирования последовательности ДНК изоформы 1T3 синтетического консенсусного антигена Сурвивин (антигена Сурвивин 1T3) в pGX0001 в сайтах BamHI и XhoI, как показано на фиг.5.
Пример 4 - Иммуногенность конструктов синтетического консенсусного антигена Сурвивин
[00215] Иммуногенность конструкций вакцины, предназначенной для нацеливания на Сурвивин человека, синтетический консенсусный антиген Сурвивин 1 (pGX1428) и синтетический консенсусный антиген Сурвивин 1T3 (pGX1429), оценивали на мышах. Экспрессию белков антигена по конструкции также оценивали in vitro методом вестерн-блоттинга.
Материалы и способы
Плазмиды
[00216] Синтетический консенсусный антиген 1 Сурвивина (pGX1428) и синтетический консенсусный антиген 1T3 Сурвивина (pGX1429) были сконструированы, как описано в настоящем документе. Для исследований in vitro и in vivo плазмиды (10 мг) были заказаны из GenScript как для pGX1428 (лот № 786114S-1/G52238), так и для pGX1429 (лот № 786114S-2/G52239). Последовательности антигенов из 10 мг плазмидных стоков подтверждали секвенированием по Сангеру.
Экспрессия антигена in vitro
[00217] Экспрессия белков антигена с помощью pGX1428 и pGX1429 была подтверждена вестерн-блоттингом. Как показано на фиг.6 клетки человеческой рабдомиосаркомы (RD) (ATCC, CCL-136), поддерживаемые в среде DMEM с 10% FBS (ThermoFisher), трансфецировали с pGX1428, pGX1429 или pGX0001 (6 мкг/10 см2 планшет) с использованием Turbofectin 8 (Origene). Через сорок восемь часов после трансфекции клетки лизировали с использованием буфера для лизиса клеток RIPA (ThermoFisher) и собирали лизат клеток. После анализа BCA (ThermoFisher) для определения концентрации общего белка 15 мкг клеточного лизата подвергали электрофорезу в 4-12% геле SDS-PAGE (ThermoFisher). Детекцию проводили с помощью моноклонального антитела против аминокислот 1-142 Сурвивина человека (Santa Cruz Biotech, клон D8, sc-17779), затем визуализировали с помощью конъюгированного с пероксидазой хрена (HRP) козьего антимышиного IgG (Santa Cruz Biotech, sc-2005) с использованием системы вестерн-блот анализа ECL (GE Amersham). В качестве контроля нагрузки блоты повторно исследовали на экспрессию актина с использованием моноклонального антитела против β-актина (Santa Cruz Biotech, клон C4, sc-47778 HRP).
Животные и иммунизации
[00218] Самки 8-недельных мышей CB6F1 были приобретены в лаборатории Джексона. Все животные содержались в помещении с регулируемой температурой и легкой цикличностью в BTS Research (Сан-Диего, Калифорния). Уход за животными осуществлялся в соответствии с руководящими принципами Национального института здравоохранения и предложением по уходу и использованию животных (ACUP) (BTS ACUP # 15-091). Мыши были разделены на девять групп, как показано в таблице 4.
Таблица 4. Группы исследований
[00219] Мышей в иммунизированных группах вакцинировали указанными дозами pGX0001, pGX1428 или pGX1429 согласно SOP R20-003147 CELLECTRA® 3P лечением мышей. Вкратце, плазмиды готовили в стерильной воде для инъекций (VetOne) так, чтобы указанная доза доставлялась путем внутримышечной инъекции в переднюю мышцу большеберцовой кости в объеме инъекции 30 мкл. За каждой внутримышечной инъекцией немедленно следовала электропорация (ЕР) с использованием адаптивного устройства электропорации постоянного тока CELLECTRA® 2000 с массивом 3P (Inovio Pharmaceuticals). Устройство было настроено на подачу двух импульсов 0,1 А с шириной импульса 52 мс, разнесенных на 1 секунду. Мыши получили 3 иммунизации с интервалом 3 недели. Мышей умерщвляли через неделю после последней иммунизации, а селезенки собирали для клеточных иммунных отсчетов. Никакой другой ткани не было собрано.
Выделение лимфоцитов селезенки
[00220] Спленоциты были асептически выделены и помещены в 5 мл среды R10 (среда 1640 Rosewell Park Memorial Institute, дополненная 10% эмбриональной бычьей сывороткой и 1% антибиотиком-антимикотиком). Спленоциты выделяли путем механического разрушения селезенки с использованием аппарата Stomacher (Seward Laboratory Systems Inc.), и полученный продукт фильтровали с использованием сита для клеток 40 мкм (BD Falcon). Полученный продукт центрифугировали и осадок обрабатывали в течение 5 минут буфером для лизиса ACK (Lonza) для лизиса эритроцитов. Спленоциты затем центрифугировали, промывали в PBS, а затем ресуспендировали в среде R10 и немедленно использовали для дальнейшего анализа.
IFNγ ELISpot
[00221] Анализ ELISpot IFNγ мыши проводили с использованием набора от MabTech (MabTech, № 3321-4APW-10) для оценки антиген-специфических клеточных ответов. Вкратце, 96-луночные планшеты, предварительно покрытые антителом против мышиного IFNγ (mAb AN18), промывали в PBS и блокировали в течение 2 часов при комнатной температуре полной культуральной средой (RPMI 1640 с добавлением 10% FBS и антибиотиков). Лимфоциты селезенки ресуспендировали в среде R10 (а затем добавляли в трех экземплярах при количестве введенных 2 × 105 клеток на лунку. Был синтезирован набор пептидов (GenScript), каждый из которых содержал 15 аминокислотных остатков, перекрывающихся 11 аминокислотами, представляющими полные белковые последовательности синтетического консенсусного антигена 1 Сурвивина и синтетического консенсусного антигена 1T3 Сурвивина. Эти наборы пептидов ресуспендировали в ДМСО (Sigma) и объединяли в концентрации пептида ~ 2 мкг/мл в два пептидных пула. Один пул пептидов содержал пептиды, соответствующие белку синтетического консенсусного антигена 1 Сурвивина, а второй пептидный пул содержал пептиды, соответствующие белку синтетического консенсусного антигена 1T3 Сурвивина. Конкавалин А (Sigma) в концентрации 5 мкг/мл использовали в качестве положительного контроля, а полную культуральную среду использовали в качестве отрицательного контроля. Планшеты инкубировали в течение 18 часов при 37°С в инкубаторе с 5% CO2. Затем добавляли биотинилированное анти-мышиное антитело для определения IFNγ (MabTech mAb R4-6A2) и планшеты инкубировали в течение 2 часов при комнатной температуре. Планшеты промывали, добавляли стрептавидин-ALP (MabTech) и планшеты инкубировали в течение 1 часа при комнатной температуре. Обнаружение пятна было выполнено с применением субстрата BCIP/NBT в соответствии с инструкциями производителя комплекта (MabTech). Пятна на планшетах подсчитывали с использованием автоматического считывателя ELISPOT (Cellular Technology). Среднее количество единиц формирования пятен (SFU) было скорректировано до 1 × 106 спленоцитов для отображения данных.
[00222] На фиг. 7A-7H антигенспецифические ответы IFNγ ELISpot представлены как число единиц, формирующих пятно IFNγ (SFU) на 1 × 106 спленоцитов, больше, чем SFU в контроле только в среде.
Проточная цитометрия
[00223] Клеточные иммунные ответы, индуцированные синтетическим консенсусным антигеном 1 Сурвивина и синтетическим консенсусным антигеном 1T3 Сурвивина, были дополнительно охарактеризованы проточной цитометрией. Вкратце, 2 × 106 спленоцитов от вакцинированных и наивных мышей сразу же стимулировали после выделения пептидов синтетического консенсусного антигена 1 Сурвивина и 1T3 Сурвивина, соответственно каждой группе, в течение 6 часов в присутствии Брефельдина A (BD Biosciences), Монензина (BD Biosciences) и FITC против мышиного антитела против CD107a (BD Biosciences, клон 1D4B). После стимуляции пептидами спленоциты центрифугировали и ресуспендировали в 20 мкл на лунку раствора BD Fc Block (BD Biosciences) мыши. Блок Fc используют при начальном разведении 1:40 в PBS и инкубируют при 4°С в течение 5 минут. После инкубации оставшиеся внеклеточные антитела (в PBS) добавляют при 30 мкл на лунку и дают возможность инкубироваться при 4°С в течение 30 минут. После добавления внеклеточного красителя конечный объем в каждой лунке составляет 50 мкл, состоящий из Fc-блока в конечном разведении 1:100 и внеклеточных антител в их соответствующих рабочих разведениях. Затем клетки окрашивали красителем жизнеспособности (Vivid V450, Thermo-Fisher) и следующими внеклеточными антителами: PerCP-Cy5.5 анти-мышиным CD4 (BD Biosciences, клон RM4-5) и APC анти-мышиным CD8a (BD Biosciences, клон 63-6.7). Клетки фиксировали и пермеабилизировали (BD Biosciences, №554714) в течение 20 минут при 4°C. Внутриклеточное окрашивание было впоследствии завершено следующими антителами: APC-Cy7 анти-мышиныи CD3e (BD Biosciences, клон 145-2C11), BV605 анти-мышиным IFNγ (BD Biosciences, клон XMG1.2), APC-R700 анти-мышиным IL-2 (BD Biosciences, клон JEs6-5H4) и PE анти-мышиным TNF-α (BD Biosciences, клон MP6-XT22). Данные ICS были собраны на 10-цветном FACS CANTO (BD Biosciences) и анализ завершен с использованием программного обеспечения FlowJo. Стратегия гейтинга проточной цитометрии показана на фиг. 8.
[00224] Для того, чтобы клетку можно было назвать антигенспецифичной с помощью проточной цитометрии, частота описанного параметра должна превышать частоту контроля только для среды. Для того чтобы клетка была идентифицирована как продуцирующая антигенспецифичный CD107a, клетка также должна быть идентифицирована как позитивная по антигенспецифической продукции IFNγ и/или IL-2 и/или TNFα, как идентифицировано с помощью Булевого гейтинга.
Статистический анализ
[00225] Статистический анализ был выполнен с использованием IBM SPSS Statistics 22 (IBM Corporation). Анализ между группами был выполнен с использованием ANOVA с честной достоверной разницей (HSD) Тьюки для специальной оценки, чтобы скорректировать множественные сравнения. Однородность дисперсии была подтверждена с использованием F-статистики перед множественными сравнениями. Для всего статистического анализа значение р 0,050 считалось значимым.
Результаты
Экспрессия белков синтетического консенсусного антигена Сурвивин
[00226] Две конструкции были сконструированы для нацеливания на Сурвивин человека, синтетический консенсусный антиген 1 Сурвивин (pGX1428) и синтетический консенсусный антиген 1T3 Сурвивин (pGX1429). Экспрессия антигенных белков синтетического консенсусного антигена 1 Сурвивина и синтетического консенсусного антигена 1Т3 Сурвивина с помощью pGX1428 и pGX1429, соответственно, была подтверждена вестерн-блоттингом. Вкратце, клетки рабдомиосаркомы человека (RD) трансфицировали плазмидами pGX1428, pGX1429 или pGX0001 (пустой вектор, отрицательный контроль). Клеточные лизаты исследовали на экспрессию белков синтетического консенсусного антигена Сурвивина с антителом против Сурвивина человека (BIRC5). Были обнаружены полосы белка с ожидаемой молекулярной массой для синтетического консенсусного антигена 1 Сурвивина (17,5 кДа) и синтетического консенсусного антигена 1T3 Сурвивина (25,3 кДа) (фиг. 6). Слабая полоса была обнаружена в отрицательном контроле (pGX0001), что, скорее всего, связано с низким уровнем экспрессии эндогенного белка Сурвивина в клеточной линии RD. Полосы анти-β-актина были обнаружены с одинаковой интенсивностью, что указывало на то, что в каждой полосе были загружены равные количества белка. Таким образом, было обнаружено, что pGX1428 и pGX1429 экспрессируют свои соответствующие антигенные белки.
Иммуногенность конструкций вакцины синтетического консенсусного антигена Сурвивина
IFNγ ELISpot
[00227] Иммуногенность двух конструкций синтетического консенсусного антигена Сурвивина оценивали в четырех дозах (10, 20, 30 и 50 мкг) с помощью IFNγ ELISpot и проточной цитометрии (n=8/группа). Мышей иммунизировали пустым вектором-основой (pGX0001) в качестве отрицательного контроля (n=4/группа). Вакцинация синтетическим консенсусным антигеном 1 Сурвивина приводила к значимым ответам IFNγ по сравнению с мышами, вакцинированными с отрицательным контролем. Тем не менее, было минимальное доказательство дозозависимого увеличения продукции IFNγ, индуцированного синтетическим консенсусным антигеном 1 Сурвивина (фиг. 10А), что свидетельствует о том, что максимальный ответ был достигнут при самой низкой дозе. В частности значение IFNγ SFU для синтетического консенсусного антигена Сурвивин составляло 1 082 ± 574, 1 186 ± 747, 1 135 ± 647 и 848 ± 350 при 10, 20, 30 и 50 мкг соответственно. Ответы IFNγ на синтетический консенсусный антиген 1 Сурвивин был значительно больше, чем наивные (2 ± 3), при дозах 10 мкг (р=0,031), 20 мкг (р=0,015) и 30 мкг (р=0,021) pGX1428, но не при дозе 50 мкг (р=0,134). Вакцинация синтетическим консенсусным антигеном 1T3 Сурвивина привела к значимым ответам IFNγ с некоторыми доказательствами дозозависимого увеличения при повышении уровня дозы (Фиг. 10D). Значение IFNγ SFU для Сурвивина 1T3 составляло 516 ± 156, 812 ± 534, 1 016 ± 654 и 818 ± 339 при 10 мкг, 20 мкг, 30 мкг и 50 мкг соответственно. Ответы IFNγ на синтетический консенсусный антиген 1T3 Сурвивин был значительно больше, чем наивные (5 ± 6), при дозах 20 мкг (р=0,039), 30 мкг (р=0,006) и 50 мкг (р=0,037) pGX1429, но не при дозе 10 мкг (р=0,337). Ответы IFNγ подытожены в таблице 5.
Таблица 5. IFN-гамма-ответы, индуцированные синтетическим консенсусным антигеном 1 Сурвивина и синтетическим консенсусным антигеном 1T3 Сурвивина.
Проточная цитометрия
[00228] Синтетический консенсусный антиген 1 Сурвивина и синтетический консенсусный антиген 1T3 Сурвивина оба вызывали более устойчивые ответы в компартменте CD4+ T-клеток по сравнению с ответами в компартменте CD8+ T-клеток (фиг. 9). Синтетический консенсусный антиген-1 Сурвивина индуцировал частоты антиген-специфических ответов CD4+Т-клеток, которые были значительно более устойчивыми, чем наивные (0,03% ± 0,05%) в группах доз 20 мкг (1,08% ± 0,65%) (р=0,024) и 50 мкг (1,21% ± 0,73%) (р=0,009), но не в группах доз 10 мкг (0,86% ± 0,31%) (p=0,105) или 30 мкг (0,82% ± 0,46%) (p=0,134) (фиг. 7B). Синтетический консенсусный антиген 1T3 Сурвивин индуцировал антиген-специфические ответы CD4+Т-клеток, которые были значительно более устойчивыми, чем наивные (0,05% ± 0,05%), в группах доз 20 мкг (1,02% ± 0,59%) (р=0,010), 30 мкг (1,08% ± 0,47%) (р=0,006) и 50 мкг (1,13% ± 0,44%) (р=0,004), но не в группе дозы 10 мкг (0,62% ± 0,35%) (р=0,248) (фиг. 7E). Цитокиновый профиль CD4+Т-клеток, специфических к синтетическому консенсусному антигену Сурвивин, был одинаковым для обеих конструкций в разных группах доз и включал в основном IFNγ+IL-2+TNFα +, IFNγ+IL-2-TNFα+или IFNγ+IL-2-TNFα-клетки (фиг. 7G, фиг. 7H). Частота антигенспецифических CD4+ Т-клеток более подробно описана в таблице 6.
Таблица 6. Ответы CD4+ клеток, индуцированные синтетическим консенсусным антигеном 1 Сурвивина и синтетическим консенсусным антигеном 1T3 Сурвивина.
ция
ция
[00229] Не было значимого различия в частоте антиген-специфических CD8+Т-клеток, индуцированных синтетическим консенсусным антигеном 1 Сурвивина (p=0,117) (фиг. 7C). Сурвивин 1T3 действительно индуцировал значительно более высокую частоту антиген-специфических CD8+T-клеток между группами доз (p=0,043). Частота антиген-специфических CD8+Т-ответов в группах, иммунизированных 10 мкг (0,15% ± 0,09%) (р=0,919), 20 мкг (0,27% ± 0,21%) (р=0,274) или 30 мкг (0,25% ± 0,14%) (р=0,377) pGX1429 не достигла статистической значимости по сравнению с наивным (0,07% ± 0,01%). Частота специфических для Сурвивина 1T3 CD8+Т-клеток достигла статистической значимости (0,36% ± 0,21%) (р=0,051) в группе, иммунизированной 50 мкг pGX1429 (фиг. 7F). Как синтетический консенсусный антиген 1 Сурвивина, так и синтетический консенсусный антиген 1T3 Сурвивина индуцировали ответы CD8+Т-клеток сходные по величине и фенотипу. Антигенспецифическими CD8+Т-клетками были в основном IFNγ+IL-2-TNFα-, IFNγ+IL-2-TNFα + (фиг. 7G, фиг. 7H). Частота антигенспецифических CD8+ Т-клеток более подробно описана в таблице 7.
Таблица 7. Ответы CD8+ клеток, индуцированные синтетическим консенсусным антигеном 1 Сурвивина и синтетическим консенсусным антигеном 1T3 Сурвивина
между группами p=0,117
[00230] Приблизительно 25% цитокин-позитивных CD4+T-клеток, индуцированных синтетическим консенсусным антигеном 1 Сурвивина (фиг. 10A) и синтетическим консенсусным антигеном 1T3 Сурвивина (фиг. 10B), также были позитивными для CD107a, что указывает на некоторый потенциал для опосредованной CD4+T-клетками цитолитической функции. Все дозы синтетического консенсусного антигена 1 Сурвивина индуцировали частоту CD4+CD107a+Т-клеток значительно превышающую наивную (0,01% ± 0,01%). В частности, частота антиген-специфических CD4+CD107a+Т-клеток составляла 0,25% ± 0,08%, 0,36% ± 0,11%, 0,21% ± 0,15% и 0,38% ± 0,13% в гуппах доз 10 мкг (р=0,013), 20 мкг (р <0,001), 30 мкг (р=0,050) и 50 мкг (р <0,001) соответственно (фиг. 10А). Синтетический консенсусный антиген 1T3 Сурвивин индуцировал частоту CD4+CD107a+T-клеток, значительно превышающую наивную (0,01 ± 0,01) во всех группах, кроме группы с дозой 10 мкг (0,18% ± 0,09%) (p=0,147). Частота антигенспецифических CD4+CD107a+Т-клеток составила 0,24% ± 0,12%, 0,27% ± 0,12% и 0,29% ± 0,16% в группах доз 20 мкг (р=0,030), 30 мкг (р=0,010) и 50 мкг (р=0,004) соответственно (фиг. 10В). Частота антигенспецифических CD4+ Т-клеток с цитолитическим потенциалом более подробно описана в таблице 8.
Таблица 8. Цитолитический потенциал антигенспецифических CD4+Т-клеток, индуцированных синтетическим консенсусным антигеном Сурвивин 1 и синтетическим консенсусным антигеном Сурвивин 1T3
[00231] Подобно величине антигенспецифических CD8+T-клеток, синтетический консенсусный антиген 1 Сурвивина не вызывал значительного изменения частоты CD8+CD107a+T-клеток среди всех групп (p=0,101) (фиг. 10C). Синтетический консенсусный антиген 1T3 Сурвивина действительно вызывал значительное изменение частоты CD8+CD107a+T-клеток между всеми группами доз (p=0,034) (фиг. 10D). Частота антигенспецифических CD8+CD107a+T-клеток значительно увеличилась выше наивных (0,03 ± 0,01) в группе, иммунизированной 50 мкг pGX1429 (0,28% ± 0,22%) (p=0,026), но не в группах, иммунизированных 10 мкг (0,11% ± 0,08%) (р=0,813), 20 мкг (0,16% ± 0,11%) (р=0,450), 30 мкг (0,16% ± 0,07%) (р=0,424) синтетического консенсусного антигена 1T3 Сурвивина. Цитокиновый профиль CD8+CD107a+Т-клеток, специфических к синтетическому консенсусному антигену Сурвивина был одинаковым для обеих конструкций в разных группах доз и включал в основном IFNγ+IL-2-TNFα +, IFNγ+IL-2-TNFα- (фиг. 10E, фиг. 10F). Частота антигенспецифических CD8+ Т-клеток с цитолитическим потенциалом более подробно описана в таблице 9.
Таблица 9. Цитолитический потенциал антигенспецифических CD8+Т-клеток, индуцированных синтетическим консенсусным антигеном Сурвивин 1 и синтетическим консенсусным антигеном Сурвивин 1T3
между группами p=0,101
Ширина ответов IFNγ, индуцированных конструкциями синтетического консенсусного антигена Сурвивина
[00232] Ширину ответов IFNγ на Сурвивин, индуцированных pGX1428 и pGX1429, исследовали путем картирования эпитопов с использованием подхода матричного пептидного пула (фиг. 11A-11D). Были исследованы объединенные лимфоциты селезенки от мышей, иммунизированных наибольшим количеством дозы pGX1428 (n=8) (фиг. 11A) или pGX1429 (n=8) (фиг. 11B).
[00233] Следующие эпитопы синтетического консенсусного антигена 1 Сурвивина присутствовали как в pGX1428, так и в pGX1429:
LPPAWQLFLKDHRISTFKN (SEQ ID NO:5) (матричные пулы 1, 2, 3, 4 и 7)
LKLDRERAKNKIAKETNNK (SEQ ID NO:6) (матричные пулы 1, 2, 3, 4 и 11)
Синтетический консенсусный антиген T3 Сурвивина представлен в pGX1429:
EWLHHFQGLFP (SEQ ID NO:7) (матричные пулы 3, 4 и 7)
[00234] Хотя общая величина клеточных иммунных ответов, индуцированных синтетическим консенсусным антигеном 1 Сурвивина и синтетическим консенсусным антигеном 1T3 Сурвивина, была аналогичной, ответы, индуцированные синтетическим консенсусным антигеном 1T3 Сурвивина (pGX1429) против области синтетического консенсусного антигена 1 Сурвивина (pGX1428) синтетического консенсуса антигена 1T3 Сурвивина был приблизительно вдвое меньше тех, которые индуцировались конструкцией синтетического консенсусного антигена 1 Сурвивина (pGX1428). Картирование эпитопов с помощью IFNγ ELISpot с использованием матричного подхода показало, что обе конструкции синтетического консенсусного антигена Сурвивина генерируют ответы на одни и те же антигенные эпитопы в синтетическом консенсусном антигене 1 Сурвивина, но ответы, обусловленные синтетическим консенсусным антигеном 1T3 Сурвивина против этих эпитопов, имеют более низкую величину. Также было установлено, что в области Т3 имеется уникальный антигенный эпитоп синтетического консенсусного антигена 1T3 Сурвивина.
[00235] Хотя общая величина клеточных иммунных ответов, индуцированных синтетическим консенсусным антигеном 1 Сурвивина (pGX1428) и синтетическим консенсусным антигеном 1T3 Сурвивина (pGX1429), была аналогичной, ответы, индуцированные синтетическим консенсусным антигеном 1T3 Сурвивина (pGX1429) против области синтетического консенсусного антигена 1 Сурвивина синтетического консенсуса антигена 1T3 Сурвивина был приблизительно вдвое меньше тех, которые индуцировались конструкцией синтетического консенсусного антигена 1 Сурвивина (pGX1428). Картирование эпитопов с помощью IFNγ ELISpot с использованием матричного подхода показало, что обе конструкции синтетического консенсусного антигена Сурвивина генерируют ответы на одни и те же антигенные эпитопы как в синтетическом консенсусном антигене 1 Сурвивина, но ответы, обусловленные синтетическим консенсусным антигеном 1T3 Сурвивина против этих эпитопов, имеют более низкую величину. Также, используя этот подход, было установлено, что в области Т3 имеется уникальный антигенный эпитоп синтетического консенсусного антигена 1T3 Сурвивина. Синтетический консенсусный антиген 1T3 Сурвивина также значительно увеличивал частоту антиген-специфических CD8+и CD8+CD107a+T-клеток по сравнению с наивными, тогда как синтетический консенсусный антиген 1 Сурвивина не увеличивал значительно антиген-специфические CD8+T-клетки у мышей. Синтетический консенсусный антиген 1T3 Сурвивина (pGX1429) был выбран для того, чтобы перейти к моновалентному исследованию приматов, не являющихся человеком, на основании его потенциала для дальнейшего расширения спектра клеточных иммунных ответов на Сурвивин по сравнению с pGX1428 у мышей.
Пример 5 - Исследования на приматах, не являющихся человеком, с использованием синтетического консенсусного антигена 1T3 Сурвивина (pGX1429).
[00236] Чтобы исследовать потенциал синтетического консенсусного Сурвивина 1T3 отдельно и в сочетании с низкой и высокой дозой IL-12, восемнадцать взрослых макак-резус, каждая из которых идентифицирована по уникальному номеру NHP ID, были разделены на 3 группы по 6 и иммунизированы pGX1429 следующим образом. Шесть животных иммунизировали с 3,0 мг pGX1429, шесть - 3,0 мг pGX1429 плюс 0,04 мг pGX6006 (opt rh IL-12) в качестве адъюванта и шесть с 3,0 мг pGX1429 плюс 0,20 мг pGX6006 (opt rh IL-12) в качестве адъюванта, что было составлено в SSC в объеме для инъекции 1,0 мл. Инъекции иммунизации вводили на 0, 4, 8 и 12 неделе. Все иммунизации проводились внутримышечно с помощью устройства CELLECTRA® 2000 5P-IM EP в объеме инъекции 1 мл, составленном в стерильном WFI, поочередно в контралатеральные конечности соответственно. Условия EP были следующими: OpBlock 0070 - IM, 0,5 А, 3 импульса, 52 мсек, 0,2 с между импульсами. Иммуногенность сурвивина оценивали на 2, 6, 10 и 14 неделе. Сурвивин-специфические ответы IFN-гамма показаны на фиг. 12 и 13. Гомология между нативным Сурвивином макаки-резус и pGX1429 приведена в таблице 10. Как показано на ФИГ. 13 и 14, повышенные Сурвивин-специфические ответы наблюдались у животных, иммунизированных синтетическим консенсусным антигеном 1T3 Сурвивин плюс 0,20 мг IL-12 в качестве адъюванта.
Выделение PBMC
[00237] Цельную кровь приматов, не являющихся человеком, собирали в пробирки для приготовления клеток с цитратом натрия (CPT CPT's BD Biosciences), содержащие антикоагулянт и гелевый барьер. Перед доставкой в течение ночи цельную кровь центрифугировали вскоре после сбора (в течение 2 часов), чтобы отделить и сконцентрировать PMBC. Эритроциты и нейтрофилы оседают на дно пробирок и удерживаются на месте гелевым барьером. Плазма и лимфоциты остаются выше гелевого барьера. Каждый CPT может содержать приблизительно 8 мл крови и поставляется при комнатной температуре. Пробирки CPT для центрифугирования были подвергнуты обработке для изоляции РВМС. После лизиса эритроцитов аммонийно-хлоридно-калиевым (ACK) буфером жизнеспособные клетки подсчитывали с использованием автоматического счетчика клеток Invitrogen Countess ™ и ресуспендировали в полной культуральной среде (RPMI 1640 с добавлением 10% FBS, антибиотиков и β-меркаптоэтанола). После завершения анализов, как описано в настоящем документе, оставшиеся PBMC замораживали в замораживающей среде (10% DMSO от Sigma в 90% FBS от Seradigm) в криопробирках и долго хранили в жидком азоте.
IFNγ ELISpot
[00238] Чтобы оценить вызванные вакциной антигенспецифические клеточные ответы, анализ ELISpot IFNγ обезьяны проводили в каждый момент времени на изолированных PMBC с использованием набора (MabTech IFNγ ELISpotPro, № 3421M-2APW-10). Вкратце, 96-луночные планшеты, предварительно покрытые антителом против Monkey IFN (mAb MT126L), промывали в PBS и блокировали в течение 2 часов при комнатной температуре с помощью полной культуральной среды (RPMI 1640 с добавлением 10% FBS, антибиотиков и β-меркаптоэтанола) NHP PBMC ресуспендировали в среде R10 (а затем добавляли в трех экземплярах при количестве введенных клеток 2 × 105 клеток на лунку. Был синтезирован набор пептидов (GenScript), каждый из которых содержал 15 аминокислотных остатков, перекрывающихся 11 аминокислотами, представляющими полные белковые последовательности синтетического консенсуса. Эти наборы пептидов ресуспендировали в ДМСО (Sigma) и объединяли в концентрации приблизительно 2 мкг/мл каждого соответствующего пептида в пулы. Все антигенспецифичные объединенные пептиды использовали в разведении 1:100, что приводило к окончательному разведению 1:200 в каждой лунке в сочетании с РВМС. Различия в размерах каждого антигенного белка приводили к образованию 2 пептидных пулов для Сурвивина.
[00239] Анти-CD3 (mAb CD-2 Mabtech) и/или PMA (Sigma) с иономицином (Sigma) использовали в качестве положительного контроля. Полная культуральная среда R10 была использована в качестве отрицательного контроля. Планшеты инкубировали в течение приблизительно 18 часов при 37°С в инкубаторе с 5% CO2. После удаления клеток и добавления конъюгированного с ALP антитела против обезьян IFNγ (MabTech Ab 7-B6-1-ALP) планшеты инкубировали в течение 2 часов при комнатной температуре. Затем сэндвич-иммуноферментный анализ проводили с использованием субстратного раствора BCIP/NBT в соответствии с инструкциями производителя набора (MabTech). Сине-черный окрашенный осадок образует пятна для выявления каждой отдельной клетки, продуцирующей IFNγ. Затем пятна сканируются и подсчитываются анализатором и программным обеспечением CTL ImmunoSpot® (Cellular Technology), а качество контролируется обученным оператором. Ответы IFNγ сообщаются в виде единиц формирования пятен (SFU) на 1×106 PBMC, превышающих SFU в элементе управления только для среды.
Таблица 10. Характеристики синтетического консенсусного антигена 1T3 Сурвивина по сравнению с нативным Сурвивином макаки-резус.
Таблица 11. Конструкция, Антиген, Доза
[00240] Группы 1, 2 и 3 получали следующее:
Группа 1-3,0 мг pGX1429 (Синтетический консенсусный Сурвивин 1T3). Составлено в SSC, 1,0 мл объем для инъекции, IM.
Группа 2-3,0 мг pGX1429 (Синтетический консенсусный Сурвивин 1T3) + 0,04 pGX6006 (opt. rIL-12). Составлено в SSC, 1,0 мл объем для инъекции, IM.
Группа 3-3,0 мг pGX1429 (Синтетический консенсусный Сурвивин 1T3) + 0,20 pGX6006 (opt. rIL-12). Составлено в SSC, 1,0 мл объем для инъекции, IM.
[00241] Все группы были иммунизированы по следующей схеме:
Иммунизация 1 (Неделя 0)
Иммунизация 2 (Неделя 4)
Иммунизация 3 (Неделя 8)
Иммунизация 4 (Неделя 12)
Иммунизация 5 (необязательно)
Results
[00242] Сурвивин-специфические ответы IFNγ показаны на фиг. 12-14 для групп 1-3, соответственно. Результаты показывают ответ в каждый момент времени через 2 недели после введения дозы. В целом, все группы и отдельные животные имели увеличение ответа к концу исследования через 2 недели после введения дозы 4 по сравнению с исходным предварительным сбором крови. Добавление более высокой дозы IL-12 (0,2 мг) приводило к большим и более последовательным ответам в каждый момент времени по сравнению с Сурвивином отдельно или Сурвивином плюс 0,04 мг IL-12. Более высокие ответы уже при PD2 были также отмечены для Сурвивина плюс IL-12 0,2 мг.
[00243] Не было различий ни в одном из физиологических параметров, измеренных вследствие иммунизации, как показано в таблицах 12-14. Не было отмечено существенных различий для эритроцитов, HCT, нейтрофилов, лимфоцитов, моноцитов, эозинофилов (результаты не показаны). Эти значения находятся в ожидаемых пределах для животных этого вида, пола и возраста, подвергающихся аналогичным экспериментальным процедурам. Любые отклонения от заявленных нормальных диапазонов носят спорадический характер, присутствуют только у одного пола и не связаны с уровнями дозы или сроками.
Таблица 12. Оценка физиологических показателей в группе 1
(#6867, 6859, 6892, 6873)
(#6867, 6859, 6892, 6873, 6879)
(#6859)
Примечание: Вне нормального диапазона *
Таблица 13. Оценка физиологических показателей в группе 2
(#6868, 6874, 6880, 6887, 6893)
(#6874, 6868, 6861)
(#6893)
(#6861)
Примечание: Вне нормального диапазона *
Таблица 14. Оценка физиологических показателей в группе 3
(#6894, 6869)
(#6894, 6869)
(#6863)
(#6894)
Примечание: Вне нормального диапазона *
[00244] Для всех групп не было значительного изменения веса в течение исследования (данные не показаны).
[00245] В целом результаты показывают, что синтетический консенсусный Сурвивин, вводимый отдельно, способен вызывать иммунный ответ у 100% NHP. Добавление адъюванта к IL-12 улучшило реакцию, отмеченную для синтетического консенсусного Сурвивина, что привело к намного более раннему, большему ответу PD2, но только с более высокой дозой IL-12.
[00246] Понятно, что вышеприведенное подробное описание и сопровождающие примеры являются просто иллюстративными и не должны рассматриваться как ограничения объема изобретения, которое определяется исключительно прилагаемой формулой изобретения и ее эквивалентами.
[00247] Различные изменения и модификации раскрытых вариантов осуществления будут очевидны для специалистов в данной области техники. Такие изменения и модификации к раскрытым вариантам осуществления, включая без ограничения изменения, относящиеся к химическим структурам, заместителям, производным, промежуточным соединениям, синтезам, композициям, составам или способам применения изобретения, могут быть сделаны без отклонения от его сущности и объема.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> INOVIO PHARMACEUTICALS, INC
YAN, Jian
SLAGER, Anna
GARMAN, Bradley
COOCH, Neil
<120> ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАЦЕЛЕННЫЕ НА СУРВИВИН, И ИХ ПРИМЕНЕНИЯ
<130> 104409.000448 / INO-1004 WO
<150> US 62/598,267
<151> 2017-12-13
<160> 7
<170> PatentIn версии 3.5
<210> 1
<211> 483
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность ДНК pGX1428, кодирующая изоформу 1
синтетического консенсусного Сурвивина
<400> 1
atggattgga cctggattct gttcctggtg gcagcagcaa cccgggtgca ctccggagcc 60
cccacactgc cccctgcctg gcagctgttt ctgaaggacc acaggatctc tacattcaag 120
aactggccct ttctggaggg atgcgcatgt gcacctgaga ggatggcaga ggcaggcttc 180
atccactgcc ctgccgagaa tgagccagat ctggcccagt gcttcttttg ttttaaggag 240
ctggagggct gggagccaga cgatgacccc atcgaggagc acaagaagca cagctccggc 300
gccgccttcc tgtctgtgaa gaagcagttt gaggagctga ccctgagcga gttcctgaag 360
ctggatcggg agagagccaa gaacaagatc gccaaggaga ccaacaacaa gaagaaggag 420
tttgaggaga cagccaagaa ggtgaggtgt gccatcgagc agctggccgc catggactga 480
taa 483
<210> 2
<211> 159
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность pGX1428, кодирующая белок изоформы 1
синтетического консенсусного Сурвивина
<400> 2
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ala Pro Thr Leu Pro Pro Ala Trp Gln Leu Phe Leu Lys
20 25 30
Asp His Arg Ile Ser Thr Phe Lys Asn Trp Pro Phe Leu Glu Gly Cys
35 40 45
Ala Cys Ala Pro Glu Arg Met Ala Glu Ala Gly Phe Ile His Cys Pro
50 55 60
Ala Glu Asn Glu Pro Asp Leu Ala Gln Cys Phe Phe Cys Phe Lys Glu
65 70 75 80
Leu Glu Gly Trp Glu Pro Asp Asp Asp Pro Ile Glu Glu His Lys Lys
85 90 95
His Ser Ser Gly Ala Ala Phe Leu Ser Val Lys Lys Gln Phe Glu Glu
100 105 110
Leu Thr Leu Ser Glu Phe Leu Lys Leu Asp Arg Glu Arg Ala Lys Asn
115 120 125
Lys Ile Ala Lys Glu Thr Asn Asn Lys Lys Lys Glu Phe Glu Glu Thr
130 135 140
Ala Lys Lys Val Arg Cys Ala Ile Glu Gln Leu Ala Ala Met Asp
145 150 155
<210> 3
<211> 696
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК последовательность pGX1429, кодирующая изоформу 1 + укороченную
изоформу 3 синтетического консенсусного Сурвивина
<400> 3
atggattgga catggattct gttcctggtg gcagcagcaa ccagggtgca ctctggagca 60
ccaacactgc cccctgcatg gcagctgttt ctgaaggacc accggatcag caccttcaag 120
aactggcctt ttctggaggg ctgcgcctgt gccccagaga gaatggcaga ggcaggcttc 180
atccactgcc cagccgagaa tgagcctgat ctggcccagt gcttcttttg ttttaaggag 240
ctggagggct gggagcctga cgatgaccca atcgaggagc acaagaagca cagctccgga 300
gcagccttcc tgagcgtgaa gaagcagttt gaggagctga cactgtccga gttcctgaag 360
ctggataggg agcgcgccaa gaacaagatc gccaaggaga ccaacaacaa gaagaaggag 420
tttgaggaga cagccaagaa ggtgcggtgt gcaatcgagc agctggcagc aatggacagg 480
ggaagaaagc ggagatccat gcagaggaag cctaccatca ggcgcaagaa tctgcgcaag 540
ctgcggagaa agtgcgccgt gccatctagc tcctggctgc cctggacaga ggcctctggc 600
tggagctgtc tggtgcccga gtggctgcac cacttccagg gactgtttcc tggagccacc 660
tccctgccag tgggaccact ggccatgtct tgataa 696
<210> 4
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность pGX1429, кодирующая белок изоформы 1 + укороченной
изоформы 3 синтетического консенсусного Сурвивина
<400> 4
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ala Pro Thr Leu Pro Pro Ala Trp Gln Leu Phe Leu Lys
20 25 30
Asp His Arg Ile Ser Thr Phe Lys Asn Trp Pro Phe Leu Glu Gly Cys
35 40 45
Ala Cys Ala Pro Glu Arg Met Ala Glu Ala Gly Phe Ile His Cys Pro
50 55 60
Ala Glu Asn Glu Pro Asp Leu Ala Gln Cys Phe Phe Cys Phe Lys Glu
65 70 75 80
Leu Glu Gly Trp Glu Pro Asp Asp Asp Pro Ile Glu Glu His Lys Lys
85 90 95
His Ser Ser Gly Ala Ala Phe Leu Ser Val Lys Lys Gln Phe Glu Glu
100 105 110
Leu Thr Leu Ser Glu Phe Leu Lys Leu Asp Arg Glu Arg Ala Lys Asn
115 120 125
Lys Ile Ala Lys Glu Thr Asn Asn Lys Lys Lys Glu Phe Glu Glu Thr
130 135 140
Ala Lys Lys Val Arg Cys Ala Ile Glu Gln Leu Ala Ala Met Asp Arg
145 150 155 160
Gly Arg Lys Arg Arg Ser Met Gln Arg Lys Pro Thr Ile Arg Arg Lys
165 170 175
Asn Leu Arg Lys Leu Arg Arg Lys Cys Ala Val Pro Ser Ser Ser Trp
180 185 190
Leu Pro Trp Thr Glu Ala Ser Gly Trp Ser Cys Leu Val Pro Glu Trp
195 200 205
Leu His
210
<210> 5
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> матричные пулы 1, 2, 3, 4 и 7
<400> 5
Leu Pro Pro Ala Trp Gln Leu Phe Leu Lys Asp His Arg Ile Ser Thr
1 5 10 15
Phe Lys Asn
<210> 6
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> матричные пулы 1, 2, 3, 4 и 11
<400> 6
Leu Lys Leu Asp Arg Glu Arg Ala Lys Asn Lys Ile Ala Lys Glu Thr
1 5 10 15
Asn Asn Lys
<210> 7
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> матричные пулы 3, 4 и 7
<400> 7
Glu Trp Leu His His Phe Gln Gly Leu Phe Pro
1 5 10
<210> 8
<211> 232
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность pGX1429 полной длины, кодирующая белок
изоформы 1 + укороченной изоформы 3 синтетического консенсусного
Сурвивина
<400> 8
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ala Pro Thr Leu Pro Pro Ala Trp Gln Leu Phe Leu Lys
20 25 30
Asp His Arg Ile Ser Thr Phe Lys Asn Trp Pro Phe Leu Glu Gly Cys
35 40 45
Ala Cys Ala Pro Glu Arg Met Ala Glu Ala Gly Phe Ile His Cys Pro
50 55 60
Ala Glu Asn Glu Pro Asp Leu Ala Gln Cys Phe Phe Cys Phe Lys Glu
65 70 75 80
Leu Glu Gly Trp Glu Pro Asp Asp Asp Pro Ile Glu Glu His Lys Lys
85 90 95
His Ser Ser Gly Ala Ala Phe Leu Ser Val Lys Lys Gln Phe Glu Glu
100 105 110
Leu Thr Leu Ser Glu Phe Leu Lys Leu Asp Arg Glu Arg Ala Lys Asn
115 120 125
Lys Ile Ala Lys Glu Thr Asn Asn Lys Lys Lys Glu Phe Glu Glu Thr
130 135 140
Ala Lys Lys Val Arg Cys Ala Ile Glu Gln Leu Ala Ala Met Asp Arg
145 150 155 160
Gly Arg Lys Arg Arg Ser Met Gln Arg Lys Pro Thr Ile Arg Arg Lys
165 170 175
Asn Leu Arg Lys Leu Arg Arg Lys Cys Ala Val Pro Ser Ser Ser Trp
180 185 190
Leu Pro Trp Thr Glu Ala Ser Gly Trp Ser Cys Leu Val Pro Glu Trp
195 200 205
Leu His His Phe Gln Gly Leu Phe Pro Gly Ala Thr Ser Leu Pro Val
210 215 220
Gly Pro Leu Ala Met Glu Thr Ser
225 230
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАЦЕЛЕННЫЕ НА СУРВИВИН, И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2751253C1 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАЦЕЛЕННЫЕ НА BORIS, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2759681C1 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАЦЕЛЕННЫЕ НА BORIS, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2799786C2 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАПРАВЛЕННЫЕ НА LEMD1, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2760984C1 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАПРАВЛЕННЫЕ НА MUC16, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2777918C2 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАПРАВЛЕННЫЕ НА MUC16, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2750689C1 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ, НАЦЕЛЕННЫЕ НА PRAME, И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2748903C1 |
| МЕЗОТЕЛИН-НАЦЕЛЕННЫЕ ВАКЦИНЫ ОТ РАКА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2751252C1 |
| МЕЗОТЕЛИН-НАЦЕЛЕННЫЕ ВАКЦИНЫ ОТ РАКА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2830879C2 |
| ДНК-ВАКЦИНЫ ПРОТИВ ОПУХОЛЕВОГО РОСТА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2004 |
|
RU2343195C2 |
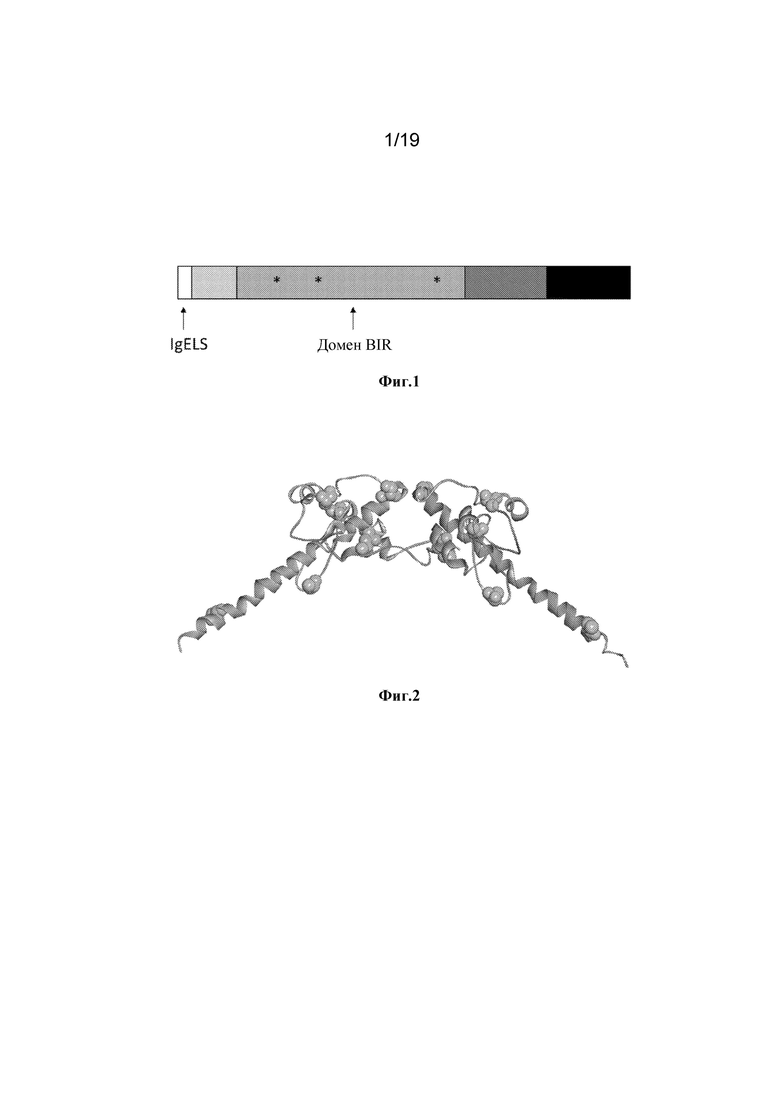
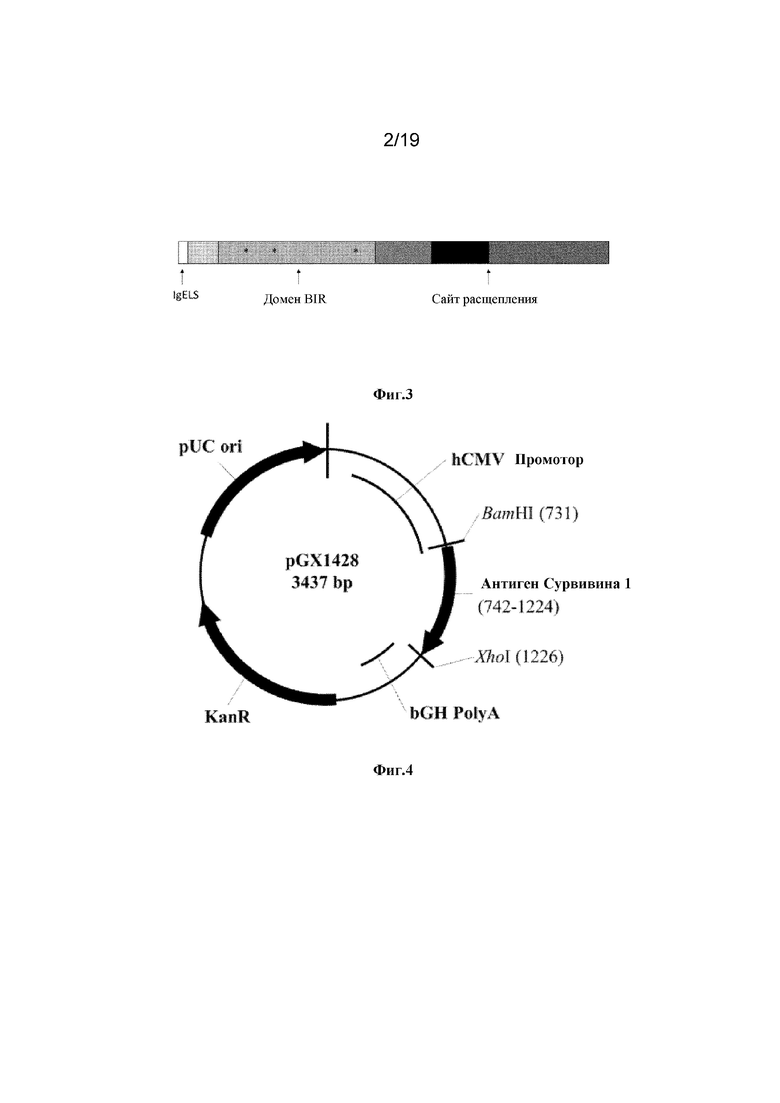
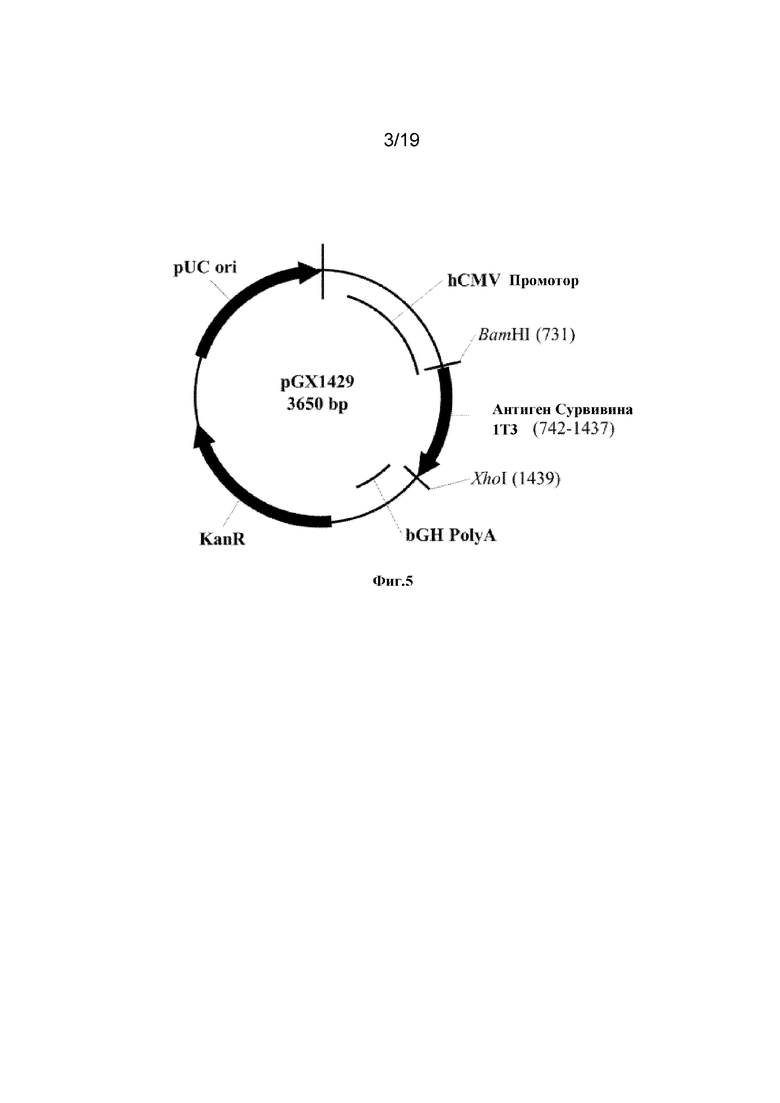
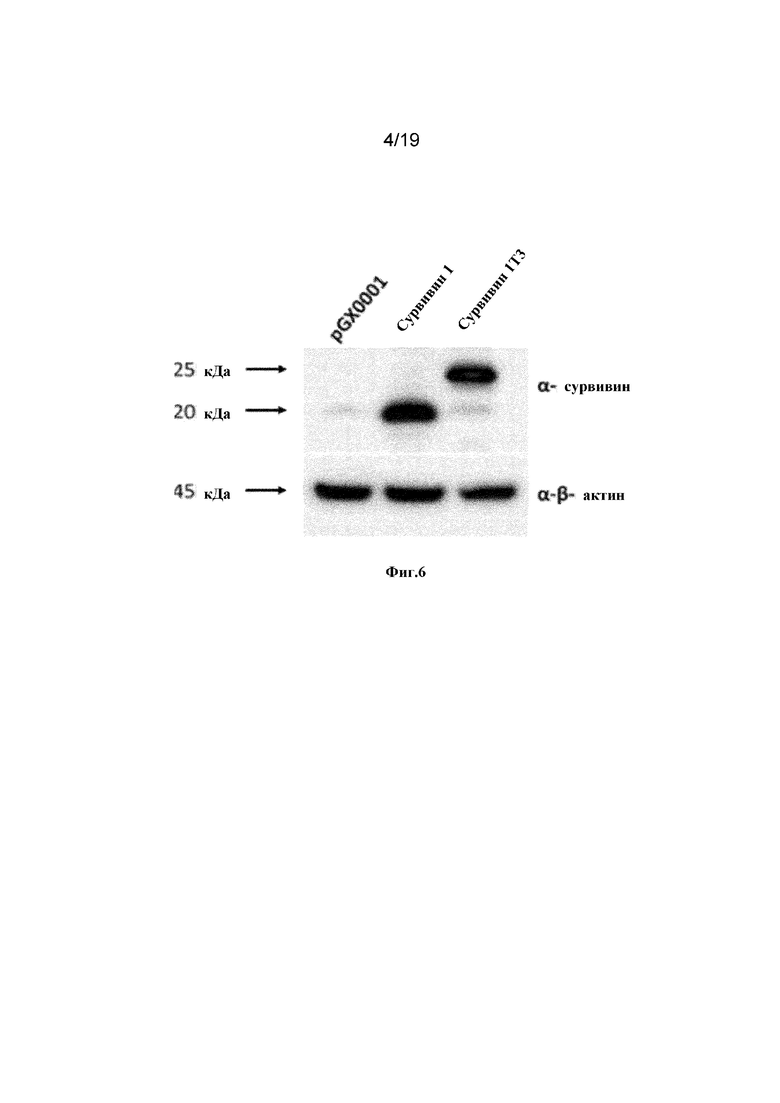
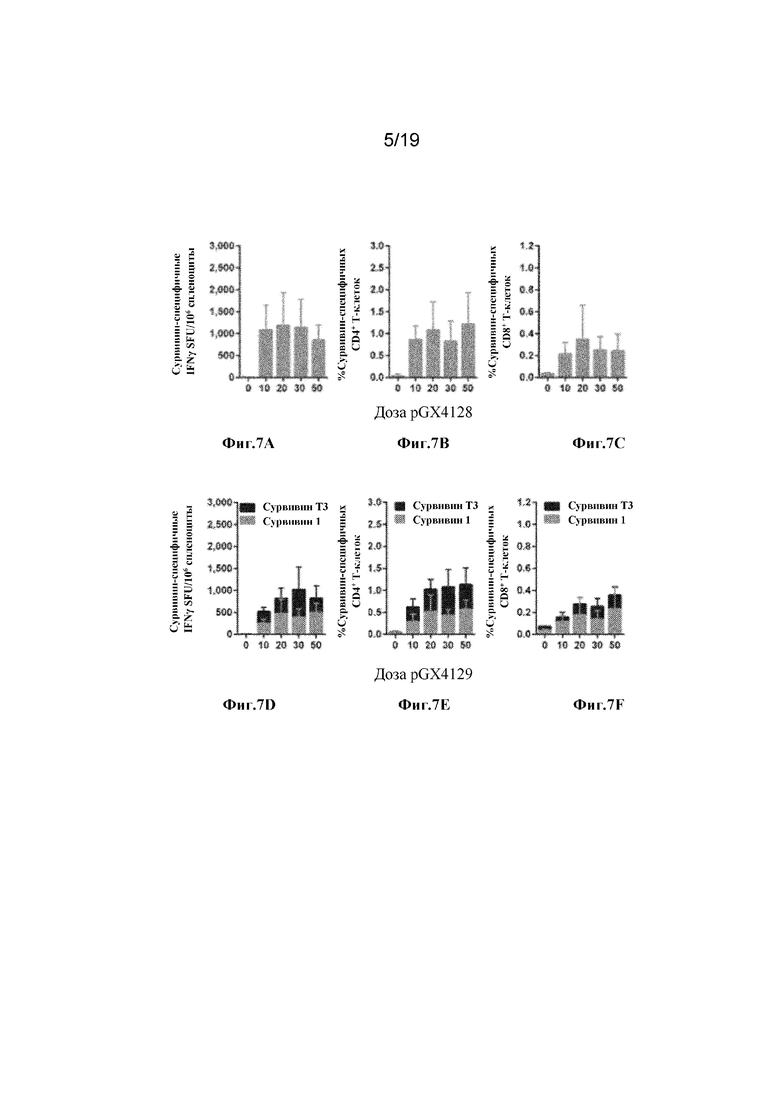

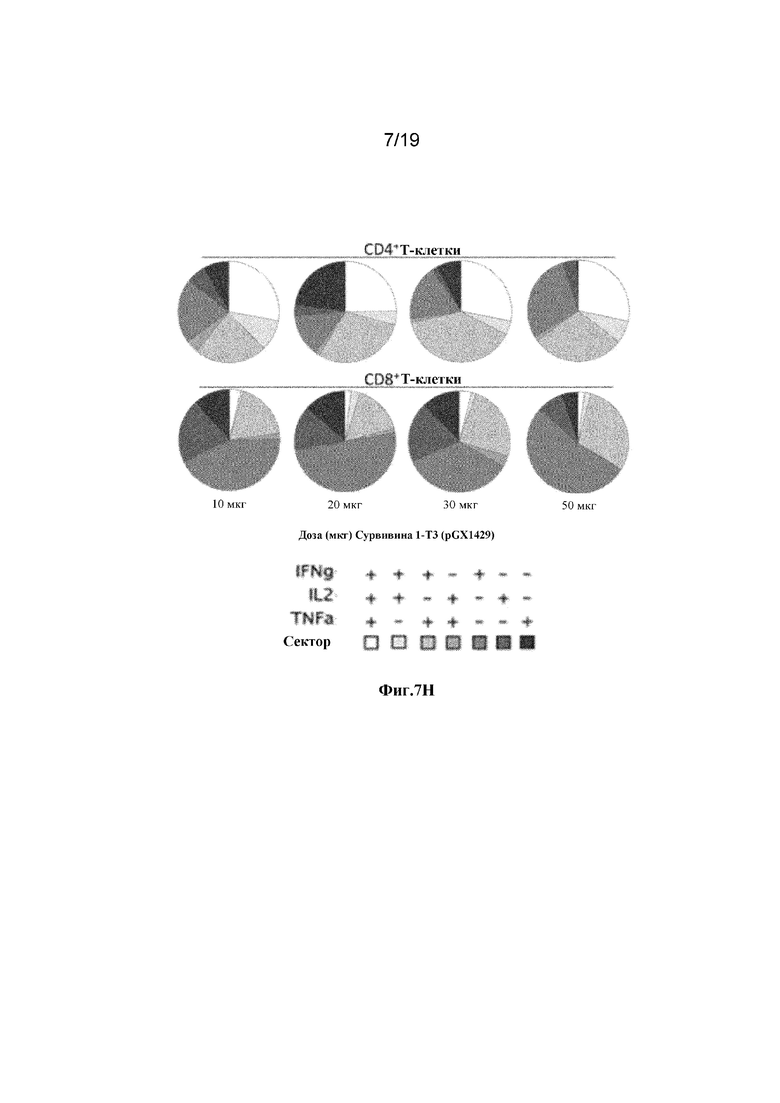
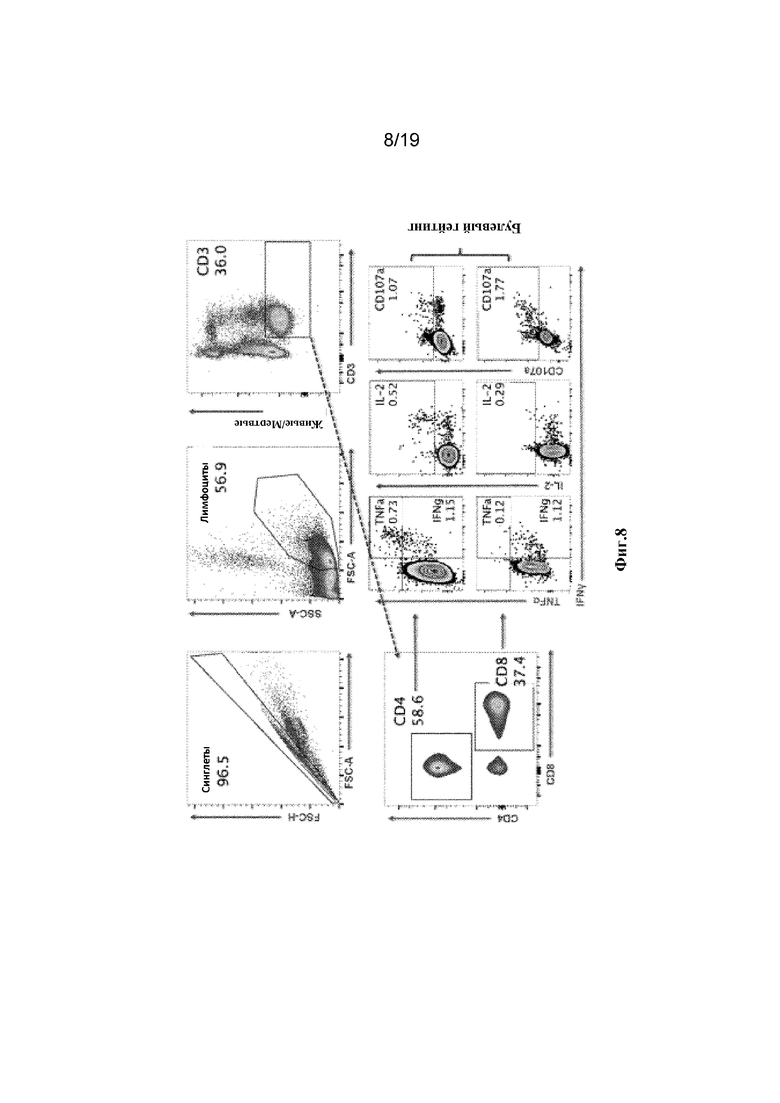
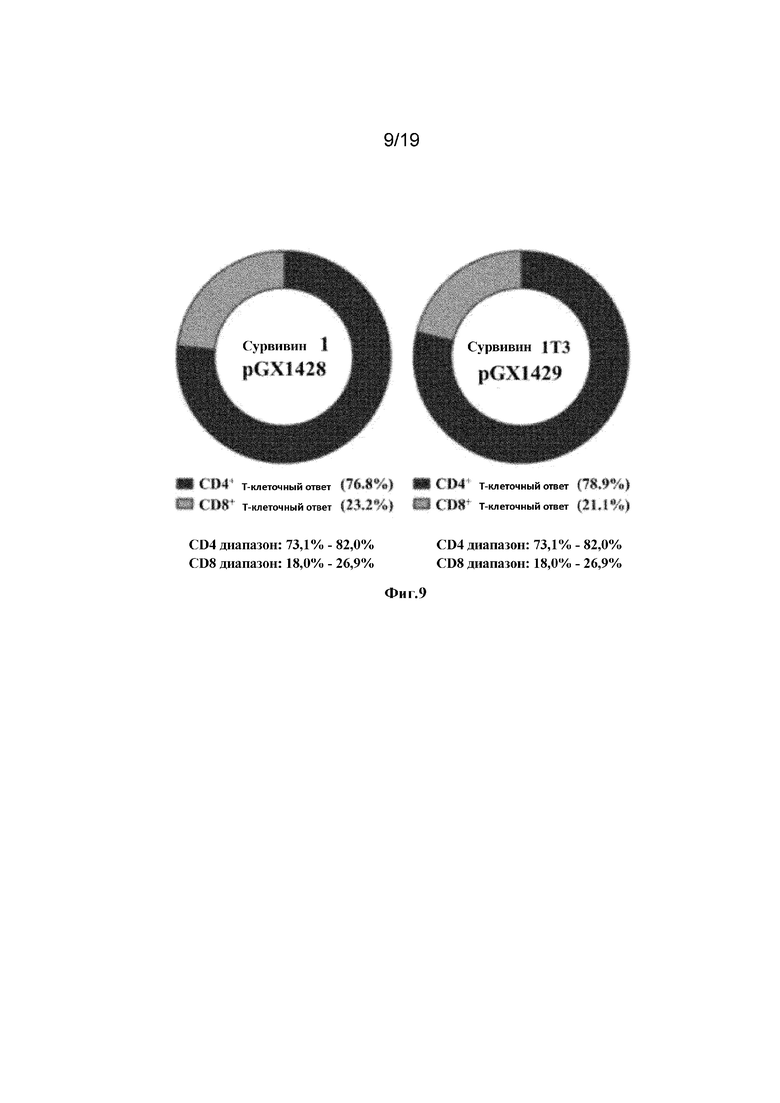



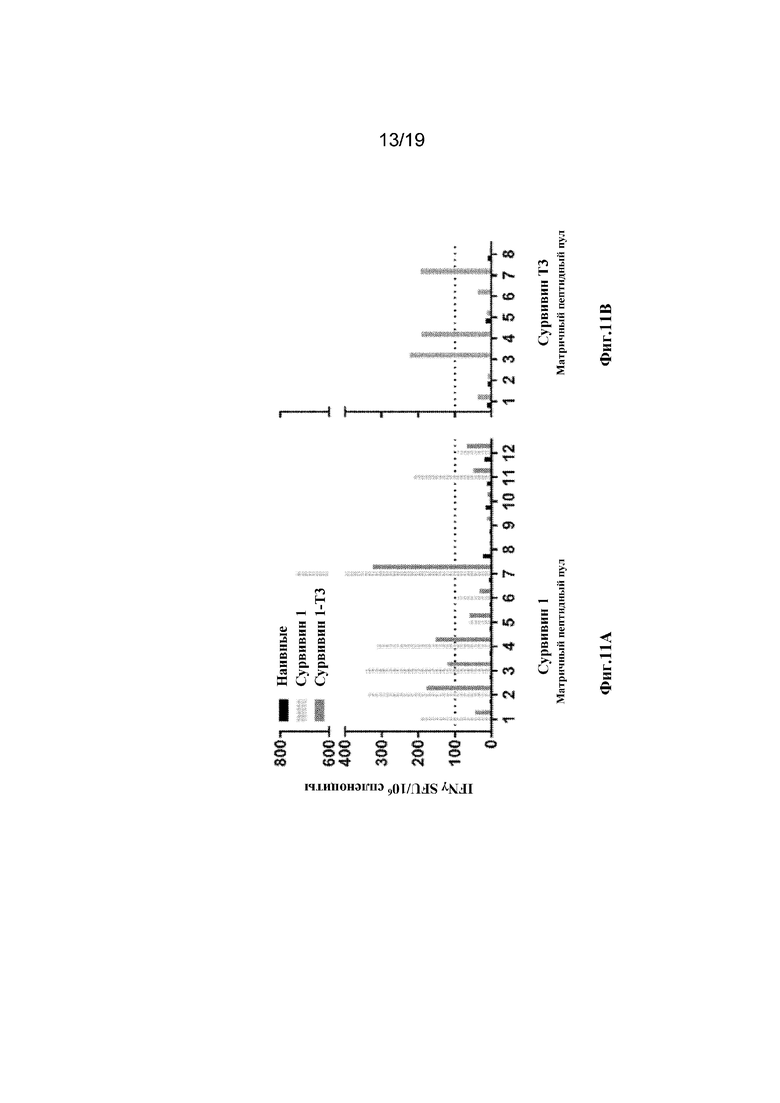

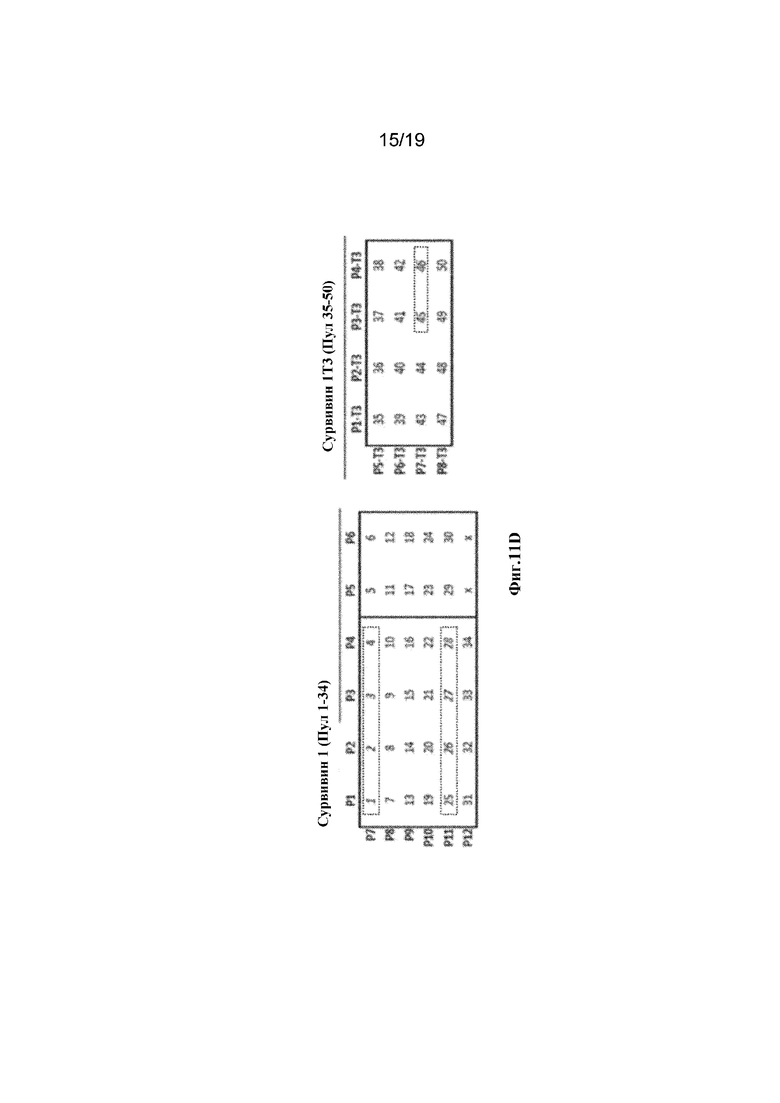
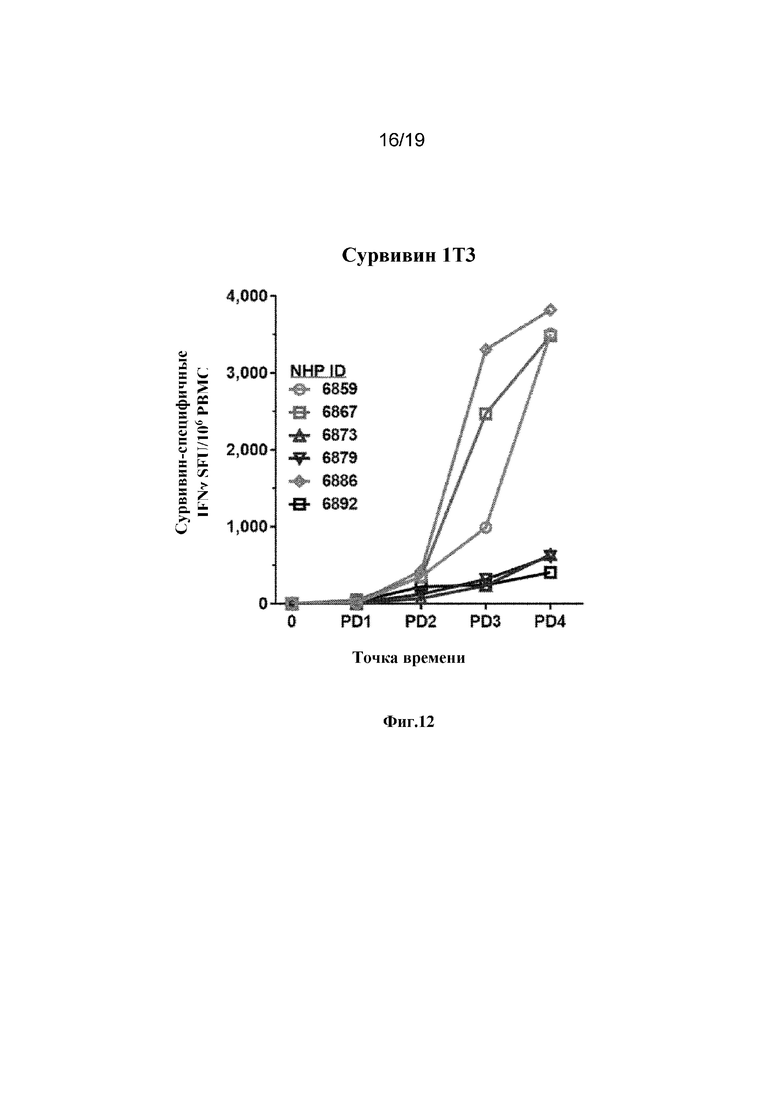
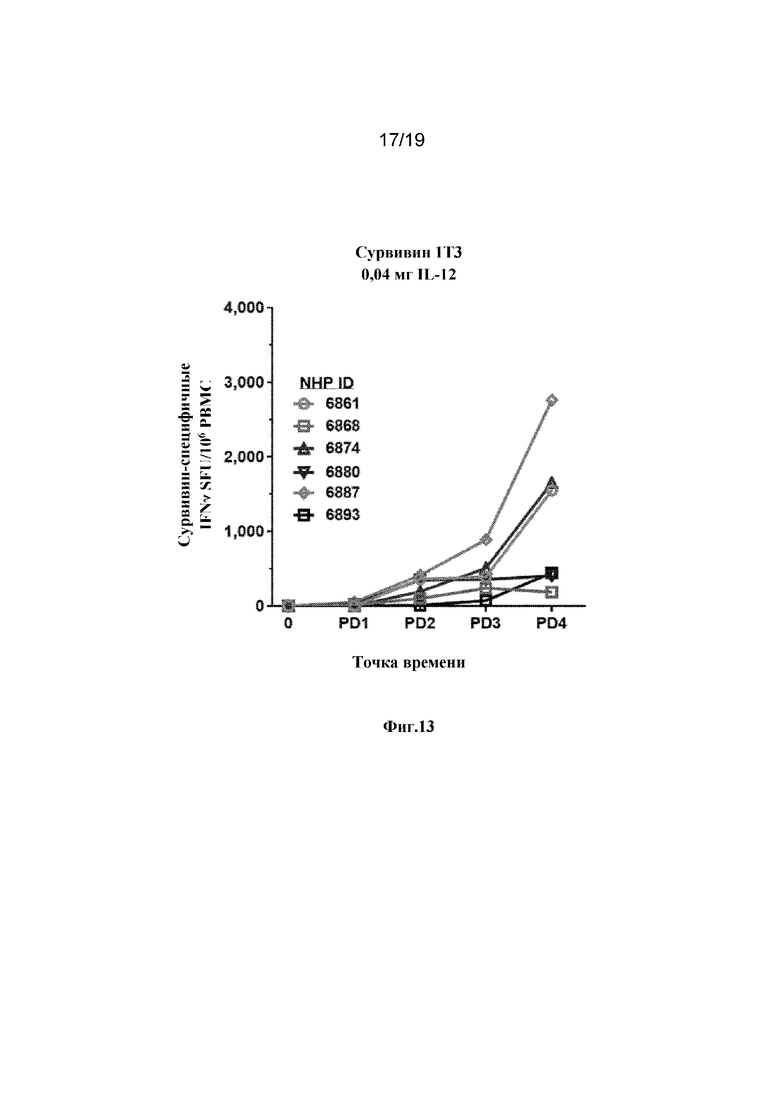
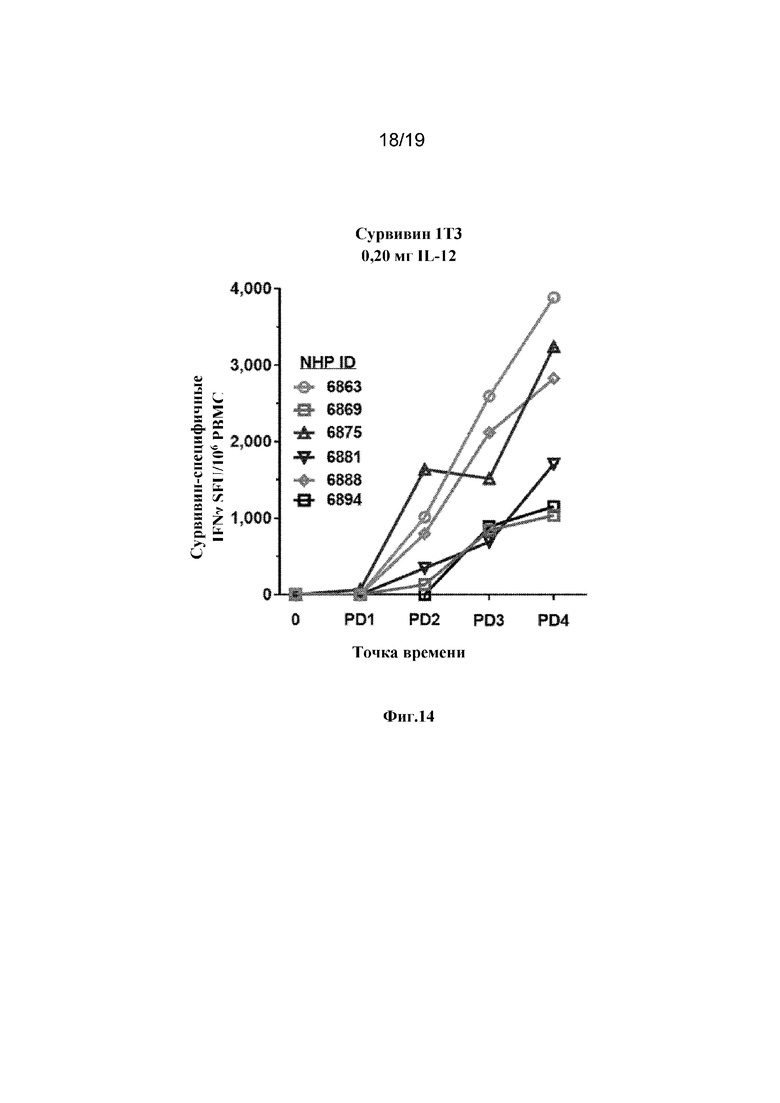
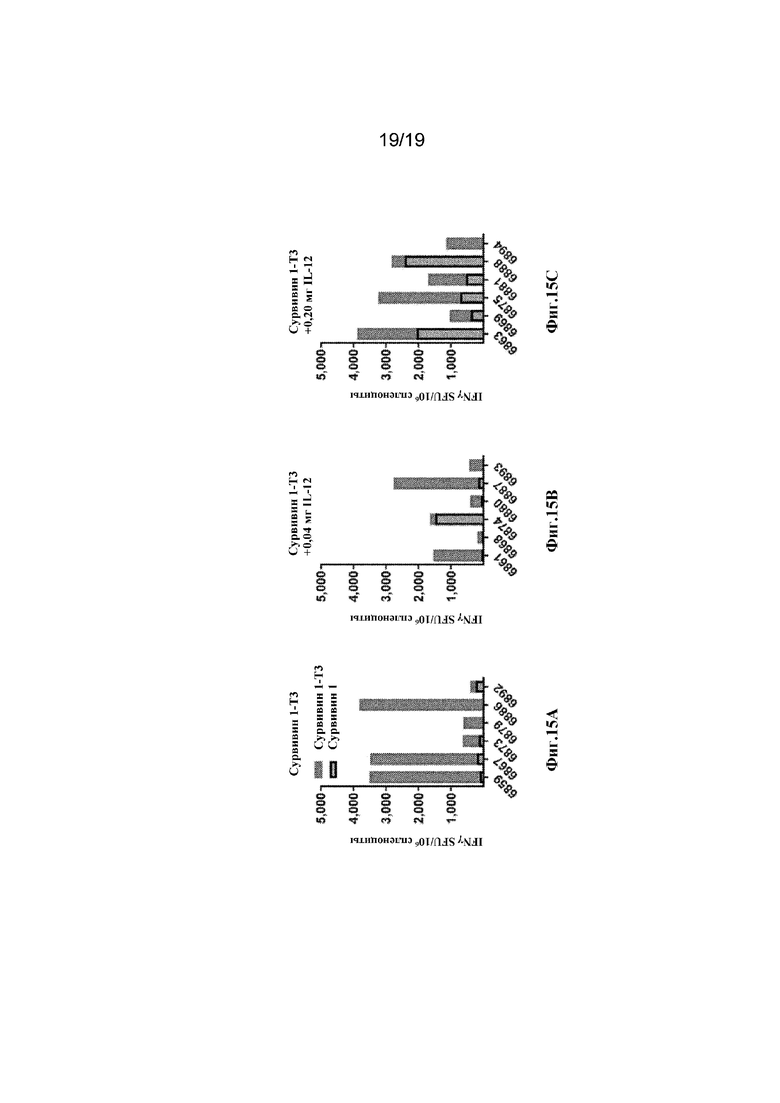
Изобретение относится к биотехнологии. Представлены молекула нуклеиновой кислоты, которая кодирует синтетический консенсусный антиген Сурвивина (варианты), синтетический консенсусный антиген Сурвивина (варианты), экспрессионный вектор, иммуногенная композиция (варианты), вакцина для лечения или предотвращения Сурвивин-экспрессирующего рака, способ лечения субъекта с Сурвивин-экспрессирующей раковой клеткой, способ вакцинации субъекта против Сурвивин-экспрессирующей раковой клетки. Изобретение позволяет получить безопасные и эффективные вакцины и способы их применения для профилактики и/или лечения рака и снижения смертности у субъектов, страдающих от рака. 14 н. и 8 з.п. ф-лы, 14 табл., 32 ил., 5 пр.
1. Молекула нуклеиновой кислоты, которая кодирует синтетический консенсусный антиген Сурвивина, где указанная молекула нуклеиновой кислоты кодирует белок, содержащий SEQ ID NO: 5, SEQ ID NO: 6 и аланин в положениях 51, 65 и 101 по отношению к SEQ ID NO: 2.
2. Молекула нуклеиновой кислоты, которая кодирует синтетический консенсусный антиген Сурвивина, где указанная молекула нуклеиновой кислоты кодирует белок, содержащий SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 и аланин в положениях 51, 65 и 101 по отношению к SEQ ID NO: 8.
3. Синтетический консенсусный антиген Сурвивина, содержащий SEQ ID NO: 5, SEQ ID NO: 6 и аланин в положениях 51, 65 и 101 по отношению к SEQ ID NO: 2.
4. Синтетический консенсусный антиген Сурвивина, содержащий SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 и аланин в положениях 51, 65 и 101 по отношению к SEQ ID NO: 8.
5. Молекула нуклеиновой кислоты, которая кодирует синтетический консенсусный антиген Сурвивина, где указанная молекула нуклеиновой кислоты кодирует белок, содержащий SEQ ID NO: 5 и SEQ ID NO: 6, разделенные аминокислотной последовательностью, соответствующей
WPFLEGCACAPERMAEAGFIHCPAENEPDLAQCFFCFKELEGWEPDDDPIEEHKKHSSGAAFLSVKKQFEELTLSEF.
6. Молекула нуклеиновой кислоты, которая кодирует синтетический консенсусный антиген Сурвивина, где указанная молекула нуклеиновой кислоты кодирует белок, содержащий SEQ ID NO: 5, SEQ ID NO: 6 и SEQ ID NO: 7, где SEQ ID NO: 5 и SEQ ID NO: 6 разделены аминокислотной последовательностью, соответствующей WPFLEGCACAPERMAEAGFIHCPAENEPDLAQCFFCFKELEGWEPDDDPIEEHKKHSSGAAFLSVKKQFEELTLSEF, и SEQ ID NO: 6 и SEQ ID NO: 7 разделены аминокислотной последовательностью, соответствующей EFEETAKKVRCAIEQLAAMDRGRKRRSMQRKPTIRRKNLRKLRRKCAVPSSSWLPWTEASGWSCLVP.
7. Синтетический консенсусный антиген Сурвивина, содержащий SEQ ID NO: 5 и SEQ ID NO: 6, разделенные аминокислотной последовательностью, соответствующей
WPFLEGCACAPERMAEAGFIHCPAENEPDLAQCFFCFKELEGWEPDDDPIEEHKKHSSGAAFLSVKKQFEELTLSEF.
8. Синтетический консенсусный антиген Сурвивина, содержащий SEQ ID NO: 5, SEQ ID NO: 6 и SEQ ID NO: 7, где SEQ ID NO: 5 и SEQ ID NO: 6 разделены аминокислотной последовательностью, соответствующей WPFLEGCACAPERMAEAGFIHCPAENEPDLAQCFFCFKELEGWEPDDDPIEEHKKHSSGAAFLSVKKQFEELTLSEF, и
SEQ ID NO: 6 и SEQ ID NO: 7 разделены аминокислотной последовательностью, соответствующей
EFEETAKKVRCAIEQLAAMDRGRKRRSMQRKPTIRRKNLRKLRRKCAVPSSSWLPWTEASGWSCLVP.
9. Экспрессионный вектор, содержащий молекулу нуклеиновой кислоты по любому из пп.1, 2, 5 или 6.
10. Экспрессионный вектор по п.9, где указанный экспрессионный вектор представляет собой плазмиду.
11. Иммуногенная композиция, содержащая эффективное количество молекулы нуклеиновой кислоты по п.1, 2, 5 или 6 и фармацевтически приемлемый носитель.
12. Иммуногенная композиция, содержащая эффективное количество вектора по п.9 или 10 и фармацевтически приемлемый носитель.
13. Вакцина для лечения или предотвращения Сурвивин-экспрессирующего рака, содержащая эффективное количество вектора по п.9 или 10.
14. Вакцина по п.13, дополнительно содержащая фармацевтически приемлемый наполнитель.
15. Вакцина по п.13 или 14, дополнительно содержащая адъювант.
16. Вакцина по п.15, где адъювант представляет собой IL-12, IL-15, IL-28 или RANTES.
17. Способ лечения субъекта с Сурвивин-экспрессирующей раковой клеткой, включающий введение терапевтически эффективного количества вакцины по любому из пп.13-16.
18. Способ по п.17, где введение включает электропорацию.
19. Способ по п.17, где введение происходит в одном или в более местах у субъекта.
20. Способ вакцинации субъекта против Сурвивин-экспрессирующей раковой клетки, включающий введение количества вакцины по любому из пп.13-16, эффективного для индукции гуморального или клеточного иммунного ответа.
21. Способ по п.20, где введение включает электропорацию.
22. Способ по п.20, где введение происходит в одном или в более местах у субъекта.
| Токарный резец | 1924 |
|
SU2016A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| СЕЛЕДЦОВ В.И | |||
| Ксеновакцино-терапия в лечении злокачественных заболеваний, Сибирский онкологический журнал, 2010, N 3 (39), с 48-57. | |||
Авторы
Даты
2022-07-29—Публикация
2018-12-13—Подача