Изобретение относится к области органической химии и фармацевтики и представляет собой новые соли [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата. Данные соли проявляют фармакологическую активность в отношении функциональных заболеваний желудочно-кишечного тракта.
В клинической практике терапевта, врача общей практики и гастроэнтеролога значительную часть заболеваний составляют функциональные заболевания желудочно-кишечного тракта. Функциональные расстройства кишечника (ФРК) включают группу гетерогенных клинических состояний, которые проявляются симптомами со стороны среднего и нижнего отделов желудочно-кишечного тракта и не сопровождаются какими-либо структурными, системными либо метаболическими изменениями. Несмотря на отсутствие органической основы, функциональные заболевания снижают качество жизни пациентов и наносят большой экономический ущерб обществу как по прямым показателям затрат на медицинское обслуживание и лечение, так и по непрямым показателям, включающим компенсацию временной нетрудоспособности.
Функциональные заболевания органов желудочно-кишечного тракта (в соответствии с Римскими критериями IV) включают:
1. расстройства функции пищевода: функциональная загрудинная боль пищеводного происхождения, функциональная изжога, гиперсенситивный пищевод, ком в пищеводе (Globus), функциональная дисфагия;
2. гастродуоденальные расстройства: функциональная диспепсия, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагия, чрезмерная неспецифическая отрыжка;
3. расстройства, сопровождающиеся тошнотой и рвотой: хронический синдром тошноты и рвоты, синдром циклической рвоты, каннабиноидиндуцированный рвотный синдром, синдром руминации у взрослых;
4. расстройства функции кишечника: синдром раздраженного кишечника (СРК) (в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый), функциональный запор, функциональная диарея, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство, опиоидиндуцированный запор;
5. расстройства центрального генеза, проявляющиеся абдоминальной болью: болевой абдоминальный синдром центрального генеза, опиоидиндуцированная гастроинтестинальная гипералгезия;
6. расстройства функции желчного пузыря и сфинктера Одди: билиарная боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди, функциональное панкреатическое расстройство сфинктера Одди.
Функциональные заболевания органов желудочно-кишечного тракта возникают также на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, билиарного рефлюкс-гастрита и рефлюкс-эзофагита, острых и хронических форм панкреатита: острого панкреатита, идиопатического острого рекуррентного панкреатита, хронического панкреатита, а также состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в т.ч. постхолецистэктомического синдрома, панкреатита после эндоскопической ретроградной холангиопанкреатографии.
Во многих странах, начиная с 1969 г., для лечения функциональных расстройств кишечника, в основном при синдроме раздраженного кишечника (СРК), применяется [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоат. Эффективность [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата для снижения абдоминальной боли была продемонстрирована в различных клинических исследованиях. Длительное время полагали, что влияние [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата связано с его спазмолитической активностью и считали, что этот препарат действует наподобие миотропного спазмолитика мебеверина. Однако позднее были обнаружены новые данные, касающиеся механизма действия [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата, нехарактерные для спазмолитических препаратов. В экспериментальных и клинических исследованиях было показано модулирующее влияние [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата на моторную функцию желудочно-кишечного тракта (ЖКТ), которое проявлялось в его нормализующих эффектах на гипо- и гиперкинетические нарушения моторики ЖКТ при терапевтической и хирургической патологии. [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоат оказывает значительное обезболивающее действие. При проведении экспериментальных исследований выяснилось, что [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоат является агонистом опиатных рецепторов и его модулирующее влияние на моторику ЖКТ и обезболивающий эффект определяются также благодаря этому механизму действия. Действуя на энкефалинергическую систему кишечника, он регулирует перистальтику на всем протяжении ЖКТ.
По своей структуре [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоат является третичным алифатическим амином

Его отличительная особенность - это аномально низкое для третичного алифатического амина значение константы кислотности pKBH+=6.25 [1]. Для сравнения такие распространенные в органическом синтезе основания как триэтиламин и диизопропилэтиламин имеют значения pKBH+=10.87 и 10.75 соответственно. Как следствие данной особенности, [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоат не образует термодинамически стабильные твердые соли со многими органическими кислотами. Так, известно, что стабильных солей с [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоатом не образуют такие кислоты как уксусная и бензойная [2]. Таким, образом, получение новых солей этого соединения является сложной задачей. Одна из основных известных лекарственных форм [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата это его соль с малеиновой кислотой: [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата малеат.

Авторами настоящего изобретения были получены новые соединения общей структурной формулы I

где R1, R2 представляют собой H, Cl, Br, при этом хотя бы один из R1, R2 является Cl или Br.
Также настоящее соединение относится к Е-изомерам соединения общей формулы I.
Также настоящее соединение относится к Z-изомерам соединения общей формулы I.
Данные соли получаются при взаимодействии [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата и соответствующей галоген- или дигалоген-замещенной 4-оксо-4-(2,4,5-триэтоксифенил)-бут-2-еновой кислоты.
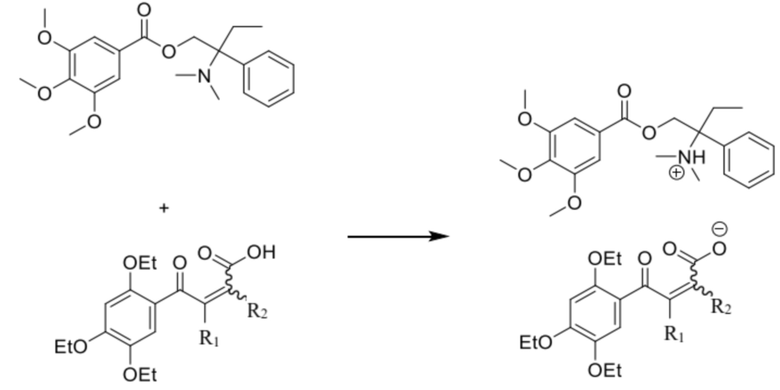 ,
,
где R1, R2 представляют собой H, Cl, Br, при этом по меньшей мере один из R1, R2 является Cl или Br.
Техническим результатом заявленного изобретения является получение новых стабильных соединений общей формулы (I), обладающих улучшенной фармакологической активностью, что обеспечивается повышенной степенью и скоростью абсорбции при снижении скорости элиминации и экскреции.
Данные соли получают классической реакцией ионного обмена при взаимодействии основания [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата с соответствующей галоген- или дигалоген-замещенной 4-оксо-4-(2,4,5-триэтоксифенил)-бут-2-еновой кислотой [3].
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя новое соединение общей формулы (I) и по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, дезинтегранты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгицгиды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также иные фармацевтически приемлемые поверхностно-активные вещества, и смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как бензиловый спирт, уротропин, этилендиаминтетрауксусная кислота, бензойная кислота, хлорбутанол, сорбиновая кислота, парабены, алкилпиридиний, бензетоний и их фармацевтически приемлемые соли и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, таких как гидрофильные полимерные замедлители высвобождения, например, производные целлюлозы, полиэтиленоксид, желатин, поливиниловый спирт, поливинилпирролидон, альгинаты, карбомеры, гидрофобные замедлители высвобождения, такие как глицерилбегенат, моностеарат алюминия. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, буферные растворы, а также их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры (такие как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Для регулирования pH могут быть использованы различные органические и неорганические кислоты, такие как яблочная, аскорбиновая, лимонная, уксусная, янтарная, винная, фумаровая, молочная, аспарагиновая, глутаровая, глутаминовая, сорбиновая кислоты. Примерами диспергирующих агентов и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, коллоидный диоксид кремния, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы, эликсиры или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или получены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные [4]. Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с действующим веществом по настоящему изобретению или его фармацевтически приемлемой солью может включать и другие активные субстанции, в том числе обладающие активностью, при условии, что они не вызывают нежелательных эффектов.
Термин «эффективное количество» означает количество действующего вещества, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает наступление одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании.
Термин «фармацевтически приемлемый» означает, что данное вещество или композиция, в отношении которых применяется этот термин, должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и безопасны для того, кого лечат этим веществом или композицией.
Термины «содержащий», «содержит» означает, что указанные комбинации, композиции и наборы включают перечисленные компоненты, но не исключают включение других компонентов.
«Стабильность» представляет собой способность лекарственного средства сохранять в заданных пределах свойства и характеристики качества в течение его срока годности (срока хранения) и периода применения при соблюдении установленных условий хранения. Стабильность лекарственного средства является необходимым условием обеспечения его терапевтического эффекта или отсутствия у него побочных реакций. В зависимости от сохраняемых свойств и характеристик качества различают следующие типы стабильности лекарственных средств: - химическую стабильность, при которой сохраняются химическая целостность и активность действующего вещества в пределах, указанных в спецификации. В том числе включает в себя фотостабильность; - физическую стабильность, при которой сохраняются первоначальные физические свойства лекарственного средства, в том числе внешний вид, вкус, однородность, растворимость, суспендируемость и др.; - микробиологическую стабильность, при которой сохраняются стерильность, или микробиологическая чистота лекарственного средства в соответствии с указанными требованиями, или эффективность входящих в его состав антимикробных консервантов в указанных пределах; - токсикологическую стабильность, при которой не происходит заметного повышения токсичности лекарственного препарата; - терапевтическую стабильность, при которой терапевтический эффект лекарственного препарата остается неизменным. В некоторых случаях стабильность обусловлена меньшей гигроскопичностью соединений.
Раскрытие сущности изобретения
Настоящее изобретение представляет собой Соединения общей формулы (I)
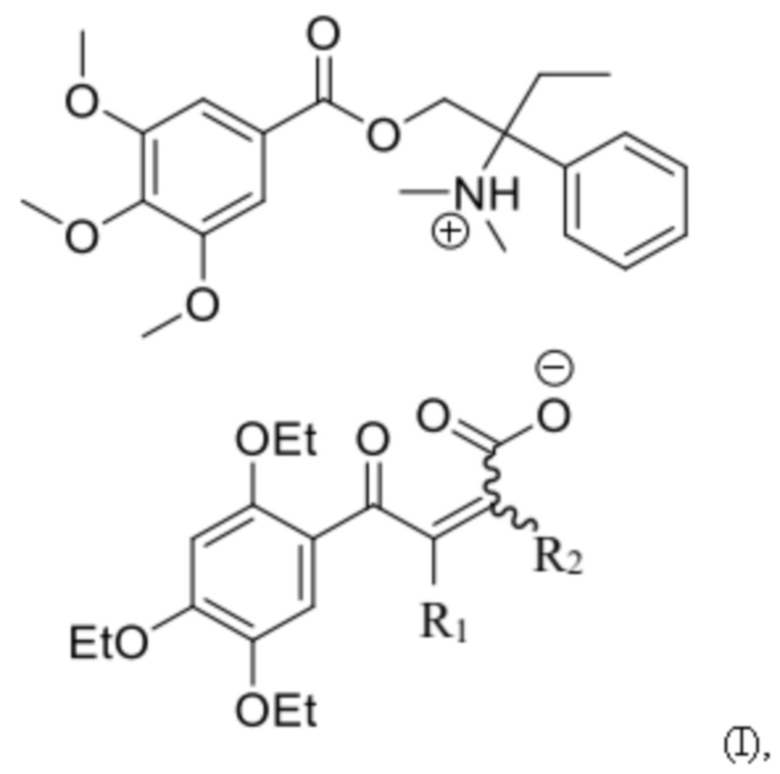
где R1, R2 представляют собой H, Cl, Br, при этом хотя бы один из R1, R2 является Cl или Br.
Также настоящее изобретения относится к Z-изомерам и Е-изомерам соединения общей формулы (I).
Наиболее предпочтительными являются соединения общей формулы (I), представленные в таблице 1.
Таблица 1. Наиболее предпочтительные соединения общей формулы (I) согласно настоящему изобретению.



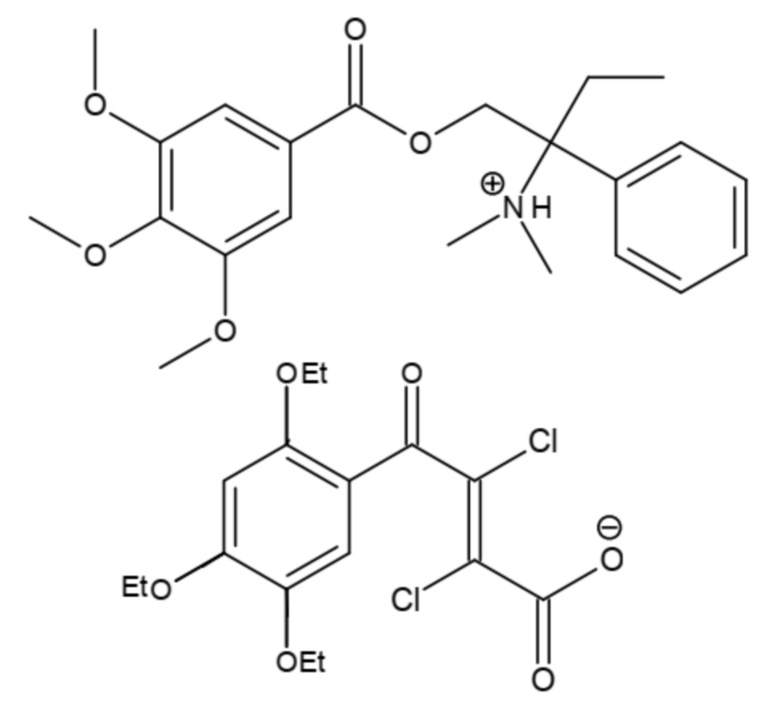

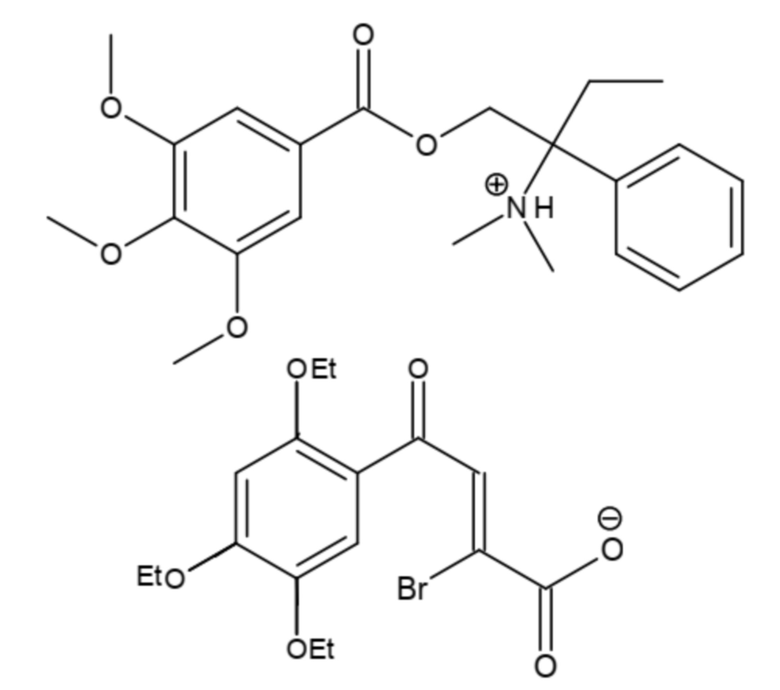
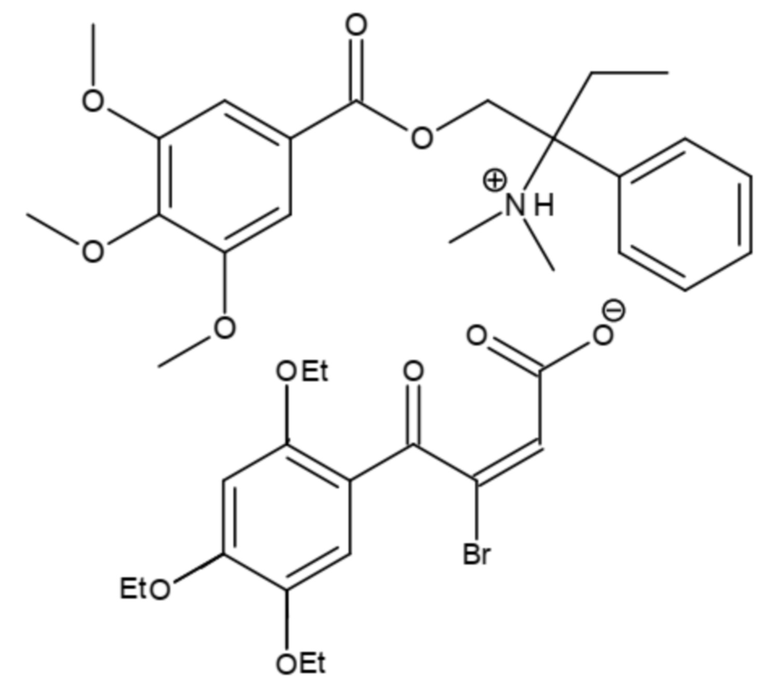





Предметом настоящего изобретения также является фармацевтическая композиция для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта, содержащая эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний, характеризующаяся тем, что функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода: функциональную загрудинную боль пищеводного происхождения, функциональную изжогу, гиперсенситивный пищевод, ком в пищеводе, глобус и/или функциональную дисфагию.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства: функциональную диспепсию, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагию и/или чрезмерную неспецифическую отрыжку.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой: хроническим синдромом тошноты и рвоты, синдромом циклической рвоты, каннабиноидиндуцированным рвотным синдромом и/или синдромом руминации у взрослых.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, в т.ч. сопровождающиеся висцеральной гиперчувствительностью: синдром раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функциональный запор, функциональную диарею, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство и/или опиоидиндуцированный запор.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью: болевым абдоминальным синдромом центрального генеза и/или опиоидиндуцированной гастроинтестинальной гипералгезией.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди: билиарную боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди и/или функциональное панкреатическое расстройство сфинктера Одди.
Более предпочтительной является фармацевтическая композиция для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита и/или состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Предметом настоящего изобретения также является лекарственное средство для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта в форме таблеток или капсул, либо порошка для приготовления суспензии для приема внутрь, помещенных в фармацевтически приемлемую упаковку, причем упомянутое средство содержит в эффективном количестве соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний, характеризующееся тем, что функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода: функциональную загрудинную боль пищеводного происхождения, функциональную изжогу, гиперсенситивный пищевод, ком в пищеводе, глобус и/или функциональную дисфагию.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства: функциональную диспепсию, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагию и/или чрезмерную неспецифическую отрыжку.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой: хроническим синдромом тошноты и рвоты, синдромом циклической рвоты, каннабиноидиндуцированным рвотным синдромом и/или синдромом руминации у взрослых.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, в т.ч. сопровождающиеся висцеральной гиперчувствительностью: синдром раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функциональный запор, функциональную диарею, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство и/или опиоидиндуцированный запор.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью: болевым абдоминальным синдромом центрального генеза и/или опиоидиндуцированной гастроинтестинальной гипералгезией.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди: билиарную боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди и/или функциональное панкреатическое расстройство сфинктера Одди.
Более предпочтительным является лекарственное средство для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита и/или состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Предметом настоящего изобретения также является готовая лекарственная форма для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта в форме таблеток или капсул, помещенных в фармацевтически приемлемую упаковку, причем упомянутая лекарственная форма содержит в эффективном количестве соединение общей формулы I или фармацевтическую композицию, содержащую эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний, характеризующаяся тем, что функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода: функциональную загрудинную боль пищеводного происхождения, функциональную изжогу, гиперсенситивный пищевод, ком в пищеводе, глобус и/или функциональную дисфагию.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства: функциональную диспепсию, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагию и/или чрезмерную неспецифическую отрыжку.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой: хроническим синдромом тошноты и рвоты, синдромом циклической рвоты, каннабиноидиндуцированным рвотным синдромом и/или синдромом руминации у взрослых.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, в т.ч. сопровождающиеся висцеральной гиперчувствительностью: синдром раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функциональный запор, функциональную диарею, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство и/или опиоидиндуцированный запор.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью: болевым абдоминальным синдромом центрального генеза и/или опиоидиндуцированной гастроинтестинальной гипералгезией.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди: билиарную боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди и/или функциональное панкреатическое расстройство сфинктера Одди.
Более предпочтительной является готовая лекарственная форма для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита и/или состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Предметом настоящего изобретения также является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний, характеризующееся тем, что функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода: функциональную загрудинную боль пищеводного происхождения, функциональную изжогу, гиперсенситивный пищевод, ком в пищеводе, глобус и/или функциональную дисфагию.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства: функциональную диспепсию, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагию и/или чрезмерную неспецифическую отрыжку.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой: хроническим синдромом тошноты и рвоты, синдромом циклической рвоты, каннабиноидиндуцированным рвотным синдромом и/или синдромом руминации у взрослых.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, в т.ч. сопровождающиеся висцеральной гиперчувствительностью: синдром раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функциональный запор, функциональную диарею, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство и/или опиоидиндуцированный запор.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью: болевым абдоминальным синдромом центрального генеза и/или опиоидиндуцированной гастроинтестинальной гипералгезией.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди: билиарную боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди и/или функциональное панкреатическое расстройство сфинктера Одди.
Более предпочтительным является применение соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита и/или состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Предметом настоящего изобретения также является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний, характеризующееся тем, что функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода: функциональную загрудинную боль пищеводного происхождения, функциональную изжогу, гиперсенситивный пищевод, ком в пищеводе, глобус и/или функциональную дисфагию.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства: функциональную диспепсию, постпрандиальный дистресс-синдром, синдром эпигастральной боли, расстройства, сопровождающиеся отрыжкой, аэрофагию и/или чрезмерную неспецифическую отрыжку.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой: хроническим синдромом тошноты и рвоты, синдромом циклической рвоты, каннабиноидиндуцированным рвотным синдромом и/или синдромом руминации у взрослых.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, в т.ч. сопровождающиеся висцеральной гиперчувствительностью: синдром раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функциональный запор, функциональную диарею, функциональное вздутие живота, неспецифическое функциональное кишечное расстройство и/или опиоидиндуцированный запор.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью: болевым абдоминальным синдромом центрального генеза и/или опиоидиндуцированной гастроинтестинальной гипералгезией.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди: билиарную боль, функциональные расстройства желчного пузыря, функциональное билиарное расстройство сфинктера Одди и/или функциональное панкреатическое расстройство сфинктера Одди.
Более предпочтительным является применение фармацевтической композиции, содержащей эффективное количество соединения общей формулы I или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний органов желудочно-кишечного тракта, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита и/или состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Предметом настоящего изобретения является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, синдрома раздраженного кишечника (СРК), в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени (включая стеатогепатит с любой стадией фиброза), острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
Более предпочтительным является применение соединения общей формулы I для получения фармацевтической композиции, содержащей эффективное количество соединения общей формулы I и по меньшей мере один фармацевтически приемлемый носитель, лекарственного средства, содержащего соединение формулы I или фармацевтическую композицию, содержащую эффективное количество соединения формулы I и по меньшей мере один фармацевтически приемлемый носитель, или готовой лекарственной формы, содержащей эффективное количество соединения общей формулы I, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе в т.ч. постхолецистэктомического синдрома.
Далее приведены примеры осуществления изобретения, которые иллюстрируют, но не ограничивают изобретение.
Оборудование и реактивы
Химические сдвиги (м.д.) для спектров ЯМР 1Н определяли относительно остаточного сигнала растворителя в спектрах ЯМР 1Н: 2.50 м.д. для ДМСО-d6, 3.31 м.д. для метанола-d4 (CD3OD). Наблюдаемые константы спин-спинового взаимодействия (J, Гц) в протонных спектрах измерены в приближении первого порядка. Мультиплетность сигналов: с (синглет), д (дублет), дд (дублет дублетов), т (триплет), кв (квартет), дкв (дублет квартетов), м (мультиплет) и уш (уширенный).
Полноту протекания реакций, величины Rf и чистоту продуктов контролировали методом ТСХ на пластинах. Детектирование проводилось с помощью УФ лампы. Для разделения смесей методом колоночной хроматографии использовали силикагель (0.060-0.200 mm, 60 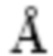 ).
).
Пример 1. Синтез соединений общей формулы (I) (на примере синтеза 2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еноат [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата).
Синтез соединения формулы I представляет собой многостадийный процесс.
(Z)-2,3-Дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еновую кислоту получали в три стадии.
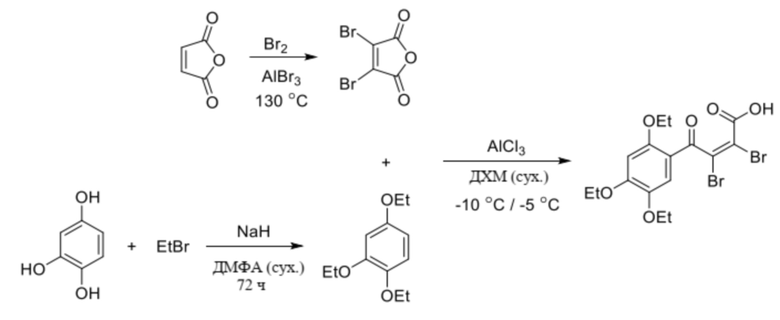
На первой стадии бромированием малеинового ангидрида в присутствие кислоты Льюиса (бромистого алюминия) получали диброммалеиновый ангидрид (3,4-дибромфуран-2,5-дион) [5, 6].

В толстостенную стеклянную ампулу с завинчивающейся крышкой поместили малеиновый ангидрид и AlBr3. После прибавления брома, ампулу плотно закрыли и реакционную смесь перемешивали при 130°С в течение 8 часов. Охлажденную до комнатной температуры ампулу медленно и осторожно открывали. Содержимое ампулы смыли в стакан хлористого метилена. Не растворившийся осадок отфильтровали, фильтрат выдерживали в бане ацетон/сухой лед при -45°С в течение получаса. Образовавшийся осадок - диброммалеиновый ангидрид - быстро отфильтровали и промыли ледяным хлористым метиленом.
В структуре вещества нет протонов, спектр ЯМР для него не снимали.
Параллельно 1,2,4-тригидроксибензол алкилировали этилбромидом [7].

В колбе 1,2,4-тригидроксибензол растворяли в сухом N,N-диметилформамид (ДМФА) и растворы под аргоном охлаждали до 0-4°С в бане лед/вода. Затем порциями прибавляли гидрид натрия в течение 15-20 минут. Не убирая охлаждение, в реакционную смесь прикапывали бромистый этил, следя за тем, чтобы температура не поднималась выше 10°С (примерно в течение получаса). По окончании прикапывания, охлаждение убирали и реакционную смесь перемешивали при комнатной температуре в течение 3-х суток. Затем реакционный раствор выливали в ледяную дистиллированную воду и продукт экстрагировали хлористым метиленом. Органический слой сушили над Na2SO4, фильтровали и наносили на силикагель. Продукт выделяли с помощью колоночной хроматографии - элюент 2% этилацетат в петролейном эфире. Продукт представляет собой желтое масло, кристаллизующееся при стоянии и охлаждении.
1H ЯМР (400 МГц, ДМСО-d6) δ, м.д.: 6.81 (д, J = 8.7 Гц, 1H), 6.51 (д, J = 2.8 Гц, 1H), 6.37 (дд, J = 8.7, 2.9 Гц, 1H), 4.00 - 3.89 (м, 6H), 1.35 - 1.18 (м, 9H). (1Н ЯМР см. в разделе 6.1)
Полученный 1,2,4-триэтоксибензол ацилировали диброммалеиновым ангидридом по реакции Фриделя-Крафтса в присутствии кислоты Льюиса (хлористого алюминия).
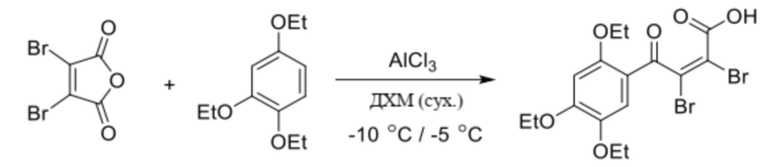
К раствору 3,4-дибромфуран-2,5-диона в сухом хлористом метилене (дихлорметан, ДХМ) под аргоном при охлаждении (-10°С / -5°С) прибавили AlCl3. Далее, не убирая охлаждение, из капельной воронки прибавляли раствор эфира (1,2,4-триэтоксибензола) в течение 20 минут следя за тем, чтобы температура не поднималась выше -5°С. Реакционную смесь перемешивали при -10°С/-5°С еще полчаса и выливали в охлажденный 1M раствор соляной кислоты. Продукт экстрагировали хлористым метиленом. Органический слой сушили над Na2SO4, фильтровали через стеклянный фильтр Шотта и концентрировали на роторном испарителе.
Для выделения конечного продукта, кислоту переводили в натриевую соль. Остаток (красное, частично затвердевшее масло) растворяли в смеси метанола и 5M NaOH. К раствору прибавляли SiO2 и растворитель отгоняли, таким образом, нанеся полученную натриевую соль кислоты на силикагель.
Целевой продукт в виде натриевой соли выделяли с помощью колоночной хроматографии - элюент 5% → 10% метанол в хлористом метилене. Полученную соль в виде желтого масла растворяли в метаноле и полученный раствор по каплям прибавляли к интенсивно перемешиваемой охлажденной 1M HCl. Образовавшийся белый осадок отфильтровывали, промывали водой и сушили в вакуумном сушильном шкафу при 35°С в течение 2-х часов. Полученный продукт ((Z)-2,3-Дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еновую кислоту) дополнительно перекристаллизовывали из смеси петролейный эфир/этил ацетат. Продукт представляет собой крупные прозрачные кубические кристаллы.
1H ЯМР (400 MГц, метанол-d4) δ, м.д.: 7.40 (c, 1H), 6.59 (c, 1H), 4.12 (кв, J = 7.0 Гц, 2H), 4.04 (кв, J = 7.0 Гц, 2H), 3.98 - 3.93 (уш кв, 2H), 1.43 (т, J = 7.0 Гц, 3H), 1.38 (т, J = 7.0 Гц, 3H), 1.32 - 1.29 (уш т, 3H).
Последняя стадия: синтез (Z)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еноат [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата.

Отдельные растворы [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата и (Z)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еновой кислоты в метил-трет-бутиловом эфире (МТБЭ) сливали при перемешивании вместе в один стакан. Через 3-5 секунд перемешивания выпал белый осадок, который отфильтровывали и перекристаллизовывали из смеси метанол-этилацетат. Продукт ((Z)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еноат [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата) представлял собой белое твердое вещество.
1H ЯМР (400 МГц, метанол-d4) δ, м.д.: 7.65 - 7.57 (м, 2H), 7.54 - 7.47 (м,т3H), 7.45 (с, 1H), 7.29 (с, 2H), 6.56 (с, 1H), 5.13 (д, J = 13.2 Гц, 1H), 1H под сигналом воды в районе 4.95 - 4.91 мд, 4.12 (кв, J = 7.0 Гц, 2H), 4.00 (дд, J = 8.0, 6.8 Гц, 4H), 3.85 (с, 3H), 3.83 (с, 6H), 2.67 (с, 6H), 2.44 - 2.29 (м, 1H), 2.28 - 2.19 (м, 1H), 1.41 (дт, J = 8.6, 7.0 Гц, 6H), 1.35 (т, J = 7.0 Гц, 3H), 0.81 (т, J = 7.3 Гц, 3H)
Соединения 3, 5, 7, 9 и 11 получали согласно данной методике с использованием соответствующего галоген- или дигалоген-замещенного малеинового ангидрида.
(E)-2,3-Дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еновую кислоту получали в пять стадий.

Ацетилендикарбоновую кислоту бромировали, пропуская пары брома через ее водный раствор в течение 35 ч. Полученную 1,3-дибромфумаровую кислоту переводили в ее дихлорангидрид под действием PCl5. Последующая обработка 1 экв метанола приводит к образованию метил-2,3-дибромфумароилхлорида. Ацилирование 1,2,4-триэтоксибезола удалось провести с низким выходом в условиях катализа Bi(OTf)3 с образованием метилового эфира кислоты 1E. Последующий щелочной гидролиз и разрушение натриевой соли приводит к образованию целевой кислоты.
Синтез (E)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еноат [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата
Отдельные растворы [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата и (E)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еновой кислоты в метил-трет-бутиловом эфире (МТБЭ) сливали при перемешивании вместе в один стакан. Через 3-5 секунд перемешивания выпал белый осадок, который отфильтровывали и перекристаллизовывали из смеси метанол-этилацетат. Продукт ((E)-2,3-дибром-4-оксо-4-(2,4,5-триэтоксифенил)бут-2-еноат [2-(диметиламино)-2-фенилбутил]-3,4,5-триметоксибензоата) представлял собой белое твердое вещество.
Соединения 4, 6, 8, 10 и 12 получали согласно данной методике.
Примеры, представленные ниже, показывают фармакологическую активность новых соединений общей формулы I.
В табл. 2 представлены группы исследования, сформированные по типу вводимого активного компонента и плацебо.
Все дозировки приведены в пересчете на человека.
Таблица 2. Группы исследования и дозировка активного компонента.
* в качестве плацебо использовали крахмальный раствор
Пример 2. Исследование влияния соединений общей формулы I в модели восприятия висцеральной боли.
Во всех экспериментах использовали 13-недельных самцов мышей линии C57 BL/6. 45 мышей случайным образом распределяли на 9 равных по составу группы (N=5), отличающихся вводимым соединением.
Исследование проводили для 8 соединений. Контролем служила группа мышей, получающих только носитель - крахмальный раствор (группа плацебо).
Колит индуцировали введением 0,1 мл TNBS (тринитробензолсульфонат) (130 мкг/мл в 30% EtOH) в толстую кишку через полиэтиленовый катетер, вставленный на 3 см в анус анестезированных изофлураном мышей. Затем мышей размещали индивидуально и ежедневно наблюдали за изменениями в массе тела, внешнем виде и поведении. Гистологическое исследование структуры слизистой оболочки, клеточного инфильтрата, абсцессов крипт кишечника и бокаловидных клеток подтвердило значительные повреждения, вызванные введением TNBS на 3-й день, а в значительной степени и на 7-й день [8].
Все препараты вводили перорально через 3 дня после введения TNBS и далее один раз в день в течение всего времени исследования.
Для оценки болевого поведения использовали тест с филаментами фон Фрея (возникновение механической аллодинии) на 28-й день после введения TNBS.
Животных помещали в приподнятую над землей акриловую камеру (15х15х15 см) с проволочной сеткой на дне. Перед началом тестирования животных оставляли в камере на 5-10 минут для адаптации. Далее брюшную полость животного стимулировали калиброванными филаментами (или нитями) фон Фрея (BIOSEB, США). Филаменты представляли собой набор из 10 стандартных пластиковых нитей, увеличивающихся в диаметре. Жесткость нитей, выражаемая как минимальное усилие необходимое для сгибания волоска, возрастала при такой калибровке логарифмически с абсолютными значениями от 0,6 граммов до 26 граммов. У каждой мыши порог чувствительности определяли в трех повторах (всего 6 прикладываний с интервалом в 10 секунд для каждого филамента; интервал между последовательным прикладыванием разных филаментов составлял 2 минуты). Кончиком нити прикасались к брюшной поверхности с усилием, необходимым для сгибания волоска, и удерживали волосок в таком положении 6-8 секунд. Положительный ответ регистрировали, если животное резко вздрагивало во время касания. Порог чувствительности определяли по минимальному давлению, вызывающему рефлекторную реакцию вздрагивания (4 раза из 6 прикладываний).
Для каждой группы исследования (n=5) рассчитывали среднюю оценку, полученную в соответствующем тесте, и стандартную ошибку среднего для каждого значения.
Таблица 3. Влияние соединения общей формулы I на поведение мышей в тесте висцеральной боли, вызванной колитом.
* - достоверное отличие эффекта соединения общей формулы I (уровень значимости р<0,05) от плацебо.
В группах, получающих соединение общей формулы I, показатели механической аллодинии значительно снижены, что свидетельствует об эффективности применения соединения по настоящему изобретению для лечения хронической боли в брюшной полости.
Пример 3. Исследование влияния соединения общей формулы I на спазмолитический эффект.
Спазмолитическое действие соединений по настоящему изобретению на желчные пути было исследовано на собаках под наркозом. Исследование проводили на беспородных собаках обоего пола, имеющих массу тела 6-10 кг. 45 животных случайным образом распределяли на 9 равных по составу группы (N=5), отличающихся вводимым соединением. Сформированные группы животных и информация по дозировкам соответственно описаны в таблице 2 выше. Все дозы приведены в пересчете на человека.
Перед экспериментом собаки голодали 24 ч. Животным однократно внутрижелудочно вводили с помощью зонда исследуемый препарат за час до операции, в соответствии с представленными в таблице 2 группами, после чего животных анестезировали пентобарбиталом натрия (30 мг/кг, в/в) с последующими дополнительными инъекциями 10 мг/кг каждые 2 часа. После того, как животное было зафиксировано в положении на спине и трахеотомизировано для интубации трахеи, общий желчный проток, желчный пузырь и часть двенадцатиперстной кишки были обнажены лапаротомией.
Во всех экспериментах параметры, описанные ниже, были записаны на полиграфе одновременно с давлением бедренной артерии, которое регистрировали с помощью датчика давления, соединенного со стеклянной канюлей в бедренной артерии.
Стеклянную канюлю вводили в общий желчный проток как можно ближе к холедоходуоденальному соединению (CDJ). Через эту канюлю CDJ перфузировали физиологическим раствором, нагретым до 37°С при постоянном давлении или постоянной скорости потока. Перфузату позволяли вытекать из двенадцатиперстной кишки через виниловую трубку. Перфузионный поток из флакона в общий желчный проток регистрировали счетчиком капель, помещенным между резервуаром и канюлей. Либо перфузию проводили с постоянной скоростью с помощью инфузионного насоса. В каждом эксперименте подбирали подходящую скорость перфузии в диапазоне 0,5-2,0 мл/мин. Давление перфузии непрерывно регистрировали с помощью датчика давления, помещенного между насосом и канюлей [9].
После удаления желчи из желчного пузыря латексный баллон вводили в желчный пузырь через небольшой разрез на дне и заполняли теплой водой. Давление желчного пузыря доводили до приблизительно 35 см H2O (водяного столба) для анализа расслабляющего эффекта. Давление в желчном пузыре регистрировали с помощью датчика давления.
Таблица 4. Влияние соединений на спазмолитический эффект.
* - достоверное отличие эффекта соединения общей формулы I (уровень значимости р<0,05) от плацебо
Данные эксперимента, представленные в табл. 4, при внутрижелудочном введении соединений по настоящему изобретению показывают снижение сопротивления при прохождении через холедоходуоденальное соединение и снижение давления желчного пузыря, а также увеличение потока желчи. Эти результаты убедительно свидетельствуют о том, что соединения общей формулы I способствуют релаксации желчных путей и подавлению спазма, что обусловливает желчегонный эффект (холерез).
Пример 4. Исследование влияния соединения общей формулы I на функцию сфинктера Одди.
Исследование влияния соединения по настоящему изобретению на функционирование сфинктера Одди было исследовано на собаках под наркозом. Исследование проводили на беспородных собаках обоего пола, имеющих массу тела 6-10 кг. 45 животных случайным образом распределяли на 9 равных по составу группы (N=5), отличающихся дозировкой вводимого состава. Сформированные группы животных и информация по дозировкам соответственно описаны в таблице 2 выше. Все дозы приведены в пересчете на человека.
Животным однократно внутрижелудочно вводили с помощью зонда исследуемый препарат за час до манометрии сфинктера Одди (СОМ), в соответствии с представленными в таблице 2 группами.
Затем выполняли СОМ у голодных собак, перенесших холецистэктомию и установку модифицированных канюль Томаса двенадцатиперстной кишки, центрированных напротив желчного сосочка.
После осторожного обнажения сосочка манометрический катетер глубоко вводили в общий желчный проток. Билиарный катетер медленно выводили через сфинктер до тех пор, пока зона высокого давления (HPZ) не была обнаружена путем мониторинга отслеживания давления, после чего положение фиксировали на время всего исследования. Измеряли давление и частоту сокращений сфинктера Одди [10].
Таблица 5. Влияние соединения общей формулы I на функцию сфинктера Одди.
* - достоверное отличие эффекта соединения общей формулы I (уровень значимости р<0,05) от плацебо
Результаты этого исследования демонстрируют статистически значимую (уровень значимости р<0,05) релаксацию сфинктера Одди с одновременным снижением частоты его сокращений при внутрижелудочном введении соединения общей формулы I в сравнении с плацебо (Табл. 5).
Список литературы
1. Nagasaki, M.; Komori, S.; Ohashi, H. Effect of trimebutine on voltage-activated calcium current in rabbit ileal smooth muscle cells. Br. J. Pharmacol. 1993, 110, 399.
2. Заявка WO 2013/134869 Al.
3. Патент GB 1342547 A.
4. Berge S.M., Bighley L.D., Monkhouse D.C.: «Pharmaceutical Salts» // Journal of Pharmaceutical Sciences, V. 66, № 1, 1977, P. 1-19.
5. P. Nuhn, A. Herrmann and M. Radman, "Synthesis of substituted benzoylacrylic acids as potential inhibitors of phospholipase A2," Pharmazie, vol. 54, no. 2, pp. 93 - 98, 1999.
6. G. Roberge and P. Brassard, "A Convenient Synthesis of Some Highly Functionalized Chromones and Indenones," Synthetic Communications, vol. 9, pp. 129 - 139, 1979.
7. U. H. Hirt, M. F. H. Schuster, A. N. French, O. G. Wiest and T. Wirth, "Chiral hypervalent organo-iodine(III) compounds," European Journal of Organic Chemistry, vol. 8, pp. 1569 - 1579, 2001.
8 de Araujo AD et al. Selenoether oxytocin analogues have analgesic properties in a mouse model of chronic abdominal pain // Nature Communications, 2014, 5, 3165.
9. Hiroshi et al. Biliary spasmolytic action of 3-(2,4,5-trieyjoxybenzoyl)propionic acid (aa-149) in dogs, Europ. J. of Pharm., 1978, v.48, pp.:309-317.
10. Satoh H. et al., Relaxing action of trepibutone (AA-149), Japan. J. Pharmacol., 1981, v.31, pp.:587-592.
Группа изобретений относится к области органической химии и фармацевтики и направлена на лечение функциональных заболеваний желудочно-кишечного тракта. Представлено соединение общей структурной формулы I, где R1, R2 представляют собой H, Cl, Br, при этом хотя бы один из R1, R2 является Cl или Br. Описаны фармацевтическая композиция, содержащая указанное выше соединение, лекарственное средство и готовая лекарственная форма для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта. Кроме того, представлено применение соединения формулы I и фармацевтической композиции для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта, а также для фармацевтической композиции и лекарственного средства. Технический результат: обеспечение эффективного лечения функциональных заболеваний желудочно-кишечного тракта. 9 н. и 49 з.п. ф-лы, 5 табл., 4 пр.
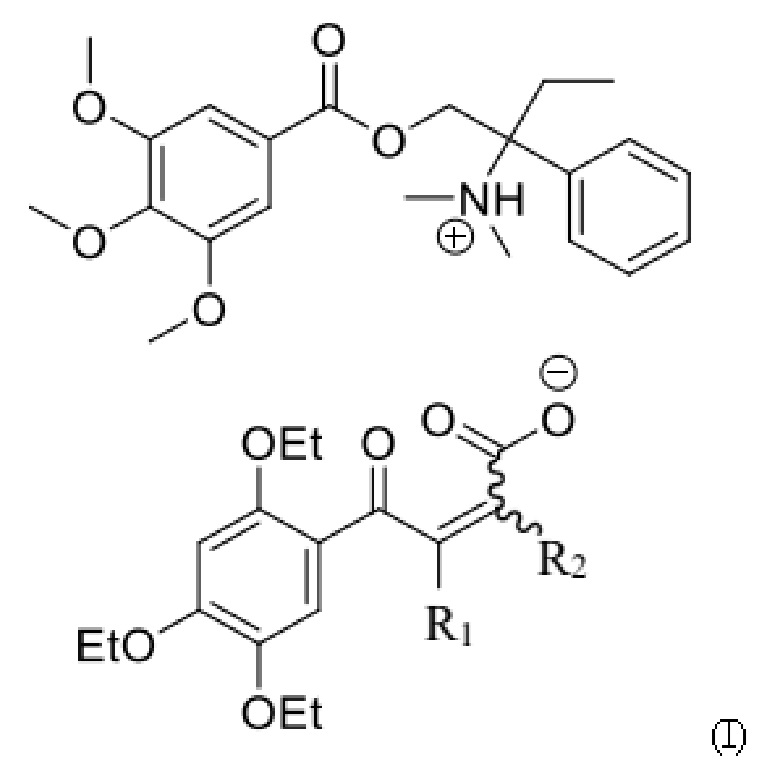
1. Соединение общей формулы I:

где R1, R2 представляют собой Н, Cl, Br, при этом хотя бы один из R1, R2 является Cl или Br.
2. Соединение по п. 1, выбранное из следующих:




3. Фармацевтическая композиция для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта, содержащая эффективное количество соединения по пп. 1, 2 и по меньшей мере один фармацевтически приемлемый носитель.
4. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
5. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
6. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
7. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
8. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
9. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
10. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
11. Фармацевтическая композиция по п. 3, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
12. Лекарственное средство для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта в форме таблеток или капсул, помещенных в фармацевтически приемлемую упаковку, причем упомянутое средство содержит в эффективном количестве соединение по пп. 1, 2 или фармацевтическую композицию по п. 3.
13. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
14. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
15. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
16. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
17. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
18. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
19. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
20. Лекарственное средство по п. 12, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
21. Готовая лекарственная форма для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта в форме таблеток или капсул, порошка для приготовления суспензий, помещенных в фармацевтически приемлемую упаковку, причем упомянутая готовая лекарственная форма содержит в эффективном количестве соединение по пп. 1, 2 или фармацевтическую композицию по п. 3.
22. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
23. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
24. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
25. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
26. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
27. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
28. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
29. Готовая лекарственная форма по п. 21, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
30. Применение соединения по пп. 1, 2 для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
31. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
32. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
33. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
34. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
35. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
36. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
37. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
38. Применение соединения по п. 30, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
39. Применение фармацевтической композиции по п. 3 или готовой лекарственной формы по п. 21 для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
40. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
41. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
42. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
43. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
44. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
45. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
46. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
47. Применение по п. 39, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
48. Применение соединения по пп. 1, 2 для получения фармацевтической композиции по пп. 3-11.
49. Применение соединения по пп. 1, 2 для получения лекарственного средства по пп. 12-20 для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
50. Применение соединения по пп. 1, 2 для получения готовой лекарственной формы по пп. 21-29 для лечения или профилактики функциональных заболеваний желудочно-кишечного тракта.
51. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции пищевода, выбранные из функциональной загрудинной боли пищеводного происхождения, функциональной изжоги, гиперсенситивного пищевода, кома в пищеводе, гобуса и/или функциональной дисфагии.
52. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой гастродуоденальные расстройства, выбранные из функциональной диспепсии, постпрандиального дистресс-синдрома, синдрома эпигастральной боли, расстройства, сопровождающегося отрыжкой, аэрофагии и/или чрезмерной неспецифической отрыжки.
53. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства, сопровождающиеся тошнотой и рвотой, выбранные из хронического синдрома тошноты и рвоты, синдрома циклической рвоты, каннабиноидиндуцированного рвотного синдрома и/или синдрома руминации у взрослых.
54. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции кишечника, выбранные из расстройства функции кишечника, сопровождающиеся висцеральной гиперчувствительностью, СРК, в том числе СРК с преобладанием запора, СРК с преобладанием диареи, СРК, смешанный вариант, СРК неклассифицируемый, функционального запора, функциональной диареи, функционального вздутия живота, неспецифического функционального кишечного расстройства и/или опиоидиндуцированного запора.
55. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства центрального генеза, проявляющиеся абдоминальной болью, выбранные из болевого абдоминального синдрома центрального генеза и/или синдрома опиоидиндуцированной гастроинтеральной гиперплазии.
56. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой расстройства функции желчного пузыря и сфинктера Одди, выбранные из билиарной боли, функциональных расстройств желчного пузыря, функционального билиарного расстройства сфинктера Одди и/или функционального панкреатического расстройства сфинктера Одди.
57. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне желчнокаменной болезни, холецистита, холангита, холестатических заболеваний печени различного генеза, неалкогольной и алкогольной жировой болезни печени, включая стеатогепатит с любой стадией фиброза, острых и хронических форм панкреатита, билиарного рефлюкс-гастрита и рефлюкс-эзофагита.
58. Применение по пп. 48-50, где функциональные заболевания органов желудочно-кишечного тракта представляют собой протекающие как самостоятельно, так и на фоне состояний после оперативных вмешательств на желчном пузыре и желчных путях, поджелудочной железе, в том числе постхолецистэктомического синдрома.
| ПРОИЗВОДНЫЕ 2-АМИНО-2-ФЕНИЛАЛКАНОЛА, ИХ ПОЛУЧЕНИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2009 |
|
RU2486174C2 |
| Комбинация для лечения функциональных заболеваний органов желудочно-кишечного тракта | 2019 |
|
RU2733719C1 |
| RU 2014138619 A, 10.05.2016 | |||
| WO 2016044951 A1, 31.03.2016 | |||
| WO 2019112300 A1, 13.06.2019. | |||
Авторы
Даты
2022-08-02—Публикация
2021-04-22—Подача