Изобретение относится к аналитическим сенсорным системам и может быть использовано для детектирования активных форм кислорода в биологических и иных пробах, а также при проведении хемилюминесцентного иммунологического анализа с повышенной чувствительностью.
На сегодняшний день остро стоит вопрос о поиске быстродействующих, чувствительных и бюджетных сенсоров для ранней диагностики социально-значимых заболеваний, таких как сахарный диабет, инфаркт миокарда и оксидативный стресс организма. Состояние оксидативного стресса характеризуется высокой концентрацией активных форм кислорода (АФК) в организме, которые подавляют систему антиоксидантной защиты человека. Установлено, что АФК токсичны для сперматозоидов и ведут к мужскому бесплодию, а также участвуют во множестве воспалительных процессов. Избыточная концентрация АФК, высвобождаемых клетками иммунной системы, может привести к повреждению клеточных мембран и ДНК, что, в конечном счёте, приводит к гибели клеток и повреждению тканей. Таким образом, быстрое и точное определение концентрации АФК в биологических пробах является важнейшей предпосылкой правильной постановки диагноза и определения стратегии лечения.
Традиционные подходы к анализу и диагностике оксидативного стресса отличаются рядом недостатков, к которым относятся необходимость забора больших объёмов исследуемого материала (аналита), длительная пробоподготовка с использованием флуоресцентных маркеров, а также дороговизна аналитического оборудования. Поэтому разработка новых высокочувствительных, быстродействующих и доступных по стоимости систем для определения оксидативного стресса организма приобретает особое значение.
Ключевым преимуществом хемилюминесцентных (ХЛ) устройств является то, что для их функционирования не нужен ни источник оптического излучения, ни флуоресцентные маркеры. Это обстоятельство существенно упрощает конструкцию приборов, уменьшает их вес и конечную стоимость. Однако эти преимущества не могут быть использованы в полной мере из-за того, что хемилюминофоры, применяемые в биомедицине, имеют низкую эффективность. Причиной низкой эффективности ХЛ является конкуренция безыизлучательных каналов дезактивации возбуждённых в результате химической реакции молекул с процессом излучения света. В этой связи разработка методов повышения эффективности хемилюминофоров и оптимизации процессов сбора и регистрации ХЛ излучения является актуальной задачей.
Для экспресс-диагностики оксидативного стресса как правило используют ёмкости относительно больших (для аналитическо-диагностических приборов) объёмов, например кюветы, микроцентрифужные пробирки типа Эппендорф или культуральные луночные планшеты. Для изучения процессов образования активных форм кислорода в различных жидких средах запатентован малогабаритный прибор «Устройство для анализа люминесценции растворов» (Патент РФ №152424 МПК G01N 21/76, дата приоритета 20.02.2015, опубликован 27.05.2015), имеющее в комплектации блок управления дозатором жидкости. В данном устройстве исследуемое вещество помещают в пробирки микроцентрифужные пробирки с объемом 1.5 мл, что приводит к необходимости отбора больших объемов исследуемого материала.
Известен прибор для регистрации сверхслабых световых потоков «Устройство автоматического хемилюминометра» (Патент РФ №146739, МПК G01N 21/76, дата приоритета 13.03.2014, опубликован 20.10.2014), позволяющий проводить иммунохимические исследования и анализы свободно-радикальных патологий. Предложенное техническое решение позволяет увеличить производительность за счет использования стандартного луночного планшета с количеством проб до 96, однако рабочий объем одной лунки составляет 0.1-0.2 мл, что также приводит к необходимости отбора больших объемов исследуемого материала.
В Патенте «Микроволнововый триггер, индуцирующий металл-усиленную хемилюминесценцию (МТ МУХ), и её пространственный и временной контроль» (Патент USA №9075018 B2, МПК G01N 21/763, G01N 21/76, G01N 33/54306, G01N 33/5438, G01N 33/553, Y10T 436/143333, Y10T 436/144444, Y10T 436/145555, Y10T 436/147777, Y10T 436/201666, Y10T 436/21, Y10T 436/23, дата приоритета 13.02.2006, опубликован 07.07.2015) представлена ХЛ система, предназначенная для визуализации структур и элементов с использованием плазмонного эффекта от металлических поверхностей, визуально наблюдаемое свечение которых вызвано химическими и биологическими реакциями на основе эффекта ХЛ. Контраст в визуализации ХЛ изображений улучшается за счёт использования микроволнового излучения, и дополнительно за счёт использования металлических наноструктур. В данном патенте не проработаны вопросы сравнения интенсивности ХЛ в пробе и референтным образце, что не позволяет использовать его для определения оксидативного стресса.
Способ улучшения предела детектирования молекул аналита описан в патенте «Метод и устройство для хемилюминесцентного анализа» (Патент USA №20190195806 A1, МПК G01N 21/76, B01L 3/5027, G01N 21/05, G01N 33/582, G01N 33/587, G01N 33/725, B01L 2300/0663, B01L 2300/0877, B01L 2300/0883, B01L 2300/123, G01N 2021/0346, дата приоритета 13.02.2016, опубликован 07.07.2015), в котором используются коллоидные растворы серебряных и золотых наночастиц. Для сокращения расхода аналита использован микрофлюидный чип из полидиметилсилоксана (PDMS). Несмотря на заявленную в патенте возможность перехода от миллилитровых объемов аналита к микролитровым, следует отметить, что для поддержания заявленной повышенной чувствительности ХЛ сенсора, работающего в проточном режиме, требуется постоянное добавление коллоидных наночастиц благородных металлов в раствор хемилюминофора.
Известен патент «Люминометр» (Патент РФ №180961 U1, МПК G01N 21/01, G01N 21/76, дата приоритета 14.07.2017, опубликован 02.07.2018), содержащий шарнирно сочленённый корпус, состоящий из верхней и нижней частей, в которых расположены кюветное отделение и электронная система управления, включающая твердотельный фотоумножитель, блок усиления сигналов, блок питания, блок управления, счётчик импульсов, USB-порт, датчик положения верхней части корпуса и аккумуляторную батарею.
Зарегистрировано изобретение «Устройство для анализа хеми- и биолюминесценции жидких сред» (Патент РФ №2452937 С1, МПК G01N 21/76, дата приоритета 15.02.2011, опубликован 10.06.2012) на устройство для анализа ХЛ растворов, содержащее кюветное отделение для исследуемого или референтного образца, нагреватель, ФЭУ, интерфейс, блок управления, электропривод и блок питания, соединенные по электрической цепи и подключенные к персональному компьютеру. Несмотря то, что устройство включает в себя дополнительные вспомогательные объекты (термодатчики, нагреватель и дозаторы), к числу его явных недостатков следует отнести невозможность проводить быстрый сравнительный анализ содержания активных форм кислорода в исследуемых образцах.
В настоящее время для регистрации ХЛ сигнала в стационарных приборах используются различные методы. Однако в портативных приборах в большинстве случаев используются фотоэлектронные умножители (ФЭУ). Как правило, регистрация ХЛ сигнала осуществляется последовательно для каждого образца: сначала определяется интенсивность ХЛ референтного образца с заранее известным содержанием АФК, затем регистрируются сигналы от исследуемых образцов. Этот же подход лежит в основе «Устройства для экспрессного определения концентрации активных форм кислорода в водных растворах» (Патент РФ №162866 U1, МПК G01N 21/76, дата приоритета 30.12.2015, опубликован 27.06.2016), где для проведения серийных измерений используется одна кювета. Основным недостатком приведенного устройства является необходимость постоянного промывания кюветы для записи референтного сигнала ХЛ при условии использования разных исследуемых веществ и компонентов.
Наиболее близким по технической сущности к заявляемому объекту является портативное устройство, описанное в патенте «Микрофлюидное устройство для детектирования хемилюминесценции» (Патент CN №212780531 U, МПК G01N 21/76, B01L 3/00, дата приоритета 01.09.2020, опубликован 23.03.2021). Устройство предназначено для количественного определения биологического потребления кислорода (БПК) в пробе воды в зависимости от концентрации загрязняющих её органических веществ. Принцип работы устройства основан на оптическом эффекте ХЛ молекул люминола, возникающей в каналах микрофлюидного чипа. Устройство включает в себя микрофлюидную систему, насос для ввода с помощью трубок жидкости из емкости с реактивами в виде хемилюминофора, в частности люминола, и исследуемыми образцами, в виде проб воды, в микрофлюидный чип, выходы которого связаны трубками с емкостью для слива, фотоприемник для регистрации ХЛ и микроустройство для контроля температуры. Описанное устройство отличается разделением микрофлюидного чипа на реакционную зону с клапанным каналом Теслы для перемешивания дрожжевой суспензии и пробы воды, а также зону ХЛ со спиралевидным одиночным микроканалом, предназначенную для быстрого перемешивания растворов образца с люминолом и дальнейшего наблюдения генерации ХЛ свечение в присутствие пробы воды. Ввод образца воды происходит одновременно с вводом суспензии дрожжей в реакционном канале при использовании перистальтического насоса с заданной скоростью потока. ХЛ люминола при активации смешанным раствором образца воды с дрожжами регистрируется в режиме реального времени с помощью фотоприемника в виде ФЭУ, расположенного под микрофлюидным чипом. Однако недостатками этого устройства является длительность времени для сравнительного анализа, что в свою очередь не исключает возможности загрязнения микроканалов продуктами реакции контрольного образца, а также отсутствие светонепроницаемого корпуса, что вызывает необходимость проводить регистрацию ХЛ свечения в темной комнате. Это обстоятельство не позволяет получать достоверные данные об интенсивности ХЛ исследуемых проб.
Задачей, на решение которой направлено заявляемое изобретение, является повышение быстродействия и увеличения чувствительности детектирования, а также сокращения расхода объема потребления биологических и иных проб, содержащих АФК. Поставленная задача решается за счет достижения технического результата, заключающегося в кодировании ХЛ излучения, идущего с различных каналов микрофлюидного чипа, путем его поляризации и увеличении его интенсивности. Технический результат достигается за счет того, устройство для хемилюминесцентного анализа содержания активных форм кислорода в биологических и иных пробах, содержит насос для ввода с помощью трубок жидких реактивов из емкостей с хемилюминофором и исследуемыми пробами в микрофлюидный чип, выход которого связан трубкой с емкостью для слива, и фотоприемник, отличается тем, что микрофлюидный чип и фотоприемник помещены в светонепроницаемый корпус, причем микрофлюидный чип выполнен по меньшей мере двухканальным и включает диэлектрическую подложку с нанесенной на нее метаповерхностью из обработанных лазерным излучением металлических наночастиц, обладающих локализованным плазмонным резонансом в спектральной полосе хемилюминесценции используемого хемилюминофора, а в светонепроницаемый корпус также включены два линейных взаимно-ортогонально ориентированных поляризатора, наложенных на различные каналы микрофлюидного чипа, и расположенные друг за другом по ходу распространения излучения вращатель поляризации, выполненный, например, в виде жидкокристаллической твист-ячейки, электрические входы которой подключены к выходам генератора управляющих импульсов напряжения, третий линейный поляризатор излучения, совпадающий по ориентации с одним из линейных поляризаторов, наложенных на микрофлюидный чип, фотоприемник, выполненный с функцией счета фотонов.
Сущность изобретения поясняется фигурами 1-8 и их кратким описанием, указанным ниже.
Фиг. 1. Принципиальная схема устройства для хемилюминесцентного анализа.
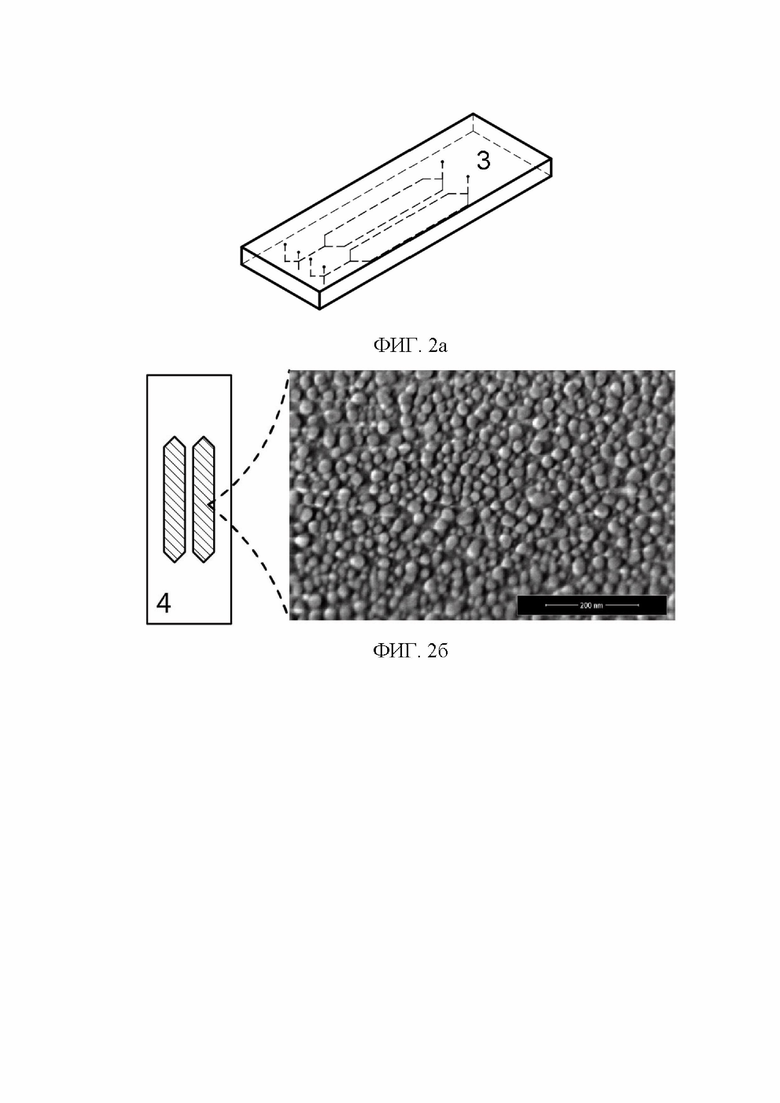
Фиг. 2. Микрофлюидный чип. Гибкая прозрачная полимерная часть из PDMS c двумя микроканалами (а) и диэлектрическая подложка с металлическим покрытием из наночастиц (б). На вставке приведен снимок серебряных наночастиц со сканирующего электронного микроскопа.
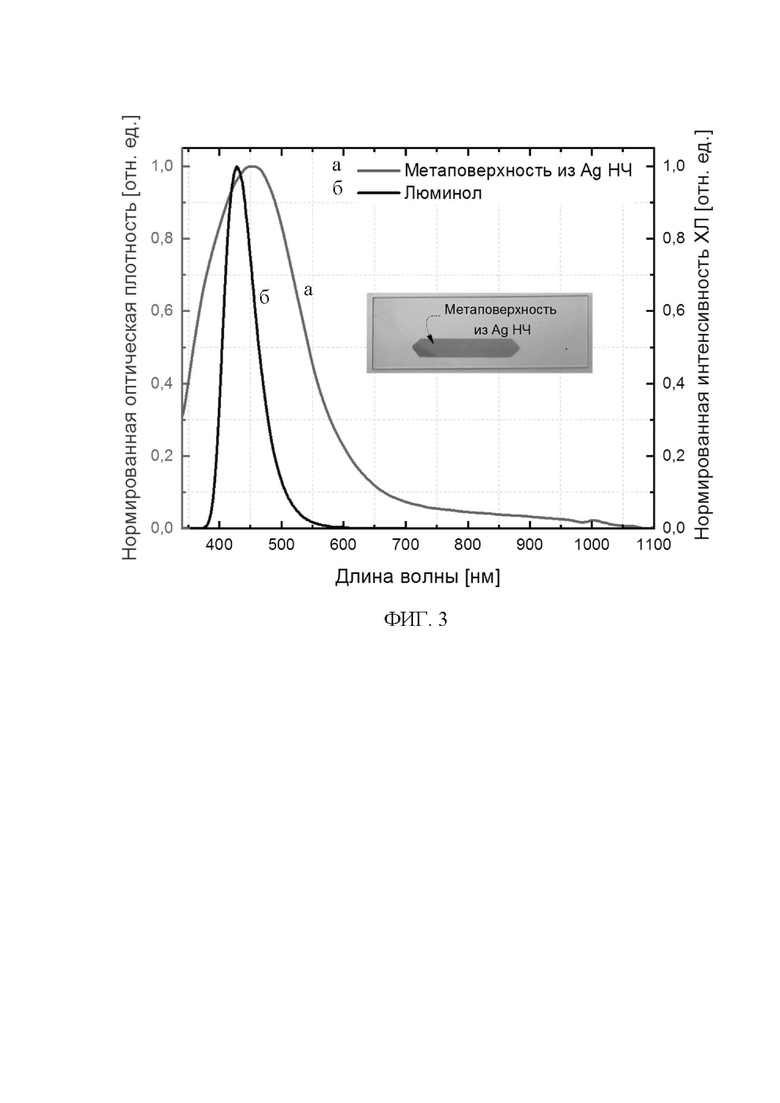
Фиг. 3. Спектральное перекрытие полосы поглощения метаповерхности из серебряных (Ag) наночастиц (а) и полосы хемилюминесценции молекул люминола (б).
Фиг. 4. Кинетика хемилюминесцентной реакции люминола при активации пероксидом водорода (H2O2): (а) микрофлюидный канал без метаповерхности из серебряных наночастиц и (б) микрофлюидный канал с метаповерхностью из серебряных наночастиц.
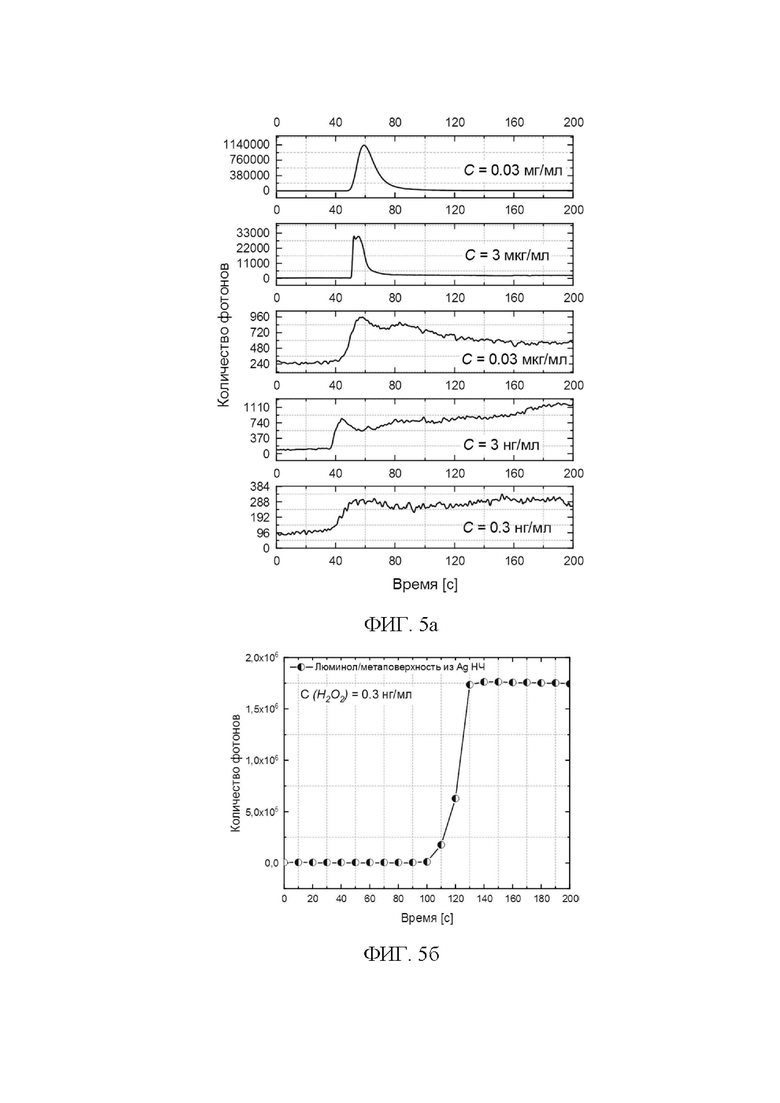
Фиг. 5. Кинетика хемилюминесцентной реакции люминола в присутствии плазмонной метаповерхности из серебряных наночастиц при активации пероксидом водорода (H2O2) различной концентрации: время накопления 100 мс (а) и 10000 мс (б).
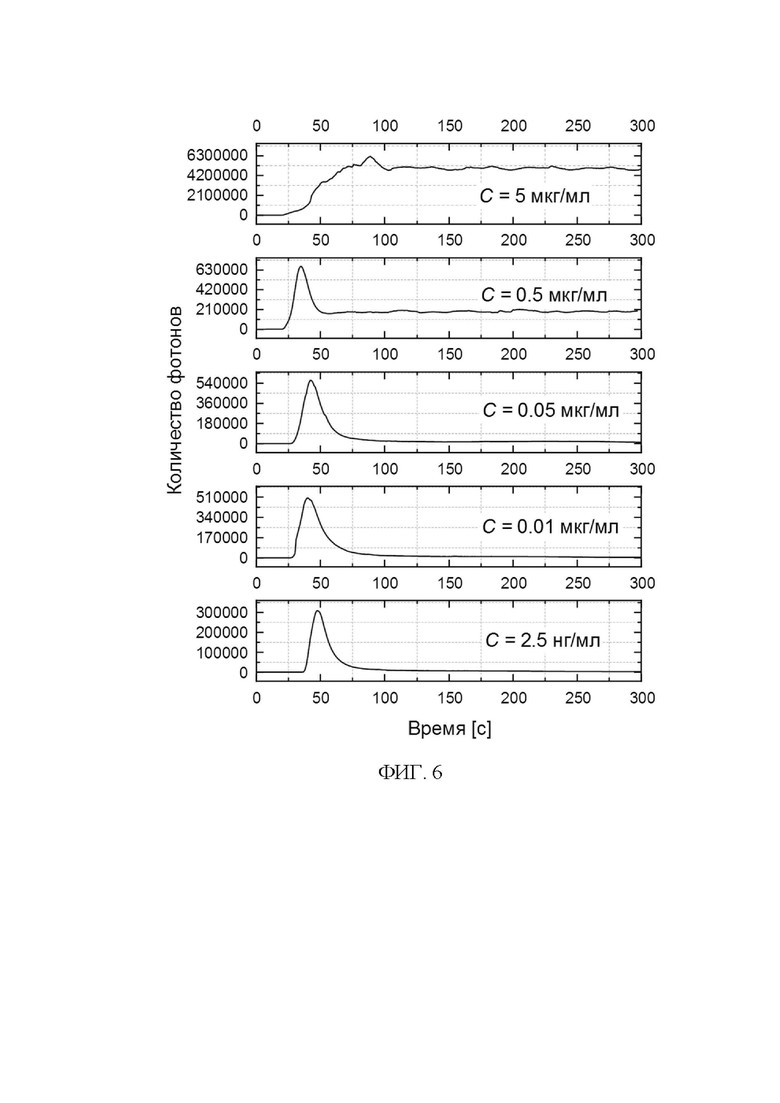
Фиг. 6. Кинетика хемилюминесцентной реакции люминола в присутствии плазмонной метаповерхности из серебряных наночастиц при активации гипохлоритом натрия (NaOCl) различной концентрации.
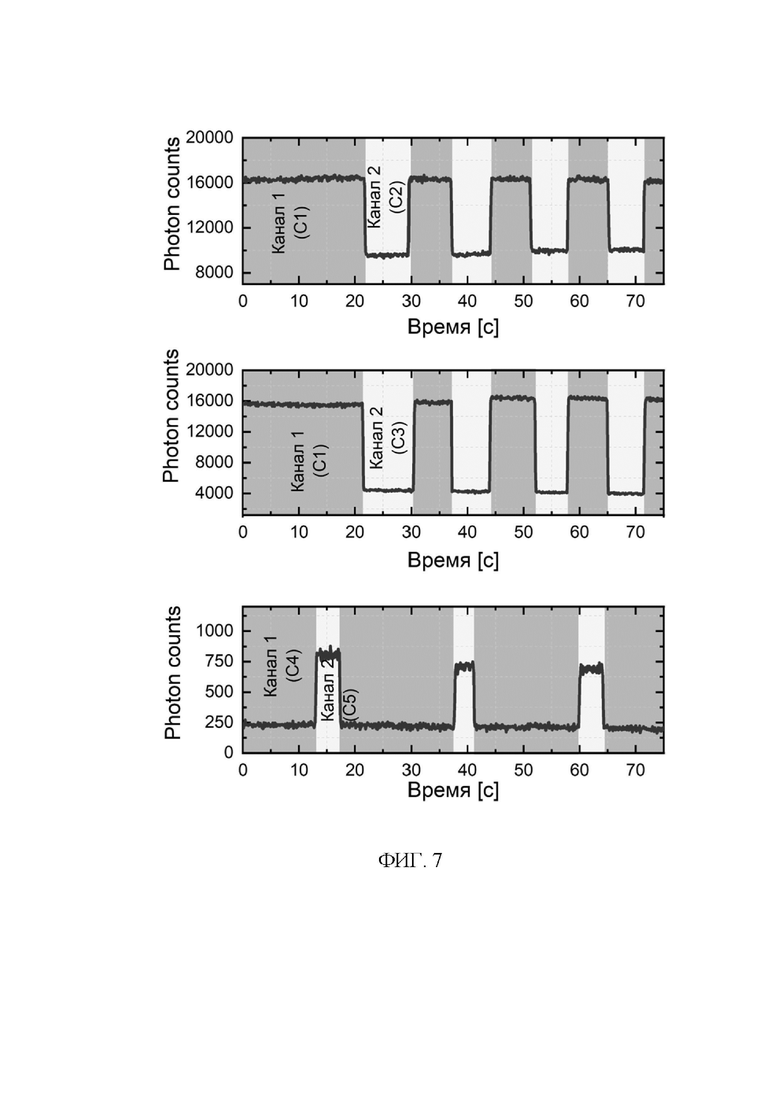
Фиг. 7. Демонстрация попеременной регистрации кинетики хемилюминесцентной реакции люминола, с помощью вращателя поляризации.
Фиг. 8. Фотография устройства для хемилюминесцентного анализа.
Устройство для хемилюминесцентного (ХЛ) анализа (Фиг. 1), состоит из светонепроницаемого корпуса, включающий крышку 1 и основание 2, защищающий фотоприемник ХЛ излучения от посторонней засветки. Ключевым элементом устройства является микрофлюидный чип, состоящий из сборки гибкой прозрачной полимерной части 3 с микроканалами с заданными параметрами, изготовленными литографическим методом, с диэлектрической подложкой 4 с нанесенными на нее металлическими (например, серебряными) наночастицами. Для поступления растворов, микрофлюидный чип соединён через силиконовые трубки 5 с четырехканальным инфузионным насосом 6, включающим в себя шприцы с необходимыми растворами: хемилюминофора (например, люминола) 7 с исследуемыми образцами 8 для сравнительного канала микрофлюидного чипа (Канал 2), и хемилюминофора 9 с референтным образцом 10 (Канал 1). Для позиционирования микрофлюидного чипа внутри основания 2 светонепроницаемого корпуса вставлены цилиндрические неодимовые магниты, которые точно сопрягаются с прозрачной полимерной частью 3 и с поляризаторами 11. Два расположенных в одной плоскости линейных поляризатора 11, наложенных на гибкую прозрачную полимерную часть 3 так, что угол между их главными плоскостями пропускания равен 90°, обеспечивают преобразование ХЛ излучение каналов с референтным образцом и исследуемыми образцами в линейно-поляризованное. Модуляция ХЛ сигнала осуществляется с помощью вращателя поляризации 12, выполненного, например, в виде жидкокристаллической твист-ячейки. Поляризатор 13 служит для определения закодированного поляризованного ХЛ излучения с каналов микрофлюидного чипа. Для вращения плоскости поляризации электрические входы вращателя 12 поляризации подключены к выходам генератора управляющих импульсов напряжения 14. Регистрация ХЛ излучении осуществляется с помощью фотоприемника 15, поддерживающего функцию счета фотонов. Для управления генератором управляющих импульсов напряжения 14, фотоприемником 15 и визуализации регистрируемых данных в режиме реального времени используется персональный компьютер 16. Сбор отработанных растворов осуществляется в специальную емкость 17.
Устройство работает следующим образом.
Сперва подготавливается щелочной раствор люминола с концентрацией 0.1 М с pH~12-13 и набирается в шприц 7 и шприц 9. Раствор с референтным образцом набирается в шприц 10, а раствор с исследуемым образцом в шприц 8, после чего шприцы закрепляются в каретке инфузионного насоса 6. Затем для получения корректных данных и снижении паразитных шумов при регистрации кинетики реакции ХЛ рекомендуется выдержать фотоприёмник 15 не менее 30 минут в темноте. Далее с одной стороны микрофлюидного чипа силиконовые трубки 5 подключаются к шприцам 7, 8, 9, 10 с необходимыми растворами, а с другой стороны - к емкости для слива 17. Генератор управляющих импульсов напряжения 14, обеспечивающий управление вращателем поляризации 12, подключается к сети переменного тока 220 В с частотой 50 Гц с помощью кабеля питания и к персональному компьютеру 16 через USB-кабель. Далее необходимо запустить программное обеспечение для фотоприемника 15, выход которого соединен с персональным компьютером 16 с помощью USB кабеля. Для последующего анализа данных следует зарегистрировать базовую линию с необходимым временем экспозиции (допустимо от 10 мс). После того как зарегистрирована базовая линия, в инфузионном насосе 6 выставляется скорость подачи жидкости (допустимо от 5 до 50 мкл/мин), и запускается закачка растворов из шприцов 7, 8, 9, 10 в микрофлюидный чип 3 через герметично скрепленные с ним трубки 6. Затем растворы из шприцов с люминолом 9 и референтным образцом 10 поступают в Канал 1 микрофлюидного чипа и перемешиваются в реакционном участке микрофлюидного чипа, индуцируя тем самым ХЛ свечение. Аналогичным образом ХЛ свечение должно наблюдаться в Канале 2, когда растворы с люминолом 7 и исследуемыми образцами 9 начнут взаимодействовать друг с другом. Затем ХЛ излучение Каналов 1 и 2, проходя через соответствующие им поляризаторы 11, поляризуется, и в результате чего излучение Канала 1 будет поляризовано перпендикулярно излучению Канала 2. Затем ХЛ излучение обоих каналов проходит через вращатель поляризации 12, который в свою очередь вращает плоскость поляризации излучения на 90° в отсутствии на его электрических входах напряжения, либо не изменяет плоскость поляризации при установлении с помощью генератора управляющих импульсов 14 напряжения равным U~1.5 В. Далее излучение проходит через поляризатор 13 сигналов каналов с референтным образцом и исследуемыми образцами и в зависимости от напряжения на выходе генератора управляющих импульсов напряжения поочередно попадает на фотоприемник. В результате этих операций, на мониторе персонального компьютера 16 отображается зависимость количества фотонов от времени, т.н. кинетика ХЛ реакции, приходящих на фотоприемник с Каналов 1 и 2 микрофлюидного чипа. После чего, на основании полученных данных проводится как качественная, так и количественная оценка АФК в растворе с исследуемым образцом по сравнению с референтным образцом с известной концентрацией. Для регистрации стабильного ХЛ отклика целесообразным является пропустить через микрофлюидный чип порядка 120-240 мкл смешанных растворов с хемилюминофором/исследуемым образцом и хемилюминофором/референтным образцом. Анализ экспериментальных данных показал, что объем одного канала в микрофлюидном чипе не превышает 60 мкл. Технические характеристики фотоприемника 15 и вращателя поляризации 12 позволяют использовать устройство и с другими хемилюминофорами, чьи полосы излучения лежат в спектральном диапазоне от 400 нм до 700 нм. В качестве фотоприемника 15 ХЛ излучения может быть установлен приемник Photon Counting Head H11890-210 (Hamamatsu, Япония).
Пример 1.
Для повышения чувствительности, сокращения расхода проб и увеличения быстродействия анализа ХЛ устройства был использован микрофлюидный чип с внедренными в него металлическими наночастицами. Гибкая полимерная часть 3 (Фиг. 2а), была изготовлена из оптически прозрачного полидиметилсилоксана (PDMS) с использованием стандартной мягкой литографии [Bukatin A.S., Mukhin I.S., Malyshev E.I., Kukhtevich I.V., Evstrapov A.A., Dubina M.V. Fabrication of high-aspect-ratio microstructuresin polymer microfluid chips for in vitro single-cell analysis//Technical Physics. - 2016. - V. 61, № 10. - P. 1566-1571]. Собранный микрофлюидный чип из гибкой полимерной части 3 и диэлектрической подложки 4 с металлическими наночастицами, содержит в себе два отдельных ромбовидных канала, необходимых для проведения сравнительного анализа (Фиг. 2а), и четыре отверстия для ввода и два отверстия для вывода растворов. Для обеспечения наилучшей чувствительности детектирования АФК с металлическими наночастицами высота каналов должна не превышать 10 мкм. В свою очередь, серебряные наночастицы (Фиг. 2б) на подложке были получены методом осаждения из паровой фазы в вакуумной камере PVD-75 (Kurt J. Lesker) согласно процедуре в работе [Leonov N. B. et al. Evolution of the optical properties and morphology of thin metal films during growth and annealing //Optics and spectroscopy. - 2015. - Т. 119. - №. 3. - С. 450-455.] при использовании необходимой маски. Последующий высокотемпературный отжиг серебряных наночастиц привел к самоорганизации металлических нанокластеров на поверхности подложки за счет поверхностной диффузии атомов серебра. Анализ снимка со сканирующего электронного микроскопа показал, что наночастицы имеют округлую форму с размерами от 10 нм до 200 нм (Фиг. 2б). Чтобы значительно повысить их устойчивость к воздействию химических реагентов, согласно процедуре, описанной в работе [Dadadzhanov D. R. et al. Self-organized plasmonic metasurfaces: The role of the Purcell effect in metal-enhanced chemiluminescence (MEC)//Sensors and Actuators B: Chemical. - 2021. - Т. 333. - С. 129453.], подложки были подвергнуты воздействию импульсного лазерного излучения с дозой энергии 80 мДж/см2 на длине волны 3-ей гармоники Nd:YAG - лазера (SOLAR Laser System) - 355 н. Обработка лазерным излучением позволяет избежать расход металлических наночастиц в ходе анализа, и допускает многократное использование микрофлюидных чипов за счет их фиксации на поверхности диэлектрической подложки. Также стоит отметить, что одно из необходимых условий усиления сигнала ХЛ выполняется за счет практически полного спектрального перекрытия полосы поглощения серебра и полосы ХЛ люминола, как показано на Фиг 3. Спектр ХЛ люминола имеет максимум на длине волны 428 нм, в то время как максимум поглощения плазмонного резонанса метаповерхности из серебряных наночастиц приходится на 450 нм. Для сравнительной демонстрации эффекта усиления ХЛ люминола был использован микрофлюидный чип, в котором только один канал имел включения из металлических наночастиц на диэлектрической подложке (вставка на Фиг.3). Далее заранее подготовленный 3 % раствор перекиси водорода и щелочной раствор люминола с pH = 12.7 был одновременно введен в микрофлюидный чип со скоростью 1.5 мкл/мин сперва в Канал 1 без наночастиц, а затем в Канал 2 с наночастицами. Из кинетики ХЛ на Фиг. 4 видно, что свечение люминола без наночастиц (а) резко возрастает, спустя некоторое время спадает и практически не меняется. В случае использования метаповерхности из металлических наночастиц с люминолом (б) наблюдается ярко выраженный рост интенсивности ХЛ, который со временем выходит на уровень насыщения. Сопоставление значений интенсивности ХЛ в Каналах 1 и 2 за промежуток времени, в котором сигналы стабильны, показало, что интенсивность ХЛ в канале с серебряными наночастицами в 3 раза выше, чем в канале без наночастиц (т. н. фактор усиления ХЛ). Усиление интенсивности ХЛ достигается вследствие эффекта Парселла, при котором происходит увеличение скорости радиационного распада возбуждённых молекул хемилюминофора, находящихся вблизи наночастиц [Sauvan C. et al. Theory of the spontaneous optical emission of nanosize photonic and plasmon resonators //Physical Review Letters. - 2013. - Т. 110. - №. 23. - С. 237401.]. Таким образом, использование плазмонной метаповерхности позволяет увеличить интенсивность ХЛ без увеличения объёма аналита и без усложнения процедуры измерения, но и также исключить применение дополнительных химических катализаторов ХЛ [Iranifam M. Chemiluminescence reactions enhanced by silver nanoparticles and silver alloy nanoparticles: applications in analytical chemistry //TrAC Trends in Analytical Chemistry. - 2016. - Т. 82. - С. 126-142.].
Пример 2.
Для демонстрации возможности детектирования АФК предлагаемым устройством, была проведена регистрация кинетики ХЛ реакции люминола с метаповерхностью из металлических наночастиц при активации молекулами пероксида водорода (Фиг. 5 а, б) и гипохлоритом натрия (Фиг. 6) с различной концентрацией. Как видно из Фиг. 5а, интенсивность ХЛ с течение времени начинает резко увеличиваться, а затем резко спадает до стационарного уровня. Для оценки уровня оксидативного стресса, вызванного присутствием пероксида водорода, целесообразно оценивать этот показатель по трём критериям. Первый критерий рассматривает оценку отношения максимумов интенсивностей исследуемого и референтного образцов при первой яркой вспышке, например, в районе 40 с на всех графиках кинетики ХЛ на Фиг. 5а. Второй критерий рассматривает оценку отношений средних значений интенсивности ХЛ исследуемого и референтного образцов при достижении стационарного состояния после резкой вспышки. Последний критерий оценки предусматривает сравнение среднего значения площади под кривой ХЛ реакции со средним значением площади под кривой для референтного образца за одинаковые временные промежутки. Из Фиг. 5а также видно, что ХЛ устройство, при времени накопления сигнала 100 мс, позволяет детектировать присутствие молекул пероксида водорода вплоть до 0.3 нг/мл. Разумеется, достижение более качественной кинетики ХЛ также может осуществлено с помощью увеличения времени накопления сигнала ХЛ, что подтверждается при времени накопления 10000 мс и при ранее использованной концентрации пероксида водорода (0.3 нг/мл) (Фиг. 5б). Для подтверждения возможности детектирования активных форм кислорода другого типа был использован водный раствор гипохлорита натрия с различной концентрацией, как указано на Фиг. 6. Было продемонстрировано, что ХЛ устройство способно зарегистрировать содержание гипохлорита в образце до 2.5 нг/мл. Объем используемых смешанных растворов в одном канале не превышал 250 мкл. Таким образом, была показана работоспособность ХЛ устройства регистрации ХЛ люминола на примере детектирования АФК (пероксида водорода и гипохлорита). Также было продемонстрировано преимущество использования метаповерхности из металлических наночастиц, внедренной в микрофлюидный чип, которая не только повышает чувствительность детектирования АФК, но и характеризуется хорошей устойчивостью на поверхности диэлектрической подложке при контакте со щелочным раствором люминола. Многократное использование микрофлюидного чипа с метаповерхностью подтверждается стабильным ХЛ сигнал в течение длительного времени. Показано, что использование микрофлюидного чипа существенно позволяет сократить объем образца с перекисью водорода (H2O2) и гипохлоритом натрия (NaClO).
Пример 3.
Результат работы предлагаемого устройства показан на Фиг. 7, где приведены три графика, отображающие кинетики ХЛ реакции люминола с серебряными наночастицами при активации NaClO различной концентрации (см. таблицу 1).
В отсутствие напряжения на вращателе поляризации 12 плоскость поляризации падающего ХЛ излучения поворачивалась на 90°, что обеспечивало прохождение ХЛ излучения Канала 1 на фотоприемник 15 и, в то же время, блокировало излучение из Канала 2 с концентрацией NaClO отличной от концентрации в Канале 1. При подаче напряжения U~1.5 В на электрические входы вращателя поляризации 12 в виде жидкокристаллической твист-ячейки, где молекулы жидкого кристалла выстраиваются вдоль направления распространения света, поворота плоскости поляризации излучения не происходит и, в результате, на фотоприемник 15 попадает излучение Канала 2, а излучение Канала 1 блокируется. Количественный и качественный анализ содержания АФК в образцах может происходить путем сопоставление полученных данных с Канала 1 и Канала 2. При использовании микрофлюидного чипа с большим числом микроканалов поляризационные состояния ХЛ излучения исследуемых каналов должно быть одинаковым, но отличным от поляризации излучения референтного канала. Многочисленные эксперименты показали, что переключение излучения ХЛ отклика с референтного и анализируемых образцах может быть осуществлено с частотой от 0.5 Гц до 500 Гц. В данной конфигурации при установлении времени накоплении 10 мс, как видно на Фиг. 7 заметить стабильный переменный ХЛ сигнал, варьирующийся с различной частотой. В случае применения устройства в реальных условиях время до получения первичного результата/диагноза о степени содержания АФК будет существенно сокращено. Исходя из экспериментальных данных о времени регистрации кинетики ХЛ реакции двух образцов с различной концентрацией NaClO, которое составило порядка 70 секунд. В отличие от традиционных устройств для ХЛ анализа, устройство является крайне компактным и мобильным, что подтверждается его габаритами Фиг.8, где в центре расположен светонепроницаемый корпус с ключевыми компонентами устройства, описанными ранее, а с противоположных сторон размещены инфузионный насос, генератор управляющих импульсов напряжения и емкость для сбора отработанных материалов.
Таким образом, регистрация ХЛ откликов от различного рода АФК демонстрирует работоспособность ХЛ устройства при регистрации ХЛ сигнала поочередно с двух каналов за счет поляризации их излучений переключения фотоприемника на регистрацию излучения от референтного или анализируемого образца с заданной частотой. Использование кодирования сигналов референтного и анализируемого образцов с помощью поляризации излучения позволяет не только сократить время измерения, но и избавиться от движущихся деталей, (например, оптомеханических систем перемещения и вращения), что упрощает использование прибора и повышает надёжность его работы. Оптическая схема позволяет переключать фотоприёмник излучения между измерениями интенсивности ХЛ и кинетики реакции в референтном и анализируемом образцах с варьируемой частотой, что позволяет избавиться от низкочастотных помех и выделить на их фоне полезный сигнал.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОЙ ОЦЕНКИ БАЛАНСА ПРО- И АНТИОКСИДАНТОВ В ОТДЕЛАХ ГОЛОВНОГО МОЗГА ЖИВОТНОГО | 2013 |
|
RU2523403C1 |
| СПОСОБ СЕРТИФИКАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1995 |
|
RU2124202C1 |
| Способ дифференциальной диагностики форм воспаления бактериального риносинусита | 2020 |
|
RU2741211C1 |
| СПОСОБ ДИАГНОСТИКИ IN VITRO СПЕЦИФИЧЕСКОЙ СЕНСИБИЛИЗАЦИИ ОРГАНИЗМА К БАКТЕРИАЛЬНЫМ АЛЛЕРГЕНАМ | 2014 |
|
RU2587327C2 |
| Люминесцентный сенсор концентрации ионов тяжёлых металлов (преимущественно кобальта) в воде на основе квантовых точек тройного состава | 2019 |
|
RU2733917C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ МАСТИТА У КОРОВ | 2011 |
|
RU2485914C2 |
| СПОСОБ ХЕМИЛЮМИНЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ ФЕНОЛОВ | 2010 |
|
RU2467312C2 |
| Способ количественного определения селективно связанных белков-маркеров заболеваний в планарных ячейках биочипа и устройство для его осуществления | 2021 |
|
RU2776889C1 |
| Способ определения концентрации свинца (II) в водных образцах | 2019 |
|
RU2715478C1 |
| СПОСОБ ПОДБОРА ОПТИМАЛЬНОЙ ДОЗЫ МАГНИТНОЙ ИНДУКЦИИ ПРИ ОБЩЕЙ МАГНИТОТЕРАПИИ | 2004 |
|
RU2282189C1 |



Изобретение относится к аналитическим сенсорным системам и может быть использовано для детектирования активных форм кислорода в биологических и иных пробах, а также при проведении хемилюминесцентного иммунологического анализа с повышенной чувствительностью. Устройство для хемилюминесцентного анализа содержания активных форм кислорода в биологических и иных пробах содержит насос для ввода с помощью трубок жидких реактивов из емкостей с хемилюминофором и исследуемыми пробами в микрофлюидный чип, выход которого связан трубкой с емкостью для слива, и фотоприемник, при этом микрофлюидный чип и фотоприемник помещены в светонепроницаемый корпус, причем микрофлюидный чип выполнен по меньшей мере двухканальным и содержит диэлектрическую подложку с нанесенной на нее метаповерхностью из обработанных лазерным излучением металлических наночастиц, обладающих локализованным плазмонным резонансом в спектральной полосе хемилюминесценции используемого хемилюминофора, а в светонепроницаемый корпус также включены два линейных взаимно-ортогонально ориентированных поляризатора, наложенных на различные каналы микрофлюидного чипа, расположенные друг за другом по ходу распространения излучения вращатель поляризации и установленный непосредственно перед входом фотоприемника третий линейный поляризатор излучения, совпадающий по ориентации с одним из линейных поляризаторов, наложенных на микрофлюидный чип. Техническим результатом является кодирование путем поляризации хемилюминесцентного излучения и увеличение его интенсивности. 1 з.п. ф-лы, 8 ил., 1 табл.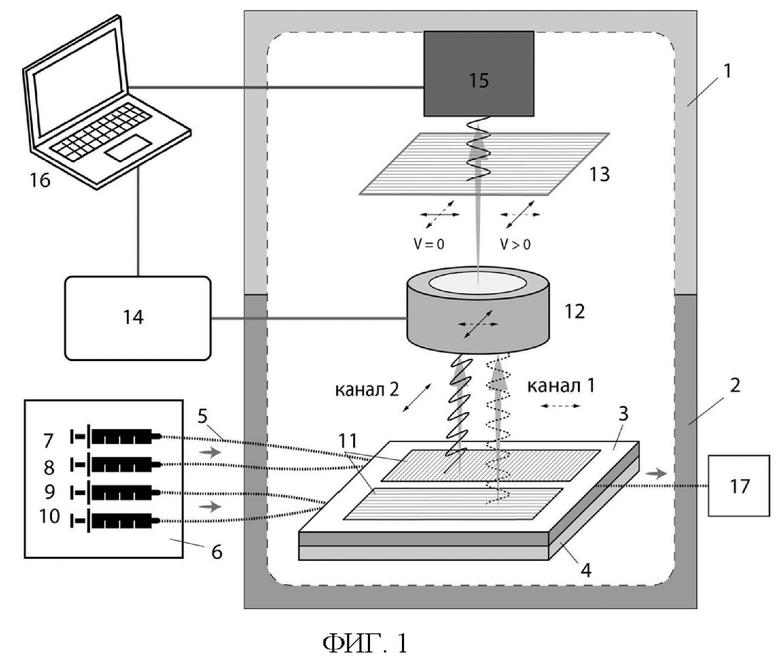
1. Устройство для хемилюминесцентного анализа содержания активных форм кислорода в биологических и иных пробах, содержащее насос для ввода с помощью трубок жидких реактивов из емкостей с хемилюминофором и исследуемыми пробами в микрофлюидный чип, выход которого связан трубкой с емкостью для слива, и фотоприемник, отличающееся тем, что микрофлюидный чип и фотоприемник помещены в светонепроницаемый корпус, причем микрофлюидный чип выполнен по меньшей мере двухканальным и содержит диэлектрическую подложку с нанесенной на нее метаповерхностью из обработанных лазерным излучением металлических наночастиц, обладающих локализованным плазмонным резонансом в спектральной полосе хемилюминесценции используемого хемилюминофора, а в светонепроницаемый корпус также включены два линейных взаимно-ортогонально ориентированных поляризатора, наложенных на различные каналы микрофлюидного чипа, расположенные друг за другом по ходу распространения излучения вращатель поляризации и установленный непосредственно перед входом фотоприемника третий линейный поляризатор излучения, совпадающий по ориентации с одним из линейных поляризаторов, наложенных на микрофлюидный чип.
2. Устройство для хемилюминесцентного анализа содержания активных форм кислорода в биологических и иных пробах по п. 1, отличающееся тем, что вращатель поляризации выполнен в виде жидкокристаллической твист-ячейки, электрические входы которой подключены к выходам генератора управляющих импульсов напряжения, а фотоприемник выполнен с функцией счета фотонов.
| CN 212780531 U, 23.03.2021 | |||
| 0 |
|
SU162866A1 | |
| УСТРОЙСТВО ДЛЯ АНАЛИЗА ХЕМИ- И БИОЛЮМИНЕСЦЕНЦИИ ЖИДКИХ СРЕД | 2011 |
|
RU2452937C1 |
| 0 |
|
SU180961A1 | |
Авторы
Даты
2022-10-11—Публикация
2021-12-27—Подача