Изобретение относится к медицине, в частности, к медицинской химии, и может быть использовано для оценки взаимодействия лекарственных препаратов и биологически активных веществ с катионами кальция и магния.
Кальций и магний, являющиеся вторым и третьим по распространенности внутриклеточными катионами, играют важную роль в функционировании сердечно-сосудистой и нервной системы [1]. В частности, под контролем данных катионов осуществляется регуляция сократительного состояния кардиомиоцитов, гладкомышечных клеток, обеспечивается формирование потенциала действия пейсмекерных клеток, а также передача нервного импульса [2].
Магний является кофактором более, чем 300 ферментативных реакций, при этом универсальность его участия в биохимических процессах обуславливается способностью к образованию комплексов магния с молекулами АТФ, что обеспечивает высвобождение энергии через активацию магний - зависимых АТФ-аз [3]. Благодаря наличию антагонистических взаимоотношений с кальцием, а также участию в энергообеспечении ионных каналов мембран митохондрий и саркоплазматических ретикулумов, магний представляется важнейшим регулятором внутриклеточного электролитного баланса. Показано, что при увеличении внутриклеточного кальциево-магниевого соотношения, возникающего в случае преобладания кальция и снижения магния, происходит активация кальций-зависимых протеаз и липаз, что приводит к повреждению мембран кардиомиоцитов [4].
С позиций электрофизиологии магний способствует уменьшению автоматизма сердца, удлинению предсердной, желудочковой и атриовентрикулярной проводимости, угнетению ранних и задержанных постдеполяризаций. Под контролем магния находятся 2, 3 и 4 фазы потенциала действия сократительных кардиомиоцитов и 0,3 фазы потенциала действия пейсмекерных клеток [5]. В 0 фазе потенциала действия пейсмекерных клеток и во 2 фазе потенциала действия сократительных кардиомиоцитов внутриклеточные и внеклеточные концентрации магния регулируют кальциевый ток за счет ингибирования кальциевых каналов L-типа [6], предотвращая тем самым внутриклеточную перегрузку кальцием и возможную цитотоксичность [7]. Описанная модуляция работы кальциевых каналов L-типа зависит от концентраций ионов магния и состояния фосфорилирования, поскольку связывание магния ингибирует фосфорилированный канал от прохождения конформационных изменений, которые приводят к его более частому открытию [8, 9]. В 3 фазе потенциала действия концентрации внутриклеточного магния обеспечивают контроль выхода калия из клетки через калиевые каналы внутреннего и задержанного выпрямления. Эта регуляция имеет решающее значение для процессов реполяризации и приводит к продлению периода рефрактерности [10, 11]. Удлинение интервала QT на ЭКГ - распространенный признак гипо- и гипермагниевых состояний, которые могут являться триггерами аритмий через механизм ранних постдеполяризаций. Состояние покоя клеточной мембраны в фазе 4 поддерживается активностью Na+-K+-АТФ-азного насоса и натрий-кальциевого обменника. Данные активные транспортеры требуют затрат энергии от гидролиза АТФ для противотокового перемещения ионов натрия и калия через цитоплазматическую мембрану, вопреки соответствующих им градиентам концентрации, что способствует поддержанию трансмембранного потенциала и снижению цитоплазматических концентраций натрия. Магний при этом играет роль не только в образовании и гидролизе АТФ, но и непосредственно в обеспечении открытия и закрытия цитоплазматических доменов Na+-K+-помпы [12]. Кроме того, в эту фазу внутреннее выпрямление калия модулируется за счет блокирования калиевых каналов внутриклеточным магнием [11].
Представляется интересным влияние магния на передачу импульса в вегетативной нервной системе за регуляции высвобождения медиаторов из пресинаптической мембраны. В адренергических синапсах обратный захват норадреналина опосредуется магний-зависимой Na+-K+-АТФ-азой, причем под контролем магния находятся процессы инактивации и резервирования нейромедиатора путем связывания его в гранулах. В холинергических синапсах магний тормозит высвобождение ацетилхолина, сопряженное с поступлением ионов кальция [5,6].
Доказано, что дефицит кальция и магния ассоциирован с развитием ряда сердечно-сосудистых заболеваний [13, 14, 15, 16] и расстройств деятельности нервной системы [17], при этом условия формирования дефицита данных элементов могут быть универсальны и связаны с особенностями питьевого режима, питания, наличием коморбидной патологии, а также употреблением лекарственных препаратов [2, 6, 18].
Обобщая вышеизложенное, можно заключить, что оценка взаимодействия катионов кальция и магния с лекарственными препаратами и биологически активными веществами в одинаковых условиях представляет теоретический и практический интерес.
Задача при создании способа - сопоставить комплексообразующие свойства лекарственных препаратов и биологически активных веществ по отношению к кальцию и магнию в одинаковых условиях.
В качестве аналогов настоящего изобретения использованы следующие источники информации:
1. способ оценки комплексообразующих свойств лекарственных веществ по отношению к соединениям магния (RU 2680519, G01N 33/48, G01N 33/15), оценивающий влияние органических веществ на гетерогенный процесс образования фосфатов магния [19].
2. способ оценки взаимодействия лекарственных препаратов с катионами магния (RU 2712048, G01N 33/15) [20].
Обозначенные способы основаны на оценке способности анализируемых ионов металлов к участию в гетерогенных реакциях при наличии в системе органических лигандов, однако их использование для изучения свойств лекарственных препаратов выявляет следующие функциональные ограничения:
- в патенте RU 2680519 [19] используемая буферная система не обладает достаточной буферной емкостью по кислоте, чтобы анализировать растворы лекарственных препаратов с рН≥9 без существенных изменений условий протекания реакции и свойств образующейся твердой фазы.
Наиболее близким, принятым за прототип, для предлагаемого способа является патент RU 2712048 [20], в основе которого лежит турбидимитрическое определение величины светопропускания в ходе гетерогенной реакции образования фосфатов магния в присутствии анализируемого вещества или без него. Формирование гетерогенной фазы гидрофосфатов и фосфатов магния происходит при добавлении в фосфатный буфер раствора сульфата магния. Органические вещества, находящиеся в системе, затрудняют образование гетерогенной фазы за счет комплексообразующего взаимодействия с катионами магния, что влечет изменение светопропускания на определенную величину, по сравнению с контрольным опытом.
Заявляемый способ взаимодействия лекарственных препаратов и биологически активных веществ с катионами кальция и магния, основан на расчете коэффициента комплексообразующей активности (Кка) по отношению к катионам магния, составные компоненты которого определяются турбидимитрическим методом как результат изменения светопропускания в системе, содержащей гетерогенную фазу, образующуюся при добавлении раствора катиона магния к фосфатному буферу со значением рН в диапазоне 8,2-8,3; в отсутствии органических лигандов (контрольный опыт), в присутствии анализируемого лекарственного препарата (основной опыт), а также в присутствии стандартного комплексообразователя - трилона Б (опыт со стандартом); расчет коэффициента комплексообразующей активности учитывает содержание общего органического углерода в системе и осуществляется по формуле:
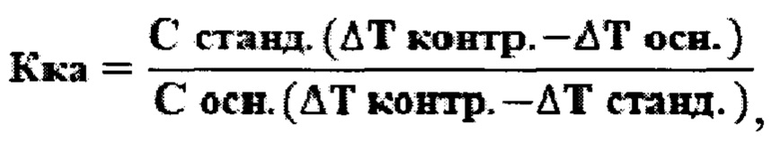
где
Кка - коэффициент комплексообразующей активности,
ΔΤ контр., % - изменение величины светопропускания в гетерогенной системе, не содержащей органических лигандов (контрольный опыт),
ΔΤ станд., % - изменение величины светопропускания в опыте со стандартом;
ΔΤ осн., % - изменение величины светопропускания в гетерогенной системе, содержащей анализируемый лекарственный препарат (основной опыт), при этом
 расчет комплексообразующей активности проводят два раза: по катиону магния KKa(Mg) и по катиону кальция Кка(Са);
расчет комплексообразующей активности проводят два раза: по катиону магния KKa(Mg) и по катиону кальция Кка(Са);
 гетерогенную фазу образуют при взаимодействии фосфатного буфера с раствором катиона кальция и при взаимодействии фосфатного буфера с раствором магния и концентрация кальция в системе должна быть в 15-20 раз ниже, чем концентрация магния;
гетерогенную фазу образуют при взаимодействии фосфатного буфера с раствором катиона кальция и при взаимодействии фосфатного буфера с раствором магния и концентрация кальция в системе должна быть в 15-20 раз ниже, чем концентрация магния;
 в формуле для расчета комплексообразующей активности по отношении к катионам кальция:
в формуле для расчета комплексообразующей активности по отношении к катионам кальция:
- С станд., мг/л (по ООУ) - концентрация лиганда в опыте со стандартом в перерасчете на ООУ, которая за счет комплексобразующего взаимодействия с кальцием препятствует образованию гетерогенной фазы,
- С осн., мг/л (по ООУ) - концентрация анализируемого лекарственного препарата или биологически активного вещества в основном опыте в перерасчете на ООУ, которая за счет комплексобразующего взаимодействия с кальцием затрудняет образование гетерогенной фазы.
После расчета коэффициентов комплексообразующей активности по катиону магния и по катиону кальция, сопоставляют комплексообразующие свойства лекарственных препаратов и биологически активных веществ по отношению к кальцию и магнию.
Пример:
В таблице 1 представлены: молярные массы, расчетные значения содержания общего органического углерода (ООУ) и концентрация вещества в лекарственных препаратах (ЛП) - «Адреналин», «Норадреналин», «Допамин» и биологически активных веществ «Ацетилхолин» и «Трилон Б».
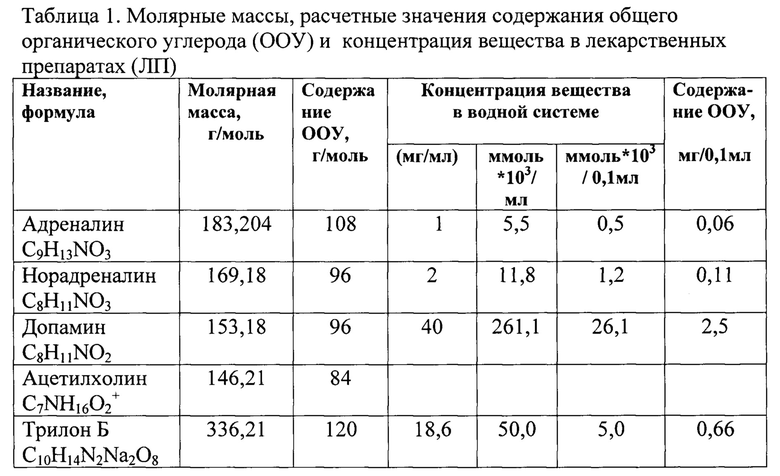
Лекарственные препараты содержат разное количество активного вещества и пересчет комплексообразующей активности на ммоль затруднителен в виду существенной разницы в содержании вещества в 0,1 мл (см. табл. 1 - разница более, чем в 50 раз), поэтому целесообразно относить свойства к мг ООУ. Кроме того, при анализе свойств биологически активных веществ с неопределенной формулой, содержание ООУ можно измерить анализатором ООУ.
В таблице 2, 3 представлены экспериментальные данные по определению коэффициента комплексообразующей активности по отношению к магнию и кальцию соответственно.
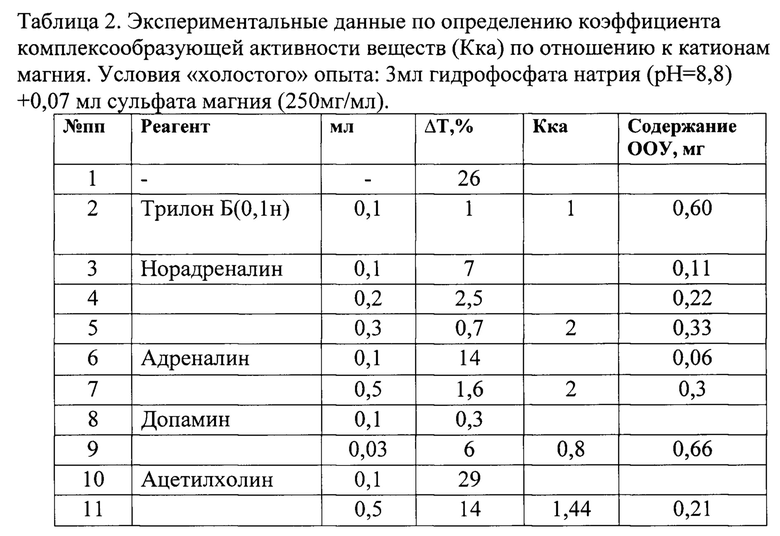

Из экспериментальных данных следует, что комплексообразующая активность адреналина, норадреналина по отношению к катионам магния в 2 раза выше, чем у трилона Б (при прочих равных условиях). Ацетилхолин также имеет высокую комплексообразующую активность по отношению к катионам магния (Кка=1,44). По отношению к катионам кальция комплексообразующую активность проявляет только адреналин (Кка=0,64).
Полученные данные позволяют в сопоставительном анализе in vitro оценить влияние медиаторов вегетативной нервной системы на формирование субстрата для развития внутри- и внеклеточной дисэлетролитэмии с позиции образования комплексных соединений с катионами кальция и магния, что важно для понимания патофизиологических особенностей развития нарушений сердечного ритма, в частности, вегетативного генеза.
Использованные источники информации:
1. Jahnen-Dechent, W. Magnesium basics / W. Jahnen-Dechent, Μ. Ketteler // Clin. Kidney J. - 2012. - Vol. 5, №2. - P. 3-14.
2. Shechter, M. Magnesium and cardiovascular system// Magnes.Res.- 2010. - Vol. 23. - P. 60-72.
3. Maguire, Μ. E. Magnesium chemistry and biochemistry / Μ. E. Maguire, J. A. Cowan // Biometals. - 2002. - Vol. 15. - P. 203-210.
4. Swaminathan, R. Magnesium metabolism and its disorders / R. Swaminathan // Clin. Biochem. Rev. - 2003. - Vol. 24, №2. - P. 47-66.
5. De Baaij, J. H. Magnesium in man: implications for health and disease / J. H. de Baaij, J. H. Hoenderop, R. J. Bindels // Physiol. Rev. - 2015. - Vol. 95, №1. - P. 1-46.
6. Role of magnesium in cardiovascular diseases / D. Kolte, K. Vijayaraghavan, S. Khera [et al.] // Cardiol. Rev. - 2014. - Vol. 22, №4. - P. 182-192.
7. Wang, M. Regulation of L-type calcium current by intracellular magnesium in rat cardiac myocytes / M. Wang, M. Tashiro, J. R. Berlin // J. Physiol. - 2004. -Vol. 555, №2. - P. 383-396.
8 White, R. E. Effects of intracellular free magnesium on calcium current in isolated cardiac myocytes / R. E. White, H.C. Hartzell // Science. - 1988. - Vol. 239, №4841. - P. 778-780.
9. Regulation of cation channels in cardiac and smooth muscle cells by intracellular magnesium / K. Mubagwa, A. Gwanyanya, S. Zakharov [et al.] // Arch. Biochem. Biophys. - 2007. - Vol. 458. - P. 73-89.
10. Duchatelle-Gourdon, I. Modulation of the delayed rectifier potassium current in frog cardiomyocytes by betaadrenergic agonists and magnesium / I. Duchatelle-Gourdon, H. C. Hartzell, A. A. Lagrutta // J. Physiol. - 1989. - Vol. 415. - P. 251-274.
11. Role of Mg (2+) block of the inward rectifier К (+) current in cardiac repolarization reserve: a quantitative simulation / K. Ishihara, N. Sarai, K. Asakura [et al.] // J. Mol. Cell Cardiol. - 2009. - Vol. 47, №l. - P. 76-84.
12. ATP and magnesium drive conformational changes of the Na+/K+-ATPase cytoplasmic headpiece / L. Grycova, P. Sklenovsky, Z. Lansky [et al.] // Biochim. Biophys. Acta. - 2009. - Vol. 1788, №5. - P. 1081-1091.
13. Abbott R.D. al. Dietary magnesium intake and the future risk of coronary heart disease (the Honolulu Heart Program). Am J Cardiol. 2003;92(6). P. 665-669.
14. Low serum magnesium and the development of atrial fibrillation in the community: the Framingham Heart Study. / A.M. Khan, S.A., Lubitz, L.M. Sullivan [et al.] // Circulation. - 2013. - Vol.127, №1. - P. 33-38.
15. Magnesium and the risk of cardiovascular events: a meta-analysis of prospective cohort studies / X.Qu, F. Jin, Y. Hao [et al.]. PLoS ONE - Vol. 8, №3 - e57720.
16. Seelig, M.S. Metabolic Sindrom-X. A complex of common diseases -diabetes, hypertension, heart disease, dyslipidemia and obesity - marked by insulin resistance and low magnesium/high calcium // Mineral Res. Intern. Tech. Prod. Infor. – 2003. - P. 1-11.
17. Murck, H. Magnesium and affective disorders. Nutr Neurosci. - 2002. Vol. 5, №6. - P. 375-389.
18. Шилов, A.M. Дефицит магния и сердечно-сосудистые заболевания: патофизиология и лечение в условиях первичного звена здравоохранения / A.M. Шилов, А.О. Осия // Российский медицинский журнал. - 2014. - №2. - С. 87-93.
19. Белоконова Н.А. Способ оценки комплексообразующих свойств лекарственных веществ по отношению к соединениям магния / Н.А. Белоконова, Н.А., Н.В. Изможерова, Бахтин В.М. // Патент на изобретение РФ №2680519.
20. Белоконова Н.А. Способ оценки взаимодействия лекарственных препаратов с катионами магния / Н.А. Белоконова, Я.Г. Божко, М.В. Архипов // Патент на изобретение РФ №2712048.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ВЗАИМОДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ С КАТИОНАМИ МАГНИЯ | 2019 |
|
RU2712048C1 |
| СПОСОБ ОЦЕНКИ КОМПЛЕКСООБРАЗУЮЩИХ СВОЙСТВ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ ПО ОТНОШЕНИЮ К СОЕДИНЕНИЯМ МАГНИЯ | 2017 |
|
RU2680519C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОМПЛЕКСООБРАЗУЮЩЕЙ АКТИВНОСТИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В ВОДНЫХ СИСТЕМАХ ПО ОТНОШЕНИЮ К СОЕДИНЕНИЯМ ЖЕЛЕЗА(III) ИЛИ МЕДИ(II) | 2017 |
|
RU2657437C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2011 |
|
RU2458686C1 |
| НАНОФОРМА ФОСФОЛИПИДНОГО ПРЕПАРАТА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ (САШЕ) И СПОСОБ ЕЕ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2010 |
|
RU2463057C2 |
| ПРОДУКТЫ, СОДЕРЖАЩИЕ МАГНИЙ, И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2571344C1 |
| КОМПОЗИЦИЯ ДЛЯ РЕГУЛЯЦИИ МИКРОЭЛЕМЕНТНОГО ОБМЕНА В ПОЛОСТИ РТА | 2019 |
|
RU2722306C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕЛЕОБРАЗУЮЩИХ ФОСФАТОВ ДЕКСТРАНА | 2010 |
|
RU2455007C1 |
| КОНЪЮГАТ НАНОАЛМАЗА С ПИРОФОСФАТАЗОЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2542411C1 |
| N-ОКСИДЫ ОКТАГИДРО-ПИРРОЛО[3,4-b]ПИРРОЛА | 2008 |
|
RU2486187C2 |
Изобретение относится к медицине, в частности к медицинской химии. Раскрыт способ оценки взаимодействия лекарственных препаратов и биологически активных веществ с катионами кальция и магния, включающий расчет коэффициента комплексообразующей активности катионов магния - Кка, составные компоненты которого определяются турбидимитрическим методом как результат изменения светопропускания в системе, содержащей гетерогенную фазу, образующуюся при добавлении раствора катиона магния к фосфатному буферу со значением рН в диапазоне 8,2-8,3 в отсутствие органических лигандов - контрольный опыт, в присутствии анализируемого лекарственного препарата - основной опыт, а также в присутствии стандартного комплексообразователя - трилона Б - опыт со стандартом. Расчет комплексообразующей активности проводят два раза: по катиону магния - Кка и по катиону кальция - Кка, для расчета коэффициента комплексообразующей активности по катиону кальция гетерогенную фазу образуют при взаимодействии фосфатного буфера с раствором катиона кальция, при этом концентрация кальция в системе должна быть в 15-20 раз ниже, чем концентрация магния, а в формуле для расчета комплексообразующей активности по отношению к катионам кальция используют значения Сстанд., мг/л - концентрация лиганда в опыте со стандартом в перерасчете на общий органический углерод, которая за счет комплексообразующего взаимодействия с кальцием препятствует образованию гетерогенной фазы и Сосн., мг/л - концентрация анализируемого лекарственного препарата в основном опыте в перерасчете на общий органический углерод, которая за счет комплексообразующего взаимодействия с кальцием затрудняет образование гетерогенной фазы. Изобретение обеспечивает возможность оценивать комплексообразующие свойства лекарственных препаратов и биологически активных веществ по отношению к кальцию и магнию в одних условиях. 1 пр., 3 табл.
Способ оценки взаимодействия лекарственных препаратов и биологически активных веществ с катионами кальция и магния, включающий расчет коэффициента комплексообразующей активности катионов магния - Кка, составные компоненты которого определяются турбидимитрическим методом как результат изменения светопропускания в системе, содержащей гетерогенную фазу, образующуюся при добавлении раствора катиона магния к фосфатному буферу со значением рН в диапазоне 8,2-8,3 в отсутствие органических лигандов - контрольный опыт, в присутствии анализируемого лекарственного препарата - основной опыт, а также в присутствии стандартного комплексообразователя - трилона Б - опыт со стандартом, расчет коэффициента комплексообразующей активности осуществляют с учетом содержания общего органического углерода в системе по формуле
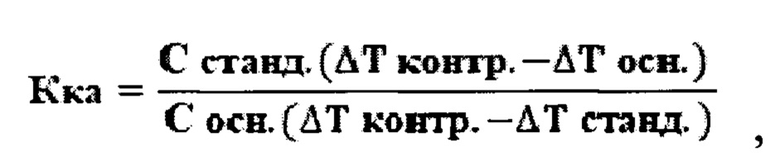
где Кка - коэффициент комплексообразующей активности,
Сстанд., мг/л - концентрация лиганда в опыте со стандартом в перерасчете на общий органический углерод,
Сосн., мг/л - концентрация анализируемого лекарственного препарата в основном опыте в перерасчете на общий органический углерод,
ΔΤконтр., % - изменение величины светопропускания в гетерогенной системе, не содержащей органических лигандов - контрольный опыт,
ΔТстанд., % - изменение величины светопропускания в опыте со стандартом;
ΔΤосн., % - изменение величины светопропускания в гетерогенной системе, содержащей анализируемый лекарственный препарат - основной опыт, отличающийся тем, что расчет комплексообразующей активности по формуле проводят два раза: по катиону магния - Кка и по катиону кальция - Кка, для расчета коэффициента комплексообразующей активности по катиону кальция гетерогенную фазу образуют при взаимодействии фосфатного буфера с раствором катиона кальция, при этом концентрация кальция в системе должна быть в 15-20 раз ниже, чем концентрация магния, а в формуле для расчета комплексообразующей активности по отношению к катионам кальция используют значения Сстанд., мг/л - концентрация лиганда в опыте со стандартом в перерасчете на общий органический углерод, которая за счет комплексообразующего взаимодействия с кальцием препятствует образованию гетерогенной фазы и Сосн., мг/л - концентрация анализируемого лекарственного препарата в основном опыте в перерасчете на общий органический углерод, которая за счет комплексообразующего взаимодействия с кальцием затрудняет образование гетерогенной фазы.
| СПОСОБ ОЦЕНКИ ВЗАИМОДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ С КАТИОНАМИ МАГНИЯ | 2019 |
|
RU2712048C1 |
| СПОСОБ ОЦЕНКИ КОМПЛЕКСООБРАЗУЮЩИХ СВОЙСТВ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ ПО ОТНОШЕНИЮ К СОЕДИНЕНИЯМ МАГНИЯ | 2017 |
|
RU2680519C1 |
| DASTA J.F | |||
| et al | |||
| Comparison of visual and turbidimetric methods for determining short-term compatibiiity of intravenous critical-care drugs // American Journal of Hospital Pharmacy, 1988, V.45, pp.2361-2366. | |||
Авторы
Даты
2023-01-31—Публикация
2022-11-07—Подача