Область техники
Данное изобретение относится к применению гликоалкалоидов, таких как соласонин и соламаргин, при лечении рака, такого как рак кожи, а также к композициям для применения при таком лечении. Более конкретно, данное изобретение относится к обеспечению улучшенной, по существу стабильной лекарственной формы гликоалкалоидов, которая минимизирует или снижает разложение указанных активных молекул.
Уровень техники
Цитотоксическая химиотерапия остается одним из главных вариантов лечения для борьбы с раком. Однако эффективность химиотерапии ограничена тем фактом, что не все опухоли отвечают оптимальным образом. Таким образом, однонаправленная химиотерапия с применением существующих лекарств нечасто приводит к исцелению. Кроме того, при использовании только одного агента часто возникают опухолевые клетки, устойчивые к лекарству. Более того, большинство стандартных химиотерапевтических препаратов действуют на все быстро делящиеся нормальные и раковые клетки, и они были изначально идентифицированы благодаря уничтожению клеток в целом, посредством процесса, известного как бессистемная цитотоксичность. Таким образом, стандартные химиотерапевтические средства не являются избирательными и имеют низкий профиль безопасности.
Апоптоз представляет собой форму клеточной гибели, в котором запрограммированная последовательность событий приводит к уничтожению клеток без высвобождения вредных веществ в окружающее пространство. Апоптоз уничтожает старые клетки, ненужные клетки и пораженные клетки. Каждый день в организме человека апоптозу подвергаются около 50 миллиардов клеток. Для каждой нормальной клетки существует определенное время для жизни и время для гибели. Если апоптоз не срабатывает должным образом, то клетки, которые должны быть уничтожены, могут сохраняться и становиться бессмертными, например, в раковом образовании. Рак может начинаться в любом месте организма. Он возникает, когда клетки растут бесконтрольно и вытесняют нормальные клетки. В раковых клетках процесс апоптоза отсутствует, но деление клеток сохраняется, что приводит к избыточному количеству раковых клеток, склонных к распространению в другие части тела (метастаз).
Прицельные терапевтические средства, вызывающие апоптоз, в настоящее время являются ориентиром для большинства работ в области создания противораковых лекарств. Другие прицельные терапии могут включать агенты, которые вызывают гибель клеток посредством онкоза (ишемической гибели клеток) и/или некроза.
Таким образом, большой интерес для лечения рака вызывают отдельные вещества или комбинации, которые могут вызывать гибель раковых клеток.
Гликоалкалоиды представляют собой конъюгированные формы стероидных алкалоидов, которые содержат сахарный фрагмент, связанный с алкалоидным фрагментом. Сахарный фрагмент может представлять собой моносахарид, дисахарид, олигосахарид или полисахарид. Установлено, что некоторые гликоалкалоиды, полученные из растений, являются ядовитыми или обладают противораковыми свойствами.
Например, соласодин [(3β,22α,25R)-спирозол-5-ен-3-ол] представляет собой химическое соединение стероидного алкалоида пасленового типа со скелетом С27 холестана, которое встречается в растениях семейства Solanaceae. Химическая структурная формула соласодина представлена ниже.
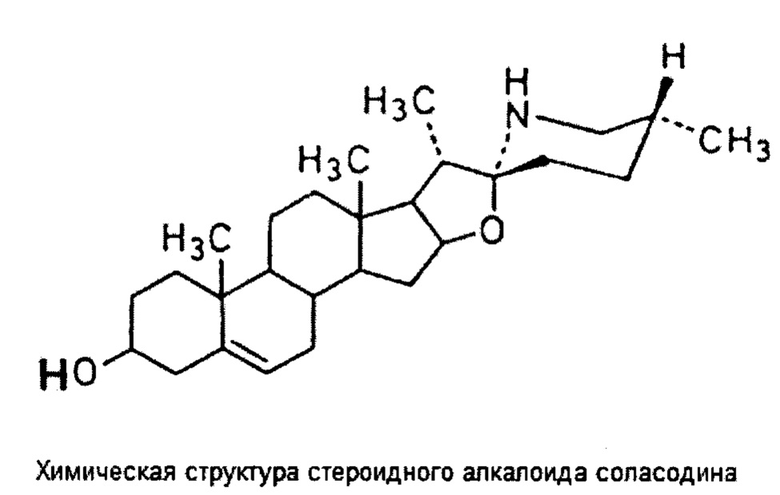
И соласонин [(22R,25R)-спиро-5-ен-3β-ил-α-L-рамнопиранозил-(1->2gal)-O-β-D-глюкопиранозил-(1->3gal)-β-D-галактопираноза], и соламаргин [(22R,25R)-спиро-5-ен-3β-ил-α-L-рамнопиранозил-(1->glu)-O-α-L-рамнопиранозил-(1->4glu)-β-D-глюкопираноза] представляют собой производные гликоалкалоидных конъюгатов соласодина и состоят из рамнозидов соласодина (SR).
Соласонин представляет собой тригликозидный конъюгат, содержащий фрагменты рамнозы, глюкозы и галактозы. Соламаргин также представляет собой тригликозидный конъюгат, но содержит два фрагмента рамнозы и один фрагмент глюкозы.
По своей сути, сахарные (т.е. гликозидные) фрагменты гликоалкалоидов-производных соласодина могут состоять из моно-, ди- и тригликозидов. Смесь таких природных гликоалкалоидов-производных соласодина идентифицирована в плодах Solatium Sodomaeum L., который является видом пасленового растения, известным как дурман обыкновенный. Указанная смесь экстрагирована из плодов дурмана обыкновенного и обозначена как ВЕС. Указанная смесь гликоалкалоидов состоит из 33% тригликозида соласонина, 33% тригликозида соламаргина и 34% их соответствующих моно- и дигликозидов, т.е. моно- и дигликозидов соласодина. Другими словами, все гликозиды в указанной смеси содержат один и тот же агликон, соласодин. Показано, что гликоалкалоиды из указанной смеси являются активными против рака у животных, а также против кожных опухолей у человека.
Гликоалкалоиды SR направленно воздействуют на определенные мутантные (измененные) белки в ряде раковых клеток.
ВЕС® и CORAMSINE® (например, компании Solbec Pharmaceuticals Ltd) представляют собой смеси соласонина и соламаргина с противораковыми свойствами. CORAMSINE® состоит из двух соласодиновых гликоалкалоидов, соласонина и соламаргина в соотношении 1:1 (мас./мас), т.е. без моно- и дигликозидов соласодина, которые встречаются в смеси ВЕС®. Существует ряд других доступных химиотерапевтических агентов с различным механизмом действия. Они включают противоопухолевые антибиотики, антимитотические агенты, гормоны, антиангиогенные лекарства, цитокины, антиметаболиты и алкилирующие агенты.
Существует потребность в новых и эффективных лекарственных комбинациях, которые можно использовать для подавления роста раковых клеток или предпочтительно уничтожать (например, посредством киллинга) раковые клетки и, следовательно, эффективно лечить рак. Данное изобретение направлено на повышение эффективности и/или результативности лечения пациента, достигаемой с применением монотерапии CORAMSINE® или ВЕС®, с помощью комбинированной терапии с другими химиотерапевтическими агентам, например, с другим механизмом(-ами) действия, отличным от механизма действия SR гликоалкалоидов.
Эффективность любого противоракового/противоопухолевого агента при лечении рака зависит не только от типа и/или количества используемого противоракового агента, но и от состава используемой терапевтической лекарственной формы. Например, концентрации гликоалкалоидов, необходимые для достижения терапевтической эффективности для кожи, могут быть на несколько порядков больше, чем концентрации, которые необходимы для тех же гликоалкалоидов для достижения терапевтической эффективности в исследованиях на культурах раковых клеток. Одной из причин этого является то, что в исследованиях на клеточных культурах используемая среда обычно представляет собой суспензию, а в случае рака кожи у пациентов среда может быть более густой, полутвердой кремовой консистенции.
Следует понимать, что для исследований в клеточных культурах приведение в контакт (биодоступность) активного ингредиента с раковыми клетками является гораздо более полным, чем в случае активного ингредиента в форме крема, наносимого на раковые клетки кожи тела человека.
Таким образом, данное изобретение направлено на обеспечение гликоалкалоидов и их лекарственных форм для взаимодействия с клетками-мишенями, которые можно использовать для облегчения действия рака и опухолей у млекопитающих, и которые могут по меньшей мере частично преодолевать один или более из вышеуказанных недостатков или обеспечивать людей применимой альтернативой.
Условия хранения кристаллических, полукристаллических и порошкообразных рамнозидов соласодина рассмотрены ранее (WO 200061153А1). Однако стабильность гликоалкалоидов в растворах, гелях и кремах не описана ранее.
В предыдущей работе было показано, что при нормальных условиях хранения может происходить некоторое разложение гликоалкалоидов в чистой или получистой кристаллической или полукристаллической форме. После хранения свободные сахара, образовавшиеся во время хранения, необходимо удалять до применения гликоалкалоидов, находившихся на хранении, при составлении терапевтических композиций во избежание снижения противораковой эффективности. Несмотря на то, что разложение противоопухолевых препаратов было незначительным при хранении рамнозидов соласодина в течение короткого периода времени, наблюдали существенное снижение противоопухолевой активности, которое было обусловлено свободными сахарами, образовавшимися в результате сегрегации рамнозидов соласодина.
Соответственно, данное изобретение направлено также на обеспечение улучшенной, по существу стабильной лекарственной формы конъюгатов гликоалкалоидов, которая обеспечивает снижение разложения указанных активных молекул, присутствующих в лекарственной форме.
Сущность изобретения
В работе, которая легла в основу данного изобретения, автор данной заявки стремился к идентификации лекарственных форм гликоалкалоидных композиций, которые, например, могут быть пригодными для местного применения для лечения кожных заболеваний, таких как рак кожи и/или опухолевый рост на коже, и для минимизации или уменьшения нежелательного гидролиза гликоалкалоидов в лекарственной форме, приводящего к высвобождению свободных (неконъюгированных) сахаров (таких как рамнозные сахариды) из гликоалкалоидов в лекарственную форму. Автор данной заявки предположил, что такие улучшенные лекарственные формы будут иметь положительный результат благодаря улучшенной терапевтической эффективности по меньшей мере по двум причинам. Во-первых, уменьшение гидролиза гликоалкалоида в лекарственной форме может обеспечивать сохранение количества или концентрации активного (не гидролизованного) гликоалкалоида в лекарственной форме, достаточной для достижения терапевтического эффекта даже после продолжительного периода хранения лекарственной формы. И во-вторых, минимизация или уменьшение образования свободных сахарных фрагментов в лекарственной форме может усиливать терапевтическую эффективность не гидролизованных гликоалкалоидов, присутствующих в лекарственной форме, inter alia посредством уменьшения конкуренции свободных сахаров за белки, связывающие гликоалкалоидные рецепторы, которые могут экспрессироваться пораженными клетками, тем самым минимизируя или уменьшая ингибирующее действие свободных сахаров, которое они оказывают на терапевтическую эффективность не гидролизованных гликоалкалоидов в лекарственной форме.
Кроме того, в работе, которая легла в основу данного изобретения, автор заявки стремился идентифицировать химиотерапевтические агенты, которые можно использовать в комбинации с гликоалкалоидами по данному изобретению, посредством чего указанная комбинация(-ии) обеспечит преимущественный синергетический эффект на лечение одного или более заболеваний, связанных с раком(-ами) или опухолями. Например, такие химиотерапевтические агенты можно использовать в качестве дополнительных компонентов в комбинации с гликоалкалоидами в терапевтических композициях по данному изобретению.
Соответственно, в одном широком аспекте данного изобретения предложена улучшенная, по существу стабильная местная лекарственная форма конъюгатов гликоалкалоидов, которая минимизирует или уменьшает разложение указанных активных молекул. Композиции по данному изобретению в соответствии с данным широким аспектом, в общем, пригодны для введения пациентам в виде геля или крема, и/или их можно адаптировать для местного введения.
Соответственно, в одном примере данного изобретения предложена композиция для местного применения, содержащая по меньшей мере гликоалкалоид, по меньшей мере один модификатор вязкости и по меньшей мере один кератолитический агент.
Гликоалкалоид, используемый в композиции по данному изобретению, выбран из группы, содержащей любые гликоалкалоиды формулы I:
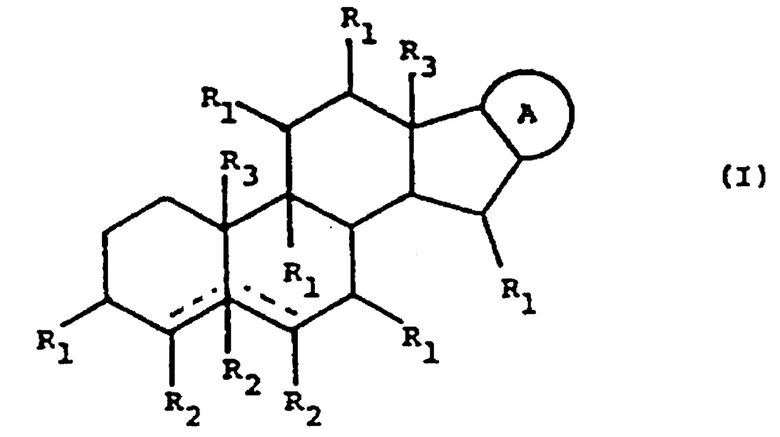
где:
каждая пунктирная линия независимо выбрана из одинарной связи и двойной связи, так что либо обе пунктирные линии представляют собой двойные связи, либо одна из пунктирных линий представляет собой двойную связь, а другая пунктирная линия представляет собой одинарную связь, либо обе пунктирные линии представляют собой одинарные связи;
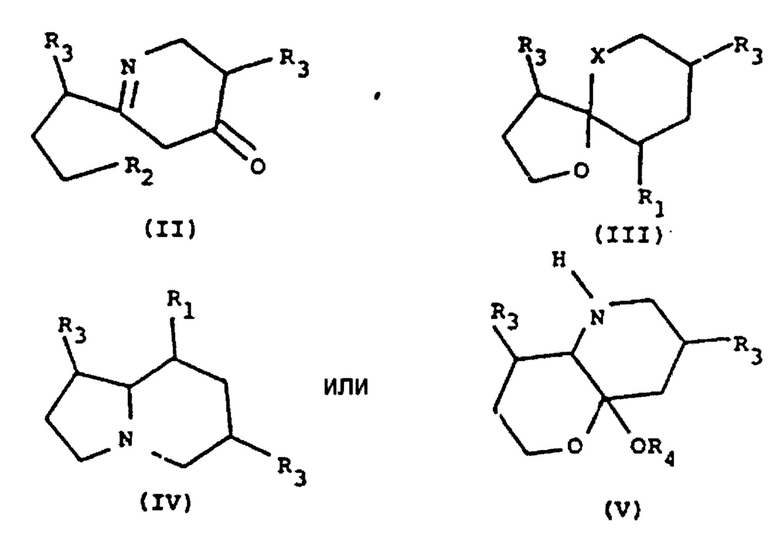
А: представляет собой радикал, выбранный из следующих радикалов, имеющих общие формулы (II) - (V):
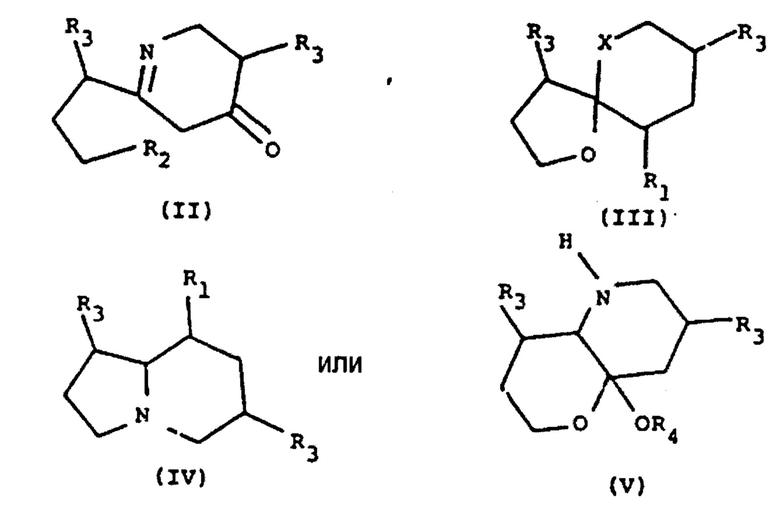
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино, оксо и OR4;
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино и OR4;
каждый из R3 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, алкила и R4-алкилена;
каждый из R4 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, углевода и углеводного производного;
«X» представляет собой радикал, выбранный из группы, содержащей -СН2-, -О- и -NH2-; и
при этом указанное гликоалкалоидное соединение содержит по меньшей мере одну группу R4, где R4 представляет собой углевод или его производное, выбранное из группы, состоящей из: глицеринового альдегида, глицерозы, эритрозы, треозы, рибозы, арабинозы, ксилозы, ликсозы, альтрозы, аллозы, гулозы, маннозы, глюкозы, идозы, галактозы, талозы, рамнозы, дигидроксиацетона, эритрулозы, рибулозы, ксилулозы, псикозы, фруктозы, сорбозы, тагатозы и других гексоз, гептоз, октоз, наноз, декоз, дезоксисахаров с разветвленными цепями (например, апиоза, гамамелоза, стрептоза, кордицепоза, микароза и кладиноза), соединений, в которых альдегидные, кетоновые или гидроксильные группы замещены (например, N-ацетил, ацетил, метил, замещение СН2ОН), сахарных спиртов, сахарных кислот, бензимидазолов, енольных солей углеводов, сахариновых кислот и фосфатов сахаров.
В одном примере указанная композиция может содержать множество различных гликоалкалоидов, выбранных из формулы 1. Если композиция содержит только один гликоалкалоид, то указанный гликоалкалоид присутствует в композиции в терапевтически эффективном количестве. Если в композиции содержатся несколько гликоалкалоидов, то каждый гликоалкалоид может присутствовать в субтерапевтическом количестве, но указанные два или более гликоалкалоидов в комбинации оказывают терапевтический эффект.
Кроме того, указанная композиция также может содержать второй компонент в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия. Предпочтительно, второй компонент представляет собой митотический ингибитор, алкилирующий агент или антибиотик.
Модификатор вязкости может быть любым пригодным модификатором вязкости или может быть гелеобразующим агентом и/или модификатором вязкости, не содержащим рамнозу, выбранным из группы, состоящей из: гуаровой камеди, камеди бобов рожкового дерева, ксантановой камеди, желатина, полоксамера, карбомера и производных целлюлозы. В предпочтительном варианте реализации по меньшей мере один модификатор вязкости представляет собой ксантановую камедь.
По меньшей мере один кератолитический агент может быть любым пригодным кератолитическим агентом. В одном варианте реализации кератолитический агент выбран из группы, состоящей из: альфа-гидроксикислот, выбранных из: гликолевой кислоты, молочной кислоты, яблочной кислоты, лимонной кислоты и винной кислоты; бета-гидроксикислот, выбранных из: салициловой кислоты, 3-гидроксипропионовой кислоты, бета-гидроксимасляной кислоты, бета-гидрокси-бета-метилбутирата и карнитина; азелаиновой кислоты, пероксида бензоила, мочевины, трихлоруксусной кислоты (ТСА), карболовой кислоты (фенол), кротонового масла, ацетона и серы. В предпочтительном варианте реализации по меньшей мере один кератолитический агент выбран из группы, состоящей из: молочной кислоты, салициловой кислоты и мочевины. В другом варианте реализации указанная композиция содержит кератолитический агент, содержащий по меньшей мере одну альфа-гидроксикислоту, описанную в данном документе, и может дополнительно содержать кератолитический агент, содержащий по меньшей мере одну бета-гидроксикислоту, описанную в данном документе. Например, указанная композиция может содержать молочную кислоту, салициловую кислоту и мочевину.
Например, действующая композиция может состоять из около 0,2-2% мас./мас. ксантановой камеди, около 5-10% мас./мас. молочной кислоты, около 5-10% мас./мас. салициловой кислоты и около 3-5% мас./мас. мочевины. В альтернативном варианте реализации композиция может содержать около 1% мас./мас. ксантановой камеди, около 10% мас./мас. молочной кислоты, около 10% мас./мас. салициловой кислоты и около 5% мас./мас. мочевины.
В одном варианте реализации композиция представляет собой гель или крем, и/или предназначена для местного введения.
В другом варианте реализации указанная композиция по существу не содержит свободных сахаридов такого типа, которые могут ингибировать взаимодействие между гликоалкалоидами и их клеткой-мишенью. Например, композиция по существу не содержит свободных рамнозных сахаридов или рамнозоподобных молекул.
В данном контексте следует понимать, что термин «свободный сахарид» относится к любому сахариду, такому как моно-, ди-, три-, олиго- или полисахарид, или его производному, которое не связано с алкалоидом.
Во втором широком аспекте данного изобретения предложен способ получения или производства композиции для местного применения, описанной в данном документе в соответствии с первым широким аспектом. Указанный способ может включать комбинирование и/или смешивание, и/или растворение терапевтически эффективного количества гликоалкалоида или множества различных гликоалкалоидов, например, где каждый гликоалкалоид выбран из группы гликоалкалоидов формулы I, описанной выше в данном документе, с определенным количеством по меньшей мере одного регулятора вязкости и с определенным количеством по меньшей мере одного кератолитического агента. Например, если указанный способ включает комбинирование и/или смешивание, и/или растворение только одного гликоалкалоида, то указанный гликоалкалоид необходимо комбинировать и/или смешивать, и/или растворять в терапевтически эффективном количестве. Альтернативно, если для получения композиции комбинированию и/или смешиванию, и/или растворению подлежат несколько различных гликоалкалоидов, то каждый из различных типов гликоалкалоидов можно комбинировать и/или смешивать, и/или растворять в субтерапевтическом количестве, но указанные два или более различных гликоалкалоидов в комбинации должны иметь терапевтический эффект.
Например, способ согласно данному аспекту включает растворение, комбинирование и/или смешивание гликоалкалоида в фармацевтически приемлемом носителе, разбавителе и/или вспомогательном веществе, пригодном для локальной доставки композиции. Например, носитель, разбавитель и/или вспомогательное вещество может быть водным или неводным. В одном таком примере фармацевтически приемлемый носитель, вспомогательное вещество и/или разбавитель содержит любой один или оба из указанного по меньшей мере одного модификатора вязкости и указанного по меньшей мере одного кератолитического агента.
В одном варианте реализации способ получения композиции для местного применения согласно данному аспекту может дополнительно включать комбинирование и/или смешивание, и/или растворение второго компонента в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия.
В другом варианте реализации способ получения композиции для местного применения согласно данному аспекту может дополнительно включать удаление, например, из любой полученной комбинации, или смеси, или композиции свободных сахаридов, которые могут ингибировать взаимодействие между гликоалкалоидами и их клеткой-мишенью. Например, указанный способ может включать удаление из любой полученной комбинации, или смеси, или композиции свободных рамнозных сахаридов или рамнозоподобных молекул.
В третьем широком аспекте данного изобретения предложена композиция для местного применения, полученная осуществлением способа в соответствии с указанным вторым широким аспектом, описанным выше в данном документе.
В четвертом широком аспекте данного изобретения также предложен способ лечения опухолевого роста, включающий стадию введения терапевтически эффективного синергетического количества композиции, описанной в данном документе. В пятом широком аспекте данного изобретения дополнительно предложен способ лечения пациента, имеющего или страдающего от кожного заболевания, связанного с раком, вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями, и/или псориаза. Указанный способ включает местное введение указанному пациенту терапевтически эффективного количества местной композиции по любому аспекту изобретения, описанного в данном документе.
В одном варианте реализации стадия введения включает нанесение терапевтически эффективного количества указанной композиции на область болезненного состояния пациента. Например, указанный способ включает местное нанесение указанной композиции на кожу пациента. В одном таком примере пациент имеет или страдает от рака кожи и/или опухоли кожи, и указанный способ включает местное нанесение терапевтически эффективного количества указанной композиции на ту область кожи пациента, которая содержит рак кожи и/или опухоль кожи. В другом примере пациент имеет или страдает от кожного заболевания, связанного с вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями, и/или псориаза, и указанный способ включает местное нанесение терапевтически эффективного количества указанной композиции на ту область кожи пациента, которая содержит инфицированные, воспаленные и/или пораженные клетки кожи в результате инфекционных, воспалительных заболеваний и/или псориаза. Предпочтительно, пациентом является человек.
Следует понимать, что термин «пациент» в данном контексте, в соответствии с любым аспектом, вариантом реализации и/или примером данного изобретения, описанный в данном контексте, включает субъекта-человека.
В шестом широком аспекте данного изобретения дополнительно предложено применение композиции для местного применения по любому из аспектов, описанных в данном документе, при местном лечении кожного заболевания, связанного с раком, вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями, и/или псориаза.
В седьмом широком аспекте данного изобретения также предложено применение композиции по любому из аспектов, описанных в данном документе, в производстве местного лекарственного средства для местного лечения кожного заболевания, связанного с раком, вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями, и/или псориаза. В восьмом широком аспекте данного изобретения дополнительно предложено применение по меньшей мере гликоалкалоида, по меньшей мере одного модификатора вязкости и по меньшей мере одного кератолитического агента в производстве местного лекарственного средства для лечения кожного заболевания, связанного с раком, вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями, и/или псориаза. В одном примере лекарственное средство составлено для местного нанесения на кожу пациента, имеющего или страдающего от указанного кожного заболевания. Например, лекарственное средство предназначено для лечения рака кожи и/или опухоли кожи у пациента, и указанное лекарственное средство составлено для нанесения на ту область кожи пациента, которая содержит рак кожи и/или опухоль кожи.
В одном варианте реализации гликоалкалоид, используемый в указанном лекарственном средстве, выбран из группы, содержащей гликоалкалоиды формулы I:
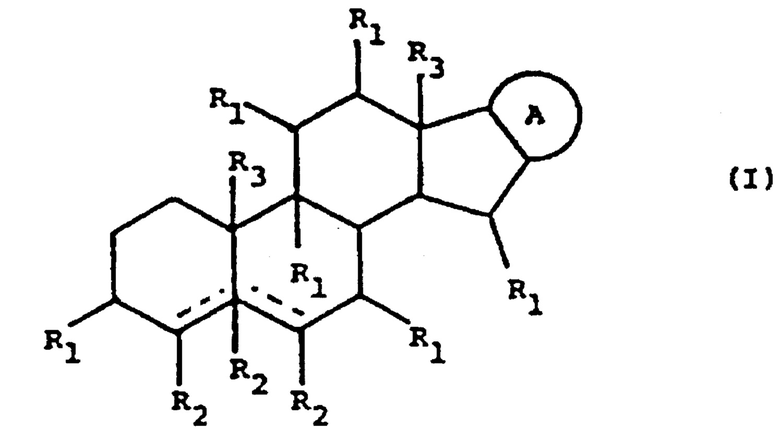
где:
каждая пунктирная линия независимо выбрана из одинарной связи и двойной связи, так что либо обе пунктирные линии представляют собой двойные связи, либо одна из пунктирных линий представляет собой двойную связь, а другая пунктирная линия представляет собой одинарную связь, либо обе пунктирные линии представляют собой одинарные связи;
А: представляет собой радикал, выбранный из следующих радикалов, имеющих общие формулы (II) - (V):
каждый из R1 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино, оксо и OR4;
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино и OR4;
каждый из R3 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, алкила и R4-алкилена;
каждый из R4 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, углевода и углеводного производного;
«X» представляет собой радикал, выбранный из группы, содержащей -СН2-, -О- и -NH2-; и
где указанное гликоалкалоидное соединение содержит по меньшей мере одну группу R4, где R4 представляет собой углевод или его производное, выбранное из группы, состоящей из глицеринового альдегида, глицерозы, эритрозы, треозы, рибозы, арабинозы, ксилозы, ликсозы, альтрозы, аллозы, гулозы, маннозы, глюкозы, идозы, галактозы, талозы, рамнозы, дигидроксиацетона, эритрулозы, рибулозы, ксилулозы, псикозы, фруктозы, сорбозы, тагатозы и других гексоз, гептоз, октоз, наноз, декоз, дезоксисахаров с разветвленными цепями (например, апиоза, гамамелоза, стрептоза, кордицепоза, микароза и кладиноза), соединений, в которых альдегидные, кетоновые или гидроксильные группы замещены (например, N-ацетил, ацетил, метил, замещение СН2ОН), сахарных спиртов, сахарных кислот, бензимидазолов, енольных солей углеводов, сахариновых кислот и фосфатов сахаров.
В одном варианте реализации указанное лекарственное средство содержит множество гликоалкалоидов, выбранных из формулы I.
В другом варианте реализации указанное лекарственное средство содержит второй компонент в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия.
В другом варианте реализации по данному аспекту указанный модификатор вязкости выбран из группы, состоящей из: гуаровой камеди, камеди бобов рожкового дерева, ксантановой камеди, желатина, полоксамера, карбомера и производных целлюлозы. Например, модификатор вязкости представляет собой ксантановую камедь.
В другом варианте реализации по данному аспекту указанный кератолитический агент выбран из группы, состоящей из: альфа-гидроксикислот, выбранных из: гликолевой кислоты, молочной кислоты, яблочной кислоты, лимонной кислоты и винной кислоты; бета-гидроксикислот, выбранных из: салициловой кислоты, 3-гидроксипропионовой кислоты, бета-гидроксимасляной кислоты, бета-гидрокси-бета-метилбутирата и карнитина; азелаиновой кислоты, пероксида бензоила, мочевины, трихлоруксусной кислоты (ТСА), карболовой кислоты (фенол), кротонового масла, ацетона и серы. Например, указанная композиция содержит кератолитический агент, содержащий по меньшей мере одну альфа-гидроксикислоту, описанную в данном документе, и может дополнительно содержать кератолитический агент, содержащий по меньшей мере одну бета-гидроксикислоту, описанную в данном документе. Например, кератолитический агент выбран из группы, состоящей из: молочной кислоты, салициловой кислоты и мочевины. В одном примере указанная композиция может содержать молочную кислоту, салициловую кислоту и мочевину.
В другом варианте реализации по данному аспекту указанное лекарственное средство содержит около 0,2-2% мас./мас. ксантановой камеди, около 5-10% мас./мас. молочной кислоты, около 5-10% мас./мас. салициловой кислоты и около 3-5% мас./мас. мочевины. В другом варианте реализации по данному аспекту указанное лекарственное средство содержит около 1% мас./мас. ксантановой камеди, около 10% мас./мас. молочной кислоты, около 10% мас./мас. салициловой кислоты и около 5% мас./мас. мочевины. В другом варианте реализации по данному аспекту указанное лекарственное средство составлено в виде геля или крема, и/или предназначено для местного введения. В другом варианте реализации по данному аспекту указанное лекарственное средство по существу не содержит свободных сахаридов такого типа, которые могут ингибировать взаимодействие между гликоалкалоидами и их клеткой-мишенью. Например, указанное лекарственное средство по существу не содержит свободных рамнозных сахаридов или рамнозоподобных молекул.
Краткое описание графических материалов
На чертеже представлено графическое изображение, демонстрирующее влияние добавления свободной рамнозы (5 мМ) и повышающихся концентраций (0, 5, 10, 15 и 20 мкМ) композиции экстракта ВЕС на процент выживания клеток злокачественной меланомы. Свободная рамноза демонстрирует защитный эффект против действия противораковых соединений ВЕС.
Подробное описание изобретения
Общая информация
Специалистам в данной области техники понятно, что в отношении изобретения, описанного в данном документе, могут быть сделаны различные вариации и модификации, отличные от специально описанных, без отступления от его сущности и объема. Данное изобретение включает все такие вариации и модификации. Данное изобретение также включает все стадии, признаки, композиции, компоненты, аспекты, примеры и варианты реализации, упомянутые или указанные в данном описании, отдельно или в совокупности, и любые и все комбинации любых двух или более из указанных стадий или признаков.
Каждый документ, ссылка, патентная заявка или патент, указанные в данном контексте, выше или ниже по тексту, полностью включены в данный документ в явном виде посредством ссылки, что означает, что их следует читать и рассматривать как часть данного текста. То есть документ, ссылка, патентная заявка или патент, цитированный в данном контексте, в данном контексте не приведен повторно исключительно для лаконичности.
Любые инструкции производителя, описания, спецификации продуктов и технологические карты для любых продуктов, упомянутых в данном документе или в любом документе, включенном посредством ссылки, также включены в данный документ посредством ссылки, и их можно использовать при практическом осуществлении данного изобретения.
Данное изобретение не ограничено объемом любых конкретных аспектов, вариантов реализации или примеров, описанных в данном документе, которые предназначены лишь для целей иллюстрации. Функционально эквивалентные продукты, композиции веществ, лекарственные формы и способы в явном виде входят в объем изобретения, описанного в данном документе.
Определения некоторых терминов, использованных в данном контексте, приведены в подробном описании данного изобретения и относятся ко всему тексту. Если не указано иное, все другие научные и технические термины, используемые в данном документе, имеют то же значение, которое обычно подразумевается специалистом в области, к которой относится данное изобретение.
Например, вариант реализации и аспект, описанный в данном документе, можно применять с соответствующими поправками в отношении каждого и всех остальных примеров, вариантов реализации и аспектов, если специально не указано иное.
Определения
В тексте данного описании и формулы изобретения, если контекстом не требуется иное, то термин «содержит» или его варианты, такие как «содержащий» следует понимать как включение указанной стадии, или элемента, или целого числа, или группы стадий, или элементов, или целых чисел, но не исключение любой другой стадии, или элемента, или целого числа, или группы стадий, или элементов, или целых чисел. Следует понимать, что могут быть сделаны различные модификации и изменения в отношении вариантов реализации, описанных в данном документе, без отступления от сущности и объема изобретения, описанного в данном документе.
В настоящем описании, если не указано иное или контекстом не требуется иное, то ссылка на одну стадию, композицию или вещество, группу стадий или группу композиций вещества, включает одну и множество (т.е. одну или более) таких стадий, композиций или вещества, групп стадий или групп композиций вещества. Следует отметить, что в данном контексте и в прилагаемой формуле изобретения формы единственного числа включают ссылку на множественное число, если из контекста очевидно не следует иное. Так, например, ссылка на «гликоалкалоид», или «конъюгат гликоалкалоида», или «конъюгат соласодина» включает множество таких гликоалкалоидов, конъюгатов гликоалкалоидов или конъюгатов соласодина и т.д.
Термин «по существу стабильный» в тексте данного описания в отношении стабильности композиций, лекарственных форм и лекарственных средств по данному изобретению следует понимать как означающий, что содержание или концентрация по меньшей мере около 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% описанного активного ингредиента(-ов) в указанной лекарственной форме, или композиции, или лекарственном средстве сохраняет свою структурную целостность и остается не гидролизованной или не подверженной разложению в указанной лекарственной форме, или композиции, или лекарственном средстве относительно содержания или концентрации описанного активного ингредиента(-ов) в форме готового состава по истечении по меньшей мере 3 месяцев, более предпочтительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев или по меньшей мере 2 лет, или по меньшей мере 3 лет, или по меньшей мере 4 лет. В некоторых вариантах реализации по существу стабильная композиция или лекарственная форма является такой, в которой концентрация или содержание по меньшей мере около 90% описанного активного ингредиента(-ов) в указанной лекарственной форме, или композиции, или лекарственном средстве остается не гидролизованной или не подверженной разложению в указанной лекарственной форме, или композиции, или лекарственном средстве относительно концентрации или содержания активного ингредиента в форме готового состава по истечении по меньшей мере 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев или по меньшей мере 2 лет, или по меньшей мере 4 лет.
Например, концентрацию или содержание описанного активного ингредиента(-ов) в лекарственной форме, или композиции, или лекарственном средстве, которое остается не гидролизованным или не подверженным разложению в указанной лекарственной форме, или композиции, или лекарственном средстве, определяют после хранения лекарственной формы, или композиции, или лекарственного средства при комнатной температуре или 25°С и необязательно при относительной влажности 60% в течение по меньшей мере 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев или по меньшей мере 2 лет, или по меньшей мере 4 лет с момента производства лекарственной формы, или композиции, или лекарственного средства.
Например, «по существу стабильную» композицию, лекарственную форму и лекарственное средство по данному изобретению следует понимать как включающие такие композиции, лекарственные формы и лекарственные средства, в которых содержание или концентрация по меньшей мере 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гликоалкалоидов, входящих в состав указанных лекарственных форм, композиций или лекарственных средств, остается в форме конъюгатов, негидролизованных или не подверженных распаду или разложению на их соответствующий агликон соласодина и фрагменты свободного сахара(-ов) (т.е. по меньшей мере около 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гликоалкалоидов не подвержены разложению с высвобождением свободных сахаридов, таких как свободные рамнозные сахариды или рамнозоподобные молекулы) по истечении по меньшей мере 3 месяцев, более предпочтительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев или по меньшей мере 2 лет, или по меньшей мере 3 лет, или по меньшей мере 4 лет. В некоторых примерах концентрация или содержание по меньшей мере около 90% гликоалкалоидов, входящих в состав лекарственных форм, композиций или лекарственных средств, остается в форме их конъюгатов по истечении по меньшей мере 3 месяцев, более предпочтительно 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев или по меньшей мере 2 лет, или по меньшей мере 3 лет, или по меньшей мере 4 лет. Например, содержание или концентрацию гликоалкалоидов, которые остаются в форме их конъюгатов, определяют после хранения композиции, лекарственной формы или лекарственного средства при комнатной температуре или 25°С в течение вышеуказанного периода.
Альтернативно или дополнительно, термин «по существу стабильная» в отношении композиции, лекарственной формы и лекарственного средства по данному изобретению следует понимать как включающий указанные композиции, лекарственные формы и лекарственные средства, которые по существу не содержат свободных сахаридов такого типа, которые ингибируют взаимодействие между гликоалкалоидами и их клеткой-мишенью, таких как рамнозные сахариды или рамнозоподобные молекулы. Например, указанное лекарственное средство по существу не содержит свободных рамнозных сахаридов или рамнозоподобных молекул.
При использовании в данном описании термин «производное» или «получен из» следует понимать как обозначение того, что определенное целое может быть получено из конкретного источника, хотя не обязательно из указанного источника.
Для упрощения описания изобретения термины «гликоалкалоид», «конъюгат соласодина» и «рамнозид соласодина (SR)» использованы взаимозаменяемо. Они использованы в данном контексте для обозначения любого соединения, которое содержит молекулу соласодина и по меньшей мере один остаток рамнозы.
Термин «рамноза» означает дезоксисахар на основе сахарида общей формулы С6Н12О5. Для целей данного описания и формулы изобретения, если специально не указано иное, термин «рамноза» включает рамнозу формулы С6Н12О5, а также ее функциональные производные.
Термин «замещенная рамноза» означает остаток рамнозы, который содержит по меньшей мере одну гидроксильную группу, замещенную по меньшей мере одной алкильной группой. Например, гидроксильная группа может быть замещена метальной группой. Термин «замещенный рамнозид соласодина» означает конъюгат соласодина по данному изобретению, содержащий по меньшей мере одну замещенную рамнозу.
Для упрощения описания данного изобретения термины «углевод» и «сахарид» использованы в данном контексте для обозначения любого соединения, которое можно объективно сконструировать так, чтобы оно имело эмпирическую формулу CnH2nOn (где n представляет собой положительное число). Указанные термины включают моносахариды, дисахариды, олигосахариды и полисахариды, такие как сахара, крахмал и целлюлоза и т.д. Термин «модификатор вязкости» означает любой агент, который может обеспечивать регулирование, изменение или контролирование вязкости субстрата, такого как (но не ограничиваясь этим) жидкость, крем или гель. Термин «вязкость» соответствует неформальной концепции «густоты».
В данном описании и формуле изобретения термин «свободный сахарид» относится к любому сахариду, такому как моно-, ди-, три-, олиго- или полисахарид, или его производному, которое не связано с алкалоидом.
Специальная информация
Предыдущей работе автора данного изобретения, рассмотренной в WO 2000061153А1, описано, что свободные сахара (сахара, не конъюгированные с гликоалкалоидами) в препаратах экстрагированных полукристаллических гликоалкалоидов ВЕС необходимо удалять из таких препаратов перед их введением в эффективные противораковые лекарственные формы. Это является необходимым, inter alia, поскольку при хранении полукристаллических препаратов ВЕС происходит некоторый гидролиз гликоалкалоидов, что приводит к высвобождению свободных фрагментов рамнозы. Это означает, что (i) активные гликоалкалоидные соединения (т.е. активные гликоалкалоидные молекулы, при их наличии) и (ii) свободная рамноза препятствуют противораковой эффективности оставшихся гликоалкалоидов, не подверженных гидролизу.
Остается неизвестным, как ведут себя промытые полукристаллические препараты ВЕС, не содержащие свободных сахаров, при введении в лекарственные формы, такие как, например, лекарственные формы для местного введения, такие как кремы или гели, для противоракового и/или другого терапевтического применения.
Данные автора заявки, представленные в следующих рабочих примерах, демонстрируют, что в терапевтических композициях гликоалкалоидов, таких как композиции, составленные для местного введения (например, кремы), также крайне желательно предотвращать гидролиз гликоалкалоидов и высвобождение свободных сахаров (таких как рамноза) в таких лекарственных формах.
Соответственно, на основании работы автора заявки, представленной в данном документе, автор данной заявки пришел к выводу, что, например, в отношении применения местных лекарственных форм (например, кремов или гелей) в терапии рака кожи и/или опухолей кожи, определенные ингредиенты, которые сами по себе повышают противораковую эффективность гликоалкалоидов в местных лекарственных формах, а также предотвращают разложение и стабилизируют противораковую активность гликоалкалоидов, будут иметь наибольшее преимущество для введения в такие лекарственные формы для достижения улучшенного и эффективного лечения рака кожи и/или опухолей кожи, например, в течение клинического периода.
Соответственно, на основании работы, представленной в настоящем документе, автор данной заявки пришел к выводу, что существует два требования для получения терапевтически эффективной лекарственной формы, такой как местная лекарственная форма (например, крем) гликоалкалоидов. Во-первых, лекарственная форма должна обеспечивать уменьшение или минимизацию гидролиза терапевтически активных гликоалкалоидов в лекарственной форме, чтобы сохранять активные гликоалкалоиды в лекарственной форме в соответствующем терапевтически эффективном (например, противораковом) количестве или концентрации. Во-вторых, лекарственная форма должна обеспечивать уменьшение, или минимизацию, или предотвращение высвобождения свободных сахаров, таких как свободная рамноза (т.е. в результате гидролиза гликоалкалоидов), поскольку свободные сахара, такие как рамноза, конкурируют с негидролизованными гликоалкалоидами за рецепторы на пораженных клетках (например, раковых или опухолевых клетках), тем самым снижая терапевтическую эффективность гликоалкалоидов при введении лекарственной формы пациенту или приведении ее в контакт с пораженными клетками (например, раковыми или опухолевыми клетками).
Результаты, представленные в следующих рабочих примерах, демонстрируют, что сахарные фрагменты свободной рамнозы (например, которые могут присутствовать в противораковой лекарственной форме гликоалкалоидов) препятствуют связыванию гликоалкалоидов с рамноза-связывающими белками (RBP), первоначально описанными как эндогенные эндоцитированные лектины (EEL). RBP представляют собой мутантные белки, которые, как было показано ранее, присутствуют на поверхности некоторых раковых клеток. Нормальные, нераковые клетки могут не иметь RBP или содержать их гораздо меньше, чем на раковых клетках. Не ограничиваясь какой-либо теорией или конкретным механизмом действия, автор данной заявки полагает, что гликоалкалоиды рамнозида соласодина (SR) по данному изобретению специфически связываются с RBP на раковых клетках, что приводит к интернализации гликоалкалоидов SR в раковые клетки. Затем, после интернализации в раковую клетку фрагмент соласодина, SR проявляет свою противоопухолевую активность, инициируя гибель раковых клеток, например, посредством каскадов, опосредованных апоптозом, ишемической гибелью клетки (также известной как онкоз) или некрозом. Соответственно, автор данной заявки пришел к выводу, что разработка противоракового лекарства, направленного на рецепторы RBP, может обеспечить дальнейшее развитие противораковой терапии.
Соответственно, в работе, которая легла в основу данного изобретения, автор данной заявки сделал предположение, что гликоалкалоиды SR по данному изобретению можно использовать, например, в качестве прицельной противораковой и/или противоопухолевой терапии, направленной на раковые и/или опухолевые клетки с рецепторами RBP. В работе, которая легла в основу данного изобретения, автор данной заявки дополнительно сделал предположение, что гликоалкалоиды SR. по данному изобретению имеют противораковый механизм действия, отличный от используемых в настоящее время химиотерапевтических агентов, таких как противоопухолевые антибиотики, антимитотические агенты, гормоны, антиангиогенные лекарства, цитокины, антиметаболиты и алкилирующие агенты. Таким образом, автор данной заявки сделал предположение, что гликоалкалоиды по данному изобретению можно использовать, inter alia, в качестве монотерапии против рака или в комбинации с вышеуказанными противоопухолевыми агентами.
Соответственно, в одном примере данного изобретения предложена композиция для местного применения, содержащая по меньшей мере гликоалкалоид, по меньшей мере один модификатор вязкости и по меньшей мере один кератолитический агент.Более конкретно, в данном изобретении предложена, например, улучшенная, по существу стабильная лекарственная форма конъюгатов гликоалкалоидов для местного применения, которая минимизирует или снижает разложение указанных активных молекул гликоалкалоидов. Композиции по данному изобретению, в общем, пригодны для введения пациентам в виде геля или крема, и/или их можно адаптировать для местного введения. Гликоалкалоид, используемый в композиции по данному изобретению, выбран из группы, содержащей любые гликоалкалоиды формулы I:
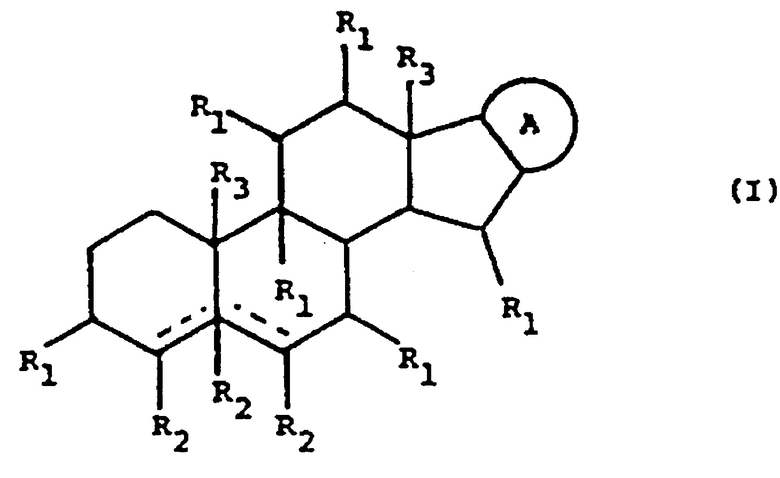
где:
каждая пунктирная линия независимо представляет собой одинарную связь или двойную связь, так что либо обе пунктирные линии представляют собой двойные связи, либо одна из пунктирных линий представляет собой двойную связь, а другая пунктирная линия представляет собой одинарную связь, либо обе пунктирные линии представляют собой одинарные связи;
А: представляет собой радикал, выбранный из следующих радикалов, имеющих общие формулы (II) - (V):
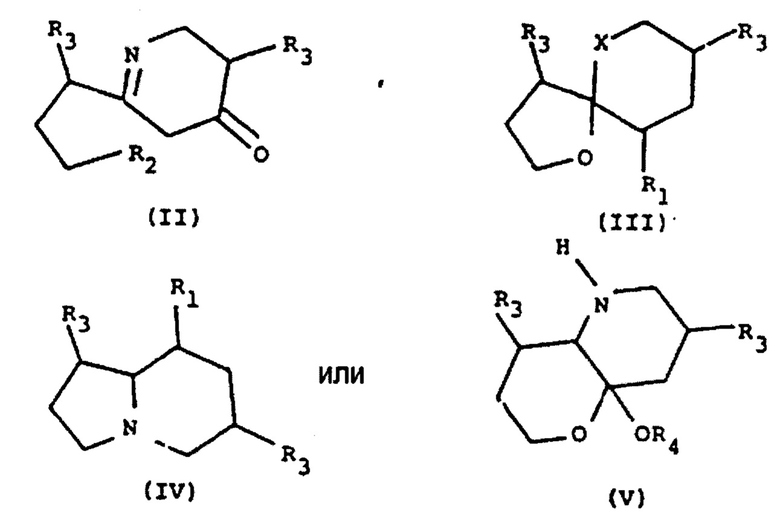
каждый из R1 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино, оксо и OR4;
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино и OR4;
каждый из R3 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, алкила и R4-алкилена;
каждый из R4 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, углевода и углеводного производного;
«X» представляет собой радикал, выбранный из группы, содержащей -СН2-, -О- и -NH2-; и
где указанное гликоалкалоидное соединение содержит по меньшей мере одну группу R4, где R4 представляет собой углевод или его производное, выбранное из группы, содержащей глицериновый альдегид, глицерозу, эритрозу, треозу, рибозу, арабинозу, ксилозу, ликсозу, альтрозу, аллозу, гулозу, маннозу, глюкозу, идозу, галактозу, талозу, рамнозу, дигидроксиацетон, эритрулозу, рибулозу, ксилулозу, псикозу, фруктозу, сорбозу, тагатозу и другие гексозы, гептозы, октозы, нанозы, декозы, дезоксисахара с разветвленными цепями (например, апиозу, гамамелозу, стрептозу, кордицепозу, микарозу и кладинозу), соединения, в которых альдегидные, кетоновые или гидроксильные группы замещены (например, N-ацетил, ацетил, метил, замещение CH2OH), сахарные спирты, сахарные кислоты, бензимидазолы, енольные соли углеводов, сахариновые кислоты и фосфаты сахаров.
В соответствии с данным примером, указанная композиция может содержать множество различных гликоалкалоидов, выбранных из формулы I. Если композиция содержит только один гликоалкалоид, то указанный гликоалкалоид присутствует в композиции в терапевтически эффективном количестве. Если в композиции содержатся несколько гликоалкалоидов, то каждый гликоалкалоид может присутствовать в субтерапевтическом количестве, но указанные два или более гликоалкалоидов в комбинации оказывают терапевтический эффект.
Гликоалкалоиды, используемые в указанной композиции, могут быть различными. Предпочтительно, указанные гликоалкалоиды представляют собой тригликозидные гликоалкалоиды, гликозиды соласодина или выбраны из группы гликоалкалоидов, состоящей из: соламаргина, соласонина, соланина, томатина, соланокапсина и 26-аминофуростана.
Гликоалкалоиды могут быть хиральными, могут представлять собой стереоизомеры и их смеси, включая энантиомеры и/или диастереоизомеры. Кроме того, гликоалкалоиды могут быть получены из природных источников, могут быть синтезированы или получены посредством химической модификации других гликоалкалоидов.
Количество используемых гликоалкалоидов может варьироваться, как и их относительные доли в указанной композиции. Однако если композиция содержит два гликоалкалоида, они могут присутствовать в соотношении, выбранном из группы соотношений, состоящей из приблизительно: 1:6 - 1:0,5; 1:5; 1:4; 1:3; 1:2, 1:1,5 и 1:1.
Предпочтительно, гликоалкалоиды представляют собой соламаргин и соласонин в соотношении от около 1:6 до 6:1, или более предпочтительно в соотношении от около 1:4 до 4:1, от 1:3 до 3:1 или от 1:2 до 2:1.
Если указанные гликоалкалоиды представляют собой соламаргин и соласонин, и они присутствуют в соотношении 1:1, то указанные гликоалкалоиды предпочтительно являются выделенными. Альтернативно, если указанные гликоалкалоиды представляют собой соласонин и соламаргин, то они предпочтительно составляют не менее 66% гликозидов в указанной композиции. В одном варианте реализации в соответствии с данным примером, композиция гликоалкалоидов содержит соотношение 33% соласонина, 33%) соламаргина и 34% их соответствующих моно- и дигликозидов, в которых агликон представляет собой соласодин. В одном варианте реализации в соответствии с данным примером, композиция гликоалкалоидов представляет собой ВЕС™ или CORAMSINE® (например, производства компании Solbec Pharmaceuticals Ltd).
В предпочтительном форме данного изобретения композиция гликоалкалоидов по существу не содержит поздно элюируемых продуктов разложения.
Предпочтительно, указанные гликоалкалоиды составляют долю более 70%-90% гликозидов в композиции, более предпочтительно 91-95% и еще более предпочтительно 96-100% гликозидов в композиции.
Количество гликоалкалоидов в композициях по данному изобретению может варьироваться в зависимости от предполагаемого конечного применения. Предпочтительно, указанные композиции содержат около 0,001% - 5% или 10% гликоалкалоидов, более предпочтительно 0,01%) - 5% или 10%, и еще более предпочтительно 0,1% - 5% или 10% гликоалкалоидов.
Фактическая концентрация гликоалкалоидов в композиции может варьироваться и зависит по меньшей мере от природы заболевания, подлежащего лечению, и от состояния субъекта, подлежащего лечению. Практикующие специалисты могут определить наиболее подходящую дозу с помощью стандартных навыков и с учетом различных параметров, применимых в таких ситуациях. Например, если заболевание представляет собой рост опухоли, то чем больше раковая нагрузка у конкретного пациента, тем выше доза гликоалкалоидов, которую можно вводить пациенту и которую он может хорошо переносить. Предпочтительно, концентрация алкалоидов, вводимых в составе комбинированной терапии, меньше, чем в сравнимой ситуации при их введении в качестве монотерапии. Количество или концентрация (мас./мас.) гликоалкалоида в готовой композиции может составлять около 0,1 мг/кг - 100 мг/кг, 1 мг/кг - 80 мг/кг, 5 мг/кг - 60 мг/кг или 10 мг/кг - 40 мг/кг, или 0,5-5 мг/кг, или 0,75-4 мг/кг, или 1-3 мг/кг. Предпочтительно, количество или концентрация (мас./мас.) гликоалкалоида в готовой композиции составляет около 0,5-5 мг/кг, 0,74-4 мг/кг или 1-3 мг/кг. В одном примере композиция представляет собой кремовую лекарственную форму, содержащую 0,005%) (мас./мас.) гликоалкалоидов.
Указанная композиция также может содержать второй компонент в форме по меньшей мере одного терапевтического агента, пригодного для лечения рака, вирусных инфекций, бактериальных инфекций, паразитарных инфекций, грибковых инфекций, воспалительных заболеваний и/или псориаза.
Если указанную композицию используют для лечения опухолевого заболевания, то композиция также может содержать второй компонент в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия. Для целей данного изобретения «ядерный механизм действия» означает, что химиотерапевтический агент действует внутри ядра раковой клетки, у него или вблизи него. Например, указанный агент может препятствовать митозу посредством подавления образования, посредством связывания или иного нарушения функции одного или более белков или структур, участвующих в митозе, таких как тубулин, микротрубочки, центриолы или веретена. Альтернативно или дополнительно, указанный агент может действовать на или вблизи нуклеиновых кислот в ядре посредством повреждения, разрушения, сшивания или связывания с нуклеиновыми кислотами или иного нарушения функции ДНК или РНК, например, ингибируя или иным образом препятствуя транскрипции и/или трансляции. Альтернативно или дополнительно, указанный агент может действовать на один или более ферментов или кофакторов, связанных со структурой ДНК, например, указанный агент может действовать на топоизомеразы, тем самым препятствуя укладке ДНК в соответствующую спиральную структуру.
Указанная композиция также может содержать второй компонент в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия. Предпочтительно, второй компонент представляет собой митотический ингибитор, алкилирующий агент или антибиотик.
Если второй компонент представляет собой митотический ингибитор, он может быть растительным алкалоидом, таким как алкалоид, выбранный из группы, состоящей из: алкалоидов барвинка, таксанов, подофиллотоксинов и аналогов каптотекана. В одной конкретной форме данного изобретения второй компонент представляет собой винорелбин, тартрат винорелбина или паклитаксел, или их функциональные эквиваленты. Если второй компонент представляет собой алкилирующий агент, он может быть выбран из группы, состоящей из: солей металлов, нитрозомочевин, производных газа иприта, этилениминов, алкилсульфонатов, гидразинов и триазинов. В одной конкретной форме данного изобретения второй компонент представляет собой мехолретамин или дакарбазин, или их функциональные эквиваленты.
Если второй компонент представляет собой антибиотик, он может быть выбран из группы, состоящей из: антрациклинов и хромомицинов. В одной конкретной форме данного изобретения второй компонент представляет собой доксорубицин или его функциональный эквивалент.
В одном предпочтительном примере второй компонент содержит по меньшей мере один химиотерапевтический агент с ядерным механизмом действия, выбранный из группы: доксорубицина, азотистого иприта, топотекана и гемцитабина, 5-фторурацила, CAMP, оксалиплатина, митомицина С, таксола, триметрексата, топотекана, 5-фторурацила в комбинации с оксалиплатином и 5-фторурацила в комбинации CAMP, цисплатина, гемцитабина, иресса, навалбина, таксола, триметрексата и топотекана, кармустина, цисплатина, дакарбазина, навалбина, азотистого иприта, таксола и темозоломида.
Для целей данного изобретения «функциональные эквиваленты; представляют собой структурно и/или функционально родственные соединения, которые предположительно имеют такой же преимущественный эффект, как названное соединение, при их использовании в комбинации с гликоалкалоидными соединениями, описанными в данном документе.
Модификатор вязкости
Термин «модификатор вязкости» означает любой агент, который может обеспечивать регулирование, изменение или контролирование вязкости субстрата, такого как (но не ограничиваясь этим) жидкость, крем или гель. Термин «вязкость» соответствует неформальной концепции «густоты».
Модификатор вязкости может быть любым пригодным модификатором вязкости или может быть гелеобразующим агентом и/или модификатором вязкости, не содержащим рамнозу, выбранным из группы, состоящей из: гуаровой камеди, камеди бобов рожкового дерева, ксантановой камеди, желатина, полоксамера, карбомеров и производных целлюлозы.
В одном варианте реализации гелеобразующий агент или модификатор вязкости представляет собой ксантановую камедь.
Ксантановая камедь представляет собой вещество, получаемое бактериальной ферментацией или синтетическим путем, которое используют в пищевых продуктах в качестве гелеобразующего агента и загустителя. Она представляет собой полисахарид, состоящий из глюкозы, маннозы и глюкуроновой кислоты.
Кератолитические агенты
Кератолитические агенты играют важную роль во многих кремовых лекарственных формах. Их используют для отшелушивания кожи посредством ослабления и отделения наружного слоя кожи.
По меньшей мере один кератолитический агент может быть любым пригодным кератолитическим агентом. В одном варианте реализации кератолитический агент выбран из группы, состоящей из: альфа-гидроксикислот, выбранных из: гликолевой кислоты, молочной кислоты, яблочной кислоты, лимонной кислоты и винной кислоты; бета-гидроксикислот, выбранных из: салициловой кислоты, 3-гидроксипропионовой кислоты, бета-гидроксимасляной кислоты, бета-гидрокси-бета-метилбутирата и карнитина; азелаиновой кислоты, пероксида бензоила, мочевины, трихлоруксусной кислоты (ТСА), карболовой кислоты (фенол), кротонового масла, ацетона и серы. Указанная композиция может содержать кератолитический агент, содержащий по меньшей мере одну альфа-гидроксикислоту, описанную в данном документе, и может дополнительно содержать по меньшей мере один кератолитический агент, содержащий по меньшей мере одну бета-гидроксикислоту, описанную в данном документе.
В предпочтительном варианте реализации по меньшей мере один кератолитический агент выбран из группы, состоящей из: молочной кислоты, салициловой кислоты и мочевины. Например, указанная композиция может содержать молочную кислоту, салициловую кислоту и мочевину.
В одном варианте реализации кератолитический агент представляет собой бета-гидроксикислоту, салициловую кислоту. Салициловая кислота действует на кожу, повышая содержание влаги в коже и растворяя вещество, которое обеспечивает удерживание кожи в форме единого целого (катерины). В результате этого клетки кожи проще отшелушиваются и имитируют клеточную суспензию.
В одном варианте реализации кератолитический агент представляет собой мочевину. Мочевина повышает содержание влаги в коже, размягчая/растворяя роговое вещество (кератин), удерживающее верхний слой клеток кожи в связанном состоянии. Указанный эффект способствует отшелушиванию отмерших клеток кожи, включая раковые клетки, погибшие под действием гликоалкалоидов, и способствует удерживанию влаги в коже.
Лекарственные средства по данному изобретению, пригодные для применения у животных и, в частности, у людей, как правило, должны быть по существу стабильными в условиях производства и хранения. Лекарственные средства по данному изобретению, содержащие рамнозиды соласодина, можно составлять в форме твердого вещества, раствора, микроэмульсии, липосомы или других упорядоченных структур, пригодных для обеспечения высокой концентрации лекарства.
Фактические уровни доз рамнозидов соласодина в лекарственном средстве по данному изобретению могут варьироваться в соответствии с природой биологически активного материала, а также потенциально повышенной эффективностью благодаря преимуществам обеспечения и введения рамнозидов соласодина (например, повышенной растворимости).
В данном контексте «терапевтически эффективное количество» относится к такому количеству гликоалкалоида или к такому количеству терапевтической композиции, лекарственной формы или лекарственного средства по данному изобретению, содержащего гликоалкалоид, которое необходимо для обеспечения терапевтического ответа у человека или животного субъекта. Количество, эффективное для такого применения, зависит от: требуемого терапевтического эффекта; способа введения; эффективности рамнозидов соласодина; требуемой продолжительности лечения; стадии и тяжести заболевания, подлежащего лечению; массы и общего состояния здоровья пациента; и решения врача, назначающего препарат.
В одном варианте реализации рамнозиды соласодина можно комбинировать с другим биологически активным материалом в одном лекарственном средстве.
Например, действующая композиция может состоять из 0,2-2% мас./мас. ксантановой камеди, 5-10% мас./мас. молочной кислоты, 5-10% мас./мас. салициловой кислоты и 3-5% мас./мас. мочевины. В альтернативном варианте реализации композиция может содержать 1% мас./мас. ксантановой камеди, 10% мас./мас. молочной кислоты, 10% мас./мас. салициловой кислоты и 5% мас./мас. мочевины.
В одном варианте реализации композиция представляет собой гель или крем, и/или предназначена для местного введения.
В одном примере композиция представляет собой крем, содержащий один или более из эмульгирующего воска, белого мягкого парафина, жидкого парафина, пропиленгликоля и воды, например, в качестве кремовой основы. Необязательно, кремовая композиция может дополнительно содержать хлоркрезол.
Во втором варианте реализации указанная композиция по существу не содержит свободных сахаридов такого типа, которые могут ингибировать взаимодействие между гликоалкалоидами и их клеткой-мишенью.
В предпочтительном форме данного изобретения указанная композиция по существу не содержит сахаридов. В частности, термин «свободный сахарид» относится к любому сахариду, такому как моно-, ди-, три-, олиго- или полисахарид, или его производному, которое не связано с алкалоидом. В весьма предпочтительной форме данного изобретения указанная композиция не содержит рамнозы или рамнозоподобных молекул.
Не ограничиваясь какой-либо конкретной теорией или конкретным механизмом действия, автор данного изобретения сделал предположение, что в случае композиций для местного применения по данному изобретению, используемых для лечения рака или опухолей кожи, по меньшей мере один кератолитический агент (например, выбранный из салициловой кислоты, молочной кислоты и мочевины) может действовать как скраб(-ы), который может обеспечивать удаление массы отмерших клеток с кожи, включая, например, клетки кератинового слоя, которые могут отшелушиваться, например, над раком кожи или опухолями кожи, еще не вышедшими на поверхность кожи. Такое действие может способствовать тому, чтобы гликоалкалоиды в композициях по данному изобретению достигали раковых или опухолевых клеток на коже, взаимодействовали с ними и уничтожали их, без уничтожения нормальных, неинфицированных или нераковых клеток.
Способы получения
Фармацевтические композиции и лекарственные средства по данному изобретению могут содержать гликоалкалоид(-ы) по данному изобретению вместе с по меньшей мере одним модификатором вязкости и по меньшей мере одним кератолитическим агентом, например, в качестве фармацевтически приемлемых носителей, вспомогательных веществ и/или разбавителей. Необязательно, фармацевтические композиции или лекарственные средства по данному изобретению могут дополнительно содержать один или более дополнительных фармацевтически приемлемых носителей, вспомогательных веществ или разбавителей, а также другие агенты, обычно используемые при получении фармацевтически приемлемых композиций.
Способы получения композиций или лекарственных средств по данному изобретению, содержащих один или более активных ингредиентов, общеизвестны в данной области техники. Такие композиции обычно составляют для предполагаемого способа доставки, и обычно они содержат один или более фармацевтически приемлемых носителей, вспомогательных веществ и/или разбавителей.
В одном примере способ получения композиций или лекарственных средств по данному изобретению включает комбинирование, и/или смешивание, и/или растворение одного или более гликоалкалоидов формулы I по данному изобретению с фармацевтически приемлемым носителем, разбавителем и/или вспомогательным веществом.
В другом примере указанный способ включает получение композиций или лекарственных средств, содержащих множество различных гликоалкалоидов, и указанный способ включает комбинирование, и/или смешивание, и/или растворение каждого из различных гликоалкалоидов по отдельности с фармацевтически приемлемым носителем, разбавителем и/или вспомогательным веществом с получением отдельной разовой дозы для отдельного введения каждого из различных гликоалкалоидов.
Например, способ получения композиций или лекарственных средств по данному изобретению может включать растворение, комбинирование и/или смешивание гликоалкалоида(-ов) с фармацевтически приемлемым носителем, разбавителем и/или вспомогательным веществом, пригодным для местной доставки композиции. В одном таком примере носитель, разбавитель и/или вспомогательное вещество может быть водным или неводным. В другом примере фармацевтически приемлемый носитель, вспомогательное вещество и/или разбавитель содержит любой один или оба из указанного по меньшей мере одного модификатора вязкости и указанного по меньшей мере одного кератолитического агента по данному изобретению. Необязательно, указанный способ может дополнительно включать растворение, и/или комбинирование, и/или смешивание гликоалкалоида и/или по меньшей мере одного модификатора вязкости, и/или по меньшей мере одного кератолитического агента с одним или более дополнительными фармацевтическими носителями, вспомогательными веществами или разбавителями, а также с другими агентами, обычно используемыми при получении фармацевтически приемлемых композиций.
«Фармацевтически приемлемый носитель», или «фармацевтически приемлемое вспомогательное вещество», или «фармацевтически приемлемый разбавитель» представляет собой материал, который не является биологически или иным образом нежелательным, т.е. указанный материал можно применять для индивидуума вместе с активными агентами, не вызывая неприемлемых биологических эффектов или без неблагоприятного взаимодействия с любыми другими компонентами композиции, в которой он содержится.
В одном примере композиции и лекарственные средства по данному изобретению в качестве носителей, вспомогательных веществ и/или разбавителей содержат один или более модификаторов вязкости и один или более кератолитических агентов по данному изобретению, как описано выше.
Альтернативно или дополнительно, композиции или лекарственные средства по данному изобретению могут дополнительно содержать пригодные носители, вспомогательные вещества и разбавители, которые являются фармацевтически приемлемыми и совместимыми с активным ингредиентом. Некоторые примеры пригодных носителей, вспомогательных веществ и разбавителей включают, без ограничения, воду, солевой раствор, этанол, диметилсульфоксид (ДМСО), декстрозу, циклодекстрины, такие как гидроксипропил-бета-циклодекстрин, глицерин, этоксилаты жирных кислот марок Teric и Ecoteric, лактозу, сахарозу, сорбит, маннит, крахмалы, гуммиарабик, фосфаты кальция, альгинат, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, водный сироп, метилцеллюлозу, метил- и пропилгидроксибензоаты, тальк, стеарат магния и минеральное масло, или их комбинации.
Композиции и лекарственные средства по данному изобретению могут дополнительно содержать смазывающие агенты, рН-буферные агенты, смачивающие агенты, эмульгирующие и суспендирующие агенты или консерванты. Примеры таких пригодных дополнительных агентов включают:
a) поверхностно-активные вещества и полимеры, включая, но не ограничиваясь этим, полиэтиленгликоль (ПЭГ), поливинилпирролидон (ПВП), поливиниловый спирт, кросповидон, сополимер поливинилпирролидона и поливинилакрилата, производные целлюлозы, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, карбоксиметилэтилцеллюлозу, фталат гидроксипропилметилцеллюлозы, полиакрилаты и полиметакрилаты, мочевину, сахара, многоатомные спирты и их полимеры, эмульгаторы, арабинозу, крахмал, органические кислоты и их соли, винилпирролидон и винилацетат; и/или
b) связующие агенты, такие как различные целлюлозы и поперечно сшитый поливинилпирролидон, микрокристаллическая целлюлоза; и/или
c) смазывающие агенты, такие как агенты, которые влияют на сыпучесть порошка, подлежащего прессованию, включая коллоидный диоксид кремния, тальк, стеариновую кислоту, стеарат магния, стеарат кальция, силикагель; и/или
d) консерванты, такие как сорбат калия, метилпарабен, пропилпарабен, бензойная кислота и ее соли, другие сложные эфиры пара-гидроксибензойной кислоты, такие как бутилпарабен, спирты, такие как этиловый или бензиловый спирт, фенольные соединения, такие как фенол, или четвертичные соединения, такие как хлорид бензалкония; и/или
e) буферы; и/или
f) разбавители, такие как фармацевтически приемлемые инертные наполнители, такие как микрокристаллическая целлюлоза, лактоза, двухосновной фосфат кальция, сахариды и/или смеси любых вышеуказанных; и/или
g) смачивающие агенты, такие как кукурузный крахмал, картофельный крахмал, маисовый крахмал и модифицированные крахмалы, кроскармеллоза натрия, кросповидон, крахмалгликолят натрия и их смеси; и/или
h) гелеобразующие (стабилизирующие эмульсию) агенты, такие как: гуаровая камедь, камедь бобов рожкового дерева, ксантановая камедь, желатин и производные целлюлозы (такие как гидроксиэтилцеллюлоза).
Конкретный выбор компонентов для включения в композиции или лекарственные средства, описанные в данном документе, в целом, зависит от активных агентов и заболевания, подлежащего лечению.
Композиции и лекарственные средства по данному изобретению адаптированы для местной доставки. Любые системы местной доставки могут быть пригодными для введения композиций по данному изобретению, в зависимости от предпочтительной схемы лечения.
Лекарственные формы для местного применения, описанные выше, можно получать посредством растворения, или комбинирования, или смешивания активного агента в водном или неводном носителе. В целом, пригодна любая жидкость, крем или гель, или подобное вещество, которое не взаимодействует существенным образом с активными или любыми другими ингредиентами, которые могут быть введены в композицию, и которое является не раздражающим. Также можно использовать соответствующие не поддающиеся разбрызгиванию вязкие, полутвердые или твердые формы, которые содержат носитель, совместимый с местным применением и предпочтительно имеющий динамическую вязкость больше, чем у воды.
Пригодные лекарственные формы хорошо известны специалистам в данной области техники и включают, но не ограничиваются этим, растворы, суспензии, эмульсии, кремы, гели, мази, порошки, линименты, бальзамы, аэрозоли, трансдермальные пластыри и т.д., которые при необходимости стерилизуют или смешивают со вспомогательными агентами, например, консервантами, стабилизаторами, эмульгаторами, смачивающими агентами, ароматизаторами, окрашивающими агентами, регуляторами запаха, загустителями, такими как природные камеди, и т.д. Особенно предпочтительные лекарственные формы для местного применения включают мази, кремы или гели.
Мази обычно получают с применением либо (1) маслянистой основы, т.е. основы, состоящей из нелетучих масел или углеводородов, таких как белый вазелин или минеральной масло, либо (2) абсорбирующей основы, т.е. основы, состоящей из безводного вещества или веществ, которые могут поглощать воду, например, безводного ланолина. Традиционно, после получения маслянистой или абсорбирующей основы добавляют активный агент в количестве, необходимом для получения требуемой концентрации.
Кремы представляют собой эмульсии масла в воде. Они состоят из масляной фазы (внутренней фазы), обычно содержащей нелетучие масла, углеводороды и т.п., воски, вазелин, минеральное масло и т.п., и водной фазы (непрерывной фазы), содержащей воду и любые водорастворимые вещества, такие как добавленные соли. Указанные две фазы стабилизируют с помощью эмульгирующего агента, например, поверхностно-активного агента, такого как лаурилсульфат натрия; гидрофобных коллоидов, таких как гуммиарабик, коллоидные глины, вигум и т.п. При получении эмульсии обычно добавляют активный агент в количестве, необходимом для достижения требуемой концентрации. В одном примере стабильная кремовая лекарственная форма по данному изобретению включает кремовые лекарственные формы, содержащие гликоалкалоид(-ы), причем разделение масляной и водной фаз крема является незначительным или отсутствует после хранения лекарственной формы при комнатной температуре или при 25°С по истечении по меньшей мере 3 месяцев, или по меньшей мере 6 месяцев, или по меньшей мере 12 месяцев, или по меньшей мере 24 месяцев, или по меньшей мере 36 месяцев, или по меньшей мере 48 месяцев после производства кремовой лекарственной формы.
Гели содержат основу, выбранную из маслянистой основы, воды или эмульсионно-суспензионной основы. К указанной основе добавляют гелеобразующий агент, который образует в основе матрицу, повышая ее вязкость. Примеры гелеобразующих агентов представляют собой гидроксипропилцеллюлозу, карбомеры, полимеры акриловой кислоты и т.п. Традиционно, активный агент добавляют в лекарственную форму в требуемой концентрации до момента добавления гелеобразующего агента.
Обычное количество лекарственной формы для местного применения, которое наносят на поврежденную ткань, зависит от размера поврежденной ткани и концентрации активного агента в лекарственной форме.
Могут быть желательными лекарственные формы для местного применения с контролируемым высвобождением. Композиции можно внедрять в инертную матрицу, которая обеспечивает возможность высвобождения по механизму диффузии или выщелачивания, т.е. в камеди. В фармацевтическую композицию также можно вводить медленно разлагающиеся матрицы. Другой формой контролируемого высвобождения является способ, основанный на терапевтической системе Oros (Alza Corp.), т.е. композицию заключают в полупроницаемую мембрану, которая обеспечивает возможность проникновения внутрь воды и вытеснения композиции через одно небольшое отверстие под действием осмоса. Некоторые энтеросолюбильные покрытия также имеют эффект замедленного высвобождения.
Для получения оптимального пленочного покрытия можно использовать смесь материалов. Пленочное покрытие можно получать в дражировочном котле или в псевдоожиженном слое, или нанесением покрытия посредством прессования.
Активные агенты могут быть включены в указанные композиции в виде множества мелких частиц в форме гранул или пеллет с размером частиц около 1 мм. Лекарственная форма для введения капсул также может быть в виде порошка, слегка спрессованной массы или даже в виде таблеток. Активные агенты также можно включать в композиции в форме капсул с фиксированной дозой порошка для ингаляции, составленных для использования в ингаляторах, например, как в случае порошковых капсул, используемых в устройстве ULTIBRO® BREEZHALER®. Активный агент(-ы) можно получать прессованием. Микрочастицы можно получать различными способами, известными специалистам в данной области техники, например, выпариванием растворителя, десольватацией, комплексной коацервацией, с использованием полимер/полимерной несовместимости, межфазной полимеризации и т.д.
Гидрофильные полимеры, образующие микрочастицы, могут присоединяться к направляющему белку, который обеспечивает возможность специфического связывания микрочастицы с выбранными клетками-мишенями или тканями, несущими молекулу-мишень (например, характеристический маркер). Например, гидрофильные полимеры могут конъюгироваться с фрагментом антитела Fab'. Пептиды меньшего размера из гипервариабельной области или из другого пептида, взаимодействующего со специфическим лигандом клеточной поверхности, также могут конъюгироваться с указанными комплексами. Наиболее предпочтительно, указанные антитела или фрагменты антител направлены против молекул-мишеней, связанных с раковыми тканями или клетками.
Терапевтическое применение
Терапевтическое применение композиций и лекарственных средств по данному изобретению включает лечение, например, местное лечение различных заболеваний, например, при лечении рака, вирусных инфекций, бактериальных инфекций, паразитарных инфекций, грибковых инфекций, воспалительных заболеваний и/или псориаза.
В одном варианте реализации композиции и лекарственные средства по данному изобретению предназначены для лечения, например, местного лечения рака кожи и/или опухолей кожи.
Способы лечения
Композиции и лекарственные средства по данному изобретению можно использовать клинически для лечения различных заболеваний, например, при лечении рака, вирусных инфекций, бактериальных инфекций, паразитарных инфекций, грибковых инфекций, воспалительных заболеваний и/или псориаза. Таким образом, композиции и лекарственные средства по данному изобретению могут обеспечивать разработку новых способов лечения различных заболеваний.
Соответственно, в данном изобретении также предложен способ лечения пациента, имеющего или страдающего от кожного заболевания, связанного с раком, вирусными инфекциями, бактериальными инфекциями, паразитарными инфекциями, грибковыми инфекциями, воспалительными заболеваниями и/или псориаза, включающий стадию нанесения на область болезненного состояния терапевтически эффективного количества композиции, описанной в данном документе.
В предпочтительной форме данного изобретения также предложен способ лечения опухолевого роста, включающий стадию введения терапевтически эффективного синергетического количества композиции, описанной в данном документе. В другой предпочтительной форме данного изобретения также предложен способ лечения рака кожи и/или роста опухоли кожи, включающий стадию местного нанесения терапевтически эффективного количества композиции, описанной в данном документе, на область кожи, содержащую указанный рак кожи и/или рост опухоли кожи.
Не ограничиваясь какой-либо теорией и предполагаемым механизмом действия, автор данной заявки полагает, что композиции, описанные в данном документе, имеют преимущество, поскольку они обеспечивают доставку по существу стабильной лекарственной формы со сниженным или минимальным разложением гликоалкалоидных активных агентов. В этом отношении сделано гипотетическое предположение, что указанная композиция гликоалкалоидов обеспечивает более высокую восприимчивость инфицированных или целевых болезненных клеток (например, клеток болезненного состояния кожи, таких как раковые клетки, клетки, участвующие в росте опухоли, клетки, инфицированные бактериями, вирусами, паразитами или грибками, клетки кожи, связанные с псориазом и/или воспалительной реакцией на коже) к указанной композиции, например, посредством повышения проницаемости мембраны, в частности, ядерной мембраны.
В особенно предпочтительной форме данного изобретения указанную композицию используют для лечения опухолевого заболевания. В данном случае указанная композиция также может содержать второй компонент в форме по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия.
Комбинация гликоалкалоидов и химиотерапевтических агентов, описанная в данном документе, демонстрирует интересные свойства при приведении в контакт с раковыми клетками ex vivo. При введении пациентам, указанная композиция обеспечивает более высокий результат лечения пациента, по сравнению с соответствующими монотерапиями и по сравнению с аддитивным эффектом соответствующих монотерапий. В этом отношении более низкие дозы могут предотвращать или ослаблять один или более побочных эффектов, связанных с химиотерапевтическими агентами, при введении в допустимой дозе, используемой для монотерапии.
Рост опухоли может быть связан с различными видами рака, включая рак, выбранный из группы, состоящей из: меланом и немеланомных заболеваний кожи, включая лигнинную меланому, солнечный кератоз, кератоакантому, базальноклеточную карциному, плоскоклеточную карциному (например, поверхностную плоскоклеточную карциному кожи) и актинический кератоз.
Композиции, используемые в способе по данному изобретению, также могут содержать фармацевтически приемлемый носитель.
Если указанная композиция содержит соединения, отличные от указанных гликоалкалоидов, то такие другие соединения можно вводить в отдельных лекарственных формах. При раздельном введении указанные композиции можно вводить одновременно или последовательно. Для целей данного изобретения «одновременно» означает, что композиции вводят в одно время или в пределах одного часа друг от друга. Если композиции вводят с интервалом более одного часа, то считают, что их вводят последовательно.
Композиции по данному изобретению следует вводить в единичной лекарственной форме, которая является терапевтически эффективной. Единичная лекарственная форма в данном контексте относится к физически дискретным единицам, пригодным в качестве однократных доз для субъектов, подлежащих лечению, каждая единица содержит некоторое количество активного вещества, рассчитанное для обеспечения требуемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Характеристики единичных лекарственных форм по данному изобретению продиктованы и напрямую зависят от по меньшей мере (а) уникальных характеристик активного вещества и конкретного ожидаемого терапевтического эффекта, и от (b) ограничений, существующих в области составления композиций, таких как активное вещество для предполагаемого лечения. Таким образом, количество активного соединения, подлежащее введению, в значительной степени зависит от токсичности и собственной активности соединения, от субъекта, подлежащего лечению, и степени необходимого лечения. Точное количество соединения, которое необходимо ввести, может зависеть от решения практикующего специалиста и может быть индивидуальным для каждого субъекта. Предпочтительно, дозы активных агентов, вводимых в соответствии с комбинированной терапией по данному изобретению, меньше, чем обычные дозы тех же активных агентов при использовании в монотерапии.
Композиции и лекарственные средства по данному изобретению могут быть составлены для ежедневного или периодического введения, например, местного введения. Например, указанные композиции и лекарственные средства можно вводить ежедневно в течение по меньшей мере около 3 дней, или по меньшей мере 4 дней, или по меньшей мере 5 дней, или по меньшей мере 6 дней, или по меньшей мере 1 недели, или по меньшей мере около 2 недель, или по меньшей мере около 3 недель, или по меньшей мере около 4 недель, или по меньшей мере около 5 недель, или по меньшей мере около 6 недель, или по меньшей мере около 7 недель, или по меньшей мере около 8 недель, или по меньшей мере около 9 недель, или по меньшей мере около 10 недель, или по меньшей мере около 11 недель, или по меньшей мере около 12 недель, или по меньшей мере около 13 недель, или по меньшей мере около 14 недель, или по меньшей мере около 15 недель, или по меньшей мере около 16 недель, или по меньшей мере около 17 недель, или по меньшей мере около 18 недель, или по меньшей мере около 19 недель, или по меньшей мере около 20 недель, или по меньшей мере около 21 недели, или по меньшей мере около 22 недель, или по меньшей мере около 23 недель, или по меньшей мере около 24 недель, или по меньшей мере около 25 недель, или по меньшей мере около 6 месяцев, или по меньшей мере около одного года, или более одного года. В одном предпочтительном примере указанную композицию вводят в течение по меньшей мере 3 дней. В другом предпочтительном примере указанную композицию вводят в течение по меньшей мере около 13 недель или по меньшей мере около 3 месяцев.
В другом примере указанную композицию можно вводить периодически, например, два раза в сутки, или три раза в сутки, или более трех раз в сутки, или через день, или каждый третий день, или каждый четвертый день, или каждый пятый день, или каждый шестой день, или один раз в две недели в течение по меньшей мере около 2 недель, или по меньшей мере около 3 недель, или по меньшей мере около 4 недель, или по меньшей мере около 5 недель, или по меньшей мере около 6 недель, или по меньшей мере около 7 недель, или по меньшей мере около 8 недель, или по меньшей мере около 9 недель, или по меньшей мере около 10 недель, или по меньшей мере около 11 недель, или по меньшей мере около 12 недель, или по меньшей мере около 13 недель, или по меньшей мере около 14 недель, или по меньшей мере около 15 недель, или по меньшей мере около 16 недель, или по меньшей мере около 17 недель, или по меньшей мере около 18 недель, или по меньшей мере около 19 недель, или по меньшей мере около 20 недель, или по меньшей мере около 21 недели, или по меньшей мере около 22 недель, или по меньшей мере около 23 недель, или по меньшей мере около 24 недель, или по меньшей мере около 25 недель, или по меньшей мере около 6 месяцев, или по меньшей мере около одного года, или более одного года.
В одном предпочтительном примере указанную композицию вводят по меньшей мере два раза в сутки или по меньшей мере каждые 12 часов в течение по меньшей мере 3 последовательных дней. В альтернативном примере указанную композицию можно вводить посредством ежедневного нанесения до 10 раз с интервалами по меньшей мере 0,5 часа для более быстрого достижения терапевтического эффекта (например, для устранения ракового или опухолевого поражения кожи).
В другом примере указанную композицию можно вводить в течение периода введения, составляющего по меньшей мере около 1 недели, или по меньшей мере около 2 недель, или по меньшей мере около 3 недель, или по меньшей мере около 4 недель, или по меньшей мере около 5 недель, или по меньшей мере около 6 недель, или по меньшей мере около 7 недель, или по меньшей мере около 8 недель, или по меньшей мере около 9 недель, или по меньшей мере около 10 недель, или по меньшей мере около 11 недель, или по меньшей мере около 12 недель, или по меньшей мере около 13 недель, или по меньшей мере около 14 недель, или по меньшей мере около 15 недель, или по меньшей мере около 16 недель, или по меньшей мере около 17 недель, или по меньшей мере около 18 недель, или по меньшей мере около 19 недель, или по меньшей мере около 20 недель, или по меньшей мере около 21 недели, или по меньшей мере около 22 недель, или по меньшей мере около 23 недель, или по меньшей мере около 24 недель, или по меньшей мере около 25 недель, или по меньшей мере около 6 месяцев, или по меньшей мере около одного года или более одного года, с последующим периодом прекращения применения и последующим периодом введения, составляющим по меньшей мере около 1 недели или по меньшей мере около 2 недель, или по меньшей мере около 3 недель, или по меньшей мере около 4 недель, или по меньшей мере около 5 недель, или по меньшей мере около 6 недель, или по меньшей мере около 7 недель, или по меньшей мере около 8 недель, или по меньшей мере около 9 недель, или по меньшей мере около 10 недель, или по меньшей мере около 11 недель, или по меньшей мере около 12 недель, или по меньшей мере около 13 недель, или по меньшей мере около 14 недель, или по меньшей мере около 15 недель, или по меньшей мере около 16 недель, или по меньшей мере около 17 недель, или по меньшей мере около 18 недель, или по меньшей мере около 19 недель, или по меньшей мере около 20 недель, или по меньшей мере около 21 недели, или по меньшей мере около 22 недель, или по меньшей мере около 23 недель, или по меньшей мере около 24 недель, или по меньшей мере около 25 недель, или по меньшей мере около 6 месяцев, или по меньшей мере около одного года, или более одного года.
В одном примере композиция или лекарственное средство по данному изобретению содержит около 0,005% (мас./мас.) гликоалкалоидов. В другом примере композиция или лекарственное средство по данному изобретению можно наносить местно на пораженную область кожи по меньшей мере два раза в сутки в течение по меньшей мере 3 последовательных дней, например, с использованием герметичной повязки, например, два раза в сутки или каждые 12 часов в течение 3 последовательных дней. Хотя возможно также более частное нанесение, например, нанесение каждые 0,5 часа до 10 последовательных раз.
Предпочтительно (например, если композиция или лекарственное средство представляет собой кремовую или гелеобразную лекарственную форму), указанную композицию или лекарственное средство наносят тонким слоем и равномерно по всей площади обработки кожи, так чтобы покрыть очаг поражения или болезненного состояния кожи герметичной повязкой во избежание высыхания лекарственного средства или композиции после нанесения на кожу. Предпочтительно, лекарственное средство или композицию не наносят в большом количестве, так что область нанесения композиции или лекарственного средства выступает на 0,5 см на визуально нормальную кожу вокруг кромки очага или пораженной области кожи.
В одном примере композицию или лекарственное средство по данному изобретению наносят до устранения ракового/опухолевого очага и/или до устранения бактериального, вирусного, грибкового, инфекционного и/или воспалительного поражения, и/или псориаза, и предпочтительно пораженное/болезненное состояние кожи заменяется нормальной, здоровой кожей (например, определяемой визуально).
Примеры
Пример 1: Получение гликозида соласодина, не содержащего сахара
В данном примере представлен способ получения препарата гликоалкалоида, который по существу не содержит (т.е. не имеет в составе) свободных сахаридов, включая сахариды такого типа, которые ингибируют взаимодействие между гликоалкалоидами и их клеткой-мишенью.
Препарат гликозида соласодина, не содержащий сахара, получали следующим образом: 50 кг ягод Solanum Sodomaeum помещали в промышленную мясорубку (оснащенную электрическим двигателем мощностью 1 л.с., 1425 об./мин.) с размером отверстий решетки 3 мм.
Суспензию разбавляли 3% уксусной кислотой (рН 2,5) (пищевой марки) до объема 200 л. Полутвердый раствор перерабатывали в гомогенизаторе Silverson в течение 15 минут. Смешивание продолжали еще 4 часа с помощью мешалки из нержавеющей стали в лопастном смесителе при комнатной температуре при 30 об./мин. (Flamingo CMG, 0,75 кВт, с регулятором скорости вращения).
Раствор оставляли стоять в течение ночи без перемешивания. Затем раствор фильтровали через муслиновую ткань. Затем фильтрат пропускали через проточную центрифугу (3,5 л.с.) при 1455 об./мин. Прозрачный фильтрат нагревали до 50°С в емкости из нержавеющей стали с двойной рубашкой. Добавляли концентрированный аммиак (марки х.ч.) до рН около 10. Наблюдали образование осадка. Осадок оставляли оседать и охлаждаться (около 24 часов). Надосадочную жидкость осторожно декантировали. Осадок растворяли в 25 л 3% водного раствора уксусной кислоты. Раствор центрифугировали на проточной центрифуге, как описано выше. Надосадочную жидкость собирали в емкость из нержавеющей стали с двойной рубашкой и нагревали до 50°С при непрерывном перемешивании (30 об./мин., 30 мин.).
Гликоалкалоиды повторно осаждали посредством добавления концентрированного раствора аммиака до рН около 10. Раствор оставляли остывать с выпадением осадка (около 24 часов). Надосадочную жидкость осторожно декантировали и промывали осадок, используя 50 л воды, и оставляли для выпадения осадка на 24 часа, как описано ранее. Надосадочную жидкость декантировали. Указанный прием повторяли четыре раза.
Наконец, осадок растворяли в 10 л спирта при 75°С и фильтровали в горячем виде через фильтровальную бумагу Whatman №1. Надосадочную жидкость сушили при 50°С. В результате получали мелкий полукристаллический порошок. Выход составлял 505 г, т.е. 1,01%.
Промывая экстракт в хлороформе, полностью удаляли агликоновые соласодины. Соласодин был растворим в фазе хлороформа, а сахара были растворимы в водной фазе. Гликоалкалоиды во всех таких условиях оставались нерастворимыми.
Пример 2: Анализ стабильности гликозидов соласодина.
В данном примере описано получение различных кремовых форм гликоалкалоидов для местного применения, содержащих по меньшей мере один кератолитический агент и содержащих или не содержащих модификатор вязкости (например, в качестве вспомогательных веществ и/или носителей), а также оценка стабильности гликоалкалоида, активного агента в таких лекарственных формах. Приведенные результаты также демонстрируют получение новой, по существу стабильной и эффективной композиции для местного применения, содержащей по меньшей мере гликоалкалоид, по меньшей мере один модификатор вязкости и по меньшей мере один кератолитический агент, с большим сроком годности, для применения в терапии.
В предыдущих исследованиях рака кожи человека испытывали кремовые лекарственные формы, содержащие гликоалкалоиды, в течение пяти месяцев после изготовления крема. Результаты были исключительными. В указанных исследованиях было показано только присутствие активных гликоалкалоидов. Однако не указана их концентрация. См., например, WO 2000061153А1.
В данном исследовании кремовые лекарственные формы получали из полукристаллического препарата гликозида соласодина, не содержащего сахара, например, полученного в соответствии со способом, описанным в Примере 1. Реальные кремовые лекарственные формы получали так, как подробно описано в WO 2000061153 А1 (полное содержание которого включено в данный документ посредством ссылки). Использовали эмульгирующий воск, белый мягкий парафин (10% мас./мас.), жидкий парафин (10%) мас./мас.), пропиленгликоль (5%) и воду для получения кремовой основы, и в качестве консерванта добавляли хлоркрезол (1%).
Стабильность гликозида соласодина в кремовой лекарственной форме, содержащей по массе 5% мочевины и 10% салициловой кислоты, но не содержащей молочной кислоты и агента для стабилизации эмульсии, испытывали в течение 48 часов с момента получения лекарственной формы, и результаты представлены в Таблице 1. Внешний вид оценивали путем сравнения со стандартной, имеющейся в продаже кремовой композицией соламаргина. Использовали высокоэффективную жидкостную хроматографию (ВЭЖХ) для определения количества соламаргина в креме, по существу так, как описано в WO 2000061153 А1.
В данном документе указано, что даже после удаления свободных (не конъюгированных) сахаров посредством промывания полукристаллических рамнозидов соласодина (например, как описано в Примере 1) перед введением в композицию рамнозидов соласодина, и при использовании указанной композиции в кремовой лекарственной форме для лечения рака кожи, нестабильность рамнозидов соласодина сохраняется.


С - Соответствует
F - Не соответствует
Кроме того, при использовании указанной кремовой лекарственной форме в клинических условиях в течение продолжительного периода времени наблюдали, что при старении кремовой лекарственной формы эффективность указанной кремовой лекарственной формы очевидно уменьшается с течением времени.
В то же время было отмечено, что стабильность кремов сильно зависит от температуры, что приводит к разделению масляной и водной фаз при комнатной температуре. В дополнительных исследованиях установлено, что указанная кремовая лекарственная форма имеет два определенных недостатка:
- Тепловая нестабильность кремовой лекарственной формы даже при комнатной температуре; и
- Разложение гликоалкалоидов в кремовой лекарственной форме.
Указанные два недостатка дополнительно изучали для определения возможности их преодоления.
Для ингибирования разложения рамнозидов соласодина в кремовые лекарственные формы добавляли молочную кислоту в различных концентрациях от 1 до 10% (мас./мас.). Сразу возникала одна проблема. Эмульсия крема подвергалась дестабилизации при концентрациях молочной кислоты более 4% (мас./мас.).
Для преодоления вышеуказанного недостатка стабильности кремовой лекарственной формы необходимо модифицировать первоначально составленный крем.
Изучали различные агенты для стабилизации эмульсии. В конечном итоге, для обеспечения стабильности эмульсии использовали ксантановую камедь. Исследовали кремовые лекарственные формы ВЕС с использованием различных количеств ксантановой камеди (Xg). 0,2% (мас./мас.) Xg в лекарственной форме приводило к незначительному загустеванию. Оптимальная концентрация в креме составила 1,0% Xg. Получали густую теплостойкую эмульсию. Более высокое содержание Xg приводило к нежелательной скользкой текстуре крема.
На основании указанных достижений далее было возможно исследовать повышающиеся концентрации молочной кислоты и/или других компонентов в кремовых лекарственных формах и определять, как указанные концентрации связаны со стабильностью и предотвращением разложения рамнозидов соласодина вследствие гидролиза в указанных кремах.
Было установлено, что молочная кислота в концентрациях более 4% по массе в кремовой лекарственной форме оптимальна для обеспечения стабильности крема.
Это было неожиданным, поскольку ранее предполагалось, что молочная концентрация в таких концентрациях, а также 10% (мас./мас.) салициловая кислота (содержащаяся в кремах в качестве кератолитического агента) будут обусловливать очень низкое значение рН с высокой кислотностью и, следовательно, будут вызывать гидролиз гликоалкалоидов ВЕС. Было показано, что это не происходит.
Известно, что HCl в низких концентрациях (менее 1% по массе) гидролизует гликоалкалоиды. HCl является сильной кислотой и имеет значение рКа менее -2. Молочная кислота является слабой кислотой и имеет значение рКа 3,86. Слабая кислота имеет значение рКа в воде в примерном диапазоне от -2 до 12. Сильные кислоты имеют значение рКа менее -2. Салициловая кислота, хотя и не слишком растворимая в воде, растворима в кремовой эмульсии и имеет значение рКа 2,97. Таким образом, разность кислотности HCl по сравнению с молочной кислотой и салициловой кислотой близка к 5 порядкам величины. Это может объяснять, почему гликоалкалоиды ВЕС являются по существу стабильными в кремовой форме в присутствии слабых кислот в концентрациях до 10% молочной кислоты и до 10% салициловой кислоты по массе.
Для имитации характеристик клеточной суспензионной среды, в которой очень низкие концентрации указанных гликоалкалоидов проявляют эффективные противораковые свойства, к кремовой лекарственной форме, содержащей гликоалкалоид, добавляли определенные вспомогательные вещества, представленные в Таблице 2, для получения новой и более стабильной лекарственной формы, чем получали ранее или описано выше.
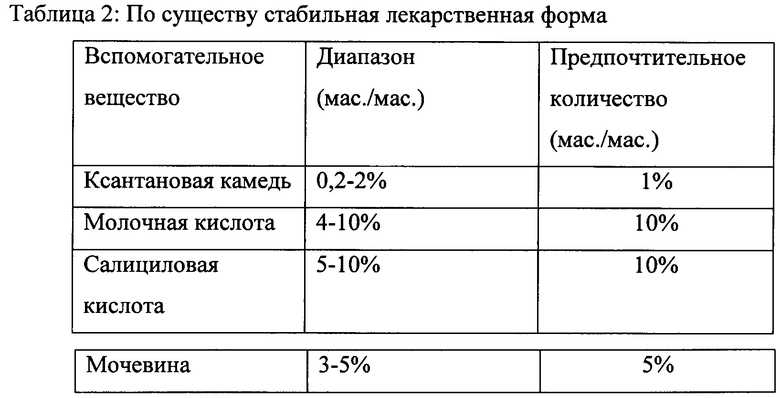
В частности, исследовали влияние добавления салициловой кислоты, мочевины и ксантановой камеди на стабильность полученной лекарственной формы, как показано в Таблице 3.
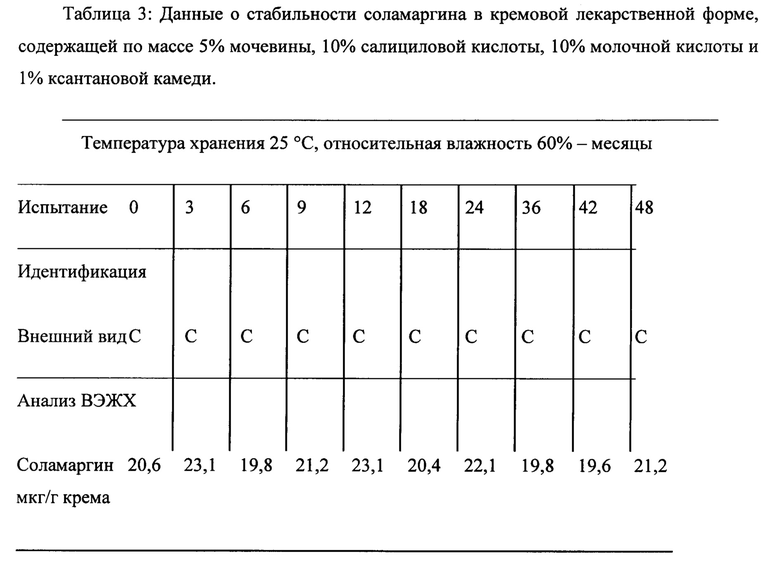
С - Соответствует
F - Не соответствует
Действительно, присутствие салициловой кислоты (10% мас./мас.), мочевины (5% мас./мас.) и ксантановой камеди (1% мас./мас.) в кремовой лекарственной форме для местного применения было преимущественным для получения заметных результатов лечения рака кожи с применением очень низких концентраций ВЕС, приближающихся к тому уровню ВЕС, который был весьма эффективным в исследованиях на культуре раковых клеток.
Как упомянуто выше, существенные недостатки, связанные со стабильностью и полной эффективностью первоначальной эмульсионной кремовой лекарственной формы гликоалкалоида, содержащей 5% мочевины, 10% салициловой кислоты, не содержащей молочной кислоты и не содержащей агента для стабилизации эмульсии, для лечения рака кожи, обусловливали ограничение ее терапевтического применения.
На основании исследований с ксантановой камедью и молочной кислотой, была разработана конкретная иллюстративная лекарственная форма, представленная в Таблице 2, содержащая определенные вспомогательные вещества для преодоления недостатков первоначальной нестабильности эмульсии и нестабильности гликоалкалоидов ВЕС в кремовых лекарственных формах.
Указанная новая кремовая лекарственная форма для местного применения с соответствующими вспомогательными веществами обеспечивала получение по существу стабильной, эффективной новой кремовой лекарственной формы для местного применения со сроком годности более 4 лет при клиническом использовании.
Пример 3: Влияние свободных (не конъюгированных) сахаров на терапевтическую активность гликоалкалоидов
В данном примере показано, что свободные (не конъюгированные) сахарные фрагменты, такие как свободная рамноза, снижают терапевтическую противораковую/противоопухолевую эффективность гликоалкалоидов SR по данному изобретению.
Для определения влияния свободных сахарных фрагментах на противоопухолевую активность гликоалкалоидов SR по данному изобретению, определяли противораковую активность повышающихся концентраций экстракта гликоалкалоидов ВЕС в условиях клеточной культуры в отсутствие свободной рамнозы, и отдельно в присутствии 5 мМ рамнозы. Для этого раковые клетки меланомы инкубировали с повышающимися концентрациями (0-20 мкг/мл) экстракта ВЕС (который состоял из постоянной смеси соламаргина, соласонина и ди- и моногликозидов соласодина) в присутствии или в отсутствие свободной рамнозы. Результаты представлены на Фиг. 1.
Как показано на Фиг. 1, повышающиеся концентрации ВЕС приводят к уменьшению выживания клеток меланомы, с LD50 12 мкг/мл ВЕС и LD100 около 20 мкг/мл ВЕС. При введении с раковые клетки меланомы 5 мМ свободной рамнозы совместно с ВЕС, выживают практически все клетки меланомы.
Соответственно, в данном примере показано, что свободные сахара, такие как рамноза, оказывают защитный эффект против противораковой и/или противоопухолевой терапевтической эффективности соединений гликоалкалоидов по данному изобретению. Указанные данные дополняют in vivo исследования саркомы 180 у мышей, описанные в W2000061153A1.
Пример 4: Влияние различных лекарственных комбинаций на опухолевые клетки ex vivo В данном примере показан синергетический противораковый эффект композиций, содержащих гликоалкалоид по данному изобретению, испытанных в комбинации с другими химиотерапевтическими агентами, например, агентами, имеющими ядерный механизм действия, и указанный эффект определяли с помощью ex vivo анализов, измеряя клеточную гибель (посредством апоптоза) раковых или опухолевых клеток.
Полученные данные подтверждают предположение, что лабораторные результаты EVA (ex vivo анализа) очень хорошо коррелируют с клиническими наблюдениями. Данный подход подкреплен несколькими научными статьями, включающими более 650 опубликованных клинических корреляций (см., например, Principles and Practice of Oncology Updates: том 7, №12, 1993), которые обобщены в Таблице 4. Как показано в Таблице 4, представленные опубликованные клинические корреляции свидетельствуют о том, что EVA имеет чувствительность 96,1% и специфичность 87,1% (Таблица 4). Кроме того, было показано, что анализ чувствительности к химиотерапевтическим препаратам EVA коррелирует с ответом, временем прогрессирования и выживанием. Опухолеспецифическая положительная и отрицательная точность прогноза более подробно представлена ниже в Таблице 4:
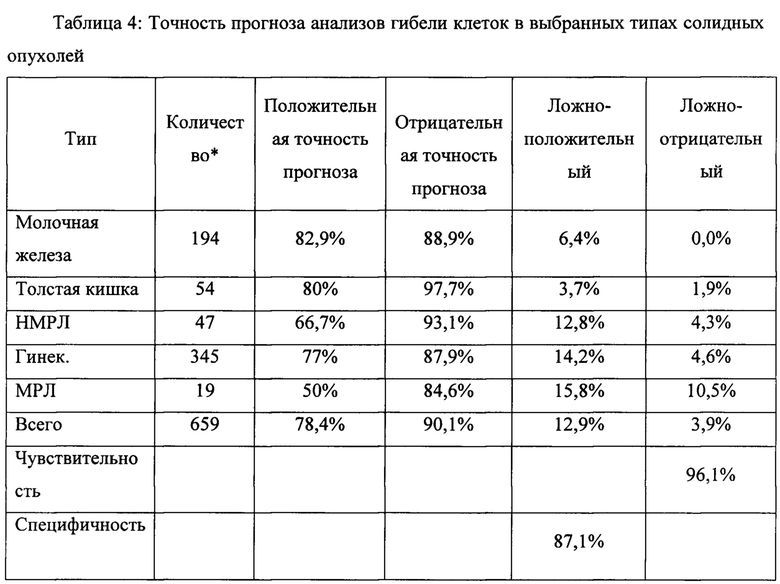
Положительная точность прогноза: если анализ предсказывал чувствительность, и наблюдали ответ
Отрицательная точность прогноза: если анализ предсказывал чувствительность, и не наблюдали ответ.
* Количество опубликованных клинических корреляций
Ранее считалось, что раковые клетки перерастают нормальные, здоровые клетки. Теперь известно, что раковые клетки действительно переживают нормальные клетки; это не значит, что они слишком сильно растут, по факту они слишком долго живут. Анализы ех vivo учитывают это и измеряют процесс клеточной гибели, а не клеточной пролиферации/роста. Принципиальная технология ex vivo анализа обеспечивает измерения апоптозных конечных точек, которые лучше отражают влияние химиотерапии in vivo. В анализе ex vivo также можно измерять неапоптозные конечные точки, включая: методы измерения содержания АТФ (люминесцентные), определения МТТ (митохондриальной активности) и целостности мембран, в качестве дополнительных конечных точек гибели клеток. Поскольку ранее было показано, что Coramsine® имеет неапоптозный механизм действия, проводили ex vivo исследования для испытания Coramsine® с использованием неапоптозных конечных точек.
Свежие образцы человеческих опухолей разрушали механически и ферментативно, и полученные сфероиды суспендировали в модифицированной среде RPMA 1640, в целом, в соответствии со способами, описанными в Nagourney R.A. et al (2003).
Повторно суспендированные сфероиды обрабатывали препаратом CORAMSINE® [который состоит из двух гликоалкалоидов соласодина, соласонина и соламаргина в соотношении 1:1 (мас./мас.)] в комбинации с различными другими химиотерапевтическими агентами, в целом, в соответствии со способами, описанными в Nagourney R.A. et al (2003). В некоторых случаях CORAMSINE® испытывали в комбинации с несколькими другими химиотерапевтическими агентами.
Синергию определяли с помощью технологии среднего эффекта, описанного в публикации Chou and Talalay (1987), и, в целом, в соответствии со способами, изложенными в Nagourney R.A. et al (2003).
Результаты представлены в следующих таблицах. Информация об «активности» выражена как показатель концентрации при выживании 50% клеток. Релевантные сокращения/эквивалентная номенклатура: 5FU - 5-фторурацил; BCNU - кармустин (BiCNU®); CAMP - комбинация циклофосфамида (Cytoxan®), доксорубицина (Adriamycin®), метотрексата (Mexate®) и прокарбазина (Matulane®); CDDP - цисплатин; DOX - доксорубицин (Adriamycin®, гидроксидаунорубицин); DTIC (®) - дакарбазин (DIC, карбоксамид имидазола); GEM - гемцитабин (Gemzar®); IRES - Iressa® (гефитиниб); L-OHP - оксалиплатин (Eloxatin®); ММС - митомицин С; NAV - Navelbine® (винорелбин); NM - азотистый иприт (мехлоретамин, хлорметин, мустин, Mustargen®); TAX - Taxol® (паклитаксел); ТМТХ - триметрексат; TMZ - темозоломид (Temodar®, Temodal®); ТОРО - топотекан (Hycamtin) и COR - Coramsine®.
1. Рак почек
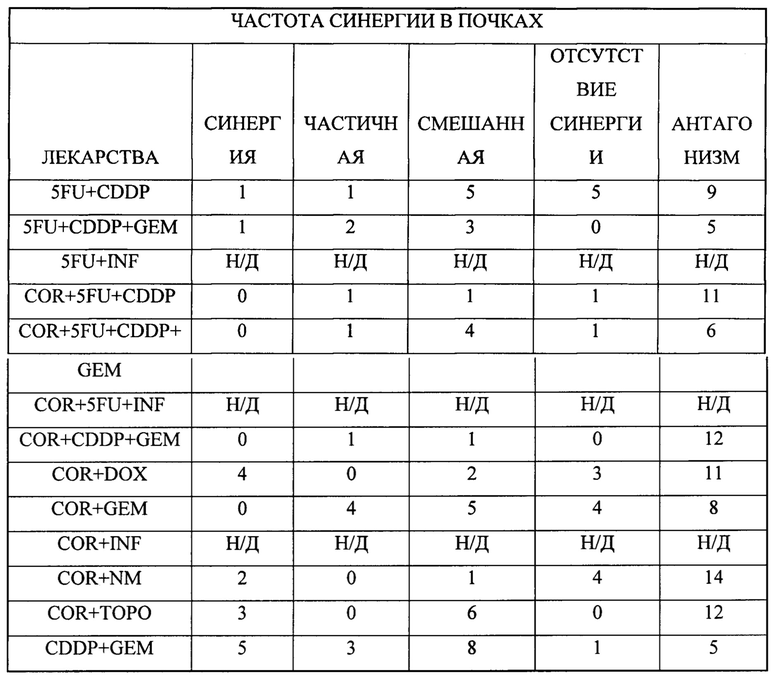
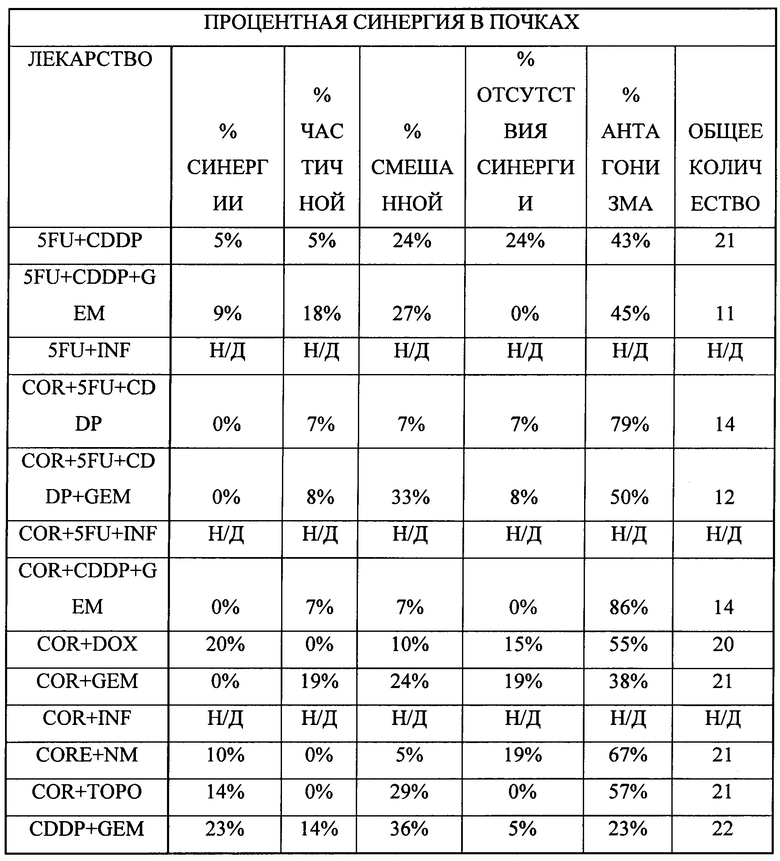
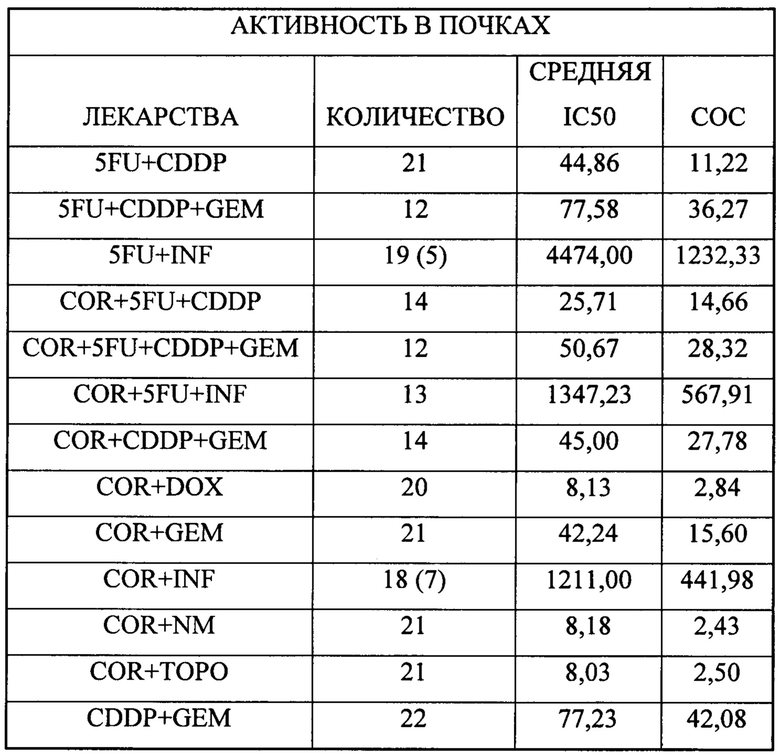
2. Рак толстой и прямой кишок
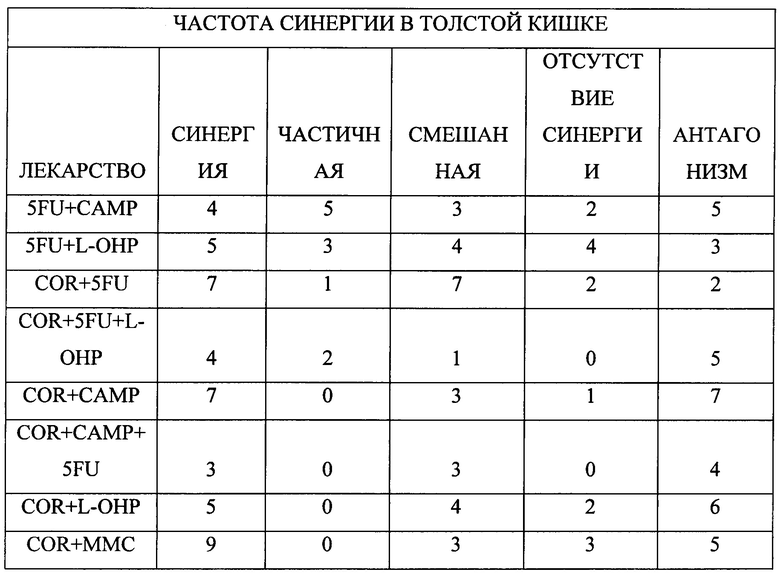
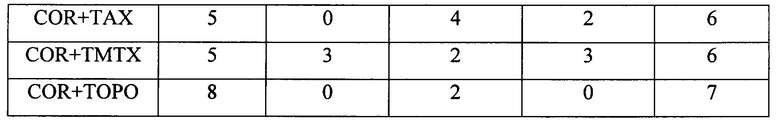

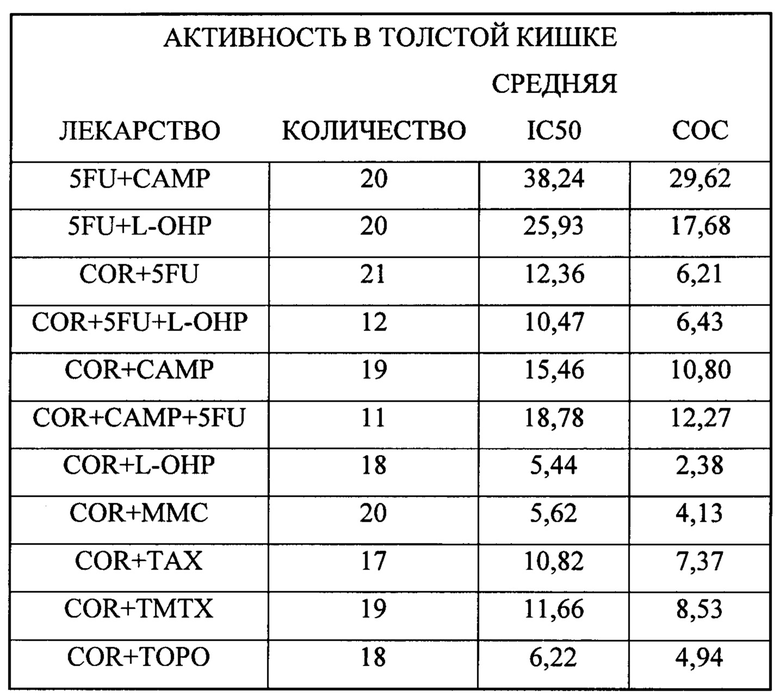
3. Немелкоклеточный рак легких 4
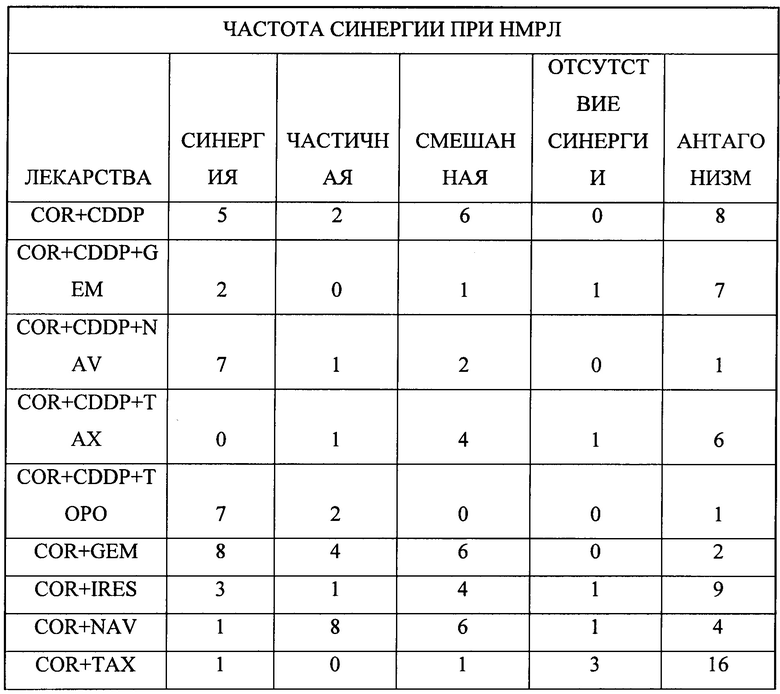

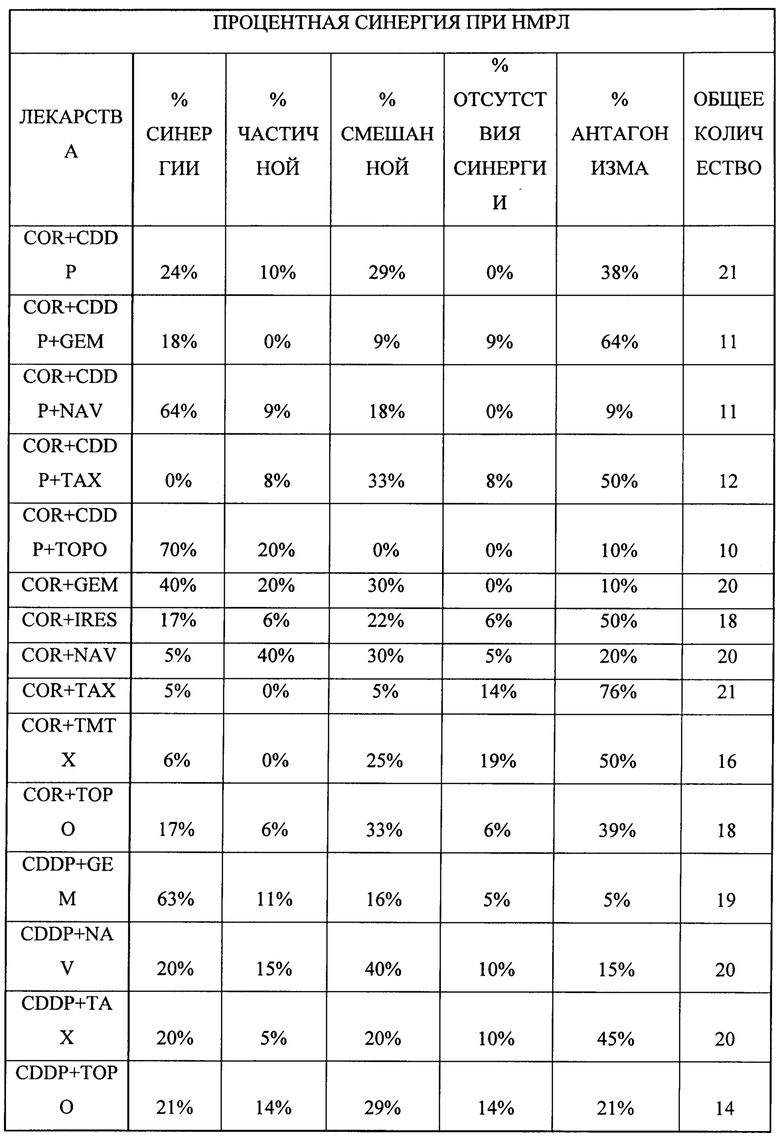
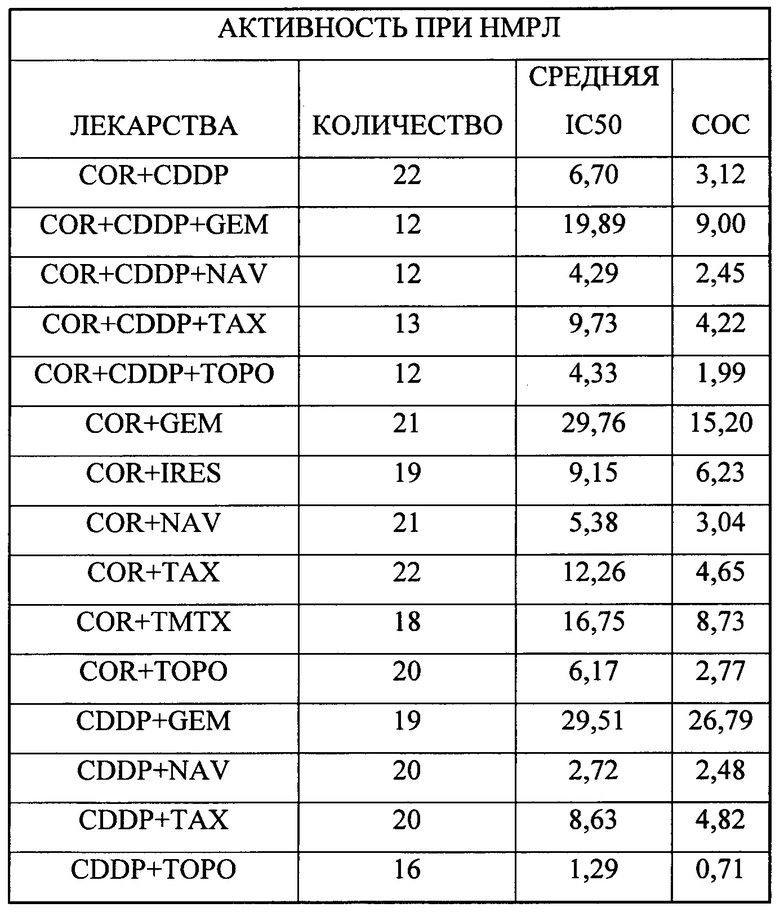
4. Меланома
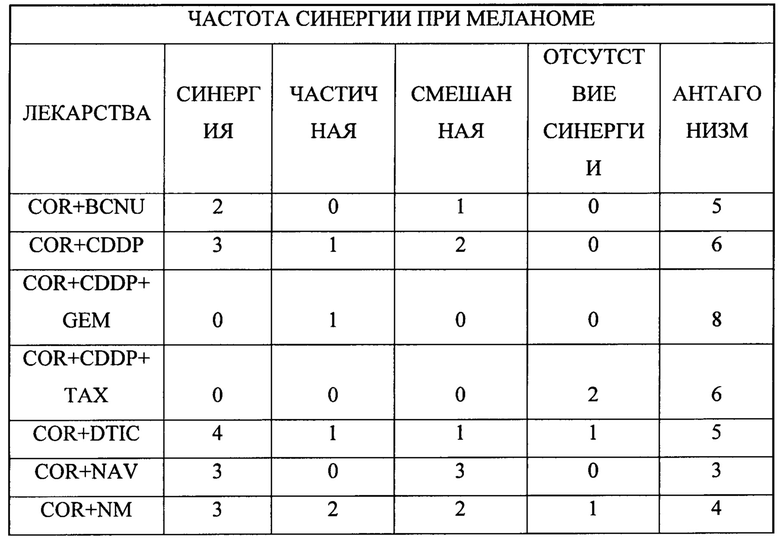
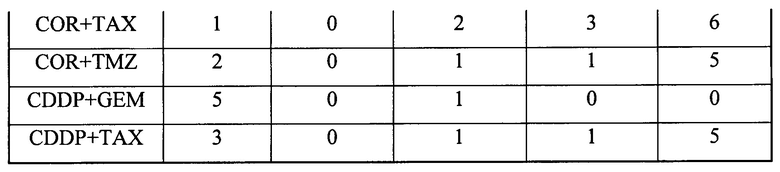
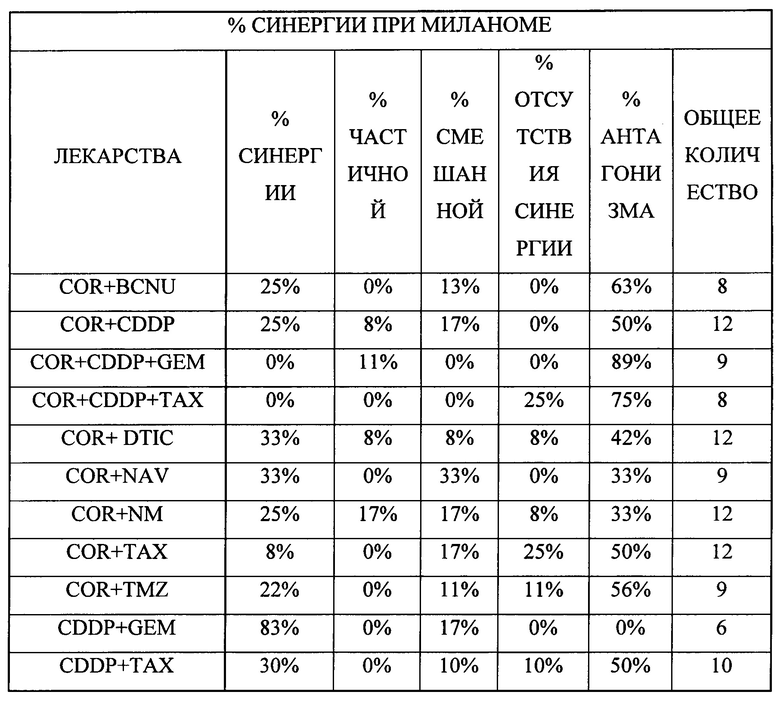
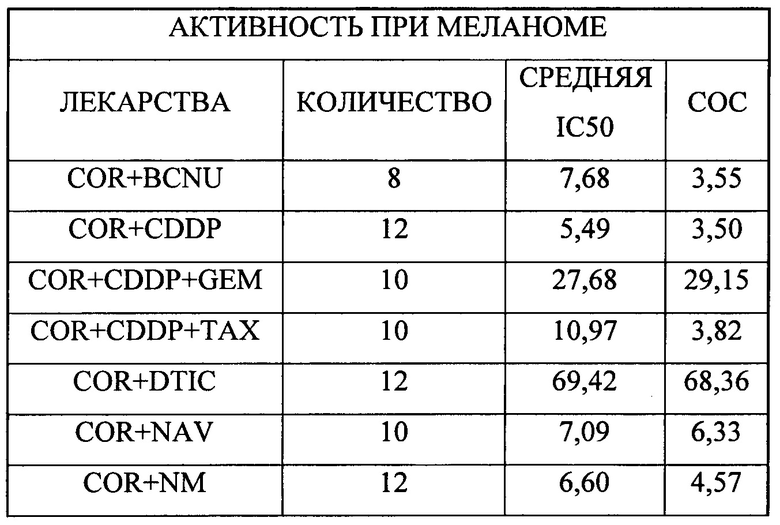
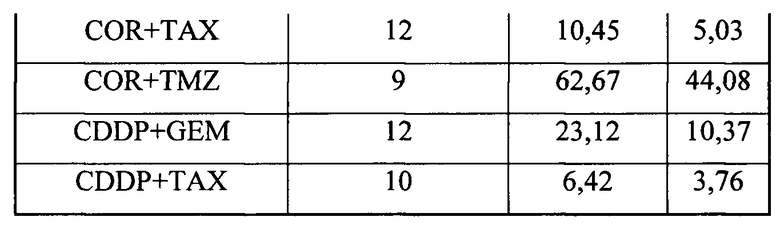
Как можно видеть из представленных выше таблиц, CORAMSINE действует синергетически с рядом химиотерапевтических агентов с ядерным механизмом действия, в отношении нескольких иллюстративных видов рака.
ССЫЛКИ
Nagourney R.A., Sommers B.L., Harper S.M., Radecki S., Evans S.S. (2003) Ex vivo analysis of topotecan: advancing the application of laboratory-based clinical therapeutics. British Journal of Cancer 89, 1789-1795.
Chou T-C., Talalay P. (1987) Applications for the median-effect principle for the assessment of low-dose risk of carcinogens and for the quantitation of synergism and antagonism of chemotherapeutic agents. In New Avenues in Developmental Cancer Chemotherapy. Harrap K.R., Conneros T.A. (eds) pp 37-64, Orlando, FL: Academic Press Inc.

Группа изобретений относится к лечению рака. Композиция для местного применения для лечения рака кожи и/или опухоли кожи содержит по меньшей мере один гликоалкалоид, по меньшей мере один модификатор вязкости и по меньшей мере один кератолитический агент, где по меньшей мере один гликоалкалоид включает гликозид соласодина, по меньшей мере один модификатор вязкости представляет собой ксантановую камедь, по меньшей мере один кератолитический агент представляет собой молочную кислоту, при этом композиция содержит 0,2-2% мас./мас. ксантановой камеди, 4-10% мас./мас. молочной кислоты, 5-10% мас./мас. салициловой кислоты и 3-5% мас./мас. мочевины. Также раскрыты способ получения композиции и композиция, полученная данным способом, способ лечения рака кожи и/или опухоли кожи у пациента, применение композиции при местном лечении рака кожи и/или опухоли кожи и в производстве лекарственного средства для местного лечения рака кожи и/или опухоли кожи, применение по меньшей мере одного гликоалкалоида с по меньшей мере одним модификатором вязкости и с по меньшей мере одним кератолитическим агентом в производстве лекарственного средства для местного лечения рака кожи и/или опухоли кожи. Группа изобретений обеспечивает улучшенную стабильную лекарственную форму гликоалкалоидов. 7 н. и 26 з.п. ф-лы, 1 ил., 16 табл., 4 пр.
1. Композиция для местного применения, пригодная для лечения рака кожи и/или опухоли кожи, содержащая по меньшей мере один гликоалкалоид, по меньшей мере один модификатор вязкости и по меньшей мере один кератолитический агент, где по меньшей мере один гликоалкалоид включает гликозид соласодина, причем по меньшей мере один указанный модификатор вязкости представляет собой ксантановую камедь, при этом по меньшей мере один указанный кератолитический агент представляет собой молочную кислоту, и при этом композиция содержит 0,2-2% мас./мас. ксантановой камеди, 4-10% мас./мас. молочной кислоты, 5-10% мас./мас. салициловой кислоты и 3-5% мас./мас. мочевины.
2. Композиция по п. 1, дополнительно содержащая гликоалкалоид, выбранный из группы, содержащей любые гликоалкалоиды формулы I:
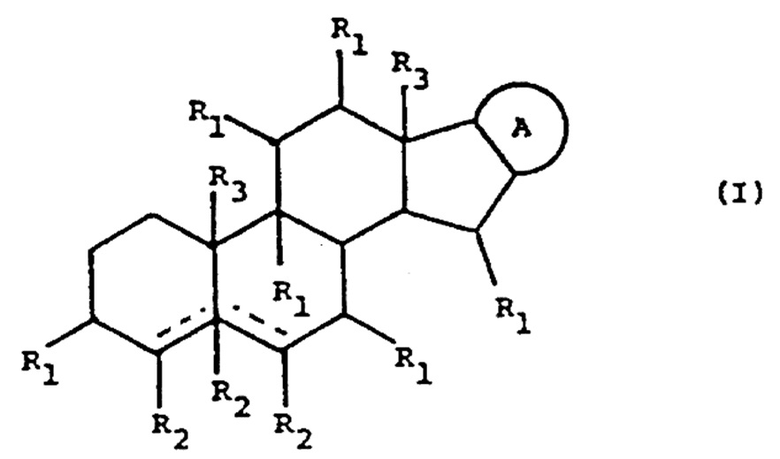
где:
каждая из пунктирных линий независимо выбрана из одинарной связи и двойной связи;
A представляет собой радикал, выбранный из радикалов, имеющих общие формулы (II) – (V):
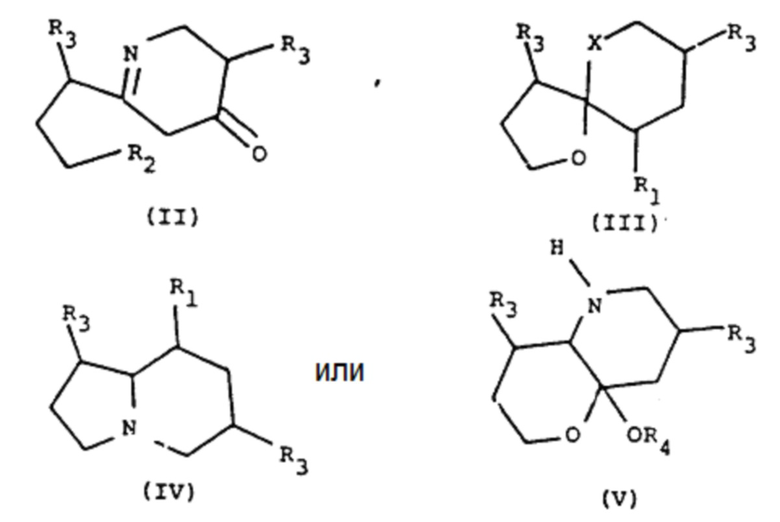
каждый из R1 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино, оксо и OR4;
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино и OR4;
каждый из R3 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, алкила и R4-алкилена;
каждый из R4 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, углевода и углеводного производного;
«X» представляет собой –NH2-; и
где указанный по меньшей мере один гликоалкалоид содержит по меньшей мере одну группу R4, где R4 представляет собой углевод или его производное, выбранное из группы, состоящей из глицеринового альдегида, глицерозы, эритрозы, треозы, рибозы, арабинозы, ксилозы, ликсозы, альтрозы, аллозы, гулозы, маннозы, глюкозы, идозы, галактозы, талозы, рамнозы, дигидроксиацетона, эритрулозы, рибулозы, ксилулозы, псикозы, фруктозы, сорбозы, тагатозы, других гексоз, гептоз, октоз, наноз, декоз, дезоксисахаров с разветвленными цепями, апиозы, гамамелозы, стрептозы, кордицепозы, микарозы и кладинозы, соединений, в которых альдегидные, кетоновые или гидроксильные группы являются замещенными, сахарных спиртов, сахарных кислот, бензимидазолов, енольных солей углеводов, сахариновых кислот и фосфатов сахаров.
3. Композиция по п. 2, содержащая множество гликоалкалоидов, выбранных из формулы I.
4. Композиция по п. 3, дополнительно содержащая по меньшей мере один химиотерапевтический агент с ядерным механизмом действия.
5. Композиция по любому из пп. 1-4, содержащая 5-10% мас./мас. молочной кислоты.
6. Композиция по любому из пп. 1-5, содержащая 1% мас./мас. ксантановой камеди, 10% мас./мас. молочной кислоты, 10% мас./мас. салициловой кислоты и 5% мас./мас. мочевины.
7. Композиция по любому из пп. 1-6, представляющая собой гель или крем и/или предназначенная для местного введения.
8. Композиция по любому из пп. 1-7, отличающаяся тем, что не содержит свободных рамнозных сахаридов.
9. Композиция по любому из пп. 1-8, содержащая множество гликоалкалоидов, причем по меньшей мере один гликоалкалоид в указанном множестве гликоалкалоидов включает гликозид соласодина.
10. Композиция по любому из пп. 1-9, где по меньшей мере один гликоалкалоид включает соласонин и/или соламаргин.
11. Композиция по любому из пп. 1-10, содержащая (i) смесь тригликозида соласонина, тригликозида соламаргина и моно- и дигликозидов соласодина или (ii) смесь тригликозида соласонина и тригликозида соламаргина в соотношении 1:1 мас./мас. без моно- и дигликозидов соласодина.
12. Композиция по п. 11, содержащая (i) смесь гликоалкалоидов, состоящую из 33% мас./мас. тригликозида соласонина, 33% мас./мас. тригликозида соламаргина и 34% мас./мас. моно- и дигликозидов соласодина, или (ii) смесь тригликозида соласонина и тригликозида соламаргина в соотношении 1:1 (мас./мас.) без моно- и дигликозидов соласодина.
13. Способ получения композиции по любому из пп. 1-12, включающий комбинирование терапевтически эффективного количества указанного гликоалкалоида или множества различных гликоалкалоидов и 0,2-2% мас./мас. ксантановой камеди, 4-10% мас./мас. молочной кислоты, 5-10% мас./мас. салициловой кислоты и 3-5% мас./мас. мочевины.
14. Способ по п. 13, включающий растворение указанного гликоалкалоида в фармацевтически приемлемом носителе, разбавителе и/или вспомогательном веществе или комбинирование указанного гликоалкалоида с фармацевтически приемлемым носителем, разбавителем и/или вспомогательным веществом.
15. Способ по п. 13 или 14, дополнительно включающий комбинирование по меньшей мере одного химиотерапевтического агента с ядерным механизмом действия.
16. Способ по любому из пп. 13-15, дополнительно включающий удаление свободных сахаридов.
17. Композиция для местного применения, пригодная для лечения рака кожи и/или опухоли кожи, полученная способом по любому из пп. 13-16.
18. Способ лечения рака кожи и/или опухоли кожи у пациента, включающий стадию местного введения указанному пациенту терапевтически эффективного количества композиции по любому из пп. 1-12.
19. Способ по п. 18, включающий местное нанесение указанной композиции на кожу пациента.
20. Способ по п. 18 или 19, отличающийся тем, что указанный пациент имеет или страдает от рака кожи и/или опухоли кожи и указанный способ включает местное нанесение терапевтически эффективного количества указанной композиции на ту область кожи пациента, которая содержит рак кожи и/или опухоль кожи.
21. Применение композиции для местного нанесения по любому из пп. 1-12 при местном лечении рака кожи и/или опухоли кожи.
22. Применение композиции по любому из пп. 1-12 в производстве лекарственного средства для местного лечения рака кожи и/или опухоли кожи.
23. Применение по меньшей мере одного гликоалкалоида с по меньшей мере одним модификатором вязкости и с по меньшей мере одним кератолитическим агентом в производстве лекарственного средства для местного лечения рака кожи и/или опухоли кожи, где по меньшей мере один гликоалкалоид включает гликозид соласодина, причем по меньшей мере один указанный модификатор вязкости представляет собой ксантановую камедь, и при этом по меньшей мере один указанный кератолитический агент представляет собой молочную кислоту, и где лекарственное средство содержит 0,2-2% мас./мас. ксантановой камеди, 4-10% мас./мас. молочной кислоты, 5-10% мас./мас. салициловой кислоты и 3-5% мас./мас. мочевины.
24. Применение по п. 23, отличающееся тем, что указанное лекарственное средство дополнительно содержит гликоалкалоид, выбранный из группы, содержащей любые гликоалкалоиды формулы I:
 м
м
где:
каждая из пунктирных линий независимо выбрана из одинарной связи и двойной связи;
A представляет собой радикал, выбранный из радикалов, имеющих общие формулы (II) – (V):
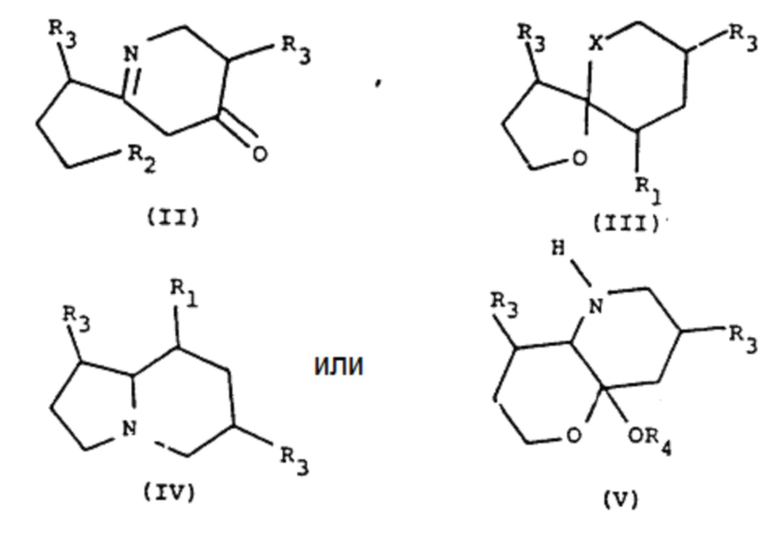
каждый из R1 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино, оксо и OR4;
каждый из R2 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, амино и OR4;
каждый из R3 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, алкила и R4-алкилена;
каждый из R4 представляет собой радикал, независимо выбранный из группы, состоящей из водорода, углевода и углеводного производного;
«X» представляет собой –NH2-; и
где указанный по меньшей мере один гликоалкалоид содержит по меньшей мере одну группу R4, где R4 представляет собой углевод или его производное, выбранное из группы, состоящей из глицеринового альдегида, глицерозы, эритрозы, треозы, рибозы, арабинозы, ксилозы, ликсозы, альтрозы, аллозы, гулозы, маннозы, глюкозы, идозы, галактозы, талозы, рамнозы, дигидроксиацетона, эритрулозы, рибулозы, ксилулозы, псикозы, фруктозы, сорбозы, тагатозы, других гексоз, гептоз, октоз, наноз, декоз, дезоксисахаров с разветвленными цепями, апиозы, гамамелозы, стрептозы, кордицепозы, микарозы и кладинозы, соединений, в которых альдегидные, кетоновые или гидроксильные группы являются замещенными, сахарных спиртов, сахарных кислот, бензимидазолов, енольных солей углеводов, сахариновых кислот и фосфатов сахаров.
25. Применение по п. 24, отличающееся тем, что указанное лекарственное средство содержит множество гликоалкалоидов, выбранных из формулы I.
26. Применение по любому из пп. 23-25, отличающееся тем, что указанное лекарственное средство дополнительно содержит по меньшей мере один химиотерапевтический агент с ядерным механизмом действия.
27. Применение по любому из пп. 23-26, отличающееся тем, что указанное лекарственное средство содержит 5-10% мас./мас. молочной кислоты.
28. Применение по любому из пп. 23-27, отличающееся тем, что указанное лекарственное средство содержит 1% мас./мас. ксантановой камеди, 10% мас./мас. молочной кислоты, 10% мас./мас. салициловой кислоты и 5% мас./мас. мочевины.
29. Применение по любому из пп. 23-28, отличающееся тем, что указанное лекарственное средство составлено в форме геля или крема для местного введения.
30. Применение по любому из пп. 23-29, отличающееся тем, что указанное лекарственное средство не содержит свободных рамнозных сахаридов.
31. Применение по любому из пп. 23-30, отличающееся тем, что указанное лекарственное средство содержит множество гликоалкалоидов, при этом по меньшей один гликоалкалоид в указанном множестве гликоалкалоидов включает гликозид соласодина.
32. Применение по любому из пп. 23-31, отличающееся тем, что по меньшей мере один гликоалкалоид включает соласонин и/или соламаргин.
33. Применение по любому из пп. 23-32, отличающееся тем, что указанное лекарственное средство содержит (i) смесь тригликозида соласонина, тригликозида соламаргина и моно- и дигликозидов соласодина или (ii) смесь тригликозида соласонина и тригликозида соламаргина в соотношении 1:1 (мас./мас.) без моно- и дигликозидов соласодина.
| Воздухораспределитель для автоматических тормозов | 1940 |
|
SU61153A1 |
| Прибор для нахождения центра | 1927 |
|
SU10546A1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ МИТОХОНДРИАЛЬНЫХ ЗАБОЛЕВАНИЙ | 1999 |
|
RU2279880C2 |
| Cham B.E | |||
| et al | |||
| Topical treatment of malignant and premalignant skin lesions by very low concentrations of a standard mixture (BEC) of solasodine glycosides // CANCER LETTERS, V | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная мусоросжигательная печь-снеготаялка | 1920 |
|
SU183A1 |
Авторы
Даты
2023-04-28—Публикация
2017-03-03—Подача