Область техники
Настоящее изобретение относится к области терапии, особенно в онкологии. Оно относится к применению аллопуринола или его фармацевтически приемлемых солей для лечения или предупреждения химиотерапевтически-индуцированной ладонно-подошвенной эритродизестезии (palmar plantar erythrodysesthesia - PPE). Оно также относится к фармацевтическим композициям, включающим аллопуринол, и к способам лечения PPE.
Уровень техники
К раку относится группа заболеваний, при которых патологические клетки способны бесконтрольно делиться. Раковые клетки могут проникать в окружающие ткани и могут переноситься через кровоток и лимфатическую систему к другим частям тела. Существует несколько основных видов рака. Карцинома является раком, который начинает развиваться в коже или в тканях, которые выстилают или покрывают внутренние органы. Саркома является раком, который начинает развиваться в костях, хрящах, жире, мышцах, кровеносных сосудах или другой соединительной или поддерживающей ткани. Лейкоз является раком, который начинает развиваться в кроветворной ткани, такой как костный мозг, и приводит к образованию большого количества патологических клеток крови и поступлению их в кровоток. Лимфома и множественная миелома относятся к раку, который начинает развиваться в клетках иммунной системы.
Доступно несколько способов лечения рака, включая хирургический и лучевую терапию для локализованного заболевания, и лекарственные средства, которые разрушают раковые клетки (химиотерапия). Химиотерапия играет важную роль в лечении рака, поскольку она необходима для лечения распространенного рака с отдаленными метастазами и часто полезна для уменьшения размеров опухоли перед хирургическим лечением (неоадъювантная терапия). Ее также используют после хирургического лечения или лучевой терапии (адъювантная терапия) для разрушения любых оставшихся раковых клеток или профилактики рецидивирования рака.
Разработано большое количество противораковых лекарственных средств, основанных на различных способах действия: наиболее часто используют алкилирующие агенты, которые воздействуют непосредственно на ДНК (такие как цисплатин, карбоплатин, оксаплатин, бусульфан, хлорамбуцил, циклофосфамид, ифосфамид, дакарбазин); антиметаболиты, которые препятствуют синтезу ДНК и РНК (такие как 5-фторурацил, капецитабин, 6-меркаптопурин, метотрексат, гемцитабин, цитарабин (ara-C), флударабин); антрациклины, которые интерферируют с ферментами, задействованными в репликации ДНК (такие как даунорубицин, доксорубицин, эпирубицин, идарубицин, митоксантрон); дезинтеграторы микротрубочек (таксаны, такие как паклитаксел и доцетаксел или алкалоиды барвинка, такие как винбластин, винкристин и винорелбин); ингибиторы топоизомеразы (такие как этопозид, доксорубицин, топотекан и иринотекан); гормональные терапевтические средства (такие как тамоксифен, флутамид) и предложенные в последнее время направленные терапевтические средства (такие как ингибиторы EGFR, цетуксимаб, гефитиниб или ингибитор протеин тирозинкиназы иматиниб).
Химиотерапия рака может состоять из одного лекарственного средства или комбинаций лекарственных средств, которые доставляются циклами. Цикл состоит из лечения одним или более лекарственными средствами с последующим периодом отдыха.
Развитие химиотерапии в последние десятилетия значительно улучшило лечение рака, что привело к эффективному лечению некоторых видов рака и улучшенной выживаемости или времени до прогрессирования при других видах рака. В настоящее время, большинство химиотерапевтических средств вводят внутривенно; однако более широкое применение получают пероральные химиотерапевтические лекарственные средства.
К сожалению, большинство химиотерапевтических лекарственных средств не способны отличать раковую клетку от здоровой клетки. Поэтому химиотерапия часто воздействует на нормальные ткани и органы организма, что приводит к осложнению лечения или побочным эффектам. В дополнение к проблемам, которые они вызывают, побочные эффекты могут создать препятствия врачу для доставки предписанной дозы химиотерапевтического средства, уменьшая вероятность правильного лечения рака. К самым частым побочным эффектам химиотерапии относятся анемия, нейтропения, тромбоцитопения, усталость, облысение, тошнота и рвота, воспаление слизистых оболочек и боль.
Ладонно-подошвенная эритродизестезия (PPE) впервые была описана Zuehlke в 1974 как эритематозные высыпания на ладонях и подошвах, связанные с терапией митотаном (Zuehlke, R.K. Dermatologica, 1974, 148 (2), 90-92). PPE является характерной и относительно частой токсической реакцией, связанной с некоторыми химиотерапевтическими агентами. Это болезненная припухлость и эритематозные высыпания, локализованные на ладонях и подошвах, которым часто предшествует дисестезия, обычно в форме ощущения покалывания, и часто сопутствует отек. Высыпание может стать буллезным, а затем подвергнуться десквамации без рубцевания, и боль постепенно усиливается. Эритема может также появляться в околоногтевых областях. В основном она ограничена руками и стопами, руки обычно поражаются более сильно, чем стопы.
Гистологически при PPE наблюдается умеренный спонгиоз, рассеянные некротические и дискератотические кератиноциты и вакуольная дегенерация базального слоя. Кожные изменения в большинстве случаев включают расширенные кровеносные сосуды, папилярный отек и рассеянные поверхностные периваскулярные лимфогистиоцитарные инфильтраты, которые в различной степени можно обнаружить в эпидермисе.
PPE заметно отличается от других патологических кожных реакций и рассмотрена в статье Nagore E. et al., Am J Clin Dermatol. 2000, 1(4), 225-234, которая приведена здесь в качестве ссылки в полном объеме.
Тяжесть PPE можно классифицировать согласно следующим степеням WHO:
1. Дисестезия/парестезия, покалывание в руках и стопах.
2. Дискомфорт при удержании объектов и после ходьбы, безболезненная припухлость или эритема.
3. Болезненная эритема и припухлость ладоней и ступней, околоногтевая эритема и припухлость.
4. Десквамация, образование язв, образование пузырей, сильная боль.
Другая градация основана на критериях Национального института рака США:
1. Кожные изменения или дерматит без боли (т.е. эритема, шелушение).
2. Кожные изменения с болью, не нарушающие функцию.
3. Кожные изменения с болью, нарушающие функцию.
Среди агентов, которые, как сообщается, вызывают PPE, наиболее частыми индукторами являются фторурацил (5-FU), Капецитабин (Xeloda®), пегилированый липосомальный доксорубицин (Caelyx®/Doxil®), цитарабин (Cytosar-U®), флоксуридин (FUDR®), тегафур и идарубицин (Idamycin®).
Фторурацил является фторированным пиримидином, который внутриклеточно метаболизируется до его активной формы, фторуридин монофосфата, который ингибирует синтез ДНК. Этот препарат показан при нескольких видах рака, помимо прочего в качестве адъювантной или палиативной терапии при раке молочной железы, колоректальном раке, раке желудка и поджелудочной железы. Точно установлены преимущества адъювантной химиотерапии на основе фторурацила в сокращении риска рецидива и продления выживаемости у больных с резецированным раком толстой кишки, особенно при III стадии заболевания. Преимущества в отношении выживаемости были показаны при болюсном внутривенном введении фторурацила (425 мг/м2) с лейковорином (биомодуляция) согласно режиму клиники Мейо (пять дней, ежемесячно, в течение шести месяцев), или режиму Roswell par (еженедельное болюсное введение, шесть из каждых восьми недель, в течение восьми месяцев) (Sun W. et al. Curr Oncol Rep. 2005 May; 7(3): 181-5). Для метастатического рака толстой кишки при непрерывной инфузии в течение 24 часов большой дозы 5-FU (2600 мг/м2) и лейковорина еженедельно в течение 6 недель, с последующим периодом покоя в течение 1 или 2 недель (протокол AIO) наблюдалась лучшая выживаемость без прогрессирования в сравнении с протоколом Мейо (Kohne et al. J. Clin. Oncol., 2003, vol.21, no.20, 3721-3728).
Появляются новые комбинации фторурацила, такие как с оксалиплатином (FOLFOX) или иринотеканом (FOLFIRI), показывающие лучшую выживаемость при лечении колоректального рака (Goldberg, Oncologist 2005;10 Suppl 3: 40-8. Review). В большинстве этих комбинаций используют инфузионный фторурацил.
Несмотря на очевидные преимущества фторурацила в качестве химиотерапевтического средства, при болюсном введении и режимах непрерывной инфузии высоких доз препарата часто развивается PPE. Это является причиной уменьшения дозы или прерывания лечения. При метастатическом раке толстой кишки, пролонгированный режим 5-FU2WLV приводил к более высокой частоте развития PPE (34%) в сравнении с протоколом Мейо (13%) (J. Clin. Oncol., 1998, vol.16, 3537-3541). Инфузионный фтороурацил также ответственен за PPE при лечении рака молочной железы, см., например, Smith IE et al. Ann. Oncol. 2004, 15(5) 751-758.
Капецитабин (Xeloda®) является пролекарством, пероральным фторпиримидин карбонатом, который активизируется до фторурацила в ткани опухоли посредством тимидинфосфорилазы. Этот препарат используют в качестве адъювантной терапии для лечения рака толстой кишки, в качестве терапии первой линии при метастатическом колоректальном раке, и для лечения распространенного или метастатического рака молочной железы. В III фазе исследования, о которой недавно сообщалось, капецитабин сравнивали с комбинацией фторурацил+лейковорин (протокол Мейо) в качестве адъювантной терапии при III стадии рака толстой кишки (Twelves C. et al., N Engl. J. Med. 2005, 352, 2696-2704). Было показано, что по эффективности капецитабин эквивалентен комбинации фторурацил+лейковорин. В качестве терапии первой линии при метастатическом колоректальном раке, с помощью капецитабина достигнута ответная реакция, большая, чем при режиме Клиники Мейо с эквивалентной выживаемостью без прогрессирования и общей выживаемостью (Ван Кутсем Э. и др. Br. J. Рак 2004, 90: 1190-1197). В отношении токсичности, в обоих случаях при введении капецитабина наблюдалась меньшая частота развития стоматита и нейтропении 3 или 4 степени тяжести. Однако наблюдалась значительно более высокая частота развития ладонно-подошвенного синдрома (PPE) при введении капецитабина, чем при введении комбинации фторурацил + лейковорин, что составляло 49-60% для всех степеней злокачественности и 17% для тяжелых степеней злокачественности. Это приводило к уменьшению дозы, задержке или прерыванию лечения. При метастатическом раке молочной железы возникает подобная ситуация, капецитабин в отдельности или в комбинации с доцетакселом показывает большую эффективность в сравнении с доцетакселом, но одним из наиболее частых дозолимитирующих неблагоприятных эффектов является PPE.
Ввиду вышеизложенного, несмотря на то, что капецитабин имеет важное преимущество в том, что является пероральным лекарственным средством и более удобным для пациента, в частности при комбинированном лечении, ладонно-подошвенная эритродизестезия остается одной из главных причин для беспокойства при использовании этого лекарственного средства.
Другим лекарственным средством, которое часто ассоциируется с PPE, является пегилированный липосомальный доксорубицин, то есть доксорубицина гидрохлорид, инкапсулированный в длительно-циркулирующие стерически стабилизированные липосомы с поверхностно-связанным метоксиполиэтиленгликолем. Пегилирование защищает липосомы от распознавания иммунной системой, позволяя им достигнуть ткани или органа, характеризуемых более высокой проницаемостью эндотелия, таких как опухоль. Липосомальный доксорубицин используют для лечения распространенного рака яичников и метастатического рака молочной железы. PPE при использовании этого лекарственного средства связана с режимом введения, и частота развития относительно высока: как сообщается 37,4% для всех степеней злокачественности, и 16,4% для высокой степеней злокачественности рака яичников. Токсичность может быть уменьшена с помощью снижения интенсивности дозы (например, от 50 мг/м2 каждые 4 недели до 40 мг/м2, Rose PG, The Oncologist, 2005, 10: 205-214).
Таким образом, ладонно-подошвенная эритродизестезия является важным побочным эффектом для указанных химиотерапевтических агентов. Однако немного известно о ее причинах и в настоящее время не существует никакого средства лечения или профилактики PPE с доказанной эффективностью. Уменьшение химиотерапии, задержка или прекращение лечения может быть эффективным в уменьшении проявлений или устранении PPE, но за счет серьезного риска снижения эффективности химиотерапевтического лечения рака.
Вот некоторые из немногих предложенных способов лечения: холодные компрессы или пузыри со льдом, особенно во время химиотерапии; придания рукам или стопам приподнятого положения; увлажнение кожи; смягчающие крема для кожи, содержащие ланолин, молочную кислоту, вазелиновое масло (например, Bag Balm®, мазь на основе ланолина и производных нефти с гидроксихинолинсульфатом в качестве антисептического компонента, или Aquaphor®), и местные или пероральные кортикостероиды, такие как дексаметазон.
Пиридоксин (витамин B6) использовали для уменьшения боли при PPE (Fabian et al. Invest. New Drugs 1990, 8:57-63; Lauman MK et al., ASCO Proceedings, 2001, abstract 1565), и, по-видимому, он обеспечивает некоторое симптоматическое преимущество у больных, получающих лечение капецитабином.
Амифостин, цитопротекторный агент, использовали для профилактики PPE у больных, получающих лечение липосомальным доксорубицином (Lyass O. et al., ASCO Proceedings, 2001, abstract 2148). В патенте США №6060083 раскрыто использование местного диметилсульфоксида для лечения PPE, в частности, когда осложнение вызвано использованием пегилированного липосомального доксорубицина.
В патенте США №6979688 описано местное использование урациловой мази для лечения PPE, индуцированной фторурацилом или его предшественником.
Ни один из предложенных способов лечения все же не способен приводить к эффективному лечению или профилактике PPE. Ясно, что эффективное лечение PPE по-прежнему необходимо, чтобы раскрыть полный потенциал химиотерапевтических агентов, таких как фторурацил, капецитабин или пегилированный липосомальный доксорубицин, и различных режимов и комбинаций, в которых они применяются.
Аллопуринол является структурным изомером оксипурина, который ингибирует ксантиноксидазу, фермент, который конвертирует оксипурины в мочевую кислоту. Посредством блокирования продукции мочевой кислоты этот агент уменьшает концентрацию мочевой кислоты в сыворотке и моче, таким образом обеспечивая защиту от опосредованного мочевой кислотой конечного повреждения органов в условиях, ассоциированных с повышенной продукцией мочевой кислоты. Его использовали много лет для лечения или профилактики подагры, гиперурикемии и образования почечных камней, посредством орального или парентерального системного введения.
Также сообщалось, что аллопуринол использовали для лечения мукозита, часто индуцируемого лучевой или химиотерапией повреждения быстро делящихся клеток, выстилающих ротовую полость, глотку и желудочно-кишечный (GI) тракт. Аллопуринол используют в форме жидкостей для полоскания рта (дисперсия в воде) (porta C. et al., Am. J. Cl. Oncol. 1994, Vol.17, no.3, 246-247). Улучшенная композиция жидкостей для полоскания рта, включающих аллопуринол, карбоксиметилцеллюлозу и воду, описана в патенте JP-3106817. Hanawa et al. в Drug Dev Ind. Pharm. 2004, 30(2) 151-161 описывают другую жидкость для полоскания рта, включающую аллопуринол, полиэтиленоксид и каррагенан.
Dagher et al., в Canadian Journal of Hospital pharmacy, vol.40, no.5 1987, стр.189 раскрыто использование жидкости для полоскания рта и вагинальный 0,1% крем с аллопуринолом для лечения 5-FU-индуцированного воспаления слизистой оболочки.
Аллопуринол также вводили системно для модуляции 5-фторурацил-опосредованной миелосупрессии, в частности гранулоцитопении (Woolley at al., J. of Clinical Oncology, 1985 vol.3, no.1, 103-109). Однако преклинические исследования показали антагонизм между двумя лекарственными средствами.
В EP 278040 описано использование птеридинов или ингибиторов ксантиноксидазы, помимо аллопуринола, для лечения вызванных генетически дегенеративных заболеваний сетчатки, таких как пигментная ретинопатия, в форме вводимых местно глазных капель или глазных кремов. В этом документе нет специфического раскрытия местной композиции, содержащей аллопуринол.
В WO 94/05293 и WO 94/05291 описаны синергические композиции, включающие метилсульфонилметан (MSM) и по крайней мере один из оксипуринола или аллопуринола, и их использование для лечения патологических состояний, заболеваний и повреждений кожи, таких как ожоги, дерматит, гиперкератоз, воздействие солнца, старение кожи и т.д. Оксипуринол или аллопуринол описаны как усиливающие свойства MSM по заживлению или восстановлению кожи.
Ни в одном из процитированных документов не упоминается или предполагается, что аллопуринол может быть полезен для лечения или профилактики ладонно-подошвенной эритродизестезии.
Сущность изобретения
Неожиданно было обнаружено, что аллопуринол, при местном нанесении на ладони и ступни пациента, является очень эффективным в лечении и предупреждении ладонно-подошвенной эритродизэстезии, индуцируемой химиотерапией фторпиримидином. Как показано в примерах, местное нанесение аллопуринола пациентам, страдающим раковым заболеванием, получающим лечение методами химиотерапии, полностью исключало развитие PPE.
В одном аспекте изобретение относится к применению аллопуринола или его фармацевтически приемлемой соли в производстве лекарственного средства для лечения или профилактики ладонно-подошвенной эритродизестезии, индуцированной химиотерапией фторпиримидином.
Во втором аспекте изобретение относится к фармацевтической композиции для местного введения на руки и стопы, включающую от 1 до 10 мас.% аллопуринола или его фармацевтически приемлемой соли, при условии, что она не включает метилсульфонилметан или цетомакрогол.
В третьем аспекте изобретение относится к способу лечения или предупреждения ладонно-подошвенной эритродизестезии, индуцированной химиотерапией фторпиримидином у пациента, пораженного или имеющего вероятность поражения этим синдромом, включающий местное нанесение на руки и стопы терапевтически эффективного количества аллопуринола или его фармацевтически приемлемой соли.
Подробное описание изобретения
Ладонно-подошвенная эритродизестезия (PPE) также известна как акральная эритема, ладонно-подошвенный синдром, ладонно-подошвенная эритема, синдром Burgorf's и токсическая эритема ладоней и ступней. В контексте настоящего изобретения термин "ладонно-подошвенная эритродизестезия" включает все эти синонимы, если они описывают состояния, связанные с химиотерапией, как описано выше.
В контексте настоящего изобретения термин аллопуринол относится также к различным таутомерам соединения, так как это соединение является таутомерной смесью 1H-пиразоло[3,4-d]пиримидин-4-ола и l,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-она:
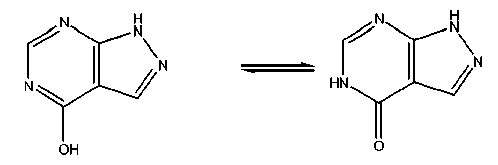
Как упомянуто выше, неожиданно было обнаружено, что местное нанесение аллопуринола или одной из его фармацевтически приемлемой соли является эффективным в лечении и профилактике PPE.
Таким образом, в одном аспекте изобретение направлено к использованию аллопуринола или его фармацевтически приемлемой соли в производстве лекарственного средства для лечения или предупреждения ладонно-подошвенной эритродизестезии, индуцированной химиотерапией фторпиримидином. В одном варианте осуществления лекарственное средство находится в форме крема. Предпочтительно крем является гидрофильным кремом.
В другом варианте осуществления лекарственное средство предназначено для лечения PPE, индуцированной фторурацилом, капецитабином или в отдельности, или в комбинации с другими агентами.
Таким образом, лекарственное средство эффективно в лечении пациентов, страдающих от рака, предпочтительно от колоректального рака, рака яичников, рака молочной железы, рака желудка и рака поджелудочной железы, и получающих химиотерапию, либо в виде адъювантной, неоадъювантной, либо паллиативной. Примеры пациентов и вариантов химиотерапии, индуцирующих PPE, были обсуждены в разделе "Уровень техники" и приведены здесь. Лекарственное средство для лечения PPE особенно эффективно у пациентов, получающих или которым планируется инфузионное введение 5-FU, капецитабина, либо в отдельности, либо в комбинации с другими агентами.
В другом варианте осуществления лекарственное средство для лечения PPE, индуцированной пегилированным доксорубицином, в частности у пациентов, получающих или планирующих получать пегилированный доксорубицин.
Не связывая с теорией, полагают, что при местном нанесении на ладони и ступни, аллопуринол действует локально на уровне эпидермиса, ингибируя метаболизм цитотоксических лекарственных средств.
Токсичность для ладоней и ступней, характеристика PPE, может развиваться вследствие специфичной местной ферментативной активности в этой области кожи ферментов, вероятно, задействованных в метаболизме цитотоксических лекарственных средств. Кератиноциты составляют до 90% эпидермальных клеток. Важно отметить, что кератиноциты ладоней и ступней имеют специфичный фенотип, такой как продукция кератина 9, гипопигментация и толстые супрабазальные слои, что отличает их от кератиноцитов кожи других областей.
Schwartz et al., в Biochem. Pharmacol., 1988, 37, 353-355 показал, что человеческие кератиноциты имеют более высокую активность тимидинфосфорилазы (TP), которая не присутствует у других животных. Эта активность ответственна за сохранение тимидина для синтеза ДНК. Другие исследования показывают сильную экспрессию TP в основном слое эпидермиса.
Тимидинфосфорилаза является ферментом, задействованным в активации 5'DFUR (метаболит капецитабина) до 5-FU. Она может также быть задействована в активации 5-FU. Тимидинфосфорилаза (TP) заметно активизируется во многих солидных опухолях, таких как колоректальный рак, рак молочной железы и почки, локально активируя пролекарства фторпиримидинов, которые "нацелены" на опухоли. Этот фермент также известен как ангиогенный тромбоцитарный фактор роста эндотелиальных клеток (PD-ECGF), который стимулирует миграцию клеток эндотелия in vitro и ангиогенез in vivo и играет важную роль в прогрессировании и метастазировании опухоли.
Fischel et al., Anti Cancer Drugs 2004, 15, 969-974, предположил, что токсичность капецитабина в ладонях и ступнях может развиваться вследствие повышенной активности TP в коже, в частности в этих областях, где, как известно, регенерация эпидермиса особенно активна. Согласно этим гипотезам, в этой области кожи могут наблюдаться высокие уровни клеточной пролиферации и активности TP, индуцирующие метаболизм лекарственного средства и ангиогенез. Таким образом, поскольку ткань ладоней и ступней проявляет сходство с тканью опухоли, вероятно, специфическая токсическая активность химиотерапевтических агентов в отношении кератиноцитов ладоней и ступней усиливается таким же образом, как и их нацеливание на пролиферирующую опухолевую ткань.
Гипотеза авторов изобретения состоит в том, что при местном введении аллопуринол действует, непосредственно или опосредованно ингибируя фермент тимидинфосфорилазу. Интересно, что Gallo et al., J. Biological Chemistry 1968, vol.243, 4943-4951, описали, что аллопуринол является селективным ингибитором дезокситимидинфосфорилазы, другое название фермента тимидинфосфорилазы. Он ингибирует TP, но не уридинфосфорилазу.
Аллопуринол может действовать, уменьшая местную продукцию активных токсических метаболитов, которые могут быть ответственны за симптомы PPE. Местное нанесение делает возможным эффективное направленное воздействие на пораженные области и позволяет избежать токсических реакций и осложнений, которые способен вызвать аллопуринол при системном введении у пациентов, страдающих раковым заболеванием, в частности это позволяет избежать интерференции с химиотерапией.
В одном варианте осуществления лечение направлено на уменьшение проявлений или профилактику PPE у пациентов, получающих лечение в виде системной химиотерапии, включающей агент, выбранный из фторурацила (5-FU) или капецитабина (Xeloda®).
В другом варианте осуществления лечение направлено на уменьшение проявлений или профилактику PPE у пациентов, получающих лечение в виде системной химиотерапии, включающей липосомальный пегилированный доксорубицин (Doxil®, Caelyx®).
Изобретение далее относится к местной фармацевтической композиции для обработки рук и стоп, включающей от 1% до 10 мас.% аллопуринола или его фармацевтически приемлемой соли, совместно по крайней мере с одним приемлемым для местного нанесения материалом-носителем, при условии, что он не включает метилсульфонилметан или цетомакрогол.
Аллопуринол является соединением, очень слабо растворимым в воде и спирте; фактически не растворимым в хлороформе и в эфире; оно растворяется в разбавленных растворах гидроксидов щелочных металлов. Его можно использовать в исходном виде, либо, для улучшения растворимости в воде, вместо основания можно использовать соль, такую как натриевая соль.
В композициях для местного применения согласно изобретению, аллопуринол или его соль обычно присутствует в количестве от приблизительно 1 до 10%, в частности от 1 до 8%, конкретнее от 1 до 6%, особенно от 1 до 5%. Концентрация аллопуринола ниже 1% является недостаточной для эффективного лечения или профилактики PPE. В концентрациях выше 10% аллопуринол может оказывать нежелательные побочные эффекты на кожу пациента.
Предпочтительный диапазон составляет от 2 до 5%, более предпочтительно от 2 до 4% от всей массы композиции. Концентрация приблизительно 3% дает хорошие результаты и является особенно предпочтительной. Все приведенные процентные показатели являются мас.%, если не указано иное.
Фармацевтические композиции согласно изобретению, подходящие для местного нанесения на руки и стопы, предпочтительно на ладони и ступни, являются, например, кремами, лосьонами, мазями, микроэмульсиями, жирными мазями, гелями, эмульсиями-гелями, пастами, пенами, настойками, растворами, пластырями, бандажами и трансдермальными терапевтическими системами. Наиболее предпочтительными являются крема или эмульсии-гели.
Кремы или лосьоны являются эмульсиями типа "масло в воде". Масляные основы, которые можно использовать, включают жирные спирты, особенно содержащие от 12 до 18 атомов углерода, например лауриловый, цетиловый или стеариловый спирт, жирные кислоты, особенно содержащие от 10 до 18 атомов углерода, например пальмитиновую или стеариновую кислоту, эфиры жирных кислот, например глицерилтрикаприлокапрат(нейтральное масло) или цетилпальмитат, воски от жидких до твердых, например изопропилмиристат, шерстяной воск или пчелиный воск, и/или углеводороды, особенно жидкие, полутвердые или твердые субстанции или их смеси, например вазелиновое масло (петролатум, Вазелин) или парафиновое масло. К подходящим эмульгаторам относятся поверхностно-активные вещества, обладающие преимущественно гидрофильными свойствами, такие как соответствующие неионные эмульгаторы, например эфиры жирных кислот и полиспиртов, и/или продукты присоединения к ним этиленоксида, в особенности - соответствующие эфиры жирных кислот с (поли)этиленгликолем, (поли)пропиленгликолем или сорбитолом, молекулы жирных кислот, содержащие в особенности от 10 до 18 атомов углерода, в особенности неполные эфиры глицерина и жирных кислот, или неполные эфиры жирных кислот и сорбитана полигидроксиэтилена, такие как эфиры жирных кислот и полиглицерина, или эфиры жирных кислот и сорбитана полиоксиэтилена (Tweens), а также эфиры жирных спиртов полиоксиэтилена или эфиры жирных кислот, молекулы жирных спиртов, в особенности содержащие от 12 до 18 атомов углерода и молекулы жирных кислот, содержащие в особенности от 10 до 18 атомов углерода, такие как эфир полигидроксиэтиленглицерола и жирной кислоты (например, Tagat S), или соответствующие ионные эмульгаторы, такие как соли щелочных металлов или сульфаты жирных спиртов, особенно имеющие от 12 до 18 атомов углерода в молекуле жирного спирта, например лаурилсульфат натрия, цетилсульфат натрия или стеарилсульфат натрия, которые обычно применяются в присутствии жирных спиртов, например цетилового спирта или стеарилового спирта. Добавками к водной фазе являются, среди прочего, агенты, которые предотвращают высыхание кремов, например увлажнители, такие как полиспирты, такие как глицерин, сорбитол, пропиленгликоль и/или полиэтиленгликоли, а также консерванты, отдушки, желирующие агенты и т.д.
Мази являются эмульсиями типа "вода в масле", которые содержат до 70%, но предпочтительно от приблизительно 20% до приблизительно 50%, воды или водной фазы. Подходящими в качестве масляной фазы являются, в особенности, углеводороды, например вазелин, парафиновое масло и/или твердые парафины, которые, для улучшения способности к связыванию воды, предпочтительно содержат подходящие гидроксисоединения, такие как жирные спирты или их эфиры, например цетиловый спирт или спирты шерстяного воска, или шерстяной воск или пчелиный воск. Эмульгаторы являются соответствующими липофильными субстанциями, например указанного выше типа, такие как эфиры жирных кислот и сорбитана (Spans), например сорбитанолеат и/или сорбитанизостеарат. Добавками к водной фазе, среди прочего, являются увлажнители, такие как полиспирты, например глицерин, пропиленгликоль, сорбитол и/или полиэтиленгликоль, а также консерванты, отдушки и т.д.
Микроэмульсии являются изотропными системами, основанными на следующих четырех компонентах: вода, сурфактант, например тензоактивный, липид, такой как неполярное или полярное масло, например парафиновое масло, природные масла, такие как оливковое или кукурузное масло, и спирт или полиспирт, содержащий липофильные группы, например 2-октилдодеканол или этоксилированные эфиры глицерина или полиглицерина. Если желательно, к микроэмульсиям могут быть добавлены другие добавки. Микроэмульсии имеют мицеллы или частицы с размерами менее 200 нм и являются прозрачными или полупрозрачными системами, формируются спонтанно и являются устойчивыми.
Жирные мази не содержат воды и содержат в качестве основания, в особенности, углеводороды, например парафин, вазелин и/или жидкие парафины, также природные или частично синтетические жиры, такие как эфиры жирных кислот и глицерина, например триглицерид кокосовой жирной кислоты, или предпочтительно отвержденные жиры, например гидрированное арахисовое масло, касторовое масло или воски, также неполные эфиры глицерина и жирных кислот, например глицерин моно- и дистеарат, а также, например, жирные спирты, увеличивающие водопоглощающую способность, эмульгаторы и/или добавки, упомянутые применительно к мазям.
В отношении гелей делают различие между водными гелями, безводными гелями и гелями, имеющими низкое содержание воды, которые состоят из набухающих, гелеобразующих материалов. В особенности используют прозрачные гидрогели, основанные на неорганических или органических макромолекулах. Высокомолекулярные неорганические компоненты, обладающие гелеобразующими свойствами, преимущественно являются водосодержащими силикатами, такими как силикаты алюминия, например бентонит, магния алюмосиликат, например вигум, или коллоидная кремневая кислота, например аэросил. В качестве высокомолекулярных используют органические субстанции, например природные, полусинтетические или синтетические макромолекулы. Природные и полусинтетические полимеры получают, например, из полисахаридов, содержащих широкое множество углеводных компонентов, таких как целлюлозы, крахмалы, трагакант, аравийская камедь и агар-агар, и желатин, альгиновую кислоту и их соли, например альгинат натрия, и их производные, такие как низшие алкилцеллюлозы, например метил- или этилцеллюлоза, низшие карбокси- или гидроксиалкилцеллюлозы, например карбоксиметил- или гидроксиэтилцеллюлоза. Компоненты синтетических гелеобразующих макромолекул являются, например, соответствующими замещенными ненасыщенными алифатическими соединениями, такими как виниловый спирт, винилпирролидин, акриловая или метакриловая кислота.
Эмульсии-гели, также называемые "эмульгели", представляют собой композиции для местного применения, которые комбинируют свойства гелей со свойствами эмульсии типа "масло в воде". В отличие от гелей, они содержат липидную фазу, которая вследствие ее восстанавливающих жир свойств позволяет втирать композицию при том, что одновременно прямая абсорбция в кожу ощущается как приятное свойство. Кроме того, можно наблюдать повышенную растворимость для липофильных активных компонентов. Одно преимущество эмульсий-гелей в сравнении с эмульсиями "масло-в-воде" состоит в усиленном охлаждающем эффекте, который обусловлен охлаждением вследствие испарения дополнительного спиртового компонента, если он присутствует.
Пены наносят, например, из герметичных контейнеров и они являются жидкими эмульсиями масло-в-воде в форме аэрозоля; незамещенные углеводороды, такие как алканы, например пропан и/или бутан, используются в качестве пропеллента. В качестве масляной фазы, используют, среди прочего, углеводороды, например парафиновое масло, жирные спирты, например цетиловый спирт, эфиры жирных кислот, например изопропилмиристат и/или другие воски. В качестве эмульгаторов используют, среди прочего, смеси эмульгаторов, имеющих преимущественно гидрофильные свойства, такие как эфиры жирных кислот и сорбитана полиоксиэтилена (Tweens), и эмульгаторов, имеющих преимущественно липофильные свойства, такие как эфиры жирных кислот и сорбитана (Spans). Также добавляют обычные добавки, такие как консерванты и т.д. Настойки и растворы, в основном, имеют этаноловую основу, к которой может быть добавлена вода и к которой добавляют, среди прочего, полиспирты, например глицерин, гликоли и/или полиэтиленгликоль, в качестве увлажнителей для уменьшения испарения, и восстанавливающие жир субстанции, такие как эфиры жирных кислот с низкомолекулярными полиэтиленгликолями, пропиленгликолем или глицерином, то есть липофильные субстанции, которые являются растворимыми в водной смеси, как замена жировых субстанций, удаляемых из кожи под воздействием этанола, и, при необходимости, другие вспомогательные средства и добавки. Подходящие настойки или растворы можно также наносить в форме спрея с помощью подходящих устройств. В этом случае, из-за проблем растворимости аллопуринола, соль является более подходящей для настоек или растворов. Трансдермальные терапевтические системы с, в частности, местной доставкой аллопуринола, содержат эффективное количество аллопуринола необязательно вместе с носителем.
Полезные носители включают абсорбируемые фармакологические подходящие растворители, помогающие проникновению активного компонента через кожу. Трансдермальные системы доставки имеют, например, форму пластыря, включающего (a) субстрат (=поддерживающий слой или пленка), (b) матрицу, содержащую активный компонент, необязательно носители и, необязательно (но предпочтительно), специальный адгезив для закрепления системы на коже, и обычно (c) защитную пленку (= антиадгезионная пленка). Матрица (b) обычно присутствует в виде смеси всех компонентов или может состоять из отдельных слоев.
Все эти системы известны специалисту в области техники. Производство фармацевтических препаратов для местного применения осуществляют с помощью способа, по существу известного, например, с помощью растворения или взвешивания аллопуринола в основе или, при необходимости, в ее части.
Композиции согласно изобретению могут также включать обычные добавки и вспомогательные вещества для дерматологических нанесений, такие как консерванты, особенно эфиры парааминобензойной кислоты, такие как метилпарабен, этилпарабен, пропилпарабен, бутилпарабен или четвертичные аммониевые соединения, такие как бензалкония хлорид, или формальдегидные доноры, такие как имидазонидинилмочевина, или спирты, такие как бензиловый спирт, феноксиэтанол, или кислоты, такие как бензойная кислота, сорбиновая кислота; кислоты или основания, используемые в качестве pH буферных наполнителей; антиоксиданты, в особенности фенольные антиоксиданты, такие как гидрохинон, токоферол и их производные, а также флавоноиды, или различные антиоксиданты, такие как аскорбиновая кислота, аскорбилпальмитат; отдушки; наполнители, такие как каолин или крахмал; пигменты или красители; UV-экранирующие агенты; увлажняющие крема, особенно глицерин, бутиленгликоль, гексиленгликоль, мочевина, гиалуроновая кислота или их производные; антисвободнорадикальные агенты, такие как витамин E или его производные; усилители проникновения, в особенности пропиленгликоль; этанол; изопропанол; диметилсульфоксид; N-метил-2-пирролидон; жирные кислоты/спирты, такие как олеиновая кислота, олеиловый спирт; терпены, такие как лимонен, ментол, 1-8 цинеол; алкиловые эфиры, такие как этилацетат, бутилацетат; агенты для образования пар ионов, такие как салициловая кислота.
Дальнейшая подробная информация относительно лекарственных форм, подходящих для местного применения, может быть получена со ссылкой на стандартные руководства, такие как Banker and Rhodes (Ed) Modern Pharmaceutics 4th ed. (2002), изданное Marcel Dekker Inc.; Harry's Cosmeticology (2000), 8th Edition, Chemical Publishing Co.; Remington's Pharmaceutical Sciences 20th ed Mack Publishing Co. (2000).
В предпочтительном варианте осуществления аллопуринол сформулирован в виде крема, предпочтительно в смягчающей основе, представляемая смягчающая основа подходит для местного нанесения на кожу, является, в основном, нетоксичной и представляет собой подходящий носитель для аллопуринола или его фармацевтически приемлемых солей. Должным образом выбранная смягчающая основа может также самостоятельно обеспечивать некоторую степень облегчения симптоматики. В конкретном случае, в качестве основы предпочтительным является увлажняющий крем.
Смягчающие вещества могут быть, например, жирными спиртами, углеводородами, триглицеридами, восками, эфирами, силиконовыми маслами и продуктами, содержащими ланолин. К жирным спиртам относятся, например, цетиловый спирт, октилдодеканол, стеариловый спирт и олеиловый спирт. Углеводороды включают минеральное масло, вазелин, парафин, сквален, полибутен, полиизобутен, гидрированный полиизобутен, церизин и полиэтилен. К триглицеридам относятся, например, касторовое масло, каприловый/каприевый триглицерид, гидрированное растительное масло, сладкое миндальное масло, масло зародышей пшеницы, кунжутное масло, гидрированное хлопковое масло, кокосовое масло, глицериды зародышей пшеницы, масло авокадо, кукурузное масло, трилаурин, гидрированное касторовое масло, масло дерева ши, масло какао, соевое масло, норковый жир, подсолнечное масло, сафлоровое масло, масло ореха макадамии, оливковое масло, масло из косточек абрикоса, масло лесного ореха и масло бурачника. К воскам относятся, например, карнаубский воск, пчелиный воск, парафин канделильского воска, масло плодов сумаха, микрокристаллический воск, масло жожоба, воск цетиловых эфиров и синтетическое масло жожоба. К эфирам относятся, например, изопропилмиристат, изопропилпальмитат, октилпальмитат, изопропиллинолеат, 12-15 алкогольбензоат, цетилпальмитат, миристилмиристат, миристиллактат, цетилацетат, пропиленгликольдикаприлат/капрат, децилолеат, стеарилгептаноат, диизостеарилмалат, октилгидроксистеарат и изопропилизостеарат. К силиконовым маслам относятся, например, диметикон (диметилполисилоксан) и циклометикон. К ланолин содержащим продуктам относятся, например, ланолин, ланолиновое масло, изопропил ланолат, ацетилированный ланолиновый спирт, ацетилированный ланолин, гидроксилированный ланолин, гидрированный ланолин и ланолиновый воск.
В предпочтительном варианте осуществления аллопуринол получают с помощью смешивания его с коммерческим кремом основой, такие как Bag Balm или Basiscreme DAC (Deutsches Arzneimittel codex).
Суточная доза лекарственной формы для местного применения, включающей аллопуринол или его фармацевтически приемлемые соли, может зависеть от различных факторов, таких как пол, возраст, вес и индивидуальное состояние пациента, а также от химиотерапии, которую он получает или будет получать.
Местные фармацевтические композиции, например, в форме кремов, эмульсий-гелей или гелей можно применять однократно, два раза или три раза в день, а также более часто в течение дня, например возможно применение от 5 до 10 раз в день, при условии, что устраняются симптомы PPE. Дозировка может варьировать в зависимости от тяжести симптомов PPE или циклов или дозировок химиотерапевтического лекарственного средства.
Фармацевтическая композиция изобретения применяется пациентами, уже страдающими от PPE в ее различных степенях, или в качестве профилактического средства пациентами, склонными к развитию PPE вследствие химиотерапевтического лечения, которое пациенту проводится или предполагается проводить.
Применение может быть более интенсивным непосредственно перед, во время и после химиотерапевтического лечения, когда риск развития PPE является более высоким, и может быть уменьшено во время периодов отдыха между циклами. Изобретение будет далее иллюстрировано посредством примеров, которые не должны пониматься как ограничивающие объем изобретения, который определен в соответствии с формулой изобретения.
Примеры
Пример 1. Получение лекарственной формы для местного применения, включающей аллопуринол
Композицию изготовили с помощью взвешивания основания аллопуринола (3 мас.% от массы всей композиции) в 5% воды и последующего добавления Basiscreme DAC (92%) и перемешивания.
Композиция основного крема DAC включает следующие компоненты:
глицеролмоностеарат: 4,0
цетиловый спирт 6,0
среднецепочечный триглицерид 7,5
белый вазелин 25,5
полиоксиэтиленглицерол моностеарат 7,0
пропиленгликоль 10,0
вода 40,0.
Получаемый в результате крем распределяют в подходящие контейнеры и оставляют на хранение. Крем легко используется пациентами.
Пример 2. Лечение ладонно-подошвенной эритродизестезии
Пациентам с колоректальной карциномой проводили химиотерапию (адъювантную или паллиативную), следуя обычным протоколам. Сразу после появления первых симптомов ладонно-подошвенной эритродизестезии после начала химиотерапии пациентам наносили крем, изготовленный в примере 1.
Характеристики пациентов, получавших лечение кремом, и назначаемый химиотерапевтический режим были следующими:
Пациенты с продвинутым или метастатическим колоректальным раком: 8
Пациенты с резецированным раком толстой кишки III стадии: 2
Химиотерапия:
5FU +LV болюсно (протокол Мейо): 1 пациент
5FU +LV инфузионно (протокол AIO): 7 пациентов
Монотерапия капецитабином: 2 пациента
Крем наносили 5 раз в сутки, на ладони и ступни, все время, пока проводили химиотерапию. Частоту уменьшали между циклами и увеличивали непосредственно до и во время проведения химиотерапии.
Результаты: после местного лечения аллопуринолом исчезли симптомы PPE, и химиотерапию можно было закончить без какого-либо сокращения дозы или задержки лечения из-за PPE. Наиболее примечательной в случае пациентов, получавших лечение в виде инфузионного введения высокой дозы 5FU24H + лейковорин, была частота развития PPE, которая, как сообщалось, составила 34%.
Пример 3. Лечение ладонно-подошвенной эритродизестезии
Пациенты, страдающие от рака толстой кишки или рака молочной железы, получавшие лечение с января 2005 по март 2007 в виде следующей схемы стандартной химиотерапии:
- Протокол AIO: инфузия высокой дозы 5FU24H + лейковорин
- FOLFOX 4 протокол: день 1: оксалиплатин, 85 мг/м2, и лейковорин, 200 мг/м2, одновременно в/в, затем 5-FU, 400 мг/м2 в/в болюсно, с последующим 600 мг/м2 непрерывно в/в; день 2: лейковорин, 200 мг/м2 в/в, затем 5-FU, 400 мг/м2 в/в болюсно, с последующим 600 мг/м2 непрерывно в/в; с повтором каждые 2 недели.
- Пероральный прием капецитабина.
Характеристики пациенты суммированы в таблице 1.
Характеристики пациентов
Средний
Разброс значений
(42-83)
0
1
2
14
0
Мужской
Женский
24
Рак молочной железы
Рак толстой кишки
27
Да
Нет
25
5-FUL: AIO
FOLFOX 4
Капецитабин
7
12
Ладонно-подошвенная эритродизестезия (PPE) появилась у 30% пациентов, получавших лечение 5-FU, и у 66% пациентов, получавших лечение капецитабином. Время появления и тяжесть симптомов были вариабельны, это суммировано в таблице 2.
Ладонно-подошвенная эритродизестезия
Общее число
Симптомы PPE
AIO
FOLFOX 4
Капецитабин
15 (35)
5 (16)
2 (7)
8 (12)
31%
28%
66%
1
2
3
5
9
33%
60%
AIO
Среднее значение
Разброс значений
FOLFOX 4
Среднее значение
Разброс значений
(23000-64800 мг)
40000 мг
(38000-42000 мг)
Среднее значение
Разброс значений
(35000-180000 мг)
Эти данные сильно коррелируют с сообщаемой частотой развития PPE.
Крем, включающий аллопуринол, изготовленный в примере 1, местно наносили пациентам 4-5 раз в день на руки и стопы. В случае отсутствия реакции на это лечение и сохранения симптомов PPE, дозу химиотерапии снижали, и в некоторых случаях прерывали. Реакции суммированы в таблице 3.
Реакция на лечение аллопуринолом
(TR)
(CR)
(PR)
(NR)
13
10
3
2
66,6%
20,0%
13,3%
(TR)
(CR)
(PR)
(NR)
5
4
1
0
80%
20%
0%
(TR)
(CR)
(PR)
(NR)
1
0
1
1
50%
50%
(TR)
(CR)
(PR)
(NR)
7
5
2
1
62,5%
25%
12,5%
CR: полная ремиссия
PR: частичная ремиссия
NR: отсутствие реакции.
У 86% пациентов наблюдалась реакция на лечение с сокращением симптомов в 20% и с полным исчезновением в 66%.
Не наблюдалось никаких токсических эффектов, связанных с местным лечением аллопуринолом, и комплаентность пациентов и улучшение симптоматики PPE были удивительными. В результате качество жизни значительно улучшилось.
У 86% пациентов, у которых развилась PPE, лечение аллопуринолом позволило завершить химиотерапию, как было запланировано.
Предложено применение аллопуринола или его фармацевтически приемлемой соли для лечения или предупреждения ладонно-подошвенной эритродизестезии (РРЕ), индуцированной химиотерапией фторпиримидинами, соответствующий способ лечения и фармацевтическая композиция для нанесения на кожу того же назначения, причем композиция не включает метилсульфонилметан или цетомакрогол. Показано сокращение, а у 66% больных - полное исчезновение симптомов РРЕ при отсутствии токсических эффектов на аллопуринол и комплаентности пациентов. 3 н. и 9 з.п. ф-лы, 3 табл.
1. Применение аллопуринола или его фармацевтически приемлемой соли для изготовления лекарственного средства для лечения или предупреждения ладонно-подошвенной эритродизестезии (РРЕ), индуцированной химиотерапией фторпиримидинами.
2. Применение по п.1, где лекарственное средство предназначено для местного нанесения на кожу, предпочтительно для местного нанесения на руки и стопы.
3. Применение по п.2, где лекарственное средство представлено в форме крема.
4. Применение по любому из пп.1-3, где ладонно-подошвенная эритродизестезия индуцирована химиотерапией 5-фторурацилом.
5. Применение по любому из пп.1-3, где ладонно-подошвенная эритродизестезия индуцирована химиотерапией капецитабином.
6. Фармацевтическая композиция для лечения или предупреждения ладонно-подошвенной эритродизестезии (РРЕ) посредством местного нанесения на кожу, включающая 1-10 мас.% от массы всей композиции аллопуринола или его фармацевтически приемлемой соли, при условии, что она не включает метилсульфонилметан или цетомакрогол.
7. Фармацевтическая композиция по п.6, дополнительно включающая пиридоксин.
8. Фармацевтическая композиция по п.6 или 7 в форме крема, предпочтительно в форме гидрофильного крема.
9. Фармацевтическая композиция по п.6 или 7, включающая от приблизительно от 1 до 8 мас.% аллопуринола или его фармацевтически приемлемой соли от массы композиции, предпочтительно от приблизительно 1 мас.% до приблизительно 5 мас.%, более предпочтительно от приблизительно 2 мас.% до приблизительно до 4 мас.%.
10. Способ лечения или предупреждения ладонно-подошвенной эритродизестезии, индуцированной химиотерапией фторпиримидином у пациента, пораженного или имеющего вероятность поражения этим синдромом, включающий местное нанесение на руки и стопы терапевтически эффективного количества аллопуринола или его фармацевтически приемлемой соли.
11. Способ по п.10, в котором химиотерапия включает лекарственное средство, выбранное из фторурацила или капецитабина.
12. Способ по п.10, в котором аллопуринол или его соль вводят в форме крема.
| Кондратьев В.Б | |||
| Осложнения химиотерапии рака ободочной кишки и методы их лечения | |||
| Практическая онкология, 2000, №1 (март), с.31-36 [он-лайн] [найдено 2010-11-18] (Найдено из базы данных YANDEX) | |||
| МИХАЙЛОВ И.Б | |||
| Настольная книга врача по клинической фармакологии | |||
| - СПб.: Фолиант, 2001, с.610-612 | |||
| Tsavaris NB et al | |||
| Decreased oral toxicity with |
Авторы
Даты
2012-01-10—Публикация
2007-05-31—Подача