Область техники, к которой относится изобретение
[0001]
Настоящее изобретение относится к новому карбоксилатному соединению, способу его получения и ароматизирующей композиции, содержащей карбоксилатное соединение, и, в частности, настоящее изобретение относится к карбоксилатному соединению, которое можно использовать в качестве исходного материала для ароматизирующих композиций, к способу его получения и к ароматизирующей композиции, содержащей карбоксилатное соединение.
Уровень техники
[0002]
Известно, что некоторые сложные эфиры представляют собой соединения, которые можно использовать в качестве ароматизаторов. Например, геранилацетат с ароматом розы, метилжасмонат, имеющий сладкий аромат жасминового типа, Фруитат (этилтрицикло[5.2.1.02,6]декан-2-карбоксилат), имеющий фруктовый аромат, и метилбензоат с интенсивным ароматом сухофруктов могут использоваться в качестве ингредиентов для ароматизирующих композиций. Кроме того, в патентном документе 1 описано, что карбоксилатное соединение, являющееся производным камфена, обладает освежающим сосновым ароматом.
Перечень ссылок
Патентные документы
[0003]
Патентный документ 1: WO 2012/063433
Сущность изобретения
Техническая задача
[0004]
Задачей настоящего изобретения является предоставление нового карбоксилатного соединения, имеющего фруктовый аромат, способа его получения, и ароматизирующей композиции, содержащей карбоксилатное соединение.
Решение задачи
[0005]
Авторы настоящего изобретения синтезировали различные соединения и исследовали их ароматы, и обнаружили, что некоторые карбоксилатные соединения имеют фруктовый аромат, что привело к осуществлению настоящего изобретения.
[0006]
Настоящее изобретение предусматривает следующие аспекты с <1> по <4>.
<1> Карбоксилатное соединение, представленное формулой (1).
[0007]
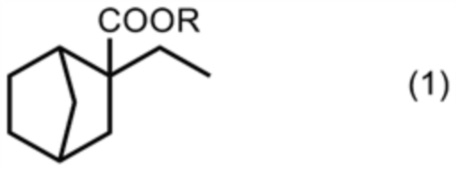
где R представляет собой алкильную группуй, имеющую от 2 до 6 атомов углерода.
[0008]
<2> Карбоксилатное соединение по <1>, где R представляет собой этильную группу, н-пропильную группу или изопропильную группу.
<3> Ароматизирующая композиция, содержащая карбоксилатное соединение, представленное формулой (1).
[0009]

где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
[0010]
<4> Способ получения карбоксилатного соединения, представленного формулой (1), путем взаимодействия соединения, представленного формулой (2), с монооксидом углерода в присутствии фтороводорода, и затем взаимодействия со спиртом, имеющим от 2 до 6 атомов углерода.
[0011]

где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
[0012]
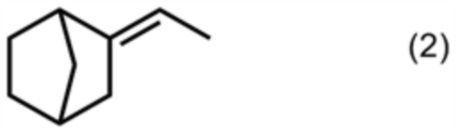
Полезные эффекты изобретения
[0013]
Карбоксилатное соединение настоящего изобретения обладает фруктовым ароматом и может использоваться в качестве ароматизирующего компонента в широком спектре продуктов, таких как туалетные принадлежности, мыла и моющие средства для одежды. Кроме того, в соответствии со способом получения карбоксилатного соединения по настоящему изобретению карбоксилатное соединение может быть получено промышленно рентабельным способом.
Описание вариантов осуществления
[0014]
Настоящее изобретение будет описано ниже с использованием вариантов осуществления. Следует отметить, что в следующем далее описании формулировки «от A до B», указывающие числовой диапазон, означают «больше или равно А и меньше или равно В» (когда А<В) или «меньше или равно А и больше или равно В» (когда А>В). Другими словами, формулировки «от A до B» указывают числовые диапазоны, включающие конечные точки A и B.
Кроме того, термины «массовые части» и «массовые %» являются синонимами терминов «весовые части» и «% масс.», соответственно.
[0015]
[Карбоксилатное соединение]
Карбоксилатное соединение настоящего изобретения представлено формулой (1) ниже.
[0016]

где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
[0017]
В формуле (1) R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода. Алкильная группа, имеющая от 2 до 6 атомов углерода, предпочтительно является линейной или разветвленной алкильной группой, и ее примеры включают этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, пентильную группу и гексильную группу. Среди перечисленного, с точки зрения ароматизирующих свойств, предпочтительны этильная группа, н-пропильная группа и изопропильная группа, и более предпочтительна этильная группа.
[0018]
Карбоксилатное соединение, представленное формулой (1), имеет стереоизомер и может быть экзоизомером или эндоизомером, или смесью экзо- и эндоизомеров в любом соотношении, и оно не имеет особых ограничений.
Среди перечисленного, экзоизомер является предпочтительным с точки зрения легкости производства и ароматизирующих свойств.
[0019]
[Способ получения карбоксилатного соединения]
Карбоксилатное соединение настоящего изобретения (карбоксилатное соединение, представленное формулой (1)) может быть преимущественно получено в промышленности способом, в котором соединение, представленное формулой (2), реагирует с монооксидом углерода в присутствии фтороводорода (далее также называемого «HF») с последующей реакцией со спиртом, имеющим от 2 до 6 атомов углерода.
В частности, соединение, представленное формулой (2), подвергают карбонилированию путем взаимодействия с монооксидом углерода в присутствии фтороводорода (HF), в результате чего получают фторангидрид, представленный формулой (3). Затем фторангидрид, представленный формулой (3), этерифицируют путем реакции его со спиртом, имеющим от 2 до 6 атомов углерода в присутствии фтороводорода.
[0020]
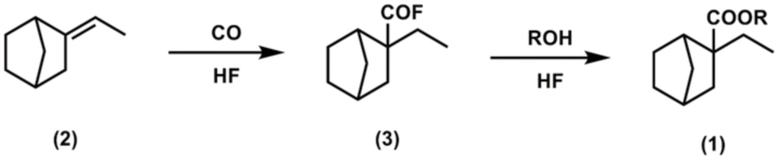
где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
[0021]
(Соединение, представленное формулой (2))
Соединение, представленное формулой (2), представляет собой 2-этилиденнорборнан и может быть получено гидрированием 5-этилиден-2-норборнена (ENB). Следует отметить, что ENB известен в качестве сырья для этиленпропилендиенового (EPDM) каучука.
[0022]
(Монооксид углерода)
Монооксид углерода, используемый в настоящем изобретении, может содержать инертный газ, такой как азот или метан. Парциальное давление монооксида углерода во время реакции находится в диапазоне предпочтительно от 0,5 до 5 МПа (изб.), и более предпочтительно - от 1 до 3 МПа (изб.). Если парциальное давление монооксида углерода выше 0,5 МПа (изб.), то реакция карбонилирования протекает достаточно быстро, и гетерогенность и побочные реакции, такие как полимеризация, не происходят одновременно, и алициклическое карбонильное соединение, которое является целевым продуктом, может быть получено с высоким выходом. Кроме того, с точки зрения нагрузки на оборудование, предпочтительно, чтобы парциальное давление монооксида углерода не превышало 5 МПа (изб.).
[0023]
(Фтороводород)
HF, используемый в настоящем изобретении, является растворителем для реакции, а также катализатором и исходным материалом, и поэтому предпочтительно использование практически безводного HF. Используемое количество HF в пересчете на молярное отношение относительно исходного соединения, представленного формулой (2), предпочтительно в 4-25 раз больше, и более предпочтительно - в 6-15 раз больше. Если молярное соотношение HF превышает в 4 раза или более, реакция карбонилирования протекает эффективно, гетерогенность и побочные реакции, такие как полимеризация, могут быть подавлены, и карбонильное соединение, которое является целевым продуктом, может быть получено с высоким выходом. Кроме того, с точки зрения стоимости сырья и производительности предпочтительно использовать HF при 25-кратном или меньшем молярном отношении.
[0024]
(Реакционный растворитель)
В реакции карбонилирования можно использовать растворитель, который полностью растворяет исходные материалы и является инертным по отношению к HF. Например, можно использовать насыщенные углеводородные соединения, такие как гексан, гептан и декан. Наличие или отсутствие и используемое количество растворителя не имеют особых ограничений и могут быть выбраны надлежащим образом. Однако с точки зрения подавления реакции полимеризации и повышения выхода, массовое отношение растворителя к исходному соединению формулы (2) предпочтительно является 0,2-2,0 -кратным, и с точки зрения производительности и энергоэффективности массовое отношение растворителя предпочтительно является 0,5-1,2 -кратным.
[0025]
(Условия реакции карбонилирования)
Реакцию карбонилирования можно проводить любым способом, например, периодическим, полупериодическим или непрерывным, что не имеет особых ограничений.
Температура реакции карбонилирования находится в диапазоне предпочтительно от -50°С до 30°С, и более предпочтительно - от -30°С до 20°С. С точки зрения скорости реакции, реакцию предпочтительно проводить при температуре -50°С или выше. Кроме того, с точки зрения снижения количества образующихся изомеров реакцию предпочтительно проводить при температуре 30°C или ниже.
Время реакции карбонилирования предпочтительно составляет не менее 1 ч с точки зрения обеспечения полноты реакции и предпочтительно не более 5 ч с точки зрения эффективности реакции. Конечная точка реакции не имеет особых ограничений, и, например, реакция может быть остановлена, когда поглощение монооксида углерода прекращается.
[0026]
В реакции карбонилирования фторангидрид (формула (3)) образуется с помощью HF и монооксида углерода. Полученный реакционный раствор фторангидрида (реакционный раствор карбонилирования) может быть очищен обычным способом, таким как дистилляция после отгонки избытка HF, и затем очищенный раствор фторангидрида можно использовать в качестве сырья на последующей стадии этерификации. Однако обычно применяется способ получения карбоксилатного соединения путем реакции, в существующем состоянии, раствора реакции карбонилирования, содержащего HF-катализатор, со спиртом.
[0027]
(Спирт)
Спирт, используемый в настоящем изобретении, представляет собой спирт, содержащий от 2 до 6 атомов углерода.
Спирт, содержащий от 2 до 6 атомов углерода, не имеет особых ограничений, и может быть надлежащим образом выбран в соответствии с целью, и примеры включают этанол, н-пропанол, изопропанол, н-бутанол, изобутанол, трет-бутанол, пентанол и гексанол. Среди перечисленного, предпочтительными являются этанол, н-пропанол, изопропанол, н-бутанол и изобутанол; этанол, н-пропанол и изопропанол являются более предпочтительными, и этанол является еще более предпочтительным.
Используемое количество спирта, содержащего от 2 до 6 атомов углерода, не имеет особых ограничений, и может быть подходящим образом выбрано в соответствии с целью, и относительно исходного соединения формулы (2) молярное отношение его используемого количества предпочтительно составляет от 0,5 до 2,0, более предпочтительно от 0,8 до 1,7, и еще более предпочтительно от 1,0 до 1,7.
[0028]
(Условия реакции этерификации)
С точки зрения повышения выхода, температура реакции этерификации предпочтительно не ниже -20°С, и с точки зрения подавления побочных реакций, таких как разложение сложного эфира и дегидратация добавленного спирта, температура реакции предпочтительно не превышает 20°C.
Время реакции этерификации предпочтительно составляет не менее 0,5 ч с точки зрения завершения реакции, и предпочтительно составляет не более 3 ч с точки зрения эффективности реакции. Конечная точка реакции не имеет особых ограничений и, например, реакция может быть остановлена, когда не наблюдается увеличения теплоты реакции.
[0029]
Полученный таким образом этерифицированный продукт представляет собой раствор комплекса карбоксилат/HF. При нагревании раствора комплекса карбоксилат/HF связи между карбоксилатом и HF разрушаются, и HF может быть переведен в пар, извлечен и повторно использован. Операция разложения этого комплекса должна проводиться как можно быстрее, чтобы избежать ухудшения качества продукта при нагревании, изомеризации и тому подобного. Чтобы ускорить термическое разложение комплекса, предпочтительно, например, разлагать комплекс при нагревании с обратным холодильником растворителя, инертного к HF (например, насыщенного алифатического углеводорода, такого как гептан, или ароматического углеводорода, такого как толуол). Кроме того, когда реакционный раствор экстрагируют в ледяную воду, предпочтительно, например, реакционный раствор экстрагируют в ледяную воду из нижней части автоклава и разделяют на масляную фазу и водную фазу, после чего масляную фазу дважды промывают 2% масс. водным раствором гидроксида натрия и дважды - дистиллированной водой, и далее обезвоживают безводным сульфатом натрия. Полученный таким образом раствор пропускают далее через испаритель для удаления низкокипящих соединений и тому подобного, и затем подвергают ректификации с помощью ректификатора, имеющего число теоретических тарелок около 20, и благодаря этому может быть получено очищенное карбоксилатное соединение.
[0030]
Следует отметить, что карбоксилатное соединение настоящего изобретения может быть получено иным способом, чем описанный выше. Например, как показано на приведенных ниже схемах, альдегидное соединение (формула (4)), полученное по реакции Дильса-Альдера между циклопентадиеном и 2-этилакролеином, может быть окислено с получением соединения карбоновой кислоты (формула (5)), затем соединение карбоновой кислоты подвергают взаимодействию со спиртом, имеющим от 2 до 6 атомов углерода, с получением сложноэфирного соединения (формула (6)), и сложноэфирное соединение затем может быть гидрировано с получением карбоксилатного соединения настоящего изобретения (карбоксилатного соединения, представленного формулой (1)). Кроме того, соединение карбоновой кислоты, представленное формулой (5), может быть получено по реакции Дильса-Альдера между циклопентадиеном и 2-этилакриловой кислотой (2-метиленмасляной кислотой).
[0031]
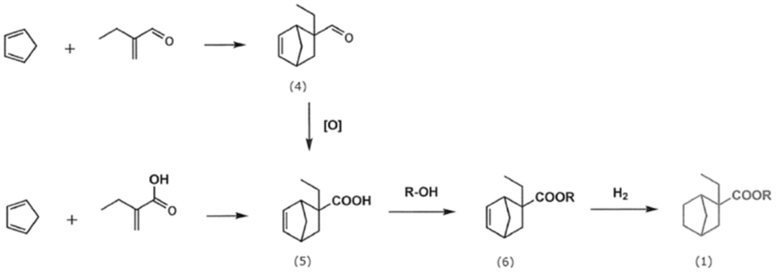
где R является алкильной группой, имеющей от 2 до 6 атомов углерода.
[0032]
Карбоксилатное соединение настоящего изобретения обладает фруктовым ароматом и поэтому может быть использовано отдельно или в сочетании с другими компонентами в качестве ароматизирующего компонента в таких продуктах, как мыла, шампуни, ополаскиватели, моющие средства, косметика, спреи, ароматические вещества, парфюмерные изделия и соли для ванн. Также можно предполагать использование в качестве синтетического промежуточного продукта для пищевых продуктов, фармацевтических препаратов, агрохимикатов, жидких кристаллов и тому подобного.
[0033]
[Ароматизирующая композиция]
Ароматизирующая композиция настоящего изобретения содержит карбоксилатное соединение, представленное формулой (1).
Ароматизирующая композиция настоящего изобретения может быть получена путем смешивания и объединения одного или более типов карбоксилатных соединений, представленных формулой (1), с другим обычно используемым ароматизирующим компонентом или желаемой ароматизирующей композицией. Смешиваемое количество карбоксилатного соединения, представленного формулой (1), различается в зависимости от типа ароматизирующей композиции, типа целевого аромата, интенсивности аромата и тому подобного, однако добавление 0,01-90% масс. к ароматизирующей композиции является предпочтительным, и добавление 0,1-50% масс. является более предпочтительным.
[0034]
Другой ароматизирующий компонент, который можно использовать в сочетании с карбоксилатным соединением настоящего изобретения, не имеет особых ограничений и может быть надлежащим образом выбран в соответствии с целью. Примеры включают:
углеводороды, такие как лимонен, α-пинен, β-пинен, терпинен, цедрен, лонгифолен и валенцен;
[0035]
спирты, такие как линалоол, цитронеллол, гераниол, нерол, терпинеол, дигидромирценол, этиллиналоол, фарнезол, неролидол, цис-3-гексенол, цедрол, ментол, борнеол, β-фенилэтиловый спирт, бензиловый спирт, фенилгексанол, 2,2,6-триметилциклогексил-3-гексанoл, 1-(2-трет-бутилциклогексилoкси)-2-бутанол, 4-изопропилциклогексанметанол, 4-метил-2-(2-метилпропил)тетрагидро-2H-пиран-4-ол, 2-метил-4-(2,2,3-триметил-3-циклопентен-1-ил)-2-бутен-1-ол, 2-этил-4-(2,2,3-триметил-3-циклопентен-1-ил)-2-бутен-1-ол, изокамфилциклогексанол и 3,7-диметил-7-метоксиоктан-2-ол;
фенолы, такие как эвгенол, тимол и ванилин;
[0036]
сложные эфиры, такие как линалилформиат, цитронеллилформиат, геранилформиат, н-гексилацетат, цис-3-гексенилацетат, линалилацетат, цитронеллилацетат, геранилацетат, неллилацетат, терпинилацетат, нопилацетат, борнилацетат, изоборнилацетат, о-трет-бутилциклогексилацетат, п-трет-бутилциклогексилацетат, трициклодеценилацетат, бензилацетат, стиралилацетат, циннамилацетат, диметилбензилкарбинилацетат, 3-пентилтетрагидропиран-4-илацетат, цитронеллилпропионат, трициклодеценилпропионат, аллилциклогексилпропионат, этил-2-циклогексилпропионат, бензилпропионат, цитронеллилбутират, диметилбензилкарбинил-н-бутират, трициклодеценилизобутират, метил-2-ноненоат, метилбензоат, бензилбензоат, метилциннамат, метилсалицилат, н-гексилсалицилат, цис-3-гексенилсалицилат, геранилтиглат, цис-3-гексенилтиглат, метилжасмонат, метилдигидрожасмонат, метил-2,4-дигидрокси-3,6-диметилбензоат, этилметилфенилглицидат, метилантранилат и фруитат;
[0037]
альдегиды, такие как н-октаналь, н-деканаль, н-додеканаль, 2-метилундеканаль, 10-ундеценаль, цитронеллаль, цитраль, гидроксицитронеллаль, диметилтетрагидробензальдегид, 4(3)-(4-гидрокси-4-метилпентил)-3-циклогексен-1-карбальдегид, 2-циклогексилпропаналь, п-трет-бутил-α-метилгидрокоричный альдегид, п-изопропил-α-метилгидрокоричный альдегид, п-этил-α,α-диметилгидрокоричный альдегид, α-амилкоричный альдегид, α-гексилкоричный альдегид, пиперональ и α-метил-3,4-метилендиоксигидрокоричный альдегид;
[0038]
кетоны, такие как метилгептенон, 4-метилен-3,5,6,6-тетраметил-2-гептанон, амилциклопентанон, 3-метил-2-(цис-2-пентен-1-ил)-2-циклопентен-1-он, метилциклопентенолон, розовый кетон, γ-метилионон, α-ионон, карбон, ментон, камфора, нуткатон, бензилацетон, анисилацетон, метил-β-нафтилкетон, 2,5-диметил-4-гидрокси-3(2H)-фуранон, мальтол, 7-ацетил-1,2,3,4,5,6,7,8-октагидро-1,1,6,7-тетраметилнафталин, мускон, циветон, циклопентадеканон и циклогекседеценон;
[0039]
ацетали и кетали, такие как этилфенилпропилацеталь ацетоальдегида, цитральдиэтилацеталь, глицеринацеталь фенилацетоальдегида и этиленгликолькеталь этилацетоацетата;
простые эфиры, такие как анетол, β-нафтилметиловый эфир, β-нафтилэтиловый эфир, лимоненоксид, розеноксид, 1,8-цинеол, рацемический или фотоактивный додекагидро-3а,6,6,9а-тетраметилнафто[2,1-b]фуран;
нитрилы, такие как цитронеллилнитрил;
[0040]
лактоны, такие как γ-ноналактон, γ-ундекалактон, σ-декалактон, γ-жасмолактон, кумарин, циклопентадеканолид, циклогексадеканолид, амбреттолид, этиленбрассилат и 11-оксагексадеканолид; и
природные эфирные масла и природные экстракты апельсина, лимона, бергамота, мандарина, перечной мяты, кудрявой мяты, лаванды, ромашки, розмарина, эвкалипта, шалфея, базилика, розы, герани, жасмина, иланг-иланга, аниса, гвоздики, имбиря, мускатного ореха, кардамона, кедра, японского кипариса, ветивера, пачули и лабданума. Кроме того, эти и другие ароматические компоненты могут быть смешаны по отдельности или в комбинации двух или более.
[0041]
Карбоксилатное соединение, представленное формулой (1), придает превосходный фруктовый аромат и, поэтому ароматизирующая композиция, содержащая карбоксилатное соединение, представленное формулой (1), может использоваться в качестве ароматизирующего компонента для различных продуктов, таких как парфюмерия и косметика, оздоровительные и гигиенические материалы, различные товары, продукты питания, парафармацевтическая продукция и фармацевтические препараты, для улучшения аромата приготавливаемого продукта.
[0042]
Ароматизирующая композиция, содержащая карбоксилатное соединение, представленное формулой (1), может быть использована в качестве ароматизирующего компонента для различных продуктов, включая, например, парфюмерные продукты, такие как духи и одеколоны; косметические средства для волос, такие как шампуни, ополаскиватели, тоники для волос, кремы для волос, муссы, гели, помады, спреи; косметические средства для кожи, такие как лосьоны для лица, сыворотки, кремы, эмульсии, маски для лица, крема-основы, пудры для лица, губные помады и различные виды макияжа; различные моющие средства для здоровья и санитарии, такие как средства для мытья посуды, средства для стирки, умягчители, дезинфицирующие моющие средства, средства для устранения запаха, ароматизаторы для помещений, средства для ухода за мебелью, средства для очистки стекол, средства для очистки мебели, очистители полов, дезинфицирующие средства, инсектициды и отбеливатели; парафармацевтические препараты, такие как зубная паста, ополаскиватель для полости рта, соли для ванн, антиперспиранты и растворы для перманентной завивки волос; прочие товары, такие как туалетная бумага и папиросная бумага; фармацевтические препараты и пищевые продукты.
[0043]
Кроме того, количество ароматизирующей композиции настоящего изобретения, которое смешивают с продуктом, не имеет особых ограничений и может быть должным образом выбрано в соответствии с целью, однако количество карбоксилатного соединения, представленного формулой (1), которое смешивают с продуктом, предпочтительно составляет 0,001-50% масс. и более предпочтительно 0,01-20% масс.
Примеры
[0044]
Настоящее изобретение будет описано более детально ниже с использованием примеров и сравнительных примеров, но настоящее изобретение не ограничивается этими примерами.
[0045]
<Условия проведения газохроматографического анализа>
Газовая хроматография осуществлялась с помощью газового хроматографа («GC-2010 Plus», доступного от Shimadzu Corporation) и капиллярной колонки («HR-1» (0,32 мм ∅ × 25 м, доступной от Shinwa Chemical Industries Ltd). В качестве условия повышения температуры температуру повышали от 100°C до 310°C со скоростью 5°C/мин.
[0046]
<ГХ-МС>
Использовали ГХ-МС спектрометр JMS-T100GCV, доступный от JEOL Ltd.
[0047]
<1H-ЯМР и 13С-ЯМР спектроскопия>
Измерения проводили при следующих условиях.
Устройство: ЯМР-спектрометр JNM-ECA500, доступный от JEOL Ltd.
Вещество внутреннего стандарта: тетраметилсилан (TMS)
[0048]
<Выход карбоксилатного соединения, соотношение изомеров>
- Выход карбоксилатного соединения (мол.%) = (количество моль карбоксилатного соединения)/(количество моль 2-этилиденнорборнана) × 100
- Соотношение изомеров (%) = (количество моль 2-этилнорборнан-экзо-2-карбоксилата)/(общее количество моль карбоксилатного соединения) × 100
[0049]
Пример 1 синтеза
(Получение 2-этилиденнорборнана гидрированием 5-этилиден-2-норборнена (ENB))
В автоклав из нержавеющей стали, имеющий внутренний объем 200 мл, оснащенный магнитной мешалкой, тремя впускными патрубками в верхней части и одним патрубком отведения в нижней части, и способный регулировать внутреннюю температуру с помощью рубашки, загружали 2,0 г Cu-Cr катализатора («N-203S», доступного от JGC Catalysts and Chemicals Ltd.) и 30 г гептана (гарантированной чистоты, доступного от Wako Pure Chemical Corporation) и активировали в течение 1 ч при 170°С при давлении водорода 1 МПа (изб.). После охлаждения дополнительно добавляли 100 г 5-этилиден-2-норборнена (доступного от Tokyo Chemical Industry Co., Ltd.), и смесь перемешивали и подвергали реакции гидрирования в течение 2 ч при 90°С и давлении водорода 2 МПа (изб.). Реакционный раствор фильтровали для удаления катализатора, и гептан, который является растворителем, отгоняли, и получали 89 г жидкого продукта реакции (далее также может называться «реакционный раствор»), содержащего 2-этилиденнорборнан в концентрации 95% масс. и 2-этилнорборнан в концентрации 5% масс. (выход: 88 мол.% (выход рассчитывали из общего количества моль 2-этилиденнорборнана и 2-этилнорборнана по отношению к количеству моль исходного материала 5-этилиден-2-норборнена). Выход 2-этилиденнорборнана составлял 84 мол.% (рассчитывали из количества моль 2-этилиденнорборнана по отношению к количеству моль 5-этилиден-2-норборнена).
Уравнение реакции показано ниже.
[0050]
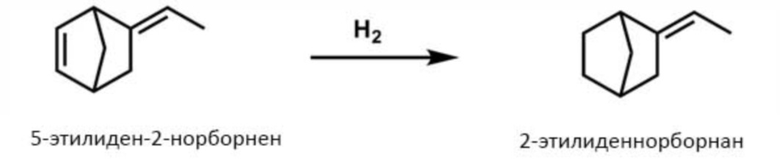
[0051]
Пример 1
(Получение этил-2-этилнорборнан-2-карбоксилата путем карбонилирования и этерификации 2-этилиденнорборнана)
Эксперимент проводили с использованием автоклава из нержавеющей стали, способного регулировать внутреннюю температуру с помощью рубашки. Автоклав имел внутренний объем 500 мл и был оснащен магнитной мешалкой, тремя впускными патрубками в верхней части и одним патрубком отведения в нижней части.
Сначала внутреннюю часть автоклава продували монооксидом углерода, после чего вводили 158 г (7,9 моль) фтороводорода, и температуру жидкости доводили до 0°C, и затем давление повышали до 2 МПа (изб.) монооксидом углерода.
В то время как температуру реакции и давление реакции поддерживали при 0°С и 2 МПа (изб.), соответственно, смешанный раствор из 82 г реакционного раствора, приготовленного в примере 1 синтеза (концентрация 2-этилиденнорборнана: 95% масс., концентрация 2-этилнорборнана: 5% масс.), и 82 г гептана (гарантированной чистоты, доступного от Wako Pure Chemical Corporation) подавали из верхней части автоклава в течение 60 мин, и проводили реакцию карбонилирования. После прекращения подачи сырья перемешивание продолжали в течение приблизительно 20 мин до тех пор, пока поглощение монооксида углерода больше не наблюдалось.
[0052]
Затем, в то время как температуру реакции поддерживали при 0°С, 46 г этанола (1,0 моль, 1,6-кратное молярное отношение относительно исходного материала 2-этилиденнорборнана) подавали из верхней части автоклава в течение 15 мин, и этерификацию проводили в течение 1 ч при перемешивании. Реакционный раствор экстрагировали из нижней части автоклава в ледяную воду, и масляную фазу и водную фазу разделяли, после чего масляную фазу дважды промывали 100 мл 2% масс. водного раствора гидроксида натрия и дважды 100 мл дистиллированной воды, и затем обезвоживали 10 г безводного сульфата натрия.
[0053]
Низкокипящие соединения удаляли из полученной жидкости с помощью испарителя, после чего жидкость подвергали ректификации (температура перегонки: 150°C, степень вакуума: 60 торр (8,0 кПа)) с помощью ректификатора, имеющего число теоретических тарелок 20, и затем анализировали с помощью газовой хроматографии с использованием внутреннего стандарта. В результате, выход карбоксилатного соединения (смесь экзо- и эндоизомеров) составил 94,1 мол.% (стандарт 2-этилиденнорборнан). Выход основного продукта этил-2-этилнорборнан-2-экзокарбоксилата составил 84,9 мол.% (стандарт 2-этилиденнорборнан, соотношение изомеров 90,3%).
Основной продукт анализировали с помощью ГХ-МС (CI+), и результаты показали молекулярную массу 197,15 ([M+H]+) относительно молекулярной массы 196,29 целевого продукта. Кроме того, значение химического сдвига по данным 1H-ЯМР и значение химического сдвига по данным 13C-ЯМР (δ м.д., стандарт TMS) в дейтерированном хлороформном растворителе были получены далее, и по этим результатам основной продукт идентифицировали как этил-2-этилнорборнан-2-карбоксилат. Следует отметить, что при идентификации с помощью ЯМР, [2] означает атом углерода или атом водорода, связанный с указанным атомом углерода, обозначенным ссылочной позицией 2 в следующей химической формуле. То же самое применимо и ниже.
[0054]
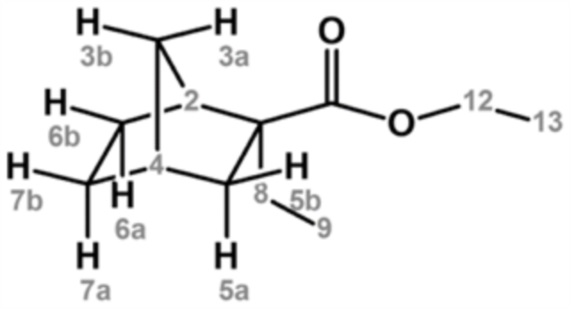
[0055]
1H ЯМР (500 МГц, CDCl3) δ (м.д.): 0,76 (т, J=7,5 Гц, 3H, [9]), 0,90 (дд, J=12,5, 3,0 Гц, 1H, [5a <эндо>]), 1,06-1,11 (м, 1H, [7a <эндо>]), 1,19-1,21 (м, 1H, [3b]), 1,23 (т, J=7,0 Гц, 3H, [13]), 1,28-1,32 (м, 1H, [3a]), 1,33-1,41 (м, 1H, [6a <эндо>]), 1,45-1,50 (м, 1H, [7b <экзо>]), 1,51-1,58 (м, 1H, [6b <экзо>]), 1,58-1,64 (м, 2H, [8]), 2,17-2,19 (м, 1H, [4]), 2,20-2,24 (м, 1H, [5b <экзо>]), 2,54 (ушир. д, J=4,0, 1H, [2]), 4,09-4,13 (м, 2H, [12])
[0056]
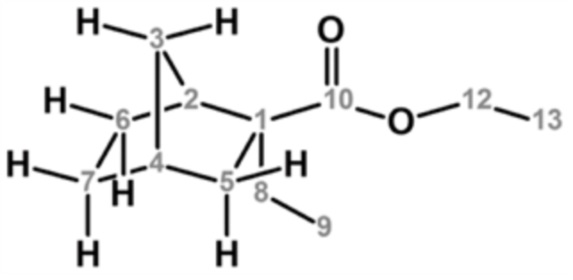
[0057]
13C ЯМР (126 МГц, CDCl3) δ (м.д.): 10,55 [9], 14,37 [13], 23,15 [6], 29,05 [7], 29,60 [8], 36,81 [4], 38,81 [3], 41,29 [5], 42,78 [2], 54,35 [1], 60,27 [12], 178,06 [10]
Этил-2-этилнорборнан-2-карбоксилат обладал фруктово-травяно-древесным ароматом.
[0058]
Пример 2
(Получение н-пропил-2-этилнорборнан-2-карбоксилата путем карбонилирования и этерификации 2-этилиденнорборнана)
Карбонилирование, этерификацию и обработку продукта реакции проводили таким же способом, как и в примере 1, за исключением того, что спирт, использованный при этерификации в примере 1, заменяли н-пропанолом.
Полученный продукт анализировали с помощью газовой хроматографии, и результаты показали, что выход карбоксилатного соединения составлял 92,9 мол.% (стандарт 2-этилиденнорборнан), и выход основного продукта н-пропил-2-этилнорборнан-экзо-2-карбоксилата составлял 83,0 мол.% (стандарт 2-этилиденнорборнан, соотношение изомеров 89,4%).
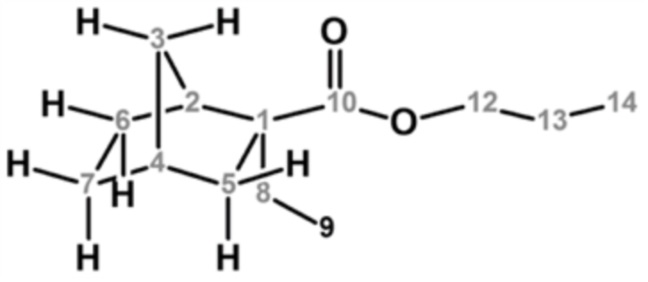
Основной продукт анализировали с помощью ГХ-МС (CI+), и результаты показали молекулярную массу 211,13 ([M+H]+) относительно молекулярной массы 210,32 целевого продукта. Кроме того, значение химического сдвига по данным 1H-ЯМР и значение химического сдвига по данным 13C-ЯМР (δ м.д., стандарт TMS) в дейтерированном хлороформном растворителе были получены далее, и по этим результатам основной продукт идентифицировали как н-пропил-2-этилнорборнан-2-карбоксилат.
[0059]
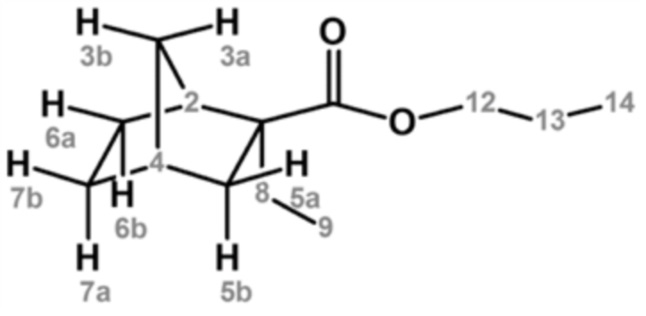
[0060]
1H ЯМР (500 МГц, CDCl3) δ (м.д.): 0,76 (т, J=7,5 Гц, 3H, [9]), 0,89-0,92 (м, 1H, [5b <эндо>]), 0,93 (т, J=7,0 Гц, 3H, [14]), 1,05-1,11 (м, 1H, [7a <эндо>]), 1,18-1,22 (м, 1H, [3b]), 1,27-1,32 (м, 1H, [3a]), 1,33-1,40 (м, 1H, [6b <эндо>]), 1,45-1,51 (м, 1H, [7b <экзо>]), 1,52-1,59 (м, 1H, [6a <экзо>]), 1,60-1,67 (м, 4H, [13], [8]), 2,17-2,19 (м, 1H, [4]), 2,20-2,24 (м, 1H, [5a <экзо>]), 2,54 (ушир. д, J=3,5 Гц, 1H, [2]), 4,98-4,05 (м, 2H, [12])
[0061]
[0062]
13C ЯМР (126 МГц, CDCl3) δ (м.д.): 10,59 [9, 14], 22,16 [13], 23,16 [6], 29,06 [7], 29,64 [8], 36,82 [4], 38,82 [3], 41,30 [5], 42,80 [2], 54,52 [1], 65,98 [12], 178,14 [10]
Кроме того, н-пропил-2-этилнорборнан-2-карбоксилат обладал фруктово-травяно-древесным ароматом.
[0063]
Пример 3
(Получение изопропил-2-этилнорборнан-2-карбоксилата путем карбонилирования и этерификации 2-этилиденнорборнана)
Карбонилирование, этерификацию и обработку продукта реакции проводили таким же способом, как и в примере 1, за исключением того, что спирт, использованный при этерификации в примере 1, заменяли изопропанолом.
Полученный продукт анализировали с помощью газовой хроматографии, и результаты показали, что выход карбоксилатного соединения составлял 92,4 мол.% (стандарт 2-этилиденнорборнан), и выход основного продукта изопропил-2-этилнорборнан-2-экзокарбоксилата составлял 81,2 мол.% (стандарт 2-этилиденнорборнан, соотношение изомеров 87,9%).
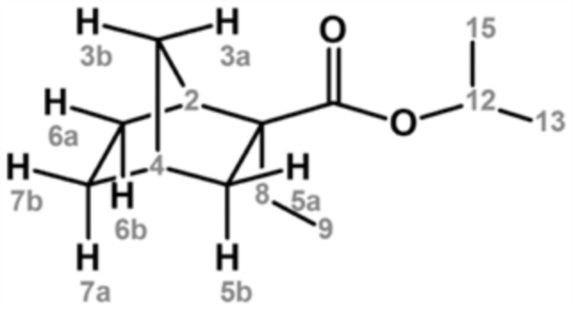
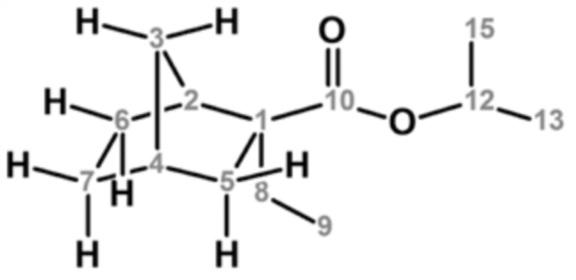
Основной продукт анализировали с помощью ГХ-МС (CI+), и результаты показали молекулярную массу 211,12 ([M+H]+) относительно молекулярной массы 210,32 целевого продукта. Кроме того, значение химического сдвига по данным 1H-ЯМР и значение химического сдвига по данным 13C-ЯМР (δ м.д., стандарт TMS) в дейтерированном хлороформном растворителе были получены далее, и по этим результатам основной продукт идентифицировали как изопропил-2-этилнорборнан-2-карбоксилат.
[0064]
[0065]
1H ЯМР (500 МГц, CDCl3) δ (м.д.): 0,76 (т, J=7,0 Гц, 3H, [9]), 0,87-0,90 (м, 1H, [5b <эндо>]), 1,05-1,11 (м, 1H, [7a <эндо>]), 1,19-1,21 (м, 7H, [3b], [13], [15]), 1,29-1,30 (м, 1H, [3a]), 1,33-1,39 (м, 1H, [6b <эндо>]), 1,45-1,51 (м, 1H, [7b <экзо>]), 1,51-1,56 (м, 1H, [6a <экзо>]), 1,56-1,64 (м, 2H, [8]), 2,16-2,19 (м, 1H, [4]), 2,19-2,22 (м, 1H, [5a <экзо>]), 2,54 (ушир. д, J=4,0 Гц, 1H, [2]), 4,96-5,01 (м, 1H, [12])
[0066]
[0067]
13C ЯМР (126 МГц, CDCl3) δ (м.д.): 10,47 [9], 21,85-21,88 [13], [15], 23,16 [6], 29,08 [7], 29,53 [8], 36,80 [4], 38,74 [3], 41,25 [5], 42,79 [2], 54,25 [1], 67,22 [12], 177,49 [10]
Кроме того, изопропил-2-этилнорборнан-2-карбоксилат имел травяно-фруктовый-яблочно-древесный аромат.
[0068]
Пример 4
<Ароматизирующая композиция>
В соответствии с составом, приведенным в таблице 1 ниже, цветочно-фруктовую ароматизирующую композицию получали с использованием карбоксилатного соединения, полученного в примере 1.
[0069]
Таблица 1
(доступный от International Flavors & Fragrances, Inc.)
(доступный от International Flavors & Fragrances, Inc.)
50BB:50% в бензилбензоате
(доступный от International Flavors & Fragrances, Inc.)
(доступный от International Flavors & Fragrances, Inc.)
[0070]
Органолептическая оценка проводилась четырьмя экспертами с опытом работы пять или более лет, и результаты показали, что все эксперты обнаружили, что цветочно-фруктовая ароматизирующая композиция, содержащая соединение из примера 1, имела сильный фруктовый аромат, отличные вкусовые качества и превосходную диффузионную способность.
Промышленная применимость
[0071]
Новое карбоксилатное соединение настоящего изобретения обладает фруктовым ароматом, и его аромат является превосходным, и, таким образом, карбоксилатное соединение настоящего изобретения эффективно в качестве ароматизирующего компонента в широком диапазоне применений, таких как туалетные принадлежности, мыла и моющие средства для одежды. Кроме того, в соответствии со способом получения карбоксилатного соединения по настоящему изобретению карбоксилатное соединение может быть получено промышленно рентабельным способом.
Настоящее изобретение относится к карбоксилатному соединению формулы (1), где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода, которое можно использовать в качестве исходного материала для ароматизирующих композиций и которое имеет фруктовый аромат, к содержащей его ароматизирующей композиции и к способу его получения. Способ получения соединения формулы 1 заключается во взаимодействии соединения, представленного формулой (2), с монооксидом углерода в присутствии фтороводорода, с последующим взаимодействием со спиртом, имеющим от 2 до 6 атомов углерода. 3 н. и 1 з.п. ф-лы, 1 табл., 4 пр.
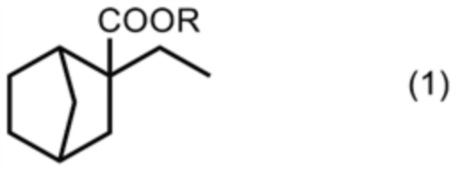
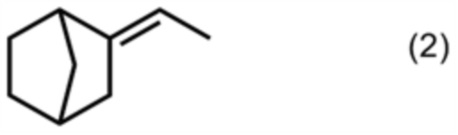
1. Карбоксилатное соединение, представленное формулой (1)
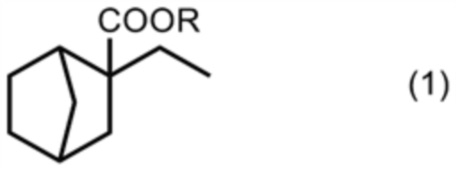 ,
,
где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
2. Карбоксилатное соединение по п.1, в котором R представляет собой этильную группу, н-пропильную группу или изопропильную группу.
3. Ароматизирующая композиция, содержащая карбоксилатное соединение, представленное формулой (1)
 ,
,
где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода.
4. Способ получения карбоксилатного соединения, представленного формулой (1), путем взаимодействия соединения, представленного формулой (2), с монооксидом углерода в присутствии фтороводорода, и затем взаимодействия со спиртом, имеющим от 2 до 6 атомов углерода
 ,
,
где R представляет собой алкильную группу, имеющую от 2 до 6 атомов углерода
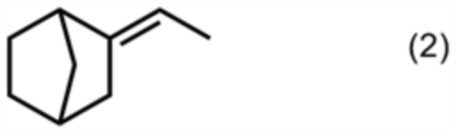 .
.
| WO 2012063433 A1, 18.05.2012 | |||
| WO 2018051776 A1, 22.03.2018 | |||
| JP 60190738 A, 28.09.1985 | |||
| US 4319036 A1, 09.03.1982 | |||
| НОВОЕ СОЕДИНЕНИЕ СЛОЖНОГО ЭФИРА КАРБОНОВОЙ КИСЛОТЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И КОМПОЗИЦИЯ ДУШИСТЫХ ВЕЩЕСТВ | 2012 |
|
RU2585761C2 |
Авторы
Даты
2023-05-15—Публикация
2019-11-07—Подача