ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Данная заявка испрашивает приоритет предварительной заявки США № 62/747 209, поданной 18 октября 2018 г., предварительной заявки США № 62/803 516, поданной 10 февраля 2019 г., и предварительной заявки США № 62/857 516, поданной 5 июня 2019 г., раскрытие которых в полном объеме включено в данный документ во всех отношениях.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[2] Настоящее изобретение в целом относится к трициклическим соединениям и их применению для лечения разнообразных показаний. В частности, данное раскрытие относится к трициклическим соединениям и их применению для лечения разнообразных видов рака, например рака предстательной железы, включая, помимо прочего, первичный/локализованный рак предстательной железы (впервые диагностированный), местно-распространенный рак предстательной железы, рецидивирующий рак предстательной железы, неметастатический устойчивый к кастрации рак предстательной железы, метастатический рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы (CRPC) и гормоночувствительный рак предстательной железы. Это изобретение также относится к трициклическим соединениям и их применению для модуляции активности андрогенового рецептора (AR), включая усеченный AR.
УРОВЕНЬ ТЕХНИКИ
[3] Андрогены опосредуют свои эффекты через андрогеновый рецептор (AR). Андрогены играют роль в широком диапазоне ответных реакций развития и физиологических реакций и участвуют в дифференцировке мужского пола, поддержании сперматогенеза и регуляции мужских гонадотропинов (R. K. Ross, G. A. Coetzee, C. L. Pearce, J. K. Reichardt, P. Bretsky, L. N. Kolonel, B. E. Henderson, E. Lander, D. Altshuler & G. Daley, Eur Urol 35, 355-361 (1999); A. A. Thomson, Reproduction 121, 187-195 (2001); N. Tanji, K. Aoki & M. Yokoyama, Arch Androl 47, 1-7 (2001)). Несколько линий доказательств показывают, что андрогены связаны с развитием канцерогенеза предстательной железы. Во-первых, андрогены вызывают канцерогенез предстательной железы на моделях грызунов (R. L. Noble, Cancer Res 37, 1929-1933 (1977); R. L. Noble, Oncology 34, 138-141 (1977)), и мужчины, получающие андрогены в форме анаболических стероидов, имеют более высокую заболеваемость раком предстательной железы (J. T. Roberts & D. M. Essenhigh, Lancet 2, 742 (1986); J. A. Jackson, J. Waxman & A. M. Spiekerman, Arch Intern Med 149, 2365-2366 (1989); P. D. Guinan, W. Sadoughi, H. Alsheik, R. J. Ablin, D. Alrenga & I. M. Bush, Am J Surg 131, 599-600 (1976)). Во-вторых, рак предстательной железы не развивается, если людей или собак кастрировать до полового созревания (J. D. Wilson & C. Roehrborn, J Clin Endocrinol Metab 84, 4324-4331 (1999); G. Wilding, Cancer Surv 14, 113-130 (1992)). Кастрация взрослых мужчин вызывает инволюцию предстательной железы и апоптоз эпителия предстательной железы, не оказывая никакого воздействия на другие наружные гениталии мужчин (E. M. Bruckheimer & N. Kyprianou, Cell Tissue Res 301, 153-162 (2000); J. T. Isaacs, Prostate 5, 545-557 (1984)). Эта зависимость от андрогенов является основным основанием для лечения рака предстательной железы с помощью химической или хирургической кастрации (андрогенной абляции), также известной как терапия андрогенной абляции (ABT) или терапия андрогенной депривации (ADT).
[4] Андрогены также играют роль в женских заболеваниях, таких как синдром поликистозных яичников, а также в раковых заболеваниях. Одним из примеров является рак яичников, при котором повышенный уровень андрогенов связан с повышенным риском развития рака яичников (K. J. Helzlsouer, A. J. Alberg, G. B. Gordon, C. Longcope, T. L. Bush, S. C. Hoffman & G. W. Comstock, JAMA 274, 1926-1930 (1995); R. J. Edmondson, J. M. Monaghan & B. R. Davies, Br J Cancer 86, 879-885 (2002)). AR был обнаружен в большинстве случаев рака яичников (H. A. Risch, J Natl Cancer Inst 90, 1774-1786 (1998); B. R. Rao & B. J. Slotman, Endocr Rev 12, 14-26 (1991); G. M. Clinton & W. Hua, Crit Rev Oncol Hematol 25, 1-9 (1997)), тогда как рецептор эстрогена-альфа (ERa) и рецептор прогестерона обнаруживаются менее чем в 50% опухолей яичников.
[5] Единственное эффективное лечение, доступное для прогрессирующего рака предстательной железы, - это отмена андрогенов, которые необходимы для выживания клеток просвета предстательной железы. Терапия андрогенной аблацией вызывает временное уменьшение опухолевой нагрузки, сопровождающееся снижением уровня простатспецифического антигена (ПСА) в сыворотке крови. К сожалению, рак предстательной железы может в конечном итоге снова вырасти в отсутствие тестикулярных андрогенов (устойчивое к кастрации заболевание) (Huber et al 1987 Scand J. Urol Nephrol. 104, 33-39). Устойчивый к кастрации рак предстательной железы, который все еще вызывается AR, биохимически характеризуется до появления симптомов по возрастанию титра сывороточного ПСА (Miller et al 1992 J. Urol. 147, 956-961). Когда болезнь становится устойчивой к кастрации, большинство пациентов умирают от нее в течение двух лет.
[6] AR имеет отдельные функциональные домены, которые включают карбокси-концевой лиганд-связывающий домен (LBD), ДНК-связывающий домен (DBD), содержащий два мотива цинковых пальцев, и N-концевой домен (NTD), который содержит две единицы активации транскрипции (tau1 и tau5) в функции активации-1 (AF-1). Связывание андрогена (лиганда) с LBD AR приводит к его активации, так что рецептор может эффективно связываться со своим специфическим консенсусным сайтом ДНК, называемым элементом отклика андрогена (ARE), на промоторных и энхансерных областях «нормальных» регулируемых андрогенами генов, таких как ПСА, для инициации транскрипции. AR может быть активирован в отсутствие андрогена путем стимуляции пути цАМФ-зависимой протеинкиназы (PKA) интерлейкином-6 (IL-6) и различными факторами роста (Culig et al 1994 Cancer Res. 54, 5474-5478; Nazareth et al 1996 J. Biol. Chem. 271, 19900-19907; Sadar 1999 J. Biol. Chem. 274, 7777-7783; Ueda et al 2002 A J. Biol. Chem. 277, 7076-7085; и Ueda et al 2002 B J. Biol. Chem. 277, 38087-38094). Было показано, что механизм лиганд-независимой трансформации AR включает: 1) увеличение количества ядерного белка AR, что указывает на ядерную транслокацию; 2) усиление комплексообразования AR/ARE; и 3) AR-NTD (Sadar 1999 J. Biol. Chem. 274, 7777-7783; Ueda et al 2002 A J. Biol. Chem. 277, 7076-7085; и Ueda et al 2002 B J. Biol. Chem. 277, 38087-38094). AR может быть активирован в отсутствие тестикулярных андрогенов с помощью альтернативных путей передачи сигнала при резистентном к кастрации заболевании, что согласуется с открытием, что ядерный белок AR присутствует во вторичных опухолях рака предстательной железы (Kim et al 2002 Am. J. Pathol. 160, 219-226; и van der Kwast et al 1991 Inter. J. Cancer 48, 189-193).
[7] Клинически доступные ингибиторы AR включают в себя нестероидные антиандрогены, такие как апалутамид, даролутамид, бикалутамид (Casodex™), нилутамид, флутамид и энзалутамид. Существует также класс стероидных антиандрогенов, таких как ацетат ципротерона и спиронолактон. И стероидные, и нестероидные антиандрогены нацелены на LBD AR и преимущественно не работают, предположительно из-за плохой аффинности и мутаций, которые приводят к активации AR этими же антиандрогенами (Taplin, M.E., Bubley, G.J., Kom Y.J., Small E.J., Uptonm M., Rajeshkumarm B., Balkm S.P., Cancer Res., 59, 2511-2515 (1999)), и конститутивно активных вариантов сплайсинга AR. Антиандрогены не влияют на конститутивно активные варианты сплайсинга AR, которые лишены лиганд-связывающего домена (LBD) и связаны с рецидивом рака предстательной железы после медицинской кастрации (Dehm SM, Schmidt LJ, Heemers HV, Vessella RL, Tindall DJ., Cancer Res 68, 5469-77, 2008; Guo Z, Yang X, Sun F, Jiang R, Linn DE, Chen H, Chen H, Kong X, Melamed J, Tepper CG, Kung HJ, Brodie AM, Edwards J, Qiu Y., Cancer Res. 69, 2305-13, 2009; Hu et al 2009 Cancer Res. 69, 16-22; Sun et al 2010 J Clin Invest. 2010 120, 2715-30) и устойчивым к абиратерону и энзалутамиду (Antonarakis et al., N Engl J Med. 2014, 371, 1028-38; Scher et al JAMA Oncol. 2016 doi: 10,1001). Традиционная терапия сосредоточена на андроген-зависимой активации AR через его C-концевой домен.
[8] Ранее сообщалось о других соответствующих антагонистах AR (см. WO 2010/000066, WO 2011/082487; WO 2011/082488; WO 2012/145330; WO 2015/031984; WO 2016/058080; и WO 2016/058082), которые связываются с полноразмерными AR и/или вариантами сплайсинга усеченной AR, которые были недавно разработаны или разрабатываются в настоящее время, включают: деструкторы AR, такие как никлозамид (Liu C et al 2014), галетерон (Njar et al 2015; Yu Z at al 2014) и ARV-330/андрогеновый рецептор PROTAC (Neklesa et al 2016 J Clin Oncol 34 suppl 2S; abstr 267); AR ингибитор DBD VPC-14449 (Dalal K et al 2014 J Biol Chem. 289(38):26417-29; Li H et al 2014 J Med Chem. 57(15):6458-67); антиандрогены апалутамид (Clegg NJ et al 2012), ODM-201 (Moilanen AM et al 2015), ODM-204 (Kallio et al J Clin Oncol 2016 vol. 34 no. 2_suppl 230), TAS3681 (Minamiguchi et al 2015 J Clin Oncol 33, suppl 7; abstr 266); и AR NTD ингибиторы 3E10-AR441bsAb (Goicochea NL et al 2015) и синтокамид (Sadar et al 2008; Banuelos et al 2016).
[9] AR-NTD также является мишенью для разработки лекарств (например, WO 2000/001813; Myung et al. J. Clin. Invest 2013, 123, 2948), поскольку NTD содержит функцию активации-1 (AF-1), которая представляет собой необходимую область для транскрипционной активности AR (Jenster et al 1991.Mol Endocrinol. 5, 1396-404). AR-NTD играет важную роль в активации AR в отсутствие андрогенов (Sadar, M.D. 1999 J. Biol. Chem. 274, 7777-7783; Sadar MD et al 1999 Endocr Relat Cancer. 6, 487-502; Ueda et al 2002 J. Biol. Chem. 277, 7076-7085; Ueda 2002 J. Biol. Chem. 277, 38087-38094; Blaszczyk et al 2004 Clin Cancer Res. 10, 1860-9; Dehm et al 2006 J Biol Chem. 28, 27882-93; Gregory et al 2004 J Biol Chem. 279, 7119-30). AR-NTD играет важную роль в гормональном прогрессировании рака предстательной железы, что было продемонстрировано применением молекул-приманок (Quayle et al 2007, Proc Natl Acad Sci U S A. 104,1331-1336).
[10] В то время как кристаллическая структура была разрешена для AR C-конца LBD, этого не было в случае NTD из-за его высокой гибкости и внутреннего беспорядка в растворе (Reid et al 2002 J. Biol. Chem. 277, 20079-20086), тем самым затрудняя виртуальную стыковку подходов к открытию лекарственных средств. Соединения, которые модулируют AR, потенциально посредством взаимодействия с доменом NTD, включают в себя соединения бисфенола, описанные в опубликованных PCT №: WO 2010/000066, WO 2011/082487; WO 2011/082488; WO 2012/145330; WO 2012/139039; WO 2012/145328; WO 2013/028572; WO 2013/028791; WO 2014/179867; WO 2015/031984; WO 2016/058080; WO 2016/058082; WO 2016/112455; WO 2016/141458; WO 2017/177307; WO 2017/210771; и WO 2018/045450, и которые включены в полном объеме в настоящий документ посредством ссылки.
[11] Транскрипционно активный андрогеновый рецептор играет важную роль в CRPC, несмотря на снижение уровня андрогенов в крови (Karantanos, T. et al Oncogene 2013, 32, 5501-5511; Harris, W. P. et al Nature Clinical Practice Urology, 2009, 6, 76-85). Механизмы резистентности AR к ADT включают в себя: сверхэкспрессию AR (Visakorpi, T. et al Nature Genetics 1995, 9, 401-406; Koivisto, P. et al Scandinavian Journal of Clinical and Laboratory Investigation Supplementum 1996, 226, 57-63); мутации с усилением функции в AR LBD (Culig Z. et al Molecular Endocrinology 1993, 7, 1541-1550); внутриопухолевый синтез андрогенов (Cai, C. et al Cancer Research 2011, 71, 6503-6513); измененная экспрессия и функция коактиваторов AR (Ueda, T. et al The Journal of Biological Chemistry 2002, 277, 38087-38094; Xu J. et al Nature Reviews Cancer 2009, 9, 615-630); аберрантные посттрансляционные модификации AR (Gioeli D. et al Molecular and Cellular Endocrinology 2012, 352, 70-78; van der Steen T. et al International Journal of Molecular Sciences 2013, 14, 14833-14859); и экспрессия вариантов сплайсинга AR (AR-V), в которых отсутствует лиганд-связывающий домен (LBD) (Karantanos, T. et al Oncogene 2013, 32, 5501-5511; Andersen R. J. et al Cancer Cell 2010, 17, 535-546; Myung J. K. et al The Journal of Clinical Investigation 2013, 123, 2948-2960; Sun S. et al The Journal of Clinical Investigation 2010, 120, 2715-2730). Антиандрогены, такие как бикалутамид и энзалутамид, нацелены на AR LBD, но не влияют на усеченные конститутивно активные AR-V, такие как AR-V7 (Li Y. et al Cancer Research 2013, 73, 483-489). Экспрессия AR-V7 связана с устойчивостью к современным гормональным препаратам (Li Y. et al Cancer Research 2013, 73, 483-489; Antonarakis E. S. et al The New England Journal of Medicine 2014, 371, 1028-1038).
[12] Несмотря на то, что в этой области достигнуты значительные успехи, остается потребность в улучшенном лечении AR-опосредованных расстройств, включая рак предстательной железы, особенно метастатический устойчивый к кастрации рак предстательной железы. Разработка соединений посредством уникального взаимодействия с AR NTD предоставит пациентам альтернативные варианты и новую надежду.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[13] Соединения по настоящему изобретению представляют собой модуляторы андрогенового рецептора, которые могут быть пригодны при лечении разнообразных заболеваний и состояний, как описано в данном документе. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IIIA):
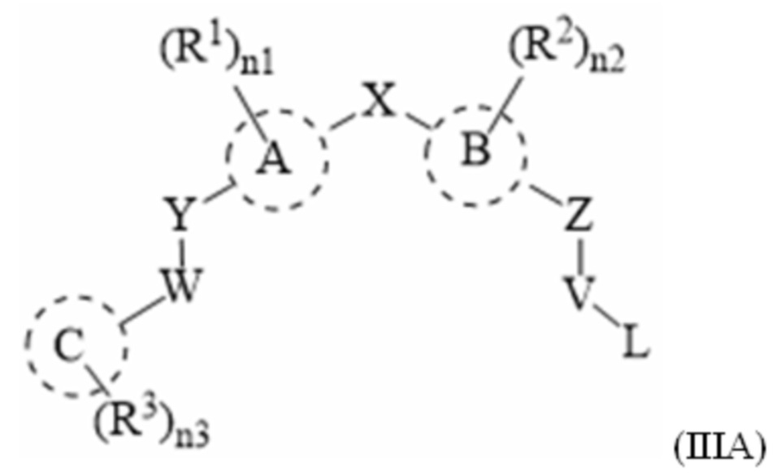
[14] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[15] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[16] C представляет собой 3-10-членное кольцо;
[17] X представляет собой связь, -(CR5R6)t- или -NR7;
[18] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2-, -NR7- или -N(COCH3)-;
[19] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[20] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[21] V представляет собой -CH2-, и L представляет собой галоген, -NH2, -CHCl2, -CCl3 или -CF3; или
[22] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[23] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[24] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[25] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[26] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[27] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[28] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[29] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[30] R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил;
[31] каждый m независимо равно 0, 1 или 2;
[32] n1 и n2, каждый независимо, равны 0, 1 или 2;
[33] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[34] R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил;
[35] каждый m независимо равно 0, 1 или 2;
[36] n1 и n2, каждый независимо, равны 0, 1 или 2;
[37] n3 равно 1, 2, 3, 4 или 5; и
[38] t равно 0, 1 или 2.
[39] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IVA):

[40] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[41] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[42] C представляет собой 3-10-членное кольцо;
[43] X представляет собой связь, -(CR5R6)t- или -NR7-;
[44] Y и Z, каждый независимо, представляют собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[45] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[46] V представляет собой -CH2-, и L представляет собой галоген, -NH2 или -CF3; или
[47] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[48] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[49] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[50] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[51] R7 представляет собой H или C1-C6 алкил;
[52] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[53] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[54] n1 и n2, каждый независимо, равны 0, 1 или 2;
[55] n3 равно 1, 2, 3, 4 или 5; и
[56] t равно 0, 1 или 2.
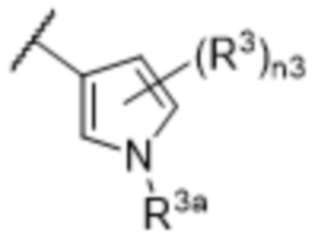
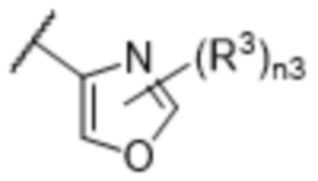
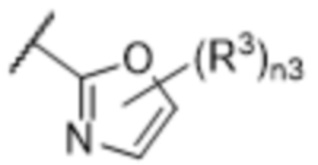
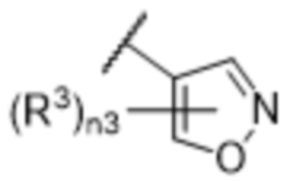
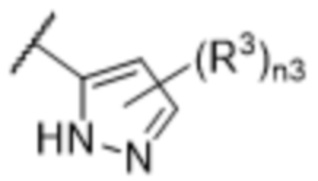
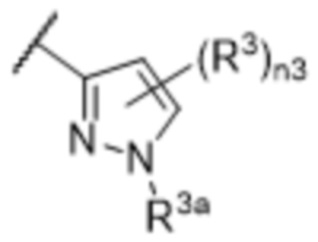
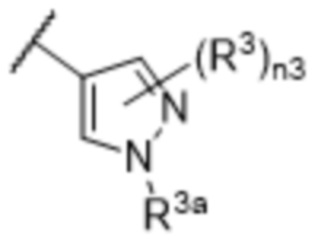
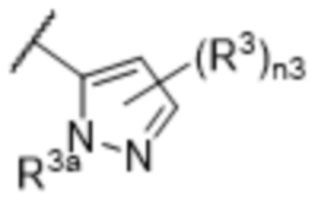
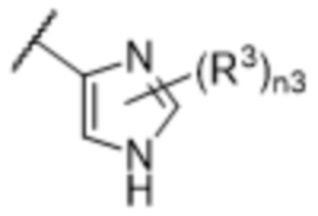
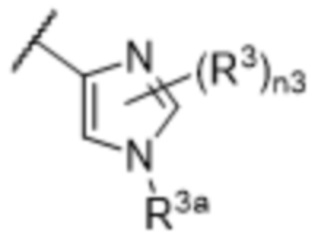
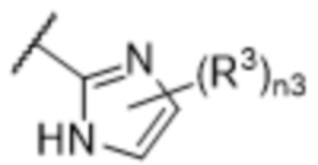
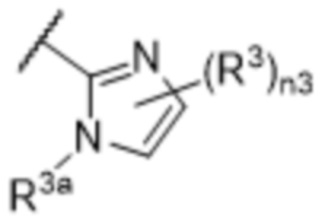
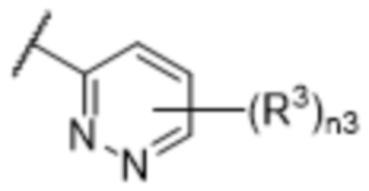
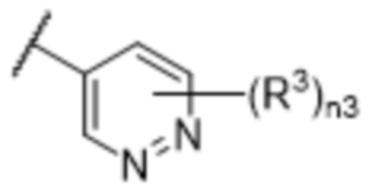
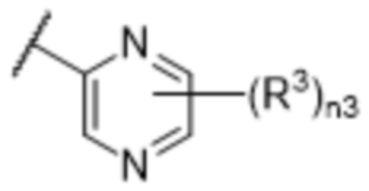
[57] В одном варианте осуществления соединения формулы (IVA) C представляет собой 5-10-членный гетероарил или арил. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5-7-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца. В некоторых вариантах осуществления настоящего изобретения C, замещенный (R3)n3, представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил, пиразин, фуран или пиримидил. В некоторых вариантах осуществления настоящего изобретения C, замещенный (R3)n3, выбран из 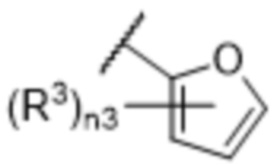 ,
, 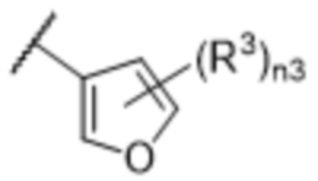 ,
, 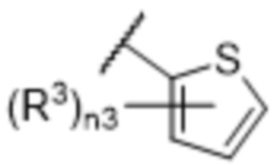 ,
, 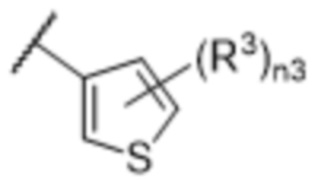 ,
, 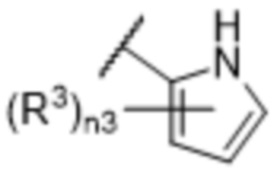 ,
, 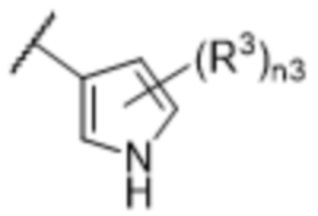 ,
, 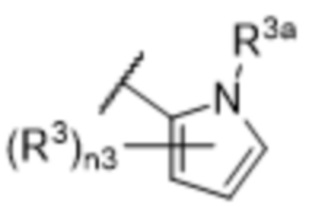 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 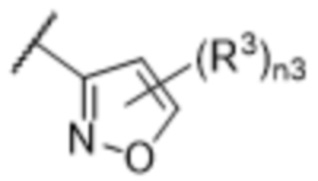 ,
, 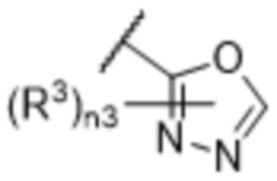 ,
, 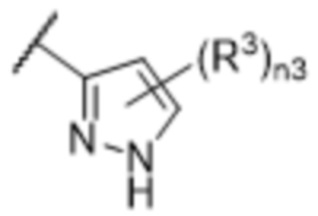 ,
, 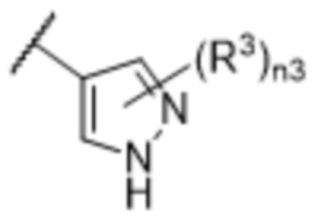 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 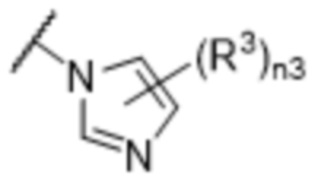 ,
, 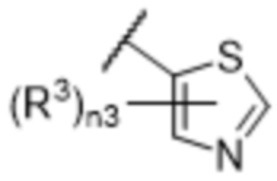 ,
, 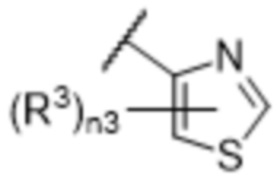 ,
, 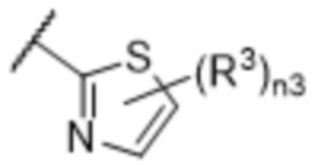 ,
,  ,
,  ,
, 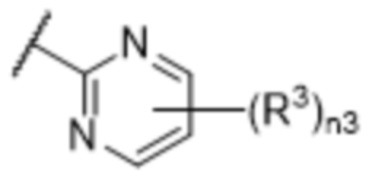 ,
, 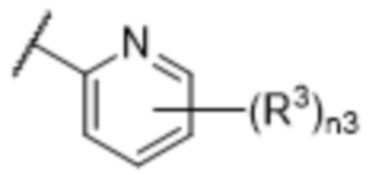 ,
, 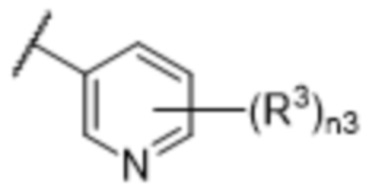 ,
, 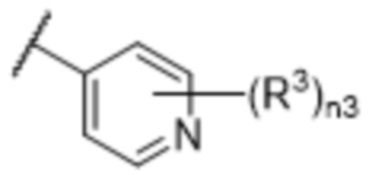 ,
,  ,
,  ,
,  или
или 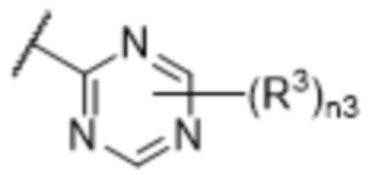 , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[58] В одном варианте осуществления соединения формулы (IVA) R1 и R2, каждый независимо, представляют собой Cl, -CN, -CF3, -OH, метил, метокси или -CONH2.
[59] В одном варианте осуществления соединения формулы (IVA),
[60] A и B представляют собой фенил;
[61] X представляет собой -(CR5R6)t-;
[62] каждый Y и Z представляют собой -O-;
[63] V представляет собой -CH2- или -CH2CH2-;
[64] L представляет собой галоген;
[65] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH или необязательно замещенный C1-C6 алкил;
[66] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил; и
[67] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил.
[68] В одном варианте осуществления соединения формулы (IVA),
[69] A и B представляют собой фенил;
[70] X представляет собой -(CR5R6)t-;
[71] W представляет собой -CH2- или -C(CH3)H-;
[72] каждый Y и Z представляют собой -O-;
[73] V представляет собой -CH2CH2-;
[74] L представляет собой галоген;
[75] R1 и R2, каждый независимо, представляют собой водород, галоген или -CN;
[76] R5 и R6, каждый независимо, представляют собой водород, или C1-C3 алкил; и
[77] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил.
[78] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (A-I):
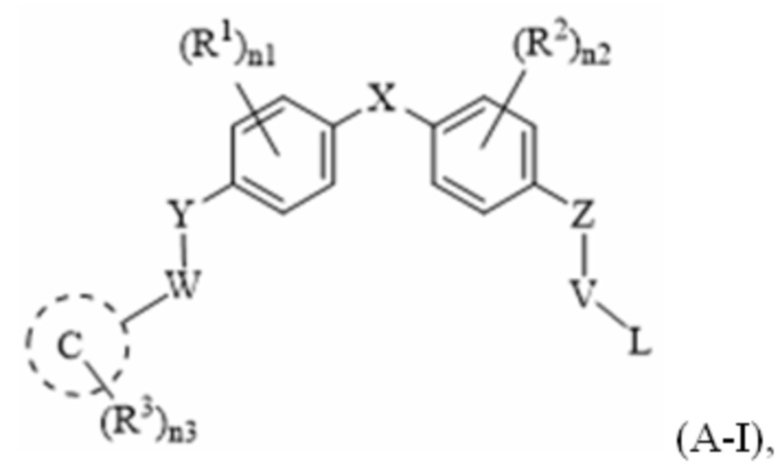
[79] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[80] C представляет собой фенил или 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[81] X представляет собой связь, -(CR5R6)t- или -NR7-;
[82] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[83] Z представляет собой связь, -CH2-, -O- или -NH-;
[84] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[85] V представляет собой -CH2-, и L представляет собой галоген, -NH2 или -CF3; или
[86] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[87] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[88] R3 выбран из -CN, C1-C3 алкокси, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[89] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[90] R7 представляет собой H или C1-C6 алкил;
[91] n1 и n2, каждый независимо, равны 0, 1 или 2;
[92] n3 равно 1, 2, 3, 4 или 5; и
[93] t равно 0, 1 или 2.
[94] В одном варианте осуществления соединения формулы (IVA),
[95] В одном варианте осуществления соединения формулы (A-I) по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[96] В одном варианте осуществления соединения формулы (A-I),
[97] X представляет собой связь или -(CR5R6)t;
[98] W представляет собой связь, -CH2- или -C(CH3)H-;
[99] Y представляет собой -O-;
[100] Z представляет собой -O-;
[101] V представляет собой -CH2- или -CH2CH2-; и
[102] L представляет собой галоген
[103] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (G-II):
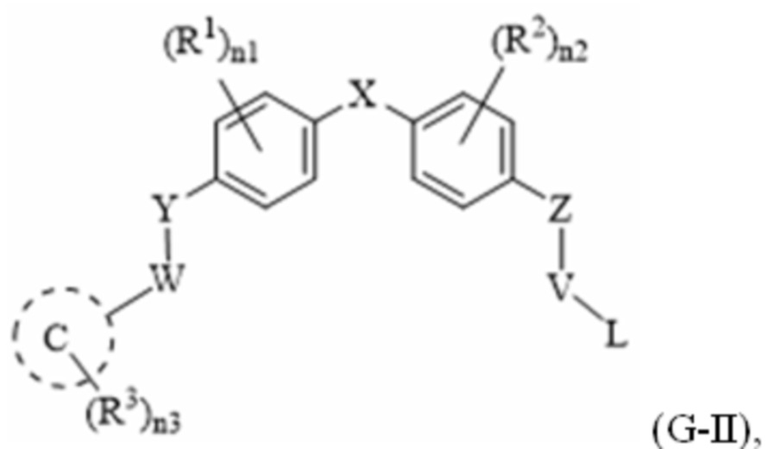
[104] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[105] C представляет собой  .
.  ,
,  ,
, 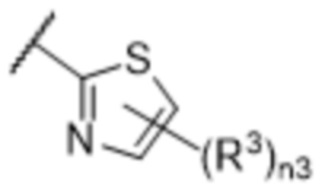 ,
, 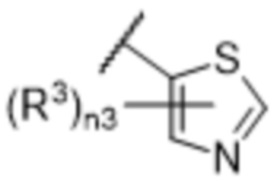 ,
, 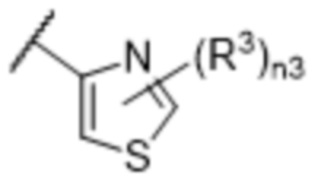 ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 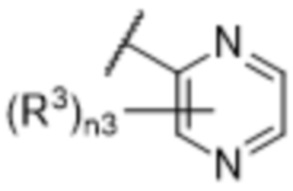 ,
,  ,
,  ,
,
или 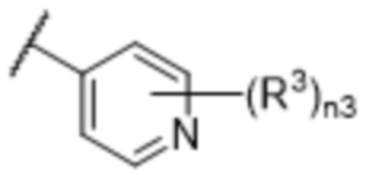 ;
;
[106] X представляет собой -(CR5R6)t-;
[107] Y представляет собой -O-;
[108] Z представляет собой -O-;
[109] W представляет собой -CH2- или -C(CH3)H-;
[110] V представляет собой -CH2CH2-;
[111] L представляет собой галоген;
[112] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[113] по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[114] R5 и R6, каждый независимо, представляют собой водород или метил;
[115] n1 и n2, каждый независимо, равны 0, 1 или 2;
[116] n3 равно 1 или 2; и
[117] t равно 1.
[118] В одном варианте осуществления соединения формулы (G-II) по меньшей мере один R3 выбран из -NHSO2CH3, -NHSO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, C1-C3 алкила, C1-C3 алкокси, -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[119] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения A1-A96, A98-A116, A118-A159, A161-A175 и A177-A234 или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и/или A204 или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[120] В одном варианте осуществления настоящего изобретения в настоящем описании предложена фармацевтическая композиция, содержащая любое из соединений формулы (IIIA) или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство, и фармацевтически приемлемый носитель. В одном варианте осуществления настоящего изобретения в настоящем описании предложена фармацевтическая композиция, содержащая любое из соединений формулы (IVA) или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство, и фармацевтически приемлемый носитель. В одном варианте осуществления настоящего изобретения в настоящем описании предложена фармацевтическая композиция, содержащая любое из соединений формулы (A-I) или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство, и фармацевтически приемлемый носитель. В одном варианте осуществления настоящего изобретения в настоящем описании предложена фармацевтическая композиция, содержащая любое из соединений формулы (G-II) или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство, и фармацевтически приемлемый носитель.
[121] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая любое из соединений A1-A96, A98-A116, A118-A159, A161-A175 и A177-A234 или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство и фармацевтически приемлемый носитель. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая любое из соединений A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и A204 или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство и фармацевтически приемлемый носитель.
[122] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложен способ лечения рака, включающий введение любого из соединений формулы (IIIA), (IVA), (A-I) или (G-II), и соединений A1-A96, A98-A116, A118-A159, A161-A175 или A177-A234 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства субъекту, нуждающемуся в этом. В одном варианте осуществления настоящего изобретения рак представляет собой рак предстательной железы. В одном варианте осуществления настоящего изобретения рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы. В другом варианте осуществления настоящего изобретения рак предстательной железы экспрессирует полноразмерный андрогеновый рецептор или усеченный вариант сплайсинга андрогенового рецептора.
[123] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложен способ лечения рака, включающий введение любого из соединений A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и A204 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[124] На Фиг. 1 проиллюстрирована дозозависимая кривая ПСА-люциферазной активности в ответ на иллюстративные примеры соединения в временно трансфицированных клетках LNCaP, обработанных синтетическим андрогеном (R1881).
[125] На Фиг. 2A проиллюстрирован процент ПСА-люциферазной активности иллюстративных примеров соединений в клетках LNCaP, временно трансфицированных ПСА (6,1kb)-люциферазным репортером и обработанных без или с R1881. На Фиг. 2B проиллюстрирован процент ПСА-люциферазной активности иллюстративных примеров соединений в клетках LNCaP, котрансфицированных вектором экспрессии для AR-V7 и ПСА-люциферазным репортером и обработанных без или с R1881.
[126] На Фиг. 3 проиллюстрирована концентрация иллюстративных примеров соединений в плазме мышей-самцов CD-1 после однократной пероральной дозы.
[127] На Фиг. 4 проиллюстрировано изменение объема опухоли у мышей-самцов NCG, несущих опухоли LNCaP, после перорального введения иллюстрированных примеров соединений.
[128] На Фиг. 5 проиллюстрировано изменение % массы тела у мышей-самцов NCG, несущих опухоли LNCaP, после перорального введения иллюстрированных примеров соединений.
[129] На Фиг. 6 проиллюстрировано индивидуальное изменение объема опухоли по сравнению с исходным уровнем, измеренным в конце эксперимента для перорального введения иллюстративных примеров соединений мышам-самцам NCG с опухолями LNCaP.
[130] На Фиг. 7 проиллюстрированы зависящие от концентрации эффекты на пролиферацию клеток LNCaP, PC3 и LNCaP95, обработанных соединением A13.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[131] Все публикации, патенты и заявки на патенты, включая любые графические материалы и приложения к ним, включены в полном объеме посредством ссылки во всех отношениях в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент, рисунок или приложение были специально и индивидуально указаны для включения в полном объеме посредством ссылки во всех отношениях.
Определения
[132] Хотя считается, что следующие термины хорошо понятны специалисту в данной области техники, следующие определения приведены для того, чтобы облегчить объяснение описанного в данном документе объекта изобретения.
[133] В настоящем описании термины «около» и/или «приблизительно» могут использоваться в сочетании с числовыми значениями и/или диапазонами. Под термином «около» понимаются значения, близкие к приведенному значению. Кроме того, фразы «менее чем около [значение]» или «более чем около [значение]» следует понимать с учетом определения термина «около», приведенного в данном документе. Термины «около» и «приблизительно» могут использоваться взаимозаменяемо.
[134] В настоящем описании для определенных количеств указаны числовые диапазоны. Следует понимать, что эти диапазоны включают все внутренние диапазоны. Таким образом, диапазон «от 50 до 80» включает в себя все возможные диапазоны (например, 51-79, 52-78, 53-77, 54-76, 55-75, 60-70 и т. д.). Кроме того, все значения в пределах данного диапазона могут быть конечной точкой для охваченного им диапазона (например, диапазон 50-80 включает диапазоны с конечными точками, такими как 55-80, 50-75 и т. д.).
[135] Термин в единственном числе относится к одному или более объектам; например, «модулятор андрогенового рецептора» относится к одному или более модуляторам андрогенового рецептора или, по меньшей мере, к одному модулятору андрогенового рецептора. По существу, термины в единственном числе, «один или более» и «по меньшей мере один» используются в данном документе взаимозаменяемо. Кроме того, отсылка к «ингибитору», указанному в единственном числе, не исключает возможности присутствия более одного ингибитора, если из контекста четко не следует наличие одного и только одного ингибитора.
[136] В контексте данного документа глагол «содержать», используемый в этом описании и в формуле изобретения, и его спряжения используются в неограничивающем смысле для обозначения того, что элементы, следующие за словом, включены, но элементы, не упомянутые конкретно, не исключаются. Настоящее изобретение может подходящим образом «включать», «состоять из» или «состоять по существу из» этапов, элементов и/или реагентов, описанных в формуле изобретения.
[137] Следует также отметить, что в формулу изобретения могут вноситься правки с целью исключения любых необязательных элементов. Следовательно, данное утверждение должно служить в качестве предварительного основания для использования такой исчерпывающей терминологии, как «исключительно», «только» и т. п. в связи с указанием элементов формулы изобретения, или использования «отрицательного» признака.
[138] Термин «фармацевтически приемлемые соли» включает в себя соли присоединения как кислот, так и оснований. Фармацевтически приемлемые соли включают в себя соли, полученные реакцией активного соединения, действующего в качестве основания, с неорганической или органической кислотой с образованием соли, например солей соляной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты, щавелевой кислоты, малеиновой кислоты, янтарной кислоты, лимонной кислоты, муравьиной кислоты, бромистоводородной кислоты, бензойной кислоты, винной кислоты, фумаровой кислоты, салициловой кислоты, миндальной кислоты, угольной кислоты и т. д. реакцией соединений с подходящей неорганической или органической кислотой любым из ряда известных способов.
[139] Термин «лечение» означает одно или более из облегчения, ослабления, отсрочки, уменьшения, улучшения или управления по меньшей мере одним симптомом состояния у субъекта. Термин «лечение» может также означать одно или более из следующих: купирование, отсрочка начала (т. е. период до клинического проявления состояния) или снижение риска развития или ухудшения состояния.
[140] Соединения по данному изобретению или их фармацевтически приемлемые соли могут содержать один или более асимметричных центров и, таким образом, могут образовывать энантиомеры, диастереомеры и другие стереоизомерные формы, которые могут быть определены с точки зрения абсолютной стереохимии как (R)- или (S)-, или же, как (D)- или (L)- в случае аминокислот. Данное раскрытие включает все такие возможные изомеры, а также их рацемические и оптически чистые формы изображены они конкретно в данном документе или нет. Оптически активные (+) и (-), (R)- и (S)- или (D)- и (L)-изомеры можно получать, используя хиральные синтоны или хиральные реагенты, или разделять, используя традиционные методы, например, хроматографию и фракционную кристаллизацию. Традиционные методики для получения/выделения отдельных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного) с применением, например, хиральной высокоэффективной жидкостной хроматографии (ВЭЖХ). Если описанные в данном документе соединения содержат олефиновые двойные связи или другие центры геометрической асимметрии, и если не указано иное, предполагается, что соединения включают и E, и Z геометрические изомеры. Подобным образом, подразумевается также, что включены все таутомерные формы.
[141] «Стереоизомеры» относится к соединениям, состоящим из одинаковых атомов, связанных одинаковыми связями, но имеющим разные трехмерные структуры, которые не являются взаимозаменяемыми. Настоящее раскрытие предусматривает разнообразные стереоизомеры и их смеси и включает «энантиомеры», которые относятся к двум стереоизомерам, молекулы которых не являются совместимыми зеркальными отражениями друг друга.
[142] «Таутомер» относится к сдвигу протона от одного атома молекулы к другому атому той же молекулы. Настоящее раскрытие включает таутомеры любых указанных соединений.
[143] «Пролекарство» относится к производному соединения по настоящему раскрытию, которое будет превращено в соединение in vivo. В одном варианте осуществления настоящего раскрытия пролекарство включает в себя соединение формулы (I), (IA), (IB), (IC), (II), (IIA), (IIIA), (IIB), (III), (IV), (V), (VA), (VI), (A), (A-I), (B)-(D), (E), (E-I)-(E-VII), (F), (G), (G-I), (G-II), (H) и (H-I), имеющее свободную гидроксильную группу (-ОН), которая ацетилирована (-OCOMe) в одном или более положениях.
[144] «Эффективное количество» означает количество препарата согласно данному изобретению, которое при введении пациенту для лечения состояния, расстройства или состояния является достаточным для осуществления такого лечения. «Эффективное количество» будет варьироваться в зависимости от активного ингредиента, состояния, расстройства или состояния, подлежащего лечению, и его серьезности, а также возраста, веса, физического состояния и восприимчивости млекопитающего, подлежащего лечению.
[145] Термин «терапевтически эффективный», применяемый к дозе или количеству, относится к тому количеству соединения или фармацевтического состава, которое достаточно для получения желаемого клинического эффекта после введения пациенту, нуждающемуся в этом.
[146] В контексте данного документа термин «субъект» может представлять собой человека, примата, не являющегося человеком, млекопитающего, крысу, мышь, корову, лошадь, свинью, овцу, козу, собаку, кошку и тому подобное. Субъекта можно заподозрить в наличии или повышенном риске развития рака, такого как рак предстательной железы, рак молочной железы, рак яичников, рак слюнной железы или рак эндометрия, или заподозрить в наличии или риске развития угрей, гирсутизме, алопеции, доброкачественных заболеваний. гиперплазии предстательной железы, кисты яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии или возрастной макулярной дегенерации. Методы диагностики различных видов рака, таких как рак предстательной железы, рак молочной железы, рак яичников, рак мочевого пузыря, рак поджелудочной железы, гепатоцеллюлярный рак, рак слюнных желез или рак эндометрия и методы диагностики для угрей, гирсутизма, алопеции, доброкачественной гиперплазии предстательной железы, кист яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии или возрастной макулярной дегенерации и клинического разграничения рака, такого как рак предстательной железы, рак молочной железы, рак яичников, рак мочевого пузыря, рак поджелудочной железы, гепатоцеллюлярный рак, рак слюнных желез или рак эндометрия, диагнозов и клинического разграничения угрей; гирсутизма, алопеции, доброкачественной гиперплазии предстательной железы, кист яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии или возрастной макулярной дегенерации известны специалистам в данной области техники.
[147] «Млекопитающее» включает людей, а также одомашненных животных, таких как лабораторные животные (например, мыши, крысы, обезьяны, собаки и т. д.), и домашних животных (например, кошки, собаки, свиньи, крупный рогатый скот, овцы, козы, лошади, кролики), и не одомашненных животных, таких как дикие животные, и т. п.
[148] Все массовые доли (т. е. «% по массе» и «% масс.» и масс./масс.), упомянутые в данном документе, если не указано иное, измерены относительно общей массы фармацевтической композиции.
[149] В контексте данного документа термины «по существу» или «существенный» относятся к полной или почти полной степени или степени действия, характеристики, свойства, состояния, структуры, элемента или результата. Например, объект, который «по существу» включен, будет означать, что объект либо полностью включен, либо почти полностью включен. Точная допустимая степень отклонения от абсолютной полноты в некоторых случаях может зависеть от конкретного контекста. Однако, вообще говоря, близость к завершению будет такова, чтобы иметь такой же общий результат, как если бы были получены абсолютное и полное завершение. Использование «по существу» в равной степени применимо при использовании в отрицательной коннотации для обозначения полного или почти полного отсутствия действия, характеристики, свойства, состояния, структуры, элемента или результата. Например, композиция, которая «по существу не содержит» других активных агентов, будет либо полностью лишена других активных агентов, либо почти полностью лишена других активных агентов, так что эффект будет таким же, как если бы в ней полностью отсутствовали другие активные агенты. Другими словами, композиция, которая «по существу не содержит» ингредиента, элемента или другого активного агента, может все же содержать такой элемент, пока не будет никакого измеримого эффекта.
[150] В контексте данного документа термины, приведенные ниже, имеют следующие значения, если не указано иное:
[151] «Амино» относится к радикалу -NH2 .
[152] «Циано» относится к радикалу -CN.
[153] «Галоген» относится к радикалу бром, хлор, фтор или иод, включая их радиоизотопы. «123I» относится к радиоактивному изотопу иода, имеющему атомную массу 123. Соединения формулы I могут содержать по меньшей мере один фрагмент 123I. На протяжении всей настоящей заявки, где структуры изображают фрагмент 123I в определенном положении, это означает, что фрагмент I в этом положении обогащен 123I. Другими словами, соединения содержат больше, чем естественное содержание 123I в указанном (ых) положении (ах). Не требуется, чтобы соединения содержали 100% 123I в указанных положениях, при условии, что 123I присутствует в количестве, превышающем естественное. Обычно изотоп 123I обогащен более чем на 50%, более чем 60%, более чем 70%, более чем на 80 или более чем на 90% по отношению к 127I. «18F» относится к радиоактивному изотопу фтора, имеющему атомную массу 18. «F» или «19F» относится к обильному нерадиоактивному изотопу фтора, имеющему атомную массу 19. Соединения формулы I могут содержать по меньшей мере один фрагмент 18F. На протяжении всей настоящей заявки, где структуры изображают фрагмент 18F в определенном положении, это означает, что фрагмент F в этом положении обогащен 18F. Другими словами, соединения содержат больше, чем естественное содержание 18F в указанном (ых) положении (ах). Не требуется, чтобы соединения содержали 100% 18F в указанных положениях, при условии, что 18F присутствует в количестве, превышающем естественное. Обычно изотоп 18F обогащен более чем на 50%, более чем 60%, более чем 70%, более чем на 80 или более чем на 90% по отношению к 19F.
[154] «Гидрокси» или «гидроксил» относятся к радикалу -OH.
[155] «Имино» относится к заместителю =NH.
[156] «Нитро» относится к радикалу -NO2.
[157] «Оксо» относится к заместителю =O.
[158] «Тиоксо» относится к заместителю =S.
[159] «Алкил» или «алкильная группа» относится к полностью насыщенному радикалу с прямой или разветвленной углеводородной цепью, имеющему от одного до двенадцати атомов углерода и присоединенному к остальной части молекулы одинарной связью. Включены алкилы, содержащие любое число атомов углерода от 1 до 12. Алкил, содержащий до 12 атомов углерода, представляет собой С1-C12 алкил, алкил, содержащий до 10 атомов углерода, представляет собой С1-C10 алкил, алкил, содержащий до 6 атомов углерода, представляет собой С1-C6 алкил и алкил, содержащий до 5 атомов углерода, представляет собой С1-C5 алкил. С1-C5 алкил включает C5 алкилы, C4 алкилы, C3 алкилы, C2 алкилы и C1 алкил (т. е. метил). C1-C6 алкил включает в себя все фрагменты, описанные выше для C1-C5 алкилов, но также включает C6 алкилы. C1-C10 алкил включает все фрагменты, описанные выше для C1-C5 алкилы и C1-C6 алкилы, но также включает C7, C8, C9 и C10 алкилы. Аналогично, C1-C12 алкил включает в себя все вышеуказанные группы, но также включает C11 и C12 алкилы. Неограничивающие примеры C1-C12 алкила включают метил, этил, н-пропил, изопропил, втор-пропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, трет-амил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил и н-додецил. Если в описании специально не указано иное, то алкильная группа может быть необязательно замещенной.
[160] «Алкилен» или «алкиленовая цепь» относится к полностью насыщенному радикалу двухвалентной углеводородной цепи с прямой или разветвленной цепью, имеющему от одного до двенадцати атомов углерода. Неограничивающие примеры C1-C12 алкилен включает метилен, этилен, пропилен, н-бутилен, этенилен, пропенилен, н-бутенилен, пропинилен, н-бутинилен и т. п. Алкиленовая цепь присоединена к остальной части молекулы через одинарную связь и к радикальной группе через одинарную связь. Точки присоединения алкиленовой цепи к остальной части молекулы и к радикальной группе могут находиться у одного атома углерода или любых двух атомов углерода в указанной цепи. Если в описании специально не указано иное, то алкиленовая цепь может быть необязательно замещенной.
[161] «Алкенил» или «алкенильная группа» относится к радикалу углеводородной цепи с прямой или разветвленной цепью, имеющему от двух до двенадцати атомов углерода и имеющему одну или более двойных углерод-углеродных связей. Каждая алкенильная группа связана с остальной частью молекулы одинарной связью. Включены алкенильные группы, содержащие любое число атомов углерода от 2 до 12. Алкенильная группа, содержащая до 12 атомов углерода, представляет собой С2-C12 алкенил, алкенил, содержащий до 10 атомов углерода, представляет собой С2-C10 алкенил, алкенильная группа, содержащая до 6 атомов углерода, представляет собой С2-C6 алкенил и алкенил, содержащий до 5 атомов углерода, представляет собой С2-C5 алкенил. C2-C5 алкенил включает C5 алкенилы, C4 алкенилы, C3 алкенилы и C2 алкенилы. C2-C6 алкенил включает в себя все фрагменты, описанные выше для C2-C5 алкенилов, но также включает C6 алкенилы. C2-C10 алкенил включает все фрагменты, описанные выше для C2-C5 алкенилы и C2-C6 алкенилы, но также включает C7, C8, C9 и C10 алкенилы. Аналогично, C2-C12 алкенил включает в себя все вышеуказанные группы, но также включает C11 и C12 алкенилы. Неограничивающие примеры C2-C12 алкенила включают этенил (винил), 1-пропенил, 2-пропенил (аллил), изопропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-гексенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-гептенил, 2-гептенил, 3-гептенил, 4-гептенил, 5-гептенил, 6-гептенил, 1-октенил, 2-октенил, 3-октенил, 4-октенил, 5-октенил, 6-октенил, 7-октенил, 1-ноненил, 2-ноненил, 3-ноненил, 4-ноненил, 5-ноненил, 6-ноненил, 7-ноненил, 8-ноненил, 1-деценил, 2-деценил, 3-деценил, 4-деценил, 5-деценил, 6-деценил, 7-деценил, 8-деценил, 9-деценил, 1-ундеценил, 2-ундеценил, 3-ундеценил, 4-ундеценил, 5-ундеценил, 6-ундеценил, 7-ундеценил, 8-ундеценил, 9-ундеценил, 10-ундеценил, 1-додеценил, 2-додеценил, 3-додеценил, 4-додеценил, 5-додеценил, 6-додеценил, 7-додеценил, 8-додеценил, 9-додеценил, 10-додеценил и 11-додеценил. Если в описании специально не указано иное, то алкильная группа может быть необязательно замещенной.
[162] «Алкенилен» или «алкениленовая группа» относится к двухвалентному радикалу углеводородной цепи с прямой или разветвленной цепью, имеющему от двух до двенадцати атомов углерода и имеющему одну или более двойных углерод-углеродных связей. Неограничивающие примеры C2-C12 алкенилена включают этен, пропен, бутен и тому подобное. Алкениленовая цепь присоединена к остальной части молекулы через одинарную связь и к радикальной группе через одинарную связь. Точки присоединения алкениленовой цепи к остальной части молекулы и к радикальной группе могут находиться у одного атома углерода или любых двух атомов углерода в указанной цепи. Если в описании специально не указано иное, то алкениленовая цепь может быть необязательно замещенной.
[163] «Алкинил» или «алкинильная группа» относится к радикалу углеводородной цепи с прямой или разветвленной цепью, имеющему от двух до двенадцати атомов углерода и имеющему одну или более тройных углерод-углеродных связей. Каждая алкинильная группа связана с остальной частью молекулы одинарной связью. Включены алкинильные группы, содержащие любое число атомов углерода от 2 до 12. Алкинильная группа, содержащая до 12 атомов углерода, представляет собой С2-C12 алкинил, алкинил, содержащий до 10 атомов углерода, представляет собой С2-C10 алкинил, алкинильная группа, содержащая до 6 атомов углерода, представляет собой С2-C6 алкинил и алкинил, содержащий до 5 атомов углерода, представляет собой С2-C5 алкинил. C2-C5 алкинил включает C5 алкинилы, C4 алкинилы, C3 алкинилы и C2 алкинилы. C2-C6 алкинил включает в себя все фрагменты, описанные выше для C2-C5 алкинилов, но также включает C6 алкинилы. C2-C10 алкинил включает все фрагменты, описанные выше для C2-C5 алкинилов и C2-C6 алкинилов, но также включает C7, C8, C9 и C10 алкинилы. Аналогично, C2-C12 алкинил включает в себя все вышеуказанные группы, но также включает C11 и C12 алкинилы. Неограничивающие примеры C2-C12 алкенила включают этинил, пропинил, бутинил, пентинил и тому подобное. Если в описании специально не указано иное, то алкильная группа может быть необязательно замещенной.
[164] «Алкинилен» или «алкиниленовая группа» относится к двухвалентному радикалу углеводородной цепи с прямой или разветвленной цепью, имеющему от двух до двенадцати атомов углерода и имеющему одну или более тройных углерод-углеродных связей. Неограничивающие примеры C2-C12 алкинилена включают этинилен, пропаргилен и тому подобное. Алкиниленовая цепь присоединена к остальной части молекулы через одинарную связь и к радикальной группе через одинарную связь. Точки присоединения алкиниленовой цепи к остальной части молекулы и к радикальной группе могут находиться у одного атома углерода или любых двух атомов углерода в указанной цепи. Если в описании специально не указано иное, то алкиниленовая цепь может быть необязательно замещенной.
[165] «Алкокси» относится к радикалу формулы -ORa, где Ra представляет собой алкильный, алкенильный или алкинильный радикал, описанный выше, содержащий от одного до двенадцати атомов углерода. Если в описании специально не указано иное, то алкокси-группа может быть необязательно замещенной.
[166] «Алкиламино» относится к радикалу формулы -NHRa или -NRaRa, где каждый Ra независимо представляет собой алкильный, алкенильный или алкинильный радикал, описанный выше, содержащий от одного до двенадцати атомов углерода. Если в описании специально не указано иное, то алкиламино-группа может быть необязательно замещенной.
[167] «Алкилкарбонил» относится к фрагменту -C(=O)Ra, где Ra представляет собой алкильный, алкенильный или алкинильный радикал, как определено выше. Неограничивающим примером алкилкарбонила является метилкарбонильный («ацетальный») фрагмент. Алкилкарбонильные группы также могут упоминаться как «Cw-Cz-ацил», где w и z изображают диапазон количества атомов углерода в Ra, как определено выше. Например, «C1-C10 ацил» относится к алкилкарбонильной группе, как определено выше, где Ra представляет собой C1-C10 алкильный, C1-C10 алкенильный или C1-C10 алкинильный радикал, как определено выше. Если в описании специально не указано иное, то алкилкарбонильная группа может быть необязательно замещенной.
[168] «Арил» относится к радикалу углеводородной кольцевой системы, содержащему водород, от 6 до 18 атомов углерода и по меньшей мере одно ароматическое кольцо. Для целей настоящего изобретения арильный радикал может быть моноциклической, бициклической, трициклической или тетрациклической кольцевой системой, которая может содержать конденсированные или мостиковые кольцевые системы. Арильные радикалы включают, но не ограничиваются ими, арильные радикалы, полученные из ацеантрилена, аценафтилена, ацефенантрилена, антрацена, азулена, бензола, хризена, флуорантена, флуорена, ассим-индацена, сим-индацена, индана, индена, нафталина, феналена, фенантрена, плейадена, пирена и трифенилена. Если в описании специально не указано иное, термин «арил» включает арильные радикалы, которые являются необязательно замещенными.
[169] «Аралкил» или «арилалкил» относится к радикалу формулы RbRc, где Rb представляет собой алкиленовую группу, описанную выше, и Rc представляет собой один или более арильных радикалов, описанных выше, например, бензил, дифенилметил и тому подобное. Если в описании специально не указано иное, то аралкильная группа может быть необязательно замещенной.
[170] «Аралкенил» или «арилалкенил» относится к радикалу формулы RbRc, где Rb представляет собой алкениленовую группу, описанную выше, и Rc представляет собой один или более арильных радикалов, описанных выше. Если в описании специально не указано иное, то аралкенильная группа может быть необязательно замещенной.
[171] «Аралкинил» или «арилалкинил» относится к радикалу формулы RbRc, где Rb представляет собой алкиниленовую группу, описанную выше, и Rc представляет собой один или более арильных радикалов, описанных выше. Если в описании специально не указано иное, то аралкинильная группа может быть необязательно замещенной.
[172] «Карбоциклил», «карбоциклическое кольцо» или «карбоцикл» относится к кольцевой структуре, в которой атомы, которые образуют кольцо, каждый, представляют собой углерод. Карбоциклические кольца могут содержать от 3 до 20 атомов углерода в кольце. Карбоциклические кольца включают арилы и циклоалкил, циклоалкенил и циклоалкинил, как определено в данном описании. Если в описании специально не указано иное, то карбоциклильная группа может быть необязательно замещенной.
[173] «Циклоалкил» относится к стабильному неароматическому моноциклическому или полициклическому полностью насыщенному углеводородному радикалу, состоящему только из атомов углерода и водорода, который может содержать конденсированные или мостиковые кольцевые системы, содержащему от трех до двадцати атомов углерода, предпочтительно содержащему от трех до десяти атомов углерода, и который присоединен к остальной части молекулы одинарной связью. Моноциклические циклоалкильные радикалы включают, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Полициклические циклоалкильные радикалы включают в себя, например, адамантил, норборнил, декалинил, 7,7-диметил-бицикло[2.2.1]гептанил и т. п. Если в описании специально не указано иное, то циклоалкильная группа может быть необязательно замещенной.
[174] «Циклоалкенил» относится к стабильному неароматическому моноциклическому или полициклическому углеводородному радикалу, состоящему только из атомов углерода и водорода, имеющему одну или более двойных углерод-углеродных связей, который может содержать конденсированные или мостиковые кольцевые системы, содержащему от трех до двадцати атомов углерода, предпочтительно содержащему от трех до десяти атомов углерода, и который присоединен к остальной части молекулы одинарной связью. Моноциклические циклоалкенильные радикалы включают, например, циклопентенил, циклогексенил, циклогептенил, циклоктенил и тому подобное. Полициклические циклоалкенильные радикалы включают, например, бицикло[2.2.1]гепт-2-енил и тому подобное. Если в описании специально не указано иное, то циклоалкенильная группа может быть необязательно замещенной.
[175] «Циклоалкинил» относится к стабильному неароматическому моноциклическому или полициклическому углеводородному радикалу, состоящему только из атомов углерода и водорода, имеющему одну или более тройных углерод-углеродных связей, который может содержать конденсированные или мостиковые кольцевые системы, содержащему от трех до двадцати атомов углерода, предпочтительно содержащему от трех до десяти атомов углерода, и который присоединен к остальной части молекулы одинарной связью. Моноциклические циклоалкинильные радикалы включают, например, циклогептинил, циклоктинил и тому подобное. Если в описании специально не указано иное, то циклоалкинильная группа может быть необязательно замещенной.
[176] «Циклоалкилалкил» относится к радикалу формулы Rb-Rd, где Rb представляет собой алкиленовую, алкениленовую или алкиниленовую группу, описанную выше, и Rd представляет собой циклоалкильный, циклоалкенильный, циклоалкинильный радикал, описанный выше. Если в описании специально не указано иное, то циклоалкилалкильная группа может быть необязательно замещенной.
[177] «Галогеналкил» относится к алкильному радикалу, как определено выше, который замещен одним или более галогеновыми радикалами, как определено выше, например, трифторметилом, дифторметилом, трихлорметилом, 2,2,2-трифторэтилом, 1,2-дифторэтилом, 3-бром-2-фторпропилом, 1,2-дибромэтилом и тому подобное. Если в описании специально не указано иное, то галогеналкильная группа может быть необязательно замещенной.
[178] «Галогеналкенил» относится к алкенильному радикалу, описанному выше, который замещен одним или более радикалами галогена, описанными выше, например, 1-фторпропенил, 1,1-дифторбутенил и тому подобное. Если в описании специально не указано иное, то галогеналкенильная группа может быть необязательно замещенной.
[179] «Галогеналкинил» относится к алкинильному радикалу, описанному выше, который замещен одним или более радикалами галогена, описанными выше, например, 1-фторпропинил, 1-дифторбутинил и тому подобное. Если в описании специально не указано иное, то галогеналкенильная группа может быть необязательно замещенной.
[180] «Гетероциклил», «гетероциклическое кольцо» или «гетероцикл» относится к стабильному 3-20-членному неароматическому, частично ароматическому или ароматическому кольцевому радикалу, который состоит из двух-двенадцати атомов углерода и одного-шести гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы. Гетероциклильные или гетероциклические кольца включают гетероарилы, как определено ниже. Если в описании специально не указано иное, гетероциклильный радикал может быть моноциклической, бициклической, трициклической или тетрациклической кольцевой системой, которая может содержать конденсированные или мостиковые кольцевые системы; и атомы азота, углерода или серы в гетероциклильном радикале могут быть необязательно окислены; атом азота может быть необязательно кватернизован; и гетероциклильный радикал может быть частично или полностью насыщенным. Примеры таких гетероциклильных радикалов включают, но не ограничиваются этим, диоксоланил, тиенил[1,3]дитианил, декагидроизохинолил, имидазолинил, имидазолидинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, оксазолидинил, пиперидинил, пиперазинил, 4-пиперидонил, пирролидинил, пиразолидинил, хинуклидинил, тиазолидинил, тетрагидрофурил, тритианил, тетрагидропиранил, тиоморфолинил, тиаморфолинил, 1-оксо-тиоморфолинил и 1,1-диоксо-тиоморфолинил. Если в описании специально не указано иное, то гетероциклильная группа может быть необязательно замещенной.
[181] «Гетероциклилалкил» относится к радикалу формулы -Rb-Re, где Rb представляет собой алкиленовую группу, как определено выше, и Re представляет собой гетероциклильный радикал, как определено выше. Если в описании специально не указано иное, то гетероциклоалкилалкильная группа может быть необязательно замещенной.
[182] «Гетероциклилалкенил» относится к радикалу формулы -Rb-Re, где Rb представляет собой алкениленовую группу, как определено выше, и Re представляет собой гетероциклильный радикал, как определено выше. Если в описании специально не указано иное, то гетероциклоалкилалкенильная группа может быть необязательно замещенной.
[183] «Гетероциклилалкинил» относится к радикалу формулы -Rb-Re, где Rb представляет собой алкиниленовую группу, как определено выше, и Re представляет собой гетероциклильный радикал, как определено выше. Если в описании специально не указано иное, то гетероциклоалкилалкинильная группа может быть необязательно замещенной.
[184] «N-гетероциклил» относится к гетероциклильному радикалу, описанному выше, содержащему по меньшей мере один атом азота, причем точка присоединения гетероциклильного радикала к остальной части молекулы находится у атома азота в гетероциклильном радикале. Если в описании конкретно не указано иное, N-гетероциклильная группа может быть необязательно замещенной.
[185] «Гетероарил» относится к радикалу 5-20-членной кольцевой системы, содержащему атомы водорода, от одного до тринадцати атомов углерода, от одного до шести гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, и по меньшей мере одно ароматическое кольцо. Для целей настоящего изобретения гетероарильный радикал может быть моноциклической, бициклической, трициклической или тетрациклической кольцевой системой, которая может содержать конденсированные или мостиковые кольцевые системы; и атомы азота, углерода или серы в гетероарильном радикале могут быть необязательно окислены; атом азота может быть необязательно кватернизован. Примеры включают, не ограничиваясь ими, азепинил, акридинил, бензимидазолил, бензотиазолил, бензиндолил, бензодиоксолил, бензофуранил, бензооксазолил, бензотиазолил, бензотиадиазолил, бензо[b][1,4]диоксепинил, 1,4-бензодиоксанил, бензонафтофуранил, бензоксазолил, бензодиоксолил, бензодиоксинил, бензопиранил, бензопиранонил, бензофуранил, бензофуранонил, бензотиенил (бензотиофен), бензотриазолил, бензо[4,6]имидазо[1,2-а]пиридинил, карбазолил, циннолинил, дибензофуранил, дибензотиофен, фуранил, фуранонил, изотиазолил, имидазолил, индазолил, индолил, индазолил, изоиндолил, индолинил, изоиндолинил, изохинолил, индолизинил, изоксазолил, нафтиридинил, оксадиазолил, 2-оксоазепинил, оксазолил, оксиранил, 1-оксидопиридинил, 1-оксидопиримидинил, 1-оксидопиразинил, 1-оксидопиридазинил, 1-фенил-1Н-пирролил, феназинил, фенотиазинил, феноксазинил, фталазинил, птеридинил, пуринил, пирролил, пиразолил, пиридинил, пиразинил, пиримидинил, пиридазинил, хиназолинил, хиноксалинил, хинолинил, хинуклидинил, изохинолинил, тетрагидрохинолинил, тиазолил, тиадиазолил, триазолил, тетразолил, триазинил и тиофен (т. е. тиенил). Если в описании специально не указано иное, то гетероарильная группа может быть необязательно замещенной.
[186] «N-гетероарил» относится к гетероарильному радикалу, описанному выше, содержащему по меньшей мере один атом азота, причем точка присоединения гетероарильного радикала к остальной части молекулы находится у атома азота в гетероарильном радикале. Если в описании конкретно не указано иное, N-гетероарильная группа может быть необязательно замещенной.
[187] «Гетероарилалкил» относится к радикалу формулы -Rb-Rf, где Rb представляет собой алкиленовую цепь, как определено выше, и Rf представляет собой гетероарильный радикал, как определено выше. Если в описании специально не указано иное, то гетероарилалкильная группа может быть необязательно замещенной.
[188] «Гетероарилалкенил» относится к радикалу формулы -Rb-Rf, где Rb представляет собой алкениленовую цепь, как определено выше, и Rf представляет собой гетероарильный радикал, как определено выше. Если в описании специально не указано иное, то гетероарилалкенильная группа может быть необязательно замещенной.
[189] «Гетероарилалкинил» относится к радикалу формулы -Rb-Rf, где Rb представляет собой алкиниленовую цепь, как определено выше, и Rf представляет собой гетероарильный радикал, как определено выше. Если в описании специально не указано иное, то гетероарилалкинильная группа может быть необязательно замещенной.
[190] «Кольцо» относится к циклической группе, которая может быть полностью насыщенной, частично насыщенной или полностью ненасыщенной. Кольцо может быть моноциклическим, бициклическим, трициклическим или тетрациклическим. Если в описании специально не указано иное, то кольцо может быть необязательно замещенным.
[191] «Тиоалкил» относится к радикалу формулы -SRa, где Ra представляет собой алкильный, алкенильный или алкинильный радикал, описанный выше, содержащий от одного до двенадцати атомов углерода. Если в описании специально не указано иное, то тиоалкильная группа может быть необязательно замещенной.
[192] В контексте данного документа термин «замещенный» означает любую из вышеуказанных групп (т. е. алкил, алкилен, алкенил, алкенилен, алкинил, алкинилен, алкокси, алкиламино, алкилкарбонил, тиоалкил, арил, аралкил, карбоциклил, циклоалкил, циклоалкенил, циклоалкинил, циклоалкилалкил, галогеналкил, гетероциклил, N-гетероциклил, гетероциклилалкил, гетероарил, N-гетероарил и/или гетероарилалкил), где по меньшей мере один атом водорода заменен связью с атомами, не являющимися водородом, такими как, но не ограничиваясь этим: атом галогена, такой как F, Cl, Br и I; атом кислорода в таких группах, как гидроксильные группы, алкокси-группы и сложноэфирные группы; атом серы в таких группах, как тиоильные группы, тиоалкильные группы, сульфоновые группы, сульфонильные группы и сульфоксидные группы; атом азота в таких группах, как амины, амиды, алкиламины, диалкиламины, ариламины, алкилариламины, диариламины, N-оксиды, имиды и енамины; атом кремния в таких группах, как триалкилсилильные группы, диалкиларилсилильные группы, алкилдиарилсилильные группы и триарилсилильные группы; и другие гетероатомы в разнообразных других группах.
[193] «Замещенная» означает также любую из представленных выше групп, в которой один или более атомов водорода заменены связью более высокого порядка (например, двойной или тройной связью) с гетероатомом, таким как кислород в оксо, карбонильных, карбоксильных и сложных эфирных группах; и азот в таких группах как имины, оксимы, гидразоны и нитрилы. Например, «замещенный» включает любую из вышеуказанных групп, в которых один или более атомов водорода заменены на -NRgRh, -NRgC(=O)Rh, -NRgC(=O)NRgRh, -NRgC(=O)ORh, -NRgSO2Rh, -OC(=O)NRgRh, -ORg, -SRg, -SORg, -SO2Rg, -OSO2Rg, -SO2ORg, =NSO2Rg и -SO2NRgRh. «Замещенный» также означает любую из вышеуказанных групп, в которой один или более атомов водород заменены на -C(=O)Rg, -C(=O)ORg, -C(=O)NRgRh, -CH2SO2Rg, -CH2SO2NRgRh. В вышеизложенном Rg и Rh являются одинаковыми или разными и независимо представляют собой водород, алкил, алкенил, алкинил, алкокси, алкиламино, тиоалкил, арил, аралкил, циклоалкил, циклоалкенил, циклоалкинил, циклоалкилалкил, галогеналкил, галогеналкенил, галогеналкинил, гетероциклил, N-гетероциклил, гетероциклилалкил, гетероарил, N-гетероарил и/или гетероарилалкил. «Замещенный» далее означает любую из вышеуказанных групп, в которой один или более атомов водородов заменены связью с амино, циано, гидроксильной, имино, нитро, оксо, тиоксо, галогеновой, алкильной, алкенильной, алкинильной, алкокси, алкиламино, тиоалкильной, арильной, аралкильной, циклоалкильной, циклоалкенильной, циклоалкинильной, циклоалкилалкильной, галогеналкильной, галогеналкенильной, галогеналкинильной, гетероциклильной, N-гетероциклильной, гетероциклилалкильной, гетероарильной, N-гетероарильной и/или гетероарилалкильной группой. Кроме того, каждый из вышеуказанных заместителей также может необязательно заменяться одним или более из вышеуказанных заместителей.
[194] В контексте данного документа, символ « 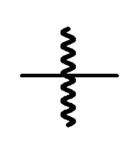 » (далее именуемый как «связь в точке присоединения») обозначает связь, которая является точкой присоединения между двумя химическими объектами, один из которых изображен как присоединенный к связи в точке присоединения, а другой не представляет не изображен как присоединенный к точке присоединения. Например, «
» (далее именуемый как «связь в точке присоединения») обозначает связь, которая является точкой присоединения между двумя химическими объектами, один из которых изображен как присоединенный к связи в точке присоединения, а другой не представляет не изображен как присоединенный к точке присоединения. Например, « 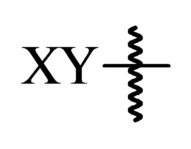 » обозначает то, что химический объект «XY» связан с другим химическим объектом через точку присоединения. Кроме того, конкретная точка присоединения к не изображенному химическому объекту может быть определена путем логического вывода. Например, соединение CH3R3, где R3 представляет собой H или «
» обозначает то, что химический объект «XY» связан с другим химическим объектом через точку присоединения. Кроме того, конкретная точка присоединения к не изображенному химическому объекту может быть определена путем логического вывода. Например, соединение CH3R3, где R3 представляет собой H или « 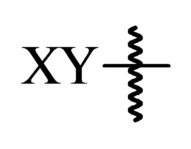 » позволяет сделать вывод, что когда R3 представляет собой «XY», связь в точке присоединения представляет собой ту же связь, что и связь, посредством которой R3 изображается как связанный с CH3.
» позволяет сделать вывод, что когда R3 представляет собой «XY», связь в точке присоединения представляет собой ту же связь, что и связь, посредством которой R3 изображается как связанный с CH3.
[195] «Конденсированная» относится к любой кольцевой структуре, описанной в настоящем документе, которая конденсирована с существующей кольцевой структурой в соединениях согласно настоящему изобретению. Если конденсированное кольцо представляет собой гетероциклильное кольцо или гетероарильное кольцо, то любой атом углерода в существующей кольцевой структуре, которая становится частью конденсированного гетероциклильного кольца или конденсированного гетероарильного кольца, может быть заменен атомом азота.
[196] Следующее описание включает в себя информацию, которая может быть подходящей для понимания настоящего изобретения. Это не признание того, что какая-либо информация, представленная в данном документе, относится к предшествующему уровню техники или относится к заявленному в настоящее время изобретению, или что любая публикация, на которую конкретно или косвенно делается ссылка, является предшествующим уровнем техники.
Соединения по настоящему раскрытию
[197] Соединение по настоящему раскрытию может применяться для модуляции андрогенового рецептора (AR). Кроме того, соединение по настоящему изобретению может быть пригодно для лечения разнообразных заболеваний и состояний, включая, но не ограничиваясь этим, рак. В некоторых вариантах осуществления настоящего изобретения рак представляет собой рак предстательной железы или рак молочной железы.
[198] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (I):
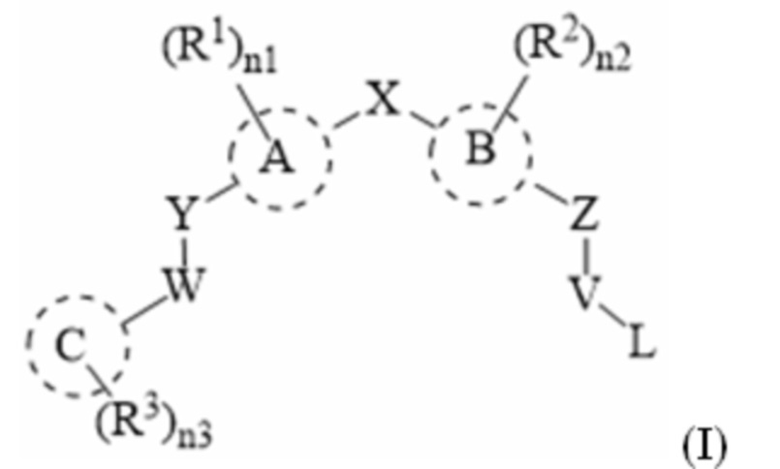
[199] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[200] A и B, каждый независимо, представляют собой арил или гетероарил;
[201] C представляет собой 3-10-членное кольцо;
[202] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[203] Y и Z, каждый независимо, представляют собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-;
[204] W и V, каждый независимо, представляют собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[205] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[206] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[207] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[208] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[209] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[210] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -OCO(C1-C6 алкил), -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[211] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[212] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), взятые вместе, образуют необязательно замещенный гетероциклил;
[213] каждый m независимо равно 0, 1 или 2;
[214] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[215] n3 равно 0, 1, 2, 3, 4 или 5; и
[216] каждое t независимо равно 0, 1 или 2.
[217] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (IA):
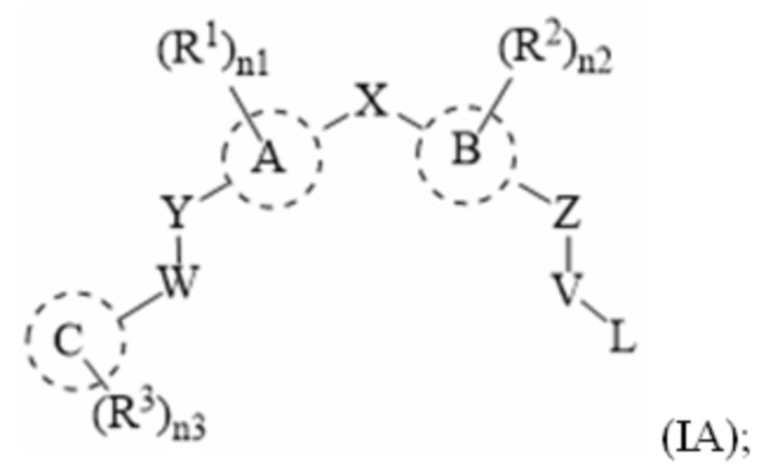
[218] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[219] A и B, каждый независимо, представляют собой арил или гетероарил;
[220] C представляет собой 3-10-членное кольцо;
[221] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[222] Y и Z, каждый независимо, представляют собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-;
[223] W и V, каждый независимо, представляют собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[224] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[225] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[226] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[227] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[228] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[229] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -OCO(C1-C6 алкил), -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[230] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[231] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), взятые вместе, образуют необязательно замещенный гетероциклил;
[232] каждый m независимо равно 0, 1 или 2;
[233] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[234] n3 равно 0, 1, 2, 3, 4 или 5; и
[235] каждое t независимо равно 0, 1 или 2.
[236] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (IB):
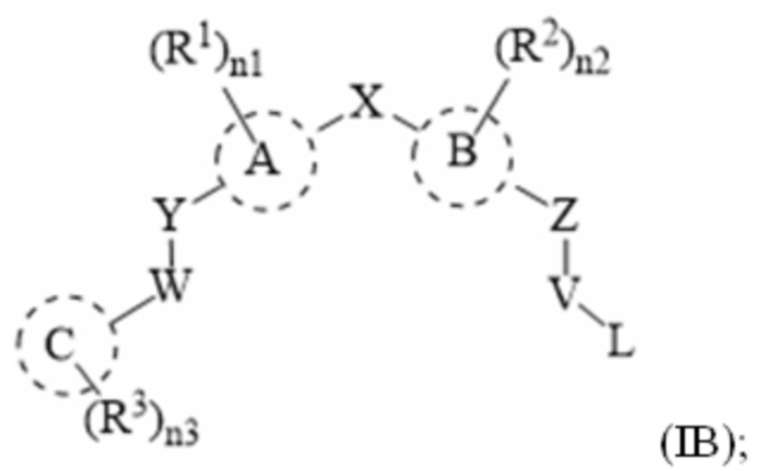
[237] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[238] A и B, каждый независимо, представляют собой арил или гетероарил;
[239] C представляет собой 3-10-членное кольцо;
[240] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[241] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[242] W представляет собой связь, -(CR8aR9a)m-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[243] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[244] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[245] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[246] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[247] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[248] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[249] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[250] R8a и R9a, каждый независимо, представляют собой водород, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[251] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкил-NH2, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[252] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), или (R14 и R16), взятые вместе, образуют необязательно замещенный гетероциклил;
[253] каждый m независимо равно 0, 1 или 2;
[254] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[255] n3 равно 0, 1, 2, 3, 4 или 5; и
[256] каждое t независимо равно 0, 1 или 2.
[257] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (IC)
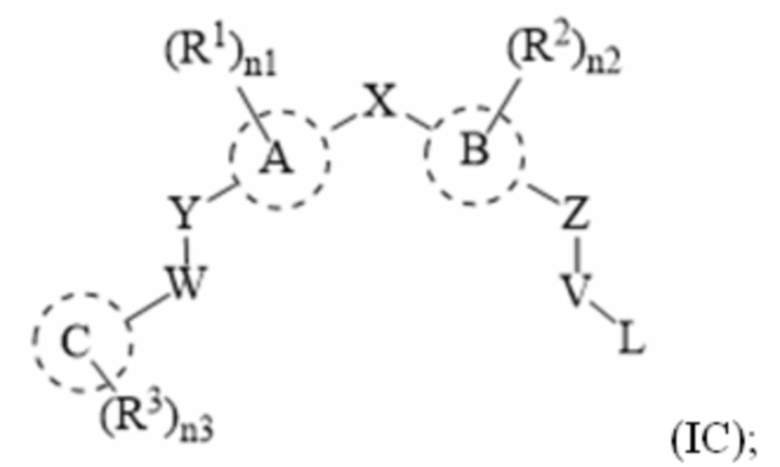
[258] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[259] A и B, каждый независимо, представляют собой арил или гетероарил;
[260] C представляет собой 3-10-членное кольцо;
[261] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[262] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[263] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, N(R7)CO-, -CONR7- или -NSO2R7-;
[264] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[265] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[266] L представляет собой водород, галоген, -CF2R10, -CF3, -CCl2R10, -CCl3, -CN, -OR10; -NR11R12 или -CONR11R12;
[267] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[268] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[269] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[270] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[271] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[272] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкил-NH2, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[273] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), или (R14 и R16), взятые вместе, образуют необязательно замещенный гетероциклил;
[274] каждый m независимо равно 0, 1 или 2;
[275] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[276] n3 равно 0, 1, 2, 3, 4 или 5; и
[277] каждое t независимо равно 0, 1 или 2.
[278] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (II):
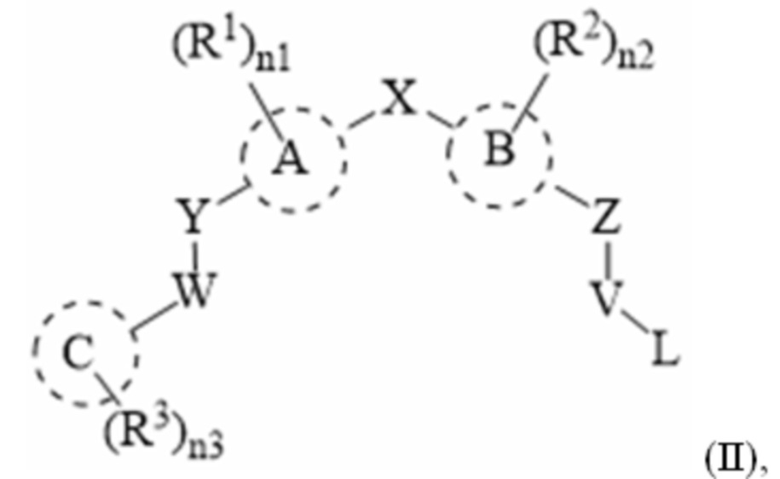
[279] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[280] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[281] C представляет собой 3-10-членное кольцо;
[282] X представляет собой связь, -(CR5R6)t- или -NR7-;
[283] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[284] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[285] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -NHCO-, -N(C1-C3 алкил)CO- или -CONH- или -CON(C1-C3 алкил)-;
[286] V представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[287] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[288] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[289] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[290] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[291] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[292] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[293] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил;
[294] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[295] каждый m независимо равно 0, 1 или 2;
[296] n1 и n2, каждый независимо, равны 0, 1 или 2;
[297] n3 равно 0, 1, 2, 3, 4 или 5; и
[298] t равно 0, 1 или 2.
[299] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IIA):
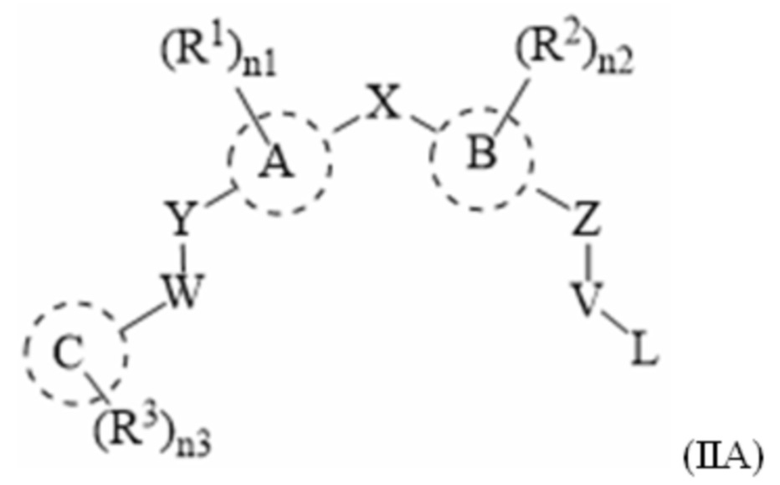
[300] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[301] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[302] C представляет собой 3-10-членное кольцо;
[303] X представляет собой связь, -(CR5R6)t- или -NR7-;
[304] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[305] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[306] W представляет собой связь, -CH2-, -C(CH3)H-, -NHCO-, -N(C1-C3 алкил)CO- или -CONH- или -CON(C1-C3 алкил)-;
[307] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[308] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[309] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[310] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[311] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[312] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[313] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[314] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил или C1-C6 алкил-NH2; или R14 и R16, взятые вместе, образуют 3-6-членный гетероциклил;
[315] каждый m независимо равно 0, 1 или 2;
[316] n1 и n2, каждый независимо, равны 0, 1 или 2;
[317] n3 равно 0, 1, 2, 3, 4 или 5; и
[318] t равно 0, 1 или 2.
[319] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IIB):
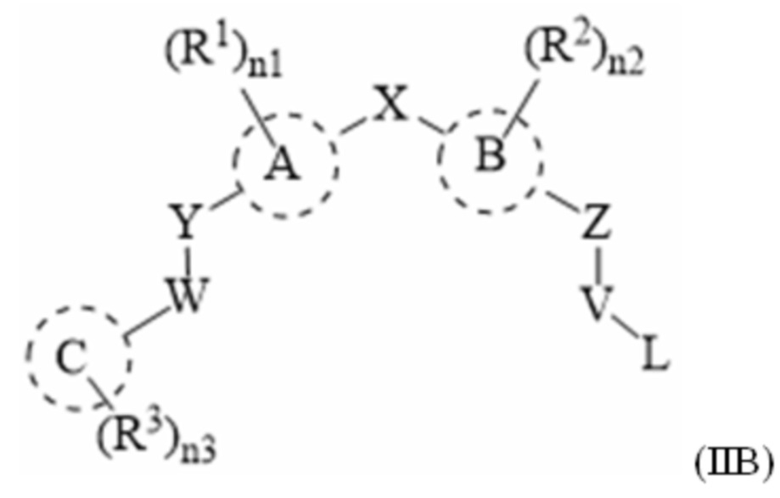
[320] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[321] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[322] C представляет собой 3-10-членное кольцо;
[323] X представляет собой связь, -(CR5R6)t- или -NR7-;
[324] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[325] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[326] W представляет собой связь, -CH2- или -C(CH3)H-;
[327] V представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[328] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[329] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[330] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[331] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[332] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[333] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[334] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[335] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил или C1-C6 алкил-NH2; или R14 и R16, взятые вместе, образуют 3-6-членный гетероциклил;
[336] каждый m независимо равно 0, 1 или 2;
[337] n1 и n2, каждый независимо, равны 0, 1 или 2;
[338] n3 равно 1, 2, 3, 4 или 5; и
[339] t равно 0, 1 или 2.
[340] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (III):

[341] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[342] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[343] C представляет собой 3-10-членное кольцо;
[344] X представляет собой связь, -(CR5R6)t- или -NR7-;
[345] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[346] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[347] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[348] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[349] L представляет собой галоген, -NH2 или -CF3;
[350] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[351] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[352] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[353] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[354] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[355] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[356] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[357] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[358] каждый m независимо равно 0, 1 или 2;
[359] n1 и n2, каждый независимо, равны 0, 1 или 2;
[360] n3 равно 0, 1, 2, 3, 4 или 5; и
[361] t равно 0, 1 или 2.
[362] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IIIA):
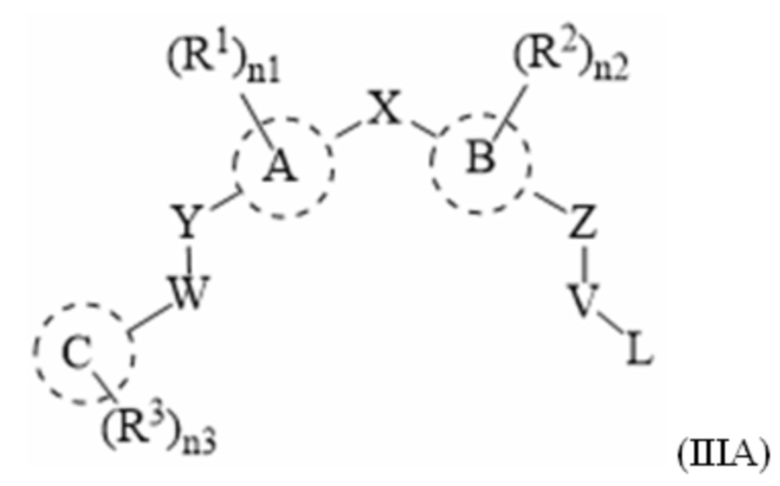
[363] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[364] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[365] C представляет собой 3-10-членное кольцо;
[366] X представляет собой связь, -(CR5R6)t- или -NR7;
[367] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2-, -NR7- или -N(COCH3)-;
[368] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[369] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[370] V представляет собой -CH2-, и L представляет собой галоген, -NH2, -CHCl2, -CCl3 или -CF3; или
[371] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[372] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[373] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[374] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[375] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[376] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[377] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[378] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[379] R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил;
[380] каждый m независимо равно 0, 1 или 2;
[381] n1 и n2, каждый независимо, равны 0, 1 или 2;
[382] n3 равно 1, 2, 3, 4 или 5; и
[383] t равно 0, 1 или 2.
[384] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (IV):
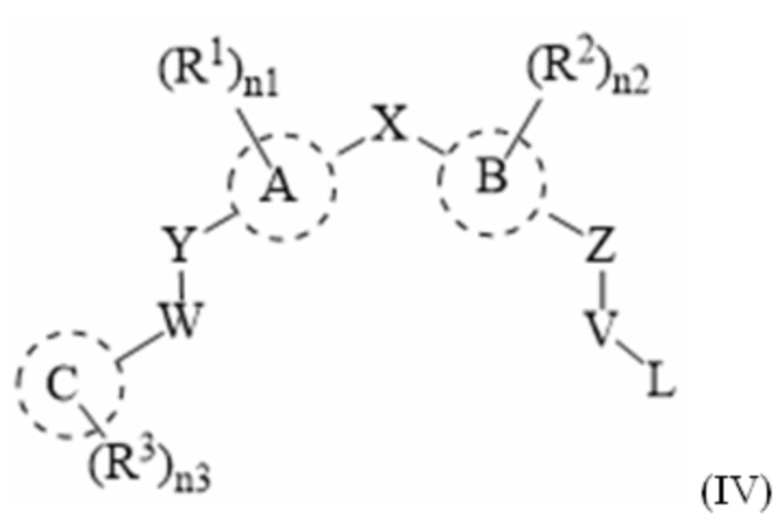
[385] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[386] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[387] C представляет собой 3-10-членное кольцо;
[388] X представляет собой связь, -(CR5R6)t- или -NR7-;
[389] Y и Z, каждый независимо, представляют собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[390] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[391] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[392] L представляет собой галоген, -NH2 или -CF3;
[393] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[394] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[395] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[396] R7 представляет собой H или C1-C6 алкил;
[397] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[398] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[399] n1 и n2, каждый независимо, равны 0, 1 или 2;
[400] n3 равно 0, 1, 2, 3, 4 или 5; и
[401] t равно 0, 1 или 2.
[402] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (V):
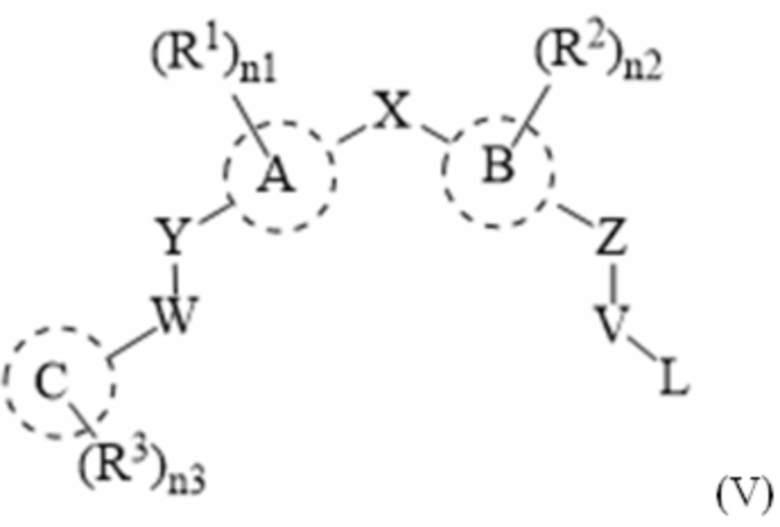
[403] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[404] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[405] C представляет собой 5-10-членный гетероарил или арил;
[406] X представляет собой связь, -(CR5R6)t- или -NR7-;
[407] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[408] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[409] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[410] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[411] L представляет собой галоген, -NH2 или -CF3;
[412] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[413] R3 выбран из водорода, галогена, оксо, =S, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[414] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[415] R7 представляет собой H или C1-C6 алкил;
[416] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил; или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил;
[417] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[418] n1 и n2, каждый независимо, равны 0, 1 или 2;
[419] n3 равно 0, 1, 2, 3, 4 или 5; и
[420] t равно 0, 1 или 2.
[421] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (VA):
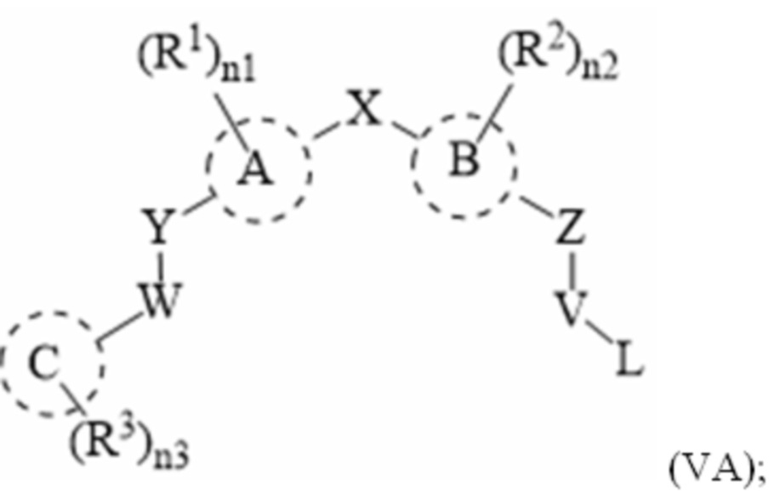
[422] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[423] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[424] C представляет собой 5-10-членный гетероарил или арил;
[425] X представляет собой связь, -(CR5R6)t- или -NR7;
[426] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[427] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[428] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[429] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[430] L представляет собой водород, галоген, -OH, -NH2 или -CF3;
[431] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[432] R3 выбран из водорода, галогена, оксо, =S, -CN, -CF3, -OH, -S(C1-C3 алкил), C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -NR14COOR16, -NR14CONR14R15, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкил) или -(C1-C6 алкил)-SO2(C1-C3 алкил);
[433] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, -NH2, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[434] R7 представляет собой H, C1-C6 алкил, -CO(C1-C6 алкил);
[435] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или -COO(C1-C6 алкил); или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил;
[436] R16 представляет собой водород, C1-C3 алкил, C1-C3 галогеналкил, C2-C3 алкенил или C2-C3 алкинил;
[437] n1 и n2, каждый независимо, равны 0, 1 или 2;
[438] n3 равно 0, 1, 2, 3, 4 или 5; и
[439] t равно 0, 1 или 2.
[440] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (VI):
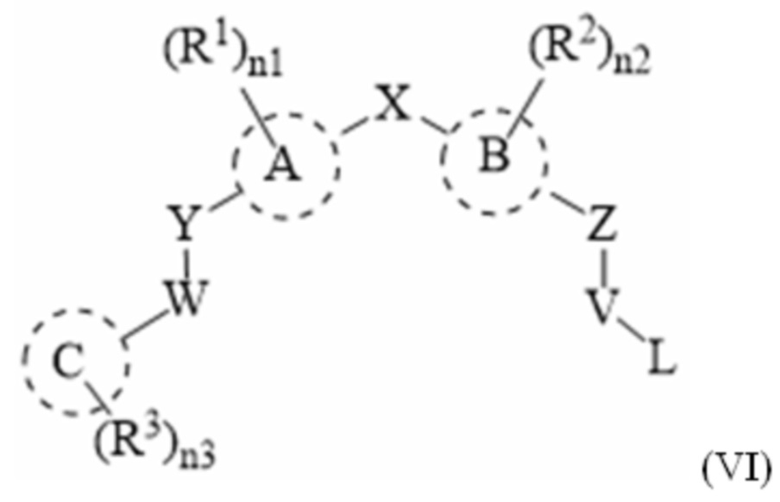
[441] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[442] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[443] C представляет собой 5-10-членный гетероциклил;
[444] X представляет собой связь, -(CR5R6)t- или -NR7-;
[445] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[446] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[447] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[448] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[449] L представляет собой галоген, -NH2 или -CF3;
[450] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[451] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[452] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[453] R7 представляет собой H или C1-C6 алкил;
[454] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[455] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[456] n1 и n2, каждый независимо, равны 0, 1 или 2;
[457] n3 равно 0, 1, 2, 3, 4 или 5; и
[458] t равно 0, 1 или 2.
[459] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (A):
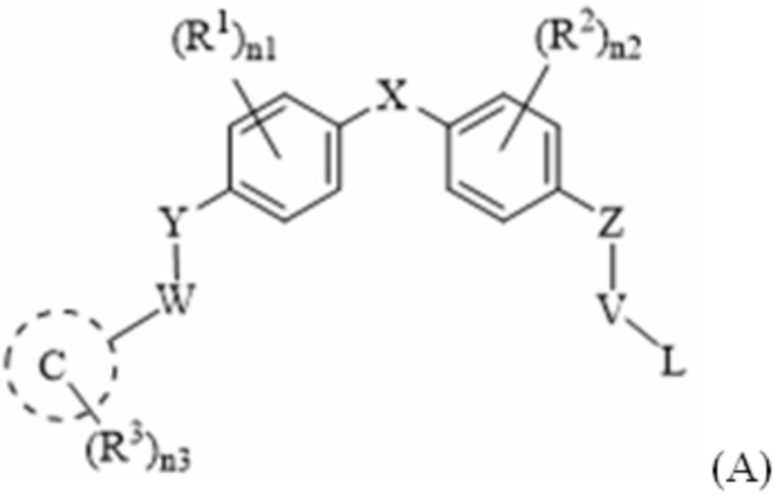
[460] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[461] C представляет собой фенил или 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[462] X представляет собой связь, -(CR5R6)t- или -NR7-;
[463] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[464] Z представляет собой связь, -CH2-, -O- или -NH-;
[465] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[466] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[467] L представляет собой галоген, -NH2 или -CF3;
[468] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[469] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[470] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[471] R7 представляет собой H или C1-C6 алкил;
[472] n1 и n2, каждый независимо, равны 0, 1 или 2;
[473] n3 равно 0, 1, 2, 3, 4 или 5; и
[474] t равно 0, 1 или 2.
[475] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (B)
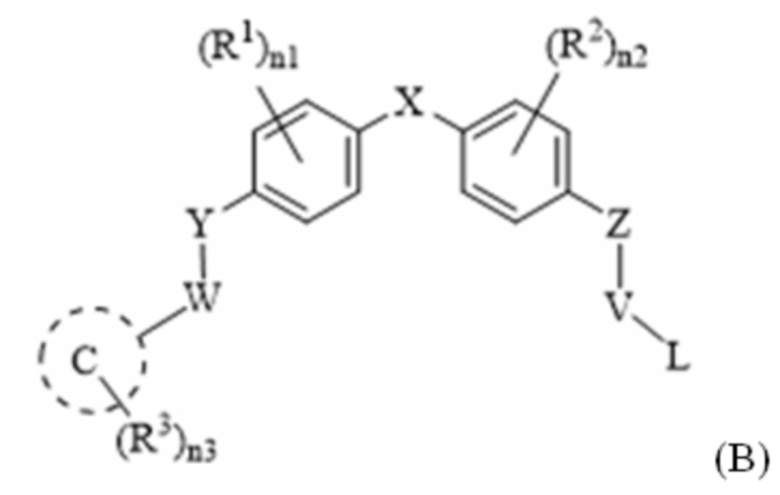
[476] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[477] C представляет собой 5-7-членный насыщенный или частично насыщенный моноциклический гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[478] X представляет собой связь, -(CR5R6)t- или -NR7-;
[479] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[480] Z представляет собой связь, -CH2-, -O- или -NH-;
[481] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[482] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[483] L представляет собой галоген, -NH2 или -CF3;
[484] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[485] R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[486] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[487] R7 представляет собой H или C1-C6 алкил;
[488] R16 представляет собой водород или C1-C3 алкил;
[489] n1 и n2, каждый независимо, равны 0, 1 или 2;
[490] n3 равно 0, 1, 2, 3, 4 или 5; и
[491] t равно 0, 1 или 2.
[492] В одном варианте осуществления соединений формулы (I), (IC), (II), (III), (IIIA), (IV), (V), (VI), (A) или (B) -V-L представляет собой -CH2CH2Cl, -CH2CH2CH2Cl, -CH2CH2NH2 или -CH2CH2CH2NH2.
[493] В одном варианте осуществления соединений формулы (I), (IC), (II), (III), (IIIA), (IV), (V), (VI), (A) или (B) -Y-W- представляет собой связь, -OCH2-, -OCH2CH2-, -OCH(CH3)-, -NH-, -NHCH2-, -NHC(=O)- или -C(=O)NH-.
[494] В одном варианте осуществления соединений формулы (I), (IC), (II), (III), (IIIA), (IV), (V), (VI), (A) или (B) X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[495] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (C):
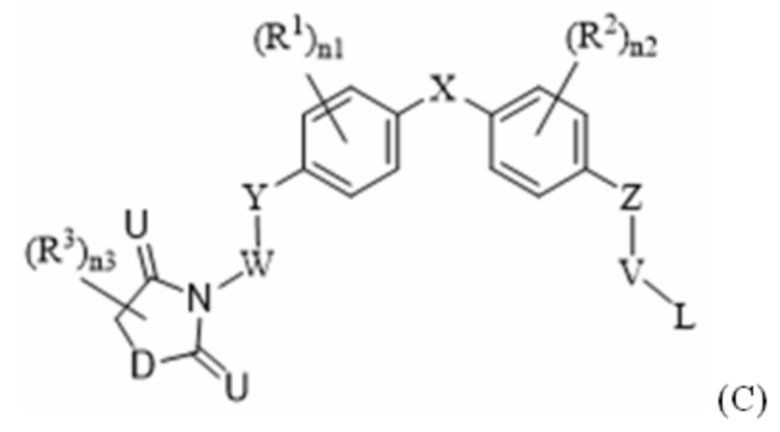
[496] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[497] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[498] X представляет собой связь, (CR5R6)t- или -NR7-;
[499] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[500] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[501] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[502] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[503] L представляет собой галоген, -NH2 или -CF3;
[504] D представляет собой -NH или -NR3;
[505] каждый U независимо представляет собой O, S или NR16;
[506] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[507] R3 выбран из водорода, галогена, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[508] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[509] R7 представляет собой H или C1-C6 алкил;
[510] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[511] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[512] n1 и n2, каждый независимо, равны 0, 1 или 2;
[513] n3 равно 0, 1, 2 или 3; и
[514] t равно 0, 1 или 2.
[515] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (D):
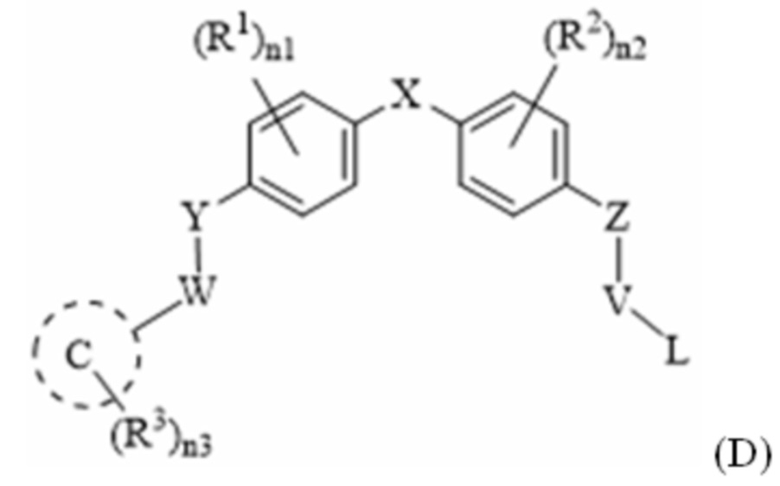
[516] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[517] C представляет собой 5- или 6-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из O, S или N, в качестве члена кольца;
[518] X представляет собой -(CR5R6)t- или -NR7-;
[519] Y представляет собой связь, -CH2-, -O- или -NH-;
[520] Z представляет собой связь, -CH2-, -O- или -NH-;
[521] W представляет собой связь, -CH2- или -C(CH3)H-;
[522] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[523] L представляет собой водород, галоген, -NH2 или -CF3;
[524] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[525] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[526] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[527] R7 представляет собой H или C1-C6 алкил;
[528] n1 и n2, каждый независимо, равны 0, 1 или 2;
[529] n3 равно 0, 1, 2, 3, 4 или 5; и
[530] t равно 0, 1 или 2.
[531] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (E):
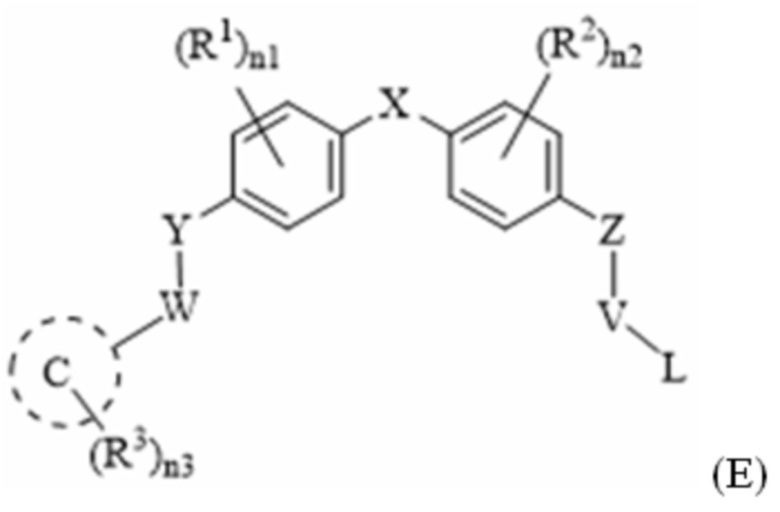
[532] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[533] C представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[534] X представляет собой -(CR5R6)t- или -NR7-;
[535] Y представляет собой связь, -CH2-, -O- или -NH-;
[536] Z представляет собой связь, -CH2-, -O- или -NH-;
[537] W представляет собой связь, -CH2- или -C(CH3)H-;
[538] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[539] L представляет собой водород или галоген;
[540] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[541] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[542] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[543] R7 представляет собой H или C1-C6 алкил;
[544] n1 и n2, каждый независимо, равны 0, 1 или 2;
[545] n3 равно 0, 1 или 2; и
[546] t равно 1 или 2.
[547] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-I):
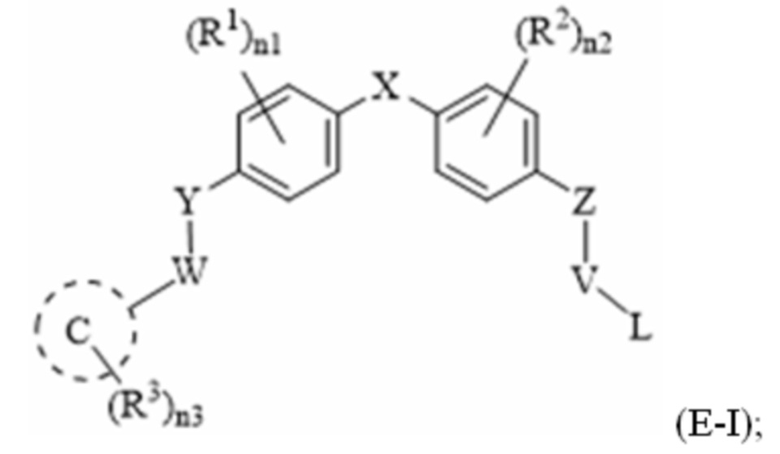
[548] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[549] C представляет собой  .
.  ,
,  ,
, 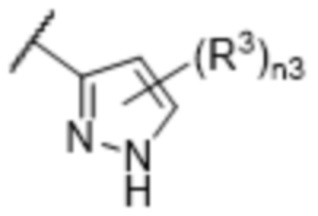 ,
,  ,
,  ,
,  ,
, 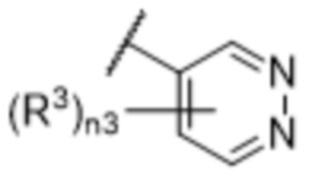 ,
, 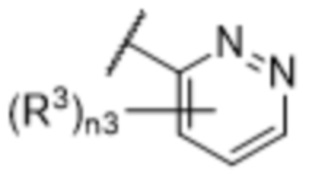 ,
,  ,
,  ,
,  или
или  ;
;
[550] X представляет собой -(CR5R6)t- или -NR7-;
[551] Y представляет собой связь, -CH2-, -O- или -NH-;
[552] Z представляет собой связь, -CH2-, -O- или -NH-;
[553] W представляет собой связь, -CH2- или -C(CH3)H-;
[554] V представляет собой -CH2-, -CH2CH2-, -CH2CH2CH2- или -CH2CHClCH2-;
[555] L представляет собой водород, -OH или галоген;
[556] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[557] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[558] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[559] R7 представляет собой H или C1-C6 алкил;
[560] n1 и n2, каждый независимо, равны 0, 1 или 2;
[561] n3 равно 0, 1 или 2; и
[562] t равно 1 или 2.
[563] В одном варианте осуществления соединений формулы (A)-(C) или (E-1) R3 выбран из водорода, F, Cl, Br, I, -CN, -CF3, -OH, метила, метокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -NHCO(C1-C3 алкила).
[564] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (F):
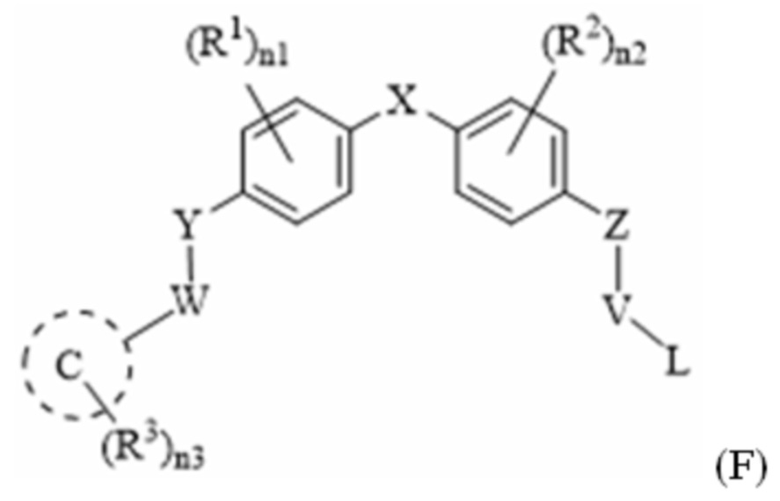
[565] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[566] C представляет собой  .
.  ,
,  ,
,  ,
,
 или
или  ;
;
[567] X представляет собой -(CR5R6)t- или -NR7-;
[568] Y представляет собой -O-;
[569] Z представляет собой -O-;
[570] W представляет собой -CH2- или -C(CH3)H-;
[571] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[572] L представляет собой водород или галоген;
[573] R1 и R2, каждый независимо, представляют собой галоген или -CN;
[574] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[575] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[576] R7 представляет собой H или C1-C6 алкил;
[577] n1 и n2, каждый независимо, равны 0, 1 или 2;
[578] n3 равно 0, 1 или 2; и
[579] t равно 1 или 2
[580] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (G):
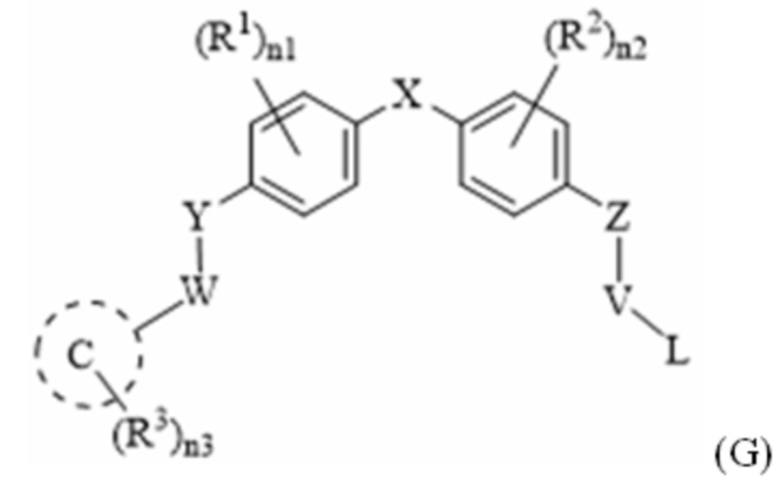
[581] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[582] C представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[583] X представляет собой -(CR5R6)t- или -NR7-;
[584] Y представляет собой -O-;
[585] Z представляет собой -O-;
[586] W представляет собой -CH2- или -C(CH3)H-;
[587] V представляет собой -CH2-, и L представляет собой водород;
[588] или альтернативно, V представляет собой -CH2CH2- или -CH2CH2CH2-, и L представляет собой галоген;
[589] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[590] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[591] R5 и R6, каждый независимо, представляют собой водород или метил;
[592] R7 представляет собой H или C1-C6 алкил;
[593] n1 и n2, каждый независимо, равны 0, 1 или 2;
[594] n3 равно 1 или 2; и
[595] t равно 1.
[596] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру (G-I)

[597] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[598] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[599] X представляет собой -(CR5R6)t-;
[600] Y представляет собой -O-;
[601] Z представляет собой -O-;
[602] W представляет собой -CH2- или -C(CH3)H-;
[603] V представляет собой -CH2CH2- или -CH2CH2CH2-;
[604] L представляет собой галоген;
[605] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[606] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[607] R5 и R6, каждый независимо, представляют собой водород или метил;
[608] n1 и n2, каждый независимо, равны 0, 1 или 2;
[609] n3 равно 1 или 2; и
[610] t равно 1.
[611] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (G-II)
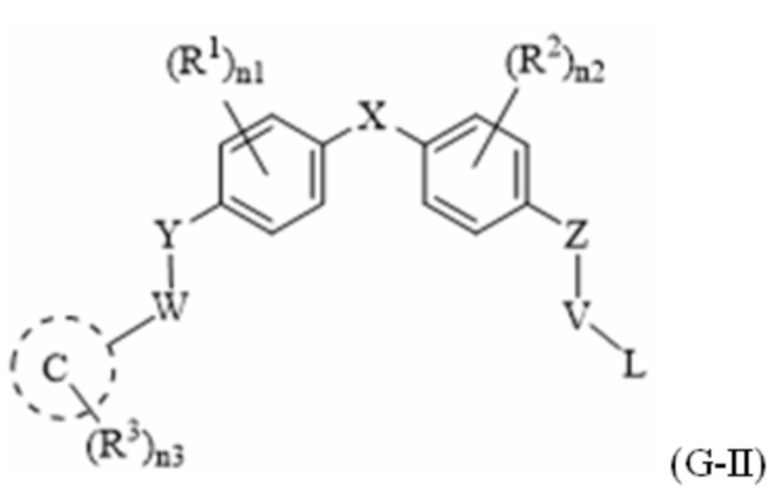
[612] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[613] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ;
;  ,
,  или
или  ;
;
[614] X представляет собой -(CR5R6)t-;
[615] Y представляет собой -O-;
[616] Z представляет собой -O-;
[617] W представляет собой -CH2- или -C(CH3)H-;
[618] V представляет собой -CH2CH2-;
[619] L представляет собой галоген;
[620] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[621] по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[622] R5 и R6, каждый независимо, представляют собой водород или метил;
[623] n1 и n2, каждый независимо, равны 0, 1 или 2;
[624] n3 равно 1 или 2; и
[625] t равно 1.
[626] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложены соединения, содержащие структуру формулы (H):
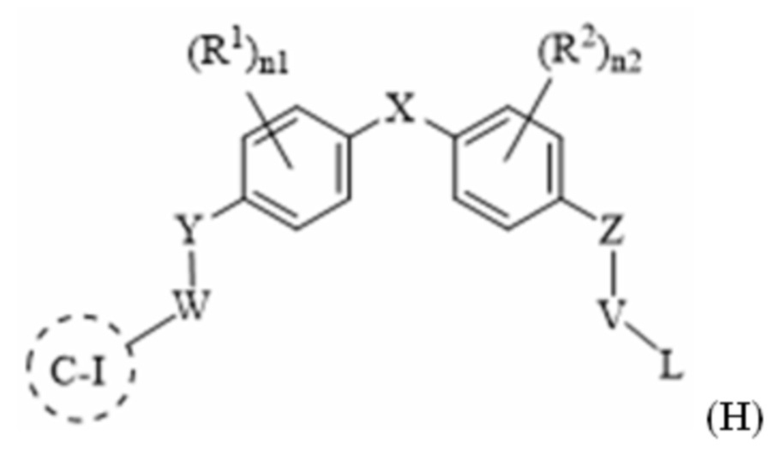
[627] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[628] C-I представляет собой 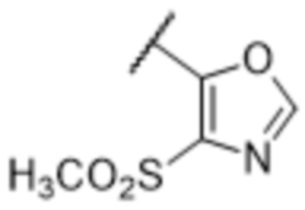 .
. 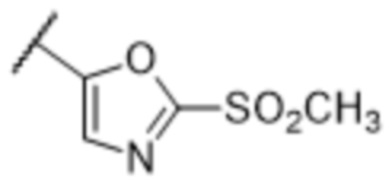 ,
,  ,
, 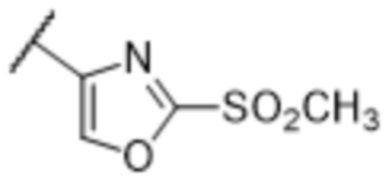 ,
, 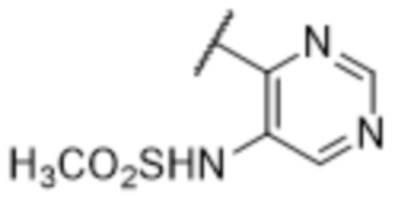 или
или 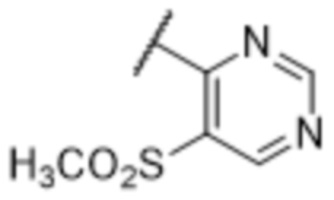 ;
;
[629] X представляет собой -(CR5R6)t- или -NR7-;
[630] Y представляет собой -O-;
[631] Z представляет собой -O-;
[632] W представляет собой -CH2- или -C(CH3)H-;
[633] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[634] L представляет собой галоген;
[635] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[636] R5 и R6, каждый независимо, представляют собой водород или метил;
[637] R7 представляет собой H или C1-C6 алкил;
[638] n1 и n2, каждый независимо, равны 0, 1 или 2; и
[639] t равно 1.
[640] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (H-I):
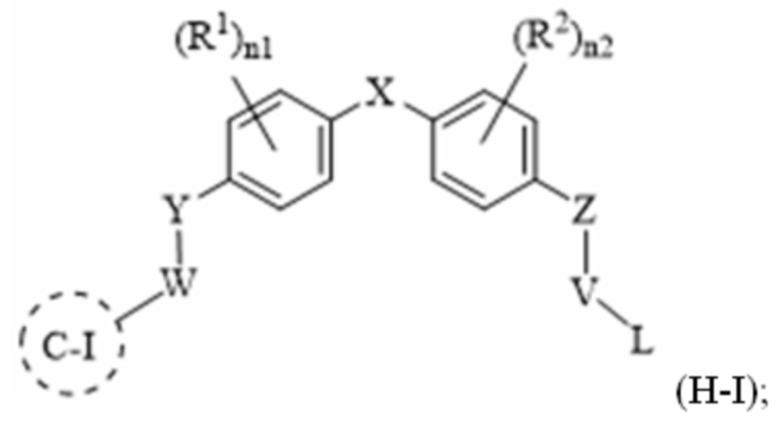
[641] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[642] C-I представляет собой  .
.  ,
,  ,
,  ,
, 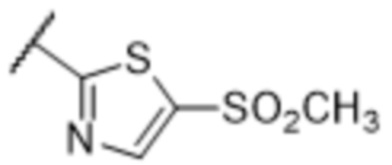 ,
, 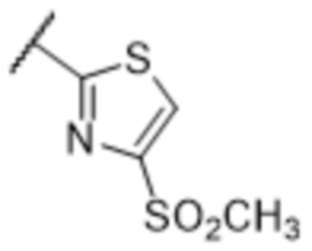 ,
, 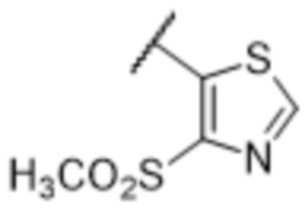 ,
, 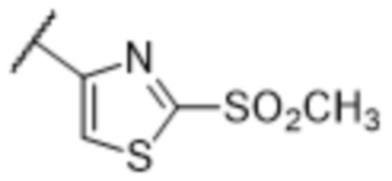 ,
, 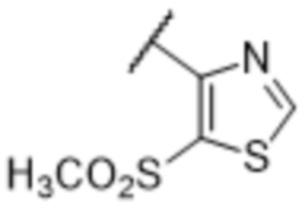 ,
, 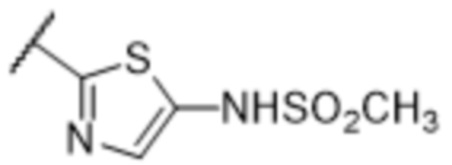 ,
, 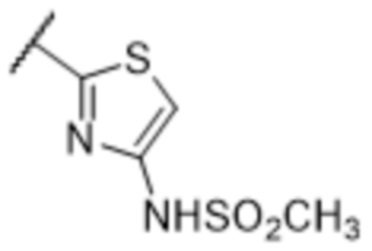 ,
, 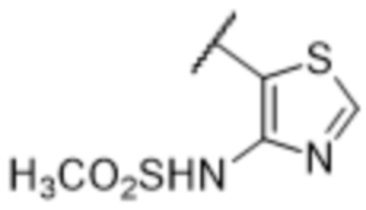 ,
, 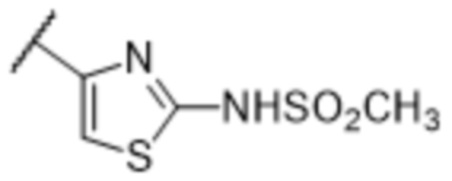 ,
, 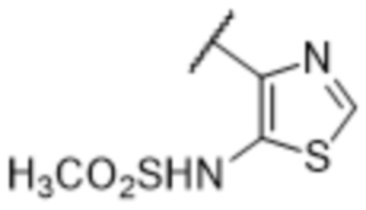 ,
,  ,
, 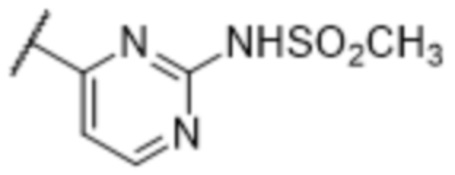 ,
,  или
или  ;
;
[643] X представляет собой -(CR5R6)t-;
[644] Y представляет собой -O-;
[645] Z представляет собой -O-;
[646] W представляет собой -CH2- или -C(CH3)H-;
[647] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[648] L представляет собой галоген;
[649] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[650] R5 и R6, каждый независимо, представляют собой водород или метил;
[651] R7 представляет собой H или C1-C6 алкил;
[652] n1 и n2, каждый независимо, равны 0, 1 или 2; и
[653] t равно 1.
[654] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-II):
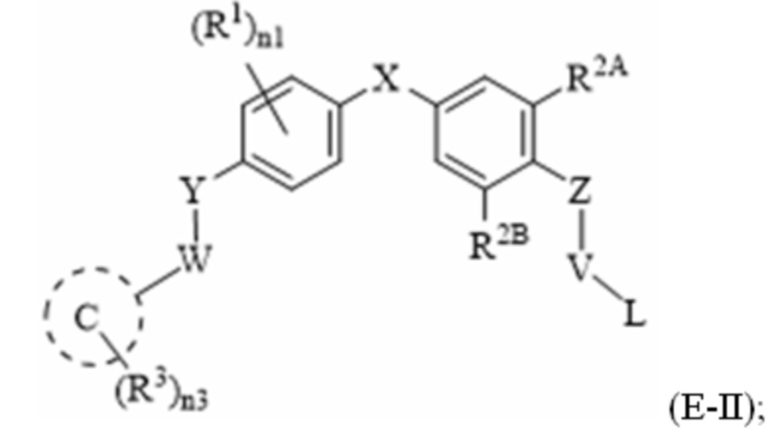
[655] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[656] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[657] X представляет собой -(CR5R6)-;
[658] Y представляет собой связь, -CH2-, -O- или -NH-;
[659] Z представляет собой связь, -CH2-, -O- или -NH-;
[660] W представляет собой связь, -CH2- или -C(CH3)H-;
[661] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[662] L представляет собой галоген;
[663] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[664] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[665] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[666] n1 равно 0, 1 или 2; и
[667] n3 равно 1 или 2;
[668] причем когда C-R3 представляет собой 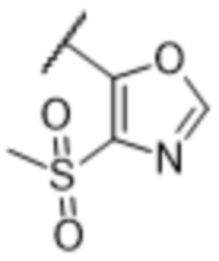 , оба R2A и R2B не представляют собой Cl.
, оба R2A и R2B не представляют собой Cl.
[669] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-III):
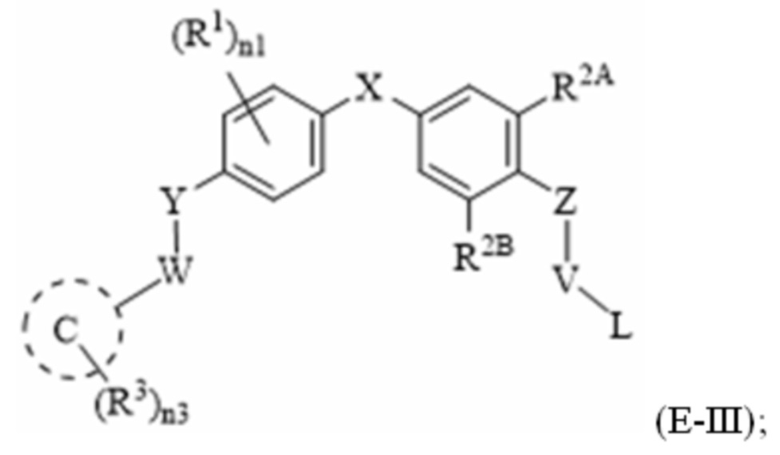
[670] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[671] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[672] X представляет собой -(CR5R6)-;
[673] Y представляет собой связь, -CH2-, -O- или -NH-;
[674] Z представляет собой связь, -CH2-, -O- или -NH-;
[675] W представляет собой связь, -CH2- или -C(CH3)H-;
[676] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[677] L представляет собой галоген;
[678] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[679] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[680] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[681] n1 равно 0, 1 или 2; и
[682] n3 равно 1 или 2;
[683] причем когда C-R3 представляет собой  , и один из R2A и R2B представляет собой Cl, тогда другой из R2A и R2B не представляет собой -CN.
, и один из R2A и R2B представляет собой Cl, тогда другой из R2A и R2B не представляет собой -CN.
[684] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-IV):

[685] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[686] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[687] X представляет собой -(CR5R6)-;
[688] Y представляет собой связь, -CH2-, -O- или -NH-;
[689] Z представляет собой связь, -CH2-, -O- или -NH-;
[690] W представляет собой связь, -CH2- или -C(CH3)H-;
[691] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[692] L представляет собой галоген;
[693] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[694] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[695] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[696] n1 равно 0, 1 или 2; и
[697] n3 равно 1 или 2.
[698] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-V):
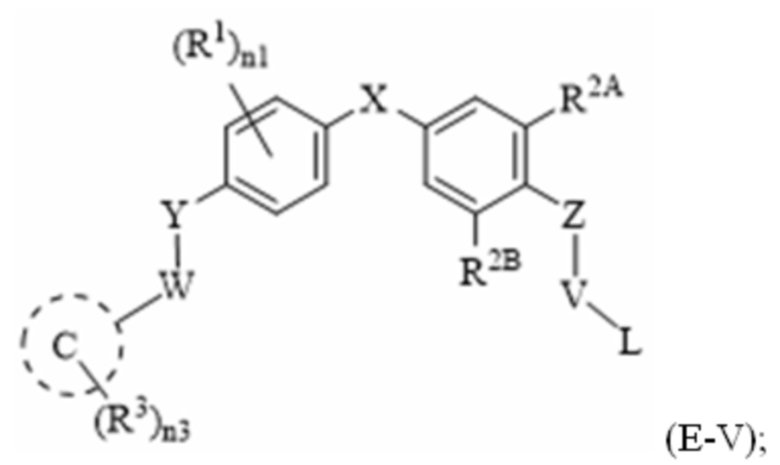
[699] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[700] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[701] X представляет собой -(CR5R6)-;
[702] Y представляет собой связь, -CH2-, -O- или -NH-;
[703] Z представляет собой связь, -CH2-, -O- или -NH-;
[704] W представляет собой связь, -CH2- или -C(CH3)H-;
[705] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[706] L представляет собой галоген;
[707] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[708] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[709] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[710] n1 равно 0, 1 или 2; и
[711] n3 равно 1 или 2;
[712] причем когда C-R3 представляет собой  , оба R2A и R2B не представляют собой Cl.
, оба R2A и R2B не представляют собой Cl.
[713] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-VI):
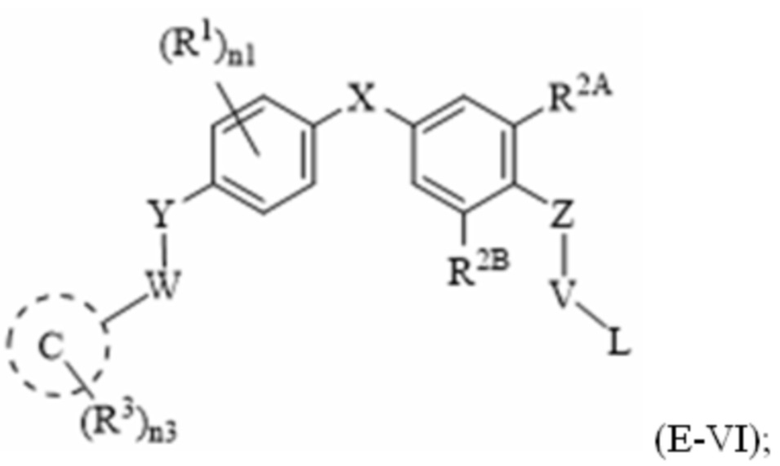
[714] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[715] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[716] X представляет собой -(CR5R6)-;
[717] Y представляет собой связь, -CH2-, -O- или -NH-;
[718] Z представляет собой связь, -CH2-, -O- или -NH-;
[719] W представляет собой связь, -CH2- или -C(CH3)H-;
[720] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[721] L представляет собой галоген;
[722] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[723] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[724] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[725] n1 равно 0, 1 или 2; и
[726] n3 равно 1 или 2;
[727] причем когда C-R3 представляет собой  , и один из R2A и R2B представляет собой Cl, тогда другой из R2A и R2B не представляет собой -CN.
, и один из R2A и R2B представляет собой Cl, тогда другой из R2A и R2B не представляет собой -CN.
[728] В одном варианте осуществления в настоящем раскрытии предложены соединения, содержащие структуру формулы (E-VII):
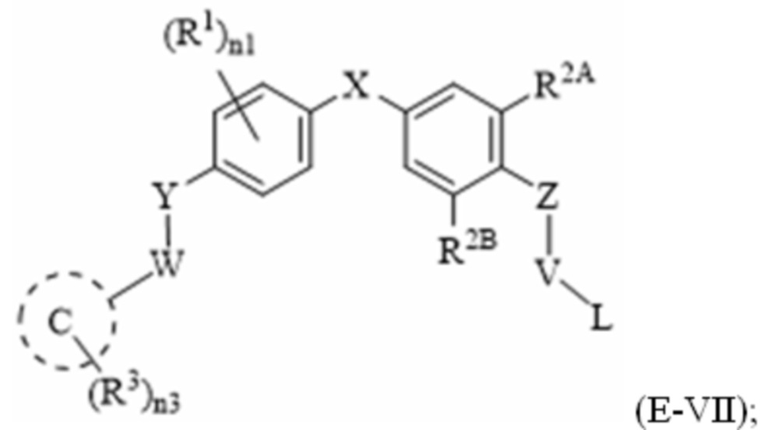
[729] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[730] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[731] X представляет собой -(CR5R6)-;
[732] Y представляет собой связь, -CH2-, -O- или -NH-;
[733] Z представляет собой связь, -CH2-, -O- или -NH-;
[734] W представляет собой связь, -CH2- или -C(CH3)H-;
[735] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[736] L представляет собой галоген;
[737] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[738] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[739] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[740] n1 равно 0, 1 или 2; и
[741] n3 равно 1 или 2.
[742] В одном варианте осуществления соединений формулы (I), (IA), (IB), (IC), (II), (IIA), (IIB), (III), (IIIA), (IV), (V), (VA) или (VI) (обозначенные формулой «(I)-(VI)»), A и B, каждый независимо, представляют собой 5- или 6-членный арил или гетероарил. В одном варианте осуществления настоящего изобретения A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена. В одном варианте осуществления настоящего изобретения каждый A и B представляют собой фенил.
[743] В другом варианте осуществления настоящего изобретения A имеет мета или пара связь с X и Y. В некоторых вариантах осуществления настоящего изобретения B имеет мета или пара связь с X и Z.
[744] В одном варианте осуществления соединений формулы (I)-(VI) A и B представляют собой фенил и имеют одну из связей, как проиллюстрировано:
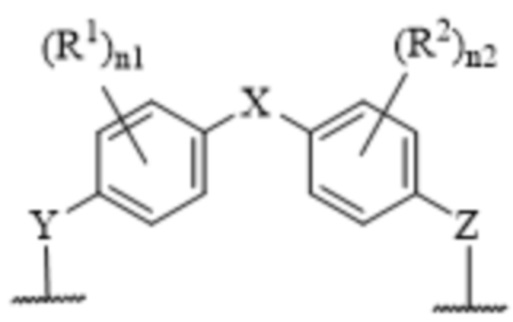 ;
; 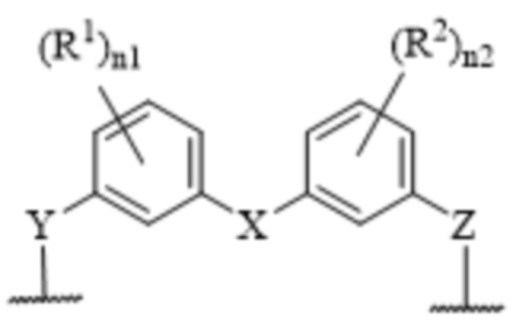 ;
; 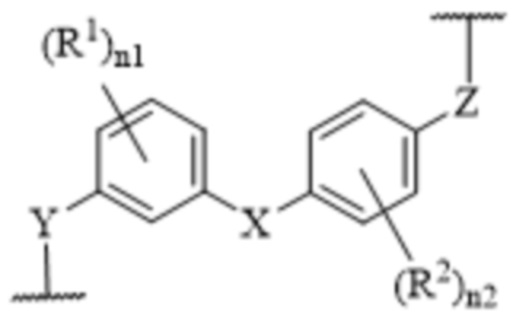 ; или
; или 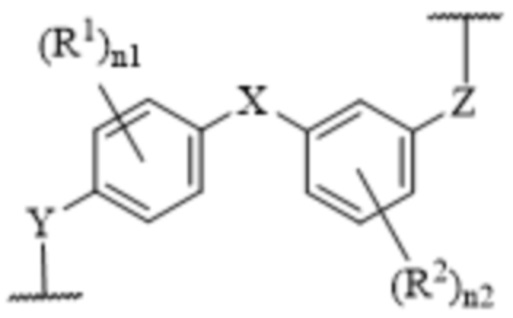 .
.
[745] В одном варианте осуществления соединений формулы (I)-(VA) и (A) (например, формула (I), (IA), (IB), (IC), (II), (IIA), (IIB), (III), (IIIA), (IV), (V) (VA) и (A)), C представляет собой арил или гетероарил. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5-10-членный арил или гетероарил. В другом варианте осуществления настоящего изобретения C представляет собой арил. В некоторых вариантах осуществления настоящего изобретения C представляет собой фенил или нафтил. В другом варианте осуществления настоящего изобретения C представляет собой арил. В некоторых вариантах осуществления настоящего изобретения C представляет собой фенил.
[746] В одном варианте осуществления соединений формулы (I)-(VA) и (A) C представляет собой гетероарил. В одном варианте осуществления настоящего изобретения C представляет собой моноциклический или бициклический гетероарил. В другом варианте осуществления настоящего изобретения C представляет собой моноциклический гетероарил. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5- или 10-членный гетероарил. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5- или 6-членный гетероарил, который необязательно замещен 1, 2, 3, 4 или 5 R3. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5- или 6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N, где гетероарил необязательно замещен 1, 2, 3, 4 или 5 R3. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5- или 6-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из O, S или N, где гетероарил необязательно замещен 1, 2, 3, 4 или 5 R3.
[747] В одном варианте осуществления соединений формулы (I)-(VA), (A) или (D) C представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил или пиримидил, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 R3. В одном варианте осуществления настоящего изобретения C, замещенный (R3)n3, представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил, пиразин, фуран или пиримидил. В одном варианте осуществления настоящего изобретения C представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил, пиразин, фуран или пиримидил, каждый из которых замещен 1, 2, 3, 4 или 5 R3.
[748] В одном варианте осуществления соединений формулы (I)-(VA), (A) или (D) C выбран из
[749]  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил. В одном варианте осуществления соединений формулы (I)-(VA), (A) или (D) C выбран из
, где R3a представляет собой C1-C3 алкил. В одном варианте осуществления соединений формулы (I)-(VA), (A) или (D) C выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 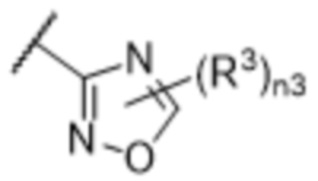 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[750] В одном варианте осуществления соединений формулы (I)-(VA), (A) или (D) C представляет собой
 .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  .
.
[751] В одном варианте осуществления настоящего изобретения C представляет собой 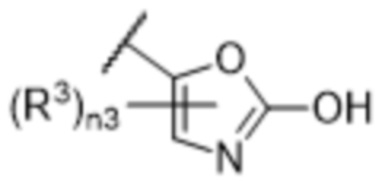 или находится в его таутомерной форме
или находится в его таутомерной форме 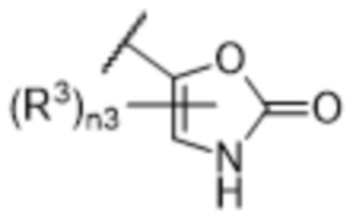 . В одном варианте осуществления настоящего изобретения C представляет собой
. В одном варианте осуществления настоящего изобретения C представляет собой 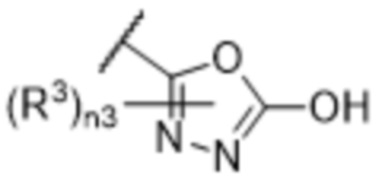 или находится в его таутомерной форме
или находится в его таутомерной форме 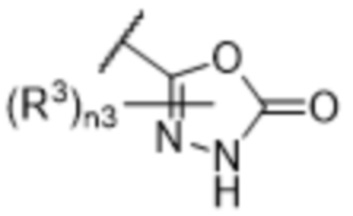 .
.
[752] В одном варианте осуществления соединений формулы (I)-(IV) C представляет собой гетероциклил. В одном варианте осуществления настоящего изобретения C представляет собой насыщенный или частично насыщенный гетероцикл. В некоторых вариантах осуществления настоящего изобретения C является моноциклическим или бициклическим. В некоторых вариантах осуществления настоящего изобретения C представляет собой 5-7-членный гетероциклил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[753] В одном варианте осуществления соединений формулы (I)-(VA), (B) и (C) C представляет собой имидазолидин, имидазолидин-дион или дигидрооксазол. В одном варианте осуществления настоящего изобретения C выбран из
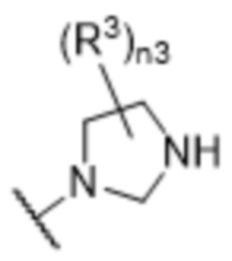 ,
, 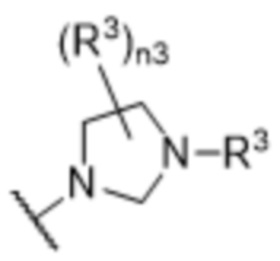 ,
, 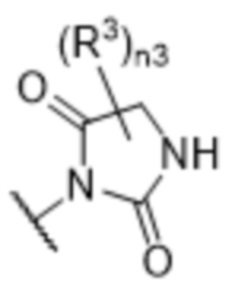 или
или 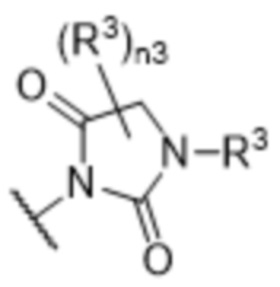 .
.
[754] В одном варианте осуществления соединений формулы (I)-(VA), (B) и (C) C представляет собой 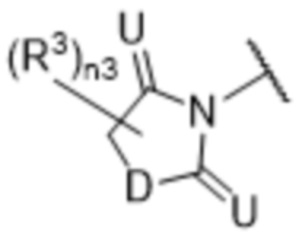 ; D представляет собой -O-, -NH- или -NR3-; и каждый U независимо представляет собой O, S или NR16. В одном варианте осуществления настоящего изобретения D представляет собой -NH- или -NR3-. В некоторых вариантах осуществления настоящего изобретения по меньшей мере один U представляет собой O. В другом варианте осуществления настоящего изобретения каждый U представляет собой O. В некоторых вариантах осуществления настоящего изобретения по меньшей мере один R3 представляет собой -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
; D представляет собой -O-, -NH- или -NR3-; и каждый U независимо представляет собой O, S или NR16. В одном варианте осуществления настоящего изобретения D представляет собой -NH- или -NR3-. В некоторых вариантах осуществления настоящего изобретения по меньшей мере один U представляет собой O. В другом варианте осуществления настоящего изобретения каждый U представляет собой O. В некоторых вариантах осуществления настоящего изобретения по меньшей мере один R3 представляет собой -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
[755] В одном варианте осуществления соединений формулы (I)-(VA) C представляет собой арил. В некоторых вариантах осуществления настоящего изобретения C представляет собой фенил или нафтил. В одном варианте осуществления соединений формулы (I)-(VA) или (A) C представляет собой фенил.
[756] В одном варианте осуществления соединений формулы (I)-(VI) C представляет собой бициклический гетероарил или гетероциклил. В одном варианте осуществления настоящего изобретения C представляет собой 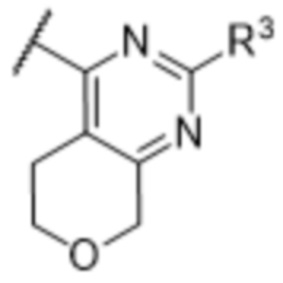 ,
, 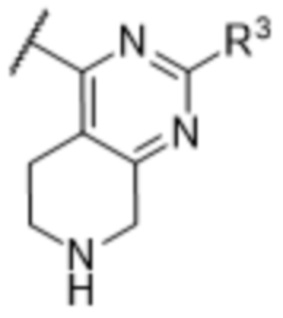 ,
, 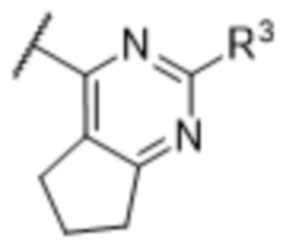 или
или 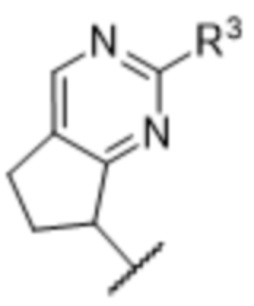 .
.
[757] В одном варианте осуществления соединений формулы (I) Z представляет собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-. В одном варианте осуществления настоящего изобретения Z представляет собой -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-. В некоторых вариантах осуществления настоящего изобретения Z представляет собой -C(=O)-.
[758] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-. В одном варианте осуществления настоящего изобретения Z представляет собой -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-. В некоторых вариантах осуществления настоящего изобретения Z представляет собой связь, -CH2-, -O- или -NCH3-. В некоторых вариантах осуществления настоящего изобретения Z представляет собой связь, -CH2-, -O- или -NH-. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) Z представляет собой -O-. В контексте данного документа «соединения формулы (I)-(IV) и (A)-(H-I)» относятся к соединениям формулы (I), (IA), (IB), (IC), (II), (IIA), (IIIA), (IIB), (III), (IV), (IVA), (V), (VA), (VI), (A), (A-I), (B)-(D), (E), (E-I)-(E-VII), (F), (G), (G-I), (G-II), (H) и (H-I).
[759] В одном варианте осуществления соединений формулы (I) Y представляет собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-. В одном варианте осуществления настоящего изобретения Y представляет собой -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-. В некоторых вариантах осуществления настоящего изобретения Y представляет собой -C(=O)-.
[760] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-. В одном варианте осуществления настоящего изобретения Y представляет собой -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-. В некоторых вариантах осуществления настоящего изобретения Y представляет собой связь, -CH2-, -O- или -NCH3-. В некоторых вариантах осуществления настоящего изобретения Y представляет собой связь, -CH2-, -O- или -NH-. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) Y представляет собой -O-.
[761] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) V представляет собой связь, -(CR8aR9a)m- или -C(=O)-. В некоторых вариантах осуществления настоящего изобретения V представляет собой связь или -(CR8aR9a)m-.
[762] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) V представляет собой -(CR8aR9a)m-, где m равно 1, 2 или 3. В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) V представляет собой -(CR8aR9a)m-, где R8a и R8b, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C1-C3 алкокси, -NR13R14, необязательно замещенный -(C1-C3 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C3 алкил)-NR14COR16, -CONR14R15 или необязательно замещенный -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил. В одном варианте осуществления настоящего изобретения V представляет собой -(CR8aR9a)m-, где R8a и R8b, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b при одном и том же атоме углерода или на другом атоме углерода, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил.
[763] В одном варианте осуществления соединений формулы (I)-(IIB) и (VA) V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-.
[764] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-, каждый необязательно замещен одним или более -OH, галогенами или C1-C3 алкилами. В другом варианте осуществления настоящего изобретения V представляет собой -CH2-, -CH2CH2-, -CH2CH(OH)CH2- или -CH2CH2CH2-. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) V представляет собой -CH2- или -CH2CH2-.
[765] В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(D) V представляет собой -CH2-, и L представляет собой галоген, -NH2 или -CF3; или V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2.
[766] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) L представляет собой водород, галоген, -CF2H, -CF3, -CN, -O(C1-C3 алкил), -NR11R12 или -CONR11R12. В одном варианте осуществления настоящего изобретения L представляет собой водород, галоген, -CF2H, -CF3, -CN, -O(C1-C3 алкил), -NH2, -NH(C1-C3 алкил), -N(C1-C3 алкил)2, -CONH2, -CONH(C1-C3 алкил) или -CON(C1-C3 алкил)2. В некоторых вариантах осуществления настоящего изобретения L представляет собой водород, галоген, -CF3 или -NH2.
[767] В некоторых вариантах осуществления соединений формулы (IC) и (IIIA) L представляет собой галоген, -CCl3, -CCl2, -CF3 или -NH2. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) L представляет собой галоген, -CF3 или -NH2. В одном варианте осуществления настоящего изобретения L представляет собой водород или галоген. В одном варианте осуществления настоящего изобретения L представляет собой галоген. В другом варианте осуществления настоящего изобретения L представляет собой Cl или Br. В одном варианте осуществления настоящего изобретения L представляет собой Cl.
[768] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) W представляет собой связь. В одном варианте осуществления настоящего изобретения W представляет собой -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-. В одном варианте осуществления настоящего изобретения W представляет собой -(CR8aR9a)m-, где m равно 1, 2 или 3. В некоторых вариантах осуществления настоящего изобретения W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-, где R7 представляет собой H или C1-C6 алкил. В некоторых вариантах осуществления настоящего изобретения W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-, где R7 представляет собой H или C1-C3 алкил. В одном варианте осуществления настоящего изобретения W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -NHCO-, -N(C1-C3 алкил)CO-, -CONH- или -CON(C1-C3 алкил)-. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(E-VI) W представляет собой связь, -CH2- или -C(CH3)H-. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) W представляет собой -CH2- или -C(CH3)H-.
[769] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) -Y-W- представляет собой связь, -OCH2-, -OCH2CH2-, -OCH(CH3)-, -NH-, -NHCH2-, -NHC(=O)- или -C(=O)NH-. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) -Y-W- представляет собой -OCH2-, -OCH2CH2- или -OCH(CH3)-.
[770] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C)
[771] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-; и
[772] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-.
[773] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C)
[774] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[775] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-; и
[776] L представляет собой галоген, -NH2 или -CF3.
[777] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) -Z-V-L представляет собой -Z-CH2CH2Cl, -Z-CH2CH2CH2Cl, -Z-CH2CH2NH2 или -Z-CH2CH2CH2NH2, где Z представляет собой связь, -O-, -NH- или -N(COCH3)-. В одном варианте осуществления настоящего изобретения -Z-V-L представляет собой -OCH3.
[778] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) -Z-V-L представляет собой -O-CH2CH2Cl или -O-CH2CH2CH2Cl.
[779] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) -V-L представляет собой -CH2CH2Cl, -CH2CH2CH2Cl, -CH2CH2NH2 или -CH2CH2CH2NH2. В одном варианте осуществления настоящего изобретения -V-L представляет собой -CH3.
[780] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-. В одном варианте осуществления настоящего изобретения X представляет собой связь -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-, где R7 представляет собой H или C1-C6 алкил. В некоторых вариантах осуществления настоящего изобретения X представляет собой связь, -(CR5R6)t- или -NR7-. В некоторых вариантах осуществления настоящего изобретения X представляет собой связь или -(CR5R6)t-. В некоторых вариантах осуществления настоящего изобретения X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2-, -CH2CH2-, -NH- или -N(C1-C6 алкил)-. В некоторых вариантах осуществления настоящего изобретения X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2-, -CH2CH2-, -NH-, -N(CH3)-, -N(CH2CH3)-, -N(iPr)- или -N(tBu)-. В некоторых вариантах осуществления настоящего изобретения X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[781] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) X представляет собой -CH2-, -C(CH3)H- или -C(CH3)2-. В одном варианте осуществления настоящего изобретения X представляет собой -C(CH3)2-.
[782] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R1 и R2, каждый независимо, представляют собой галоген, -CN, -CF3, -OH, C1-C3 алкил, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2R16, -(C1-C3 алкил)-SO2R16, 3-7-членный карбоциклил, 3-7-членный гетероциклил, фенил или 5-6-членный гетероарил.
[783] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C3 алкил, C1-C3 алкокси, необязательно замещенный -(C1-C3 алкил)-(C1-C3 алкокси), необязательно замещенный -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C3 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C3 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C3 алкил)-SO2NR14R15, -SO2R16 или необязательно замещенный -(C1-C3 алкил)-SO2R16. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, C1-C3 алкил, C1-C3 алкокси,-(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2R16 или -(C1-C3 алкил)-SO2R16.
[784] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, C1-C3 алкил или -CONR14R15. В некоторых вариантах осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, метил, метокси или -CONH2. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой водород, Cl, -CN, -CF3, -OH, метил, метокси или -CONH2. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH или метил. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой Cl, -CN, -CF3, -OH, метил, метокси или -CONH2. В одном варианте осуществления соединений формулы (I)-(VI) R1 и R2, каждый независимо, представляют собой галоген, -CN, -CF3, -OH или метил.
[785] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(E-I) R1 и R2, каждый, представляют собой галоген, метил, -CF3 или -CN. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(F) R1 и R2, каждый, представляют собой галоген или -CN. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I), по меньшей мере один из R1 и R2 представляет собой Cl или -CN. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I), по меньшей мере два из R1 и R2, каждый независимо, представляют собой Cl или -CN. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) каждый R1 и R2 представляют собой Cl или -CN.
[786] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C), R1 и R2, каждый независимо, представляют собой необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В одном варианте осуществления настоящего изобретения R1 и R2, каждый независимо, представляют собой 3-7-членныйкарбоциклил, 3-7-членныйгетероциклил, фенил или 5-6-членный гетероарил.
[787] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R1 имеет одну связь, как проиллюстрировано ниже, в отношении X и Y:
 ,
, 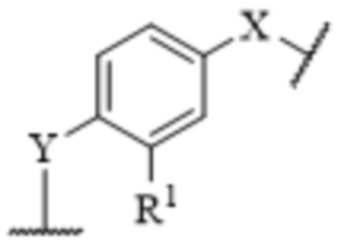 ,
,  ,
, 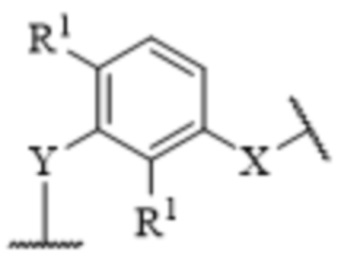 ,
, 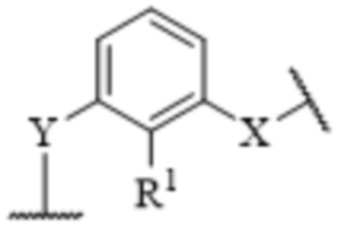 или
или 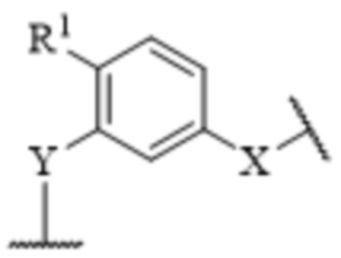 ,
,
[788] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R2 имеет одну связь, как проиллюстрировано ниже, в отношении X и Z:
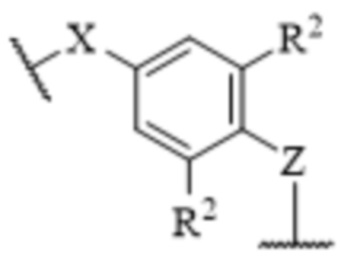 ,
, 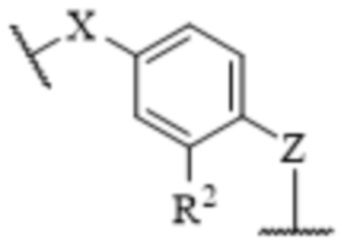 ,
, 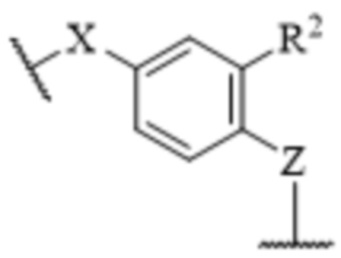 ,
, 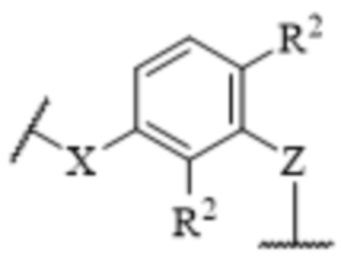 ,
, 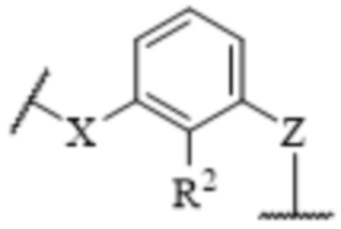 или
или 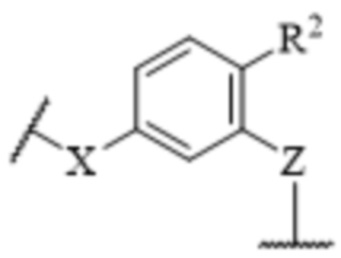 .
.
[789] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) n1 равно 0, 1 или 2. В некоторых вариантах осуществления настоящего изобретения n1 равно 0 или 1. В другом варианте осуществления настоящего изобретения n1 равно 0. В некоторых вариантах осуществления настоящего изобретения n1 равно 1. В одном варианте осуществления настоящего изобретения сумма n1 и n2 равна 0, 1, 2, 3 или 4. В некоторых вариантах осуществления настоящего изобретения сумма n1 и n2 равна 1, 2, 3 или 4. В одном варианте осуществления настоящего изобретения сумма n1 и n2 равна 2.
[790] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) n2 равно 0, 1 или 2. В некоторых вариантах осуществления настоящего изобретения n2 равно 1 или 2. В другом варианте осуществления настоящего изобретения n2 равно 0. В некоторых вариантах осуществления настоящего изобретения n2 равно 1. В некоторых вариантах осуществления настоящего изобретения n2 равно 2.
[791] В некоторых вариантах осуществления соединений (I)-(VI), (A), (A-I), (B) и (C) n3 равно 1, 2, 3, 4 или 5. В некоторых вариантах осуществления настоящего изобретения n3 равно 1, 2, 3 или 4. В одном варианте осуществления настоящего изобретения n3 равно 1, 2 или 3. В одном варианте осуществления настоящего изобретения n3 равно 1 или 2.
[792] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенного C1-C6 алкила, необязательно замещенного C2-C6 алкенила, необязательно замещенного C2-C6 алкинила, необязательно замещенного C1-C6 алкокси, необязательно замещенного -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенного -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенного -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенного -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенного -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенного -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенного -(C1-C6 алкил)-SO2NR14R15, необязательно замещенного -SO2R16, необязательно замещенного -(C1-C6 алкил)-SO2R16, необязательно замещенного карбоциклила, необязательно замещенного гетероциклила, необязательно замещенного арила или необязательно замещенного гетероарила. В некоторых вариантах осуществления настоящего изобретения R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенного C1-C6 алкила, необязательно замещенного C2-C6 алкенила, необязательно замещенного C2-C6 алкинила, необязательно замещенного C1-C6 алкокси, необязательно замещенного -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенного -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенного -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенного -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенного -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенного -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенного -(C1-C6 алкил)-SO2NR14R15, необязательно замещенного -SO2R16 или необязательно замещенного -(C1-C6 алкил)-SO2R16. В другом варианте осуществления настоящего изобретения R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, необязательно замещенный C1-C3 алкокси, необязательно замещенный -(C1-C3 алкил)-(C1-C3 алкокси), необязательно замещенный -(C1-C3 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C3 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C3 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C3 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C3 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C3 алкил)-SO2R16.
[793] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R3 выбран из -NR14SO2R16, необязательно замещенного -(C1-C6 алкил)NR14SO2R16 или необязательно замещенного -SO2R16; где R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил. В одном варианте осуществления настоящего изобретения R3 выбран из -NR14SO2R16, -(C1-C6 алкил)NR14SO2R16 или -SO2R16; где R16 представляет собой водород, C1-C3 алкил, -(C1-C3 алкил)-NH2, C3-C6 циклоалкил или фенил.
[794] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO(C1-C3 алкила), -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила). В некоторых вариантах осуществления настоящего изобретения R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила). В некоторых вариантах осуществления настоящего изобретения R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила). В одном варианте осуществления настоящего изобретения R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, метила, -SCH3, -SO2CH3, -NHSO2CH3, -NHSO2CH2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3. В одном варианте осуществления настоящего изобретения R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, метила, -SCH3, -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3. В некоторых вариантах осуществления настоящего изобретения R3 выбран из F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила). В некоторых вариантах осуществления настоящего изобретения R3 выбран из F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила). В одном варианте осуществления настоящего изобретения R3 выбран из F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, метил, -SCH3, -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3. В другом варианте осуществления настоящего изобретения R3 представляет собой -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3. В одном варианте осуществления настоящего изобретения R3 представляют собой оксо, =S, =NR16, C1-C3 алкил, -SO2(C1-C3 алкил) или -NHSO2(C1-C3 алкил). В одном варианте осуществления настоящего изобретения по меньшей мере один из R3 представляют собой оксо, =S или =NR16. В одном варианте осуществления настоящего изобретения по меньшей мере один из R3 представляют собой оксо, =S или =NR16, где R16 представляет собой H или C1-C3 алкил.
[795] В одном варианте осуществления настоящего изобретения соединений формулы (I)-(VI) и (A)-(E-VII) R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила). В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(E-VII) R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[796] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) каждый R3 при sp3 углерода выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO(C1-C3 алкила), -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила). Когда R3 при sp3 углероде представляют собой оксо, =S или =NR16, углерод становится sp2.
[797] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) каждый R3 при sp2 углерода выбран из водорода, галогена, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO(C1-C3 алкила), -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила).
[798] В одном варианте осуществления соединений формулы (I)-(VI), (A), (A-I), (B) и (C) каждый R3 при атоме углерода выбран из C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -(C1-C3 алкил)-NR13R14, -(C1-C3 алкил)NR14SO2R16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -(C1-C3 алкил)-SO2NR14R15 или -(C1-C6 алкил)-SO2(C1-C3 алкила).
[799] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(G-II) по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила). В одном варианте осуществления настоящего изобретения по меньшей мере один R3 выбран из -NHSO2CH3, -NHSO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, C1-C3 алкила, C1-C3 алкокси, -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[800] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(E-II) R3 не представляет собой водород.
[801] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(G-II) по меньшей мере один R3 представляет собой -SO2CH3, -NHSO2CH3, -NCH3SO2CH3, -NHSO2CH2CH3 или -N(CH3)SO2CH2CH3. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(G-II) по меньшей мере один R3 представляет собой -SO2CH3, -NHSO2CH3 или -NCH3SO2CH3.
[802] В одном варианте осуществления соединений формулы (I), (IA), (IB) или (IC) R3 представляет собой гетероциклил. В одном варианте осуществления настоящего изобретения R3 представляет собой гетероциклил выбран из 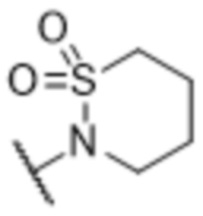 или
или 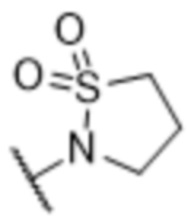 .
.
[803] В одном варианте осуществления соединений формулы (IB), (IC), (IIA) или (IIB) R3 представляет собой -NR14SO2R16, где R14 и R16 вместе образуют 5- или 6-членное кольцо, содержащее атомы азота и серы.
[804] В одном варианте осуществления соединений формулы (I), (IA), (IB) или (IC) R3 представляет собой -NR14SO2R16, где R16 представляет собой необязательно замещенный C1-C6 алкил. В одном варианте осуществления настоящего изобретения R3 представляет собой -NR14SO2R16, где R16 представляет собой C1-C6 алкил, необязательно замещенный одной или более группами, выбранными из галогена, -CN, -CF3, -OH, C1-C3 алкила, C1-C3 алкокси, -NH2, -NH(C1-C3 алкила), -N(C1-C3 алкила)2, -SCH3. В одном варианте осуществления настоящего изобретения R3 представляет собой -NR14SO2R16, где R16 представляет собой C1-C3 алкил, замещенный -NH2.
[805] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил. В некоторых вариантах осуществления настоящего изобретения R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил. В одном варианте осуществления настоящего изобретения R5 и R6 представляют собой водород, галоген, -OH или C1-C3 алкил. В одном варианте осуществления настоящего изобретения R5 и R6, каждый независимо, представляют собой водород, F, -OH, или C1-C3 алкил. В одном варианте осуществления настоящего изобретения каждый R5 и R6 независимо представляют собой водород, F, -OH или метил. В одном варианте осуществления настоящего изобретения каждый R5 и R6 представляют собой H. В одном варианте осуществления настоящего изобретения каждый R5 и R6 представляют собой метил. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) каждый R5 и R6 представляют собой H или метил.
[806] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R7 представляет собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, карбоциклил, гетероциклил, арил или гетероарил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, карбоциклил, гетероциклил, арил или гетероарил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород или C1-C6 алкил. В некоторых вариантах осуществления настоящего изобретения R7 представляет собой водород или C1-C4 алкил. В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) R7 представляет собой водород или C1-C3 алкил.
[807] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R8a и R9a, каждый независимо, представляют собой водород, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил или R8a и R9a, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил. В некоторых вариантах осуществления настоящего изобретения R8a и R8b, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил. В одном варианте осуществления настоящего изобретения R8a и R9a, каждый независимо, представляют собой водород, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15. В одном варианте осуществления соединений формулы (IB), (IC), (III) или (IIIA) R8a и R9a не представляют собой -OH. В одном варианте осуществления настоящего изобретения R8a и R9a не представляют собой -OH.
[808] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил. В одном варианте осуществления настоящего изобретения R7 и R8a, взятые вместе, образуют необязательно замещенный 3-7-членный гетероцикл.
[809] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил.
[810] В одном варианте осуществления соединений формулы (I)-(IIB) R10 представляет собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R10 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R10 представляет собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, карбоциклил, гетероциклил, арил или гетероарил. В некоторых вариантах осуществления настоящего изобретения R10 представляет собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил. В некоторых вариантах осуществления настоящего изобретения R10 представляет собой водород или C1-C3 алкил.
[811] В одном варианте осуществления соединений формулы (I)-(IIB), R11 и R12, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В одном варианте осуществления настоящего изобретения R11 и R12, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил или необязательно замещенный C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения. R11 и R12, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения. R11 и R12, каждый независимо, представляют собой водород или C1-C3 алкил.
[812] В одном варианте осуществления соединений формулы (I)-(IIB) R11 и R12, взятые вместе, образуют необязательно замещенный гетероциклил. В одном варианте осуществления настоящего изобретения R11 и R12, взятые вместе, образуют необязательно замещенный 3-7-членный гетероциклил. В другом варианте осуществления настоящего изобретения R11 и R12, взятые вместе, образуют 3-7-членный гетероциклил.
[813] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R13 и R14, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В одном варианте осуществления настоящего изобретения R13 и R14, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил или необязательно замещенный C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения R13 и R14, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения R13 и R14, каждый независимо, представляют собой водород или C1-C3 алкил.
[814] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R15 представляет собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В одном варианте осуществления настоящего изобретения R15 представляет собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил или необязательно замещенный C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения R15 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил. В некоторых вариантах осуществления настоящего изобретения R15 представляет собой водород или C1-C3 алкил.
[815] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C), R14 и R15, взятые вместе, образуют необязательно замещенный гетероциклил. В одном варианте осуществления настоящего изобретения R14 и R15, взятые вместе, образуют необязательно замещенный 3-7-членный гетероциклил. В другом варианте осуществления настоящего изобретения R14 и R15, взятые вместе, образуют 3-7-членный гетероциклил.
[816] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) R16 представляет собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил. В некоторых вариантах осуществления настоящего изобретения R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, карбоциклил, гетероциклил, арил или гетероарил. В некоторых вариантах осуществления настоящего изобретения R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил. В некоторых вариантах осуществления настоящего изобретения R16 представляет собой водород или C1-C3 алкил.
[817] В одном варианте осуществления соединений формулы (I)-(IIIA) m равно 1 или 2.
[818] В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(F) t равно 1 или 2. В одном варианте осуществления соединений формулы (I)-(VI) и (A)-(H-I) t равно 1.
[819] В одном варианте осуществления соединений формулы (I)-(VI), (A), (B) и (C) необязательный заместитель выбран из галогена, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO(C1-C3 алкила), -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила). В другом варианте осуществления настоящего изобретения необязательный заместитель выбран из галогена, -CN, -CF3, -OH, C1-C3 алкил, C1-C3 алкокси, -NH2, -SCH3, -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
[820] В одном варианте осуществления соединений формулы (I)-(VI) каждый A и B представляют собой моноциклическое кольцо.
[821] В одном варианте осуществления соединений формулы (I)-(VI) B представляет собой фенил, пиридил или пиримидил.
[822] В одном варианте осуществления соединений формулы (I)-(IIIA) оба Z и V не представляют собой связь.
[823] В одном варианте осуществления соединений формулы (I)-(VI), (A)-(C) оба Y и W не представляют собой связь.
[824] В одном варианте осуществления соединений формулы (I)-(VI) C представляет собой 4-10-членное кольцо.
[825] В одном варианте осуществления соединений формулы (D)-(H-I) X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-. В одном варианте осуществления настоящего изобретения X представляет собой -CH2-, -C(CH3)H- или -C(CH3)2-. В некоторых вариантах осуществления настоящего изобретения X представляет собой -C(CH3)2-.
[826] В одном варианте осуществления соединений формулы (D)-(H) X представляет собой -NR7-. В одном варианте осуществления настоящего изобретения X представляет собой -NH-, -N(CH3)-, -N(CH2CH3)-, -N(iPr)- или -N(tBu)-.
[827] В одном варианте осуществления соединений формулы (D)-(H-I) Y представляет собой -O-. В одном варианте осуществления соединений формулы (D)-(H-I) Z представляет собой -O-. В одном варианте осуществления соединений формулы (D)-(H-I) каждый Y и Z представляют собой -O-.
[828] В одном варианте осуществления соединений формулы (D)-(H-I) -V-L представляет собой CH2CH2Cl, -CH2CH2CH2Cl или -CH3. В некоторых вариантах осуществления настоящего изобретения -V-L представляет собой CH2CH2Cl или -CH2CH2CH2Cl.
[829] В одном варианте осуществления соединений формулы (D)-(H-I) n1 равно 0.
[830] В одном варианте осуществления соединений формулы (D)-(H-I) n2 равно 0, 1 или 2. В некоторых вариантах осуществления настоящего изобретения n2 равно 2. В некоторых вариантах осуществления настоящего изобретения n2 равно 2 и каждый R2 находится в орто-положении к Z. В другом варианте осуществления настоящего изобретения n2 равно 2 и R2 каждый находится в орто-положении к Z, где R2 представляет собой галоген или -CN.
[831] В одном варианте осуществления соединения формулы (I)-(VI) и (A)-(H-I) соединение может быть стереоизомером. Например, если X представляет собой -(CR5R6)- и R5 и R6 являются разными, углерод, присоединенный к R5 и R6 , может находиться в S конфигурации или R конфигурации.
[832] В некоторых вариантах осуществления соединений формулы (I)-(VI) и (A)-(H-I) атом водорода можно заменить атомом дейтерия.
[833] В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из Таблицы A ниже или их фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства. В одном варианте осуществления соединения формулы (I)-(VA), (A) или (D)-(H-I) соединение выбрано из соединений A3, A5, A7, A13, A17, A18, A22, A23, A24, A25, A28, A30, A31, A32, A34, A35, A38, A40, A41, A42, A45, A49, A52, A53, A54, A56, A57, A58, A62, A63, A64, A65, A68, A73, A74, A75 или A76 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A1, A2, A4, A6, A8, A9, A10, A11, A12, A14, A15, A16, A19, A20, A21, A26, A27, A29, A33, A36, A37, A39, A43, A44, A46, A47, A48, A50, A51, A55, A59, A60, A61, A66, A67, A69, A70, A71, A72, A77, A78, A79, A80, A81, A82, A83, A84, A85, A86, A87, A88, A89, A90, A91, A92, A93, A94, A95, A96 или A97 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A98-A186 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A187-A211 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A1-A211 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A212-A234 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A1-A234 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из соединений A1-A96, A98-A116, A118-A159, A161-A175 и A177-A234 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[834] В одном варианте осуществления соединения формулы (I)-(VA), (A), (A-I) или (D)-(H-I) соединение выбрано из A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и/или A204 или их фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[835]
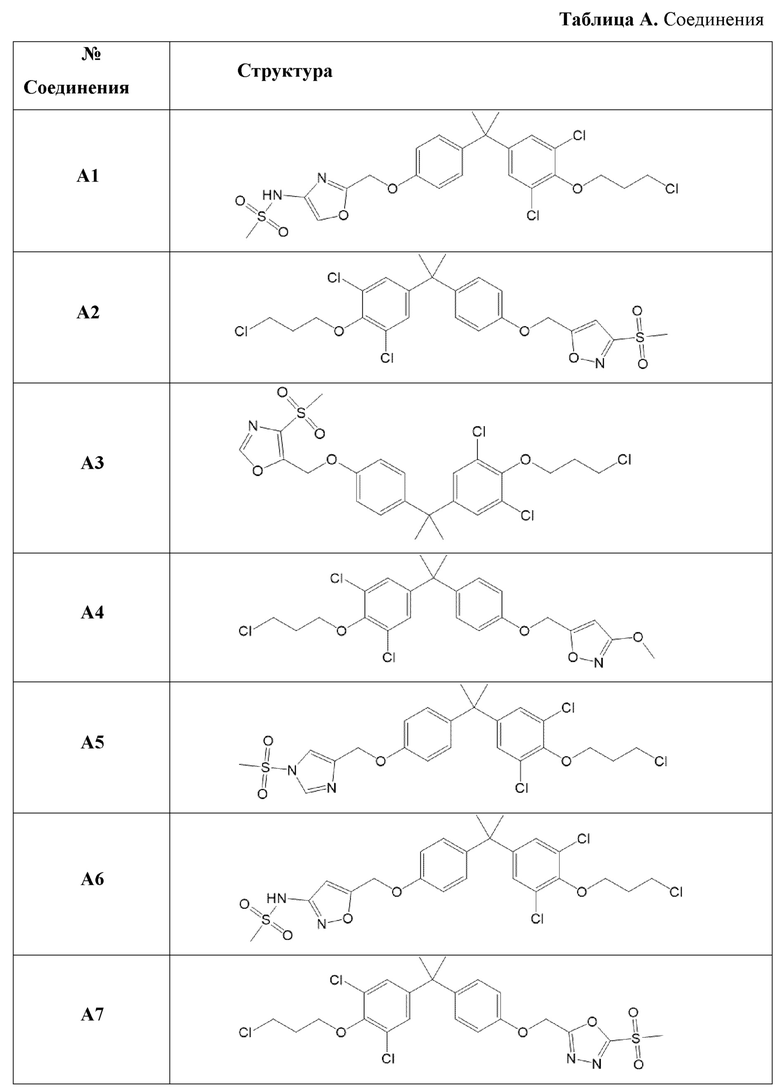
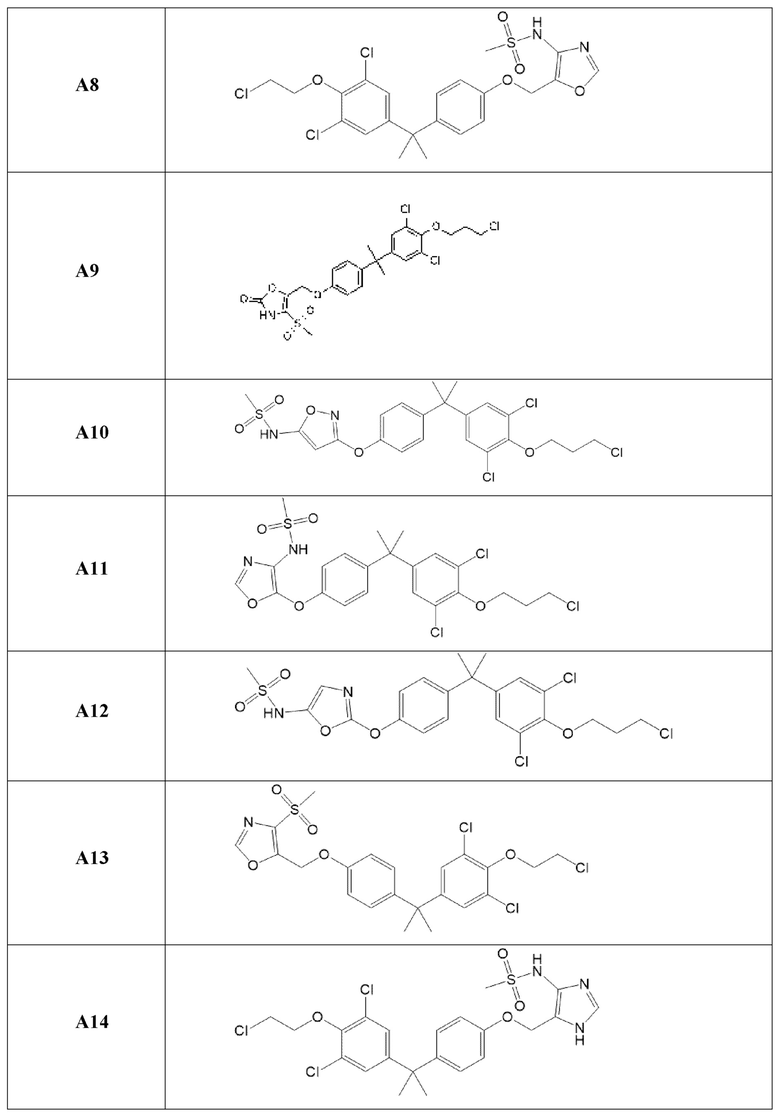
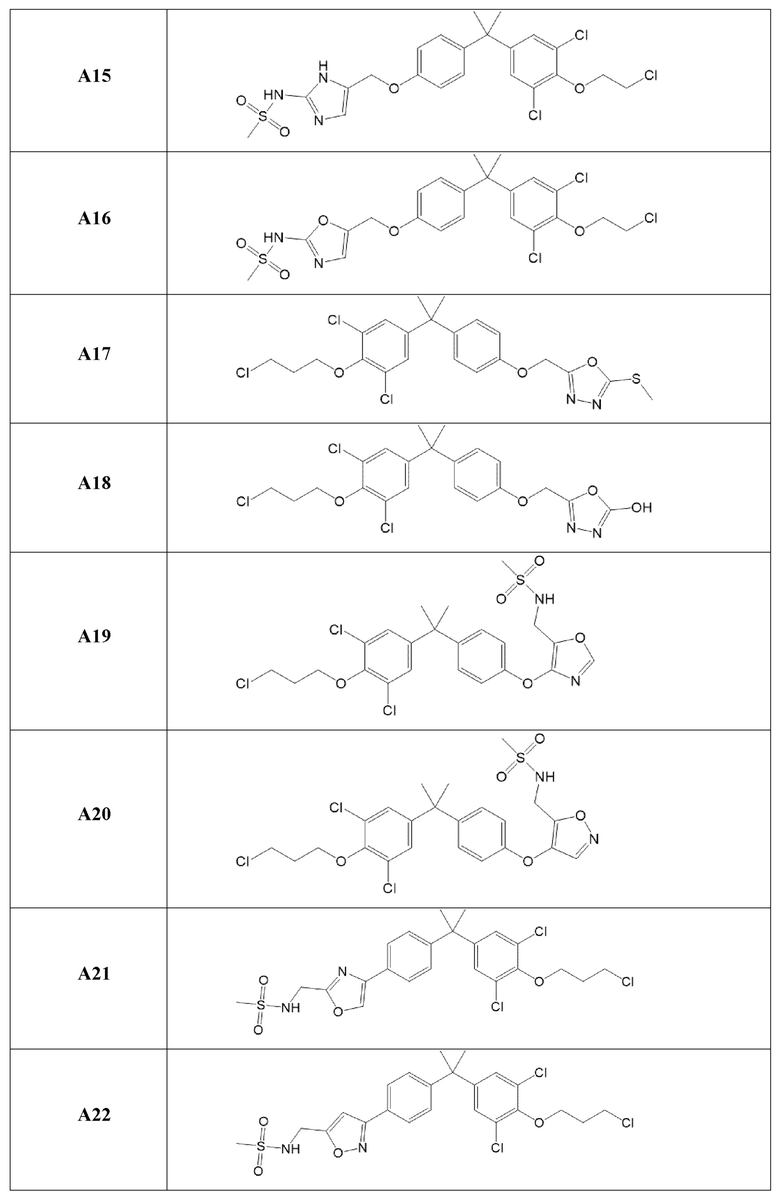
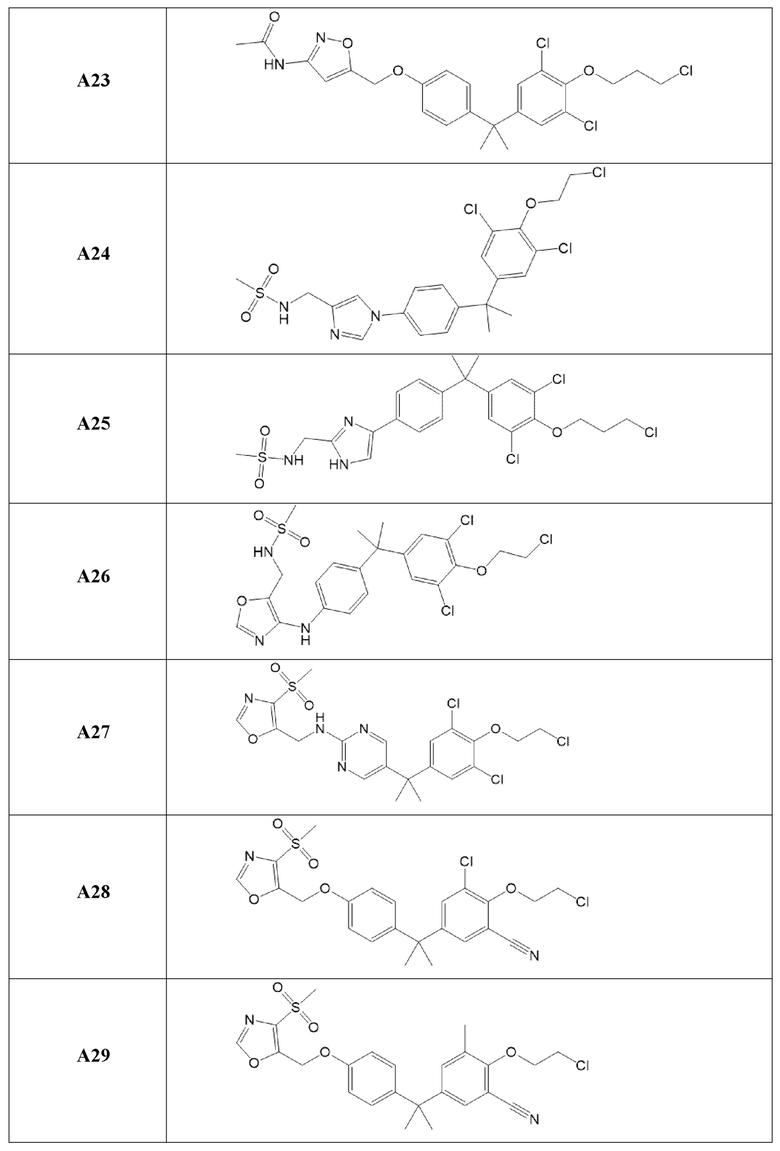
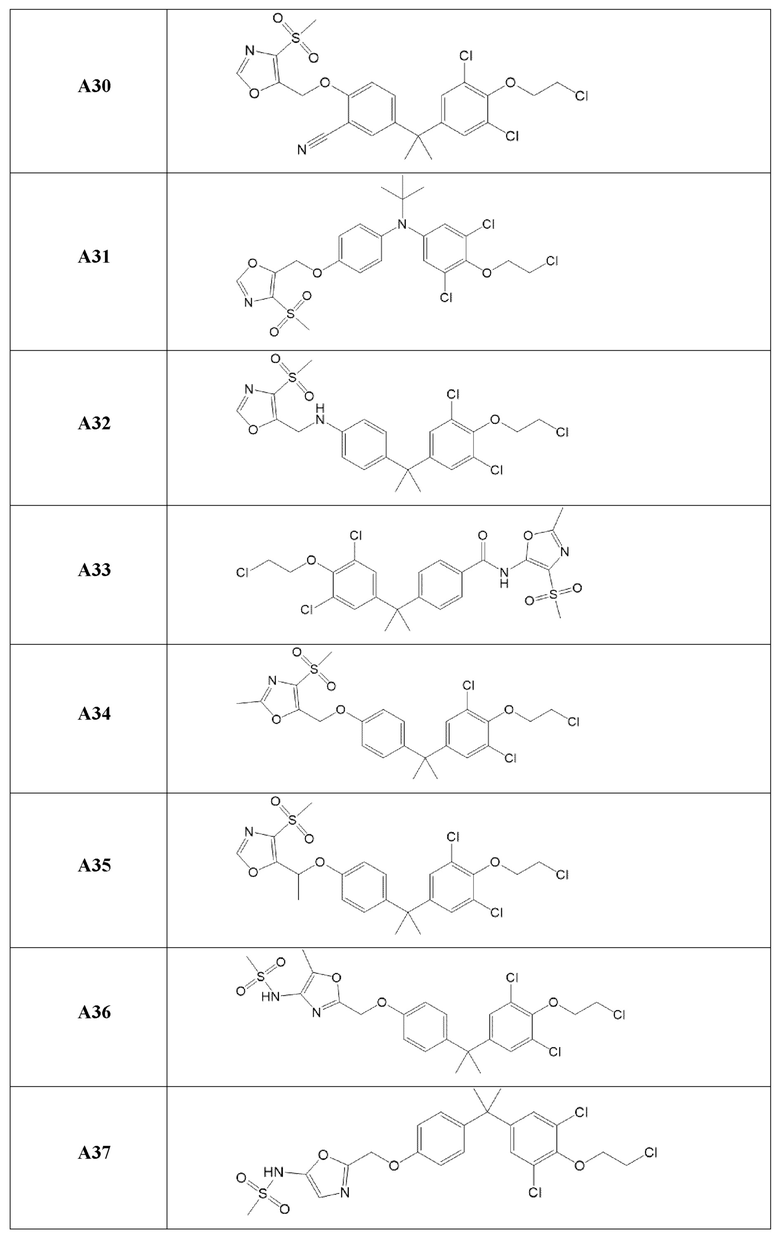
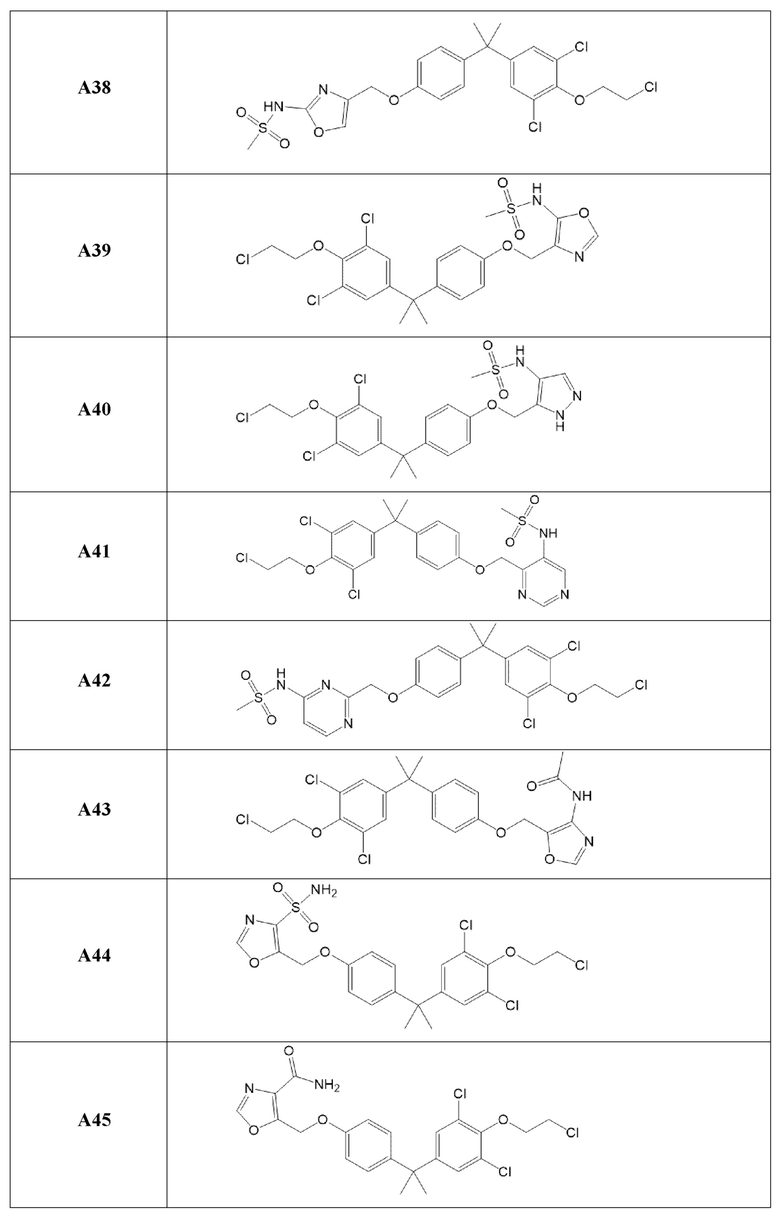
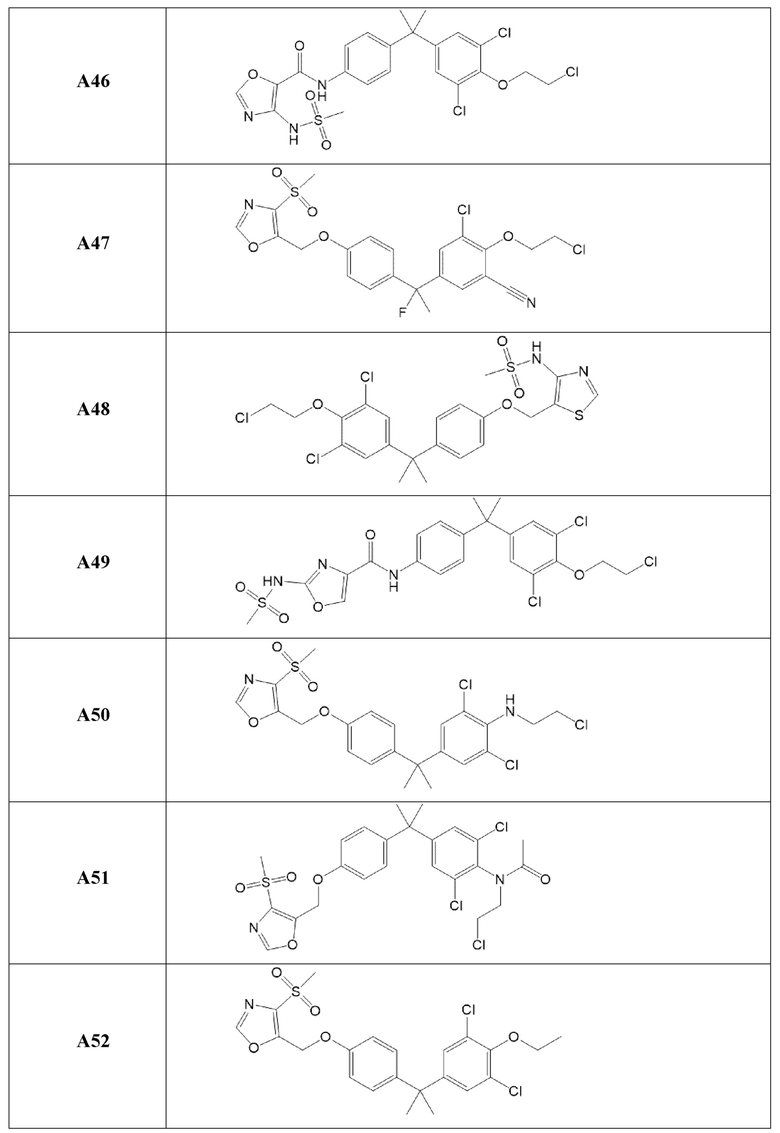
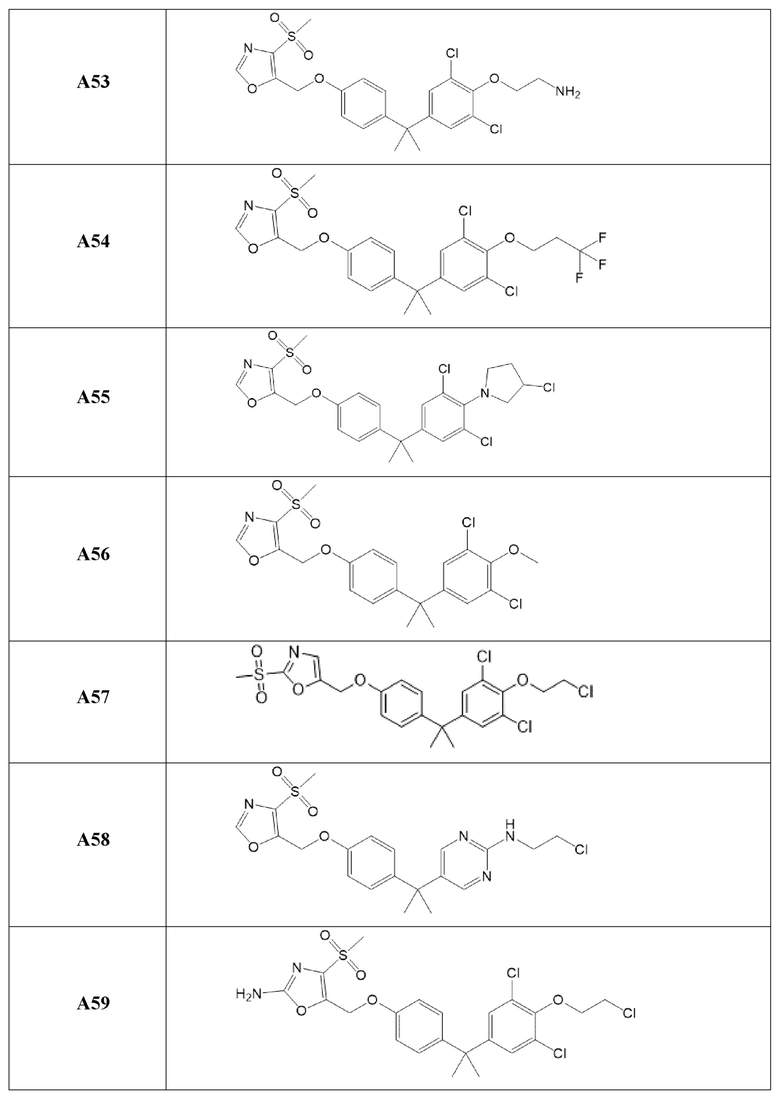
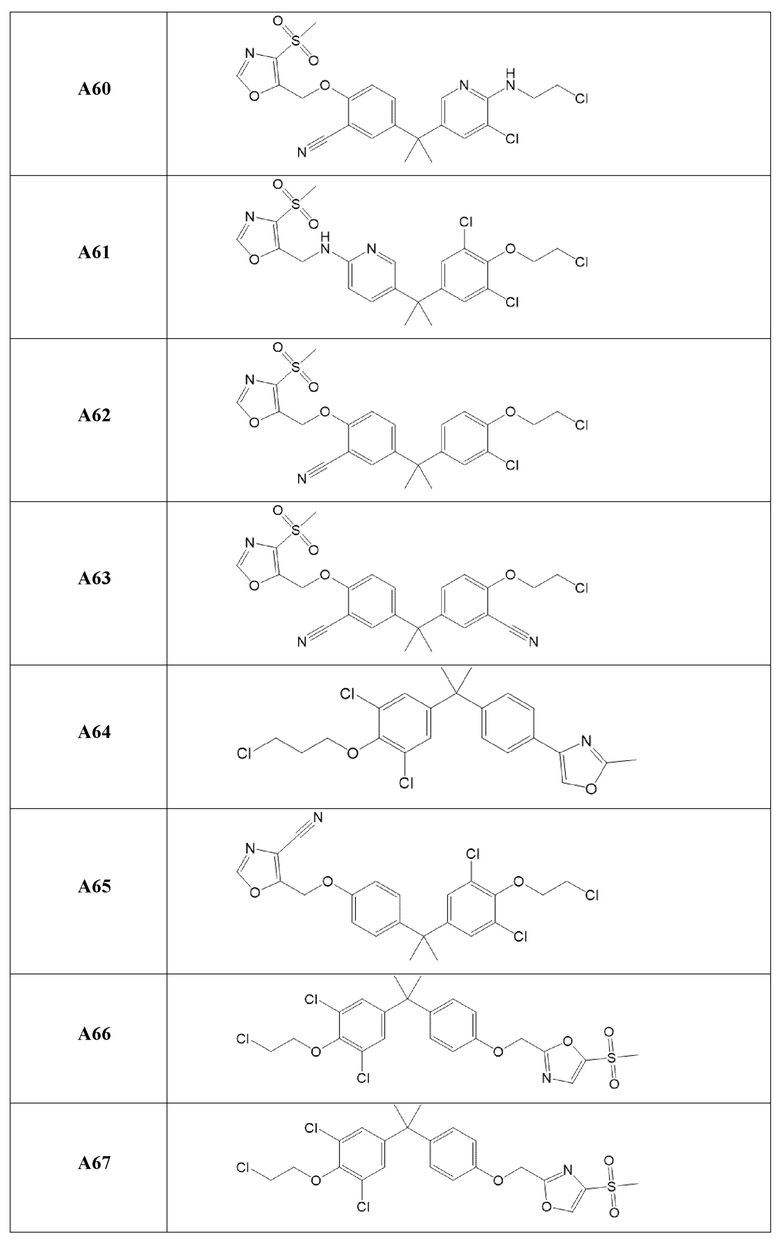
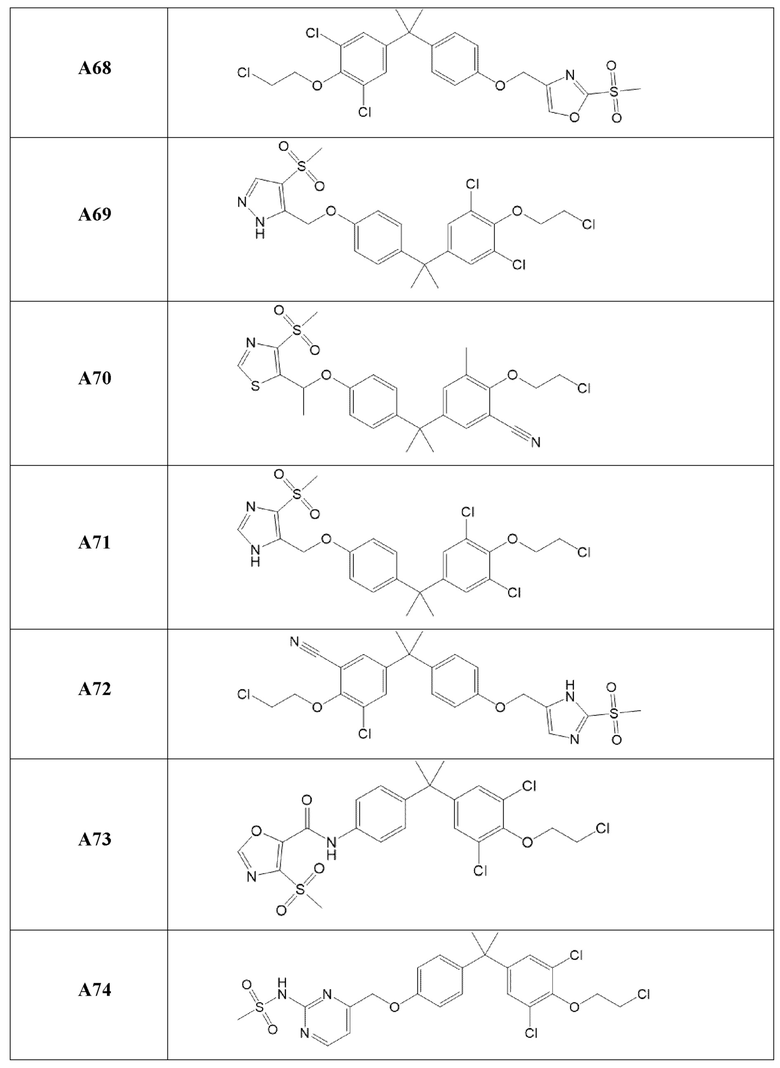
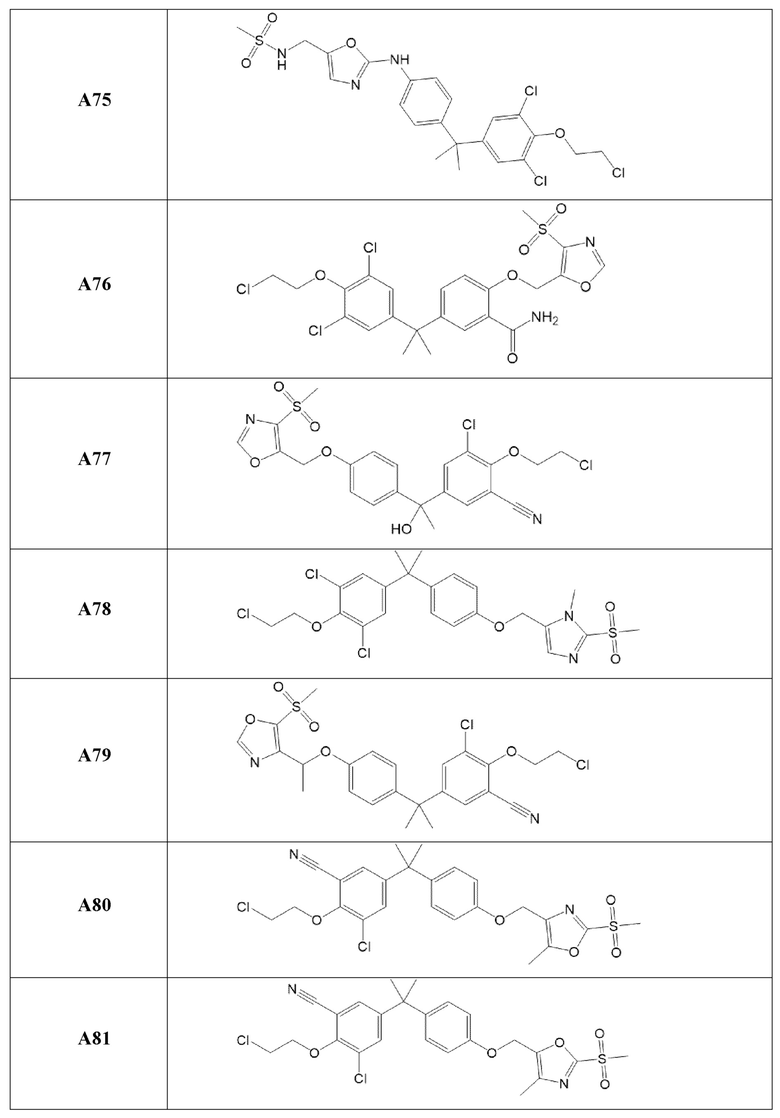

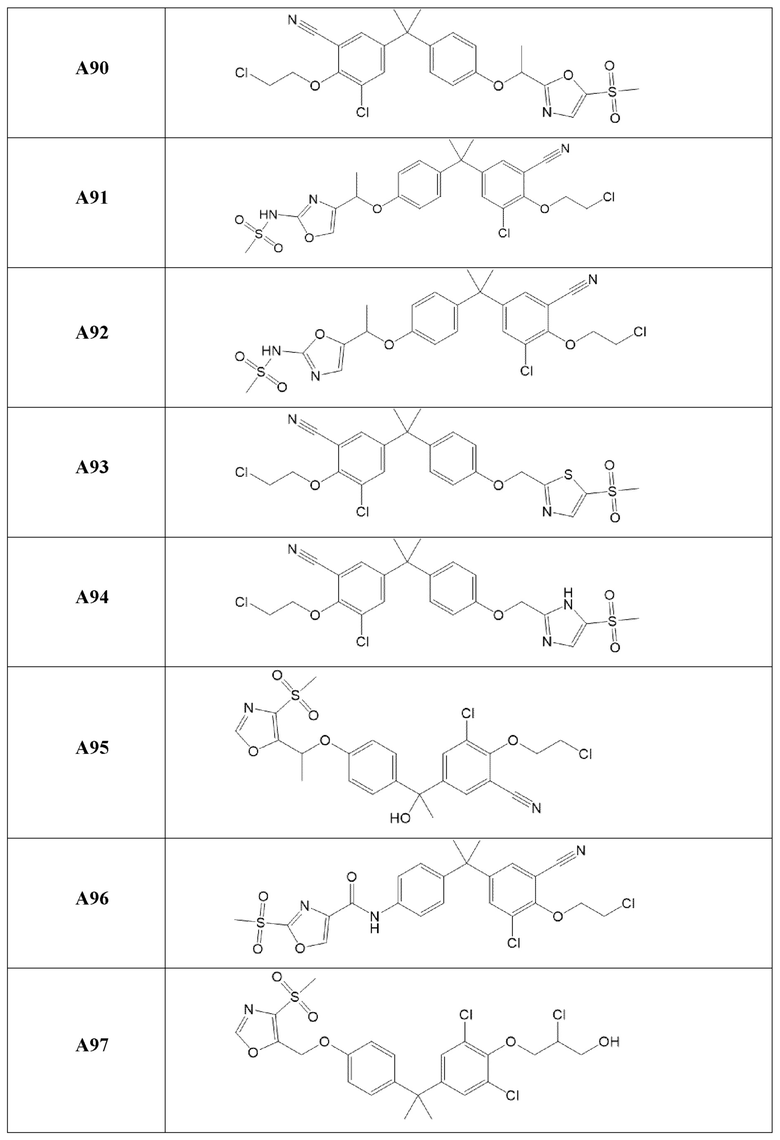
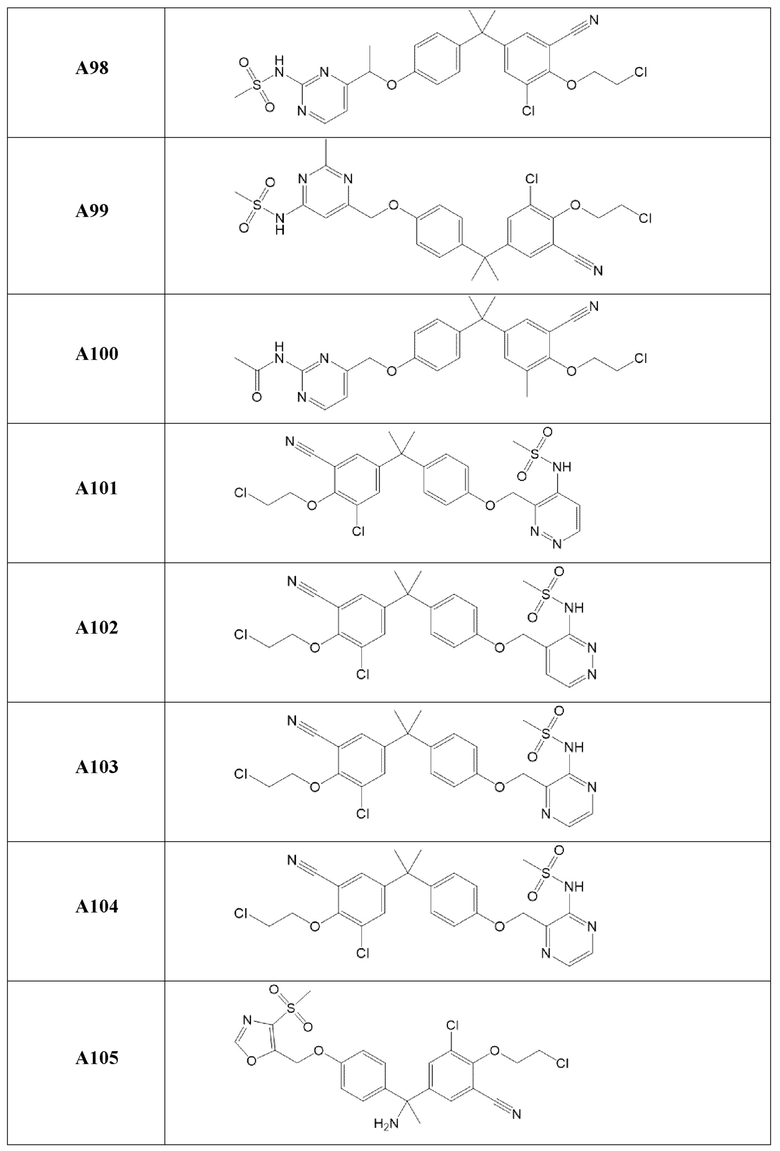
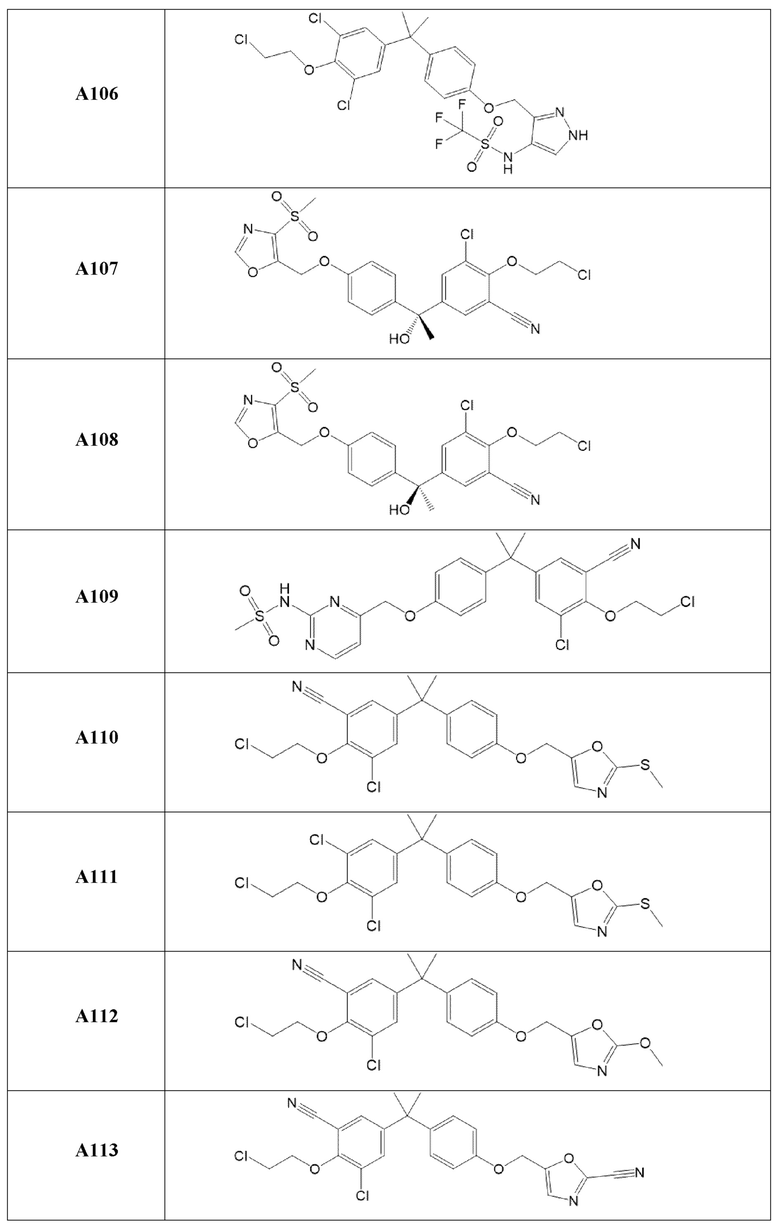
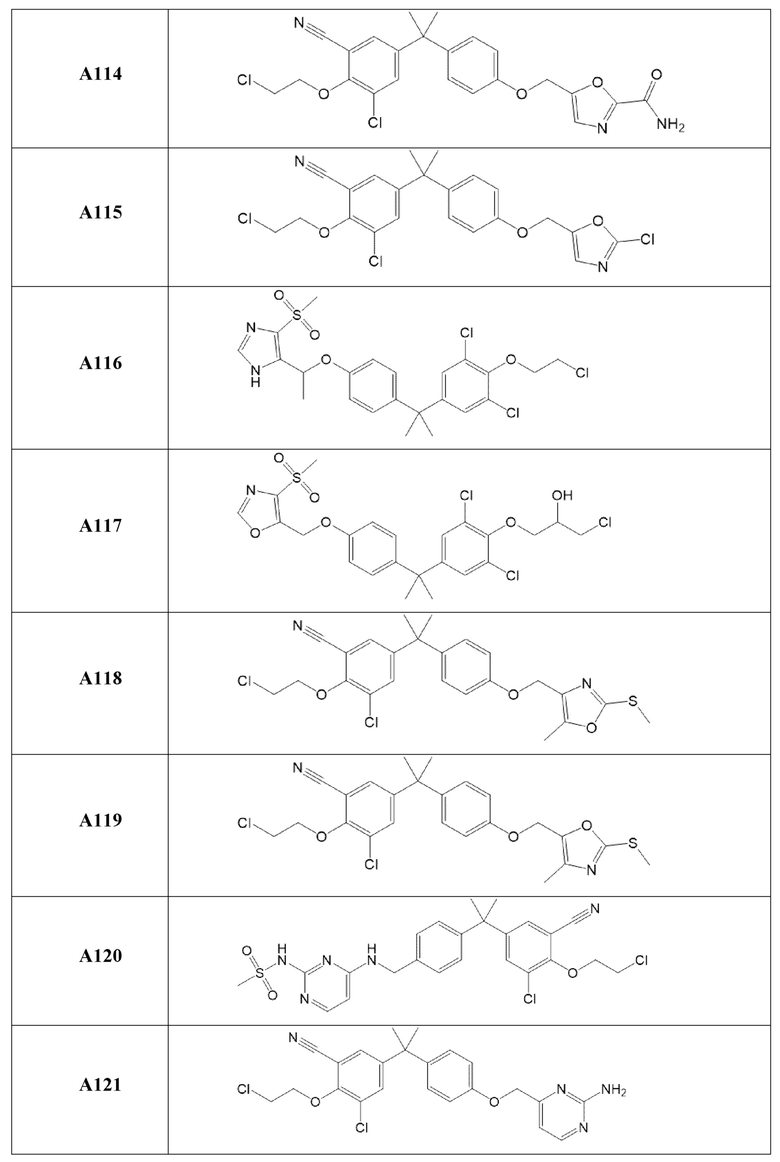
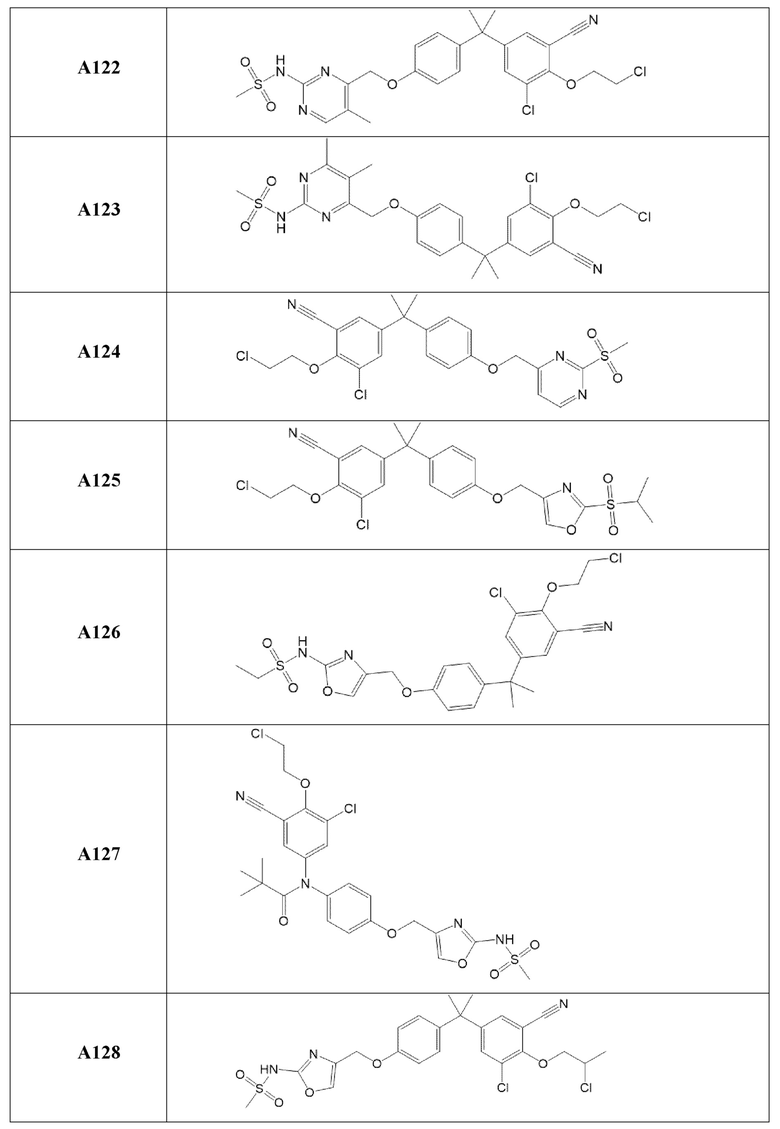
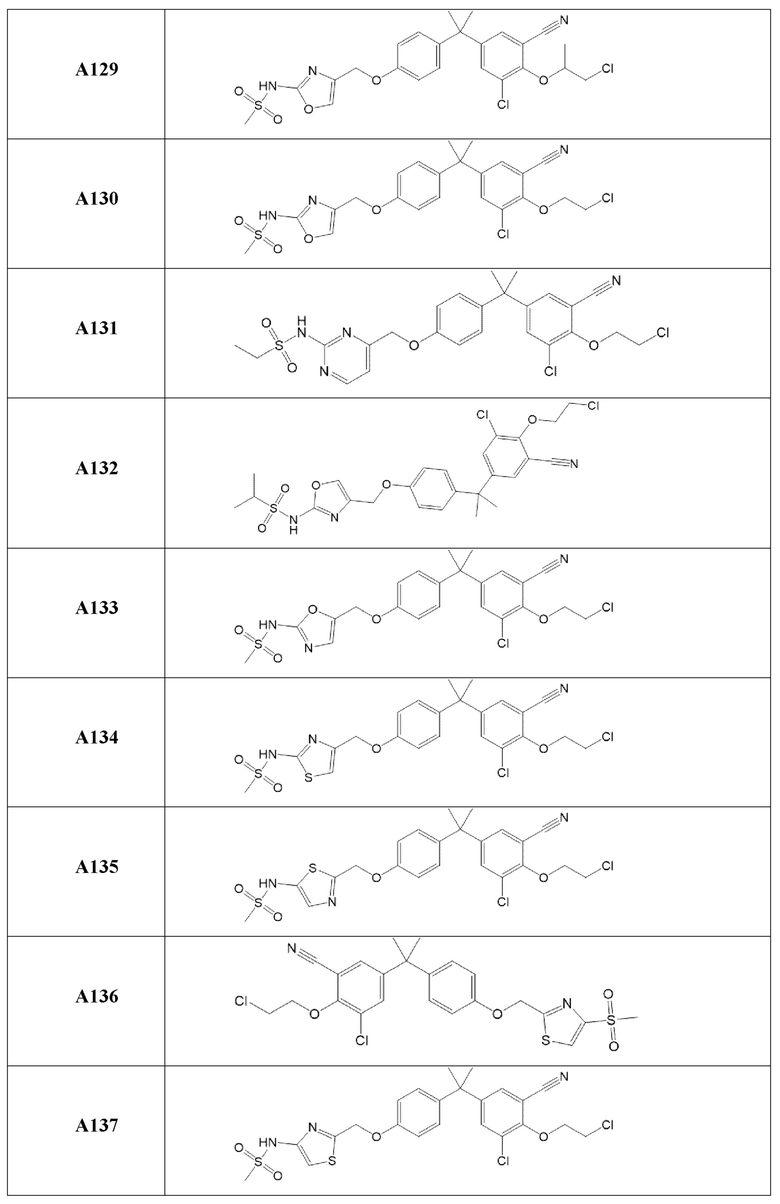
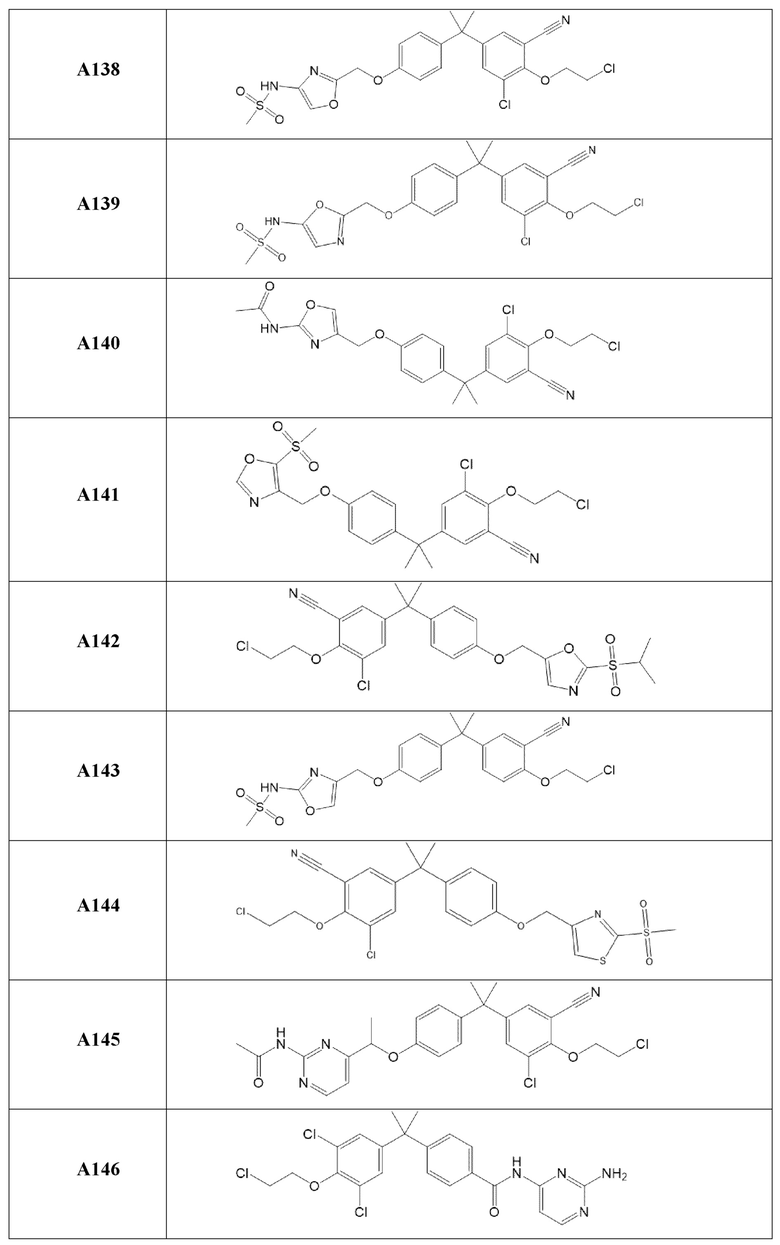
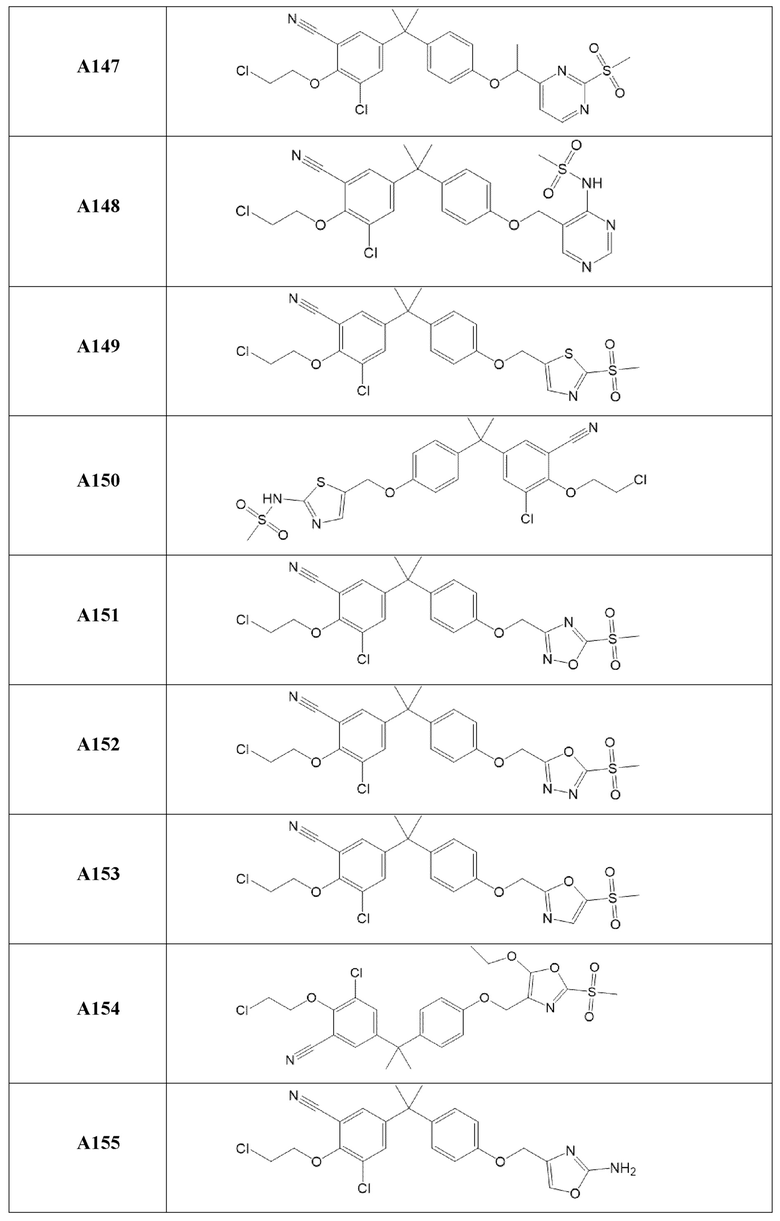
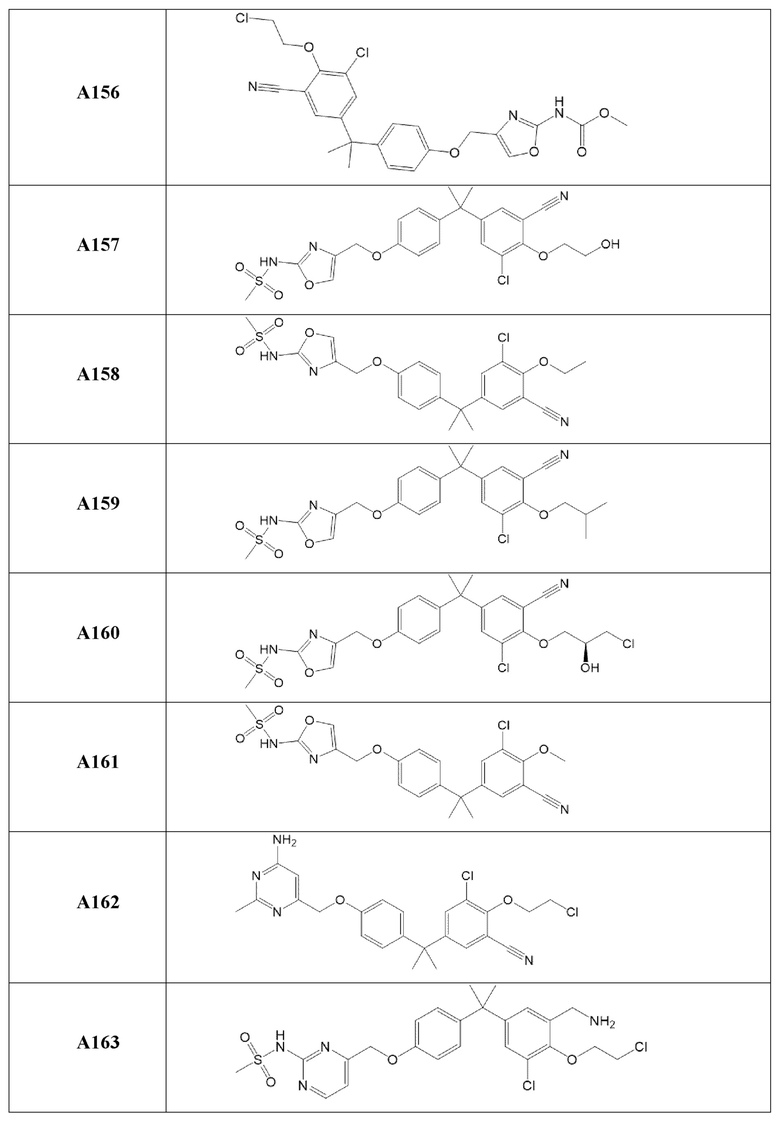
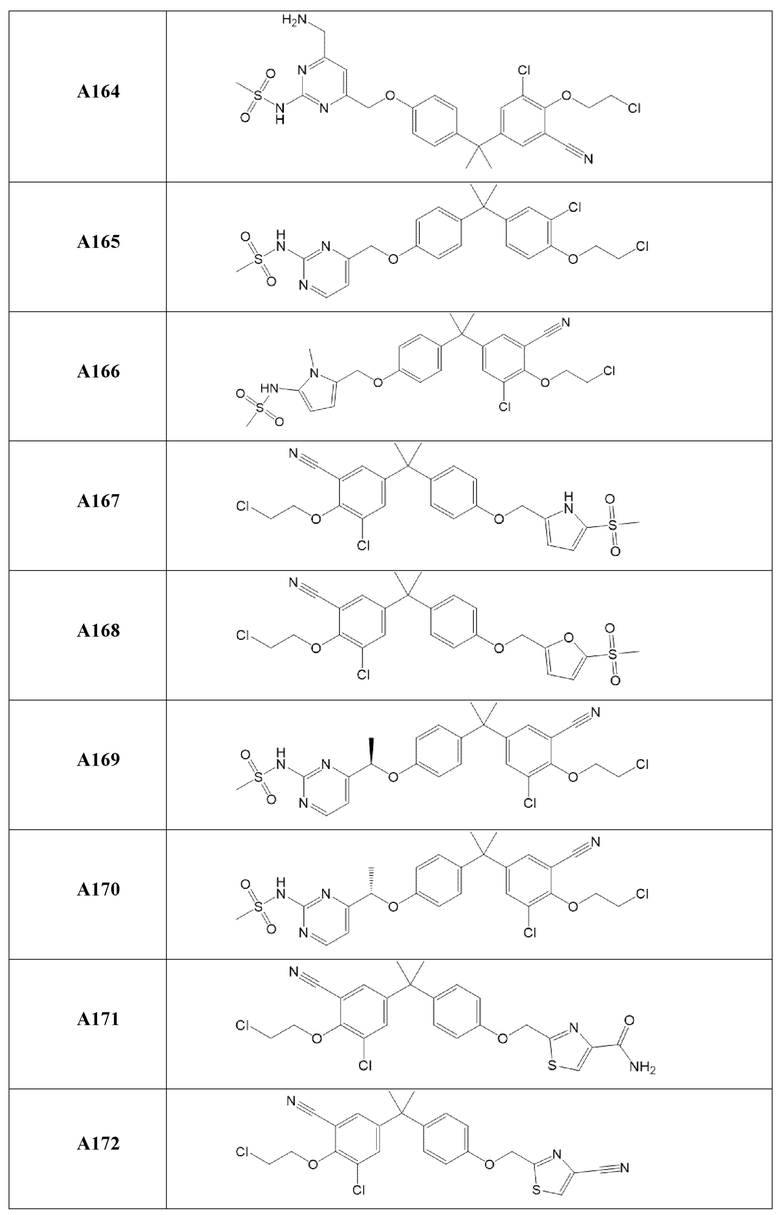
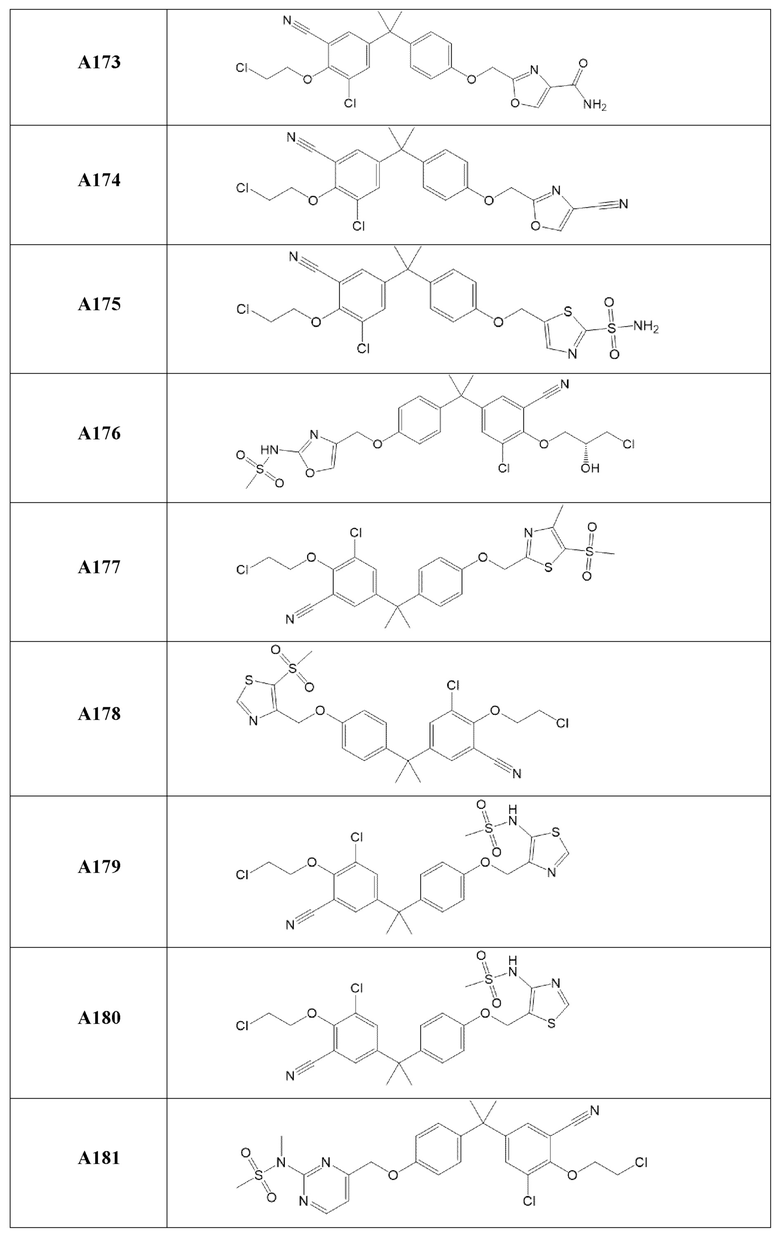
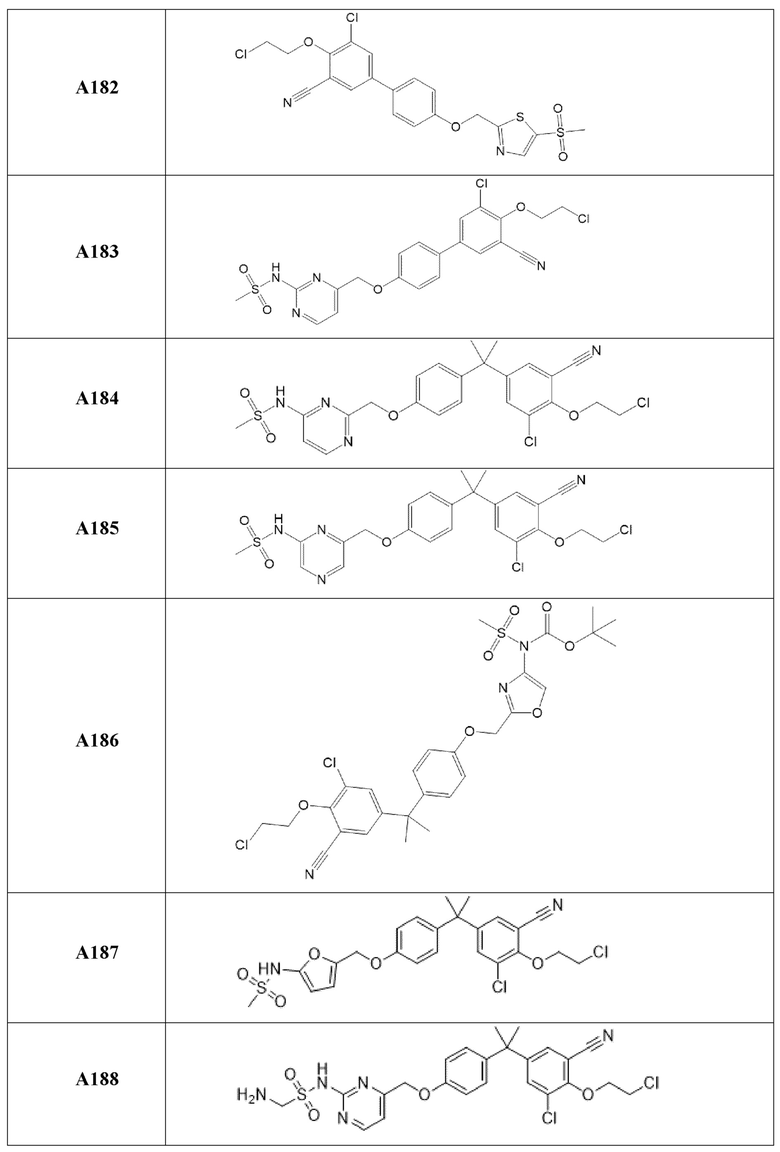
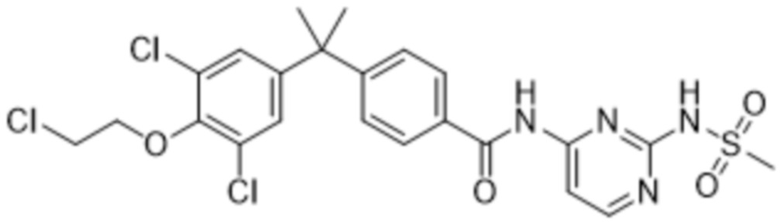
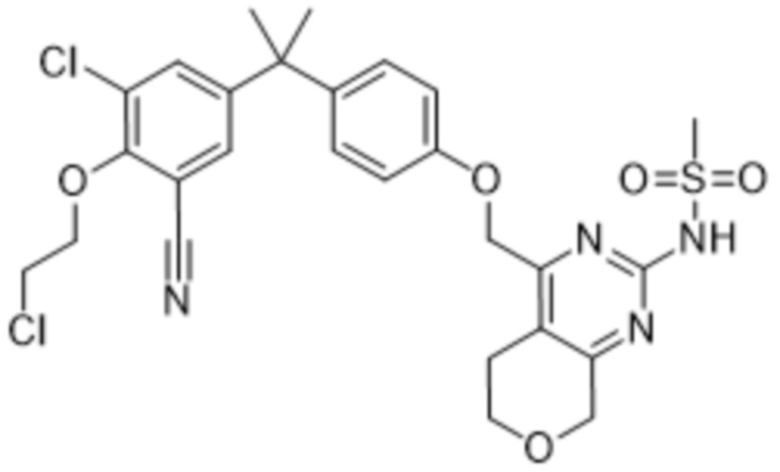
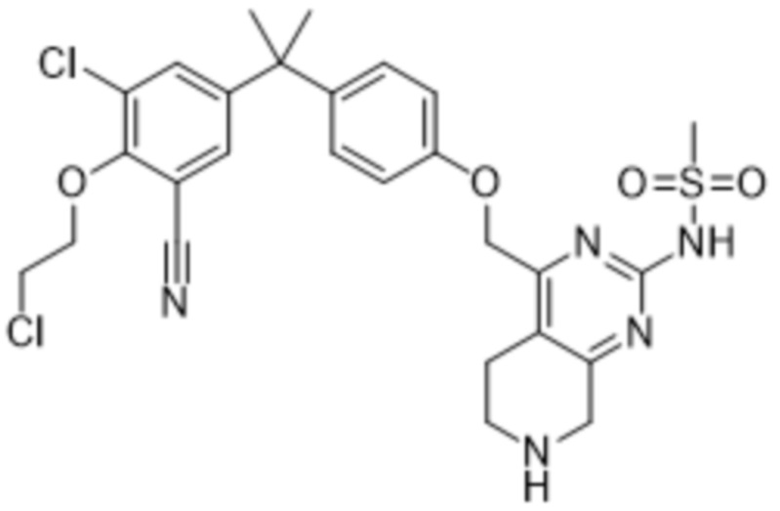
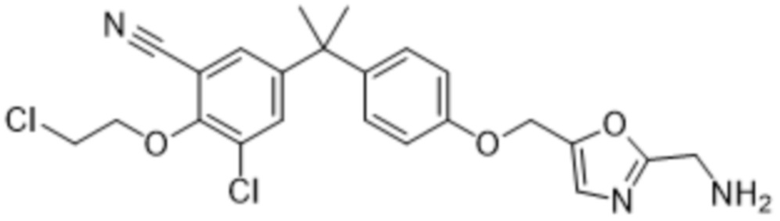
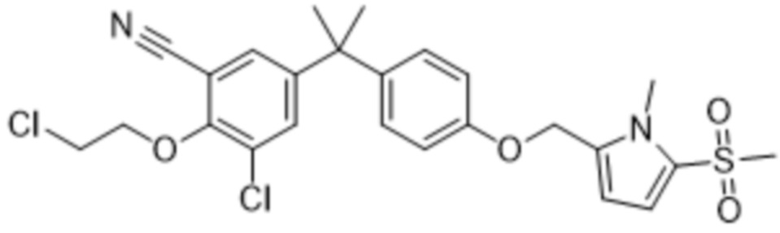
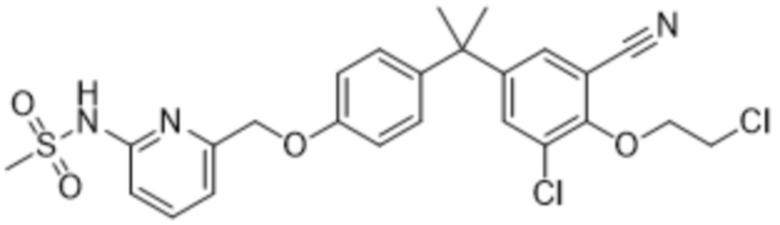
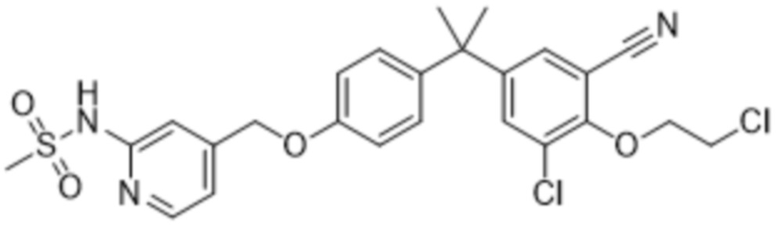

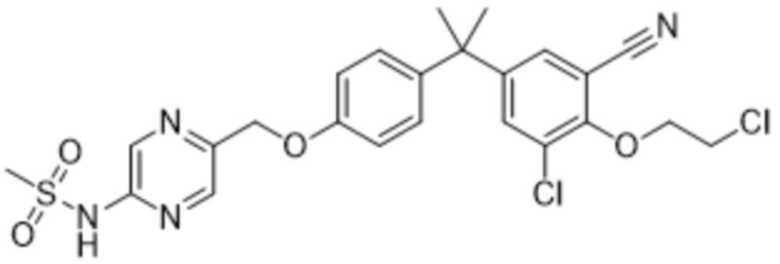
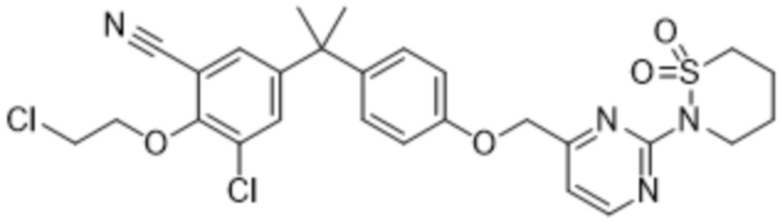
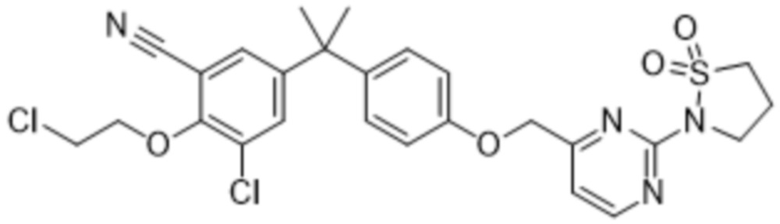
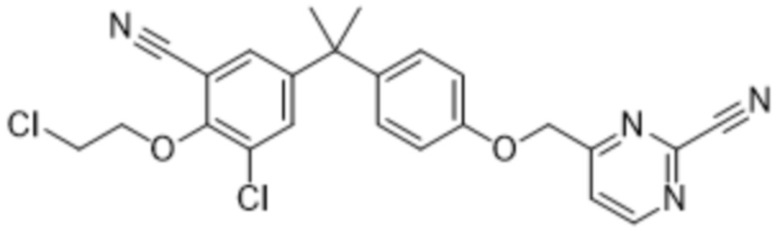
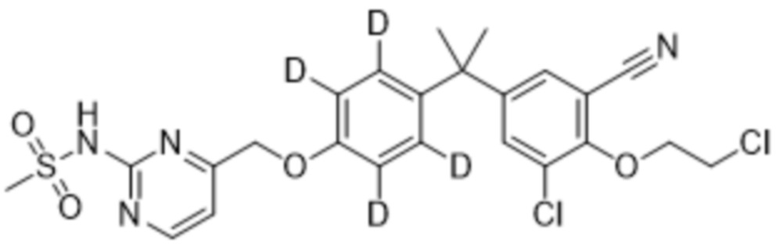

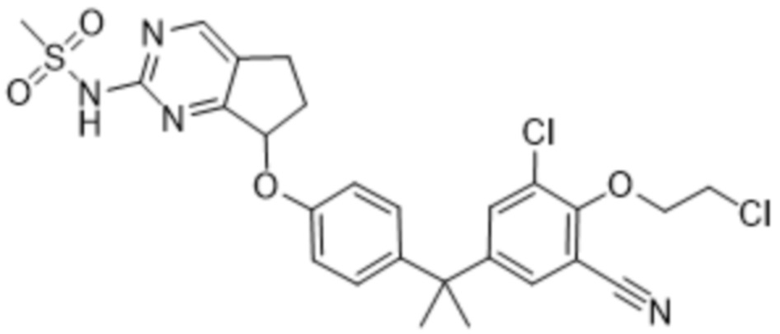
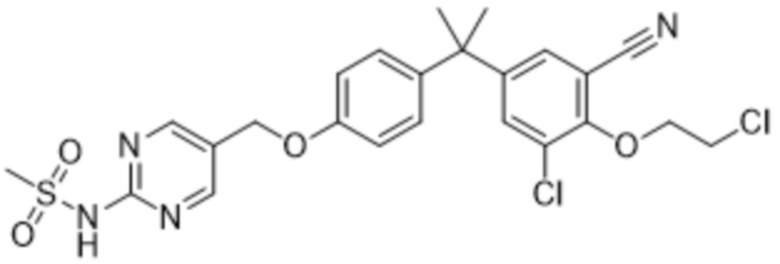
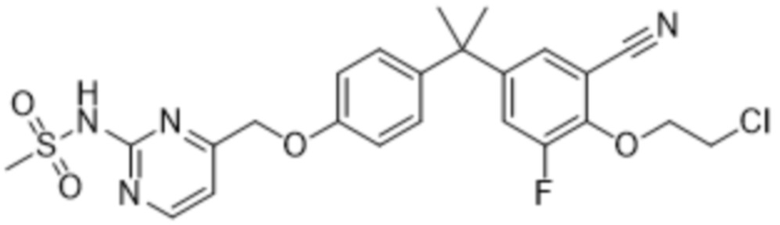
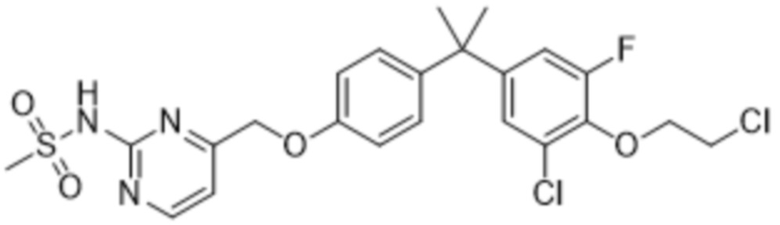
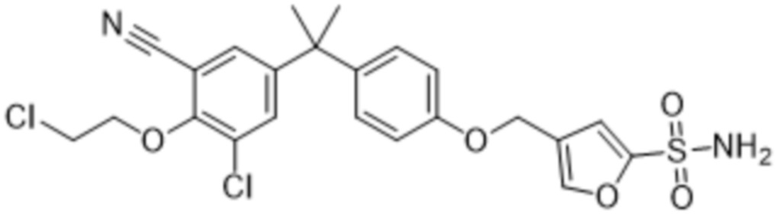


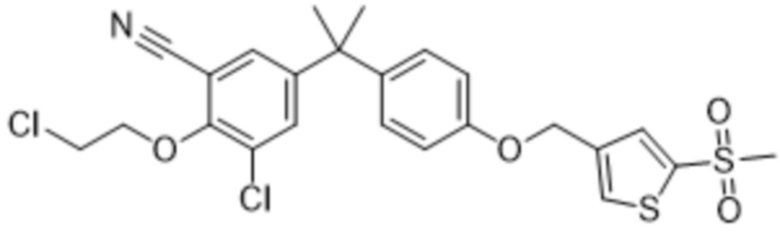
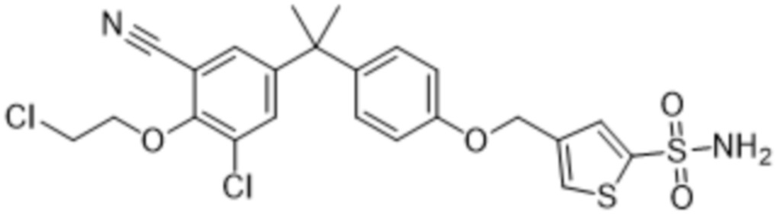

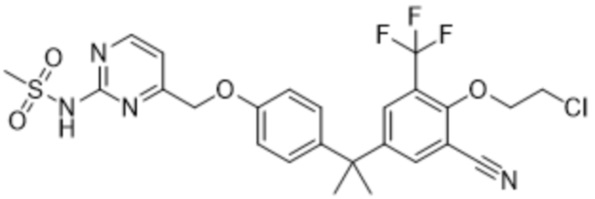

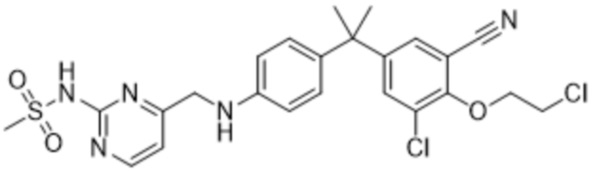
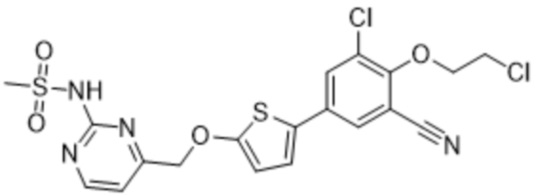
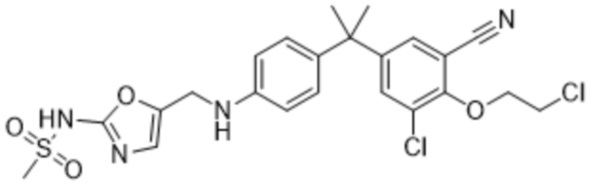
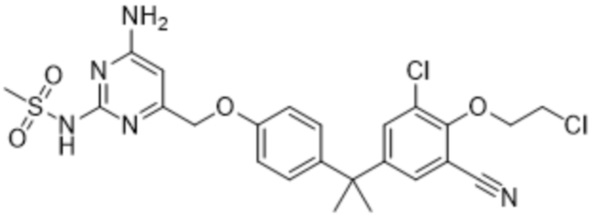
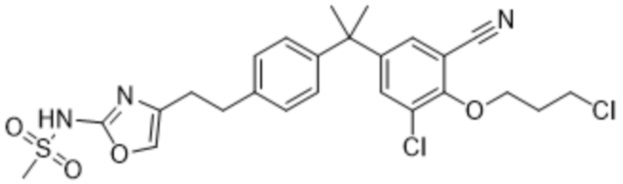
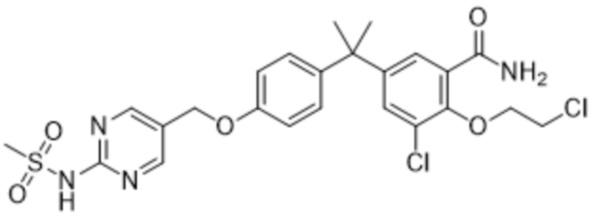
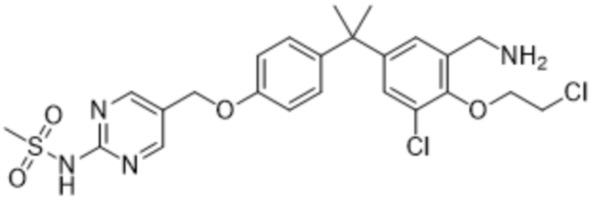

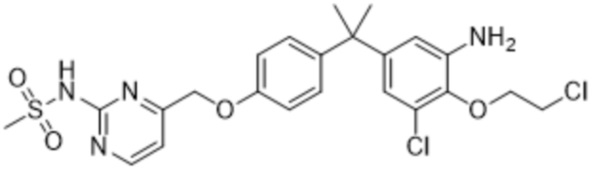
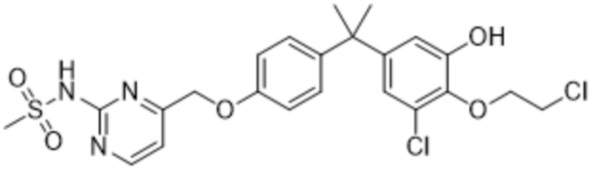
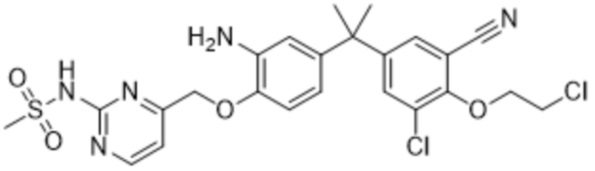
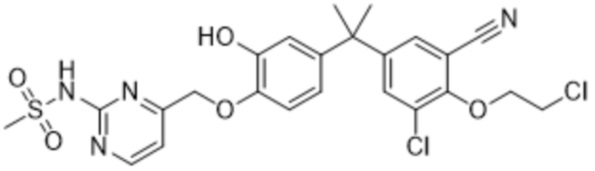

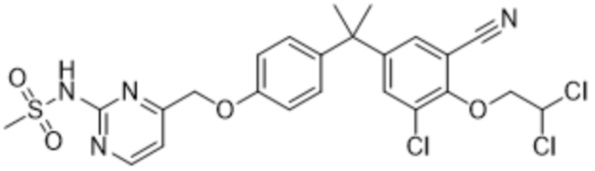
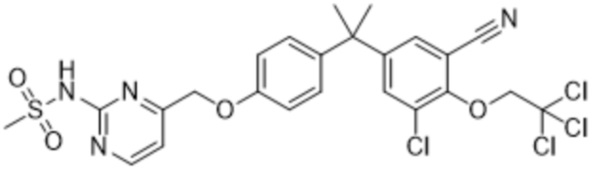
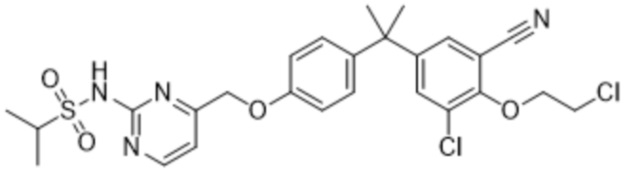
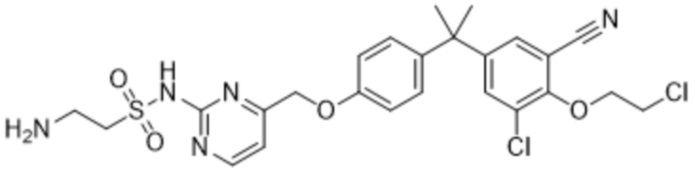
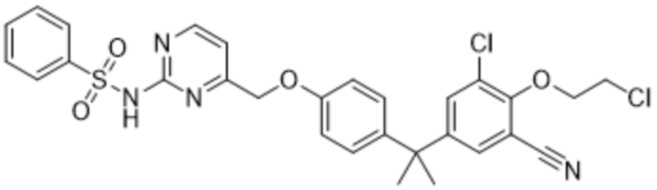
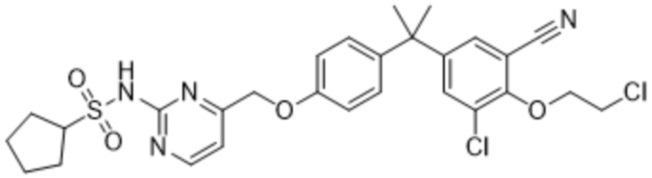
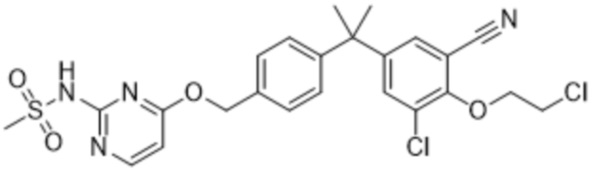
[836] В одном варианте осуществления соединения формулы (I)-(IV), (VI), (B) или (C) соединение выбрано из Таблицы B ниже или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства. В одном варианте осуществления соединения формулы (I)-(IV), (VI), (B) или (C) соединение выбрано из соединений B1, B2, B3 или B6 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства. В одном варианте осуществления соединения формулы (I)-(IV), (VI), (B) или (C) соединение выбрано из соединений B4, B5, B7, B8, B9, B10 или B11 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства. В одном варианте осуществления соединения формулы (I)-(IV), (VI), (B) или (C) соединение выбрано из соединений B1-B11 или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства.
[837]

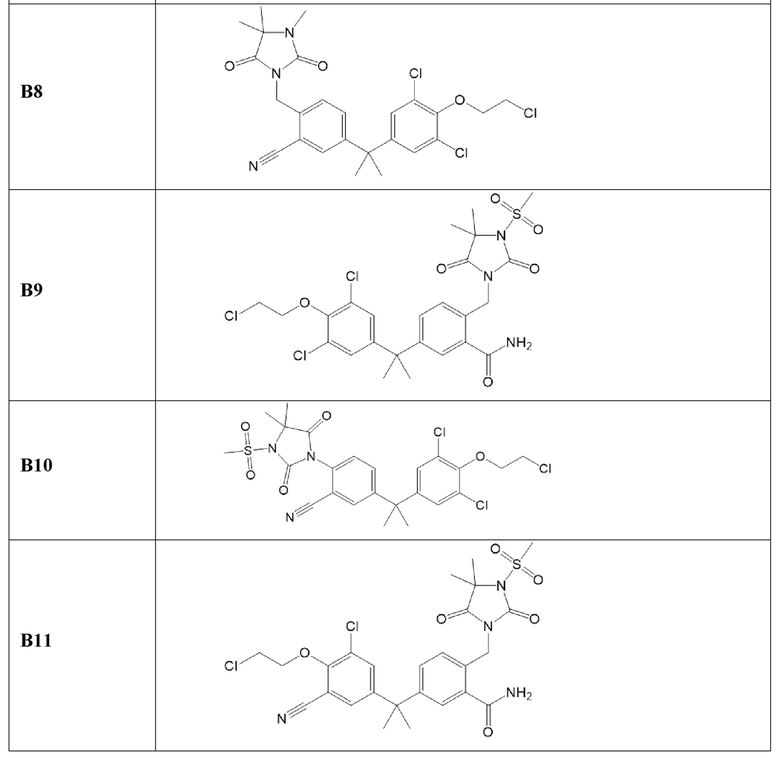
[838] В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение любой одной формулы (I), (IA), (IB), (IC), (II), (IIA), (IIIA), (IIB), (III), (IV), (IVA), (V), (VA), (VI), (A), (A-I), (B)-(D), (E), (E-I)-(E-VII), (F), (G), (G-I), (G-II), (H) и (H-I) («формула (I)-(VI) и (A)-(H-I)») или соединения Таблиц A и B или их фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A3, A5, A7, A13, A17, A18, A22, A23, A24, A25, A28, A30, A31, A32, A34, A35, A38, A40, A41, A42, A45, A49, A52, A53, A54, A56, A57, A58, A62, A63, A64, A65, A68, A73, A74, A75, A76, B1, B2, B3 или B6 или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A1, A2, A4, A6, A8, A9, A10, A11, A12, A14, A15, A16, A19, A20, A21, A26, A27, A29, A33, A36, A37, A39, A43, A44, A46, A47, A48, A50, A51, A55, A59, A60, A61, A66, A67, A69, A70, A71, A72, A77, A78, A79, A80, A81, A82, A83, A84, A85, A86, A87, A88, A89, A90, A91, A92, A93, A94, A95, A96, A97, B4, B5, B7, B8, B9, B10 или B11 или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A98-A186, или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A187-A211, или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A212-A234, или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A1-A96, A98-A116, A118-A159, A161-A175 и A177-A234, или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и/или A204 или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A1-A211 или B1-B11, или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение, выбранное из соединений A1-A234 или B1-B11, или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство. В одном варианте осуществления настоящего изобретения в настоящем раскрытии предложена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель или фармацевтически приемлемый эксципиент и соединение любой одной формулы (D)-(H-I) или его фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство.
Терапевтическое применение
[839] Настоящие соединения находят применение в любом количестве методов. Например, в некоторых вариантах осуществления соединения пригодны в способах модуляции андрогенового рецептора (AR). Соответственно, в одном варианте осуществления в настоящем раскрытии предложено применение любого из вышеуказанных соединений формулы (I)-(VI) и (A)-(H-I) или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства для модулирования активности андрогенового рецептора (AR). Например, в некоторых вариантах осуществления активность модулирующего андрогенового рецептора (AR) осуществляется в клетке млекопитающего. Модуляция андрогенового рецептора (AR) может быть у субъекта, который в этом нуждается (например, у млекопитающего), и для лечения любого из описанных состояний или заболеваний.
[840] В одном варианте осуществления настоящего изобретения модуляция AR представляет собой связывание с AR. В другом варианте осуществления настоящего изобретения модуляция AR представляет собой ингибирование AR.
[841] В одном варианте осуществления настоящего изобретения модуляция AR представляет собой модуляцию N-концевого домена (NTD) AR. В одном варианте осуществления настоящего изобретения модуляция AR представляет собой связывание с NTD AR. В другом варианте осуществления настоящего изобретения модуляция AR представляет собой ингибирование NTD AR. В одном варианте осуществления настоящего изобретения модуляция AR представляет собой модуляцию N-концевого домена (NTD) AR. В некоторых вариантах осуществления настоящего изобретения модуляция AR представляет собой ингибирующую трансактивацию N-концевого домена (NTD) андрогенового рецептора.
[842] В другом варианте осуществления настоящего изобретения модуляция активности андрогенового рецептора (AR) предназначена для лечения по меньшей мере одного показания, выбранного из группы, состоящей из: рака предстательной железы, рака молочной железы, рака яичников, рака мочевого пузыря, рака поджелудочной железы, гепатоцеллюлярного рака, рака эндометрия, карциномы слюнной железы, выпадения волос, угрей, гирсутизма, кист яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии, возрастной дегенерации желтого пятна и их комбинации. Например, в некоторых вариантах осуществления показанием является рак предстательной железы. В другом варианте осуществления настоящего изобретения рак предстательной железы представляет собой первичный/локализованный рак предстательной железы, местно-распространенный рак предстательной железы, рецидивирующий рак предстательной железы, неметастатический устойчивый к кастрации рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы (CRPC) или гормоночувствительный рак предстательной железы. Хотя в других вариантах осуществления рак предстательной железы представляет собой андрогензависимый рак предстательной железы. В другом варианте осуществления настоящего изобретения спинальная и бульбарная мышечная атрофия представляет собой болезнь Кеннеди. В другом варианте осуществления настоящего изобретения рак предстательной железы представляет собой первичный/локализованный рак предстательной железы, местно-распространенный рак предстательной железы, рецидивирующий рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы (CRPC) или гормоночувствительный рак предстательной железы. Хотя в других вариантах осуществления рак предстательной железы представляет собой андрогензависимый рак предстательной железы. В другом варианте осуществления настоящего изобретения спинальная и бульбарная мышечная атрофия представляет собой болезнь Кеннеди.
[843] В одном варианте осуществления настоящего раскрытия предложен способ лечения состояния, связанного с пролиферацией клеток у пациента, нуждающегося в этом, включающий введение соединения формулы (I)-(VI) и (A)-(H-I) или его фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства субъекту, нуждающемуся в этом. В одном варианте осуществления настоящего изобретения в настоящем изобретении предложен способ лечения рака или опухолей. В другом варианте осуществления настоящего изобретения в настоящем изобретении предложен способ лечения рака предстательной железы или рака груди.
[844] В одном варианте осуществления настоящего раскрытия способ уменьшения, ингибирования или улучшения пролиферации, включающий введение терапевтически эффективного количества соединения формулы (I)-(VI) и (A)-(H-I) или его фармацевтически приемлемой соли, таутомера или стереоизомера. В одном варианте осуществления настоящего изобретения уменьшение, ингибирование или улучшение в способе, раскрытом в данном документе, происходит in vivo. В другом варианте осуществления настоящего изобретения уменьшение, ингибирование или улучшение происходит in vitro.
[845] В одном варианте осуществления настоящего изобретения клетки в способе, раскрытом в данном документе, представляют собой раковые клетки. В одном варианте осуществления настоящего изобретения раковые клетки представляют собой клетки рака предстательной железы. В одном варианте осуществления настоящего изобретения клетки рака предстательной железы представляют собой клетки первичного/локализованного рака предстательной железы (недавно диагностированный или на ранней стадии), местнораспространенного рака предстательной железы, рецидивирующего рака предстательной железы (например, рак предстательной железы, который не отвечал на первичную терапию), метастатического рака предстательной железы, неметастатического устойчивого к кастрации рака предстательной железы, распространенного рака предстательной железы (например, после кастрации по поводу рецидивирующего рака предстательной железы), метастатического устойчивого к кастрации рак предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В одном варианте осуществления настоящего изобретения клетки рака предстательной железы представляют собой клетки первичного/локализованного рака предстательной железы (недавно диагностированный или на ранней стадии), местнораспространенного рака предстательной железы, рецидивирующего рака предстательной железы (например, рак предстательной железы, который не отвечал на первичную терапию), метастатического рака предстательной железы, распространенного рака предстательной железы (например, после кастрации по поводу рецидивирующего рака предстательной железы), метастатического устойчивого к кастрации рак предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В другом варианте осуществления настоящего изобретения клетки рака предстательной железы представляют собой клетки метастатического устойчивого к кастрации рака предстательной железы. В другом варианте осуществления настоящего изобретения клетки рака предстательной железы представляют собой клетки андроген-зависимого рака предстательной железы или клетки андроген-независимого рака предстательной железы. В одном варианте осуществления настоящего изобретения раковые клетки представляют собой клетки рака молочной железы.
[846] В одном варианте осуществления настоящего изобретения состояние или заболевание, связанное с пролиферацией клеток, представляет собой рак. В одном варианте осуществления любого из описанных в данном документе способов рак выбран из группы, состоящей из: рака предстательной железы, рака молочной железы, рака яичников, рака эндометрия, рака слюнных желез, выпадения волос, угрей, гирсутизма, кист яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии и возрастной дегенерации желтого пятна. В одном варианте осуществления настоящего изобретения состояние или заболевание представляет собой рак предстательной железы. В одном варианте осуществления настоящего изобретения рак предстательной железы выбран из первичного/локализованного рака предстательной железы, местно-распространенного рака предстательной железы, рецидивирующего рака предстательной железы, метастатического рака предстательной железы, неметастатического устойчивого к кастрации рака предстательной железы, распространенного рака предстательной железы, метастатического устойчивого к кастрации рака предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В одном варианте осуществления настоящего изобретения рак предстательной железы выбран из первичного/локализованного рака предстательной железы, местнораспространенного рака предстательной железы, рецидивирующего рака предстательной железы, метастатического рака предстательной железы, распространенного рака предстательной железы, метастатического устойчивого к кастрации рака предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В другом варианте осуществления настоящего изобретения рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы. В некоторых вариантах осуществления настоящего изобретения рак предстательной железы представляет собой клетки андроген-зависимого рака предстательной железы или андроген-независимый рак предстательной железы. В одном варианте осуществления настоящего изобретения состояние или заболевание представляет собой рак молочной железы.
[847] В другом варианте осуществления настоящего раскрытия способ уменьшения или предотвращения роста опухоли, включающий приведение в контакт опухолевых клеток с терапевтически эффективным количеством соединения (I)-(VI) и (A)-(H-I) или его фармацевтически приемлемой соли, таутомера или стереоизомера.
[848] В одном варианте осуществления настоящего изобретения уменьшение или предотвращение роста опухоли включает уменьшение объема опухоли. В одном варианте осуществления настоящего изобретения уменьшение или предотвращение роста опухоли включает полное устранение опухоли. В одном варианте осуществления настоящего изобретения уменьшение или предотвращение роста опухоли включает остановку или остановку роста существующей опухоли. В одном варианте осуществления настоящего изобретения уменьшение или предотвращение роста опухоли включает снижение скорости роста опухоли. В одном варианте осуществления настоящего изобретения уменьшение или предотвращение роста опухоли включает снижение скорости роста опухоли, так что скорость роста опухоли до лечения пациента описанными в данном документе способами (r1) выше, чем скорость роста опухоли после указанного лечения (r2), так что r1 > r2.
[849] В одном варианте осуществления настоящего изобретения уменьшение или предотвращение в способе, раскрытом в данном документе, происходит in vivo. В другом варианте осуществления настоящего изобретения лечение происходит in vitro.
[850] В одном варианте осуществления настоящего изобретения опухолевая клетка в способе, раскрытом в настоящем документе, выбрана из рака предстательной железы, рака молочной железы, рака яичников, рака эндометрия или карциномы слюнной железы. В одном варианте осуществления настоящего изобретения опухолевые клетки представляют собой опухолевые клетки рака предстательной железы. В одном варианте осуществления настоящего изобретения опухолевые клетки рака предстательной железы представляют собой опухолевые клетки первичного/локализованного рака предстательной железы, местно-распространенного рака предстательной железы, рецидивирующего рака предстательной железы, метастатического рака предстательной железы, неметастатического устойчивого к кастрации рака предстательной железы, распространенного рака предстательной железы, метастатического устойчивого к кастрации рака предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В одном варианте осуществления настоящего изобретения опухолевые клетки рака предстательной железы представляют собой опухолевые клетки первичного/локализованного рака предстательной железы, местно-распространенного рака предстательной железы, рецидивирующего рака предстательной железы, метастатического рака предстательной железы, распространенного рака предстательной железы, метастатического устойчивого к кастрации рака предстательной железы (CRPC) или гормоночувствительного рака предстательной железы. В другом варианте осуществления настоящего изобретения рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы. В некоторых вариантах осуществления настоящего изобретения рак предстательной железы представляет собой андроген-зависимый рак предстательной железы или андроген-независимый рак предстательной железы. В другом варианте осуществления настоящего изобретения опухолевые клетки представляют собой опухолевые клетки рака молочной железы.
[851] В соответствии с другим вариантом осуществления предложено применение соединений формулы (I)-(VI) и (A)-(H-I) или их фармацевтически приемлемой соли, таутомера или стереоизомера для приготовления лекарственного средства для модуляции андрогенового рецептора (AR). В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения обеспечивают метаболическую стабильность. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в микросомах печени человека (HLM), равный менее чем около 500 мкл/мин/мг белка, менее чем около 450 мкл/мин/мг белка, менее чем около 400 мкл/мин/мг белка, менее чем около 350 мкл/мин/мг белка, менее чем около 300 мкл/мин/мг белка, менее чем около 250 мкл/мин/мг белка, менее чем около 225 мкл/мин/мг белка или менее чем около 200 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM, равный менее чем около 200 мкл/мин/мг белка, менее чем около 190 мкл/мин/мг белка, менее чем около 180 мкл/мин/мг белка, менее чем около 170 мкл/мин/мг белка, менее чем около 160 мкл/мин/мг белка, менее чем около 150 мкл/мин/мг белка, менее чем около 140 мкл/мин/мг белка, менее чем около 130 мкл/мин/мг белка, менее чем около 120 мкл/мин/мг белка, менее чем около 110 мкл/мин/мг белка, менее чем около 100 мкл/мин/мг белка, менее чем около 90 мкл/мин/мг белка, менее чем около 80 мкл/мин/мг белка, менее чем около 70 мкл/мин/мг белка, менее чем около 60 мкл/мин/мг белка или менее чем около 50 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM, равный менее чем около 50 мкл/мин/мг белка, менее чем около 48 мкл/мин/мг белка, менее чем около 45 мкл/мин/мг белка, менее чем около 40 мкл/мин/мг белка, менее чем около 35 мкл/мин/мг белка, менее чем около 30 мкл/мин/мг белка, менее чем около 25 мкл/мин/мг белка, менее чем около 20 мкл/мин/мг белка или менее чем около 15 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM, равный менее чем около 15 мкл/мин/мг белка, менее чем около 14 мкл/мин/мг белка, менее чем около 13 мкл/мин/мг белка, менее чем около 12 мкл/мин/мг белка, менее чем около 11 мкл/мин/мг белка или менее чем около 10 мкл/мин/мг белка.
[852] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM, равный менее чем 12 мкл/мин/мг белка. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM в диапазоне от около 0,1 мкл/мин/мг белка до около 12 мкл/мин/мг белка. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM, равный менее чем 48 мкл/мин/мг белка. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM в диапазоне от около 12 мкл/мин/мг белка до около 48 мкл/мин/мг белка. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HLM в диапазоне от около 0,1 мкл/мин/мг белка до около 48 мкл/мин/мг белка.
[853] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[854] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[855] В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в микросомах печени мыши (MLM), равный менее чем около 500 мкл/мин/мг белка, менее чем около 450 мкл/мин/мг белка, менее чем около 400 мкл/мин/мг белка, менее чем около 350 мкл/мин/мг белка, менее чем около 300 мкл/мин/мг белка, менее чем около 250 мкл/мин/мг белка, менее чем около 225 мкл/мин/мг белка или менее чем около 200 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем около 200 мкл/мин/мг белка, менее чем около 190 мкл/мин/мг белка, менее чем около 180 мкл/мин/мг белка, менее чем около 170 мкл/мин/мг белка, менее чем около 160 мкл/мин/мг белка, менее чем около 150 мкл/мин/мг белка, менее чем около 140 мкл/мин/мг белка, менее чем около 130 мкл/мин/мг белка, менее чем около 120 мкл/мин/мг белка, менее чем около 110 мкл/мин/мг белка, менее чем около 100 мкл/мин/мг белка, менее чем около 90 мкл/мин/мг белка, менее чем около 80 мкл/мин/мг белка, менее чем около 70 мкл/мин/мг белка, менее чем около 60 мкл/мин/мг белка или менее чем около 50 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем около 50 мкл/мин/мг белка, менее чем около 48 мкл/мин/мг белка, менее чем около 45 мкл/мин/мг белка, менее чем около 40 мкл/мин/мг белка, менее чем около 35 мкл/мин/мг белка, менее чем около 30 мкл/мин/мг белка, менее чем около 25 мкл/мин/мг белка, менее чем около 20 мкл/мин/мг белка или менее чем около 15 мкл/мин/мг белка. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем около 15 мкл/мин/мг белка, менее чем около 14 мкл/мин/мг белка, менее чем около 13 мкл/мин/мг белка, менее чем около 12 мкл/мин/мг белка, менее чем около 11 мкл/мин/мг белка или менее чем около 10 мкл/мин/мг белка.
[856] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем 12 мкл/мин/мг белка. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM в диапазоне от около 0,1 мкл/мин/мг белка до около 12 мкл/мин/мг белка. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем 48 мкл/мин/мг белка. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM в диапазоне от около 12 мкл/мин/мг белка до около 48 мкл/мин/мг белка. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM в диапазоне от около 0,1 мкл/мин/мг белка до около 48 мкл/мин/мг белка.
[857] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[858] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[859] В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека (HH), равный менее чем около 500 мкл/мин/миллион клеток, менее чем около 450 мкл/мин/миллион клеток, менее чем около 400 мкл/мин/миллион клеток, менее чем около 350 мкл/мин/миллион клеток, менее чем около 300 мкл/мин/миллион клеток, менее чем около 250 мкл/мин/миллион клеток, менее чем около 225 мкл/мин/миллион клеток или менее чем около 200 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 200 мкл/мин/миллион клеток, менее чем около 190 мкл/мин/миллион клеток, менее чем около 180 мкл/мин/миллион клеток, менее чем около 170 мкл/мин/миллион клеток, менее чем около 160 мкл/мин/миллион клеток, менее чем около 150 мкл/мин/миллион клеток, менее чем около 140 мкл/мин/миллион клеток, менее чем около 130 мкл/мин/миллион клеток, менее чем около 120 мкл/мин/миллион клеток, менее чем около 110 мкл/мин/миллион клеток, менее чем около 100 мкл/мин/миллион клеток, менее чем около 90 мкл/мин/миллион клеток, менее чем около 80 мкл/мин/миллион клеток, менее чем около 70 мкл/мин/миллион клеток, менее чем около 60 мкл/мин/миллион клеток или менее чем около 50 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 50 мкл/мин/миллион клеток, менее чем около 48 мкл/мин/миллион клеток, менее чем около 45 мкл/мин/миллион клеток, менее чем около 40 мкл/мин/миллион клеток, менее чем около 35 мкл/мин/миллион клеток, менее чем около 30 мкл/мин/миллион клеток, менее чем около 25 мкл/мин/миллион клеток, менее чем около 20 мкл/мин/миллион клеток или менее чем около 15 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему раскрытию имеют in vitro метаболический клиренс в HH, равный менее чем около 15 мкл/мин/миллион клеток, менее чем около 14 мкл/мин/миллион клеток, менее чем около 13 мкл/мин/миллион клеток, менее чем около 12 мкл/мин/миллион клеток, менее чем около 11 мкл/мин/миллион клеток, менее чем около 10 мкл/мин/миллион клеток, менее чем около 9 мкл/мин/миллион клеток, менее чем около 8 мкл/мин/миллион клеток, менее чем около 8 мкл/мин/миллион клеток, менее чем около 6 мкл/мин/миллион клеток или менее чем около 5 мкл/мин/миллион клеток.
[860] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем 4 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в HH в диапазоне от около 0,1 мкл/мин/миллион клеток до около 4 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем 18 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в HH в диапазоне от около 4 мкл/мин/миллион клеток до около 18 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в HH в диапазоне от около 0,1 мкл/мин/миллион клеток до около 18 мкл/мин/миллион клеток.
[861] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 10 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 5 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 3,85 мкл/мин/миллион клеток.
[862] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 10 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в HH, равный менее чем около 5 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека, равный менее чем около 3,85 мкл/мин/миллион клеток.
[863] В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах мышей (MH), равный менее чем около 500 мкл/мин/миллион клеток, менее чем около 450 мкл/мин/миллион клеток, менее чем около 400 мкл/мин/миллион клеток, менее чем около 350 мкл/мин/миллион клеток, менее чем около 300 мкл/мин/миллион клеток, менее чем около 250 мкл/мин/миллион клеток, менее чем около 225 мкл/мин/миллион клеток или менее чем около 200 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 200 мкл/мин/миллион клеток, менее чем около 190 мкл/мин/миллион клеток, менее чем около 180 мкл/мин/миллион клеток, менее чем около 170 мкл/мин/миллион клеток, менее чем около 160 мкл/мин/миллион клеток, менее чем около 150 мкл/мин/миллион клеток, менее чем около 140 мкл/мин/миллион клеток, менее чем около 130 мкл/мин/миллион клеток, менее чем около 120 мкл/мин/миллион клеток, менее чем около 110 мкл/мин/миллион клеток, менее чем около 100 мкл/мин/миллион клеток, менее чем около 90 мкл/мин/миллион клеток, менее чем около 80 мкл/мин/миллион клеток, менее чем около 70 мкл/мин/миллион клеток, менее чем около 60 мкл/мин/миллион клеток или менее чем около 50 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 50 мкл/мин/миллион клеток, менее чем около 48 мкл/мин/миллион клеток, менее чем около 45 мкл/мин/миллион клеток, менее чем около 40 мкл/мин/миллион клеток, менее чем около 35 мкл/мин/миллион клеток, менее чем около 30 мкл/мин/миллион клеток, менее чем около 25 мкл/мин/миллион клеток, менее чем около 20 мкл/мин/миллион клеток или менее чем около 15 мкл/мин/миллион клеток. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 15 мкл/мин/миллион клеток, менее чем около 14 мкл/мин/миллион клеток, менее чем около 13 мкл/мин/миллион клеток, менее чем около 12 мкл/мин/миллион клеток, менее чем около 11 мкл/мин/миллион клеток, менее чем около 10 мкл/мин/миллион клеток, менее чем около 9 мкл/мин/миллион клеток, менее чем около 8 мкл/мин/миллион клеток, менее чем около 8 мкл/мин/миллион клеток, менее чем около 6 мкл/мин/миллион клеток или менее чем около 5 мкл/мин/миллион клеток.
[864] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B, или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем 4 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MH в диапазоне от около 0,1 мкл/мин/миллион клеток до около 4 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B, или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем 18 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MH в диапазоне от около 4 мкл/мин/миллион клеток до около 18 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MH в диапазоне от около 0,1 мкл/мин/миллион клеток до около 18 мкл/мин/миллион клеток.
[865] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 17 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 7 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 3,85 мкл/мин/миллион клеток.
[866] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 17 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 7 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A или B или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в MH, равный менее чем около 3,85 мкл/мин/миллион клеток.
[867] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любые соединения с комбинацией метаболического клиренса in vitro в HLM, MLM, HH и MH, как описано в данном документе.
[868] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[869] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B, или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка.
[870] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека и мыши менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах мышей, равный менее чем около 17 мкл/мин/миллион клеток, и in vitro метаболический клиренс в гепатоцитах человека, равный менее чем около 10 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах мышей, равный менее чем около 7 мкл/мин/миллион клеток, и in vitro метаболический клиренс в гепатоцитах человека, равный менее чем около 5 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека и мыши менее чем около 3,85 мкл/мин/миллион клеток.
[871] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в гепатоцитах мышей, равный менее чем около 17 мкл/мин/миллион клеток, и in vitro метаболический клиренс в гепатоцитах человека, равный менее чем около 10 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в гепатоцитах мышей, равный менее чем около 7 мкл/мин/миллион клеток, и in vitro метаболический клиренс в гепатоцитах человека, равный менее чем около 5 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение из Таблиц A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 3,85 мкл/мин/миллион клеток.
[872] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка, и in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши менее чем около 17 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши менее чем около 7 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши менее чем около 3,85 мкл/мин/миллион клеток.
[873] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM или MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем около 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем около 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM или MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют a) HLM и MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем 4 мкл/мин/миллион клеток. В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемая соль, таутомер или стереоизомер, причем соединения имеют a) HLM и MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка, и b) in vitro метаболический клиренс в гепатоцитах человека и мыши, равен менее чем 4 мкл/мин/миллион клеток.
[874] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 20 мкл/мин/мг белка, и in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 20 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 15 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 17 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой любое соединение Таблиц A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 12 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 7 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют HLM и MLM in vitro метаболический клиренс, равный менее чем около 11,55 мкл/мин/мг белка, in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем около 3,85 мкл/мин/миллион клеток.
[875] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 120 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 110 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 100 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 90 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 80 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, мыши, крысы, обезьяны или собаки, равный более чем около 70 минут.
[876] В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах человека, равный более чем около 120 мин.
[877] В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах мышей, равный более чем около 120 мин.
[878] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 120 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 110 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 100 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 90 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 80 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 70 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 60 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 50 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 40 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 30 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 20 минут. В некоторых вариантах осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах крысы, равный более чем около 10 минут. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[879] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 360 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 350 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 325 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 310 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 300 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 290 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 250 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 200 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 150 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 100 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах человека, равный более чем около 80 минут. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[880] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 360 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 350 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 325 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 300 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 250 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 225 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 200 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 150 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 100 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 50 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах мышей, равный более чем около 30 минут. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[881] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 360 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 350 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 325 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 300 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 250 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 225 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 200 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 150 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 100 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 50 минут. В одном варианте осуществления настоящего изобретения соединения имеют in vitro период полураспада в гепатоцитах крысы, равный более чем около 30 минут. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[882] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 80 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 90 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 100 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 110 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 115 минут. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих, равный более чем 120 минут. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер. В одном варианте осуществления настоящего изобретения микросома млекопитающего представляет собой микросому человека или мыши.
[883] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 50 мин до около 200 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 80 мин до около 180 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 100 мин до около 160 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 110 мин до около 150 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 110 мин до около 140 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 110 мин до около 130 мин. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 115 мин до около 130 мин. В другом варианте осуществления настоящего изобретения соединения по настоящему раскрытию представляют собой любое соединение Таблиц A и B или их фармацевтически приемлемую соль, таутомер или стереоизомер, имеющие in vitro период полустабильности в микросомах млекопитающих в диапазоне от около 115 мин до около 130 мин. В одном варианте осуществления настоящего изобретения микросома млекопитающего представляет собой микросому человека или мыши.
[884] В одном варианте осуществления настоящего изобретения в настоящем описании предложены соединения, которые демонстрируют блокирование андроген-индуцированной ПСА-люциферазной активности (ПСА-люциферазный анализ). В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 4500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 4000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 3500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 3000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 2500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 2000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 950 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 900 нМ.
[885] В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 890 нМ, менее чем около 880 нМ, менее чем около 870 нМ, менее чем около 860 нМ, менее чем около 850 нМ, менее чем около 840 нМ, менее чем около 830 нМ, менее чем около 820 нМ, менее чем около 810 нМ или менее чем около 800 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 790 нМ, менее чем около 780 нМ, менее чем около 770 нМ, менее чем около 760 нМ, менее чем около 750 нМ, менее чем около 740 нМ, менее чем около 730 нМ, менее чем около 720 нМ, менее чем около 710 нМ или менее чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 690 нМ, менее чем около 680 нМ, менее чем около 670 нМ, менее чем около 660 нМ, менее чем около 650 нМ, менее чем около 640 нМ, менее чем около 630 нМ, менее чем около 620 нМ, менее чем около 610 нМ или менее чем около 600 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 590 нМ, менее чем около 580 нМ, менее чем около 570 нМ, менее чем около 560 нМ, менее чем около 550 нМ, менее чем около 540 нМ, менее чем около 530 нМ, менее чем около 520 нМ, менее чем около 510 нМ или менее чем около 500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 490 нМ, менее чем около 480 нМ, менее чем около 470 нМ, менее чем около 460 нМ, менее чем около 450 нМ, менее чем около 440 нМ, менее чем около 430 нМ, менее чем около 420 нМ, менее чем около 410 нМ или менее чем около 400 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 390 нМ, менее чем около 380 нМ, менее чем около 370 нМ, менее чем около 360 нМ, менее чем около 350 нМ, менее чем около 340 нМ, менее чем около 330 нМ, менее чем около 320 нМ, менее чем около 310 нМ или менее чем около 300 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 290 нМ, менее чем около 280 нМ, менее чем около 270 нМ, менее чем около 260 нМ, менее чем около 250 нМ, менее чем около 240 нМ, менее чем около 230 нМ, менее чем около 220 нМ, менее чем около 210 нМ или менее чем около 200 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 200 нМ. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[886] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равный более чем 80 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 2000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 90 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1500 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 100 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 105 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 900 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 110 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 850 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 115 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 800 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 115 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 750 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 120 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 120 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 650 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 120 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 600 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 120 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 550 нМ. В одном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro период полураспада в микросомах млекопитающих, равную более чем около 120 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 500 нМ. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер. В одном варианте осуществления настоящего изобретения микросома млекопитающего представляет собой микросому человека или мыши.
[887] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ и HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ, и HLM и MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ, и in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ, и in vitro метаболический клиренс в гепатоцитах человека и мыши, равный менее чем 4 мкл/мин/миллион клеток.
[888] В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ; a HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка; и in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 800 нМ; a HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка; и in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток. В другом варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, или соединения, указанные в Таблицах A и B, или их фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 700 нМ; a HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка; и in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток. В одном варианте осуществления настоящего изобретения соединение, выбранное из любого соединения Таблиц A и B, или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[889] В конкретном варианте осуществления соединения по настоящему раскрытию представляют собой любое соединение из Таблиц A и B или его фармацевтически приемлемую соль, таутомер или стереоизомер, причем соединения имеют in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 1000 нМ; HLM или MLM in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка; и in vitro метаболический клиренс в гепатоцитах человека или мыши, равный менее чем 4 мкл/мин/миллион клеток.
[890] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в НН, равный менее чем 4 мкл/мин/миллион клеток. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в НН, равный менее чем 4 мкл/мин/миллион клеток, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в HH, равный менее чем 4 мкл/мин/миллион клеток, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 675 нМ. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I) или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro период полураспада HH, равный менее чем около 350 минут. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro период полураспада в HH, равный более чем около 320 минут, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro период полураспада НН, равный более чем около 350 минут, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 700 нМ.
[891] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем 15 мкл/мин/мг белка. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в MLM, равный менее чем 15 мкл/мин/мг белка, и in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в MLM, равный менее чем 15 мкл/мин/мг белка, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 675 нМ. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в МН, равный менее чем 10 мкл/мин/миллион клеток. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в MH, равный менее чем 8 мкл/мин/миллион клеток. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в МН, равный менее чем 10 мкл/мин/миллион клеток, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в MH, равный менее чем 8 мкл/мин/миллион клеток, и in vitro IC50 в ПСА-люциферазном анализе, равную менее, чем около 675 нМ. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro период полураспада MLM, равный более чем около 100 минут. В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro период полураспада МН, равный более чем около 100 минут. В одном варианте осуществления настоящего изобретения соединения имеют in vitro период полураспада в МН, равный более чем около 180 минут.
[892] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемая соль, таутомер или стереоизомер, и причем соединения имеют in vitro метаболический клиренс в МН в диапазоне от 3 мкл/мин/миллион клеток до около 20 мкл/мин/миллион клеток. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в МН в диапазоне от 3,2 мкл/мин/миллион клеток до около 18 мкл/мин/миллион клеток. В одном варианте осуществления настоящего изобретения соединения имеют in vitro метаболический клиренс в МН в диапазоне от 3,4 мкл/мин/миллион клеток до около 17 мкл/мин/миллион клеток.
[893] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro IC50 в ПСА-люциферазном анализе, равную менее чем 650 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 640 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 635 нМ.
[894] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или их фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro IC50 в ПСА-люциферазном анализе в диапазоне от 200 нМ до около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50 в ПСА-люциферазном анализе в диапазоне от около 250 нМ до около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50 в ПСА-люциферазном анализе в диапазоне от около 300 нМ до около 700 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50 в ПСА-люциферазном анализе в диапазоне от около 350 нМ до около 675 нМ.
[895] В конкретном варианте осуществления настоящего изобретения соединения по настоящему изобретению представляют собой соединения, имеющие структуру формулы (I)-(VI) и/или (A)-(H-I), или его фармацевтически приемлемую соль, таутомер или стереоизомер, и причем соединения имеют in vitro IC50 в ПСА-люциферазном анализе, равную менее чем 525 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 500 нМ. В одном варианте осуществления настоящего изобретения соединения имеют in vitro IC50в ПСА-люциферазном анализе, равную менее, чем около 450 нМ.
Фармацевтические композиции и составы
[896] Настоящее раскрытие также включает в себя фармацевтические композиции для модуляции андрогенового рецептора (AR) у субъекта. В одном варианте осуществления настоящего изобретения фармацевтическая композиция содержит одно или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват.
[897] В одном варианте осуществления настоящего раскрытия фармацевтическая композиция содержит терапевтически эффективные количества одного или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват.
[898] В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из Таблицы A, или их фармацевтически приемлемую соль или сольват. В одном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из Таблицы В, или их фармацевтически приемлемую соль или сольват.
[899] В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A3, A5, A7, A13, A17, A18, A22, A23, A24, A25, A28, A30, A31, A32, A34, A35, A38, A40, A41, A42, A45, A49, A52, A53, A54, A56, A57, A58, A62, A63, A64, A65, A68, A73, A74, A75, A76, B1, B2, B3 или B6 или их фармацевтически приемлемую соль или сольват. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A1, A2, A4, A6, A8, A9, A10, A11, A12, A14, A15, A16, A19, A20, A21, A26, A27, A29, A33, A36, A37, A39, A43, A44, A46, A47, A48, A50, A51, A55, A59, A60, A61, A66, A67, A69, A70, A71, A72, A77, A78, A79, A80, A81, A82, A83, A84, A85, A86, A87, A88, A89, A90, A91, A92, A93, A94, A95, A96, A97, B4, B5, B7, B8, B9, B10 или B11 или их фармацевтически приемлемую соль или сольват. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A98-A186. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A187-A211. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A212-A234. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A1-A96, A98-A116, A118-A159, A161-A175 и A177-A234. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A13, A57, A74, A93, A109, A112, A122, A126, A131, A134, A136, A137, A164, A168, A169, A170, A171, A172, A184, A185, A195 и/или A204, или их фармацевтически приемлемую соль, таутомер, стереоизомер или пролекарство. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A1-A211 или B1-B11. В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержит одно или более соединений, выбранных из соединений A1-A234 или B1-B11.
[900] В одном варианте осуществления настоящего изобретения фармацевтическая композиция, как описано в данном документе, содержащая одно или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват, дополнительно содержит один или более дополнительных терапевтически активных агентов. В одном варианте осуществления настоящего изобретения один или более дополнительных терапевтически активных агентов выбраны из терапевтических средств, используемых для лечения рака, неврологического заболевания, расстройства, характеризующегося аномальным накоплением α-синуклеина, нарушения процесса старения, сердечно-сосудистого заболевания, бактериальной инфекции, вирусной инфекции, митохондриальносвязанного заболевания, умственной отсталости, глухоты, слепоты, диабета, ожирения, аутоиммунного заболевания, глаукомы, наследственной оптической невропатии Лебера и ревматоидного артрита.
[901] В некоторых вариантах осуществления настоящего изобретения один или более дополнительных терапевтических агентов представляют собой ингибитор поли(АДФ-рибоза)полимеразы (PARP), включая, помимо прочего, олапариб, нирапариб, рукапариб, талазопариб; ингибитор лигандсвязывающего домена андрогенового рецептора, включая, но не ограничиваясь ими, энзалутамид, апалутамид, даролутамид, бикалутамид, нилутамид, флутамид, ODM-204, TAS3681; ингибитор CYP17, включая, помимо прочего, галетерон, абиратерон, ацетат абиратерона; ингибитор микротрубочек, включая, но не ограничиваясь ими, доцетаксел, паклитаксел, кабазитаксел (XRP-6258); модулятор PD-1 или PD-L1, включая, не ограничиваясь ими, пембролизумаб, дурвалумаб, ниволумаб, атезолизумаб; агонист гонадотропин-высвобождающего гормона, включая, но не ограничиваясь ими, ацетат ципротерона, лейпролид; ингибитор 5-альфа-редуктазы, включая, но не ограничиваясь ими, финастерид, дутастерид, туростерид, бекслостерид, изонстерид, FCE 28260, SKF105,111; ингибитор фактора роста эндотелия сосудов, включая, но не ограничиваясь ими, бевацизумаб (Авастин); ингибитор гистондеацетилазы, включая, но не ограничиваясь ими, OSU-HDAC42; ингибитор интегрина альфа-v-бета-3, включая, но не ограничиваясь ими, ВИТАКСИН; ингибитор рецептора тирозинкиназы, включая, но не ограничиваясь ими, сунитумиб; ингибитор фосфоинозитид-3-киназы, включая, но не ограничиваясь ими, алпелисиб, бупарлисиб, идеалисиб; ингибитор киназы анапластической лимфомы (ALK), включая, но не ограничиваясь ими, кризотиниб, алектиниб; антагонист рецептора эндотелина А, включая, но не ограничиваясь ими, ZD-4054; ингибитор против CTLA4, включая, но не ограничиваясь ими, MDX-010 (ипилимумаб); ингибитор белка теплового шока 27 (HSP27), включая, но не ограничиваясь, OGX 427; деструктор андрогеновых рецепторов, включая, но не ограничиваясь ими, ARV-330, ARV-110; ингибитор ДНК-связывающего домена андрогеновых рецепторов, включая, но не ограничиваясь, VPC-14449; ингибитор бромдомена и экстра-терминального мотива (BET), включая, но не ограничиваясь ими, BI-894999, GSK25762, GS-5829; ингибитор N-концевого домена андрогенового рецептора, включая, но не ограничиваясь ими, синтокамид; радиоактивный терапевтический агент, излучающий альфа-частицы, включая, но не ограничиваясь ими, радий-233 или его соль; никлозамид; или их родственные соединения; селективный модулятор эстрогенового рецептора (SERM), включая, но не ограничиваясь ими, тамоксифен, ралоксифен, торемифен, арзоксифен, базедоксифен, пипиндоксифен, лазофоксифен, энкломифен; селективный деструктор эстрогенового рецептора (SERD), включая, но не ограничиваясь ими, фулвестрант, ZB716, OP-1074, эласестрант, AZD9496, GDC0810, GDC0927, GW5638, GW7604; ингибитор ароматазы, включая, но не ограничиваясь ими, анастразол, экземестан, летрозол; селективные модуляторы прогестеронового рецептора (SPRM), включая, но не ограничиваясь ими, мифепристон, лонаприсон, онапристон, асоприснил, лонаприснил, улипристал, телапристон; ингибитор глюкокортикоидного рецептора, включая, но не ограничиваясь ими, мифепристон, COR108297, COR125281, ORIC-101, PT150; ингибиторы CDK4/6, включая пальбоциклиб, абемациклиб, рибоциклиб; антагонист рецептора HER2, включая, но не ограничиваясь ими, трастузумаб, нератиниб; мишень для млекопитающих ингибитора рапамицина (mTOR), включая, но не ограничиваясь ими, эверолимус, темсиролимус.
[902] В дополнительном варианте осуществления настоящего раскрытия фармацевтическая композиция, содержащая одно или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват, и фармацевтически приемлемый наполнитель или адъювант. Фармацевтически приемлемые эксципиенты и адъюванты добавляют в композицию или препарат для различных целей. В другом варианте осуществления настоящего изобретения фармацевтическая композиция, содержащая одно или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват, дополнительно содержит фармацевтически приемлемый носитель. В одном варианте осуществления изобретения фармацевтически приемлемый носитель включает фармацевтически приемлемый эксципиент, связующее и/или разбавитель. В одном варианте осуществления изобретения, пригодные фармацевтически приемлемые эксципиенты включают, но не ограничиваются ими, воду, солевые растворы, спирт, полиэтиленгликоли, желатин, лактозу, амилазу, стеарат магния, тальк, кремниевую кислоту, вязкий парафин, гидроксиметилцеллюлозу и поливинилпирролидон.
[903] В определенных вариантах осуществления изобретения фармацевтические композиции по данному изобретению могут дополнительно содержать другие вспомогательные компоненты, обычно встречающиеся в фармацевтических композициях, при их установленных уровнях техники. Так, например, фармацевтические композиции могут содержать дополнительные совместимые фармацевтически активные материалы, такие как, например, противозудные, вяжущие средства, местные анестетики или противовоспалительные агенты, или могут содержать дополнительные материалы, пригодные для физического составления различных лекарственных форм композиций по данному изобретению, такие как красители, вкусовые агенты, консерванты, антиоксиданты, замутнители, загустители и стабилизаторы. Однако такие материалы при добавлении не должны чрезмерно влиять на биологическую активность компонентов композиций по данному изобретению. Препараты могут быть стерилизованы и, если необходимо, смешаны со вспомогательными агентами, например, смазывающими веществами, консервантами, стабилизаторами, смачивающими агентами, эмульгаторами, солями для воздействия на осмотическое давление, буферами, красителями, ароматизаторами и/или ароматическими веществами и т. п., которые разрушительно не взаимодействуют с олигонуклеотидом (-ами) препаратом.
[904] Для целей этого раскрытия соединения по настоящему раскрытию могут быть составлены для введения разнообразными способами, включая пероральный, парентеральный, с помощью ингаляционного спрея, местный или ректальный в составах, содержащих фармацевтически приемлемые носители, адъюванты и несущие среды. Термин «парентеральный» в контексте данного документа включает подкожные, внутривенные, внутримышечные и внутриартериальные инъекции с использованием различных техник инфузии. В контексте данного документа внутриартериальная и внутривенная инъекция включает введение через катетеры.
[905] Раскрытые в данном документе соединения могут быть составлены в соответствии с обычными процедурами, адаптированными для желаемого пути введения. Соответственно, соединения, описанные в данном документе, могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать формулирующие агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Раскрытые в данном документе соединения также могут быть составлены в виде препарата для имплантации или инъекции. Таким образом, например, соединения могут быть составлены с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами или в виде труднорастворимых производных (например, в виде труднорастворимой соли). В качестве альтернативы, активный ингредиент может быть представлен в виде порошка для смешивания с подходящим носителем, например, стерильной апирогенной водой, перед использованием. Подходящие составы для каждого из этих способов введения можно найти, например, в Remington: The Science and Practice of Pharmacy, A. Gennaro, ed., 20-е издание, Lippincott, Williams & Wilkins, Филадельфия, Пенсильвания.
[906] В определенных вариантах осуществления фармацевтическую композицию по настоящему изобретению получают с использованием известных методик, включая, но не ограничиваясь ими, процессы смешивания, растворения, гранулирования, изготовления драже, отмучивания, эмульгирования, инкапсулирования, улавливания или таблетирования.
[907] В одном варианте осуществления настоящего изобретения в настоящем описании представлена фармацевтическая композиция, содержащая соединение формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват, как раскрыто в данном документе, в сочетании с фармацевтически приемлемым носителем. В одном варианте осуществления настоящего изобретения подходящие фармацевтически приемлемые носители включают, но не ограничиваются ими, инертные твердые наполнители или разбавители и стерильные водные или органические растворы. Фармацевтически приемлемые носители хорошо известны специалистам в данной области и включают, но не ограничиваются ими, от около 0,01 до около 0,1 М и предпочтительно 0,05 М фосфатного буфера или 0,8% физиологического раствора. Такие фармацевтически приемлемые носители могут быть водными или неводными растворами, суспензиями и эмульсиями. Примеры неводных растворителей, подходящих для использования в настоящей заявке, включают, но не ограничиваются ими, пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и органические сложные эфиры для инъекций, такие как этилолеат.
[908] Водные носители, подходящие для использования в настоящей заявке, включают в себя, но не ограничиваются ими, воду, этанол, спиртовые/водные растворы, глицерин, эмульсии или суспензии, включая физиологический раствор и забуференные среды. Пероральные носители могут быть эликсирами, сиропами, капсулами, таблетками и т. п.
[909] Жидкие носители, подходящие для использования в настоящей заявке, можно использовать при приготовлении растворов, суспензий, эмульсий, сиропов, эликсиров и соединений под давлением. Активный ингредиент может быть растворен или суспендирован в фармацевтически приемлемом жидком носителе, таком как вода, органический растворитель, смесь обоих или фармацевтически приемлемых масел или жиров. Жидкий носитель может содержать другие подходящие фармацевтические добавки, такие как солюбилизаторы, эмульгаторы, буферы, консерванты, подсластители, ароматизаторы, суспендирующие агенты, загустители, красители, регуляторы вязкости, стабилизаторы или регуляторы осмоса.
[910] Жидкие носители, подходящие для использования в настоящей заявке, включают в себя, но не ограничиваются ими, воду (частично содержащую добавки, как указано выше, например, производные целлюлозы, предпочтительно раствор карбоксиметилцеллюлозы натрия), спирты (включая одноатомные спирты и многоатомные спирты, например гликоли) и их производные и масла (например, фракционированное кокосовое масло и арахисовое масло). Для парентерального введения носитель может также включать в себя маслянистый эфир, такой как этилолеат и изопропилмиристат. Стерильные жидкие носители являются подходящими для стерильной жидкой формы, содержащей соединения для парентерального введения. Раскрытый в данном документе жидкий носитель для соединений под давлением может быть галогенированным углеводородом или другим фармацевтически приемлемым пропеллентом.
[911] Твердые носители, подходящие для использования в настоящей заявке, включают в себя, но не ограничиваются ими, инертные вещества, такие как лактоза, крахмал, глюкоза, метилцеллюлоза, стеарат магния, дикальцийфосфат, маннит и тому подобное. Твердый носитель может дополнительно включать в себя одно или более веществ, действующих как ароматизаторы, лубриканты, солюбилизаторы, суспендирующие агенты, наполнители, вещества, глиданты, вспомогательные средства для прессования, связующие или разрыхляющие агенты для таблеток; это также может быть инкапсулирующий материал. В порошках носитель может быть тонкоизмельченным твердым веществом, которое находится в смеси с мелкодисперсным активным соединением. В таблетках активное соединение смешивают с носителем, имеющим необходимые свойства сжатия, в подходящих пропорциях и прессуют до желаемой формы и размера. Порошки и таблетки предпочтительно содержат до 99% активного соединения. Подходящие твердые носители включают в себя, например, фосфат кальция, стеарат магния, тальк, сахара, лактозу, декстрин, крахмал, желатин, целлюлозу, поливинилпирролидин, легкоплавкие воски и ионообменные смолы. Таблетку можно получать путем прессования или формовки, необязательно, с одним или несколькими вспомогательными ингредиентами. Прессованные таблетки могут быть приготовлены путем прессования в подходящем устройстве активного ингредиента в сыпучей форме, такой как порошок или гранулы, необязательно смешанных со связующим (например, повидоном, желатином, гидроксипропилметилцеллюлозой), лубрикантом, инертным разбавителем, консервантом, разрыхлителем (например, натрия гликоляткрахмала, поперечно-сшитый повидон, поперечно-сшитая карбоксиметилцеллюлоза натрия) поверхностно-активный или диспергирующий агент. Формованные таблетки могут быть изготовлены путем формования в подходящем аппарате смеси порошкообразного соединения, увлажненного инертным жидким разбавителем. Таблетки необязательно могут быть покрыты оболочкой, или на них могут быть сделаны насечки, или они могут быть составлены так, чтобы обеспечить медленное или контролируемое высвобождение из них активного ингредиента, используя, например, гидроксипропилметилцеллюлозу в разных соотношениях для достижения желаемого профиля высвобождения. Таблетки могут быть необязательно покрыты энтеросолюбильными оболочками для обеспечения высвобождения в областях пищеварительного тракта, иных, чем желудок.
[912] Парентеральные носители, подходящие для использования в настоящей заявке, включают, но не ограничиваются ими, раствор хлорида натрия, раствор Рингера с декстрозой, декстрозу и хлорид натрия, лактат Рингера и жирные масла. Внутривенные носители включают в себя добавки для восполнения жидкости и питательных веществ, добавки для восполнения электролитов, например такие, которые основаны на декстрозе Рингера и т. п. Также могут присутствовать консерванты и другие добавки, такие как, например, противомикробные средства, антиоксиданты, хелатирующие агенты, инертные газы и тому подобное.
[913] Носители, подходящие для использования в настоящей заявке, можно при необходимости смешивать с разрыхлителями, разбавителями, гранулирующими агентами, смазывающими веществами, связующими веществами и т. п. с использованием обычных методик, известных в данной области. Носители также можно стерилизовать с использованием способов, которые не вступают в деструктивную реакцию с соединениями, как это обычно известно в данной области.
[914] К композициям по настоящему изобретению могут быть добавлены разбавители. Разбавители увеличивают объем твердой фармацевтической композиции и/или комбинации и могут облегчить обращение с фармацевтической дозированной формой, содержащей композицию и/или комбинацию, для пациента и лица, осуществляющего уход. Разбавители для твердых композиций и/или комбинаций включают в себя, например, микрокристаллическую целлюлозу (например, AVICEL), мелкодисперсную целлюлозу, лактозу, крахмал, прежелатинизированный крахмал, карбонат кальция, сульфат кальция, сахар, декстраты, декстрин, декстрозу, дигидрат двухосновного фосфата кальция, трехосновный фосфат кальция, каолин, карбонат магния, оксид магния, мальтодекстрин, маннит, полиметакрилаты (например, EUDRAGIT(r)), хлорид калия, порошкообразную целлюлозу, хлорид натрия, сорбит и тальк.
[915] Дополнительные варианты осуществления относятся к фармацевтическим составам, в которых состав выбран из группы, состоящей из твердого вещества, порошка, жидкости и геля. В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению представляет собой твердое вещество (например, порошок, таблетку, капсулу, грануляты и/или агрегаты). В определенных из таких вариантов осуществления твердая фармацевтическая композиция, содержащая один или более ингредиентов, известных в данной области, включая, но не ограничиваясь ими, крахмалы, сахара, разбавители, гранулирующие агенты, смазывающие вещества, связующие и дезинтегрирующие агенты.
[916] Твердые фармацевтические композиции, прессованные в лекарственную форму, такую как таблетка, могут включать в себя вспомогательные вещества, функции которых включают помощь в связывании активного ингредиента и других вспомогательных веществ после прессования. Связующие вещества для твердых фармацевтических композиций и/или комбинаций включают в себя гуммиарабик, альгиновую кислоту, карбомер (например, карбопол), карбоксиметилцеллюлозу натрия, декстрин, этилцеллюлозу, желатин, гуаровую камедь, трагакантовую камедь, гидрированное растительное масло, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу (например, KLUCEL), гидроксипропилметилцеллюлозу (например, METHOCEL), жидкую глюкозу, алюмосиликат магния, мальтодекстрин, метилцеллюлозу, полиметакрилаты, повидон (например, KOLLIDON, PLASDONE), прежелатинизированный крахмал, альгинат натрия и крахмал.
[917] Скорость растворения уплотненной твердой фармацевтической композиции в желудке пациента может быть увеличена путем добавления разрыхлителя к композиции и/или комбинации. Разрыхлители включают альгиновую кислоту, карбоксиметилцеллюлозу кальция, карбоксиметилцеллюлозу натрия (например, AC-DI-SOL и PRIMELLOSE), коллоидный диоксид кремния, кроскармеллозу натрия, кросповидон (например, KOLLIDON и POLYPLASDONE), гуаровую камедь, силикат магния и алюминия, микрокристаллическую целлюлозу, метилцеллюлозу, полакрилин калия, порошкообразнаую целлюлозу, прежелатинизированный крахмал, альгинат натрия, натрия гликоляткрахмала (например, EXPLOTAB), картофельный крахмал и крахмал.
[918] Глиданты могут быть добавлены для улучшения текучести неуплотненной твердой композиции и/или комбинации и для повышения точности дозирования. Вспомогательные вещества, которые могут действовать как глиданты, включают коллоидный диоксид кремния, трисиликат магния, порошкообразную целлюлозу, крахмал, тальк и трехосновный фосфат кальция.
[919] Когда лекарственную форму, такую как таблетка, изготавливают путем прессования порошковой композиции, композицию подвергают давлению со стороны пуансона и красителя. Некоторые эксципиенты и активные ингредиенты имеют тенденцию прилипать к поверхностям пуансона и красителя, что может вызвать точечную коррозию продукта и другие неровности поверхности. В композицию и/или комбинацию можно добавить лубрикант для уменьшения адгезии и облегчения высвобождения продукта из красителя. Лубриканты включают в себя стеарат магния, стеарат кальция, глицерилмоностеарат, глицерилпальмитостеарат, гидрированное касторовое масло, гидрированное растительное масло, минеральное масло, полиэтиленгликоль, бензоат натрия, лаурилсульфат натрия, стеарилфумарат натрия, стеариновую кислоту, тальк и стеарат цинка.
[920] Ароматизаторы и усилители вкуса делают лекарственную форму более вкусной для пациента. Общие ароматизаторы и усилители вкуса для фармацевтических продуктов, которые могут быть включены в композицию и/или комбинацию по настоящему изобретению, включают в себя мальтол, ванилин, этилванилин, ментол, лимонную кислоту, фумаровую кислоту, этилмальтол и винную кислоту.
[921] Твердые и жидкие композиции также могут быть окрашены с использованием любого фармацевтически приемлемого красителя для улучшения их внешнего вида и/или облегчения идентификации пациентом продукта и уровня стандартной дозировки.
[922] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению представляет собой жидкость (например, суспензию, эликсир и/или раствор). В определенных из таких вариантов осуществления жидкую фармацевтическую композицию готовят с использованием ингредиентов, известных в данной области, включая, помимо прочего, воду, гликоли, масла, спирты, ароматизаторы, консерванты и красители.
[923] Жидкие фармацевтические композиции могут быть приготовлены с использованием соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемой соли или сольвата, а также любых других твердых эксципиентов, в которых компоненты растворены или суспендированы в жидком носителе, таком как вода, растительное масло, спирт, полиэтиленгликоль, пропиленгликоль или глицерин.
[924] Например, составы для парентерального введения могут содержать в качестве обычных эксципиентов стерильную воду или физиологический раствор, полиалкиленгликоли, такие как полиэтиленгликоль, масла растительного происхождения, гидрированные нафталины и т. п. В частности, биосовместимый, биоразлагаемый лактидный полимер, сополимер лактида/гликолида или сополимеры полиоксиэтилена и полиоксипропилена могут быть подходящими наполнителями для контроля высвобождения активных соединений. Другие потенциально пригодные парентеральные системы доставки включают в себя частицы сополимера этилен-винилацетата, осмотические насосы, имплантируемые инфузионные системы и липосомы. Составы для ингаляционного введения содержат в качестве эксципиентов, например, лактозу или могут представлять собой водные растворы, содержащие, например, полиоксиэтилен-9-ауриловый эфир, гликохолат и деоксихолат, или масляные растворы для введения в форме капель для носа или в виде геля для нанесения интраназально. Составы для парентерального введения также могут включать в себя гликохолат для буккального введения, метоксалицилат для ректального введения или лимонную кислоту для вагинального введения.
[925] Жидкие фармацевтические композиции могут содержать эмульгирующие агенты для равномерного диспергирования по всей композиции и/или комбинации активного ингредиента или другого эксципиента, который не растворим в жидком носителе. Эмульгирующие агенты, которые могут быть подходящими для жидких композиций и/или комбинаций по настоящему изобретению, включают в себя, например, желатин, яичный желток, казеин, холестерин, гуммиарабик, трагакант, хондрус, пектин, метилцеллюлозу, карбомер, цетостеариловый спирт и цетиловый спирт.
[926] Жидкие фармацевтические композиции могут также содержать агент, повышающий вязкость, для улучшения ощущения продукта во рту и/или покрытия слизистой оболочки желудочно-кишечного тракта. Такие агенты включают в себя гуммиарабик, бентонит альгиновой кислоты, карбомер, карбоксиметилцеллюлозу кальция или натрия, цетостеариловый спирт, метилцеллюлозу, этилцеллюлозу, желатин-гуаровую камедь, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, мальтодекстрин, поливиниловый спирт, повидон, пропиленкарбонат, альгинат пропиленгликоля, альгинат натрия, натрия гликоляткрахмала, трагакант крахмала и ксантановая камедь.
[927] Для улучшения вкуса могут быть добавлены подсластители, такие как аспартам, лактоза, сорбит, сахарин, сахарин натрия, сахароза, аспартам, фруктоза, маннит и инвертный сахар.
[928] Консерванты и хелатирующие агенты, такие как спирт, бензоат натрия, бутилированный гидроксилтолуол, бутилированный гидроксианизол и этилендиаминтетрауксусная кислота, могут быть добавлены в количествах, безопасных для проглатывания, для повышения стабильности при хранении.
[929] Жидкая композиция также может содержать буфер, такой как глюконовая кислота, молочная кислота, лимонная кислота или уксусная кислота, глюконат натрия, лактат натрия, цитрат натрия или ацетат натрия. Выбор эксципиентов и используемых количеств может быть легко определен специалистом по рецептуре на основе опыта и рассмотрения стандартных процедур и справочных материалов в данной области.
[930] В одном варианте осуществления настоящего изобретения фармацевтическую композицию готовят для введения путем инъекции (например, внутривенного, подкожного, внутримышечного и т. д.). В определенных из таких вариантов осуществления фармацевтическая композиция содержит носитель и приготовлена в водном растворе, таком как вода, или физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или физиологический солевой буфер. В определенных вариантах осуществления включены другие ингредиенты (например, ингредиенты, которые способствуют растворимости или служат в качестве консервантов). В некоторых вариантах осуществления суспензии для инъекций готовят с использованием подходящих жидких носителей, суспендирующих агентов и т. п. Определенные фармацевтические композиции для инъекций представлены в стандартной лекарственной форме, например, в ампулах или в контейнерах для нескольких доз. Определенные фармацевтические композиции для инъекций представляют собой суспензии, растворы или эмульсии в масляных или водных носителях и могут содержать составные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Определенные растворители, подходящие для использования в фармацевтических композициях для инъекций, включают в себя, но не ограничиваются ими, липофильные растворители и жирные масла, такие как кунжутное масло, синтетические сложные эфиры жирных кислот, такие как этилолеат, или триглицериды, и липосомы. Водные суспензии для инъекций могут содержать вещества, которые увеличивают вязкость суспензии, такие как натрий-карбоксиметилцеллюлоза, сорбит или декстран. Необязательно, такие суспензии могут также содержать подходящие стабилизаторы или агенты, которые увеличивают растворимость фармацевтических агентов, что позволяет приготовить высококонцентрированные растворы.
[931] Стерильный препарат для инъекций может также представлять собой стерильный раствор или суспензию для инъекций в нетоксичном парентерально приемлемом разбавителе или растворителе, таком как раствор в 1,3-бутандиоле, или приготовленный в виде лиофилизированного порошка. К приемлемым носителям и растворителям, которые можно использовать, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла можно обычно использовать в качестве растворителя или суспендирующей среды. Для этой цели можно использовать любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, аналогичным образом могут использоваться при приготовлении инъекционных препаратов. Составы для внутривенного введения могут включать в себя растворы в стерильном изотоническом водном буфере. Когда существуют необходимости, составы могут также содержать солюбилизирующее средство и местный анестетик для облегчения боли в месте инъекции. Обычно ингредиенты в единичную дозированную форму вводятся по отдельности или смешанными вместе, например в виде сухого лиофилизированного порошка или безводного концентрата в герметически закрытом контейнере, таком как ампула или саше, с указанием количества действующего вещества. Если соединение должно вводиться путем инфузии, оно может быть распределено в составе с бутылкой для инфузии, содержащей стерильную воду фармацевтического качества, физиологический раствор или декстрозу/воду. Когда соединение вводят путем инъекции, то может прилагаться ампула стерильной воды для инъекций или солевой раствор, чтобы ингредиенты можно было смешивать перед введением.
[932] Подходящие составы дополнительно включают в себя водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатики, бактерицидные антибиотики и растворенные вещества, которые придают составу изотоничность жидкостям организма предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать в себя суспендирующие агенты и загустители.
[933] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению составлена в виде препарата пролонгированного действия. Определенные такие депо-препараты обычно действуют дольше, чем не-депо-препараты. В определенных вариантах осуществления такие препараты вводят имплантацией (например, подкожно или внутримышечно) или внутримышечной инъекцией. В определенных вариантах осуществления депо-препараты получают с использованием подходящих полимерных или гидрофобных материалов (например, эмульсии в приемлемом масле) или ионообменных смол или в виде труднорастворимых производных, например, в виде труднорастворимой соли.
[934] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению содержит систему доставки. Примеры систем доставки включают в себя, но не ограничиваются ими, липосомы и эмульсии. Определенные системы доставки применимы для приготовления определенных фармацевтических композиций, включая композиции, содержащие гидрофобные соединения. В определенных вариантах осуществления используют определенные органические растворители, такие как диметилсульфоксид.
[935] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению содержит систему сорастворителей. Некоторые из таких систем сорастворителей включают в себя, например, бензиловый спирт, неполярное поверхностно-активное вещество, смешивающийся с водой органический полимер и водную фазу. В определенных вариантах осуществления такие системы сорастворителей используют для гидрофобных соединений. Неограничивающим примером такой системы сорастворителей является система сорастворителей VPD, которая представляет собой раствор абсолютного этанола, содержащий 3% мас./об. бензилового спирта, 8% мас./об. неполярного поверхностно-активного вещества полисорбата 80 и 65% мас./об. полиэтиленгликоля 300. Пропорции таких систем сорастворителей можно значительно варьировать без значительного изменения их характеристик растворимости и токсичности. Кроме того, идентичность компонентов сорастворителей может варьироваться: например, вместо полисорбата 80 можно использовать другие поверхностно-активные вещества; фракционный размер полиэтиленгликоля может варьироваться; другие биосовместимые полимеры могут заменять полиэтиленгликоль, например, поливинилпирролидон; и другие сахара или полисахариды могут заменять декстрозу.
[936] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению включает в себя систему с замедленным высвобождением. Неограничивающим примером такой системы с замедленным высвобождением является полупроницаемая матрица из твердых гидрофобных полимеров. В определенных вариантах осуществления системы с замедленным высвобождением могут, в зависимости от их химической природы, высвобождать фармацевтические агенты в течение часов, дней, недель или месяцев.
[937] Подходящие фармацевтические композиции по настоящему изобретению могут быть определены в соответствии с любым клинически приемлемым путем введения композиции субъекту. Способ введения композиции частично зависит от причины и/или места. Специалист в данной области признает преимущества определенных путей введения. Способ включает введение эффективного количества агента или соединения (или композиции, содержащей агент или соединение) для достижения желаемого биологического ответа, например количества, эффективного для облегчения, улучшения или предотвращения, полностью или частично, симптома состояния, требующего лечения, например, онкологические и неврологические расстройства. В разнообразных аспектах путь введения является системным, например, пероральным или путем инъекции. Агенты или соединения или их фармацевтически приемлемые соли или производные вводят перорально, назально, трансдермально, легочно, ингаляционно, буккально, сублингвально, внутрибрюшинно, подкожно, внутримышечно, внутривенно, ректально, внутриплеврально, интратекально, внутрипортально и парентерально. Альтернативно или дополнительно, путь введения является местным, например местным, внутриопухолевым и периопухолевым. В некоторых вариантах осуществления настоящего изобретения соединение вводят перорально.
[938] В определенных вариантах осуществления фармацевтическая композиция по настоящему изобретению приготовлена для перорального введения. В определенных из таких вариантов осуществления фармацевтическую композицию составляют путем комбинирования одного или более агентов и фармацевтически приемлемых носителей. Определенные из таких носителей позволяют составлять фармацевтические композиции в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, суспензий, суспензий и т. п. для перорального приема субъектом. Подходящие вспомогательные вещества включают в себя, но не ограничиваясь ими, наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; препараты целлюлозы, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовую камедь, метилцеллюлозу, гидроксипропилметилцеллюлозу, натриевую соль карбоксиметилцеллюлозы и/или поливинилпирролидон (PVP). В определенных вариантах осуществления такую смесь необязательно измельчают и необязательно добавляют вспомогательные вещества. В определенных вариантах осуществления фармацевтические композиции формируют с получением таблеток или ядер драже. В определенных вариантах осуществления добавляют разрыхлители (например, сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия).
[939] В определенных вариантах осуществления ядра драже имеют покрытия. В определенных таких вариантах осуществления могут использовать концентрированные растворы сахаров, которые могут необязательно содержать гуммиарабик, тальк, поливинилпирролидон, карбопол-гель, полиэтиленгликоль и/или диоксид титана, растворы лаков и подходящие органические растворители или смеси растворителей. В покрытия таблеток или драже могут быть добавлены красители или пигменты.
[940] В определенных вариантах осуществления фармацевтические композиции для перорального введения представляют собой капсулы из желатина с плотной посадкой. Определенные из таких вставляемых капсул содержат один или более фармацевтических агентов по настоящему изобретению в смеси с одним или более наполнителями, такими как лактоза, связующими веществами, такими как крахмалы, и/или лубрикантами, такими как тальк или стеарат магния, и, необязательно, стабилизаторами. В определенных вариантах осуществления фармацевтические композиции для перорального введения представляют собой мягкие герметичные капсулы из желатина и пластификатора, такого как глицерин или сорбит. В определенных мягких капсулах один или более фармацевтических агентов по настоящему изобретению растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, могут быть добавлены стабилизаторы.
[941] В определенных вариантах осуществления фармацевтические композиции готовят для буккального введения. Определенные из таких фармацевтических композиций представляют собой таблетки или пастилки, приготовленные обычным способом.
[942] В определенных вариантах осуществления фармацевтическая композиция приготовлена для чрескожного введения. В определенных из таких вариантах осуществления в композиции используются обеспечивающие проникновение вещества, подходящие для проницаемого барьера. Такие пенетранты обычно известны в данной области техники.
[943] В определенных вариантах осуществления фармацевтическую композицию готовят для введения путем ингаляции. Определенные из таких фармацевтических композиций для ингаляции готовят в форме аэрозольного спрея в герметичной упаковке или небулайзере. Некоторые из таких фармацевтических композиций содержат пропеллент, например дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ. В определенных вариантах осуществления используя аэрозоль под давлением, дозированная единица может быть определена с помощью клапана, который подает отмеренное количество. В определенных вариантах осуществления могут быть составлены капсулы и картриджи для использования в ингаляторе или инсуффляторе. Определенные из таких составов содержат порошковую смесь фармацевтического агента по данному изобретению и подходящую порошковую основу, такую как лактоза или крахмал.
[944] В других вариантах осуществления соединение по настоящему изобретению вводят внутривенным путем. В дополнительных вариантах осуществления парентеральное введение могут осуществлять болюсным или инфузионным способом.
[945] В определенных вариантах осуществления фармацевтическую композицию готовят для ректального введения, такую как суппозиторий или удерживающая клизма. Определенные из таких фармацевтических композиций содержат известные ингредиенты, такие как масло какао и/или другие глицериды.
[946] В определенных вариантах осуществления фармацевтическая композиция приготовлена для местного применения. Определенные из таких фармацевтических композиций содержат мягкие увлажняющие основы, такие как мази или кремы. Иллюстративные примеры подходящих мазевых основ включают в себя, но не ограничиваются ими, вазелин, вазелин плюс летучие силиконы и ланолина, и эмульсии воды в масле. Иллюстративные примеры подходящих кремовых основ включают в себя, но не ограничиваются ими, холодный крем и гидрофильную мазь.
[947] В определенных вариантах осуществления терапевтически эффективное количество достаточно для предотвращения, облегчения или ослабления симптомов заболевания или для продления выживаемости субъекта, подвергаемого лечению. Определение терапевтически эффективного количества находится в пределах компетенции специалистов в данной области техники.
[948] В определенных вариантах осуществления одно или более соединений формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемая соль или сольват составлены в виде пролекарства. В определенных вариантах осуществления при введении in vivo пролекарство химически превращается в биологически, фармацевтически или терапевтически более активную форму. В определенных вариантах осуществления пролекарства являются пригодными, потому что их легче вводить, чем соответствующую активную форму. Например, в определенных случаях пролекарство может быть более биодоступным (например, при пероральном введении), чем соответствующая активная форма. В определенных случаях пролекарство может иметь улучшенную растворимость по сравнению с соответствующей активной формой. В определенных вариантах осуществления пролекарства являются менее растворимыми в воде, чем соответствующая активная форма. В определенных случаях такие пролекарства обладают превосходной способностью проникать через клеточные мембраны, причем растворимость в воде отрицательно сказывается на подвижности. В определенных вариантах осуществления пролекарство представляет собой сложный эфир. В определенных из таких вариантов осуществления сложный эфир метаболически гидролизуется до карбоновой кислоты при введении. В определенных случаях соединение, содержащее карбоновую кислоту, является соответствующей активной формой. В определенных вариантах осуществления пролекарство включает в себя короткий пептид (полиаминокислоту), связанный с кислотной группой. В определенных таких вариантах осуществления при введении пептид расщепляется с образованием соответствующей активной формы.
[949] В определенных вариантах осуществления пролекарство получают путем модификации фармацевтически активного соединения таким образом, чтобы активное соединение регенерировалось при введении in vivo. Пролекарственный препарат может быть разработан с возможностью изменять метаболическую стабильность или характеристики транспорта лекарственного препарата, маскировать побочные эффекты или токсичность, улучшать вкусовые качества лекарственного препарата или изменять другие характеристики или свойства лекарственного препарата. Благодаря знанию фармакодинамических процессов и метаболизма лекарственных препаратов in vivo, специалисты в данной области после того, как будет известно фармацевтически активное соединение, смогут разработать пролекарственные препараты данного соединения (см., например, Nogrady (1985) Medicinal Chemistry A Biochemical Approach, Oxford University Press, New York, pages 388-392).
[950] В разнообразных аспектах количество соединения формулы (I)-(VI) и/или (A)-(H-I) или их фармацевтически приемлемую соль или сольват или соединения, раскрытые в Таблицах A и B, или их фармацевтически приемлемую соль или сольват, можно вводить от около 0,001 мг/кг до около 100 мг/кг веса тела (например, от около 0,01 мг/кг до около 10 мг/кг или от около 0,1 мг/кг до около 5 мг/кг).
[951] Концентрация описанного соединения в фармацевтически приемлемой смеси будет варьироваться в зависимости от нескольких факторов, включая дозировку вводимого соединения, фармакокинетические характеристики применяемых соединений и путь введения. Агент можно вводить в виде разовой дозы или в повторных дозах. Режим дозирования с применением соединений по настоящему изобретению выбран в соответствии с множеством факторов, включая тип, вид, возраст, вес, пол и медицинское состояние пациента; тяжесть состояния, подлежащего лечению; способ введения; функция почек и печени пациента; и конкретное применяемое соединение или его соль. Лечение можно проводить ежедневно или чаще, в зависимости от ряда факторов, включая общее состояние здоровья пациента, а также состав и способ введения выбранного соединения (соединений). Средний квалифицированный врач или ветеринар может легко определить и прописать эффективное количество лекарственного средства, необходимое для предотвращения, противодействия или остановки прогрессирования состояния.
[952] Соединения или фармацевтические композиции по настоящему изобретению можно производить и/или вводить в виде однократной или множественной единичной дозы.
[953] После общего описания данного изобретения его будет легче понять, если обратиться к следующим примерам, которые предоставлены в качестве иллюстрации и не предназначены для ограничения настоящего изобретения.
ПРИМЕРЫ
[954] Теперь раскрытие, в целом описываемое, будет более легко понято со ссылкой на следующие примеры, которые включены только в целях иллюстрации определенных аспектов и вариантов осуществления настоящего изобретения и не предназначены для ограничения изобретения.
[955] Синтетическое получение
[956] Новые соединения по настоящему изобретению можно получить множеством способов, известных специалисту в области органического синтеза. Соединения по настоящему изобретению могут быть синтезированы с использованием способов, описанных ниже, вместе с синтетическими методами, известными в области синтетической органической химии, или их вариациями, которые оценят специалисты в данной области.
[957] Получение соединений может включать защиту и снятие защиты с разнообразных химических групп. Необходимость защиты и снятия защиты, а также выбор подходящих защитных групп может быть легко определен специалистом в данной области техники. Химия защитных групп может быть найдена, например, в Greene and Wuts, Protective Groups in Organic Synthesis, 44th. Ed., Wiley & Sons, 2006, также как в Jerry March, Advanced Organic Chemistry, 4th edition, John Wiley & Sons, publisher, New York, 1992, которые в полном объеме включены в данный документ посредством ссылки.
[958] Соединения по настоящему изобретению можно получить с помощью литературных методов, цитируемых в нижеследующем тексте. На следующих схемах изображены установленные, известные синтезы этих остовов.
[959] Группы и/или заместители соединений по настоящему изобретению могут быть синтезированы и присоединены к этим остовам с помощью литературных методов, цитируемых в нижеследующем тексте. На следующих схемах изображены известные методы выполнения этого соединения.
[960] Общий синтез
[961] Соединения по настоящему изобретению можно синтезировать с использованием следующих методов. Приведены общие условия реакции, и продукты реакции могут быть очищены общеизвестными методами, включая кристаллизацию, хроматографию на силикагеле с использованием различных органических растворителей, таких как гексан, циклогексан, этилацетат, метанол и т. п., препаративную высокоэффективную жидкостную хроматографию или препаративную обращенно-фазную высокоэффективную жидкостную хроматографию.
[962] Иллюстративный пример синтеза
[963] Пример 1: Синтез 5-[[4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенокси]метил]-4-метилсульфонилоксазола (A3)
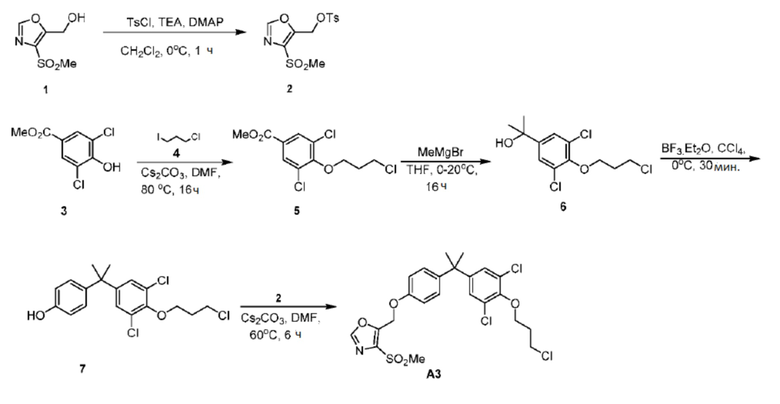
[964] (4-Метилсульфонилоксазол-5-ил)4-метилбензолсульфонат (2): К раствору 4-метилсульфонилоксазол-5-ола (1) (0,10 г, 0,56 ммоль), TEA (0,11 г, 1,1 ммоль) и DMAP (14 мг, 0,11 моль) в ДХМ(3 мл) прибавляли тозилхлорид (0,10 г, 0,52 ммоль) по каплям при 0°C. Затем раствор перемешивали при одной и той же температуре в течение 1 часа. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (5 мл), экстрагировали ДХМ (3 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (4-метилсульфонилоксазол-5-ил)4-метилбензолсульфоната (2) (0,11 г, выход: 56,6%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,98 (с, 1 H), 7,93 (д, J=8,40 Гц, 2 H), 7,42 (д, J=8,80 Гц, 2 H), 4,95 (с, 2 H), 3,22 (с, 3 H).
[965] Метил-3,5-дихлор-4-(3-хлорпропокси)бензоат (5): К смеси метил-3,5-дихлор-4-гидроксибензоата (3) (100,0 г, 0,45 моль) и Cs2CO3 (293,2 г, 0,90 моль) в ДМФА (1,5 л) прибавляли 1-хлор-3-иодпропан (4) (102,2 г, 0,50 моль), и смесь перемешивали при 80°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь охлаждали, погасили водой (3,5 л) и экстрагировали MTBE (1,0 л x 2). Объединенные органические слои промывали солевым раствором (1 л), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением метил-3,5-дихлор-4-(3-хлорпропокси)бензоата (70,0 г, выход: 52,0%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 2,29 (к, J=6,03 Гц, 2 H), 3,85 (т, J=6,36 Гц, 2 H), 3,91 (с, 3 H), 4,22 (т, J=5,70 Гц, 2 H), 7,92-8,00 (м, 2 H).
[966] 2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ол (6): К раствору 3,5-дихлор-4-(3-хлорпропокси)бензоата (5) (70,0 г, 0,24 моль) в ТГФ (500 мл) прибавляли MeMgBr (400 мл, 1,20 моль) при 0°C в атмосфере N2 . Смесь перемешивали при 20°C в течение 16 часов в атмосфере N2 . ТСХ показала, что реакция завершилась. Смесь выливали в H2O (500 мл), экстрагировали EtOAc (200 мл x 5), и объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ола (44,0 г, выход: 62,9%) в виде желтого масла. 1H ЯМР (400 МГц,CHCl3-d) δ 1,56 (с, 6 H), 2,29 (к, J=6,06 Гц, 2 H), 3,87 (т, J=6,39 Гц, 2 H), 4,13-4,19 (м, 2 H), 7,41 (с, 2 H).
[967] 4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенол (7): К раствору 2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ола (6) (20,0 г, 67,2 ммоль) и фенола (7,0 г, 73,9 ммоль) в CCl4 (400 мл) прибавляли BF3.Et2O (16,6 мл, 134,2 ммоль) по каплям при 0°C в атмосфере N2 . Смесь перемешивали при 0°C в течение 30 мин. ТСХ показала, что реакция завершилась. Полученную смесь выливали в H2O (300 мл), экстрагировали ДХМ (300 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (500 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенола (18,0 г, выход: 71,7%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,12 (с, 2H), 7,10-7,05 (м, 2H), 6,79-6,75 (м, 2H), 4,65 (с, 1H), 4,15 (т, J=5,7 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 2,28 (к, J=6,1 Гц, 2H), 1,62 (с, 6H).
[968] 5-[[4-[1-[3,5-Дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенокси]метил]-4-метилсульфонил-оксазол (A3): К суспензии 4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенола (7) (0,135 г, 0,36 ммоль) и Cs2CO3 (0,197 г, 0,6 ммоль) в ДМФА (3 мл) прибавляли (4-метилсульфонилоксазол-5-ил)метил-4-метилбензолсульфонат (2) (0,1 г, 0,3 ммоль) при 25°C. Смесь перемешивали при 60°C в течение 6 часов. ЖХ-МС показала, что реакция завершилась. Полученную смесь выливали в H2O (8 мл) и экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCl) с получением 5-[[4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенокси]метил]-4-метилсульфонил-оксазола (A1) (37,9 мг, выход: 23,6%) в виде желтого масла. Чистота ВЭЖХ (220 нм): 96,25%. 1H ЯМР (400 МГц, CHCl3-d) δ 7,99 (с, 1H), 7,16-7,10 (м, 4H), 6,94 (д, J=8,82 Гц, 2H), 5,42 (с, 2H), 4,15 (т, J=5,73 Гц, 2H), 3,86 (т, J=6,50 Гц, 2H) 3,18 (с, 3H), 2,28 (квин., J=6,17 Гц, 2 H), 1,62 (с, 6H). ЖХ-МС (M+23) m/z: рассчит. 533; найдено 556.
[969] Пример 2: Синтез 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси) метил)-1-(метилсульфонил)-1H-имидазола (A5)
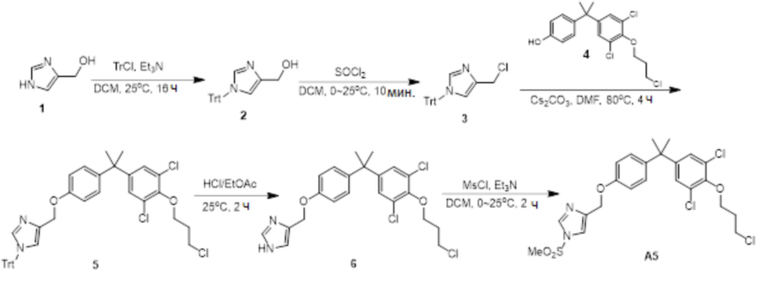
[970] (1-Тритил-1H-имидазол-4-ил)метанол (2): К раствору (1H-имидазол-4-ил)метанола (0,5 г, 5,3 ммоль) и Et3N (1,1 г, 10,2 ммоль) в ДХМ (20 мл) прибавляли TrCl (1,5 г, 5,3 ммоль) и смесь перемешивали при 50°C в течение 4 часов. ТСХ показала, что реакция завершилась. Реакционную смесь охлаждали, погасили водой (40 мл), экстрагировали ДХМ (5 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением (1-тритил-1H-имидазол-4-ил)метанола (2) (1,0 г, выход: 76,8%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,37-7,44 (м, 9H), 7,29 (д, J=1,34 Гц, 2H), 7,10 (дд, J=8,01, 1,41 Гц, 6H), 4,87 (т, J=5,56 Гц, 1H), 4,33 (д, J=5,50 Гц, 2H).
[971] 4-(Хлорметил)-1-тритил-1H-имидазол (3): К раствору (1-тритилимидазол-4-ил)метанола (2) (200 мг, 0,6 ммоль) в ДХМ (3 мл) прибавляли SOCl2 (0,2 мл, 2,9 ммоль) по каплям при 0°C, и смесь перемешивали при 25°C в течение 10 мин. ТСХ показала, что реакция завершилась. Реакционную смесь концентрировали при пониженном давлении с получением 4-(хлорметил)-1-тритил-1H-имидазола (3) (150 мг, выход: 71,1%) в виде желтого масла.
[972] 4-((4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1-тритил-1H-имидазол (5): Смесь 4-(хлорметил)-1-тритил-1H-имидазола (3) (150 мг, 0,4 ммоль), Cs2CO3 (272 мг, 0,8 ммоль) и 4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенола (4) (156 мг, 0,4 ммоль) в MeCN (5 мл) перемешивали при 80°C в течение 4 часов. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали, выливали в H2O (10 мл), экстрагировали EtOAc (4 мл x 2), и объединенные органические слои промывали солевым раствором (4 мл x 5), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1-тритил-1H-имидазола (5) (150 мг, выход: 71,1%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ=7,45 (д, J=1,2 Гц, 1H), 7,38-7,30 (м, 9H), 7,19-7,06 (м, 10H), 6,95-6,86 (м, 3H), 4,99 (с, 2H), 4,14-4,10 (м, 2H), 3,86 (т, J=6,5 Гц, 2H), 2,28 (квин., J=6,1 Гц, 2H), 1,62 (с, 6H).
[973] 4-((4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1H-имидазол (6): Раствор 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1-тритил-1H-имидазола (5) (150 мг, 0,2 ммоль) в HCl/EtOAc (4 M, 2 мл) перемешивали при 25°C в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Реакционную смесь отфильтровали, и фильтрат концентрировали при пониженном давлении с получением 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1H-имидазола (6) (95 мг, выход: 97,2%) в виде бесцветного масла. ЖХ-МС (M+1) m/z: рассчит. 452,1; найдено 452,9.
[974] 4-((4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1-(метилсульфонил)-1H-имидазол (A5): К смеси 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1H-имидазола (6) (80 мг, 0,2 ммоль) и TEA (0,1 мл, 0,5 ммоль) в ДХМ (2 мл) прибавляли метансульфонилхлорид (41 мг, 0,4 ммоль) по каплям при 0°C, и смесь перемешивали при 25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь разбавляли водой (20 мл), экстрагировали ДХМ (5 мл x 3), и объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (NH4HCO3) с получением 4-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-1-(метилсульфонил)-имидазола (A5) (16 мг, выход: 16,6%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,99 (д, J=1,3 Гц, 1H), 7,40 (с, 1H), 7,15-7,12 (м, 4H), 6,95-6,90 (м, 2H), 5,05 (с, 2H), 4,15 (т, J=5,7 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,30 (с, 3H), 2,31-2,26 (м, 2H), 1,63 (с, 6H). ЖХ-МС (220 нм): 95,2%. ЖХ-МС (M+1) m/z: рассчит. 530,1; найдено 531,0.
[975] Пример 3: Синтез 2-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-5-(метилсульфонил)-1,3,4-оксадиазола (A7)
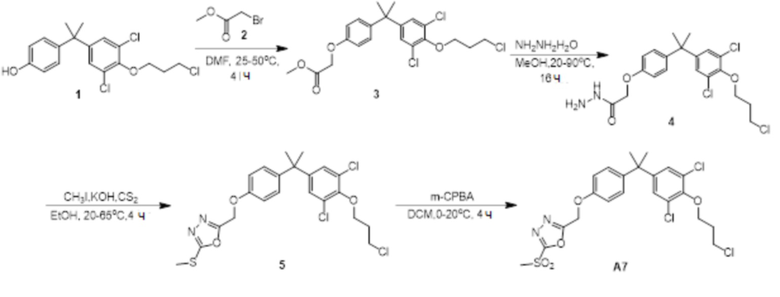
[976] Метил-2-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)ацетат (3): К раствору 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенола (1) (1,00 г, 2,6 ммоль) и метил-2-бромацетата (2) (0,49 г, 3,2 ммоль) в ДМФА (10 мл) прибавляли Cs2CO3 (1,30 г, 4,0 ммоль) при 25°C. Смесь перемешивали при 50°C в течение 4 часов. ЖХ-МС показала, что реакция завершилась. Смесь гасили водой (20 мл) и экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 5), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением метил-2-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)ацетата (3) (1,00 г, выход: 70%) в виде бесцветного масла. ЖХ-МС (M+23) m/z: рассчит. 444,07; найдено 467,1.
[977] 2-(4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси) ацетогидризид (4): К раствору метил-2-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)ацетата (3) (1,32 г, 2,9 ммоль) в MeOH (10 мл) прибавляли NH2NH2.H2O (0,59 г, 11,8 ммоль) при 20°C. Смесь перемешивали при 90°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь гасили водой (10 мл) и экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл x2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 2-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)ацетогидразида (4) (1,0 г, выход: 75,8%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ м.д.: 7,73 (шир., 1 H), 7,11-7,14 (д, J=8,9 Гц, 2 H), 7,11 (с, 2 H), 6,84 (д, J=8,9 Гц, 2 H), 4,58 (с, 2 H), 4,14-4,16 (т, J=5,2 Гц, 2 H), 3,94 (шир., 1 H), 3,86 (т, J=6,4 Гц, 2 H), 2,28 (м, 2 H), 1,62 (с, 6 H).
[978] 3-(1-(4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)этил)-5-метилтио)-4H-пиразол (5): К раствору 2-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)ацетогидразида (4) (500 мг, 1,12 ммоль) в MeOH (2 мл) прибавляли KOH (75 мг, 1,33 ммоль) и CS2 (76 мг, 2,8 ммоль) при 20°C. Смесь перемешивали при 65°C в течение 2 часов. Затем CH3I (2 мл) прибавляли к реакционной смеси, и перемешивали при 65°C в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Смесь гасили водой (20 мл) и экстрагировали EtOAc (10 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (20 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 3-(1-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)этил)-5-(метилтио)-4H-пиразола (5) (300 мг, выход: 54,5%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 7,14 (д, J=8,9 Гц, 2 H), 7,11 (с, 2 H), 6,94 (д, J=8,9 Гц, 2 H), 5,22 (с, 1 H), 4,15 (т, J=5,8 Гц, 2 H), 3,86 (т, J=6,4 Гц, 2 H), 2,74 (с, 3 H), 2,28 (т, J=5,99 Гц, 2 H), 1,62 (с, 6 H).
[979] 2-((4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-5-(метилсульфонил)-1,3,4-оксадиазол (A7): К раствору 3-(1-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)этил)-5-(метилтио)-4H-пиразола (5) (220 мг, 0,49 ммоль) в ДХМ (5 мл) прибавляли м-ХПБК (чистота 85%, 226 мг, 4,03 ммоль) при 0 °C. Реакцию перемешивали при 20°C в течение 4 часов. ЖХ-МС показала, что реакция завершилась. Смесь гасили насыщенным водным Na2S2O3 (5 мл) и насыщенным водным NaHCO3 (5 мл), затем экстрагировали ДХМ (10 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением 2-((4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенокси)метил)-5-(метилсульфонил)-1,3,4-оксадиазола (A7) (74 мг, выход: 31,6%) в виде бесцветного масла. 1H ЯМР (400 МГц, ДМСО-d6) δ м. д. 7,14 (д, J=8,9 Гц, 2 H), 7,11 (с, 2 H), 6,95 (д, J=8,8 Гц, 2 H), 5,35 (с, 2 H), 4,15 (т, J=5,73 Гц, 2 H), 3,86 (т, J=6,39 Гц, 2 H), 3,50 (с, 3 H), 2,28 (т, J=6,06 Гц, 2 H), 1,63 (с, 6 H). ЖХ-МС (220 нм): 97%. ЖХ-МС M+H+) m/z: рассчит. 532,04, найдено 533,1.
[980] Пример 4: Синтез 5-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)-4-(метилсульфонил)оксазола (A13)

[981] Этил-4-бромоксазол-5-карбоксилат (2): К раствору этилоксазол-5-карбоксилата (1) (100,0 г, 0,71 моль) в ТГФ (500 мл) и DMPU (500 мл) прибавляли LiHMDS (1,0 M, 921 мл, 921 ммоль) по каплям при -78°C в атмосфере N2, и смесь перемешивали в течение 1,5 часов. Затем Br2 (54,5 мл, 1,06 моль) прибавляли по каплям при одной и той же температуре, и полученную смесь перемешивали в течение 0,5 часов. ТСХ показала, что исходный материал исчез. Полученный раствор выливали при комнатной температуре в насыщенный водный NH4Cl (1000 мл), экстрагировали EtOAc (500 мл x 3). Объединенные органические слои промывали солевым раствором (500 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением этил-4-бромоксазол-5-карбоксилата (25,0 г, чистота: 90%, выход: 11%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d): δ 7,94 (с, 1H), 4,43 (к, J=7,3 Гц, 2H), 1,42 (т, J=7,2 Гц, 3H)
[982] Этил-4-(метилтио)оксазол-5-карбоксилат (3): Смесь этил-4-бромоксазол-5-карбоксилата (2) (28,0 г, 127 ммоль) и NaSMe (10,8 г, 153 ммоль) в EtOH (400 мл) перемешивали при 80°C в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Полученный раствор охлаждали и концентрировали при пониженном давлении. Остаток разбавляли водой (300 мл) и экстрагировали EtOAc (300 мл x 3). Объединенные органические слои промывали солевым раствором (300 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением этил-4-метилсульфанилоксазол-5-карбоксилата (13,0 г, выход: 80%, выход: 43,7%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d): δ 7,91 (с, 1H), 4,40 (к, J=7,2 Гц, 2H), 2,62 (с, 3H), 1,41 (т, J=7,2 Гц, 3H).
[983] Этил-4-(метилсульфонил)оксазол-5-карбоксилат (4): Раствор этил-4-метилсульфанилоксазол-5-карбоксилата (3) (2,9 г, 15,5 ммоль) и м-ХПБК (10,0 г, 46,5 ммоль) в ДХМ (10 мл) перемешивали при 25°C в течение 16 часов. Завершение реакции зафиксировали по ТСХ. Реакционную смесь гасили насыщ. водным Na2S2O3 (100 мл) и насыщ. водным NaHCO3 (100 мл). Смесь экстрагировали ДХМ (60 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением этил-4-метилсульфонилоксазол-5-карбоксилата (1,20 г, выход: 35,3%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d): δ 8,04 (с, 1H), 4,50 (к, J=7,1 Гц, 2H), 3,38 (с, 3H), 1,44 (т, J=7,2 Гц, 3H).
[984] (4-(Метилсульфонил)оксазол-5-ил)метанол (5): К раствору этил-4-метилсульфонилоксазол-5-карбоксилата (4) (1.2 г, 5.47 ммоль) в ТГФ (10 мЛ) прибавляли LiBH4 (179 мг, 8.21 ммоль) при 0°C. Смесь перемешивали при 0°C в течение 1 часа. ТСХ показала, что реакция завершилась. Смесь гасили водным раствором HCl (3M, 2 мЛ) при 0°C и экстрагировали EtOAc (10 мЛ x 3). Объединенные органические слои промывали солевым раствором (3 мЛ), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением (4-метилсульфонилоксазол-5-ил) метанол (900 мг, выход: 92,8%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d): δ=7.92 (с, 1H), 4.93 (с, 2H), 3.24 (с, 3H).
[985] 5-(Хлорметил)-4-(метилсульфонил)оксазол (6): К раствору этил-4-метилсульфонилоксазол-5-карбоксилата (5) (700 мг, 3.95 ммоль) в ДХМ (10 мЛ) и ДМФА (0.5 mL) прибавляли SOCl2 (1.44 мЛ, 19.8 ммоль) при 0°C. Смесь перемешивали при 25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь гасили H2O (15 мЛ), экстрагировали ДХМ (10 мЛ x 3). Объединенные органические слои промывали солевым раствором (10 мЛ x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 5-( хлорметил)-4- метилсульфонилоксазола (700 мг, выход: 90.6%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7.99 (с, 1H), 4.94 (с, 2H), 3.22 (с, 3H).
[986] Метил 3,5-дихлор-4-(2-хлорэтокси)бензоат (9): Смесь метил 3,5-дихлор-4-гидроксибензоата (7) (10.0 г, 45.2 ммоль), Cs2CO3 (36.9 г, 113 ммоль) и 1-бром-2-хлорэтан (26.0 г, 181 ммоль) в ДМФА (60.0 мЛ) перемешивали при 70°C в течение 1 часа. ТСХ показала, что реакция завершилась. Полученный раствор охлаждали и разбавляли водой (150 мЛ), экстрагировали EtOAc (100 мЛ x 3). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением метил-3,5-дихлор-4-(2-хлорэтокси)бензоата (10,0 г, выход: 78,0%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=8.01-7.97 (м, 2H), 4.35 (т, J=6.2 Гц, 2H), 3.93 (с, 3H), 3.89 (т, J=6.2 Гц, 2H).
[987] 2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ол (10): К раствору MeMgBr (3 M, 65.6 мЛ, 197 ммоль) в ТГФ (30 мЛ) прибавляли метил 3,5-дихлор-4-(2- хлорэтокси)бензоат (9) (9.3 г, 32.8 ммоль) в ТГФ (50 мЛ) по каплям при 0°C. Реакционную смесь перемешивали при 0°C в течение 1 часа и ТСХ показала, что реакция завершилась. Смесь добавляли к насыщ. водному раствору NH4Cl (300 мЛ) и экстрагировали EtOAc (200 мЛ x 3). Объединенные органические слои промывали солевым раствором (200 мЛ), сушили над Na2SO4, фильтровали и концентрировали с получением 2-[3,5-дихлор-4-(2-хлорэтокси)фенил]пропан-2-ола (9,0 г, выход: 96,8%) в виде желтого масла..1H ЯМР (400 МГц, CHCl3-d) δ=7.42 (с, 2H), 4.27 (т, J=6.3 Гц, 2H), 3.87 (т, J=6.3 Гц, 2H), 1.55 (с, 6H).
[988] 4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенол (11): К раствору 2-[3,5-дихлор-4-(2- хлорэтокси)фенил]пропан-2-ол (9.0 г, 31.7 ммоль) (10) и фенол (3.58 г, 38.1 ммоль) в CCl4 (100 мЛ) добавляли BF3·Et2O (7.83 мЛ, 63.5 ммоль) по каплям при 0°C в атмосфере N2. Смесь перемешивали при 0°C в течение 1 часа. ЖХ-МС ТСХ показала, что реакция почти завершена. Смесь добавляли к воде (150 мЛ) и экстрагировали ДХМ (100 мл x 3). Объединенные органические слои промывали солевым раствором (100 мЛ), сушили над Na2SO4, фильтровали и концентрировали. Раствор неочищенного продукта очищали посредством ЖХСД (нейтральный) с получением 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метилэтил]фенола (7.0 г, выход: 61.3%) в виде желтого масла. 1H ЯМР (400 МГц, CHLOROFORM-d) δ=7.13 (с, 2H), 7.10-7.04 (м, 2H), 6.79-6.74 (м, 2H), 4.81 (шир. с, 1H), 4.26 (т, J=6.3 Гц, 2H), 3.86 (т, J=6.4 Гц, 2H), 1.62 (с, 6H).
[989] 5-((4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)-4-(метилсульфонил)оксазол (A13): Раствор 5-(хлорметил)-4-метилсульфонил-оксазола (6) (500 мг, 2,56 ммоль), 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенола (11) (919 мг, 2,56 ммоль) и Cs2CO3 (1,67 г, 5,11 ммоль) в ДМФА (20 мл) перемешивали при 25°C в течение 2 часов. Затем полученный раствор перемешивали при 40°C в течение 0,5 ч. Завершение реакции зафиксировали по ТСХ. Реакционную смесь гасили водой (50 мл), и смесь экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (30 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 5-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-4-метилсульфонил-оксазола (528 мг, выход: 39,8%) в виде белого твердого вещества. 1H ЯМР (400 МГц, Хлороформ-d) δ=7,92 (с, 1H), 7,09-7,02 (м, 4H), 6,89-6,83 (м, 2H), 5,34 (с, 2H), 4,18 (т, J=6,4 Гц, 2H), 3,79 (т, J=6,4 Гц, 2H), 3,11 (с, 3H), 1,54 (с, 6H). МС (M+H+) m/z: рассчит., 517,0; найдено 518,1, 540,0.
[990] Пример 5: Синтез N-((3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)метансульфонамида (A22)
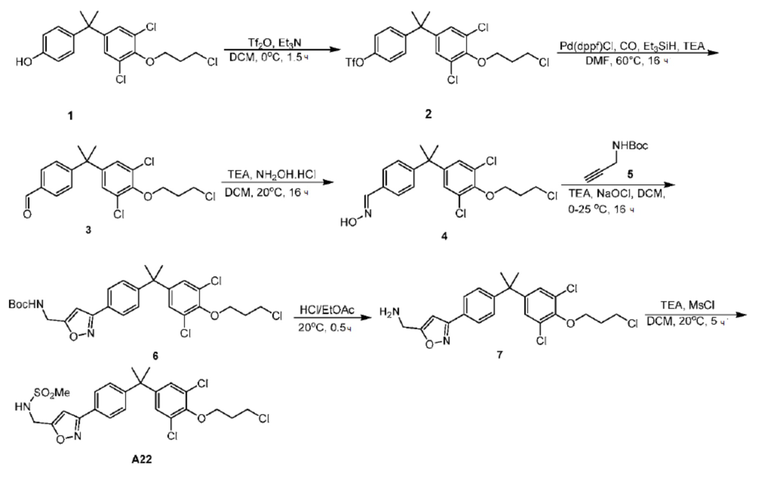
[991] 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенилтрифторметансульфонат (2): К раствору 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенола (1) (4,0 г, 10,7 ммоль) и Et3N (4,5 мл, 54,7 ммоль) в ДХМ(40 мл) прибавляли трифторметансульфоновый ангидрид (5,4 г, 19,3 ммоль) по каплям при 0°C в атмосфере N2. Смесь перемешивали при одной и той же температуре в течение 1,5 ч. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (60 мл), экстрагировали ДХМ (20 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенилтрифторметансульфоната (4,0 г, выход: 73,4%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,29-7,27 (м, 2H), 7,22-7,19 (м, 2H), 7,11 (с, 2H), 4,17 (т, J=6,3 Гц, 2H), 3,87 (т, J=6,3 Гц, 2H), 3,87 (т, J=6,2 Гц, 2H), 1,66 (с, 6H).
[992] 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегид (3): К раствору 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенилтрифторметансульфоната (6) (4,0 г, 7,9 ммоль), Et3SiH (1,9 мл, 11,9 ммоль) и Et3N (2,2 мл, 15,8 ммоль) в ДМФА (50 мл) прибавляли Pd(dppf)Cl2 (290 мг, 0,4 ммоль) при 20°C. Реакционную смесь перемешивали при 60°C в течение 16 часов в атмосфере CO при 50 фунтов на кв. дюйм. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали, выливали в H2O (100 мл), экстрагировали EtOAc (40 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегида (2,6 г, выход: 85,2%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 10,02 (с, 1 H), 7,83 (д, J=8,8 Гц, 2 H), 7,41 (д, J=8,8 Гц, 2 H), 7,13 (с, 2 H), 4,18 (т, J=5,8 Гц, 2 H), 3,88 (т, J=6,4 Гц, 2 H), 2,31 (м, 2 H), 1,70 (с, 6 H).
[993] (E)-4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегида оксим (4): К раствору 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегида (0,5 г, 1,3 ммоль) (3) в ДХМ (5 мл) прибавляли NH2OH.HCl (117 мг, 1,7 ммоль) и TEA (0,5 мл, 3,9 ммоль) при 20°C в атмосфере N2. Реакционную смесь перемешивали при одной и той же температуре в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Смесь выливали в H2O (10 мл) и экстрагировали ДХМ (10 мл x 3). Органические слои промывали солевым раствором (10 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегида оксим (4) (0,410 г, выход: 78,9%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ=8,13 (с, 1H), 7,52 (д, J=8,4 Гц, 2H), 7,37 (с, 1H), 7,23 (д, J=8,4 Гц, 2H), 7,12 (с, 2H), 4,15 (т, J=5,6 Гц, 2H), 3,86 (т, J=6,5 Гц, 2H), 2,28 (квин., J=6,1 Гц, 2H), 1,65 (с, 6H). МС (M+H+) m/z: рассчит. 399,0; найдено 399,8.
[994] трет-Бутил-((3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)карбамат (6): К раствору 4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)бензальдегида оксима (4) (320 мг, 0,80 ммоль) в ДХМ (10 мл) прибавляли водный NaClO (7,0%, 1,3 г, 1,2 ммоль) по каплям при 0°C. Реакционную смесь перемешивали в течение 5 мин. Трет-бутилпроп-2-ин-1-илкарбамат (5) (120 мг, 0,80 ммоль) и TEA (0,22 мл, 1,6 ммоль) прибавляли к данной реакционной смеси при 0°C. Смесь перемешивали при 0°C~25°C в течение 16 часов. ЖХ-МС показал ~50% желаемого продукта и ~10% оставшегося исходного материала 2. Смесь выливали в H2O (10 мл), экстрагировали ДХМ (10 мл x 2). Объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении и очищали ЖХСД с получением трет-бутил-((3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)карбамата (0,22 г, выход: 51%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,72 (д, J=8,60 Гц, 2 H) 7,31 (д, J=8,60 Гц, 2 H) 7,10-7,20 (м, 2 H) 6,48 (с, 1 H) 5,03 (шир. с, 1 H) 4,48 (шир. д, J=6,17 Гц, 2 H) 4,16 (т, J=5,73 Гц, 2 H) 3,86 (т, J=6,39 Гц, 2 H) 2,29 (к, J=6,06 Гц, 2 H) 1,68 (с, 6 H) 1,47 (с, 9 H). МС (M+H+) m/z: рассчит. 552,1; найдено 553,2.
[995] (3-(4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метанамина гидрохлорид (7): Раствор трет-бутил-((3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)карбамата (6) (190 мг, 0,34 ммоль) в HCl/EtOAc (4 M, 3 мл, 12 ммоль) перемешивали при 20°C в течение 0,5 часа. ЖХ-МС показала, что реакция завершилась. Смесь концентрировали при пониженном давлении с получением (3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метанамина гидрохлорид (7) (60 мг, выход: 36%) в виде коричневого масла. МС (M+H+) m/z: рассчит. 452,1; найдено 453,1.
[996] N-((3-(4-(2-(3,5-Дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)метансульфонамид (A22): К раствору [3-[4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенил]изоксазол-5-ил]метанамина (7) (60 мг, 0,13 ммоль) в ДХМ (3 мл) прибавляли TEA (40 мг, 0,40 ммоль) и MsCl (18 мг, 0,16 ммоль) в атмосфере N2 при 0°C. Реакционную смесь перемешивали при 20°C в течение 5 ч. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (5 мл) и экстрагировали ДХМ (10 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением N-((3-(4-(2-(3,5-дихлор-4-(3-хлорпропокси)фенил)пропан-2-ил)фенил)изоксазол-5-ил)метил)метансульфонамида (A22) (5 мг, выход: 7,11%) в виде коричневого масла. Чистота ЖХ-МС (220 нм): 89,4%. 1H ЯМР (400 МГц, CHCl3-d) δ=7,73 (шир. д, J=7,9 Гц, 2H), 7,31 (шир. д, J=8,2 Гц, 2H), 7,14 (с, 2H), 6,60 (с, 1H), 4,89-4,80 (м, 1H), 4,54 (д, J=6,2 Гц, 2H), 4,16 (т, J=5,6 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 2,99 (с, 3H), 2,33-2,25 (м, 2H), 1,68 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит. 530,0; найдено 531,0.
[997] Пример 6: Синтез N-(трет-бутил)-3,5-дихлор-4-(2-хлорэтокси)-N-(4-((4-(метил-сульфонил)оксазол-5-ил)метокси)фенил)анилина (A31)
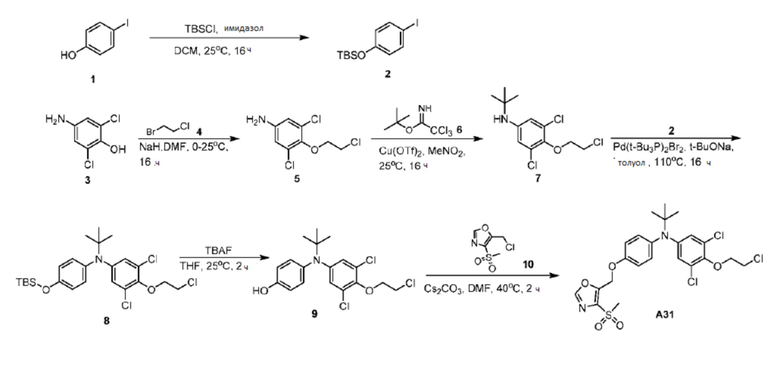
[998] трет-Бутил-(4-иодфенокси)-диметилсилан (2): К раствору 4-иодфенола (1) (3,0 г, 13,6 ммоль) и имидазола (1,9 г, 27,3 ммоль) в ДХМ (30 мл) прибавляли TBSCl (1,8 г, 12,3 ммоль) при 25°C. Затем смесь перемешивали при одной и той же температуре в течение 16 часов. ТСХ показала, что реакция завершилась. Реакционную смесь промывали водой (10 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением трет-бутил-(4-иодфенокси)-диметилсилана (2) (2,5 г, выход: 54,8%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,57-7,44 (м, 2H), 6,67-6,55 (м, 2H), 1,02-0,93 (м, 9H), 0,19 (с, 6H).
[999] 3,5-Дихлор-4-(2-хлорэтокси)анилин (5): К раствору 4-амино-2,6-дихлорфенола (3) (5,0 г, 28,1 ммоль) в ДМФА (50 мл) порциями прибавляли NaH (чистота 60%, 1,1 г, 28,1 ммоль) при 0°C в атмосфере N2 . После перемешивания при одной и той же температуре в течение 15 мин прибавляли 1-бром-2-хлорэтан (4) (4,4 г, 30,9 ммоль), и полученную смесь перемешивали при 25°C в течение 16 часов. ТСХ показала, что реакция завершилась. Полученную смесь гасили насыщенным водным раствором NH4Cl (100 мл) и экстрагировали EtOAc (50 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 3,5-дихлор-4-(2-хлорэтокси)анилина (5) (2,5 г, выход: 37%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 6,64-6,55 (м, 2H), 4,18 (т, J=6,4 Гц, 2H), 3,84 (т, J=6,4 Гц, 2H), 3,69-3,58 (м, 2H).
[1000] N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)анилин (7): К раствору 3,5-дихлор-4-(2-хлорэтокси)анилина (5) (1,0 г, 4,16 ммоль) и трет-бутил-2,2,2-трихлорэтанимидата (6) (2,27 г, 10,4 ммоль) в MeNO2 (10 мл) прибавляли трифторметансульфонат меди (II) (1,5 г, 4,16 ммоль) в атмосфере N2 . Затем полученную в результате смесь перемешивали при 25°C в течение 16 часов. ТСХ показала на завершение реакции. Смесь гасили водным раствором NaHCO3 (5 мл) и экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)анилина (7) (460 мг, выход: 37,3%) в виде коричневой смолы. 1H ЯМР (400 МГц, CHCl3-d) δ 6,64 (с, 2H), 4,19 (т, J=6,4 Гц, 2H), 3,84 (т, J=6,4 Гц, 2H), 1,37-1,29 (м, 9H).
[1001] N-трет-Бутил-N-[4-[трет-бутил(диметил)силил]оксифенил]-3,5-дихлор-4-(2-хлорэтокси)анилин (8): К смеси N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)анилина (7) (210 мг, 0,71 ммоль), трет-бутил-(4-иодфенокси)-диметилсилана (237 мг, 0,71 ммоль) и t-BuONa (162 мг, 1,77 ммоль) в толуоле (5 мл) прибавляли тритретбутилфосфинбромидпалладий (I) (55 мг, 0,07 ммоль) в атмосфере N2 . Затем полученную в результате смесь перемешивали при 110°C в течение 16 часов. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали и погасили водой (2 мл) и экстрагировали EtOAc (2 мл x3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением N-трет-бутил-N-[4-[трет-бутил(диметил)силил]оксифенил]-3,5-дихлор-4-(2-хлорэтокси)анилина (8): (125 мг, выход: 35,1%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 6,99-6,93 (м, 2H), 6,86-6,77 (м, 2H), 6,70 (с, 2H), 4,18 (т, J=6,4 Гц, 2H), 3,83 (т, J=6,5 Гц, 2H), 1,37 (с, 9H), 1,04-0,94 (м, 9H), 0,26-0,21 (м, 6H).
[1002] 4-[N-трет-Бутил-3,5-дихлор-4-(2-хлорэтокси)анилино]фенол (9): К раствору N-трет-бутил-N-[4-[трет-бутил(диметил)силил]оксифенил]-3,5-дихлор-4-(2-хлорэтокси)анилина (8) (150 мг, 0,29 ммоль) в ТГФ (5 мл) прибавляли TBAF (1 M, 1,0 мл, 1 ммоль). Затем полученную смесь перемешивали при 25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь гасили водой (5 мл) и экстрагировали EtOAc (3 мл x 3). Объединенные органические слои промывали водой (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали с получением 4-[N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)анилино]фенола (9) (110 мг, выход: 94,9%) в виде желтой смолы. 1H ЯМР (400 МГц, CHCl3-d) δ 7,03-6,93 (м, 2H), 6,87-6,79 (м, 2H), 6,72 (с, 2H), 4,18 (т, J=6,4 Гц, 2H), 3,83 (т, J=6,4 Гц, 2H), 1,37 (с, 9H).
[1003] N-трет-Бутил-3,5-дихлор-4-(2-хлорэтокси)-N-[4-[(4-метилсульфонилоксазол-5-ил)-метокси]-фенил]анилин (A31): К смеси 4-[N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)анилино]фенола (9) (110 мг, 0,283 ммоль) и Cs2CO3 (277 мг, 0,85 ммоль) в ДМФА (5 мл) прибавляли 5-(хлорметил)-4-метилсульфонил-оксазол (10) (83 мг, 0,42 ммоль). Затем полученную смесь перемешивали при 40°C в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали, погасили водой (5 мл) и экстрагировали EtAOc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением N-трет-бутил-3,5-дихлор-4-(2-хлорэтокси)-N-[4-[(4-метилсульфонил-оксазол-5-ил)-метокси]-фенил]анилина (A31) (36,5 мг, выход: 23,5%) в виде желтого твердого вещества. Чистота ВЭЖХ (220 нм): 91,7%. 1H ЯМР (400 МГц, CHCl3-d) δ 8,01 (с, 1H), 7,06-7,02 (м, 2H), 6,99-6,94 (м, 2H), 6,73 (с, 2H), 5,41 (с, 2H), 4,17 (т, J=6,4 Гц, 2H), 3,82 (т, J=6,4 Гц, 2H), 3,20 (с, 3H), 1,35 (с, 9H). ЖХ-МС (M+Na+) m/z: рассчит. 546,1; найдено 569,1.
[1004] Пример 7: Синтез 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-((4-(метилсульфонил)оксазол-5-ил)метил)анилина гидрохлорида (A32)
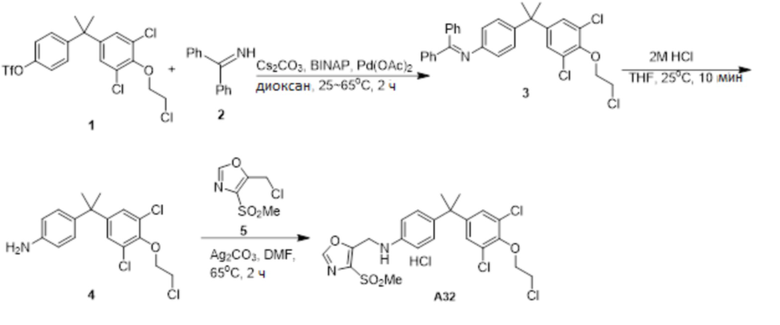
[1005] 4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-(дифенилметилен)анилин (3): К смеси 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенилтрифторметансульфоната (1) (5,0 г, 10,2 ммоль), дифенилметанимина (2) (1,8 г, 10,2 ммоль), Cs2CO3 (6,6 г, 20,3 ммоль) и BINAP (1,3 г, 5,08 ммоль) в 1,4-диоксане (100 мл) прибавляли Pd(OAc)2 (0,5 г, 2,0 ммоль) при 25°C в атмосфере N2 . Смесь перемешивали при 65°C в течение 2 ч. ТСХ показала, что реакция завершилась. Полученный раствор охлаждали, погасили H2O (100 мл), экстрагировали EtOAc (30 мл x 2). Объединенные органические слои промывали солевым раствором (40 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-(дифенилметилен)анилина (4,5 г, выход: 84,6%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,78-7,74 (м, 2H), 7,63-7,57 (м, 2H), 7,45-7,38 (м, 2H), 7,32-7,27 (м, 2H), 7,14-7,07 (м, 2H), 7,03-6,94 (м, 4H), 6,66 (д, J=8,6 Гц, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,58 (с, 6H).
[1006] 4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)анилин гидрохлорид (4): К раствору 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-(дифенил метилен)анилина (3) (4,5 г, 8,6 ммоль) в ТГФ (50 мл) прибавляли водную HCl (2 M, 15 мл) и смесь перемешивали при 25°C в течение 15 мин. ТСХ показала, что реакция завершилась. Смесь концентрировали при пониженном давлении и очищали колоночной хроматографией на силикагеле с получением 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)анилина гидрохлорида (2,5 г, выход: 81,0%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 10,54 (шир. с, 2H), 7,48 (шир. д, J=8,6 Гц, 2H), 7,31-7,27 (м, 2H), 7,09 (с, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,3 Гц, 2H), 1,63 (с, 6H).
[1007] 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-((4-(метилсульфонил)оксазол-5-ил)метил)анилин гидрохлорид (A32): К суспензии 5-(хлорметил)-4-(метилсульфонил)оксазола (5) (200 мг, 0,5 ммоль) и Ag2CO3 (564 мг, 0,2 ммоль) в ДМФА (2 мл) прибавляли 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)анилин (4) (382 мг, 0,1 ммоль), и смесь перемешивали при 65°C в течение 2 часов. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали, выливали в H2O (6 мл), экстрагировали EtOAc (2 мл x 2). Объединенные органические слои промывали солевым раствором (4 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCl) с получением 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)-N-((4-(метилсульфонил)оксазол-5-ил) метил)анилина гидрохлорида (A32) (20 мг, выход: 3,8%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 7,85 (с, 1H), 7,16-7,09 (м, 4H), 7,04-6,93 (м, 2H), 4,80 (с, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,16 (с, 3H), 1,61 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 516,0; найдено 517,0.
[1008] Пример 8: Синтез 5-(1-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилсульфонил)оксазола (A35)

[1009] 4-(Метилтио)оксазол-5-карбоновая кислота (2): К раствору этил-4-метилсульфанилоксазол-5-карбоксилата (1) (1 г, чистота 80%, 4,3 ммоль) в ТГФ (10 мл) и H2O (4 мл) прибавляли NaOH (300 мг, 8,6 ммоль) при 25°C, и смесь перемешивали при одной и той же температуре в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Смесь подкисляли до pH=3 водным раствором HCl (3 M, 3 мл) и экстрагировали EtOAc (15 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 4-(метилтио)оксазол-5-карбоновой кислоты (2) (0,7 г, чистота 80%, выход: 82,3%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 7,99 (с, 1H), 2,65 (с, 3H). ЖХ-МС (M+1) m/z: рассчит.: 531,0; найдено 532,0.
[1010] N-Метокси-N-метил-4-(метилтио)оксазол-5-карбоксамид (4): К смеси 4-(метилтио)оксазол-5-карбоновой кислоты (2) (0,7 г, 4,4 ммоль) в ТГФ (5 мл) и ДМФА (5 мл) прибавляли HATU (2,5 г, 6,6 ммоль) при 25°C в атмосфере N2. После перемешивания при одной и той же температуре в течение 15 минут прибавляли N-метоксиметанамина гидрохлорид (3) (0,6 г, 5,7 ммоль) и TEA (3,1 мл, 22,0 ммоль), и полученную смесь перемешивали при 25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Реакционную смесь разбавляли H2O (10 мл), экстрагировали EtOAc (10 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением N-метокси-N-метил-4-(метилтио)оксазол-5-карбоксамида (4) (0,5 г, выход: 56,2%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,90 (с, 1H), 4,12 (к, J=7,1 Гц, 1H), 3,81 (с, 3H), 3,30 (с, 3H), 2,58 (с, 3H).
[1011] 1-(4-(Метилтио)оксазол-5-ил)этенон (5): К смеси N-метокси-N-метил-4-(метилтио)оксазол-5-карбоксамида (4) (0,4 г, 1,9 ммоль) в ТГФ (8 мл) прибавляли MeMgBr (3 M, 0,8 мл, 2,4 ммоль) при 0°C в атмосфере N2, и полученную смесь перемешивали при одной и той же температуре в течение 1 часа. ТСХ показала, что реакция завершилась. Реакционную смесь гасили насыщенным водным NH4Cl (4 мл), экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 1-(4-(метилтио)оксазол-5-ил)этенона (5) (0,4 г, 75% чистота, выход: 96,2%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,89 (с, 1H), 2,62 (с, 3H), 2,50 (с, 3H).
[1012] 1-(4-(Метилтио)оксазол-5-ил)этанол (6): К смеси 1-(4-(метилтио)оксазол-5-ил)этанона (5) (0,4 г, 2,3 ммоль) в ТГФ (8 мл) прибавляли NaBH4 (0,1 г, 2,7 ммоль) при 0°C в атмосфере N2 , и смесь перемешивали при одной и той же температуре в течение 1 часа. ТСХ показала, что реакция завершилась. Реакционную смесь гасили насыщенным водным NH4Cl (4 мл), экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 1-(4-(метилтио)оксазол-5-ил)этанола (6) (0,2 г, выход: 54,9%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,83 (с, 1H), 5,12 (шир. д, J=5,5 Гц, 1H), 2,44 (с, 3H), 1,58 (д, J=6,6 Гц, 3H).
[1013] 5-(1-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилтио)оксазол (8): К смеси 1-(4-(метилтио)оксазол-5-ил)этанола (6) (0,2 г, 1,1 ммоль), 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенола (7) (0,4 г, 1,1 ммоль) и PPh3 (0,6 г, 2,3 ммоль) в ТГФ (2 мл) прибавляли DEAD (0,3 г, 1,7 ммоль) при 0°C в атмосфере N2, и смесь перемешивали при 25°C в течение 16 часов. ТСХ показала, что реакция завершилась. Реакционную смесь гасили H2O (5 мл), экстрагировали EtOAc (6 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 5-(1-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилтио)оксазола (8) (50 мг, выход: 8,83%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,85-7,82 (м, 1H), 7,11-7,03 (м, 4H), 6,88 (д, J=8,8 Гц, 2H), 5,51 (к, J=6,6 Гц, 1H), 4,24 (т, J=6,4 Гц, 2H), 3,84 (т, J=6,4 Гц, 2H), 2,35 (с, 3H), 1,69 (д, J=6,6 Гц, 3H), 1,58 (с, 6H).
[1014] 5-(1-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилсульфонил)оксазол (A35): К смеси 5-(1-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилтио)оксазола (8) (50 мг, 0,1 ммоль) прибавляли м-ХПБК (чистота 80%, 64 мг, 0,3 ммоль) в ДХМ (3 мл) при 25°C, и смесь перемешивали при одной и той же температуре в течение 16 часов. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили H2O (5 мл), экстрагировали EtOAc (6 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением 5-(1-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)этил)-4-(метилсульфонил)оксазола (21,7 мг, выход: 40,8%) в виде белого твердого вещества. Чистота ВЭЖХ (220 нм): 98,5%. 1H ЯМР (400 МГц, CHCl3-d) δ=7,94 (с, 1H), 7,14-7,03 (м, 4H), 6,92 (д, J=8,9 Гц, 2H), 6,10 (к, J=6,5 Гц, 1H), 4,26 (т, J=6,3 Гц, 2H), 3,86 (т, J=6,3 Гц, 2H), 3,06 (с, 3H), 1,74 (д, J=6,7 Гц, 3H), 1,59 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 531,0; найдено 532,0, 534,0.
[1015] Пример 9: Синтез N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)оксазол-2-ил)метансульфонамида (A38)
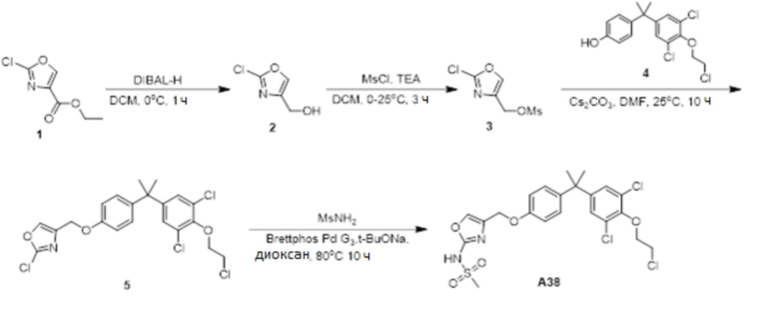
[1016] (2-Хлороксазол-4-ил)метанол (2): К раствору этил-2-хлороксазол-4-карбоксилата (1) (1,0 г, 5,7 ммоль) в ДХМ (20 мл) прибавляли DIBAL-H (1 M в толуоле 8,5 мл, 8,5 ммоль) по каплям при 0°C в атмосфере N2. Смесь перемешивали при одной и той же температуре в течение 1 часа. ТСХ показала, что реакция завершилась. Смесь гасили насыщенным водным NH4Cl (20 мл), затем экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением (2-хлороксазол-4-ил)метанола (2) (470 мг, выход: 62%) в виде коричневого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,59 (с, 1H), 4,58 (д, J=0,8 Гц, 2H).
[1017] (2-Хлороксазол-4-ил)метил метансульфонат (3): К смеси (2-хлороксазол-4-ил)метанола (2) (0,47 г, 3,52 ммоль) и TEA (1 мл, 7,04 моль) в ДХМ (15 мл) прибавляли метансульфонилхлорид (444 мг, 3,87 ммоль) при 0°C. Смесь перемешивали при 0-25°C в течение 3 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (30 мл), экстрагировали ДХМ (10 мл x 2). Объединенные органические слои промывали солевым раствором (20 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (2-хлороксазол-4-ил)метилметансульфоната (3) (800 мг, чистота 70%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,77 (с, 1H), 5,14 (д, J=0,8 Гц, 2H), 3,08 (с, 3H).
[1018] 2-Хлор-4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)оксазол (5): К раствору (2-хлороксазол-4-ил)метилметансульфоната (3) (0,70 г, 3,31 ммоль) в ДМФА (10 мл) прибавляли 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенол (4) (1,19 г, 3,31 ммоль) и Cs2CO3 (2,16 г, 6,62 ммоль). Полученную смесь перемешивали при 25°C в течение 10 часов. ЖХ-МС показала, что реакция завершилась. Смесь выливали в H2O (30 мл) и экстрагировали EtOAc (30 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 2-хлор-4-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]оксазола (0,50 г, выход: 31,8%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,68 (с, 1H), 7,15-7,11 (м, 4H), 6,92-6,87 (м, 2H), 4,97 (д, J=0,8 Гц, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,63 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 473,0; найдено 474,1.
[1019] N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)оксазол-2-ил)метансульфонамид (A38): К раствору 2-хлор-4-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]оксазола (5) (10 мг, 0,02 ммоль) в 1,4-диоксане (0,2 мл) прибавляли метансульфонамид (2,4 мг, 0,02 ммоль), Brettphos Pd G3 (2 мг, 20% масс.) и t-BuONa (3 мг, 0,03 ммоль). Смесь перемешивали при 80°C в течение 10 часов в атмосфере N2 . ЖХ-МС показал 5% желаемого МС и 90% исходного материала. Полученные 20 реакционных смесей охлаждали и объединяли. Смесь отфильтровали, и фильтрат концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением N-[[5-бром-4-[4-[1-[3,5-дихлор-4-(3-хлорпропокси)фенил]-1-метил-этил]фенил]оксазол-2-ил]метил]метансульфонамида (2 мг, выход: 1,8%) в виде бледно-желтого твердого вещества. ЖХ-МС (220 нм): 85,79%. 1H ЯМР (400 МГц, CHCl3-d) δ 7,16 (д, J=8,8 Гц, 2H), 7,12 (с, 2H), 7,08 (с, 1H), 6,86 (д, J=8,8 Гц, 2H), 4,86 (с, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,09 (с, 3H), 1,64 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 532,04; найдено 533,0.
[1020] Пример 10: Синтез N-[3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1H-пиразол-4-ил]метансульфонамида (A40)
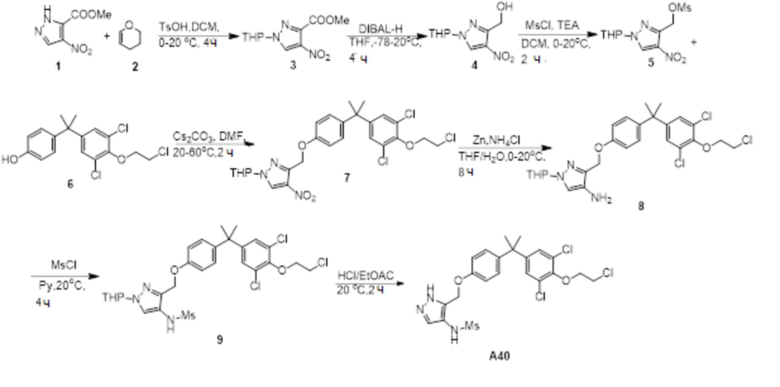
[1021] Метил-4-нитро-1-тетрагидропиран-2-ил-пиразол-3-карбоксилат (3): К раствору метил-4-нитро-1H-пиразол-5-карбоксилата (1) (2,00 г, 1,17 ммоль) в ДХМ (20 мл) прибавляли 3,4-дигидро-2H-пиран (2) (3,11 г, 14,0 ммоль) и пара-толуолсульфоновую кислоту (0,20 г, 1,17 ммоль) при 20°C. Смесь перемешивали при той же температуре в течение 4 часа. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в воду (100 мл) и экстрагировали ДХМ (30 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл), сушили над Na2SO4, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением метил-4-нитро-1-тетрагидропиран-2-ил-пиразол-3-карбоксилата (3) (2,7 г, выход: 90,5%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 8,39 (с, 1 H), 5,44 (дд, J=9,04, 2,87 Гц, 1 H), 4,06-4,15 (м, 1 H), 4,00 (с, 3 H), 3,74 (ддд, J=11,69, 9,04, 4,41 Гц, 1 H), 2,23 (дд, J=12,79, 3,09 Гц, 1 H), 1,86-2,07 (м, 3 H), 1,63-1,77 (м, 4 H), 1,57 (с, 6 H). ЖХ-МС (220 нм): 68% Точная масса 255,09; найдено 256,0.
[1022] (4-нитро-1-тетрагидропиран-2-ил-пиразол-3-ил)метанол (4): К раствору метил-4-нитро-1-тетрагидропиран-2-ил-пиразол-3-карбоксилата (3) (1,00 г, 3,92 ммоль) в ТГФ (10 мл) прибавляли DIBALH (7,8 мл, 7,8 ммоль, 1,0 моль/л в толуоле) при -78°C в атмосфере N2, и смесь перемешивали при 20°C в течение 4 часов. ЖХ-МС показала, что реакция завершилась. Смесь гасили водой (20 мл) и экстрагировали EtOAc (30 мл x 5). Объединенные органические слои промывали солевым раствором (20 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (4-нитро-1-тетрагидропиран-2-ил-пиразол-3-ил)метанола (70,0%, 0,90 г, выход: 70,8%) в виде бесцветного масла. Чистота ВЭЖХ (220 нм): 69%. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 8,39 (с, 1 H), 5,37 (дд, J=9,17, 2,69 Гц, 1 H), 4,93 (с, 2 H), 4,06-4,14 (м, 1 H), 3,70-3,77 (м, 1 H), 2,13-2,22 (м, 1 H), 1,87-2,09 (м, 2 H), 1,64-1,77 (м, 4 H). ЖХ-МС (M+H+) m/z: рассчит.: 227,09; найдено 250,2.
[1023] 3-(Хлорметил)-4-нитро-1-тетрагидропиран-2-ил-пиразол (5): К раствору (4-нитро-1-тетрагидропиран-2-ил-пиразол-3-ил)метанола (4) (1,3 г, 5,72 ммоль) в ДХМ (13 мл) прибавляли триэтиламин (1,2 г, 1,14 ммоль) при 20°C. Метансульфонилхлорид (0,8 г, 6,87 ммоль) добавляли по каплям при 0°C. Реакцию перемешивали при 20°C в течение 4 часов. ТСХ показала, что реакция завершилась. Смесь гасили водой (30 мл) и экстрагировали ДХМ (30 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (40 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 3-(хлорметил)-4-нитро-1-тетрагидропиран-2-ил-пиразола (5) (60,0%, выход: 30,9%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ м.д. 8,39 (с, 1 H), 5,38 (дд, J=9,26, 2,65 Гц, 1 H), 4,88 (с, 2 H), 3,75 (м, 2 H), 1,86 (м, 2 H), 1,67-1,77 (м, 4 H).
[1024] 3-[[4-[1-[3,5-Дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-4-нитро-1-тетрагидропиран-2-ил-пиразол (7): К раствору 3-(хлорметил)-4-нитро-1-тетрагидропиран-2-ил-пиразола (5) (0,20 г, 0,814 ммоль) в ДМФА (2 мл) прибавляли CS2CO3 (0,4 г, 1,22 ммоль) и 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенол (0,18 г, 0,49 ммоль) (6) при 20°C. Смесь перемешивали в течение 2 часов при 60°C. ЖХ-МС показала, что реакция завершилась. Смесь гасили водой (10 мл) и экстрагировали EtOAc (10 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл x 5), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-4-нитро-1-тетрагидропиран-2-ил-пиразола 3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-4-нитро-1-тетрагидропиран-2-ил-пиразола (7) (50,0% чистота, 0,20 г, выход: 21,6%) в виде бесцветного масла. ЖХ-МС (M+Na+) m/z: рассчит.: 567,1; найдено 590,2.
[1025] 3-[[4-[1-[3,5-Дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1-тетрагидропиран-2-ил-пиразол-4-амин (8): К раствору 3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-4-нитро-1-тетрагидропиран-2-ил-пиразол (7) (1.0 г, 1.76 ммоль) в ТГФ/H2O (6 мЛ/3 мЛ) добавляли NH4Cl (0.282 г, 5.27 ммоль) при 20 °C, Zn (0.575 г, 8.79 ммоль) добавляли к смеси при 0°C. Смесь перемешивали при 20°C в течение 8 часов. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили водой (10 мЛ) и экстрагировали EtOAc (10 мЛ x 3). Объединенные органические слои промывали солевым раствором (10 мЛ), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью препаративной ВЭЖХ (ТФУ) с получением 3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1-тетрагидропира-2-ил-пиразола-4-амина (8) (60 мг, выход: 6.3%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 7.07-7.17 (м, 4 H) 6.89-6.99 (м, 2 H), 5.23 (д, J=9.48 Гц, 1 H), 5.10 (с, 2 H), 4.24-4.30 (м, 2 H), 4.05 (д, J=11.47 Гц, 1 H), 3.83-3.89 (м, 2 H), 3.63-3.72 (м, 1 H), 2.06 (м, 2 H), 2.02 (с, 1 H), 1.62 (с, 6 H). ЖХ-МС (M+H+) m/z: рассчит: 537.14; найдено 538.2.
[1026] N-[3-[[4-[1-[3,5-Дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1-тетрагидропиран-2-ил-пиразол-4-ил]метансульфонамид (9): К раствору 3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил] фенокси]метил]-1-тетрагидропиран-2-ил-пиразол-4-амин (8) (60 мг, 0.111 ммоль) в ДХМ (0.5 мЛ) добавляли пиридин (17.6 мг, 0.223 ммоль) при 20°C. Мезилхлорид (0.0129 мЛ, 0.167 ммоль) добавляли по каплям к реационной смеси при 0°C. Смесь перемешивали при 20°C в течение 4 часов. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили водой (5 мЛ) и экстрагировали ДХМ (1 мЛ x 3). Объединенные органические слои промывали солевым раствором (10 мЛ), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением N-[3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1-тетрагидропиран-2-ил-пиразола-4-ил]метансульфонамида (9) (70 мг, выход: 81.5%) в виде бесцветного масла. Чистота ВЭЖХ (220 нм): 79%. ЖХ-МС (M+Na+) m/z: рассчит.: 615.1; найдено 616.2.
[1027] N-[3-[[4-[1-[3,5-Дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1H-пиразол-4-ил]метансульфонамид (A40): Раствор N-[3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1-тетрагидропиран-2-ил-пиразол-4-ил]метансульфонамида (9) (70 мг, 0,113 ммоль) в HCl/EtOAc (4M, 2 мл) перемешивали при 20°C в течение 2 часов. ЖХ-МС показала, что реакция завершилась. Смесь концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением N-[3-[[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенокси]метил]-1H-пиразол-4-ил]метансульфонамида (A40) (11,6 мг, выход: 18,2%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 7,71 (с, 1 H), 7,10-7,17 (м, 4 H), 6,89-6,94 (м, 2 H), 6,22 (с, 1 H), 5,21 (с, 2 H), 4,26 (т, J=6,39 Гц, 2 H), 3,86 (т, J=6,28 Гц, 2 H), 2,90 (с, 3 H), 1,62 (с, 6 H). ЖХ-МС (M+Na+) m/z: рассчит.: 531,06; найдено 532,1.
[1028] Пример 11: Синтез N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил) пиримидин-5-ил)метансульфонамида (A41):
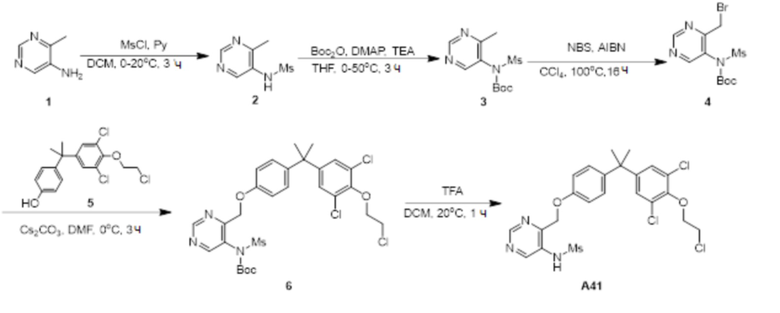
[1029] N-(4-Метилпиримидин-5-ил)метансульфонамид (2): К раствору 4-метилпиримидин-5-амина (1) (3,0 г, 27,5 ммоль) и пиримидина (10,9 г, 0,137 моль) в ДХМ (30 мл) прибавляли метансульфонилхлорид (6,3 г, 55,0 ммоль) при 0°C, и полученную смесь перемешивали при 20°C в течение 3 часов. ТСХ показала, что реакция завершилась. Смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением N-(4-метилпиримидин-5-ил)метансульфонамида (2) (1,0 г, 19,4%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ м.д. 8,98 (с, 1 H), 8,76 (с, 1 H), 6,68 (шир. с, 1 H), 3,13 (с, 3 H), 2,61 (с, 3 H).
[1030] трет-Бутил-(4-метилпиримидин-5-ил)(метилсульфонил)карбамат (3): К раствору N-(4-метилпиримидин-5-ил)метансульфонамида (2) (1,0 г, 5,34 ммоль) и TEA (1,1 г, 10,7 ммоль), DMAP (196 мг, 1,60 ммоль) в ТГФ (15 мл) прибавляли трет-бутоксикарбонил трет-бутил карбонат (1,75 г, 8,01 ммоль) при 0°C, и полученную смесь перемешивали при 50°C в течение 3 часов. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали и погасили водой (20 мл). Смесь экстрагировали EtOAc (10 мл x 5). Объединенные органические слои промывали солевым раствором (20 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением трет-бутил-N-(4-метилпиримидин-5-ил)-N-метилсульфонил-карбамата (3) (1,0 г, выход: 65,2%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ м.д. 9,07 (с, 1 H), 8,46 (с, 1 H), 3,53 (с, 3 H), 2,56 (с, 3 H), 1,49 (с, 9 H).
[1031] трет-Бутил-(4-(бромметил)пиримидин-5-ил)(метилсульфонил)карбамат (4): К смеси трет-бутил-N-(4-метилпиримидин-5-ил)-N-метилсульфонил-карбамата (3) (1,0 г, 3,48 ммоль) и NBS (929 мг, 5,22 ммоль) в CCl4 (20 мл) прибавляли AIBN (495 мг, 3,48 ммоль) в атмосфере N2, и полученную смесь перемешивали при 100°C в течение 16 часов. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали и погасили водой (40 мл), а затем экстрагировали ДХМ (10 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением трет-бутил-N-(бромметил)пиримидин-5-ил)-N-метилсульфонил-карбамата (4) (170 мг, выход: 13,3%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ м. д. 9,20 (шир. с, 1 H), 8,60 (шир. с, 1 H), 4,59 (д, J=10,64 Гц, 1 H), 4,42 (д, J=10,64 Гц, 1 H), 3,57-3,60 (м, 3 H), 1,48-1,51 (м, 9 H). ЖХ-МС (M+H+) m/z: 367,0; найдено 368,0.
[1032] трет-Бутил-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидин-5-ил)(метилсульфонил)карбамат (6): К смеси 4-(1-(3,5-дихлор-4-(2-хлорэтокси)фенил)-1-метил-этил)фенола (5) (134 мг, 0,37 ммоль) и Cs2CO3 (181 мг, 0,56 ммоль) в ДМФА (5 мл) прибавляли трет-бутил-N-(4-(бромметил)пиримидин-5-ил)-N-метилсульфонил-карбамат (4) (170 мг, 0,37 ммоль) при 0°C в атмосфере N2, и полученную смесь перемешивали при той же температуре в течение 3 часов. ТСХ показала, что реакция завершилась. Смесь выливали в воду (10 мл) и экстрагировали EtOAc (5 мл x 5). Объединенные органические слои промывали солевым раствором (10 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением трет-бутил-N-(4-((4-(1-(3,5-дихлор-4-(2-хлорэтокси)фенил)-1-метил-этил)фенокси)метил)пиримидин-5-ил)-N-метилсульфонил-карбамата (6) (50 мг, выход: 20,9%) в виде светлого масла. 1H ЯМР (400 МГц, CHCl3-d) δ м.д. 9,18 (с, 1 H), 8,62 (с, 1 H), 7,12 (с, 2 H), 7,09 (с, 2 H), 6,85-6,91 (м, 2 H), 5,15-5,30 (м, 2 H), 4,24 (т, J=6,28 Гц, 2 H), 3,85 (т, J=6,28 Гц, 2 H), 3,52 (с, 3 H), 1,60 (с, 6 H), 1,37 (с, 9 H).
[1033] N-(4-((4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидин-5-ил)метансульфонамид (A41): Смесь трет-бутил-N-(4-((4-(1-(3,5-дихлор-4-(2-хлорэтокси)фенил)-1-метил-этил)фенокси)метил)пиримидин-5-ил)-N-метилсульфонил-карбамата (6) (50 мг, 0,062 ммоль) в ДХМ (5,0 мл) и ТФУ (0,5 мл) перемешивали при 20°C в течение 1 часа. ЖХ-МС показала, что реакция завершилась. Полученную смесь концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением N-(4-((4-(1-(3,5-дихлор-4-(2-хлорэтокси)фенил)-1-метил-этил)фенокси)метил)пиримидин-5-ил) метансульфонамида (A41) (8 мг, выход: 23,7%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ м.д. 9,01 (д, J=4,40 Гц, 2 H), 7,81 (шир. с, 1 H), 7,16 (д, J=8,93 Гц, 2 H), 7,10 (с, 2 H), 6,93 (д, J=8,93 Гц, 2 H), 5,36 (с, 2 H), 4,26 (т, J=6,36 Гц, 2 H), 3,86 (т, J=6,36 Гц, 2 H), 3,03 (с, 3 H), 1,62 (с, 6 H). ЖХ-МС (M+H+) m/z: 545,05; найдено 546,0. ВЭЖХ чистота (220 нм): 84,4%.
[1034] Пример 12: Синтез N-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)-2-(метилсульфонамидо)оксазол-4-карбоксамида (A49)

[1035] Этил-2-(метилсульфонамидо)оксазол-4-карбоксилат (2): К раствору метансульфонамида (3,3 г, 34,2 ммоль) в ДМФА (30 мл) порциями прибавляли NaH (1,3 г, чистота 60%, 34,2 ммоль) при 0°C в атмосфере N2 . Смесь перемешивали при 0°C в течение 0,5 часа, а затем к данной смеси прибавляли этил-2-хлороксазол-4-карбоксилат (1) (3,0 г, 17,1 ммоль). Полученную смесь перемешивали при 60°C в течение 10 часов. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили H2O (10 мл) и непосредственно очищали обращенно-фазной ЖХСД (ТФУ) с получением этил-2-(метансульфонамидо)оксазол-4-карбоксилата (2) (1,17 г, выход: 29,2%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,61 (с, 1H), 4,39 (к, J=7,2 Гц, 2H), 3,12 (с, 3H), 1,37 (т, J=7,2 Гц, 3H). ЖХ-МС (M+H)+ m/z: рассчит. 234,03; найдено 235,1.
[1036] 2-(Метилсульфонамидо)оксазол-4-карбоновая кислота (3): К смеси этил-2-(метансульфонамидо)оксазол-4-карбоксилата (2) (100 мг, 0,43 ммоль) в ТГФ (3 мл) и H2O (1 мл) прибавляли LiOH.H2O (72 мг, 1,7 ммоль) при 25°C. Смесь перемешивали при той же температуре в течение 10 часа. ЖХ-МС показала, что реакция завершилась. Смесь доводили pH до 4 водной HCl (2 M), а затем концентрировали при пониженном давлении с получением 2-(метансульфонамидо)оксазол-4-карбоновой кислоты (3) (90 мг, 65% чистота) в виде желтого твердого вещества. 1H ЯМР (400 МГц, MeOH-d4) δ 7,94 (с, 1H), 3,08 (с, 3H). ЖХ-МС (M-H)- m/z: рассчит. 206,0; найдено 204,9.
[1037] N-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)-2-(метилсульфонамидо)оксазол-4-карбоксамид (A49): К раствору 2-(метан-сульфонамидо)оксазол-4-карбоновой кислоты (3) (60 мг, 0,3 ммоль) в ДМФА (3 мл) прибавляли 4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилин (4) (104 мг, 0,3 ммоль), HATU (133 мг, 0,35 ммоль) и TEA (0,12 мл, 0,9 ммоль) при 25°C. Смесь перемешивали при той же температуре в течение 3 часа. ЖХ-МС показала, что реакция завершилась, смесь гасили H2O (1 мл) и непосредственно очищали препаративной ВЭЖХ (ТФУ) с получением N-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]фенил]-2-(метансульфонамидо)оксазол-4-карбоксамида (A49) (23,2 мг, выход: 14,6%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d) δ 8,44 (с, 1H), 7,91 (с, 1H), 7,56 (д, J=8,8 Гц, 2H), 7,21 (д, J=8,8 Гц, 2H), 7,13 (с, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,32 (с, 3H), 1,65 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит. 545,03; найдено 546,0.
[1038] Пример 13: Синтез 5-((4-(2-(3,5-дихлор-4-(3,3,3-трифторпропокси)фенил)пропан-2-ил)фенокси)метил)-4-(метилсульфонил)оксазола (A54)
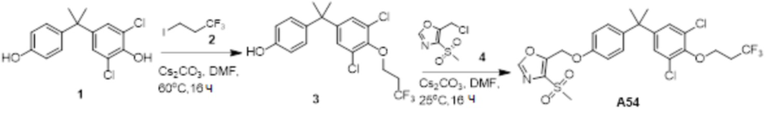
[1039] 2,6-Дихлор-4-(2-(4-гидроксифенил)пропан-2-ил)фенол (3): К раствору 2,6-дихлор-4-[1-(4-гидроксифенил)-1-метил-этил]фенола (1) (0,2 г, 0,67 ммоль) в ДМФА (2 мл) прибавляли 1,1,1-трифтор-3-иодпропан (2) (1,5 г, 6,7 ммоль) и Cs2CO3 (0,66 г, 2,0 ммоль). Полученную реакционную смесь перемешивали при 60°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь охлаждали и выливали в воду (10 мл), экстрагировали EtOAc (10 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл x 3), сушили над Na2SO4, фильтровали и концентрировали. Остаток очищали препаративной ТСХ с получением 4-[1-[3,5-дихлор-4-(3,3,3-трифторпропокси)фенил]-1-метил-этил]фенола (3) (80 мг, выход: 30,2%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,13 (с, 2H), 7,09-7,05 (м, 2H), 6,78-6,75 (м, 2H), 4,71 (с, 1H), 4,21 (т, J=6,8 Гц, 2H), 2,78-2,66 (м, 2H), 1,62 (с, 6H).
[1040] 5-((4-(2-(3,5-Дихлор-4-(3,3,3-трифторпропокси)фенил)пропан-2-ил)фенокси)метил)-4-(метилсульфонил)оксазол (A54): К смеси 4-[1-[3,5-дихлор-4-(3,3,3-трифторпропокси)фенил]-1-метил-этил]фенола (3) (40 мг, 0,10 ммоль) и 5-(хлорметил)-4-метилсульфонил-оксазола (4) (24 мг, 0,12 ммоль) в ДМФА (0,5 мл) прибавляли Cs2CO3 (66 мг, 0,20 ммоль), и смесь перемешивали при 25°C в течение 16 часов. ЖХ-МС показала, что реакция завершилась. Смесь выливали в воду (2 мл) и экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ТСХ с получением 5-[[4-[1-[3,5-дихлор-4-(3,3,3-трифторпропокси)фенил]-1-метил-этил]фенокси]метил]-4-метилсульфонилоксазола (A54) (18 мг, выход: 29,9%) в виде желтого масла. Чистота ЖХ-МС: (220 нм): 93,3%. 1H ЯМР (400 МГц, CHCl3-d) δ 8,00 (с, 1H), 7,16-7,12 (м, 4H), 6,94 (д, J=8,8 Гц, 2H), 5,42 (с, 2H), 4,22 (т, J=6,8 Гц, 2H), 3,19 (с, 3H), 2,78-2,64 (м, 2H), 1,62 (с, 6H). ЖХ-МС (M+NH4+) m/z: рассчит. 551,1; найдено 569,0.
[1041] Пример 14: Синтез 2-(2-хлорэтокси)-5-(2-(3-циано-4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A63)
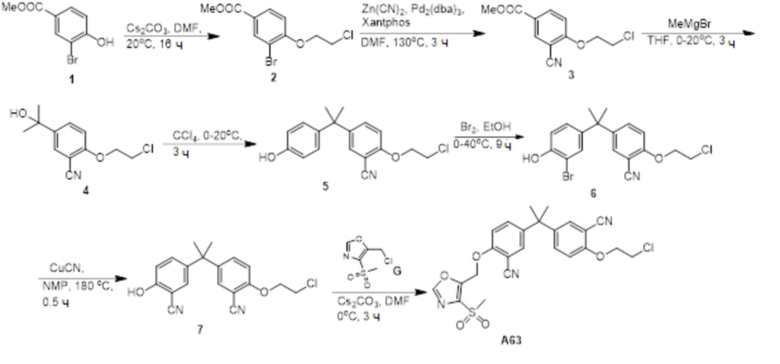
[1042] Метил-3-бром-4-(2-хлорэтокси)бензоат (2): К раствору метил-3-бром-4-гидроксибензоата (1) (15 г, 65 ммоль) в ДМФА (100 мл) прибавляли 1-бром-2-хлорэтан (11 г, 78 ммоль) и Cs2CO3 (32 г, 97 ммоль) в атмосфере N2 при 20°C. Затем реакционную смесь перемешивали при одной и той же температуре в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (100 мл), экстрагировали EtOAc(100 мл x 2). Объединенные органические слои промывали солевым раствором (100 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали ЖХСД с получением метил-3-бром-4-(2-хлорэтокси)бензоата (2) (13 г, выход: 67%) в виде белого твердого вещества. 1H ЯМР(400 МГц, CHCl3-d) δ 8,29-8,21 (м, 1H), 8,02-7,90 (м, 1H), 6,91 (д, J=8,6 Гц, 1H), 4,35 (т, J=6,1 Гц, 2H), 3,95-3,86 (м, 5H).
[1043] Метил-4-(2-хлорэтокси)-3-цианобензоат (3): К раствору метил-3-бром-4-(2-хлорэтокси)бензоата (2) (0,6 г, 2,0 ммоль) в ДМФА (20 мл) прибавляли Zn(CN)2 (0,72 г, 6,1 ммоль), Xantphos (0,1 г, 0,2 ммоль) и Pd2(dba)3 (0,18 г, 0,2 ммоль) в атмосфере N2 при 20°C. Реакционную смесь перемешивали при 130°C в течение 3 часов. ТСХ показала, что реакция завершилась. Тринадцать партий реакционных загрузок объединяли , а затем выливали в H2O (50 мл). Смесь экстрагировали EtOAc (80 мл x 3). Объединенные органические слои промывали солевым раствором (80 мл x 4), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали ЖХСД с получением метил-4-(2-хлорэтокси)-3-цианобензоата (3) (4,60 г, выход: 72,2%) в виде коричневого твердого вещества. 1H ЯМР(400 МГц, CHCl3-d) δ 8,27 (с, 1H), 8,22 (дд, J=2,1, 8,9 Гц, 1H), 7,02 (д, J=8,8 Гц, 1H), 4,41 (с, 2H), 3,92 (с, 3H), 3,92-3,88 (м, 2H).
[1044] 2-(2-Хлорэтокси)-5-(2-гидроксипропан-2-ил)бензонитрил (4): К раствору MeMgBr (3 M, 24 мл, 72 ммоль,) в ТГФ (20 мл) прибавляли метил-4-(2-хлорэтокси)-3-цианобензоат (3) (4,3 г, 18 ммоль) в ТГФ (40 мл) по каплям в атмосфере N2 при 0°C. Затем реакционную смесь перемешивали при 20°C в течение 3 часов. ЖХ-МС показала, что реакция завершилась. Смесь выливали в насыщенном водном NH4Cl (20 мл) и экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 2), сушили над Na2SO4, фильтровали, концентрировали при пониженном давлении . Остаток очищали ЖХСД с получением 2-(2-хлорэтокси)-5-(2-гидроксипропан-2-ил)бензонитрила (4) (2,9 г, выход: 67,4%) в виде коричневого масла. 1H ЯМР(400 МГц, CHCl3-d) δ=7,71 (д, J=2,4 Гц, 1H), 7,67 (дд, J=2,3, 8,7 Гц, 1H), 6,98-6,92 (м, 1H), 4,34 (т, J=6,1 Гц, 2H), 3,87 (т, J=6,2 Гц, 2H), 1,57 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит. 239,1; найдено: 240,1.
[1045] 2-(2-Хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрил (5): К смеси 2-(2-хлорэтокси)-5-(2-гидроксипропан-2-ил)бензонитрила (4) (2,9 г, 12,1 ммоль) и фенола (1,4 г, 14,5 ммоль) в CCl4 (40 мл) прибавляли BF3·Et2O (3,0 мл, 24 ммоль) по каплям в атмосфере N2 при 0°C. Затем реакционную смесь перемешивали при 20°C в течение 3 часов. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенном водном NaHCO3 (40 мл), экстрагировали ДХМ (20 мл x 2). Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (5) (2,77 г, выход: 72,5%) в виде коричневого масла. 1H ЯМР(400 МГц, CHCl3-d) δ 7,46 (с, 1H), 7,39-7,33 (дд, J=8,8 Гц, 1H), 7,05 (д, J=8,6 Гц, 2H), 6,88-6,83 (д, J=8,8 Гц, 1H), 6,80-6,73 (д, J=8,4 Гц, 2H), 5,00 (с, 1H), 4,31 (т, J=6,2 Гц, 2H), 3,85 (т, J=6,2 Гц, 2H), 1,63 (с, 6H).
[1046] 5-(2-(3-Бром-4-гидроксифенил)пропан-2-ил)-2-(2-хлорэтокси)бензонитрил (6): К раствору 2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (5) (1,35 г, 4,27 ммоль) в EtOH (30 мл) прибавляли Br2 (0,22 мл, 4,27 ммоль) по каплям в атмосфере N2 при 0°C. Затем реакционную смесь перемешивали при 20°C в течение 3 часов, а затем при 40°C в течениедополнительных 6 часов. ЖХ-МС показал наличие 23% исходного материала и 73% желаемого продукта в реакционной смеси. Смесь выливали в насыщенном водном Na2SO3(20 мл) затем концентрировали при пониженном давлении, чтобы удалить EtOH. Полученный раствор экстрагировали EtOAc (20 мл x 2). Объединенные органические слои промывали солевым раствором (20 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 5-(2-(3-бром-4-гидроксифенил)пропан-2-ил)-2-(2-хлорэтокси)бензонитрила (6) (1,16 г, выход: 68,7%) в виде коричневого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,45 (д, J=2,4 Гц, 1H), 7,37-7,31 (д, J=8,8 Гц, 1H), 7,30-7,28 (м, 1H), 7,03-6,98 (м, 1H), 6,96-6,92 (м, 1H), 6,87 (д, J=8,8 Гц, 1H), 5,44 (шир. с, 1H), 4,32 (т, J=6,2 Гц, 2H), 3,86 (т, J=6,2 Гц, 2H), 1,63 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит. 393,0; найдено: 393,8.
[1047] 2-(2-Хлорэтокси)-5-(2-(3-циано-4-гидроксифенил)пропан-2-ил)бензонитрил (7): К раствору 5-(2-(3-бром-4-гидроксифенил)пропан-2-ил)-2-(2-хлорэтокси) бензонитрила (6) (0,60 г, 1,52 ммоль) в NMP (5 мл) прибавляли CuCN (0,68 г, 7,6 моль) в атмосфере N2 при 20°C. Реакционную смесь перемешивали при 180°C в течение 0,5 часа. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (20 мл), экстрагировали EtOAc (10 мл x2). Объединенные органические слои промывали солевым раствором (10 мл x 6), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали ЖХСД с получением 2-(2-хлорэтокси)-5-(2-(3-циано-4-гидроксифенил)пропан-2-ил)бензонитрила (7) (130 мг, выход: 25,1%) в виде коричневого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,44-7,41 (м, 1H), 7,35 (д, J=2,4 Гц, 1H), 7,32 (дд, J=2,5, 8,9 Гц, 1H), 7,23 (дд, J=2,4, 8,8 Гц, 1H), 6,91 (д, J=7,3 Гц, 1H), 6,90-6,88 (дд, J=2,5, 8,9 Гц, 1H), 6,10 (шир., 1H), 4,37-4,28 (т, J=6,2 Гц, 2H), 3,87 (т, J=6,2 Гц, 2H), 1,64 (с, 6H).
[1048] 2-(2-Хлорэтокси)-5-(2-(3-циано-4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрил (A63): К раствору 2-(2-хлорэтокси)-5-(2-(3-циано-4-гидроксифенил)пропан-2-ил)бензонитрила (7) (130 мг, 0,38 ммоль) в ДМФА (2 мл) прибавляли 5-(хлорметил)-4-(метилсульфонил)оксазол (G) (75 мг, 0. 38 моль) и Cs2CO3 (249 мг, 0,76 ммоль) в атмосфере N2. Реакционную смесь перемешивали при 0°C в течение 3 часов. ЖХ-МС показала, что реакция завершилась. Смесь разбавляли EtOAc (5 мл) и выливали в H2O (5 мл). Водную фазу экстрагировали EtOAc (5 мл x2). Объединенные органические слои промывали солевым раствором (5 мл x 4), затем сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали препаративной ВЭЖХ (ТФУ) с получением 2-(2-хлорэтокси)-5-(2-(3-циано-4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A63) (53 мг, выход: 27,8%) в виде белого твердого вещества. Чистота ЖХ-МС (220 нм): 91,1%. 1H ЯМР(400 МГц, CHCl3-d) δ=8,04 (с, 1H), 7,41 (шир. с, 2H), 7,39-7,29 (м, 2H), 7,15-7,04 (м, 1H), 6,94-6,85 (д, J= 8,9 Гц, 1H), 5,51 (с, 2H), 4,33 (шир. т, J=6,0 Гц, 2H), 3,87 (шир. т, J=6,0 Гц, 2H), 3,25 (с, 3H), 1,64 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит. 499,1; найдено 500,1.
[1049] Пример 15: Синтез N-((2-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)амино)оксазол-5-ил)метил)метансульфонамида (A75)
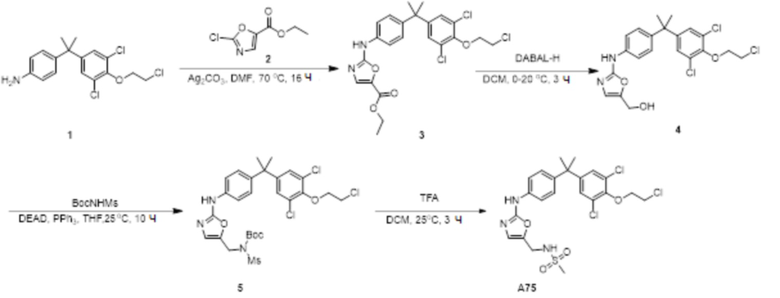
[1050] Этил-2-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)амино)оксазол-5-карбоксилат (3): К раствору 4-[1-[3,5-дихлор-4-(2-хлорэтокси)-фенил]-1-метил-этил]анилина (1) (1,00 г, 2,5 ммоль) в ДМФА (10 мл) прибавляли Ag2CO3 (1,05 г, 3,81 моль) и этил-2-хлороксазол-5-карбоксилат (2) (0,668 г, 3,81 ммоль) в атмосфере N2 при 20°C. Потом смесь перемешивали при 70°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь охлаждали, выливали в H2O (50 мл) и экстрагировали EtOAc (25 мл x 2). Органические слои объединяли и промывали солевым раствором (20 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением этил-2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-карбоксилата (3) (0,7 г, выход: 56,2%) в виде коричневого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,62 (с, 1H), 7,46 (с, 1H), 7,43 (д, J=8,8 Гц, 2H), 7,20 (д, J=8,8 Гц, 2H), 7,14 (с, 2H), 4,37 (к, J=7,2 Гц, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,64 (с, 6H), 1,38 (т, J=7,2 Гц, 3H).
[1051] (2-((4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)амино)оксазол-5-ил)метанол (4): К раствору этил-2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-карбоксилата (3) (0,6 г, 1,2 ммоль) в ДХМ (10 мл) прибавляли DIBAL-H (1 M в толуоле, 2,4 мл, 2,4 ммоль) в атмосфере N2 при 0°C. Затем полученную в результате смесь перемешивали при 20°C в течение 3 часов. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенный водный NH4Cl (20 мл) и экстрагировали ДХМ (10 мл x 3). Органические слои промывали солевым раствором (15 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением [2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-ил]-метанола (4) (410 мг, выход: 74,6%) в виде коричневого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,38 (д, J=8,8 Гц, 2H), 7,17 (д, J=8,8 Гц, 2H), 7,14 (с, 2H), 6,81 (с, 1H), 4,60 (с, 2H), 4,26 (т, J=6,4Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,63 (с, 6H).
[1052] трет-Бутил-((2-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)-амино)оксазол-5-ил)метил)(метилсульфонил)карбамат (5): К смеси [2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-ил]метанола (4) (50 мг, 0,1 ммоль) и трет-бутил-N-метилсульфонилкарбамата (21 мг, 0,1 ммоль) в ТГФ (3 мл) прибавляли PPh3 (58 мг, 0,22 ммоль) и DEAD (29 мг, 0,16 ммоль). Смесь перемешивали при 25°C в течение 10 часов в атмосфере N2. ЖХ-МС показала, что было обнаружено 30% желаемого продукта. Смесь концентрировали и очищали препаративной ТСХс получением трет-бутил-N-[[2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-ил]метил]-N-метилсульфонил-карбамата (5) (25 мг, выход: 36,0%) в виде бесцветного масла. 1H ЯМР (400 МГц, CHCl3-d) δ 7,39 (д, J=8,8 Гц, 2H), 7,16 (д, J=8,8 Гц, 2H), 7,13 (с, 2H), 6,84 (с, 1H), 4,86 (с, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,24 (с, 3H), 1,63 (с, 9H), 1,53 (с, 6H).
[1053] N-((2-((4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)амино)оксазол-5-ил)метил)метансульфонамид (A75): Раствор трет-бутил-N-[[2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-ил]метил]-N-метилсульфонил-карбамат а(5) (25 мг, 0,04 ммоль) в ДХМ (2 мл) и ТФУ (0,2 мл) перемешивали при 25°C в течение 3 часов. ЖХ-МС показала, что реакция завершилась. Смесь концентрировали и очищали препаративной ВЭЖХ (ТФУ) с получением N-[[2-[4-[1-[3,5-дихлор-4-(2-хлорэтокси)фенил]-1-метил-этил]анилино]оксазол-5-ил]метил]метансульфонамида (4,6 мг, выход: 21,9%) в виде желтого масла. Чистота ЖХ-МС (220 нм): 86%. 1H ЯМР (400 МГц, CHCl3-d) δ 7,36-7,33 (м, 2H), 7,25-7,22 (м, 2H), 7,11 (с, 2H), 7,02 (с, 1H), 5,18 (с, 1H), 4,36 (с, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,87 (т, J=6,4 Гц, 2H), 3,00 (с, 3H), 1,64 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 531,0; найдено 531,6.
[1054] Пример 16: Синтез 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-1,5,5-триметилимидазолидин-2,4-диона (B2)
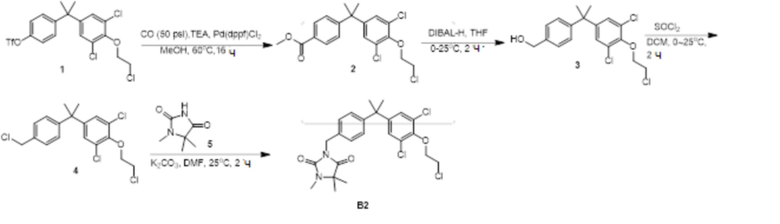
[1055] Метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоат (2): К раствору 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил трифторметансульфоната (1) (600 мг, 1,7 ммоль) и TEA (1 мл, 5,0 ммоль) в MeOH (15 мл) прибавляли Pd(dppf)Cl2 (200 мг, 0,3 ммоль). Полученную смесь перемешивали при 50 фунтов на кв. дюйм в атмосфере CO, и смесь нагревали при 60°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (30 мл), экстрагировали EtOAc (10 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (4 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ТСХ с получением метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоата (2) (300 мг, выход: 44,5%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 8,00-7,90 (м, 2H), 7,27-7,23 (м, 2H), 7,09 (с, 2H), 4,28-4,21 (м, 2H), 3,90 (с, 3H), 3,87-3,81 (м, 2H), 1,68-1,62 (м, 6H).
[1056] (4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанол (3): К раствору метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоата (2) (300 мг, 0,7 ммоль) в ТГФ (3 мл) прибавляли DIBAL-H (1,00 M, 2 мл) при 0°C , и смесь перемешивали при 0-25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (15 мл), экстрагировали EtOAc (5 мл x 2). Объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанола (3) (170 мг, выход: 60,9%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,32 (д, J=8,3 Гц, 2H), 7,24-7,18 (м, 2H), 7,17-7,11 (м, 2H), 4,75-4,63 (м, 2H), 4,31-4,22 (м, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,70-1,61 (м, 6H).
[1057] 1,3-Дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензол (4): К раствору (4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанола (3) (40 мг, 0,1 ммоль) в ДХМ (2 мл) прибавляли SOCl2 (0,1 мл, 1,1 ммоль) при 0°C, и смесь перемешивали при 0-25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (10 мл), экстрагировали ДХМ (3 мл x 2). Объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 1,3-дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензола (4) (40 мг, выход: 95,3%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,36-7,30 (м, 2H), 7,20 (д, J=8,4 Гц, 2H), 7,15-7,15 (м, 1H), 7,14 (с, 1H), 4,59 (с, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,68-1,62 (м, 6H).
[1058] 3-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-1,5,5-триметилимидазолидин-2,4-дион (B2): К смеси 1,5,5-триметилимидазолидин-2,4-диона (5) (20 мг, 0,2 ммоль) и K2CO3 (70 мг, 0,5 ммоль) в ДМФА (3 мл) прибавляли 1,3-дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензол (4) (50 мг, 0,1 ммоль) при 25°C, и смесь перемешивали при одной и той же температуре в течение 2 часов. ЖХ-МС показала, что реакция завершилась.Смесь выливали в H2O (10 мл), экстрагировали EtOAc (5 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (5 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCl) с получением 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-1,5,5-триметилимидазолидин-2,4-диона (B2) (20 мг, выход: 31,8%) в виде бесцветного масла. Чистота ЖХ-МС (220 нм): 96,1%. 1H ЯМР (400 МГц, CHCl3-d) δ=7,30-7,25 (м, 1H), 7,28-7,25 (м, 1H), 7,30-7,25 (м, 1H), 7,15-7,10 (м, 2H), 7,10-7,08 (м, 2H), 4,66-4,57 (м, 2H), 4,24 (т, J=6,4 Гц, 2H), 3,89-3,77 (м, 2H), 2,87 (с, 3H), 1,65-1,54 (м, 6H), 1,41-1,34 (м, 6H). ЖХ-МС (M+H+) m/z: рассчит.: 496,1; найдено 497,1.
[1059] Пример 17: Синтез 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметил-1-(метилсульфонил)имидазолидин-2,4-диона (B3)
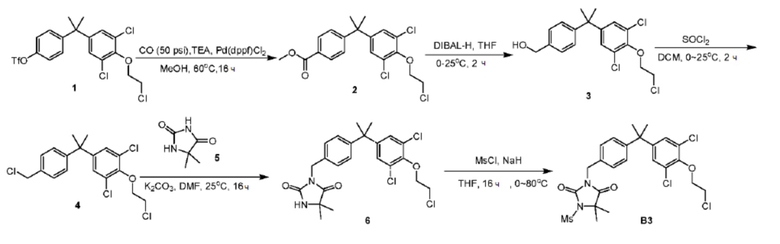
[1060] Метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоат (2): К раствору 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил трифторметансульфоната (1) (600 мг, 1,7 ммоль) и TEA (1 мл, 5,0 ммоль) в MeOH (15 мл) прибавляли Pd(dppf)Cl2 (200 мг, 0,3 ммоль). Полученную смесь перемешивали при 50 фунтов на кв. дюйм в атмосфере CO, и смесь нагревали при 60°C в течение 16 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (30 мл), экстрагировали EtOAc (10 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (4 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ТСХ с получением метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоата (2) (300 мг, выход: 44,5%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ 8,00-7,90 (м, 2H), 7,27-7,23 (м, 2H), 7,09 (с, 2H), 4,28-4,21 (м, 2H), 3,90 (с, 3H), 3,87-3,81 (м, 2H), 1,68-1,62 (м, 6H).
[1061] (4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанол (3): К раствору метил-4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензоата (2) (300 мг, 0,7 ммоль) в ТГФ (3 мл) прибавляли DIBAL-H (1,00 M, 2 мл) при 0°C , и смесь перемешивали при 0-25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (15 мл), экстрагировали EtOAc (5 мл x 2). Объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанола (3) (170 мг, выход: 60,9%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,32 (д, J=8,3 Гц, 2H), 7,24-7,18 (м, 2H), 7,17-7,11 (м, 2H), 4,75-4,63 (м, 2H), 4,31-4,22 (м, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,70-1,61 (м, 6H).
[1062] 1,3-Дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензол (4): К раствору (4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенил)метанола (3) (40 мг, 0,1 ммоль) в ДХМ (2 мл) прибавляли SOCl2 (0,1 мл, 1,1 ммоль) при 0°C, и смесь перемешивали при 0-25°C в течение 2 часов. ТСХ показала, что реакция завершилась. Смесь выливали в H2O (10 мл), экстрагировали ДХМ (3 мл x 2). Объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 1,3-дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензола (4) (40 мг, выход: 95,3%) в виде желтого масла. 1H ЯМР (400 МГц, CHCl3-d) δ=7,36-7,30 (м, 2H), 7,20 (д, J=8,4 Гц, 2H), 7,15-7,15 (м, 1H), 7,14 (с, 1H), 4,59 (с, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,68-1,62 (м, 6H).
[1063] 3-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметилимидазолидин-2,4-дион (6): К смеси 1,3-дихлор-2-(2-хлорэтокси)-5-(2-(4-(хлорметил)фенил)пропан-2-ил)бензола (4) (100 мг, 0,2 ммоль) и 5,5-диметилимидазолидин-2,4-диона (5) (30 мг, 0,2 ммоль) в ДМФА (5 мл) прибавляли K2CO3 (100 мг, 0,8 ммоль) при 25°C, и смесь перемешивали при 25°C в течение 16 часов. ЖХ-МС показала, что реакция завершилась. Смесь выливали в H2O (15 мл), экстрагировали EtOAc (5 мл x 2). Объединенные органические слои промывали солевым раствором (5 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметилимидазолидин-2,4-диона (6) (40 мг, выход: 64,8%) в виде желтого масла. Чистота ЖХ-МС (220 нм): 97,7%. 1H ЯМР (400 МГц, CHCl3-d) δ=7,16-7,08 (м, 4H), 6,83 (д, J=8,8 Гц, 2H), 5,36 (с, 1H), 5,27 (с, 1H), 4,51 (с, 2H), 4,45 (с, 2H), 4,17-4,12 (м, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,31 (с, 3H), 2,28 (квин., J=6,1 Гц, 2H), 1,62 (с, 6H), 1,49 (с, 9H). ЖХ-МС (M+H+) m/z: рассчит.: 482,1; найдено 483,2.
[1064] 3-(4-(2-(3,5-Дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметил-1-(метилсульфонил)имидазолидин-2,4-дион (B3): К раствору 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметилимидазолидин-2,4-диона (6) ((40 мг, 0,1 ммоль) в ТГФ (2 мл) прибавляли мезилхлорид (0,1 мл, 0,2 ммоль) и NaH (60,0%, 6 мг, 0,2 ммоль) при 0°C, и смесь перемешивали при 80°C в течение 16 часов.ТСХ показала, что реакция завершилась. Реакционную смесь гасили насыщенным водным NH4Cl (10 мл) и экстрагировали EtOAc (3 мл x 2). Объединенные органические слои промывали солевым раствором (3 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCl) с получением 3-(4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)бензил)-5,5-диметил-1-(метилсульфонил)имидазолидин-2,4-диона (5 мг, выход: 10,8%) в виде желтого масла. Чистота ЖХ-МС (220 нм): 81,8%. 1H ЯМР (400 МГц, CHCl3-d) δ=7,31-7,28 (м, 2H), 7,20-7,14 (м, 2H), 7,14-7,11 (м, 2H), 4,71-4,65 (м, 2H), 4,27 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,38 (с, 3H), 1,76-1,71 (м, 6H), 1,64 (с, 6H). ЖХ-МС (M+H+) m/z: рассчит.:526, найдено: 527.
[1065] Пример 18: Синтез 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A28)
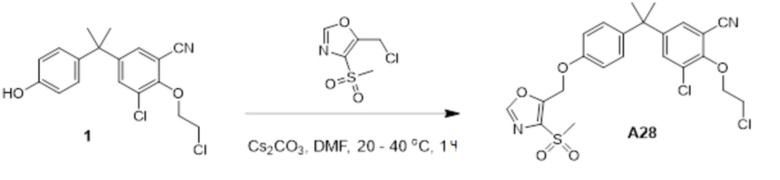
[1066] К смеси 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (900 мг, 2,6 ммоль) в ДМФА (10 мл) прибавляли Cs2CO3 (167 мг, 5,1 ммоль) и 5-(хлорметил)-4-(метилсульфонил)оксазол (750 мг, 3,9 ммоль) в атмосфере N2 при 20°C. Смесь перемешивали при 40°C в течение 1 часов. ТСХ показала, что реакция завершилась. Смесь охлаждали до комнатной температуры, выливали в H2O (40 мл) и экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали солевым раствором (20 мл x 4), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД, а затем растирали с MTBE: EtOAc =10 мл: 2 мл с получением 3-хлор-2-(2-хлорэтокси)5-(2-(4-((4-(метилсульфонил)оксазол-5-ил)этокси)фенил)пропан-2-ил)бензонитрила (310 мг, выход: 23,2%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,00 (с, 1H), 7,43 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,13 (д, J=8,4 Гц, 2H), 6,96 (д, J=8,8 Гц, 2H), 5,42 (с, 2H), 4,43 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,4 Гц, 2H), 3,21 (с, 3H), 1,64 (с, 6H). ЖХ-МС (220 нм): 97,8%. Точная масса: 508,1; найдено 509,1, 511,1.
[1067] Пример 19: Синтез 2-(2-хлорэтокси)-3-метил-5-(2-(4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A29)
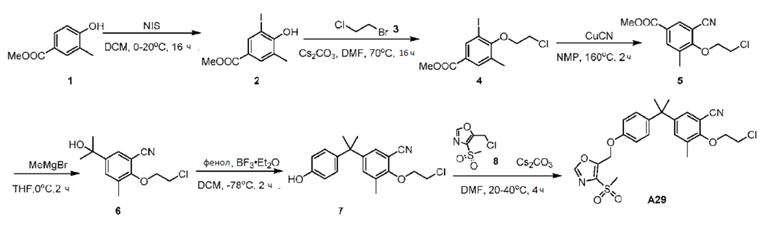
[1068] Метил-4-гидрокси-3-иод-5-метилбензоат (2): К раствору метил-4-гидрокси-3-метил-бензоата (3,0 г, 18,0 ммоль) в ДХМ (30 мл) прибавляли NIS (4,0 г, 18,0 ммоль) при 0°C в атмосфере N2. Смесь перемешивали при 20°C в течение 16 ч. ТСХ показала, что реакция завершилась. Смесь выливали в воду (20 мл), экстрагировали ДХМ (30 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением метил-4-гидрокси-3-иод-5-метил-бензоата (3,6 г, выход: 68,3%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,21 (д, J=1,2 Гц, 1 H), 7,80 (с, 1 H), 5,70 (с, 1 H), 3,89 (с, 3 H), 2,34 (с, 3 H).
[1069] Метил-4-(2-хлорэтокси)-3-иод-5-метилбензоат (4): К смеси метил-4-гидрокси-3-иод-5-метил-бензоата (3,6 г, 12,3 ммоль) и 1-бром-2-хлорэтан (1,9 г, 13,6 ммоль) в ДМФА (80 мл) прибавляли Cs2CO3 (8,0 г, 24,7 ммоль), и смесь перемешивали при 70°C в течение 16 ч. ТСХ показала, что реакция завершилась. Смесь охлаждали и выливали в воду (80 мл), экстрагировали EtOAc (50 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением метил-4-(2-хлорэтокси)-3-иод-5-метил-бензоата (2,3 г, выход: 52,6%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ=8,31 (д, J=1,6 Гц, 1 H), 7,87-7,86 (м, 1 H), 4,17 (т, J=6,0 Гц, 2 H), 3,89-3,95 (м, 5 H), 2,41 (с, 3 H).
[1070] Метил 4-(2-хлорэтокси)-3-циано-5-метилбензоат (5): К раствору метил-4-(2-хлорэтокси)-3-иод-5-метил-бензоата (2,1 г, 6,0 ммоль) в NMP (20 мл) прибавляли CuCN (637 мг, 7,1 ммоль) в атмосфере N2 , и смесь перемешивали при 160°C в течение 2 ч. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали и выливали в воду (60 мл) и экстрагировали EtOAc (30 мл x 3). Объединенные органические слои промывали солевым раствором (30 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением метил-4-(2-хлорэтокси)-3-циано-5-метил-бензоата (0,7 г, выход: 46,6%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CHCl3-d): δ 8,13 (д, J=2,0 Гц, 1 H), 8,09 (д, J=1,2 Гц, 1 H), 4,54 (т, J=5,6 Гц, 2 H), 3,93 (с, 3 H), 3,89 (т, J=5,6 Гц, 2 H), 2,39 (с, 3 H). ЖХ-МС (220 нм): 78,1%. Точная масса: 253,1; найдено: 254,1.
[1071] 2-(2-хлорэтокси)-5-(2-гидроксипропан-2-ил)-3-метилбензонитрил (6): К смеси метил-4-(2-хлорэтокси)-3-циано-5-метил-бензоата (500 мг, 2,1 ммоль) и TEA (1,7 мл, 11,8 ммоль) в ТГФ (10 мл) прибавляли MeMgBr (3M, 9,8 ммоль, 3,3 мл) по каплям при 0°C в атмосфере N2, и смесь перемешивали при 0°C в течение 2 ч. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенном водном NH4Cl (20 мл), экстрагировали EtOAc (10 мл x 4), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением 2-(2-хлорэтокси)-5-(2-гидроксипропан-2-ил)-3-метилбензонитрила (250 мг, выход: 50,0%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,55 (с, 2 H), 4,38 (т, J=5,6 Гц, 2 H), 3,87 (т, J=5,6 Гц, 2 H), 2,36 (с, 3 H), 1,57 (с, 6 H).
[1072] 2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)-3-метилбензонитрил (7): К раствору 2-(2-хлорэтокси)-5-(2-гидрокси-2-метил-этил)-3-метил-бензонитрила (250 мг, 1,0 ммоль) и фенола (110 мг, 1,2 ммоль) в ДХМ (3 мл) прибавляли BF3.Et2O (0,5 мл, 2 ммоль) при -78°C в атмосфере N2 , и смесь перемешивали при одной и той же температуре в течение 2 ч. ТСХ показала, что реакция завершилась. Смесь выливали в воду (5 мл) и экстрагировали ДХМ (5 мл x 3). Объединенные органические слои промывали солевым раствором (15 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением 2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)-3-метилбензонитрила (220 мг, выход: 67,7%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ=7,29 (д, J= 2,4 Гц, 1H), 7,21 (д, J= 2,0 Гц, 1H), 7,06 (д, J= 6,4 Гц, 2H), 6,76 (д, J= 6,8 Гц, 2H), 4,73 (с, 1H), 4,36 (т, J=6,0 Гц, 2 H), 3,86 (т, J=6,0 Гц, 2 H), 2,29 (с, 3H), 1,63 (с, 6H)
[1073] 2-(2-хлорэтокси)-3-метил-5-(2-(4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрил (A29): К смеси 2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)-3-метилбензонитрила (100 мг, 0,3 ммоль) и 5-(хлорметил)-4-метилсульфонил-оксазола (60 мг, 0,3 ммоль) в ДМФА (3 мл) прибавляли Cs2CO3 (200 мг, 0,6 ммоль) при 20°C, и смесь перемешивали при 40°C в течение 4 ч. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали, фильтровали и очищали препаративной ВЭЖХ (ТФУ) с получением 2-(2-хлорэтокси)-3-метил-5-(2-(4-((4-(метилсульфонил)оксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (26 мг, выход: 17,5%) в виде желтого масла. 1H ЯМР (400 МГц, MeOD): δ 8,39 (с, 1 H), 7,33-7,35 (м, 1 H), 7,31-7,32 (м, 1 H), 7,16 (д, J=8,8 Гц, 2 H), 6,96 (д, J=8,8 Гц, 2 H), 5,41 (с, 2 H), 4,32 (т, J=5,6 Гц, 2 H), 3,88 (т, J=5,4 Гц, 2 H), 3,18 (с, 3 H), 2,28 (с, 3 H), 1,64 (с, 6 H). ЖХ-МС: (220 нм): 98,8%. Точная масса: 488,1; найдено 489,0.
[1074] Пример 20: Синтез N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамида (A74)
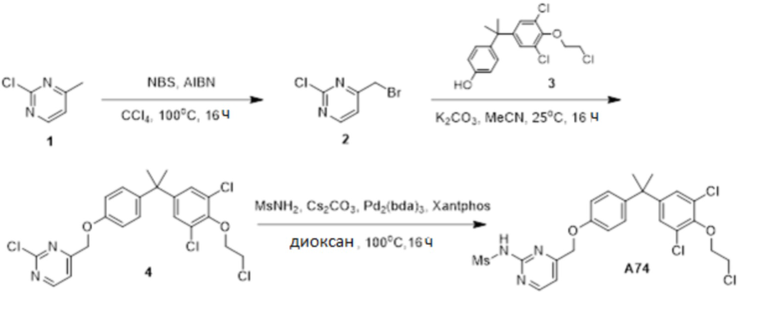
[1075] 4-(бромметил)-2-хлорпиримидин (2): К смеси 2-хлор-4-метил-пиримидина (5,0 г, 38,9 ммоль) и NBS (10,4 г, 58,3 ммоль) в CCl4 (100 мл) прибавляли AIBN (2,18 г, 19,4 ммоль) при 20°C, и смесь перемешивали при 100°C в течение 16 ч. ЖХ-МС показала, что большая часть исходного материала была поглощена. Смесь охлаждали, прибавляли в воду (200 мл) и экстрагировали ДХМ (100 мл x 5). Объединенные органические фазы промывали солевым раствором (200 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали ЖХСД с получением 4-(бромметил)-2-хлорпиридина (2,0 г, выход: 24,8%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,65 (д, J=5,2 Гц, 1H), 7,45 (д, J=5,2 Гц, 1H), 4,43 (с, 2H).
[1076] 2-хлор-4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидин (4): К смеси 4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенола (0,2 г, 0,6 ммоль) и 4-(бромметил)-2-хлорпиримидина (127 мг, 0,6 ммоль) в MeCN (5 мл) прибавляли K2CO3 (115 мг, 0,83 ммоль), и смесь перемешивали при 25°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Полученную смесь гасили насыщенным водным NH4Cl (5 мл), экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-хлор-4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидина (270 мг, выход: 82,9%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,66 (д, J=5,2 Гц, 1H), 7,56 (д, J=5,2 Гц, 1H), 7,16 (д, J=8,8 Гц, 2H), 7,13 (с, 2H), 6,88 (д, J=8,8 Гц, 2H), 5,15 (с, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 1,63 (с, 6H).
[1077] N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси) метил)пиримидин -2-ил)метансульфонамид (A74): К смеси 2-хлор-4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидина (200 мг, 0,3 ммоль), метансульфонамида (62,6 мг, 0,66 ммоль), Cs2CO3 (322 мг, 0,99 ммоль) в безводном диоксане (8 мл) прибавляли Pd2(dba)3 (30,1 мг, 0,03 ммоль) и Xantphos (38,1 мг, 0,06 ммоль), и смесь перемешивали при 100°C в течение 16 ч в атмосфере N2. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали, выливали в воду (10 мл), экстрагировали EtOAc (10 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением желаемого продукта N-(4-((4-(2-(3,5-дихлор-4-(2-хлорэтокси)фенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамида (61,4 мг, выход: 34,2%) в виде светлого красно-зеленого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,61 (д, J=5,2 Гц, 1H), 7,29 (д, J=5,2 Гц, 1H), 7,16-7,11 (м, 4H), 6,88 (д, J=8,8 Гц, 2H), 5,09 (с, 2H), 4,26 (т, J=6,4 Гц, 2H), 3,86 (т, J=6,4 Гц, 2H), 3,47 (с, 3H), 1,63 (с, 6H). ЖХ-МС: (220 нм): 98,1%. Точная масса: 543,1; найдено 544.
[1078] Пример 21: Синтез 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилсульфонил)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (A93)
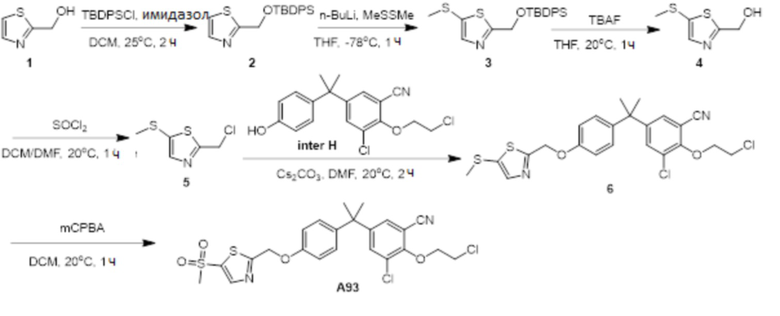
[1079] 2-(((трет-бутилдифенилсилил)окси)метил)тиазол (2): К смеси тиазол-2-илметанола (1,0 г, 8,7 ммоль) и имидазол (1,2 г, 17,4 ммоль) в ДХМ (50 мл) порциями прибавляли TBDPSCl (2,9 г, 10,4 ммоль) в при 25°C. Смесь перемешивали при одной и той же температуре в течение 2 ч. ТСХ показала, что реакция завершилась. Реакционную смесь гасили водой (80 мл) и экстрагировали ДХМ (50 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 2-(((трет-бутилдифенилсилил)окси)метил)тиазола (3,0 г, выход: 97,7%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ=7,73-7,70 (м, 4H), 7,48-7,45 (м, 1H), 7,44-7,38 (м, 6H), 7,31 (д, J=3,2 Гц, 1H), 5,02 (с, 2H), 1,14 (с, 9H).
[1080] 2-(((трет-бутилдифенилсилил)окси)метил)-5-(метилтио)тиазол (3): К раствору 2-(((трет-бутилдифенилсилил)окси)метил)тиазола (4,2 г, 11,9 ммоль) в ТГФ (80 мл) прибавляли n-BuLi (2,50 M, 9,50 мл) по каплям при -78°C в атмосфере N2. Смесь перемешивали при одной и той же температуре в течение 30 мин. Затем к данной смеси по каплям прибавляли 1,2-диметилдисульфан (2,2 г, 23,8 ммоль) при -78°C в атмосфере N2 и перемешивали в течение 30 мин. ТСХ показала, что реакция завершилась. Реакционную смесь выливали в насыщенном водном NH4Cl (100 мл) и экстрагировали EtOAc (50 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-(((трет-бутилдифенилсилил)окси)метил)-5-(метилтио)тиазола (4,6 г, выход: 96,9%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,74-7,67 (м, 4H), 7,60 (с, 1H), 7,48-7,38 (м, 6H), 4,92 (с, 2H), 2,50 (с, 3H), 1,13 (с, 9H).
[1081] (5-(метилтио)тиазол-2-ил)метанол (4): К раствору 2-(((трет-бутилдифенилсилил)окси)метил)-5-(метилтио)тиазола (5,4 г, 13,5 ммоль) в безводном ТГФ (27 мл) прибавляли TBAF (1,00 M, 27,0 мл) по каплям при 20°C и перемешивали при одной и той же температуре в течение 1 часа. ТСХ показала, что реакция завершилась. Реакционную смесь погасили водой (50 мл). Водный слой экстрагировали EtOAc (30 мл x 3). Объединенные органические слои промывали солевым раствором (30 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением (5-(метилтио)тиазол-2-ил)метанола (1,4 г, выход: 64,3%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,63 (с, 1H), 4,91 (д, J=5,6 Гц, 2H), 2,72 (т, J=6,0 Гц, 1H), 2,49 (с, 3H).
[1082] 2-(хлорметил)-5-(метилтио)тиазол (5): К раствору (5-(метилтио)тиазол-2-ил)метанола (0,4 г, 2,5 ммоль) в ДХМ (5 мл) прибавляли SOCl2 (0,5 мл, 7,4 ммоль) при 20 °C, затем прибавляли ДМФА (0,1 мл). Смесь перемешивали при одной и той же температуре в течение 1 ч. ТСХ показала, что реакция завершилась. Реакционную смесь концентрировали при пониженном давлении. Остаток гасили водой (10 мл) и экстрагировали ДХМ (10 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-(хлорметил)-5-(метилтио)тиазола (0,4 г, выход: 89,7%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,63 (с, 1H), 4,82 (с, 2H), 2,52 (с, 3H).
[1083] 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилтио)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (6): К смеси 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (100 мг, 0,3 ммоль) и 2-(хлорметил)-5-(метилтио)тиазола (103 мг, 0,6 ммоль) в ДМФА (3 мл) прибавляли Cs2CO3 (186 мг, 0,6 ммоль), и смесь перемешивали при 20°C в течение 2 ч. ЖХ-МС показала, что реакция завершилась. Полученную смесь гасили водой (10 мл) и экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилтио)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (80 мг, выход: 56,8%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,66 (с, 1H), 7,44 (с, 1H), 7,33 (с, 1H), 7,12 (шир. д, J=8,4 Гц, 2H), 6,95 (шир. д, J=8,8 Гц, 2H), 5,30 (с, 2H), 4,42 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 2,50 (с, 3H), 1,65 (с, 6H).
[1084] 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилтио)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (A93): Суспензию 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилтио)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (80 мг, 0,16 ммоль) и м-ХПБК (80,0%, 105 мг, 0,49 ммоль) в ДХМ (3 мл) перемешивали при 20°C в течение 1 ч. ЖХ-МС показала, что реакция завершилась. Полученную смесь выливали в насыщенном водном NaHCO3 (3 мл) и экстрагировали ДХМ (3 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (ТФУ) с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилсульфонил)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (64,2 мг, выход: 75,4%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,31 (с, 1H), 7,45 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,16 (д, J=8,8 Гц, 2H), 6,95 (д, J=8,8 Гц, 2H), 5,40 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,25 (с, 3H), 1,66 (с, 6H). ЖХ-МС (220 нм): 99,5%. Точная масса: 524,0; найдено 525,1, 527,1.
[1085] Пример 22: Синтез N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси) метил)пиримидин-2-ил)метансульфонамида N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамида (A109)
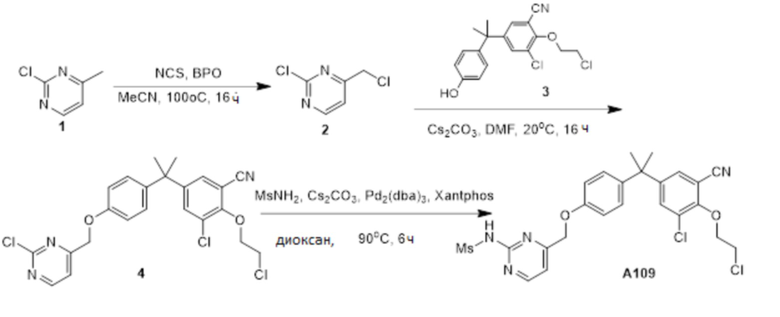
[1086] 2-хлор-4-(хлорметил)пиримидин (2): К смеси 2-хлор-4-метил-пиримидина (50,0 г, 398 ммоль) и NCS (77,9 г, 583 ммоль) в MeCN (250 мл) порциями прибавляли бензоилбензолкарбопероксоат (28,3 г, 117 ммоль) при 20°C, и смесь перемешивали при 100°C в течение 16 ч в атмосфере N2. ТСХ показала, что большая часть исходного материала была поглощена и появилось два новых пятна. Смесь охлаждали до комнатной температуры, выливали в воду (500 мл) и экстрагировали EtOAc (200 мл x 3). Органические слои объединяли и промывали солевым раствором (200 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 2-хлор-4-(хлорметил)пиримидина (22 г, выход: 31,2%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,69 (д, J=5,2 Гц, 1H), 7,54 (д, J=5,0 Гц, 1H), 4,61 (с, 2H).
[1087] 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((2-хлорпиримидин-4-ил)метокси)фенил)пропан-2-ил)бензонитрил (4): К смеси 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (18,0 г, 51,4 ммоль) и 2-хлор-4-(хлорметил)пиримидина (10,1 г, 61,7 ммоль) в ДМФА (150 мл) прибавляли Cs2CO3 (33,5 г, 103,4 ммоль) при 20°C, и смесь перемешивали при одной и той же температуре в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (300 мл) и экстрагировали EtOAc (150 мл x 3). Объединенные органические слои промывали солевым раствором (150 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((2-хлорпиримидин-4-ил)метокси)фенил)пропан-2-ил)бензонитрила (15,5 г, выход: 63,3%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,67 (д, J=5,2 Гц, 1H), 7,56 (д, J=5,2 Гц, 1H), 7,45 (д, J=2,4 Гц, 1H), 7,35-7,29 (м, 1H), 7,13 (д, J=8,8 Гц, 2H), 6,90 (д, J=8,8 Гц, 2H), 5,16 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 1,65 (с, 6H).
[1088] N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамид (A109): К смеси 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((2-хлорпиримидин-4-ил)метокси)фенил)пропан-2-ил)бензонитрила (15,5 г, 32,5 ммоль), метансульфонамида (9,3 г, 97,5 ммоль), Cs2CO3 (21,2 г, 65,0 ммоль) и Xantphos (1,88 г, 3,25 ммоль) в 1,4-диоксане (450 мл) прибавляли Pd2(dba)3 (3,0 г, 3,3 ммоль) при 20°C, и смесь перемешивали при 90°C в течение 6 ч в атмосфере N2. ЖХ-МС показала, что реакция завершилась. Смесь охлаждали до комнатной температуры, выливали в воду (300 мл) и экстрагировали EtOAc (300 мл x 3). Объединенные органические слои промывали солевым раствором (300 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением неочищенного продукта, а затем дополнительно очищали препаративной ВЭЖХ (ТФУ) с получением N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси) метил)пиримидин-2-ил)метансульфонамида (5,30 г, выход: 30,1%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=10,02 (шир. с, 1H), 8,69 (д, J=5,2 Гц, 1H), 7,45 (д, J=2,4 Гц, 1H), 7,34-7,31 (м, 1H), 7,30 (д, J=5,2 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 6,91 (д, J=8,8 Гц, 2H), 5,13 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,47 (с, 3H), 1,65 (с, 6H). ЖХ-МС (220 нм): 99,0%. Точная масса: 534,09; найдено 535,1, 537,0.
[1089] Пример 23: Синтез N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)оксазол-2-ил)метансульфонамида (A122)

[1090] 2-Хлор-4-(1-этоксивинил)-5-метилпиримидин (2): К смеси 2,4-дихлор-5-метил-пиримидина (10,0 г, 61,3 ммоль) и трибутил(1-этоксивинил)станнана (22,2 г, 0,0613 моль) в ДМФА (200 мл) прибавляли Pd(PPh3)2Cl2 (2,15 г, 3,1 ммоль) при 20°C, и смесь перемешивали при 100°C в течение 5 ч в атмосфере N2. ТСХ показала, что реакция завершилась. Реакционную смесь гасили раствором KF (30 г, 0,172 моль, растворено в 500 мл воды), фильтровали и экстрагировали EtOAc (100 мл x 3). Объединенные органические слои промывали солевым раствором (100 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 2-хлор-4-(1-этоксивинил)-5-метил-пиримидина (6,0 г, выход: 41,5%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3): δ 8,40 (с, 1H), 5,01 (д, J=2,4 Гц, 1H), 4,55 (д, J=2,4 Гц, 1H), 3,94 (к, J=7,2 Гц, 2H), 2,38 (с, 3H), 1,41 (т, J=7,2 Гц, 3H).
[1091] Этил-2-хлор-5-метилпиримидин-4-карбоксилат (3): O3 (газ) барботировали в раствор 2-хлор-4-(1-этоксивинил)-5-метил-пиримидина (2) (чистота: 50,0%, 6,0 г, 0,0151 моль) в ДХМ (60,0 мл) при -30°C в течение 0,5 часа. ТСХ показала, что реакция завершилась. O2 и N2 барботировали в раствор, указанный выше, при 10°C в течение 0,5 ч. (CH3)2S (10,0 мл, 0,0151 моль) прибавляли в данный раствор, и смесь перемешивали в течение 0,5 ч при 20°C. ТСХ показала, что реакция завершилась. Смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением этил-2-хлор-5-метилпиримидин-4-карбоксилата (1,70 г, выход: 56,1%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ 8,62 (с, 1H), 4,48 (к, J=7,2 Гц, 2H), 2,50 (с, 3H), 1,44 (т, J=7,2 Гц, 3H).
[1092] Этил-2-(N-(2,4-диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-карбоксилат (4): К смеси этил-2-хлор-5-метилпиримидин-4-карбоксилата (3) (0,20 г, 0,997 ммоль) и N-[(2,4-диметоксифенил)метил]метансульфонамида (0,49 г, 1,99 ммоль) в ДМФА (5,0 мл) прибавляли NaH (60,0%, 0,076 г, 1,99 ммоль) при 0°C. Смесь перемешивали при 60°C в течение 6 ч. ЖХ-МС показала, что реакция завершилась. Смесь гасили насыщенным водным NH4Cl (10 мл) и экстрагировали EtOAc (15 мл x 3). Объединенные органические слои объединяли и промывали солевым раствором (15 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением этил-2-(N-(2,4-диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-карбоксилата (0,180 г, выход: 44,1%) в виде бесцветного масла. 1H ЯМР (400 МГц,CDCl3): δ 8,53 (с, 1H), 7,33-7,29 (м, 1H), 6,42-6,37 (м, 2H), 5,29 (с, 2H), 4,44 (к, J=7,2 Гц, 2H), 3,78 (с, 3H), 3,66 (с, 3H), 3,36 (с, 3H), 2,44 (с, 3H), 1,43 (т, J=7,2 Гц, 3H).
[1093] N-(2,4-Диметоксибензил)-N-(4-(гидроксиметил)-5-метилпиримидин-2-ил)метансульфонамид (5): К раствору этил-2-(N-(2,4-диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-карбоксилата (4) (0,18 г, 0,44 ммоль)) в ТГФ (5 мл) порциями прибавляли LiBH4 (0,038 г, 1,8 ммоль) при 0°C. Смесь перемешивали при 20°C в течение 2 ч. ТСХ показала, что реакция завершилась. Смесь гасили насыщенным водным NH4Cl (20 мл), экстрагировали EtOAc (10 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле с получением N-(2,4-диметоксибензил)-N-(4-(гидроксиметил)-5-метилпиримидин-2-ил)метансульфонамида (0,080 г, выход: 50%) в виде бесцветного масла. 1H ЯМР (400 МГц,CDCl3): δ 8,29 (с, 1H), 7,25 (шир. с, 1H), 6,45-6,41 (м, 2H), 5,31 (с, 2H), 4,63 (д, J=4,8 Гц, 2H), 4,03 (т, J=4,8 Гц, 1H), 3,78 (с, 3H), 3,74 (с, 3H), 3,41 (с, 3H), 2,12 (с, 3H).
[1094] (2-(N-(2,4-Диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-ил)метил метансульфонат (6): К раствору N-(2,4-диметоксибензил)-N-(4-(гидроксиметил)-5-метилпиримидин-2-ил)метансульфонамида (5) (0,10 г, 0,272 ммоль) в ДХМ (2 мл) прибавляли TEA (0,0759 мл, 0,544 ммоль) и MsCl (0,047 г, 0,41 ммоль) при 0°C. Смесь перемешивали при 20°C в течение 0,5 ч в атмосфере N2. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили насыщенным водным раствором NH4Cl (2 мл), экстрагировали ДХМ (3 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (2-(N-(2,4-диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-ил)метилметансульфоната (0,15 г, неочищенный). 1H ЯМР (400 МГц, CDCl3): δ 8,39 (с, 1H), 7,24 (с, 1H), 6,39 (с, 2H), 5,29-5,28 (м, 2H), 4,54 (с, 2H), 3,78 (с, 6H), 3,62 (с, 3H), 3,28 (с, 3H), 2,80 (с, 3H).
[1095] N-(4-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-5-метилпиримидин-2-ил)-N-(2,4-диметоксибензил)метансульфонамид (7): К раствору (2-(N-(2,4-диметоксибензил)метилсульфонамидо)-5-метилпиримидин-4-ил)метилметансульфоната (6) (0,10 г, 0,22 ммоль) в ДМФА (2,0 мл) прибавляли Cs2CO3 (0,15 г, 0,45 ммоль) и 3-хлор-2-(2-хлорэтокси)-5-[1-(4-гидроксифенил)-1-метил-этил]бензонитрил (Int H) (0,079 г, 0,22 ммоль) при 20°C. Смесь перемешивали при 20°C в течение 10 ч. ТСХ показала, что реакция завершилась. Смесь гасили H2O (3 мл), экстрагировали EtOAc (3 мл x 3). Объединенные органические слои промывали солевым раствором (4 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-5-метилпиримидин-2-ил)-N-(2,4-диметоксибензил)метансульфонамида (0,10 г, неочищенный) в виде желтого масла, который непосредственно использовали без дополнительной очистки.
[1096] N-(4-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-5-метилпиримидин-2-ил)метансульфонамид (A122): К раствору N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-5-метилпиримидин-2-ил)-N-(2,4-диметоксибензил)метансульфонамида (7) (0,05 г, неочищенный) в ДХМ (1 мл) прибавляли ТФУ (0,0159 мл, 0,214 ммоль), и смесь перемешивали при 20°C в течение 15 мин. ЖХ-МС показала, что реакция завершилась. Смесь гасили H2O (2 мл), экстрагировали ДХМ (3 мл x 3). Объединенные органические слои промывали солевым раствором (2 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-5-метилпиримидин-2-ил)метансульфонамида (чистота: 100%, 7 мг, выход: 17,8%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3): δ 8,41 (с, 2H), 8,25-8,30 (шир., 1H), 7,44 (д, J=2,4 Гц, 1H), 7,31 (д, J=2,4 Гц, 1H), 7,11 (д, J=6,8 Гц, 2H), 6,92 (д, J=6,8 Гц, 2H), 5,12 (с, 2H), 4,42 (т, J=6,1 Гц, 2H), 3,88 (т, J=6,4 Гц, 2H), 3,41 (с, 3H), 2,35 (с, 3H), 1,64 (с, 6H). ЖХ-МС: (220 нм): 100%. Точная масса: 548,1; найдено 549,2, 551,1.
[1097] Пример 24: Синтез N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-2-ил)метансульфонамида (A134)
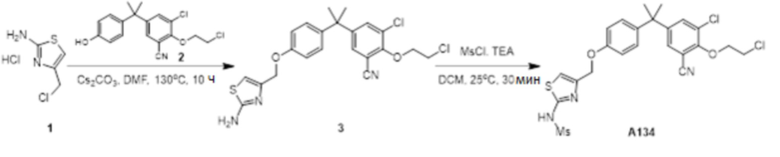
[1098] 5-(2-(4-((2-Аминотиазол-4-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-(2-хлорэтокси)бензонитрил (3): К смеси 4-(хлорметил)тиазол-2-амина гидрохлорида (1) (200 мг, 1,08 ммоль) и 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (2) (378 мг, 1,08 ммоль) в ДМФА (5 мл) прибавляли Cs2CO3 (1,4 г, 4,32 моль) при 20°C , и смесь перемешивали при 130°C в течение 10 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь охлаждали, погасили водой (10 мл). Смесь экстрагировали ДХМ (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ВЭЖХ (FA) с получением 5-(2-(4-((2-аминотиазол-4-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-(2-хлорэтокси)бензонитрила (3) (15,0 мг, выход: 3%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=7,44 (с, 1H), 7,32 (с, 1H), 7,11 (шир. д, J=6,6 Гц, 2H), 6,93 (шир. с, 2H), 6,53 (шир. с, 1H), 5,06-4,83 (м, 2H), 4,42 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 1,64 (с, 6H).
[1099] N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-2-ил)метансульфонамид (A134): К смеси 5-(2-(4-((2-аминотиазол-4-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-(2-хлорэтокси)бензонитрила (3) (15,0 мг, 0,03 ммоль) и TEA (0,01 мл, 0,10 ммоль) в ДХМ (1 мл) прибавляли метансульфонилхлорид (4,46 мг, 0,03 ммоль), и смесь перемешивали при 25°C в течение 30 мин (установили две группы Ms согласно ЖХ-МС). Затем в реакционную смесь прибавляли Cs2CO3 (21,1 мг, 0,0649 моль) в H2O (0,5 мл). Смесь перемешивали при 50°C в течение 10 мин. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили водой (2 мл) и экстрагировали ДХМ (3 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCOOH) с получением N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-2-ил)метансульфонамида (A134) (1,8 мг, выход: 10,3%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,44 (д, J=2,2 Гц, 1H), 7,32 (д, J=2,2 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 6,90 (д, J=8,8 Гц, 2H), 6,49 (с, 1H), 4,98 (с, 2H), 4,43 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 3,01 (с, 3H), 1,65 (с, 6H). ЖХ-МС: (220 нм): 94,9%. Точная масса: 539,1; найдено 540,0/542,0.
[1100] Пример 25: Синтез 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((4-(метилсульфонил)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (A136)
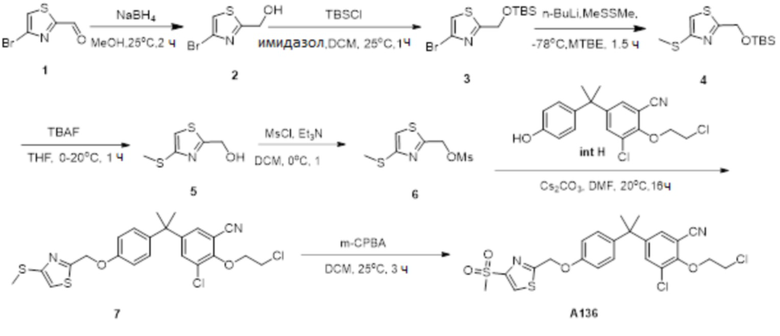
[1101] (4-Бромтиазол-2-ил)метанол (2): К раствору 4-бромтиазол-2-карбальдегида (10,4 г, 0,0542 моль) в MeOH (150 мл) прибавляли NaBH4 (4,10 г, 0,108 моль) при 0°C. Смесь перемешивали при 25°C в течение 2 ч. ТСХ показала, что реакция завершилась и наблюдали одно новое пятно. Смесь гасили водой (70 мл), перемешивали в течение 0,5 ч и концентрировали для удаления большей части MeOH. Водный слой экстрагировали EtOAc (30 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (SiO2, Петролейный эфир/Этилацетат=от 10:1 до 3:1) с получением (4-бромтиазол-2-ил)метанола (10,0 г, 0,0515 моль, выход: 95,2%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ 7,23 (с, 1H), 4,96 (д, J=6,0 Гц, 2H), 2,79 (т, J=6,0 Гц, 1H).
[1102] 4-Бром-2-(((трет-бутилдиметилсилил)окси)метил)тиазол (3): К раствору (4-бромтиазол-2-ил)метанола (11,7 г, 0,0603 моль) в ДХМ (120 мл) прибавляли имидазол (8,21 г, 0,121 моль) и трет-бутил-хлор-диметилсилан (10,0 г, 0,0663 моль). Смесь перемешивали при 25°C в течение 1 ч. ТСХ показал, что исходный материал был поглощен, и наблюдали одно новое пятно. Реакционную смесь выливали в воду (100 мл), экстрагировали ДХМ (70 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (70 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением (4-бромтиазол-2-ил)метокси-трет-бутил-диметилсилана (17,0 г, 0,0551 моль, выход: 91,5%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ 7,18 (с, 1H), 4,95 (с, 2H), 0,96 (с, 9H), 0,14 (с, 6H).
[1103] 2-(((трет-Бутилдиметилсилил)окси)метил)-4-(метилтио)тиазол (4): К раствору (4-бромтиазол-2-ил)метокси-трет-бутил-диметилсилана (11,5 г, 0,0373 моль) в MTBE (300 мл) прибавляли n-BuLi (2,50 M, 17,9 мл, 0,0448 моль) по каплям при -78°C в атмосфере N2. Смесь перемешивали при -78°C в течение 30 мин. Затем прибавляли MeSSMe (14,3 г, 0,152 моль) при -78°C и перемешивали при одной и той же температуре в течение 1 ч. ЖХ-МС показала, что было обнаружено 70% желаемого МС. Смесь погасили насыщ. раствором Раствор NH4Cl (100 мл), экстрагировали EtOAc (30 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением неочищенного трет-бутил-диметил-[(4-метилсульфанилтиазол-2-ил)метокси]силана (90,0%, 10,0 г, 0,0327 моль, выход: 87,6%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ 6,87 (с, 1H), 4,95 (с, 2H), 2,53 (с, 3H), 0,96 (с, 9H), 0,14 (с, 6H).
[1104] (4-(Метилтио)тиазол-2-ил)метанол (5): К раствору (4-бромтиазол-2-ил)метокси-трет-бутил-диметилсилана (12,0 г, 0,0389 моль) в ТГФ (150 мл) прибавляли TBAF (1,00 M, 46,7 мл, 0,0467 моль) при 0°C. Смесь перемешивали при 20°C в течение 1 ч. ТСХ показала, что реакция завершилась. Реакционную смесь выливали в воду (50 мл), экстрагировали EtOAc (30 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением (4-метилсульфанилтиазол-2-ил)метанола (3,60 г, 0,0223 моль, выход: 57,4%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ 6,89 (с, 1H), 4,94 (шир. д, J=2,0 Гц, 2H), 2,95 (шир. с, 1H), 2,54 (с, 3H).
[1105] (4-(Метилтио)тиазол-2-ил)метилметансульфонат (6): К смеси (4-метилсульфанилтиазол-2-ил)метанола (3,40 г, 0,0211 моль) и TEA (0,432 мл, 0,00310 моль) в ДХМ (50 мл) прибавляли MsCl (1,96 мл, 0,0253 моль) при 0°C. Смесь перемешивали при 0°C в течение 1 ч. ТСХ показал, что исходный материал был поглощен, и наблюдали одно новое пятно. Реакционную смесь выливали в воду (30 мл), экстрагировали ДХМ (15 мл x 3). Объединенные органические слои промывали солевым раствором (40 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (4-метилсульфанилтиазол-2-ил)метилметансульфоната (5,40 г, 0,0226 моль, неочищенный) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ 6,99 (с, 1H), 5,45 (с, 2H), 3,10 (с, 3H), 2,55 (с, 3H).
[1106] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((4-(метилтио)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (7): К суспензии (4-метилсульфанилтиазол-2-ил)метилметансульфоната (80,0%, 3,08 г, 0,0103 моль) и Cs2CO3 (5,58 г, 0,0171 моль) в ДМФА (20 мл) прибавляли 3-хлор-2-(2-хлорэтокси)-5-[1-(4-гидроксифенил)-1-метил-этил]бензонитрил (3,00 г, 0,00857 моль) при 20°C. Смесь перемешивали при 20°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (50 мл), экстрагировали EtOAc (30 мл x 3). Объединенные органические слои промывали солевым раствором (30 мл x 3), фильтровали и концентрировали при пониженном давлении с получением 3-хлор-2-(2-хлорэтокси)-5-[1-метил-1-[4-[(4-метилсульфанилтиазол-2-ил)метокси]фенил]этил]бензонитрил (3,20 г, 0,00648 моль, выход: 75,7%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ 7,44 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,12 (д, J=8,4 Гц, 2H), 6,99-6,91 (м, 3H), 5,34 (с, 2H), 4,42 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,4 Гц, 2H), 2,56 (с, 3H), 1,64 (с, 6H).
[1107] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((4-(метилсульфонил)тиазол-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (A136): К раствору 3-хлор-2-(2-хлорэтокси)-5-[1-метил-1-[4-[(4-метилсульфанилтиазол-2-ил)метокси]фенил]этил]бензонитрила (3,00 г, 0,00608 моль) в ДХМ (50 мл) прибавляли м-ХПБК (80,0%, 5,25 г, 0,0243 моль) при 0°C. Смесь перемешивали при 25°C в течение 3 ч. ЖХ-МС показала, что реакция завершилась и обнаружили 60% желаемого продукта. Смесь гасили водой (30 мл). Смесь экстрагировали ДХМ (20 мл x 3). Объединенные органические слои промывали солевым раствором (50 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением 3-хлор-2-(2-хлорэтокси)-5-[1-метил-1-[4-[(4-метилсульфонилтиазол-2-ил)метокси]фенил]этил]бензонитрила (A136) (1,71 г, 0,00325 моль, выход: 53,5%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ 8,22 (с, 1H), 7,45 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,0 Гц, 1H), 7,15 (д, J=6,8 Гц, 2H), 6,95 (д, J=6,8 Гц, 2H), 5,39 (с, 2H), 4,43 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,23 (с, 3H), 1,66 (с, 6H).
[1108] Пример 26: Синтез N-(2-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)метансульфонамида (A137)
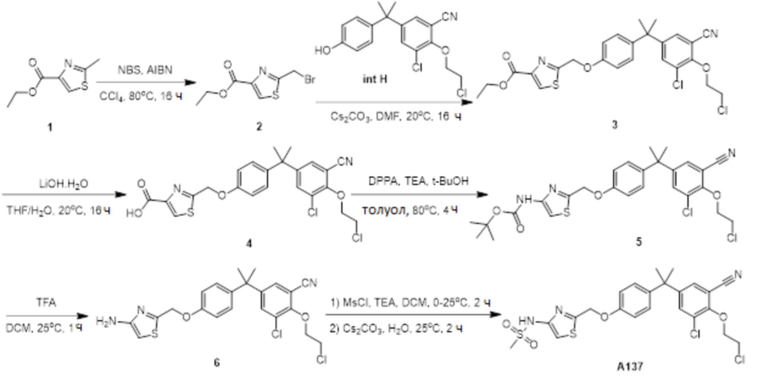
[1109] Этил-2-метилтиазол-4-карбоксилат (2): К смеси этил-2-метилоксазол-4-карбоксилата (1) (10,0 г, 58,4 ммоль) и AIBN (0,959 г, 5,84 ммоль) в CCl4 (80 мл) прибавляли NBS (12,5 г, 70,1 ммоль) при 20°C, и смесь перемешивали при 80°C в течение 16 ч. ТСХ показал, что образовалось новое пятно и остался след от исходного материала. Реакционную смесь выливали в H2O (150 мл) и экстрагировали ДХМ (80 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (80 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали силикагелем с получением этил-2-метилоксазол-4-карбоксилата (2) (4,6 г, выход: 31,5%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,23 (с, 1H), 4,77 (с, 2H), 4,41 (к, J=6,8 Гц, 2H), 1,42 (т, J=7,2 Гц, 3H).
[1110] Этил-2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоксилат (3): Раствор 3-хлор-2-(2-хлорэтокси)-5-(1-(4-гидроксифенил)-1-метил-этил)бензонитрила (int H) (0,5 г, 1,43 ммоль), этил-2-(бромметил)тиазол-4-карбоксилата (2) (0,428 г, 1,71 ммоль) и Cs2CO3 (0,93, 2,86 ммоль) в ДМФА (10 мл) перемешивали при 20°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (15 мл) и экстрагировали EtOAc (15 мл x 3). Объединенные органические слои промывали солевым раствором (10 мл x 3), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали силикагелем с получением этил-2-((4-(1-(3-хлор-4-(2-хлорэтокси)-5-циано-фенил)-1-метил-этил)фенокси)метил)тиазол-4-карбоксилата (3) (0,6 г, выход: 80,9%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,27 (с, 1H), 7,44 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,12 (д, J=8,8 Гц, 2H), 5,41 (с, 2H), 4,44-4,09 (м, 4H), 3,88 (т, J=6,4 Гц, 2H), 1,65 (с, 1H), 1,43 (т, J=7,6 Гц, 3H).
[1111] 2-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоновая кислота (4): Раствор этил-2-((4-(1-(3-хлор-4-(2-хлорэтокси)-5-циано-фенил)-1-метил-этил)фенокси)метил)тиазол-4-карбоксилата (3) (0,5 г, 0,963 ммоль) и LiOH.H2O (0,162 г, 3,85 ммоль) в ТГФ (3 мл) и H2O (3 мл) перемешивали при 20°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (8 мл). рH водного слоя доводили до 3~4, добавляя водный раствор HCl (3M). Водный слой отделяли и экстрагировали EtOAc (8 мл x 3). Объединенные органические слои промывали солевым раствором (8 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоновой кислоты (4) (0,4 г, выход: 84,6%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,34 (с, 1H), 7,44 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,14 (д, J=8,8 Гц, 2H), 6,95 (д, J=8,8 Гц, 2H), 5,41 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,4 Гц, 2H), 1,65 (с, 6H).
[1112] трет-Бутил-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)карбамат (5): К раствору 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоновой кислоты (4) (0,1 г, 0,204 ммоль) и TEA (0,0851 мл, 0,000611 моль) в толуоле (1,0 мл) прибавляли t-BuOH (1,0 мл) и DPPA (0,132 мл, 0,611 ммоль) в атмосфере N2 . Смесь перемешивали при 90°C в течение 4 ч. ЖХ-МС показала, что исходное вещество было поглощено. Смесь выливали в H2O (6 мл), экстрагировали ДХМ (3 мл x 2). И объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали силикагелем с получением трет-бутил-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)карбамата (5) (0,11 г, выход: 96,1%) в виде белого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,43 (д, J=2,4 Гц, 1H), 7,33 (д, J=2,4 Гц, 1H), 7,25 (с, 1H), 7,11 (д, J=8,8 Гц, 2H), 6,93 (д, J=8,8 Гц, 2H), 5,25 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 1,65 (с, 6H), 1,53 (с, 9H).
[1113] 5-(2-(4-((4-Аминотиазол-2-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-пропоксибензонитрил (6): К раствору трет-бутил-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)карбамата (5) (0,1 г, 0,0178 ммоль) в ДХМ (1 мл) прибавляли ТФУ (0,1 мл) и перемешивали при 25°C в течение 2 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в насыщенном водном растворе NaHCO3 (4 мл) и экстрагировали ДХМ (2 мл x 3). Объединенные органические слои промывали солевым раствором (2 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 5-(2-(4-((4-аминотиазол-2-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-пропоксибензонитрила (6) (30 мг, выход: 35,1%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,44 (д, J=2,0 Гц, 1H), 7,33 (д, J=2,4 Гц, 1H), 7,25 (с, 1H), 7,11 (д, J=8,8 Гц, 2H), 6,94 (д, J=8,8 Гц, 2H), 5,24 (с, 2H), 4,42 (т, J=2,4 Гц, 2H), 3,88 (т, J=2,4 Гц, 2H), 1,65 (с, 6H)
[1114] N-(2-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)метансульфонамид (A137): К раствору 5-(2-(4-((4-аминотиазол-2-ил)метокси)фенил)пропан-2-ил)-3-хлор-2-пропоксибензонитрила (6) (50 мг, 0,108 ммоль) и TEA (21,9 мг, 0,216 ммоль) в ДХМ (2 мл) прибавляли метансульфонилхлорид (18,6 мг, 0,0649 ммоль) по каплям при 0°C в атмосфере азота, и смесь перемешивали при 25°C в течение 2 ч. (установили две группы Ms). Затем к смеси прибавляли Cs2CO3 (0,141 г, 0,433 ммоль) и H2O (1 мл) и перемешивали при 25°C в течение 2 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (4 мл). Водный слой экстрагировали EtOAc (4 мл x 3). Объединенные органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении . Остаток очищали препаративной ВЭЖХ (HCOOH) с получением продукта N-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-ил)метансульфонамида (A137) (10 мг, выход: 17,1%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=7,44 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 7,04 (с, 1H), 7,00 (с, 1H), 6,94 (д, J=8,8 Гц, 2H), 5,29 (с, 2H), 4,46 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,12 (с, 3H), 1,65 (с, 6H). ЖХ-МС: (220 нм): 93,78%. Точная масса: 540,5; найдено: 540,1/542,1.
[1115] Пример 27: Синтез 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоксамида (A171)
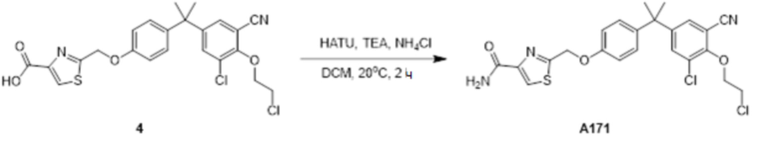
[1116] К раствору 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоновой кислоты (4) (20 мг, 0,0407 ммоль), NH4Cl (5,4 мг, 0,102 ммоль), HATU (0,0186 г, 0,0488 ммоль) в ДХМ (1,00 мл) прибавляли TEA (8,2 мг, 0,0814 ммоль) при 20°C. Смесь перемешивали при одной и той же температуре в течение 2 ч. ЖХ-МС показала, что исходное вещество было поглощено. Смесь выливали в H2O (4 мл) и экстрагировали ДХМ (3 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (4 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCOOH) с получением 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоксамида (A171) (9,2 мг, выход: 46,1%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,19 (с, 1H), 7,44 (д, J=2,2 Гц, 1H), 7,32 (д, J=2,2 Гц, 1H), 7,14 (шир. д, J=8,8 Гц, 2H), 6,95 (д, J=8,8 Гц, 2H), 5,60 (шир. с, 1H), 5,34 (с, 2H), 4,43 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 1,66 (с, 6H). ЖХ-МС (220 нм): 99,5%. Точная масса: 489,0; найдено 490.
[1117] Пример 28: Синтез 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбонитрила (A172)
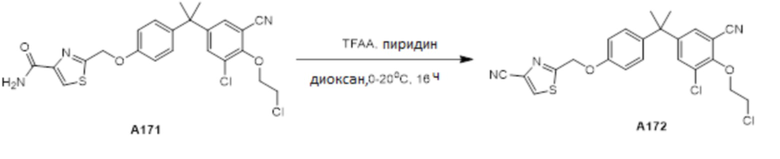
[1118] К раствору 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбоксамида (A171) (20 мг, 0,0408 ммоль) и пиридина (3,27 мг, 0,0413 ммоль) в диоксане (2,0 мл) прибавляли ТФУА (17,4 мг, 0,00827 ммоль) в атмосфере N2 при 0°C. Затем реакционную смесь перемешивали при 20°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (4 мл). Реакционную смесь отделяли и экстрагировали EtOAc (4 мл x 3). Органические слои промывали солевым раствором (4 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (HCOOH) с получением продукта 2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)тиазол-4-карбонитрила (A172) (10 мг, выход: 52,1%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,05 (с, 1H), 7,44 (д, J=2,2 Гц, 1H), 7,31 (д, J=2,2 Гц, 1H), 7,15 (д, J=8,8 Гц, 2H), 6,94 (д, J=8,8 Гц, 2H), 5,37 (с, 2H), 4,43 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 1,65 (с, 6H). ЖХ-МС (220 нм): 100,0%. Точная масса: 471,0; найдено 472,0.
[1119] Пример 29: Синтез N-(4-(аминометил)-6-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамида (A164)
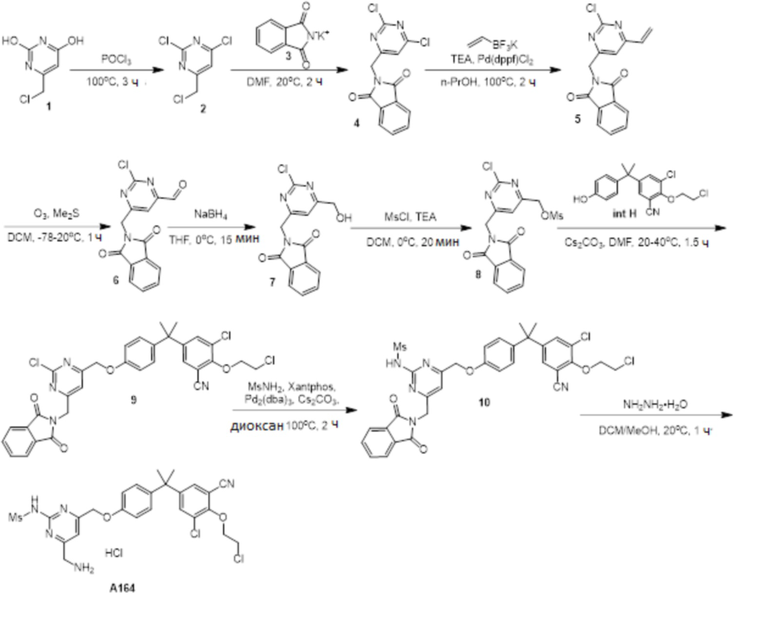
[1120] 2,4-Дихлор-6-(хлорметил)пиримидин (2): Суспензию 6-(хлорметил)пиримидин-2,4-диола (1) (1,50 г, 9,34 ммоль) в POCl3 (10 мл) перемешивали при 100 °C в течение 3 ч. ТСХ показала, что реакция завершилась. Твердое вещество растворяли, и реакционная смесь становилась коричневой. Полученную смесь охлаждали, концентрировали при пониженном давлении. Остаток гасили водой (20 мл) и экстрагировали EtOAc (10 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД (петролейный эфир/EtOAc=10/1) с получением 2,4-дихлор-6-(хлорметил)пиримидина (2) (1,5 г, выход: 81,3%) в виде светло-желтого масла. 1H ЯМР (400 МГц, CDCl3) δ =7,55 (с, 1H), 4,59 (с, 2H).
[1121] 2-((2,6-Дихлорпиримидин-4-ил)метил)изоиндолин-1,3-дион (4): Суспензию 2,4-дихлор-6-(хлорметил)пиримидина (2) (1,5 г, 7,60 ммоль) и 1,3-диоксоизоиндолин-2-ида калия (3) (1,55 г, 8,36 ммоль) в ДМФА (20 мл) перемешивали при 20 °C в течение 2 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь гасили водой (60 мл) и экстрагировали EtOAc (40 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали R-ЖХСД с получением 2-((2,6-дихлорпиримидин-4-ил)метил)изоиндолин-1,3-диона (4) (1,5 г, выход: 64,1%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ =8,00 (с, 1H), 7,96-7,92 (м, 2H), 7,92-7,87 (м, 2H), 4,92 (с, 2H).
[1122] 2-((2-Хлор-6-винилпиримидин-4-ил)метил)изоиндолин-1,3-дион (5): Суспензию 2-((2,6-дихлорпиримидин-4-ил)метил)изоиндолин-1,3-диона (4) (1,5 г, 4,87 ммоль), трифтор(винил)боргидрида калия (0,587 г, 4,38 ммоль), TEA (0,746 мл, 5,36 ммоль) и Pd(dppf)Cl2 (0,249 г, 0,34 ммоль) в n-PrOH (80 мл) перемешивали при 100 °C в течение 2 ч в атмосфере N2. ЖХ-МС показала, что реакция завершилась. Затем полученную смесь гасили насыщенным водным NH4Cl (50 мл) и экстрагировали EtOAc (30 мл x3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (80 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 2-((2-хлор-6-винилпиримидин-4-ил)метил)изоиндолин-1,3-диона (5) (~80,0% по H ЯМР, 0,8 г) в виде желтого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ=7,96-7,93 (м, 2H), 7,92-7,88 (м, 2H), 7,72 (с, 1H), 6,82-6,73 (м, 1H), 6,55 (дд, J=1,0, 17,4 Гц, 1H), 5,83 (дд, J=1,0, 10,7 Гц, 1H), 4,90 (с, 2H).
[1123] 2-Хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-карбальдегид (6): К раствору 2-((2-хлор-6-винилпиримидин-4-ил)метил)изоиндолин-1,3-диона (5) (80,0%, 0,7 г, 1,87 ммоль) в ДХМ (20 мл) барботировали O3 при -78°C в течение 15 мин. Затем в раствор барботировали O2 в течение 10 мин при одной и той же температуре, пока реакционная смесь не станет бесцветной. Me2S (2 мл) прибавляли при -78°C, и смесь перемешивали при 20°C в течение 1 ч. ТСХ показала, что реакция завершилась. Полученную смесь гасили водой (20 мл) и экстрагировали ДХМ (10 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-карбальдегида (6) (470 мг, выход: 83,4%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ=9,96 (с, 1H), 7,95 (дд, J=3,2, 5,4 Гц, 2H), 7,82 (дд, J=2,8, 5,6 Гц, 2H), 7,63 (с, 1H), 5,08 (с, 2H).
[1124] 2-((2-Хлор-6-(гидроксиметил)пиримидин-4-ил)метил)изоиндолин-1,3-дион (7): К раствору 2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-карбальдегида (6) (490 мг, 1,62 ммоль) в ТГФ (10 мл) прибавляли NaBH4 (24,7 мг, 0,65 ммоль) в воду (0,5 мл) по каплям при 0°C. Реакционную смесь перемешивали при одной и той же температуре в течение 15 мин. ЖХ-МС показала, что реакция завершилась. Остаток распределяли между EtOAc (10 мл) и водой (10 мл). Водный слой экстрагировали EtOAc (5 мл x 3). Объединенные органические слои промывали солевым раствором (5 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 2-((2-хлор-6-(гидроксиметил)пиримидин-4-ил)метил)изоиндолин-1,3-диона (7) (430 мг, выход: 78,5%) в виде светло-желтого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ=7,98-7,94 (м, 2H), 7,93-7,89 (м, 2H), 7,61 (с, 1H), 5,76 (т, J=5,9 Гц, 1H), 4,95 (с, 2H), 4,54 (д, J=5,9 Гц, 2H).
[1125] (2-Хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-ил)метилметансульфонат (8): К раствору 2-((2-хлор-6-(гидроксиметил)пиримидин-4-ил)метил)изоиндолин-1,3-диона (7) (410 мг, 1,35 ммоль)) и TEA (0,3 мл, 2,03 ммоль) в ДХМ (10 мл) прибавляли MsCl (170 мг, 1,49 ммоль) при 0°C. Реакционную смесь перемешивали при одной и той же температуре в течение 20 мин. ТСХ показала, что реакция завершилась. Реакционную смесь гасили насыщенным водным NH4Cl (10 мл) и экстрагировали ДХМ (10 мл x 2). Объединенные органические слои промывали солевым раствором (10 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-ил)метилметансульфоната (8) (500 мг, выход: 97,0%) в виде желтого масла, которое непосредственно использовали на следующей стадии. 1H ЯМР (400 МГц, CDCl3) δ=7,94 (дд, J=2,8, 5,4 Гц, 2H), 7,83-7,79 (м, 2H), 7,35 (с, 1H), 5,25 (с, 2H), 5,01 (с, 2H), 3,15 (с, 3H).
[1126] 3-Хлор-5-(2-(4-((2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-ил)метокси)фенил)пропан-2-ил)-2-(2-хлорэтокси)бензонитрил (9): Суспензию (2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-ил)метилметансульфоната (8) (500 мг, 1,31 ммоль), 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (int H) (436 мг, 1,24 ммоль) и Cs2CO3 (853 мг, 2,62 ммоль) в ДМФА (10 мл) перемешивали при 20°C в течение 16 ч. Затем смесь перемешивали при 40°C в течение 0,5 ч. ЖХ-МС показала, что реакция завершилась. Полученную смесь гасили насыщенным водным раствором NH4Cl (10 мл) и водой (10 мл). Водный слой экстрагировали EtOAc (10 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением 3-хлор-5-(2-(4-((2-хлор-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-4-ил)метокси)фенил)пропан-2-ил)-2-(2-хлорэтокси)бензонитрила (9) (300 мг, 36,0%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=7,92 (дд, J=3,0, 5,4 Гц, 2H), 7,80 (дд, J=3,0, 5,4 Гц, 2H), 7,46-7,43 (м, 2H), 7,33 (д, J=2,4 Гц, 1H), 7,11 (д, J=8,8 Гц, 2H), 6,86 (д, J=8,8 Гц, 2H), 5,11 (с, 2H), 4,99 (с, 2H), 4,43 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 1,65 (с, 6H).
[1127] N-(4-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-2-ил)метансульфонамид (10): Суспензию N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-2-ил)метансульфонамида (10) (180 мг, 0,28 ммоль), метансульфонамида (80,8 мг, 0,85 ммоль), Cs2CO3 (184 мг, 0,57 ммоль), Xantphos (32,8 мг, 0,056 ммоль) и Pd2(dba)3 (25,9 мг, 0,028 ммоль) в диоксане (6 мл) перемешивали при 100°C в течение 2 ч. ТСХ показала, что реакция завершилась. Полученную смесь охлаждали, погасили насыщенным водным NH4Cl (5 мл) и водой (5 мл). Водный слой экстрагировали EtOAc (5 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (5 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-2-ил)метансульфонамида (10) (150 мг, выход: 76,3%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,92 (дд, J=3,2, 5,4 Гц, 2H), 7,79 (дд, J=3,2, 5,4 Гц, 2H), 7,45 (д, J=2,2 Гц, 1H), 7,34 (д, J=2,6 Гц, 1H), 7,25 (с, 1H), 7,12 (д, J=8,8 Гц, 2H), 6,89 (д, J=8,8 Гц, 2H), 5,05 (с, 2H), 4,96 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,25 (с, 3H), 1,66 (с, 6H).
[1128] N-(4-(Аминометил)-6-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамид (A164): Раствор N-(4-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)-6-((1,3-диоксоизоиндолин-2-ил)метил)пиримидин-2-ил)метансульфонамида (10) (50 мг, 0,072 ммоль) и NH2NH2·H2O (80,0%, 0,0218 мл, 0,36 ммоль) в MeOH (1 мл) и ДХМ (0,5 мл) перемешивали при 20°C в течение 1 ч. ЖХ-МС показала, что реакция завершилась. Полученную смесь доводили pH до 4~5, прибавляя водную HCl (1 N), и остаток очищали с помощью препаративной ВЭЖХ (HCl) с получением N-(4-(аминометил)-6-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-2-ил)метансульфонамида (A164) (5,54 мг, выход: 13,6%) в виде белого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ =11,52 (с, 1H), 8,45 (с, 3H), 7,63 (с, 1H), 7,58 (с, 1H), 7,39 (с, 1H), 7,20 (д, J=8,4 Гц, 2H), 6,98 (д, J=8,8 Гц, 2H), 5,14 (с, 2H), 4,41 (т, J=4,8 Гц, 2H), 4,22 (с, 2H), 3,95 (т, J=4,8 Гц, 2H), 3,42 (с, 3H), 1,63 (с, 6H). ЖХ-МС (220 нм): 99,7%. Точная масса: 563,12; найдено 564,1.
[1129] Пример 30: Синтез 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилсульфонил)фуран-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (A168)
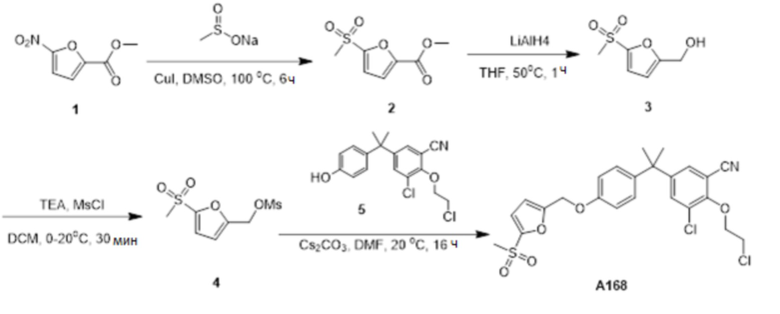
[1130] Метил-5-(метилсульфонил)фуран-2-карбоксилат (2): Суспензию метил-5-нитрофуран-2-карбоксилата (1,0 г, 4,9 ммоль), метансульфоната натрия (115 мг, 9,8 ммоль) и CuI (139 мг, 7,3 ммоль) в ДМСО (30 мл) перемешивали при 100°C в течение 6 ч в атмосфере N2. ТСХ показала, что реакция завершилась. Смесь охлаждали. Реакционную смесь разбавляли EtOAc (30 мл) и погасили водой (70 мл). Смесь фильтровали, и фильтрат экстрагировали EtOAc (10 мл). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением метил-5-(метилсульфонил)фуран-2-карбоксилата (0,3 г, выход: 30,1%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,25 (д, J=3,4 Гц, 1H), 7,22 (д, J=3,4 Гц, 1H), 3,96 (с, 3H), 3,23 (с, 3H).
[1131] (5-(Метилсульфонил)фуран-2-ил)метанол (3): К раствору метил-5-(метилсульфонил)фуран-2-карбоксилата (0,3 г, 1,5 ммоль) в ТГФ (3 мл) прибавляли LiBH4 (128 мг, 5,9 ммоль) в атмосфере N2 при 20°C. Смесь перемешивали при 50 °C в течение 1 ч. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенном водном NH4Cl (5 мл) и экстрагировали EtOAc (3 мл x 3). Объединенные органические слои промывали солевым раствором (3 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (5-(метилсульфонил)фуран-2-ил)метанола (220 мг, выход: 85,0%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,14 (д, J=3,4 Гц, 1H), 6,48 (д, J=3,4 Гц, 1H), 4,72 (д, J=6,0 Гц, 2H), 3,17 (с, 3H), 1,97 (т, J=6,4 Гц, 1H).
[1132] (5-(Метилсульфонил)фуран-2-ил)метилметансульфонат (4): К раствору (5-(метилсульфонил)фуран-2-ил)метанола (110 мг, 0,6 ммоль) в ДХМ (2 мл) прибавляли TEA (0,18 г, 1,87 ммоль) и MsCl (107 мг, 0,936 моль) при 0 °C в атмосфере N2. Смесь перемешивали при 20 °C в течение 30 мин. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенном водном растворе NH4Cl (2 мл). Смесь экстрагировали ДХМ (2 мл x 3). Объединенные органические слои промывали солевым раствором (1 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением (5-(метилсульфонил)фуран-2-ил)метилметансульфоната (80,0%, 150 мг, выход: 75,6%) в виде светло-желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=7,17 (д, J=3,4 Гц, 1H), 6,70 (д, J=3,4 Гц, 1H), 5,25 (с, 2H), 3,19 (с, 3H), 3,07 (с, 3H)
[1133] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилсульфонил)фуран-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (A168): К раствору (5-(метилсульфонил)фуран-2-ил)метилметансульфоната (150 мг, 0,6 ммоль) в ДМФА (2,00 мл) прибавляли 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрил (207 мг, 0,6 ммоль) и Cs2CO3 (384 мг, 1,2 ммоль) в атмосфере N2 при 20°C. Смесь перемешивали при 20°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Смесь выливали в H2O (5 мл). Смесь экстрагировали EtOAc (3 мл x 2). Объединенные органические слои промывали солевым раствором (2 мл x 4), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((5-(метилсульфонил)фуран-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (A168) (62 мг, выход: 20,7%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=7,44 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,17 (д, J=3,2 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 6,90 (д, J=8,8 Гц, 2H), 6,59 (д, J=3,2 Гц, 1H), 5,07 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,18 (с, 3H), 1,65 (с, 6H). ЖХ-МС: (220 нм): 32,43%. Точная масса: 507,1; найдено 508,1.
[1134] Пример 31: Синтез (R)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамида (A169) и (S)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамида (A170)
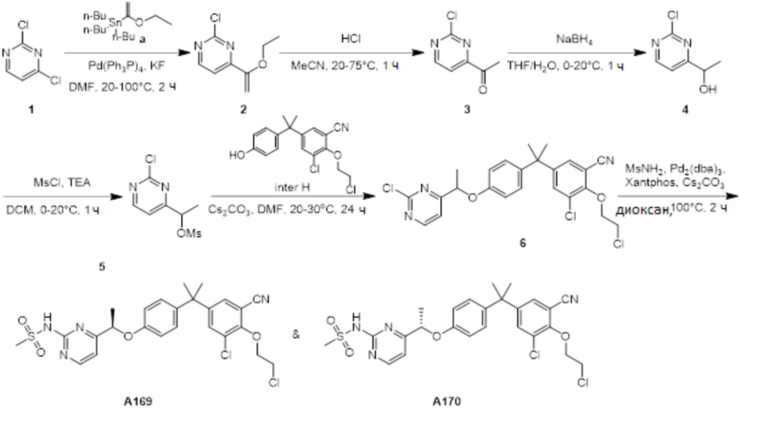
[1135] 2-Хлор-4-(1-этоксивинил)пиримидин (2): К раствору 2,4-дихлорпиримидина (1) (20,0 г, 0,134 моль) в ДМФА (250 мл) прибавляли трибутил(1-этоксивинил)станнан (53,3 г, 0,148 моль), Pd(PPh3)4 (7,7 г, 0,0067 моль) и KF (23,4 г, 0,403 моль) при 20 °C в атмосфере N2. Смесь перемешивали при 100°C в течение 2 ч в атмосфере N2. ТСХ показала, что реакция завершилась. Смесь выливали в воду (500 мл). Реакционную смесь фильтровали, и фильтр-прессную лепешку промывали 200 мл воды, сушили в вакууме с получением 2-хлор-4-(1-этоксивинил)пиримидина (2) (25,0 г, неочищенный) в виде желтого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 8,79 (д, J=5,0 Гц, 1 H), 7,64 (д, J=5,0 Гц, 1 H), 5,54 (д, J=2,2 Гц, 1 H), 4,72 (д, J=2,2 Гц, 1 H), 3,95 (к, J=6,8 Гц, 2 H), 1,34 (т, J=7,0 Гц, 3 H).
[1136] 1-(2-Хлорпиримидин-4-ил)этанон (3): К раствору 2-хлор-4-(1-этоксивинил)пиримидина (2) (25 г, неочищенный) в MeCN (100 мл) прибавляли HCl (10,0%, 100 мл) при 20°C. Смесь перемешивали при 75°C в течение 1 часа. ТСХ показала, что реакция завершилась. Смесь концентрировали для удаления MeCN. Смесь экстрагировали EtOAc (50 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД (петролейный эфир:EtOAc= от 10:1 до 5:1) с получением 1-(2-хлорпиримидин-4-ил)этанона (3) (11,0 г, выход за две стадии: 52,3%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ м.д. 8,79 (д, J=4,89 Гц, 1 H), 7,77 (д, J=4,89 Гц, 1 H), 2,61-2,68 (м, 3 H).
[1137] 1-(2-Хлорпиримидин-4-ил)этанол (4): К раствору 1-(2-хлорпиримидин-4-ил)этанона (3) (11,0 г, 0,0703 моль) в ТГФ (50,0 мл) и H2O (50,0 мл) прибавляли NaBH4 (2,92 г, 0,0773 моль) при 0°C. Смесь перемешивали в течение 1 часа при 20°C. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенном водном NH4Cl (100 мл) и экстрагировали EtOAc (30 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (50 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали на колонке (петролейный эфир:EtOAc=от 10:1 до 5:1) с получением 1-(2-хлорпиримидин-4-ил)этанола (4) (5,50 г, выход: 49,4%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ м.д. 8,62 (д, J=5,0 Гц, 1 H), 7,38 (д, J=5,0 Гц, 1 H), 4,84-4,94 (м, 1 H), 2,98 (д, J=5,0 Гц, 1 H), 1,55 (д, J=6,8 Гц, 2 H), 1,52-1,53 (м, 1 H).
[1138] 1-(2-Хлорпиримидин-4-ил)этилметансульфонат (5): К раствору 1-(2-хлорпиримидин-4-ил)этанола (4) (14,0 г, 0,0883 моль) и TEA (24,6 мл, 0,177 моль) в ДХМ (200 мл) прибавляли метансульфонилхлорид (15,2 г, 0,132 моль) при 0°C. Смесь перемешивали при 20°C в течение 1 ч. ЖХ-МС показала, что реакция завершилась. Смесь выливали в воду (400 мл) и экстрагировали ДХМ (100 мл x 3). Объединенные органические слои промывали солевым раствором (200 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении с получением 1-(2-хлорпиримидин-4-ил)этилметансульфоната (5) (19,0 г, 0,0803 моль, выход: 90,9%) в виде желтого масла.
[1139] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-(1-(2-хлорпиримидин-4-ил)этокси)фенил)пропан-2-ил)бензонитрил (6): К раствору 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (int H) (20,0 г, 0,0571 моль) в ДМФА (250 мл) прибавляли 1-(2-хлорпиримидин-4-ил)этилметансульфонат (5) (18,9 г, 0,0799 моль) и Cs2CO3 (37,2 г, 0,114 моль) при 20°C. Смесь перемешивали при 20°C в течение 20 ч и 30 °C в течение 4 ч. ТСХ показала, что реакция завершилась. Смесь выливали в насыщенный водный раствор NH4Cl (200 мл) и воду (200 мл). Водный слой экстрагировали EtOAc (300 мл X 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (300 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД (петролейный эфир:EtOAc=от 10:1 до 5:1) с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-(1-(2-хлорпиримидин-4-ил)этокси)фенил)пропан-2-ил)бензонитрила (6) (14,8 г, 0,0302 моль, выход: 52,8%) в виде желтого масла.
1H ЯМР (400 МГц, CDCl3) δ=8,60 (д, J=5,2 Гц, 1H), 7,45-7,41 (м, 2H), 7,29 (д, J=2,4 Гц, 1H), 7,06 (д, J=8,8 Гц, 2H), 6,78 (д, J=8,8 Гц, 2H), 5,33-5,28 (м, 1H), 4,42 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 1,69 (д, J=6,6 Гц, 3H), 1,62 (с, 6H).
[1140] (R)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамид (A169) и (S)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамид (A170): Суспензию 3-хлор-2-(2-хлорэтокси)-5-(2-(4-(1-(2-хлорпиримидин-4-ил)этокси)фенил)пропан-2-ил)бензонитрила (6) (8,00 г, 0,0163 моль), метансульфонамида (4,65 г, 0,0489 моль), Cs2CO3 (10,6 г, 0,0326 моль), Xantphos (1,89 г, 0,00326 моль) и Pd2(dba)3 (1,49 г, 0,00163 моль) в диоксане (250 мл) перемешивали при 100°C в течение 2 ч в атмосфере N2. ТСХ показала, что реакция завершилась. Полученную смесь гасили насыщенным водным NH4Cl (100 мл) и водой (100 мл). Водный слой экстрагировали EtOAc (100 мл x 3). Объединенные органические слои промывали солевым раствором (100 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали ЖХСД с получением неочищенного продукта. Смесь очищали препаративной ВЭЖХ (FA) и СФХ с получением (R)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамида (1,77 г, выход: 19,8%, пик 1 в СФХ называли как A169) 1H ЯМР (400 МГц, CDCl3) δ=8,56 (д, J=5,1 Гц, 1H), 8,35 (шир. с, 1H), 7,43 (д, J=2,2 Гц, 1H), 7,29 (д, J=2,1 Гц, 1H), 7,17 (д, J=5,1 Гц, 1H), 7,05 (д, J=8,7 Гц, 2H), 6,79 (д, J=8,8 Гц, 2H), 5,23 (к, J=6,7 Гц, 1H), 4,42 (т, J=6,2 Гц, 2H), 3,88 (т, J=6,2 Гц, 2H), 3,49 (с, 3H), 1,67 (д, J=6,6 Гц, 3H), 1,62 (с, 6H). ЖХ-МС (220 нм): 98,4%. Точная масса: 548,1; найдено 549,1. (S)-N-(4-(1-(4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)этил)пиримидин-2-ил)метансульфонамид (1,23 г, выход: 13,7%, пик 2 в СФХ называли как A170) в виде светло-желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,69 (шир. с, 1H), 8,58 (д, J=5,3 Гц, 1H), 7,43 (д, J=1,6 Гц, 1H), 7,29 (д, J=1,6 Гц, 1H), 7,17 (д, J=5,1 Гц, 1H), 7,05 (шир. д, J=8,6 Гц, 2H), 6,79 (д, J=8,7 Гц, 2H), 5,23 (к, J=6,3 Гц, 1H), 4,42 (т, J=6,1 Гц, 2H), 3,88 (т, J=6,1 Гц, 2H), 3,49 (с, 3H), 1,67 (д, J=6,6 Гц, 3H), 1,62 (с, 6H). ЖХ-МС (220 нм): 98,6%. Точная масса: 548,1; найдено 549,1.
[1141] Пример 32: Синтез N-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-4-ил)метансульфонамида (A184)

[1142] 2-(Бромметил)-4-хлорпиримидин (2): К смеси 4-хлор-2-метил-пиримидина (10,0 г, 7,8 ммоль) и AIBN (5,1 г, 31,1 ммоль) в CCl4 (100 мл) прибавляли NBS (16,6 г, 93,3 ммоль) при 25°C , и смесь перемешивали при 80°C в течение 16 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь охлаждали до комнатной температуры, выливали в H2O (150 мл) и экстрагировали ДХМ (80 мл x 2). Органические слои объединяли и промывали солевым раствором (80 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 2-(бромметил)-4-хлорпиримидина (1,7 г, выход 10,5%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,64 (д, J=5,6 Гц, 1H), 7,29 (д, J=5,2 Гц, 1H), 4,56 (с, 2H).
[1143] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((4-хлорпиримидин-2-ил)метокси)фенил)пропан-2-ил) бензонитрил (4): К смеси 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (300 мг, 0,9 ммоль) и 2-(бромметил)-4-хлорпиримидина (444 мг, 2,1 ммоль) в ДМФА (5 мл) порциями прибавляли NaH (60%, 39 мг, 1,0 ммоль) при 0 °C в атмосфере N2, и смесь перемешивали при 0 °C в течение 4 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в H2O (10 мл), экстрагировали EtOAc (8 мл x 3). Объединенные органические слои промывали солевым раствором (12 мл x 4), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((4-хлорпиримидин-2-ил)метокси)фенил)пропан-2-ил) бензонитрила (300 мг, выход: 73,5%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=8,68 (д, J=5,2 Гц, 1H), 7,43 (д, J=2,4 Гц, 1H), 7,33-7,32 (м, 2H), 7,09 (д, J=8,8 Гц, 2H), 6,94 (д, J=9,2 Гц, 2H), 5,27 (с, 2H), 4,42 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 1,64 (с, 6H).
[1144] N-(2-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-4-ил)метансульфонамид (A184): К раствору 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((4-хлорпиримидин-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (100 мг, 0,2 ммоль) в диоксане (2 мл) прибавляли метансульфонамид (60 мг, 6,3 ммоль), Xantphos (24,3 мг, 0,06 ммоль), Cs2CO3 (137 мг, 0,4 ммоль) и Pd2(dba)3 (19,2 мг, 0,02 ммоль) при 100 °C в атмосфере N2. Смесь перемешивали при 100 °C в течение 5 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь охлаждали до комнатной температуры, погасили водой (4 мл) и экстрагировали ДХМ (3 мл x 3). Объединенные органические слои промывали солевым раствором (6 мл x 2), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали колоночной хроматографией на силикагеле и препаративной ВЭЖХ (FA) с получением N-(2-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиримидин-4-ил) метансульфонамида (A184) (8,4 мг, выход: 7,84%) в виде белого твердого вещества. 1H ЯМР (400 МГц, ДМСО) δ=8,31-8,36 (м, 1H), 7,63 (д, J=2,4 Гц, 1H), 7,55 (д, J=2,4 Гц, 1H), 7,13 (д, J=8,8 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 7,06 (с, 1H), 6,93 (д, J=8,8 Гц, 2H), 5,16 (с, 2H), 4,43 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 3,39 (с, 3H), 1,61 (с, 6H). ЖХ-МС (220 нм): 98,6%. Точная масса: 534,10; найдено 535,1.
[1145] Пример 33: Синтез N-(6-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиразин-2-ил)метансульфонамида (A185)
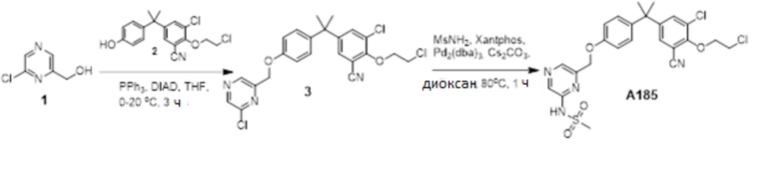
[1146] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((6-хлорпиразин-2-ил)метокси)фенил)пропан-2-ил)бензонитрил (3): К раствору (6-хлорпиразин-2-ил)метанола (1) (0,500 г, 3,46 ммоль), 3-хлор-2-(2-хлорэтокси)-5-(1-(4-гидроксифенил)-1-метил-этил)бензонитрила (2) (0,606 г, 1,73 ммоль) и трифенилфосфана (1,09 г, 4,15 ммоль) в ТГФ (10,0 мл) прибавляли DIAD (0,817 мг, 4,15 ммоль) при 0oC и перемешивали при 25°C в течение 3 ч в атмосфере N2. ТСХ показала, что реакция завершилась. Смесь выливали в воду (20 мл) и экстрагировали EtOAc (15 мл x 3), объединенные органические слои промывали солевым раствором (5 мл x 2), сушили над Na2SO4, фильтровали и концентрировали с получением неочищенного продукта, который очищали колоночной хроматографией на силикагеле с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((6-хлорпиразин-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (3) (чистота: 90,0%, 0,400 г, выход: 21,8%) в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ=8,75 (с, 1H), 8,58 (с, 1H), 7,44 (д, J=2,4 Гц, 1H), 7,33 (д, J=2,0 Гц, 1H), 7,13 (д, J=8,8 Гц, 2H), 6,93 (д, J=8,8 Гц, 2H), 5,22 (с, 2H), 4,43 (т, J=6,4 Гц, 2H), 3,88 (т, J=6,0 Гц, 2H), 1,65 (с, 6H).
[1147] N-(6-((4-(2-(3-Хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиразин-2-ил)метансульфонамид (A185): К раствору 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((6-хлорпиразин-2-ил)метокси)фенил)пропан-2-ил)бензонитрила (3) (120 мг, 0,25 ммоль) в 1,4-диоксане (3,00 мл) прибавляли метансульфонамид (71,8 мг, 0,76 ммоль), трис(дибензилиденацетон)дипалладий(0) (14,5 мг, 0,025 ммоль), Xantphos (14,6 мг, 0,025 ммоль) и Cs2CO3 (0,164 г, 0,50 ммоль) при 20°C в атмосфере N2. Смесь перемешивали при 100°C в течение 3 ч. ЖХ-МС показала, что реакция завершилась. Реакционную смесь выливали в воду (10 мл) и экстрагировали EtOAc (3 мл x 3). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением N-(6-((4-(2-(3-хлор-4-(2-хлорэтокси)-5-цианофенил)пропан-2-ил)фенокси)метил)пиразин-2-ил)метансульфонамида (A185) (38 мг, чистота: 96,0%, выход: 27,1%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ=8,58 (с, 1H), 8,48 (с, 1H), 7,45 (д, J=2,4 Гц, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,14 (д, J=8,8 Гц, 2H), 6,95 (д, J=8,8 Гц, 2H), 5,16 (с, 2H), 4,43 (т, J=6,0 Гц, 2H), 3,88 (т, J=6,4 Гц, 2H), 3,33 (с, 3H), 1,66 (с, 6H). ЖХ-МС (220 нм): 96,8%. Точная масса: 534,09; найдено 535,0.
[1148] Пример 34: Синтез 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((2-метоксиоксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A112)
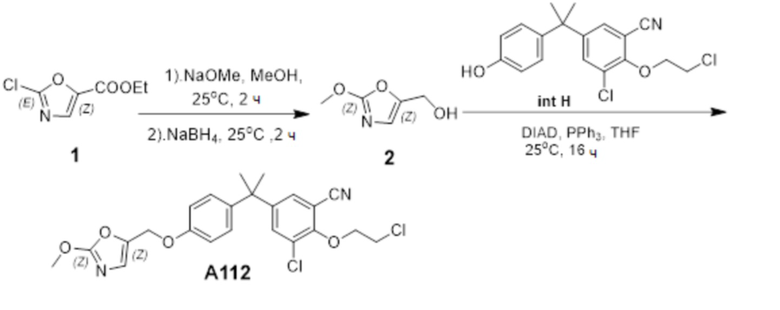
[1149] (2-Метоксиоксазол-5-ил)метанол (2): К смеси этил-2-хлороксазол-5-карбоксилата (300 мг, 1,7 ммоль) в MeOH (5 мл) прибавляли NaOMe (138 мг, 2,6 ммоль) при 25°C, и смесь перемешивали при 25°C в течение 2 ч. Затем NaBH4 (259 мг, 6,8 ммоль) прибавляли к смеси и перемешивали при 25°C в течение дополнительных 2 ч. ТСХ показал, что исходный материал был поглощен, и наблюдали одно новое пятно. Смесь фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением (2-метоксиоксазол-5-ил)метанола (110 мг, выход: 49,9%) в виде желтого масла. 1H ЯМР (400 МГц, CD3OD) δ=6,74 (с, 1H), 4,44 (с, 2H), 4,04 (с, 3H).
[1150] 3-Хлор-2-(2-хлорэтокси)-5-(2-(4-((2-метоксиоксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрил (A112): К смеси (2-метоксиоксазол-5-ил)метанола (35 мг, 0,27 ммоль), 3-хлор-2-(2-хлорэтокси)-5-(2-(4-гидроксифенил)пропан-2-ил)бензонитрила (95 мг, 0,27 ммоль) и (C6H5)3P (142 мг, 0,5 ммоль) в ТГФ (4 мл) прибавляли DIAD (0,1 мл, 0,5 ммоль) при 25°C в атмосфере N2. Смесь перемешивали при 25°C в течение 2 ч. ЖХ-МС показала, что исходный материал был поглощен, и наблюдали один новый пик. Смесь выливали в воду (15 мл), экстрагировали EtOAc (4 мл x 2). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (6 мл), сушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ (FA) с получением 3-хлор-2-(2-хлорэтокси)-5-(2-(4-((2-метоксиоксазол-5-ил)метокси)фенил)пропан-2-ил)бензонитрила (A112) (9,05 мг, выход: 7,6%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3) δ=7,43 (д, J=2,4 Гц, 1H), 7,33 (д, J=2,4 Гц, 1H), 7,11 (д, J=8,8 Гц, 2H), 6,91 (д, J=2,4 Гц, 2H), 6,85 (с, 1H), 4,92 (с, 2H), 4,42 (т, J=6,4 Гц, 2H), 4,08 (с, 3H), 3,88 (т, J=6,0 Гц, 2H), 1,65 (с, 6H). ЖХ-МС (220 нм): 98,1%. Точная масса: 460,1; найдено: 461,2.
[1151] Характеристики синтезированных иллюстративных примеров соединений представлены в Таблице C.
[1152]
[1153] Биологические исследования
[1154] Пример 35: Активность типичных соединений в клеточных анализах
[1155] ПСА (6,1kb)-люциферазный репортер содержит функциональные ARE (элементы отклика андрогена), с которыми AR связывается в ответ на андроген, чтобы индуцировать активность люциферазы. Клетки LNCaP временно трансфицировали ПСА (6,1 kb)-люциферазным репортером в течение 24 часов, а затем предварительно обрабатывали несущей средой (ДМСО) или указанной концентрацией типичных соединений в течение одного часа перед добавлением синтетического андрогена, R1881 (1 нМ ). После 24 ч инкубации с R1881 клетки собирали и определяли относительную активность люциферазы (Фиг. 1). Для определения IC50 обработки были нормализованы до контрольной активности несущей среды, индуцированной R1881 (Таблица 1A).
[1156] Люциферазный анализ: Клетки лизировали с использованием буфера для пассивного лизиса (Promega), а затем собирали в 96-луночные планшеты для культивирования тканей с V-образным дном. Лизаты центрифугировали при 4°C в течение 5 минут при 3000 об./мин. Для измерения люминесценции лизатов клеток LNCaP использовали систему люциферазного анализа Firefly (Promega) в соответствии с протоколом производителя. Относительные единицы люминесценции (RLU) в клеточных лизатах детектировали в течение 10 секунд с использованием люминометра Promega GloMax-Multi Detection (Promega). Значения были нормализованы по содержанию белка. Для расчета значений IC50 использовали программное обеспечение для построения графиков GraphPad Prism.
[1157] Статистический анализ проводили с использованием GraphPad Prism (версия 6.01 для Windows; Ла-Хойя, Калифорния, США). Сравнения между группой лечения и контрольной группами сравнивали с использованием двустороннего дисперсионного анализа с апостериорными тестами Даннета и Таки. Различия считались статистически значимыми при значениях P менее чем 0,05.
[1158] Таблица 1A иллюстрирует диапазоны IC50 соединений из Таблиц A и B из люциферазного анализа. На Фиг. 1 проиллюстрирована дозозависимая кривая для типичных соединений, проиллюстрированных в Таблице 1А. Соединение X и EPI-002 имеют следующие структуры:

[1159] % Ингибирования ПСА-Luc %, значения IC50 типичных соединений проиллюстрированы в Таблице 1В.
[1160] Анализ LBD-экспрессирующего репортера: Чтобы оценить, конкурируют ли типичные соединения (соединения A13, A28, A38, A74, A93 и A109) с лигандом (агонистом) за лиганд-связывающий домен (LBD) рецепторов стероидных гормонов (которые были бы вне мишени), использовался анализ GeneBLAzer (Thermo Fisher). В этом анализе используются клетки, которые стабильно экспрессируют химерный слитый белок, содержащий LBD рецептора стероидного гормона, слитого с ДНК-связывающим доменом (DBD) GAL4 вместе с бета-лактамазным репортером под транскрипционным контролем вышестоящей активаторной последовательности (UAS). Когда агонист связывается с LBD химерного слитого белка GAL4 (DBD)-стероидного гормона (LBD), белок связывается с UAS, что приводит к экспрессии бета-лактамазы. Были протестированы LBD андрогенового рецептора (AR), рецептора прогестерона-бета (PRβ), глюкокортикоидного рецептора (GR), рецептора эстрогена-α (ERα) и рецептора эстрогена-β (ERβ), и рассчитаны IC50 для ингибирования максимальной активности, достигаемой с помощью агониста. См. Таблица 1C.
[1161] Анализ пролиферации клеток : Пролиферацию/жизнеспособность клеток измеряли в клетках LNCaP и PC3 с аламаровым синим, а пролиферацию измеряли в клетках LN-CaP95 с включением BrdU. В клетках LNCaP специфическую пролиферацию AR рассчитывают путем измерения разницы между контрольными клетками, обработанными 0,1 нМ R1881 или без него. См. Таблицу 1D и Фиг. 7.
[1162] Анализ транскрипционной активности AR-V7 : Транскрипционную активность AR-V7 измеряли в клетках LNCaP, временно котрансфицированных вектором экспрессии для AR-V7 и ПСА-люциферазным репортером и инкубированных с типичными соединениями в присутствии или в отсутствие синтетического андрогена, R1881. В качестве контроля клетки LNCaP трансфицировали плазмидой pcDNA (без вставки AR-V7) с R1881 или без нее. См. Фиг. 2A-2B.
[1163] Результаты этого примера подтверждают, что соединения по настоящему раскрытию являются селективными по отношению к AR NTD.
[1164]
Диапазон IC50
Диапазон IC50
[1165]
IC50 (нМ)
[1166]
[1167]
[1168] Пример 36: Анализы стабильности
[1169] Анализ стабильности микросом: Анализ стабильности микросом представляет собой широко используемую модель in vitro для характеристики метаболического превращения ферментами фазы I, такими как ферменты цитохрома P450 (CYP). Поскольку известно, что метаболизм сильно варьирует у разных видов, анализ стабильности микросом обычно проводят у нескольких видов. Стабильность микросом тестируемого соединения может быть оценена с использованием микросом печени или кишечника человека, крысы, мыши или других животных для прогнозирования внутреннего клиренса.
[1170] Анализ проводили в 96-луночных микротитрационных планшетах при 37 °C. Реакционные смеси (25 мкл) содержали конечную концентрацию 1 мкМ тестируемого соединения, 0,5 мг/мл белка микросом печени и 1 мМ НАДФН и/или 1 мМ UDPGA (с аламетицином) в 100 мМ фосфате калия, pH 7,4, буфер с 3 мМ MgCl2. Инкубацию выполняли при N=1, но при необходимости может быть проведена повторная инкубация в каждый момент времени. В каждый момент времени (например, 0, 15, 30 и 60 минут) 150 мкл гасящего раствора (100% ацетонитрила с 0,1% муравьиной кислоты) с внутренним стандартом переносили в каждую лунку. Помимо контролей нулевой минуты, смеси, содержащие те же компоненты, за исключением НАДФН, также могут быть приготовлены в качестве отрицательного контроля. Верапамил был включен в качестве положительного контроля для проверки эффективности анализа. Планшеты герметично закрывали, встряхивали и центрифугировали при 4°C в течение 15 минут при 4000 об./мин. Супернатант переносят на свежие планшеты для анализа ЖХ/МС/МС.
[1171] Обобщенные условия: [Соединение] = 1 мкМ, [LM] = 0,5 мг/мл, [NADPH] = 1 мМ и/или [UDPGA] = 1 мМ, буфер=100 мМ фосфата калия, pH 7,4 с 3 мМ MgCl2, время=0, 15, 30 и 60 мин, и температура=37°C
[1172] Все образцы анализировали методом ЖХ/МС/МС с использованием прибора AB Sciex API 4000, подключенного к насосной системе Shimadzu LC-20AD LC. Аналитические пробы разделяли на колонке с обращенной фазой ВЭЖХ Waters Atlantis T3 dC18 (20 мм x 2,1 мм) при скорости потока 0,5 мл/мин. Подвижная фаза состояла из 0,1% муравьиной кислоты в воде (растворитель A) и 0,1% муравьиной кислоты в 100% ацетонитриле (растворитель B).
[1173] Степень метаболизма рассчитывают как исчезновение тестируемого соединения по сравнению с инкубацией в течение 0 минут. Начальные скорости рассчитывают для концентрации соединения и используют для определения значений периода полураспада (t1/2), а затем и внутреннего клиренса (Clint).
[1174] Clint = (0,693)(1/ t1/2 (мин))(г печени/кг массы тела) (мл инкубации/мг микросомального белка) (45 мг микросомального белка/г массы печени)
[1175] Анализ стабильности гепатоцитов: Прекращение внутреннего клиренса in vitro (Clint) для лекарственных препаратов-кандидатов на ранней стадии открытия является обычной практикой в фармацевтической промышленности. Значения Clint лекарственных препаратов-кандидатов может помочь подтвердить, является ли метаболизм основным путем выведения, при сравнении с общим клиренсом организма in vivo. Гепатоциты входят в число обычно используемых in vitro систем для измерения клиренса. Сообщалось, что гепатоциты сохраняют большую часть метаболической активности фазы I и фазы II, и поэтому это подходящий инструмент для оценки внутреннего клиренса для потенциальных лекарственных препаратов-кандидатов.
[1176] Метаболическую стабильность тестируемого соединения оценивали с использованием гепатоцитов человека и мыши, а также можно использовать гепатоциты крысы, мыши или других животных для прогнозирования внутреннего клиренса. Криоконсервированные гепатоциты удаляли из резервуара с жидким азотом и размораживали на водяной бане при 37 °C. Как только клетки оторвались от стенки пузырька, их декантировали в 48 мл теплой среды HT. Клетки центрифугировали четыре минуты при 420 об./мин (50 g). После удаления супернатанта осадок ресуспендировали в теплой среде DMEM. Плотность клеток подсчитывали с помощью гемацитометра.
[1177] Анализ проводили в 96-луночных микротитрационных планшетах. Соединения инкубировали 0, 60, 120 и 180 минут при 37°C с гепатоцитами. Реакционные смеси (50 мкл) содержали конечную концентрацию 1 мкМ тестируемого соединения, 0,5 миллиона клеток/мл гепатоцитов в среде DMEM. В каждый момент времени (например, 0, 1, 2 и 3 часа) 200 мкл гасящего раствора (100% ацетонитрила с 0,1% муравьиной кислоты) с внутренним стандартом переносили в каждую лунку. Мидазолам был включен в качестве положительного контроля для проверки эффективности анализа. Планшеты герметично закрывали и центрифугировали при 4°C в течение 15 минут при 4000 об./мин. Супернатант переносят на свежие планшеты для анализа ЖХ/МС/МС.
[1178] Обобщенные условия (настраиваемые): [Соединение] = 1 мкМ, Положительный контроль: мидазолам и/или налоксон, [Гепатоциты] = 0,5 миллиона клеток/мл, время=0, 60, 120 и 180 мин, t=37°C.
[1179] Все образцы анализировали методом ЖХ/МС/МС с использованием прибора AB Sciex API 4000, подключенного к насосной системе Shimadzu LC-20AD LC. Аналитические пробы разделяли на колонке с обращенной фазой ВЭЖХ Waters Atlantis T3 dC18 (20 мм x 2,1 мм) при скорости потока 0,5 мл/мин. Подвижная фаза состояла из 0,1% муравьиной кислоты в воде (растворитель A) и 0,1% муравьиной кислоты в 100% ацетонитриле (растворитель B).
[1180] Степень метаболизма рассчитывали как исчезновение тестируемого соединения по сравнению с инкубациями 0-мин контроля реакции. Начальные уровни были рассчитаны для концентрации соединения и использованы для определения значений t1/2, а затем и внутреннего клиренса, Clint.
[1181] Clint = (0,693)(1/ t1/2 (мин))(мл инкубация/миллион клеток)
[1182] Результаты анализа метаболической стабильности типичных соединений из Таблиц A и B перечислены в Таблице 2A ниже. Результаты анализа метаболической стабильности типичных соединений из Таблиц A и B для гепатоцитов человека изображены в Таблице 2B. Период полураспада типичных соединений в микросомах печени и гепатоцитах изображен в Таблицах 2C и 2D.
[1183]
1 Для MLM и HLM: *** представляет Cl < 12 мкл/мин/мг белка, ** представляет Cl в диапазоне 12-48 мкл/мин/мг белка, * представляет Cl в диапазоне ≥ 48 мкл/мин/мг белка.
2 Для MH: *** представляет Cl < 4 мкл/мин/миллион клеток, ** представляет Cl в диапазоне 4-18 мкл/мин/миллион клеток, * представляет Cl в диапазоне ≥ 18 мкл/мин/миллион клеток.
[1184]
[1185]
[1186]
[1187] Пример 37: In Vivo фармакокинетические свойства
[1188] Целью этого исследования является определение фармакокинетики тестируемых соединений в плазме после перорального введения через желудочный зонд (п/о) мышам-самцам CD-1.
[1189] Животноводство: Животные были помещены в группы во время акклиматизации и исследования. Среду в помещении для животных контролировали (целевые условия: температура от 18 до 26 °C, относительная влажность от 30 до 70%, 12 часов искусственного освещения и 12 часов темноты). Температуру и относительную влажность контролировали ежедневно. Животным не давали пищи по меньшей мере за 12 часов до введения. Все животные имели доступ к сертифицированной диете для грызунов ad libitum через 4 часа после введения дозы.
[1190] Состав дозировки: приготовили 85-100 мкл основного раствора типичных соединений данного раскрытия в ДМСО в концентрации 50 мМ; 1,5% об./об. Tween 80 прибавляли и осторожно перемешивали; 95,5% об./об. физиологический раствор мягко прибавляли к органической фазе. Раствор медленно перемешивали обратным пипетированием до получения прозрачного раствора.
[1191] Введение дозы: составы доз вводили через желудочный зонд в соответствии с типовой инструкцией учреждения. Объем дозы определяли по массе тела животных, собранной утром в день введения дозы.
[1192] Сбор образцов: забор крови (около 0,05 мл на момент времени) выполняли из подкожной вены каждого животного в полипропиленовые пробирки в каждый момент времени (0, 0,25, 0,5, 1, 2, 4, 8, 12, и 24 ч). Все образцы крови переносили в предварительно охлажденные пробирки, содержащие 2 мкл K2-EDTA (0,5 М), и помещали на влажный лед до центрифугирования. Каждый собранный образец крови перед центрифугированием помещали во влажный лед. Каждую собранную кровь центрифугировали в течение 15 минут при 4°C и 3000 g для сбора плазмы. Образцы плазмы хранили в полипропиленовых пробирках, быстро замораживали на сухом льду и хранили при -70 ± 10°C до анализа ЖХ/МС/МС.
[1193] Биоаналитический анализ. Метод ЖХ-МС/МС для количественного определения тестируемого соединения в биологической матрице был разработан без соблюдения требований GLP. Для метода, включающего LLOQ, применяли калибровочную кривую с по меньшей мере 7 ненулевыми калибровочными стандартами.
[1194] Данные о зависимости концентрации в плазме от времени анализировали с помощью некомпартментных подходов с использованием программы Phoenix WinNonlin 6.3. Приведены Cl, Vdss, C0, Cmax, Tmax, T½, AUC(0-t), AUC(0-inf), MRT(0-t), MRT(0-inf), %F (пероральная доступность) и графики зависимости концентрации плазмы от времени. На Фиг. 3 проиллюстрирована кривая зависимости концентрации типичных соединений у мышей от времени, измеренной в плазме.
[1195] В Таблицах 3A проиллюстрированы ФК параметры, определенные для разовой дозы типичных соединений п/о мышам (5 мг/кг).
[1196]
[1197] Пример 38: Активность типичных соединений in vivo в модели ксенотрансплантатов LNCaP
[1198] Рост опухоли измеряли у мышей-самцов NCG, несущих опухоли LNCaP. Кастрацию проводили, когда опухоли достигали ~ 100 мм3, и дозирование (60 мг/кг п/о каждый день) начали через 1 неделю после кастрации. См. Фиг. 4. Массу тела мышей измеряли каждые две недели у животных, которые не проявляли токсичности, связанной с лекарственным средством. См. Фиг. 5. Изменение индивидуального объема опухоли по сравнению с исходным уровнем, измеренным в конце эксперимента. См. Фиг. 6. Данные, представленные на Фиг. 4-6, иллюстрируют, что типичные соединения проявляли активность и вызывали частичную регрессию роста опухоли. Cmin при 5 мг/кг п/о и экстраполированная Cmin в эффективности типичных соединений приведены в Таблице 4.
[1199]
[1200] Пронумерованные варианты осуществления изобретения
[1201] В некоторых вариантах осуществления настоящего изобретения настоящее раскрытие относится к следующим вариантам осуществления.
[1202] Вариант осуществления изобретения 1: Соединение, имеющее структурную формулу (I):

[1203] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1204] A и B, каждый независимо, представляют собой арил или гетероарил;
[1205] C представляет собой 3-10-членное кольцо;
[1206] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[1207] Y и Z, каждый независимо, представляют собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-;
[1208] W и V, каждый независимо, представляют собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1209] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1210] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1211] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1212] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1213] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1214] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -OCO(C1-C6 алкил), -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1215] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[1216] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), взятые вместе, образуют необязательно замещенный гетероциклил;
[1217] каждый m независимо равно 0, 1 или 2;
[1218] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[1219] n3 равно 0, 1, 2, 3, 4 или 5; и
[1220] каждое t независимо равно 0, 1 или 2.
[1221] Вариант осуществления изобретения 2: Соединение по варианту осуществления настоящего изобретения 1, где A и B, каждый независимо, представляют собой 5- или 6-членный арил или гетероарил.
[1222] Вариант осуществления изобретения 3: Соединение по варианту осуществления настоящего изобретения 1 или 2, где A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена.
[1223] Вариант осуществления изобретения 4: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-3, где A имеет мета- или пара-связь с X и Y.
[1224] Вариант осуществления изобретения 5: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-4, где B имеет мета- или пара-связь с X и Z.
[1225] Вариант осуществления изобретения 6: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-5, где С представляет собой 5-10-членный гетероарил или арил.
[1226] Вариант осуществления изобретения 7: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-6, где С представляет собой 5-7-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1227] Вариант осуществления изобретения 8: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-7, где С представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил или пиримидил.
[1228] Вариант осуществления изобретения 9: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-7, где C, который необязательно замещен R3, выбран из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[1229] Вариант осуществления изобретения 10: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-6, где С представляет собой фенил или нафтил.
[1230] Вариант осуществления изобретения 11: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-5, где С представляет собой 5-10-членный гетероциклил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1231] Вариант осуществления изобретения 12: Соединение по варианту осуществления настоящего изобретения 11, где
[1232] C представляет собой 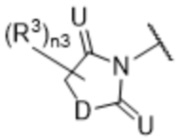 ;
;
[1233] D представляет собой -O-, -NH- или -NR3-; и
[1234] каждый U независимо представляет собой O, S или NR16.
[1235] Вариант осуществления изобретения 13: Соединение по варианту осуществления настоящего изобретения 11, где С представляет собой имидазолидин, имидазолидин-дион или дигидрооксазол.
[1236] Вариант осуществления изобретения 14: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-13, где Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-.
[1237] Вариант осуществления изобретения 15: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-14, где W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-, где R7 представляет собой H или C1-C3 алкил.
[1238] Вариант осуществления изобретения 16: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-15, где:
[1239] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-; и
[1240] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-.
[1241] Вариант осуществления изобретения 17: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-16, где:
[1242] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1243] V представляет собой -CH2-, -CH2CH2-, -CH2CH2CH2-; и
[1244] L представляет собой галоген, -NH2 или -CF3.
[1245] Вариант осуществления изобретения 18: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-17, где X представляет собой связь или -(CR5R6)t-.
[1246] Вариант осуществления изобретения 19: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-18, где X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[1247] Вариант осуществления изобретения 20: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-19, где R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, C1-C3 алкил, C1-C3 алкокси,-(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2R16, -(C1-C3 алкил)-SO2R16, 3-7-членный карбоциклил, 3-7-членный гетероциклил, фенил или 5-6-членный гетероарил.
[1248] Вариант осуществления изобретения 21: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-20, где R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, C1-C3 алкил, C1-C3 алкокси,-(C1-C3 алкил)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2R16 или -(C1-C3 алкил)-SO2R16.
[1249] Вариант осуществления изобретения 22: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-21, где R1 и R2, каждый независимо, представляют собой галоген, -CN, -CF3, -OH, метил, метокси или -CONH2.
[1250] Вариант осуществления изобретения 23: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-22, где R1 и R2, каждый независимо, представляют собой Cl, -CN, -CF3, -OH, метил, метокси или -CONH2.
[1251] Вариант осуществления изобретения 24: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-23, где n1 и n2, каждый независимо, равны 0, 1 или 2.
[1252] Вариант осуществления изобретения 25: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-24, отличающееся тем, что сумма n1 и n2 равно 0, 1, 2, 3 или 4.
[1253] Вариант осуществления изобретения 26: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-25, где R3 выбран из водорода, галогена, оксо, =S или =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -(C1-C3 алкила)-(C1-C3 алкокси), -(C1-C3 алкил)-OH, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO(C1-C3 алкила), -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила).
[1254] Вариант осуществления изобретения 27: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-26, где R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила).
[1255] Вариант осуществления изобретения 28: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-27, где R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, метила, -SCH3, -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
[1256] Вариант осуществления изобретения 29: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-28, где по меньшей мере один из R3 представляет собой -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
[1257] Вариант осуществления изобретения 30: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-29, где по меньшей мере один из R3 представляют собой оксо, =S, =NR16.
[1258] Вариант осуществления изобретения 31: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-30, где R8a и R9a, каждый независимо, представляют собой водород, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил.
[1259] Вариант осуществления изобретения 32: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-30, где R8a и R9a не представляют собой -OH.
[1260] Вариант осуществления изобретения 33: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (II):

[1261] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1262] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1263] C представляет собой 3-10-членное кольцо;
[1264] X представляет собой связь, -(CR5R6)t- или -NR7;
[1265] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1266] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1267] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -NHCO-, -N(C1-C3 алкил)CO- или -CONH- или -CON(C1-C3 алкил)-;
[1268] V представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1269] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1270] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1271] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1272] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1273] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1274] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1275] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1276] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1277] каждый m независимо равно 0, 1 или 2;
[1278] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1279] n3 равно 0, 1, 2, 3, 4 или 5; и
[1280] t равно 0, 1 или 2.
[1281] Вариант осуществления изобретения 34: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (III):

[1282] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1283] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1284] C представляет собой 3-10-членное кольцо;
[1285] X представляет собой связь, -(CR5R6)t- или -NR7;
[1286] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1287] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1288] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1289] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1290] L представляет собой галоген, -NH2 или -CF3;
[1291] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1292] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1293] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1294] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[1295] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1296] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1297] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1298] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1299] каждый m независимо равно 0, 1 или 2;
[1300] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1301] n3 равно 0, 1, 2, 3, 4 или 5; и
[1302] t равно 0, 1 или 2.
[1303] Вариант осуществления изобретения 35: Соединение по варианту осуществления настоящего изобретения 33 или 34, где R8a и R9a, каждый независимо, представляют собой водород, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15.
[1304] Вариант осуществления изобретения 36: Соединение по варианту осуществления настоящего изобретения 33 или 34, где R8a и R9a не представляют собой -OH.
[1305] Вариант осуществления изобретения 37: Соединение по вариантам осуществления изобретения1, отличающееся тем, что соединение имеет структуру формулы (IV):

[1306] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1307] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1308] C представляет собой 3-10-членное кольцо;
[1309] X представляет собой связь, -(CR5R6)t- или -NR7;
[1310] Y и Z, каждый независимо, представляют собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1311] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1312] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1313] L представляет собой галоген, -NH2 или -CF3;
[1314] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1315] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1316] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1317] R7 представляет собой H или C1-C6 алкил;
[1318] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1319] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1320] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1321] n3 равно 0, 1, 2, 3, 4 или 5; и
[1322] t равно 0, 1 или 2.
[1323] Вариант осуществления изобретения 38: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-37, где С представляет собой 5-10-членный гетероарил или арил.
[1324] Вариант осуществления изобретения 39: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-38, где С представляет собой 5-7-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1325] Вариант осуществления изобретения 40: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-39, где С представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил или пиримидил.
[1326] Вариант осуществления изобретения 41: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-39, где C, который необязательно замещен R3, выбран из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[1327] Вариант осуществления изобретения 42: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-38, где С представляет собой фенил или нафтил.
[1328] Вариант осуществления изобретения 43: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-37, где С представляет собой 5-10-членный гетероциклил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1329] Вариант осуществления изобретения 44: Соединение по варианту осуществления настоящего изобретения 43, где
[1330] C представляет собой  ;
;
[1331] D представляет собой -O-, -NH- или -NR3-; и
[1332] каждый U независимо представляет собой O, S или NR16.
[1333] Вариант осуществления изобретения 45: Соединение по варианту осуществления настоящего изобретения 43, где С представляет собой имидазолидин, имидазолидин-дион или дигидрооксазол.
[1334] Вариант осуществления изобретения 46: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-45, где A имеет мета- или пара-связь с X и Y.
[1335] Вариант осуществления изобретения 47: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-46, где B имеет мета- или пара-связь с X и Z.
[1336] Вариант осуществления изобретения 48: Соединение по любому одному из вариантов осуществления настоящего изобретения 33-47, где n1 и n2, каждый независимо, равны 0, 1 или 2.
[1337] Вариант осуществления изобретения 49: Соединение по вариантам осуществления изобретения1, отличающееся тем, что соединение имеет структуру формулы (V): 
[1338] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1339] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1340] C представляет собой 5-10-членный гетероарил или арил;
[1341] X представляет собой связь, -(CR5R6)t- или -NR7;
[1342] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1343] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1344] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1345] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1346] L представляет собой галоген, -NH2 или -CF3;
[1347] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1348] R3 выбран из водорода, галогена, оксо, =S, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1349] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1350] R7 представляет собой H или C1-C6 алкил;
[1351] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1352] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1353] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1354] n3 равно 0, 1, 2, 3, 4 или 5; и
[1355] t равно 0, 1 или 2.
[1356] Вариант осуществления изобретения 50: Соединение по варианту осуществления настоящего изобретения 49, где С представляет собой 5-7-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1357] Вариант осуществления изобретения 51: Соединение по варианту осуществления настоящего изобретения 49 или 50, где С представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил или пиримидил.
[1358] Вариант осуществления изобретения 52: Соединение по варианту осуществления настоящего изобретения 49, где C, который необязательно замещен R3, выбран из 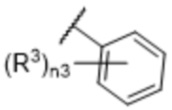 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[1359] Вариант осуществления изобретения 53: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-52, где A имеет мета- или пара-связь с X и Y.
[1360] Вариант осуществления изобретения 54: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-53, где B имеет мета- или пара-связь с X и Z.
[1361] Вариант осуществления изобретения 55: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-54, где каждый A и B представляют собой фенил.
[1362] Вариант осуществления изобретения 56: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-55, где -Z-V-L представляет собой -Z-CH2CH2Cl, -Z-CH2CH2CH2Cl, -Z-CH2CH2NH2 или -Z-CH2CH2CH2NH2, где Z представляет собой связь, -O-, -NH- или -N(COCH3)-.
[1363] Вариант осуществления изобретения 57: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-56, где -Y-W- представляет собой связь, -OCH2-, -OCH2CH2-, -OCH(CH3)-, -NH-, -NHCH2-, -NHC(=O)- или -C(=O)NH-.
[1364] Вариант осуществления изобретения 58: Соединение по любому одному из вариантов осуществления настоящего изобретения 49-57, где X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[1365] Вариант осуществления изобретения 59: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (VI):

[1366] где:
[1367] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1368] C представляет собой 5-10-членный гетероциклил;
[1369] X представляет собой связь, -(CR5R6)t- или -NR7;
[1370] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1371] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1372] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1373] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1374] L представляет собой галоген, -NH2 или -CF3;
[1375] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1376] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1377] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1378] R7 представляет собой H или C1-C6 алкил;
[1379] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил; и
[1380] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1381] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1382] n3 равно 0, 1, 2, 3, 4 или 5; и
[1383] t равно 0, 1 или 2.
[1384] Вариант осуществления изобретения 60: Соединение по варианту осуществления настоящего изобретения 57, где С представляет собой 5-7-членный насыщенный или частично насыщенный гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1385] Вариант осуществления изобретения 61: Соединение по варианту осуществления настоящего изобретения 59 или 60, где С представляет собой имидазолидин, имидазолидин-дион или дигидрооксазол.
[1386] Вариант осуществления изобретения 62: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-61, где C, который необязательно замещен R3, выбран из
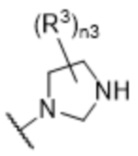 ,
, 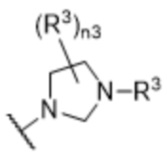 ,
, 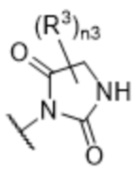 или
или 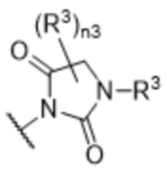 .
.
[1387] Вариант осуществления изобретения 63: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-62, где A имеет мета- или пара-связь с X и Y.
[1388] Вариант осуществления изобретения 64: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-63, где B имеет мета- или пара-связь с X и Z.
[1389] Вариант осуществления изобретения 65: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-64, где каждый A и B представляют собой фенил.
[1390] Вариант осуществления изобретения 66: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-65, где -V-L представляет собой -CH2CH2Cl, -CH2CH2CH2Cl, -CH2CH2NH2 или -CH2CH2CH2NH2, и Z представляет собой связь, -O-, -NH- или -N(COCH3)-.
[1391] Вариант осуществления изобретения 67: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-66, где -Y-W- представляет собой связь, -OCH2-, -OCH2CH2-, -OCH(CH3)-, -NH-, -NHCH2-, -NHC(=O)- или -C(=O)NH-.
[1392] Вариант осуществления изобретения 68: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-67, где X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[1393] Вариант осуществления изобретения 69: Соединение по любому одному из вариантов осуществления настоящего изобретения 59-68 , где R3 представляют собой оксо, =S, =NR16, C1-C3 алкил, -SO2(C1-C3 алкил) или -NHSO2(C1-C3 алкил).
[1394] Вариант осуществления изобретения 70: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (A):

[1395] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1396] C представляет собой фенил или 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[1397] X представляет собой связь, -(CR5R6)t- или -NR7;
[1398] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1399] Z представляет собой связь, -CH2-, -O- или -NH-;
[1400] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1401] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1402] L представляет собой галоген, -NH2 или -CF3;
[1403] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1404] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[1405] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[1406] R7 представляет собой H или C1-C6 алкил;
[1407] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1408] n3 равно 0, 1, 2, 3, 4 или 5; и
[1409] t равно 0, 1 или 2.
[1410] Вариант осуществления изобретения 71: Соединение по варианту осуществления настоящего изобретения 70, где С представляет собой 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1411] Вариант осуществления изобретения 72: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (B)

[1412] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1413] C представляет собой 5-7-членный насыщенный или частично насыщенный моноциклический гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[1414] X представляет собой связь, -(CR5R6)t- или -NR7;
[1415] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1416] Z представляет собой связь, -CH2-, -O- или -NH-;
[1417] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1418] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1419] L представляет собой галоген, -NH2 или -CF3;
[1420] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1421] R3 выбран из водорода, F, Cl, Br, I, оксо, =S, =NR16, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[1422] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[1423] R7 представляет собой H или C1-C6 алкил;
[1424] R16 представляет собой водород или C1-C3 алкил;
[1425] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1426] n3 равно 0, 1, 2, 3, 4 или 5; и
[1427] t равно 0, 1 или 2.
[1428] Вариант осуществления изобретения 73: Соединение по любому одному из вариантов осуществления настоящего изобретения 70-72, где -V-L представляет собой -CH2CH2Cl, -CH2CH2CH2Cl, -CH2CH2NH2 или -CH2CH2CH2NH2.
[1429] Вариант осуществления изобретения 74: Соединение по любому одному из вариантов осуществления настоящего изобретения 70-73, где -Y-W- представляет собой связь, -OCH2-, -OCH2CH2-, -OCH(CH3)-, -NH-, -NHCH2-, -NHC(=O)- или -C(=O)NH-.
[1430] Вариант осуществления изобретения 75: Соединение по любому одному из вариантов осуществления настоящего изобретения 70-74, где X представляет собой связь, -CH2-, -C(CH3)H-, -C(CH3)2- или -CH2CH2-.
[1431] Вариант осуществления изобретения 76: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (C):

[1432] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1433] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1434] X представляет собой связь, -(CR5R6)t- или -NR7;
[1435] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1436] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1437] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7;
[1438] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1439] L представляет собой галоген, -NH2 или -CF3;
[1440] D представляет собой -NH или -NR3;
[1441] каждый U независимо представляет собой O, S или NR16;
[1442] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1443] R3 выбран из водорода, галогена, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1444] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1445] R7 представляет собой H или C1-C6 алкил;
[1446] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил; или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил;
[1447] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1448] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1449] n3 равно 0, 1, 2 или 3; и
[1450] t равно 0, 1 или 2.
[1451] Вариант осуществления изобретения 77: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (D):

[1452] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1453] C представляет собой 5- или 6-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из O, S или N, в качестве члена кольца;
[1454] X представляет собой -(CR5R6)t- или -NR7-;
[1455] Y представляет собой связь, -CH2-, -O- или -NH-;
[1456] Z представляет собой связь, -CH2-, -O- или -NH-;
[1457] W представляет собой связь, -CH2- или -C(CH3)H-;
[1458] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1459] L представляет собой водород, галоген, -NH2 или -CF3;
[1460] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1461] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[1462] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[1463] R7 представляет собой H или C1-C6 алкил;
[1464] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1465] n3 равно 0, 1, 2, 3, 4 или 5; и
[1466] t равно 0, 1 или 2.
[1467] Вариант осуществления изобретения 78: Соединение по вариантам осуществления изобретения1, отличающееся тем, что соединение имеет структуру формулы (E) 
[1468] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1469] C представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[1470] X представляет собой -(CR5R6)t- или -NR7-;
[1471] Y представляет собой связь, -CH2-, -O- или -NH-;
[1472] Z представляет собой связь, -CH2-, -O- или -NH-;
[1473] W представляет собой связь, -CH2- или -C(CH3)H-;
[1474] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1475] L представляет собой водород или галоген;
[1476] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1477] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NHSO2CH3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)CO(C1-C3 алкила);
[1478] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[1479] R7 представляет собой H или C1-C6 алкил;
[1480] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1481] n3 равно 0, 1 или 2; и
[1482] t равно 1 или 2.
[1483] Вариант осуществления изобретения 79: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (F):

[1484] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1485] C представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[1486] X представляет собой -(CR5R6)t- или -NR7-;
[1487] Y представляет собой -O-;
[1488] Z представляет собой -O-;
[1489] W представляет собой -CH2- или -C(CH3)H-;
[1490] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1491] L представляет собой водород или галоген;
[1492] R1 и R2, каждый независимо, представляют собой галоген или -CN;
[1493] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[1494] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[1495] R7 представляет собой H или C1-C6 алкил;
[1496] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1497] n3 равно 0, 1 или 2; и
[1498] t равно 1 или 2.
[1499] Вариант осуществления изобретения 80: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (G):

[1500] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1501] C представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[1502] X представляет собой -(CR5R6)t- или -NR7-;
[1503] Y представляет собой -O-;
[1504] Z представляет собой -O-;
[1505] W представляет собой -CH2- или -C(CH3)H-;
[1506] V представляет собой -CH2-, и L представляет собой водород;
[1507] или альтернативно, V представляет собой -CH2CH2- или -CH2CH2CH2-, и L представляет собой галоген
[1508] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1509] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[1510] R5 и R6, каждый независимо, представляют собой водород или метил;
[1511] R7 представляет собой H или C1-C6 алкил;
[1512] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1513] n3 равно 1 или 2; и
[1514] t равно 1.
[1515] Вариант осуществления изобретения 81: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (H)

[1516] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1517] C-I представляет собой  .
.  ,
,  ,
,  ,
,  или
или  ;
;
[1518] X представляет собой -(CR5R6)t- или -NR7-;
[1519] Y представляет собой -O-;
[1520] Z представляет собой -O-;
[1521] W представляет собой -CH2- или -C(CH3)H-;
[1522] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1523] L представляет собой галоген;
[1524] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1525] R5 и R6, каждый независимо, представляют собой водород или метил;
[1526] R7 представляет собой H или C1-C6 алкил;
[1527] n1 и n2, каждый независимо, равны 0, 1 или 2; и
[1528] t равно 1.
[1529] Вариант осуществления изобретения 82: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-69, где каждый A и B представляют собой моноциклическое кольцо.
[1530] Вариант осуществления изобретения 83: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-69, где B представляет собой фенил, пиридил или пиримидил.
[1531] Вариант осуществления изобретения 84: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-36, где Z и V одновременно не представляют собой связь.
[1532] Вариант осуществления изобретения 85: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-78, где Y и W одновременно не представляют собой связь.
[1533] Вариант осуществления изобретения 86: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-48, где С представляет собой 4-10-членное кольцо.
[1534] Вариант осуществления изобретения 87: Соединение, выбранное из соединений A1-A97 , или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[1535] Вариант осуществления изобретения 88: Соединение, выбранное из соединений A98-A186 , или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[1536] Вариант осуществления изобретения 89: Соединение, выбранное из соединений A187-A211, или его фармацевтически приемлемая соль.
[1537] Вариант осуществления изобретения 90: Соединение, выбранное из соединений B1-B11 , или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[1538] Вариант осуществления изобретения 91: Соединение, имеющее структурную формулу (IA):

[1539] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1540] A и B, каждый независимо, представляют собой арил или гетероарил;
[1541] C представляет собой 3-10-членное кольцо;
[1542] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[1543] Y и Z, каждый независимо, представляют собой связь, -(CR8R9)m-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2- или -NR7-;
[1544] W и V, каждый независимо, представляют собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1545] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1546] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1547] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1548] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1549] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1550] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -OCO(C1-C6 алкил), -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1551] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[1552] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), взятые вместе, образуют необязательно замещенный гетероциклил;
[1553] каждый m независимо равно 0, 1 или 2;
[1554] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[1555] n3 равно 0, 1, 2, 3, 4 или 5; и
[1556] каждое t независимо равно 0, 1 или 2.
[1557] Вариант осуществления изобретения 92: Соединение по варианту осуществления настоящего изобретения 91, отличающееся тем, что соединение имеет структуру формулы (VA): 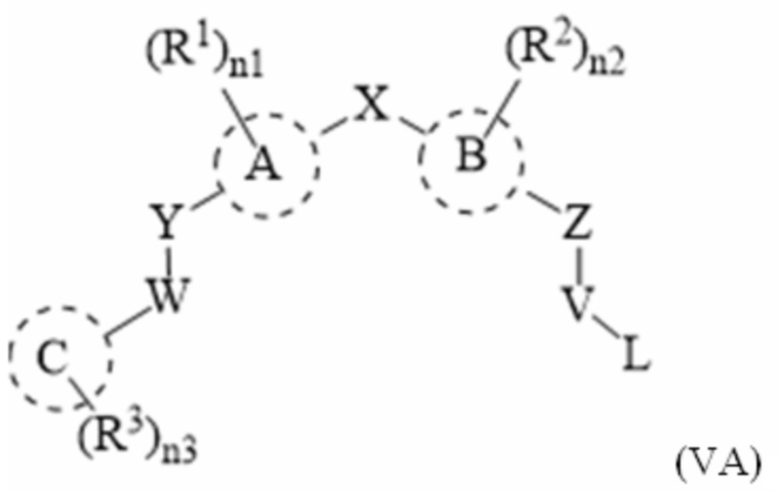
[1558] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1559] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1560] C представляет собой 5-10-членный гетероарил или арил;
[1561] X представляет собой связь, -(CR5R6)t- или -NR7;
[1562] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1563] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1564] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1565] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[1566] L представляет собой водород, галоген, -OH, -NH2 или -CF3;
[1567] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1568] R3 выбран из водорода, галогена, оксо, =S, -CN, -CF3, -OH, -S(C1-C3 алкил), C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -NR14COOR16, -NR14CONR14R15, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкил) или -(C1-C6 алкил)-SO2(C1-C3 алкил);
[1569] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, -NH2, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1570] R7 представляет собой H, C1-C6 алкил, -CO(C1-C6 алкил);
[1571] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или -COO(C1-C6 алкил); или R14 и R15 , взятые вместе, образуют 3-6-членный гетероциклил;
[1572] R16 представляет собой водород, C1-C3 алкил, C1-C3 галогеналкил, C2-C3 алкенил или C2-C3 алкинил;
[1573] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1574] n3 равно 0, 1, 2, 3, 4 или 5; и
[1575] t равно 0, 1 или 2.
[1576] Вариант осуществления изобретения 93: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-7, 33-39 и 49, где C, который необязательно замещен R3, выбран из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[1577] Вариант осуществления изобретения 94: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (E-I):
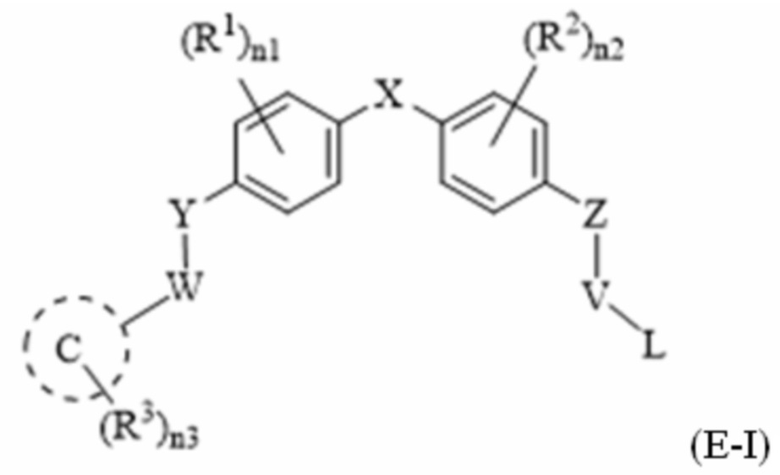
[1578] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1579] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1580] X представляет собой -(CR5R6)t- или -NR7-;
[1581] Y представляет собой связь, -CH2-, -O- или -NH-;
[1582] Z представляет собой связь, -CH2-, -O- или -NH-;
[1583] W представляет собой связь, -CH2- или -C(CH3)H-;
[1584] V представляет собой -CH2-, -CH2CH2-, -CH2CH2CH2- или -CH2CHClCH2-;
[1585] L представляет собой водород, -OH или галоген;
[1586] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1587] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[1588] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[1589] R7 представляет собой H или C1-C6 алкил;
[1590] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1591] n3 равно 0, 1 или 2; и
[1592] t равно 1 или 2.
[1593] Вариант осуществления изобретения 95: Соединение по варианту осуществления настоящего изобретения 94, где R3 выбран из водорода, F, Cl, Br, I, -CN, -CF3, -OH, метила, метокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила) или -NHCO(C1-C3 алкила).
[1594] Вариант осуществления изобретения 96: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (G-I):

[1595] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1596] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1597] X представляет собой -(CR5R6)t-;
[1598] Y представляет собой -O-;
[1599] Z представляет собой -O-;
[1600] W представляет собой -CH2- или -C(CH3)H-;
[1601] V представляет собой -CH2CH2- или -CH2CH2CH2-;
[1602] L представляет собой галоген
[1603] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1604] R3 выбран из -NHSO2CH3, -N(CH3)SO2CH3 или -SO2CH3;
[1605] R5 и R6, каждый независимо, представляют собой водород или метил;
[1606] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1607] n3 равно 1 или 2; и
[1608] t равно 1.
[1609] Вариант осуществления изобретения 97: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (H-I):
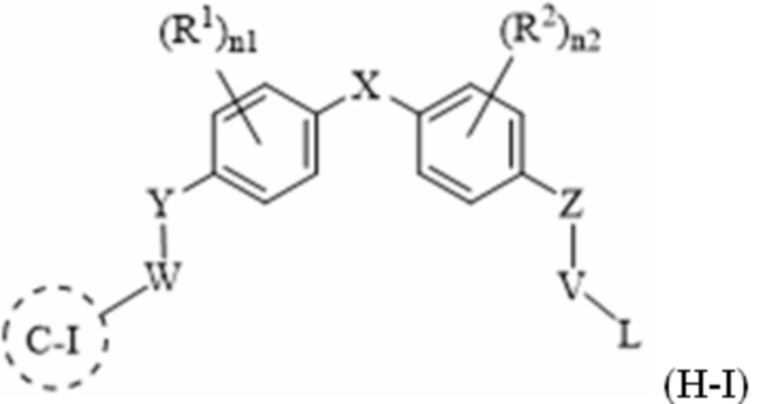
[1610] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1611] C-I представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1612] X представляет собой -(CR5R6)t-;
[1613] Y представляет собой -O-;
[1614] Z представляет собой -O-;
[1615] W представляет собой -CH2- или -C(CH3)H-;
[1616] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1617] L представляет собой галоген;
[1618] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1619] R5 и R6, каждый независимо, представляют собой водород или метил;
[1620] R7 представляет собой H или C1-C6 алкил;
[1621] n1 и n2, каждый независимо, равны 0, 1 или 2; и
[1622] t равно 1.
[1623] Вариант осуществления изобретения 98: Соединение по варианту осуществления настоящего изобретения 1, отличающееся тем, что соединение имеет структуру формулы (E-II)

[1624] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1625] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1626] X представляет собой -(CR5R6)-;
[1627] Y представляет собой связь, -CH2-, -O- или -NH-;
[1628] Z представляет собой связь, -CH2-, -O- или -NH-;
[1629] W представляет собой связь, -CH2- или -C(CH3)H-;
[1630] V представляет собой -CH2-, -CH2CH2- или -CH2CH2CH2-;
[1631] L представляет собой галоген;
[1632] R1, R2A и R2B, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1633] R3 выбран из водорода, F, Cl, Br, I, оксо, -CN, -CF3, -OH, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[1634] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[1635] n1 равно 0, 1 или 2; и
[1636] n3 равно 1 или 2;
[1637] причем когда C-R3 представляет собой  , оба R2A и R2B не представляют собой Cl.
, оба R2A и R2B не представляют собой Cl.
[1638] Вариант осуществления изобретения 99: Соединение, имеющее структуру формулы (IB):
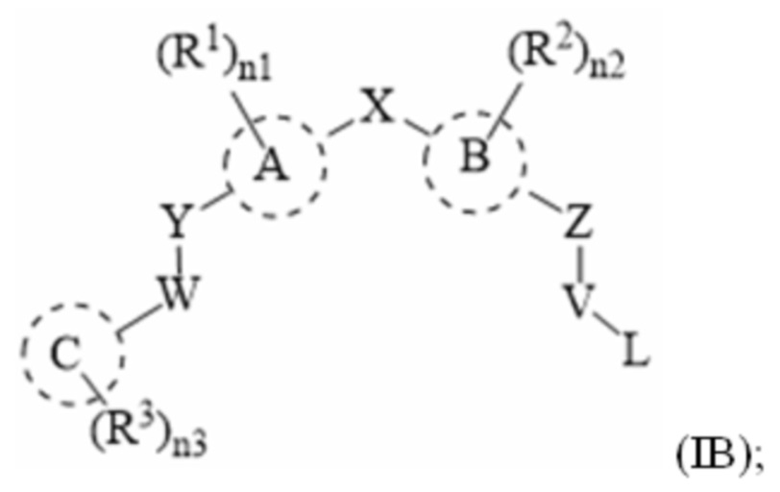
[1639] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1640] A и B, каждый независимо, представляют собой арил или гетероарил;
[1641] C представляет собой 3-10-членное кольцо;
[1642] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[1643] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1644] W представляет собой связь, -(CR8aR9a)m-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1645] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1646] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[1647] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1648] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1649] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1650] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1651] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1652] R8a и R9a, каждый независимо, представляют собой водород, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1653] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкил-NH2, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[1654] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), или (R14 и R16), взятые вместе, образуют необязательно замещенный гетероциклил;
[1655] каждый m независимо равно 0, 1 или 2;
[1656] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[1657] n3 равно 0, 1, 2, 3, 4 или 5; и
[1658] каждое t независимо равно 0, 1 или 2.
[1659] Вариант осуществления изобретения 100: Соединение, имеющее структуру формулы (IIA):
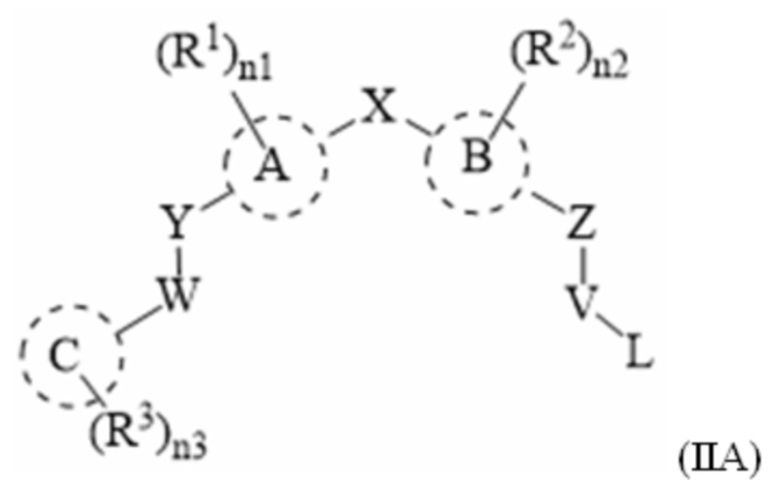
[1660] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1661] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1662] C представляет собой 3-10-членное кольцо;
[1663] X представляет собой связь, -(CR5R6)t- или -NR7-;
[1664] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1665] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1666] W представляет собой связь, -CH2-, -C(CH3)H-, -NHCO-, -N(C1-C3 алкил)CO- или -CONH- или -CON(C1-C3 алкил)-;
[1667] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[1668] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1669] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1670] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1671] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1672] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1673] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1674] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил или C1-C6 алкил-NH2; или R14 и R16, взятые вместе, образуют 3-6-членный гетероциклил;
[1675] каждый m независимо равно 0, 1 или 2;
[1676] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1677] n3 равно 0, 1, 2, 3, 4 или 5; и
[1678] t равно 0, 1 или 2.
[1679] Вариант осуществления изобретения 101: Соединение, имеющее структуру формулы (IIB):
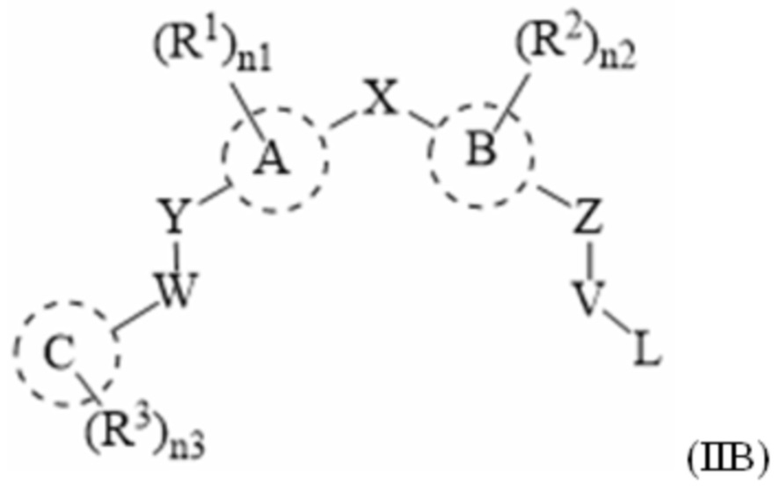
[1680] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1681] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1682] C представляет собой 3-10-членное кольцо;
[1683] X представляет собой связь, -(CR5R6)t- или -NR7-;
[1684] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1685] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1686] W представляет собой связь, -CH2- или -C(CH3)H-;
[1687] V представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1688] L представляет собой водород, галоген, -CF2R10, -CF3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1689] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1690] R3 выбран из водорода, галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1691] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1692] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1693] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1694] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1695] R7, R10 и R16, каждый независимо, представляют собой водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил или C1-C6 алкил-NH2; или R14 и R16, взятые вместе, образуют 3-6-членный гетероциклил;
[1696] каждый m независимо равно 0, 1 или 2;
[1697] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1698] n3 равно 1, 2, 3, 4 или 5; и
[1699] t равно 0, 1 или 2.
[1700] Вариант осуществления изобретения 102: Соединение, имеющее структуру формулы (IC):
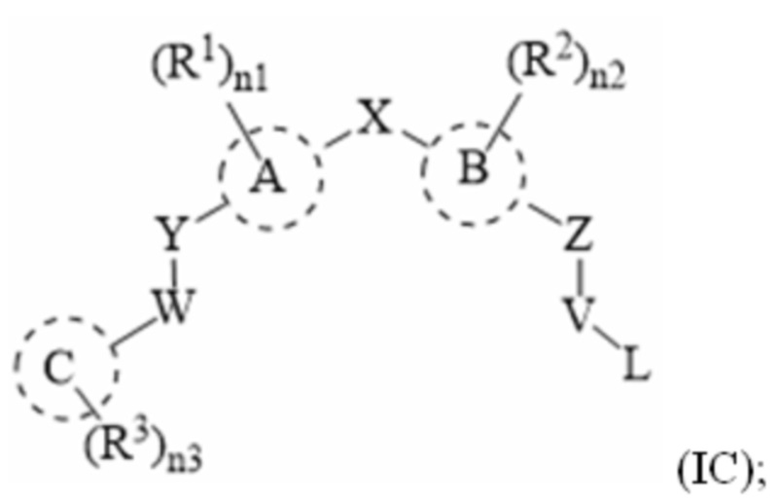
[1701] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1702] A и B, каждый независимо, представляют собой арил или гетероарил;
[1703] C представляет собой 3-10-членное кольцо;
[1704] X представляет собой связь, -(CR5R6)t-, -O-, -C(=O)-, -S-, -S(=O)-, -SO2-, -NR7-, -N(R7)CO-, -CON(R7)- или -NSO2R7-;
[1705] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1706] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, N(R7)CO-, -CONR7- или -NSO2R7-;
[1707] Z представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2- или -NR7-;
[1708] V представляет собой -CH2-, -CH2CH2-, -CH(CH3)CH2-, -CH2CH(CH3)- или -CH2CH2CH2-;
[1709] L представляет собой водород, галоген, -CF2R10, -CF3, -CCl2R10, -CCl3, -CN, -OR10; -NR11R12 или -CONR11R12;
[1710] R1 и R2, каждый независимо, представляют собой водород, дейтерий, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1711] R3 представляет собой водород, галоген, оксо, =S, =NR16, -CN, -CF3, -OH, -SR16, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COOR16, -NR14COR16, -NR14CONR14R15, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил;
[1712] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R5 и R6, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1713] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1714] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкокси, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR14R15, необязательно замещенный -(C1-C6 алкил)-CONR14R15, необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R8a и R8b, взятые вместе, образуют необязательно замещенный карбоциклил или необязательно замещенный гетероциклил;
[1715] R7, R10 и R16, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный C1-C6 алкил-NH2, C1-C6 галогеналкил, C2-C6 галогеналкенил, C2-C6 галогеналкинил, необязательно замещенный карбоциклил, необязательно замещенный -CO(C1-C6 алкил), -CO(необязательно замещенный гетероциклил), необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или R7 и R8a, взятые вместе, образуют необязательно замещенный гетероциклил;
[1716] R11, R12, R13, R14 и R15, каждый независимо, представляют собой водород, необязательно замещенный C1-C6 алкил, необязательно замещенный C2-C6 алкенил, необязательно замещенный C2-C6 алкинил, необязательно замещенный -COO(C1-C6 алкил), необязательно замещенный карбоциклил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; или (R11 и R12) или (R14 и R15), или (R14 и R16), взятые вместе, образуют необязательно замещенный гетероциклил;
[1717] каждый m независимо равно 0, 1 или 2;
[1718] n1 и n2, каждый независимо, равны 0, 1, 2, 3 или 4;
[1719] n3 равно 0, 1, 2, 3, 4 или 5; и
[1720] каждое t независимо равно 0, 1 или 2.
[1721] Вариант осуществления изобретения 103: Соединение, имеющее структурную формулу (IIIA):

[1722] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1723] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1724] C представляет собой 3-10-членное кольцо;
[1725] X представляет собой связь, -(CR5R6)t- или -NR7;
[1726] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2-, -NR7- или -N(COCH3)-;
[1727] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1728] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1729] V представляет собой -CH2-, и L представляет собой галоген, -NH2, -CHCl2, -CCl3 или -CF3; или
[1730] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[1731] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1732] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1733] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1734] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[1735] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1736] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1737] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1738] R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил;
[1739] каждый m независимо равно 0, 1 или 2;
[1740] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1741] n3 равно 1, 2, 3, 4 или 5; и
[1742] t равно 0, 1 или 2.
[1743] Вариант осуществления изобретения 104: Соединение, имеющее структурную формулу (G-II)
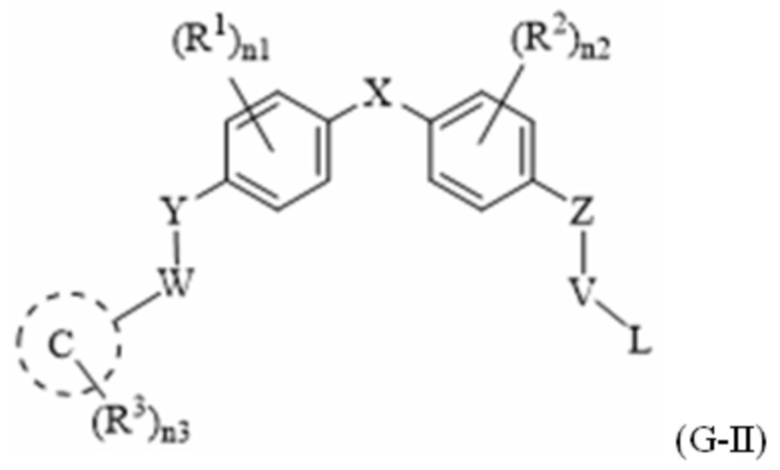
[1744] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1745] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1746] X представляет собой -(CR5R6)t-;
[1747] Y представляет собой -O-;
[1748] Z представляет собой -O-;
[1749] W представляет собой -CH2- или -C(CH3)H-;
[1750] V представляет собой -CH2CH2-;
[1751] L представляет собой галоген;
[1752] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1753] по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[1754] R5 и R6, каждый независимо, представляют собой водород или метил;
[1755] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1756] n3 равно 1 или 2; и
[1757] t равно 1.
[1758] Вариант осуществления изобретения 105: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-104, где по меньшей мере один из R3 представляет собой -CN, -OCH3, -SO2CH3, -NHSO2CH3, -CH2NHSO2CH3, -SO2NH2, -CONH2 или -NHCOCH3.
[1759] Вариант осуществления изобретения 106: Соединение, выбранное из соединений A212-A234, или его фармацевтически приемлемая соль.
[1760] Вариант осуществления изобретения 107: Фармацевтическая композиция, содержащая соединение по любому одному из вариантов осуществления изобретения 1-106 и фармацевтически приемлемый носитель.
[1761] Вариант осуществления изобретения 108: Фармацевтическая композиция по варианту осуществления изобретения 107, дополнительно содержащий один или более дополнительных терапевтических агентов.
[1762] Вариант осуществления изобретения 109: Фармацевтическая композиция по варианту осуществления изобретения 108, отличающаяся тем, что один или более дополнительных терапевтических агентов предназначены для лечения рака предстательной железы, рака молочной железы, рака яичников, рака мочевого пузыря, рака поджелудочной железы, гепатоцеллюлярного рака, рака эндометрия, карциномы слюнной железы, выпадения волос, угрей, гирсутизма, кист яичников, поликистозных заболеваний яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии или возрастной дегенерации желтого пятна.
[1763] Вариант осуществления изобретения 110: Фармацевтическая композиция по варианту осуществления изобретения 108, отличающаяся тем, что один или более дополнительных терапевтических агентов представляют собой ингибитор поли(АДФ-рибоза)полимеразы (PARP), включая, помимо прочего, олапариб, нирапариб, рукапариб, талазопариб; ингибитор лигандсвязывающего домена андрогенового рецептора, включая, но не ограничиваясь ими, энзалутамид, апалутамид, даролутамид, бикалутамид, нилутамид, флутамид, ODM-204, TAS3681; ингибитор CYP17, включая, помимо прочего, галетерон, абиратерон, ацетат абиратерона; ингибитор микротрубочек, включая, но не ограничиваясь ими, доцетаксел, паклитаксел, кабазитаксел (XRP-6258); модулятор PD-1 или PD-L1, включая, не ограничиваясь ими, пембролизумаб, дурвалумаб, ниволумаб, атезолизумаб; агонист гонадотропин-высвобождающего гормона, включая, но не ограничиваясь ими, ацетат ципротерона, лейпролид; ингибитор 5-альфа-редуктазы, включая, но не ограничиваясь ими, финастерид, дутастерид, туростерид, бекслостерид, изонстерид, FCE 28260, SKF105,111; ингибитор фактора роста эндотелия сосудов, включая, но не ограничиваясь ими, бевацизумаб (Авастин); ингибитор гистондеацетилазы, включая, но не ограничиваясь ими, OSU-HDAC42; ингибитор интегрина альфа-v-бета-3, включая, но не ограничиваясь ими, ВИТАКСИН; ингибитор рецептора тирозинкиназы, включая, но не ограничиваясь ими, сунитумиб; ингибитор фосфоинозитид-3-киназы, включая, но не ограничиваясь ими, алпелисиб, бупарлисиб, идеалисиб; ингибитор киназы анапластической лимфомы (ALK), включая, но не ограничиваясь ими, кризотиниб, алектиниб; антагонист рецептора эндотелина А, включая, но не ограничиваясь ими, ZD-4054; ингибитор против CTLA4, включая, но не ограничиваясь ими, MDX-010 (ипилимумаб); ингибитор белка теплового шока 27 (HSP27), включая, но не ограничиваясь, OGX 427; деструктор андрогеновых рецепторов, включая, но не ограничиваясь ими, ARV-330, ARV-110; ингибитор ДНК-связывающего домена андрогеновых рецепторов, включая, но не ограничиваясь, VPC-14449; ингибитор бромдомена и экстра-терминального мотива (BET), включая, но не ограничиваясь ими, BI-894999, GSK25762, GS-5829; ингибитор N-концевого домена андрогенового рецептора, включая, но не ограничиваясь ими, синтокамид; радиоактивный терапевтический агент, излучающий альфа-частицы, включая, но не ограничиваясь ими, радий-233 или его соль; никлозамид; или их родственные соединения; селективный модулятор эстрогенового рецептора (SERM), включая, но не ограничиваясь ими, тамоксифен, ралоксифен, торемифен, арзоксифен, базедоксифен, пипиндоксифен, лазофоксифен, энкломифен; селективный деструктор эстрогенового рецептора (SERD), включая, но не ограничиваясь ими, фулвестрант, ZB716, OP-1074, эласестрант, AZD9496, GDC0810, GDC0927, GW5638, GW7604; ингибитор ароматазы, включая, но не ограничиваясь ими, анастразол, экземестан, летрозол; селективные модуляторы прогестеронового рецептора (SPRM), включая, но не ограничиваясь ими, мифепристон, лонаприсон, онапристон, асоприснил, лонаприснил, улипристал, телапристон; ингибитор глюкокортикоидного рецептора, включая, но не ограничиваясь ими, мифепристон, COR108297, COR125281, ORIC-101, PT150; ингибиторы CDK4/6, включая пальбоциклиб, абемациклиб, рибоциклиб; антагонист рецептора HER2, включая, но не ограничиваясь ими, трастузумаб, нератиниб; мишень для млекопитающих ингибитора рапамицина (mTOR), включая, но не ограничиваясь ими, эверолимус, темсиролимус.
[1764] Вариант осуществления изобретения 111: Способ модуляции активности андрогенового рецептора, включающий введение соединения по любому из вариантов осуществления изобретения 1-106 субъекту, нуждающемуся в этом.
[1765] Вариант осуществления изобретения 112: Способ по любому из вариантов осуществления 111, отличающийся тем, что модуляция активности андрогенового рецептора предназначено для лечения состояния или заболевания, выбранного из рака предстательной железы, рака молочной железы, рака яичников, рака мочевого пузыря, рака поджелудочной железы, гепатоцеллюлярного рака, рака эндометрия, карциномы слюнной железы, выпадения волос, угрей, гирсутизма, кист яичников, поликистоза яичников, преждевременного полового созревания, спинальной и бульбарной мышечной атрофии или возрастной дегенерации желтого пятна.
[1766] Вариант осуществления изобретения 113: Способ лечения рака, включающий введение соединения по любому из вариантов осуществления изобретения 1-106 субъекту, нуждающемуся в этом.
[1767] Вариант осуществления изобретения 114: Способ по варианту осуществления изобретения 113, отличающийся тем, что рак выбран из рака предстательной железы, рака молочной железы, рака яичников, рака мочевого пузыря, рака поджелудочной железы, гепатоцеллюлярного рака, рака эндометрия или карциномы слюнной железы.
[1768] Вариант осуществления изобретения 115: Способ по варианту осуществления изобретения 113, отличающийся тем, что рак представляет собой рак предстательной железы.
[1769] Вариант осуществления изобретения 116: Способ по варианту осуществления изобретения 115, отличающийся тем, что рак предстательной железы представляет собой первичный или локализованный рак предстательной железы, местно-распространенный рак предстательной железы, рецидивирующий рак предстательной железы, распространенный рак предстательной железы, метастатический рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы и гормоночувствительный рак предстательной железы. Способ по варианту осуществления изобретения 115, отличающийся тем, что рак предстательной железы представляет собой первичный или локализованный рак предстательной железы, местно-распространенный рак предстательной железы, рецидивирующий рак предстательной железы, распространенный рак предстательной железы, метастатический рак предстательной железы, неметастатический устойчивый к кастрации рак предстательной железы, метастатический устойчивый к кастрации рак предстательной железы и гормоночувствительный рак предстательной железы.
[1770] Вариант осуществления изобретения 117: Способ по варианту осуществления изобретения 115, отличающийся тем, что рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы.
[1771] Вариант осуществления изобретения 118: Способ по варианту осуществления изобретения 115, отличающийся тем, что рак предстательной железы экспрессирует полноразмерный андрогеновый рецептор или усеченный вариант сплайсинга андрогенового рецептора.
[1772] Вариант осуществления изобретения 119: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 1000 нМ.
[1773] Вариант осуществления изобретения 120: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 900 нМ.
[1774] Вариант осуществления изобретения 121: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50 в ПСА-люциферазном анализе, равную менее чем около 800 нМ.
[1775] Вариант осуществления изобретения 122: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 700 нМ.
[1776] Вариант осуществления изобретения 123: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 600 нМ.
[1777] Вариант осуществления изобретения 124: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 500 нМ.
[1778] Вариант осуществления изобретения 125: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50 в ПСА-люциферазном анализе, равную менее чем около 400 нМ.
[1779] Вариант осуществления изобретения 126: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет in vitro IC50в ПСА-люциферазном анализе, равную менее чем около 300 нМ.
[1780] Вариант осуществления изобретения 127: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106 или 119--126, отличающееся тем, что соединение имеет in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка в микросомах млекопитающих.
[1781] Вариант осуществления изобретения 128: Соединение по варианту осуществления настоящего изобретения 126, отличающаяся тем, что микросомы млекопитающих представляют собой микросомы человека.
[1782] Вариант осуществления изобретения 129: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106 или 119-128, отличающееся тем, что соединение имеет in vitro метаболический клиренс в гепатоцитах млекопитающих, равный менее чем 4 мкл/мин/миллион клеток.
[1783] Вариант осуществления изобретения 130: Соединение по варианту осуществления настоящего изобретения 128, отличающаяся тем, что микросомы млекопитающих представляют собой микросомы человека.
[1784] Вариант осуществления изобретения 131: Соединение по любому одному из вариантов осуществления изобретения 1-106, отличающееся тем, что соединение имеет:
[1785] (a) in vitro IC50 в ПСА-люциферазном анализе, равную менее чем около 1000 нМ;
[1786] (b) in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка в микросомах млекопитающих; и
[1787] (c) in vitro метаболический клиренс в гепатоцитах млекопитающих, равный менее чем 4 мкл/мин/миллион клеток.
[1788] Вариант осуществления изобретения 132: Соединение по любому одному из вариантов осуществления настоящего изобретения 1-106, отличающееся тем, что соединение имеет:
[1789] (a) in vitro IC50 в ПСА-люциферазном анализе, равную менее чем около 1000 нМ;
[1790] (b) in vitro метаболический клиренс, равный менее чем 12 мкл/мин/мг белка в микросомах человека; и
[1791] (c) in vitro метаболический клиренс в гепатоцитах человека, равный менее чем 4 мкл/мин/миллион клеток.
[1792] Вариант осуществления изобретения 133: Соединения по любому одному из вариантов осуществления изобретения 119-132, отличающиеся тем, что ПСА-люциферазный анализ проводят, как описано в Примере 35.
[1793] Вариант осуществления изобретения 134: Соединения по любому одному из вариантов осуществления изобретения 119-132, отличающиеся тем, что метаболический клиренс измеряют согласно Примеру 36.
[1794] Вариант осуществления изобретения 135: Соединение, имеющее структуру формулы (IIIA):
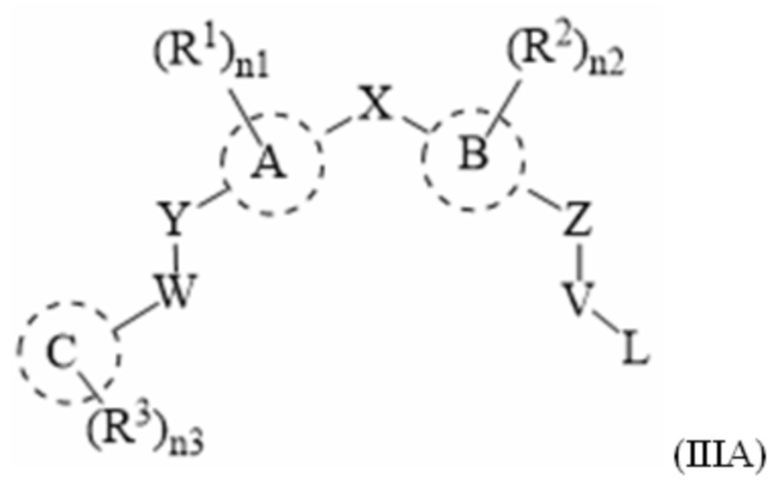
[1795] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1796] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1797] C представляет собой 3-10-членное кольцо;
[1798] X представляет собой связь, -(CR5R6)t- или -NR7;
[1799] Y представляет собой связь, -(CR8R9)m-, -O-, -S-, -S(=O)-, -SO2-, -NR7- или -N(COCH3)-;
[1800] W представляет собой связь, -(CR8aR9a)m-, -C(=O)-, -N(R7)CO-, -CONR7- или -NSO2R7-;
[1801] Z представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1802] V представляет собой -CH2-, и L представляет собой галоген, -NH2, -CHCl2, -CCl3 или -CF3; или
[1803] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[1804] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16 или необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1805] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1806] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1807] R7 представляет собой водород, C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил;
[1808] R8 и R9, каждый независимо, представляют собой водород, галоген или C1-C3 алкил;
[1809] R8a и R9a, каждый независимо, представляют собой водород, -OH, галоген, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14COR16, -(C1-C3 алкил)-NR14COR16, -CONR14R15 или -(C1-C3 алкил)-CONR14R15; или R8a и R8b, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1810] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1811] R16 представляет собой водород, необязательно замещенный C1-C3 алкил, необязательно замещенный C2-C3 алкенил, необязательно замещенный C2-C3 алкинил, C3-C6 циклоалкил или фенил;
[1812] каждый m независимо равно 0, 1 или 2;
[1813] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1814] n3 равно 1, 2, 3, 4 или 5; и
[1815] t равно 0, 1 или 2.
[1816] Вариант осуществления изобретения 136: Соединение по варианту осуществления изобретения 135, отличающееся тем, что соединение имеет структуру формулы (IVA):
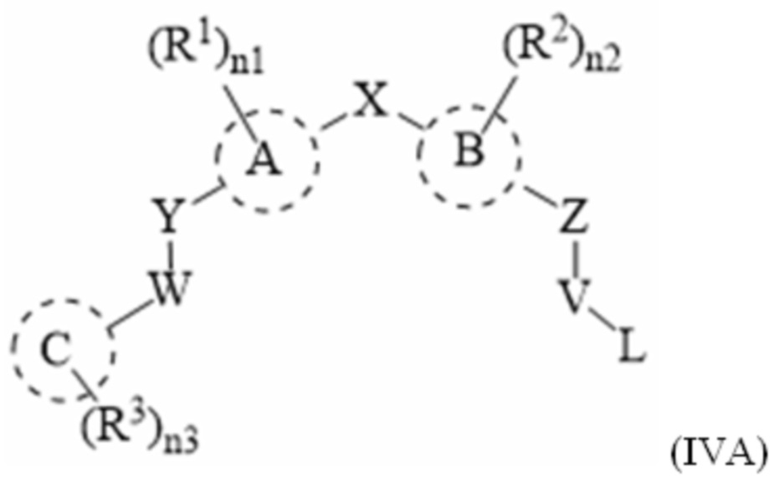
[1817] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1818] A и B, каждый независимо, выбран из фенила, пиридила, пиримидила или тиофена;
[1819] C представляет собой 3-10-членное кольцо;
[1820] X представляет собой связь, -(CR5R6)t- или -NR7;
[1821] Y и Z, каждый независимо, представляют собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1822] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1823] V представляет собой -CH2-, и L представляет собой галоген, -NH2 или -CF3; или
[1824] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[1825] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH, необязательно замещенный C1-C6 алкил, необязательно замещенный C1-C6 алкокси, необязательно замещенный -(C1-C6 алкил)-(C1-C6 алкокси), необязательно замещенный -(C1-C6 алкил)-OH, -NR13R14, необязательно замещенный -(C1-C6 алкил)-NR13R14, -NR14SO2R16, необязательно замещенный -(C1-C6 алкил)NR14SO2R16, -NR14COR16, необязательно замещенный -(C1-C6 алкил)-NR14COR16, -CONR13R14, необязательно замещенный -(C1-C6 алкил)-CONR14R15, -SO2NR14R15, необязательно замещенный -(C1-C6 алкил)-SO2NR14R15, необязательно замещенный -SO2R16, необязательно замещенный -(C1-C6 алкил)-SO2R16;
[1826] R3 выбран из галогена, оксо, =S, =NR16, -CN, -CF3, -OH, -S(C1-C3 алкила), C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -NR13R14, -(C1-C3 алкил)-NR13R14, -NR14SO2R16, -(C1-C3 алкил)NR14SO2R16, -NR14COR16, -(C1-C6 алкил)-NR14COR16, -CONR14R15, -(C1-C3 алкил)-CONR14R15, -SO2NR14R15, -(C1-C3 алкил)-SO2NR14R15, -SO2(C1-C3 алкила) или -(C1-C6 алкил)-SO2(C1-C3 алкила);
[1827] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH, C1-C3 алкил, C2-C3 алкенил, C2-C3 алкинил или C1-C3 алкокси; или R5 и R6, взятые вместе, образуют необязательно замещенный 3-6-членный карбоциклил или гетероциклил;
[1828] R7 представляет собой H или C1-C6 алкил;
[1829] R13, R14 и R15, каждый независимо, представляют собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил; или R14 и R15, взятые вместе, образуют 3-6-членный гетероциклил;
[1830] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил;
[1831] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1832] n3 равно 1, 2, 3, 4 или 5; и
[1833] t равно 0, 1 или 2.
[1834] Вариант осуществления изобретения 137: Соединение по варианту осуществления изобретения 135 или 136, где С представляет собой 5-10-членный гетероарил или арил
[1835] Вариант осуществления изобретения 138: Соединение по варианту осуществления изобретения 137, где С представляет собой 5-7-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца.
[1836] Вариант осуществления изобретения 139: Соединение по варианту осуществления изобретения 138, где C, замещенный (R3)n3, представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил, пиразин, фуран или пиримидил.
[1837] Вариант осуществления изобретения 140: Соединение по любому одному из вариантов осуществления изобретения 135-139, где C, замещенный (R3)n3, выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  , где R3a представляет собой C1-C3 алкил.
, где R3a представляет собой C1-C3 алкил.
[1838] Вариант осуществления изобретения 141: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-140, где R1 и R2, каждый независимо, представляют собой Cl, -CN, -CF3, -OH, метил, метокси или -CONH2.
[1839] Вариант осуществления изобретения 142: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-141, где:
[1840] A и B представляют собой фенил;
[1841] X представляет собой -(CR5R6)t-;
[1842] каждый Y и Z представляют собой -O-,
[1843] V представляет собой -CH2- или -CH2CH2-;
[1844] L представляет собой галоген;
[1845] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, -OH или необязательно замещенный C1-C6 алкил;
[1846] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил; и
[1847] R16 представляет собой водород, C1-C3 алкил, C2-C3 алкенил или C2-C3 алкинил.
[1848] Вариант осуществления изобретения 143: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-142, где:
[1849] R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
[1850] W представляет собой -CH2- или -C(CH3)H-;
[1851] V представляет собой -CH2CH2-; и
[1852] R1 и R2, каждый независимо, представляют собой водород, галоген или -CN.
[1853] Вариант осуществления изобретения 144: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-143, отличающееся тем, что соединение имеет структуру формулы (A-I):
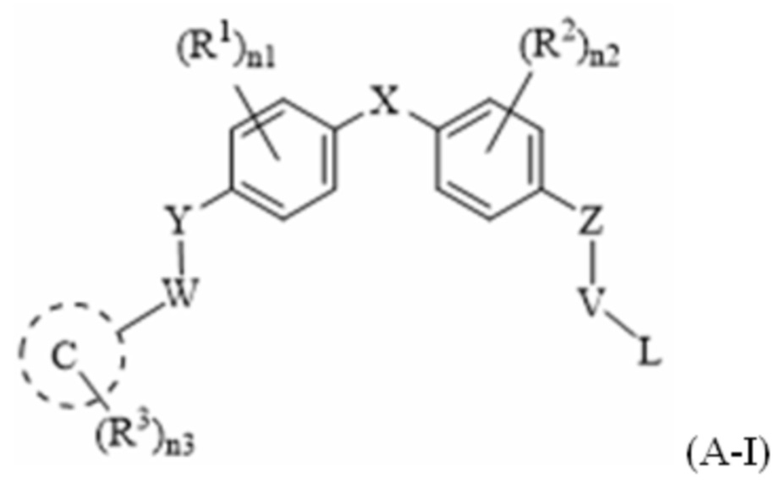
[1854] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1855] C представляет собой 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
[1856] X представляет собой связь, -(CR5R6)t- или -NR7;
[1857] Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
[1858] Z представляет собой связь, -CH2-, -O- или -NH-;
[1859] W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
[1860] V представляет собой -CH2-, и L представляет собой галоген, -NH2 или -CF3; или
[1861] V представляет собой -CH2CH2-, и L представляет собой галоген или -NH2;
[1862] R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
[1863] R3 выбран из -CN, C1-C3 алкокси, CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[1864] R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
[1865] R7 представляет собой H или C1-C6 алкил;
[1866] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1867] n3 равно 1, 2, 3, 4 или 5; и
[1868] t равно 0, 1 или 2.
[1869] Вариант осуществления изобретения 145: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-144, где: по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[1870] Вариант осуществления изобретения 146: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-145, где:
[1871] X представляет собой связь или -(CR5R6)t;
[1872] W представляет собой связь, -CH2- или -C(CH3)H-;
[1873] Y представляет собой -O-;
[1874] Z представляет собой -O-;
[1875] V представляет собой -CH2- или -CH2CH2-; и
[1876] L представляет собой галоген.
[1877] Вариант осуществления изобретения 147: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-146, отличающееся тем, что соединение имеет структуру формулы (G-II):
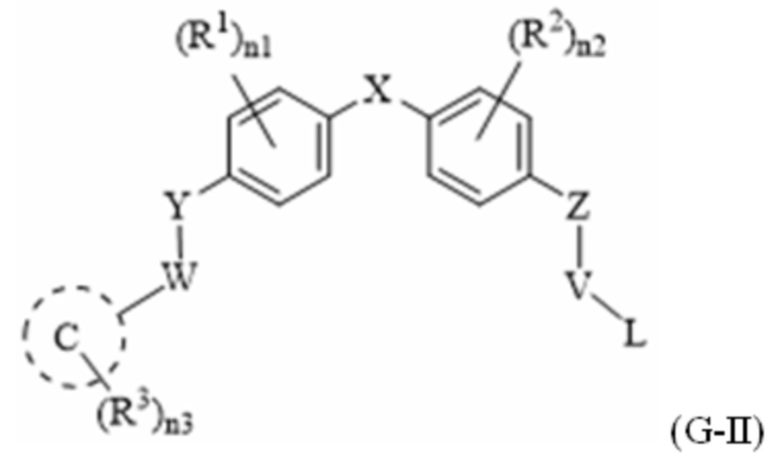
[1878] или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство, где:
[1879] C представляет собой  .
.  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
[1880] X представляет собой -(CR5R6)t-;
[1881] Y представляет собой -O-;
[1882] Z представляет собой -O-;
[1883] W представляет собой -CH2- или -C(CH3)H-;
[1884] V представляет собой -CH2CH2-;
[1885] L представляет собой галоген;
[1886] R1 и R2, каждый независимо, представляют собой Cl или -CN;
[1887] по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
[1888] R5 и R6, каждый независимо, представляют собой водород или метил;
[1889] n1 и n2, каждый независимо, равны 0, 1 или 2;
[1890] n3 равно 1 или 2; и
[1891] t равно 1.
[1892] Вариант осуществления изобретения 148: Соединение по любому одному из вариантов осуществления настоящего изобретения 135-147, где: по меньшей мере один R3 выбран из -NHSO2CH3, -NHSO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, C1-C3 алкила, C1-C3 алкокси, -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
[1893] Вариант осуществления изобретения 149: Соединение, выбранное из соединений A1-A96, A98-A116, A118-A159, A161-A175 или A177-A234 , или его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[1894] Вариант осуществления изобретения 150: Соединение по варианту осуществления настоящего изобретения 149, отличающееся тем, что соединение выбрано из
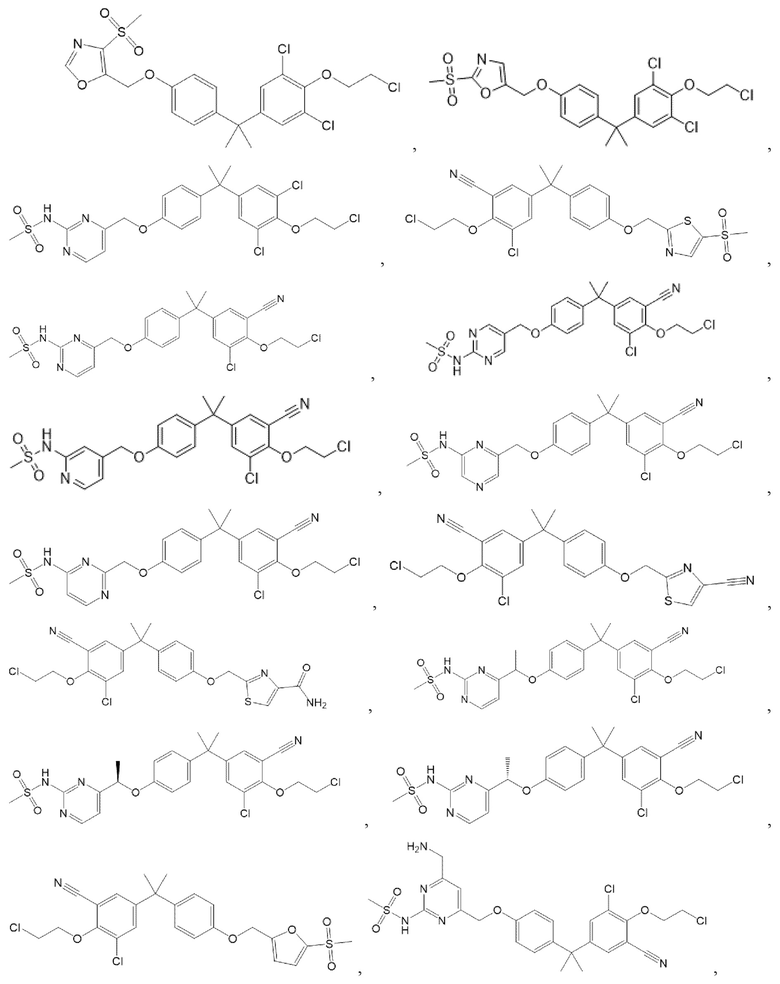
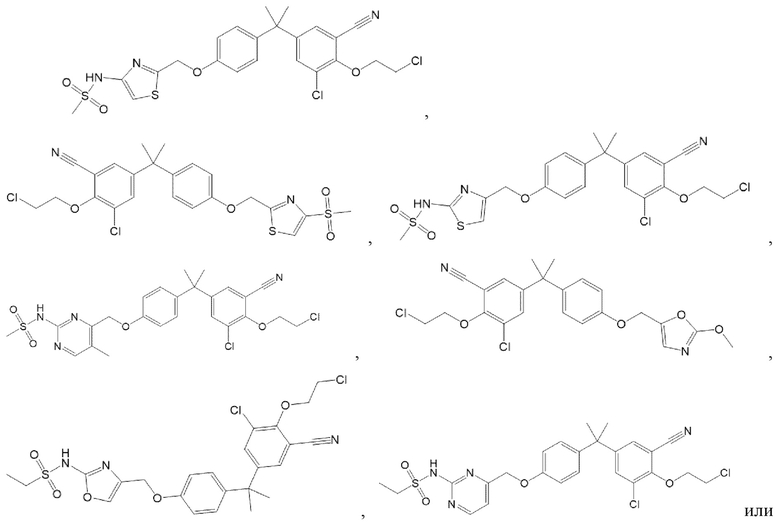
его фармацевтически приемлемая соль, таутомер, стереоизомер или пролекарство.
[1895] Вариант осуществления изобретения 151: Фармацевтическая композиция, содержащая соединение по любому одному из вариантов осуществления изобретения 135-150 и фармацевтически приемлемый носитель
[1896] Вариант осуществления изобретения 152: Способ лечения рака, включающий введение соединения, фармацевтически приемлемой соли, таутомера, стереоизомера или пролекарства любого одного из соединений по вариантам осуществления изобретения 135-150 или любой фармацевтической композиции по варианту осуществления изобретения 151 субъекту, нуждающемуся в этом.
[1897] Вариант осуществления изобретения 153: Способ по варианту осуществления изобретения 152, отличающийся тем, что рак представляет собой рак предстательной железы.
[1898] Вариант осуществления изобретения 154: Способ по варианту осуществления изобретения 153, отличающийся тем, что рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы.
[1899] Вариант осуществления изобретения 155: Способ по варианту осуществления изобретения 154, отличающийся тем, что рак предстательной железы экспрессирует полноразмерный андрогеновый рецептор или усеченный вариант сплайсинга андрогенового рецептора.
[1900] Публикации, обсуждаемые в настоящем документе, предназначены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в настоящем документе не должно истолковываться как признание того, что настоящее изобретение не имеет права датировать такую публикацию более ранней датой в силу предшествующего изобретения.
[1901] Хотя настоящее изобретение было описано в связи с его предложенными конкретными вариантами осуществления, следует понимать, что оно допускает дальнейшие модификации, и настоящая заявка предназначена для охвата любых вариаций, путей применения или адаптаций настоящего изобретения, следуя, в целом, принципам настоящего раскрытия и включая такие отклонения от настоящего раскрытия, которые входят в известную или обычную практику в области техники, к которой относится настоящее изобретение, и которые могут быть применены к существенным признакам, изложенным в настоящем документе выше и далее в объеме прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 3-(1-ОКСОИЗОИНДОЛИН-2-ИЛ)ПИПЕРИДИН-2,6-ДИОНА И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2795850C2 |
| ТРИЦИКЛИЧЕСКИЕ КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ПИРИДИН-2-ОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ BRD4 | 2016 |
|
RU2734959C2 |
| N1-(4-(5-(ЦИКЛОПРОПИЛМЕТИЛ)-1-МЕТИЛ-1H-ПИРАЗОЛ-4-ИЛ)ПИРИДИН-2-ИЛ)ЦИКЛОГЕКСАН-1,4-ДИАМИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ СK1 И/ИЛИ IRAK1 ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2761457C2 |
| ПРОИЗВОДНЫЕ 3-(5-ГИДРОКСИ-1-ОКСОИЗОИНДОЛИН-2-ИЛ) ПИПЕРИДИН-2,6-ДИОНА И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С БЕЛКОМ С "ЦИНКОВЫМИ ПАЛЬЦАМИ" 2 (IKZF2) СЕМЕЙСТВА IKAROS | 2019 |
|
RU2797559C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ MAT2A И СПОСОБЫ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2809987C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2808165C2 |
| ЦИАНОТИЕНОТРИАЗОЛОДИАЗЕПИНЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2750164C2 |
| ПРОИЗВОДНЫЕ 2-ЗАМЕЩЕННЫХ ФЕНИЛ-5, 7-ДИГИДРОКАРБИЛ-3, 7-ДИГИДРОПИРРОЛО [2, 3-d] ПИРИМИДИН-4-ОНОВ, ИХ ПОЛУЧЕНИЕ И ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2323220C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2665571C2 |
| АНТИВИРУСНЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2505539C2 |
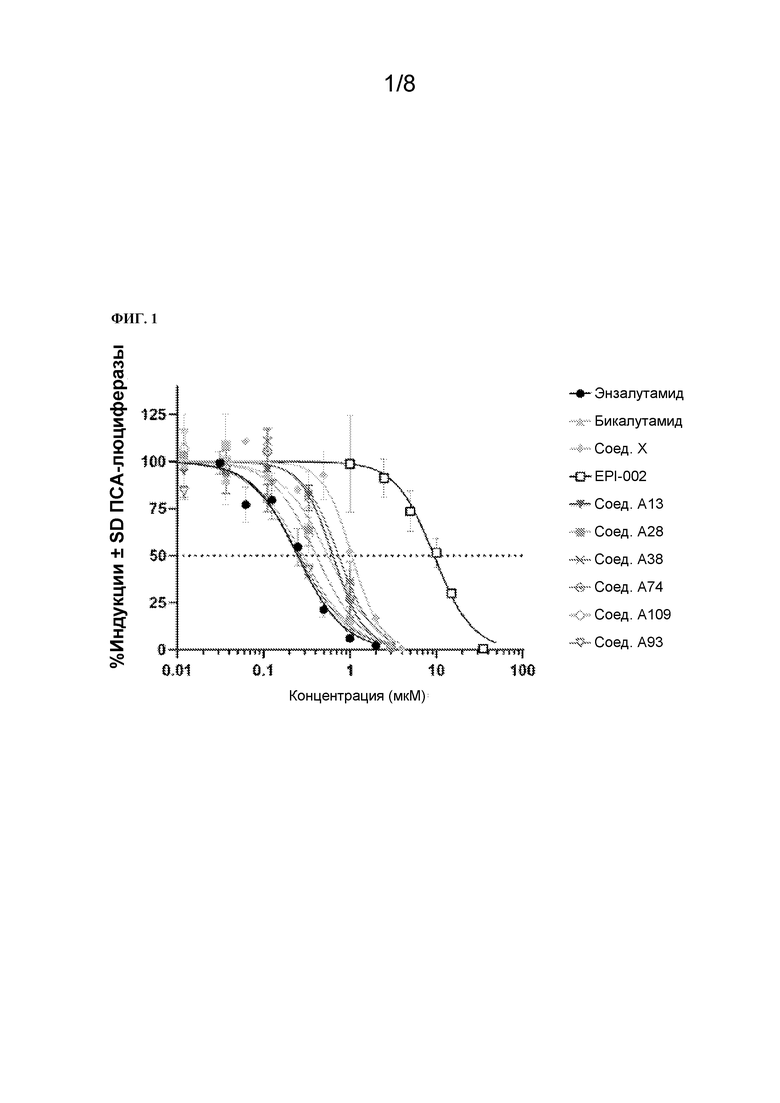
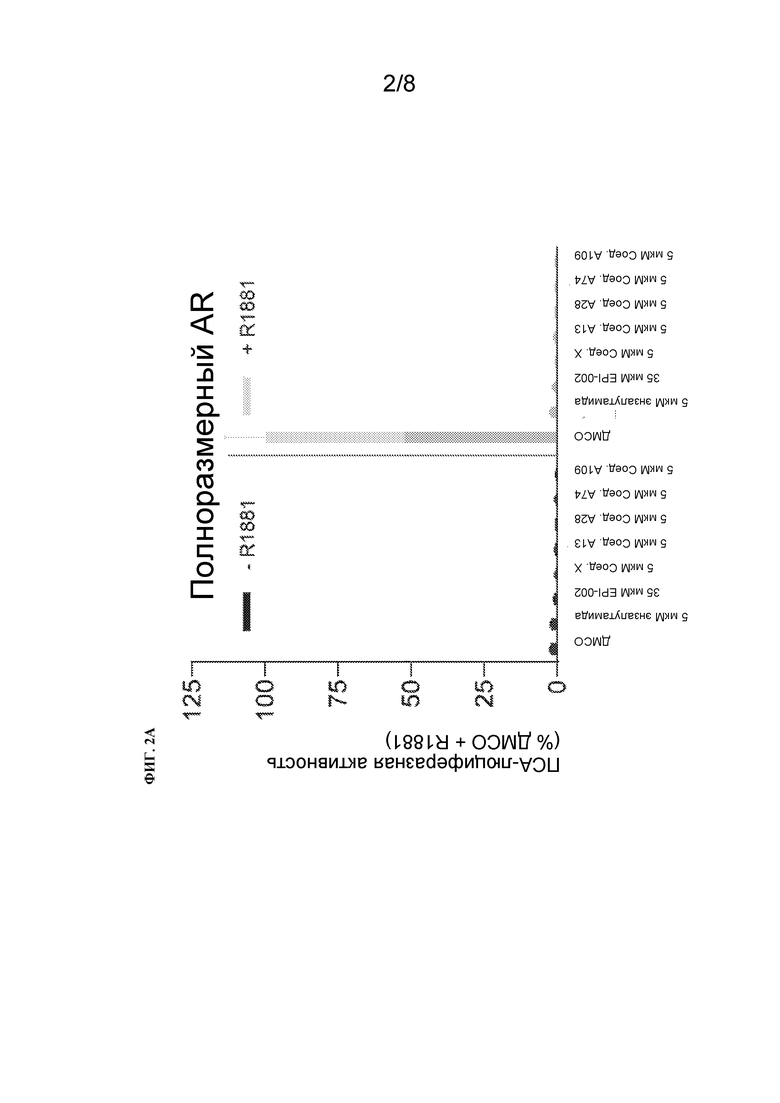
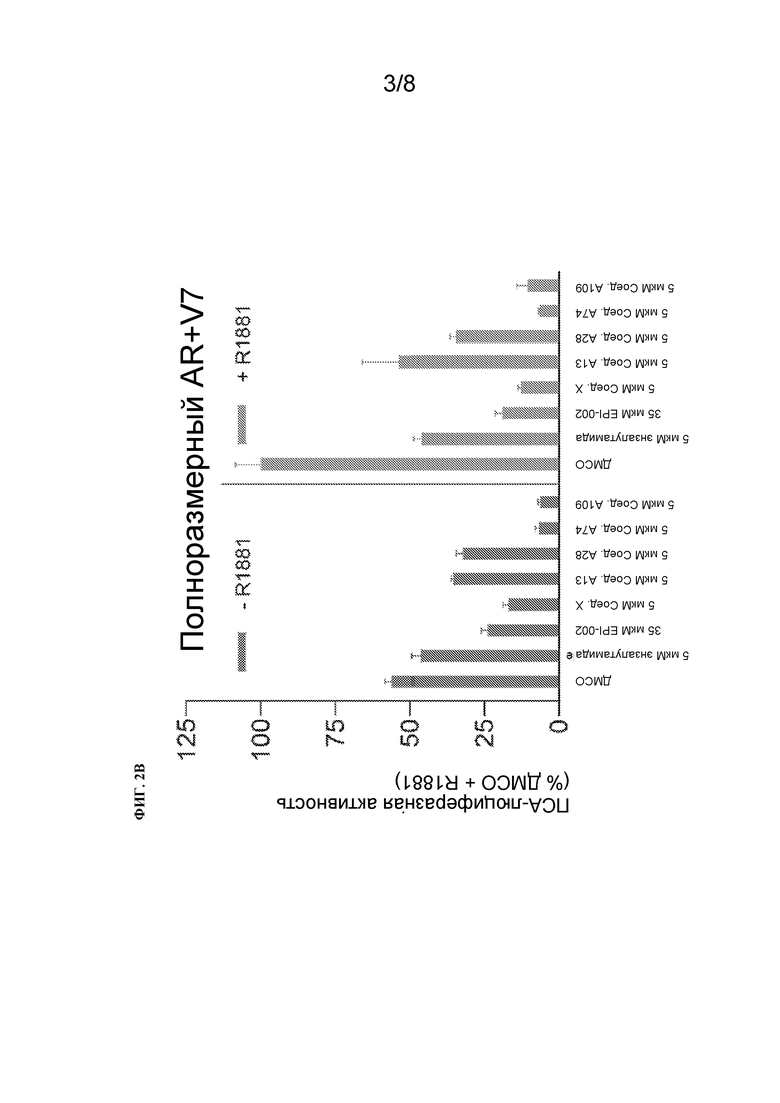
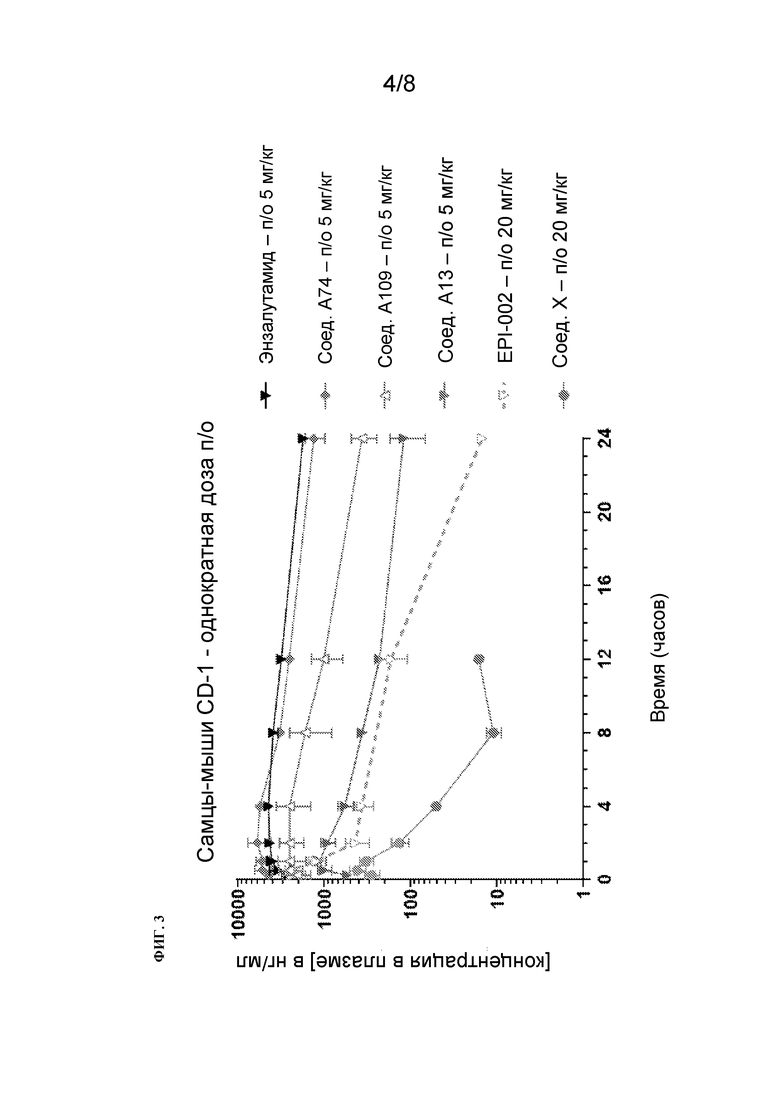
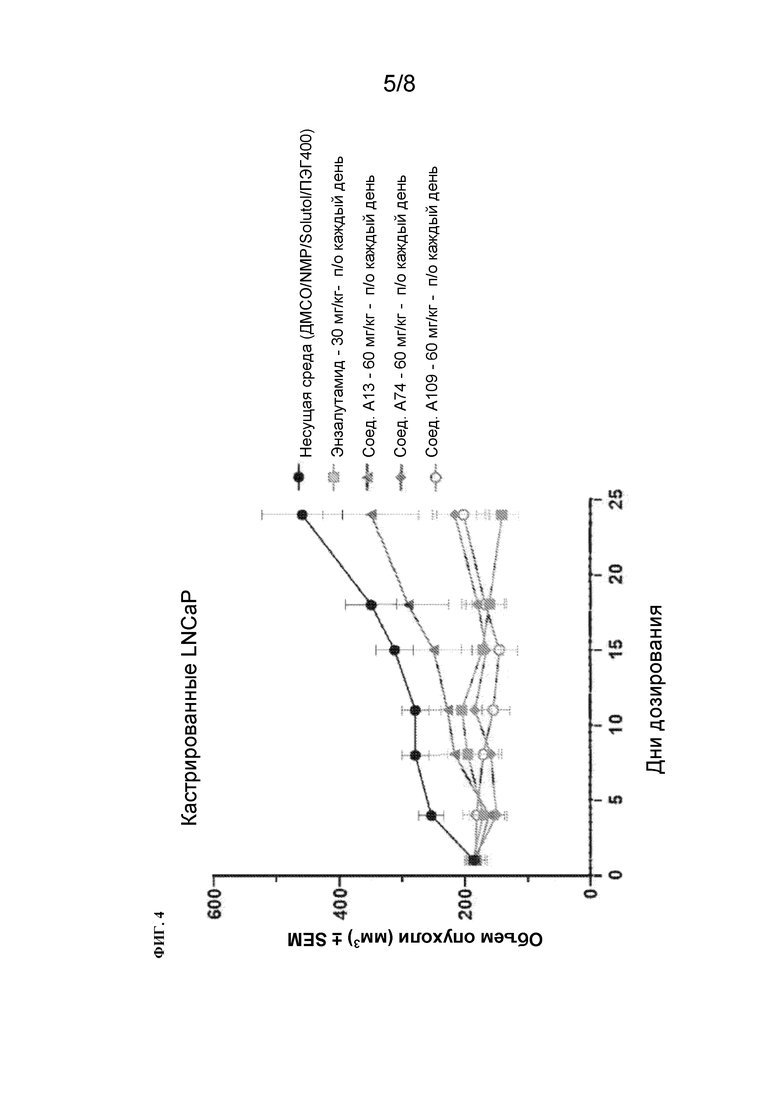
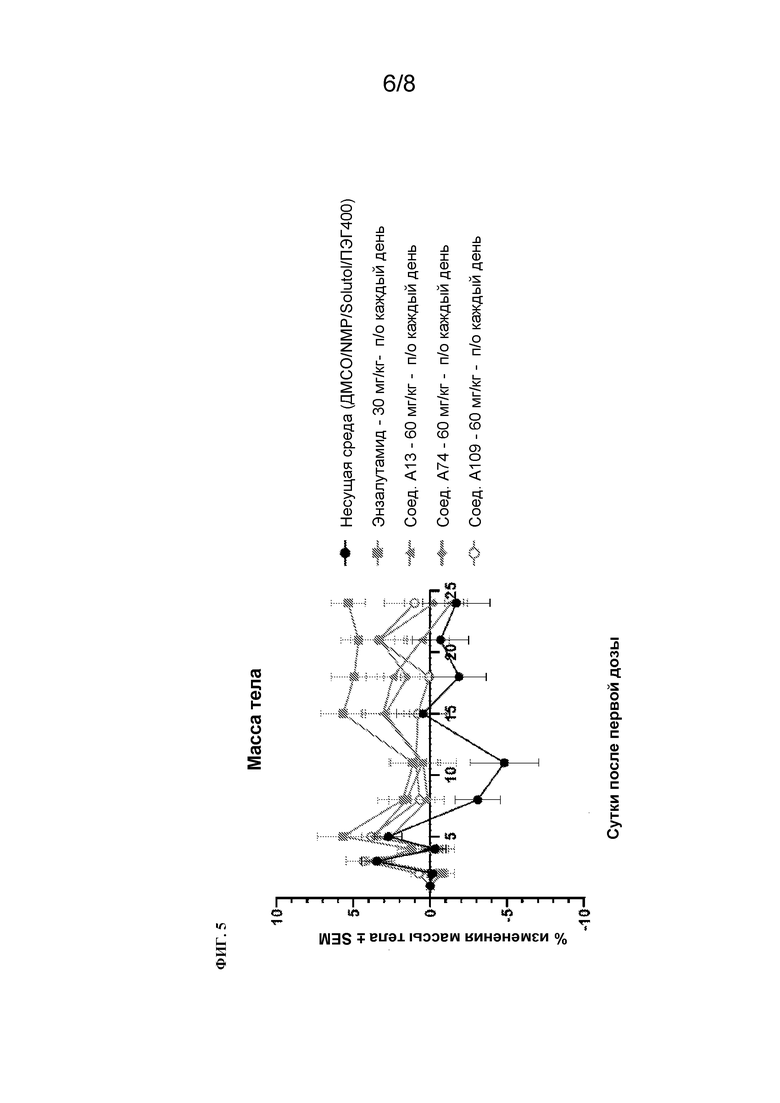
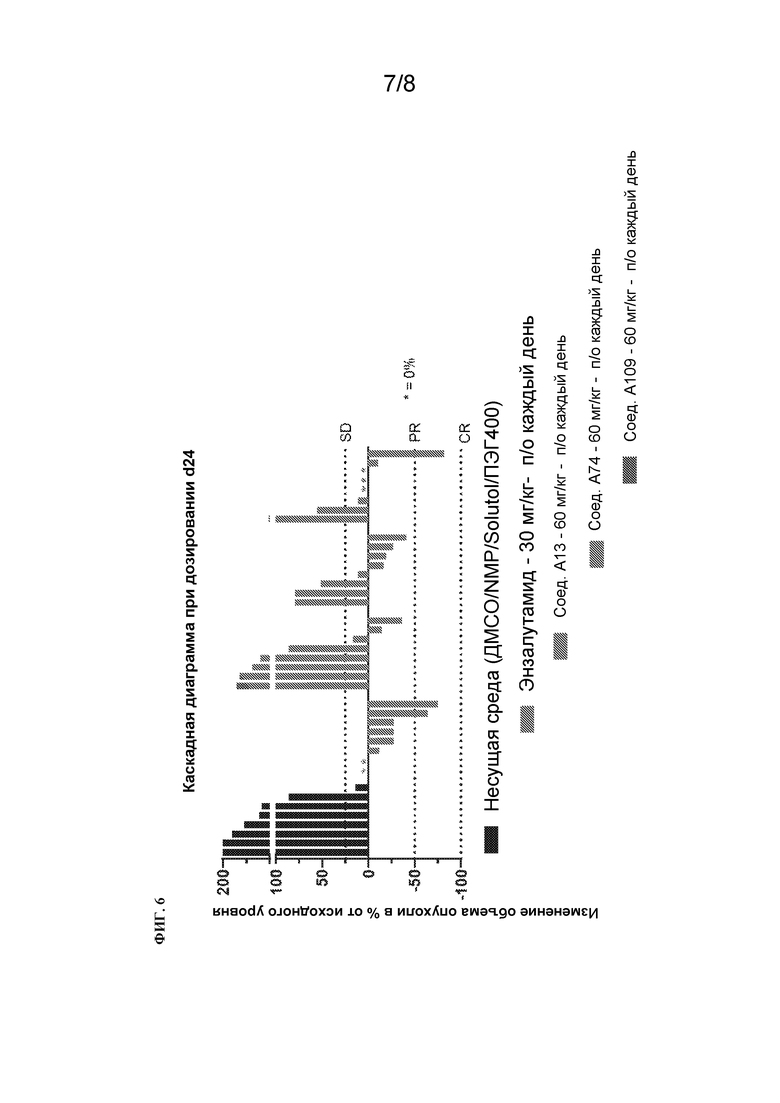
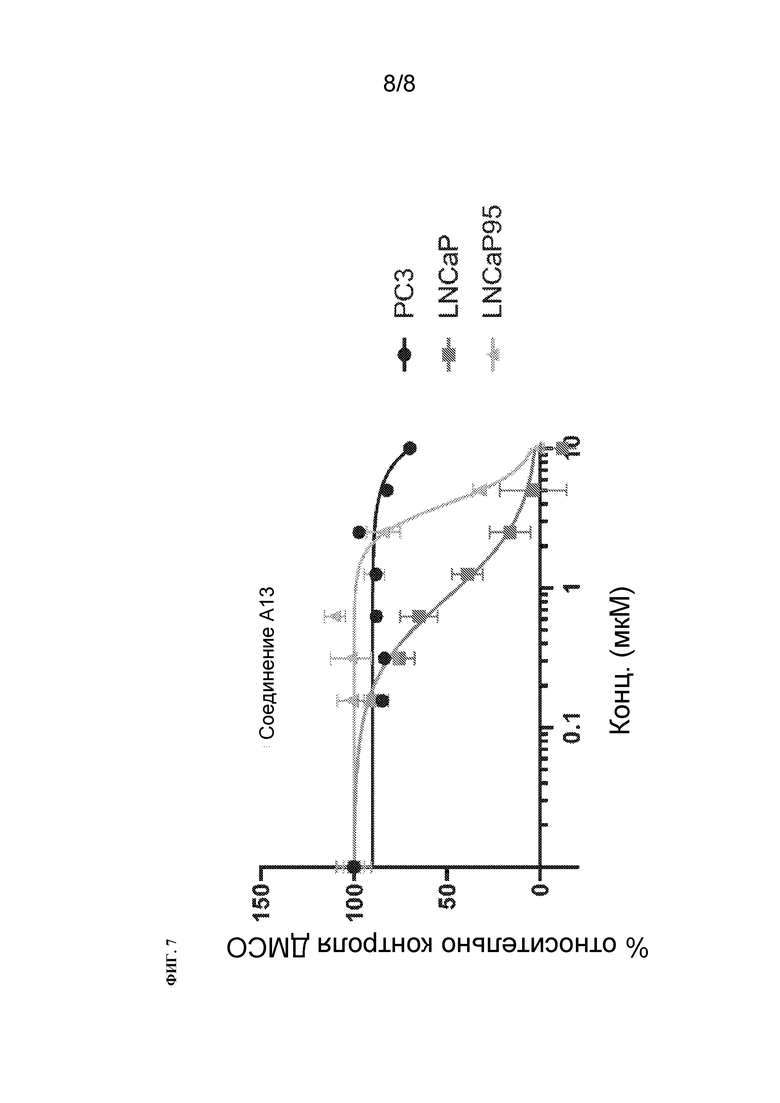
Изобретение относится к соединению, имеющему структуру формулы (A-I), или к его фармацевтически приемлемой соли или стереоизомеру, где C представляет собой 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца; X представляет собой связь, -(CR5R6)t- или -NR7; Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-; Z представляет собой связь, -CH2-, -O- или -NH-; W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-; V представляет собой -CH2- и L представляет собой галоген, -NH2 или -CF3; или V представляет собой -CH2CH2- и L представляет собой галоген или -NH2; R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2; R3 выбран из -CN, C1-C3 алкокси, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила); R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил; R7 представляет собой H или C1-C6 алкил; n1 и n2, каждый независимо, равны 0, 1 или 2; n3 равен 1, 2, 3, 4 или 5; и t равен 0, 1 или 2. Изобретение также относится к фармацевтической композиции, обладающей ингибирующей активностью в отношении андрогенного рецептора (AR), на основе указанного соединения. Технический результат – получены новые соединения и фармацевтическая композиция на их основе, которые могут найти применение в медицине в качестве эффективных средств для лечения рака предстательной железы. 7 н. и 14 з.п. ф-лы, 7 ил., 4 табл., 38 пр.
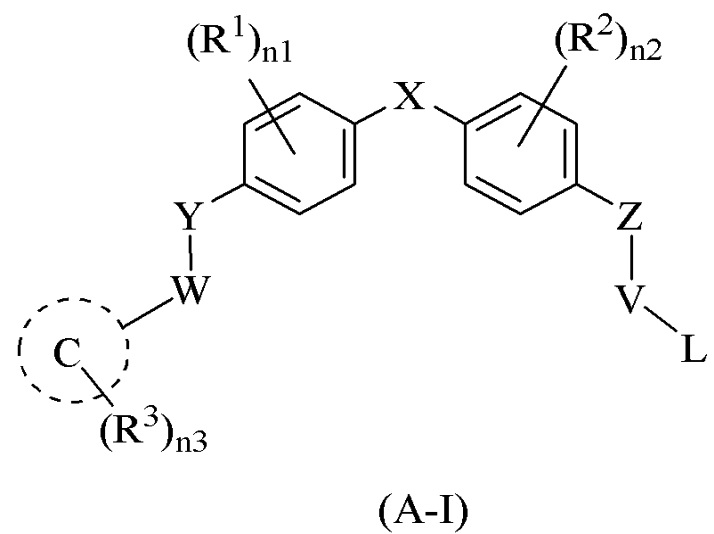
1. Соединение, имеющее структуру формулы (A-I)
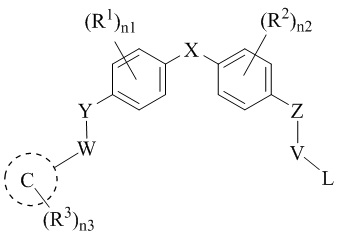
(A-I),
или его фармацевтически приемлемая соль или стереоизомер, где:
C представляет собой 5-7-членный моноциклический гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из O, S или N в качестве члена кольца;
X представляет собой связь, -(CR5R6)t- или -NR7;
Y представляет собой связь, -CH2-, -C(CH3)H-, -O-, -S-, -NH-, -NCH3- или -N(COCH3)-;
Z представляет собой связь, -CH2-, -O- или -NH-;
W представляет собой связь, -CH2-, -C(CH3)H-, -C(=O)-, -N(R7)CO- или -CONR7-;
V представляет собой -CH2- и L представляет собой галоген, -NH2 или -CF3; или
V представляет собой -CH2CH2- и L представляет собой галоген или -NH2;
R1 и R2, каждый независимо, представляют собой водород, галоген, -CN, -CF3, метил или -CONH2;
R3 выбран из -CN, C1-C3 алкокси, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
R5 и R6, каждый независимо, представляют собой водород, галоген, -OH или C1-C3 алкил;
R7 представляет собой H или C1-C6 алкил;
n1 и n2, каждый независимо, равны 0, 1 или 2;
n3 равен 1, 2, 3, 4 или 5; и
t равен 0, 1 или 2.
2. Соединение по п. 1, где C, замещенный (R3)n3, представляет собой пиразол, имидазол, оксазол, оксадиазол, оксазолон, изоксазол, тиазол, пиридил, пиразин, фуран или пиримидил.
3. Соединение по п. 1, где C, замещенный (R3)n3, выбран из
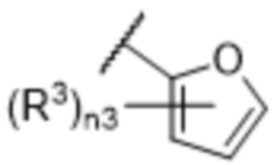 ,
, 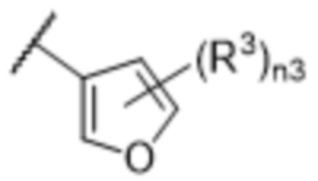 ,
, 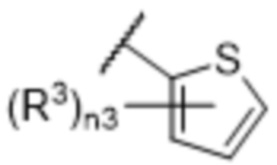 ,
, 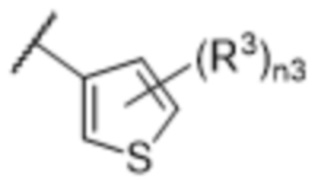 ,
, 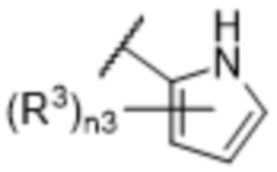 ,
, 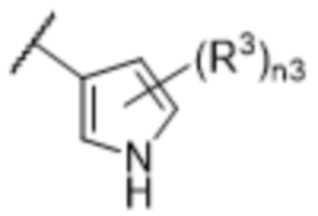 ,
, 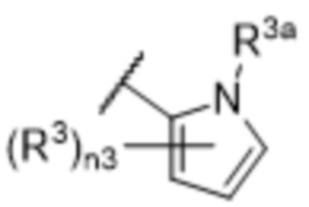 ,
, 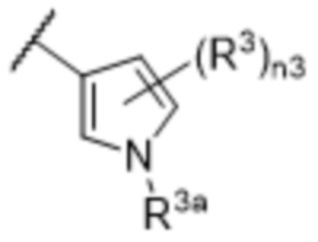 ,
, 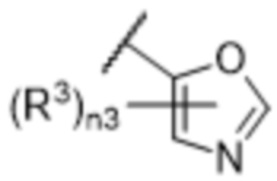 ,
, 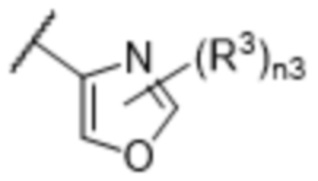 ,
, 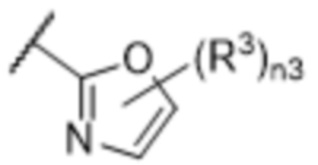 ,
, 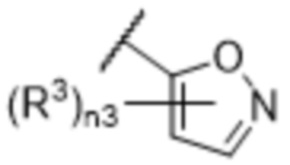 ,
, 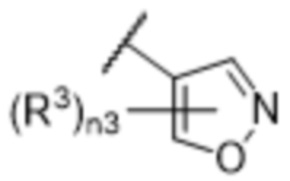 ,
, 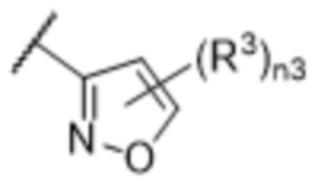 ,
, 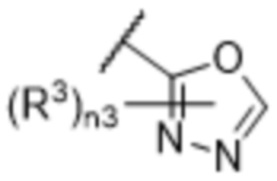 ,
, 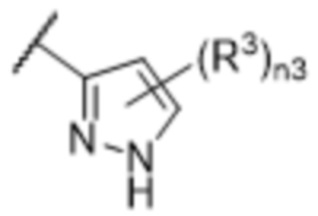 ,
,  ,
, 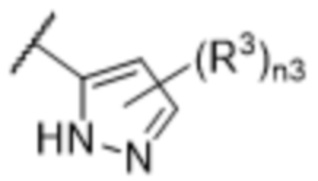 ,
, 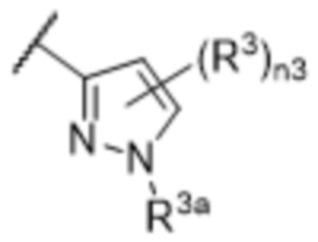 ,
, 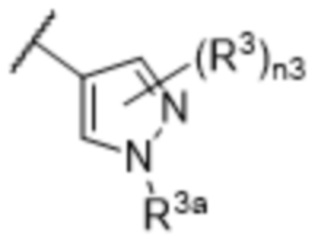 ,
, 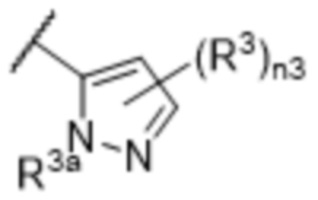 ,
,  ,
, 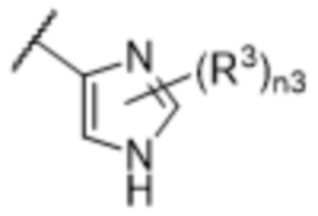 ,
, 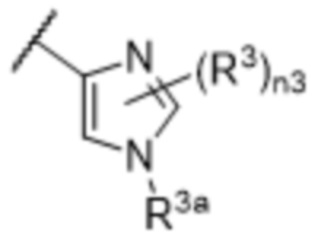 ,
, 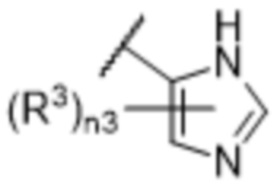 ,
,  ,
, 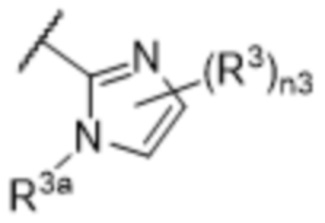 ,
, 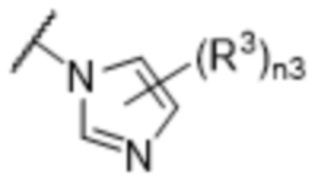 ,
, 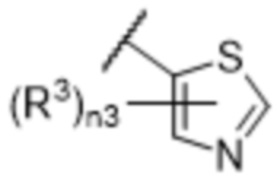 ,
, 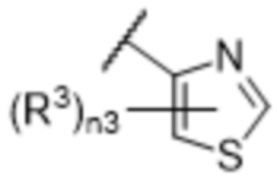 ,
, 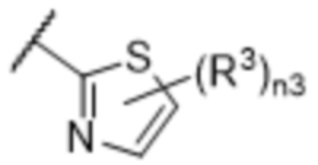 ,
, 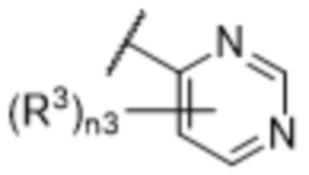 ,
, 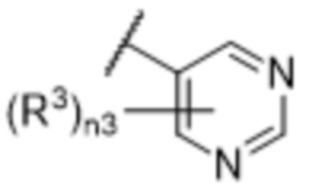 ,
, 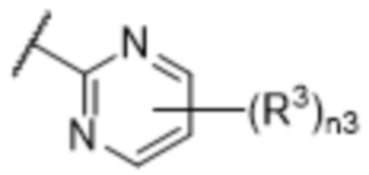 ,
, 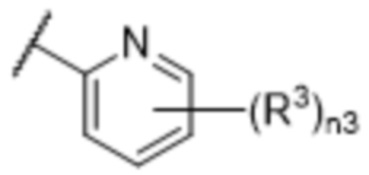 ,
, 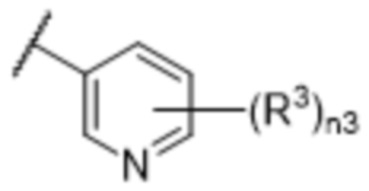 ,
, 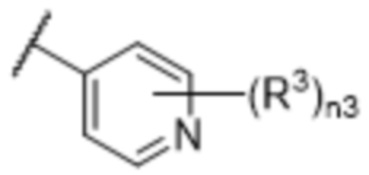 ,
, 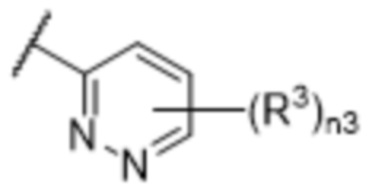 ,
, 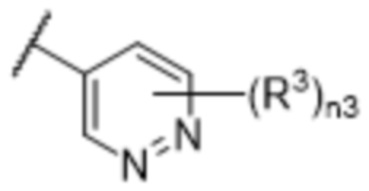 ,
, 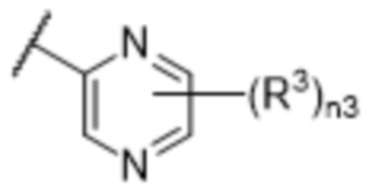 или
или 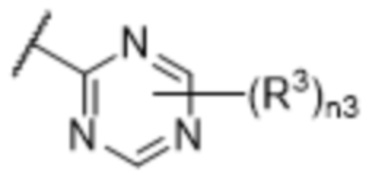 ,
,
где R3a представляет собой C1-C3 алкил; и n3 равен 1 или 2.
4. Соединение по п. 1, где:
X представляет собой -(CR5R6)t-;
каждый Y и Z представляют собой -O-;
V представляет собой -CH2- или -CH2CH2-; и
L представляет собой галоген.
5. Соединение по п. 4, где:
R5 и R6, каждый независимо, представляют собой водород или C1-C3 алкил;
W представляет собой -CH2- или -C(CH3)H-;
V представляет собой -CH2CH2-; и
R1 и R2, каждый независимо, представляют собой водород, галоген или -CN.
6. Соединение по п. 1, где
по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкила)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
7. Соединение по п. 1, где:
X представляет собой связь или -(CR5R6)t;
W представляет собой связь, -CH2- или -C(CH3)H-;
Y представляет собой -O-;
Z представляет собой -O-;
V представляет собой -CH2- или -CH2CH2-; и
L представляет собой галоген.
8. Соединение по п. 1, отличающееся тем, что соединение имеет структуру формулы (G-II)
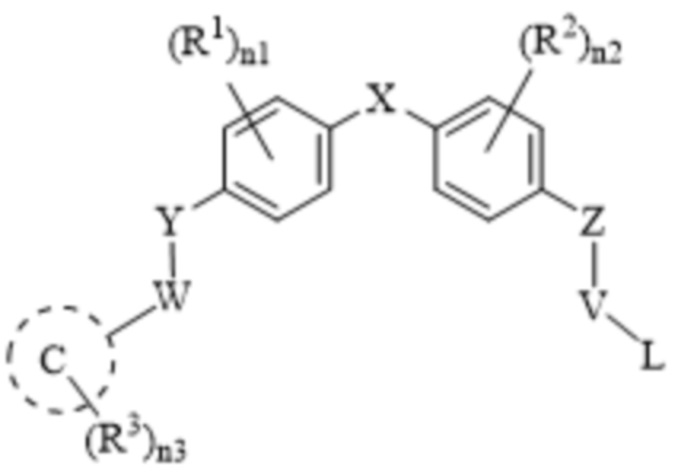
(G-II),
или его фармацевтически приемлемая соль или стереоизомер, где:
C представляет собой  .
. 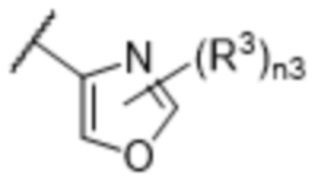 ,
, 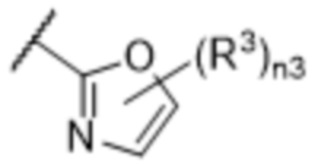 ,
, 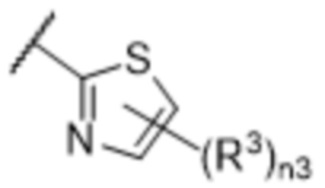 ,
, 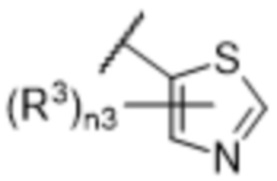 ,
, 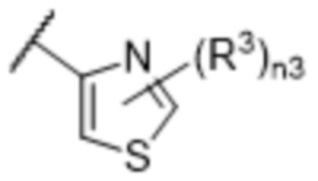 ,
,  ,
,  ,
,  ,
,  ,
, 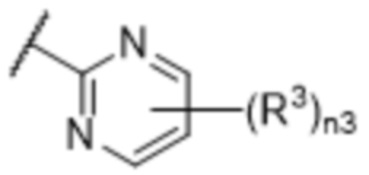 ,
, 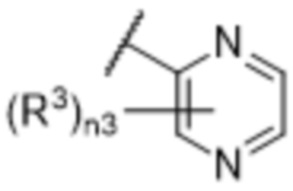 ,
,  ,
,  или
или  ;
;
X представляет собой -(CR5R6)t-;
Y представляет собой -O-;
Z представляет собой -O-;
W представляет собой -CH2- или -C(CH3)H-;
V представляет собой -CH2CH2-;
L представляет собой галоген;
R1 и R2, каждый независимо, представляют собой Cl или -CN;
по меньшей мере один R3 выбран из -CN, C1-C3 алкокси, -CONH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, -CF3, C1-C3 алкила, C2-C3 алкенила, C2-C3 алкинила, C1-C3 алкокси, -S(C1-C3 алкила), -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -NHSO2CF3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -CH2NHSO2CH3, -CH2N(CH3)SO2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила);
R5 и R6, каждый независимо, представляют собой водород или метил;
n1 и n2, каждый независимо, равны 0, 1 или 2;
n3 равно 1 или 2; и
t равно 1.
9. Соединение по п. 8, где
по меньшей мере один R3 выбран из -NHSO2CH3, -NHSO2CH2CH3 или -SO2CH3, а другой R3, если присутствует, выбран из -CN, C1-C3 алкила, C1-C3 алкокси, -SO2(C1-C3 алкила), -NH2, -(C1-C3 алкил)NH2, -NHSO2CH3, -N(CH3)SO2CH3, -NHSO2CH2CH3, -N(CH3)SO2CH2CH3, -SO2NH2, -CONH2, -CON(C1-C3 алкила)2, -CONH(C1-C3 алкила), -NHCO(C1-C3 алкила), -N(CH3)COO(C1-C3 алкила), -NHCOO(C1-C3 алкила) или -N(CH3)COO(C1-C3 алкила).
10. Соединение, выбранное из группы, состоящей из:


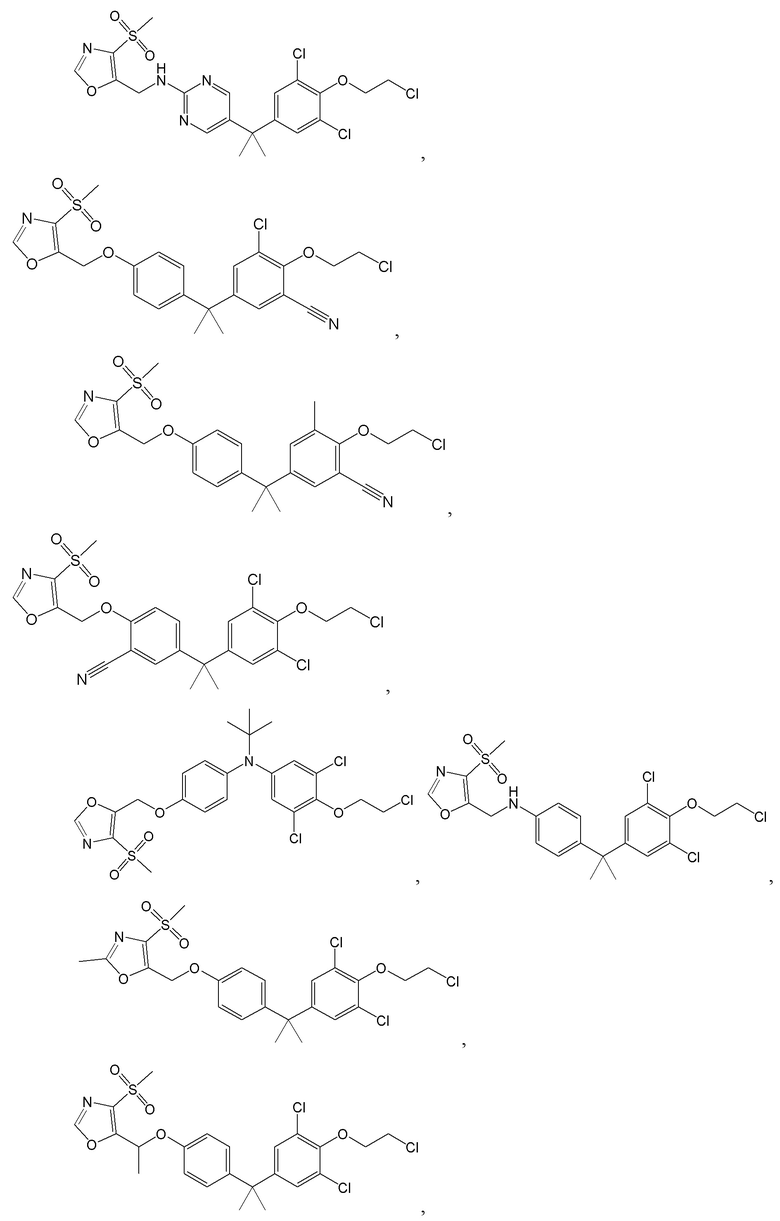
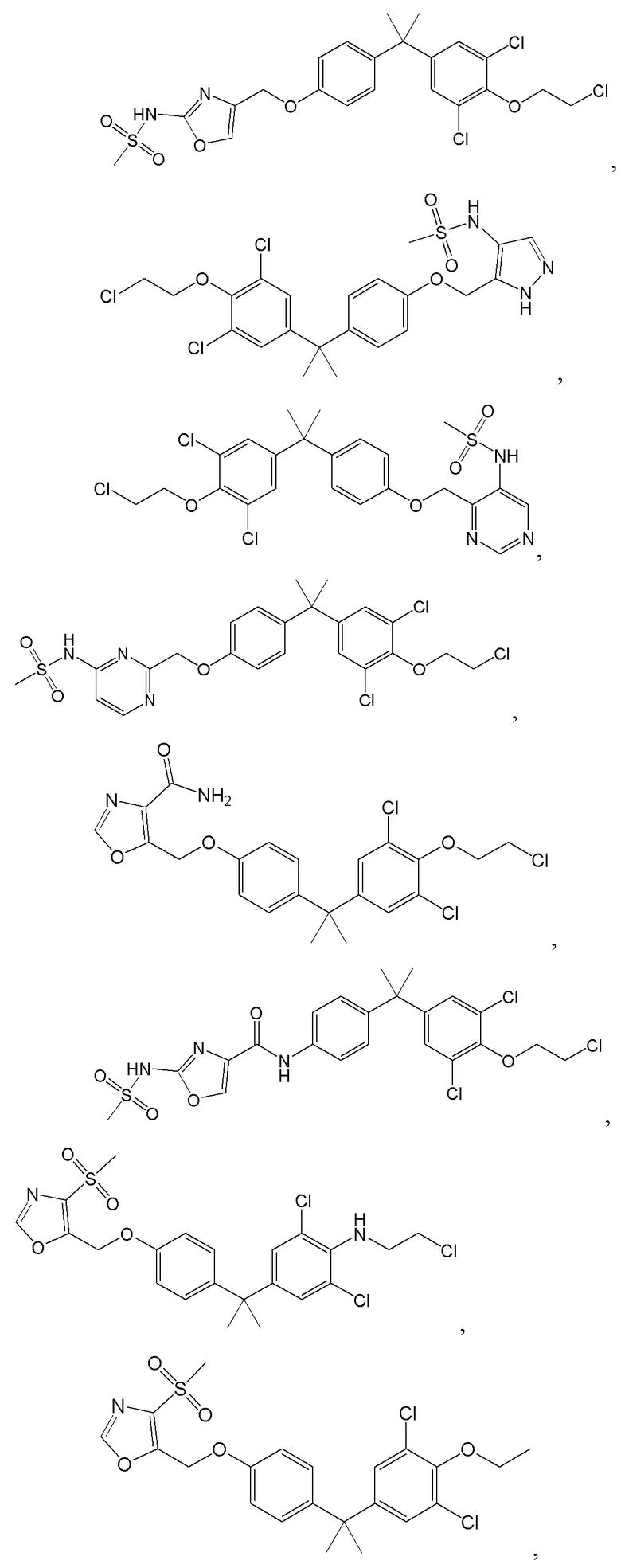
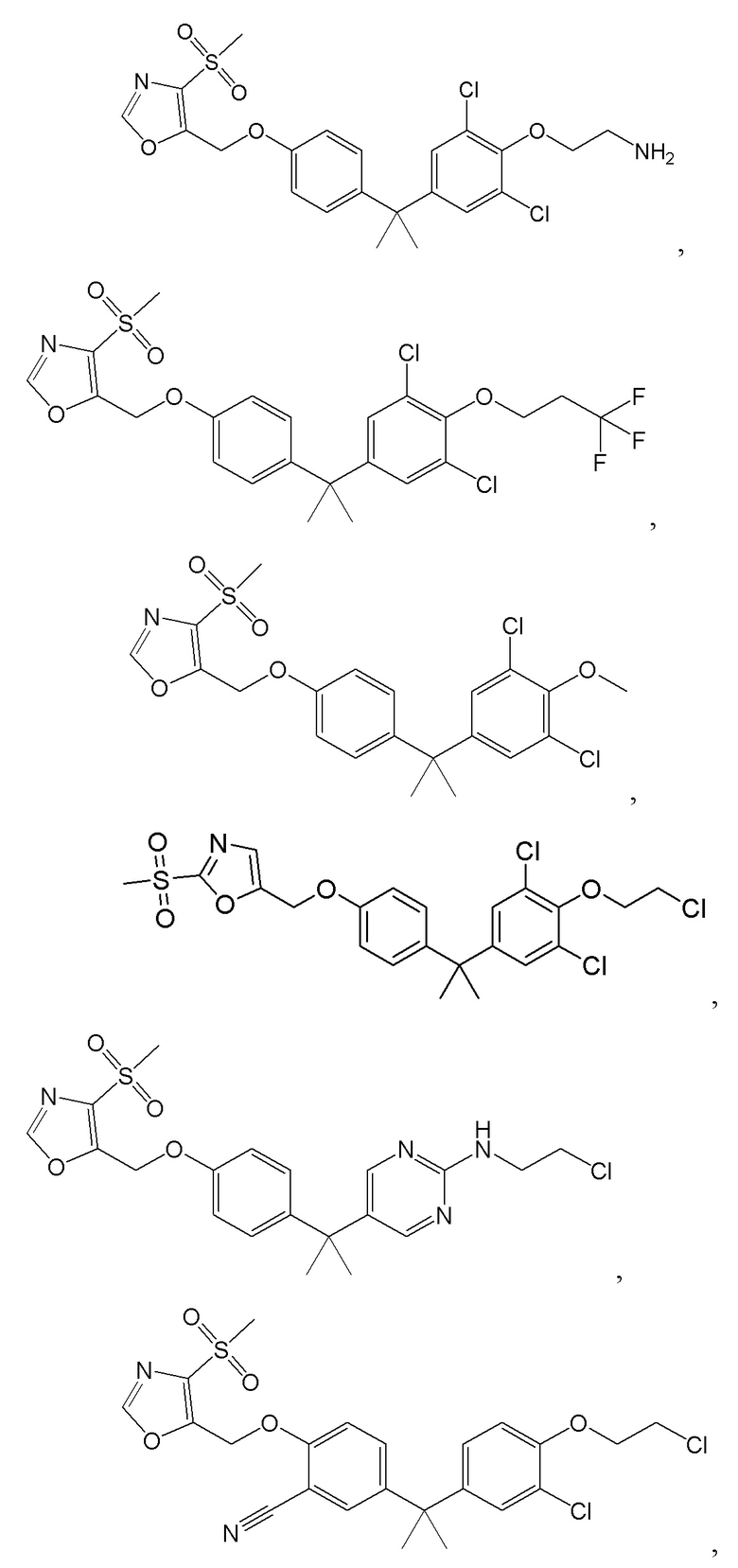
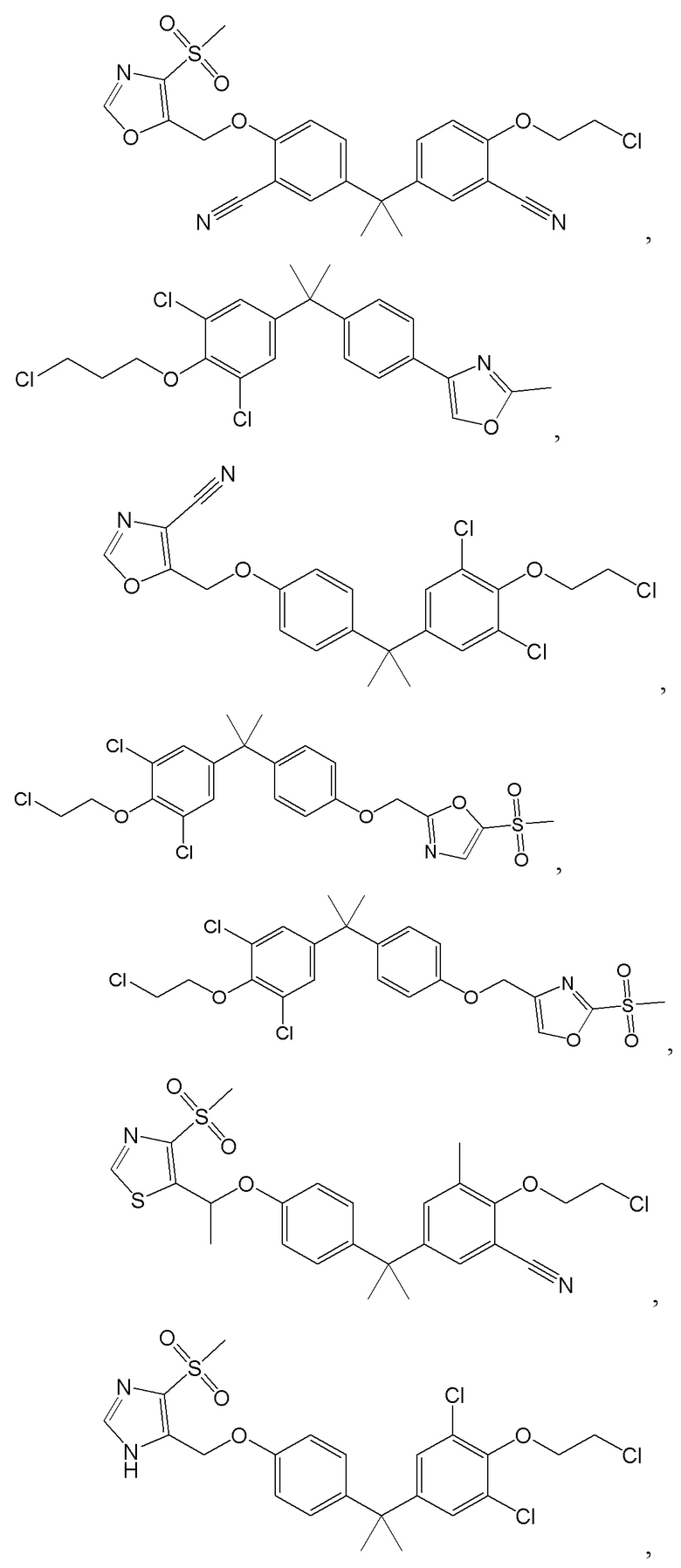
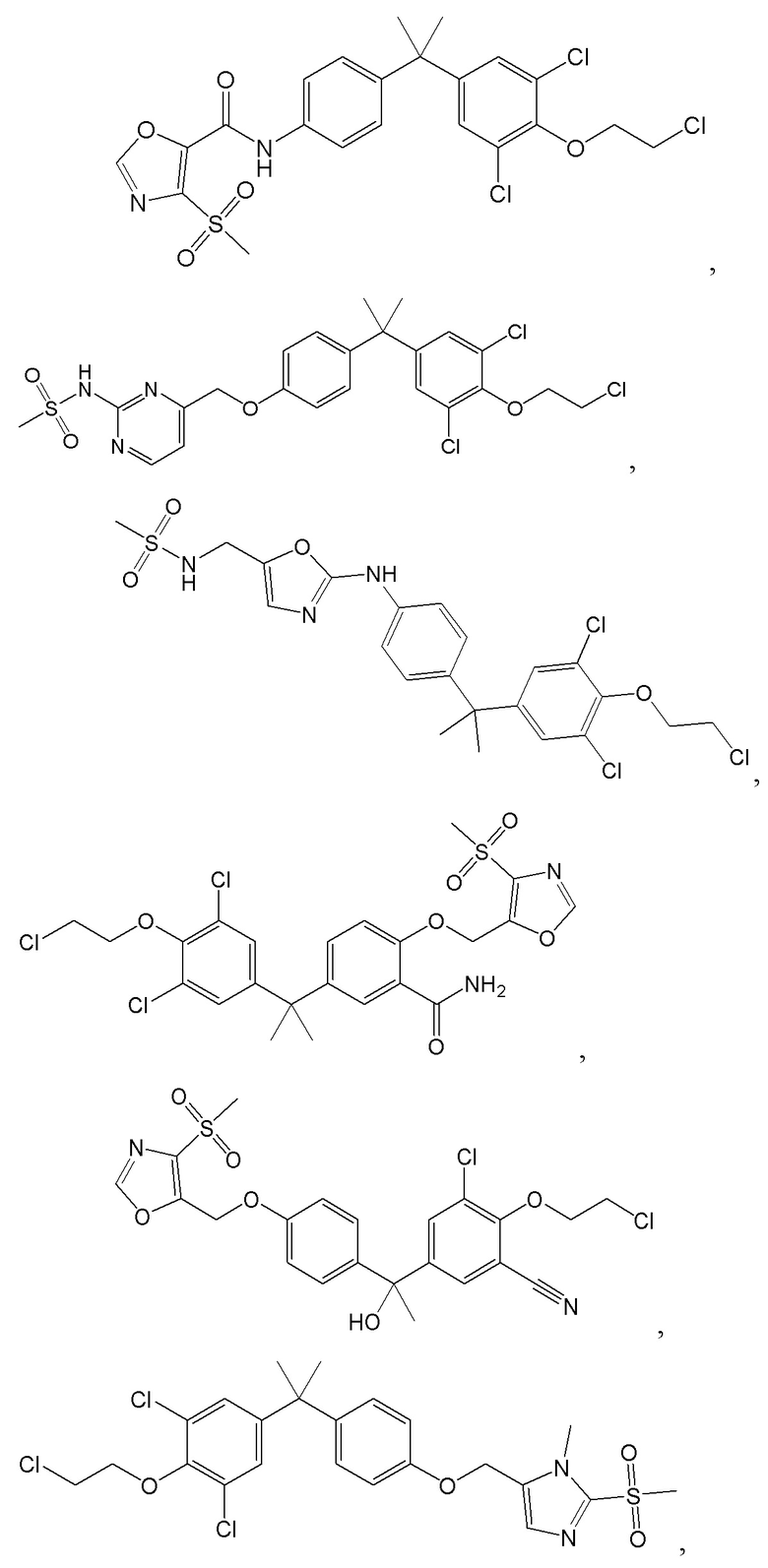
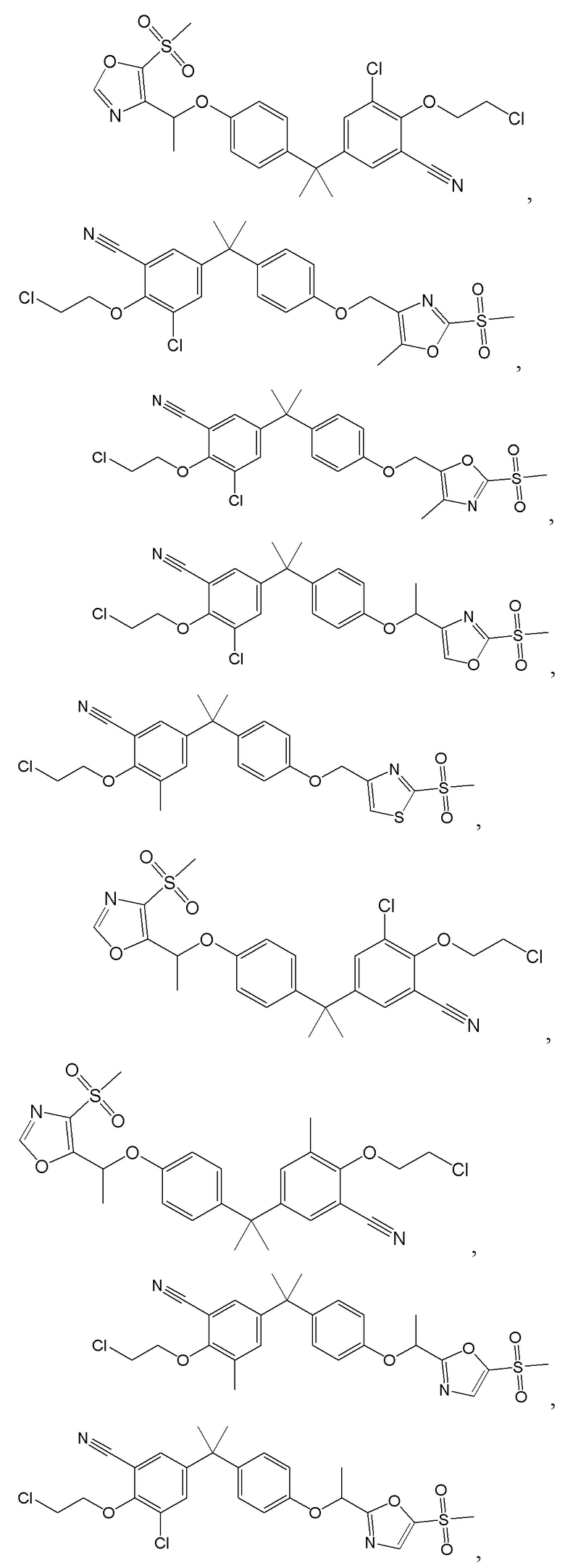

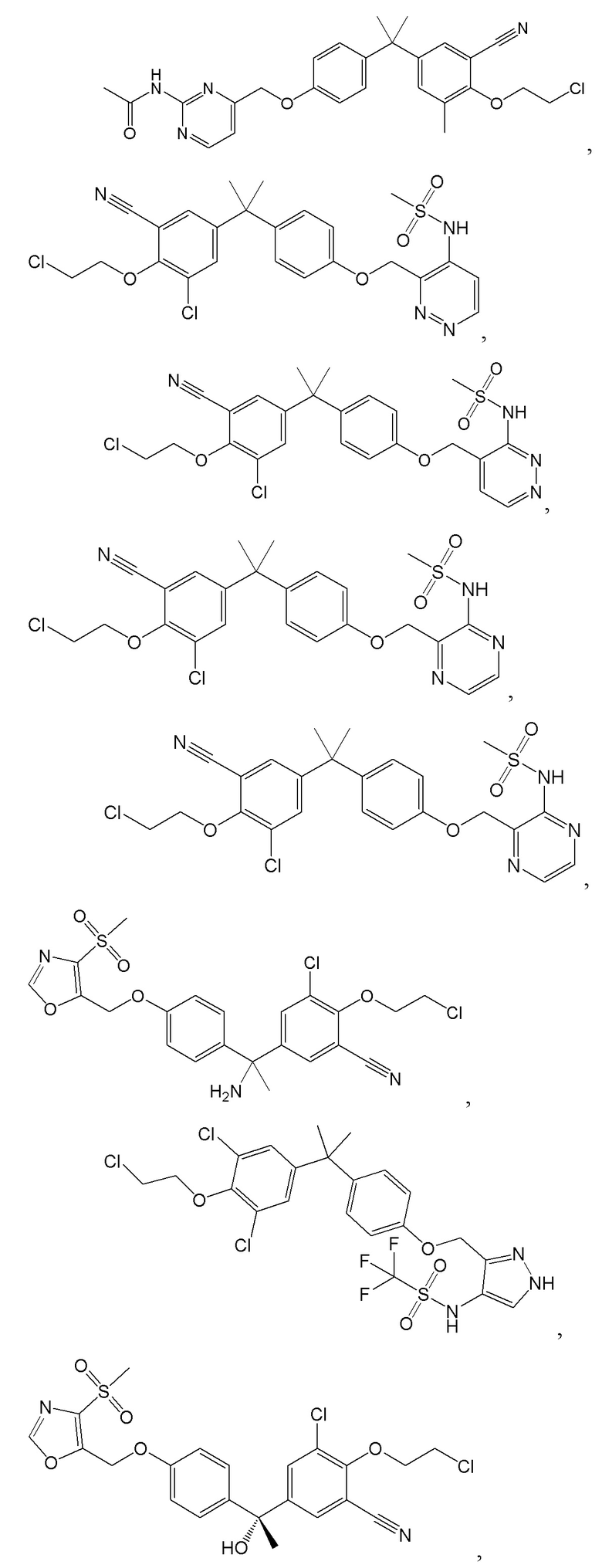

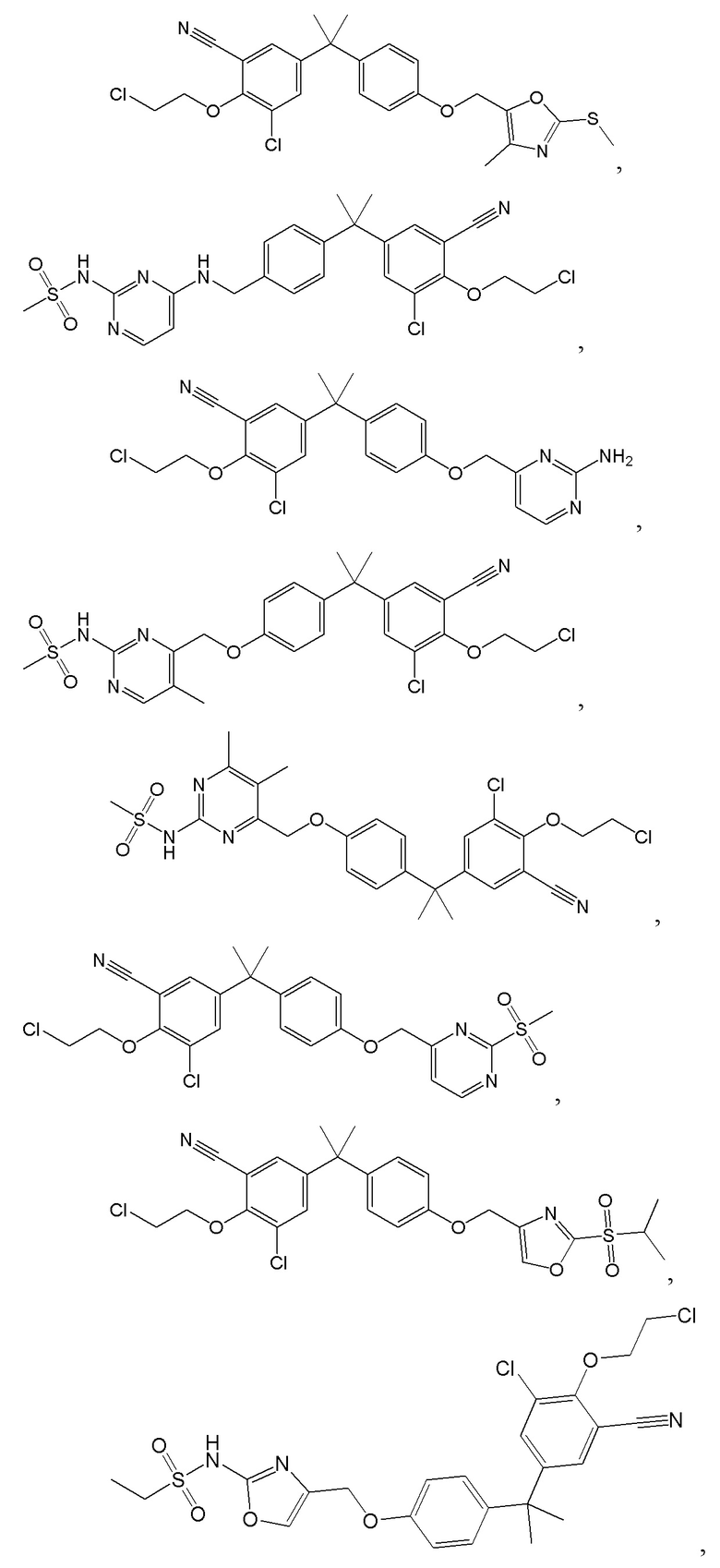
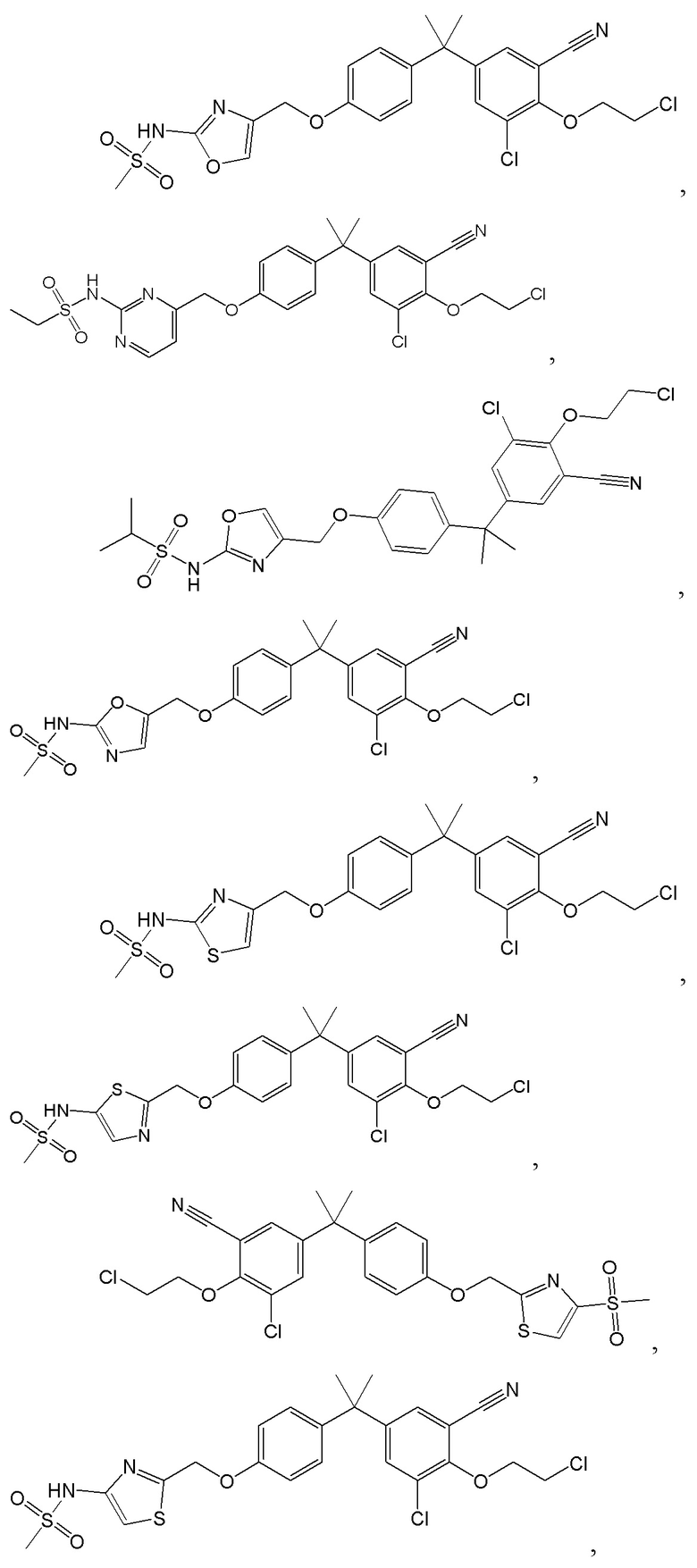
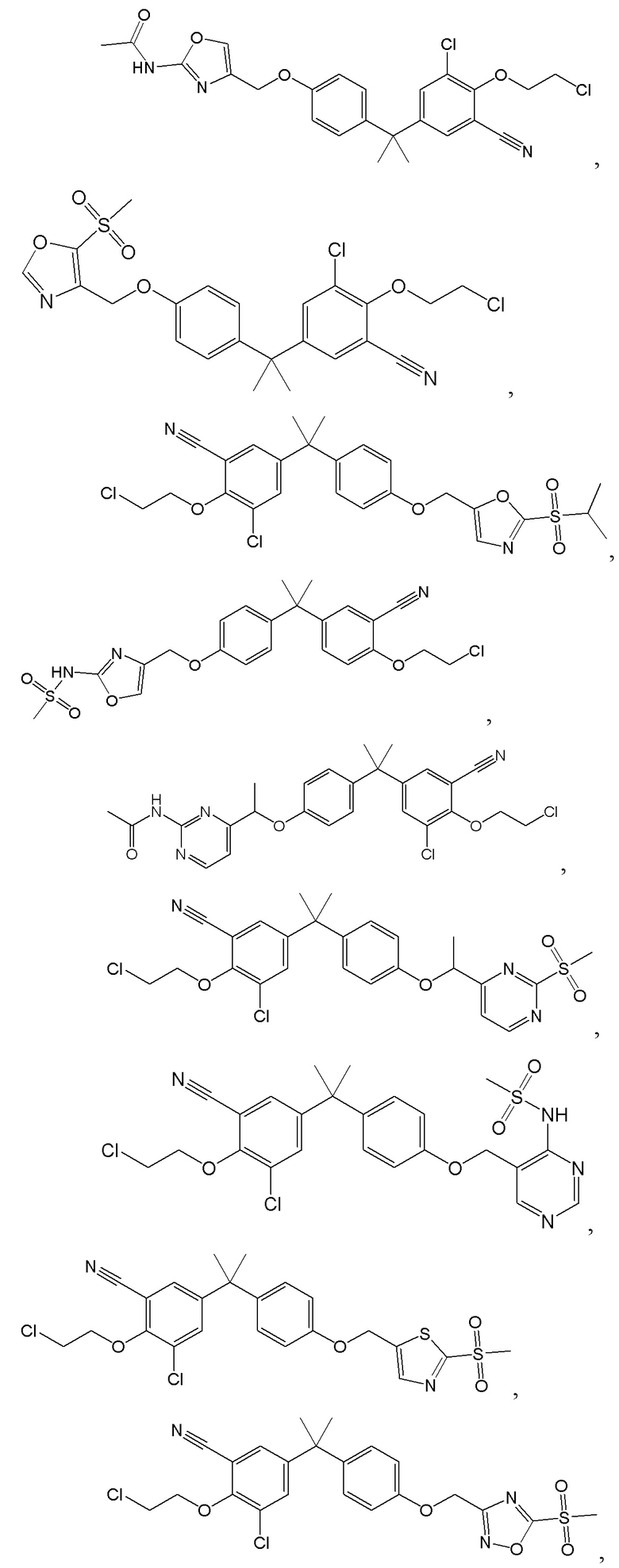
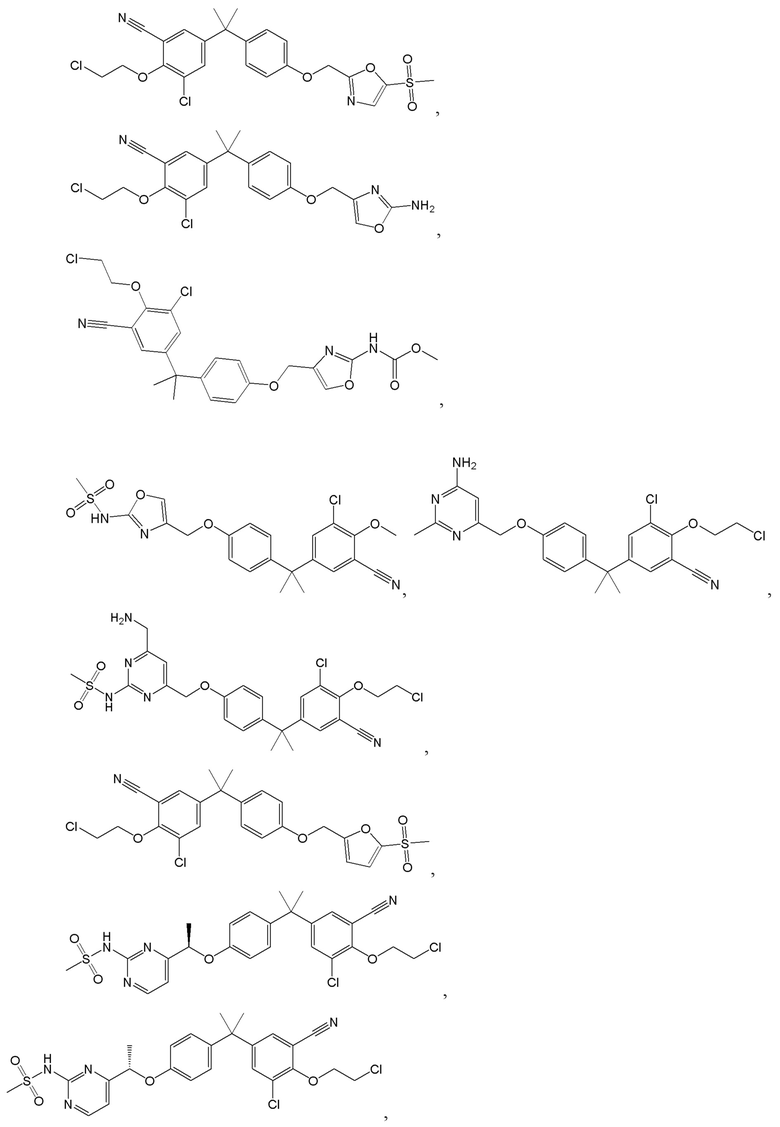
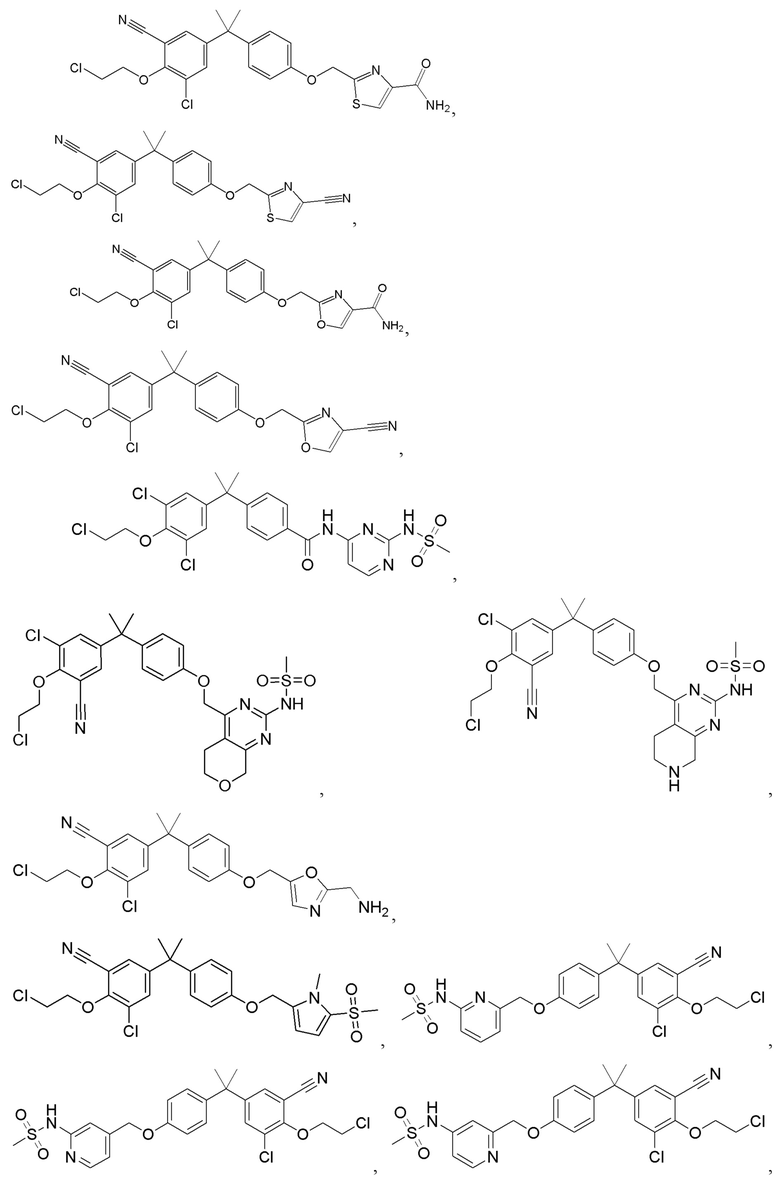

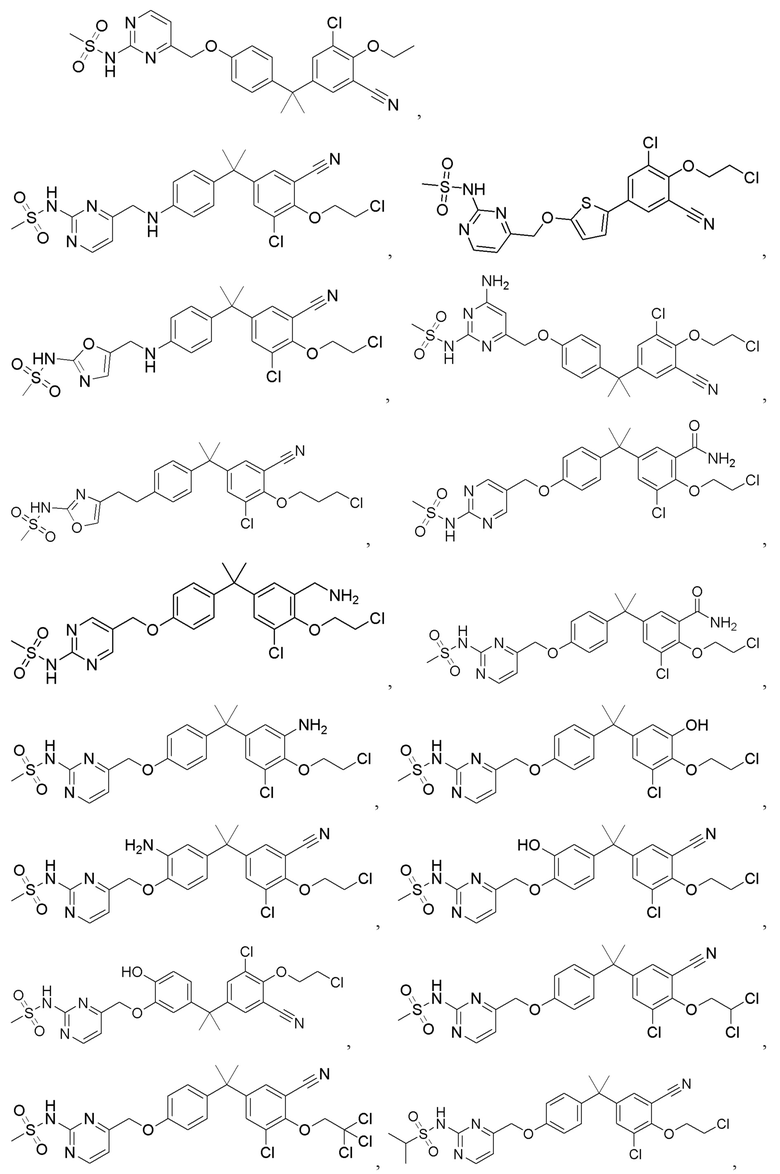
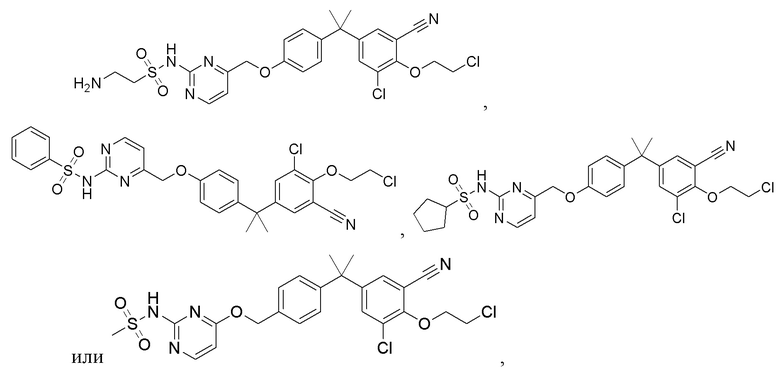
или его фармацевтически приемлемая соль или стереоизомер.
11. Соединение по п. 10, отличающееся тем, что соединение выбрано из:
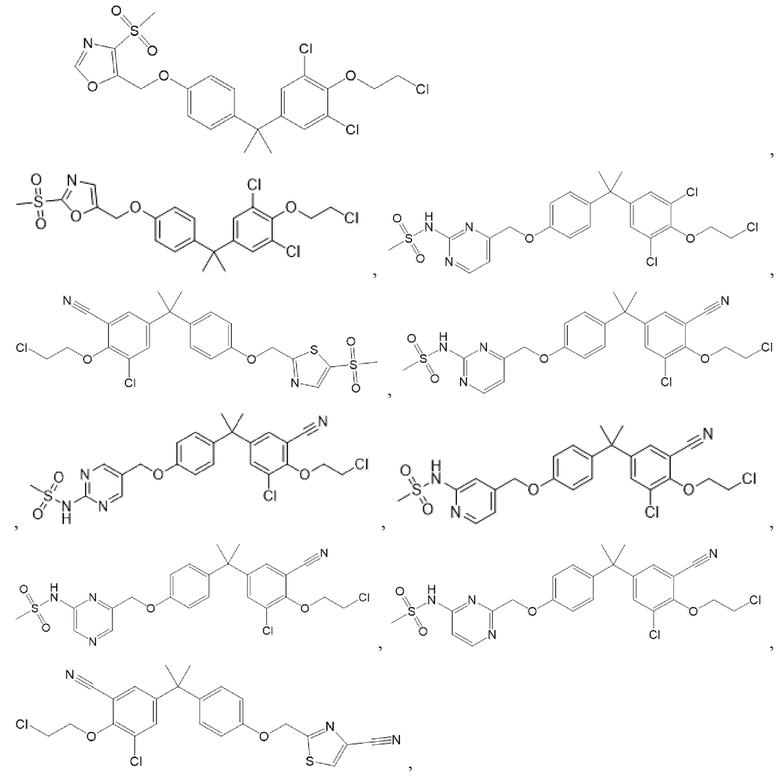
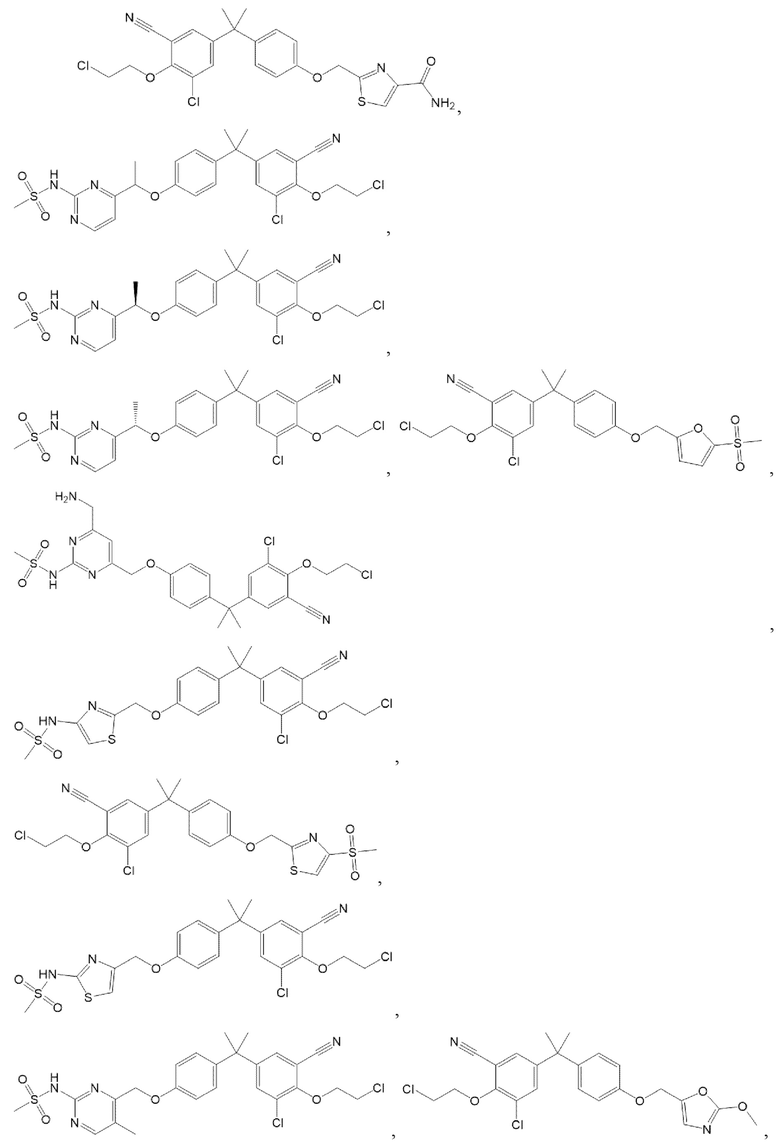
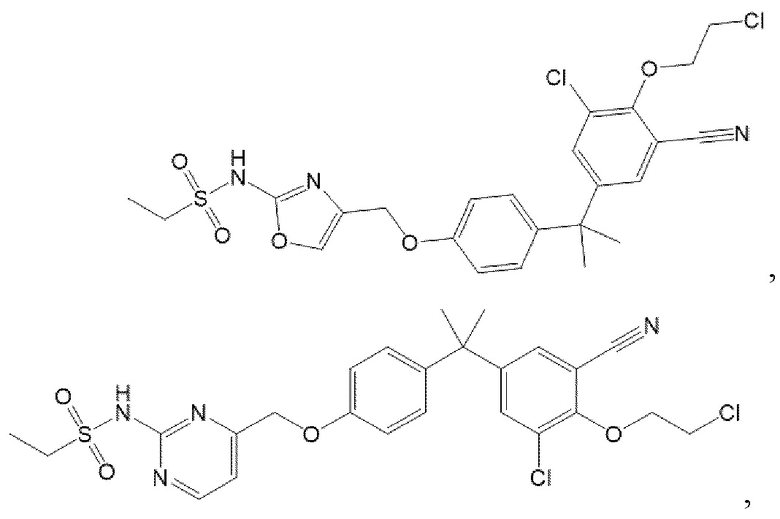
или его фармацевтически приемлемая соль или стереоизомер.
12. Соединение по п.11, представляющее собой
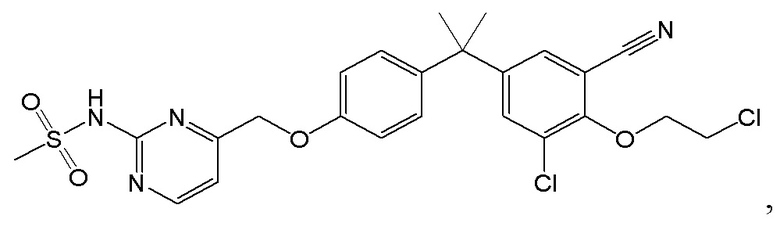
или его фармацевтически приемлемая соль или стереоизомер.
13. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении андрогенного рецептора (AR), содержащая эффективное количество соединения по п. 1 и фармацевтически приемлемый носитель.
14. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении андрогенного рецептора (AR), содержащая эффективное количество соединения по п. 4 и фармацевтически приемлемый носитель.
15. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении андрогенного рецептора (AR), содержащая эффективное количество соединения по п. 10 и фармацевтически приемлемый носитель.
16. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении андрогенного рецептора (AR), содержащая эффективное количество соединения по п. 12 и фармацевтически приемлемый носитель.
17. Способ лечения рака предстательной железы, включающий введение эффективного количества соединения, фармацевтически приемлемой соли или стереоизомера соединения по п. 1 субъекту, нуждающемуся в этом.
18. Способ по п. 17, отличающийся тем, что рак предстательной железы представляет собой метастатический устойчивый к кастрации рак предстательной железы.
19. Способ по п. 17, отличающийся тем, что рак предстательной железы экспрессирует полноразмерный андрогеновый рецептор или усеченный вариант сплайсинга андрогенового рецептора.
20. Способ по п. 17, отличающийся тем, что соединение выбрано из:
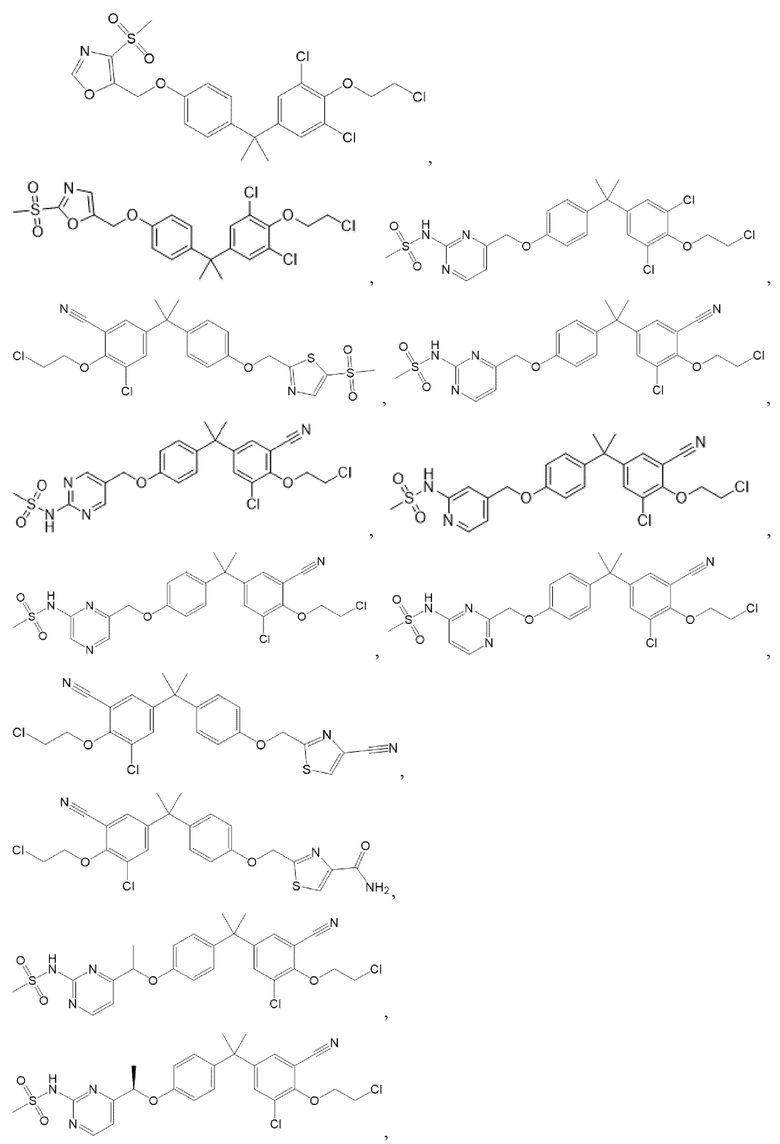
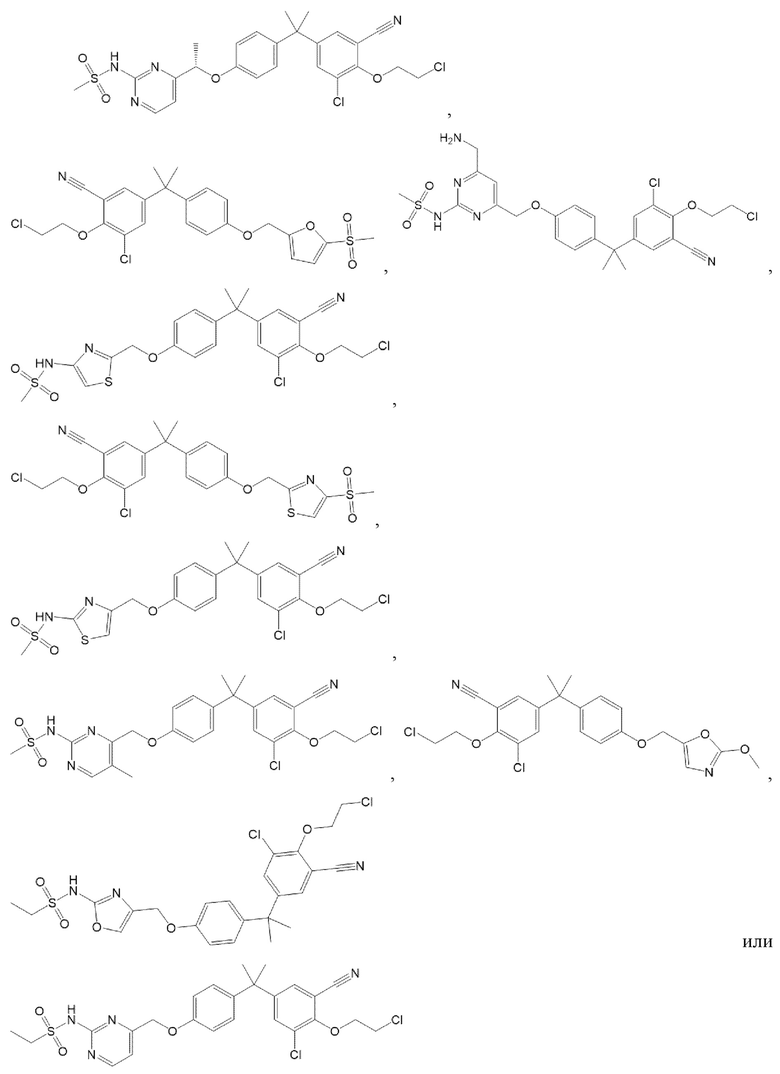
или его фармацевтически приемлемой соли или стереоизомера.
21. Способ по п. 20, где соединение представляет собой 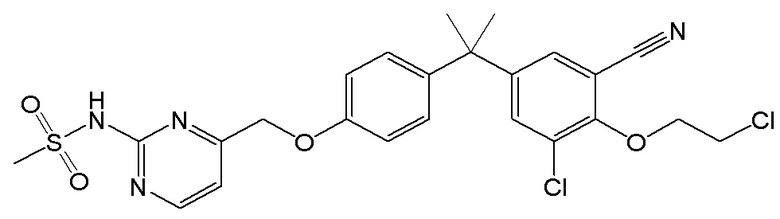 или его фармацевтически приемлемую соль или стереоизомер.
или его фармацевтически приемлемую соль или стереоизомер.
| WO 2016112455 A1, 21.07.2016 | |||
| WO 2012139039 A2, 11.10.2012 | |||
| US 20170298033 A1, 19.10.2017 | |||
| Способ получения резиновой смески | 1927 |
|
SU9199A1 |
Авторы
Даты
2023-06-07—Публикация
2019-10-18—Подача