Перекрестная ссылка на родственную заявку
В данной заявке испрашивается приоритет по предварительной патентной заявке №62/664,917, поданной 30 апреля 2018, которая полностью включена в данное описание посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение, в общем, относится к цеолитам типа шабазита (СНА) с низким содержанием кремния, имеющим высокую долю Al в каркасе цеолита и поэтому высокую кислотность, способу получения СНА-цеолитов с низким содержанием диоксида кремния и способам селективного каталитического восстановления с использованием раскрытых цеолитов.
Уровень техники
Оксиды азота (NOx) издавна известны как загрязняющие газы, главным образом из-за их коррозионного действия. Фактически они являются основной причиной кислотных дождей. Наибольшим источником загрязнения NOx являются их выбросы в выхлопных газах дизельных автомобилей и стационарных источников, таких как угольные электростанции и турбины. Чтобы избежать этих вредных выбросов используют SCR (селективное каталитическое восстановление) на цеолитных катализаторах, применяемых для преобразования NOx в азот и воду.
Таким образом, существует постоянная потребность в улучшенном микропористом кристаллическом материале, который имеет повышенные рабочие характеристики и свойства гидротермальной стабильности, для обеспечения избирательного каталитического восстановления NOx в выхлопных газах.
Алюмосиликатные цеолиты типа СНА являются важные компонентами в коммерческих системах селективного каталитического восстановления (SCR) для снижения выбросов NOx в автомобилях. Вследствие экстремальных условий, которым автомобильные катализаторы SCR подвергаются во время работы, коммерческие СНА-цеолиты должны демонстрировать высокую термическую и гидротермальную стабильность.
В данном документе раскрыты цеолитные материалы и способ получения таких материалов, которые направлены на преодоление одной или нескольких проблем, изложенных выше и/или других проблем предшествующего уровня техники.
Сущность изобретения
Раскрыт материал, который содержит микропористый кристаллический материал, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15 и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более.
Также раскрыт способ селективного каталитического восстановления оксидов азота в выхлопном газе. В варианте осуществления способ содержит по меньшей мере частичное контактирование выхлопных газов с изделием, содержащим микропористый кристаллический материал, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15 и долю Al, которая при определении по адсорбции n-пропиламина составляет 0.63 или более. Этап контактирования можно выполнять в присутствии аммиака, мочевины, соединения, образующего аммиак, или углеводородного соединения.
Также раскрыт способ получения микропористого кристаллического материала, описанного в настоящем документе, например, имеющего молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более. В варианте осуществления способ содержит смешивание источников оксида алюминия, диоксида кремния, щелочного металла, органического структурообразующего агента и воды для образования геля, нагревание геля в автоклаве для образования кристаллического СНА-продукта и кальцинирование указанного СНА-продукта.
Краткое описание чертежей
Прилагаемая фигуры включены в состав описания изобретения и составляют часть этого описания изобретения.
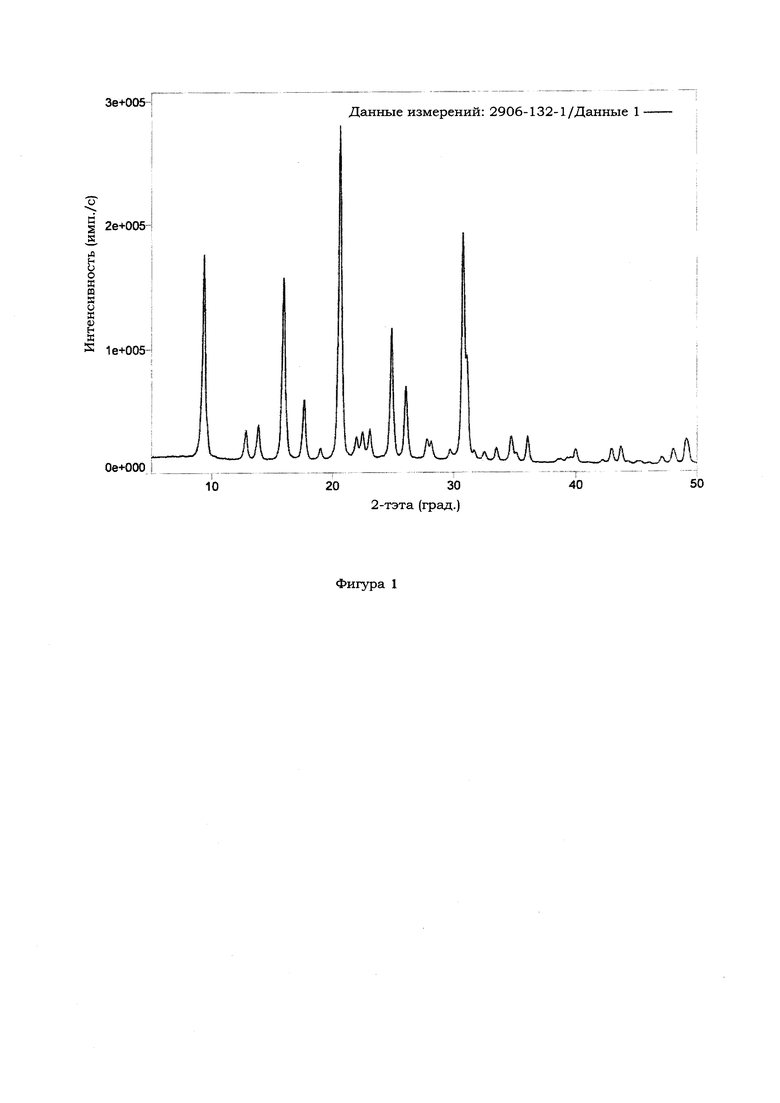
Фиг. 1 - рентгеновская дифрактограмма продукта из заявленного шабазита, полученного в соответствии с Примером 1.
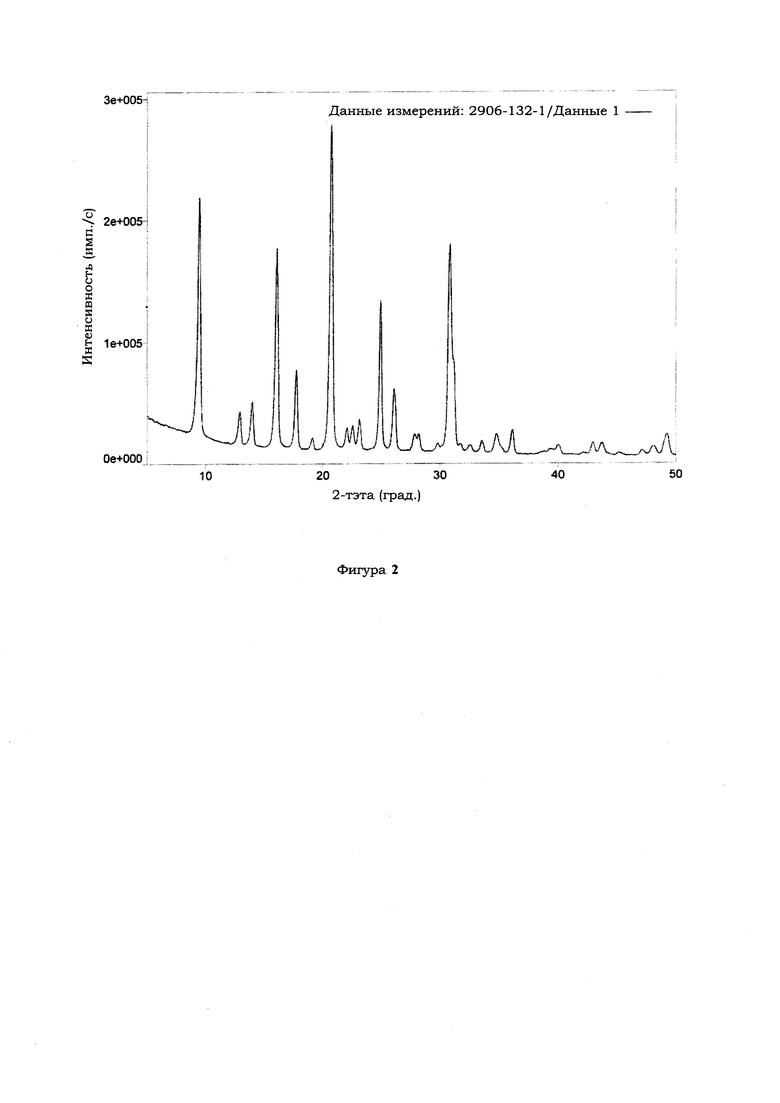
Фиг. 2 - рентгеновская дифрактограмма продукта из заявленного шабазита, полученного в соответствии с Примером 4.
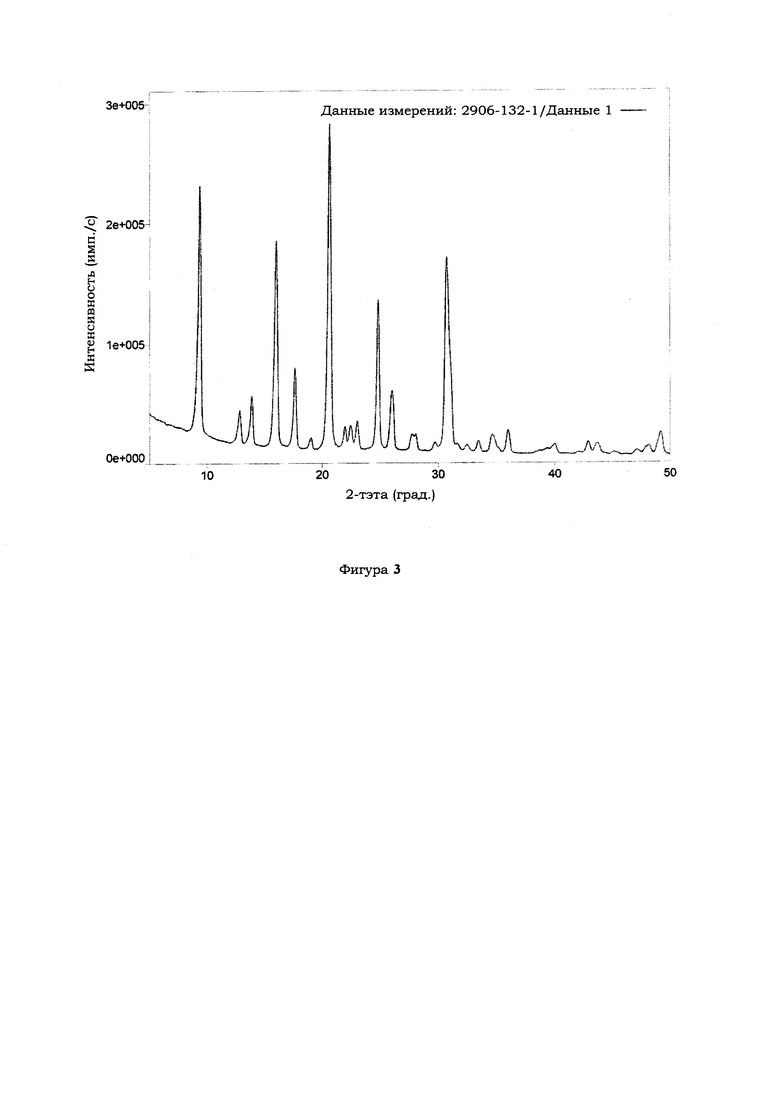
Фиг. 3 - рентгеновская дифрактограмма продукта из заявленного шабазита, полученного в соответствии с Примером 7.
Определения
"Гидротермально стабильный" означает иметь способность сохранять определенный процент исходной площади поверхности и/или объема микропор после воздействия условий повышенной температуры и/или влажности (по сравнению с комнатной температурой) в течение определенного периода времени. Например, в одном варианте осуществления это означает сохранение по меньшей мере 65%, например, по меньшей мере 70%. по меньшей мере 80%, по меньшей мере 90% или даже по меньшей мере 95% площади своей поверхности, объема микропор и интенсивности рентгеновской дифрактограммы (XRD) после воздействия условий, имитирующих условия, присутствующие в выхлопных газах автомобиля, такие как температуры до 800°С, включая температуры в диапазоне от 700°С до 800°С, например, от 775°С до 800°С, в присутствии до 10 объемных процент (об.%) водяного пара в течение времени до 1 часа или даже до 16 часов, например, в течение времени от 1 до 16 часов.
"Исходная площадь поверхности" означает площадь поверхности только что полученного кристаллического материала до воздействия на него каких-либо условий старения.
"Объем микропор" используется для обозначения общего объема пор, имеющих диаметр менее 20 ангстрем. "Исходные объем микропор" означает объем микропор только что полученного кристаллического материала до воздействия на него каких-либо условий старения. Объем микропор, в частности, определяется по методам измерений ВЕТ с использованием способа оценки, называемого способом t-графика (или иногда просто t-способом), описываемым в литературе (Journal of Catalysis 3,32 (1964)).
В данном документе "объем мезопор" означает объем пор, имеющих диаметр от более 20 ангстрем до предела, составляющего 600 ангстрем.
Точно так же "участок микропор" относится к площади поверхности в порах менее 20 ангстрем, а "площадь мезопор" относится к площади поверхности в порах между 20 ангстремами и 600 ангстремами.
"Кислотность" представляет собой число кислотных центров Бренстеда в цеолитном материале, выраженное в ммолях кислотных центров Бренстеда на грамм цеолита. В данном документе число кислотных центров Бренстеда определяется адсорбцией n-пропиламина. Каждый А1. который находится в положении каркаса цеолита, дает начало одному кислотному центру Бренстеда.
"Доля А1 в каркасе цеолита" представляет собой отношение числа кислотных центров Бренстеда, определяемых адсорбцией n-пропиламина, и общего числа А1 в материале, определяемого элементным анализом.
“Кислотный центр Бренстеда" - это элемент, с которым связан атом водорода, который соединение должно содержать, чтобы в какой-либо реакции оно проявило свойство кислоты. Кислоты Бренстеда - это соединения, способные отдавать протон (доноры протона). В более общем смысле, кислотный центр Бренстеда в относится к определенному участку или месту в материале или молекуле, которые могут отдавать протон (Н+) другим соединениям.
“Элементный анализ’" - качественное обнаружение и количественное определение содержания элементов и элементного состава веществ, материалов и различных объектов с помощью различных видов спектрометрии.
"Определены структурной комиссией Международной ассоциации цеолитов" означает структуры, которые включены, но не ограничиваются ими, в структуры, описанные в "Атласе типов цеолитных каркасов", изд. Baerlocher и др. Шестое пересмотренное издание (Elsevier 2007), которое полностью включено в настоящий документ посредством ссылки.
"Двойные 6-членные кольца (d6r)" представляют собой структурообразующею единицу, описываемую в "Атласе типов каркасов цеолитов", изд. Baerlocher и др. Шестое Переработанное и исправленное издание (Elsevier 2007), которая полностью включена в настоящий документ посредством ссылки.
"Селективное каталитическое восстановление" или "SCR" относится к восстановление NOx (как правило, с помощью мочевины и/или аммиака) в присутствии кислорода для образования азот и H2O.
"Выхлопной газ" относится к любому отработавшему газу, образующемуся в процессе промышленного производства или промышленной эксплуатации и в двигателях внутреннего сгорания, например, от любого вида автомобиля.
Используемая в данном документе фраза "выбранный из" относится к выбору отдельных компонентов или комбинации двух (или более) компонентов. Например, описываемый в данном документе каталитически активный металл может быть выбран из меди и железа, что означает, что металл может включать медь или железо или комбинацию меди и железа.
Заявителями был обнаружен полезный микропористый кристаллический материал, имеющий высокую кислотность, например, более 1,35, и низкое количество диоксида кремния, например, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15. например, 10-14 или 12-14 или даже 13-14. Раскрытые материалы особенно полезны для селективного каталитического восстановления оксидов азота.
Полезный диапазон кислотности определяется и. следовательно, является функцией общего содержания Al. Например, при SAR в диапазоне 13-14 кислотность, как правило, составляет от 1,35 до 1,8 ммоль/г. например от 1,40 до 1,75 ммоль/г или от 1,50 до 1,70 ммоль/г. В частности, для материала, имеющего SAR в диапазоне 10-15, кислотность, как правило, находится в диапазоне 1,35-2,0 ммоль/г, например от 1,40 ммоль/г до 2,0 ммоль/г, или от 1,50 ммоль/г до 2,0 ммоль/г, или от 1,60 ммоль/г до 2,0 ммоль/г, или от 1,70 ммоль/г до 2,0 ммоль/г, или даже от 1,80 ммоль/г до 2,0 ммоль/г.
Полезные диапазоны для доли Al в каркасе цеолита составляют 0,63 или более, например от 0,63 до 1,00, или от 0.65 до 1,00, или от 0,70 до 1.00.
В варианте осуществления микропористый кристаллический материал может содержать кристаллическую структуру, имеющую структурный код СНА (шабазит).
В варианте осуществления микропористый кристаллический материал может дополнительно включать по меньшей мере один каталитически активный металл, такой как медь или железо. В варианте осуществления каталитически активный металл включает медь (Cu), которая присутствует в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25.
В варианте осуществления, микропористый кристаллический материал, описываемый в данном документе, содержит крупнокристаллический материал, такой как материал, имеющий при определении с помощью SEM-анализа (анализа с использованием электронного растрового микроскопа) средний размер кристаллов в диапазоне от 0,5 мкм до 5 мкм.
В варианте осуществления раскрывается микропористый кристаллический материал, имеющий СНА-структуру с молярным отношением диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, например 12-14, и долю Al, которая при определении по адсорбции n-пропиламина составляет 0,63 или более, например от 0,63 до 1,0 или даже от 0,65 до 1,0. Кислотность материала, полученного в соответствии с этим вариантом осуществления, как правило, составляет от 1.35 ммоль/г до 1.8 ммоль/г. Микропористый кристаллический материал этого варианта осуществления дополнительно включает по меньшей мере один каталитически активный металл, при этом медь или железо являются необязательными металлами. Когда каталитически активный металл содержит медь (Cu), она должен присутствовать в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25. Кроме того, желательно, чтобы микропористый кристаллический материал СНА этого варианта осуществления имел средний размер кристаллов в диапазоне от 0,5 мкм до 5 мкм.
Также раскрыт способ селективного каталитического восстановления оксидов азота в выхлопном газе. В варианте осуществления способ содержит по меньшей мере частичное контактирование выхлопных газов с изделием, содержащим микропористый кристаллический материал, описываемый в данном документе. Например, раскрытый способ SCR содержит по меньшей мере частичное контактирование выхлопных газов с изделием, содержащим микропористый кристаллический материал имеющий СНА-структуру, молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, такое как 12-14, и долю Al, которая при определении по адсорбции n-пропиламина составляет 0.63 или более, например от 0,63 до 1,0 или даже от 0.65 до до 1,0. Кислотность материала, используемого в этом способе, как правило, варьируется от 1,35 ммоль/г до 1,8 ммоль/г. СНА-материалы, используемые в этом способе SCR, дополнительно включают по меньшей мере один каталитически активный металл, причем медь или железо являются необязательными металлами. Когда каталитически активный металл включает медь (Cu), она должен присутствовать в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25. Кроме того, желательно, чтобы микропористый кристаллический материал СНА этого варианта осуществления имел средний размер кристаллов в диапазоне от 0,5 мкм до 5 мкм.
Этап контактирования этого способа SCR, как правило, выполняют в присутствии аммиака, мочевины, соединения, образующего аммиак, или углеводородного соединения.
Также раскрыт способ получения микропористого кристаллического материала, описываемого в данном документе. В варианте осуществления способ содержит смешивание источников оксида алюминия, диоксида кремния, щелочесодержащей добавки, органического структурообразующего агента и воды для образования геля. Способ, дополнительно содержит нагревание геля в автоклаве для образования кристаллического СНА-продукта и кальцинирование указанного СНА-продукта.
В варианте осуществления способ, дополнительно содержит введение по меньшей мере одного каталитически активного металла, такого как медь или железо, в микропористый кристаллический материал посредством жидкофазного или твердофазного ионного обмена, пропитки, прямого синтеза или их комбинации.
В варианте осуществления каталитически активный металл включает медь (Cu), которая присутствует в атомном соотношении Cu:Al, составляющем более 0,24, например, по меньшей мере 0,25.
Способ, описываемый в данном документе, использует органический структурообразующий агент для образования получаемого цеолитного материала. В варианте осуществления органический структурообразующий агент содержит гидроксид N,N,N-триметил-1-адамантиламмония.
В варианте осуществления щелочесодержащая добавка содержит источник калия или натрия или смесь натрия и калия. Примеры включают в себя, соответственно, гидроксид калия, алюминат калия, гидроксид натрия и алюминат натрия.
В варианте осуществления источники алюминия включают в себя, но не ограничиваются ими: алюминат натрия, соли алюминия, гидроксид алюминия, алюминийсодержащие цеолиты, алкоксиды алюминия или оксид алюминия. Источники диоксида кремния могут включать в себя, но не ограничиваются ими, силикат натрия, силикат калия, силикагель, золь диоксида кремния, коллоидальный диоксид кремния, диоксид кремния, оксид алюминия, цеолиты, алкоксиды кремния или осажденный диоксид кремния.
В варианте осуществления гель нагревают в автоклаве при температуре в диапазоне от 120°С до 200°С в течение 1-100 часов, например, при 180°С в течение 48 часов. Гель можно перемешивать со скоростью 150 об/мин. Способ может дополнительно содержать фильтрацию геля для образования твердого продукта, промывание твердого продукта денонсированной водой, сушку промытого продукта, кальцинирование высушенного продукта и аммонийный обмен в кальцинированном продукте.
Методы измерений
Измерения площади поверхности. Площадь поверхности определялась в соответствии с хорошо известным методом BET (Брунауэра-Эммета-Теллера) по адсорбции азота, также называемым "методом BET". В данном документе при применении метода BET к материалам в соответствии с раскрытием настоящего изобретения следуют общей процедуре и руководству ASTM (Американского общества по испытаниям материалов) D4365-95. Чтобы гарантировать постоянное состояние измеряемого образца, все образцы проходят предварительную обработку. Подходящая предварительная обработка включает в себя нагревание образца, например, до температуры от 400°С до 500°С, в течение времени, достаточном для удаления свободной воды, например от 3 часов до 5 часов. В одном варианте осуществления предварительная обработка состоит в нагревании каждого образца до 500°С в течение 4 часов.
Измерения объема микропор. Объем микропор, в частности, определяется по методам измерений BET с использованием способа оценки, называемого способом t-графика (или иногда просто t-способом), описываемым в литературе (Journal of Catalysis 3,32 (1964)).
Измерения кислотности. Так как n-пропиламин селективно хемосорбируется (химически адсорбируется) на кислотных центрах Бренстеда СНА, то n-пропиламин использовали в качестве молекулярного зонда для определения кислотности СНА-материалов. Для измерения использовалась система термогравиметрического анализатора (TGA), в которой физически адсорбированный n-пропиламин удалялся нагреванием до 280°С, а химически адсорбированный n-пропиламин определялся по изменению массы в диапазоне температур 280-500°С. Значения кислотности (плотности кислотных центров) рассчитывались в единицах ммоль/г по изменению массы между 280°С и 500°С. Для расчета значения кислотности см. статью D. Parrillo и др., Applied Catalysis, т. 67, с. 107-118, 1990, которая включена в данный документ посредством ссылки.
"Каталитические SCR-тесты". Активность материалов, подвергнутых гидротермальному старению, в отношении конверсии NOx с использованием NH3 в качестве восстановителя тестировалась с использованием реактора проточного типа. Образцы порошкового цеолита прессовали и просеивали до размеров 35/70 меш и загружали в кварцевый трубчатый реактор. Состав газа для NH3-SCR включал в себя 500 ч./млн NO, 500 ч./млн NH3, 5 об.% O2, 0,6% H2O и остальное N2. Объемная скорость составляла 50000 ч-1. Температуру реактора повышали от 150 до 550°С, и конверсию NO определяли с помощью инфракрасного анализатора MKS MultiGas в каждой точке температуры.
Сохранение XRD. Площади пиков XRD только что полученных и обработанных паром образцов после Cu-обмена были измерены для расчета значения сохранения XRD. то есть доли площади первоначального пика XRD, сохранившейся после обработки паром. При расчете площади были использованы пики XRD между 19-32 градусами 2-тэта. Сохранение XRD было рассчитано как отношение площади пика образца после обработки паром к площади пика образца до обработки паром.
ПРИМЕРЫ
Ниже приводятся неограничивающие иллюстративные Примеры, дополнительно раскрывающие настоящее изобретение.
Пример 1 - Синтез 14 SAR СНА
1009 г денонсированной воды, 155 г гидроксида N,N,N-триметил-1-адамантиламмония (Sachem, раствор 25 масс. %), 12 г гидроксида калия (EMD Millipore, 71,4 масс. % K2O) и 2 г гидроксида натрия (Southern Ionics, раствор 50 масс. %) были сначала смешаны вместе. Затем в смесь было добавлено 276 г золя диоксида кремния (Nalco, 40 масс. % SiO2). Затем в смесь было добавлено 47,5 г алюмината натрия (Southern Ionics, 23,5 масс. % Al2O3). Затем было добавлено 0,7 г порошка синтезированного шабазитного цеолита (14 SAR). Молярный состав геля был [16,8 SiO2 : 1: 0 Al2O3 : 0,8 K2O : 1,7 Na2O : 1,7 ТМААОН : 672 H2O]. Полученный гель был кристаллизован при 180°С в течение 48 часов в автоклаве из нержавеющей стали (Parr Instruments, 2000 мл) при перемешивании со скоростью 150 об/мин. Извлеченное твердое вещество было подвергнуто фильтрации, промывке денонсированной водой и сушке на воздухе при 105°С в течение ночи. Полученный после синтеза продукт имел рентгеновскую дифрактограмму шабазита и, как показано в Таблице 1, отношение SiO2/Al2O3 (SAR) 13,5. Рентгеновская дифрактограмма Примера 1 показана на Фиг. 1. Средний размер кристаллов на SEM-изображении в Примере 1 составляет 1,4 мкм.
Пример 2 - Кальцинирование 14 SAR СНА при 550°С
Высушенный порошок цеолита из Примера 1 был подвергнут кальцинированию на воздухе в течение 1 часа при 450°С, а затем в течение 6 часов при 550°С со скоростью нагревания 3°С/мин. После кальцинирования образец был подвергнут аммонийному обмену с помощью раствора нитрата аммония. После аммонийного обмена SAR образца составляло 13,5. содержание Na2O - 0,00 масс. %, а K2O - 0.22 масс. %. Кислотность образца после аммонийного обмена, определенная по адсорбции n-пропиламина, составила 1.60 ммоль/г. Свойства образца после аммонийного обмена представлены в Таблице 1.
Пример 3 - Cu-обмен образца из Примера 2
После аммонийного обмена цеолит из Примера 2 был подвергнут Cu-обмену с помощью нитрата меди, чтобы достигнуть содержания CuO, составляющего 5,0 масс. % CuO. После Cu-обмена этот материал был дополнительно обработан паром при 800°С в течение 16 часов в 10% H2O/воздух.
Пример 4 - Синтез 12 SAR СНА
375 г денонсированной воды, 273 г гидроксида N,N,N-триметил-1-адамантиламмония (Sachem, раствор 25 масс. %), 16 г гидроксида калия (EMD Millipore, 71,4 масс. % K2O) и 12 г гидроксида натрия (Southern Ionics, раствор 50 масс. %) были сначала смешаны вместе. Затем в смесь было добавлено 605 г золя диоксида кремния (Nalco, 40 масс. % SiO2). Затем в смесь было добавлено 97 г алюмината натрия (Southern Ionics, 23,5 масс. % Al2O3). Затем было добавлено 120 г раствора сульфата алюминия (7.6 масс. % Al2O3). В заключение было добавлено 3,3 г затравочного материала с топологией СНА. Молярный состав геля был [12,5 SiO2 : 1: 0 Al2O3 : 0,4 K2O : 1,3 Na2O : 1,0 ТМААОН: 188 H2O]. Полученный гель был кристаллизован при 160°С в течение 48 часов в автоклаве из нержавеющей стали (Parr Instruments, 2000 мл) при перемешивании со скоростью 150 об/мин. Извлеченное твердое вещество было подвергнуто фильтрации, промывке деионизированной водой и сушке на воздухе при 105°С в течение ночи. Полученный после синтеза продукт имел рентгеновскую дифрактограмму шабазита и, как показано в Таблице 1, отношение SiO2/Al2O3 (SAR) 12,3. Рентгеновская дифрактограмма Примера 4 показана на Фиг. 2. Средний размер кристаллов на SEM-изображении в Примере 4 составляет 0,9 мкм.
Пример 5 - Кальцинирование 12 SAR СНА при 550°С
Высушенный порошок цеолита из Примера 4 был подвергнут кальцинированию на воздухе в течение 1 часа при 450°С, а затем в течение 6 часов при 550°С со скоростью нагревания 3°С/мин. После кальцинирования образец был подвергнут аммонийному обмену с помощью раствора нитрата аммония. После аммонийного обмена SAR образца составляло 12,3, содержание Na2O - 0,00 масс. %, а K2O - 0,13 масс. %. Кислотность образца после аммонийного обмена, определенная по адсорбции n-пропиламина, составила 1,79 ммоль/г. Свойства образца после аммонийного обмена представлены в Таблице 1.
Пример 6 - Cu-обмен образца из Примера 5
После аммонийного обмена цеолит из Примера 5 был подвергнут Cu-обмену с помощью нитрата меди, чтобы достигнуть содержания CuO, составляющего 5,0 масс. % CuO. После Cu-Обмена этот материал был дополнительно обработан паром при 775°С в течение 16 часов в 10% H2O/воздух.
Пример 7 - Синтез 12 SAR СНА
200 г денонсированной воды. 375 г гидроксида N,N,N-триметил-1-адамантиламмония (Sachem, раствор 25 масс. %), 15 г гидроксида калия (EMD Millipore, 71,4 масс. % K2O) и 20 г гидроксида натрия (Southern Ionics, раствор 50 масс. %) были сначала смешаны вместе. Затем в смесь было добавлено 664 г золя диоксида кремния (Nalco, 40 масс. % SiO2). Затем в смесь было добавлено 94 г алюмината натрия (Southern Ionics, 23,5 масс. % Al2O3). Затем было добавлено 132 г раствора сульфата алюминия (7,6 масс. % Al2O3). В заключение было добавлено 3,6 г затравочного материала с топологией СНА. Молярный состав геля был [13,4 SiO2 : 1: 0 Al2O3 : 0,3 K2O : 1,4 Na2O : 1,3 ТМААОН: 174 H2O]. Полученный гель был кристаллизован при 160°С в течение 48 часов в автоклаве из нержавеющей стали (Parr Instruments, 2000 мл) при перемешивании со скоростью 150 об/мин. Извлеченное твердое вещество было подвергнуто фильтрации, промывке денонсированной водой и сушке на воздухе при 105°С в течение ночи. Полученный после синтеза продукт имел рентгеновскую дифрактограмму шабазита и, как показано в Таблице 1, отношение SiO2/Al2O3 (SAR) 13,0. Рентгеновская дифрактограмма Примера 7 показана на Фиг. 3. Средний размер кристаллов на SEM-изображении в Примере 7 составляет 1,3 мкм.
Пример 8 - Кальцинирование 13 SAR СНА при 550°С
Высушенный порошок цеолита из Примера 7 был подвергнут кальцинированию на воздухе в течение 1 часа при 450°С, а затем в течение 6 часов при 550°С со скоростью нагревания 3°С/мин. После кальцинирования образец был подвергнут аммонийному обмену с помощью раствора нитрата аммония. После аммонийного обмена SAR образца составляло 13,0, содержание Na2O - 0,00 масс. %, а K2O - 0,11 масс. %. Кислотность образца после аммонийного обмена, определенная по адсорбции n-пропиламина, составила 1,68 ммоль/г. Свойства образца после аммонийного обмена представлены в Таблице 1.
Пример 9 - Cu-обмен образца из Примера 8
Подвергнутый аммонийному обмену цеолит из Примера 8 был подвергнут Cu-обмену с помощью Cu-нитрата для достижения содержания CuO, составляющего 5,0 масс. % CuO. Полученный после Cu-обмена материал был дополнительно обработан паром при 775°С в течение 16 часов в 10% H2O/воздух.
Сравнительный Пример 1 - Кальцинирование 14 SAR СНА при 650°С
Высушенный порошок цеолита из Примера 1 был подвергнут кальцинированию на воздухе в течение 1 часа при 450°С, а затем в течение 6 часов при 650°С со скоростью нагревания 3°С/мин. После кальцинирования образец был подвергнут аммонийному обмену с помощью раствора нитрата аммония. После аммонийного обмена SAR образца составляло 13,5, содержание Na2O - 0,00 масс. %, а K2O - 0,16 масс. %. Кислотность образца после аммонийного обмена, определенная по адсорбции n-пропиламина, составила 1,34 ммоль/г.
Сравнительный Пример 2 - Cu-обмен образца из Сравнительного Примера 1
После аммонийного обмена порошок цеолита из Сравнительного Примера 1 был подвергнут Cu-обмену с помощью Cu-нитрата для достижения содержания CuO, составляющего 5.0 масс. % CuO. Полученный после Cu-обмена материал был дополнительно обработан паром при 800°С в течение 16 часов в 10% H2O/воздух.
Сравнительный Пример 3-14 SAR СНА
14.1 SAR СНА синтезировали из геля, содержащего денонсированную воду, гидроксид N,N,N-триметил-1-адамантиламмония, гидроксид калия, гидроксид натрия, золь диоксида кремния, алюминат натрия, раствор сульфата алюминия и затравочный материал с топологией СНА. Извлеченное твердое вещество было подвергнуто фильтрации, промывке деионизированной водой и сушке. Полученный после синтеза продукт имел рентгеновскую дифрактограмму шабазита и отношение SiO2/Al2O3 (SAR) 14,1. После кальцинирования образец был подвергнут аммонийному обмену с помощью раствора нитрата аммония. Кислотность образца после аммонийного обмена, определенная по адсорбции n-пропиламина, составила 1,19 ммоль/г.
Сравнительный Пример 4 - Cu-обмен образца из Сравнительного Примера 3
После аммонийного обмена порошок цеолита из Сравнительного Примера 3 был подвергнут Cu-обмену с помощью Cu-нитрата для достижения содержания CuO, составляющего 5,5 масс. % CuO. Полученный после Cu-обмена материал был дополнительно обработан паром при 775°С в течение 16 часов в 10% H2O/воздух.
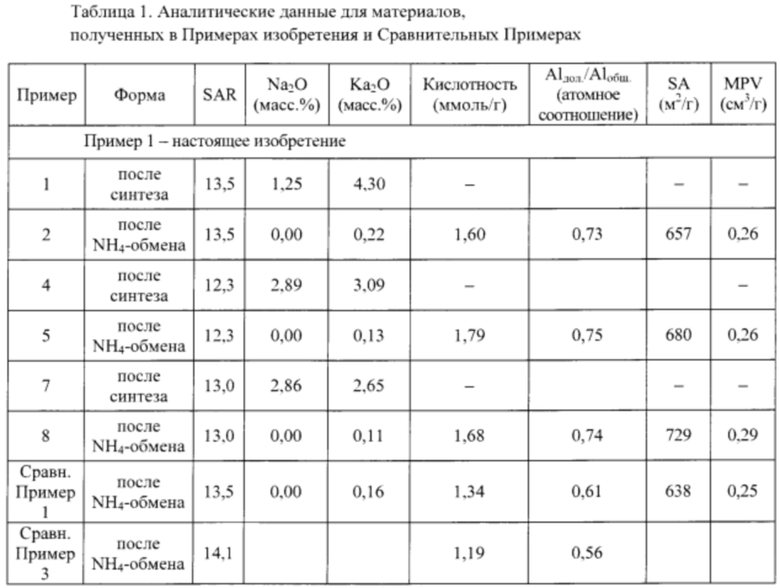
Для получения сохранения XRD рентгеновские дифрактограммы материалов после Cu-обмена были измерены до и после гидротермальной обработки, и результаты измерений представлены в Таблице 2. Цеолит, полученный с использованием описанных в данном документе способов, оставался высококристаллическим после гидротермальной обработки при температуре 775°С или 800°С, а Сравнительные Примеры с низкой долей Al в каркасе цеолита имели более низкое сохранение XRD.
Была также произведена оценка SCR-активности заявленных Примеров и Сравнительных Примеров, и результаты оценки представлены Таблице 3. После аммонийного обмена цеолиты были подвергнуты Cu-обмену с помощью нитрата меди, чтобы достигнуть содержания CuO. составляющего 5,0-5,5 масс. % CuO. После Cu-обмена эти материалы был дополнительно обработаны паром при 775°С или 800°С в течение 16 часов в 10% H2O/воздух. Примеры в соответствии с изобретением с высокой долей Al в каркасе цеолита сохраняли более высокую стабильность и имели более высокую конверсию NOx при низких температурах, таких как 150°С и 200°С.
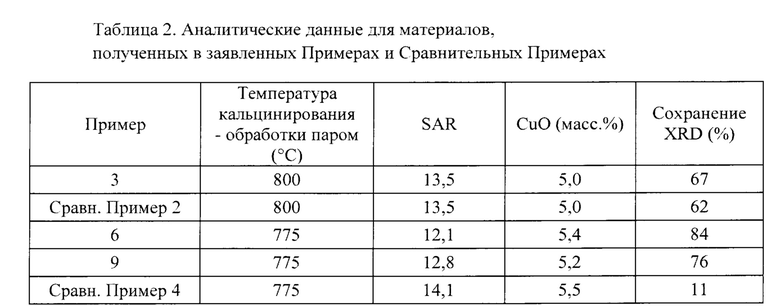
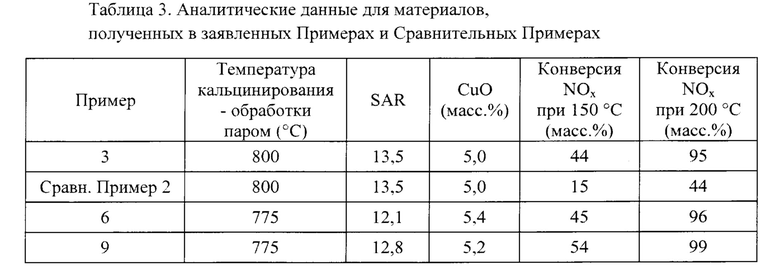
Как видно из Таблицы 3, эффективность конверсии NOx при 150°С и 200°С была значительно ниже для микропористых кристаллических материалов, имеющих долю Al в каркасе цеолита менее 0,63 (при определении по адсорбции n-пропиламина для получения доли Al в каркасе цеолита), даже когда материалы имеют одно и то же молярное отношение диоксида кремния к оксиду алюминия (SAR) (т.е. в диапазоне от 10 до 15) и одно и то же содержание меди в масс. % как материалы, имеющие долю Al в каркаса выше 0,63.
Если не указано иное, все числа, выражающие количества ингредиентов, условия реакции и т.д., используемые в описании и формуле изобретения, следует понимать как снабженные во всех случаях термином "примерно". Следовательно, если не указано иное, числовые параметры, приведенные в нижеследующем описании и прилагаемой формуле изобретения, являются приблизительными, и могут варьироваться в зависимости от требуемых свойств, получение которых является задачей настоящего изобретения. Другие варианты осуществления изобретения будут очевидны специалистам в данной области техники из рассмотрения описания и практики изобретения, раскрытого в данном документе. Предполагается, что описание и примеры следует рассматривать только как иллюстративные, а истинный объем изобретения определяется следующей формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ МИКРОПОРИСТЫЙ КРИСТАЛЛИЧЕСКИЙ МАТЕРИАЛ, ВКЛЮЧАЮЩИЙ МОЛЕКУЛЯРНЫЕ СИТА ИЛИ ЦЕОЛИТ, ИМЕЮЩИЙ ВОСЬМИКОЛЬЦЕВУЮ СТРУКТУРУ ОТКРЫТЫХ ПОР, И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2445166C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2727801C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2754003C1 |
| ЦЕОЛИТНЫЕ КАТАЛИЗАТОРЫ, СОДЕРЖАЩИЕ МЕТАЛЛЫ | 2013 |
|
RU2634899C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2704820C2 |
| SCR КАТАЛИЗАТОР | 2014 |
|
RU2765730C2 |
| SCR КАТАЛИЗАТОР | 2014 |
|
RU2697482C1 |
| ФЕРРИЕРИТ С МАЛЫМ РАЗМЕРОМ КРИСТАЛЛОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2640072C9 |
| КАТАЛИЗАТОР ДЛЯ ОБРАБОТКИ ВЫХЛОПНОГО ГАЗА | 2016 |
|
RU2733997C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛООБМЕННЫХ МИКРОПОРИСТЫХ МАТЕРИАЛОВ ПОСРЕДСТВОМ ТВЕРДОФАЗНОГО ИОННОГО ОБМЕНА | 2014 |
|
RU2678303C2 |
Изобретение относится к каталитической химии. Согласно изобретению предложен микропористый кристаллический материал для селективного каталитического восстановления оксида азота в выхлопном газе, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, кислотность в диапазоне от 1,35 ммоль/г до 2,0 ммоль/г и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более. Также изобретение относится к способу селективного каталитического восстановления оксидов азота в выхлопном газе, содержащему по меньшей мере частичное контактирование указанных выхлопных газов с изделием, содержащим микропористый кристаллический материал, и к способу получения микропористого кристаллического материала. Технический результат - повышение рабочих характеристик материала для селективного каталитического восстановления оксидов азота в выхлопном газе, а также селективное каталитическое восстановление оксидов азота в выхлопном газе. 3 н. и 23 з.п. ф-лы, 3 ил., 3 табл., 13 пр.
1. Микропористый кристаллический материал для селективного каталитического восстановления оксида азота в выхлопном газе, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, кислотность в диапазоне от 1,35 ммоль/г до 2,0 ммоль/г и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более.
2. Микропористый кристаллический материал по п. 1, отличающийся тем, что содержит кристаллическую структуру, имеющую структурный код СНА.
3. Микропористый кристаллический материал по п. 1, отличающийся тем, что доля Al в каркасе цеолита при определении по адсорбции n-пропиламина варьируется от 0,63 до 1,00.
4. Микропористый кристаллический материал по п. 1, отличающийся тем, что SAR варьируется в диапазоне 12-14.
5. Микропористый кристаллический материал по п. 1, отличающийся тем, что дополнительно включает по меньшей мере один каталитически активный металл.
6. Микропористый кристаллический материал по п. 5, отличающийся тем, что по меньшей мере один каталитически активный металл включает медь или железо.
7. Микропористый кристаллический материал по п. 6, отличающийся тем, что каталитически активный металл включает Cu (медь), которая присутствует в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25.
8. Микропористый кристаллический материал по п. 7, отличающийся тем, что после обработки паром при 775-800°С в течение 16 часов указанный материал имеет сохранение XRD, составляющее по меньшей мере 65%.
9. Микропористый кристаллический материал по п. 1, отличающийся тем, что указанный материал имеет средний размер кристаллов в диапазоне от 0,5 мкм до 5 мкм.
10. Способ селективного каталитического восстановления оксидов азота в выхлопном газе, содержащий:
по меньшей мере частичное контактирование указанных выхлопных газов с изделием, содержащим микропористый кристаллический материал, имеющий молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, кислотность в диапазоне от 1,35 ммоль/г до 2,0 ммоль/г и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более.
11. Способ по п. 10, отличающийся тем, что этап контактирования выполняют в присутствии аммиака, мочевины, соединения, образующего аммиак, или углеводородного соединения.
12. Способ по п. 10, отличающийся тем, что материал содержит кристаллическую структуру, имеющую структурный код СНА.
13. Способ по п. 10, отличающийся тем, что доля Al в каркасе цеолита при определении по адсорбции n-пропиламина варьируется от 0,63 до 1,00.
14. Способ по п. 10, отличающийся тем, что SAR варьируется в диапазоне 12-14.
15. Способ по п. 10, отличающийся тем, что дополнительно включает по меньшей мере один каталитически активный металл, выбранный из меди или железа.
16. Способ по п. 15, отличающийся тем, что каталитически активный металл включает медь, которая присутствует в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25.
17. Способ по п. 15, отличающийся тем, что после обработки паром при 775-800°С в течение 16 часов материал имеет сохранение XRD, составляющее по меньшей мере 65%.
18. Способ по п. 10, отличающийся тем, что указанный материал имеет средний размер кристаллов в диапазоне от 0,5 мкм до 5 мкм.
19. Способ получения микропористого кристаллического материала для селективного каталитического восстановления оксида азота в выхлопном газе, имеющего молярное отношение диоксида кремния к оксиду алюминия (SAR) в диапазоне от 10 до 15, кислотность в диапазоне от 1,35 ммоль/г до 2,0 ммоль/г и долю Al в каркасе цеолита, которая при определении по адсорбции n-пропиламина составляет 0,63 или более, содержит:
смешивание источников оксида алюминия, диоксида кремния, щелочесодержащей добавки, органического структурообразующего агента, воды и не обязательно затравочного материала для образования геля;
нагревание геля в автоклаве для образования кристаллического СНА-продукта;
кальцинирование указанного СНА-продукта;
и аммонийный обмен указанного СНА-продукта.
20. Способ по п. 19, отличающийся тем, что дополнительно содержит введение по меньшей мере одного каталитически активного металла в микропористый кристаллический материал посредством жидкофазного или твердофазного ионного обмена, пропитки, прямого синтеза или их комбинаций.
21. Способ по п. 19, отличающийся тем, что по меньшей мере один каталитически активный металл включает медь или железо.
22. Способ по п. 19, отличающийся тем, что каталитически активный металл содержит Cu, которая присутствует в атомном соотношении Cu:Al, составляющем по меньшей мере 0,25.
23. Способ по п. 22, отличающийся тем, что после обработки паром при 775-800°С в течение 16 часов материал имеет сохранение XRD, составляющее по меньшей мере 65%.
24. Способ по п. 19, отличающийся тем, что органический структурообразующий агент содержит гидроксид N,N,N-триметил-1-адамантиламмония.
25. Способ по п. 19, отличающийся тем, что щелочесодержащая добавка содержит источник калия или натрия или их смесь.
26. Способ по п. 19, отличающийся тем, что указанный материал имеет средний размер кристаллов от 0,5 мкм до 5 мкм.
| US 2017107114 A1, 20.04.2017 | |||
| US 2017107114 A1, 20.04.2017 | |||
| US 2017107114 A1, 20.04.2017 | |||
| WO 2014160289 A1, 02.10.2014 | |||
| WO 2014160289 A1, 02.10.2014 | |||
| US 2014112852 A1, 24.04 | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| СПОСОБ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАЦИЕНТОВ С ПОСЛЕОПЕРАЦИОННЫМИ ВЕНТРАЛЬНЫМИ ГРЫЖАМИ | 2017 |
|
RU2657190C1 |
| СИГНАЛЬНЫЙ ПРИБОР К УСТРОЙСТВАМ ДЛЯ УКАЗАНИЯ УРОВНЯ ВОДЫ В БАКЕ | 1927 |
|
SU7659A1 |
| ЦЕОЛИТНЫЕ МАТЕРИАЛЫ ТИПА СНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ С ПРИМЕНЕНИЕМ ЦИКЛОАЛКИЛАММОНИЕВЫХ СОЕДИНЕНИЙ | 2013 |
|
RU2627399C2 |
| ЦЕОЛИТНЫЙ КАТАЛИЗАТОР, СОДЕРЖАЩИЙ МЕТАЛЛ | 2011 |
|
RU2614411C2 |
| CN 102099116 A, 15.06.2011. | |||
Авторы
Даты
2023-11-16—Публикация
2019-04-30—Подача