Настоящее изобретение относится к способу получения металлообменных микропористых материалов или смесей металлообменных микропористых материалов посредством воздействия на физическую смесь оксида металла или соли металла, или их комбинации, и микропористого материала, имеющего ионообменную способность, или смеси, содержащей такие материалы, атмосферой, содержащей аммиак и один или более оксидов азота.
Cu- и Fe-обменные микропористые материалы, такие как цеолиты и цеотипы, являются эффективными катализаторами для восстановления NOx, например, в выхлопах электрических станций, или в выхлопах дизельных двигателей, как при стационарных, так и при транспортных применениях. Каталитическое восстановление NOx обозначается как SCR (селективное каталитическое восстановление). Двумя наиболее известными вариантами способа SCR для восстановления NOx являются (1) углеводородное SCR (HC-SCR), в котором углеводороды применяются в качестве восстановителя, и (2) аммиак-SCR (NH3-SCR, в котором аммиак применяется в качестве восстановителя. В случае HC-SCR, источником углеводородов является дизельное топливо, также применяемое для дизельного двигателя, или остаточные углеводороды в выхлопном газе из-за неполного сгорания. Общая методика для применения NH3-SCR состоит во впрыске мочевины в поток выхлопного газа, которая расщепляется с получением необходимого NH3 для реакции SCR.
Общий способ получения металлообменных цеолитов состоит в контакте цеолита с раствором желаемого иона металла, с последующей фильтрацией, промывкой, сушкой и кальцинацией, при высоких температурах (например >500°С). Следовательно, согласно этой общей методике, контакт цеолита с подходящим раствором, содержащим ионы Cu, Co или Fe, как например нитрат меди, ацетат меди, ацетат кобальта, нитрат железа, сульфат меди или железа, где цеолит находится в Na+, K+, Н+, NH4+ форме, или в форме другого катиона, будет, как правило, приводить к получению материала, который показывает каталитическую активность для SCR реакции с углеводородами или NH3. Выбор аниона соли металла в принципе является случайным, но, как правило, анионы выбираются таким образом, чтобы была достигнута достаточная растворимость, легкое удаление в ходе получения, безопасность при обработке, и отсутствие взаимодействия с цеолитом неблагоприятным образом.
Большинство цеолитных структур являются активными катализаторами для углеводородного SCR и NH3 SCR после ионного обмена с Cu, Со или Fe, наиболее известными примерами являются ZSM-5, бета, SSZ-13 и цеолит Y, но другие типы цеолитов тоже, как известно, показывают активность для SCR после ионного обмена. [В. Moden, J. Donohue, W. Cormier, H. Li, Stud. Surf. Sci. Catal. 2008, 174, 1219-1222.; O. a Anunziata, A.R. Beltramone, Z. Juric, L.B. Pierella, F.G. Requejo, Appl. Catal. A Gen. 2004, 264, 93-101.; M. Moliner, C. Franch, E. Palomares, M. Grill, A. Corma, Chem. Commun. (Camb). 2012, 48, 8264-6.;  , C. Alonso-Escobar, J.L. Jorda, I. Peral,
, C. Alonso-Escobar, J.L. Jorda, I. Peral,  , A. Corma, A.E. Palomares, F. Rey, G. Guilera, J. Catal. 2012, 295, 22-30.; A.E. Palomares, J. Prato, A. Corma, Catal. Today 2002, 75, 367-371.] В сущности, активность для реакции SCR обусловлено ионообменивающимися Cu, Со или Fe, и тем, что местное химическое окружение этих ионов в различных цеолитных структурах очень подобно, и не очень зависит от кристаллической структуры цеолита. Поэтому можно ожидать каталитическую активность для любого Cu, Co и Fe обменивающегося цеолита, или, в общем, если данный катион, как известно, имеет некоторую SCR активность в одном типе цеолитов, можно ожидать SCR активность также в других цеолитах. Различия в активности в различных цеолитных структурах может возникать в результате различий в стабильности каркасной структуры цеолита или в стабильности обменных Cu или Fe в цеолитах [S. Brandenberger,
, A. Corma, A.E. Palomares, F. Rey, G. Guilera, J. Catal. 2012, 295, 22-30.; A.E. Palomares, J. Prato, A. Corma, Catal. Today 2002, 75, 367-371.] В сущности, активность для реакции SCR обусловлено ионообменивающимися Cu, Со или Fe, и тем, что местное химическое окружение этих ионов в различных цеолитных структурах очень подобно, и не очень зависит от кристаллической структуры цеолита. Поэтому можно ожидать каталитическую активность для любого Cu, Co и Fe обменивающегося цеолита, или, в общем, если данный катион, как известно, имеет некоторую SCR активность в одном типе цеолитов, можно ожидать SCR активность также в других цеолитах. Различия в активности в различных цеолитных структурах может возникать в результате различий в стабильности каркасной структуры цеолита или в стабильности обменных Cu или Fe в цеолитах [S. Brandenberger,  , М. Casapu, A. Tissler, R. Althoff, Appl. Catal. В Environ. 2011, 101, 649-659.;
, М. Casapu, A. Tissler, R. Althoff, Appl. Catal. В Environ. 2011, 101, 649-659.;  , Т.V.W. Janssens, A. Kustov, M. Grill, A. Puig-Molina, L. F. Lundegaard, R.R. Tiruvalam,
, Т.V.W. Janssens, A. Kustov, M. Grill, A. Puig-Molina, L. F. Lundegaard, R.R. Tiruvalam,  , A. Corma, J. Catal. 2014,309, 477-490.].
, A. Corma, J. Catal. 2014,309, 477-490.].
Ионообменная способность цеолитов возникает в результате того, что некоторые атомы Si каркасной структуры замещаются на атомы алюминия или другие гетероатомы. Так как формальный заряд Si составляет 4+, и формальный заряд Al составляет 3+, такое замещение создает эффективный отрицательный заряд в кристалле цеолита, или путем изоморфного замещения на другие гетероатомы, имеющие более низкий формальный заряд, чем Si, который уравновешивается положительным ионом, например, Н+, NH4+, Na+ или K+. Cu и Fe также могут образовывать подходящие катионы для уравновешивания этого отрицательного заряда, что является причиной того, что Cu и Fe обменные цеолиты могут быть получены описанным выше способом. Цеолиты представляют собой пористые кристаллические алюмосиликаты. Существуют также другие силикаты, которые не являются алюмосиликатами, с пористой кристаллической структурой и способностью ионного обмена, например, материалы цеотипа, такие как силикоалюмофосфаты (SAPO). Ионообменная способность возникает в результате такого же явления: некоторые из атомов каркасной структуры замещается на атом с другим валентным состоянием, и соответственно требуется компенсация заряда обмениваемыми ионами. Примером такого материала является SAPO материал, который является пористым кристаллическим фосфатом алюминия, в котором некоторые атомы фосфора (формальный заряд 5+) замещаются на Si (формальный заряд 4+). SAPO материалы, обменивающиеся на Fe или Cu, также известны в качестве эффективных катализаторов как для HC-SCR, так и для NH3-SCR, наиболее известным примером такого материала является Cu-SAPO-34.
Несмотря на то, что способ ионного обмена для материалов на основе цеолитов и силикоалюмофосфатных материалов по существу является таким же, существует значительная разница в эффективности ионного обмена. Например, материалы SSZ-13 и SAPO-34 имеют такую же СНА кристаллическую структуру, с по существу таким же размером пор и структурой. Тем не менее, при ионном обмена на основе раствора с Cu, атомы Cu распределяются по всему объему материалы SSZ-13, тогда как Cu имеет склонность к осаждению на наружной поверхности кристаллов с SAPO-34 [ , A. Katerinopoulou, R.R. Tiruvalam, А. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161]. Как следствие, степень ионного обмена с Cu в SAPO-34 материале, полученном методикой ионного обмена на основе раствора, в общем является низкой, и загрузки Сu в SAPO-34, полученном этим способом, в общем значительно ниже, чем в аналогичном материале SSZ-13. Следовательно, свеже ионообменявшиеся Cu-SAPO-34 цеолиты в общем имеют низкую активность для SCR. Известно, что для получения значительно высокой активности для реакции SCR с SAPO-34 материалом необходима активация при высоких температурах (>750°С). (
, A. Katerinopoulou, R.R. Tiruvalam, А. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161]. Как следствие, степень ионного обмена с Cu в SAPO-34 материале, полученном методикой ионного обмена на основе раствора, в общем является низкой, и загрузки Сu в SAPO-34, полученном этим способом, в общем значительно ниже, чем в аналогичном материале SSZ-13. Следовательно, свеже ионообменявшиеся Cu-SAPO-34 цеолиты в общем имеют низкую активность для SCR. Известно, что для получения значительно высокой активности для реакции SCR с SAPO-34 материалом необходима активация при высоких температурах (>750°С). ( , A. Katerinopoulou, R.R. Tiruvalam, A. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161). Было показано, что такая методика нагревания вызывает перераспределение Cu по SAPO-34 кристаллам, применяя более высокую степень Cu ионного обмена.
, A. Katerinopoulou, R.R. Tiruvalam, A. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161). Было показано, что такая методика нагревания вызывает перераспределение Cu по SAPO-34 кристаллам, применяя более высокую степень Cu ионного обмена.
Альтернативная методика введения ионов в кристаллические микропористые материалы заключается в твердофазном ионном обмене, она включает получение сухой смеси в твердом состоянии микропористых материалов и соединения катионов, вводимых в микропористые кристаллы, с последующей некоторой подходящей обработкой, которая направляет катионы в микропористые материалы. (G.L. Price, in:, J.R. Regalbuto (Ed.), Catalyst Preparation: Science and Engineering, CRC Press, Boca Raton, London, New York, 2007, pp. 283-296.)
В заявке на патент США 2013/0108544 раскрывается способ получения ионообменных микропористых материалов путем получения частиц оксида металла или соли металла на поверхности кристаллов SAPO-34, с последующим нагреванием при 500-800°С, предпочтительно 650-750°С, с получением катионов металлов, в течение периода 12-72 часа. Частицы оксида металла или соли металла образуются на поверхности кристаллов SAPO-34 посредством импрегнирования или осаждения. Эта методика отличается от обычного ионного обмена, так как рассматриваемая стадия ионного обмена осуществляется после удаления жидкости, необходимой для импрегнирования или депонирования. Методика предполагает высокую температуру и длительные периоды нагревания. Методика может осуществляться в сухом или влажном воздухе. Вариация этого способа описывается в D. Wang, L. Zhang, J. Li, K. Kamasamudram, W.S. Epling, Catal. Today (2013), DOI 10.1016/j.cattod.2013.11.040 и M. Zamadics, X. Chen, L. Kevan, J. Phys. Chem. (1992) 5488. Вместо получения частиц оксида металла на поверхности кристаллов SAPO, SAPO-34 в форме Н физически смешивается с CuО и нагревается до 800°С в течение 12 часов. Осуществление Си ионного обмена может быть подтверждено в обеих публикациях.
Некоторый твердофазный ионный обмен может происходить между смесью оксида меди и H-ZSM-5 цеолита при 550°С в газообразной смеси, типичной для селективного каталитического восстановления оксидов азота аммиаком, т.е. около 500 частей на миллион NO, 530 частей на миллион NH3, 5% Н2O, 10% О2 в N2, как следует из наблюдения, что обработка смеси CuO и H-ZSM-5 обеспечивает материал с SCR активностью, которая подобна активности обычного Cu-ионообменного H-ZSM-5, и что ни CuO, ни H-ZSM-5 сам по себе не показывает такую активность. ( , Т.V.W. Janssens, A. Kustov, М. Grill, А. Puig-Molina, L.F. Lundegaard, R.R. Tiruvalam, P. Concepcion, A. Corma, J. Catal. 2014, 309, 477-490.)
, Т.V.W. Janssens, A. Kustov, М. Grill, А. Puig-Molina, L.F. Lundegaard, R.R. Tiruvalam, P. Concepcion, A. Corma, J. Catal. 2014, 309, 477-490.)
Применение смесей оксида меди и смесей цеолита для удаления соединений, содержащих азот, при очистке выхлопного газа также известно из патента ЕР 1787720. Катализаторы в этом патенте во всех случаях нагревались до 500°С.
В патенте ЕР 955080 раскрывается способ введения Cu, Fe, Со, Mn, Pd, Rh или Pt в цеолиты с отношением Si/Al выше 5, посредством физического смешивания (i) аммониевых солей, NH3/NH4+-цеолитов или N-coдержащих соединений, и (ii) цеолита с отношением Si/Al выше 5, и (iii) активного соединения, выбранного из соединения одного или более вышеописанных металлов, при комнатной температуре и атмосферном давлении, и нагревания до по меньшей мере 300°С до тех пор, пока процесс ионного обмена не будет завершен, с последующим охлаждением до комнатной температуры. В процессе нагревания на смесь предпочтительно воздействуют аммиак или амин-содержащей атмосферой, со скоростью нагревания выше 10 K в минуту.
В заявке на патент US 2013004398 раскрывается способ введения Fe в цеолиты посредством воздействия на цеолиты пентакарбонилом железа, что обеспечивает получение цеолитов с большим числом сайтов железа, чем катионных положений, и равномерное распределение железа в цеолите. Применяя такой способ, SCR активные Fe-бета катализаторы могут быть получены при 200°С. Получение Fe-SSZ-13 (СНА) катализатора включает 48 ч обработки при 700°С под паром.
В заявках на патент US 2010075834 и WO 08009453 раскрывается способ получения ионообменных (легированных металлом) посредством смешивания цеолита и соединения активного металла и измельчения смеси. Смесь затем нагревают до заданной температуры и хранят при этой температуре в течение определенного периода времени. В ходе нагревания давление в реакторе уменьшается до 0-200 мбар. Раскрытая температура для получения Fe-бета катализатора составляет 500°С.
Настоящее изобретение построено на обнаружении, что получение металлообменных кристаллических микропористых материалов значительно улучшается при осуществлении твердофазного ионного обмена с физической смесью оксида и/или соли металла и кристаллического микропористого материала в атмосфере, содержащей NO и NH3. Это совершено неожиданно в виду того факта, что NO сам по себе не усиливает процесс ионного обмена.
Преимущество настоящего изобретения состоит в том, что металлобменный микропористый материал может быть получен при температуре ниже 300°С. Это обеспечивает путь получения SCR активных микропористых материалов при температуре ниже 300°С.
В соответствии с вышеописанным обнаружением, настоящее изобретение обеспечивает способ твердофазного ионного обмена для получения металлообменных кристаллических микропористых материалов или смесей, содержащих кристаллические микропористые материалы, включающий стадии предоставления сухой смеси, содержащей а) один или более кристаллические микропористые материалы, которые проявляют ионообменную способность, и b) одно или более соединений металлов; нагревания смеси в газообразной атмосфере, содержащей аммиак и один или более оксидов азота, до температуры и в течение времени, достаточных для инициации и осуществления твердофазного ионного обмена ионов соединения металла и ионов кристаллического микропористого материала; и получения кристаллического металлообменного микропористого материала.
Более подробно настоящее изобретение описывается в следующем далее описании изобретения и в формуле изобретения.
Кристаллическими микропористыми материалами, которые могут применяться в способе согласно настоящему изобретению, может быть любой микропористый материал с ионообменной способностью.
Предпочтительно микропористыми материалами, имеющими ионообменную способность, являются цеолиты, которыми являются алюмосиликаты, или материалы цеотипа, такие как силикоалюмофосфаты, с любой кристаллической структурой, например, но без ограничения к этому, AEI, AFX, СНА, KFI, LTA, IMF, ITH, MEL, MFI, SZR, TUN, *BEA, ВЕС, FAU, FER, MOR, LEV.
Наиболее известными примерами таких материалов, подходящих для применения а реакции SCR, являются, но без ограничения к этому, ZSM-5, цеолит Y, бета цеолит, SSZ-13, SSZ-39, SSZ-62, шабазит, и SAPO-34, SAPO-44, ферриерит и TNU-9.
В предпочтительном варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где кристаллические микропористые материалы находятся в H+ или NR4+-форме.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где кристаллические микропористые материалы содержат органический структурообразующий агент.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где соединениями металлов являются оксиды металлов, нитраты металлов, фосфаты металлов, сульфаты металлов, оксалаты металлов, ацетаты металлов или их комбинация.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где металлы в соединениях металлов выбираются из группы Fe, Cu и Co, или их комбинаций.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где соединения металлов содержат один или более оксидов Cu.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где оксидами азота являются монооксид азота, диоксид азота или их смесь.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где содержание аммиака в атмосфере составляет от 1 до 5000 об. частей на миллион.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где содержание одного или более оксидов азота в атмосфере составляет от 1 до 5000 об. частей на миллион.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где мольное отношение аммиака и оксидов азота больше 0,01, предпочтительно от 0,2 до 1.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где содержание кислорода в атмосфере составляет 1 об. % или менее.
В другом варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота, где содержание воды в атмосфере составляет 5 об. % или менее.
В другом предпочтительном варианте выполнения настоящего изобретения на указанную смесь воздействуют атмосферой, содержащей аммиак и один или более оксидов азота при температуре в интервале от 100°С и не более 300°С, предпочтительно от 150°С до 250°С.
Другим объектом настоящего изобретения является металлобменный кристаллический микропористый материал или смеси металлообменных кристаллических микропористых материалов, полученные способом согласно любому из вышеописанных вариаций и вариантов выполнения настоящего изобретения.
Еще одним объектом настоящего изобретения является способ удаления оксидов азота из выхлопного газа путем селективного каталитического восстановления восстановителем, включающий контакт выхлопного газа с катализатором, содержащим металлообменный кристаллический микропористый материал или смеси металлообменных кристаллических микропористых материалов, полученные способом согласно любому из вышеописанных вариаций и вариантов выполнения настоящего изобретения.
В варианте выполнения способа удаления оксидов азота согласно настоящему изобретению восстановителем являются аммиак или его предшественник.
В варианте выполнения способа удаления оксидов азота согласно настоящему изобретению восстановителем являются углеводороды.
Пример 1
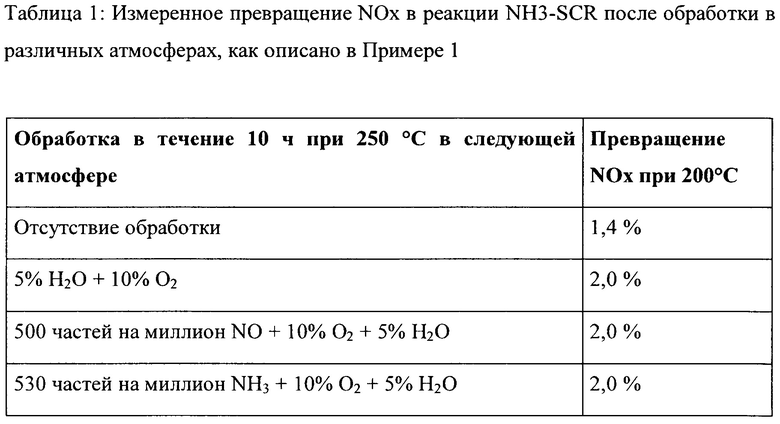
Катализатор получили путем смешивания CuO и H-ZSM-5 цеолита до содержания 12.5 мас. % CuO. Образец катализатора поместили в кварцевый-U трубчатый реактор, и нагрели до 250°С в течение 10 ч в контролируемой газообразной атмосфере. После нагревания катализатор охладили до 200°С подвергли воздействию газовой смеси 500 частей на миллион NO, 533 частей на миллион NH3, 5% Н2О, 10% О2 в N2, и превращение NO измеряли при объемной скорости 2700 нл/г кат час, в качестве меры активности SCR материала. В Таблице 1 приводится обзор газообразных смесей для обработки, применяемых в ходе 10-ти часовой стадии получения катализатора, вместе с активностью SCR полученного таким образом катализатора, измеренной затем в виде превращения NO.
На основании результатов, приведенных в Таблице 1, ясно, что наиболее высокая активность SCR достигается, когда катализаторы получают путем нагревания с NH3, присутствующим в газе для обработки. Присутствие NO усиливает эффект NH3, тогда как его эффект является только очень ограниченным или эффект отсутствует, если NO присутствует без NH3. Когда вода и/или кислород присутствуют в ходе нагревания, получают менее активные материалы, и поэтому присутствие воды и кислорода рассматривается как менее благоприятное.

Пример 2.
Этот пример показывает, что укорочение продолжительности нагревания при 250°С от 10 часов до 5 часов оказывает только небольшой эффект на SCR активность материала. Образцы катализатора получают как описано в Примере 1. Один образец нагревают до 250°С в газообразной атмосфере, содержащей NH3 и NO в течение 10 часов, другой образец нагревают до 250°С в газообразной атмосфере, содержащей NH3 и NO в течение 5 часов. Измерение активности NH3-SCR при 200°С, как описано в Примере 1, показало, что превращение NO при нагревании материала в течение 5 часов составляет 50,8%, и при нагревании материала в течение 10-53.0%. Это показывает, что начальный период нагревания при 250°С является наиболее важным для получения активного материала.
Пример 3
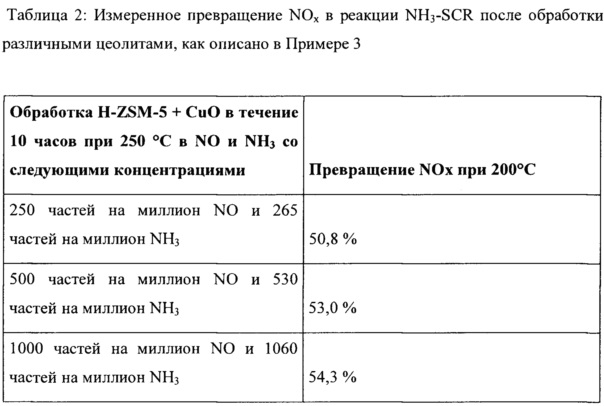
Этот пример показывает, что способ согласно настоящему изобретению может осуществляться с применением широко многообразия концентраций аммиака и оксидом азота с получением ионообменных цеолитов для получения SCR материалов. Катализаторы получают согласно Примеру 1. Катализаторы также тестируют согласно методике, но концентрации NO и NH3 варьируются согласно Таблице 2. Результаты показывают, что концентрации NO и NH3 могут варьироваться в широком диапазоне концентраций.
Пример 4
Этот пример показывает, что способ согласно настоящему изобретению может применяться для получения SCR активных материалов на основе цеолитов с различными кристаллическими структурами. Получили катализаторы и измерили превращение NO согласно методике, описанной в Примере 1, но вместо H-ZSM-5 применяли Н-бета цеолит или H-SSZ-13 цеолит. В Таблице 3 показано измеренное превращение NO посредством применения различных цеолитных материалов.

Пример 5.
Этот пример показывает, что способ согласно настоящему изобретению не ограничен до цеолитов, которые представляют собой микропористые алюминаты диоксида кремния, но также может применяться для других микропористых материалов с ионообменной способностью. Получили катализатор и измерили превращение NO согласно методике, описанной в Примере 1, но вместо H-ZSM-5 применяли материал H-SAPO-34. Измеренное превращение NO составило 28.0%. Необходимо отметить, что SCR-активный SAPO-34 не нагревался более чем до 250°С после добавления Cu. Этот пример иллюстрирует, что способ согласно настоящему изобретению обеспечивает путь получения активного катализатора на основе SAPO-34 без необходимости активации при повышенных температурах (>700°С), что характерно для обычных ионообменных SAPO-34 материалов [ , A. Katerinopoulou, R.R. Tiruvalam, A. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161.], после добавления Сu к микропористому материалу.
, A. Katerinopoulou, R.R. Tiruvalam, A. Kustov, P.G. Moses, P. Concepcion, A. Corma, ACS Catal. 2013, 3, 2158-2161.], после добавления Сu к микропористому материалу.
Пример 6.
Этот пример показывает, что способ согласно настоящему изобретению предпочтительно применяется при диапазоне температур 150-300°С. Порошкообразную смесь, содержащую 30 мг Н-бета цеолита и 3 мг CuO помещают в реактор и подвергают воздействию в течение 5 часов газообразной смесью, содержащей 500 частей на миллион NH3 и 500 частей на миллион NO в N2 при заданной температуре предварительной обработки. После предварительной обработки температуру заменяют на 200°С, и образец подвергают воздействию газообразной смеси, содержащей 600 частей на миллион NH3, 500 частей на миллион NO, 10% О2, 6% Н2О в N2, при общей скорости потока 300 нмл/мин, и превращение NO измерили как меру SCR активности материала. В Таблице 4 приведен обзор температур обработки, вместе с SCR активность полученного таким образом катализатора, измеренной затем как превращение NO.


Из таблицы 4 видно, что значительное повышение превращения NO наблюдается при температуре выше 150°С, что указывает на более эффективный ионный обмен в этом диапазоне температур.
Пример 7.
Этот пример показывает, что отношение NH3/NO в газообразной атмосфере, содержащей NH3 и оксид азота, может варьироваться в широком диапазоне. Порошкообразную смесь, содержащую 30 мг Н-бета цеолита и 3 мг CuO, поместили в реактор и подвергли воздействию в течение 5 часов газообразной смеси для обработки, содержащей 500 частей на миллион NO и заданное количество NH3, при 250°С. После обработки образец охладили до 200°С и подвергли воздействию газообразной смеси 600 частей на миллион NH3, 500 частей на миллион NO, 10% О2, 6% Н2О в N2, при общей скорости потока 300 нмл/мин, и превращение NO измеряли в качестве меры SCR активности материала. В Таблице 5 приводится обзор содержания NH3 и отношения NH3/NO в газообразной смеси для обработки, вместе с SCR активностью полученного таким образом катализатора, измеренной затем в виде превращения NO.

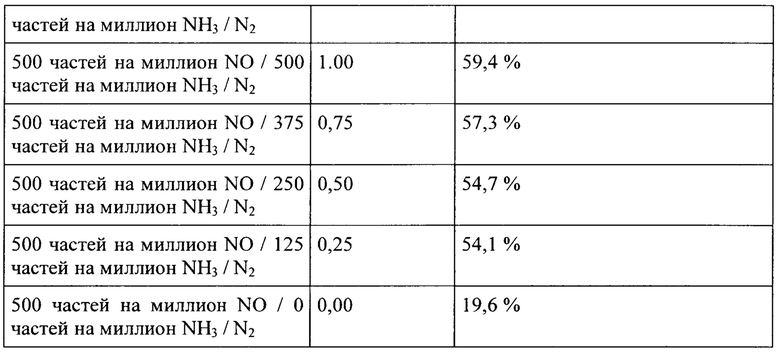
На основании данных, приведенных в Таблице 5, можно увидеть, что процесс ионного обмена согласно настоящему изобретению является эффективным для широкого диапазона составов газообразной атмосферы для обработки, содержащей NH3 и NO. Если NH3 не присутствует, превращение NOx является значительно более низким, указывая на менее эффективный процесс ионного обмена. Положительный эффект NO на процесс ионного обмена в присутствии NH3 ясно виден на основании усиления превращения NO по сравнению с таким превращением после обработки только в NH3.
Пример 8.
Этот пример показывает, что процесс ионного обмена способом согласно настоящему изобретению является более эффективным при низких концентрациях кислорода. Порошкообразную смесь, содержащую 30 мг Н-бета цеолита и 3 мг CuO помещают в реактор и подвергают в течение 5 часов обработке газообразной смесью, содержащей 500 частей на миллион NO, 500 частей на миллион NH3, и 0, 1, 5, или 10% кислорода, при 250°С. После предварительной обработки, образец охладили до 200°С и подвергли воздействию газообразной смеси, содержащей 600 частей на миллион NH3, 500 частей на миллион NO, 10% О2, 6% Н2О в N2, при общей объемной скорости 300 нмл/мин, и превращение NO измерили в качестве меры SCR активности материала. В Таблице 6 приводится обзор концентрации кислорода в газообразной смеси для обработки, вместе с SCR активностью полученного таким образом катализатора, измеренной затем в виде превращения NO.

На основании Таблицы 6 видно, что превращение NOx после обработки в газе, содержащем 1-10% О2, является почти таким же, тогда как превращение NOx после обработки в газе без кислорода значительно выше, что указывает на более эффективный ионный обмен в этом случае.
Пример 9.
Этот пример показывает, что процесс ионного обмена способом согласно настоящему изобретению является более эффективным при температурах ниже 300°С. Порошкообразную смесь, содержащую 30 мг Н-бета цеолита и 3 мг CuO помещают в реактор и подвергают в течение 5 часов обработке газообразной смесью, содержащей 500 частей на миллион NO и 500 частей на миллион NH3 в азоте при различных температурах в диапазоне 150-450°С. После предварительной обработки, образец охладили до 200°С и подвергли воздействию газообразной смеси, содержащей 600 частей на миллион NH3, 500 частей на миллион NO, 10% О2, 6% H2О в N2, при общей объемной скорости 300 нмл/мин, и превращение NO измерили в качестве меры SCR активности материала. В Таблице 7 приводится обзор температуры обработки и соответствующей SCR активностью полученного таким образом катализатора, измеренной затем в виде превращения NOx при 200°С.

Результаты, приведенные в Таблице 7, показывают, что превращение NOx после обработки в диапазоне 200-325°С является самым высоким, указывая на то, что процесс ионного обмена согласно настоящему изобретения является наиболее эффективным в этом диапазоне температур.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛООБМЕННЫХ МЕТАЛЛОАЛЮМОФОСФАТОВ ПОСРЕДСТВОМ ИОННОГО ОБМЕНА В ТВЕРДОМ СОСТОЯНИИ ПРИ НИЗКИХ ТЕМПЕРАТУРАХ | 2014 |
|
RU2672095C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛООБМЕННЫХ ЦЕОЛИТОВ ПОСРЕДСТВОМ ИОННОГО ОБМЕНА В ТВЁРДОМ СОСТОЯНИИ ПРИ НИЗКИХ ТЕМПЕРАТУРАХ | 2014 |
|
RU2674152C2 |
| ЦЕОЛИТНЫЙ КАТАЛИЗАТОР, СОДЕРЖАЩИЙ МЕТАЛЛ | 2011 |
|
RU2614411C2 |
| ЦЕОЛИТНЫЕ КАТАЛИЗАТОРЫ, СОДЕРЖАЩИЕ МЕТАЛЛЫ | 2013 |
|
RU2634899C2 |
| СМЕШАННЫЕ КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МЕТАЛЛ-МЕЛКОПОРИСТОЕ МОЛЕКУЛЯРНОЕ СИТО С 8-ЧЛЕННЫМИ КОЛЬЦАМИ, КАТАЛИТИЧЕСКИЕ УСТРОЙСТВА, СИСТЕМЫ И СПОСОБЫ | 2013 |
|
RU2717953C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2704820C2 |
| СОДЕРЖАЩЕЕ МЕДЬ МОЛЕКУЛЯРНОЕ СИТО ИЗ ЛЕВИНА ДЛЯ СЕЛЕКТИВНОГО ВОССТАНОВЛЕНИЯ NOx | 2010 |
|
RU2600565C2 |
| КАТАЛИЗАТОРЫ СКВ: ПЕРЕХОДНЫЙ МЕТАЛЛ/ЦЕОЛИТ | 2008 |
|
RU2506989C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2727801C2 |
| КАТАЛИТИЧЕСКИЕ КОМПОЗИЦИИ МОЛЕКУЛЯРНОГО СИТА, КАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ, СИСТЕМЫ И СПОСОБЫ | 2015 |
|
RU2754003C1 |
Изобретение относится к способу получения металлообменных микропористых материалов, выбранных из группы, состоящей из цеолита или материалов цеотипа, имеющего каркасную структуру MFI, ВЕА или СНА, или смесей указанных металлообменных кристаллических микропористых материалов, и способу удаления оксидов азота из выхлопного газа посредством селективного каталитического восстановления восстановителем в присутствии полученного катализатора. Способ получения металлообменного кристаллического микропористого материала включает стадии предоставления сухой смеси, содержащей а) одно или более кристаллических микропористых материалов, которые проявляют ионообменную способность, и b) одно или более соединений металлов, причем металлы в соединениях металлов выбирают из группы Fe, Со и Cu; нагревания смеси в газообразной атмосфере, содержащей аммиак и один или более оксидов азота, кислород в количестве 1 об. % или менее и воду в количестве 5 об. % или менее, до температуры и в течение времени, достаточных для инициации и осуществления твердофазного ионного обмена ионов соединения металла и ионов кристаллического микропористого материала; и получения кристаллического металлообменного микропористого материала. Получение металлообменных кристаллических микропористых материалов значительно улучшается при осуществлении твердофазного ионного обмена с физической смесью оксида и/или соли металла и кристаллического микропористого материала в атмосфере, содержащей NO и NH3. Преимущество настоящего изобретения состоит в том, что металлобменный микропористый материал может быть получен при температуре ниже 300°С. 2 н. и 11 з.п. ф-лы, 7 табл., 9 пр.
1. Способ получения металлообменного кристаллического микропористого материала, выбранного из группы, состоящей из цеолита или материалов цеотипа, имеющего каркасную структуру MFI, ВЕА или СНА, или смесей указанных металлообменных кристаллических микропористых материалов, включающий стадии предоставления сухой смеси, содержащей а) одно или более кристаллических микропористых материалов, которые проявляют ионообменную способность, и b) одно или более соединений металлов, причем металлы в соединениях металлов выбирают из группы Fe, Со и Cu; нагревания смеси в газообразной атмосфере, содержащей аммиак и один или более оксидов азота, кислород в количестве 1 об. % или менее и воду в количестве 5 об. % или менее, до температуры и в течение времени, достаточных для инициации и осуществления твердофазного ионного обмена ионов соединения металла и ионов кристаллического микропористого материала; и получения кристаллического металлообменного микропористого материала.
2. Способ по п. 1, в котором цеолит или материалы цеотипа выбирают из группы, состоящей из ZSM-5, бета цеолита, SSZ-13, SSZ-62, шабазита и SAPO-34, SAPO-44.
3. Способ по п. 1, в котором кристаллический микропористый материал или смеси кристаллических микропористых материалов находятся в Н или NH4 форме.
4. Способ по п. 1, в котором соединение металла выбирают из группы оксидов металла, нитратов металла и фосфатов, сульфатов, оксалатов, ацетатов металла или их комбинации.
5. Способ по п. 1, в котором соединения металлов представляют собой один или более оксидов Сu.
6. Способ по п. 1, в котором оксид азота выбирают из монооксида азота и диоксида азота и их смесей.
7. Способ по п. 1, в котором содержание аммиака в атмосфере составляет от 1 до 5000 об. частей на миллион.
8. Способ по п. 1, в котором содержание одного или более оксидов азота в газообразной атмосфере составляет от 1 до 5000 об. частей на миллион.
9. Способ по п. 1, в котором мольное отношение аммиака к оксидам азота составляет более 0,01, предпочтительно от 0,2 до 1.
10. Способ по любому из пп. 1-9, в котором смесь нагревают в газообразной атмосфере, содержащей аммиак и один или более оксидов азота, до температуры менее 300°С, предпочтительно в интервале от 100°С до менее 300°С и наиболее предпочтительно от 150°С до 250°С.
11. Способ удаления оксидов азота из выхлопного газа посредством селективного каталитического восстановления восстановителем, включающий предоставление катализатора, содержащего металлообменный кристаллический микропористый материал, выбранный из группы, состоящей из цеолита или материалов цеотипа, имеющего каркасную структуру MFI, ВЕА или СНА, или смесь указанных металлообменных кристаллических микропористых материалов, включающий стадии предоставления сухой смеси, содержащей а) одно или более кристаллических микропористых материалов, которые проявляют ионообменную способность, и b) одно или более соединений металлов, причем металлы в соединениях металлов выбирают из группы Fe, Со и Cu; нагревания смеси в газообразной атмосфере, содержащей аммиак и один или более оксидов азота, кислород в количестве 1 об. % или менее и воду в количестве 5 об. % или менее, до температуры и в течение времени, достаточных для инициации и осуществления твердофазного ионного обмена ионов соединения металла и ионов кристаллического микропористого материала; и получения кристаллического металлообменного микропористого материала; и приведение в контакт выхлопного газа с указанным катализатором.
12. Способ по п. 11, в котором восстановителем является аммиак или его предшественник.
13. Способ по п. 11, в котором восстановителем являются углеводороды.
| Peter N.R.Vennestrom et | |||
| al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| КАТОК ДЛЯ ФОРМОВКИ КИРПИЧЕЙ ПРЯМОУГОЛЬНОГО СЕЧЕНИЯ ИЗ РАЗЛИТОЙ ПО ПОЛЮ СУШКИ ТОРФЯНОЙ МАССЫ | 1923 |
|
SU477A1 |
| US 20130251611 A1, 26.09.2013 | |||
| НОВЫЙ МИКРОПОРИСТЫЙ КРИСТАЛЛИЧЕСКИЙ МАТЕРИАЛ, ВКЛЮЧАЮЩИЙ МОЛЕКУЛЯРНЫЕ СИТА ИЛИ ЦЕОЛИТ, ИМЕЮЩИЙ ВОСЬМИКОЛЬЦЕВУЮ СТРУКТУРУ ОТКРЫТЫХ ПОР, И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2445166C2 |
| Di Wang et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| Blanka Wichterlova, Effect of water vapour and ammonia on the solid-solid interaction of Cu oxide with Y-type zeolite: Preparation of catalyst for reduction of nitric oxide with ammonia at low temperature, Applied Catalysts A: General, 103, 1993, pp | |||
| Нож для надрезывания подошвы рантовой обуви | 1917 |
|
SU269A1 |
Авторы
Даты
2019-01-25—Публикация
2014-10-15—Подача