Родственные заявки и включение посредством ссылки
По настоящей заявке испрашивается приоритет для предварительной заявки на патент США 62/829400, поданной 4 апреля 2019, содержание которой включено в настоящий документ посредством ссылки во всей полноте. Также сделана ссылка на WO 2006/072065 и патенты США №№ 6,103,526; 9,610,345; 9,669,087 и 10,450,351; описания которых включены в настоящий документ посредством ссылки во всей полноте.
Вышеупомянутые заявки и все документы, процитированные в них или во время их делопроизводства («процитированные документы»), и все документы, процитированные или упомянутые в процитированных приложениях, и все документы, процитированные или упомянутые в данном документе («процитированные здесь документы»), и все документы, процитированные или упомянутые в цитируемых здесь документах, вместе с любыми инструкциями производителя, описаниями, техническими характеристиками и описаниями продуктов для любых продуктов, упомянутых здесь или в любом документе, включенном в настоящий документ посредством ссылки, тем самым включены в настоящую заявку посредством ссылки и могут использоваться в практике изобретения. Более конкретно, все документы, на которые есть ссылки, включены посредством ссылки в той же степени, как если бы каждый отдельный документ был специально и индивидуально указан как включенный посредством ссылки.
Заявление относительно списка последовательностей
Список последовательностей, связанный с настоящим приложением, обеспечивается в текстовом формате вместо бумажной копии и, таким образом, включен в описание посредством ссылки. Имя текстового файла, содержащего список последовательностей, - BI 19-AH009_ST25 (sequence listing).txt. Текстовый файл имеет размер 188 КБ; создан 6 апреля 2020, и он подается в электронном виде через EFS-Web одновременно с подачей описания.
Область техники, к которой относится изобретение
В настоящей заявке раскрывается рекомбинантный бакуловирусный вектор, содержащий полинуклеотид, кодирующий ORF2 свиного цирковируса 3 типа (PCV3). В настоящем документе также раскрыты композиции и вакцины, произведенные из ORF2, полученной из бакуловируса, PCV3 и ORF2 BaculoG/PCV3. Также раскрыт рекомбинантный бакуловирусный вектор, содержащий мутантный полинуклеотид, кодирующий ORF2 свиного цирковируса 3 типа (PCV3). Также раскрыты композиции и вакцины, полученные из мутантной ORF2 PCV3 бакуловирусного происхождения, и ORF2 BaculoG/PCV3.
Предшествующий уровень техники
Цирковирус свиней 3 типа (PCV3) представляет собой вирус без оболочки с икосаэдрической одноцепочечной ДНК (оцДНК), принадлежащий к роду Circovirus в семействе Circoviridae. Геном кодирует две основные открытые рамки считывания (ORF), где ORF1 кодирует связанный с репликацией белок (rep), а ORF2 кодирует белок вирусного капсида (cap), который определяет антигенные характеристики вируса. PCV3 генетически отличается от цирковируса свиней 2 типа (PCV2); в частности, между двумя вирусами существует только 48% идентичности аминокислот в гене rep и 26% идентичности аминокислот в гене cap.
О PCV3 впервые сообщили в 2016 в США Palinski, Rachel, et al. «A Novel Porcine Circovirus Distantly Related to Known Circoviruses Is Associated with Porcine Dermatitis and Nephropathy Syndrome and Reproductive Failure». Journal of Virology, vol. 91, no.1, 26 Oct. 2016. С тех пор вирус был обнаружен во всем мире, включая Германию, Японию, Корею, Россию, Китай, Таиланд, Италию, Испанию, Данию, Южную Корею, Польшу, Бразилию, Колумбию, Индию, Сербию и Швецию. Хотя на сегодняшний день тестирование ограничено, обнаружение PCV3 в ретроспективных образцах указывает на то, что вирус, вероятно, циркулировал в популяциях свиней во всем мире за десятилетия до первоначальных отчетов 2017 года. Предполагается, что по мере расширения тестирования PCV3 будет обнаруживаться в большем количестве стран и в более старых образцах.
Кроме того, в китайской патентной заявке CN109207441A, озаглавленной «Cap-белок 3 типа рекомбинантного, экспрессируемого бакуловирусом цирковируса свиней, и его способ конструирования и праймер», испрашивается приоритет для заявки CN201810912587.1A, поданной 12 августа 2018 г. В заявке описывается конструкция бакуловируса для экспрессии ORF2 PCV3 для производства белков Cap 3 типа цирковируса свиней.
Заявка CN109207441A, озаглавленная «Cap-белок 3 типа рекомбинантного бакуловируса, экспрессирующего цирковирус свиней, и его способ конструирования и праймер», заявляет о приоритете заявки CN201810912587.1A, поданной 12 августа 2018 г. В заявке описано введение экспрессируемой бакуловирусом ORF2 PCV3, у мышей, и предоставлены данные ИФА о сероконверсии.
Заявка CN109207522A, озаглавленная «Рекомбинантный бакуловирус, экспрессирующий усеченный Сар белок цирковируса свиней 3 типа, способ его конструирования и праймер», заявляет о приоритете CN201810912585.2A, поданной 12 августа 2018 г. Заявка описывает применение усеченного бакуловирусного CAP/ORF2 у мышей, и предоставляет данные ИФА по сероконверсии.
Кроме того, патент США 10450351 (т.е. с серийным номером заявки 15/768356), озаглавленный «Иммуногенные композиции цирковируса свиней 3 типа и способы их изготовления и использования» был впервые опубликован как US 2018/0305410 A1 25 октября 2018 г. В нем испрашивается приоритет для предварительной заявки на патент 62/242 866, поданной 16 октября 2015 г. (изобретатель Ben Hause, передавший права на патент Исследовательскому фонду Канзасского университета). См. также Palinski, Rachel, et al. Journal of Virology, vol. 91, no. 1, 26 Oct. 2016, doi:10.1128/jvi.01879-16. Published online October 26, 2016. Документ относится к PCV3 из тканей, «собранных у четырех свиноматок с фермы с хронической плохой репродуктивной способностью, которые умерли с острыми клиническими симптомами, соответствующими PDNS (синдрому дерматита и нефропатии поросят)». Хотя в заявке на патент не указано, где находилась ферма, в ней описано, что данные иммуногистохимии (IHC) и количественной ПЦР (кПЦР) дали отрицательный результат на PCV2, вирус репродуктивного и респираторного синдрома свиней (PRRSV) и вирус гриппа A (IAV) у свиноматок и мумифицированных, мертворожденных и/или слабых плодов. В этой заявке на патент описывается выделение вируса, но не культуры размножающихся клеток.
Примеры в патенте '351 описывают детекцию кПЦР гена капсида PCV3, выделение вируса, клонирование капсидного белка PCV3, разработку моноклонального антитела против капсида PCV3, детекцию PCV3 и разработку рекомбинантного ИФА для капсида PCV3. Однако никаких исследований или данных по вакцинам не описано.
Недавно была опубликована статья, описывающая интраназальную инокуляцию 4- и 8-недельных поросят, свободных от специфических патогенов, инфекционным клоном ДНК PCV3 для оценки патогенеза PCV3. Однако не обсуждались вакцины для предотвращения заражения PCV3. Jiang, Haijun, et al. «Induction of Porcine Dermatitis and Nephropathy Syndrome in Piglets by Infection with Porcine Circovirus Type 3». Journal of Virology, vol. 93, no. 4, 28 Nov. 2018, doi:10.1128/jvi.02045-18.
Цитирование или идентификация любого документа в этой заявке не является признанием того, что такой документ может быть использован в качестве известного уровня техники для настоящего изобретения.
Изложение сущности изобретения
Раскрыты антигенные белки ORF2 PCV3 и их варианты, которые можно использовать для вакцинации или лечения животных, в частности свиней.
Как правило, свиньей является молодая свинья.
В некоторых аспектах настоящего изобретения животное представляет собой поросенка. Как правило, поросенок имеет возраст не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
В некоторых аспектах настоящего изобретения свинья представляет собой свиноматку или свинью до первого опороса.
В некоторых аспектах настоящего изобретения свинья представляет собой свиноматку или свинью до первого опороса (т.е. свиноматку, которая не опоросилась) в возрасте менее 1 года, обычно более 4 месяцев и менее 1 года, обычно в возрасте более 5 месяцев и до 1 года, обычно от 6 месяцев до 1 года, обычно от 4 до 8 месяцев, обычно от 5 до 8 месяцев, обычно от 5 до 7 месяцев, обычно от 5 до 6 месяцев.
В некоторых аспектах настоящего изобретения свинья представляет собой беременную свиноматку в возрасте менее 1 года, обычно в возрасте более 4 месяцев и менее 1 года, обычно в возрасте более 5 месяцев и менее 1 года, обычно в возрасте от 6 месяцев до 1 года.
В некоторых аспектах настоящего изобретения свинья представляет собой свинью до осеменения в возрасте менее 1 года, обычно более 4 месяцев и менее 1 года, обычно более 5 месяцев и менее 1 года, обычно от 6 месяцев до 1 года, обычно от 4 до 8 месяцев, обычно от 5 до 8 месяцев, обычно от 5 до 7 месяцев, обычно от 5 до 6 месяцев.
Раскрыта разработка бакуловирусной ORF2 PCV3, экспрессированной из «BaculoG/PCV3 ORF2», композиций и трех вакцин: живой вакцины BaculoG/PCV3 ORF2, P9 с адъювантом 50% ISA 207VG; живой вакцины BaculoG/PCV3 ORF2, P9 с адъювантом 20% карбополом, и контрольной живой вакцины BaculoG/без вставки, P4, с адъювантом 20% карбополом. Были предоставлены данные, показывающие эффективность вакцин для предотвращения заболевания PCV3.
Также раскрыта разработка ORF2 PCV3 бакуловирусного происхождения, полученной из убитого вируса.
Также раскрыта разработка ORF2 PCV3 бакуловирусного происхождения, полученной из мутантного убитого вируса.
Таким образом, в первом аспекте настоящее изобретение относится к композиции, содержащей белок ORF2 PCV3, предпочтительно антигенный белок ORF2 PCV3 (антиген ORF2 PCV3). Указанная композиция в дальнейшем также называется «композицией по настоящему изобретению». Также было понятно, что термин «композиция по настоящему изобретению», как описано в настоящей заявке, эквивалентен термину «раскрытая композиция».
Предпочтительно композиция по настоящему изобретению дополнительно включает ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизатора, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии, иммуномодулирующего агента и/или любой их комбинации.
Настоящее изобретение также относится к белку ORF2 цирковируса свиней 3 типа (PCV3), и ветеринарно приемлемому носителю, включающему растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор, вектор экспрессии, иммуномодулирующий агент и/или любую их комбинацию.
В одном варианте осуществления ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию. В другом варианте осуществления ветеринарно приемлемый носитель включает адъювант.
ORF2 PCV3 может принадлежать к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., “Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains,” Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4). Таким образом, PCV3, как упомянуто в настоящей заявке, представляет собой любую филогенетическую ветвь PCV3 или комбинацию клад, или предпочтительно выбран из группы, состоящей из PCV3a и PCV3b, и наиболее предпочтительно выбран из группы, состоящей из PCV3a1, PCV3b1, PCV3b2 и PCV3c. Таким образом, композиция по настоящему изобретению предпочтительно содержит белок ORF2 PCV3, выбранный из группы, состоящей из белка ORF2 PCV3a и белка ORF2 PCV3b, или наиболее предпочтительно содержит белок ORF2 PCV3, любой филогенетической клады PCV3 или комбинации клад, или выбранный из группы, состоящей из белка ORF2 PCV3a1, белка ORF2 PCV3b1 и белка ORF2 PCV3b2. В другом варианте осуществления белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности или гомологии последовательности с SEQ ID NO: 1. Предпочтительно белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 4. В соответствии с особо предпочтительным аспектом белком ORF2 PCV3 является рекомбинантный белок или наиболее предпочтительно рекомбинантный белок, экспрессируемый бакуловирусом. Таким образом, композиция предпочтительно содержит рекомбинантный белок ORF2 PCV3 или наиболее предпочтительно содержит белок ORF2 PCV3, экспрессируемый бакуловирусом.
В другом варианте осуществления белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3, полученный в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV3. Предпочтительно вектор экспрессии представляет собой бакуловирус.
В еще одном варианте осуществления композиция дополнительно содержит белок ORF2 PCV2, который может быть результатом экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV2. Предпочтительно вектор экспрессии представляет собой бакуловирус.
Кроме того, композиция может дополнительно содержать по меньшей мере один дополнительный антиген дополнительного патогена свиней. Дополнительный антиген или антигены патогенов свиней включают антиген PRRSV, бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген вируса болезни Ауески или псевдобешенства, антиген IAV, антиген вируса чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV), антиген Pasteurella multocida, антиген Erysipelothrix rhusiopathiae или антиген Mycoplasma hyorhinis.
В другом варианте осуществления белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или от 2 до примерно 400 мкг/мл, или от 4 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или от 2 до примерно 200 мкг/мл, или от 4 до примерно 200 мкг/мл, или от 8 до примерно 200 мкг/мл, или от 0,35 до примерно 100 мкг/мл, или 2 до примерно 100 мкг/мл, или от 4 до примерно 100 мкг/мл, или от 8 до примерно 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или от 2 до примерно 50 мкг/мл, или от 4 до примерно 50 мкг/мл, или от 8 до примерно 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до примерно 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл. В конкретном варианте осуществления композиция может содержать белок ORF2 PCV3 в количестве в диапазоне примерно от 1,5 до 2,0 мкг/мл композиции. Например, в одном из вариантов осуществления доза композиции в 1 мл может включать около 1,6 мкг белка ORF2 PCV3.
В другом варианте осуществления белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или от 2 до примерно 400 мкг/дозу, или от 4 до примерно 400 мкг/дозу, или от 8 до примерно 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или от 2 до примерно 200 мкг/дозу, или от 4 до примерно 200 мкг/дозу, или от 8 до примерно 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или от 2 до примерно 100 мкг/дозу, или от 4 до примерно 100 мкг/дозу, или от 8 до примерно 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или от 2 до примерно 50 мкг/дозу, или от 4 до примерно 50 мкг/дозу, или от 8 до примерно 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу. В конкретном варианте осуществления композиция может содержать общий белок ORF2 PCV3 и PCV2 в количестве в диапазоне примерно от 1,5 до 2,0 мкг/мл композиции. Например, в одном варианте осуществления доза композиции в 1 мл может включать примерно 1,6 мкг объединенного белка ORF2 PCV3 и PCV2.
В другом варианте осуществления адъювант включает гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию типа вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерил три- (каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитол олеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, а ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; адъювантную систему RIBI; Блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
В еще одном варианте осуществления может применяться примерно от 50 мкг до 2000 мкг адъюванта, или адъювант присутствует в количестве примерно 250 мкг/мл в дозе композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу. В конкретном варианте осуществления композиция может включать адъювант в диапазоне примерно от 750 мкг до 2,5 мг на дозу композиции. Например, в одном из вариантов осуществления доза композиции может включать примерно 1 мг адъюванта.
В одном варианте осуществления иммуномодулирующий агент включает интерлейкин (интерлейкины), интерферон (интерфероныы) или другой цитокин (цитокины).
Дозировка антибиотика (антибиотиков) может составлять примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика (антибиотиков). Например, вариант осуществления композиции может включать менее примерно 30 мкг/мл антибиотика (антибиотиков).
В одном из вариантов осуществления антибиотик (антибиотики) включает гентамицин.
Композиция по настоящему описанию может содержать (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры из клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, экспрессирующим указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации. В одном варианте осуществления примерно 90% компонентов (i) - (iii) могут иметь размер менее 1 мкм, а pH указанной композиции доводят до примерно 6,5-7,5. В другом варианте осуществления BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса. В другом варианте осуществления композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI. Композиция может содержать примерно 1 мг Карбопола или Карбопола 971. Например, вариант осуществления композиции может включать культуру клеток, обработанную BEI с концентрацией примерно 5 мМ для инактивации бакуловируса. В некоторых вариантах осуществления доза композиции может включать остаточный BEI и/или примерно 1 мг Карбопола, Карбопола 971 или их комбинации.
Любая композиция по изобретению может быть составлена и/или упакована для применения разовой дозы или однократной вакцинации, а также для режима множественных доз. Предполагается, что однократное введение позволяет преодолеть присутствие материнских антител.
В одном варианте осуществления композиция может представлять собой PCV3 и PPV (предпочтительно упакованные в VLP) и/или PRRSV, предпочтительно для использования у свиноматок/свиней племенного возраста. В таком варианте осуществления предусмотрена одна или несколько доз для введения.
Согласно другому аспекту композиция по настоящему изобретению представляет собой иммуногенную композицию.
Изобретение также относится к композиции по настоящему изобретению для использования в качестве лекарственного средства.
Кроме того, композиция по настоящему изобретению предназначена для использования в качестве вакцины.
Согласно особо предпочтительному аспекту, композиция по настоящему изобретению предназначена для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и других патогенов свиней, и/или (iv) PCV3, PCV2 и других патогенов свиней.
Согласно другому предпочтительному аспекту композиция по настоящему изобретению предназначена для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфицирования PCV3 у животного, причем указанным животным предпочтительно является свинья.
Кроме того, композиция по настоящему изобретению предназначена для использования в способе индукции иммунного ответа против PCV3 у свиньи, в частности, предпочтительно у беременной свиноматки.
В соответствии с еще одним аспектом, композиция по настоящему изобретению предназначена для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у поросенка, при этом поросенок должен находиться на вскармливании свиноматкой, которой вводили композицию.
Таким образом, настоящее изобретение дополнительно обеспечивает композицию по настоящему изобретению для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у поросенка, при этом поросенок должен находиться на вскармливании свиноматкой, которой вводили композицию по настоящему изобретению, и при этом предпочтительно указанная свиноматка, которой вводили композицию, является свиноматкой, которой вводили иммуногенную композицию, когда указанная свиноматка была беременна, в частности указанным поросенком, или является свиньей до осеменения.
Предпочтительно композицию по настоящему изобретению для использования в любом из вышеупомянутых способов вводят внутримышечно или интрадермально, в частности указанной свиноматке.
Настоящее изобретение также включает способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, включающий введение животному любой из описанных в настоящей заявке композиций. Животное может быть свиньей. Предпочтительно свинья может быть свиньей до первого опороса, поросенком или свиноматкой. Свинья до первого опороса или поросенок могут быть не старше 15 недель или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели. Применение может быть осуществлено в течение по меньшей мере 1, 2 или 3 недель от контакта с вирулентным цирковирусом свиней. Применение может быть осуществлено в течение по меньшей мере 1, 2 или 3 недель после контакта с вирулентным цирковирусом свиней. Для некоторых аспектов применение может включать однократное введение или введение путем однократного введения, или однократное введение одной дозы белка по настоящему изобретению или композиции по настоящему изобретению; а не режим многократной вакцинации или многодозовый режим. Для некоторых аспектов применение может включать режим многократной вакцинации или применения многократных доз белка по настоящему изобретению или композиции по настоящему изобретению.
Кроме того, настоящее изобретение обеспечивает способ иммунизации субъекта, включающий введение субъекту композиции по настоящему изобретению.
Кроме того, настоящее изобретение обеспечивает способ иммунизации свиней против клинического заболевания, вызванного по меньшей мере одним патогеном у указанного животного, где указанный способ включает стадию введения животному композиции по настоящему изобретению, при этом указанная иммуногенная композиция не вызывает клинических признаков инфекции, но способна вызывать иммунный ответ, который иммунизирует животное против патогенных форм указанного по меньшей мере одного патогена, и при этом указанный по меньшей мере один патоген предпочтительно представляет собой PCV3.
Кроме того, настоящее изобретение обеспечивает способ индукции выработки антител, специфичных к PCV3, у свиноматки, где указанный способ включает введение композиции по настоящему изобретению. Свиноматка может быть беременной свиноматкой. В качестве альтернативы свиноматка может быть свиньей до первого опороса (т.е. свиноматкой, которая не опоросилась), предпочтительно свиноматкой перед осеменением.
Кроме того, настоящее изобретение обеспечивает способ уменьшения или предотвращения клинических признаков или клинических симптомов, вызванных инфекцией PCV3 у поросят, при этом указанный способ включает:
- введение композиции по настоящему изобретению свиноматке, и
- обеспечение кормления указанного поросенка указанной свиноматкой,
и при этом указанная свиноматка предпочтительно является беременной свиноматкой, в частности указанным поросенком.
Предпочтительно, последние вышеупомянутые способы включают стадии:
- введение композиции по настоящему изобретению свиноматке, беременной указанным поросенком,
- обеспечение рождения указанной свиноматкой указанного поросенка, и
- обеспечение кормления указанного поросенка указанной свиноматкой.
Кроме того, настоящее изобретение обеспечивает способ уменьшения клинических признаков и/или клинических симптомов, вызванных инфицированием вирусом эпидемической диареи свиней (PEDV) у поросят, при этом поросенка должна кормить свиноматка, которой была введена композиция по настоящему изобретению.
Предпочтительно в любом из вышеупомянутых способов, где это применимо, композицию по настоящему изобретению вводят внутримышечно или интрадермально, в частности указанной свиноматке.
Согласно другому предпочтительному аспекту иммуногенную композицию по настоящему изобретению вводят дважды, в частности внутримышечно или интрадермально, указанной свиноматке.
В другом предпочтительном аспекте клинические признаки, упомянутые в настоящей заявке, выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
В другом предпочтительном аспекте клинические признаки, как указано в настоящей заявке, выбраны из группы, состоящей из выталкивания мумифицированных, мертворожденных и/или слабых плодов.
В еще одном предпочтительном аспекте клинические симптомы, как упомянуто в настоящей заявке, выбраны из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
В еще одном предпочтительном аспекте клинические симптомы, как упомянуто в настоящей заявке, выбраны из группы, состоящей из развития или производства мумифицированного, мертворожденного и/или слабого плода.
Настоящее изобретение также охватывает использование любой из раскрытых здесь композиций в любом из раскрытых здесь способов, или использование белка ORF2 PCV3, отдельно или в комбинации, из любой из описанных здесь композиций для применения при приготовлении композиции для индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (III) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, или для использования в способе индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
В одном варианте осуществления композиция может представлять собой PCV3 и PPV (предпочтительно упакованные в VLP) и/или PRRSV, предпочтительно для использования у свиноматок/свиней до первого опороса. В таком варианте осуществления предусмотрена одна или несколько доз для введения. Этот конкретный вариант осуществления включает использование белка ORF2 PCV3 в сочетании с белком PPV, и при необходимости белком PRRSV для использования в приготовлении композиции для индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа PCV3 и PPV, и при необходимости PSSRV, или для использования в способе индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против PCV3 и PPV, и при необходимости PSSRV.
В этом варианте осуществления композиция может содержать (i) белок ORF2 цирковируса свиней 3 типа (PCV3), белок парвовируса (PPV), и при необходимости белок PRRSV (вируса респираторного и репродуктивного синдрома свиней), и (ii) ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизатора, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии, иммуномодулирующего агента и/или любой их комбинации. Ветеринарно-приемлемый носитель может включать адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию. Ветеринарно-приемлемый носитель может включать адъювант. Композиция может быть использована в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3, PPV и/или PRRSV. В одном варианте осуществления композиция может быть использована в способе индукции иммунного ответа против PCV3 у свиньи, в частности, предпочтительно у беременной свиноматки. В другом варианте осуществления композиция может быть использована в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3, у поросят, где поросенок должен получать вскармливание свиноматкой, которой была введена композиция. Композицию может вводить внутримышечно или интрадермально. Вариант осуществления также относится к способу индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3, PPV и/или PRRSV, который может включать введение животному любой из вышеуказанных композиций. Вариант осуществления также относится к способу иммунизации свиней против клинического заболевания, вызванного по меньшей мере одним патогеном у указанного животного, где указанный способ включает стадию введения животному любой из вышеуказанных композиций, при этом указанная иммуногенная композиция не вызывает клинических признаков инфекции, но способна вызывать иммунный ответ, который иммунизирует животное против патогенных форм указанного по меньшей мере одного патогена.
PPV представляет собой автономный реплицирующийся вирус подсемейства Parvovirinae из рода Protoparvovirus в семействе Parvoviridae, содержащий одноцепочечную молекулу ДНК длиной около 5100 нуклеотидов (Cotmore et al., 2014: Arch Virol.: 159(5): 1239-1247; Molitor et al., 1984: Virology: 137(2):241-54). В вирионы упакована только минусовая цепь ДНК. Геном вируса кодирует три капсидных белка (VP1, VP2, VP3) и один неструктурный белок (NS1). Капсид парвовируса имеет диаметр около 22-25 нанометров и состоит из субъединиц VP1 и VP2. Эти белки происходят из подвергнутых альтернативному сплайсингу версий одной и той же молекулы РНК и, таким образом, перекрываются в последовательности. Кроме того, парвовирус свиней проявляет высокий уровень сходства последовательностей с вирусом панлейкопении кошек, парвовирусами собак и парвовирусом грызунов (Ranz et al., 1989: J. gen. Virol: 70: 2541-2553).
Белок PPV может происходить из инактивированной или убитой целой клетки или из субъединицы PPV. Предпочтительно белок PPV представляет собой рекомбинантный белок PPV.
В Европейском патенте ЕР 0551449А1 раскрыт способ получения субъединичной вакцины VP2 против парвовируса свиней. Cadar D et al. (Infection, Genetics and Evolution 2012, 12: 1163-1171) описывают филогению и эволюционную генетику парвовируса свиней у диких кабанов. Streck A. F et al. (Journal of General Virology 2011, 92: 2628-2636) описывают высокую скорость вирусной эволюции капсидного белка парвовируса свиней. WO 88/02026 относится к вакцинам на основе пустых вирусных капсидов. Martinez C et al. (Vaccine 1992, 10 (10): 684-690) раскрывает получение пустых капсидов свиного парвовируса с высокой иммуногенной активностью. Xu F et al. (Applied and Environmental Microbiology 2007, 73 (21): 7041-7047) описывают индукцию иммунных ответов у мышей после внутрижелудочного введения Lactobacillus casei, продуцирующих белок VP2 парвовируса свиньи. Патент США № 10485866 раскрывает иммуногенные композиции, содержащие вирусный белок 2 PPV (VP2), преимущественно мутантный PPV VP2, содержащий одну или несколько мутаций.
Термин «свиной парвовирус» или «PPV» хорошо известен специалисту в данной области техники. Однако «свиной парвовирус» представляет собой автономный реплицирующийся вирус из рода Рarvovirus в семействе Parvoviridae, содержащий одноцепочечную молекулу ДНК. Геном вируса кодирует три капсидных белка (VP1, VP2, VP3) и один неструктурный белок (NS1). Заболевание, вызываемое PPV у свиней, часто называют SMEDI (сокращение от мертворождения, мумификации, гибели эмбриона и бесплодия). Термин «свиной парвовирус» охватывает все возможные штаммы, генотипы, фенотипы и серотипы парвовируса свиней. Термин «вирусный белок 2» или «VP2» относится к капсидному белку VP2 парвовируса свиньи. Термин «вирусный белок 2» или «VP2» хорошо известен специалисту в данной области техники.
Репродуктивно-респираторный синдром свиней (PRRS) рассматривается многими как наиболее серьезное заболевание, поражающее в настоящее время свиноводство во всем мире. Вирус PRRS (PRRSV) представляет собой оболочечный одноцепочечный РНК-вирус, относящийся к семейству Arteriviridae. Антигенные характеристики различных изолятов вируса PRRS сильно различаются, а эффективные меры по предотвращению инфекций ограничены. Существуют три основные группы вакцин против PRRS, аттенуированный модифицированный живой вирус (MLV), вакцины с убитым вирусом или рекомбинантные вакцины. Белки вирусной оболочки вируса PRRSV обычно подразделяются на основные и минорные белки в зависимости от количества белков в вирионе. Основными белками оболочки вируса являются gp5 (ORF 5) и M (ORF 6), которые образуют димер. Минорные белки оболочки - это gp2 (ORF2), gp3 (ORF3), gp4 (ORF4) и E (ORF2b) и, вероятно, недавно идентифицированный вирусный белок gp5a (ORF 5a). Активный антигенный компонент может включать ORF4, ORF5, ORF6 или ORF7 вируса PRRSV.
Рекомбинантный антиген PRRSV может быть экспрессирован в векторной вакцине PRRSV или композиции, которая включает один или несколько сконструированных рекомбинантных аденовирусных векторов, которые несут и экспрессируют определенные антигены PRRSV, и при необходимости фармацевтически или ветеринарно приемлемый носитель, адъювант, наполнитель или растворитель. Предпочтительно вектор представляет собой аденовирусный вектор, хотя также рассматриваются другие векторы, такие как бакуловирус.
PRRSV может быть любым штаммом, поскольку описанные в настоящей заявке новые композиции и способы по изобретению универсально применимы ко всем известным и еще не обнаруженным штаммам PRRSV. Вирус PRRSV существует в виде двух генотипов, называемых типами «US» и «EU», которые имеют примерно 50% гомологию последовательностей (Dea S. et al. (2000). Arch Virol 145: 659-88). Эти два генотипа также можно различить по их иммунологическим свойствам. Большая часть информации о секвенировании различных изолятов основана на структурных белках, а именно на белке оболочки GP5, который составляет только около 4% вирусного генома, тогда как о неструктурных белках (nsp) известно очень мало. Выделение вируса PRRSV и производство вакцин описано в ряде публикаций (WO 92/21375, WO 93/06211, WO93/ 03760, WO 93/07898, WO 96/36356, EP 0676467, EP 0732340, EP 0835930, US 10039821). Антиген PRRSV включает минорные белки PRRS (например, gp2, gp3, gp4, gp5a, gp5 или E) в любой комбинации, и при необходимости включает дополнительные основные белки PRRS (например, gp5 или M). Например, антигены PRRSV могут отображаться на поверхности вирусоподобных частиц (VLP). В других вариантах осуществления растворимые версии антигенов можно вводить животному-хозяину, при этом происходит олигомеризация (включая тримеризацию) белков друг с другом или дополнительно с компонентами VSV-G или других вирусных белков, или любая олигомеризация (включая мотивы тримеризации) (например, мотивы из бактериального GCN4 и т.п.). Более того, предполагается, что TM/CT-домены поверхностных гликопротеинов вируса типа I выполняют ту же функцию, что и соответствующие домены из VSV-G, и, следовательно, взаимозаменяемы с ними.
В некоторых вариантах осуществления один или несколько векторов содержат либо нуклеотидную последовательность, кодирующую антиген E PRRSV, полипептид, эктодомен или его вариант; либо нуклеотидную последовательность, кодирующую модифицированный антиген gp2, gp3, gp4, gp5a, gp5 или M, полипептид, эктодомен или его вариант PRRSV, при этом существующая последовательность клеточной локализации gp2, gp3, gp4, gp5a, gp5 или M была заменена детерминантной последовательностью экспрессии на клеточной поверхности из гетерологичного гена. В некоторых вариантах осуществления один или несколько векторов содержат смесь двух векторов: первый вектор, экспрессирующий минорные белки PRRSV с перенацеливанием, и второй вектор, экспрессирующий основные белки PRRSV с перенацеливанием.
В предпочтительном варианте осуществления иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят нуждающемуся субъекту в двух дозах. Однако иммуногенная композиция, содержащая PCV3, PPV и/или PRRSV, может быть введена в двух или более дозах, причем первую дозу вводят до введения второй (бустерной) дозы. Предпочтительно вторую дозу вводят по меньшей мере через 15 дней после первой дозы. Более предпочтительно вторую дозу вводят между 15 и 40 днями после первой дозы. Еще более предпочтительно вторую дозу вводят по меньшей мере через 17 дней после первой дозы. Еще более предпочтительно вторую доза вводят между 17 и 30 днями после первой дозы. Еще более предпочтительно вторую дозу вводят по меньшей мере через 19 дней после первой дозы. Еще более предпочтительно вторую дозу вводят между 19 и 25 днями после первой дозы. Наиболее предпочтительно вторую дозу вводят по меньшей мере через 21 день после первой дозы. Еще более предпочтительно вторую дозу вводят примерно через 21 день после первой дозы или через 21 день после первой дозы. В предпочтительном аспекте схемы двукратного введения как первую, так и вторую дозу иммуногенной композиции, содержащей PCV3, PPV и/или PRRSV, вводят в одинаковом количестве. Предпочтительно каждая доза находится в предпочтительных количествах, указанных выше, при этом доза 1 мл или 2 мл для первой и второй доз является наиболее предпочтительной. В дополнение к первому и второму режимам дозирования альтернативный вариант осуществления включает дополнительные последующие дозы. Например, в этих аспектах может быть введена третья, четвертая или пятая доза. Предпочтительно последующую третью, четвертую и пятую дозы вводят в том же количестве, что и первую дозу, при этом временные рамки между дозами соответствуют времени между первой и второй дозами, упомянутыми выше.
Объем дозы для каждого субъекта зависит от способа вакцинации и возраста субъекта. Предпочтительно общий объем составляет примерно от 0,2 мл до 5 мл, более предпочтительно примерно от 0,5 мл до 3,0 мл, еще более предпочтительно примерно от 1,0 мл до 2,5 мл, еще более предпочтительно примерно от 1,0 мл до 2,0 мл. Наиболее предпочтительный объем составляет 1 мл; 1,5 мл; 2 мл или 2,5 мл на дозу.
Иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, предпочтительно вводят местно или системно. Подходящие способы введения, обычно используемые, представляют собой пероральное или парентеральное введение, такое как интраназальное, внутривенное, интрадермальное, трансдермальное, внутримышечное, интраперитонеальное, подкожное, а также ингаляционное введение. Однако, в зависимости от природы и механизма действия соединения, иммуногенная композиция также может быть введена другими путями. Например, такие другие пути включают внутрикожный, внутривенный, внутрисосудистый, внутриартериальный, интраперитонеальный, интратекальный, интратрахеальный, внутрикожный, интракардиальный, интралобальный, интралобарный, интрамедуллярный, внутрилегочный, интраректальный и интравагинальный. Однако более предпочтительно иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят подкожно или внутримышечно. Наиболее предпочтительно иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят внутримышечно.
В одном аспекте указанную иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят внутримышечно.
В одном аспекте указанную иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят свиньям до первого опороса и/или свиноматкам.
Предпочтительно, иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят свиньям до первого опороса и/или свиноматкам в возрасте по меньшей мере 3 месяцев, более предпочтительно в возрасте по меньшей мере 4 месяцев, наиболее предпочтительно по меньшей мере в возрасте 5 месяцев.
В одном аспекте иммуногенную композицию вводят свиньям до первого опороса и/или свиноматкам в возрасте по меньшей мере 3 месяцев.
В одном аспекте указанную иммуногенную композицию, содержащую PCV3, PPV и/или PRRSV, вводят свиньям до первого опороса и/или свиноматкам до беременности.
В режиме двухфазной вакцинации вторую дозу указанной иммуногенной композиции, содержащей PCV3, PPV и/или PRRSV, предпочтительно вводят свиньям до первого опороса и/или свиноматкам за 2, 3, 4 или 5 недель до спаривания/осеменения, наиболее предпочтительно примерно за 3 недели до спаривания/осеменения. Предпочтительно первую дозу указанной иммуногенной композиции вводят свиньям до первого опороса и/или свиноматкам за 2, 3, 4, 5 или 6 недель до введения второй дозы, наиболее предпочтительно примерно за 3 недели до введения второй дозы. Однако после применения режима двухфазной вакцинации предпочтительно, чтобы свиней до первого опороса и/или свиноматок ревакцинировали каждые 3, 4, 5, 6, 7 или 8 месяцев, наиболее предпочтительно примерно каждые 6 месяцев.
В одном из аспектов настоящего изобретения указанную иммуногенную композицию вводят свиньям до первого опороса и/или свиноматкам во время беременности и лактации.
В одном из аспектов настоящего изобретения иммуногенная композиция безопасна для свиней до первого опороса и/или свиноматок во время беременности и лактации.
Кроме того, утверждается, что вакцина способна защитить племенных свиней до первого опороса и свиноматок при заражении PCV3 в течение всей беременности, или двух триместров, или по меньшей мере одного триместра в течение 114 дней беременности.
Также утверждается, что вакцина способна значительно снизить количество мумифицированных, мертворожденных и слабых плодов у вакцинированных свиней до первого опороса и свиноматок, вакцинированных при заражении PCV3 в течение всей беременности, или двух, или по меньшей мере одного триместра в течение 114 дней беременности.
В одном из аспектов настоящего изобретения иммуногенная композиция безопасна для свиней до первого опороса и/или свиноматок с 30 дней беременности, предпочтительно с 40 дней беременности.
Предпочтительно, иммуногенная композиция, содержащая PCV3, PPV и/или PRRSV, содержит от 0,1 мкг до 150 мкг, предпочтительно от 0,25 мкг до 75 мкг, более предпочтительно от 0,5 мкг до 37,5 мкг, еще более предпочтительно от 0,5 мкг до 15 мкг, наиболее предпочтительно от 0,5 до 6 мкг антигена PCV3, PPV и/или PRRS. Иммуногенная композиция, содержащая PCV3, PPV и/или PRRSV, может находиться в количествах примерно 0,25 мкг; 0,5 мкг; 0,75 мкг; 1 мкг; 1,25 мкг; 1,5 мкг; 1,75 мкг; 2 мкг; 2,25 мкг; 2,5 мкг; 2,75 мкг; 3 мкг; 3,5 мкг; 4 мкг; 4,5 мкг; 5 мкг; 5,5 мкг; 6 мкг; 6,5 мкг; 7 мкг; 7,5 мкг; 8 мкг; 8,5 мкг; 9 мкг; 9,5 мкг; 10 мкг; 10,5 мкг; 11 мкг; 11,5 мкг; 12 мкг; 12,5 мкг; 13 мкг; 13,5 мкг; 14 мкг; 14,5 мкг или 15 мкг.
В одном аспекте настоящего изобретения иммуногенная композиция содержит от 0,1 до 150 мкг антигена VP2 PPV, предпочтительно от 0,5 до 30 мкг иммуногенной композиции, содержащей антигены PCV3, PPV и/или PRRS.
В одном аспекте иммуногенная композиция защищает от гомологичного и/или гетерологичного заражения.
Белок ORF2 PCV3 может продуцироваться системой экспрессии бакуловируса в культивируемых клетках насекомых. Способ может включать инактивацию бакуловируса. Инактивацию проводят способами, известными в данной области техники. Например, при химической инактивации подходящий образец вируса или образец сыворотки, содержащий вирус, обрабатывают в течение достаточного периода времени достаточным количеством или концентрацией инактивирующего агента при достаточно высокой (или низкой, в зависимости от инактивирующего агента) температуре или pH для инактивации вируса. Инактивацию путем нагревания проводят при температуре и в течение периода времени, достаточных для инактивации вируса. Инактивацию облучением проводят с использованием длины волны света или другого источника энергии в течение периода времени, достаточного для инактивации вируса. Вирус считается инактивированным, если он не может заразить восприимчивую к инфекции клетку. Инактивация может включать тепловую обработку или использование агента, инактивирующего вирус. Инактивирующий агент может включать азиридиновое соединение, такое как BEI.
Настоящее изобретение также включает рекомбинантный вектор, содержащий полинуклеотидную последовательность, кодирующую полипептидную последовательность, кодирующую белок ORF2 PCV3. ORF2 PCV3 может быть из группы a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включен в настоящий документ посредством ссылки); см., например, таблицу 4). В другом варианте осуществления белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности или гомологии последовательности с SEQ ID NO: 4. Рекомбинантный вектор может быть бакуловирусом. В другом варианте осуществления рекомбинантный вектор может иметь по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности или гомологии последовательности с SEQ ID NO: 2.
Следует отметить, что в настоящем изобретении, и в частности, в формуле изобретения и/или параграфах такие термины, как «содержит», «содержащийся», «содержащий» и т.п., могут иметь значение, приписываемое им в Патентном законодательстве США; например, они могут означать «включает», «включенный», «включающий» и тому подобное, и что такие термины, как «состоящий по существу из» и «состоит по существу из», имеют значение, приписываемое им в Патентном законодательстве США, например, они допускают элементы, не перечисленные явно, но исключающие элементы, которые встречаются в предыдущем уровне техники или которые влияют на основную или новую характеристику изобретения.
Свинья, молодая свинья или поросенок, которым вводят вакцину, могут иметь антитела против PCV, такие как PCV2 и/или PCV3, например, материнские антитела.
Эти и другие варианты осуществления раскрыты или очевидны из следующего подробного описания и охватываются им.
Следует отметить, что в настоящем изобретении, и в частности, в формуле изобретения и/или параграфах такие термины, как «содержать», «содержит», «содержащий» и т.п., могут иметь значение, приписываемое им в патентном законодательстве США; например, они могут означать «включает», «включенный», «включающий» и тому подобное, и что такие термины, как «состоящий по существу из» и «состоит по существу из», имеют значение, приписываемое им в патентном законодательстве США, например, они допускают элементы, не перечисленные явно, но исключающие элементы, которые встречаются в предыдущем уровне техники или которые влияют на основную или новую характеристику изобретения.
Эти и другие варианты осуществления раскрыты или очевидны из следующего подробного описания и охватываются им.
Краткое описание чертежей
Файл патента или заявки содержит по меньшей мере один чертеж, выполненный в цвете. Копии данного патента или публикации заявки на патент с цветными чертежами будут предоставлены Ведомством по запросу и при уплате необходимой пошлины.
Следующее подробное описание, данное в качестве примера, но не предназначенное для ограничения изобретения только конкретными описанными вариантами осуществления, может быть лучше всего понято в сочетании с прилагаемыми чертежами.
На фигуре 1 показана нуклеотидная последовательность ORF2 PCV3 в рекомбинантном бакуловирусе BaculoG/PCV3 ORF2, SEQ ID NO: 1.
На фигуре 2 показана фигура 2 из WO 2020/206452, содержание которой включено в настоящий документ посредством ссылки. фиг.2 из WO 2020/206452 представляет последовательность рекомбинантного бакуловируса BaculoG/PCV3 ORF2, SEQ ID NO: 2.
На фигуре 3 показана карта рекомбинантного бакуловируса, содержащего ген ORF2 PCV3 под контролем полиэдринового промотора бакуловируса (BaculoG/PCV3 ORF2 Клон 4B4-2E12 Pre-MSV p8).
На фигуре 4 показано медианное значение log10 геномных копий ДНК PCV3/мл в сыворотке крови в день исследования; Группы 1-5.
На фигуре 5 показано медианное значение log10 геномных копий ДНК PCV3/мл по группе в день исследования в образцах фекалий; группы 1-5.
На фигуре 6 показано медианное значение log10 геномных копий ДНК PCV3/мл по группе в день исследования в образцах из носа; группы 1-5.
На фигуре 7 показаны скорректированные по исходному уровню средние ректальные температуры (°F) для группы по способу наименьших квадратов по дням исследования.
На фигуре 8 показаны скорректированные по исходному уровню, средние по группам данные по способу наименьших квадратов для суточного веса (кг) по дням; группы 1-5.
На фигуре 9 показана средняя температура тела (°F) в группе по дням.
На фигуре 10 показана информация о последовательности PCV3 в ПЦР-позитивном гомогенате ткани, использованном для зараженного материала (SEQ ID NO: 3-5).
На фигуре 11 показано среднее значение ПЦР для Групп 1-5 от семи до сорока девяти дней.
На фигуре 12 показано медианное значение ПЦР для Групп 7-9 от семи до сорока девяти дней.
На фигуре 13 показано медианные значения ПЦР для фекалий для групп 1-5 от семи до сорока девяти дней.
На фигуре 14 показаны медианные значения ПЦР для назальных мазков для групп 1-5 от семи до сорока девяти дней
На фигуре 15 показано среднее арифметическое значение ректальной температуры для групп 1-6 с четырнадцати до сорока девяти дней оценки.
На фигуре 16 показаны средние значения температуры по способу наименьших квадратов по группам и дням для групп 1-5.
На фигуре 17 показана линейная диаграмма, показывающая средние ректальные температуры животных (скорректированную на основе наименьших квадратов) по группам и дням для групп 1-5.
На фигуре 18 показаны среднеарифметические значения массы тела для групп 1-6 от четырнадцати до сорока девяти дней.
На фигуре 19 показан линейный график, показывающий средние значения массы тела (по способу наименьших квадратов) по группам и дням для групп 1-5.
На фигуре 20 показан линейный график, изображающий данные для средних значений по способу наименьших квадратов для массы тела (с поправкой на исходный уровень) по группам и дням.
На фигуре 21 показан график истории производства пре-MSV+1.
На фигуре 22A показано количество клеток, а на фигуре 22B показана жизнеспособность и размер клеток во время инфицирования ORF2 BaculoG/PCV3.
На фигуре 23 показан анализ собранных жидкостей ORF2 BaculoG/PCV3.
На фигуре 24 показаны изображения инактивации через 72 часа.
На фигуре 25 показано сравнение способом вестерн-блоттинга условий инактивации антигена ORF2 BaculoG/PCV3 - после инактивации.
На фигуре 26 показан флуоресцентный дот-блоттинг ORF2 PCV3.
На фигуре 27 показан график наблюдаемой виремии в выборке популяции свиней после заражения на основе log10 геномных копий/мл. Все контрольные свиньи были виремическими, как определено с помощью ПЦР в каждой точке отбора проб во время фазы заражения, и вирусная нагрузка в каждой точке отбора проб во время фазы заражения была значительно снижена вакцинацией (P≤0,0050).
На фигуре 28 показан график измеренных средних ректальных температур (°F) до заражения (D12, D13, D14) и после заражения (D14.5-D20).
На фигуре 29 показан график наблюдаемой виремии у свиней до первого опороса, зараженных на Д83 (40 дней беременности). Цифры указывают количество геномных копий/мл. Ось Y отображается в линейном масштабе для точного представления нулевых значений. Стрелки указывают введение первичной вакцины, ревакцинации и контрольного заражения.
На фигуре 30 показана гистограмма, демонстрирующая процент пораженных поросят на основе наблюдаемого числа подвергшихся аутолизу, разрушенных, мумифицированных поросят, рожденных от свиноматок на опоросе в каждой опытной группе.
На фигуре 31 показано выравнивание аминокислотной последовательности капсида PCV3 с капсидом свиного PCV2 и капсидом вируса болезни клюва и пера (BFDV).
На фигуре 33 показана структура мутанта ORF2 PCV3 в петле FG, имеющего мутации в лизинах и гистидинах.
На фигуре 33 показана структура мутанта ORF2 PCV3, в котором нативный стоп-кодон для капсидного белка PCV3 был мутирован, а С-конец был удлинен до следующего стоп-кодона.
На фигуре 34 показаны нуклеотидные и аминокислотные последовательности мутанта ORF2 PCV3 в петле FG, имеющего мутации в лизинах и гистидинах, и мутанта ORF2 PCV3, в котором нативный стоп-кодон для капсидного белка PCV3 был мутирован, а С-конец был удлинен до следующий стоп-кодон (SEQ ID NO: 6-9).
На фигуре 35 показана аминокислотная последовательность мутанта ORF2 PCV3 «FG-PC» (SEQ ID NO: 10).
Подробное описание изобретения
Настоящее изобретение относится к вакцине против PCV3.
Предполагается любая последовательность PCV3. См., например, Phan, Tung Gia, et al. «Detection of a Novel Circovirus PCV3 in Pigs with Cardiac and Multi-Systemic Inflammation». Virology Journal, vol. 13, no. 1, 2016, p. 184, doi:10.1186/s12985-016-0642-z. Published November 11, 2016, и Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3, описание которых включено в качестве ссылки.
Последовательности генома PCV3 ORF2 и PCV3 были получены из KT869077 (GenBank). Был использован полный геном PCV3 в плазмиде, описанный в примерах. ORF2 и весь геном были синтезированы в Genscript.
Две дополнительные конструкции, рециркуляризованные геном PCV3, полученные двумя разными способами, были использованы в культуре клеток для сохранения вируса.
Следующие последовательности представлены в списке последовательностей:
ORF2 PCV3 «FG» представляет собой антигенный белок согласно настоящему изобретению, который включает аминокислотные замены в петле FG природного белка ORF2 PCV3.
PCV3 ORF2 «PC» представляет собой антигенный белок согласно настоящему изобретению, который включает удлинение из аминокислот на С-конце природного белка ORF2 PCV3.
В предпочтительном аспекте полипептид по настоящему изобретению представляет собой рекомбинантный белок ORF2 PCV3, такой как рекомбинантный белок ORF2 PCV3, экспрессируемый бакуловирусом. Используемый здесь термин «рекомбинантный белок ORF2 PCV3», в частности, относится к молекуле белка, которая экспрессируется из молекулы рекомбинантной ДНК, такой как полипептид, который продуцируется способами рекомбинантной ДНК. пример таких способов включает случай, когда ДНК, кодирующую экспрессируемый белок, вставляют в подходящий вектор экспрессии, предпочтительно бакуловирусный вектор экспрессии, который, в свою очередь, используют для трансфекции, или, в случае бакуловирусного вектора экспрессии, для инфицирования клетки-хозяина, с целью производства белка или полипептида, кодируемого ДНК. Термин «рекомбинантный белок ORF2 PCV3», используемый в настоящей заявке, таким образом, в частности, относится к молекуле белка, которая экспрессируется из молекулы рекомбинантной ДНК.
Согласно конкретному примеру, рекомбинантный белок ORF2 PCV3 получают способом со следующими стадиями: ген ORF2 PCV3 клонируют в бакуловирусный вектор переноса; вектор переноса используют для получения рекомбинантного бакуловируса, содержащего указанный ген, путем гомологичной рекомбинации в клетках насекомых, и белок ORF2 PCV3 затем экспрессируется в клетках насекомых во время инфицирования рекомбинантным бакуловирусом.
Также понятно, что термин «рекомбинантный белок PCV3, состоящий из последовательности», в частности, также относится к любой котрансляционной и/или посттрансляционной модификации или модификациям последовательности, на которую воздействует клетка, в которой экспрессируется полипептид. Таким образом, термин «рекомбинантный белок ORF2 PCV3, состоящий из последовательности», как описано в настоящей заявке, также относится к последовательности, имеющей одну или несколько модификаций, произведенных клеткой, в которой экспрессируется полипептид, в частности, модификаций аминокислотных остатков, произведенных в биосинтезе белка и/или процессинге белка, предпочтительно выбранных из группы, состоящей из гликозилирования, фосфорилирования и ацетилирования.
Предпочтительно, рекомбинантный белок ORF2 PCV3 согласно настоящему описанию продуцируется или может быть получен бакуловирусной системой экспрессии, в частности, в культивируемых клетках насекомых.
В еще одном предпочтительном аспекте полипептид по настоящему изобретению представляет собой белок ORF2 PCV3, содержащий или состоящий из аминокислотной последовательности, имеющей по меньшей мере 90%, предпочтительно по меньшей мере 92%, более предпочтительно по меньшей мере 94%, еще более предпочтительно по меньшей мере 96%, еще более предпочтительно по меньшей мере 98%, или, в частности, 100% идентичности последовательности с аминокислотной последовательностью SEQ ID NO: 4.
«Идентичность последовательности», как известно в данной области техники, относится к взаимосвязи между двумя или более полипептидными последовательностями, или двумя или более полинуклеотидными последовательностями, а именно эталонной последовательностью и данной последовательностью, которую нужно сравнить с эталонной последовательностью. Идентичность последовательностей определяют путем сравнения данной последовательности с эталонной последовательностью после того, как последовательности были оптимально выровнены для получения наивысшей степени сходства последовательностей, что определяется соответствием между строками таких последовательностей. После такого выравнивания идентичность последовательностей устанавливают на основе положения за положением, например, последовательности являются «идентичными» в конкретном положении, если в этом положении нуклеотиды или аминокислотные остатки идентичны. Общее количество таких идентичностей положений затем делят на общее количество нуклеотидов или остатков в эталонной последовательности, чтобы получить процент идентичности последовательности. Идентичность последовательности можно легко вычислить известными способами, включая, помимо прочего, способы, описанные в Computational Molecular Biology, Lesk, A. N., ed., Oxford University Press, New York (1988), Biocomputing: Informatics and Genome Projects, Smith, D. W., ed., Academic Press, New York (1993); Computer Analysis of Sequence Data, Part I, Griffin, A. M., and Griffin, H. G., eds., Humana Press, New Jersey (1994); Sequence Analysis in Molecular Biology, von Heinge, G., Academic Press (1987); Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M. Stockton Press, New York (1991), и Carillo, H., and Lipman, D., SIAM J. Applied Math., 48: 1073 (1988), руководства которых включены в настоящую заявку посредством ссылки. Предпочтительные способы определения идентичности последовательностей предназначены для обеспечения максимального совпадения между тестируемыми последовательностями. Способы определения идентичности последовательностей кодифицированы в общедоступных компьютерных программах, которые определяют идентичность последовательностей между данными последовательностями. примеры таких программ включают, без ограничения, пакет программ GCG (Devereux, J., et al., Nucleic Acids Research, 12 (1): 387 (1984)), BLASTP, BLASTN и FASTA (Altschul, SF et al., J. Molec. Biol., 215: 403-410 (1990). Программа BLASTX общедоступна в NCBI и других источниках (BLAST Manual, Altschul, S. et al., NCVI NLM NIH Bethesda, Md. 20894, Altschul, SF et al., J. Molec. Biol., 215: 403-410 (1990), руководства которых включены в настоящую заявку посредством ссылки). Эти программы оптимально выравнивают последовательности, используя размеры гэпов по умолчанию, чтобы получить наивысший уровень идентичности последовательности между данной и эталонной последовательностями. В качестве иллюстрации под полинуклеотидом с нуклеотидной последовательностью, имеющей по меньшей мере, например, 85%, предпочтительно 90%, еще более предпочтительно 95% «идентичности последовательности» с эталонной нуклеотидной последовательностью, подразумевается, что нуклеотидная последовательность данного полинуклеотида идентична эталонной последовательности, за исключением того, что данная полинуклеотидная последовательность может включать до 15, предпочтительно до 10, еще более предпочтительно до 5 точечных мутаций на каждые 100 нуклеотидов эталонной нуклеотидной последовательности. Другими словами, в полинуклеотиде, содержащем нуклеотидную последовательность, имеющую по меньшей мере 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности относительно эталонной нуклеотидной последовательности, до 15%, предпочтительно 10%, еще более предпочтительно 5% нуклеотидов в эталонной последовательности может быть удалено или заменено другим нуклеотидом, или количество нуклеотидов до 15%, предпочтительно 10%, еще более предпочтительно 5% от общего количества нуклеотидов в эталонной последовательности может быть вставлено в эталонную последовательность. Эти мутации эталонной последовательности могут происходить в 5'- или 3'-концевых положениях эталонной нуклеотидной последовательности или в любом месте между этими концевыми положениями, перемежаясь либо индивидуально среди нуклеотидов в эталонной последовательности, либо в одной или нескольких смежных группах в эталонной последовательности. Аналогично, для полипептида, содержащего данную аминокислотную последовательность, имеющую по меньшей мере, например, 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности последовательности с эталонной аминокислотной последовательностью, подразумевается, что данная аминокислотная последовательность полипептида идентична эталонной последовательности, за исключением того, что данная полипептидная последовательность может включать до 15, предпочтительно до 10, еще более предпочтительно до 5 аминокислотных изменений на каждые 100 аминокислот эталонной аминокислотной последовательности. Другими словами, для получения данной полипептидной последовательности, имеющей по меньшей мере 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности последовательности с эталонной аминокислотной последовательностью, до 15%, предпочтительно до 10%, еще более предпочтительно до 5% аминокислотных остатков в эталонной последовательности может быть удалено или заменено другой аминокислотой, или количество аминокислот до 15%, предпочтительно до 10%, еще более предпочтительно до 5% от общего количества аминокислотных остатков в эталонной последовательности может быть вставлено в эталонную последовательность. Эти изменения эталонной последовательности могут происходить в амино- или карбокси-концевых положениях эталонной аминокислотной последовательности или в любом месте между этими концевыми положениями, с вкраплениями либо индивидуально среди остатков в эталонной последовательности, либо в одной или нескольких смежных группах в эталонной последовательности. Предпочтительно, чтобы неидентичные положения остатков различались консервативными аминокислотными заменами. Однако консервативные замены не учитываются при определении идентичности последовательностей.
«Гомология последовательностей» в контексте настоящего описания относится к способу определения родства двух последовательностей. Для определения гомологии последовательностей оптимально выравнивают две или более последовательностей и при необходимости вводят гэпы. Однако, в отличие от «идентичности последовательностей», консервативные аминокислотные замены учитываются как совпадение при определении гомологии последовательностей. Другими словами, для получения полипептида или полинуклеотида, имеющего 95% гомологии последовательности с эталонной последовательностью, 85%, предпочтительно 90%, еще более предпочтительно 95% аминокислотных остатков или нуклеотидов в эталонной последовательности должно соответствовать или содержать консервативную замену другой аминокислотой или нуклеотидом, или рядом аминокислот или нуклеотидов до 15%, предпочтительно до 10%, еще более предпочтительно до 5% от общего числа аминокислотных остатков или нуклеотидов, не включая консервативные замены, в эталонной последовательности могут быть вставлены в эталонную последовательность. Предпочтительно гомологичная последовательность включает по меньшей мере участок из 50, еще более предпочтительно 100, еще более предпочтительно 250, еще более предпочтительно 500 нуклеотидов.
«Консервативная замена» относится к замене аминокислотного остатка или нуклеотида другим аминокислотным остатком или нуклеотидом, имеющим аналогичные характеристики или свойства, включая размер, гидрофобность и т.д., так что общая функциональность существенно не изменяется.
Настоящее изобретение также охватывает мутации белков PCV3, такие как мутации капсидного белка PCV3, но не ограничиваясь ими. Несмотря на расхождение аминокислотных последовательностей капсида между PCV2 и вирусом болезни клюва и пера (BFDV), кристаллические структуры очень похожи, несмотря на расхождение их последовательностей. Предпочтительно мутации PCV3 предназначены для стабилизации вирусоподобных частиц (VLP). Капсидный белок PCV3 должен самособираться в VLP, однако уровень экспрессии белка PCV3 значительно ниже по сравнению с капсидным белком PCV2. В частности, только около 20% белка собирается в VLP, тогда как оставшиеся 80% белка объединяются в нерастворимую фракцию.
В некоторых вариантах осуществления вариантный белок по настоящему изобретению способен давать более высокий выход VLP, чем белок, кодируемый SEQ ID No. 1. Понятно, что более высокий выход, в частности, например, относится к более высокому молярному выходу. Альтернативно экспрессируемый вариантный белок по настоящему изобретению способен к более масштабной сборке VLP CAP (белок капсида (ORF2)), чем белок, кодируемый SEQ ID No. 1. примеры более высоких выходов включают по меньшей мере на 5% увеличенный выход или по меньшей мере на 10% увеличенный выход, или по меньшей мере на 15% увеличенный выход, или по меньшей мере на 20% увеличенный выход, или по меньшей мере на 25% увеличенный выход, или по меньшей мере на 30% увеличенный выход, или по меньшей мере на 35% увеличенный выход, или по меньшей мере на 40% увеличенный выход, или по меньшей мере на 50% увеличенный выход. Таким образом, например, если без модификации белка ORF2 PCV3 путем бакуловирусной экспрессии существует 20% растворимого белка PCV3 (VLP) и 80% нерастворимого белка PCV3, например, по данным вестерн-блоттинга, а при модификации, вместо этого имеется 25%, или 30%, или 35%, или 40%, или 45%, или 50%, или 55%, или 60% или более растворимого белка PCV3 (VLP) (при этом произошло увеличение на 5%, или 10%, или на 15%, или на 20%, или на 25%, или на 30%, или на 35%, или на 40%, или на 45% и т.д. растворимого белка PCV3 (VLP)), то это обеспечивает более высокий выход. Предпочтительно, от модификации белка ORF2 PCV3 выход VLP (растворимые белки PCV3) составляет по меньшей мере 50% от белков PCV3, экспрессируемых рекомбинантной бакуловирусной системой.
Анализы и методики, подходящие для использования в настоящем изобретении, включают те, которые использовались для отслеживания или количественной оценки сборки и разборки белка капсида цирковируса свиней (ORF2) в вирусоподобные частицы (VLP), и они включают иммуноферментный анализ (ИФА), ДСН/ПАГЭ, при необходимости с окрашиванием серебром или красителем кумасси, вестерн-блоттинг или иммуноблоттинг, эксклюзионную хроматографию (SEC), динамическое рассеяние света (DLS) или многоугловое рассеяние света (MALS), трансмиссионную электронную микроскопию (ТЭМ), аналитическое ультра-центрифугирование и флуоресцентный спектроскопический анализ (ФСА), при необходимости в сочетании с высокоэффективной жидкостной хроматографией (ВЭЖХ). Дополнительные подходящие методики могут также включать тесты на замедление образования комплексов белок-нуклеиновая кислота в агарозном геле, тесты иммуннодиффузии, например, одномерную радиальную иммунодиффузию (ОРИД), анализ траекторий движения наночастиц (NTA), метаболическое мечение и хемилюминесцентные анализы на основе ферментов. Каждый из этих анализов хорошо известен в данной области техники и описан, например, в Fang, Mingli et al. «Detection of the Assembly and Disassembly of PCV2b Virus-Like Particles Using Fluorescence Spectroscopy Analysis» Intervirology vol. 58, 2015, pp. 318-323; Thompson, Christine et al. «Analytical technologies for influenza virus-like particle candidate vaccines: challenges and emerging approaches» Virology Journal vol 10, 2013, p. 141; Steppert, Petra et al. «Quantification and characterization of virus-like particles by size-exclusion chromatography and nanoparticle tracking analysis» Journal of Chromatography A vol. 1487, 2017, pp. 89-99; Yadav, Shalini et al. «A facile quantitative assay for viral particle genesis reveals cooperativity in virion assembly and saturation of an antiviral protein» Virology, vol 429, No. 2, 2012, pp. 155-162, и Zeltins, Andris «Construction and Characterization of Virus-Like Particles: A Review» Molecular Biotechnology vol. 53, 2013, pp. 92-107, каждый из которых включен в настоящий документ посредством ссылки во всей полноте.
В одном аспекте вариантный белок по настоящему изобретению способен давать более высокий выход VLP, чем белок, кодируемый SEQ ID No. 1, при определении с помощью вестерн-блоттинга. Другими словами, вариантный белок по настоящему изобретению способен к большей сборке CAP VLP, чем белок, кодируемый SEQ ID No. 1, при определении с помощью вестерн-блоттинга.
В различных вариантах осуществления, обсуждаемых в настоящей заявке, существует мутация или мутации капсидного белка ORF2 PCV3, например, для увеличения выхода VLP. Например, в различных вариантах осуществления в петле FG может быть одна, две, три или четыре мутации. В качестве примеров и обсуждений здесь представлены варианты осуществления, которые могут включать SKKK петли FG белка ORF2 PCV3, замененный на QPFS (например, мотив белка ORF2 PCV2). Выполняя замену (замены), специалист в данной области техники может применить изобретение путем замены только S на Q, или только замены первого K на P, или только замены второго K на F, или только замены третьего K на S, или любых комбинаций из этих замен, например, S на Q и первый K на P или S на Q и второй K на F или S на Q и третий K на S, или S на Q и первый K на P и второй K на F, или S на Q и первый K на P и третий K на S и т.д. Аналогичным образом, в этих вариантах осуществления, в дополнение или в качестве альтернативы замене (заменам) или мутации (мутациям) в петле FG, специалист в данной области техники может осуществить изобретение путем добавления аминокислот к С-концу белка ORF2 PCV3. Без удлинения или добавления на С-конце белок ORF2 PCV3 может быть в трехмерной структуре скрытым, а не экспонированным, как С-конец других цирковирусных ORF2 или капсидных белков. В вариантах осуществления, где имеется удлинение или добавление С-конца белка ORF2 PCV3, может быть выгодным удлинение или добавление к С-концу белка ORF2 PCV3 с мотивом из другого цирковируса, такого как, например, PCV2. Таким образом, например, специалист в данной области техники может удлинить или добавить к C-концу белка ORF2 PCV3 аминокислоты, обнаруженные на C-конце белка ORF2 PCV2 или капсидного белка, такие как аминокислоты 215-234 или 215-233 белка ORF2 PCV2 или капсидного белка. Специалист в данной области техники может удлинить или добавить к белку ORF2 PCV3 или капсидному белку эпитоп (эпитопы) белка ORF2 PCV2 или капсидного белка. В этой связи следует упомянуть Trible et al., “Antibody Recognition of Porcine Circovirus Type 2 Capsid Protein Epitopes after Vaccination, Infection and Disease, Clinical and Vaccine Immunology 18(5): 749-757 (2011) doi:10.1128/CVI.00418-10 (включен в настоящий документ посредством ссылки). Сообщается, что в PCV2 иммунореактивные области белка ORF2 (капсида) находятся между остатками 47 и 85, 165 и 200 и 200 и 233. Реагирующие на антитела области белка ORF2 (капсида) PCV2 находятся между аминокислотами 23 и 43, 71 и 85, 117 и 131, а также 171 и 202. Область белка ORF2 (капсида) PCV2, состоящая из аминокислот с 117 по 131, считается доминирующей областью распознавания антителами, а аминокислоты 156–162, 175–192, 195–202 и 228–223 считаются связанными с распознаванием антителами. Другой эпитоп белка ORF2 (капсида) PCV2 представляет собой 169-STIDYFQPNNKR, например, аминокислоты 169-180 (где аминокислотные остатки Y-173, F-174, Q-175 и K-179 могут способствовать распознаванию антителами). Другими эпитопами белка ORF2 (капсида) PCV2 могут быть аминокислоты 43-233, 43-135, 43-160, 91-160, 43-180, 160-233, 135-233 и 91-233, а также аминокислоты 169-188. Любой из них или любая комбинация этих эпитопов ORF2 PCV2 может быть удлинением С-конца или добавлением к белку ORF2 (капсиду) PCV3. В этом отношении упоминается, что удлинение С-конца ORF2 PCV3 может составлять до примерно 200 аминокислот, или примерно до 190 аминокислот, или примерно до 185 аминокислот, или примерно до 180 аминокислот, или примерно до 175 аминокислот, или примерно до 170 аминокислот, или примерно до 165 аминокислот, или примерно до 160 аминокислот, или примерно до 155 аминокислот, или примерно до 150 аминокислот, или примерно до 145 аминокислот, или примерно до 140 аминокислот, или примерно до 135 аминокислот, или примерно до 130 аминокислот, или примерно до 125 аминокислот, или примерно до 120 аминокислот, или примерно до 115 аминокислот или примерно до 110 аминокислот, или примерно до 105 аминокислот, или примерно до 100 аминокислот, примерно до 90 аминокислот, или примерно до 80 аминокислот, или примерно до 70 аминокислот, или примерно до 60 аминокислот, или примерно до 50 аминокислот, или примерно до 40 аминокислот, или примерно до 30 аминокислот в длину; например, от 1-50 аминокислот, или 10-50 аминокислот, или 10-40 аминокислот, или от 20 до 40 аминокислот, или примерно 30 аминокислот в длину.
В вариантах осуществления, где композиция содержит белок ORF2 (капсид) PCV3 по изобретению, например, такой белок, который был мутирован, например, где мутация включает добавление или удлинение С-конца, например, где добавление или удлинение С-конца включает эпитоп (эпитопы) белка ORF2 (капсида) PCV2, и композиция также включает белок ORF2 (капсид) PCV2 (например, для однократного введения против PCV2 и PCV3 или по показаниям, ими обусловленными, или для лечения симптомов или состояния, например, каждый может быть получен бакуловирусной экспрессией, например, отдельно или с одним или несколькими антигенами патогена свиней, такими как антиген (антигены) или патоген (патогены) свиньи, раскрытые в данном изобретении), причем может быть предпочтительно, чтобы эпитоп (эпитопы) белка ORF2 (капсида) PCV2 были из филогенетической ветви, которая является такой же или отличной от филогенетической ветви белка ORF2 (капсида) PCV2, включенного в композицию. Например, если компонент белка ORF2 (капсида) PCV2 происходит из штаммов PCV2a (на котором основан Ingelvac CircoFlex), может быть предпочтительно, чтобы добавление или удлинение капсидного белка ORF2 PCV3 (C-конец) происходило из другой филогенетической ветви, например, из генотипа PCV2b, PCV2c или PCVd-mPCV2b. В связи с генотипами, штаммами или филогенетической ветвью PCV2 следует упомянуть Franzo et al., «Revisiting the taxonomical classification of Porcine Circovirus type w (PCV2): still a real challenge», Virol J 12: 131 (2015) doi: 10.1186/s12985-015-0361-x (включено в настоящую заявку посредством ссылки). Может быть предпочтительно, чтобы добавление или удлинение С-конца капсидного белка ORF2 PCV3 было той же филогенетической ветви, штамма или генотипа, что и компонент капсидного белка ORF2 PCV2 композиции, или другой филогенетической ветви, штамма или генотипа, но представляло эпитоп капсидного белка ORF2 PCV2, который обеспечивает иммунологический ответ против одной или нескольких филогенетических ветвей, штаммов или генотипов PCV2. В связи с вышеизложенным, и в более общем плане, в связи с мутантными капсидными белками ORF2 PCV3 по настоящему изобретению, обсуждаемыми повсеместно в данном описании, изобретение охватывает молекулы нуклеиновых кислот, кодирующие такие мутантные капсидные белки ORF2 PCV3, векторы, такие как бакуловирусные векторы (см. ЕР 2460821 A2, включенный в настоящее описание посредством ссылки, вместе с документами, цитируемыми в нем, в части способов и материалов для экспрессии капсидного белка ORF2 PCV2 с помощью бакуловирусной системы экспрессии, который можно использовать для осуществления настоящего изобретения для экспрессии капсидного белка ORF2 PCV3, включая такие мутантные белки, как описаны в настоящей заявке, а также капсидный белок ORF2 PCV2, если необходимо включить его в композицию по настоящему изобретению), содержащие такие молекулы нуклеиновых кислот, и способы получения или экспрессии таких мутантных капсидных белков ORF2 PCV3 по настоящему изобретению, например, с помощью инфицирования или трансфекции соответствующих клеток вектором (например, если вектор является бакуловирусом, соответствующая клетка может быть клеткой насекомого, или клеткой Sf, или клеткой Sf+; см. EP 2 460 821 A2, включенный в настоящее описание посредством ссылки, вместе с документами, цитируемыми в нем). Предпочтительно извлекать или выделять белок после экспрессии или продукции, например, путем отделения твердых веществ и сохранения жидкой части или надосадочной жидкости, которая содержит растворимый белок (например, VLP). Композиции, обсуждаемые в этом абзаце, а также во всем этом описании, могут содержать мутантный капсидный белок ORF2 PCV3 (и при необходимости дополнительно капсидный белок ORF2 PCV2 и/или один или несколько дополнительных антигенов патогена свиней) в количествах, обсуждаемых в данном описании, и могут вводиться в режиме (режимах), как обсуждается в данном описании, например, в виде единственной или однократной дозы, и могут вводиться таким образом свиньям или поросятам, как обсуждается в настоящем описании.
В контексте изобретения белок по настоящему изобретению в качестве антигена в композиции, такой как иммунологическая композиция, предотвращает или лечит связанное с инфекцией PCV3 заболевание или состояние у субъекта, например, путем индукции, стимуляции или усиления иммунного ответа против PCV3.
Предыдущие исследования показали, что экспрессия полноразмерного гена кэпа PCV3 и NLS-доменов, присутствующих в N-концевом мотиве, богатом аргинином (ARM), может вызывать неправильное сворачивание белка и индуцировать образование кольцевых вирусных комплексов размером 10-12 нм (Sarker et al. Nat Commun. 2016 Oct 4; 7():13014). Wang et al. (AMB Expr 10, 3 (2020) https://doi.org/10.1186/s13568-019-0940-0) сообщил о способности VLP PCV3 к самосборке, при этом он был успешно экспрессирован в E. coli и применен при разработке ИФА для тестирования специфических антител в клинической сыворотке свиней. В частности, для достижения высокого уровня экспрессии рекомбинантного Cap PCV3 в E. coli, ген полного Cap дикого типа (wt-eCap) был амплифицирован из клинических образцов, и три оптимизированных целых фрагмента Cap (opti-eCap) и один оптимизированный фрагмент гена Cap с удаленным сигналом ядерной локализации (NLS) (opti-dCap), кодирующие ту же аминокислотную последовательность, что и wt-eCap, были синтезированы с учетом предпочтительных кодонов E. coli. В отличие от настоящего изобретения, если не принимать во внимание NLS капсида PCV3, указанные области не разрабатывались с прицелом на сборку и/или стабильность VLP. Кроме того, удаление NLS не обязательно приводит к улучшению сборки VLP. Однако варианты осуществления изобретения могут включать удаление или изменение капсидного белка NLS ORF2 PCV3, например, в дополнение к одной или нескольким мутациям петли FG и/или удлинению (удлинениям) С-конца, обсуждаемым в настоящей заявке.
В предпочтительном варианте осуществления настоящее изобретение охватывает мутантные области, кодирующие положительно заряженные аминокислоты в белках PCV, таких как капсидный белок PCV3, но не ограничиваясь им. В частности, капсид PCV3 содержит большое количество положительного заряда в петле FG, которая находится на границе раздела 5 складки капсида PCV3. Большое количество положительного заряда в этой области может привести к появлению сил отталкивания в отсутствии нуклеиновой кислоты, как и следовало ожидать от VLP. В одном варианте осуществления изобретения положительно заряженные аминокислоты мутируют на нейтральные и/или отрицательно заряженные аминокислоты. В предпочтительном варианте осуществления лизины и гистидин в этой петле мутированы на аминокислоты из капсида PCV2 (SEQ ID NO: 6).
В одном из вариантов осуществления настоящее изобретение относится к сконструированному белку ORF2 PCV3, содержащему уменьшенные количества положительно заряженных аминокислот по сравнению с нети-мышинышининженерным белком ORF2 PCV3. Несконструированный белок может быть белком ORF2 PCV3 дикого типа или природным белком, или может быть белком ORF2, уже модифицированным для другой цели, для которой необходимо улучшить активность образования капсида, например, улучшить самосборку в присутствии или при отсутствии упаковываемого полинуклеотида.
В одном из вариантов осуществления одна или несколько положительно заряженных аминокислот являются замещенными, например, одно или несколько из лизина, аргинина или гистидина, или их комбинации. В одном варианте осуществления заменены две или более положительно заряженных аминокислот. В одном варианте осуществления заменены три или более положительно заряженных аминокислоты. В некоторых вариантах осуществления заряд, связанный с областью белка ORF2, такой как петля FG, но не ограничиваясь этим, становится более отрицательным путем замены одной или нескольких отрицательно заряженных аминокислот. В некоторых вариантах осуществления положительно заряженные аминокислоты заменены аминокислотами, которые заряжены менее положительно, и/или положительно заряженные аминокислоты заменены аминокислотами, заряженными более отрицательно. То есть заряд области ORF2 может быть получен путем изменения за счет удаления положительного заряда, добавления отрицательного заряда, или того и другого.
В предпочтительном варианте осуществления настоящее изобретение включает добавление дополнительных аминокислот к белкам PCV, таким как капсидный белок PCV3, но не ограничиваясь этим. Короткая длина гидрофобного С-конца капсида PCV3 может привести к тому, что С-конец будет скрыт в капсиде, и может привести к нестабильности VLP в отсутствии нуклеиновой кислоты. В противоположность этому, C-конец капсидных белков PCV2 и BFDV выступает из капсида. В одном варианте осуществления С-конец капсида PCV3 удлиняют примерно на 1-50 аминокислот, примерно на 10-40 аминокислот или примерно на 20-30 аминокислот. В другом варианте осуществления C-конец капсида PCV3 удлиняют примерно на 20, примерно на 21, примерно на 22, примерно на 23, примерно на 24, примерно на 25, примерно на 26, примерно на 27, примерно на 28, примерно на 29, примерно на 30, примерно на 31, примерно на 32, примерно на 33, примерно на 34, примерно на 35, примерно на 36, примерно на 37, примерно на 38, примерно на 39 или примерно на 40 аминокислот. В предпочтительном варианте осуществления C-конец капсидного белка PCV3 удлиняют путем мутации стоп-кодона. В особо предпочтительном варианте осуществления природный стоп-кодон для капсидного белка PCV3 мутирован, и С-конец удлинен до следующего стоп-кодона в последовательности вируса (SEQ ID NO: 7). В другом варианте осуществления C-конец капсида PCV может быть удлинен и/или заменен на C-конец других цирковирусов свиней. C-конец капсидного белка PCV3 может быть увеличен по длине примерно от 50 до 200 аминокислот, примерно от 60 до 190 аминокислот, примерно от 70 до 180 аминокислот, примерно от 80 до 170 аминокислот, примерно от 90 до 160 аминокислот, или примерно от 100 до 150 аминокислот.
В некоторых вариантах осуществления C-концевое удлинение включает добавление аминокислот на C-конце капсида PCV3, например, путем мутации стоп-кодона. Стоп-кодон можно мутировать путем делеции, замены или вставки. В некоторых вариантах осуществления C-концевое удлинение включает вставку аминокислот рядом с C-концом, включая вставку аминокислот с одним остатком от C-конца, или двумя остатками от C-конца, или тремя остатками, или четырьмя остатками, или пятью остатками, или шестью, или семью, или восемью, или более остатками перед С-концом, но не ограничиваясь этим. В одном варианте остатки могут представлять собой любой набор отрицательно заряженных аминокислот.
Следует понимать, что белки по изобретению могут отличаться от точных последовательностей, проиллюстрированных и описанных в настоящей заявке. Таким образом, изобретение предусматривает делеции, добавления и замены в показанных последовательностях до той степени, при которой эти последовательности все еще функционируют в соответствии со способами изобретения. В связи с этим особо предпочтительные замены обычно носят консервативный характер, т.е. такие замены, которые происходят в пределах семейства аминокислот. Например, аминокислоты обычно делятся на четыре семейства: (1) кислые - аспартат и глутамат; (2) основные - лизин, аргинин, гистидин; (3) неполярные - аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан, и (4) незаряженные полярные - глицин, аспарагин, глутамин, цистеин, серин, треонин, тирозин. Фенилаланин, триптофан и тирозин иногда классифицируют как ароматические аминокислоты. Обоснованно предсказуемо, что выделенная или неприродная замена лейцина изолейцином или валином, или, наоборот, аспартата глутаматом, или, наоборот, треонина серином, или, наоборот, или аналогичная консервативная замена аминокислоты структурно родственной аминокислотой не будет иметь большого влияния на биологическую активность. Следовательно, белки, имеющие практически такую же аминокислотную последовательность, что и проиллюстрированные и описанные последовательности, но имеющие минорные аминокислотные замены, которые существенно не влияют на иммуногенность белка, входят в объем данного изобретения.
Данное изобретение также включает нуклеотидные последовательности, кодирующие функционально и/или антигенно эквивалентные варианты и производные антигенов по изобретению и их функционально эквивалентные фрагменты. Эти функционально эквивалентные варианты, производные и фрагменты проявляют способность сохранять антигенную активность. Например, изменения в последовательности ДНК, которые не изменяют кодируемую аминокислотную последовательность, а также те, которые приводят к консервативным заменам аминокислотных остатков, одной или нескольким делециям или добавлениям аминокислот и замене аминокислотных остатков на аминокислотные аналоги, являются такими, которые не оказывают существенного влияния на свойства кодируемого полипептида. Консервативные аминокислотные замены - глицин/аланин; валин/изолейцин/ лейцин; аспарагин/глутамин; аспарагиновая кислота/глутаминовая кислота; серин/ треонин/метионин; лизин/аргинин, и фенилаланин/тирозин/триптофан. В одном варианте осуществления варианты содержат по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96 %, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% гомологии или идентичности с представляющим интерес антигеном, эпитопом, иммуногеном, пептидом или полипептидом.
В некоторых вариантах осуществления замена вводит консервативное изменение, которое заменяет аминокислоту другой аминокислотой с аналогичной химической структурой, аналогичными химическими свойствами или аналогичным объемом боковой цепи. Введенные аминокислоты могут иметь полярность, гидрофильность или гидрофобность, сходную с аминокислотами, которые они заменяют. Консервативные замены аминокислот хорошо известны в данной области техники. Если аминокислоты имеют сходную полярность, это также можно определить по шкале гидрофобности для боковых цепей аминокислот.
Консервативные аминокислотные изменения также могут быть определены посредством ссылки на семейство оценочных матриц Point Accepted Mutation (PAM) или BLOcks Substitution Matrix (BLOSUM) для сохранения аминокислотной последовательности. Таким образом, консервативные аминокислотные изменения могут быть членами группы эквивалентности, представляющей собой набор аминокислот, имеющих взаимно положительные оценки в представлении сходства оценочной матрицы, выбранной для использования при выравнивании эталонных и мутантных полипептидных цепей.
Следует понимать, что неполярные аминокислоты включают аминокислоты с алифатическими боковыми цепями и аминокислоты с ароматическими боковыми цепями. Аминокислота пролин классифицируется как неполярная, но она также обладает свойством жесткости и может вызывать изменения во вторичной структуре. Например, пролины часто находятся на концах спиралей. Кроме того, в зависимости от конкретного контекста боковой цепи данного аминокислотного остатка, например, аминокислоты тирозина, обычно классифицируемого как неполярный из-за его ароматического кольца, может иметь функциональные эффекты, аналогичные полярным аминокислотным остаткам, таким как треонин через его гидроксильную группу. Таким образом, для целей изобретения тирозин можно рассматривать как неполярную, так и полярную аминокислоту. Кроме того, аминокислоты, которые описываются как полярные или гидрофильные, могут быть незаряженными или заряженными, а также могут быть основными или кислотными. Хорошо известно, что аминокислота гистидин имеет значение pKa около 7, так что при нейтральном pH в зависимости от белковой среды он может быть протонирован или не протонирован на своей боковой цепи и, таким образом, может нести или не нести заряд. Таким образом, для целей изобретения гистидин можно рассматривать как полярно заряженный или полярный незаряженный аминокислотный остаток.
Обсуждаемые здесь мутации обычно вводят в белок с использованием способов, известных в данной области техники, таких как сайт-направленный мутагенез белка, ПЦР и способы перетасовки генов, или с использованием множественных мутагенных олигонуклеотидов в циклах сайт-направленного мутагенеза. Таким образом, мутации могут вводиться направленным или случайным образом. Таким образом, способ мутагенеза дает один или несколько полинуклеотидов, кодирующих один или несколько различных мутантов.
Разработка рекомбинантного бакуловируса, содержащего ген ORF2 свиного цирковируса 3, под контролем бакуловирусного полиэдринового промотора (BaculoG/PCV3 ORF2 Clone 4B4-2E12 Pre-MSV p8; лот № 3624-039) описана в примере 1. В некоторых вариантах осуществления использование такого рекомбинантного бакуловируса, описанного в примере 1, в вакцине может включать убитые и/или инактивированные версии рекомбинантного вируса. Альтернативно, в некоторых вакцинах рекомбинантный вирус, например, подобный тому, который показан в примере 1, может использоваться как живой модифицированный вирус.
На фиг.1B представлена последовательность ORF2 рекомбинантного бакуловируса BaculoG/PCV3, SEQ ID NO: 2. Аннотации для основных последовательностей взяты из записи Genbank NC_001623. Специалист в данной области техники поймет, что от конструкции к конструкции следует ожидать незначительные мутации в основной цепи, учитывая сложность последовательности ДНК. Карта конструкции показана на фиг.2. Вектор экспрессии бакуловируса, BaculoG/PCV3 ORF2, может быть использован для разработки вакцин против PCV3 и/или контролей. Предпочтительные адъюванты для данной вакцины и/или контроля могут различаться в зависимости от типа используемого вектора экспрессии, например, для живой, живой модифицированной, инактивированной или убитой вакцины. Эффективность адъюванта может варьировать в зависимости от статуса используемого вектора (например, вируса). Количество адъюванта, используемого в вакцине, может быть заранее определено, например, заранее определенный процент может быть выбран так, чтобы он находился в заданном диапазоне (например, массовый процент и/или объемный процент в вакцине) для данного адъюванта и/или комбинации адъювантов. В некоторых случаях, например, при использовании живых вакцин можно использовать несколько адъювантов. Например, в некоторых вариантах осуществления может использоваться комбинация адъювантов, таких как карбопол и Montanide ISA 207VG. Альтернативно, вакцина, которая включает живой вектор экспрессии, такой как BaculoG/PCV3 ORF2, может быть дополнена адъювантом ISA 207VG и/или карбополом. Например, адъювант может присутствовать в вакцине в заранее определенной концентрации. Например, вакцина может содержать ISA 207VG в концентрации 50% от массы вакцины. Альтернативно, другая вакцина, включающая живую ORF2 BaculoG/PCV3, может включать адъювант, такой как карбопол, в количестве 20% от объема вакцины.
Вакцины, которые включают убитые векторы экспрессии, такие как вирусы, могут включать карбопол в качестве адъюванта. Например, вакцина, которая включает убитый ORF2 BaculoG/PCV3, может в некоторых вариантах осуществления включать карбопол в качестве эффективного адъюванта. Например, такая вакцина может включать заранее определенное количество адъюванта, например, заранее определенный массовый или объемный процент вакцины. В частности, вакцина, которая включает убитый ORF2 BaculoG/PCV3, может включать карбопол в количестве 20% от объема вакцины. В качестве альтернативы вакцина может включать убитый ORF2 BaculoG/PCV3 и адъювант в количестве примерно 50% от массы раствора вакцины. Например, вакцина, которая включает убитый BaculoG/PCV3 ORF2, может включать ISA 207VG в качестве адъюванта в предварительно определенном массовом проценте вакцины, таком как пятьдесят процентов.
Например, бакуловирусный вектор экспрессии BaculoG/PCV3 ORF2 был использован для разработки двух вакцин против PCV3 и контроля, как описано в настоящей заявке.
Разработка BaculoG/PCV3 ORF2, P9; живой вакцины с адъювантом 50% ISA 207VG (способы, использованные для разработки вакцины, раскрыты в примере 3).
Разработка BaculoG/PCV3 ORF2, P9; живой вакцины с адъювантом 20% карбополом (способы, использованные для разработки вакцины, раскрыты в примере 4).
Разработка контроля - BaculoG/без вставки, P4; живой вакцины с адъювантом 20% карбополом (способы, использованные для разработки вакцины, раскрыты в примере 5).
Разработка BaculoG/PCV3 ORF2, P9; убитой вакцины с адъювантом 50% ISA 207VG (способы, использованные для разработки вакцины, раскрыты в примере 3).
Разработка BaculoG/PCV3 ORF2, P9; убитой вакцины с адъювантом 20% карбополом (способы, использованные для разработки вакцины, раскрыты в примере 4).
Разработка контроля - BaculoG/без вставки, P4; убитой вакцины с адъювантом 20% карбополом (способы, использованные для разработки вакцины, раскрыты в примере 5).
Эффективность вакцин можно тестировать с использованием целого вируса PCV3 и ткани, положительной по результатам ПЦР (небольшое количество). Гомогенаты из тканей могут быть получены и секвенированы. Гомогенаты и/или целый вирус можно использовать для заражения вакцинированных животных.
Например, для того, чтобы проверить эффективность вакцин, были предоставлены целый вирус PCV3 и ПЦР-положительная ткань (небольшое количество). Были получены и секвенированы гомогенаты из тканей. Гомогенаты и целый вирус использовали для заражения вакцинированных животных.
Вакцина с субъединицей рекомбинантного белка ORF2 PCV3 и/или иммуногенная композиция из настоящего изобретения может быть получена с использованием способа из WO 2006/072065, пример 1, модифицированного для экспрессии белка ORF2 PCV3 (а не белка ORF2 PCV2).
Кодирующая последовательность ORF2 PCV3 может быть амплифицирована с помощью полимеразной цепной реакции (ПЦР) из геномной ДНК PCV3 и/или синтетической ORF2 PCV3. Сайты рестрикции можно использовать для вставки необходимой кодирующей последовательности в вектор переноса. Например, в некоторых вариантах осуществления амплифицированная кодирующая последовательность ORF2 PCV3 может включать консенсусную последовательность Козака (см., например, Kozak M (October 1987) Nucleic Acids Res. 15 (20): 8125-8148) сразу за 5' стартового кодона вместе с фланкирующими сайтами рестрикционных ферментов.
В некоторых вариантах осуществления амплифицированная кодирующая последовательность ORF2 PCV3 может быть субклонирована в бакуловирусный вектор переноса с использованием фланкирующих сайтов рестрикции для создания необходимого вектора переноса. Например, амплифицированная кодирующая последовательность ORF2 PCV3 может быть субклонирована в бакуловирусный вектор переноса с использованием фланкирующих сайтов рестрикции для создания векторов переноса, таких как ORF2 pVL1392-PCV3 или ORF2 pVL1393-PCV3. Могут использоваться другие векторы переноса, широко известные в данной области техники. Рекомбинантный бакуловирус может быть получен путем котрансфекции клеток насекомых вектором переноса и ДНК бакуловируса. Используемая ДНК бакуловируса может включать линеаризованную и/или кольцевую ДНК бакуловируса. Например, в одном из вариантов осуществления рекомбинантный бакуловирус может быть получен путем котрансфекции клеток насекомых Sf9 (Spodoptera frugiperda) вектором переноса (например, таким как pVL1392-PCV3 ORF2 и/или pVL1393-PCV3) и линеаризованной ДНК бакуловируса BaculoGoldTM. Линеаризованная ДНК бакуловируса может происходить из вируса ядерного полиэдроза Autographa californica (AcNPV) и может содержать летальную делецию в локусе полиэдрина, поэтому сохранение жизнеспособного бакуловируса может быть произведено при котрансфекции вектором переноса, таким как pVL1392-PCV3. ORF2 и/или pVL1393-PCV3 ORF2. Полученный рекомбинантный бакуловирус может включать кодирующую последовательность ORF2 PCV3 под контролем полиэдринового промотора бакуловируса. Рекомбинантный бакуловирус можно амплифицировать в клетках насекомых Sf9 и затем очистить путем клонирования с лимитирующими разведениями на клетках насекомых Sf9. В некоторых вариантах осуществления может использоваться полноразмерная кольцевая ДНК бакуловируса, такая как Bac-to-Bac. Например, Bac-to-Bac может использовать опосредованную транспозоном рекомбинацию для вставки интересующего гена в полиэдриновый локус. Также можно использовать другие способы, известные в данной области техники. В некоторых вариантах осуществления способ может быть выбран с учетом потенциальной воспроизводимости способа во время коммерциализации. Например, могут быть выбраны бакуловирусы, которые придают вакцине повышенную стабильность.
В некоторых вариантах осуществления после посева во флаконы с культурой основных клеток флаконы можно инкубировать при заданной температуре и в течение определенного периода времени. Например, культуру можно инкубировать при 27°C в течение четырех часов. Затем в каждую колбу можно засеять рекомбинантный бакуловирус, содержащий ген ORF2 PCV3. Например, плазмида pVL1392, содержащая ген ORF2 PCV3, может быть котрансфицирована ДНК бакуловируса BaculoGold® (BD Biosciences Pharmingen) в клетках насекомых Sf+ (Protein Sciences, Мериден, Коннектикут) для получения рекомбинантного бакуловируса, содержащего ген ORF2 PCV3. Рекомбинантный бакуловирус, содержащий ген ORF2 PCV3, может быть очищен от бляшек, и исходный вакцинный вирус (MSV) может быть размножен на линии клеток SF+, разделен на аликвоты и хранится при -70°C. MSV может быть положительно идентифицирован как бакуловирус ORF2 PCV3 с помощью ПЦР-ПДРФ с использованием праймеров, специфичных для бакуловируса. Клетки насекомых, инфицированные бакуловирусом ORF2 PCV3 для генерации MSV или рабочего вируса для посева, могут экспрессировать антиген ORF2 PCV3, выявляемый поликлональной сывороткой или моноклональными антителами в непрямом флуоресцентном анализе антител. Кроме того, идентичность бакуловируса ORF2 PCV3 может быть подтверждена N-концевым аминокислотным секвенированием. Бакуловирус MSV ORF2 PCV3 также тестируют на чистоту в соответствии с 9 C.F.R., Разделы 113.27(c), 113.28 и 113.55. Каждый рекомбинантный бакуловирус, засеянный во флаконы с перемешиванием, может иметь различную множественность инфицирования (MOI).
После посева бакуловируса флаконы можно инкубировать при 27±2°C в течение 7 дней, а также в течение этого времени можно перемешивать со скоростью 100 об./мин. Во флаконах можно использовать вентилируемые колпачки для обеспечения потока воздуха. Образцы из каждого флакона можно брать каждые 24 часа в течение следующих 7 дней. После экстракции каждый образец можно центрифугировать, отделить осадок и надосадочную жидкость, а затем подвергнуть микрофильтрации через мембрану с размером пор 0,45-1,0 мкм.
Количество ORF3 в полученных образцах затем может быть определено количественно с помощью ИФА. Анализ ИФА можно проводить с антителом против PCV3, разведенным до 1:6000 в 0,05 М карбонатном буфере (pH 9,6). Затем 100 мкл антитела можно поместить в лунки планшета для микротитрования, закрыть и инкубировать в течение ночи при 37°С. Затем планшет трижды промывают промывочным раствором, который содержит 0,5 мл Твин 20 (Sigma, Сент-Луис, Миссури), 100 мл 10 D-PBS (Gibco Invitrogen, Карлсбад, Калифорния) и 899,5 мл дистиллированной воды. Затем в каждую лунку добавляют 250 мкл блокирующего раствора (5 г обезжиренного сухого молока (Nestle, Глендейл, Калифорния) в 10 мл D-PBS QS на 100 мл с дистиллированной водой). Следующим шагом является промывание тестового планшета и добавление предварительно разведенного антигена. Предварительно разведенный антиген получают путем добавления 200 мкл раствора разбавителя (0,5 мл Твин 20 в 999,5 мл фосфатно-солевой буфер Дульбекко (D-PBS)) в каждую лунку на планшете для разведения. Затем образец разбавляют в соотношении 1:240 и 1:480, и затем 100 мкл каждого из этих разбавленных образцов добавляют в одну из верхних лунок на планшете для разведения (т.е. в одну верхнюю лунку помещают 100 мкл разведения 1:240, а в другую лунку 100 мкл разведения 1:480). Затем можно выполнить последовательные разведения для оставшейся части планшета, удалив 100 мкл из каждой последующей лунки и перенеся их в следующую лунку на планшете. В каждой лунке осуществляют перемешивание перед следующим переносом. Промывание тестового планшета включает трехкратное промывание планшета промывочным буфером. Затем планшет герметично закрывают и инкубируют в течение часа при 37°C, а затем еще трижды промывают промывочным буфером. Используемое антитело для обнаружения представляет собой антитело к ORF2 PCV. Его разбавляют до 1–300 в растворе разбавителя, и затем в лунки добавляют 100 мкл разведенного проявляющего антитела. Затем планшет герметично закрывают и инкубируют в течение часа при 37°C перед трехкратным промыванием промывочным буфером. Затем готовят разбавитель для конъюгата, добавляя нормальную кроличью сыворотку (Jackson Immunoresearch, Вест-Гроув, Пенсильвания) к раствору разбавителя до концентрации 1%.
Конъюгат антитных способовмышиного козьего антитела (H+1) и пероксидазы хрена (Jackson Immunoresearch) разводят в разбавителе для конъюгата до 1:10 000. Затем в каждую лунку добавляют 100 мкл разведенного конъюгата антител. Затем планшет герметично закрывают и инкубируют в течение 45 минут при 37°C перед трехкратным промыванием промывочным буфером. В каждую лунку добавляют 100 мкл субстрата (TMB Peroxidase Substrate, Kirkgaard and Perry Laboratories (KPL), Гейтерсберг, Мэриленд), смешанного с равным объемом пероксидазного субстрата B (KPL). Планшет инкубируют при комнатной температуре в течение 15 минут. Затем во все лунки добавляют 100 мкл раствора 1 н HCl, чтобы остановить реакцию. Затем планшет пропускают через считывающее устройство для ИФА.
Предпочтительные клетки насекомых можно культивировать и продуцировать белок ORF2 PCV3 в бессывороточных условиях, например, бессывороточные клетки насекомых согласно US 6 103 526 (линия клеток expresSF+).
Предусмотрены адъюванты, надосадочные жидкости клеточных культур, консерванты, стабилизирующие агенты, вирусные векторы, иммуномодулирующие агенты и дозировки, раскрытые в патентах США № 9610345 и 9669087, оба включены в настоящее описание посредством ссылки.
Используемая в настоящей заявке иммуногенная композиция эффективна для индукции иммунного ответа против PCV3 и предотвращения, снижения и/или уменьшения тяжести клинических симптомов, связанных с инфекцией PCV3. Композиция обычно содержит по меньшей мере один антиген PCV3.
PCV3 у молодых свиней может проявлять широкий спектр симптомов, и во многих случаях отдельные животные проявляют лишь небольшую часть потенциальных симптомов. Симптомы, связанные с присутствием PCV3, включают виремию, выделение вируса, например, присутствие вирусных нуклеиновых кислот в выделениях из организма, таких как молозиво, молоко, фекалии, слюна и мазки из глаз. Например, Jiang et al., «Induction of porcine dermatitis and nephropathy syndrome in piglets by infection with porcine circovirus type 3», J. Virol. doi:10.1128/JVI.02045-18, описание которого включено в качестве ссылки, относится к инокуляции поросят PCV3 и наблюдению за результирующими клиническими признаками. Настоящее изобретение относится к лечению и/или уменьшению симптомов дерматита свиней и синдрома нефропатии (PDNS)-подобного заболевания свиней, лимфоцитарной дисплазии и некроза у свиней, вызванных PCV3, путем введения композиции по изобретению.
Простое присутствие антител, особенно у молодых свиней или поросят, например, свиней или поросят в возрасте менее 15 недель, например, в возрасте менее 10 недель, например, в возрасте менее 6 недель, например, менее 3, 2 или 1 недели или при рождении, может не указывать на контакт с PCV3 и/или заболевание. Молодые свиньи или поросята, которые подверглись воздействию и/или имеют антитела против PCV3, все еще могут получить пользу от композиций согласно настоящему описанию, например, за счет уменьшения, предотвращения или снижения тяжести симптомов.
Таким образом, композиции согласно настоящему описанию могут быть использованы в способах индукции иммунного ответа, который может быть защитным иммунным ответом, а также в способах уменьшения или предотвращения, или снижения тяжести симптомов, а также в дозировках, составах и тому подобном для уменьшения, предотвращения или снижения тяжести симптомов, как и для способов вызова иммунного ответа. Таким образом, в настоящей заявке, где описаны способы индукции иммунного ответа, эти способы можно применять на практике для уменьшения, предотвращения или снижения тяжести симптомов, и описанные здесь композиции, которые полезны для индукции иммунного ответа, также применимы и для композиций, предназначенных для уменьшения, предотвращения или снижения тяжести симптомов (а также в качестве композиций для индукции иммунного ответа).
Если не указано иное, все технические и научные термины, используемые в настоящей заявке, имеют те же значения, которые обычно понимаются рядовым специалистом в области техники, к которой принадлежит это изобретение. Используемый здесь термин «иммуногенная композиция» относится к любой фармацевтической композиции, содержащей антиген PCV3, и эта композиция может быть использована для предотвращения или лечения заболевания или состояния, связанного с инфекцией PCV3, у субъекта. Предпочтительная иммуногенная композиция может индуцировать, стимулировать или усиливать иммунный ответ против PCV3. Таким образом, термин охватывает как субъединичные иммуногенные композиции, как описано ниже, так и композиции, содержащие полностью убитый или ослабленный и/или инактивированный PCV3.
Термин «субъединичная иммуногенная композиция» в контексте настоящего описания относится к композиции, содержащей по меньшей мере один иммуногенный полипептид или антиген, но не все антигены, происходящие от антигена из PCV3 или гомологичные ему. Такая композиция практически не содержит интактного PCV3. Таким образом, «субъединичную иммуногенную композицию» получают из по меньшей мере частично очищенных или фракционированных (предпочтительно в значительной степени очищенных) иммуногенных полипептидов из PCV3 или их рекомбинантных аналогов. Субъединичная иммуногенная композиция может содержать субъединичный антиген или представляющие интерес антигены, по существу свободные от других антигенов или полипептидов из PCV3, или во фракционированной форме. Предпочтительная иммуногенная субъединичная композиция включает белок ORF2 PCV3, как описано ниже.
«Иммунологический или иммунный ответ» на композицию или вакцину представляет собой развитие у хозяина клеточного и/или опосредованного антителами иммунного ответа на интересующую композицию или вакцину. Обычно «иммунный ответ» включает один или несколько из следующих эффектов: выработка или активация антител, В-клеток, хелперных Т-клеток, супрессорных Т-клеток и/или цитотоксических Т-клеток и/или γδ T клеток, специально направленных на антиген или антигены, включенные в интересующую композицию или вакцину, но не ограничивается этим. Предпочтительно, чтобы хозяин проявлял либо терапевтический, либо защитный иммунологический ответ, так что устойчивость к новой инфекции будет увеличиваться, и/или будет уменьшаться клиническая тяжесть заболевания. Такая защита будет продемонстрирована либо уменьшением количества или тяжести, либо отсутствием одного или нескольких симптомов, связанных с инфекциями PCV3, как описано выше.
Термины «иммуногенный» белок или полипептид, или «антиген» в контексте настоящего описания относятся к аминокислотной последовательности, которая вызывает иммунологический ответ, как описано выше. «Иммуногенный» белок или полипептид, как здесь используется, включает полноразмерную последовательность любых белков PCV3, их аналогов или их иммуногенных фрагментов. Термин «иммуногенный фрагмент» относится к фрагменту белка, который включает один или несколько эпитопов и, таким образом, вызывает иммунологический ответ, описанный выше. Такие фрагменты можно идентифицировать с использованием любого количества способов картирования эпитопов, хорошо известных в данной области техники. См., например, «Epitope Mapping Protocols» in «Methods in Molecular Biology», Vol. 66 (Glenn E. Morris, Ed., 1996) Humana Press, Totowa, N.J. Например, линейные эпитопы могут быть определены путем одновременного синтеза большого количества пептидов на твердых носителях, где пептиды соответствуют частям белковой молекулы, и взаимодействия пептидов с антителами, пока пептиды все еще прикреплены к подложкам. Такие способы известны в данной области техники и описаны, например, в патентах США 4,708,871; Geysen et al. (1984) Proc. Natl. Acad. Sci. USA 81:3998-4002; Geysen et al. (1986) Molec. Immunol. 23:709-715, все они включены в настоящую заявку посредством ссылки. Точно так же конформационные эпитопы легко идентифицируются путем определения пространственной конформации аминокислот, например, с помощью рентгеновской кристаллографии и 2-мерного ядерного магнитного резонанса. См., например, Epitope Mapping Protocols, выше.
Синтетические антигены также включены в определение, например, полиэпитопы, фланкирующие эпитопы и другие рекомбинантные или синтетические антигены. См., например, Bergmann et al. (1993) Eur. J. Immunol. 23:2777-2781; Bergmann et al. (1996), J. Immunol. 157:3242-3249; Suhrbier, A. (1997), Immunol. and Cell Biol. 75:402-408; Gardner et al., (1998) 12th World AIDS Conference, Geneva, Switzerland, Jun. 28-Jul. 3, 1998.
В предпочтительном варианте осуществления настоящего изобретения обеспечивается иммуногенная композиция, которая индуцирует иммунный ответ и, более предпочтительно, обеспечивает защитный иммунитет против клинических признаков инфекции PCV3. Композиция наиболее предпочтительно содержит полипептид или его фрагмент, экспрессируемый ORF2 PCV3, в качестве антигенного компонента композиции. ДНК и белок ORF2 PCV3, используемые в настоящей заявке для приготовления композиций и в рамках процессов, представленных в настоящей заявке, представляют собой высоко консервативный домен в изолятах PCV3, и, таким образом, любая ORF2 PCV3 будет эффективна в качестве источника ДНК и/или полипептида ORF2 PCV3, как используется здесь. Предпочтительный белок ORF2 PCV3 транслируется с нуклеотидной последовательности SEQ ID NO. 1. В настоящей заявке представлен предпочтительный полипептид ORF2 PCV3, но специалистам в данной области техники понятно, что эта последовательность может варьироваться в пределах 6-10% по гомологии последовательностей и при этом сохранять антигенные характеристики, которые делают ее полезной в иммуногенных композициях. Более того, антигенная характеристика модифицированного антигена все еще сохраняется, когда модифицированный антиген дает по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 100% защитного иммунитета по сравнению с белком ORF2 PCV3, кодируемым полинуклеотидной последовательностью SEQ ID NO: 1. «Иммуногенная композиция» в контексте настоящего описания означает белок ORF2 PCV3, который вызывает «иммунологический ответ» у хозяина клеточного и/или опосредованного антителами иммунного ответа на белок ORF2 PCV3. Предпочтительно эта иммуногенная композиция способна вызывать или усиливать иммунный ответ против PCV3, тем самым обеспечивая защитный иммунитет против инфекции PCV3 и снижая частоту, тяжесть или предотвращая один или несколько, а предпочтительно все связанные с этим клинические признаки.
В некоторых формах иммуногенные части белка ORF2 PCV3 используются в качестве антигенного компонента в композиции. Используемый здесь термин «иммуногенная часть» относится к усеченным и/или замещенным формам или фрагментам белка ORF2 PCV3 и/или полинуклеотида, соответственно. Предпочтительно такие усеченные и/или замещенные формы или фрагменты будут содержать по меньшей мере 6 смежных аминокислот из полноразмерного полипептида ORF2. Более предпочтительно, усеченные или замещенные формы или фрагменты будут содержать по меньшей мере 10, более предпочтительно по меньшей мере 15 и еще более предпочтительно по меньшей мере 19 смежных аминокислот из полноразмерного полипептида ORF2. Кроме того, понятно, что такие последовательности могут быть частью более крупных фрагментов или усеченных форм.
Другой предпочтительный полипептид ORF2 PCV3, представленный в настоящей заявке, кодируется нуклеотидной последовательностью SEQ ID NO: 1. Однако специалистам в данной области техники понятно, что эта последовательность может варьироваться в пределах 6-20% по гомологии последовательностей и при этом сохранять антигенные характеристики, которые делают её полезной в иммуногенных композициях. В некоторых формах в качестве антигенного компонента в композиции используют усеченную или замещенную форму или фрагмент этого полипептида PVC3 ORF2. Предпочтительно такие усеченные или замещенные формы или фрагменты будут содержать по меньшей мере 18 смежных нуклеотидов из полноразмерной нуклеотидной последовательности ORF2. Более предпочтительно, усеченные или замещенные формы или фрагменты будут иметь по меньшей мере 30, более предпочтительно по меньшей мере 45 и еще более предпочтительно по меньшей мере 57 смежных нуклеотидов полноразмерной нуклеотидной последовательности ORF2, например SEQ ID NO: 1.
«Идентичность последовательности», как известно в данной области техники, относится к взаимосвязи между двумя или более полипептидными последовательностями, или двумя или более полинуклеотидными последовательностями, а именно, эталонной последовательностью и данной последовательностью, которую нужно сравнить с эталонной последовательностью. Идентичность последовательностей определяют путем сравнения данной последовательности с эталонной последовательностью после того, как последовательности были оптимально выровнены для получения наивысшей степени сходства последовательностей, что определяется соответствием между нитями таких последовательностей. После такого выравнивания идентичность последовательностей подтверждают на основе положения за положением, например, последовательности «идентичны» в конкретном положении, если в этом положении нуклеотиды или аминокислотные остатки идентичны. Общее количество таких идентичностей положений затем делят на общее количество нуклеотидов или остатков в эталонной последовательности, чтобы получить процент идентичности последовательности. Идентичность последовательности можно легко вычислить известными способами, включая, помимо прочего, способы, описанные в Computational Molecular Biology, Lesk, A. N., ed., Oxford University Press, New York (1988), Biocomputing: Informatics and Genome Projects, Smith, D. W., ed., Academic Press, New York (1993); Computer Analysis of Sequence Data, Part I, Griffin, A. M., and Griffin, H. G., eds., Humana Press, New Jersey (1994); Sequence Analysis in Molecular Biology, von Heinge, G., Academic Press (1987); Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M. Stockton Press, New York (1991); and Carillo, H., and Lipman, D., SIAM J. Applied Math., 48: 1073 (1988), руководства которых включены в настоящую заявку посредством ссылки. Предпочтительными способами определения идентичности последовательностей являются такие, которые разработаны таким образом, чтобы обеспечить совпадение между тестируемыми последовательностями в наиболее длинном участке. Способы определения идентичности последовательностей кодифицированы в общедоступных компьютерных программах, которые определяют идентичность последовательностей между данными последовательностями. Примеры таких программ включают, помимо прочего, пакет программ GCG Devereux, J., et al., Nucleic Acids Research, 12(1):387 (1984)), BLASTP, BLASTN and FAS TA (Altschul, S. F. et al., J. Molec. Biol., 215:403-410 (1990). Программа BLASTX общедоступна в NCBI и других источниках (BLAST Manual, Altschul, S. et al., NCVI NLM NIH Bethesda, Md. 20894, Altschul, SF et al., J. Molec. Biol., 215: 403-410 (1990), руководства которых включены в настоящее описание посредством ссылки). Эти программы оптимально выравнивают последовательности, используя веса гэпов по умолчанию для получения наивысшего уровня идентичности последовательностей между данной и эталонной последовательностями. В качестве иллюстрации для полинуклеотида, имеющего нуклеотидную последовательность, имеющую по меньшей мере, например, 85%, предпочтительно 90%, еще более предпочтительно 95% «идентичности последовательности» по отношению к эталонной нуклеотидной последовательности, предполагается, что нуклеотидная последовательность данного полинуклеотида идентична эталонной последовательности, за исключением того, что указанная полинуклеотидная последовательность может включать до 15, предпочтительно до 10, еще более предпочтительно до 5 точечных мутаций на каждые 100 нуклеотидов эталонной нуклеотидной последовательности. Другими словами, в полинуклеотиде, имеющем нуклеотидную последовательность, имеющую по меньшей мере 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности относительно эталонной нуклеотидной последовательности, до 15%, предпочтительно 10%, еще более предпочтительно 5% нуклеотидов в эталонной последовательности может быть удалено или заменено другим нуклеотидом, или количество нуклеотидов до 15%, предпочтительно до 10%, еще более предпочтительно до 5% от общего количества нуклеотидов в эталонной последовательности может быть вставлено в эталонную последовательность. Эти мутации эталонной последовательности могут происходить в 5’- или 3’-концевых положениях эталонной нуклеотидной последовательности или в любом месте между этими концевыми положениями, либо располагаясь по отдельности среди нуклеотидов в эталонной последовательности, либо смежно в одной или нескольких группах в эталонной последовательности. Аналогично, для полипептида, содержащего данную аминокислотную последовательность, имеющую по меньшей мере, например, 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности последовательности с эталонной аминокислотной последовательностью, подразумевается, что данная аминокислотная последовательность полипептида идентична эталонной последовательности, за исключением того, что данная полипептидная последовательность может включать до 15, предпочтительно до 10, еще более предпочтительно до 5 аминокислотных изменений на каждые 100 аминокислот эталонной аминокислотной последовательности. Другими словами, для получения данной полипептидной последовательности, имеющей по меньшей мере 85%, предпочтительно 90%, еще более предпочтительно 95% идентичности последовательности с эталонной аминокислотной последовательностью, до 15%, предпочтительно до 10%, еще более предпочтительно до 5% аминокислотных остатков в эталонной последовательности могут быть удалены или заменены другой аминокислотой, или количество аминокислот до 15%, предпочтительно до 10%, еще более предпочтительно до 5% от общего количества аминокислотных остатков в эталонной последовательности может быть вставлено в эталонную последовательность. Эти изменения эталонной последовательности могут происходить в амино- или карбокси-концевых положениях эталонной аминокислотной последовательности или в любом месте между этими концевыми положениями, либо по отдельности среди остатков в эталонной последовательности, либо вместе в одной или нескольких группах в эталонной последовательности. Предпочтительно, чтобы неидентичные положения остатков различались консервативными аминокислотными заменами. Однако консервативные замены не учитываются при определении идентичности последовательностей.
«Гомология последовательностей» в контексте настоящего описания относится к способу определения родства двух последовательностей. Для определения гомологии последовательностей оптимально выравнивают две или более последовательностей и при необходимости вводят гэпы. Однако, в отличие от «идентичности последовательностей», консервативные аминокислотные замены учитываются как совпадение при определении гомологии последовательностей. Другими словами, для получения полипептида или полинуклеотида, имеющего 95% гомологию последовательности с эталонной последовательностью, 85%, предпочтительно 90%, еще более предпочтительно 95% аминокислотных остатков или нуклеотидов в эталонной последовательности должны соответствовать друг другу или содержать консервативную замену на другую аминокислоту или нуклеотид, или по сравнению с эталонной последовательностью могут быть вставлены аминокислоты или нуклеотиды в количестве до 15%, предпочтительно до 10%, еще более предпочтительно до 5% от общего количества аминокислотных остатков или нуклеотидов, не включая консервативные замены. Предпочтительно гомологичная последовательность включает по меньшей мере удлинение из 50, еще более предпочтительно по меньшей мере 100, еще более предпочтительно по меньшей мере 250 и еще более предпочтительно по меньшей мере 500 нуклеотидов.
«Консервативная замена» относится к замене аминокислотного остатка или нуклеотида другим аминокислотным остатком или нуклеотидом, имеющим аналогичные характеристики или свойства, включая размер, гидрофобность и т.д., так что общая функциональность существенно не изменяется.
«Выделенный» означает преобразованный «руками человека» из своего естественного состояния, то есть, если термин относится к природному элементу, то этот элемент был изменен или удален из своей первоначальной среды, или и то, и другое. Например, полинуклеотид или полипептид, естественно присутствующий в живом организме, не «выделен», но тот же полинуклеотид или полипептид, выделенный из сосуществующих материалов в его естественном состоянии, является «выделенным», как используется здесь этот термин.
Таким образом, иммуногенная композиция, используемая в настоящей заявке, также относится к композиции, которая содержит белок ORF2 PCV3, где указанный белок ORF2 PCV3 представляет собой любой из белков, описанных выше.
Согласно дополнительному аспекту, белок ORF2 PCV3 обеспечивается в иммунологической композиции на уровне включения антигена, эффективном для индукции необходимого иммунного ответа, а именно снижения частоты, уменьшения тяжести или предотвращения одного или нескольких клинических признаков, связанных с инфекцией PCV3. Предпочтительно уровень включения белка ORF2 PCV3 составляет по меньшей мере 0,2 мкг антигена/мл конечной иммуногенной композиции (мкг/мл), более предпочтительно примерно от 0,2 до 400 мкг/мл, еще более предпочтительно примерно от 0,3 до 200 мкг/мл, еще более предпочтительно примерно от 0,35 до 100 мкг/мл, еще более предпочтительно примерно от 0,4 до 50 мкг/мл, еще более предпочтительно примерно от 0,45 до 30 мкг/мл, еще более предпочтительно примерно от 0,6 до 15 мкг/мл, еще более предпочтительно примерно от 0,75 до 8 мкг/мл, еще более предпочтительно примерно от 1,0 до 6 мкг/мл, еще более предпочтительно примерно от 1,3 до 3,0 мкг/мл, еще более предпочтительно примерно от 1,4 до 2,5 мкг/мл, еще более предпочтительно примерно от 1,5 до 2,0 мкг/мл, и наиболее предпочтительно примерно 1,6 мкг/мл.
Согласно дополнительному аспекту, уровень включения антигена ORF2 составляет по меньшей мере 0,2 мкг белка ORF2 PCV3, как описано выше, на дозу конечной антигенной композиции (мкг/дозу), более предпочтительно примерно от 0,2 до 400 мкг/дозу, еще более предпочтительно примерно от 0,3 до 200 мкг/дозу, еще более предпочтительно примерно от 0,35 до 100 мкг/дозу, еще более предпочтительно примерно от 0,4 до 50 мкг/дозу, еще более предпочтительно примерно от 0,45 до 30 мкг/дозу, еще более предпочтительно примерно от 0,6 до 15 мкг/дозу, еще более предпочтительно примерно от 0,75 до 8 мкг/дозу, еще более предпочтительно примерно от 1,0 до 6 мкг/дозу, еще более предпочтительно примерно от 1,3 до 3,0 мкг/дозу, еще более предпочтительно примерно от 1,4 до 2,5 мкг/дозу, еще более предпочтительно примерно от 1,5 до 2,0 мкг/дозу и наиболее предпочтительно примерно 1,6 мкг/дозу. В одном из вариантов осуществления антиген ORF2 (например, белок ORF2 PCV3) может присутствовать в дозе конечной композиции в диапазоне примерно от 1,3 до 3 мкг. Например, конечная антигенная композиция может включать примерно 1,6 мкг белка ORF2 PCV3 в дозе 1 мл.
Полипептид ORF2 PCV3, используемый в иммуногенной композиции в соответствии с настоящим изобретением, может быть получен любым способом, включая выделение и очистку ORF2 PCV3, стандартный синтез белка и рекомбинантную способологию. Предпочтительные способы получения полипептида ORF2 PCV3 представлены в заявке на патент США сер. № 11/034,797, идеи и содержание которого включены в настоящую заявку посредством ссылки. Вкратце, чувствительные клетки инфицируют рекомбинантным вирусным вектором, содержащим кодирующие последовательности ДНК ORF2 PCV3, полипептид ORF2 PCV3 экспрессируется рекомбинантным вирусом, а экспрессированный полипептид ORF2 PCV3 выделяют из надосадочной жидкости фильтрацией и инактивируют любым традиционным способом, предпочтительно с использованием бинарного этиленимина, который затем нейтрализуют, чтобы остановить процесс инактивации.
Используемая в настоящей заявке иммуногенная композиция также обозначается как композиция, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, и (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, предпочтительно рекомбинантного бакуловируса. Кроме того, иммуногенная композиция может содержать (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, предпочтительно рекомбинантного бакуловируса, и (iii) часть надосадочной жидкости клеточной культуры.
Используемая в настоящей заявке иммуногенная композиция также относится к композиции, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, предпочтительно рекомбинантного бакуловируса и (iii) часть культуры клеток; при этом около 90% компонентов могут иметь размер менее 1 мкм.
Используемая в настоящей заявке иммуногенная композиция также относится к композиции, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, и (iv) инактивирующий агент для инактивации рекомбинантного вирусного вектора, предпочтительно BEI, где около 90% компонентов (i) – (iii) могут иметь размер менее 1 мкм. Предпочтительно BEI присутствует в концентрациях, эффективных для инактивации бакуловируса. Эффективные концентрации описаны выше.
Используемая здесь иммуногенная композиция также относится к композиции, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, (iii) часть клеточной культуры, (iv) инактивирующий агент для инактивации рекомбинантного вирусного вектора, предпочтительно BEI, и (v) нейтрализующий агент для остановки инактивации, опосредованной инактивирующим агентом, где около 90% компонентов (i) – (iii) может иметь размер менее 1 мкм. Предпочтительно, если инактивирующим агентом является BEI, указанная композиция содержит тиосульфат натрия в количествах, эквивалентных BEI.
Полипептид включается в композицию, которую можно вводить животному, чувствительному к инфекции PCV3. В предпочтительных формах композиция может также включать дополнительные компоненты, известные специалистам в данной области техники (см. также Remington's Pharmaceutical Sciences. (1990). 18th ed. Mack Publ., Easton). Кроме того, композиция может включать один или несколько ветеринарно- приемлемых носителей. Используемый здесь термин «ветеринарно приемлемый носитель» включает любые и все растворители, дисперсионные среды, покрытия, адъюванты, стабилизирующие агенты, разбавители, консерванты, антибактериальные и противогрибковые агенты, изотонические агенты, агенты, замедляющие адсорбцию, и тому подобное. В предпочтительном варианте осуществления иммуногенная композиция содержит белок ORF2 PCV3, как предусмотрено здесь, предпочтительно в концентрациях, описанных выше, который смешан с адъювантом, предпочтительно карбополом, и физиологическим раствором.
Специалисты в данной области техники поймут, что используемая здесь композиция может включать известные физиологически приемлемые стерильные растворы для инъекций. Для приготовления готового к применению раствора для парентеральной инъекции или инфузии водные изотонические растворы, такие как, например, физиологический раствор или соответствующие растворы белков плазмы легко доступны. Кроме того, иммуногенные и вакцинные композиции по настоящему изобретению могут включать разбавители, изотонические агенты, стабилизаторы или адъюванты. Разбавители могут включать воду, физиологический раствор, декстрозу, этанол, глицерин и т.п. Изотонические агенты могут включать, среди прочего, хлорид натрия, декстрозу, маннит, сорбит и лактозу. Стабилизаторы включают, среди прочего, альбумин и щелочные соли этилендиаминтетрауксусной кислоты.
«Адъюванты» в контексте настоящего описания могут включать гидроксид алюминия и фосфат алюминия, сапонины, например, Quil A, QS-21 (Cambridge Biotech Inc., Кембридж, Массачусетс), GPI-0100 (Galenica Pharmaceuticals, Inc., Бирмингем, Алабама), эмульсию вода-в-масле, эмульсию масло-в-воде, эмульсию вода-в-масле-в-воде. Эмульсия может быть основана, в частности, на легком жидком парафиновом масле (типа Европейской Фармакопеи), изопреноидном масле, таком как сквалан или сквалановое масло, полученное в результате теолигомеризации алкенов, в частности изобутена или децена; сложных эфирах кислот или спиртов, содержащих линейную алкильную группу, в частности растительных маслах, этилолеате, ди-(каприлате/капрате) пропиленгликоля, три-(каприлате/капрате) глицерина или диолеате пропиленгликоля; сложных эфирах разветвленных жирных кислот или спиртов, в частности сложных эфирах изостеариновой кислоты. Масло используют в сочетании с эмульгаторами для образования эмульсии. Эмульгаторы предпочтительно представляют собой неионные поверхностно-активные вещества, в частности сложные эфиры сорбитана, маннида (например, ангидроманнитололеат), гликоля, полиглицерина, пропиленгликоля и олеиновой, изостеариновой, рицинолевой или гидроксистеариновой кислоты, которые при необходимости являются этоксилированными, и блок-сополимеры полиоксипропилена-полиоксиэтилена, в частности продукты Плюроник, особенно L121. См. Hunter et al., Theory and Practical Application of Aduvants (Ed Stewart-Tull, D. E. S.). John Wiley and Sons, NY, стр. 51-94 (1995) и Todd et al., Vaccine 15: 564-570 (1997).
Например, можно использовать эмульсию SPT, описанную на странице 147 книги “Vaccine Design, The Subunit and Adjuvant Approach» edited by M. Powell and M. Newman, Plenum Press, 1995, и эмульсию MF59, описанную на странице 183 этой же книги.
Еще одним примером адъюванта является соединение, выбранное из полимеров акриловой или метакриловой кислоты и сополимеров малеинового ангидрида и алкенильного производного. Предпочтительными адъювантными соединениями являются полимеры акриловой или метакриловой кислоты, которые являются сшитыми, особенно с полиалкениловыми эфирами сахаров или многоатомных спиртов. Эти соединения известны под термином «Карбомер» (Phameuropa Vol. 8, No. 2, June 1996). Специалисты в данной области техники могут также сослаться на патент США No. US 2909462, в котором описаны такие акриловые полимеры, поперечно сшитые полигидроксилированным соединением, имеющий по меньшей мере 3 гидроксильные группы, предпочтительно не более 8, причем атомы водорода по меньшей мере трех гидроксилов заменены ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода. Предпочтительными радикалами являются радикалы, содержащие от 2 до 4 атомов углерода, например, винилы, аллилы и другие этиленненасыщенные группы. Сами ненасыщенные радикалы могут содержать другие заместители, такие как метил. Продукция, продаваемая под названием Карбопол; (BF Goodrich, Огайо, США), является особо пригодной. Они поперечно сшиты аллил-сахарозой или аллил-пентаэритритом. Среди них можно отметить Карбопол 974P, 934P и 971P. Наиболее предпочтительным является использование Карбопола, в частности использование Карбопола 971P, предпочтительно в количествах примерно от 500 мкг до 5 мг на дозу, еще более предпочтительно в количестве примерно от 750 мкг до 2,5 мг на дозу, и наиболее предпочтительно в количество примерно 1 мг на дозу. В частности, доза конечной композиции может включать Карбопол или Карбопол 971 в диапазоне примерно от 750 мкг до 2,5 мг карбопола. Например, в некоторых вариантах осуществления доза конечной композиции может включать примерно 1 мг Карбопола 971.
Дополнительные подходящие адъюванты включают систему адъювантов RIBI (Ribi Inc.), блок-сополимер (CytRx, Атланта, Джорджия), SAF-M (Chiron, Эмеривилл, Калифорния), монофосфориллипид A, адъювант авридин-липид-амин, термолабильный энтеротоксин из E.coli (рекомбинантный или другой), токсин холеры, IMS 1314 или мурамилдипептид среди многих других, но не ограничиваются ими.
Предпочтительно адъювант добавляют в количестве примерно от 100 мкг до 10 мг на дозу. Еще более предпочтительно адъювант добавляют в количестве примерно от 100 мкг до 10 мг на дозу. Еще более предпочтительно адъювант добавляют в количестве примерно от 500 мкг до 5 мг на дозу. Еще более предпочтительно адъювант добавляют в количестве примерно от 750 мкг до 2,5 мг на дозу. Наиболее предпочтительно адъювант добавляют в количестве примерно 1 мг на дозу.
Кроме того, композиция может включать один или несколько фармацевтически приемлемых носителей. Используемый здесь термин «фармацевтически приемлемый носитель» включает любые и все растворители, дисперсионные среды, покрытия, стабилизирующие агенты, разбавители, консерванты, антибактериальные и противогрибковые агенты, изотонические агенты, агенты, замедляющие адсорбцию, и тому подобное. Наиболее предпочтительно, композиция, представленная в настоящей заявке, содержит белок ORF2 PCV3, выделенный из надосадочной жидкости клеток, культивируемых in vitro, при этом указанные клетки были инфицированы рекомбинантным вирусным вектором, содержащим ДНК ORF2 PCV3 и экспрессирующим белок ORF2 PCV3, и при этом указанную клеточную культуру обрабатывали примерно от 2 п до 8 мМ BEI, предпочтительно примерно 5 мМ BEI для инактивации вирусного вектора, и эквивалентной концентрацией нейтрализующего агента, предпочтительно раствора тиосульфата натрия в конечной концентрации примерно от 2 до 8 мМ, предпочтительно примерно 5 мМ.
Настоящее изобретение также относится к иммуногенной композиции, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, (iv) инактивирующий агент для инактивации рекомбинантного вирусного вектора, предпочтительно BEI, и (v) нейтрализующий агент, чтобы остановить инактивацию, опосредованную инактивирующим агентом, предпочтительно тиосульфат натрия в количествах, эквивалентных BEI, и (vi) подходящий адъювант, предпочтительно Карбопол 971 в количествах, описанных выше; при этом около 90% компонентов (i) – (iii) имеют размер менее 1 мкм. Согласно дополнительному аспекту эта иммуногенная композиция дополнительно содержит фармацевтически приемлемую соль, предпочтительно фосфатную соль в физиологически приемлемых концентрациях. Предпочтительно pH указанной иммуногенной композиции доводят до физиологического значения pH, то есть примерно от 6,5 до 7,5.
В одном из вариантов осуществления иммуногенная композиция может относиться к композиции, которая включает в дозе 1 мл (i) по меньшей мере некоторое количество белка ORF2 PCV3, (ii) бакуловирус, экспрессирующий указанный белок ORF2 PCV3, (iii) культуру клеток, (iv) инактивирующий агент ( например, BEI) с концентрацией в диапазоне примерно от 2 до 8 мМ, (v) нейтрализующий агент (например, тиосульфат натрия) в количествах, эквивалентных инактивирующему агенту, и (vi) заданное количество адъюванта (например, Карбопола 971), и (vii) фосфатную соль в физиологически приемлемой концентрации. В некоторых вариантах осуществления компоненты могут быть выбраны так, что 90% комбинации компонентов, которая включает (i) белок ORF2 PCV3, (ii) бакуловирус, экспрессирующий белок, и (iii) культуру клеток, имела размер менее 1 мкм. Кроме того, в некоторых вариантах осуществления один или несколько компонентов иммуногенной композиции могут быть выбраны таким образом, чтобы иммуногенная композиция имела pH в диапазоне примерно от 6,5 до 7,5. Выбор компонентов и/или определения в отношении количеств и/или концентраций могут зависеть от различных факторов, которые влияют на стабильность иммуногенной композиции, простоту производства, доступность материалов, возраст, рост и/или состояние животных, подлежащих лечению, и/или требуемые результаты.
Например, иммуногенная композиция в контексте настоящего описания также относится к композиции, которая содержит на один мл (i) по меньшей мере 1,6 мкг белка ORF2 PCV3, описанного выше, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, (iv) примерно от 2 до 8 мМ BEI, (v) тиосульфат натрия в количествах, эквивалентных по BEI, и (vi) примерно 1 мг Карбопола 971, и (vii) фосфатную соль в физиологически приемлемой концентрации, где примерно 90% компонентов (i) – (iii) могут иметь размер менее 1 мкм, а pH указанной иммуногенной композиции доводят примерно до 6,5-7,5.
Иммуногенные композиции могут дополнительно включать один или несколько других иммуномодулирующих агентов, таких как, например, интерлейкины, интерфероны или другие цитокины (такие, как ИЛ-1, ИЛ-2, ИЛ-7, ИФН-альфа, ИФН-бета, ИФН-гамма и др., но не ограничиваясь ими). Иммуногенные композиции также могут включать гентамицин и мертиолят. Хотя количества и концентрации адъювантов и добавок, используемых в контексте настоящего изобретения, могут быть легко определены специалистом в данной области техники, настоящее изобретение рассматривает композиции, содержащие примерно от 50 мкг до 2000 мкг адъюванта. В некоторых вариантах осуществления может быть предпочтительным использовать адъюванты в количестве примерно 250 мкг адъюванта на одну миллилитровую дозу вакцинной композиции. В некоторых вариантах осуществления иммуногенная композиция может включать антибиотики в концентрации в диапазоне примерно от 1 мкг/мл до 60 мкг/мл. Например, иммуногенная композиция может включать менее примерно 30 мкг/мл антибиотиков.
Используемая в настоящей заявке иммуногенная композиция также относится к композиции, которая включает (i) любой из белков ORF2 PCV3, описанных выше, предпочтительно в концентрациях, описанных выше, (ii) по меньшей мере часть вирусного вектора, экспрессирующего указанный белок ORF2 PCV3, (iii) часть клеточной культуры, (iv) инактивирующий агент для инактивации рекомбинантного вирусного вектора, предпочтительно BEI, и (v) нейтрализующий агент, чтобы остановить инактивацию, опосредованную инактивирующим агентом, предпочтительно тиосульфат натрия в количествах, эквивалентных BEI; (vi) подходящий адъювант, предпочтительно Карбопол 971 в количествах, описанных выше; (vii) фармацевтически приемлемую концентрацию солевого буфера, предпочтительно фосфатной соли, и (viii) антимикробно-активный агент; при этом около 90% компонентов (i) – (iii) имеют размер менее 1 мкм.
Композицию согласно изобретению можно применять интрадермально, интратрахеально или интравагинально. Композицию предпочтительно можно применять внутримышечно или интраназально, наиболее предпочтительно внутримышечно. В организме животного может оказаться полезным применение фармацевтических композиций, как описано выше, посредством внутривенной или прямой инъекции в ткани-мишени. Для системного применения предпочтительны внутривенный, внутрисосудистый, внутримышечный, интраназальный, внутриартериальный, интраперитонеальный, пероральный, орогастральный или интратекальный пути введения. Более местное нанесение может осуществляться подкожно, интрадермально, интрадермально, интракардиально, интралобально, интрамедуллярно, внутрилегочно или непосредственно в обрабатываемой ткани или рядом с ней (соединительной, костной, мышечной, нервной, эпителиальной ткани). В зависимости от необходимой продолжительности и эффективности лечения композиции согласно настоящему описанию можно вводить один или несколько раз, а также с перерывами, например, ежедневно в течение нескольких дней, недель или месяцев и в различных дозировках. Предусмотрены как разовая доза, так и множественные дозы. Также рассматриваются комбинированные вакцины с другими антигенами патогенов свиней. Предпочтительные комбинированные композиции содержат белок ORF2 PCV3 и PPV, антиген PRRSV, антиген M. hyopneumoniae (надосадочную жидкость или бактерин) или антиген PRRSV и антиген M. hyopneumoniae (надосадочную жидкость или бактерин), или любую комбинацию вышеперечисленного с белком ORF2 PCV2.
В некоторых вариантах осуществления может быть разработан режим дозирования для доставки эффективных количеств ORF2 PCV3 для индукции необходимого эффекта, такого как иммунный ответ у животного и/или их потомства. Определения в отношении режимов дозирования могут быть связаны с необходимыми результатами, компонентами, выбранными для использования в иммуногенной композиции, путем введения, таким как парентеральное и/или подкожное введение, количеством или введенными дозами, например, однократным введением или множественными дозами, и/или конкретными свойствами животного или популяции животных, подлежащих лечению, например, возрастом, размером и/или состоянием животных. Состояние животных может относиться, например, к состоянию здоровья, состоянию беременности, размеру и т.д. Таким образом, свиноматкам и поросятам могут потребоваться разные эффективные дозы.
Как указано выше, способы лечения могут отличаться в зависимости от необходимого результата. Например, свиноматку можно лечить для ингибирования и/или предотвращения состояний, связанных с цирковирусом свиньи, или свиноматку можно лечить для ингибирования и/или предотвращения негативных эффектов инфекции цирковирусом свиньи у ее поросят.
Режим дозирования может включать одну или несколько доз иммуногенной композиции, которая включает заранее определенное количество белка ORF2 PCV3. Например, режим дозирования может включать дозы в диапазоне примерно от 2 мкг до 400 мкг белка ORF2 PCV3. В одном из вариантов осуществления режим дозирования конкретной иммуногенной композиции может включать более примерно двух микрограммов белка ORF2 PCV3. В некоторых случаях каждая доза конкретной иммуногенной композиции во многих случаях включает белок ORF2 PCV3 в количестве, превышающем примерно 4 мкг. Некоторые варианты осуществления режима дозирования для иммуногенной композиции могут включать иммуногенные композиции в дозах по меньшей мере примерно 8 мкг белка ORF2 PCV3. Например, некоторые режимы дозирования иммуногенной композиции, раскрытые в настоящей заявке, могут быть структурированы таким образом, чтобы по меньшей мере одна доза включала более чем примерно 16 мкг необходимого белка ORF2 PCV3.
В одном из вариантов осуществления режим дозирования может быть выбран на основе необходимой экспрессии конкретного белка ORF2 PCV3 в организме животного. Например, учитывая иммуногенную композицию, которая включает соответствующий вектор и/или систему экспрессии для свиней, может быть необходимо, чтобы вектор, доставленный в иммуногенной композиции, был способен доставлять белок ORF2 PCV3 в количестве, которое находится в диапазоне примерно от 2 мкг до 400 мкг in vivo. В одном варианте осуществления схема дозирования конкретной иммуногенной композиции построена так, чтобы доставить животному количество белка ORF2 PCV3, превышающее примерно 2 мкг. В некоторых случаях схема дозирования конкретной иммуногенной композиции построена так, чтобы доставить животному количество белка ORF2 PCV3, превышающее примерно 4 мкг. Некоторые варианты режима дозирования иммуногенной композиции структурированы так, чтобы доставлять животному количество белка ORF2 PCV3, превышающее примерно 8 мкг. Например, некоторые режимы дозирования иммуногенной композиции, раскрытые в настоящей заявке, могут быть структурированы таким образом, чтобы животному можно было доставить более чем примерно 16 мкг необходимого белка ORF2 PCV3.
Режимы дозирования могут также включать руководство по поводу путей и/или времени введения. Например, может быть необходимо доставить дозу иммуногенной композиции поросенку в определенном возрасте, в частности, в возрасте около 1, 2 или 3 недель в зависимости от иммуногенных композиций и необходимых результатов. В некоторых случаях поросятам можно вводить иммуногенные композиции в возрасте примерно от 7 дней до 28 дней. В варианте схемы дозирования свиньям можно вводить иммуногенную композицию в возрасте примерно от 14 дней до 26 дней. Например, окно введения для поросят может быть выбрано в диапазоне примерно от 16 дней до 26 дней. Некоторые варианты схемы дозирования могут включать введение иммуногенной композиции поросенку в возрасте примерно от 18 дней до 24 дней.
Иммуногенная композиция может включать рекомбинантный белок ORF2 PCV3. В частности, иммуногенная композиция может включать рекомбинантный белок ORF2 PCV3, экспрессированный из бакуловирусов.
Кроме того, в некоторых случаях иммуногенная композиция, которая включает рекомбинантный белок ORF2 PCV3, может быть введена в комбинации с одной или несколькими дозами дополнительных антигенов, например, антигенов из ORF2 PCV2, PPV, PRRSV и/или M. hyopneumoniae («М. Нуо»). Антиген вируса РРСС может быть аттенуированной живой вакциной. Антиген М.Нуо может быть бактерином, надосадочной жидкостью или комбинацией бактерина и надосадочной жидкости.
Несколько доз иммуногенных композиций можно вводить в режиме дозирования. Например, режим дозирования может быть составлен из дозы иммуногенной композиции, которая включает рекомбинантный белок ORF2 PCV3, и дозы иммуногенной композиции, которая включает рекомбинантный белок ORF2 PCV2. В одном случае дозы могут включать приблизительно эквивалентные количества рекомбинантного белка ORF2 PCV3 и белка ORF2 PCV2. Вариант схемы дозирования может включать дозы иммуногенных композиций, которые включают рекомбинантный белок ORF2 PCV3 и рекомбинантный ORF2 PCV2, оба из которых могут быть экспрессированы с использованием бакуловирусных систем экспрессии.
Вариант осуществления иммуногенной композиции рекомбинантной ORF2 PCV3 может включать дополнительные антигены, например, антигены, такие как рекомбинантные белки из ORF2 PCV3, а также аттенуированный живой PRRSV и/или бактерин, надосадочная жидкость или комбинация бактерина и надосадочной жидкости M. Hyo. Некоторые варианты осуществления иммуногенной композиции могут включать рекомбинантные белки, экспрессируемые бакуловирусом из ORF2 PCV3 и ORF2 PCV2, а также антигены PRRSV (например, аттенуированную живую вакцину) и/или M. Hyo (например, бактерин и/или надосадочную жидкость). Кроме того, в некоторых случаях иммуногенная композиция может включать белок ORF2 PCV3 в комбинации с белком ORF2 PCV2, аттенуированный живой вирус PRRSV и/или бактерин M. Hyo и/или надосадочную жидкость.
Иммуногенные композиции могут включать рекомбинантный белок ORF2 PCV3 и рекомбинантный белок ORF2 PCV2. В одном случае дозы могут включать приблизительно эквивалентные количества рекомбинантного белка ORF2 PCV3 и белка ORF2 PCV2. Вариант схемы дозирования может включать дозы иммуногенных композиций, которые включают рекомбинантный белок ORF2 PCV3 и рекомбинантный ORF2 PCV2, оба из которых могут быть экспрессированы с использованием систем экспрессии бакуловирусов.
Некоторые варианты осуществления иммуногенной композиции могут включать рекомбинантные белки, экспрессируемые бакуловирусом из ORF2 PCV3, а также антигены PRRSV и/или M. Hyo. Кроме того, рекомбинантные белки из ORF2 PCV3 и ORF2 PCV2 могут быть объединены с антигенами PRRSV и/или M. Hyo с образованием иммуногенной композиции. Как описано выше, дополнительные антигены могут включать аттенуированный живой вирус PRRSV, и/или бактерин M Hyo, и/или надосадочную жидкость.
Например, иммуногенная композиция может содержать рекомбинантный белок ORF2 PCV3 и рекомбинантный белок ORF2 PCV2. В некоторых случаях иммуногенная композиция включает приблизительно эквивалентные количества рекомбинантного белка ORF2 PCV3 и белка ORF2 PCV2. Некоторые варианты осуществления иммуногенной композиции могут включать комбинацию рекомбинантных белков, экспрессируемых бакуловирусом, из ORF2 PCV3 и ORF2 PCV2, а также PRRSV и/или M. Hyo.
Режимы дозирования могут быть использованы для улучшения экономики свиноводства. Например, иммуногенные композиции, такие как вакцины, можно вводить свиноматкам и/или поросятам для защиты свиноматок, поросят, или тех и других.
В частности, вакцинация свиноматок перед беременностью может снизить количество мумифицированных, мертворожденных и/или слабых поросят при опоросе, если свиноматки заражены PCV3. Обычно считается, что PCV3 является репродуктивным заболеванием. Кроме того, использование вакцины на основе экспрессии инактивированным бакуловирусом ORF2 PCV3 может снижать и/или ингибировать репликацию вируса у свиноматок. Это снижение репликации может снизить количество мумий при опоросе у вакцинированных свиноматок примерно на 4%. Такое сокращение может иметь значительные экономические последствия для производителей свиней.
Кроме того, утверждается, что вакцина способна защитить племенных свинок и свиноматок при заражении PCV3 на протяжении всей беременности, или двух триместров, или по меньшей мере одного триместра в течение 114 дней беременности.
Также утверждается, что вакцина способна значительно снизить количество мумий, мертворожденных и ослабленных плодов у вакцинированных свинок и свиноматок, вакцинированных при заражении PCV3, в течение всей беременности, или двух триместров, или по меньшей мере одного триместра в течение 114 дней беременности.
Схема дозирования может включать вакцинацию молодых свиноматок (т.е. в 5-месячном возрасте или младше) по меньшей мере одной дозой иммуногенной композиции, как описано в настоящей заявке, перед осеменением. Доза иммуногенной композиции, описанная в настоящей заявке, может вводиться внутримышечно в виде дозы один (1) мл до осеменения. В некоторых вариантах осуществления свиноматкам можно вводить одну или несколько доз вакцины. Например, может быть введена первая вакцина, за которой следует ревакцинация через 21 день и до осеменения. В некоторых вариантах осуществления свиноматки могут быть осеменены в период от 14 дней до 21 дня после ревакцинации. Эти временные рамки могут позволить свиноматкам выработать иммунный ответ. Использование такого режима дозирования может уменьшить и/или подавить количество мумий при опоросе.
Кроме того, использование режима дозирования, который включает введение дозы 1 мл иммуногенной композиции, которая включает антиген PCV3 (т.е. рекомбинантную ORF2 PCV3), позволяет снижать, уменьшать и/или ингибировать лимфоаденопатию, лимфоидное истощение и/или многоядерные/гигантские гистиоциты у свиней, инфицированных PCV3.
В некоторых вариантах осуществления режим дозирования для вакцинации поросят в возрасте примерно 3 недель с использованием вакцины ORF2 PCV3, экспрессированной бакуловирусом, позволяет снизить вирусную нагрузку, если поросята впоследствии заражаются PCV3. Например, количество реплицирующегося вируса в тканях вакцинированных поросят может быть снижено по сравнению с невакцинированными поросятами. Кроме того, вакцинация поросят вакциной ORF2 PCV3 позволяет снизить смертность, клинические признаки, макроскопические поражения и/или гистологические нарушения у вакцинированных поросят по сравнению с невакцинированными поросятами, которые впоследствии подвергаются воздействию PCV3.
Термин «иммуностимулятор» в контексте настоящего описания означает любой агент или композицию, которые могут запускать иммунный ответ сразу, предпочтительно без инициирования или усиления специфического иммунного ответа, например, иммунного ответа против конкретного патогена. Кроме того, рекомендуется вводить иммуностимулятор в подходящей дозе. Предпочтительно иммуностимулятор представляет собой гемоцианин лимфы улитки (KLH) и/или неполный адъювант Фрейнда (IFA). В данном контексте иммуностимулятор играет роль не адъюванта, а усилителя заражения. Предпочтительно KLH эмульгируют в IFA, содержащем 1 мг KLH/мл, который можно вводить внутримышечно за два дня до и через два дня после контрольного заражения.
В соответствии с дополнительным соображением, обеспечивается антигенный белок цирковируса свиней 3 типа (PCV3), где указанный белок является функциональным антигенным вариантом белка ORF2 PCV3, и указанный белок, в частности, также называется «белком, рассматриваемым дополнительно» в дальнейшем.
Предпочтительно, белок, рассматриваемый дополнительно, представляет собой функциональный антигенный вариант белка ORF2 PCV3, кодируемого SEQ ID № 1.
В одном предпочтительном аспекте белок, рассматриваемый дополнительно, включает замены и/или удлинения ORF2 PCV3.
В другом предпочтительном аспекте белок, рассматриваемый дополнительно, представляет собой функциональный антигенный вариант белка, кодируемого SEQ ID №1, и/или функциональный антигенный вариант способен давать более высокий выход вирусоподобных частиц (VLP), чем белок, кодируемый SEQ ID № 1.
Предпочтительно, указанный функциональный антигенный вариант способен давать более высокий выход VLP, чем белок, кодируемый SEQ ID № 1, при определении с помощью вестерн-блоттинга.
Согласно одному предпочтительному аспекту указанный функциональный антигенный вариант имеет меньше положительно заряженных аминокислотных остатков, чем белок, кодируемый SEQ ID No. 1.
Согласно другому предпочтительному аспекту указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, и при этом предпочтительно эти замены включают замены одного или нескольких остатков S и/или K и/или остатка H мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
Согласно еще одному предпочтительному аспекту, указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замены одного или нескольких остатков S и/или остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
Согласно еще одному предпочтительному аспекту указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замены остатка S или остатка H и всех из остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
В еще одном предпочтительном аспекте указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замену по меньшей мере S и/или H и любого K мотива SKKKH петли FG белка, кодируемого SEQ ID №1 с Q, P, F или S.
В еще одном предпочтительном аспекте указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замену мотива SKKK в мотиве SKKKH петли FG белка, кодируемого SEQ ID No. 1, на QPFS, или замену мотива KKKH в мотиве SKKKH петли FG белка, кодируемого SEQ ID No. 1, на QPFS.
В еще одном дополнительном предпочтительном аспекте указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID № 1, 2, 5, 6 или 7.
В еще одном предпочтительном аспекте указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID No. 1, 2, 5, 6 или 7.
Согласно особо предпочтительному аспекту, указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, предпочтительно, где указанное удлинение является всей последовательностью или включает последовательность из цирковируса, и предпочтительно где по меньшей мере часть указанного удлинения заменяет концевую последовательность SVL белка, кодируемого SEQ ID No. 1
Согласно другому предпочтительному аспекту указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, и где указанное удлинение составляет от 1 до 100 аминокислот.
Согласно дополнительному предпочтительному аспекту указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, и где указанное удлинение составляет от 1 до 50 аминокислот.
Согласно еще одному предпочтительному аспекту, указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, и где указанное удлинение составляет от 1 до 30 аминокислот.
В одном особо предпочтительном аспекте указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1.
Предпочтительно указанное удлинение составляет от 1 до 30 аминокислот и/или указанное удлинение включает всю последовательность VKININLTPPVATSRVPSRALPLRFGCGHR.
В другом предпочтительном аспекте указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID No. 1, 2, 5, 6 или 7.
В предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей идентичность последовательностей и/или гомологию последовательностей по меньшей мере примерно 80%, или по меньшей мере примерно 85%, или по меньшей мере примерно 86%, или по меньшей мере примерно 87%, или по меньшей мере примерно 88%, или по меньшей мере примерно 89%, например, в диапазоне примерно от 83% до 89%, например 84%, или 85%, или 86%, или 87%, или 88%, или 89% идентичности последовательности и/или гомологии последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет одну или несколько замен в петле FG.
В предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей идентичность последовательностей и/или гомологию последовательностей по меньшей мере примерно 80%, или по меньшей мере примерно 85%, или по меньшей мере примерно 86%, или по меньшей мере примерно 87%, или по меньшей мере примерно 88%, или по меньшей мере примерно 89%, например, в диапазоне примерно от 83% до 89%, например 84%, или 85%, или 86%, или 87%, или 88%, или 89% идентичности последовательности и/или гомологии последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок является рекомбинантным белком, и где указанный белок имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1.
В предпочтительном аспекте указанный вариантный белок содержит петлю FG, имеющую одну или несколько замен в петле FG, и дополнительно содержит С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, где последовательность вариантного белка включает или состоит из аминокислотной последовательности, имеющей идентичность последовательности и/или гомологию последовательности по меньшей мере примерно 80%, или по меньшей мере примерно 85%, или по меньшей мере примерно 86%, или по меньшей мере примерно 87%, или по меньшей мере примерно 88%, или по меньшей мере примерно 89%, например, в диапазоне примерно от 83% до 89%, например, 84%, 85%, 86%, 87%, 88% или 89% идентичности последовательности и/или гомологии последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
В другом предпочтительном аспекте белок, рассматриваемый дополнительно, представляет собой рекомбинантный белок, полученный методами рекомбинантной ДНК.
В еще одном предпочтительном аспекте белок, рассматриваемый дополнительно, представляет собой белок, экспрессируемый бакуловирусом.
Предпочтительно указанный PCV3 представляет собой любую филогенетическую ветвь PCV3 или комбинацию филогенетических ветвей.
Предпочтительно указанный PCV3 выбран из группы, состоящей из PCV3a и PCV3b.
В частности, указанный PCV3 предпочтительно выбран из группы, состоящей из PCV3a1, PCV3b1 и PCV3b2.
PCV3 также может быть выбран из PCV3c (BMC Vet Res. 2019 Jul 15; 15 (1): 244. Doi: 10.1186 / s12917-019-1977-7).
Более конкретно, указанная ORF2 PCV3 предпочтительно принадлежит к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4).
В предпочтительном аспекте указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
В другом предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 6.
В еще одном предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 7.
В еще одном предпочтительном аспекте указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
В еще одном предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
В еще одном предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет одну или несколько замен в петле FG.
В предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
В другом предпочтительном аспекте указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1.
Согласно предпочтительному аспекту, указанный белок представляет собой рекомбинантный белок в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
Согласно предпочтительному аспекту указанный белок представляет собой рекомбинантный белок, полученный в результате его экспрессии бакуловирусным вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
В другом предпочтительном аспекте предоставлена нуклеотидная последовательность, которая кодирует белок, рассматриваемый дополнительно, и где указанный нуклеотид также именуется «нуклеотидной последовательностью, рассматриваемой дополнительно» в дальнейшем.
В дополнительном предпочтительном аспекте предоставлен вектор, содержащий нуклеотидную последовательность, рассматриваемую дополнительно, и где указанный вектор также называется в дальнейшем «вектором, рассматриваемым дополнительно».
Также обеспечивается рекомбинантный вектор, содержащий нуклеотидную последовательность, рассматриваемую дополнительно.
Кроме того, обеспечивается хозяин экспрессии, которого трансформируют или трансфицируют нуклеотидной последовательностью, рассматриваемой дополнительно, и при этом указанный хозяин экспрессии также именуется здесь и далее «хозяином экспрессии, рассматриваемым дополнительно».
Также обеспечивается хозяин бакуловирусной экспрессии, который трансформирован или трансфицирован нуклеотидной последовательностью, рассматриваемой дополнительно, и где указанный хозяин бакуловирусной экспрессии также называется «хозяином бакуловирусной экспрессии, рассматриваемым дополнительно».
Кроме того, обеспечивается способ получения белка, рассматриваемого дополнительно, включающий экспрессию нуклеотидной последовательности, рассматриваемой дополнительно.
Также обеспечивается способ получения белка, рассматриваемого дополнительно, при этом способ включает экспрессию вектора, рассматриваемого дополнительно.
Кроме того, обеспечивается способ получения белка, рассматриваемого дополнительно, при этом способ включает экспрессию рекомбинантного вектора, рассматриваемого дополнительно.
Также обеспечивается способ получения белка, рассматриваемого дополнительно, включающий культивирование хозяина экспрессии, рассматриваемого дополнительно, чтобы вызвать экспрессию белка.
Кроме того, обеспечивается способ получения белка, рассматриваемого дополнительно, включающий трансфекцию хозяина экспрессии нуклеотидной последовательностью, рассматриваемой дополнительно, или вектором, рассматриваемым дополнительно, и культивирование хозяина экспрессии, чтобы вызвать экспрессия белка.
Также обеспечивается способ получения белка, рассматриваемого дополнительно, включающий культивирование хозяина для бакуловирусной экспрессии, рассматриваемого дополнительно, чтобы вызвать экспрессию белка.
Также обеспечивается способ получения белка, рассматриваемого дополнительно, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью, рассматриваемой дополнительно, или вектором, рассматриваемым дополнительно, и культивирование хозяина для бакуловирусной экспрессии, чтобы вызвать экспрессию белка.
Предпочтительно, в любом из вышеупомянутых способов получения белка, рассматриваемого дополнительно, инактивирующий агент используют, когда достигнуты достаточные уровни экспрессированного белка, и где инактивирующим агентом предпочтительно является бинарный этиленимин (BEI), когда используют достаточный уровень. экспрессированного белка.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где около 90% компонентов (i) - (iii) имеют размер менее 1 мкм.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят примерно до 6,5-7,5.
Предпочтительно, любой из вышеупомянутых способов получения белка, рассматриваемого дополнительно, включает продукцию белка бакуловирусной системой экспрессии в культивируемых клетках насекомых.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает продукцию белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает продукцию белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус.
Предпочтительно, любой из вышеуказанных способов получения белка, рассматриваемого дополнительно, включает продукцию белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение.
Предпочтительно, любой из вышеупомянутых способов получения белка, рассматриваемого дополнительно, включает продукцию белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение, где азиридиновое соединение включает BEI.
Кроме того, обеспечивается белок, который может быть получен любым из вышеупомянутых способов получения белка, рассматриваемых дополнительно.
Также обеспечивается композиция, содержащая белок, получаемый любым из вышеуказанных способов получения белка, рассматриваемых дополнительно, и при этом композиция предпочтительно включает носитель, разбавитель или наполнитель. Кроме того, обеспечивается композиция, которую можно получить любым из вышеуказанных способов получения белка, рассматриваемых дополнительно, и где композиция предпочтительно включает носитель, разбавитель или наполнитель.
В частности, любая из упомянутых композиций также именуется в дальнейшем «композицией, рассматриваемой дополнительно».
В композиции, рассматриваемой дополнительно, белок предпочтительно присутствует в количестве от 0,2 до примерно 400 мкг/мл, или от 2 до примерно 400 мкг/мл, или от 4 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или от 2 до примерно 200 мкг/мл, или от 4 до примерно 200 мкг/мл, или от 8 до примерно 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или от 2 до примерно 100 мкг/мл, или от 4 до примерно 100 мкг/мл, или от 8 до примерно 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл или примерно 1,6 мкг/мл.
Предпочтительно композиция, рассматриваемая дополнительно, включает любой один или несколько из растворителя, дисперсионной среды, покрытия, стабилизирующего агента, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии и/или иммуномодулирующего агента.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, в которой носитель, разбавитель или наполнительно представляет собой любой один или несколько из адъюванта, иммуномодулирующего агента, надосадочной жидкости клеточной культуры, вирусного вектора или вектора экспрессии, или любой их комбинации.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, в которой носитель, разбавитель или наполнитель включает адъювант.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, в которой носитель, разбавитель или наполнитель включает адъювант, где адъювант включает один или несколько из полимеров акриловой или метакриловой кислоты; сополимера малеинового ангидрида и алкенильного производного; сшитого полимера акриловой или метакриловой кислоты; полимера акриловой или метакриловой кислоты, сшитого с полиалкениловым эфиром сахара или полиспирта; карбомера; акрилового полимера, поперечно сшитого полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопола; Карбопола 974P; Карбопола 934P; Карбопола 971P; гидроксида алюминия; фосфата алюминия; сапонина; Quil A; QS-21; GPI-0100; эмульсии типа вода в масле; эмульсии масло-в-воде; эмульсии вода-в-масле-в-воде; эмульсии на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидного масла; сквалана; скваланового масла, полученного в результате олигомеризации алкенов, изобутена или децена; (а) сложного эфира (эфиров) кислоты (кислот) или спирта (спиртов), содержащего линейную алкильную группу; растительного масла (масел); этилолеата; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлата/капрата); диолеата пропиленгликоля; сложного эфира (эфиров) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложного эфира (эфиров) изостеариновой кислоты; неионного поверхностно-активного вещества (веществ); сложного эфира (эфиров) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированной, ангидроманнитололеата; блок-сополимеров полиоксипропилена и полиоксиэтилена, продукта Плюроник, адъювантной системы RIBI; блок-сополимера; SAF-M; монофосфориллипида А; авридинового липидно-аминового адъюванта; термолабильного энтеротоксина из E. coli (рекомбинантного или другого); токсина холеры; IMS 1314 или мурамилдипептида.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, в которой носитель, разбавитель или наполнитель включает адъювант, где адъювант включает Карбопол или Карбопол 971.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, в которой носитель, разбавитель или наполнитель включает адъювант, где адъювант присутствует в количестве примерно от 50 мкг до 2000 мкг от композиции, или где адъювант присутствует в дозе композиции примерно 250 мкг/мл, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг от композиции, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг от композиции; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг от композиции, или адъювант присутствует в количестве примерно 1 мг от композиции.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая иммуномодулирующий агент.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая иммуномодулирующий агент, и при этом иммуномодулирующий агент представляет собой один или несколько из интерлейкина (интерлейкинов), интерферона (интерферонов) или другого цитокина (цитокинов).
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая антибиотик (антибиотики).
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая антибиотик (антибиотики), где антибиотик (антибиотики) включает гентамицин.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая антибиотик (антибиотики), и где композиция содержит примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков).
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая антибиотик (антибиотики), и где композиция содержит примерно от 1 мкг/мл до менее примерно 30 мкг/мл антибиотика (антибиотиков).
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая дополнительный антиген.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном ORF2 PCV3.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном PCV3.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, содержащая дополнительный антиген из дополнительного патогена свиней.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая дополнительно содержит антиген дополнительного патогена свиней, при этом указанный патоген представляет собой один или несколько антигенов PCV2, PRRSV (вируса респираторного и репродуктивного синдрома свиней), антиген бактерина Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген свиной чумы (классической или африканской, или их комбинацию), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген свиного парвовируса (PPV) или антиген Pasteurella multocida.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая дополнительно содержит антиген дополнительного патогена свиней, при этом указанная композиция дополнительно содержит один или несколько из антигена PCV2, антигена PRRSV и антигена PPV.
Предпочтительно представлена композиция, рассматриваемая дополнительно, дополнительно содержащая антиген PCV2.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая дополнительно содержит антиген PCV2, где антиген PCV2 представляет собой рекомбинантный белок ORF2 PCV2.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая дополнительно содержит антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2, экспрессируемый рекомбинантным бакуловирусом.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, находящаяся в лекарственной форме.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая составлена и/или упакована для введения однократной дозы или однократного введения.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая составлена и/или упакована для режима множественных доз.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая составлена и/или упакована для двухдозового режима.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 10 доз указанной композиции.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 50 доз указанной композиции.
Предпочтительно, обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 100 доз указанной композиции.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 200 доз указанной композиции.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая находится в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 250 доз указанной композиции.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая содержит антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2, экспрессируемый рекомбинантным бакуловирусом, и где либо белок, либо объединенное общее количество белка ORF PCV3 и белка ORF PCV2 присутствует в количестве примерно от 0,2 до 400 мкг/дозу, или от 2 до примерно 400 мкг/дозу, или от 4 до примерно 400 мкг/дозу. или от 8 до примерно 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или от 2 до примерно 200 мкг/дозу, или от 4 до примерно 200 мкг/дозу, или от 8 до примерно 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или от 2 до примерно 100 мкг/дозу, или от 4 до примерно 100 мкг/дозу, или от 8 до примерно 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая содержит соль.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая содержит инактивированный вирусный вектор и/или надосадочную жидкость клеточной культуры.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая содержит инактивированный вирусный вектор и надосадочную жидкость клеточной культуры.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая включает (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, экспрессирующим указанный белок, (iv) инактивирующий агент, или инактивирующий агент, включающий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая включает (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, экспрессирующим указанный белок, (iv) инактивирующий агент, или инактивирующий агент, включающий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации, и где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая представляет собой иммуногенную композицию, содержащую белок, рассматриваемый дополнительно, и носитель, разбавитель или наполнитель.
Предпочтительно обеспечивается композиция, рассматриваемая дополнительно, которая представляет собой иммуногенную композицию, содержащую белок, рассматриваемый дополнительно, и носитель, разбавитель или наполнитель, и дополнительный антиген, как указано выше.
Также обеспечивается способ создания композиции, рассматриваемой дополнительно, где белок, рассматриваемый дополнительно, смешивают с носителем, разбавителем или наполнителем.
Кроме того, обеспечивается способ создания композиции, рассматриваемой дополнительно, где белок, рассматриваемый дополнительно, смешивают с носителем, разбавителем или наполнителем, и дополнительным антигеном.
Кроме того, для использования в качестве лекарственного средства обеспечивается белок, рассматриваемый дополнительно.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в качестве вакцины.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у животного.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиней.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у молодых свиней.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят; при этом поросят должны вскармливать свиноматки, которым вводили белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиноматок.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у беременных свиноматок, свиней до первого опороса или подсвинков для осеменения.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у животных.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у свиней.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у молодых свиней.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у поросят.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у поросят; при этом поросята должны получать кормление от свиноматок, которым вводили белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у свиноматок.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции иммунного ответа против PCV3 у беременных свиноматок, свиней до первого опороса или подсвинков до осеменения.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является свиньей.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является молодой свиньей.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или предотвращения инфекции PCV3 у животного, где указанное животное является поросенком.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен вскармливаться свиноматкой, которой был введен белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или предотвращения инфекции PCV3 у животного, где указанное животное является свиноматкой.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное является свиньей.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное является молодой свиньей.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное представляет собой поросенка.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное представляет собой поросенка, и при этом поросенок должен вскармливаться свиноматкой, которой был введен белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное является свиноматкой.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при иммунизации животного против PCV3, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, или элиминации, или нейтрализации экспрессии вируса PCV3 у животного.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, или элиминации, или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиньей.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, или элиминации, или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является молодой свиньей.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен вскармливаться свиноматкой, которой был введен белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, или элиминации, или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиноматкой.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в способе снижения, или элиминации, или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное является свиньей.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой молодую свинью.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка.
Также белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен вскармливаться свиноматкой, которой был введен белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное является свиноматкой.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
Предпочтительно указанный белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанному животному внутримышечно или интрадермально.
Предпочтительно, указанный белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанному животному в сочетании с другим антигеном, предпочтительно, когда другой патоген является антигеном патогена свиней.
Предпочтительно, указанный белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном ORF2 PCV3, предпочтительно, когда другой патоген является антигеном патогена свиней.
Предпочтительно, указанный белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном PCV3, предпочтительно, когда другой патоген является антигеном патогена свиньи.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где указанное животное представляет собой свиноматку, беременную поросенком.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанное животное представляет собой свиноматку, беременную поросенком, и при этом поросенок должен вскармливаться свиноматкой, которой вводили белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанное животное является свиноматкой, и при этом указанный белок, рассматриваемый дополнительно, или указанную композицию, рассматриваемую дополнительно, вводят дважды указанной свиноматке.
Предпочтительно указанным животным является свиноматка, и при этом указанный белок, рассматриваемый дополнительно, или указанную композицию, рассматриваемую дополнительно, вводят указанной свиноматке только дважды.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанное животное является поросенком, и где белок, рассматриваемый в дальнейшем, или композицию, рассматриваемую дополнительно, вводят указанному поросенку один раз.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, в которых указанное животное является поросенком, и при этом белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанному поросенку только один раз.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, в которых указанное животное является свиноматкой, и где белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят дважды указанной свиноматке, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где указанное животное является свиноматкой, и при этом белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят дважды указанной свиноматке, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где указанное животное является свиноматкой, и при этом белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят указанной свиноматке только дважды, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанное животное является поросенком, и где белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят один раз указанному поросенку, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где указанное животное является поросенком, и где белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят один раз указанному поросенку, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где указанное животное является поросенком, и где белок, рассматриваемый дополнительно, или композицию, рассматриваемую дополнительно, вводят только один раз указанному поросенку, и где указанное применение не включает введение какого-либо другого антигена PCV3 указанному животному до или во время введения указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где введение животному при применении состоит из однодозовой, однократной вакцинации или единственного введения одной дозы указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где введение животному при применении состоит из режима многократной вакцинациии или режима нескольких доз указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где введение животному при применении состоит из двукратной вакцинации, или двукратного применения дозы указанного белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, при котором введение животному осуществляют в течение по меньшей мере 1, 2 или 3 недель контакта с вирулентным цирковирусом свиней.
Кроме того, обеспечивается белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, где животным является поросенок не старше 15-недельного возраста, или не старше 6-недельного возраста, или не старше 3-х недельного возраста, или не старше 2-х недельного возраста, или не старше 1-недельного возраста.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанный белок, рассматриваемый дополнительно, предназначен для любого из вышеупомянутых применений.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где указанный белок, рассматриваемый дополнительно, предназначен для использования в двух или более случаях, упомянутых выше.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, при этом указанная композиция, рассматриваемая дополнительно, предназначена для любого из вышеуказанных применений.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, в которых животному вводят второй антиген перед введением белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где второй антиген вводят животному одновременно с введением белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеуказанных применений, где второй антиген вводят животному в то же время и в той же композиции, что и при введении белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где второй антиген вводят животному в то же время и в другой композиции, чем при введении белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для любого из вышеупомянутых применений, где второй антиген вводят животному после введения белка, рассматриваемого дополнительно, или композиции, рассматриваемой дополнительно.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при вакцинации свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у свиньи, где белок находится в иммуногенной композиции, которую вводят свинье в одной дозе.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, где белок находится в иммуногенной композиции, которую вводят свинье только в одной дозе.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье в двух дозах.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в двух дозах.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в качестве единственного антигена PCV3 для вакцинации молодой свиньи, чтобы уменьшить тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье в одной дозе.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в качестве единственного антигена PCV3 для вакцинации молодой свиньи, чтобы уменьшить тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в одной дозе.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в качестве единственного антигена PCV3 для вакцинации молодой свиньи, чтобы уменьшить тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье в двух дозах.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для использования в качестве единственного антигена PCV3 для вакцинации молодой свиньи, чтобы уменьшить тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в двух дозах.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где одну дозу иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок, рассматриваемый дополнительно, представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок является антигенным компонентом в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
В настоящей заявке также представлена иммуногенная композиция, рассматриваемая дополнительно, для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где только одну дозу иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок, рассматриваемый дополнительно, представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно, где белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок является антигенным компонентом в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
Кроме того, белок, рассматриваемый дополнительно, или композиция, рассматриваемая дополнительно, обеспечивается для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где две дозы иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок, рассматриваемый дополнительно, представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно, белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок является антигенным компонентом в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
Также обеспечивается иммуногенная композиция, рассматриваемая дополнительно, для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где только две дозы иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок, рассматриваемый дополнительно, представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок является антигенным компонентом в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
Предпочтительно, в любом из вышеупомянутых применений указанные клинические признаки или симптомы выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
Предпочтительно, в любом из вышеупомянутых применений указанные клинические признаки или симптомы выбираются из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
Предпочтительно, в любом из вышеупомянутых применений указанные клинические признаки или симптомы выбраны из группы, состоящей из развития или продукции мумифицированного, мертворожденного и/или слабого плода.
Предпочтительно при любом из вышеупомянутых применений указанные клинические признаки или симптомы представляют собой или включают выталкивание мумифицированного, мертворожденного и/или слабого плода.
Настоящее изобретение теперь будет описано посредством следующих наборов пунктов. Для простоты ссылки эти наборы пунктов были помечены как набор пунктов A, набор пунктов B и т.д. Раскрытие в каждом наборе пунктов в равной степени применимо к настоящему изобретению. Аналогичным образом раскрытие информации в каждом наборе пунктов в равной степени применимо ко всем остальным пунктам:
НАБОР ПУНКТОВ A:
Набор пунктов A - Настоящее изобретение теперь будет описано посредством следующего набора пронумерованных пунктов (набор пунктов A). Раскрытие в этом наборе пунктов в равной степени применимо к настоящему изобретению. Подобным образом раскрытие в этом наборе пунктов в равной степени применимо к каждому из других наборов пунктов.
1. Композиция, содержащая:
белок ORF2 цирковируса свиней 3 типа (PCV3), и
ветеринарно приемлемый носитель, включающий растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, и иммуномодулирующий агент, или любую их комбинацию.
2. Композиция по п.1, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
3. Композиция по п.1, где ветеринарно приемлемый носитель включает адъювант.
4. Композиция по любому из пп.1-3, где ORF2 PCV3 относится к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4).
5. Композиция по любому из пп.1-3, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
6. Композиция по любому из пп.1-5, где белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3 в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV3.
7. Композиция по п.6, где вектор экспрессии представляет собой бакуловирус.
8. Композиция по любому из пп.1-7, дополнительно содержащая белок ORF2 PCV2.
9. Композиция по п.8, где белок ORF2 PCV2 получен при экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV2.
10. Композиция по п.9, где вектор экспрессии представляет собой бакуловирус.
11. Композиция по любому из пп.1-10, дополнительно содержащая дополнительный антиген дополнительного патогена свиней.
12. Композиция по п.11, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, или антиген Pasteurella multocida.
13. Композиция по любому из пп.1-12, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
14. Композиция по любому из пп.1-12, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
15. Композиция по любому из пп.1-14, где адъювант включает гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в- масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащих линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/ капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой кислоты, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитололеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, Карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; адъювантную систему RIBI; блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
16. Композиция по любому из пп.1-15, содержащая примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл в дозе композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
17. Композиция по любому из пп.1-16, где иммуномодулирующий агент включает интерлейкин (интерлейкины), интерферон (интерфероны) или другой цитокин (цитокины), или гемоцианин лимфы улитки (KLH), или KLH, эмульгированный с неполным адъювантом Фрейнда (KLH/ICFA).
18. Композиция по любому из пп.1-17, содержащая примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика (антибиотиков).
19. Композиция по любому из пп.1-18, где антибиотик (антибиотики) включает гентамицин.
20. Композиция по любому из пп.1-19, содержащая (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
21. Композиция по п.20, где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доведен примерно до 6,5-7,5.
22. Композиция по п.20 или 21, где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
23. Композиция по любому из пп.1-22, составленная и/или упакованная для введения единичной дозы или однократной иммунизации, а не для режима множественных доз.
24. Способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, включающий введение животному композиции, определенной в любом из пунктов 1-23.
25. Способ по п.25, где животное представляет собой свинью.
26. Способ по п.25, где свинья представляет собой молодую свинью, или поросенка.
27. Способ по п.26, где молодая свинья или поросенок имеют возраст не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
28. Способ по п.26, где введение осуществляют в течение по меньшей мере 1, 2 или 3 недель после контакта с вирулентным цирковирусом свиней.
29. Способ по любому из пп.24-28, где введение включает единственную, введение путем однократного введения, или однократное введение одной дозы; а не режим многократной вакцинации или многократного введения.
30. Использование композиции по любому из пп.1-23 в способе любого из пунктов 24-29, или применение белка ORF2 PCV3, одного или в комбинации, в любой из композиций по пп.1-23, для использования при приготовлении композиции с целью индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, или для использования в способе индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
31. Способ получения композиции по любому из пп.1-23, включающий продукцию белка ORF2 PCV3 с помощью системы экспрессии бакуловируса в культивируемых клетках насекомых.
32. Способ по п.31, включающий инактивацию бакуловируса.
33. Способ по п.32, в котором инактивация включает тепловую обработку или использование агента, инактивирующего вирус.
34. Способ по п.25, где агент, инактивирующий вирус, включает азиридиновое соединение.
35. Способ по п. 26, где азиридиновое соединение включает BEI.
36. Рекомбинантный вектор, содержащий полинуклеотидную последовательность, кодирующую полипептидную последовательность, кодирующую белок ORF2 PCV3.
37. Рекомбинантный вектор по п. 36, где ORF2 PCV3 относится к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4).
38. Рекомбинантный вектор по п.36, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности или гомологии последовательности с SEQ ID NO: 1.
39. Рекомбинантный вектор по любому из пп.36-38, представляющий собой бакуловирус.
40. Рекомбинантный вектор по п.39, включающий по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности или гомологии последовательности с SEQ ID NO: 2.
НАБОР ПУНКТОВ B:
Набор пунктов B - Настоящее изобретение теперь будет описано посредством следующего набора пронумерованных пунктов (Набор пунктов B). Раскрытие в этом наборе пунктов в равной степени применимо к настоящему изобретению. Подобным образом раскрытие в этом наборе пунктов в равной степени применимо к каждому из других наборов пунктов.
1. Композиция, содержащая белок ORF2 цирковируса свиней 3 типа (PCV3), предпочтительно антигенный белок ORF2 PCV3 (антиген ORF2 PCV3).
2. Композиция по п.1, дополнительно содержащая ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизирующего агента, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии, иммуномодулирующего агента и/или любой их комбинации.
3. Композиция, в частности композиция по пп.1 или 2, содержащая: белок ORF2 цирковируса свиней 3 типа (PCV3), и ветеринарно приемлемый носитель, содержащий растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный или экспрессирующий вектор, иммуномодулирующий агент и/или любую их комбинацию.
4. Композиция по любому из пп.1-3, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
5. Композиция по любому из пп.1-4, где ветеринарно приемлемый носитель включает адъювант.
6. Композиция по любому из пп.1-5, где PCV3 выбран из группы, состоящей из PCV3a и PCV3b.
7. Композиция по любому из пп.1-6, где PCV3 представляет собой любую филогенетическую ветвь PCV3 или выбран из группы, состоящей из PCV3a1, PCV3b1, PCV3b2 и PCV3c.
8. Композиция по любому из пп.1-7, где ORF2 PCV3 относится к группе a1, b1 или b2.
9. Композиция по любому из пп.1-8, где белок ORF2 CV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
10. Композиция по любому из пп.1-9, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90% идентичности последовательности с последовательностью SEQ ID NO: 4.
11. Композиция по любому из пп.1-10, где белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3.
12. Композиция по любому из пп.1-11, где белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3 в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV3.
13. Композиция по п.12, где вектор экспрессии представляет собой бакуловирус.
14. Композиция по любому из пп.1-13, где белок ORF2 PCV3 представляет собой ORF2 PCV3, экспрессируемый рекомбинантным бакуловирусом.
15. Композиция по любому из пп.1-14, дополнительно включающая белок ORF2 PCV2, предпочтительно антигенный белок ORF2 PCV2 (антиген ORF2 PCV2).
16. Композиция по п.15, где белок ORF2 PCV2 получен при экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV2.
17. Композиция по п.16, где вектор экспрессии представляет собой бакуловирус.
18. Композиция по любому из пп.1-17, дополнительно включающая дополнительный антиген дополнительного патогена свиней.
19. Композиция по п.18, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV) или антиген Pasteurella multocida, или их комбинацию.
20. Композиция по любому из пп.1-19, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл. или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
21. Композиция по любому из п.п 1-20, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
22. Композиция по любому из пп.2-21, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/ капрат) пропиленгликоля; глицерилтри-(каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитол олеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
23. Композиция по любому из пп.2-22, содержащая примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл на дозу композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
24. Композиция по любому из пп.2-23, где иммуномодулирующий агент включает интерлейкин (интерлейкины), интерферон (интерфероны) или другой цитокин (цитокины).
25. Композиция по любому из пп.1-24, содержащая примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика (антибиотиков).
26. Композиция по любому из пп.1-25, где антибиотик (антибиотики) включает гентамицин.
27. Композиция по любому из пп.1-26, включающая (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
28. Композиция по п.27, где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят примерно до 6,5-7,5.
29. Композиция по пп.27 или 28, где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
30. Композиция по любому из пп.1-29, где указанная композиция составлена и/или упакована для однократного введения или однократного введения композиции, а не для режима множественных доз, или где указанная композиция составлена и/или упакована для многодозового режима введения композиции.
31. Композиция по любому из пп.1-30, являющаяся иммуногенной композицией.
32. Композиция по любому из пп.1-31 для использования в качестве лекарственного средства.
33. Композиция по любому из пп.1-31 для использования в качестве вакцины.
34. Композиция по любому из пп.1-31 для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV 2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
35. Композиция по любому из пп.1-31 для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для использования в способе лечения или профилактики инфекции PCV3 у животного, причем указанное животное предпочтительно представляет собой свинью.
36. Композиция по любому из пп.1-31 для применения в способе индукции иммунного ответа против PCV3 у этой молодой свиньи, в частности, предпочтительно у беременной свиноматки.
37. Композиция по любому из пп.1-31 для использования в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у поросят, при этом поросенок должен вскармливаться свиноматкой, которой вводили композицию.
38. Композиция для применения по п.37, где указанная свиноматка, которой вводили композицию, представляет собой свиноматку, которой вводили иммуногенную композицию, когда указанная свиноматка была беременна, в частности, указанным поросенком, или в период до осеменения.
39. Композиция для применения по любому из пп.32-38, где указанная композиция предназначена для введения внутримышечно или интрадермально.
40. Композиция для применения по любому из пп.36-39, предназначенная для введения указанной свиноматке внутримышечно или интрадермально.
41. Способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, включающий введение животному композиции, указанной в любом из пп.1-31.
42. Способ по п. 41, в котором животное представляет собой свинью.
43. Способ по п. 42, где свинья представляет собой молодую свинью, или поросенка.
44. Способ по пп.42 или 43, где свинья является свиноматкой.
45. Способ иммунизации субъекта, включающий введение субъекту композиции по любому из пп.1-31.
46. Способ иммунизации свиней против клинического заболевания, вызванного по меньшей мере одним патогеном у указанного животного, включающий стадию введения животному композиции по любому из пп.1-31, при этом указанная иммуногенная композиция не вызывает клинических признаков инфекции, но способна вызывать иммунный ответ, который иммунизирует животное против патогенных форм указанного по меньшей мере одного патогена.
47. Способ по п.46, где указанным по меньшей мере одним патогеном является PCV3.
48. Способ индукции выработки антител, специфичных к PCV3, у свиноматки, включающий введение указанной свиноматке композиции по любому из пп.1-31.
49. Способ уменьшения или предотвращения клинических признаков или клинических симптомов, вызванных инфекцией PCV3 у поросят, при этом указанный способ включает введение композиции по любому из пп.1-31 свиноматке и предоставление указанному поросенку возможности вскармливания указанной свиноматкой.
50. Способ по п.49, в котором указанная свиноматка является беременной свиноматкой, в частности, указанным поросенком, или подсвинком до осеменения.
51. Способ по пп. 49 или 50, включающий этапы введения композиции по любому из пп.1-31 свиноматке, беременной указанным поросенком, обеспечения рождения указанной свиноматкой указанного поросенка и обеспечения вскармливания указанного поросенка указанной свиноматкой.
52. Способ уменьшения клинических признаков и/или клинических симптомов, вызванных инфицированием PEDV у поросят, при котором поросенок должен вскармливаться свиноматкой, которой была введена композиция по любому из пп.1-31.
53. Способ по любому из пп.45-52, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят внутримышечно или интрадермально указанной свиноматке.
54. Способ по любому из пп.45-53, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят дважды указанной свиноматке.
55. Способ по любому из пп.45-54, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят дважды мукозально, предпочтительно дважды интраназально, указанной свиноматке.
56. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где указанные клинические признаки выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
57. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические признаки выбраны из группы, состоящей из выталкивания мумифицированного, мертворожденного и/или слабого плода.
58. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические симптомы выбраны из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
59. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические симптомы выбраны из группы, состоящей из развития или продукции мумифицированного, мертворожденного и/или слабого плода.
60. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где свинья или поросенок имеют возраст не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
61. Способ по п.60, где введение осуществляют в течение по меньшей мере 1, 2 или 3 недель воздействия вирулентного цирковируса свиней.
62. Композиция для применения по любому из пп.32-41 или способ по любому из пп.42-55, где введение включает единственное однократное введение, или однократное введение композиции в единчственной, одной дозе; а не режим многократного введения или многократного дозирования, или где введение состоит из однодозового, однократного введения, или однократного введения одной дозы; а не режима многократного введения или многократного дозирования, или где введение включает режим многократного введения или введения множества доз композиции, или где введение включает схему двукратного введения или введения двух доз композиции, или где введение состоит из режима двукратного введения или введения двух доз композиции.
63. Применение композиции по любому из пп.1-31 в способе по любому из пп.42-55, или применение белка ORF2 PCV3, отдельно или в комбинации, из любой из композиций по п.п 1-31, для использования при приготовлении композиции для индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, или для использования в способе индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
64. Способ получения композиции по любому из пп.1-31, включающий получение белка ORF2 PCV3 с помощью бакуловирусной системы экспрессии в культивируемых клетках насекомых.
65. Способ по п.64, включающий инактивацию бакуловируса.
66. Способ по п.65, где инактивация включает тепловую обработку или использование агента, инактивирующего вирус.
67. Способ по п.66, где агент, инактивирующий вирус, включает азиридиновое соединение.
68. Способ по п.67, где азиридиновое соединение включает BEI.
69. Рекомбинантный вектор, содержащий полинуклеотидную последовательность, кодирующую полипептидную последовательность, кодирующую белок ORF2 PCV3.
70. Рекомбинантный вектор по п.69, где ORF2 PCV3 относится к группе a1, b1 или b2.
71. Композиция, содержащая (i) белок ORF2 цирковируса свиней 3 типа (PCV3), белок парвовируса (PPV) и, при необходимости, белок PRRSV (вируса респираторного и репродуктивного синдрома свиней), и (ii) ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизатора, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии, иммуномодулирующего агента и/или любой их комбинации.
72. Композиция по п.71, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
73. Композиция по пп.71 или 72, где белок PPV представляет собой капсидный белок PPV VP2.
74. Композиция по любому из пп.71-73, где белок PRRSV представляет собой ORF4, ORF5, ORF6 или ORF7 вируса PRRS.
75. Композиция по пп.73 или 74, где белок PPV и/или белок PRRSV экспрессируются в векторе.
76. Композиция по любому из пп.71-75, представляющая собой иммуногенную композицию, вводимую в двух дозах свинье.
77. Композиция по п.76, где свинья является свиньей до первого опороса или свиноматкой.
78. Композиция по пп.76 или 77, где введение осуществляют до спаривания/осеменения, до беременности, во время беременности или во время лактации.
79. Композиция по любому из пп.76-78, где иммуногенная композиция содержит от 0,1 мкг до 150 мкг, предпочтительно от 0,25 мкг до 75 мкг, более предпочтительно от 0,5 мкг до 37,5 мкг, еще более предпочтительно от 0,5 мкг до 15 мкг, наиболее предпочтительно от 0,5 мкг до 6 мкг антигена PCV3, PPV и/или PRRSV.
80. Композиция по любому из пп.76-79, где иммуногенную композицию вводят внутримышечно.
81. Способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против цирковируса свиней 3 типа (PCV3), включающий парентеральное или подкожное применение у свиней однократной вакцинации, однократного введения или однократной дозы (i) по меньшей мере от 2 мкг до примерно 400 мкг рекомбинантного белка ORF2 PCV3, экспрессируемого бакуловирусной системой, и (ii) ветеринарно приемлемого носителя, содержащего растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, иммуномодулирующий агент и/или любую их комбинацию.
82. Способ по п.81, в котором свинья представляет собой поросенка, молодую свинью, или свиноматку, или подсвинка до осеменения.
83. Способ по п.81 или п.82, где свинья имеет возраст примерно 1 неделю, или 2 недели, или 3 недели, или 7-28, или 7-22, или 14-22, или 16-22, или 21±5 дней.
84. Способ по любому из пп.81-83, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
85. Способ по любому из пп.81-84, где ORF2 PCV3 представляет собой любую филогенетическую ветвь PCV3, или из группы PCV3a, PCV3a1, PCV3b, PCV3b1 или PCV3b.
86. Способ по любому из пп.81-85, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO : 1 или гомологии последовательности с SEQ ID NO: 1, SEQ ID NO: 6 или SEQ ID NO: 7.
87. Способ по любому из пп.81-86, где однократная вакцинация, однократное введение или однократная доза дополнительно включает белок ORF2 PCV2 или дополнительный антиген дополнительного патогена свиней.
88. Способ по п.87, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV) или антиген Pasteurella multocida, или их комбинацию.
89. Способ по любому из пп.81-88, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными, или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атомов углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитололеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; Блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
90. Способ по любому из пп.81-89, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл. мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
91. Способ по п.87, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
92. Способ по любому из пп.81-91, включающий примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл на дозу композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
93. Способ по любому из пп.82-92, где иммуномодулирующий агент включает интерлейкин, интерферон или другой цитокин.
94. Способ по любому из пп.81-93, где однократная вакцинация, однократное введение или однократная доза дополнительно включает примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика.
95. Способ по п.84, где антибиотик включает гентамицин.
96. Способ по любому из пп.81-95, где однократная вакцинация, однократное введение или однократная доза включает (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
97. Способ по п.96, где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят примерно до 6,5-7,5.
98. Способ по пп.96 или 97, где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит около 1 мг Карбопола или Карбопола 971.
99. Способ по любому из пп.81-98, дополнительно включающий уменьшение или предотвращение клинических признаков или заболевания, вызванного инфекцией PCV3 или вирусом эпидемической диареи свиней (PEDV), у беременной свиноматки или поросенка.
100. Способ по п.99, где уменьшение или предотвращение клинических признаков или заболевания у поросенка включает кормление поросенка свиноматкой, получавшей введение путем однократного введения, однократное введение или однократную дозу.
101. Способ по п.99, где уменьшение или предотвращение клинических признаков или заболевания у поросенка включает введение путем однократного введения, однократного введения или однократной дозы у беременной свиноматки.
102. Способ по п.101, дополнительно включающий кормление поросенка свиноматкой после рождения поросенка свиноматкой.
103. Способ по любому из пп.99–102, где клиническим признаком является снижение среднесуточного привеса, смертность, развитие, продукция или выталкивание мумифицированного, мертворожденного и/или слабого плода, макроскопическое поражение, гистологическое нарушение, репликация PCV3 в ткани или виремия PCV3.
104. Способ по любому из пп.81-103, где парентеральное или подкожное введение является внутримышечным или интрадермальным.
105. Неприродный белок ORF2 PCV3, содержащий сконструированную петлю FG, где петля FG содержит три или менее положительно заряженных аминокислот.
106. Белок ORF2 PCV3 по п.105, где петля FG содержит две положительно заряженные аминокислоты.
107. Белок ORF2 PCV3 по п.105, где петля FG содержит одну положительно заряженную аминокислоту.
108. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют положительно заряженные аминокислоты.
109. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют остатки аргинина и лизина.
110. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют остатки аргинина, лизина и гистидина.
111. Белок ORF2 PCV3 по п.105, где петля FG содержит QPFSYH, LSRGF или MASGF.
112. Неприродный белок ORF2 PCV3, содержащий сконструированное С-концевое удлинение.
113. Белок ORF2 PCV3 по п.112, где С-концевое удлинение включает примерно от 1 до 10, примерно от 5 до 20 или примерно от 10 до 30 аминокислот.
114. Белок ORF2 PCV3 по п.112, в котором С-концевое удлинение включает примерно от 1 до 10, или примерно от 5 до 20, или примерно от 10 до 30 аминокислот, примерно от 50 до 200 аминокислот, примерно от 60 до 190 аминокислот, примерно от 70 до 180 аминокислот, примерно от 80 до 170 аминокислот, примерно от 90 до 160 аминокислот, или примерно от 100 до 150 аминокислот.
115. Белок ORF2 PCV3 по п.112, где С-концевое удлинение содержит С-концевые аминокислоты из другого капсидного белка.
116. Белок ORF2 PCV3 по п.115, где C-концевое удлинение включает C-концевые аминокислоты из капсида PCV2, такого как капсид BFDV или капсид CaCV.
117. Белок ORF2 PCV3 по п.112, где С-концевое удлинение включает EFNLKDPPLN, PK или QFAPNNPSTEFDYETGRQL.
118. Способ получения самособирающегося капсидного белка ORF2 PCV3, который включает замену одной или нескольких аминокислот из аргинина, лизина или гистидина в петле FG на незаряженные положительно аминокислоты.
119. Способ усиления самосборки капсидного белка ORF2 PCV3, который включает добавление или вставку аминокислотных остатков на С-конце белка.
120. Способ по п.118, который включает добавление или вставку от 1 до 10, или примерно от 5 до 20, или примерно от 10 до 30 аминокислот, примерно от 50 до 200 аминокислот, примерно от 60 до 190 аминокислот, примерно от 70 до 180 аминокислот, примерно от 80 до 170 аминокислот, примерно от 90 до 160 аминокислот, или примерно от 100 до 150 аминокислот.
121. Способ по п.119, который включает добавление или вставку аминокислот из другого капсидного белка.
122. Способ по п.121, где добавленные или вставленные аминокислоты взяты из капсида PCV2, такого как капсид BFDV или капсид CaCV.
123. Способ по п.121, где добавленные или вставленные аминокислоты включают EFNLKDPPLN, PK или QFAPNNPSTEFDYETGRQL.
124. Композиция, содержащая белок PCV по любому из пп.105–117 или белок, полученный способом по любому из пп.118–123, в количестве, вызывающем иммунный ответ или защитный иммунный ответ против PCV3 и/или его клинических симптомов, при однократном введении, и ветеринарно приемлемый носитель, включающий растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, иммуномодулирующий агент и/или любую их комбинацию.
125. Композиция по п.124, где белок ORF2 PCV3 кодируется SEQ ID NO: 6 или SEQ ID NO: 7.
126. Композиция по пп.124 или 125, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
127. Композиция по любому из пп.124-126, дополнительно включающая белок ORF2 PCV2, предпочтительно антигенный белок ORF2 PCV2 (антиген ORF2 PCV2) или дополнительный антиген дополнительного патогена свиней.
128. Композиция по п.127, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV), или антиген Pasteurella multocida, или их комбинацию.
129. Композиция по любому из пп.124-128, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными, или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такие как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI -0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитололеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; Блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
130. Композиция по любому из пп.124-129, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
131. Композиция по любому из пп.124-130, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 мкг/дозу до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
132. Композиция по любому из пп.124-131, содержащая примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл на дозу композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
133. Композиция по любому из пп.125-132, где иммуномодулирующий агент включает интерлейкин, интерферон или другой цитокин.
134. Вектор, содержащий и экспрессирующий белок PCV по любому из пп.105–117 или белок, полученный способом по любому из пп.118–123.
135. Вектор по п.134, где белок PCV экспрессируется с помощью SEQ ID NO: 6 или SEQ ID NO: 7.
136. Вектор по пп.134 или 135, представляющий собой бакуловирус.
137. Способ получения композиции по любому из пп.125-133, включающий получение белка ORF2 PCV3 с помощью бакуловирусной системы экспрессии в культивируемых клетках насекомых.
138. Способ по п.137, дополнительно включающий инактивацию бакуловируса.
139. Способ по п.138, где инактивация включает тепловую обработку или использование агента, инактивирующего вирус.
140. Способ по п.139, где агент, инактивирующий вирус, включает азиридиновое соединение.
141. Способ по п.140, где азиридиновое соединение включает BEI.
НАБОР ПУНКТОВ C:
Набор пунктов C - Настоящее изобретение теперь будет описано посредством следующего набора пронумерованных пунктов (набор пунктов C). Раскрытие в этом наборе пунктов в равной степени применимо к настоящему изобретению. Подобным образом раскрытие в этом наборе пунктов в равной степени применимо к каждому из других наборов пунктов.
1. Антигенный белок цирковируса свиней 3 типа (PCV3), где указанный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант.
2. Белок по п.1, где указанный белок ORF2 PCV3 представляет собой белок, кодируемый SEQ ID No. 1.
3. Белок по пп.1 или 2, представляющий собой функциональный антигенный вариант ORF2 PCV3.
4. Белок по любому из предыдущих пунктов, представляющий собой функциональный антигенный вариант белка, кодируемого SEQ ID No. 1.
5. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант способен давать более высокий выход вирусоподобных частиц (VLP), чем белок, кодируемый SEQ ID No. 1.
6. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант способен давать более высокий выход VLP, чем белок, кодируемый SEQ ID No. 1, как можно определить с помощью вестерн-блоттинга.
7. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет меньше положительно заряженных аминокислотных остатков, чем белок, кодируемый SEQ ID No. 1.
8. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1.
9. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замены одного или нескольких из остатка S и/или остатков K и/или остатка H мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
10. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замены одного или нескольких из остатка S и/или остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No.1.
11. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замены остатка S или остатка H и всех остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
12. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замену по меньшей мере S и/или H и любого K мотива SKKKH петли FG белка, кодируемого SEQ ID No.1, на Q, P, F или S.
13. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замену мотива SKKK в мотиве SKKKH петли FG белка, кодируемого SEQ ID No.1, на QPFS, или замену мотива KKKH в мотиве SKKKH петли FG белка, кодируемого SEQ ID No.1, на QPFS.
14. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
15. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
16. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, выходящую за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, предпочтительно, где указанное удлинение является полным или включает последовательность из вируса Сircoviridae, и предпочтительно в котором по меньшей мере часть указанного удлинения заменяет концевую последовательность SVL белка, кодируемого SEQ ID No.1.
17. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, и где указанное удлинение составляет от 1 до 100 аминокислот.
18. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, и где указанное удлинение составляет от 1 до 50 аминокислот.
19. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, и где указанное удлинение составляет от 1 до 30 аминокислот.
20. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, где указанное удлинение составляет от 1 до 30 аминокислот, и где указанное удлинение включает всю часть последовательности VKININLTPPVATSRVPSRALPLRFGCGHR.
21. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, где указанное удлинение составляет от 1 до 30 аминокислот, и где указанное удлинение включает всю последовательность VKININLTPPVATSRVPSRALPLRFGCGHR.
22. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID No. 1, 2, 5, 6 или 7.
23. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
24. Белок по любому из предыдущих пунктов, где указанный белок представляет собой рекомбинантный белок, полученный способами рекомбинантной ДНК.
25. Белок по любому из предыдущих пунктов, представляющий собой белок, экспрессируемый бакуловирусом.
26. Белок по любому из предыдущих пунктов, где указанный PCV3 выбран из группы, состоящей из PCV3a и PCV3b.
27. Белок по любому из предыдущих пунктов, где указанный PCV3 представляет собой любую филогенетическую ветвь PCV3, или выбран из группы, состоящей из PCV3a1, PCV3b1, PCV3b2 и PCV3c.
28. Белок по любому из предыдущих пунктов, где указанная ORF2 PCV3 принадлежит к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.1186/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4).
29. Белок по любому из предыдущих пунктов, где указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
30. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO:1 или гомологии последовательности с SEQ ID NO: 6.
31. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO:1 или гомологии последовательности с SEQ ID NO:7.
32. Белок по любому из предыдущих пунктов, где указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
33. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, или белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет одну или несколько замен в петле FG.
34. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4 , 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, или белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1.
35. Белок по любому из предыдущих пунктов, представляющий собой рекомбинантный белок в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
36. Белок по любому из предыдущих пунктов, представляющий собой рекомбинантный белок, полученный в результате его экспрессии бакуловирусным вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
37. Нуклеотидная последовательность, кодирующая белок по любому из предыдущих пунктов.
38. Вектор, содержащий нуклеотидную последовательность по любому из предыдущих пунктов.
39. Рекомбинантный вектор, содержащий нуклеотидную последовательность по любому из предыдущих пунктов.
40. Хозяин экспрессии, трансформированный или трансфицированный нуклеотидной последовательностью по любому из предыдущих пунктов.
41. Хозяин бакуловирусной экспрессии, трансформированный или трансфицированный нуклеотидной последовательностью по любому из предыдущих пунктов.
42. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию нуклеотидной последовательности по любому из предыдущих пунктов.
43. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию вектора по любому из предыдущих пунктов.
44. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию рекомбинантного вектора по любому из предыдущих пунктов.
45. Способ получения белка по любому из предыдущих пунктов, включающий культивирование хозяина экспрессии по любому из предыдущих пунктов, чтобы вызвать экспрессию белка.
46. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина экспрессии, чтобы вызвать экспрессию белка.
47. Способ получения белка по любому из предыдущих пунктов, включающий культивирование хозяина для бакуловирусной экспрессии по любому из предыдущих пунктов, чтобы вызвать экспрессию белка.
48. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии, чтобы вызвать экспрессию белка.
49. Способ по любому из предыдущих пунктов, где инактивирующий агент используют, когда достигнуты достаточные уровни экспрессированного белка.
50. Способ по любому из предыдущих пунктов, где инактивирующий агент, содержащий бинарный этиленимин (BEI), используют, когда достигнуты достаточные уровни экспрессированного белка.
51. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белок, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок.
52. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белок, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где около 90% компонентов (i) - (iii) имеют размер менее 1 мкм.
53. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят до примерно 6,5-7,5.
54. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых.
55. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса.
56. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус.
57. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение.
58. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение, где азиридиновое соединение включает BEI.
59. Белок, получаемый способом по любому из предыдущих пунктов.
60. Композиция, содержащая белок, получаемый способом по любому из предыдущих пунктов.
61. Композиция, которую можно получить способом по любому из предыдущих пунктов.
62. Композиция, содержащая белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель.
63. Композиция, содержащая белок по любому из предыдущих пунктов и ветеринарно приемлемый носитель, разбавитель или наполнитель.
64. Композиция по любому из предыдущих пунктов, в которой белок присутствует в количестве от 0,2 до примерно 400 мкг/мл, или от 2 до примерно 400 мкг/мл, или от 4 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или от 2 примерно до 200 мкг/мл, или от 4 до примерно до 200 мкг/мл, или от 8 до примерно 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или от 2 до примерно 100 мкг/мл, или от 4 до примерно 100 мкг/мл, или от 8 до примерно 100 мкг/мл, или примерно от 4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
65. Композиция, включающая белок по любому из предыдущих пунктов, содержащая одно или несколько из растворителя, дисперсионной среды, покрытия, стабилизирующего агента, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии и/или иммуномодулирующего агента.
66. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель представляет собой любой одно или несколько из адъюванта, иммуномодулирующего агента, надосадочной жидкости клеточной культуры, вирусного вектора или вектора экспрессии, или любой их комбинации.
67. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант.
68. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант включает один или несколько из полимера акриловой или метакриловой кислоты; сополимера малеинового ангидрида и алкенильного производного; сшитого полимера акриловой или метакриловой кислоты; полимера акриловой или метакриловой кислоты, сшитого с полиалкениловым эфиром сахара или полиспирта; карбомера; акрилового полимера, поперечно сшитого полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопола; Карбопола 974P; Карбопола 934P; Карбопола 971P; гидроксида алюминия; фосфата алюминия; сапонина; Quil A; QS-21; GPI-0100; эмульсии вода-в-масле; эмульсии масло-в-воде; эмульсии вода-в-масле-в-воде; эмульсии на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидного масла; сквалана; скваланового масла, полученного в результате олигомеризации алкенов, изобутена или децена; сложного эфира (эфиров) кислоты (кислот) или спирта (спиртов), содержащего линейную алкильную группу; растительного масла (масел); этилолеата; ди-(каприлата/капрата) пропиленгликоля; глицерилтри-(каприлата/капрата); диолеата пропиленгликоля; сложного эфира (эфиров) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложного эфира (эфиров) изостеариновой кислоты; неионного поверхностно-активного вещества (веществ); сложного эфира (эфиров) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированного, ангидроманнитололеата; блок-сополимеров полиоксипропилена и полиоксиэтилена, продукта Плюроник, адъювантной системы RIBI; блок-сополимера; SAF-M; монофосфориллипида А; авридинового липидно-аминового адъюванта; термолабильного энтеротоксина из E. coli (рекомбинантного или другого); токсина холеры; IMS 1314 или мурамилдипептида.
69. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант включает Карбопол или Карбопол 971.
70. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант присутствует в количестве примерно от 50 мкг до 2000 от композиции, или где адъювант присутствует в дозе композиции примерно 250 мкг/мл, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг от композиции, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг от композиции; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг от композиции, или адъювант присутствует в количестве примерно 1 мг от композиции.
71. Композиция по любому из предыдущих пунктов, содержащая иммуномодулирующий агент.
72. Композиция по любому из предыдущих пунктов, содержащая иммуномодулирующий агент, и где иммуномодулирующий агент представляет собой один или несколько из интерлейкина (интерлейкинов), интерферона (интерферонов) или другого цитокина (цитокинов).
73. Композиция по любому из предыдущих пунктов, где композиция содержит антибиотик (антибиотики).
74. Композиция по любому из предыдущих пунктов, где содержащая антибиотик (антибиотики), где антибиотик (антибиотики) включает гентамицин.
75. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики), и где композиция содержит примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков).
76. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики), и где композиция содержит примерно от 1 мкг/мл до менее примерно 30 мкг/мл антибиотика (антибиотиков).
77. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген.
78. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном ORF2 PCV3.
79. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном PCV3.
80. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген дополнительного патогена свиней.
81. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген дополнительного патогена свиней, при этом указанный патоген представляет собой любой один или несколько из антигенов PCV2, PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактеринового антигена Mycoplasma hyopneumoniae, антигена надосадочной жидкости Mycoplasma hyopneumoniae, антигена болезни Ауески или псевдобешенства, антигена свиного гриппа, антигена чумы свиней (классической или африканской, или их комбинации), антигена Actinobacillus pleuropneumoniae, антигена Escherichia coli, антигена парвовируса свиней (PPV) или антигена Pasteurella multocida.
82. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген дополнительного патогена свиней, причем указанная композиция дополнительно содержит один или несколько из антигена PCV2, антигена PRRSV и антигена PPV.
83. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2.
84. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2.
85. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой рекомбинантный белок ORF2 PCV2.
86. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2, экспрессируемый рекомбинантным бакуловирусом.
87. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме.
88. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для введения разовой дозы или однократной вакцинации.
89. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для режима приема нескольких доз.
90. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для режима приема двух доз.
91. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера.
92. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 10 доз указанной композиции.
93. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 50 доз указанной композиции.
94. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 100 доз указанной композиции.
95. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 200 доз указанной композиции.
96. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и где указанная лекарственная форма доставляется из контейнера, содержащего большое количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 250 доз указанной композиции.
97. Композиция по любому из предыдущих пунктов, содержащая антиген PCV2, где антиген PCV2 представляет собой рекомбинантный бакуловирус, экспрессирующий белок ORF2 PCV2, и где либо белок, либо комбинированное общее количество белка ORF2 PCV3 и белка ORF PCV2 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или от 2 до примерно 400 мкг/дозу, или от 4 до примерно 400 мкг/дозу. или от 8 до примерно 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или от 2 до примерно 200 мкг/дозу, или от 4 до примерно 200 мкг/дозу, или от 8 до примерно 200 мкг/дозу, или примерно 0,35 до 100 мкг/дозу, или от 2 до примерно 100 мкг/дозу, или от 4 до примерно 100 мкг/дозу, или от 8 до примерно 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
98. Композиция по любому из предыдущих пунктов, содержащая соль.
99. Композиция по любому из предыдущих пунктов, содержащая инактивированный вирусный вектор и/или надосадочную жидкость клеточной культуры.
100. Композиция по любому из предыдущих пунктов, содержащая инактивированный вирусный вектор и надосадочную жидкость клеточной культуры.
101. Композиция по любому из предыдущих пунктов, содержащая (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
102. Композиция по любому из предыдущих пунктов, содержащая (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации, и где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
103. Композиция по любому из предыдущих пунктов, представляющая собой иммуногенную композицию, содержащую белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель.
104. Композиция по любому из предыдущих пунктов, представляющая собой иммуногенную композицию, содержащую белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель, и дополнительный антиген по любому из предыдущих пунктов.
105. Способ получения композиции по любому из предыдущих пунктов, где белок по любому из предыдущих пунктов смешивают с носителем, разбавителем или наполнителем.
106. Способ получения композиции по любому из предыдущих пунктов, где белок по любому из предыдущих пунктов смешивают с носителем, разбавителем или наполнителем, и дополнительным антигеном.
107. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в качестве лекарственного средства.
108. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в качестве вакцины.
109. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у животного.
110. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиней.
111. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов. пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у молодых свиней.
112. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят.
113. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят; при этом поросята должны получать вскармливание от свиноматок, которым вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
114. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиноматок.
115. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для использования в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у беременных свиноматок, свиней до первого опороса, или подсвинков до осеменения.
116. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов. пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у животных.
117. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у свиней.
118. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у молодых свиней.
119. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у поросят.
120. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у поросят; при этом поросята должны получать вскармливание свиноматками, которым вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
121. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у свиноматок.
122. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у беременных свиноматок, свиней до первого опороса или подсвинков до осеменения.
123. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного.
124. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является свиньей.
125. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой молодую свинью.
126. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой поросенка.
127. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов. пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
128. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является свиноматкой.
129. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов. пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
130. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3.
131. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное является свиньей.
132. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой молодую свинью.
133. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой поросенка.
134. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
135. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное является свиноматкой.
136. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
137. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного.
138. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиньей.
139. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой молодую свинью.
140. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или прекращения экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка.
141. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
141. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиноматкой.
142. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения в способе уменьшения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
143. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного.
144. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное является свиньей.
145. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой молодую свинью.
146. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка.
147. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
148. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное является свиноматкой.
149. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
150. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят указанному животному внутримышечно или интрадермально.
151. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят указанному животному вместе с другим антигеном, предпочтительно при этом другой патоген является антигеном патогена свиней.
152. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном ORF2 PCV3, предпочтительно, где другой патоген является антигеном патогена свиней.
153. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном PCV3, предпочтительно, где другой патоген является антигеном патогена свиньи.
154. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой свиноматку, беременную поросенком.
155. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой свиноматку, беременную поросенком, и при этом поросенок должен получать вскармливание свиноматкой, которой вводили белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов.
156. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где указанный белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов вводят дважды указанной свиноматке.
157. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где указанный белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят только дважды указанной свиноматке.
158. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку.
159. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят только один раз указанному поросенку.
160. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов дважды вводят указанной свиноматке, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
161. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов дважды вводят указанной свиноматке, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
162. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят только дважды указанной свиноматке, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
163. Белок по любому из предыдущих пунктов или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
164. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
165. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов, или нуклеотидную последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композицию по любому из предыдущих пунктов вводят только один раз указанному поросенку, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
166. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при применении состоит из однодозовой, однократной вакцинации или однократного введения одной дозы указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
167. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при применении состоит из режима многократной вакцинации или режима введения нескольких доз указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
168. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при применении состоит из двукратного введения, или двукратного введения дозы указанного белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
169. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному осуществляют в течение по меньшей мере 1, 2 или 3 недель воздействия вирулентного цирковируса свиней.
170. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где животным является поросенок в возрасте не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
171. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или указанная композиция по любому из предыдущих пунктов предназначена для применения по любому из предыдущих пунктов.
172. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов предназначен для применения по любому из предыдущих пунктов.
173. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанная композиция по любому из предыдущих пунктов предназначена для применения по любому из предыдущих пунктов.
174. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному перед введением белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
175. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному одновременно с введением белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
176. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному в то же время и в той же композиции, что и при введении белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
177. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному в то же время и в другой композиции, при введении белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
178. Белок по любому из предыдущих пунктов, или нуклеотидная последовательность по любому из предыдущих пунктов, или вектор экспрессии по любому из предыдущих пунктов, или хозяин экспрессии по любому из предыдущих пунктов, или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному после введения белка по любому из предыдущих пунктов, или нуклеотидной последовательности по любому из предыдущих пунктов, или вектора экспрессии по любому из предыдущих пунктов, или хозяина экспрессии по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
179. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации свиней для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у свиней, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье в одной дозе.
180. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в одной дозе.
181. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье в двух дозах.
182. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в двух дозах.
183. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции. которую вводят этой молодой свинье в одной дозе.
184. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции. которую вводят этой молодой свинье только в одной дозе.
185. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции. которую вводят этой молодой свинье в двух дозах.
186. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции. которую вводят этой молодой свинье только в двух дозах.
187. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где одну дозу иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
188. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где только одну дозу иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
189. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где две дозы иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
190. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где только две дозы иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
191. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
192. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
193. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из развития или продукции мумифицированного плода.
194. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы представляют собой или включают выталкивание мумифицированного, мертворожденного и/или слабого плода.
НАБОР ПУНКТОВ D:
Набор пунктов D - Настоящее изобретение теперь будет описано посредством следующего набора пронумерованных пунктов (Набора пунктов D). Раскрытие в этом наборе пунктов в равной степени применимо к настоящему изобретению. Подобным образом раскрытие в этом наборе пунктов в равной степени применимо к каждому из других наборов пунктов.
1. Антигенный белок цирковируса свиней 3 типа (PCV3), являющийся функциональным антигенным вариантом белка ORF2 PCV3.
2. Белок по п.1, где указанный белок ORF2 PCV3 представляет собой белок, кодируемый SEQ ID No. 1.
3. Белок по пп.1 или 2, содержащий замены и/или удлинения ORF2 PCV3.
4. Белок по любому из предыдущих пунктов, представляющий собой функциональный антигенный вариант белка, кодируемого SEQ ID No.1.
5. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант способен давать более высокий выход вирусоподобных частиц (VLP), чем белок, кодируемый SEQ ID No.1.
6. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант способен давать более высокий выход VLP, чем белок, кодируемый SEQ ID No.1, как можно определить с помощью вестерн-блоттинга.
7. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет меньше положительно заряженных аминокислотных остатков, чем белок, кодируемый SEQ ID No.1.
8. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1.
9. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замены одного или нескольких остатков S, и/или остатков K и/или остатка H мотива SKKKH петли FG белка, кодируемого SEQ ID No. 1.
10. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No. 1, где эти замены включают замены одного или нескольких из остатка S, и/или остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No.1.
11. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замены остатка S или остатка H и всех остатков K мотива SKKKH петли FG белка, кодируемого SEQ ID No.1.
12. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замену по меньшей мере S и/или H и любого K из мотива SKKKH петли FG белка, кодируемого SEQ ID No.1, на Q, P, F или S.
13. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замену мотива SKKK в мотиве SKKKH петли FG белка, кодируемого SEQ ID No.1, на QPFS, или замену мотива KKKH в мотиве SKKKH петли FG белка, кодируемого SEQ ID No.1, на QPFS.
14. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
15. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
16. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, предпочтительно, где указанное удлинение является полным или включает последовательность от цирковируса, и предпочтительно где по меньшей мере часть указанного удлинения заменяет концевую последовательность SVL белка, кодируемого SEQ ID No.1.
17. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, и где указанное удлинение составляет от 1 до 100 аминокислот.
18. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1, и где указанное удлинение составляет от 1 до 50 аминокислот.
19. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, и где указанное удлинение составляет от 1 до 30 аминокислот.
20. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, где указанное удлинение составляет от 1 до 30 аминокислот, и где указанное удлинение включает всю часть последовательности VKININLTPPVATSRVPSRALPLRFGCGHR.
21. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, где указанное удлинение составляет от 1 до 30 аминокислот, и где указанное удлинение включает всю последовательность VKININLTPPVATSRVPSRALPLRFGCGHR.
22. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NО: 1, 2, 5, 6 или 7.
23. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID NO: 1, 2, 5, 6 или 7.
24. Белок по любому из предыдущих пунктов, представляющий собой рекомбинантный белок, полученный методами рекомбинантной ДНК.
25. Белок по любому из предыдущих пунктов, представляющий собой белок, экспрессируемый бакуловирусом.
26. Белок по любому из предыдущих пунктов, где указанный PCV3 выбран из группы, состоящей из PCV3a и PCV3b.
27. Белок по любому из предыдущих пунктов, где указанный PCV3 представляет собой любую филогенетическую ветвь PCV3 или выбран из группы, состоящей из PCV3a1, PCV3b1, PCV3b2 и PCV3c.
28. Белок по любому из предыдущих пунктов, где указанная ORF2 PCV3 принадлежит к группе a1, b1 или b2 (с использованием обозначения подтипа Fux et al., «Full genome characterization of porcine circovirus type 3 isolates reveals the existence of two distinct groups of virus strains», Virology Journal (2018) 15:25, DOI 10.118/s12985-018-0929-3 (включено в настоящий документ посредством ссылки); см., например, таблицу 4).
29. Белок по любому из предыдущих пунктов, где указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
30. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO:1 или гомологии последовательности с SEQ ID NO:6.
31. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO:1 или гомологии последовательности с SEQ ID NO:7.
32. Белок по любому из предыдущих пунктов, где указанный белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок.
33. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, или белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок является рекомбинантным белком, и где указанный белок имеет одну или несколько замен в петле FG.
34. Белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4 , 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, или белок по любому из предыдущих пунктов, где указанный вариантный белок содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3, 4, 8, 9 или 10, и/или где белок представляет собой рекомбинантный белок, и где указанный белок имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No. 1.
35. Белок по любому из предыдущих пунктов, представляющий собой рекомбинантный белок в результате его экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
36. Белок по любому из предыдущих пунктов, представляющий собой рекомбинантный белок, полученный в результате его экспрессии бакуловирусным вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок.
37. Нуклеотидная последовательность, кодирующая белок по любому из предыдущих пунктов.
38. Вектор, содержащий нуклеотидную последовательность по любому из предыдущих пунктов.
39. Рекомбинантный вектор, содержащий нуклеотидную последовательность по любому из предыдущих пунктов.
40. Хозяин экспрессии, трансформированный или трансфицированный нуклеотидной последовательностью по любому из предыдущих пунктов.
41. Хозяин бакуловирусной экспрессии, трансформированный или трансфицированный нуклеотидной последовательностью по любому из предыдущих пунктов.
42. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию нуклеотидной последовательности по любому из предыдущих пунктов.
43. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию вектора по любому из предыдущих пунктов.
44. Способ получения белка по любому из предыдущих пунктов, включающий экспрессию рекомбинантного вектора по любому из предыдущих пунктов.
45. Способ получения белка по любому из предыдущих пунктов, включающий культивирование хозяина экспрессии по любому из предыдущих пунктов, чтобы вызвать экспрессию белка.
46. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для экспрессии, чтобы вызвать экспрессию белка.
47. Способ получения белка по любому из предыдущих пунктов, включающий культивирование хозяина для бакуловирусной экспрессии по любому из предыдущих пунктов, чтобы вызвать экспрессию белка.
48. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии для того, чтобы вызвать экспрессию белка.
49. Способ по любому из предыдущих пунктов, где инактивирующий агент используют, когда достигнуты достаточные уровни экспрессии белка.
50. Способ по любому из предыдущих пунктов, где инактивирующий агент, включающий бинарный этиленимин (BEI), используют, когда достигнуты достаточные уровни экспрессированного белка.
51. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующую указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок.
52. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм.
53. Способ получения белка по любому из предыдущих пунктов, включающий трансфекцию хозяина для бакуловирусной экспрессии нуклеотидной последовательностью вектора по любому из предыдущих пунктов и культивирование хозяина для бакуловирусной экспрессии в среде, чтобы вызвать экспрессию белка, где среда после экспрессии белка включает (i) указанный белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, и где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят до примерно 6,5-7,5.
54. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых.
55. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса.
56. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус.
57. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение.
58. Способ получения белка по любому из предыдущих пунктов, включающий получение белка бакуловирусной системой экспрессии в культивируемых клетках насекомых, и где способ включает стадию инактивации бакуловируса, и где стадия инактивации включает тепловую обработку или использование агента, инактивирующего вирус, и где агент, инактивирующий вирус, включает азиридиновое соединение, где азиридиновое соединение включает BEI.
59. Белок, получаемый способом по любому из предыдущих пунктов.
60. Композиция, содержащая белок, получаемый способом по любому из предыдущих пунктов.
61. Композиция, которую можно получить способом по любому из предыдущих пунктов.
62. Композиция, содержащая белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель.
63. Композиция, содержащая белок по любому из предыдущих пунктов и ветеринарно приемлемый носитель, разбавитель или наполнитель.
64. Композиция по любому из предыдущих пунктов, где белок присутствует в количестве от 0,2 до примерно 400 мкг/мл, или от 2 до примерно 400 мкг/мл, или от 4 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или от 8 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или от 2 примерно до 200 мкг/мл, или от 4 примерно до 200 мкг/мл, или от 8 примерно до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или от 2 до примерно 100 мкг/мл, или от 4 до примерно 100 мкг/мл, или от 8 до примерно 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
65. Композиция, содержащая белок по любому из предыдущих пунктов, включающая одно или несколько из растворителя, дисперсионной среды, покрытия, стабилизирующего агента, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии и/или иммуномодулирующего агента.
66. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель представляет собой любой один или несколько из адъюванта, иммуномодулирующего агента, надосадочной жидкости клеточной культуры, вирусного вектора или вектора экспрессии, или любой их комбинации.
67. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант.
68. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант включает один или несколько из полимера акриловой или метакриловой кислоты; сополимера малеинового ангидрида и алкенильного производного; сшитого полимера акриловой или метакриловой кислоты; полимера акриловой или метакриловой кислоты, сшитого с полиалкениловым эфиром сахара или полиспирта; карбомера; акрилового полимера, поперечно сшитого полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; Карбопола; Карбопола 974P; Карбопола 934P; Карбопола 971P; гидроксида алюминия; фосфата алюминия; сапонина; Quil A; QS-21; GPI-0100; эмульсии вода-в-масле; эмульсии масло-в-воде; эмульсии вода-в-масле-в-воде; эмульсии на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидного масла; сквалана; скваланового масла, полученного в результате олигомеризации алкенов, изобутена или децена; сложного эфира (эфиров) кислоты (кислот) или спирта (спиртов), содержащего линейную алкильную группу; растительного масла (масел); этилолеата; ди-(каприлата/капрата) пропиленгликоля; глицерилтри-(каприлата/капрата); диолеата пропиленгликоля; сложного эфира (эфиров) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложного эфира (эфиров) изостеариновой кислоты; неионного поверхностно-активного вещества (веществ); сложного эфира (эфиров) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированного, ангидроманнитололеата; блок-сополимеров полиоксипропилена и полиоксиэтилена, продукта Плюроник, адъювантной системы RIBI; блок-сополимера; SAF-M; монофосфориллипида А; авридинового липидно-аминового адъюванта; термолабильного энтеротоксина из E. coli (рекомбинантного или другого); токсина холеры; IMS 1314 или мурамилдипептида.
69. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант включает Карбопол или Карбопол 971.
70. Композиция по любому из предыдущих пунктов, где носитель, разбавитель или наполнитель включает адъювант, где адъювант присутствует в количестве примерно от 50 мкг до 2000 от композиции, или где адъювант присутствует в количество примерно 250 мкг/мл дозы композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг композиции, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг от композиции; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг от композиции, или адъювант присутствует в количестве примерно 1 мг от композиции.
71. Композиция по любому из предыдущих пунктов, содержащая иммуномодулирующий агент.
72. Композиция по любому из предыдущих пунктов, содержащая иммуномодулирующий агент, и где иммуномодулирующий агент представляет собой один или несколько из интерлейкина (интерлейкинов), интерферона (интерферонов) или другого цитокина (цитокинов).
73. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики).
74. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики), где антибиотик (антибиотики) включает гентамицин.
75. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики), и содержащая примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков).
76. Композиция по любому из предыдущих пунктов, содержащая антибиотик (антибиотики), и содержащая примерно от 1 мкг/мл до менее примерно 30 мкг/мл антибиотика (антибиотиков).
77. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген.
78. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном ORF2 PCV3.
79. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген, где указанный дополнительный антиген не является антигеном PCV3.
80. Композиция по любому из предыдущих пунктов, содержащая дополнительный антиген дополнительного патогена свиней.
81. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген дополнительного патогена свиней, где указанный патоген представляет собой любой один или несколько из антигенов PCV2, PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактеринового антигена Mycoplasma hyopneumoniae, антигена надосадочной жидкости Mycoplasma hyopneumoniae, антигена болезни Ауески или псевдобешенства, антигена свиного гриппа, антигена свиной чумы (классической или африканской, или их комбинации), антигена Actinobacillus pleuropneumoniae, антигена Escherichia coli, антигена парвовируса свиней (PPV) или антигена Pasteurella multos.
82. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген дополнительного патогена свиней, причем указанная композиция дополнительно содержит один или несколько из антигена PCV2, антигена PRRSV и антигена PPV.
83. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2.
84. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой белок ORF2 PCV2.
85. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой рекомбинантный белок ORF2 PCV2.
86. Композиция по любому из предыдущих пунктов, дополнительно содержащая антиген PCV2, где антиген PCV2 представляет собой экспрессируемый бакуловирусом рекомбинантный белок ORF2 PCV2.
87. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме.
88. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для введения разовой дозы или однократной вакцинации.
89. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для режима приема нескольких доз.
90. Композиция по любому из предыдущих пунктов, составленная и/или упакованная для режима приема двух доз.
91. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера.
92. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 10 доз указанной композиции.
93. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 50 доз указанной композиции.
94. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 100 доз указанной композиции.
95. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 200 доз указанной композиции.
96. Композиция по любому из предыдущих пунктов, находящаяся в лекарственной форме, и при этом указанная лекарственная форма доставляется из контейнера, содержащего большее количество указанной композиции, и при этом лекарственная форма указанной композиции может быть доставлена из указанного контейнера, и при этом указанный контейнер содержит по меньшей мере 250 доз указанной композиции.
97. Композиция по любому из предыдущих пунктов, содержащая антиген PCV2, где антиген PCV2 представляет собой экспрессируемый бакуловирусом рекомбинантный белок ORF2 PCV2, и где либо белок, либо комбинированные общие белки ORF2 PCV3 и ORF PCV2 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или от 2 до примерно 400 мкг/дозу, или от 4 до примерно 400 мкг/дозу. или от 8 до примерно 400 мкг/дозу, или примерно от 0,3 до примерно 200 мкг/дозу, или от 2 до примерно 200 мкг/дозу, или от 4 до примерно 200 мкг/дозу, или от 8 до примерно 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или от 2 до примерно 100 мкг/дозу, или от 4 до примерно 100 мкг/дозу, или от 8 до примерно 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или от 1,5 до примерно 2,0 мкг/дозу или примерно 1,6 мкг/дозу.
98. Композиция по любому из предыдущих пунктов, содержащая соль.
99. Композиция по любому из предыдущих пунктов, содержащая инактивированный вирусный вектор и/или надосадочную жидкость клеточной культуры.
100. Композиция по любому из предыдущих пунктов, содержащая инактивированный вирусный вектор и надосадочную жидкость клеточной культуры.
101. Композиция по любому из предыдущих пунктов, содержащая (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, включающий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
102. Композиция по любому из предыдущих пунктов, содержащая (i) белок, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, который экспрессировал указанный белок, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации, и где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
103. Композиция по любому из предыдущих пунктов, представляющая собой иммуногенную композицию, содержащую белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель.
104. Композиция по любому из предыдущих пунктов, представляющая собой иммуногенную композицию, содержащую белок по любому из предыдущих пунктов и носитель, разбавитель или наполнитель, и дополнительный антиген по любому из предыдущих пунктов.
105. Способ получения композиции по любому из предыдущих пунктов, где белок по любому из предыдущих пунктов смешивают с носителем, разбавителем или наполнителем.
106. Способ получения композиции по любому из предыдущих пунктов, где белок по любому из предыдущих пунктов смешивают с носителем, разбавителем или наполнителем, и дополнительным антигеном.
107. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в качестве лекарственного средства.
108. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в качестве вакцины.
109. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у животного.
110. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиней.
111. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у молодых свиней.
112. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят.
113. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у поросят; при этом поросята должны получать вскармливание свиноматками, которым вводили белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов.
114. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиноматок.
115. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у беременных свиноматок, свиней до первого опороса или подсвинков до осеменения.
116. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у животных.
117. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у свиней.
118. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у молодых свиней.
119. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у поросят.
120. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у поросят; при этом поросята должны получать вскармливание свиноматками, которым вводили белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов.
121. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у свиноматок.
122. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции иммунного ответа против PCV3 у беременных свиноматок, свиней до первого опороса или подсвинков до осеменения.
123. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного.
124. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой свинью.
125. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой молодую свинью.
126. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой поросенка.
127. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой был введен белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов.
128. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является свиноматкой.
129. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе уменьшения или предотвращения клинических признаков или клинических симптомов, или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
130. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3.
131. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой свинью.
132. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой молодую свинью.
133. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой поросенка.
134. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой был введен белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов.
135. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное является свиноматкой.
136. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
137. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного.
138. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой свинью.
139. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой молодую свинью.
140. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка.
141. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой был введен белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов.
141. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиноматкой.
142. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
143. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного.
144. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой свинью.
145. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой молодую свинью.
146. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка.
147. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой поросенка, и при этом поросенок должен получать вскармливание свиноматкой, которой был введен белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов.
148. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой свиноматку.
149. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного, где указанное животное представляет собой беременную свиноматку, свинью до первого опороса или подсвинка до осеменения.
150. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят указанному животному внутримышечно или интрадермально.
151. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или композицию по любой из предыдущих пунктов вводят указанному животному в комбинации с другим антигеном, предпочтительно, когда другой патоген является антигеном патогена свиней.
152. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или композицию по любой из предыдущих пунктов вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном ORF2 PCV3, предпочтительно, когда другой патоген является антигеном патогена свиней.
153. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов или композицию по любой из предыдущих пунктов вводят указанному животному вместе с другим антигеном, где указанный другой антиген не является антигеном PCV3, предпочтительно, где другой патоген является антигеном патогена свиньи.
154. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой свиноматку, беременную поросенком.
155. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой свиноматку, беременную поросенком, и при этом поросенок должен получать вскармливание свиноматкой, которой был введен белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов.
156. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где указанный белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят дважды указанной свиноматке.
157. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где указанный белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят указанной свиноматке только дважды.
158. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является поросенком, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку.
159. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является поросенком, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят указанному поросенку только один раз.
160. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят дважды указанной свиноматке, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
161. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят дважды указанной свиноматке, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
162. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является свиноматкой, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят указанной свиноматке только дважды, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
163. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное является поросенком, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
164. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят один раз указанному поросенку, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
165. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанное животное представляет собой поросенка, и где белок по любому из предыдущих пунктов или композицию по любому из предыдущих пунктов вводят указанному поросенку только один раз, и где указанное применение не включает введение любого другого антигена PCV3 указанному животному до или во время введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
166. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при использовании состоит из однодозовой, однократной вакцинации или однократного введения одной дозы указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
167. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при использовании состоит из многократной вакцинации или режима многократного введения указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
168. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному при использовании состоит из двукратной вакцинации, или двукратного введения дозы указанного белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
169. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где введение животному осуществляют в течение по меньшей мере 1, 2 или 3 недель воздействия вирулентного цирковируса свиней.
170. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов, где животным является поросенок в возрасте не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
171. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов предназначен для применения по любому из предыдущих пунктов.
172. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанный белок по любому из предыдущих пунктов предназначен для двух или более использований из предыдущих пунктов.
173. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где указанная композиция по любому из предыдущих пунктов предназначена для применения по любому из предыдущих пунктов.
174. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному перед введением белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
175. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному одновременно с введением белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
176. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному одновременно и в той же композиции, что и при введении белка по любому из предыдущих пунктов, или композиции по любому из предыдущих пунктов.
177. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному одновременно и в другой композиции, чем при введении белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
178. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения по любому из предыдущих пунктов, где второй антиген вводят животному после введения белка по любому из предыдущих пунктов или композиции по любому из предыдущих пунктов.
179. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье в одной дозе.
180. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок является иммуногенной композицией, которую вводят этой молодой свинье только в одной дозе.
181. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, где белок находится в иммуногенной композиции, которую вводят этой молодой свинье в двух дозах.
182. Белок по любому из предыдущих пунктов в качестве единственного антигена PCV3 для применения при вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в двух дозах.
183. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье в одной дозе.
184. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в одной дозе.
185. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье в двух дозах.
186. Белок по любому из предыдущих пунктов для применения в качестве единственного антигена PCV3 для вакцинации молодой свиньи с целью уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи, при этом белок находится в иммуногенной композиции, которую вводят этой молодой свинье только в двух дозах.
187. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где одну дозу иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
188. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где только одну дозу иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
189. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где две дозы иммуногенной композиции вводят этой молодой свинье в способе вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
190. Иммуногенная композиция по любому из предыдущих пунктов для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где только две дозы иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок по любому из предыдущих пунктов представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
предпочтительно белок присутствует в количестве по меньшей мере 2 мкг в одной дозе иммуногенной композиции;
где белок представляет собой антигенный компонент в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи.
191. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
192. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
193. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы выбраны из группы, состоящей из развития или рождения мумифицированного, мертворожденного и/или слабого плода.
194. Применение по любому из предыдущих пунктов, где указанные клинические признаки или симптомы представляют собой или включают выталкивание мумифицированного, мертворожденного и/или слабого плода.
Набор пунктов E - Настоящее изобретение теперь будет описано посредством следующего набора пронумерованных пунктов (Набора пунктов E). Раскрытие в этом наборе пунктов в равной степени применимо к настоящему изобретению. Подобным образом раскрытие в этом наборе пунктов в равной степени применимо к каждому из других наборов пунктов.
1. Антигенный белок цирковируса свиней 3 типа (PCV3), являющийся функциональным антигенным вариантом белка ORF2 PCV3.
2. Белок по п.1, где указанный белок ORF2 PCV3 представляет собой белок, кодируемый SEQ ID No.1.
3. Белок по пп.1 или 2, который содержит замены и/или удлинения ORF2 PCV3.
4. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант способен давать более высокий выход вирусоподобных частиц (VLP), чем белок, кодируемый SEQ ID No.1.
5. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1.
6. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет одну или несколько замен в петле FG белка, кодируемого SEQ ID No.1, где эти замены включают замены одного или нескольких из остатка S, и/или остатков K и/или остатка H мотива SKKKH петли FG белка, кодируемого SEQ ID No.1.
7. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1.
8. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант имеет С-концевую часть, которая выходит за пределы концевой последовательности SVL белка, кодируемого SEQ ID No.1, где указанное удлинение составляет от 1 до 30 аминокислот, и где указанное удлинение включает всю часть последовательности VKININLTPPVATSRVPSRALPLRFGCGHR.
9. Белок по любому из предыдущих пунктов, где указанный функциональный антигенный вариант кодируется полностью или частично SEQ ID No. 1, 2, 5, 6 или 7.
10. Белок по любому из предыдущих пунктов, где указанный функциональный вариант белка антигена содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с последовательностью SEQ ID NO: 3 , 4, 8, 9 или 10.
11. Нуклеотидная последовательность, кодирующая белок по любому из предыдущих пунктов.
12. Хозяин бакуловирусной экспрессии, трансформированный или трансфицированный нуклеотидной последовательностью по п.11.
13. Способ получения белка по любому из пп.1-10, включающий культивирование хозяина для бакуловирусной экспрессии по п.12, чтобы вызвать экспрессию белка.
14. Композиция, содержащая белок по любому из пп.1-10 и носитель, разбавитель или наполнитель.
15. Композиция по п.14, содержащая иммуномодулирующий агент.
16. Белок по любому из пп.1-10 или композиция по любому из пп.14-15 для применения в качестве вакцины.
17. Белок по любому из пп.1-10 или композиция по любому из пп.14-15 для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против PCV3 у свиней.
18. Белок по любому из пп.1-10 или композиция по любому из пп.14-15 для применения в способе лечения или профилактики инфекции PCV3 у животного, где указанное животное является свиньей.
19. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения при иммунизации животного против PCV3, где указанное животное является свиньей.
20. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения в способе снижения, элиминации или нейтрализации экспрессии вируса PCV3 у животного, где указанное животное является свиньей.
21. Белок по любому из предыдущих пунктов или композиция по любому из предыдущих пунктов для применения с целью индукции выработки антител, специфичных к PCV3, у животного.
22. Белок по любому из пп.1-10 или композиция по любому из пп.14-15 для применения в способе уменьшения или предотвращения клинических признаков, или клинических симптомов или заболевания, вызванного инфекцией PCV3 у животного, где указанное животное является свиньей.
23. Белок или композиция для применения по п.22, где указанные клинические признаки или симптомы выбраны из группы, состоящей из снижения среднесуточного привеса, смертности, макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани, виремии PCV3, развития или рождения мумифицированного, мертворожденного и/или слабого плода, выталкивания мумифицированного, мертворожденного и/или слабого плода.
24. Белок или композиция для применения по любому из пп.16-23, где введение животному при применении состоит из единственного, однократного введения или единственного, однократного введения одной дозы указанного белка или указанной композиции.
25. Белок или композиция для применения по любому из пп.16-23, где введение животному при применении состоит из двукратного введения, или двудозового введения указанного белка или указанной композиции по любому из предыдущих пунктов.
26. Белок или композиция для применения по любому из пп.16-25, где указанный белок или указанную композицию вводят указанному животному внутримышечно или интрадермально.
27. Антигенный белок цирковируса свиней 3 типа (PCV3) для применения в качестве единственного антигена PCV3 для применения при вакцинации свиньи и/или для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой свиньи, где белок находится в иммуногенной композиции, которую вводят свиньям только в одной дозе, где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант, предпочтительно, где указанный функциональный антигенный вариант его представляет собой белок по любому из пп.1-10; предпочтительно, где указанная свинья является поросенком, предпочтительно, где указанный поросенок имеет возраст не старше 15 недель.
28. Антигенный белок цирковируса свиней 3 типа (PCV3) для применения в качестве единственного антигена PCV3 для применения при вакцинации свиньи и/или для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой свиньи, при этом белок находится в иммуногенной композиции, которую вводят свиньям только в двух дозах, где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант, предпочтительно, где указанный функциональный антигенный вариант представляет собой белок по любому из пп.1-10; предпочтительно, где указанная свинья представляет собой свиноматку или подсвинка до осеменения.
29. Иммуногенная композиция для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где только одну дозу иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где указанный белок представляет собой антигенный белок цирковируса свиней 3 типа (PCV3);
где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант;
предпочтительно, где его функциональный антигенный вариант представляет собой белок по любому из пп.1-10.
30. Иммуногенная композиция для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где только одну дозу иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение одной дозы иммуногенной композиции молодой свинье в способе вакцинации снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в одной дозе иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
при этом молодая свинья является поросенком, предпочтительно, где указанный поросенок имеет возраст не старше 15 недель;
где указанный белок представляет собой антигенный белок цирковируса свиней 3 типа (PCV3);
где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант;
предпочтительно, где его функциональный антигенный вариант представляет собой белок по любому из пп.1-10.
31. Иммуногенная композиция для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у молодой свиньи;
где только две дозы иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который снижает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где указанный белок представляет собой антигенный белок цирковируса свиней 3 типа (PCV3);
где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант;
предпочтительно, где его функциональный антигенный вариант представляет собой белок по любому из пп.1-10.
32. Иммуногенная композиция для уменьшения тяжести клинических признаков или клинических симптомов, вызванных инфекцией PCV3 у молодой свиньи;
где только две дозы иммуногенной композиции вводят этой молодой свинье способом вакцинации для уменьшения тяжести клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где введение двух доз иммуногенной композиции молодой свинье в способе вакцинации уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в двух дозах иммуногенной композиции в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где белок представляет собой антигенный компонент в способе вакцинации, который уменьшает тяжесть клинических признаков или клинических симптомов, возникающих в результате инфекции PCV3 у этой молодой свиньи;
где свинья представляет собой свиноматку или подсвинка до осеменения;
где указанный белок представляет собой антигенный белок цирковируса свиней 3 типа (PCV3);
где указанный антигенный белок представляет собой белок ORF2 PCV3 или его функциональный антигенный вариант;
предпочтительно, где его функциональный антигенный вариант представляет собой белок по любому из пп.1-10.
33. Иммуногенная композиция для применения по любому из пп.29-32, где указанные клинические признаки или симптомы выбраны из группы, состоящей из снижения среднесуточного привеса, смертности, макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани, виремии PCV3, развития или рождения мумифицированного, мертворожденного и/или слабого плода, выталкивания мумифицированного, мертворожденного и/или слабого плода.
34. Иммуногенная композиция для применения по любому из пп.29-33, где указанный белок или указанную композицию вводят указанному животному внутримышечно или интрадермально.
При практическом применении любого из вариантов осуществления изобретения, белков PCV3 по изобретению, обсуждаемых по всему описанию, изобретение охватывает молекулы нуклеиновой кислоты, кодирующие белки PCV3 по изобретению, векторы, такие как бакуловирусные векторы (см. EP 2 460 821 А2, включенный сюда посредством ссылки, вместе с документами, цитируемыми в нем в отношении способов и материалов для экспрессии капсидного белка ORF2 PCV2 с помощью системы экспрессии на основе бакуловируса, можно использовать в практике настоящего изобретения для экспрессии капсидного белка ORF2 PCV3, включая такой белок ORF2 дикого типа PCV3 или мутантный капсидный белок, как описано в настоящей заявке, а также один или несколько белков одного или нескольких патогенов свиней, если необходимо, для включения их в композицию по настоящему изобретению), содержащие такие молекулы нуклеиновой кислоты, и способы для продукции или экспрессии таких мутантных белков PCV3 по изобретению, такие как инфицирование или трансфекция соответствующих клеток вектором (например, если вектор представляет собой бакуловирус, соответствующей клеткой может быть клетка насекомого, или Sf-клетка, или Sf+-клетка; см. EP 2460821 A2, включенный в настоящий документ посредством ссылки, вместе с документами, указанными в нем). Предпочтительно извлекать или изолировать белок после экспрессии или продукции, например, путем отделения твердых веществ и сохранения жидкой части или надосадочной жидкости, которая содержит растворимый белок (например, VLP), и фильтрации надосадочной жидкости. Надосадочную жидкость, содержащую растворимый белок (например, VLP), инактивируют, предпочтительно с помощью BEI, такого как примерно от 2 до 8 или примерно 5 мМ BEI, для инактивации бакуловируса. К композиции также добавляют адъювант, предпочтительно примерно 1 мг или примерно 20 об.% Карбопола или Карбопола 971. Дозировку примерно 2, 4, 8 или 16 мкг композиции в составе примерно 1 мл или примерно 2 мл в однократной или многократной дозе вводят этой молодой свинье или поросенку в возрасте не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
Настоящее изобретение будет дополнительно проиллюстрировано в следующих примерах, которые даны только для целей иллюстрации и не предназначены для ограничения раскрытия каким-либо образом. Способы молекулярного клонирования (такие, как конструирование вставок ДНК, плазмид и рекомбинантных вирусных или растительных векторов, но не ограничиваясь этим) выполняли с использованием стандартных способов молекулярной биологии, описанных J. Sambrook et. al. (Molecular Cloning: A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, 1989), и в патенте США № 8,865,183, описание которого включено посредством ссылки.
Хотя настоящее изобретение и его преимущества были подробно описаны, следует понимать, что в нем могут быть выполнены различные изменения, замены и варианты, не выходящие за рамки сущности и объема изобретения, как определено в прилагаемой формуле изобретения.
Настоящее изобретение будет дополнительно проиллюстрировано в следующих примерах, которые приведены только для целей иллюстрации и никоим образом не предназначены для ограничения изобретения.
Примеры
В представленных здесь примерах первичные данные были включены в дополнение к сводным таблицам, которые анализируют эти первичные данные. Как и в случае любых полевых испытаний, результаты не совсем одинаковы для каждого животного, и, кроме того, может быть один или несколько аномальных результатов. Однако следует понимать, что сводные таблицы представляют собой анализ первичных данных. Результаты анализа показывают эффективность настоящего изобретения.
Пример 1
Идентификация и клонирование ORF2 PCV3, а также получение и очистка ORF2 BaculoG/PCV3
Кодирующая последовательность ORF2 PCV3 (SEQ ID NO:1) была клонирована с помощью ПЦР из синтетического гена, содержащего последовательность ORF2 KT869077 (см. Fan et al., “Complete Genome Sequence of a Novel Porcine Circovirus Type 3 Strain, PCV3/CN/Hubei-618/2016, Isolated from China», Genome Announc 2017 Apr 5(15) e00100-17, Apr 13. doi: 10.1128/genomeA.00100-17, включенный в настоящее описание посредством ссылки) и встроена в плазмиду для переноса бакуловирусом pVL1393 (Invitrogen) с использованием сайтов рестрикции 5' BamHI и 3' NotI. Рестрикционный фрагмент BamHI/NotI также содержал консенсусную последовательность Козака (GCCACC) непосредственно между сайтом 5’ BamHI и стартовым кодоном ORF2 PCV3. Рекомбинантный бакуловирус, содержащий кодирующую последовательность ORF2 PCV3 под контролем полиэдринового промотора, был получен путем котрансфекции клеток насекомых Sf9 (Spodoptera frugiperda) линеаризованной ДНК бакуловируса и переноса плазмиды pVL1393-PCV3 ORF2. Полученный рекомбинантный бакуловирус, BaculoG/PCV3 ORF2, был амплифицирован в клетках насекомых Sf9 и затем очищен путем клонирования с лимитирующими разведениями. При этом делается отсылка на применение способа из EP 2460821 A2, включенного в настоящую заявку посредством ссылки, вместе с документами, цитируемыми в нем, с кодирующей последовательностью для белка ORF2 PCV3, как описано в настоящей заявке (включая то, что вышеупомянутые способы используются для получения любого мутанта, варианта или модифицированного белка ORF2 PCV3, особенно SEQ ID NO: 3, 4, 8, 9 или 10).
Кодирующую последовательность ORF2 PCV3 (SEQ ID NO:1) клонировали с помощью ПЦР из синтетического гена, содержащего последовательность ORF2 KT869077, и встраивали в бакуловирусную плазмиду для переноса VL1393, используя сайты рестрикции 5’ BamHI и 3’ NotI. Рестрикционный фрагмент BamHI/NotI также содержал консенсусную последовательность Козака (GCCACC) непосредственно между сайтом 5’ BamHI и стартовым кодоном ORF2 PCV3. Рекомбинантный бакуловирус, содержащий кодирующую последовательность ORF2 PCV3 под контролем полиэдринового промотора, был получен путем совместной трансфекции клеток насекомых Sf9 (Spodoptera frugiperda) линеаризованной ДНК бакуловируса и переноса плазмиды pVL1393-PCV3 ORF2. Полученный рекомбинантный бакуловирус, BaculoG/PCV3 ORF2, был амплифицирован в клетках насекомых Sf9 и впоследствии очищен путем клонирования с лимитирующими разведениями.
Примеры 1А, 1В, 1С
Идентификация и клонирование ORF2 PCV3 и его мутантов или вариантов (мутации петли FG, мутации петли FG и удлинение или добавление к C-концу), получение и очистка ORF2 BaculoG/PCV3 и их мутантов или вариантов (мутации петли FG, мутации петли FG и удлинение или добавление к С-концу), и его применение
Пример 1A: Молекула нуклеиновой кислоты, кодирующая белок ORF2 PCV3 SEQ ID NO: 4, была клонирована в вектор, бакуловирусный вектор (см. пример 1, см. также EP 2460821 A2, включенный в настоящую заявку посредством ссылки вместе с документами, цитируемыми в нем, в отношении способов и материалов для экспрессии капсидного белка ORF2 PCV2 с помощью системы экспрессии на основе бакуловируса) (при необходимости включения в композицию по изобретению один или несколько белков одного или нескольких патогенов свиней также могут быть экспрессированы с использованием векторной системы, такой как бакуловирусная система, или может быть включен инактивированный патоген, такой как инактивированный вирус, например PRRSV или бактерин, или надосадочная жидкость бактериальной культуры). Клетки инфицировали или трансфицировали вектором, бакуловирусным вектором (см. пример 1, пример 2, см. EP 2460821 A2, включенный в настоящую заявку посредством ссылки вместе с документами, цитируемыми в нем; клетки SF+ (Spodoptera frugiperda), инфицировали или трансфицировали с примерной MOI (множественностью заражения), равной 0,076, рекомбинантным бакуловирусом, содержащим кодирующую ORF2 гена 2 цирковируса 3 свиньи под контролем полиэдринового промотора бакуловируса).
После экспрессии или продукции белка его собирали или выделяли, например, разделяя твердые вещества и сохраняя жидкую часть или надосадочную жидкость, содержащую растворимый белок (например, VLP), и фильтруя надосадочную жидкость. Надосадочную жидкость, содержащую растворимый белок (например, VLP), инактивируют, предпочтительно с помощью BEI, такого как примерно от 2 до 8 или примерно 5 мМ BEI, для инактивации бакуловируса. Для приготовления композиции также добавляют адъювант, предпочтительно примерно 1 мг или примерно 20 об.% Карбопола или Карбопола 971. (См., например, пример 2; колбу инкубируют при 28°C ± 2°C при постоянном перемешивании примерно при 100 об./мин в течение семи дней. Клетки и среду в асептических условиях переносят в 2 центрифужных флакона по 1 л, и клетки осаждают при 15000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтруют через фильтр с размером пор 0,2 мкм и хранят при 4°C, инактивированный антиген ORF2 бакуловируса PCV3, 800 мл; адъювант Карбопол 971P (0,5% исходный раствор), 200 мл; всего 1000 мл или 1 л).
Однократную дозу (т.е. введение с помощью однократного введения или одного введения) композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг антигена ORF2 PCV3 в общем объеме 1 мл или примерно 2 мл, вводят группам свиней (например, 6 свиней в группе). Группа молодых свиней или поросят возрастом не старше 15 недель. Группа молодых свиней или поросят возрастом не старше 6 недель. Группа молодых свиней или поросят возрастом не старше 3 недель. Группа молодых свиней или поросят возрастом не старше 2 недель. Группа молодых свиней или поросят возрастом не старше 1 недели. Группа молодых свиней в качестве свиноматок, до осеменения. Применение, например, по времени, однократной дозы является одним из нижеупомянутых введений схемы многократной дозы, обсуждаемой непосредственно ниже. При однократном введении каждая из групп молодых свиней демонстрирует иммунитет, например, защитный иммунитет, против PCV3 и/или клинических признаков или симптомов, и/или снижение, или уменьшение, или предотвращение PCV3 или заболеваемости и/или клинических признаков или симптомов инфекции.
Режим множественного дозирования, то есть двукратного введения или введения двух единичных введений (например, первичная и вторичная иммунизация) с интервалом не менее недели композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг антигена ORF2 PCV3 в общем объеме 1 мл или примерно 2 мл применяют у групп свиней (например, 6 свиней на группу). Группа молодых свиней или поросят не старше 15-недельного возраста (первое введение в возрасте 2 или 3 недели и второе введение в возрасте 3 или 4 недели). Группа молодых свиней или поросят не старше 6-недельного возраста (первое введение в возрасте 2 или 3 недели и второе введение в возрасте 3, 4 или 5 недель). Группа молодых свиней или поросят в возрасте не старше 3 недель (первое введение в возрасте от 7 до 14 дней, второе введение в возрасте от 14 до 21 дня). Группа молодых свиней или поросят в возрасте не старше 2 недель (первое введение в возрасте 1 недели и второе введение в возрасте 2 недель). Группа молодых свиней или поросят в возрасте не старше 1 недели (введение в 3, 4 и 7 дни). Группа молодых свиней, представляющих собой свиноматок перед осеменением (первое введение между 4 и 6 неделями до осеменения и второе введение между 2 и 4 неделями до осеменения). При многократном введении каждая из групп молодых свиней демонстрирует иммунитет, например, защитный иммунитет, против PCV3 и/или его клинических признаков или симптомов, и/или снижение, или ослабление, или предотвращение инфекции PCV3, или частоты и/или клинических признаков или симптомов инфекции.
Пример 1B: Молекула нуклеиновой кислоты, кодирующая белок ORF2 PCV3 с SEQ ID NO: 8 (4 мутации в петле FG; петля FG белка ORF2 PCV3 заменена на петлю PCV2 (SKKK → QPFS), была клонирована в вектор, бакуловирусный вектор (см. пример 1, см. также ЕР 2460821 А2, включенный здесь посредством ссылки, вместе с документами, цитируемыми в нем в отношении способов и материалов для экспрессии мутантного капсидного белка ORF2 PCV2 через бакуловирусную систему экспрессии) (при необходимости для включения их в композицию по изобретению, один или несколько белков одного или нескольких патогенов свиней также могут быть экспрессированы с использованием векторной системы, такой как бакуловирусная система, или могут быть инактивированным патогеном, таким как инактивированный вирус, например PRRSV или бактерин, или надосадочная жидкость бактериальной культуры). Клетки инфицированы или трансфицированы вектором, бакуловирусным вектором (см. пример 1, пример 2, см. EP 2460821 A2, включенный в настоящий документ посредством ссылки вместе с документами, цитируемыми в нем; SF+ (Spodoptera frugiperda) клетки инфицированы или трансфицированы с приблизительной MOI, равной 0,076, рекомбинантным бакуловирусом, содержащим кодирующий мутантный ген ORF2 свиного цирковируса 3 под контролем бакуловирусного полиэдринового промотора).
После экспрессии или продукции мутантного белка мутантный белок извлекают или выделяют, например, разделяя твердые вещества и сохраняя жидкую часть или надосадочную жидкость, которая содержит растворимый мутантный белок (например, VLP), и фильтруя надосадочную жидкость. Надосадочную жидкость, содержащую растворимый мутантный белок (например, VLP), инактивируют, предпочтительно с помощью BEI, такого как примерно от 2 до 8 или примерно 5 мМ BEI, для инактивации бакуловируса. Для приготовления композиции также добавляют адъювант, предпочтительно примерно 1 мг или примерно 20 об.% Карбопола или Карбопола 971. (См., например, пример 2, колбу инкубируют при 28°C±2°C при постоянном перемешивании примерно при 100 об./мин в течение семи дней. Клетки и среду в асептических условиях переносят в 2 центрифужных флакона по 1 л, и клетки осаждают при 15000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтруют 0,2 мкм и хранят при 4°C, инактивированный бакуловирус, мутантный антиген ORF2 PCV3, 800 мл; Карбопол 971P (0,5% исходный раствор) адъювант, 200 мл; всего 1000 мл или 1 л). Количество VLP (растворимый мутантный белок ORF2 PCV3), полученное с мутантом, превышает количество VLP, полученного из нативной последовательности SEQ ID NO: 4.
Единичную дозу (т.е. при однократной вакцинации или однократном введении) композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг мутантного антигена ORF2 PCV3 в общем объеме 1 мл или около 2 мл, вводят группам свиней (например, 6 свиней на группу). Группа молодых свиней или поросят в возрасте не старше 15 недель. Группа молодых свиней или поросят в возрасте не старше 6 недель. Группа молодых свиней или поросят в возрасте не старше 3 недель. Группа молодых свиней или поросят в возрасте не старше 2 недель. Группа молодых свиней или поросят в возрасте не старше 1 недели. Группа молодых свиней, представляющих собой свиноматок, до осеменения. Введение, например, по времени, однократной дозы является одним из нижеупомянутых введений схемы многократной дозы, обсуждаемой непосредственно ниже. При однократном введении каждая из групп молодых свиней демонстрирует иммунитет, например, защитный иммунитет, против PCV3 и/или его клинических признаков или симптомов, и/или снижение, или уменьшение, или предотвращение инфекции PCV3 или ее частоты, и/или клинических признаков или симптомов.
Режим множественного дозирования, то есть двукратной вакцинации или два однократных введения (например, первичная и вторичная иммунизация) с интервалом не менее недели композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг мутантного антигена ORF2 PCV3 в общем объеме 1 мл или около 2 мл применяют к группам молодых свиней (например, 6 свиней в группе). Группа молодых свиней или поросят в возрасте не старше 15-недель (первое введение в возрасте 2 или 3 недель и второе введение в возрасте 3 или 4 недель). Группа молодых свиней или поросят в возрасте не старше 6-недель (первое введение в возрасте 2 или 3 недель и второе введение в возрасте 3, 4 или 5 недель). Группа молодых свиней или поросят в возрасте не старше 3 недель (первое введение в возрасте от 7 до 14 дней, второе введение в возрасте от 14 до 21 дня). Группа молодых свиней или поросят возрастом не старше 2 недель (первое введение в возрасте 1 недели и второе введение в возрасте 2 недель). Группа молодых свиней или поросят в возрасте не старше 1 недели (введение в 3, 4 и 7 дни). Группа молодых свиней, представляющих собой свиноматок до осеменения (первое введение между 4 и 6 неделями до осеменения и второе введение между 2 и 4 неделями до осеменения). При многократном введении каждая из групп молодых свиней демонстрирует иммунитет, например, защитный иммунитет, против PCV3 и/или его клинических признаков или симптомов, и/или снижение, или ослабление, или предотвращение инфекции PCV3 или ее частоты и/или ее клинических признаков или симптомов.
Пример 1C: Каждая из молекул нуклеиновой кислоты, кодирующие (а) мутантный белок ORF2 PCV3, имеющий 4 мутации в FG-петле; петля FG белка ORF2 PCV3 заменена петлей PCV2 (SKKK → QPFS) и удлинением С-конца на 30 аминокислот путем удаления стоп-кодона в природной кодирующей последовательности С-конца ORF2 PCV3 с тем, условием, что при удалении стоп-кодона, т.е. после «SVL» на С-конце природного белка ORF2 PCV3, добавляют: VKININLTPPVATSRVPSRALPLRFGCGHR, см. SEQ ID NO: 8 и 9, и (b) мутантный белок ORF2 PCV3, имеющий С-концевое удлинение на 30 аминокислот за счет удаления стоп-кодона в кодирующей последовательности С-конца природной ORF2 PCV3 с тем условием, что при удалении стоп-кодона, то есть после «SVL» на С-конце природного белка ORF2 PCV3, добавляют: VKININLTPPVATSRVPSRALPLRFGCGHR, см. SEQ ID NO: 9, была клонирована в вектор, бакуловирусный вектор (см. пример 1, см. также EP 2460821 A2, включенный в настоящую заявку посредством ссылки вместе с документами, цитируемыми в нем в отношении способов и материалов для экспрессии мутантных капсидных белков ORF2 PCV2 посредством бакуловирусной системы экспрессии) (при необходимости для их включения в композицию по изобретению, один или несколько белков одного или нескольких патогенов свиней также могут быть экспрессированы с использованием векторной системы, такой как бакуловирусная система, или может быть инактивированный патоген, такой как инактивированный вирус, например PRRSV или бактерин, или надосадочная жидкость бактериальной культуры). Клетки инфицируют или трансфицируют векторами, кодирующими (а) или (b), бакуловирусными векторами, кодирующими (а) или (b) (см. пример 1, пример 2, см. ЕР 2460821 А2, включенный в настоящую заявку посредством ссылки вместе с документами, цитируемые в нем; клетки SF+ (Spodoptera frugiperda) инфицируют или трансфицируют с приблизительной MOI 0,076 рекомбинантным бакуловирусом, содержащим кодирующий мутантный ген 2 ORF2 свиного цирковируса 3 под контролем бакуловирусного полиэдринового промотора).
После экспрессии или продукции мутантных белков (а) или (b), каждый из мутантных белков извлекают или выделяют, например, путем разделения твердых веществ и выделения жидкой части или надосадочной жидкости, содержащей растворимый мутантный белок (например, VLP), и фильтрации надосадочной жидкости. Надосадочную жидкость, содержащую растворимый мутантный белок (например, VLP), инактивируют, предпочтительно с помощью BEI, такого как примерно от 2 до 8 или примерно 5 мМ BEI, для инактивации бакуловируса. Для приготовления композиции также добавляют адъювант, предпочтительно примерно 1 мг или примерно 20 об.% Карбопола или Карбопола 971. (См., например, пример 2; колбу инкубируют при 28°C±2°C при постоянном перемешивании примерно при 100 об./мин в течение семи дней. Клетки и среду в асептических условиях переносят в 2 центрифужных флакона по 1 л, и клетки осаждают при 15000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтруют через фильтр с размером пор 0,2 мкм и хранят при 4°C, инактивированный бакуловирусный мутантный антиген ORF2 PCV3, 800 мл; Карбопол 971P (0,5% исходный раствор) адъювант, 200 мл; всего 1000 мл или 1 л). Количество VLP (растворимых мутантных белков ORF2 PCV3), полученных с каждым мутантом, больше, чем количество VLP, полученных из нативной последовательности SEQ ID NO:4. Количество VLP (растворимый мутантный белок ORF2 PCV3), полученных из мутанта, имеющего как мутацию FG петли, так и удлинение, (мутант (b)) может быть больше, чем количество VLP, полученных только из мутанта или варианта только по FG петле или только по удлинению.
Единичную дозу (т.е. введение путем однократного введения или однократное введение) композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг мутантного антигена ORF2 PCV3 (а) или (b) в общем объеме 1 мл или примерно 2 мл, вводят группам свиней (например, по 6 молодых свиней в группе). Группа молодых свиней или поросят в возрасте не старше 15 недель. Группа молодых свиней или поросят в возрасте не старше 6 недель. Группа молодых свиней или поросят в возрасте не старше 3 недель. Группа молодых свиней или поросят в возрасте не старше 2 недель. Группа молодых свиней или поросят в возрасте не старше 1 недели. Группа молодых свиней, представляющих собой свиноматок до осеменения. Введение, например, по времени, однократной дозы является одним из нижеперечисленных введений из режима многократного дозирования, обсуждаемого непосредственно ниже. При однократном введении каждой из доз (а) или (b) каждая из групп молодых свиней демонстрирует иммунитет, например, защитный иммунитет против PCV3 и/или его клинических признаков или симптомов, и/или снижение, или ослабление, или предотвращение инфекции PCV3, или ее частоты и/или ее клинических признаков или симптомов.
Режим множественного дозирования композиции, содержащей 2 мкг, 4 мкг, 8 мкг или 16 мкг мутантного антигена ORF2 PCV3 (а) или (b) в общем объеме 1 мл или примерно 2 мл то есть, двукратного введения или двух однократных введений (например, первичной иммунизации и вторичной иммунизации одним и тем же мутантом, т.е. первичную и вторичную иммунизацию осуществляют либо обоими (а), либо обоими (b), и первичную и вторичную иммунизацию осуществляют в той же дозировке), при котором между введениями имеется перерыв в одну неделю, применяют к группам молодых свиней (например, по 6 молодых свиней в группе). Группа молодых свиней или поросят в возрасте не старше 15 недель (первое введение в возрасте 2 или 3 недель и второе введение в возрасте 3 или 4 недель). Группа молодых свиней или поросят в возрасте не старше 6 недель (первое введение в возрасте 2 или 3 недель и второе введение в возрасте 3, 4 или 5 недель). Группа молодых свиней или поросят в возрасте не старше 3 недель (первое введение в возрасте от 7 до 14 дней, второе введение в возрасте от 14 до 21 дня). Группа молодых свиней или поросят в возрасте не старше 2 недель (первое введение в возрасте 1 недели и второе введение в возрасте 2 недель). Группа молодых свиней или поросят в возрасте не старше 1 недели (введение в 3, 4 и 7 дни). Группа молодых свиней, представляющих собой свиноматок перед осеменением (первое введение между 4 и 6 неделями до осеменения и второе введение между 2 и 4 неделями до осеменения). В результате многократного введения или (а), или (b) каждая из групп свиней демонстрирует иммунитет, например, защитный иммунитет, против PCV3 и/или его клинических признаки или симптомов, и/или снижение, или уменьшение, или предотвращение инфекции PCV3, или ее частоты и/или ее клинических признаков или симптомов.
Пример 2
Производство антигена ORF2 BaculoG/PCV3 для исследования
Партию антигена объемом 1 л получали во вращающейся колбе объемом 3 л путем инфицирования клеток SF+ (Spodoptera frugiperda) с приблизительной MOI, равной 0,076, рекомбинантным бакуловирусом, содержащим ген 2 ORF2 цирковируса свиней 3 под контролем бакуловирусного полиэдринового промотора (BaculoG/PCV3 ORF2 Клон 4B4-2E12 Pre-MSV p8). Колбу инкубировали при 28°C±2°C при постоянном перемешивании приблизительно при 100 об./мин в течение семи дней. Клетки и среду в асептических условиях переносили в центрифужные флаконы 2 x 1 л, и клетки осаждали при 15000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтровали через фильтр с размером пор 0,2 мкм и хранили при 4°C.
Таблица 1. Состав инактивированной бакуловирусной вакцины PCV3 ORF2
Пример 3
Оценка эффективности прототипов вакцин против цирковируса свиней 3 типа (PCV3) у молодых свиней, лишенных молозива, рожденных кесаревым сечением
Задачи примера заключаются в следующем: оценить эффективность прототипа вакцины против PCV3 умолодых свиней, рожденных путем кесарева сечения, лишенных молозива (CDCD), разработать модель заражения для PCV3 у молодых свиней CDCD, включая определение переменных первичного и вторичного исхода, подтвердить инфекционность инфекционных молекулярных клонов.
Это исследование было разработано для оценки использования целого вируса и ПЦР-положительного гомогената ткани (оба предоставлены Ветеринарной диагностической лабораторией Университета штата Айова (ISU VDL)) в качестве потенциальных контрольных материалов для будущих исследований. Кроме того, сохранение инфекционного клона PCV3 у свиней дало бы дополнительную возможность для будущих исследований модели заражения и поэтому было включено в план исследования. Поскольку прототипы вакцин были доступны, они были включены для более точной оценки модели заражения.
Таблица 2. Дизайн исследования
Всего было использовано 54 молодые свиньи. Животные были произвольно распределены на пять экспериментальных групп (n = 8-12/ группу) и одну группу строгого контроля (n = 6). Животные были размещены в трех помещениях. В 7-дневном возрасте свиней вакцинировали PCV2. В Д0 в возрасте трех недель свиней вакцинировали либо векторной конструкцией, экспрессирующей ORF2 PCV3, с адъювантом ISA 207VG, либо векторной конструкцией, экспрессирующей ORF2 PCV3, с адъювантом карбополом, либо плацебо (подобранный контроль для векторной конструкции). Свиньи были перемещены примерно в пятинедельном возрасте. На 21 день в возрасте шести недель свиней заражали либо целым вирусом, либо гомогенатом ткани. В дополнение к контрольному материалу вводили иммуностимулятор (IFA/KLH). В данном контексте иммуностимулятор играет роль не адъюванта, а усилителя заражения. В течение всего исследования периодически анализировали ректальную температуру, массу тела, собирали сыворотку, целую кровь, назальные мазки и фекальные мазки. Образцы тестировали совместно. Животных умерщвляли на Д49 или Д63, как описано в таблице 2. Собирали и оценивали множество свежих и фиксированных тканей.
Для исследования инфекционных конструкций клонов использовали всего 6 молодых свиней. Животные были произвольно распределены на три группы (n = 2 на группу) и размещены в одной комнате. В Д14, когда животным было приблизительно 5 недель, им прививали один из трех инфекционных клонов. Инокуляцию производили внутрипеченочно (под контролем УЗИ). Кроме того, животных 9-й группы прививали внутримышечно. Регистрировали ректальную температуру, массу тела, собирали образцы сыворотки, назальных и фекальных мазков периодически на протяжении всего исследования. Образцы тестировали с помощью кПЦР, чтобы определить, способны ли клоны реплицироваться. Животных умерщвляли на Д49. Множество свежих и фиксированных тканей были собрано только у животных, которые были виремическими, и было передано для оценки.
Расписание исследования показано в таблице 3.
Таблица 3
День исследования Мероприятие при исследовании
Д-22 Сбор пуповинной крови
Д-14 Вакцинация животных от PCV2 в 7-дневном возрасте
Д0 Вакцинация животных 1-6 групп (3-недельный возраст)
Сбор крови (Примечание: не собирали фекальные мазки, назальные мазки, не регистрировали температуру или вес)
Д12 Перевозка животных
Д14 Заражение животных в группах 7-9 (5-недельный возраст)
Д19 Введение KLH/ICFA животным в группах 1-6
Д21 Заражение животных в группах 1-5 (возраст 6 недель)
Д23 Введение KLH/ICFA животным в группах 1-6
Д49 Вскрытие отобранных животных в группах 4-6; все животные группы 1-3, 7-9
Д63 Вскрытие оставшихся животных в группах 4-6
Д21 - Д12 Наблюдения за общим состоянием здоровья всех животных
Д13 - Д63 Клинические наблюдения за всеми имеющимися животными
Д13, 15, 16, 19, 21, 23, 28 Ректальная температура из групп 7-9
Сбор крови, фекальные мазки, назальные мазки у животных групп 7-9
Д13, 21, 22, 23, 26, 28, 35, 42, 49 Ректальная температура из групп 1-5
Сбор крови, фекальные мазки, назальные мазки у животных 1-5 групп
Д13, 15, 16, 19, 21, 22, 23, 26, 28, 35,
42, 49 Ректальная температура из группы 6
Сбор крови, фекальные мазки, назальные мазки у животных группы 6
Д13, 21, 28, 35, 42, 49 Масса тела (все животные)
Экспериментальную вакцину (BaculoG/PCV ORF2) сравнивали с плацебо-сопоставимым контролем. Схема лечения представлена в таблице 4.
Таблица 4
207VG; L#3624-171
Вакцины вводили на Д0 внутримышечно в правую сторону шеи (2 мл), на середине расстояния между основанием уха и плечевым суставом, с использованием стерильных игл и шприцев подходящего размера. Коммерческую вакцину против PCV2 (Circoflex, серия № 3091134A) вводили всем животным в соответствии с инструкциями производителя.
Заражение целым вирусом: материал для заражения хранили при температуре -70°C±10°C до использования. Непосредственно перед заражением материал размораживали при 37°C и использовали в неразбавленном виде. Общая дозировка составляла 2 мл (1 мл интраназально/1 мл внутримышечно). На 21 день каждая свинья получала 1 мл вирусного материала интраназально и 1 мл внутримышечно. Внутримышечное введение материала для заражения осуществляли путем инъекции вирусного материала в левую сторону шеи, на середине расстояния между основанием уха и плечевым суставом, с использованием стерильных игл и шприцев подходящего размера. Введение материала для заражения интраназально осуществляли, прикрепляя распылитель на кончике носа к люэровскому шприцу объемом 5 см3. Продолжительность заражения составила 28 дней. Обычное культивирование материала проводили на чашках с кровяным агаром при 37°C в анаэробных и аэробных условиях в течение 48 часов. Роста не наблюдалось, и тест был признан удовлетворительным. Материал был протестирован способом ПЦР на наличие микоплазмы; никаких загрязнений выявлено не было. Результат кПЦР PCV3: 6,6 log10 геномных копий/мл (Cq = 23,58). Глубокое секвенирование образцов (MiSeq_127) было завершено с использованием обработки как ДНК, так и РНК. Секвенирование не привело к восстановлению PCV3.
Заражение гомогенатом ткани, положительным по ПЦР PCV3. Материал для заражения хранили при -70°C±10°C до использования. Непосредственно перед заражением материал размораживали при 37°C и использовали в неразбавленном виде. Общая дозировка составляла 2 мл (1 мл интраназально/1 мл внутримышечно). На 21 день каждая свинья получала 1 мл вирусного материала интраназально и 1 мл внутримышечно. Внутримышечное введение материала для заражения осуществляли путем инъекции вирусного материала в левую сторону шеи, на середине расстояния между основанием уха и плечевым суставом, с использованием стерильных игл и шприцев подходящего размера. Введение материала для заражения интраназально осуществляли, прикрепляя распылитель на кончике носа к люэровскому шприцу объемом 5 см3. Продолжительность заражения составила 28 дней. Обычное культивирование материала проводили на чашках с кровяным агаром при 37°C в анаэробных и аэробных условиях в течение 48 часов. Роста не наблюдалось, и тест был признан удовлетворительным. Материал был протестирован способом ПЦР на наличие микоплазмы; никаких загрязнений выявлено не было. Результат кПЦР PCV3: 9,1 log10 геномных копий/мл (Cq = 14,82). Глубокое секвенирование образцов (MiSeq_127) было завершено с использованием обработки как ДНК, так и РНК. Секвенирование привело к восстановлению полного генома PCV3 (99% нуклеотидов к PCV3 GB MG564174.1).
В таблице 5 описан иммуностимулятор, вводимый животным.
Таблица 5
На D14 молодой свиньи в группах 7 и 8 были инфицированы посредством инъекции под ультразвуковым контролем только в печень - лимфатические узлы не инокулировали. Для заражения 1 мл материала набирали в туберкулиновый шприц и присоединяли к стерильной игле 22 g x 1,5 дюйма. Иглу вводили в три разных участка печени. В каждое место вводили примерно 300 мкл. Свиньям в группе 9 вводили инокулят, как описано выше. Кроме того, им внутримышечно вводили 3 мл материала; 1,5 мл материала в мышцы шеи справа и 1,5 мл материала в мышцы шеи слева. После заражения свиньям вводили 0,5 мл Baytril в мышцы шеи справа. Группе 7 (молодые свиньи 1 и 2) вводили материал с рециркуляризованным геномом. Группе 8 (молодые свиньи 3 и 4) вводили димеризованную плазмиду. Группе 9 (молодые свиньи 5 и 6) вводили материал культуры трансфицированных клеток. В Таблице 6 показаны критерии включения/исключения, использованные в исследовании.
Таблица 6
Владелец: Boehringer Ingelheim Animal Health USA, Inc.
Молодая свинья была экспериментальной единицей. Рандомизацию молодых свиней для загона и лечения проводил статистик или назначенное лицо. До начала исследования имеющиеся данные о свиньях, информацию о подстилке и условиях содержания использовали для случайного назначения лечения в помете. Всего в группы 1-6 было включено четыре помета от 12 до 14 свиней. Всего в группы 7-9 было включено два помета с тремя молодыми свиньями. Персонал, занимающийся сбором данных или выполнением лабораторных анализов, не имел представления о распределении свиней по группам на протяжении всего исследования. Лечение проводил человек, не участвовавший в сборе данных. Было одобрено использование животных в этом исследовании. В соответствии с принятыми правилами животноводства были предоставлены адекватная подстилка и место для кормления. За молодыми свиньями ежедневно наблюдали, чтобы обеспечить доступ к достаточному количеству корма и воды и определить общее состояние здоровья животных. По прибытии на объект животные находились под ветеринарным наблюдением до конца исследования. На протяжении всего исследования животных никак не лечили. На протяжении всего исследования свиней кормили следующими лечебными кормами: UltraCare 100 Medicated (серия № 7Nov03); UltraCare 240 Medicated (серия № 8Jun25); UltraCare 500 Medicated (серия № 8Aug30), или Lean Metrics CEPS Medicated (серия № 08Nov14). После завершения исследования животных утилизировали, за исключением животного № 13, которое было кремировано на Д46.
У всех свиней ежедневно контролировали общее состояние здоровья с Д1 по Д12. Никаких отклонений не отмечено. Начиная с D13 и продолжая до конца исследования, всех свиней ежедневно наблюдали на наличие клинических признаков, как описано в таблице 7.
Таблица 7
В дни сбора данных о температуре тела температуру каждого животного регистрировали с помощью микрочипа (Destron Fearing LifeChip® с технологией Bio-Thermo Technology) и термометра Allflex (номер модели RS420-45, серийный номер C088 26001). Данные были записаны в °F. Для статистического анализа данные были скорректированы до исходного уровня. Пирексия определялась как температура выше 104°F. В дни анализа массы тела регистрировали массу тела в килограммах по калиброванной шкале.
В дни сбора крови венозную целую кровь собирали через переднюю полую вену от каждой молодой свиньи с использованием стерильной иглы Vaccutainer® подходящего размера, держателя иглы Vaccutainer® и пробирок с сепаратором сыворотки (SST). Кровь доставляли вручную, а сыворотку декантировали в два криогенных флакона с завинчивающейся крышкой и одну пробирку Falcon на 5 мл, на которой были указаны номер исследования, день исследования и идентификатор животного. Образцы сыворотки в криогенных флаконах хранили при -70°C±10°C и отслеживали с помощью электронной системы управления Freezerworks. Сыворотка была проверена способом кПЦР на наличие PCV3. Пробирки Falcon объемом 5 мл были перенесены для анализа ИФА.
У свиней собирали образцы мазков. Отдельный стерильный тампон (Fisher, кат. № 23-400-111 или аналогичный) использовали для получения пробы фекалий из прямой кишки животного или пробы из носа из одной ноздри. После отбора пробы каждый тампон помещали в пробирку, содержащую 1,0 мл минимальной эссенциальной среды (кат. номер SAFC 62892-1000M3056). Были подготовлены пробирки со средой, которые перед использованием хранили при 4°C. После использования пробирки были помечены как минимум идентификатором животного, номером исследования и датой. Пробирки хранили при -70°C±10°C и доставляли в день сбора, и обрабатывали стандартными способами. Обработанные материалы хранили во флаконах, на которых был указан по меньшей мере номер исследования, день исследования и идентификатор животного. Образцы хранили при -70°C±10°C и отслеживали с помощью электронной системы управления Freezerworks. Образцы были протестированы способом кПЦР.
Животных в группах 7-9 вскрывали на Д49. Животных в группах 1-6 умерщвляли либо в Д49, либо в Д63. Во время аутопсии макроскопические поражения регистрировали в протоколе вскрытия трупа. Исследователь или назначенное лицо собирали фиксированные формалином образцы ткани головного мозга (1/2 органа), мозжечка (1/2 органа), ствола мозга (1/2 органа), легкого (1 участок добавочной доли или области с поражением), сердца (2 среза), почки (1 срез), печени (1 срез), селезенки (1 срез), миндалины (1/2 органа), тонкой кишки (3 среза), толстой кишки (2 среза) и лимфоузлов (поверхностных паховых, трахеобронхиальных, подвздошных, брыжеечных, желудочно-печеночных и подвздошно-слепокишечных). Все фиксированные ткани помещали в один контейнер, содержащий 10% забуференный раствор формалина, таким образом, чтобы соотношение фиксированных тканей к формалину составляло 1:10. Для каждой молодой свиньи двойные образцы срезов, перечисленных выше, собирали в следующие упаковочные завязываемые мешки; 1 - головной мозг, мозжечок, ствол мозга; 2 - легкое, сердце, почка, печень, селезенка; 3 - лимфатические узлы и миндалины; 4 - тонкая кишка и толстая кишка. Пакеты со свежими тканями и сосуды с фиксированными тканями были помечены как минимум номером исследования, днем исследования и идентификатором животного. Все свежие ткани переносили на Д49 или Д63. Обращаем внимание, что ткани не собирали у животных 1 и 2 (группа 7); 4 (группа 8), или 5 и 6 (группа 9), поскольку виремия не была обнаружена с помощью количественной ПЦР.
Терминальные образцы крови собирали у следующих животных на Д63: 57 и 55 (группа 6); 53, 50, 46 и 44 (группа 5); 41, 37, 35 и 33 (группа 4). Перед забором крови свиней подвергали глубокой анестезии. Кровь собирали в пробирки SST и доставляли в день забора. Сыворотку отделяли от сгустка центрифугированием и декантировали в центрифужные пробирки объемом 50 мл, на которых были указаны номер исследования, день исследования и идентификатор животного. Образцы сыворотки отслеживали с помощью электронной системы управления FreezerWorks. Переносили половину сыворотки, собранной у каждого животного.
Статистический анализ данных проводили с использованием SAS версии 9.2 или более поздней версии (SAS, Кэри, Северная Каролина/ США, SAS Institute, Inc.). Перечни данных и сводные статистические данные по группам лечения были сгенерированы для всех переменных, если это необходимо. Данные по виремии из групп 1-5 были разделены по бинарному результату (присутствует/отсутствует) для каждого животного, и построены медианные значения ПЦР по группам и дням. Долю пораженных животных анализировали с помощью точного критерия Фишера между группами лечения; значения p менее 0,01 считали достоверными. Данные для фекальных и назальных мазков из групп 1-5 были дихотомизированы для получения двоичного результата (присутствует/отсутствует) для каждого животного, и были нанесены медианные значения ПЦР по группам и дням. Долю пораженных животных анализировали с помощью точного критерия Фишера между группами лечения; значения p менее 0,01 считались значимыми. Долю пораженных животных для групп 4 и 5 по дням анализировали с помощью теста Уилкоксона. Ректальную температуру и массу тела анализировали с использованием смешанной модели с корректировкой по базовой линии. Сообщаются средние значения наименьших квадратов по группам и дням. Были проанализированы сравнения групп по дням; значения p менее 0,01 считали достоверными.
В протокол внесены три поправки. Во-первых, из-за небольшого размера свиней был изменен протокол инокуляции инфекционного клонового материала. Во-вторых, для свиней в группах 7, 8, 9 были добавлены дополнительные даты отбора на основании результатов ПЦР. Добавлены даты: Д36, Д42 и Д49. Кроме того, аутопсия была проведена на Д49, а не на Д42. В-третьих, исследователь рекомендовал не собирать данные о массе тела и температуре на Д0, а кровь не собирать на Д7 из-за дополнительного стресса, который это может вызвать у животного.
Виремия не была обнаружена ни у одного из шести животных строгого контроля на протяжении всего исследования (группа 6). Распределение частот виремии по группам представлено в таблице 8 ниже. Групповое медианное значение log10 геномных копий ДНК PCV3/мл в день для групп 1-5 представлено на фигуре 4.
У невакцинированных свиней воздействие материала для заражения целым вирусом (WV) приводило к виремии у 100% животных (группа 3). Виремия у этих животных впервые наблюдалась между Д28 и Д42 и присутствовала у всех животных во время завершения теста (D49). Напротив, виремия была предотвращена у 94% (15/16) вакцинированных животных, подвергшихся заражению целым вирусом (p <0,001). Одно вакцинированное животное, у которого наблюдалась виремия (# 14), находилось в группе 1 и имело обнаруживаемую виремию только на Д49.
У невакцинированных свиней воздействие материала для заражения гомогенатом ткани (TH) приводило к виремии у 100% животных (группа 5). Виремия у этих животных впервые наблюдалась на 22-й день (у всех животных) и присутствовала у всех животных на момент выхода из испытания (Д49). У четырех животных (№ 53, 50, 46 и 44), которых содержали еще на две недели, обнаруживались уровни виремии во время аутопсии на Д63. Напротив, виремия была предотвращена у 42% (5/12) вакцинированных животных, подвергшихся заражению тканевым гомогенатом (p = 0,0373). Из семи вакцинированных животных, которые стали виремическими, только одно животное (№40) имело виремию с Д22 по Д49. Виремия отмечена между Д35 и Д49 у оставшихся шести вакцинированных животных. В Таблице 8 показана частота обнаружения ДНК PCV3 в сыворотке по группам лечения.
Таблица 8
позитивных
Поскольку только два животных в группе были включены в часть исследования, посвященную инфекционным клонам, исходные данные по животным и дням представлены в таблице 9. ДНК PCV3 была обнаружена у обоих животных в группах 7 и 8, но только у одного животного из группы 9. Только у одного животного (№3; группа 8) развилась виремия в течение последующих недель. Интересно, что виремия не началась до Д28.
Таблица 9. Log10 геномных копий ДНК PCV3/мл по животным и дням
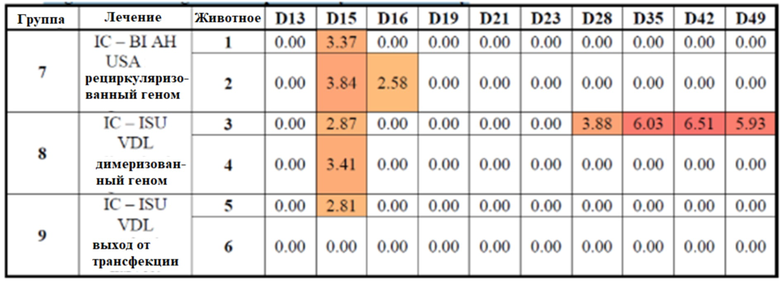
Никаких клинических признаков не наблюдалось ни у одного животного после вакцинации до Д12 (день транспортировки). На протяжении всего исследования только у двух животных (№13, группа 1; №59, группа 6) наблюдались постоянные отклонения от нормы. У трех дополнительных животных наблюдались спорадические аномалии.
Животное № 13 (группа 1), как наблюдали, имело ярко выраженные ребра и позвоночник, и оно не ело (оценка состояния тела 2) вскоре после прибытия на 13 и 14 день. На 23 день животное теряло координацию после кровотечения. На Д28 у животного была отмечена хромота левой задней ноги. Животное нашли мертвым на Д46. Макроскопическое исследование на момент смерти выявило фибринозный плеврит с мультифокальными участками ателектаза в краниальных вентральных долях легких и фибринозный перикардит. Судя по макроскопическим повреждениям, смерть была обусловлена системной бактериальной инфекцией. Смерть, вероятно, не была связана с вакцинацией или заражением, поскольку ДНК PCV3 не была обнаружена в сыворотке этого животного ни на одном этапе исследования.
У животного № 59 (группа 6) наблюдалась хромота на правую заднюю ногу с Д32-43, и было отмечено, что у него не сгибались задние конечности с D44 по 49. Поскольку это животное входило в группу строгого контроля, клинические признаки не были связаны с вакцинацией или заражением. У трех дополнительных животных наблюдались спорадические клинические признаки. Было обнаружено, что животное №14 (группа 1) имело ярко выраженные ребра и позвоночник и не ело (оценка состояния тела 2) вскоре после прибытия в AMVC на Д13. Кроме того, у животного была взлохмаченная шерсть на 16 и 17 день. Поскольку клинические признаки начинались до заражения и не проявлялись до 13 дней после вакцинации, предполагается, что эти признаки связаны с перемещением животного CDCD в молодом возрасте, а не с вакцинацией или заражением. У животного № 11 (группа 1) наблюдалось угнетение функции/летаргия (неврологическая оценка 1) на Д19. Поскольку у этого животного не было доказательств виремии на протяжении всего исследования, маловероятно, что клинические признаки были связаны с заражением. Наблюдалось, что животное № 5 (группа 9) было немного худее по сравнению с остальными животными в группе, с умеренным снижением аппетита (оценка состояния тела 1) на Д19. Поскольку на 15-й день у этого животного была обнаружена преходящая виремия, клинические признаки могли быть связаны с инфекцией. Однако клинические признаки не соответствовали предыдущей публикации [25] и были временными.
Выделение вируса с фекалиями не было обнаружено ни у одного из шести животных строгого контроля на протяжении всего исследования (группа 6). Распределение частоты выделения вируса с фекалиями по группам представлено в таблице 10. Медиана группового log10 геномных копий ДНК PCV3/мл в образцах фекалий по дням для групп 1-5 представлена на фигуре 5.
Таблица 10. Частота обнаружения ДНК PCV3 по группам в образцах фекалий
позитивных
У невакцинированных молодых свиней воздействие материала на основе целого вирусного приводило к выделению вируса в фекалиях у 88% животных (группы 3). Вирус в фекалиях у этих животных впервые наблюдали между Д35 и Д49. Напротив, выделение вируса в фекалии было предотвращено у 75% (12/16) вакцинированных животных, подвергшихся заражению целым вирусом (p = 0,0101 (группа 1 против 3); p = 0,1189 (группа 2 против 3)). В целом выделение вируса в фекалиях у вакцинированных животных было спорадическим и не соответствовало истинной инфекции.
У невакцинированных свиней заражение материалом из гомогената тканей приводило к выделению вируса в фекалиях у 100% животных (группа 5). Выделение вируса в фекалиях у этих животных было двухфазным, и у нескольких животных обнаруживались количества PCV3 в фекалиях на Д22 и снова на Д35-49. Выделение вируса в фекалиях наблюдалось у 92% вакцинированных животных. Однако, в отличие от невакцинированных животных, выделение вируса в фекалиях было наиболее распространено на Д22 и Д23 без второго пика.
ДНК PCV3 не была обнаружена ни в одном из образцов фекалий, взятых у животных в группах 7-9.
Назальное выделение вируса не было обнаружено ни у одного из животных строгого контроля на протяжении всего исследования (группа 6), за исключением животного № 59. Поскольку ДНК PCV3 была обнаружена только на Д15, а все другие образцы (сыворотка, фекалии) были отрицательными, это, вероятно, ложноположительный результат. Медиана группового log10 геномных копий ДНК PCV3/мл в образцах фекалий по дням для групп 1-5 представлена на фигуре 6. (* Считается, что обнаружение вируса в мазках из носа у животного № 59 является ложноположительным).
У невакцинированных свиней воздействие материала для заражения вирусом приводило к выделению вируса в назальном мазке у 88% животных (группа 3). Назальные выделения вируса у этих животных впервые наблюдались между Д35 и Д49. Напротив, выделение вируса из носа было предотвращено у 94% (15/16) вакцинированных животных, подвергшихся заражению целым вирусом (p = 0,0014 (группа 1 против 3); p = 0,0101 (группа 2 против 3)). Одно вакцинированное животное (№19, группа 2) с положительными результатами имело PCV2 только на Д49.
У невакцинированных свиней воздействие материала для заражения гомогенатом тканей приводило к выделению вируса из носа у 100% животных (группа 5). Выделение вируса из носа у этих животных было двухфазным, и у нескольких животных были выявляемые количества PCV3 в ноздрях на Д22 и снова на Д35-49. Назальные выделения вируса наблюдались у 100% вакцинированных животных. Однако, в отличие от невакцинированных животных, выделение вируса из носа присутствовало у большинства животных на Д22 и 23 без второго пика. Спорадическое выделение вируса наблюдалось только у двух животных после D28.
Только два животных на группу были включены в часть исследования, посвященную инфекционным клонам, необработанные данные по животным и дням представлены в таблице 11. ДНК PCV3 была обнаружена у 5/6 животных на следующий день после инокуляции (D15) и у всех животных независимо от инокулята между Д16-21. Только у одного животного (№4; группа 8) обнаруживалась ДНК PCV3 в мазках из носа после Д21.
Таблица 11. Log10 геномных копий ДНК PCV3/мл в мазках из носа по животным и дням для групп 7-9
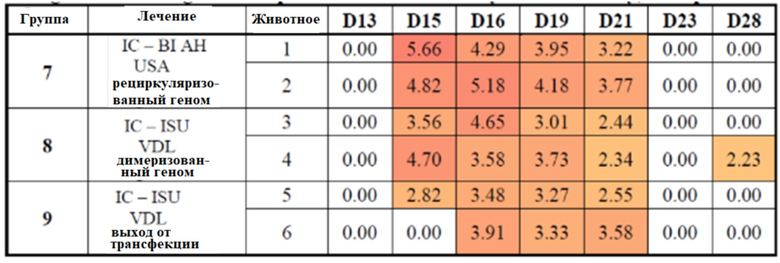
Скорректированная по базовой линии средняя ректальная температура (°F) для группы способом наименьших квадратов по дню исследования представлена на фигуре 7. Данные для группы 6 не включены в фигуру, поскольку анализ был основан на модели, и животные в группе 6 содержались в отдельном помещении. Исходные данные и описательную статистику по группам и дням можно найти в статистическом отчете, связанном с этим исследованием. Никаких различий между группами 1-3 не наблюдалось независимо от вакцинационного статуса. Вакцинированные животные, зараженные тканевым гомогенатом (группа 4), имели значительно более низкие температуры по сравнению с невакцинированными зараженными животными (группа 5) во время периода заражения (p = 0,0021).
Ни одно животное не считалось пирексическим (имевшим температуру выше 104°F) на протяжении всего исследования.
Скорректированные по базовому уровню средние значения групповых наименьших квадратов (кг) представлены для групп 1-5 на фигуре 7. Исходные данные и описательную статистику для всех групп можно найти в статистическом отчете, связанном с этим исследованием. Никаких различий между группами не наблюдалось, независимо от материала для заражения или статуса вакцинации (p> 0,1).
Первой целью этого исследования была разработка модели заражения для PCV3 у свиней CDCD и определение первичных и вторичных переменных результата. Оценивали два материала для заражения, гомогенат ткани и целый вирус. Поскольку 100% животных, подвергшихся воздействию гомогената ткани, становились виремическими в течение 24 часов после заражения и имели обнаруживаемое выделение из носа и фекалий, материал считался высоко заразным. Развитие виремии PCV3 и выделение фекальным и назальным путями не требовало совместной инфекции, поскольку другие патогены, включая PRRSV, PCV2 и PPV, не были обнаружены обычным культивированием, глубоким секвенированием и специфическими ПЦР-анализами, проводившимися на исходных тканях.
Цельновирусный материал вызвал виремию у 100% животных и выделение вируса из носа и фекалий у 88% животных, и поэтому считается заразным. Однако виремия произошла через 14 дней после заражения; значительно медленнее по сравнению с гомогенатом ткани. Гипотеза состоит в том, что задержка связана с вирусной нагрузкой исследуемого материала. В частности, значения Cq гомогената ткани и целого вируса составляли 14,82 и 23,58, соответственно, что позволяет предположить, что гомогенат ткани содержал большее количество ДНК PCV3 по сравнению с целым вирусом.
Поскольку исходные сообщения о случаях PCV3 в полевых условиях включали репродуктивную недостаточность и PDNS у свиноматок [3], была выдвинута гипотеза, что инфицирование свиней CDCD может приводить к PDNS. Однако не было никаких внешних доказательств PDNS (или другого клинического заболевания) или гипертермии после воздействия любого из контрольных материалов. Поскольку гомогенат ткани содержал большое количество вируса, а начало виремии было в пределах 24 часов, маловероятно, что инфицирование свиней CDCD только PCV3 приведет к PDNS. Следовательно, исходя из имеющихся в настоящее время данных, виремия представляется наиболее подходящим первичным параметром для применения в будущих исследованиях с использованием модели свиней CDCD. Кроме того, фекальные и назальные выделения были уменьшены, и их можно было использовать в качестве второстепенных параметров. Биологически значимых различий в температуре и массе тела не наблюдалось; эти параметры вряд ли пригодятся для будущих исследований. Поскольку другие параметры (серология, гистопатология) не оценивались во время создания отчета, они могут предоставить дополнительные параметры.
Первая цель исследования заключалась в первоначальной оценке прототипа вакцины с использованием двух разных адъювантов. В этом исследовании представлены предварительные данные о том, что одна внутримышечная доза антигена ORF2 PCV3, экспрессируемого бакуловирусом, вводимая трехнедельным свиньям, предотвращала виремию, присутствие вируса в назальном отделяемом и фекалиях после заражения целым вирусом. У животных групп 1 и 2 не было обнаружено выделения или виремии, поэтому нельзя сделать однозначный вывод о предпочтении одного адъюванта другому. Данные из групп 3 и 4 предполагают, что эффективность вакцины снижается, когда материал для заражения содержит большее количество ДНК PCV3. Следовательно, установление дозы заражения, которая приводит к инфекции, но не подавляет вакцинацию, может быть полезно для будущих исследований эффективности.
Чтобы оценить эффективность вакцинации против PCV3 на модели единственной ко-инфекции, свиней CDCD вакцинировали против PCV2 в возрасте семи дней. Основываясь на различиях в аминокислотной структуре капсида (26% идентичности аминокислот в гене cap между двумя вирусами [2]), было выдвинуто предположение, что перекрестной защиты не будет. Основываясь на результатах этого исследования, вакцинация против PCV2, по-видимому, не предотвращала виремию PCV3, поэтому маловероятно, что вакцинация против PCV2 играла какую-либо роль в отсутствии клинических проявлений заболевания.
Вторая цель этого исследования заключалась в подтверждении инфекционности инфекционных молекулярных клонов, созданных внешним сотрудником, и внутреннего молекулярного клона, созданного группой по разработке вакцины. Интересно, что внутрипеченочная инокуляция свиней CDCD инфекционными материалами клонов приводила к обнаруживаемому присутствию вируса в назальных мазках в течение семи дней после заражения. Предполагается, что временная виремия привела к распространению вируса на носовой эпителий, где произошла репликация. Для подтверждения этой гипотезы потребуются дальнейшие исследования и оценка ткани носа с помощью антиген-специфического реагента. Неизвестно, почему виремия снова была обнаружена у животного №3 в дни 28-49. Возможно, если бы использовалось большее количество животных, обнаружение виремии произошло бы у большего процента животных. Хотя развитие виремии в течение нескольких недель предполагает, что животное № 3 действительно инфицировано, инфекция носила субклинический характер. Этот результат не согласуется с недавней публикацией [25], в которой инфицирование обычных четырехнедельных свиней инфекционным клоном PCV3 приводило к PDNS.
Одна внутримышечная доза антигена ORF2 PCV3, экспрессируемого бакуловирусом, вводимая трехнедельным свиньям, предотвращала виремию, присутствие вируса в назальном и фекальном мазке после заражения материалом гомогената тканей, который считался инфекционным. В научных исследованиях или в обоснованных ожиданиях исследований эффективности виремия может использоваться в качестве основного параметра для оценки вакцинации. Для будущих основных исследований, связанных с полностью лицензированным продуктом, потребуется другой первичный параметр (обнаружение антигена PCV3 в тканях или клиническое заболевание). Инокуляция свиней CDCD инфекционным материалом клона приводила к виремии у одного животного и присутствию вируса в назальном мазке у нескольких животных. Однако никаких клинических признаков не наблюдалось.
Пример 4
Вакцина, введенная группе 1
Вакцина, обозначенная как «вакцина против цирковируса свиней, тип 3, модифицированный живой бакуловирусный вектор», была получена с помощью следующей процедуры. Партия антигена объемом 1 л была получена в вращающейся колбе объемом 3 л путем инфицирования клеток SF+ (Spodoptera frugiperda) с приблизительной MOI, равной 0,076, рекомбинантным бакуловирусом, содержащим ген ORF2 свиного цирковируса 3 типа под контролем бакуловирусного полиэдринового промотора. Колбу инкубировали при 28°C±2°C при постоянном перемешивании приблизительно при 100 об./мин в течение семи дней. Клетки и среду в асептических условиях переносили в центрифужные флаконы 2 x 1 л и клетки осаждали при 15000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтровали через фильтр с размером пор 0,2 мкм и хранили при 4°C. В состав материала входило 50% ISA207 VG, как показано в таблице 12. Вакцина удовлетворительно прошла тестирование стерильности после розлива в конечные контейнеры. Анализ безопасность на мышах перед применением материала у свиней не проводили.
Таблица 12. Состав вакцины - адъювант ISA207 VG
Пример 5
Вакцина для групп 2 и 4
Вакцина, вводимая группам 2 и 4: Способы получения - Вакцина, обозначенная как «Цирковирусная вакцина свиней, тип 3, модифицированный живой бакуловирусный вектор», была получена способом, описанным выше для группы 1. Надосадочная жидкость была объединена с 20% Карбопола, как показано в таблице 13. Вакцина удовлетворительно прошла тестирование на стерильность после розлива в окончательные контейнеры. Анализ безопасность на мышах перед применением материала у свиней не проводили.
Таблица 13. Состав вакцины - адъювант Карбопол
Пример 6
Вакцина для групп 3 и 5
Вакцина, обозначенная как «Модифицированный живой бакуловирусный вектор», представляет собой соответствующее плацебо продукта. Его готовили по следующей методике. Партию антигена 0,5 л получали в вращающейся колбе объемом 1 л путем инфицирования клеток SF+ (Spodoptera frugiperda) с приблизительной MOI, равной 0,1, рекомбинантным бакуловирусом, не содержащим вставки. Колбу инкубировали при 28°C±2°C при постоянном перемешивании приблизительно при 100 об./мин в течение четырех дней. Клетки и среду в асептических условиях переносили в центрифужный флакон на 1 л, и клетки осаждали при 10 000 g в течение 20 минут при 4°C. Полученную надосадочную жидкость фильтровали через фильтр с размером пор 0,2 мкм и хранили при 4°C. В состав материала входило 20% Карбопола, как показано в таблице 14. Вакцина удовлетворительно прошла тестирование стерильности после розлива в окончательные контейнеры. Анализ безопасность на мышах перед применением материала у свиней не проводили.
Таблица 14. Состав плацебо - адъювант Карбопол
На фигуре 10 показана информация о последовательности в PCV3 ПЦР-позитивном гомогенате ткани, использованном для инфекционного материала.
Плазмида инфекционного клона pCR-BluntII-TOPO-PCV3 была создана из gBlock генома PCV3 на 2000 пар оснований (KT869077), полученного от Integrated DNA Technologies (IDT). GBlock встраивали в вектор pCR-BluntII-TOPO и трансформировали в E.coli Stbl2. Плазмиду инфекционного клона амплифицировали и очищали из 1 л размноженной E.coli Stbl2 с использованием набора для очистки Qiagen CompactPrep Maxi-DNA Purification, следуя процедуре, рекомендованной производителем. Клон pCR-BluntII-TOPO-PCV3 3624-046.06, серия № 3718-038 разводили в стерильном ФСБ, pH 7,4 от Life Technologies Gibco, кат. № 10010-023, серия № 1967438 до конечной концентрации 400 мкг/мл плазмиды в общем объеме 4 мл. Разбавленную плазмиду переносили аликвотами в стерильный флакон с вакциной и хранили при -20°C.
Пример 7
Разработка модели заражения PCV3
Все таблицы 17, 21, 26, 31, 32-41, 42-51, 52, 54-63, 64-71, 72, 75, 76-84, 85-94, 95, 97-106, 107-117, и 118, упомянутые в примере 7, являются такими же, как таблицы 17, 21, 26, 31, 32-41, 42-51, 52, 54-63, 64-71, 72, 75, 76-84, 85-94, 95, 97-106, 107-117 и 118, приведенные в WO 2020/206452, содержание которой включено в настоящую заявку посредством ссылки.
PCV3 является новым заболеванием в мировой популяции свиней, и из-за его потенциальной корреляции с клиническим заболеванием он вызвал интерес к разработке вакцин против PCV3. Для оценки прототипов вакцин была необходима разработка модели заражения.
Как показано в следующих таблицах и фигурах, пример 7 отражает исследования, проведенные для разработки модели заражения PCV3 у молодых свиней. В частности, использовали молодых свиней, полученных после кесарева сечения, лишенных молозива («CDCD»).
Исследования были разработаны для оценки использования целого вируса и ПЦР-положительного гомогената ткани в качестве потенциальных контрольных материалов для будущих исследований. Кроме того, сохранность инфекционного клона PCV3 у свиней предоставило дополнительную возможность для будущих исследований модели заражения и поэтому было включено в план исследования.
Любые прототипы вакцин, доступные в ходе экспериментов, были включены для более точной оценки модели заражения.
PCV3 был выделен из клинического материала. Выделение вируса подтверждали с помощью кПЦР в режиме реального времени, трансмиссионной электронной микроскопии и иммунофлуоресцентного анализа с использованием подходящих антител. Было показано, что выделенный вирусный сбор не содержит других вирусов, включая PCV1, PCV2, PRRSV, SIV, коронавирусы свиней. Полученный вирус представлял собой чистую культуру. Чистота была подтверждена с помощью секвенирования следующего поколения.
Полный геном PCV3 клонировали в подходящий плазмидный вектор путем полного синтетического синтеза всего PCV3.
Геномная последовательность была подтверждена, и геном вырезали путем ферментативного расщепления плазмиды. Затем геном повторно сшивали для создания замкнутого ковалентного кольцевого генома PCV3.
Циркуляризованный геном PCV3 трансфицировали в подходящие клеточные линии для сохранения инфекционного вируса. Сохраненный вирус и/или циркуляризованный геном инокулировали молодой свинье. Циркуляризованный геном был введен в печень и паховый лимфатический узел под контролем ультразвука.
Во второй итерации были созданы плазмиды, которые содержали две копии генома PCV3. Достаточные количества очищенной плазмиды, содержащей димерный PCV3, были приготовлены для применения в разработке модели заражения и исследованиях патогенности/вирулентности.
Был получен клинический материал, включая ткани и жидкости, содержащие PCV3 с высоким титром, как определено с помощью кПЦР. Было показано, что клинический материал не содержит других вирусов свиней, включая PCV1, PCV2, PRRSV, SIV и/или коронавирусы свиней.
Клинический материал использовали для разработки модели заражения PCV3 и для исследований патогенности/вирулентности. Были проведены исследования на животных для оценки патогенности и распространения вируса с использованием различных путей инокуляции. В частности, дополнительно к другим исследуемым путям материал вируса PCV3 и/или гомогенат ткани с высоким титром инокулировали в один рог матки свиноматок на 40-й день беременности. Оценивали распространение PCV3 на плод в зараженном роге и неинокулированном роге матки. Оценивали развитие мумий в результате заражения PCV3.
Модель заражения использовали для формирования основы для оценки потенциальных вакцин.
Образцы из исследований PCV3 были протестированы, включая предварительную скрининговую ПЦР и серологию, ПЦР для модели заражения и инфекционных клонов, серологию для исследований вакцин.
Предел обнаружения, чувствительность и специфичность анализов не определяли.
Вакцины-кандидаты оценивали в различных комбинациях адъювантов. Вакцины-кандидаты включали, например, бакуловирус, экспрессирующий ORF2 PCV3, и геном PCV3, экспрессированный в плазмиде (вакцину на основе нуклеиновой кислоты). Серологический анализ был проведен для исследования вакцины.
В таблице 15 относится к дозировке продукта и условиям содержания животных. В частности, в таблице 15 показаны животные, оцененные по группам. В частности, были определены помет, конкретное животное, были ли они вакцинированы, помещение, в которой находились животные, и чан, у которого они находились.
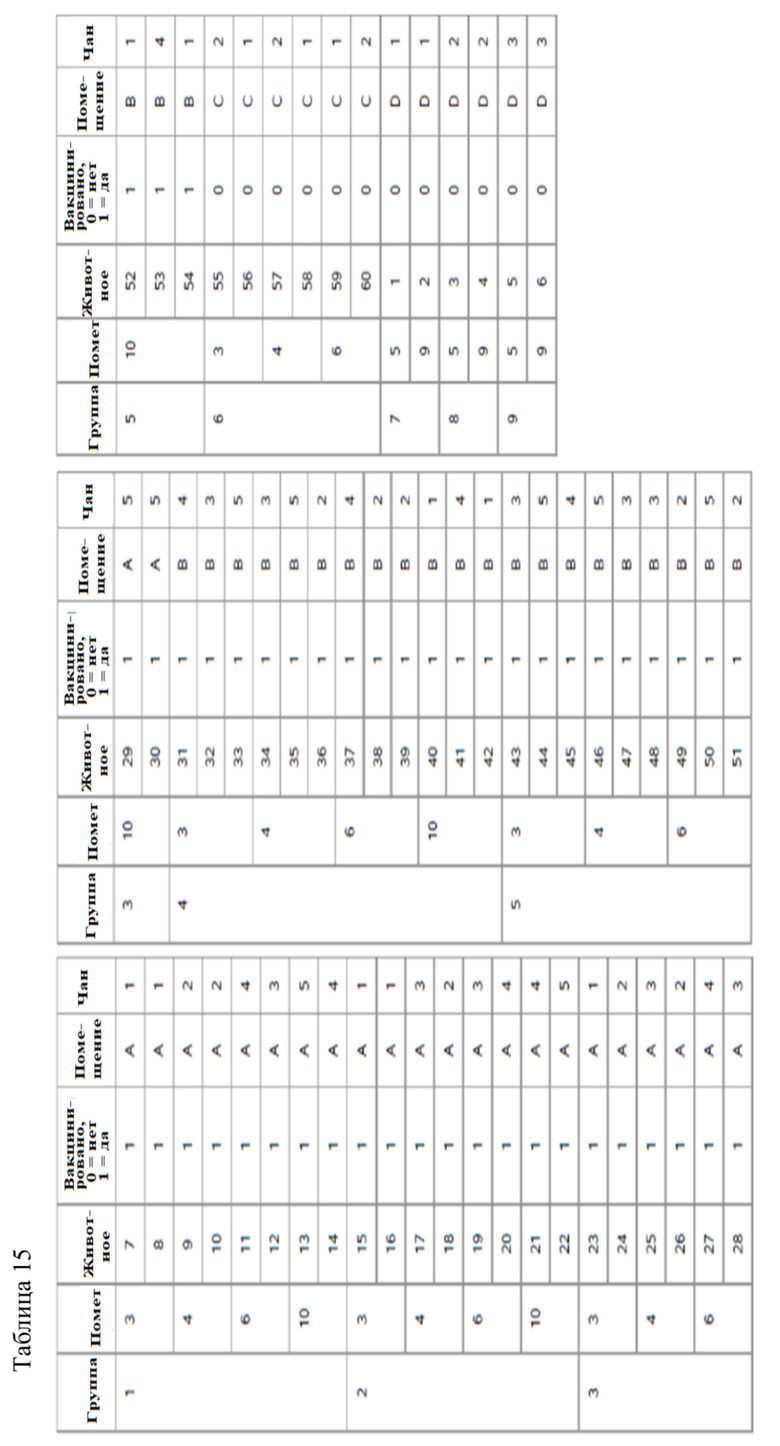
Следующие данные относятся к данным о виремии у животных и их анализу.
Как показано в таблице 16, значения виремии, измеренные с использованием кПЦР в сыворотке и показанные в логарифмических единицах геномных копий/мл, представлены по группам животных в выбранные дни исследования.
Таблица 16
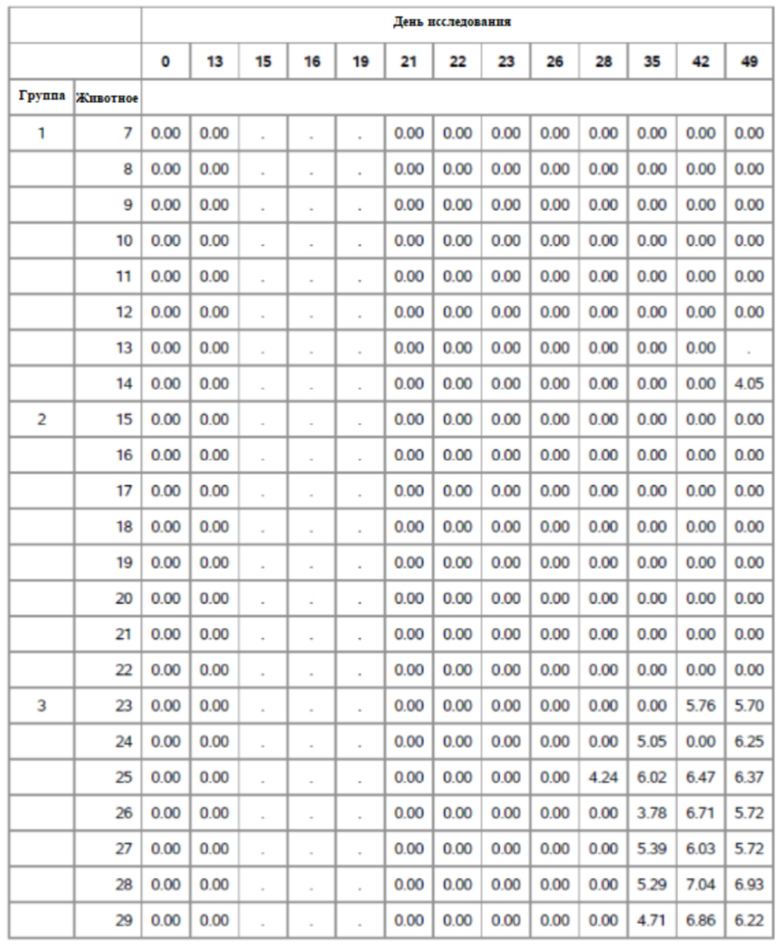
Таблица 16, продолжение
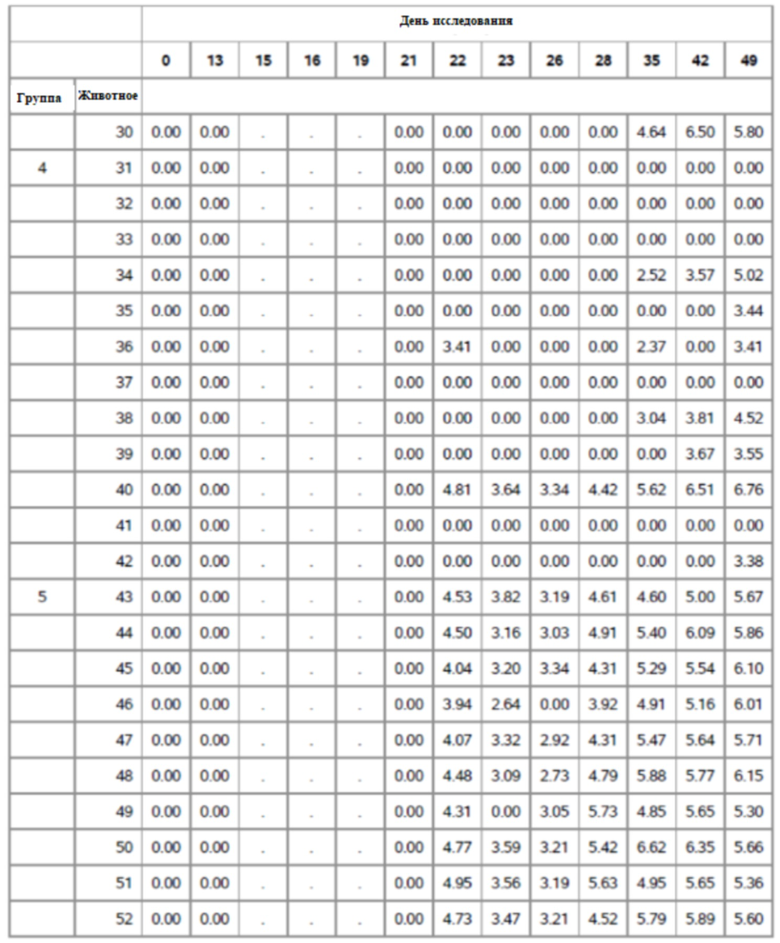
Таблица 16, продолжение
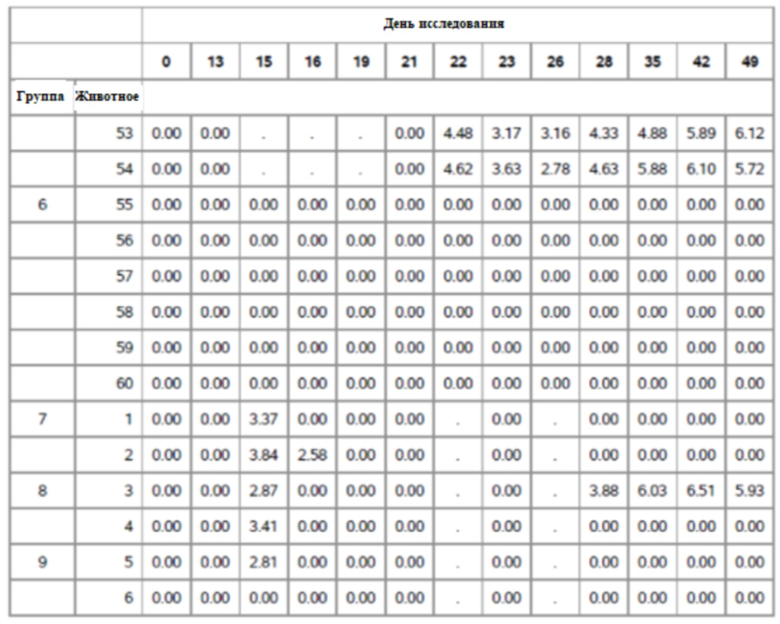
На фигуре 11 показано среднее значение ПЦР для групп 1-5 от семи до сорока девяти дней.
На фигуре 12 показано медианное значение ПЦР для групп 7-9 от семи до сорока девяти дней.
В таблице 18 представлены результаты анализа виремии для групп 1-5.
Таблица 18
Виремия (кПЦР сыворотки, log геномных копий/мл), результаты виремии по группам.
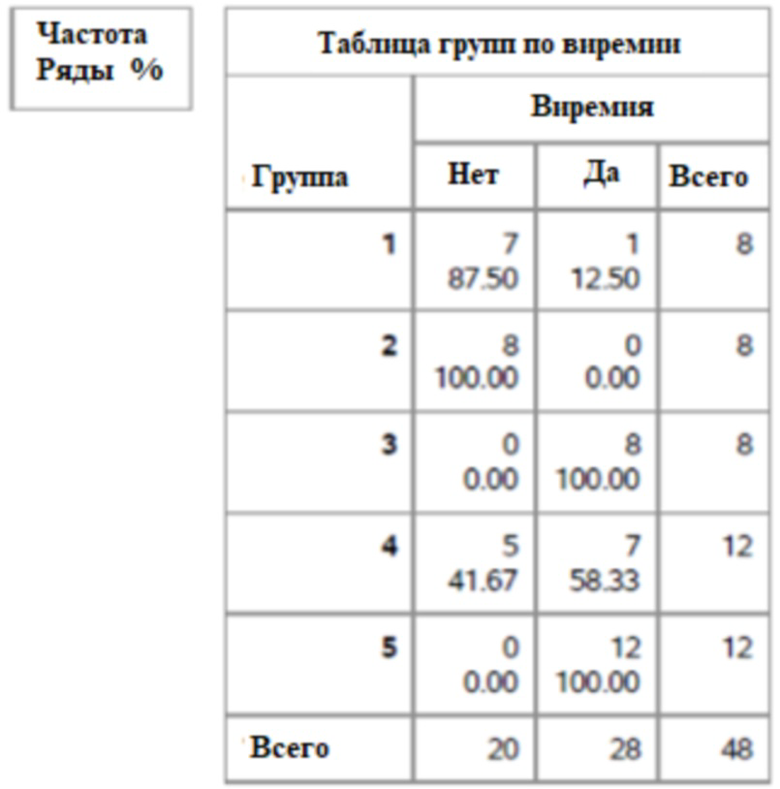
Сравнение значений Р для данных из таблицы 18 показано в таблице 19.
Таблица 19
Виремия (кПЦР сыворотки, log геномных копий/мл), сравнение значений Р по группам.
Следующие данные относятся к данным выделения вируса в фекалиях при измерении с использованием кПЦР фекалий (т.е. логарифм копий гена/мл) у субъектов-животных, и к их анализу.
Как показано в таблице 20, значения выделения вируса в фекалиях при измерении с помощью кПЦР фекалий, показанные в логарифмических геномных копиях/ мл, представлены по группам для животных в выбранные дни исследования.
Таблица 20
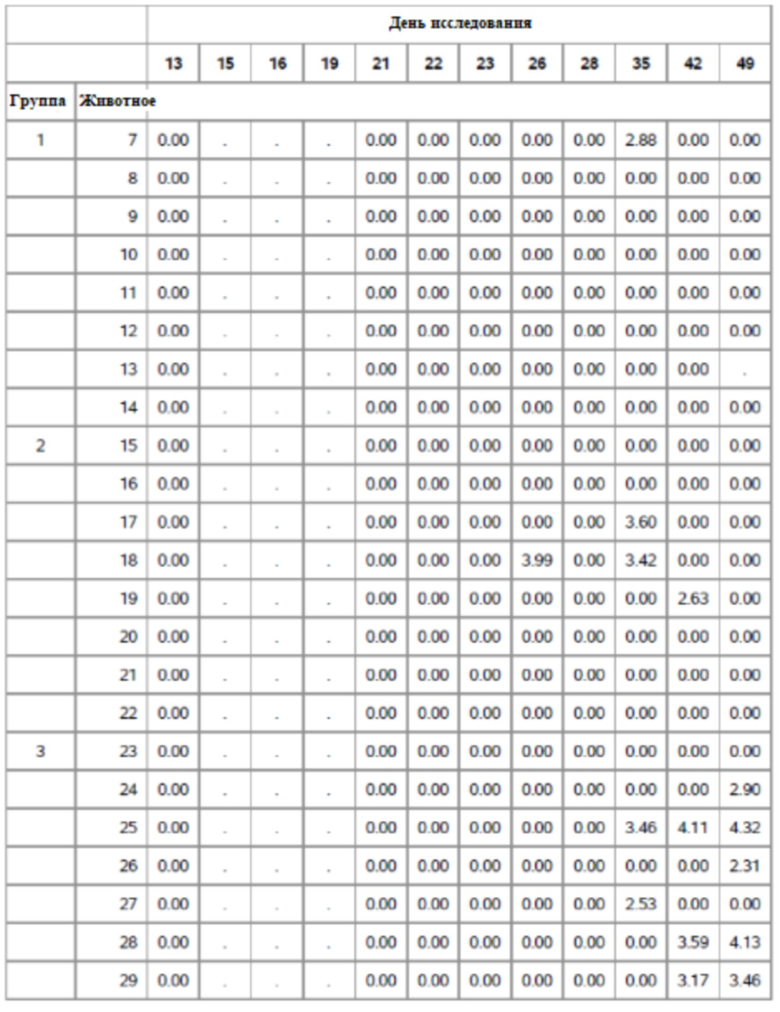
Таблица 20 (продолжение)
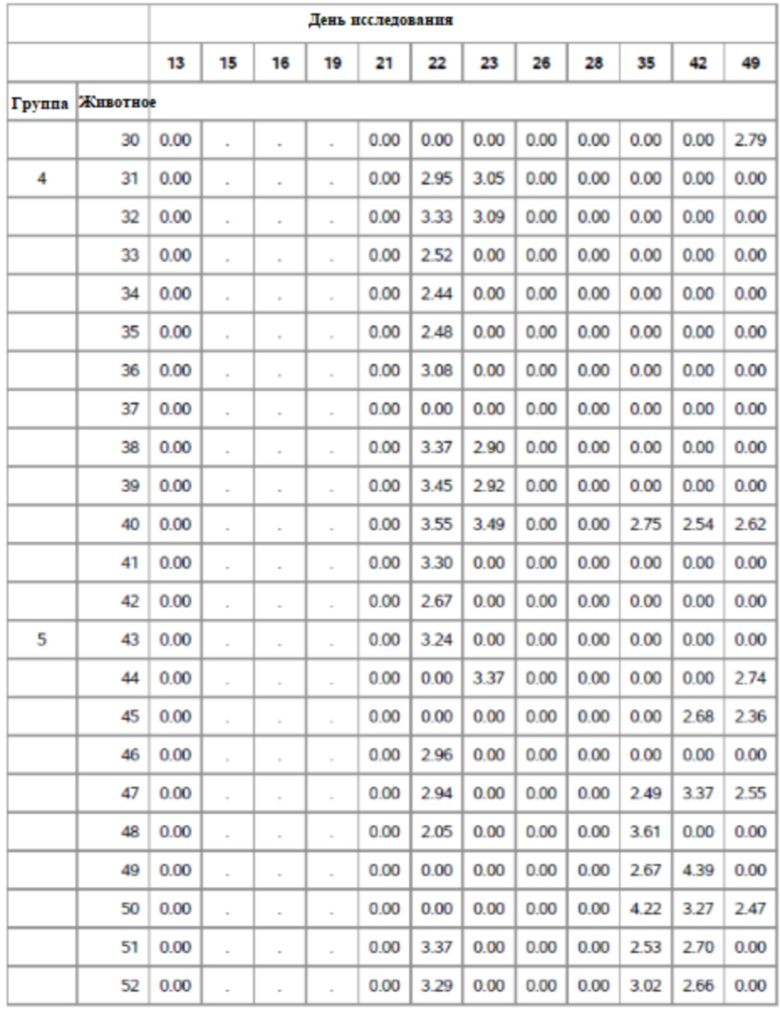
Таблица 20 (продолжение)
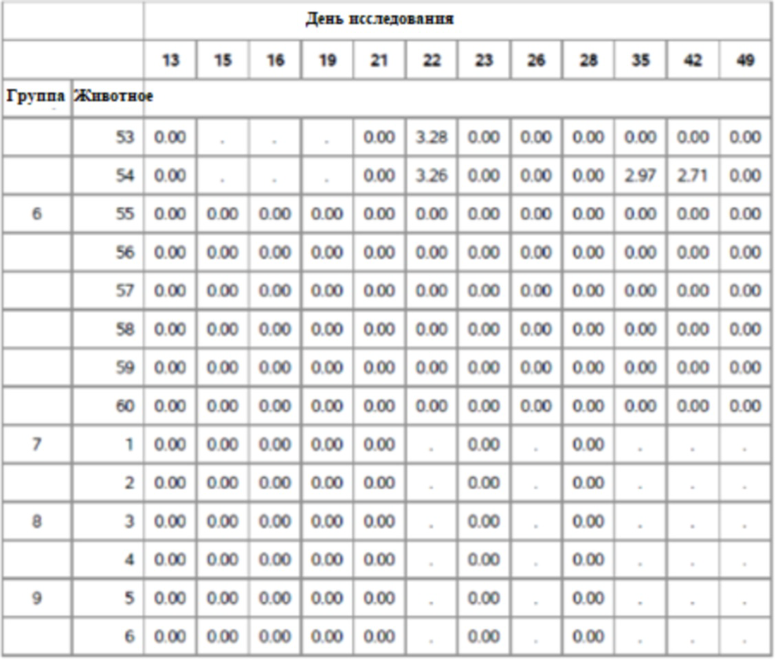
На фигуре 13 показаны медианные значения ПЦР для выделения вируса с фекалиями для групп 1-5 от семи до сорока девяти дней.
В таблице 22 представлены результаты определения выделения вируса с фекалиями для групп 1-5.
Таблица 22
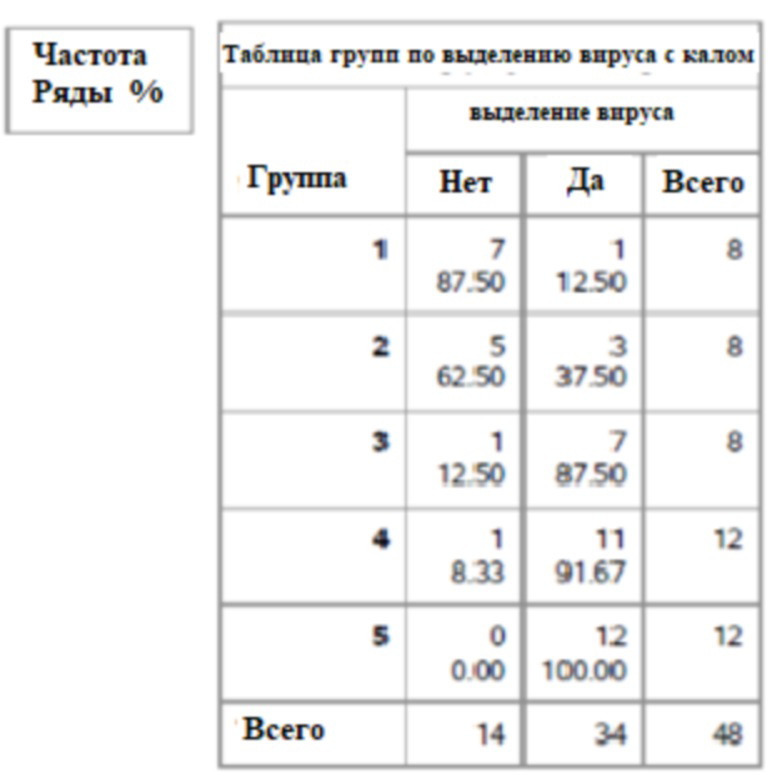
Сравнение значений P для данных из таблицы 22 (определения выделения вируса в фекалиях) показано в таблице 23.
Таблица 23
Прямое сравнение значений P (т.е. критерия Уилкоксона) для групп 4 и 5 показано в таблице 24.
Таблица 24
Следующие ниже данные относятся к данным по выделению вируса в назальном мазке при измерении с использованием кПЦР назального мазка (т.е. логарифм геномных копий/мл) у животных, и к их анализу.
Как показано в таблице 25, количество выделенного вируса в назальном мазке при измерении с помощью кПЦР назального мазка и показанные в логарифмах геномных копий/мл, представлены по группам для животных в выбранные дни исследования.
Таблица 25
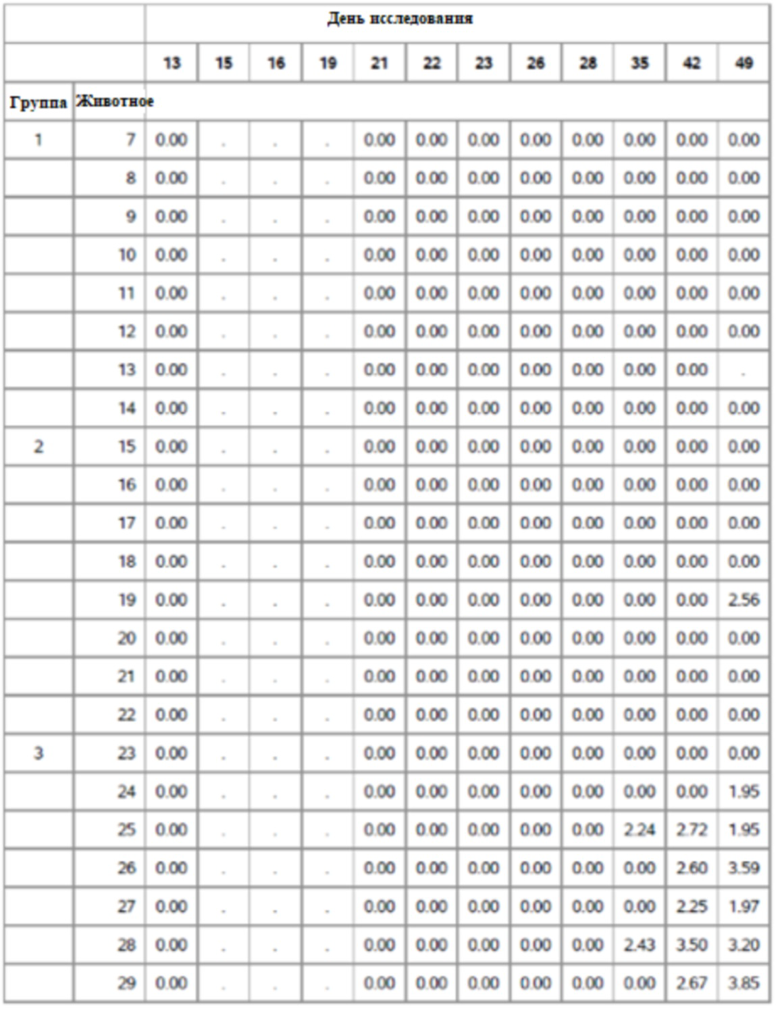
Таблица 25 (продолжение)
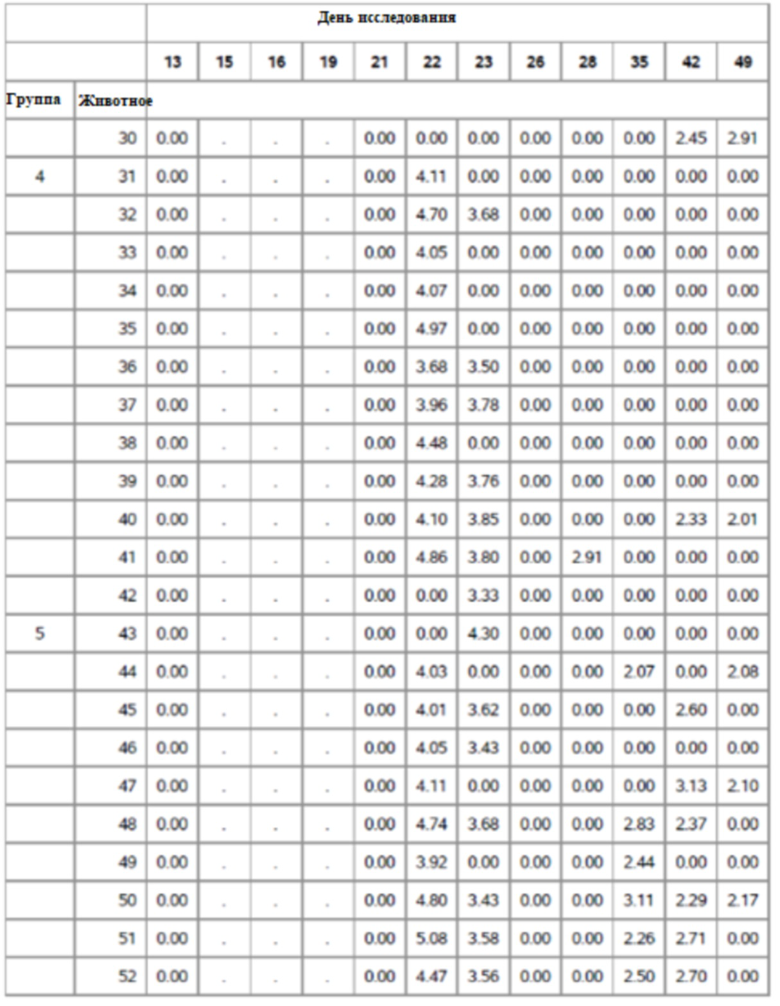
Таблица 25 (продолжение)
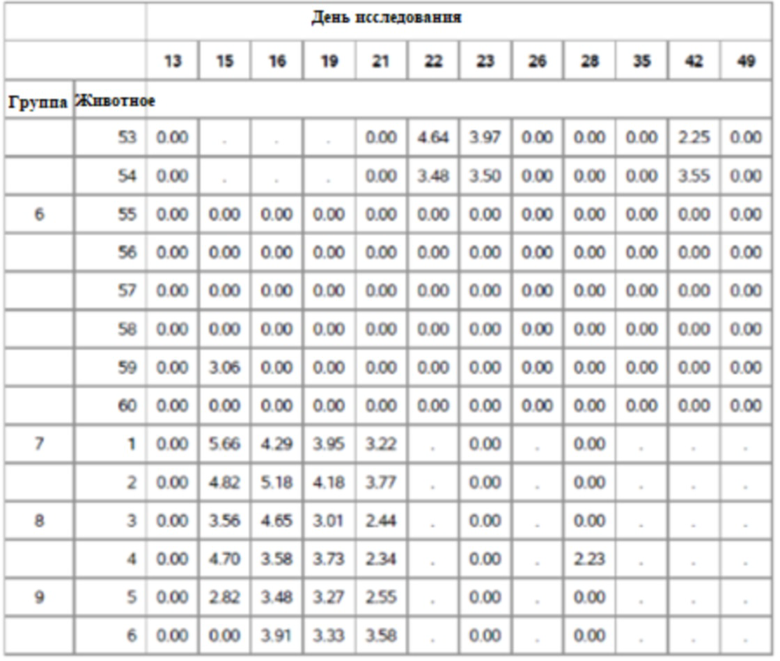
На фигуре 14 показаны медианные значения ПЦР для выделения вируса из носа для групп 1-5 от семи до сорока девяти дней.
В таблице 27 представлены результаты определения выделения вируса из носа для групп 1-5.
Таблица 27
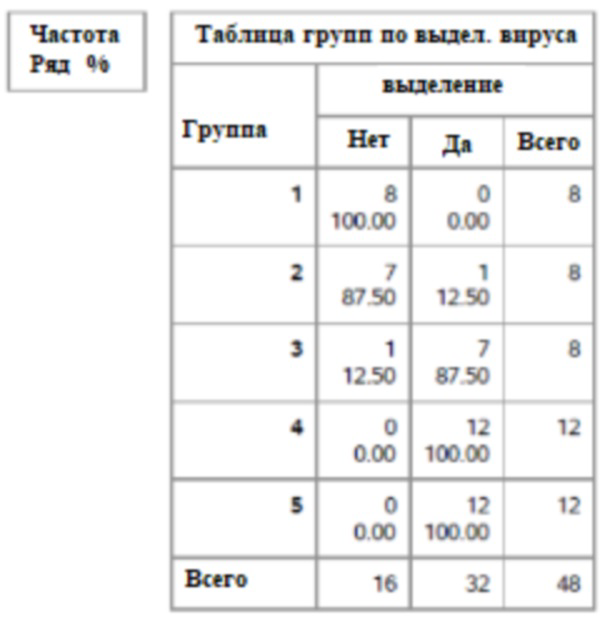
Сравнение значений P для данных таблицы 27 (определение выделения вируса из носа) показано в таблице 28.
Таблица 28
Прямое сравнение значений P (т.е. тест Уилкоксона) для групп 4 и 5 показано в таблице 29.
Таблица 29
Следующие данные относятся к показаниям ректальной температуры (ºF), измеренным у животных, и к их анализу.
Как показано в таблице 30, значения ректальной температуры, измеренные в градусах Фаренгейта, изображены по группам для животных в течение ряда дней исследования.
Таблица 30
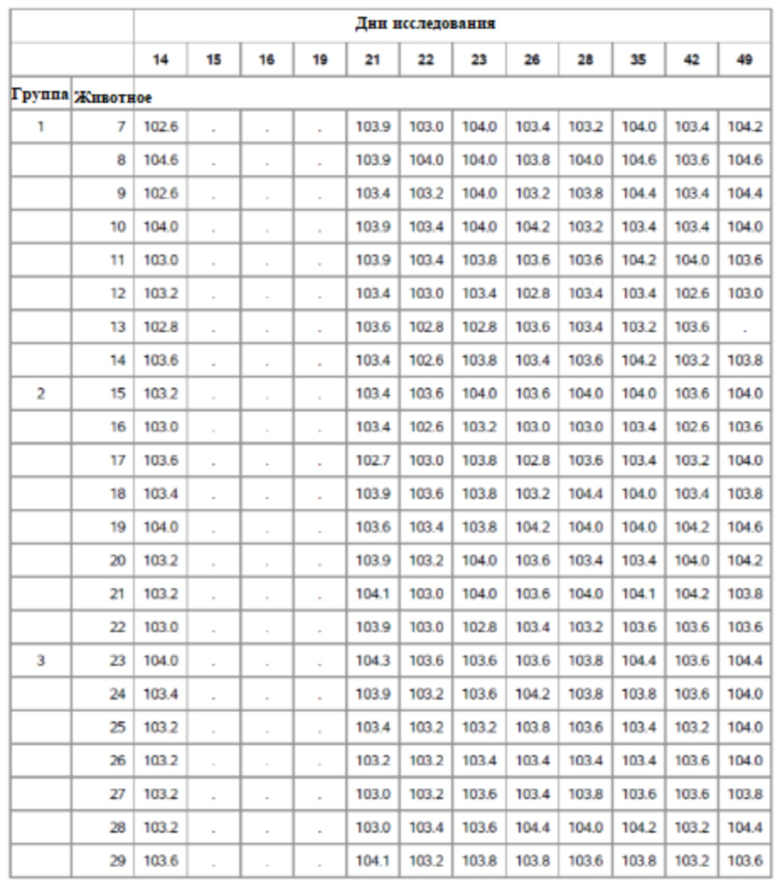
Таблица 30 (продолжение)
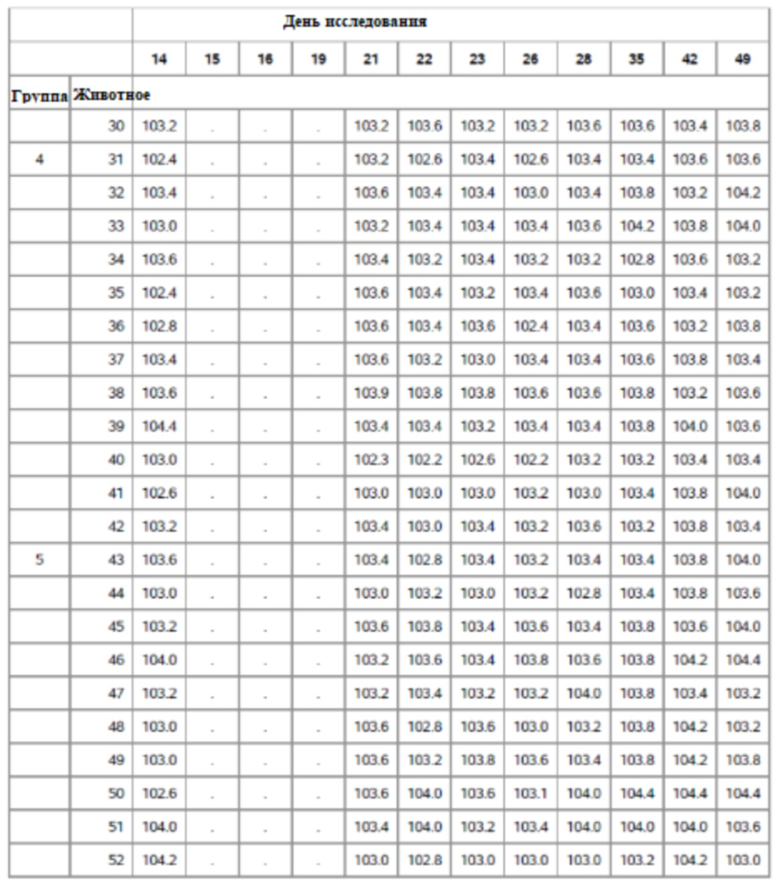
Таблица 30 (продолжение)
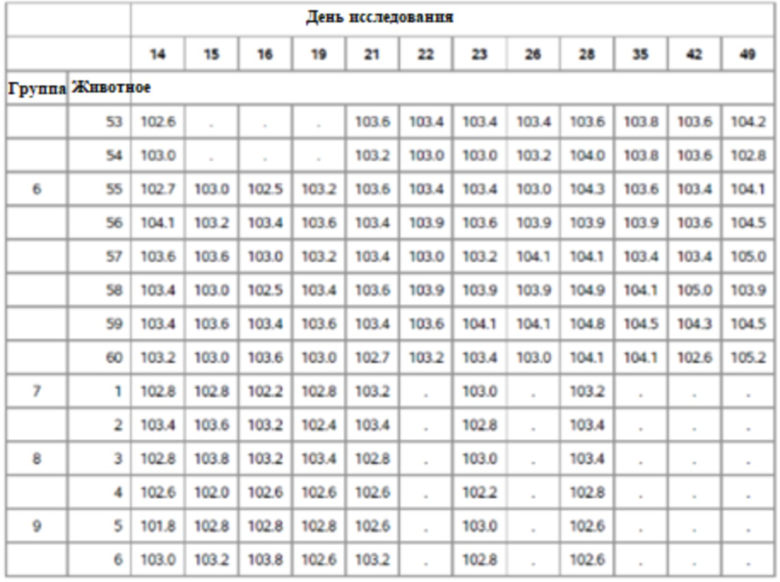
На фигуре 15 показано среднее арифметическое значение ректальной температуры для групп 1-6 с четырнадцати до сорока девяти дней оценки.
На фигуре 16 представлены средние значения температуры, полученные способом наименьших квадратов по группам и дням для групп 1-5.
В таблице 53 показывает сравнение значений P для данных, относящихся к ректальной температуре.
Таблица 53. Ректальная температура (F). Значения Р при сравнении групп
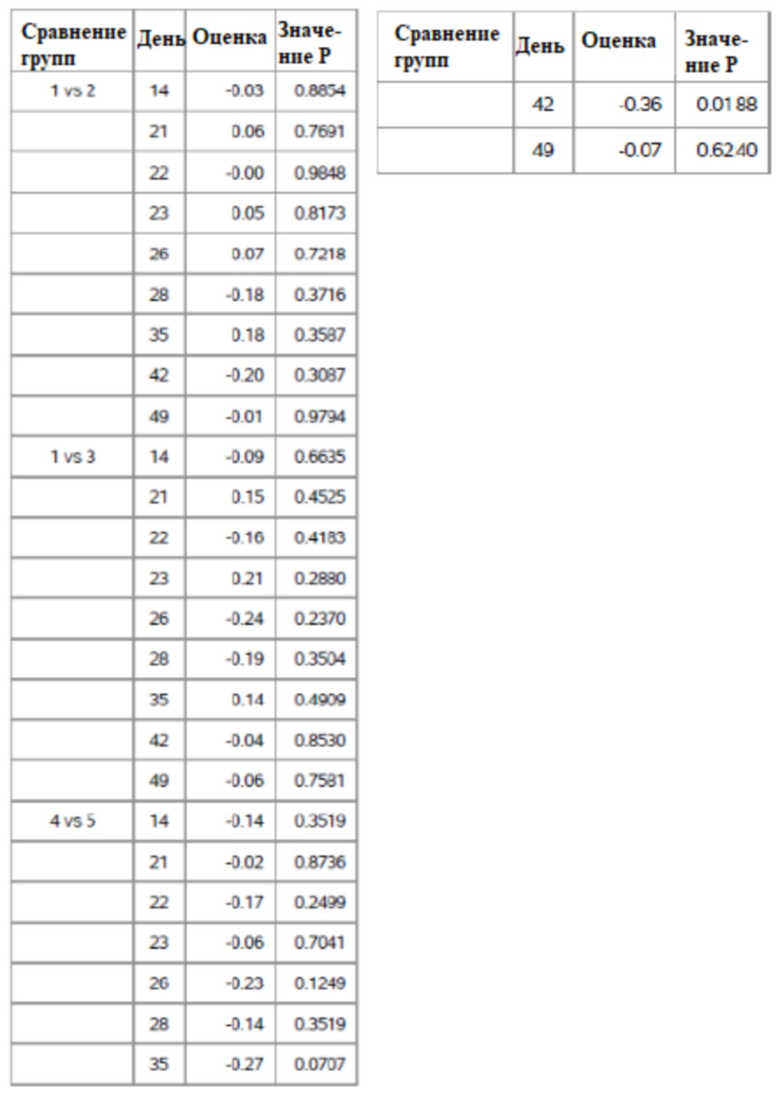
На фигуре 17 представлена линейная диаграмма, показывающая средние ректальные температуры животных (скорректированные по базовой линии на основе наименьших квадратов) по группам и дням для групп 1-5.
В таблице 73 показано сравнение значений P для различных групп (1-5).
Таблица 73. Ректальная температура (F) (с поправкой на базовую линию). Значения Р при сравнении групп
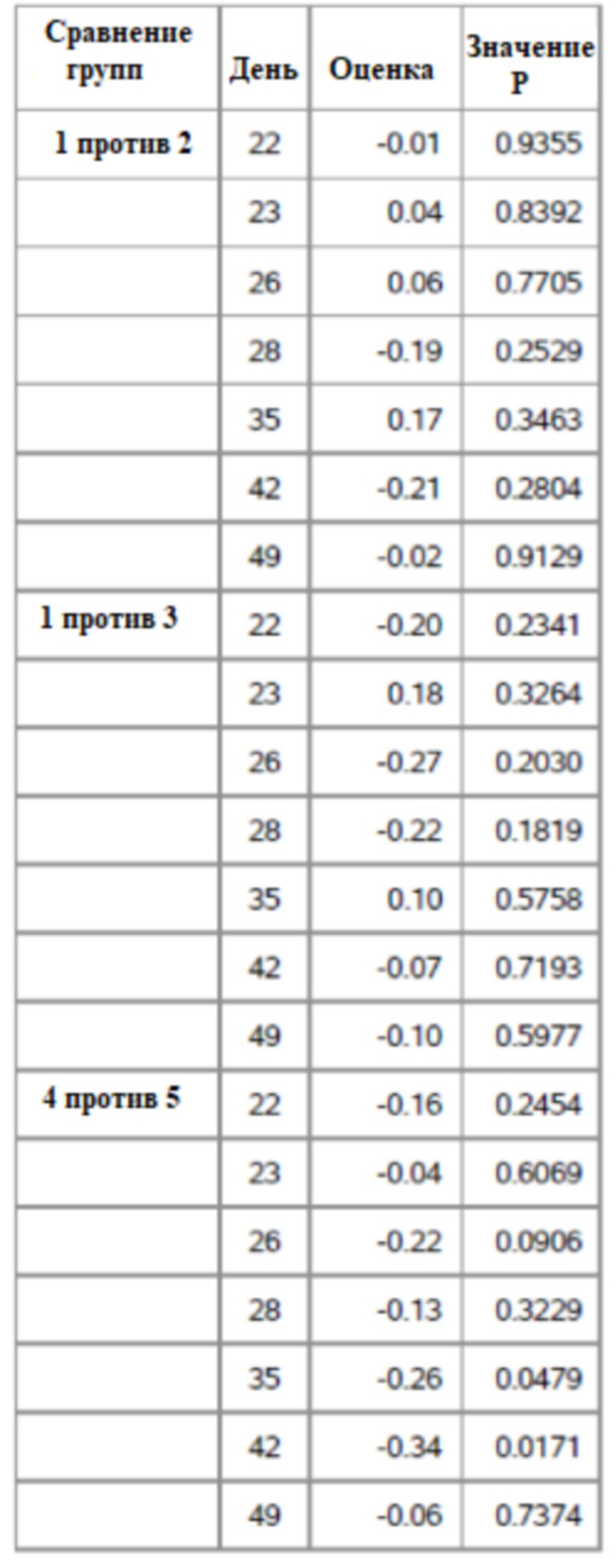
Следующие данные относятся к значениям массы тела (кг), измеренным у животных, и их анализу.
Как показано в таблице 74, значения массы тела, измеренные в килограммах, изображены по группам для животных в выбранный день исследования.
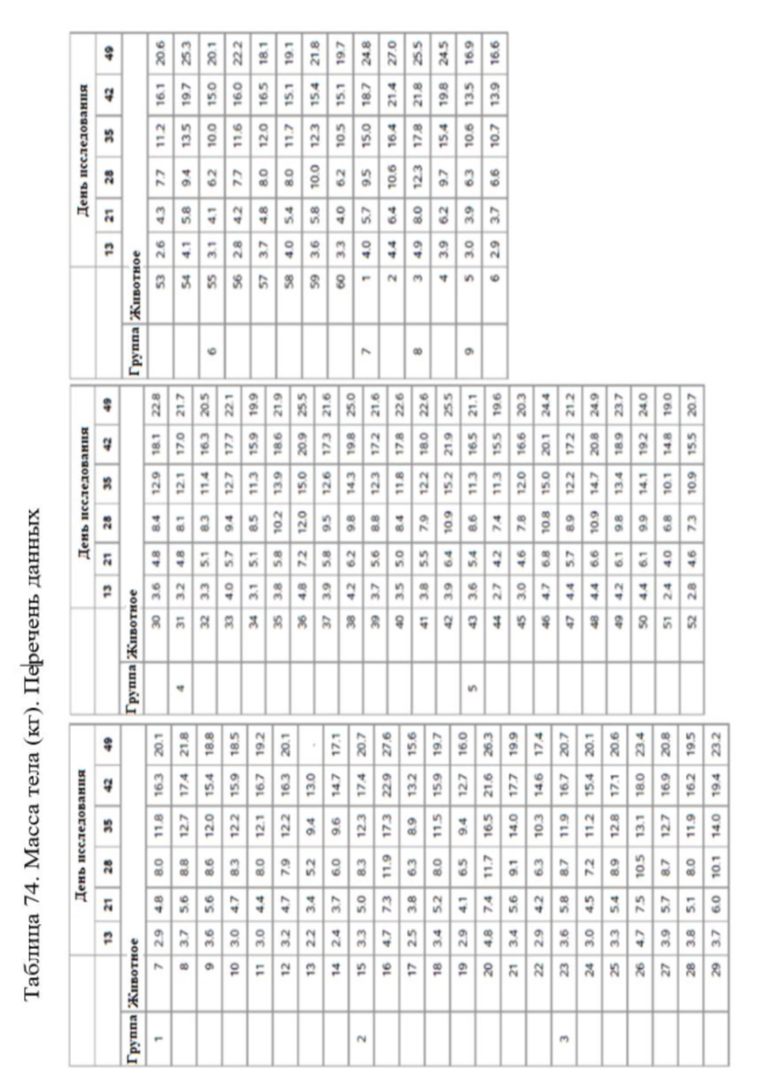

На фигуре 19 представлен линейный график, показывающий средние значения массы тела (по способу наименьших квадратов) по группам и дням для групп 1-5.
В таблице 96 представлено сравнение в группах P-значений для массы тела.
Таблица 96. Масса тела (кг). Сравнение значений Р в группах
групп
Р
—
На фиг.20 представлен линейный график, изображающий данные для средних значений наименьших квадратов для массы тела (с поправкой на исходный уровень) по группам и дням.
В таблице 119 представлена таблица P-значений для сравнения различных групп (1-5) по массе тела, корректированной по базовому уровню.
Таблица 119. Масса тела (кг) (скорректированной по базовой линии), значения Р для сравнения групп
Пример 8
Биопроцесс PCV3
Заражение осуществляли с помощью бакуловирусного посевного материала BaculoG/PCV3 ORF2 Pre-MSV. Целевая MOI составляла 0,1, а окончательная расчетная MOI - 0,1.
Параметры заражения показаны в таблице 120.
Таблица 120
• Кольцевой разбрызгиватель
• Крыльчатка с наклонными лопастями 2 х 45° и отрицательным наклоном, установленная на расстоянии примерно от одного до семи дюймов от нижней части вала мешалки.
Жидкости биореактора собирали в асептических условиях в биотейнер на 10 л, разливали в 8 центрифужных флаконов емкостью по 1 л и центрифугировали при 10000 g в течение 20 минут при 4°C. Осветленные жидкости собирали в асептических условиях в биотейнер на 10 л и фильтровали через фильтр 0,8/0,2 мм в новый биотейнер на 10 л, а окончательный отфильтрованный собранный продукт хранили при 4°C.
Десять различных условий инактивации были исследованы при 5 мМ концентрации бинарного этиленимина (BEI) при 37°C в течение 72 часов, как показано в таблице 121. Были взяты образцы для мониторинга pH (таблица 122) и растворимости ORF2 PCV3.
Таблица 121
ВДИ
NaCl
NaCl
NaCl
MgCl2
MgCl2
MgCl2
7.0
7.5
сбор (мл)
pH 7.5
На фиг.24 показаны изображения инактивации в момент времени 72 часа.
Таблица 122
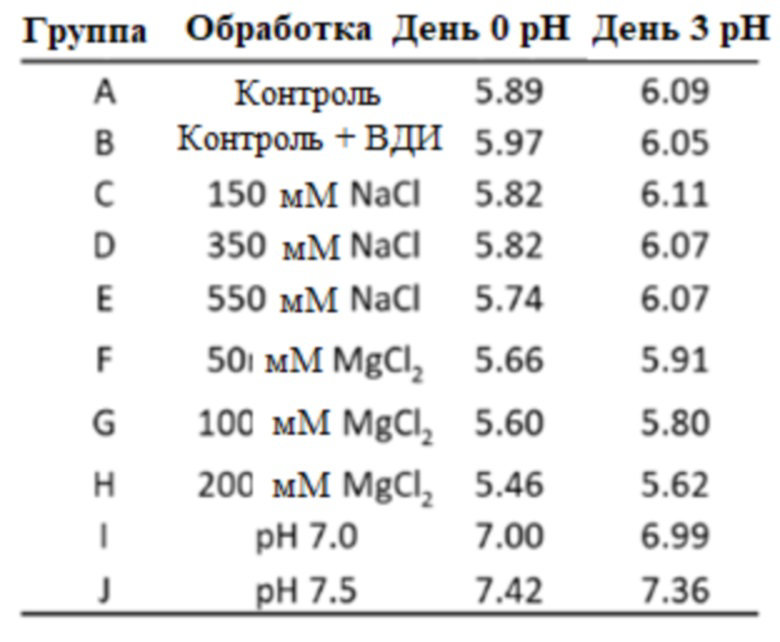
На фиг.25 показано сравнение условий инактивации антигена ORF2 BaculoG/PCV3 с помощью вестерн-блоттинга – после инактивации.
На фиг.26 показан флуоресцентный дот-блот PCV3 ORF2.
По данным этого исследования, низкий уровень ORF2 PCV3, продуцируемый в биореакторе, который аналогичен испытаниям в мешалках, и кинетика заражения свидетельствует о незначительном недостатке инокулята. После инактивации наблюдалась минимальная потеря ORF2 PCV3 из биореактора, поскольку каждое из условий оказывало минимальное влияние на растворимую ORF2, хотя MgCl2 в концентрации 200 мМ мог иметь большее влияние на наблюдаемую потерю ORF2 PCV. Потери ORF2 PCV3 в жидкостях для сбора при хранении при 4°C в течение 9 дней не наблюдалось.
Пример 9
Вакцинация молодых свиней, рожденных путем кесарева сечения, лишенных молозива, инактивированной вакциной ORF2 PCV3, экспрессируемой бакуловирусом
В этом исследовании оценивали экспериментальную вакцину PCV3 ORF2, экспрессируемую инактивированным бакуловирусом, при введении 3-недельным молодым свиньям. Рандомизированное слепое исследование с вакцинацией/заражением было проведено с использованием 50 молодых свиней, полученных путем кесарева сечения, лишенных молозива («CDCD»), возрастом 22 дня на Д0. Молодые свиньи были снабжены подстилкой и произвольно распределены по экспериментальным группам, причем однопометники содержались в одном загоне. В Д0 поросятам внутримышечно вводили контрольный продукт или плацебо, соответствующее продукту, или экспериментальную вакцину. Поросят наблюдали ежедневно на предмет общего состояния здоровья и собирали кровь для оценки сероконверсии. Всех молодых свиней заражали через 14 дней после вакцинации гомогенатом ткани (который дал положительный результат на PCV3 при ПЦР), и вскрывали через четыре недели. Клинические наблюдения проводили ежедневно после заражения до завершения исследования (Д42), а кровь собирали еженедельно для оценки виремии (PCV3 с помощью ПЦР). При аутопсии внутренние органы оценивали на предмет макроскопических повреждений, а ткани собирали для гистопатологической оценки. Гистологические препараты окрашивали, исследовали с помощью RNAScope и оценивали.
На протяжении всего исследования весь персонал, участвовавший в сборе данных или выполнении лабораторных анализов, не знал, какое лечение будет назначено свиньям. Лечение проводил исследователь, который не участвовал в сборе данных.
Использование 20 животных в контрольной группе и группе вакцины, соответственно, согласуется с предыдущими исследованиями по лицензированию вакцинации против цирковируса свиней. Были включены дополнительные животные для учета естественной убыли молодых свиней CDCD перед контрольным заражением.
Свиней снабжали подстилкой и случайным образом распределяли для лечения, принимая отдельного поросенка за экспериментальную единицу.
Все рандомизации проводили с использованием SAS версии 9.4. Использовали пометы от шести (7 помётов) или восьми (1 помёт) молодых свиней. Для произвольного распределения в экспериментальную группу случайную вариацию генерировали для каждой молодой свиньи с использованием функции RANUNI в SAS. Затем идентификаторы молодых свиней были отсортированы по помету и различным значениям. В каждом помете трем (или четырем для помета с 8 молодыми свиньями) животным с наименьшими значениями вариабельности были присвоены Т01, а остальным - Т02. Во время фазы вакцинации молодых свиней в максимально возможной степени содержали по пометам, по три или четыре молодой свиньи на брудер, с использованием брудеров в трех помещениях. Во время фазы заражения, за исключением помета из 8 молодых свиней, молодых свиней содержали по пометам, по одному помету на загон, в одном из двух помещений. Помет с 8 однопометниками размещали в двух загонах по 6 и 2 однопометника, соответственно. Для контрольного содержания загоны были рандомизированы по местам и станкам в пределах помещения путем генерации случайных значений для каждого помета, сортировки по разным значениям и согласования отсортированного порядка с комбинациями мест-станков.
Фаза вакцинации. Двадцать пять молодых свиней, рожденных посредством кесарева сечения, лишенных молозива (CDCD), в возрасте приблизительно 3 недель вакцинировали либо вакциной ORF2 PCV3, экспрессированной с помощью бакуловируса, либо контрольной вакциной, подобранной в качестве плацебо. Было установлено, что титр вируса составлял 6,76 x 106 TCID50/мл. Инактивированный антиген готовили с 20% карбополом и разливали в окончательные контейнеры. Плацебо, используемое в качестве отрицательного контроля, получали таким же образом с инактивированным антигеном из бакуловируса отрицательного контроля. Вакцину или плацебо вводили внутримышечно каждому животному. Пуповинную кровь собирали у всех молодых свиней при родах (кесарево сечение; день -22). Сыворотку отделяли и тестировали на ДНК PCV3 и ДНК PCV2 с помощью ПЦР. Все образцы были отрицательными как по PCV3, так и по PCV2. На D-2 у всех молодых свиней брали кровь для сбора сыворотки, а затем вакцинировали PCV2 Ingelvac CircoFLEX®. Все образцы сыворотки были отрицательными при ПЦР как на PCV3, так и на PCV2, и серонегативными на M. hyopneumoniae и вирус репродуктивного и респираторного синдрома свиней.
Фаза заражения: всех животных заражали гомогенатом ткани, положительным по PCV3 (1 мл интраназально и 1 мл внутримышечно) через 14 дней после вакцинации. Гемоцианин лимфы улитки (KLH), эмульгированный в неполном адъюванте Фрейнда (ICFA), содержащем 1 мг KLH/мл, вводили внутримышечно за два дня до и через два дня после заражения (таблица 123). Гомогенат ткани, использованный для заражения, был проверен на наличие посторонних агентов с помощью количественной ПЦР и глубокого секвенирования. На 42-й день животных умерщвляли. При вскрытии собирали ряд тканей. К ним относятся мозг, сердце, почки, легкие, селезенка, толстая кишка, миндалины, трахеобронхиальный лимфатический узел (TBLN), мезентериальный лимфатический узел (MLN) и внешний подвздошный лимфатический узел (ILN).
Таблица 123. Дизайн исследования
В таблице 124 описан гомогенат ткани, используемый для заражения животных PCV3.
Таблица 124
В таблице 125 предоставляет информацию о свиньях, использованных в исследовании.
Таблица 125
На D-2 у всех свиней брали кровь для сбора сыворотки, а затем вакцинировали PCV2 Ingelvac CircoFLEX®. Сыворотку немедленно ставили на лед или замораживали в BI AH USA-Ames и тестировали на ДНК PCV3 и ДНК PCV2 с помощью ПЦР в ISU-VDL. Все образцы были отрицательными при ПЦР как на PCV3, так на PCV2. Хранившиеся образцы сыворотки Д-2 (за исключением молодой свиньи № 18 и № 45 из-за отсутствия сыворотки) были представлены в ISU-VDL для подтверждения серонегативного статуса M. hyopneumoniae (отношение S/P <0,3) и вируса PRRSV (отношение S/P <0,4). Все образцы были отрицательными.
Все 50 молодых свиней соответствовали требованиям, изложенным выше, и исследователь провел оценку здоровья на Д-2, чтобы убедиться, что в исследование были включены только здоровые животные.
После начала исследования молодых свиней исключали только в случае травмы, болезни или смерти, которые могут повлиять на результат исследования. Две молодые свиньи были изъяты во время фазы вакцинации, и пять молодых свиней были изъяты во время фазы заражения.
Свинья № 5 (вакцинированная группа) наблюдалась в связи с отсутствием аппетита и снижением активности на Д6; свинья была умерщвлена и исключена из исследования на Д6. Вскрытие показало желтушную кожу, подкожную фасцию и фибрин на печени и селезенке с пятнистой поверхностью печени, и коллапс левой апикальной доли легкого. Тушу утилизировали способом компостирования.
Свинью № 4 (вакцинированная группа) усыпили и изъяли из исследования перед заражением на D14 из-за плохого состояния тела и хромоты на обеих задних ногах. При вскрытии макроскопических повреждений не наблюдалось. Тушу утилизировали путем сжигания.
Виремия: Виремию определяли как положительный результат на PCV3 с помощью ПЦР (пороговое значение цикла (Ct) <37, геномная эквивалентность 4,697 log для этого исследования). Виремию после заражения вакцинированных и контрольных животных оценивали с помощью количественной ПЦР. Все контрольные молодые свиньи были виремическими в каждой точке отбора проб во время фазы заражения (таблица 126). Три вакцинированных молодые свиньи имели положительные результаты на Д7 со значениями Ct от 35,6 до 36,7 (при ≥37 - пороговое значение для отрицательного результата), что, скорее всего, указывало на ложноположительный результат, учитывая, что все вакцинированные молодые свиньи были отрицательными на Д12 перед заражением. После заражения у двух вакцинированных молодых свиней не отмечалось виремии. В то время как до 91% вакцинированных молодых свиней действительно становились виремическими, нагрузка вируса (геномные копии) в крови была значительно снижена примерно на log у вакцинированных в каждый момент времени после заражения (P≤0,0050) по сравнению с контрольной группой (фиг.27).
Таблица 126. Частота и процент молодых свиней с виремией PCV3 в зависимости от лечения и дня

Наблюдения за общим состоянием здоровья: За всеми молодыми свиньями ежедневно наблюдали для оценки общего состояния здоровья с Д2 до Д14 с дополнительным наблюдением между 2 и 4 часами после вакцинации. Никаких клинических признаков не наблюдалось после вакцинации до Дня 6, когда у этой молодой свиньи № 5 (вакцинированная группа) наблюдалась потеря аппетита и снижение активности до изъятия из исследования по гуманным соображениям. На Д8 у молодых свиней № 12 (вакцинированная группа), № 15 (группа плацебо), № 36 (вакцинированная группа) и № 38 (группа плацебо) наблюдались грыжи. На Д9 молодая свинья №4 (вакцинированная группа) была обнаружена застрявшей между кормушкой и стенкой перед транспортировкой в VRI; в VRI у этой молодой свиньи была обнаружена хромота с опухшей правой задней ногой, которая прогрессировала до двусторонней хромоты на задние ноги на Д11, прежде чем она была изъята из исследования перед заражением на Д14.
Смертность после заражения: Молодых свиней, которые умерли или были усыплены после заражения перед тестированием на Д42, вскрывали. Две контрольные молодые свиньи (группа плацебо) и три вакцинированные молодые свиньи (вакцинированная группа) погибли или были умерщвлены во время фазы заражения. Молодая свинья № 7 (вакцинированная группа) была найдена мертвой на 26-й день. При аутопсии были выявлены закупорка менингеальных сосудов и увеличение ILN. Молодая свинья №2 (вакцинированная группа) была найдена мертвой на 30-й день. При аутопсии наблюдались хронически активный фиброзный и фибринозный перикардит и краниальная вентральная пневмония. Молодая свинья №19 (вакцинированная группа) была найдена мертвой на 31 день. У этой свиньи наблюдался маленький размер, при вскрытии не обнаруживались макроскопические повреждения, что свидетельствует о неспособности развиваться. Молодая свинья № 49 (группа плацебо) была найдена мертвой на 35 день, без предшествующих клинических признаков и с макроскопическими поражениями в виде легочного застойного явления в почках со скудным количеством белого экссудата. Молодая свинья № 15 (группа плацебо) была умерщвлена по гуманным соображениям на Д40. Эта свинья находилась в коме. Вскрытие показало умеренную гидроцефалию и диффузную гиперемию менингеальных сосудов. Ранее у этой молодой свиньи была атаксия в течение 7 дней и снижение активности в течение четырех предыдущих дней. Кроме того, у этой молодой свиньи наблюдались тяжелые респираторные симптомы (шумное дыхание) на Д35 и ухудшение состояния тела в течение 10 дней до эвтаназии.
Через 2-4 часа после заражения, а затем ежедневно во время фазы заражения, всех молодых свиней исследовали один раз в день на предмет клинических признаков, связанных с PCV3, как описано в таблице 127.
Таблица 127
Нет
Умерен-ный
Средний
Тяжелый
Тяжелый
Тяжелый
Клинические признаки наблюдались между Д21 и Д40, в большинстве случаев это небольшое снижение функции (неврологической) и умеренное увеличение частоты дыхания (таблица 128). Во время фазы заражения не отмечено диареи и дерматита.
Таблица 128
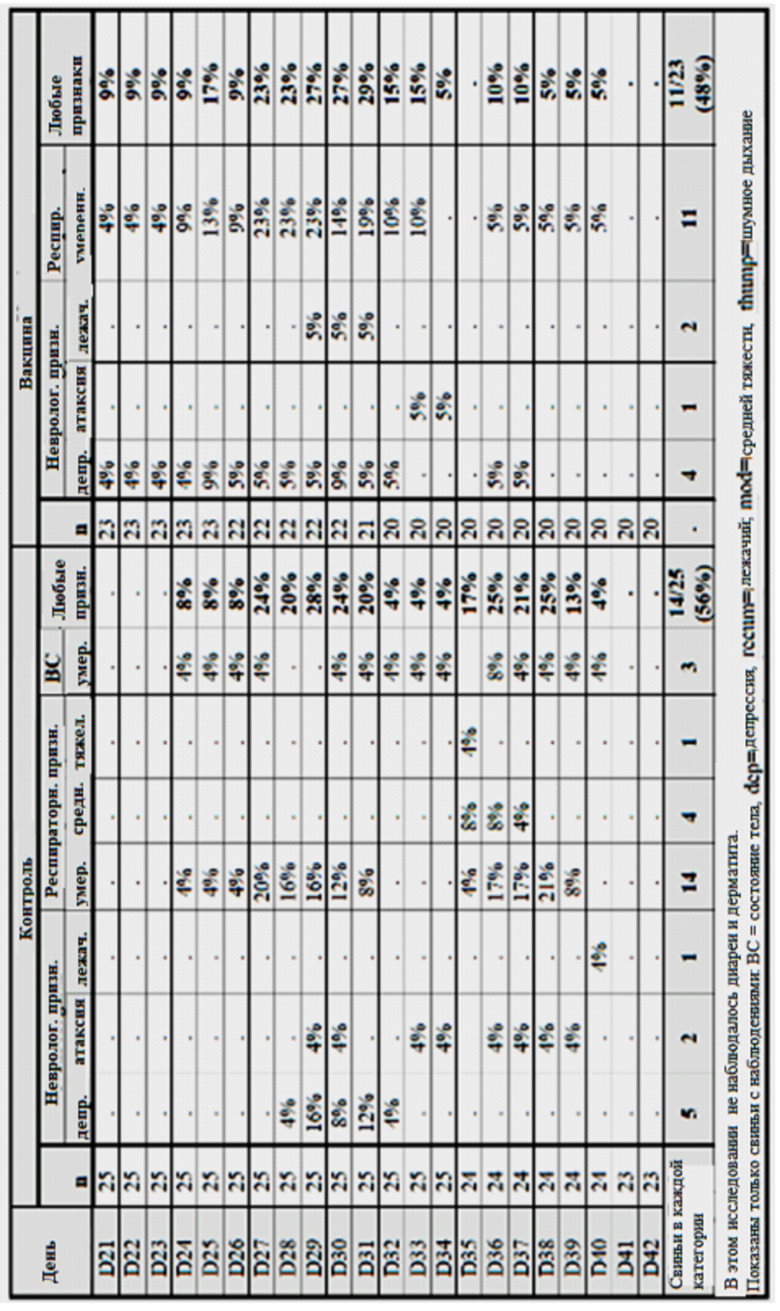
Масса тела: Всех молодых свиней взвешивали перед вакцинацией, перед заражением, через одну неделю после заражения и перед вскрытием трупа. Значения массы тела, рассчитанные по способу наименьших квадратов, у вакцинированной группы были численно (незначительно) больше в каждый момент времени (таблица 129).
Таблица 129
Температура тела: Температуру тела измеряли самокалибрующимся ректальным термометром и с помощью внутрикожных микрочипов. Температуру измеряли три раза перед контрольным заражением, для установления исходного уровня, затем через 2-4 часа после контрольного заражения, и один раз в день до 20-го дня. Средние температуры для опытных групп были в пределах 1°F в каждый из дней сбора (фиг. 28).
Общая оценка поражений: После заражения у всех молодых свиней проводили аутопсию в случае смерти или во время запланированного теста на изъятие (Д42). Исследователь провел патологоанатомическое исследование всех основных систем органов. Были добавлены конкретные патологические описания лимфатических узлов (трахеобронхиальных, наружных паховых, брыжеечных), почек, сердца и легких (таблица 130).
Таблица 130
Нет
Умерен-ный
Средний
Тяжелый
При вскрытии наблюдали очень мало повреждений. Никаких повреждений сердца, почек или кожи (дерматит) не наблюдалось. Мультифокальная гиперемия легких наблюдалась у трех вакцинированных молодых свиней, одна из которых умерла. Комментарии подтвердили, что поражения минимальны (1%). Остальные поражения представляли увеличенные лимфатические узлы у 10/25 контрольных молодых свиней и 14/23 вакцинированных молодых свиней.
Сбор ткани и гистологическая оценка: При вскрытии трупа исследователь забирал образцы мозга (мозжечок), сердца (пораженный участок, в противном случае - поперечный разрез правого и левого желудочков), почки (поперечный разрез), легкого (пораженный участок, в противном случае - добавочную долю), селезенки (поперечный разрез), толстой кишки, тонкой кишки, миндалин, трахеобронхиального лимфатического узла (TBLN), брыжеечного лимфатического узла (MLN) и пахового лимфатического узла (ILN). Все ткани молодых свиней сохраняли в контейнерах, заполненных достаточным количеством 10% забуференного раствора формалина. Через 24 часа в 10% забуференном растворе формалина ткани переносили в 70% этанол и отправляли для подготовки гистологических препаратов в ISU VDL. Образцы тканей обрабатывали для стандартного окрашивания гематоксилином и эозином (H&E). На каждом срезе H&E оценивали наличие поражений или их отсутствие. Если были отмечены отклонения, предоставляли краткое описание морфологического диагноза вместе с оценкой степени тяжести в соответствии с таблицей 131.
Таблица 131
Не наблюдали гистологических повреждений миндалин, TBLN, MLN или селезенки у какой-либо молодой свиньи. Большинство молодых свиней имели по меньшей мере легкие гистологические поражения ILN (таблица 132).
В целом, гистологические поражения головного мозга (таблица 133), почек (таблица 134), сердца (таблица 135) и легких (таблица 136) обычно были легкими, и только 2/25 контрольных молодых свиней имели гистологические поражения кишечника, одна -тонкой кишки (таблица 137) и одна - толстой кишки (таблица 138). Две молодые свиньи с гистологическими поражениями головного мозга были обнаружены мертвыми во время исследования с макроскопическими поражениями в виде менингита (№15 [группа плацебо] - гнойный и лимфоцитарный менингит и № 7 [вакцинированная группа] - бактериальный хронический активный менингит). Четыре молодые свиньи в группе плацебо и две молодые свиньи в вакцинированной группе имели поражения в двух тканях. В целом 92% контрольных молодых свиней имели гистологические нарушения, и 87% вакцинированных молодых свиней имели гистологические нарушения (таблица 139).
Таблица 132. Частота и тяжесть гистологических поражений паховых лимфатических узлов
Таблица 133. Частота и тяжесть гистологических поражений головного мозга
Таблица 134. Частота и тяжесть гистологических поражений почек
Таблица 135. Частота и тяжесть гистологических поражений сердца
Таблица 136. Частота и тяжесть гистологических поражений легких
Таблица 137. Частота и тяжесть гистологических поражений толстой кишки
Таблица 138. Частота и тяжесть гистологических поражений тонкой кишки
Таблица 139. Частота гистологических поражений по группам
Репликацию вируса в тканях вакцинированных и получавших плацебо животных после заражения оценивали с помощью RNAScope. RNAscope позволяет осуществлять специфическую маркировку и визуализацию вирусной мРНК. RNAscope обнаруживает реплицирующийся вирус в ткани, в отличие от иммуногистохимии или ПЦР, которые идентифицируют генетический материал вируса независимо от того, жив ли вирус или мертв. Ткани фиксировали и повышали проницаемость, чтобы обеспечить доступ к зонам-мишеням для вирусной репликации внутри клеток. Затем гибридизовали пару олигонуклеотидных зондов, специфичных к РНК PCV3, так, чтобы они располагались в непосредственной близости друг от друга на РНК-мишени PCV3. Детекция мРНК означает, что вирус PCV3 реплицируется, а не просто обнаруживает генетический материал PCV3. За этим последовала гибридизация молекулы амплификации сигнала (SAM), которая распознает пару специфических олигонуклеотидных зондов. В неспецифических реакциях два зонда не должны располагаться рядом друг с другом, предотвращая их гибридизацию с SAM. Сами SAM конъюгированы с ферментом. Как и в анализах гибридизации in situ, сигналы выявляют с использованием хромогенного субстрата с последующим исследованием слайдов под микроскопом в светлом поле. Слайды для РНК-анализа PCV3 окрашивали, считывали и оценивали в соответствии с таблицей 140.
Таблица 140. Шкала оценки RNAScope
Никаких доказательств репликации PCV3 не наблюдалось ни в каких срезах головного мозга/мозжечка какой-либо молодой свиньи. Почти все контрольные молодые свиньи имели по меньшей мере умеренное окрашивание PCV3 RNAScope в почках (таблица 141), сердце (таблица 142), толстой кишке (таблица 143) и тонкой кишке (таблица 144), в то время как только одна вакцинированная свинья имела слабое окрашивание в каждой из четырех тканей, и три других молодых свиньи имели слабое окрашивание в почках.
Все контрольные молодые свиньи имели окрашивание селезенки от умеренного до среднего (таблица 145) и от умеренного до сильного окрашивания ILN (таблица 146) и легких (таблица 147). Напротив, у шести вакцинированных молодых свиней не было окрашивания при RNAscope ни в одной ткани (в том числе у трех молодых свиней, умерших в фазе заражения). При максимальном окрашивании у молодых свиней с помощью RNAscope 48% контрольных животных имели показатели тяжелой степени, а остальные 52% - средней тяжести, по сравнению с только 9% вакцинированных молодых свиней, имеющей показатели тяжелой степени, и 17% - средней тяжести. Все контрольные молодые свиньи имели по меньшей мере одну ткань с реплицирующимся вирусом PCV3, в то время как 71% вакцинированных молодых свиней имели по меньшей мере одну ткань с реплицирующимся вирусом PCV3 (таблица 148). Существенным результатом исследования является разница между контролем и вакциной при оценке тканей с помощью RNAScope (таблица 149). RNAscope обнаруживает реплицирующийся вирус в ткани, в отличие от иммуногистохимии или ПЦР, которые идентифицируют генетический материал вируса, является ли он живым или мертвым. Поразительно, что все контрольные молодые свиньи имели окрашивание селезенки от умеренного до среднего, а ILN и легких - от умеренного до сильного. Напротив, у шести вакцинированных молодых свиней не было окрашивания с помощью RNAscope ни в одной ткани. Все ткани вакцинированных животных продемонстрировали значительную профилактику инфекции.
Таблица 141. Частота показателей, полученных посредством RNAscope, в почках
Таблица 142. Частота показателей, полученных посредством RNAscope, в сердце
Таблица 143. Частота показателей, полученных посредством RNAscope, в толстой кишке
Таблица 144. Частота показателей, полученных посредством RNAscope, в тонкой кишке
Таблица 145. Частота показателей, полученных посредством RNAscope, в селезенке
Таблица 146. Частота показателей, полученных посредством RNAscope, в паховых лимфоузлах
Таблица 147. Частота показателей, полученных посредством RNAscope, в легких
Таблица 148. Частота показателей по шкале RNAscope
Таблица 149. Статистические сравнения результатов анализа ткани посредством RNAscope
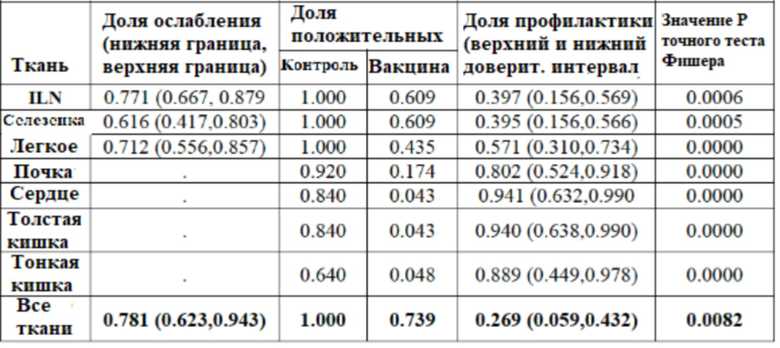
Исследование было признано достоверным на основании того, что контрольные молодые свиньи оставались серонегативными по PCV3 в течение периода вакцинации. Клиническое заболевание проявлялось клиническими признаками снижения функции (неврологической) и увеличением частоты дыхания между 7 и 26 днями после заражения, показателями смертности, привеса, виремии, крупных повреждений, микроскопическими признаками [00653] Статистический анализ данных проводили с использованием SAS версии 9.4 (SAS, Кэри, Северная Каролина / США, SAS Institute, Inc.). Перечни данных и сводные статистические данные по группам лечения были сгенерированы для всех переменных, если это необходимо.
Для аутопсии, гистопатологии, клинических наблюдений, гипертермии и RNAscope PCV3 способы анализа данных варьировали в зависимости от распределения данных для оцениваемой переменной. Как правило, данные анализировали с использованием способов, описанных ниже для доли профилактики (PF) и точного критерия Фишера, и/или доли смягчения (MF). Для некоторых переменных почти все из всех ответов относились к одной категории, поэтому анализ не проводили. Смертность анализировали аналогично, за исключением того, что анализ MF не проводили. Для клинических наблюдений с целью выявления пораженных животных использовали определение случая в течение двух или более дней с отклонениями от нормы клинических наблюдений. Кроме того, с использованием способа MF оценивали количество и продолжительность патологических клинических наблюдений. Что касается гипертермии, животные со значениями температуры на 1 градус или выше исходного уровня были идентифицированы как гиперчувствительные в течение отдельного дня.
Данные, проанализированные с использованием способов PF и точного анализа Фишера, если они еще не были дихотомическими, были разделены для получения бинарного результата (например, нормальный/ненормальный) для каждого животного. Бинарные данные были обобщены по группам с помощью частотного распределения. Кроме того, для бинарных данных был оценен относительный риск (RR) и рассчитан 95% доверительный интервал (CI) с использованием критерия Кохрана - Мантеля - Хэнзеля в процедуре SAS PROC FREQ. Затем RR и связанный CI были переведены в шкалу PF (1 - RR) для представления. Для анализа PROC FREQ использовали стратификацию по помету. Статистическая значимость была достигнута, если 95% доверительный интервал для RR не включал 0. В способе MF использовали стратифицированный подход начальной загрузки с использованием интервала максимальной плотности для построения 95% доверительного интервала для MF на основе распределения начальной загрузки. Стратификацию производили по помету. Статистическая значимость была достигнута, если в доверительном интервале не было 0.
Данные виремии анализировали с использованием обобщенного теста Фридмана (блокирование по помету) для сравнения групповых распределений виремии (количественное) в каждый момент времени после заражения. P-значения меньше 0,05 считаются статистически значимыми.
Вес до вакцинации (день -2) анализировали с использованием линейной смешанной модели по группе (фиксированный эффект), по помету (случайный эффект) и по остатку. Были оценены средние значения наименьших квадратов, и групповые сравнения были оценены с помощью P-значений. При необходимости были построены 95% доверительные интервалы. Массы тела фазы испытания (дни 12, 21, 42) были проанализированы с использованием линейной смешанной модели по группе, дню и взаимосвязи группа/день (фиксированные эффекты), помещению для испытания и станку в помещении для испытания (случайные эффекты) и неструктурированной ковариацией, представляющей собой повторяющиеся измерения на уровне каждого из животных. Были оценены средние значения наименьших квадратов, и сравнения групп были оценены с помощью P-значений по дням исследования. Среднесуточный привес устанавливали и оценивали с использованием линейного контраста условий фиксированного эффекта. При необходимости были построены 95% доверительные интервалы. P-значения меньше 0,05 считаются статистически значимыми.
Экспериментальная вакцина с инактивированным бакуловирусом, экспрессирующим ORF2 PCV3, значительно предотвращала репликацию вируса, выявленную в ILN, селезенке и легких и значительно уменьшала количество реплицирующегося вируса PCV3, обнаруживаемого во всех тканях. Вакцина также численно снизила смертность, клинические признаки, макроскопические поражения и гистологические нарушения в дополнение к численному увеличению массы тела после фазы заражения. Эти данные демонстрируют клинически значимое заболевание, сопоставляя клиническую картину с доказательствами репликации вируса PCV3 в тканях при оценке с помощью RNAscope.
Две контрольные молодые свиньи погибли во время фазы заражения; при аутопсии ни одной из молодых свиней предварительный диагноз не был установлен. Ткани ILN, селезенки и легких обеих молодых свиней имели средние или высокие показатели присутствия PCV3, а почки, сердце, толстый и тонкий кишечник имели показатель PCV3 RNAscope, равный 1. Напротив, три вакцинированных молодой свиньи, умершие после заражения, имели предварительный диагноз бактериальной септицемии или неспособности развиваться, что часто встречается у молодых свиней CDCD. Этот диагноз подтверждается результатами RNAscope, которые были отрицательными для всех тканей, поэтому вакцинированные молодые свиньи, умершие после заражения, не считаются умершими из-за PCV3.
При оценке клинических признаков 14/25 (56%) контрольных молодых свиней прошли клиническое наблюдение после заражения по сравнению с 11/23 (48%) вакцинированными молодыми свиньями. Ограниченное количество клинических признаков соответствует ожиданиям от лабораторной оценки цирковируса. Клинические наблюдения во время этого исследования аналогичны тем, что исторически наблюдались при лабораторной модели заражения PCV2.
Та же самая тенденция наблюдалась с массой тела; по способу наименьших квадратов средняя масса тела вакцинированных была на 0,92 кг больше, чем в контрольной группе, вне теста, что указывает на лучшее общее состояние здоровья (гидратация и аппетит). В то время как до 91% вакцинированных молодых свиней действительно становились виремическими, нагрузка вируса (геномных копий) в крови значительно снижалась примерно на log у вакцинированных в каждый момент времени после заражения (P≤0,0050; фиг.28) по сравнению с контролем. Немногочисленные поражения были обнаружены во время общей оценки вне теста и во время гистологического исследования. Большинство макроскопических поражений представляли собой увеличенные лимфатические узлы (10/25 контрольных молодых свиней и 14/23 вакцинированных молодых свиней), а большинство микроскопических поражений представляли собой умеренные поражения ILN.
RNAScope обнаруживает реплицирующийся вирус в ткани в отличие от иммуногистохимии или ПЦР, которые идентифицируют генетический материал вируса, независимо от того, реплицируется он или мертв. Поразительно, что все контрольные молодые свиньи имели окрашивание селезенки от умеренного до среднего, а ILN и легкого - от умеренного до сильного. Напротив, у шести вакцинированных молодых свиней не было окрашивания RNAScope ни в одной ткани. Все ткани вакцинированных животных продемонстрировали значительную профилактику инфекции (как путем анализа предотвращенной доли, так и анализа гипотез), а ILN, селезенка и легкое также продемонстрировали снижение степени тяжести за счет доли с ослабленными симптомами.
Серологические результаты были отрицательными для всех образцов во все дни. Это может быть связано с коротким интервалом между вакцинацией и контрольным заражением.
Экспериментальная вакцина с инактивированным бакуловирусом, экспрессирующим ORF2 PCV3, значительно предотвращала репликацию вируса, выявляемую в ILN, селезенке и легких, и значительно уменьшала количество реплицирующегося вируса PCV3, обнаруживаемого во всех тканях. Вакцина также численно снизила смертность, клинические признаки, макроскопические поражения и гистологические нарушения в дополнение к численному увеличению массы тела после фазы заражения. Эти данные демонстрируют клинически значимое заболевание, сопоставляя клиническую картину с оценкой и показателем RNAscope. В целом экспериментальная вакцина из убитого бакуловируса, экспрессирующего ORF2 PCV3, оказалась эффективной против PCV3.
Пример 10
Репродуктивное исследование PCV3 у свиноматок после опороса
Фаза вакцинации: в этом исследовании использовали 46 молодых свиней до осеменения (возраст ≥5 месяцев). Все самки были проверены на отсутствие вируса до вакцинации способом кПЦР на следующие агенты: PCV3, PCV2, атипичный пестивирус молодых свиней (APPV), вирус трансмиссивного гастроэнтерита (TGEV), вирус репродуктивного и респираторного синдрома свиней (PRRSV) и парвовирус молодых свиней (PPV). Было также показано, что животные являются серонегативными в отношении гриппа A и M. hyopneumoniae.
Свиньи были разделены на три группы лечения для этого исследования: 1 = отсутствие воздействия и отсутствие заражения PCV3 (NTX), получение плацебо с заражением PCV3, и вакцинация вакциной PCV3 ORF2 с заражением PCV3. Молодых свиней до осеменения вакцинировали на Д0 и Д21 в зависимости от их экспериментальных групп (2 мл внутримышечно в правую сторону шеи). Свиньям в экспериментальной группе NTX вводили вакцину плацебо и содержали отдельно от свинок других экспериментальных групп. Синхронизацию эструса осуществляли введением MATRI™ (альтреногеста) с кормом с 17 по 30 день. На 30 день P.G.600® (сывороточный гонадотропин [PMSG] и хорионический гонадотропин) вводили всем свиньям. Животных оценивали на эструс, и они были осеменены между 35-42 днями. У тридцати шести свиноматок была подтверждена беременность на D77 (D35 беременности), и их использовали в этом исследовании (таблица 150).
Таблица 150. Группы лечения и дизайн исследования
данные помета и аутопсии/сбор ткани/крови
данные помета и аутопсии/сбор ткани/крови
Фаза заражения: всех животных в группах, получавших плацебо и вакцину, заражали гомогенатом ткани, положительным по PCV3, на сроке 40 дней беременности. Гомогенат ткани PCV3 вводили по 2 мл внутримышечно и интраназально каждому животному. Гемоцианин лимфы улитки (KLH), эмульгированный в неполном адъюванте Фрейнда (ICFA), содержащем 1 мг KLH/мл, вводили за два дня до и через два дня после заражения. Гомогенат ткани, использованный для заражения, был проверен на наличие посторонних агентов с помощью количественной ПЦР и глубокого секвенирования.
Виремия: у свиноматок брали сыворотку на протяжении всего исследования и оценивали на виремию с помощью кПЦР (см. таблицу 151 и фиг.28). Цифры, выделенные жирным шрифтом в верхнем ряду таблицы 151, указывают соответствующий день исследования. Номера в таблице 151, выделенные жирным шрифтом, соответствуют измеренному количеству геномных копий PCV3/мл.
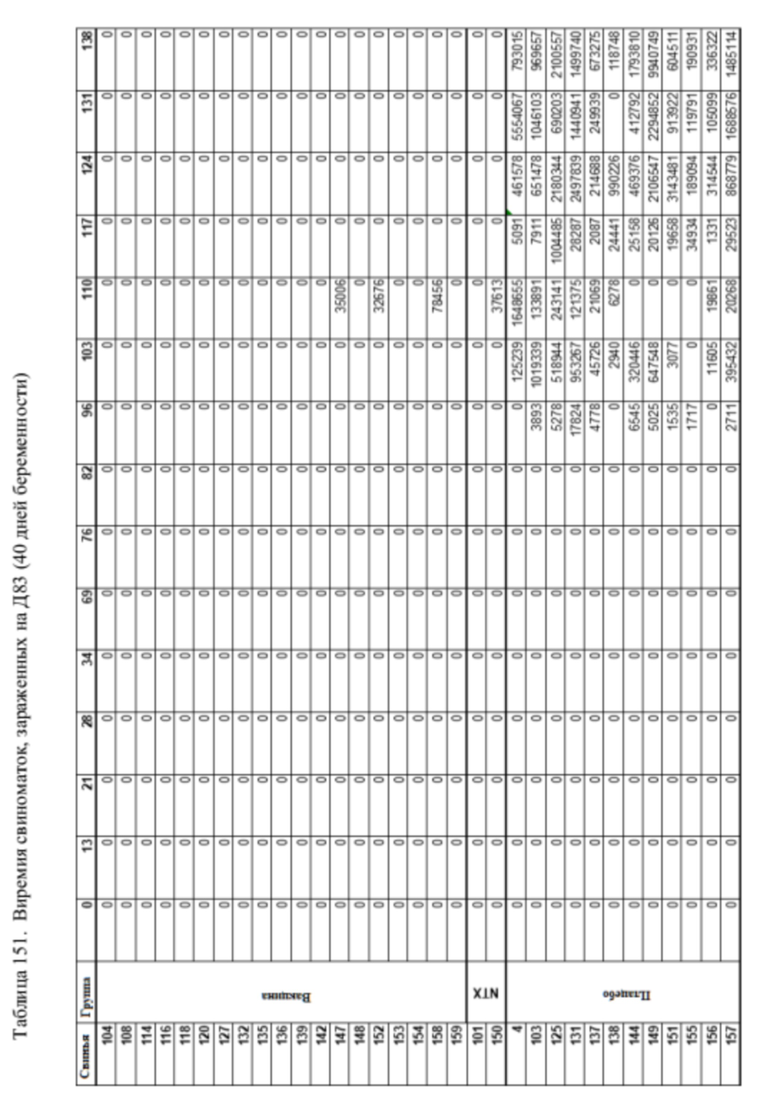
Три молодые свиньи в вакцинированной группе показали виремию на D110. Отсутствие виремии на D103 и D117 может указывать на то, что это показание было либо ложноположительным, либо было эффектом вакцины в отношении подавления репликации вируса. Аналогичным образом, одна из двух свиноматок NTX, не подвергавшихся заражению, показала виремию на D110. Животных NTX содержали отдельно, и отсутствие виремии на D103 и D117 может указывать на то, что эти показания могут быть ложноположительными. Все свиноматки, получавшие плацебо, показали виремию после заражения и продолжали иметь виремию до дня опороса. В целом, данные о виремии у свиноматок показывают, что вакцина способна подавить репликацию вируса у свиноматок.
Клинические признаки: Все молодые свиньи до осеменения были переведены на опорос. Во время опороса поросят определяли как здоровых, мумифицированных, слабых, мертворожденных и подвергшихся аутолизу. Также регистрировали любую смертность от раздавливания в первые три дня после опороса. Процент мумифицированных показан на фиг.30. По одной свиноматке в группах вакцины и плацебо не опоросились.
Согласно фигуре 30, наблюдается явное сокращение количества мумий в группе вакцины по сравнению с группой плацебо. У одной из двух свиноматок в группе NTX был один мумифицированный плод, и у обеих свиноматок был один мертворожденный поросенок.
PCV3 общепризнан репродуктивным заболеванием. В репродуктивном исследовании свиноматок вакцинировали, проводили вторичную иммунизацию и осеменяли, чтобы оценить эффект заражения PCV3. Экспериментальная вакцина с экспрессией инактивированным бакуловирусом ORF2 PCV3, по-видимому, почти полностью исключает репликацию вируса у свиноматок. Более того, при опоросе у вакцинированных свиноматок количество мумий сократилось до менее чем 4%. Это сокращение может иметь значительные экономические последствия для производителей свиней.
Пример 11
Получение мутанта ORF2 PCV3 в петле FG для усиления сборки вирусоподобных частиц
Ряд последовательностей капсида цирковируса выравнивали с капсидом цирковируса молодых свиней 3 типа (PCV3) и двумя последовательностями, по которым были доступны структурные данные: капсидом цирковируса молодых свиней типа 2 (PCV2) и капсидом вируса болезни клюва и пера (BFDV). Оценка выравниваний со структурными данными показала, что, несмотря на расхождение аминокислотных последовательностей капсида между PCV2 и BFDV, расшифрованные структуры были очень похожи. Это позволяет предположить, что структуры капсидов цирковирусов могут быть подобными, несмотря на расхождение их последовательностей (Фиг.31 и 32).
Кроме того, капсид PCV3 был единственной выровненной последовательностью цирковируса, которая содержала большие количества положительного заряда в петле FG, которая находится на поверхности 5-го порядка образования капсида PCV3. Большое количество положительного заряда в этой области может привести к силам отталкивания в отсутствии нуклеиновой кислоты, как и следовало ожидать от вирусоподобных частиц (VLP). Таким образом, лизины и гистидин в этой петле были заменены на аминокислоты из капсида PCV2 (Фиг.32). Эта последовательность была названа PCV3 ORF2 FG (SEQ ID NO: 6).
Последовательность была синтезирована в Genscript и клонирована для рекомбинантных бакуловирусов для оценки экспрессии ORF2 PCV3 и сборки в VLP.
Пример 12
Получение мутанта ORF2 PCV3 в нативном стоп-кодоне и удлинение С-конца для усиленной сборки VLP
Оценка выравниваний со структурными данными, описанными в примере 13, дополнительно показала, что капсид PCV3 имеет самую короткую С-концевую последовательность из всех выровненных последовательностей капсида цирковируса. С-конец капсидных белков PCV2 и BFDV выступает из капсида. Короткая гидрофобная природа С-конца капсида PCV3 может привести к тому, что С-конец будет скрыт в капсиде, и может привести к нестабильности VLP в отсутствии нуклеиновой кислоты. Таким образом, нативный стоп-кодон для капсидного белка PCV3 был подвергнут мутации, и С-конец был удлинен до следующего стоп-кодона в вирусной последовательности (фиг. 33). Эта последовательность была названа PCV3 ORF2 PC (SEQ ID NO: 7).
Последовательность синтезировали в Genscript и клонировали для рекомбинантных бакуловирусов для оценки экспрессии ORF2 PCV3 и сборки в VLP.
Пример 13
Данные о заражении для мутантных кандидатов ORF2 PCV3 у молодых свиней CDCD
Фаза вакцинации. Двадцать пять молодых свиней, рожденных кесаревым сечением, лишенных молозива (CDCD), в возрасте приблизительно 3 недель вакцинируют либо вакциной ORF2 бакуловируса PCV3 с повышенной экспрессией, либо контрольной вакциной, подобранной в качестве плацебо. Пуповинную кровь собирают у всех молодых свиней при родах (кесарево сечение; Д-22). Сыворотку отделяют и тестируют на ДНК PCV3 и ДНК PCV2 с помощью ПЦР. На D-2 у всех молодых свиней берут кровь для сбора сыворотки, а затем вакцинируют PCV2 Ingelvac CircoFLEX®.
Фаза заражения: всех животных заражают гомогенатом ткани, положительным по PCV3, через 14 дней после вакцинации. Гемоцианин лимфы улитки (KLH), эмульгированный в неполном адъюванте Фрейнда (ICFA), содержащем 1 мг KLH/1 мл, вводят за два дня до и через два дня после заражения (таблица 152). Гомогенат ткани, используемый для заражения, проверяют на посторонние агенты с помощью КПЦР и глубокого секвенирования. Животных умерщвляют на 42-й день. При аутопсии собирают ряд тканей, включая мозг, сердце, почки, легкие, селезенку, толстую кишку, миндалины, трахеобронхиальный лимфатический узел (TBLN), мезентериальный лимфатический узел (MLN) и внешний подвздошный лимфатический узел (ILN).
Таблица 152. Дизайн исследования
Лабораторная фаза
Виремия: Виремию после заражения вакцинированных и контрольных животных оценивают с помощью количественной ПЦР. После заражения все контрольные молодые свиньи являются виремическими. Нагрузка по виремии (количество геномных копий/мл) полностью исключена у вакцинированных.
Клинические признаки: Репликацию вируса в тканях вакцинированных и получавших плацебо животных после заражения оценивают с помощью RNAScope. RNAScope - это недавно разработанная технология, которая позволяет специально маркировать и визуализировать вирусную мРНК. RNAScope обнаруживает реплицирующийся вирус в ткани, в отличие от иммуногистохимии или ПЦР, которые идентифицируют генетический материал вируса, независимо от того, живой он или мертвый. Ткани фиксируют и пермеабилизуют, чтобы обеспечить доступ к зонам-мишеням для вирусной репликации внутри клеток. Затем гибридизуют пару олигонуклеотидных зондов, специфичных к РНК PCV3, так, чтобы они располагались в непосредственной близости друг от друга на РНК-мишени PCV3. (Детекция матричной РНК означает репликацию вируса PCV3, а не только обнаружение генетического материала PCV3). За этим следует гибридизация молекулы амплификации сигнала (SAM), которая распознает пару специфических олигонуклеотидных зондов. В неспецифических реакциях два зонда не располагаются рядом друг с другом, предотвращая их гибридизацию с SAM. Сами SAM конъюгированы с ферментом. Как и в анализах гибридизации in situ, сигналы обнаруживают с использованием хромогенного субстрата с последующим исследованием слайдов под микроскопом в светлом поле. Слайды для анализа PCV3 RNAscope окрашивают, окрашенные слайды считывают и оценивают (таблица 153).
Таблица 153. Шкала оценки RNAScope
Никаких доказательств репликации PCV3 не наблюдается ни в каких участках головного мозга/мозжечка какой-либо молодой свиньи. Почти у всех контрольных молодых свиней отмечается по меньшей мере слабое окрашивание RNAscope PCV3 в почках, сердце, толстой и тонкой кишке. За исключением одной молодой свиньи, ни у одной из других вакцинированных молодых свиней не обнаруживается окрашивания исследуемых тканей.
Экспериментальная инактивированная бакуловирусная вакцина с повышенной экспрессией ORF2 PCV3 значительно предотвращает репликацию вируса в ILN, селезенке и легких, и значительно снижает количество выявленного реплицирующегося вируса PCV3 во всех тканях. Вакцина также численно снижает смертность, клинические признаки, макроскопические поражения и гистологические нарушения в дополнение к численному повышению массы тела после фазы заражения. В целом показано, что экспериментальный бакуловирус с повышенной экспрессией ORF2 PCV3 эффективен против PCV3.
Пример 14
Данные о тестировании мутантных кандидатов ORF2 PCV3 на репродуктивной модели
Фаза вакцинации: в этом исследовании использовали 46 молодых свиней до размножения (возраст ≥5 месяцев). Все самки проходили скрининг в Ветеринарно-диагностической лаборатории Университета штата Айова (ISU-VDL) на предмет отсутствия виремии до вакцинации способом кПЦР на следующие агенты: PCV3, PCV2, атипичный пестивирус молодых свиней (APPV), вирус трансмиссивного гастроэнтерита (TGEV), вирус репродуктивного и респираторного синдрома свиней (PRRSV) и парвовирус молодых свиней (PPV). Также было показано, что животные являются серонегативными в отношении гриппа A и M. hyopneumoniae, что подтверждается ISU-VDL.
Молодых свиней до осеменения вакцинировали на Д0 и Д21 в зависимости от их экспериментальных групп. Свиньям NTX вводили вакцину плацебо. Синхронизацию эструса осуществляли введением MATRI™ (альтреногеста) с кормом с 17 по 30 день. На 30 день всем свиньям давали P.G.600. Животных оценивали на эструс и осеменяли между 35-42 днями. У 36 свиноматок была подтверждена беременность на Д77 (Д35 беременности), и они были использованы этом исследовании (таблица 154).
Таблица 154. Дизайн исследования с указанием групп лечения
Данные помета и аутопсии/сбор ткани/крови
Данные помета и аутопсии/сбор ткани/крови
Фаза заражения: всех животных заражали гомогенатом ткани, положительным по PCV3, через 40 дней беременности. Гемоцианин лимфы улитки (KLH), эмульгированный в неполном адъюванте Фрейнда (ICFA), содержащем 1 мг KLH/1 мл, вводили за два дня до и через два дня после контрольного заражения. Гомогенат ткани, использованный для заражения, был проверен на наличие посторонних агентов с помощью количественной ПЦР и глубокого секвенирования.
Лабораторная фаза
Виремия: у свиноматок брали сыворотку на протяжении всего исследования и оценивали на виремию с помощью количественной ПЦР.
Ни у одной из вакцинированных молодых свиней не обнаружено виремии ни в одном из образцов, взятых после заражения. У всех молодых свиней из групп NTX и плацебо виремия начиналась через неделю после заражения и продолжалась в течение 3-5 недель после заражения. В целом, данные о виремии у свиноматок показывают, что вакцина способна подавить репликацию вируса у свиноматок.
Клинические признаки: Все свинки были отправлены на опорос. При опоросе поросят определяли как здоровых, мумифицированных, слабых, мертворожденных и подвергшихся аутолизу. Также регистрировали любую смертность от раздавливания в первые три дня после опороса.
Наблюдается явное и значительное снижение общего количества мумий в группе вакцины по сравнению с группой плацебо. Аналогичное снижение количества мертворожденных и слабых молодых свиней наблюдается в группе вакцинированных по сравнению с группой плацебо и NTX. Кроме того, данные RNAScope по тканям указывают на значительное сокращение до полного прекращения репликации вируса в тканях вакцинированных свиноматок и молодых свиней по сравнению с тканями из групп NTX и плацебо.
PCV3 общепризнан репродуктивным заболеванием. На репродуктивной модели свиноматок вакцинируют, проводят повторную иммунизацию и осеменяют для оценки эффекта заражения PCV3. Вакцинированные животные (свиноматки и поросята) также демонстрируют снижение или устранение репликации вируса в исследуемых тканях. Экспериментальная вакцина с повышенной экспрессией инактивированным бакуловирусом ORF2 PCV3, по-видимому, почти полностью исключает репликацию вируса у свиноматок. Более того, при опоросе у вакцинированных свиноматок наблюдалось значительное сокращение количества мумий. Это сокращение может иметь значительные экономические последствия для производителей свиней.
PCV3 в комбинации с PPV
Здесь следует упомянуть WO2018/083156, раскрытие которой включено посредством ссылки.
Целью этого исследования является оценка появления иммунитета от раскрытой здесь вакцины против PCV3 (исследуемый вакцинный продукт 1 (далее именуемый «IVP1»)) при использовании в комбинации с субъединичной вакциной против парвовируса свиней, как описано в примерах, в частности полученных в соответствии с примерами 1 и 2 из WO2018/083156 (далее обозначаются как «IVP2»), и где эта смесь IVP1 и IVP2 также именуется «IVP2/IVP1» здесь и в дальнейшем.
Это исследование включает 60 молодых свиней, полученных путем кесарева сечения, лишенных молозива (CDCD), серонегативных по PCV3 и PPV, из которых 30 были вакцинированы смесью IVP2/IVP1, а 30 (контрольная группа) получали стерильный разбавитель (вода для инъекций) в возрасте 3 недель (т.е. в день исследования 0 (D0)) с последующим заражением PCV3 на D14.
Вакцинация IVP2/IVP1 приводит к значительному увеличению числа молодых свиней, серопозитивных по PCV3, виремии и данным RNAscope. К Д42 все молодой свиньи группы IVP2/IVP1 являются серопозитивными по PVC3, в то время как в контрольной группе значительно меньше молодых свиней являются позитивными.
После оценки параметров первичного результата вакцинация IVP2/IVP1 значительно снижает и/или устраняет виремию у вакцинированных. Кроме того, общий уровень гистологических нарушений, определяемый при окрашивании H&E, является более выраженным в контрольной группе, причем значительно больше молодых свиней имеют показатели средней и высокой тяжести по меньшей мере в одной категории оценки поражения, тогда как значительно меньшее количество вакцинированных молодых свиней имеют средний балл поражения, ни один из которых не был высоким. Что еще более важно, на гистологическом уровне, определяемом окрашиванием вирус-специфическим RNAScope, вакцина способна предотвращать или уменьшать репликацию вируса в тканях, включая, помимо прочего, сердце, почки, легкие, кишечник и нервную ткань.
В заключение, IVP1, используемый в сочетании с IVP2, обеспечивает эффективную активную иммунизацию 3-недельных молодых свиней CDCD при заражении вирулентным PCV3 на 14 день после вакцинации.
Пример 16
PCV3 в комбинации с PPV и PRRSV
Здесь следует упомянуть WO2018/083156 и WO2012/110489, раскрытие которых включено посредством ссылки.
Целью этого исследования с вакцинацией и заражением является предоставление данных о связанном использовании раскрытой здесь вакцины PCV3 и описанной выше (в примере 15, со ссылкой на WO2018/083156) парвовирусной субъединичной вакцины IVP2 (IVP1/IVP2, как описано выше) с вакциной MLV PRRS (указанная MLV PRRS депонирована в Европейской коллекции клеточных культур (ECACC) под номером доступа ECACC 1 1012502), описанной в примерах WO2012/110489 (названной «IVP3», и далее эта смесь обозначается как «IVP1/IVP2/IVP3» у 5-6-месячных молодых свиней.
Двадцать семь молодых свиней до осеменения получали из стада, ранее показавшего отрицательные результаты по PCV3, без предыдущего заболевания или вакцинации против PCV3. Молодых свиней произвольно распределяли на 3 экспериментальных группы, из которых n = 9 получали вакцинацию в Д0 и вторичную иммунизацию вакциной в Д21: T1 - отрицательный контроль, T2 - IVP1/IVP2/IVP3, Т3 – не получавшие лечения контрольные молодые свиньи (NTX), каждую группу размещали отдельно.
Молодых свиней вакцинировали, осеменяли и определяли беременность. примерно на 40-й день беременности (dG) всех молодых свиней инокулировали контрольным штаммом PCV3 (как описано в настоящей заявке). У молодых свиней брали кровь еженедельно, за исключением периодов синхронизации и осеменения (Д35 - Д70), и анализировали сыворотку.
Свиньям давали опороситься, и пометы исследовали на наличие мумий, мертворожденных и слабых поросят. В целом у вакцинированных молодых свиней и свиноматок не наблюдалось, или наблюдалось значительно меньшее количество мумий, мертворожденных и слабых пометов по сравнению с контролем или группами NTX.
При обследовании на виремию, в отличие от контрольных групп, у молодых свиней Т2 обнаруживается полное прекращение виремии после заражения. В заключение следует отметить, что комбинированная вакцина IVP1/IVP2/IVP3 эффективна для предотвращения виремии и инфекции PCV3 у плодов на 40dG.
При гистологическом анализе молодой свиньи Т2 способны предотвращать репликацию вируса в ключевых тканях после заражения. У контрольных молодых свиней/ свиноматок и в пометах наблюдается значительная репликация вируса и, следовательно, клиническое проявление PCV3. Это обнаруживается при окрашивании H&E и анализа вируса посредством RNAScope, которые обнаруживают репликацию вирусной мРНК в клетках и тканях. В заключение, комбинированная вакцина IVP1/IVP2/IVP3 эффективна для предотвращения клинических признаков заражения PCV3 молодых свиней, свиноматок и плодов на 40dG.
После подробного описания предпочтительных вариантов осуществления настоящего изобретения следует понимать, что изобретение, определенное в приведенных выше параграфах, не должно ограничиваться конкретными деталями, изложенными в приведенном выше описании, так как многие очевидные его вариации возможны без выхода за рамки сущности или объема настоящего изобретения.
Также в данном описании раскрыты следующие пункты:
1. Композиция, содержащая белок ORF2 цирковируса молодых свиней 3 типа (PCV3).
2. Композиция по п.1, дополнительно содержащая ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизирующего агента, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии и иммуномодулирующего агента, или любой их комбинации.
3. Композиция, в частности композиция по пп.1 или 2, содержащая: белок ORF2 цирковируса молодых свиней 3 типа (PCV3), и ветеринарно приемлемый носитель, включающий растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, и иммуномодулирующий агент или любую их комбинацию.
4. Композиция по любому из пп.1-3, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
5. Композиция по любому из пп.1-4, где ветеринарно приемлемый носитель включает адъювант.
6. Композиция по любому из пп.1-5, где PCV3 выбран из любой филогенетической ветви PCV3 или комбинации филогенетических ветвей, или группы, состоящей из PCV3a и PCV3b.
7. Композиция по любому из пп.1-6, где PCV3 представляет собой любую филогенетическую ветвь PCV3, или выбран из группы, состоящей из PCV3a1, PCV3b1, PCV3b2 и PCV3c.
8. Композиция по любому из пп.1-7, где ORF2 PCV3 относится к группе a1, b1 или b2.
9. Композиция по любому из пп.1-8, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1.
10. Композиция по любому из пп.1-9, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, имеющей по меньшей мере 90% идентичности последовательности с последовательностью SEQ ID NO: 4.
11. Композиция по любому из пп.1-10, где белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3.
12. Композиция по любому из пп.1-11, где белок ORF2 PCV3 представляет собой рекомбинантный белок ORF2 PCV3 в результате его экспрессии вектором экспрессии, содержащий полинуклеотидную последовательность, кодирующую белок ORF2 PCV3.
13. Композиция по п.12, где вектор экспрессии представляет собой бакуловирус.
14. Композиция по любому из пп.1-13, где белок ORF2 PCV3 представляет собой экспрессируемый бакуловирусом рекомбинантный ORF2 PCV3.
15. Композиция по любому из пп.1-14, дополнительно содержащая белок ORF2 PCV2, предпочтительно антигенный белок ORF2 PCV2 (антиген ORF2 PCV2).
16. Композиция по п.15, где белок ORF2 PCV2 получен при экспрессии вектором экспрессии, содержащим полинуклеотидную последовательность, кодирующую белок ORF2 PCV2.
17. Композиция по п.16, где вектор экспрессии представляет собой бакуловирус.
18. Композиция по любому из пп.1-17, дополнительно содержащая дополнительный антиген дополнительного патогена свиней.
19. Композиция по п.18, в которой дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы молодых свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV) или антиген Pasteurella multocida, или их комбинацию.
20. Композиция по любому из пп.1-19, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
21. Композиция по любому из пп.1-20, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
22. Композиция по любому из пп.2-21, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый с полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, а ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, или изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/ капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитол олеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; Блок-сополимер; SAF-М; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
23. Композиция по любому из пп.2-22, содержащая примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл в дозе композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
24. Композиция по любому из пп.2-23, где иммуномодулирующий агент включает интерлейкин (интерлейкины), интерферон (интерфероны) или другой цитокин (цитокины).
25. Композиция по любому из пп.1-24, содержащая примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика (антибиотиков).
26. Композиция по любому из пп.1-25, где антибиотик (антибиотики) включает гентамицин.
27. Композиция по любому из пп.1-26, содержащая (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, экспрессирующим указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в количествах, эквивалентных инактивирующему агенту или BEI; (vi) адъювант, или адъювант, включающий Карбопол, или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
28. Композиция по п.27, где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят до примерно 6,5-7,5.
29. Композиция по пп.27 или 28, где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или примерно 5 мМ BEI, и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
30. Композиция по любому из пп.1-29, где указанная композиция составлена и/или упакована для однократного применения одной дозы или однократной иммунизации композицией, а не для режима множественных доз, или где указанная композиция составлена и/или упакована для режима приема нескольких доз композиции, или где указанная композиция составлена и/или упакована для двукратного введения дозы или двукратной иммунизации композицией.
31. Композиция по любому из пп.1-30, которая является иммуногенной композицией.
32. Композиция по любому из пп.1-31 для применения в качестве лекарственного средства.
33. Композиция по любому из пп.1-31 для применения в качестве вакцины.
34. Композиция по любому из пп.1-31 для применения в способе индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3 и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
35. Композиция по любому из пп.1-31 для применения в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у животного, или для применения в способе лечения или профилактики инфекции PCV3 у животного, причем указанное животное предпочтительно представляет собой молодую свинью.
36. Композиция по любому из пп.1-31 для применения в способе индукции иммунного ответа против PCV3 у этой молодой свиньи, в частности, предпочтительно у беременной свиноматки.
37. Композиция по любому из пп.1-31 для применения в способе уменьшения или предотвращения клинических признаков или заболевания, вызванного инфекцией PCV3 у поросят, при этом поросенок должен получать вскармливание свиноматкой, у которой применяли композицию.
38. Композиция для применения по п.37, где указанная свиноматка, у которой применяли композицию, представляет собой свиноматку, которой вводили иммуногенную композицию, когда указанная свиноматка была беременна, в частности, указанным поросенком, или подсвинка до осеменения.
39. Композиция для применения по любому из пп.32-38, предназначенная для введения внутримышечно или интрадермально.
40. Композиция для применения по любому из пп.36-39, предназначенная для введения указанной свиноматке внутримышечно или интрадермально.
41. Способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против (i) PCV3, и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, включающий введение животному композиции, указанной в любом из пп.1-31.
42. Способ по п. 41, где животное представляет собой свинью.
43. Способ по п. 42, где свинья представляет собой молодую свинью, или поросенка.
44. Способ по п. 42 или 43, где свинья представляет собой свиноматку.
45. Способ иммунизации субъекта, включающий введение субъекту композиции по любому из пп.1-31.
46. Способ иммунизации молодых свиней против клинического заболевания, вызванного по меньшей мере одним патогеном у указанного животного, включающий стадию введения животному композиции по любому из пп.1-31, при этом указанная иммуногенная композиция не вызывает клинических признаков инфекции, но способна вызывать иммунный ответ, который иммунизирует животное против патогенных форм указанного по меньшей мере одного патогена.
47. Способ по п.46, где указанным по меньшей мере одним патогеном является PCV3.
48. Способ индукции выработки антител, специфичных для PCV3 у свиноматки, включающий введение указанной свиноматке композиции по любому из пп.1-31.
49. Способ уменьшения или предотвращения клинических признаков или клинических симптомов, вызванных инфекцией PCV3 у поросят, включающий введение композиции по любому из пп.1 по 31 свиноматке и обеспечение кормления указанной свиноматкой указанного поросенка.
50. Способ по п.49, где указанная свиноматка является беременной свиноматкой, в частности, указанным поросенком, или является подсвинком до осеменения.
51. Способ по пп.49 или 50, включающий этапы введения композиции по любому из пп.1-31 свиноматке, беременной указанным поросенком, рождения указанной свиноматкой указанного поросенка и вскармливания указанного поросенка указанной свиноматкой.
52. Способ уменьшения клинических признаков и/или клинических симптомов, вызванных инфицированием PEDV у поросят, при котором поросенок должен получать вскармливание свиноматкой, которой вводили композицию по любому из пп.1-31.
53. Способ по любому из пп.45-52, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят внутримышечно или интрадермально указанной свиноматке.
54. Способ по любому из пп.45-53, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят дважды указанной свиноматке.
55. Способ по любому из пп.45-54, где указанную иммуногенную композицию, или указанную вакцину или фармацевтическую композицию вводят дважды через слизистую оболочку, предпочтительно дважды интраназально, указанной свиноматке.
56. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где указанные клинические признаки выбраны из группы, состоящей из снижения среднесуточного привеса и смертности.
57. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические признаки выбраны из группы, состоящей из выталкивания мумифицированного, мертворожденного и/или слабого плода.
58. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические симптомы выбраны из группы, состоящей из макроскопических повреждений, гистологических нарушений, репликации PCV3 в ткани и виремии PCV3.
59. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где клинические симптомы выбраны из группы, состоящей из развития или производства мумифицированного, мертворожденного и/или слабого плода.
60. Композиция для применения по любому из пп.32-40 или способ по любому из пп.41-55, где свинья или поросенок имеет возраст не старше 15 недель, или не старше 6 недель, или не старше 3 недель, или не старше 2 недель, или не старше 1 недели.
61. Способ по п. 60, где введение осуществляют в течение по меньшей мере 1, 2 или 3 недель после контакта с вирулентным цирковирусом молодых свиней.
62. Композиция для применения по любому из пп.32-41 или способ по любому из пп.42-55, где введение включает введение путем однократного введения одной дозой или однократное применение одной дозы композиции; а не режим многократной вакцинации или многократного введения, или где введение состоит из однократной вакцинации одной дозой или однократного введения одной дозы; а не из режима многократной вакцинации или многократного введения дозы, или где введение включает режим многократной вакцинации или многократного введения дозы композиции, или где введение включает режим двукратной вакцинации или двукратного введения дозы композиции, или где введение состоит из режима двукратной вакцинации или режима введения двух доз композиции.
63. Использование композиции по любому из пп.1-31 в способе по любому из пп. 42-55, или использование белка ORF2 PCV3, отдельно или в комбинации, с любой из композиций по пп.1-31, для применения при приготовлении композиции для индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3, и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней, или для применения в способе индукции иммунологического или иммунного ответа, или защитного иммунного или иммунологического ответа против (i) PCV3, и/или (ii) PCV2 и PCV3, и/или (iii) PCV3 и другого патогена свиней, и/или (iv) PCV3, PCV2 и другого патогена свиней.
64. Способ приготовления композиции по любому из пп.1-31, включающий получение белка ORF2 PCV3 с помощью бакуловирусной системы экспрессии в культивируемых клетках насекомых.
65. Способ по п.64, включающий инактивацию бакуловируса.
66. Способ по п.65, где инактивация включает тепловую обработку или использование агента, инактивирующего вирус.
67. Способ по п.66, где агент, инактивирующий вирус, включает азиридиновое соединение.
68. Способ по п.67, где азиридиновое соединение включает BEI.
69. Рекомбинантный вектор, содержащий полинуклеотидную последовательность, кодирующую полипептидную последовательность, кодирующую белок ORF2 PCV3.
70. Рекомбинантный вектор по п.69, где ORF2 PCV3 относится к группе a1, b1 или b2.
71. Композиция, содержащая (i) белок ORF2 цирковируса молодых свиней 3 типа (PCV3), белок парвовируса (PPV), и при необходимости белок PRRSV (вируса респираторного и репродуктивного синдрома свиней), и (ii) ветеринарно приемлемый носитель, выбранный из группы, состоящей из растворителя, дисперсионной среды, покрытия, стабилизатора, разбавителя, консерванта, противомикробного агента, противогрибкового агента, изотонического агента, агента, замедляющего адсорбцию, адъюванта, надосадочной жидкости клеточной культуры, стабилизирующего агента, вирусного вектора, вектора экспрессии и иммуномодулирующего средства, или любой их комбинации.
72. Композиция по п.71, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
73. Композиция по пп.71 или 72, где белок PPV представляет собой капсидный белок PPV VP2.
74. Композиция по любому из пп.71-73, где белок PRRSV представляет собой ORF4, ORF5, ORF6 или ORF7 вируса PRRS.
75. Композиция по пп.73 или 74, где белок PPV и/или белок PRRSV экспрессируется в векторе.
76. Композиция по любому из пп.71-75, представляющая собой иммуногенную композицию, вводимую в двух дозах свинье.
77. Композиция по п.76, где свинья является молодой свиньей до первого опороса или свиноматкой.
78. Композиция по пп.76 или 77, где введение осуществляют до спаривания/ осеменения, до беременности, во время беременности или во время лактации.
79. Композиция по любому из пп.76-78, где иммуногенная композиция содержит от 0,1 мкг до 150 мкг, предпочтительно от 0,25 мкг до 75 мкг, более предпочтительно от 0,5 мкг до 37,5 мкг, еще более предпочтительно от 0,5 мкг до 15 мкг, наиболее предпочтительно от 0,5 мкг до 6 мкг антигена PCV3, PPV и/или PRRSV.
80. Композиция по любому из пп.76-79, где иммуногенную композицию вводят внутримышечно.
81. Способ индукции иммунного ответа или иммунологического ответа, или защитного иммунного или иммунологического ответа против цирковируса свиней 3 (PCV3), включающий парентеральное или подкожное применение у свиней однократной вакцинации, однократного введения или однократной дозы (i) по меньшей мере от 2 мкг до примерно 400 мкг рекомбинантного белка ORF2 PCV3, экспрессируемого бакуловирусной системой, и (ii) ветеринарно приемлемого носителя, содержащего растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, и иммуномодулирующий агент, или любую их комбинацию.
82. Способ по п.81, где свинья представляет собой поросенка, молодую свинью, или свиноматку, или подсвинка до осеменения.
83. Способ по пп.81 или п. 82, где свинья имеет возраст примерно 1 неделю, или 2 недели, или 3 недели, или 7-28, или 7-22, или 14-22, или 16-22, или 21±5 дней.
84. Способ по любому из пп.81-83, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии, или любую их комбинацию.
85. Способ по любому из пп.81-84, где ORF2 PCV3 происходит из любой филогенетической ветви PCV3 или комбинации филогенетических ветвей, или группы PCV3a, PCV3a1, PCV3b, PCV3b1 или PCV3b.
86. Способ по любому из пп.81-85, где белок ORF2 PCV3 содержит или состоит из аминокислотной последовательности, кодируемой полинуклеотидной последовательностью, имеющей по меньшей мере 90%, или по меньшей мере 91%, или по меньшей мере 92%, или по меньшей мере 93%, или по меньшей мере 94%, или по меньшей мере 95%, или по меньшей мере 96%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% идентичности последовательности с SEQ ID NO: 1 или гомологии последовательности с SEQ ID NO: 1, SEQ ID NO: 6 или SEQ ID NO: 7.
87. Способ по любому из пп.81-86, где однократная вакцинация, однократное введение или однократная доза дополнительно включает белок ORF2 PCV2 или дополнительный антиген дополнительного патогена свиней.
88. Способ по п.87, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV) или антиген Pasteurella multocida, или их комбинацию.
89. Способ по любому из пп.81-88, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенными ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитол олеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; Блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
90. Способ по любому из пп.81-89, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
91. Способ по п.87, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
92. Способ по любому из пп.81-91, включающий примерно от 50 мкг до примерно 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл в дозе композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
93. Способ по любому из пп.82-92, где иммуномодулирующий агент включает интерлейкин, интерферон или другой цитокин.
94. Способ по любому из пп.81-93, где однократная вакцинация, однократное введение или однократная доза дополнительно включает примерно от 1 мкг/мл до 60 мкг/мл антибиотика (антибиотиков) или менее примерно 30 мкг/мл антибиотика.
95. Способ по п. 84, где антибиотик включает гентамицин.
96. Способ по любому из пп.81-95, где однократная вакцинация, однократное введение или однократная доза включает (i) белок ORF2 PCV3, (ii) по меньшей мере часть бакуловируса, экспрессирующего указанный белок ORF2 PCV3, (iii) часть культуры клеток, которые были инфицированы или трансфицированы рекомбинантным бакуловирусом, экспрессирующим указанный белок ORF2 PCV3, (iv) инактивирующий агент, или инактивирующий агент, содержащий бинарный этиленимин (BEI), (v) тиосульфат натрия, или тиосульфат натрия в эквивалентных количествах для инактивирующего агента или BEI; (vi) адъювант, или адъювант, содержащий Карбопол или Карбопол 971, и (vii) фосфатную соль в физиологически приемлемой концентрации.
97. Способ по п.96, где примерно 90% компонентов (i) - (iii) имеют размер менее 1 мкм, а pH указанной композиции доводят до примерно 6,5-7,5.
98. Способ по пп.96 или 97, где BEI получен из культуры клеток, обработанной примерно от 2 до 8 или примерно 5 мМ BEI для инактивации бакуловируса, и/или композиция содержит примерно от 2 до 8 или около 5 мМ BEI и/или композиция содержит примерно 1 мг Карбопола или Карбопола 971.
99. Способ по любому из пп.81-98, дополнительно включающий уменьшение или предотвращение клинических признаков или заболевания, вызванного инфекцией PCV3 или вирусом эпидемической диареи молодых свиней (PEDV), у беременной свиноматки или поросенка.
100. Способ по п.99, где уменьшение или предотвращение клинических признаков или заболевания у молодых свиней включает кормление поросенка свиноматкой, у которой применяли введение путем однократного введения, однократное введение или однократную дозу.
101. Способ по п.99, где уменьшение или предотвращение клинических признаков или заболевания у молодых свиней в ключает введение путем однократного введения, однократное введение или однократную дозу у беременной свиноматки.
102. Способ по п.101, дополнительно включающий вскармливание поросенка свиноматкой после того, как свиноматка родила поросенка.
103. Способ по любому из пп.99–102, где клиническим признаком является снижение среднесуточного привеса, смертность, развитие, производство или выталкивание мумифицированного, мертворожденного и/или слабого плода, макроскопическое поражение, гистологическое нарушение, репликация PCV3 в ткани или виремия PCV3.
104. Способ по любому из пп.81-103, где парентеральное или подкожное введение является внутримышечным или интрадермальным.
105. Неприродный белок ORF2 PCV3, включающий сконструированную петлю FG, где петля FG содержит три или менее положительно заряженных аминокислоты.
106. Белок ORF2 PCV3 по п.105, где петля FG содержит две положительно заряженные аминокислоты.
107. Белок ORF2 PCV3 по п.105, где петля FG содержит одну положительно заряженную аминокислоту.
108. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют положительно заряженные аминокислоты.
109. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют остатки аргинина и лизина.
110. Белок ORF2 PCV3 по п.105, где в петле FG отсутствуют остатки аргинина, лизина и гистидина.
111. Белок ORF2 PCV3 по п.105, где петля FG содержит QPFSYH, LSRGF или MASGF.
112. Неприродный белок ORF2 PCV3, содержащий сконструированное С-концевое удлинение.
113. Белок ORF2 PCV3 по п.112, где С-концевое удлинение включает примерно от 1 до 10, примерно от 5 до 20 или примерно от 10 до 30 аминокислот.
114. Белок ORF2 PCV3 по п.112, где С-концевое удлинение включает примерно от 1 до 10, или примерно от 5 до 20, или примерно от 10 до 30 аминокислот, примерно от 50 до 200 аминокислот, примерно от 60 до 190 аминокислот, примерно от 70 до 180 аминокислот, примерно от 80 до 170 аминокислот, примерно от 90 до 160 аминокислот или примерно от 100 до 150 аминокислот.
115. Белок ORF2 PCV3 по п.112, где С-концевое удлинение содержит С-концевые аминокислоты из другого капсидного белка.
116. Белок ORF2 PCV3 по п.115, где C-концевое удлинение включает C-концевые аминокислоты из капсида PCV2, в виде капсида BFDV или капсида CaCV.
117. Белок ORF2 PCV3 по п.112, где С-концевое удлинение включает EFNLKDPPLN, PK или QFAPNNPSTEFDYETGRQL.
118. Способ получения самособирающегося капсидного белка ORF2 PCV3, который включает замену одной или нескольких аминокислот аргинина, лизина или гистидина в петле FG на незаряженные положительно аминокислоты.
119. Способ усиления самосборки капсидного белка ORF2 PCV3, который включает добавление или вставку аминокислотных остатков на С-конце белка.
120. Способ по п.118, включающий добавление или вставку от 1 до 10, или примерно от 5 до 20, или примерно от 10 до 30 аминокислот, примерно от 50 до 200 аминокислот, примерно от 60 до 190 аминокислот, примерно от 70 до 180 аминокислот, примерно от 80 до 170 аминокислот, примерно от 90 до 160 аминокислот или примерно от 100 до 150 аминокислот.
121. Способ по п.119, включающий добавление или вставку аминокислот из другого капсидного белка.
122. Способ по п.121, где добавленные или вставленные аминокислоты происходят из капсида PCV2, в виде капсида BFDV или капсида CaCV.
123. Способ по п.121, где добавленные или вставленные аминокислоты включают EFNLKDPPLN, PK или QFAPNNPSTEFDYETGRQL.
124. Композиция, содержащая белок PCV по любому из пп.105–117 или белок, полученный способом по любому из пп.118–123, в количестве, необходимом для индукции иммунного ответа или защитного иммунного ответа против PCV3 и/или его клинических симптомов, при однократном введении, и ветеринарно приемлемый носитель, включающий растворитель, дисперсионную среду, покрытие, стабилизирующий агент, разбавитель, консервант, противомикробный агент, противогрибковый агент, изотонический агент, агент, замедляющий адсорбцию, адъювант, надосадочную жидкость клеточной культуры, стабилизирующий агент, вирусный вектор или вектор экспрессии, и иммуномодулирующий агент, или любую их комбинацию.
125. Композиция по п.124, где белок ORF2 PCV3 кодируется SEQ ID NO:6 или SEQ ID NO:7.
126. Композиция по пп.124 или 125, где ветеринарно приемлемый носитель включает адъювант, иммуномодулирующий агент, надосадочную жидкость клеточной культуры, вирусный вектор или вектор экспрессии или любую их комбинацию.
127. Композиция по любому из пп.124-126, дополнительно включающая белок ORF2 PCV2, предпочтительно антигенный белок ORF2 PCV2, или дополнительный антиген дополнительного патогена свиней.
128. Композиция по п. 127, где дополнительный антиген дополнительного патогена свиней включает антиген PRRSV (вируса респираторного и репродуктивного синдрома свиней), бактериновый антиген Mycoplasma hyopneumoniae, антиген надосадочной жидкости Mycoplasma hyopneumoniae, антиген болезни Ауески или псевдобешенства, антиген свиного гриппа, антиген чумы молодых свиней (классической или африканской, или их комбинации), антиген Actinobacillus pleuropneumoniae, антиген Escherichia coli, антиген парвовируса свиней (PPV) или антиген Pasteurella multocida, или их комбинацию.
129. Композиция по любому из пп.124-128, где адъювант включает полимер акриловой или метакриловой кислоты; сополимер малеинового ангидрида и алкенильного производного; сшитый полимер акриловой или метакриловой кислоты; полимер акриловой или метакриловой кислоты, сшитый с полиалкениловым эфиром сахара или полиспирта; карбомер; акриловый полимер, поперечно сшитый полигидроксилированным соединением, имеющий по меньшей мере 3 и не более 8 гидроксильных групп с атомами водорода по меньшей мере трех гидроксилов, при необходимости замещенными или замещенным ненасыщенными алифатическими радикалами, имеющими по меньшей мере 2 атома углерода, с указанными радикалами, содержащими от 2 до 4 атома углерода, такими как винилы, аллилы и другие этиленненасыщенные группы, и ненасыщенные радикалы сами могут содержать другие заместители, такие как метил; карбопол; Карбопол 974P; Карбопол 934P; Карбопол 971P; гидроксид алюминия; фосфат алюминия; сапонин; Quil A; QS-21; GPI-0100; эмульсию вода-в-масле; эмульсию масло-в-воде; эмульсию вода-в-масле-в-воде; эмульсию на основе легкого жидкого парафинового масла или адъюванта типа Европейской Фармакопеи, изопреноидное масло; сквалан; сквалановое масло, полученное в результате олигомеризации алкенов, изобутена или децена; сложный эфир (эфиры) кислоты (кислот) или спирта (спиртов), содержащий линейную алкильную группу; растительное масло (масла); этилолеат; ди-(каприлат/капрат) пропиленгликоля; глицерилтри-(каприлат/капрат); диолеат пропиленгликоля; сложный эфир (эфиры) разветвленной жирной кислоты (кислот) или спирта (спиртов); сложный эфир (эфиры) изостеариновой кислоты; неионное поверхностно-активное вещество (вещества); сложный эфир (эфиры) сорбитана, или маннида, или гликоля, или полиглицерина, или пропиленгликоля, или олеиновой, или изостеариновой кислоты, или рицинолевой кислоты, или гидроксистеариновой кислоты, при необходимости этоксилированный, ангидроманнитол олеат; блок-сополимеры полиоксипропилена и полиоксиэтилена, продукт Плюроник, адъювантную систему RIBI; Блок-сополимер; SAF-M; монофосфориллипид А; авридиновый липидно-аминовый адъювант; термолабильный энтеротоксин из E. coli (рекомбинантный или другой); токсин холеры; IMS 1314 или мурамилдипептид.
130. Композиция по любому из пп.124-129, где белок ORF2 PCV3 присутствует в количестве от 0,2 до примерно 400 мкг/мл, или примерно от 0,3 до 200 мкг/мл, или примерно от 0,35 до 100 мкг/мл, или примерно от 0,4 до 50 мкг/мл, или примерно от 0,45 до 30 мкг/мл, или примерно от 0,6 до 15 мкг/мл, или примерно от 0,75 до 8 мкг/мл, или примерно от 1,0 до 6 мкг/мл, или примерно от 1,3 до 3,0 мкг/мл, или примерно от 1,4 до 2,5 мкг/мл, или примерно от 1,5 до 2,0 мкг/мл, или примерно 1,6 мкг/мл.
131. Композиция по любому из пп.124-130, где белок ORF2 PCV3 или общие белки ORF2 PCV2 и PCV3 присутствуют в количестве примерно от 0,2 до 400 мкг/дозу, или примерно от 0,3 до 200 мкг/дозу, или примерно от 0,35 до 100 мкг/дозу, или примерно от 0,4 до 50 мкг/дозу, или примерно от 0,45 до 30 мкг/дозу, или примерно от 0,6 до 15 мкг/дозу, или примерно от 0,75 до 8 мкг/дозу, или примерно от 1,0 до 6 мкг/дозу, или примерно от 1,3 до 3,0 мкг/дозу, или примерно от 1,4 до 2,5 мкг/дозу, или примерно от 1,5 до 2,0 мкг/дозу, или примерно 1,6 мкг/дозу.
132. Композиция по любому из пп.124-131, содержащая примерно от 50 мкг до 2000 мкг адъюванта, или где адъювант присутствует в количестве примерно 250 мкг/мл в дозе композиции, или адъювант присутствует в количестве примерно от 100 мкг до 10 мг на дозу, или где адъювант присутствует в количестве примерно от 500 мкг до 5 мг на дозу; адъювант присутствует в количестве примерно от 750 мкг до 2,5 мг на дозу, или адъювант присутствует в количестве примерно 1 мг на дозу.
133. Композиция по любому из пп.125-132, где иммуномодулирующий агент включает интерлейкин, интерферон или другой цитокин.
134. Вектор, содержащий и экспрессирующий белок PCV по любому из пп.105–117 или белок, продуцируемый способом по любому из пп.118–123.
135. Вектор по п.134, где белок PCV экспрессируется SEQ ID NO: 6 или SEQ ID NO: 7.
136. Вектор по пп.134 или 135, представляющий собой бакуловирус.
137. Способ получения композиции по любому из пп.125-133, включающий получение белка ORF2 PCV3 с помощью бакуловирусной системы экспрессии в культивируемых клетках насекомых.
138. Способ по п.137, дополнительно включающий инактивацию бакуловируса.
139. Способ по п.138, где инактивация включает тепловую обработку или использование агента, инактивирующего вирус.
140. Способ по п.139, где агент, инактивирующий вирус, включает азиридиновое соединение.
141. Способ по п. 140, где азиридиновое соединение включает BEI.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110>БЕРИНГЕР ИНГЕЛЬХАЙМ ЭНИМАЛ ХЕЛТ ЮЭсЭй ИНК.
<120>ВАКЦИНЫ ПРОТИВ СВИНОГО ЦИРКОВИРУСА 3 ТИПА (PCV3),ИХ ПРОИЗВОДСТВО
И ПРИМЕНЕНИЕ
<130>BI 19-AH009
<160>10
<170>PatentIn version 3.5
<210>1
<211>645
<212>DNA
<213>Porcine circovirus
<400>1
atgagacaca gagctatatt cagaagaaga ccccgcccaa ggagacgacg acgccacaga 60
aggcgctatg ccagaagacg actattcatt aggaggccca cagctggcac atactacaca
120
aagaaatact ccacaatgaa cgtcatatcc gttggaaccc ctcagaataa caagccctgg
180
cacgccaacc acttcattac ccgcctaaac gaatgggaaa ctgcaattac ctttgaatat
240
tataagatac taaaaatgaa agttacactc agccctgtaa tttctccggc tcagcaaaca
300
aaaactatgt tcgggcacac agccatagat ctagacggcg cctggaccac aaacacttgg
360
ctccaagacg acccttatgc ggaaagttcc actcgtaaag ttatgacttc taaaaaaaaa
420
cacagccgtt acttcacccc caaaccactt ctggcgggaa ctaccagcgc tcacccagga
480
caaagcctct tctttttctc cagacccacc ccatggctca acacatatga ccccaccgtt
540
caatggggag cactgctttg gagcatttat gtcccggaaa aaactggaat gacagacttc
600
tacggcacca aagaagtttg gattcgttac aagtccgttc tctga 645
<210>2
<211>134448
<212>DNA
<213>Porcine circovirus
<400>2
gaattctacc cgtaaagcga gtttagtttt gaaaaacaaa tgacatcatt tgtataatga 60
catcatcccc tgattgtgtt ttacaagtag aattctatcc gtaaagcgag ttcagttttg
120
aaaacaaatg agtcatacct aaacacgtta ataatcttct gatatcagct tatgactcaa
180
gttatgagcc gtgtgcaaaa catgagataa gtttatgaca tcatccactg atcgtgcgtt
240
acaagtagaa ttctactcgt aaagccagtt cggttatgag ccgtgtgcaa aacatgacat
300
cagcttatga ctcatacttg attgtgtttt acgcgtagaa ttctactcgt aaagcgagtt
360
cggttatgag ccgtgtgcaa aacatgacat cagcttatga gtcataatta atcgtgcgtt
420
acaagtagaa ttctactcgt aaagcgagtt gaaggatcat atttagttgc gtttatgaga
480
taagattgaa agcacgtgta aaatgtttcc cgcgcgttgg cacaactatt tacaatgcgg
540
ccaagttata aaagattcta atctgatatg ttttaaaaca cctttgcggc ccgagttgtt
600
tgcgtacgtg actagcgaag aagatgtgtg gaccgcagaa cagatagtaa aacaaaaccc
660
tagtattgga gcaataatcg atttaaccaa cacgtctaaa tattatgatg gtgtgcattt
720
tttgcgggcg ggcctgttat acaaaaaaat tcaagtacct ggccagactt tgccgcctga
780
aagcatagtt caagaattta ttgacacggt aaaagaattt acagaaaagt gtcccggcat
840
gttggtgggc gtgcactgca cacacggtat taatcgcacc ggttacatgg tgtgcagata
900
tttaatgcac accctgggta ttgcgccgca ggaagccata gatagattcg aaaaagccag
960
aggtcacaaa attgaaagac aaaattacgt tcaagattta ttaatttaat taatattatt
1020
tgcattcttt aacaaatact ttatcctatt ttcaaattgt tgcgcttctt ccagcgaacc
1080
aaaactatgc ttcgcttgct ccgtttagct tgtagccgat cagtggcgtt gttccaatcg
1140
acggtaggat taggccggat attctccacc acaatgttgg caacgttgat gttacgttta
1200
tgcttttggt tttccacgta cgtcttttgg ccggtaatag ccgtaaacgt agtgccgtcg
1260
cgcgtcacgc acaacaccgg atgtttgcgc ttgtccgcgg ggtattgaac cgcgcgatcc
1320
gacaaatcca ccactttggc aactaaatcg gtgacctgcg cgtctttttt ctgcattatt
1380
tcgtctttct tttgcatggt ttcctggaag ccggtgtaca tgcggtttag atcagtcatg
1440
acgcgcgtga cctgcaaatc tttggcctcg atctgcttgt ccttgatggc aacgatgcgt
1500
tcaataaact cttgtttttt aacaagttcc tcggtttttt gcgccaccac cgcttgcagc
1560
gcgtttgtgt gctcggtgaa tgtcgcaatc agcttagtca ccaactgttt gctctcctcc
1620
tcccgttgtt tgatcgcggg atcgtacttg ccggtgcaga gcacttgagg aattacttct
1680
tctaaaagcc attcttgtaa ttctatggcg taaggcaatt tggacttcat aatcagctga
1740
atcacgccgg atttagtaat gagcactgta tgcggctgca aatacagcgg gtcgcccctt
1800
ttcacgacgc tgttagaggt agggccccca ttttggatgg tctgctcaaa taacgatttg
1860
tatttattgt ctacatgaac acgtatagct ttatcacaaa ctgtatattt taaactgtta
1920
gcgacgtcct tggccacgaa ccggacctgt tggtcgcgct ctagcacgta ccgcaggttg
1980
aacgtatctt ctccaaattt aaattctcca attttaacgc gagccatttt gatacacgtg
2040
tgtcgatttt gcaacaacta ttgtttttta acgcaaacta aacttattgt ggtaagcaat
2100
aattaaatat gggggaacat gcgccgctac aacactcgtc gttatgaacg cagacggcgc
2160
cggtctcggc gcaagcggct aaaacgtgtt gcgcgttcaa cgcggcaaac atcgcaaaag
2220
ccaatagtac agttttgatt tgcatattaa cggcgatttt ttaaattatc ttatttaata
2280
aatagttatg acgcctacaa ctccccgccc gcgttgactc gctgcacctc gagcagttcg
2340
ttgacgcctt cctccgtgtg gccgaacacg tcgagcgggt ggtcgatgac cagcggcgtg
2400
ccgcacgcga cgcacaagta tctgtacacc gaatgatcgt cgggcgaagg cacgtcggcc
2460
tccaagtggc aatattggca aattcgaaaa tatatacagt tgggttgttt gcgcatatct
2520
atcgtggcgt tgggcatgta cgtccgaacg ttgatttgca tgcaagccga aattaaatca
2580
ttgcgattag tgcgattaaa acgttgtaca tcctcgcttt taatcatgcc gtcgattaaa
2640
tcgcgcaatc gagtcaagtg atcaaagtgt ggaataatgt tttctttgta ttcccgagtc
2700
aagcgcagcg cgtattttaa caaactagcc atcttgtaag ttagtttcat ttaatgcaac
2760
tttatccaat aatatattat gtatcgcacg tcaagaatta acaatgcgcc cgttgtcgca
2820
tctcaacacg actatgatag agatcaaata aagcgcgaat taaatagctt gcgacgcaac
2880
gtgcacgatc tgtgcacgcg ttccggcacg agctttgatt gtaataagtt tttacgaagc
2940
gatgacatga cccccgtagt gacaacgatc acgcccaaaa gaactgccga ctacaaaatt
3000
accgagtatg tcggtgacgt taaaactatt aagccatcca atcgaccgtt agtcgaatca
3060
ggaccgctgg tgcgagaagc cgcgaagtat ggcgaatgca tcgtataacg tgtggagtcc
3120
gctcattaga gcgtcatgtt tagacaagaa agctacatat ttaattgatc ccgatgattt
3180
tattgataaa ttgaccctaa ctccatacac ggtattctac aatggcgggg ttttggtcaa
3240
aatttccgga ctgcgattgt acatgctgtt aacggctccg cccactatta atgaaattaa
3300
aaattccaat tttaaaaaac gcagcaagag aaacatttgt atgaaagaat gcgtagaagg
3360
aaagaaaaat gtcgtcgaca tgctgaacaa caagattaat atgcctccgt gtataaaaaa
3420
aatattgaac gatttgaaag aaaacaatgt accgcgcggc ggtatgtaca ggaagaggtt
3480
tatactaaac tgttacattg caaacgtggt ttcgtgtgcc aagtgtgaaa accgatgttt
3540
aatcaaggct ctgacgcatt tctacaacca cgactccaag tgtgtgggtg aagtcatgca
3600
tcttttaatc aaatcccaag atgtgtataa accaccaaac tgccaaaaaa tgaaaactgt
3660
cgacaagctc tgtccgtttg ctggcaactg caagggtctc aatcctattt gtaattattg
3720
aataataaaa caattataaa tgtcaaattt gttttttatt aacgatacaa accaaacgca
3780
acaagaacat ttgtagtatt atctataatt gaaaacgcgt agttataatc gctgaggtaa
3840
tatttaaaat cattttcaaa tgattcacag ttaatttgcg acaatataat tttattttca
3900
cataaactag acgccttgtc gtcttcttct tcgtattcct tctctttttc atttttctcc
3960
tcataaaaat taacatagtt attatcgtat ccatatatgt atctatcgta tagagtaaat
4020
tttttgttgt cataaatata tatgtctttt ttaatggggt gtatagtacc gctgcgcata
4080
gtttttctgt aatttacaac agtgctattt tctggtagtt cttcggagtg tgttgcttta
4140
attattaaat ttatataatc aatgaatttg ggatcgtcgg ttttgtacaa tatgttgccg
4200
gcatagtacg cagcttcttc tagttcaatt acaccatttt ttagcagcac cggattaaca
4260
taactttcca aaatgttgta cgaaccgtta aacaaaaaca gttcacctcc cttttctata
4320
ctattgtctg cgagcagttg tttgttgtta aaaataacag ccattgtaat gagacgcaca
4380
aactaatatc acaaactgga aatgtctatc aatatatagt tgctgatatc atggagataa
4440
ttaaaatgat aaccatctcg caaataaata agtattttac tgttttcgta acagttttgt
4500
aataaaaaaa cctataaata ttccggatta ttcataccgt cccaccatcg ggcgcggatc
4560
cgccaccatg agacacagag ctatattcag aagaagaccc cgcccaagga gacgacgacg
4620
ccacagaagg cgctatgcca gaagacgact attcattagg aggcccacag ctggcacata
4680
ctacacaaag aaatactcca caatgaacgt catatccgtt ggaacccctc agaataacaa
4740
gccctggcac gccaaccact tcattacccg cctaaacgaa tgggaaactg caattacctt
4800
tgaatattat aagatactaa aaatgaaagt tacactcagc cctgtaattt ctccggctca
4860
gcaaacaaaa actatgttcg ggcacacagc catagatcta gacggcgcct ggaccacaaa
4920
cacttggctc caagacgacc cttatgcgga aagttccact cgtaaagtta tgacttctaa
4980
aaaaaaacac agccgttact tcacccccaa accacttctg gcgggaacta ccagcgctca
5040
cccaggacaa agcctcttct ttttctccag acccacccca tggctcaaca catatgaccc
5100
caccgttcaa tggggagcac tgctttggag catttatgtc ccggaaaaaa ctggaatgac
5160
agacttctac ggcaccaaag aagtttggat tcgttacaag tccgttctct gagcggccgc
5220
tgcagatctg atcctttcct gggacccggc aagaaccaaa aactcactct cttcaaggaa
5280
atccgtaatg ttaaacccga cacgatgaag cttgtcgttg gatggaaagg aaaagagttc
5340
tacagggaaa cttggacccg cttcatggaa gacagcttcc ccattgttaa cgaccaagaa
5400
gtgatggatg ttttccttgt tgtcaacatg cgtcccacta gacccaaccg ttgttacaaa
5460
ttcctggccc aacacgctct gcgttgcgac cccgactatg tacctcatga cgtgattagg
5520
atcgtcgagc cttcatgggt gggcagcaac aacgagtacc gcatcagcct ggctaagaag
5580
ggcggcggct gcccaataat gaaccttcac tctgagtaca ccaactcgtt cgaacagttc
5640
atcgatcgtg tcatctggga gaacttctac aagcccatcg tttacatcgg taccgactct
5700
gctgaagagg aggaaattct ccttgaagtt tccctggtgt tcaaagtaaa ggagtttgca
5760
ccagacgcac ctctgttcac tggtccggcg tattaaaaca cgatacattg ttattagtac
5820
atttattaag cgctagattc tgtgcgttgt tgatttacag acaattgttg tacgtatttt
5880
aataattcat taaatttata atctttaggg tggtatgtta gagcgaaaat caaatgattt
5940
tcagcgtctt tatatctgaa tttaaatatt aaatcctcaa tagatttgta aaataggttt
6000
cgattagttt caaacaaggg ttgtttttcc gaaccgatgg ctggactatc taatggattt
6060
tcgctcaacg ccacaaaact tgccaaatct tgtagcagca atctagcttt gtcgatattc
6120
gtttgtgttt tgttttgtaa taaaggttcg acgtcgttca aaatattatg cgcttttgta
6180
tttctttcat cactgtcgtt agtgtacaat tgactcgacg taaacacgtt aaataaagct
6240
tggacatatt taacatcggg cgtgttagct ttattaggcc gattatcgtc gtcgtcccaa
6300
ccctcgtcgt tagaagttgc ttccgaagac gattttgcca tagccacacg acgcctatta
6360
attgtgtcgg ctaacacgtc cgcgatcaaa tttgtagttg agctttttgg aattatttct
6420
gattgcgggc gtttttgggc gggtttcaat ctaactgtgc ccgattttaa ttcagacaac
6480
acgttagaaa gcgatggtgc aggcggtggt aacatttcag acggcaaatc tactaatggc
6540
ggcggtggtg gagctgatga taaatctacc atcggtggag gcgcaggcgg ggctggcggc
6600
ggaggcggag gcggaggtgg tggcggtgat gcagacggcg gtttaggctc aaatgtctct
6660
ttaggcaaca cagtcggcac ctcaactatt gtactggttt cgggcgccgt ttttggtttg
6720
accggtctga gacgagtgcg atttttttcg tttctaatag cttccaacaa ttgttgtctg
6780
tcgtctaaag gtgcagcggg ttgaggttcc gtcggcattg gtggagcggg cggcaattca
6840
gacatcgatg gtggtggtgg tggtggaggc gctggaatgt taggcacggg agaaggtggt
6900
ggcggcggtg ccgccggtat aatttgttct ggtttagttt gttcgcgcac gattgtgggc
6960
accggcgcag gcgccgctgg ctgcacaacg gaaggtcgtc tgcttcgagg cagcgcttgg
7020
ggtggtggca attcaatatt ataattggaa tacaaatcgt aaaaatctgc tataagcatt
7080
gtaatttcgc tatcgtttac cgtgccgata tttaacaacc gctcaatgta agcaattgta
7140
ttgtaaagag attgtctcaa gctcggatcc cgcacgccga taacaagcct tttcattttt
7200
actacagcat tgtagtggcg agacacttcg ctgtcgtcga cgtacatgta tgctttgttg
7260
tcaaaaacgt cgttggcaag ctttaaaata tttaaaagaa catctctgtt cagcaccact
7320
gtgttgtcgt aaatgttgtt tttgataatt tgcgcttccg cagtatcgac acgttcaaaa
7380
aattgatgcg catcaatttt gttgttccta ttattgaata aataagattg tacagattca
7440
tatctacgat tcgtcatggc caccacaaat gctacgctgc aaacgctggt acaattttac
7500
gaaaactgca aaaacgtcaa aactcggtat aaaataatca acgggcgctt tggcaaaata
7560
tctattttat cgcacaagcc cactagcaaa ttgtatttgc agaaaacaat ttcggcgcac
7620
aattttaacg ctgacgaaat aaaagttcac cagttaatga gcgaccaccc aaattttata
7680
aaaatctatt ttaatcacgg ttccatcaac aaccaagtga tcgtgatgga ctacattgac
7740
tgtcccgatt tatttgaaac actacaaatt aaaggcgagc tttcgtacca acttgttagc
7800
aatattatta gacagctgtg tgaagcgctc aacgatttgc acaagcacaa tttcatacac
7860
aacgacataa aactcgaaaa tgtcttatat ttcgaagcac ttgatcgcgt gtatgtttgc
7920
gattacggat tgtgcaaaca cgaaaactca cttagcgtgc acgacggcac gttggagtat
7980
tttagtccgg aaaaaattcg acaccacaac tatgcacgtt cgtttgactg gtacgccgtc
8040
ggcgtgttaa catacaagtt gctaaccggc ggccgacacc catttgaaaa aagcgaagac
8100
gaaatgttgg acttgaatag catgaagcgt cgtcagcaat acaatgacat tggcgtttta
8160
aaacacgttc gtaacgttaa cgctcgtgac tttgtgtact gcctaacaag atacaacata
8220
gattgtagac tcacaaatta caaacaaatt ataaaacatg agtttttgtc gtaaaaatgc
8280
cacttgtttt acgagtagaa ttctacgtgt aacacacgat ctaaaagatg atgtcatttt
8340
ttatcaatga ctcatttgtt ttaaaacaga cttgttttac gagtagaatt ctacgtgtaa
8400
agcatgatcg tgagtggtgt taataaaatc ataaaaatta ttgtaaatgt ttattattta
8460
aaaacgattc aaatatataa taaaaacaat ctacatctat ttcttcacaa tccataacac
8520
acaacaggtc catcaatgag tttttgtctt tatccgacat actatgtgca tgtaacaaat
8580
caaatacatc ttttaaattt ttatacacat ctttacattg tctaccaaaa tctttaataa
8640
ccctataaca aggaaaagac ttttcttctt gcgtggtttt gccgcgcaga tattgaaata
8700
aaatgtgcat gcacgacaac ttgtgtttac taaaatgctc cttgcctata ccgcaaaacc
8760
ggccatacat ttcggcgatt acacgcggac aattgtacga ttcgtctacg tgtaaacgat
8820
catcataatc actcttgcgc aaacgaataa attttttcac cgcttccgac aaacgaggca
8880
ccaattcggc gggcacgctt cgatacatta ttctgtgcac ataagttacc acacaaaatt
8940
tattgtacca ccatccgaca acgtcgttat tagggttgaa cacgttggcg atgcgcagca
9000
gtttcccgtt tctcatgaaa tattcaaagc ggcccaaaat aatttgcaag caatccaaca
9060
tgtcttgaga aatttctcgt tcaaaattgt tcaaagagaa tatctgccat ccgttttgaa
9120
cgcgcacgct gacgggaacc accgcatcga tttgctccaa cacttcacgg acgttatcgt
9180
cgatgcccat cgtttcgctg gtgctgaacc aatgggaaag gctcttgatg gaatcgcccg
9240
cgtctatcat cttgaccgct tcgtcaaagg tgcaactgcc gctcttcaaa cgccgcatag
9300
cggtcacgtc ccgctctatg cacgacatac cgtttacgta cgattctgat aggtattcct
9360
gaactatacg gtaatggtga tacgactcgc catacacgtc gtgcacctca ttgtatttag
9420
cataataatt gtaaattatt aactttgcag cgagagacat gttgtcagta aagcggtgct
9480
aggctcaata atactgatgt acaggcacgc gtgctattta tatataattt cgcaaggagg
9540
ggagctgtta tcggttgcta ttattaaaga atggccgtct gtttttatca caagcttggc
9600
agcctcaacc atgaagcgtc gtcattgtaa attaaattct ctgcctcaag aattatttga
9660
caagattgtc gagtatttat ctttatctga ttactgcaat ttggtgcttg tctgtaaaag
9720
accttctagt aaatataacg tgatatttga tagtactaat caccaacatt tgaaaggcgt
9780
gtacaaaaag acagacgtgc aaataacaag ctacaacgaa tacatcaact gtatttgcaa
9840
cgaactgaga caagacgaat tctatgccaa atcatcatgg attgcgagta tttgcggtca
9900
ccagagagcg acaattttta gtgtaacaaa taaacaagta gaaatgaaat atcatttgta
9960
taatatagca attgtggaaa gtgaagattg caacggattt tacccatttg agccaacgcg
10020
cgattgttta atatgcaaac aaaaaaacca atgtcctcgt aattcattta ttgtttcgtt
10080
gtgtaaatat ttagaaaaac aaaatgtaca atcaaacttt atatattatt tatacgaaat
10140
aaatacataa taataactat tatacatgtt tttattttac aatacttcct gtataacctc
10200
tctaactaca ttaggagtac aatccacgtc aattacacgt ttagctattt ttctaatttt
10260
gtaatgttta tcgtagagtt tttcgttaat acattgaata gccaacaagg gatttgggtg
10320
cacaccgtca tagagtactt ccatgtcgtc ttcaaagcgc atttttcgct tgcgaaaatg
10380
ccgctcttgg cccaaaacaa aagcgagttt gatgcggtcg tcgatgcgtt ccgaaaatac
10440
ggccaaatgc tggtgtttgg tgatgtcgcg cggaaacgtc accgtgccat ttttgctttc
10500
cgccacgacg gcggttttca atttttcggc cgactgcagc atgttaagtt tggcgtcgag
10560
ttcgtgcaaa cgcaattcaa actgctcaaa cctgttgccc acctcgttct tgaacgtctc
10620
gtgggtgacc ataaattttt cgctgtttgc attcagtttc tttacatgtt ttaaaacaga
10680
ttcaatcttg tcgcgcaaat catcacgctc gccttcagtt tgaatgtgca gcaacgcgtt
10740
gcttttgttg gcaaaattta accgcatcaa aatttccaac aacccgtgct tggtcgcgaa
10800
caatgcgccc aacgagttga gatcgcgttt ggatctctgt ttgtgaaaaa caatttcgtt
10860
taaatggtaa acttgatcgc cgtcccaatt gcaatcaagt atgtcgtcgt gcgcaatttc
10920
aagacctttg caaaaatcta tcacattgta gcattttgcg ttcgtgtcgc tgtgcacgta
10980
tctgtacttg aaactgtgcg tgttgcattt gaatgagtcc catttaacga tgtgcgacca
11040
ttgttgggcg tttatgtggt actttttgta gtcgtctgca ttgaaccgat cttcggcggc
11100
gatggcgtcg ttgtcgttgt caccggacca catccaccag ttccataacc aggatagcat
11160
tgctttagct tgtctagcaa ttcctttgtt atacaacgag aaaatttcgt tcccttataa
11220
ttatagctgt acggtgcgcg tatttgtttg ttaacgttac aaaaaatatc cctgtccacg
11280
tccggccaat actgcaacgt gagcgcgtcc aagtttgaat cttgcatatg cggaacgtac
11340
aaacgtacgg cctctctcac acaatgcgca aaactgcccg gctgaatgta atcactgtcc
11400
aactttgcag gtttctcgaa agccttgtac cgatgcacgc gaacattttg agcggacgtg
11460
attttaaact tgtcggtgaa ttttaaccac aaatgaaatc cacggttgcc ggtatacatg
11520
actcttgaca cgttctcttc cgtgtaaaac aacagaaacg ccgtggcgcc aatgtaaatt
11580
ttcagcatta aatcgtgttc gtcaacataa tttttgtaat cggcgtctac gacccattcc
11640
ctgccgccgc cgtcgtccaa cggtttgacg tgcacgtcgg acactttgtt ttgcacaata
11700
taactataca attgtgcgga ggtatcaaaa tatctgtcgg cgtgaatcca gcgcgcgttg
11760
accgtcatga acgcgtactt gcggctgtcg ttgtacgcaa tggcgtccca catcatgtcg
11820
acgcgcttct gcgtataatt gcacactaac atgttgccct ttgaacttga cctcgattgt
11880
gttaattttt ggctataaaa aggtcaccct ttaaaatttg ttacataatc aaattaccag
11940
tacagttatt cggtttgaag caaaatgact attctctgct ggcttgcact gctgtctacg
12000
cttactgctg taaatgcggc caatatattg gccgtgtttc ctacgccagc ttacagccac
12060
catatagtgt acaaagtgta tattgaagcc cttgccgaaa aatgtcacaa cgttacggtc
12120
gtcaagccca aactgtttgc gtattcaact aaaacttatt gcggtaatat cacggaaatt
12180
aatgccgaca tgtctgttga gcaatacaaa aaactagtgg cgaattcggc aatgtttaga
12240
aagcgcggag tggtgtccga tacagacacg gtaaccgccg ctaactacct aggcttgatt
12300
gaaatgttca aagaccagtt tgacaatatc aacgtgcgca atctcattgc caacaaccag
12360
acgtttgatt tagtcgtcgt ggaagcgttt gccgattatg cgttggtgtt tggtcacttg
12420
tacgatccgg cgcccgtaat tcaaatcgcg cctggctacg gtttggcgga aaactttgac
12480
acggtcggcg ccgtggcgcg gcaccccgtc caccatccta acatttggcg cagcaatttc
12540
gacgacacgg aggcaaacgt gatgacggaa atgcgtttgt ataaagaatt taaaattttg
12600
gccaacatgt ccaacgcgtt gctcaaacaa cagtttggac ccaacacacc gacaattgaa
12660
aaactacgca acaaggtgca attgcttttg ctaaacctgc atcccatatt tgacaacaac
12720
cgacccgtgc cgcccagcgt gcagtatctt ggcggaggaa tccatcttgt aaagagcgcg
12780
ccgttgacca aattaagtcc ggtcatcaac gcgcaaatga acaagtcaaa aagcggaacg
12840
atttacgtaa gttttgggtc gagcattgac accaaatcgt ttgcaaacga gtttctttac
12900
atgttaatca atacgttcaa aacgttggat aattacacca tattatggaa aattgacgac
12960
gaagtagtaa aaaacataac gttgcccgcc aacgtaatca cgcaaaattg gtttaatcaa
13020
cgcgccgtgc tgcgtcataa aaaaatggcg gcgtttatta cgcaaggcgg actacaatcg
13080
agcgacgagg ccttggaagc cgggataccc atggtgtgtc tgcccatgat gggcgaccag
13140
ttttaccatg cgcacaaatt acagcaactc ggcgtagccc gcgccttgga cactgttacc
13200
gtttccagcg atcaactact agtggcgata aacgacgtgt tgtttaacgc gcctacctac
13260
aaaaaacaca tggccgagtt atatgcgctc atcaatcatg ataaagcaac gtttccgcct
13320
ctagataaag ccatcaaatt cacagaacgc gtaattcgat atagacatga catcagtcgt
13380
caattgtatt cattaaaaac aacagctgcc aatgtaccgt attcaaatta ctacatgtat
13440
aaatctgtgt tttctattgt aatgaatcac ttaacacact tttaattacg tcaataaatg
13500
ttattcacca ttatttacct ggtttttttg agaggggctt tgtgcgactg cgcacttcca
13560
gcctttataa acgctcacca accaaagcag gtcattattg tgccaggacg ttcaaaggcg
13620
aaacatcgaa atggagtctg ttcaaacgcg cttatgtgcc agtagcaatc aatttgctcc
13680
gttcaaaaag cgccagcttg ccgtgccggt cggttctgtg aacagtttga cacacaccat
13740
cacctccacc accgtcacca gcgtgattcc aaaaaattat caagaaaaac gtcagaaaat
13800
atgccacata atatcttcgt tgcgtaacac gcacttgaat ttcaataaga tacagtctgt
13860
acataaaaag aaactgcggc atttgcaaaa tttgctaaga aaaaagaacg aaattattgc
13920
cgagttggtt agaaaacttg aaagtgcaca gaagaagaca acgcacagaa atattagtaa
13980
accagctcat tggaaatact ttggagtagt cagatgtgac aacacaattc gcacaattat
14040
tggcaacgaa aagtttgtaa ggagacgttt ggccgagctg tgcacattgt acaacgccga
14100
gtacgtgttt tgccaagcac gcgccgatgg agacaaagat cgacaggcac tagcgagtct
14160
gctgacggcg gcgtttggtt cgcgagtcat agtttatgaa aatagtcgcc ggttcgagtt
14220
tataaatccg gacgagattg ctagtggtaa acgtttaata attaaacatt tgcaagatga
14280
atctcaaagt gatattaacg cctattaatt tgaaaggtga ggaagagccc aattgcgttg
14340
agcgcattac cataatgcca tgtattttaa tagatactga gatctgttta aatgtcagat
14400
gccgttctcc ttttgccaaa ttcaaagtat tgattattgt agatggcttt gatagcgctt
14460
atattcaggc taccttttgt agcattagcg atagtgtaac aattgttaac aaatctaacg
14520
aaaagcatgt aacgtttgac gggtttgtaa ggccggacga tgaaggtaca acaatgcctt
14580
atgtcattgg accattatat tctgtcgacg ctgctgtcgc cgaccgtaaa gtgaaggacg
14640
tggtggattc aattcaaaac caacagacaa tgttaaaagt atttattaac gaggctaatg
14700
tgtataacaa atggaatatg cttaaaggtt taatttataa taataacaat gaatctgttt
14760
tagtaaaata atgtagtaaa atttataaag gtagataaaa attataatat taataaaaaa
14820
aataatgtta ctaaatgggt tcctgcgtta aattatttta cgggtagaca gctattaact
14880
attttattta tttttaaatt taaataaatg tattgttaga aaattgtgtt gttttattag
14940
tataacgaaa aaatacatga cataaaccgc ttccaatttt ggtcacacaa actcttgtgt
15000
ggatagttta cgtaatgagt taaataggcg ggcagttgtc cgctaaacgt gtcggtggtc
15060
aagtagatgt gcattaattt acgacaaccc aaagcggggc cgcttatgtc aagtattttt
15120
ttcacaaaat tggtaatggt ttcgttttgt tccttgtaca aacacatgtc ggtgtgatcg
15180
ttgacgcacg agttgtacga ttccgccggc aggttggcaa acaagcgctt gagatgcttg
15240
agtctgcgtt caattttata atcaaacttg ttggtgaaaa tgtctttcag caagcacatt
15300
aactggtcgt tcaaaacgcg ctgcaacgac gacaccaaca catgatattc gtttccaaaa
15360
agcgaaaaat ttttgatgca gcggtccgcg ttgaagggtc gtttcataat gcgcacgttg
15420
acaaaaaaca cgttgaaaga cagcggggct gtggttattt taacgccgtt gtcggtatac
15480
tcgtcgacgc cgtctgcgct tgttatgtca atttgtagcg caaatctaac caaatcaaac
15540
tcatcgttgt actgtgtctt tatgcatttt atatggcggt ttaagtgcaa gttgatttgg
15600
ccgtttaatc tataggctcc gttttgataa catttcagca ctaccaacgg atccgacatg
15660
taaacttgac gcgttagcac gtccaattca gcgtaatgtt ggtcgacgca tttttgtaaa
15720
ttagtttgca ggttgcaaaa catttttgcg caaaagccgt aatagtcaaa atctatgcat
15780
tttaatgcgc ttctgtcgtc gtcaatatgg catgtcacgg ctgcgcctcc agttaacacg
15840
aataaaccgc cgttttcgca aactacggct tcgaaacaat ctttgataaa tgccaacttt
15900
gctttagcca caattttatc gcgcaggcga tcttcaatat cctttgtcgt aatataaggt
15960
aggacgccaa gatttagttg attcaacaaa cgttccataa tgaatagcgg cgacgcaaca
16020
cgactacact gttcaaatgc gcacgcaaaa caaacccttg caactttatt tgccaatcgt
16080
aatcacagta gtttttacga gtacgccatc gcgtttgtaa gcacattgct ttttaaaaat
16140
aatttaaatt taatgaccgc gtgcaatttg atcaactcgt tgatcaactt tgaactcaac
16200
atgtttggta aaagtttatt gctaaatgga tttgttaatt tctgcattgc taacagcgac
16260
ggggttacga ttcaacataa aatgttaacc aacgtgttaa gttttttgtt ggaaaaatat
16320
tattaaaaat aaataaataa acttgttcag ttctaattat tgttttattt tttataaaat
16380
aatacaattt tatttataca ttaatacttt ggtatttatt aatacaatta tttacaatac
16440
tttatttaca ctataatact ttatttacat tagtactaaa ttaatactaa attacgctaa
16500
tactaaatta atactttata taatcaaaaa taatacttta tataatactt tctaatcatc
16560
ataaacgggt aatagttttt tctcttgaaa tttacgctgc aactcttcgc taaaacacat
16620
gggcggtgga gtgggagcgg gtggagtagg agtccttacg ggtttgatgg gcgacagttc
16680
tctggacttg cggaacagct tgggcgaaag cgtcggcgtg cgccgactaa tgatttcttc
16740
atccggcaac ggaggctcgc acattgtgca cgcgtccggt gaggtacaca aaactttctt
16800
gggcacgctg tacaccggct tgggcacgct atatgtgttg ccaaaataga actcgttgtg
16860
gttgccgaac ggagacgatg ggtgtgaaga cggcgatggc tgtgaagaca agtccgaagg
16920
cgcgataaaa gatgaaagtg tttctgaaac cgaagtggtg gtagaagtgg tagaaggcgg
16980
gtgcgttacg gcaaccacgc tgctgctatt tctgccttcg gagaccactt ccagcaatct
17040
agagttactc tctcgttctt cgcggcgata gtcaatgtcg caataatgtt cataagatgc
17100
cttttcggct tcggcgcgcc ttttcatgta tatgttgtga cgcatctcct ttaactgcac
17160
gtacaaattc cagcattgca cagccagtat cgtaagcacg cccattatga ttacgggata
17220
attttgatta aacacggtcg gctcgtgatc gcttacaatc gctcggcaca tgatgcattt
17280
tttgtaaatg ttcacataca cacagttttg gctcaaggtt tcggtatttg cgtagtcaat
17340
ttccagatac acgatagagt tccagcacat tgattccaaa tcgtagtgac gatataaaac
17400
atctagcgcc ggtagatgac catttttgaa cacgtagatt tgaaacgcgg caaacagcat
17460
ccaacacagc ccagtgatca cgtttaccat aatacacgtg atagcgacgt aaaagttttc
17520
tttcgcattg aaatttacat ttgtgtttga agagctgctg cgatttttcg tccacacgat
17580
aatcttccat ataaaataaa acatgtaaaa taatatccac atgccgaacg ccagcattat
17640
cggtatagat agattgataa ccgattgctt tccttcaatt tccagcaaaa acgcgtatct
17700
gctgtctatc actcccatta tagataacac aaacactatc agatatgcta ataataatga
17760
ggcattaagc ccgaattgta aaactgcagt gattttattt aacattttga atatttaatt
17820
caacaactaa gtaatggcaa tatgtatcga gtactgatcg tgtttttcct gttcgtgttt
17880
ctttatatag tgtaccagcc cttttatcag gcatacttgc atatcggaca tgcccaacaa
17940
gattacaatg acacgttgga cgataggatg gattacattg aatccgtaat gcgtagaagg
18000
cactacgtgc cgattgaagc gttgcccgca atcaggtttg atactaatct cggcacgttg
18060
gccggtgaca cgattaaatg catgtcggtg cctttgtttg ttagtgacat tgacctgccg
18120
atgtttgatt gtagtcagat atgcgataac ccgtctgcgg cgtatttctt tgtcaacgaa
18180
acggatgtgt ttgtggtcaa cggccacaga ctgacggtgg gcggatactg ctccactaat
18240
agtttgcccc gcaactgtaa tcgcgagacg agcgtcattt taatgagtct caatcagtgg
18300
acgtgcatag ccgaggaccc gcgttactat gcgggcacag ataacatgac gcaactcgca
18360
ggcagacaac actttgaccg cattatgccc ggacagagtg ataggaacgt cctgtttgac
18420
cgattactag gccgagaggt gaacgtgacc actaacacgt ttcgccgcag ctgggacgag
18480
ttgctggagg acggcactag gcggttcgaa atgcgctgca acgcccgaga taacaacaat
18540
aatctcatgt ttgttaatcc gcttaatccc ctcgagtgtc tcccgaacgt gtgcactaac
18600
gttagcaacg tgcacaccag tgttagaccc gtatttgaaa cgggagagtg tgactgcggc
18660
gacgaagcgg tcacgcgtgt tacgcacatt gtgccggggg acaggacctc tatgtgtgcc
18720
agcattatag atggcctgga taaaagtacg gcatcatata gatatcgcgt agagtgcgtt
18780
aatctgtaca cctctattct aaattattct aataacaaat tgttatgtcc cagtgacact
18840
tttgatagta acacggacgc agcttttgcc tttgaagtgc ccggctccta ccctttatcg
18900
cgcaacggca tcaacgagcc aacttatcgc ttttatcttg ataccagatc tcgagttaat
18960
tacaatgacg tcagagggca gttatcttaa ttgtgataac acaaacaata agtcatttaa
19020
atgttacgtc agtagttagt atataagccg tacatgttgg cttgcaaatt cagtcaatat
19080
caggctttta tcatggacgg tgtaaagctg ctagggacgt gcgcgctaat aattttgtta
19140
tcgacgacga gtacagttgt cgggcgtgac cgtatcacgt ttacgccgat agaagatagc
19200
gcaggcctca tgtttgaacg catgtacggc ttgcgacatc atacagacga cagatttgtg
19260
tttgtgaaaa aattcaattt tgtttcggtg ctgcaagagc tcaataatat caaatctaaa
19320
attgaattat atgaagcgca agtttcaact tgcacaaacg tcagacaaat aaaacagaac
19380
agatcgagta tcatcaaagc tcgcattgaa aatcagctgc agtttttgac gcaactaaac
19440
aaaaatctca tcacatactc tgtggaaagc agcattttaa gcaacgacgt gctggacaac
19500
atcgatctgg aatatgacga cagcggtgag tttgacgttt acgacgaata cgaacagcct
19560
tcgcattgga gcaacatgac tgtatccgac gcgcaagctt tgctccgaaa cccgcccaaa
19620
gacagagtaa tgtttttgga catggttacc accagcgacg tgagcagcaa atacgaagaa
19680
tacataaact gcattgtgag caaccgtacc gttgaaaacg agtgcatgtt tttagccaac
19740
atgatgaacg tgctcaacga caaattggac gacgcagcag ctttggccaa gatgctggag
19800
cgaatagtaa aacaaacgcg aaagaacaaa ctcaacatct ccaacacggt tatagacgac
19860
gacacgctgc taacggaaat gaaaaaatta acacaaactt tatacaacca aaaccgcgtg
19920
tgggtagtgg attttaacaa ggacatgaat agttatttcg atttgtcgca agcgtataaa
19980
ttgcatttat atgttgattt aaacacggtc attatgttta ttaccatgcc attgttaaaa
20040
tccaccgccg tttcgtttaa tttgtatcgc gtcatgacgg tgcctttttg caggggcaaa
20100
atgtgtctgc ttatcatttc gggcaatgaa tactttggga ttacagacag caaaaactat
20160
tatgtgcccg tatctgataa ctttagacaa gattgccaag agtttacggg ctacaatgag
20220
tttttgtgtc ccgaaactga gccgattgcc actatgaact cgaaagtgtg cgagattgaa
20280
atgtttatgg gtcgatatag cgacgacgtg gacaacatgt gcgacattag ggtggccaat
20340
tataatccca aaaaagctta cgtgaacact ttaatagact accgaaaatg gttgtacatt
20400
tttccaaaca cgaccgtgtc cgtccactat tattgtcacg acgcgcttgt agaagttgat
20460
acaaaagttt cgcccggcgt tggtgttatg ttttcgacta tggcgcaaac gtgttcgatt
20520
agaataacgt atgatgtgac cataactgta gattcgcgat tttatgtcag ccattcaact
20580
acatactggc ctaaaaagaa atttaatttt aacaactaca tcgaccaaat gttgcttgaa
20640
aaagcgacca ccagttttat accgactgtt gacaatttta cccggcccgt tttattgcaa
20700
cttcctcata aatttcacat taaagattac acatcgacgc cccatcattt tttccatcag
20760
tctaaaattt acaccaacag cgcggcgccc gacgaagact cgcaagacga cagtaatacc
20820
accgtggtaa ttatcgctat tgtcgctgca atgatcctat tctgtggatt attgttattt
20880
ttgttttgct gtataaaaaa acggtgtcat caatcaaata acgtggttgt gcaatacaaa
20940
aataacaatg aatttgtcac aatttgcaat aatttagaag acaatcgagc atacattaat
21000
ttacctaatg aatacgatag cgatgatatg ccaaaaccat tgtacccttt acttggcttt
21060
aatgatgatt tgttaaaaga tgataaacct gtgttgtacc ctatgattat agaaagaata
21120
aaataaaaca tgtataattg aaataaatat attatttaat aaaatgtttt ttatttatat
21180
actattttct attacatatt ccaatgcaca caaatgttta atggctatca gttttaattt
21240
tactaattcg tctaaacaaa aattattcac ttgctgtttt tcatccattt gacatatggc
21300
gtttataaat aattcgctgt gttttatgaa cgaatcgtaa accgctgcct gggccttcag
21360
cacggtcggc gcattgtatt tttgggtaaa gtacgcaata tttttagtca aacacagaga
21420
ttttaaatct ttttcattta tatccaagtc ggaacaatcg tatacaaaat ctagcttttc
21480
actttcgggc gcgcccagat actggtttac gagttcgagc tgctccactt ggcctttgat
21540
atcggccgct atgcacaaca ttttgtcgat tgcagtttca ttgtttttaa cataataatt
21600
tttaactttt ttattttgca atttaatcaa actatttaaa ttcgcttgac ctttcttaca
21660
aagcgcagtt aatatgcaag acattttgac ttataataaa aaacaaaact tttatatatt
21720
catttattgt tcaataataa caaatattcc aggcttaaaa gctaacgaat agggcttttc
21780
ggtaattttc ttattattca tgtccgtcat ctgcatctct ttgccgtact tgacgccgtc
21840
aatggtgccc atcatgtaca ttttaatctc ctccgaaggt ccgtctattt tgtccatttc
21900
gaacaatcta tcaaaatctt caacgctcat tctctgcata tcaagaggaa cgtttctgat
21960
ctttccggtg gcgtaaattg atccgttgtt gtcacggttg attatgtaaa accgacgaat
22020
caacatgtcg cgctcgctag ttttgttctt atccggcaaa tgaatgcaca cgtttggttc
22080
catcttcaaa ggaaaatcgc tttgcaagtg tttttgcaaa atgttgccaa atatattgtt
22140
gtgtttgtga atgtctccgt attgaatgct aaaaaactgg ccaaagttgc ttttggcacg
22200
ttttatggtt ccaaagtcgg aaaaccaaaa tccgcagggc ttgccctgca ctcttggacc
22260
gatggtgtac gtagtcttgc cgttggccgg ctccaacacc acgatatttt tatcgggctc
22320
gggatacaac ttgtcttccc attcgtgcaa actgttcaaa ttagacagtc gacaaaattc
22380
gtttttcaaa aatctgcctt cgaaacaact acaattcagt attgaaaagt tgcctcgttt
22440
cacattaatc gccatctgct cctgccacaa catcttcgtc aactcgtgtg gctccaattg
22500
aatggacgac ggcgtaaaat agcacattac gcccgtttcg tcgtgtttca cgttaaaagc
22560
gccgctgttg tacggcacca gctgctggtc ctcaccacct tccgatcttt cccgcttcgg
22620
ctggttgtcg tcgctgctcg aatatccatc gccaatcttg cgtttagttg ccatgctacc
22680
gacgtgcgct gtctgctgtg gttcaagtct aattgaagtg tttcacagaa tataagatat
22740
ataataaata tggacgactc tgttgccagc atgtgcgtag acaacgcgtt tgcgtacact
22800
actgacgatt tattgaaaaa tattcctttt agtcattcca aatgcgcccc tttcaagcta
22860
caaaattaca ccgttttgaa gcggttgagc aacgggttta tcgacaagta tgtggacgtg
22920
tgctctatca gcgagttgca aaagtttaat tttaagatag atcggctaac caactacata
22980
tcaaacattt tcgagtacga gtttgtagtt ttagaacacg atttgtccac agtgcacgtc
23040
attaacgccg aaacaaaaac caaactgggc catataaacg tgtcgctaaa ccaaaacgac
23100
gcaaacgtgc tcattttgac cgtaacttta acgagctaaa atgaacgagg acacgccccc
23160
gttttatttt atcagcgtgt gtgacaactt tcgcgacaac accgccgaac acgtattcga
23220
catgttaata gaaagacata gttcgtttga aaattatccc attgaaaaca cggcgtttat
23280
taacagcttg atcgttaacg ggtttaaata caatcaagtt gacgatcacg ttgtgtgcga
23340
gtattgcgaa gcagaaataa aaaattggtc cgaagacgag tgtattgaat atgcacacgt
23400
aaccttgtcg ccgtattgcg cgtatgctaa caagatcgcc gagcgtgaat cgtttggcga
23460
caacattacc atcaacgctg tactagtgaa agaaggcaaa cccaagtgtg tgtacagatg
23520
catgtccaat ttacagtcgc gtatggatac gtttgttaac ttttggcctg ccgcattgcg
23580
tgacatgatt acaaacattg cggaagcggg acttttttac acgggtcgcg gagacgaaac
23640
tgtgtgtttc ttttgcgact gttgcgtacg tgattggcat actaatgaag acacctggca
23700
gcgacacgcc gccgaaaacc cgcaatgtta ttttgtattg tcggtgaaag gtaaagaatt
23760
ttgtcaaaac tcaattactg tcactcacgt tgataaacgt gacgacgaca atttaaacga
23820
aaacgccgac gacattgagg aaaaatatga atgcaaagtc tgtctcgaac gccaacgcga
23880
cgccgtgctt atgccgtgtc ggcatttttg cgtttgcgtt cagtgttatt ttggattaga
23940
tcaaaagtgt ccgacgtgtc gtcaggacgt caccgatttt ataaaaatat ttgtggtgta
24000
ataaaatggt gttcaacgtg tactacaacg gctattatgt ggaaaaaaaa ttctccaagg
24060
agtttttaat tcatattgcg cctgatttga aaaacagcgt cgactggaac ggcagcacgc
24120
gcaaacagct gcgcgttcta gacaagcgcg cctacaggca ggtgttgcac tgcaacggca
24180
gatactactg gcccgatggc acaaagtttg tctctcatcc gtacaacaaa tctattcgca
24240
cgcacagcgc aacagtcaaa cggaccgaca gctcgcatcg attaaaaagc cacgtggtcg
24300
acaaacgacc gcgccgctct ttagattctc ctcgcttgga cggatatgtt ttggcatcgt
24360
cgcccatacc acacagcgac tggaatgaag aactaaagct gtacgcccag agccacggct
24420
acgacgacta cgacgacaat ttagaagatg gcgaaatcga cgaacgtgac tctttaaaaa
24480
gtttaaataa tcatctagac gacttgaatg tattagaaaa acaataaaac atgtattaaa
24540
aataataata ataaaactat attttgtaat atataatgta ttttatttaa aaattgtcta
24600
ttccgtagtt gagaaagttt tgtcttgact tcataactct cttctccata ttctgcagct
24660
cgtttacgtt ttttgtgacg cttttaattt tctcaaaatg ctggctgtca atagttattt
24720
tttgcttttg tctattaatt tcttccaatt gagattttaa atctcgctga gattgagatg
24780
cgttgtaatt ccttgagaac atcttgagaa aacatacaga tgaggtaaaa cagcatcttt
24840
tatccaaatt aggagttaat tattattcat ttgtatcgcg accatttgct cgtacacatc
24900
ttccataaaa tggttatttt tattgcgata agtgttggca ttgacatttt gcaaatgtcg
24960
taggttaaag gggcaaatgg gctgcgtggc cgataaaaga ttccagttca acaatccctc
25020
ttcgcccccg tttaacttga aaatggcgct acacgtttct acgctatcgt gttcctgttg
25080
agtggcgcac ggttcgacca gtatcatctt gtgatatgcg gttttgacat tcatgtgcaa
25140
cggaataact tgcgggtcat cgcattcgtc ggaattaagc tttaaatggc gtccgtatgc
25200
tttccaaagt ttttcgtcgt cgaaccgcgg cactgcttgc aagtcgacgc ggggaaacgg
25260
cgctctgtac aaaacgccta aattcaaaaa ctgattgcat tgttgcagct ctgtccaatc
25320
gacgcgattt ttgtaatttt gaaacagcat caggttgaac gccgcgctgg cgcgcacgtt
25380
tgtaatcact gtgtaattga tcagcttgtg ccaatactgg gcattgaaat tttcttcaaa
25440
ctcatttcta aactctggat gcgcaaacat gtgtctaatg tagtacgcgg gcggggcgtt
25500
gaacgcagtc catttgtcaa tacacttcca gtctgaatgt aacgtgttca ccaaaccggg
25560
atattcgtca aacacgagca tgtgatccga ccacggtatg ctgtgggcga tcaattttag
25620
ttcttgcacg cggccttcgc gtaagcaata caaaatgagc gcgtcgctga tcttgacaca
25680
gtcttgcatg tacgcggaca aattaacgtt ttccatacag ctcacattgt ttattagcgc
25740
cgtgttcaag tgtttgtatt tggacacata atcgtagttg atgtactgtt taatgggttc
25800
ttgaaaccat tcttttagta gtatgtgact ggccactatg cgtttccaat ttaatttgtg
25860
tgcgtatttt tgctgcaccg acaacgagag gttattgtaa tttttggata tttcttccat
25920
gtccaacaag tccccaaacg cgagtataaa atcttgcgtc aaaaattttt gctcagacac
25980
caacgaccag atcaaatgtg atttaaacct gttggcgatt gttatcgaca acggcgaaat
26040
tgaaataatt ttccaatcca acttgttgcg aaacacgtga ataaaatcga cgcgtccgta
26100
acattcgcgc gatatgcgct tccaaaacgt gtcatcttgc aaattaagca aatagacacg
26160
attgttggga gatttgacgg ccaattcaat tatttttata tattcttttt gctttaaagc
26220
gcgttgtagc acttgggttg gagccatgtc gactgaagct ccacgctgtt tgaagcaagg
26280
tgaccgtttt ggtcggcatg ttcaaacgtc gattacatgt ttgctttgca tcaaaatggc
26340
gtaattaatt aagaaacaac atgaaagcca tctgcatcat tagcggcgat gttcatggaa
26400
aaatttattt tcaacaagaa tcagcgaatc aaccgcttaa aattagcggc tatttgttaa
26460
atttgcctcg aggtttgcac ggctttcacg tgcacgaata tggcgacacg agcaacggtt
26520
gcacgtcggc cggtgagcac tttaatccca ccaatgagga ccacggcgct cccgatgctg
26580
aaattaggca tgttggcgac ttgggcaaca taaaatcggc tggctacaat tcactgaccg
26640
aagtaaacat gatggacaac gttatgtctc tatatggccc gcataatatt atcggaagaa
26700
gtttggtcgt gcacacggac aaagacgatt tgggccttac cgatcatccg ttgagcaaaa
26760
caaccggcaa ttctggcggc cgtttgggat gcggaataat tgccatatgt aaatgatgtc
26820
atcgttctaa ctcgctttac gagtagaatt ctacgtgtaa aacataatca agagatgatg
26880
tcatttgttt ttcaaaactg aactcaagaa atgatgtcat ttgtttttca aaactgaact
26940
ggctttacga gtagaattct acttgtaacg catgatcaag ggatgatgtc atttgttttt
27000
caaaaccgaa ctcgctttac gagtagaatt ctacttgtaa aacataatcg aaagatgatg
27060
tcatttgttt tttaaaattg aactggcttt acgagtagaa ttctacttgt aaaacacaat
27120
cgagagatga tgtcatattt tgcacacggc tctaattaaa ctcgctttac gagtaaaatt
27180
ctacttgtaa cgcatgatca agggatgatg tattggatga gtcatttgtt tttcaaaact
27240
aaactcgctt tacgagtaga attctacttg taacgcacga tcaagggatg atgtcattta
27300
tttgtgcaaa gctgatgtca tcttttgcac acgattataa acactaatca aataatgact
27360
catttgtttt caaaactgaa ctcgctttac gagtagaatt ctacttgtaa aacacaatca
27420
agggatgatg tcattataca atgatgtcat ttgtttttca aaactaaact cgctttacga
27480
gtagaattct acgtgtaaaa cacaatcaag ggatgatgtc atttactaaa ataaaataat
27540
tatttaaata aaaatgtttt tattgtaaaa tacacattga ttacacgtga catttacgat
27600
ggcgaacaat aatttcactt tttatattag gacacgacgt gtatatagga aagcttaagc
27660
gtttcaataa agccatggcg tacacgctaa gcttgcccag cttgcggctc tttgaaatct
27720
gtagttttcg gggagtaccg tcgttcttca gtgccacata cgtcaacttg cgatcgtaca
27780
ctttataata cgtgttgtag ttattttttt ccagaaattc cctcataaag caatccttgg
27840
ataaagtttt tgatccgtac agttggccac accggtccat gcacaggtac acacacgtga
27900
tggcgttttg aatgacgatg cgatttctgt caacggcaac gcgcttgaat atggtgtcga
27960
cgttgtccga ttcaatggtt ccgtaaacag ctccgtctgg atttactgcc aaaaactgcc
28020
ggttaataaa cagctggccg ggaatagacg tgcccgtgat gtgtgtcagc agagctgagc
28080
agtcagccat agaggctaga gctacaagtg ccagcaagcg atacatgatg aactttaatt
28140
ccccacagca aactggcgct tttatataaa aatttgggcc atttttggcg attagataat
28200
ttttgaagat tagataatat tgagattagt taataatttg tgtgattaga taacttttta
28260
gggtattgcg cattataaat caaggtcgag ttgtataaac tgctctggcg tgtaaaactg
28320
cagacttaag ttttttgcaa acactcggtc tgaatcgcta aaatctttct gaccggtggt
28380
tagattaatt cggccagccg cgtcgcccac ataaaaagat tgttccttgt caatatgcgt
28440
aaactgtttg gccatctcgc gccacattcc cgtgtcgggc tttcgatgct catccttgtt
28500
gggcgacaca taaaacgata tgggcacgcc agtagctttt ttaatattct ctaatttata
28560
taataaatcg ctcgctttga ttttgccgga acctaaatgg gcttggttcg taaaaacaac
28620
taaatcgtag cctaattcgt acaaacgctt tagcttgtgt gcgcacggaa ggagctgcca
28680
gtcgtctggg ttttttggaa atttggaccg tgtctttgag ctaattagcg tgccgtccaa
28740
atcaaaagcc gcaattttgg ttcttttagc gccgtcatga accgcgtacg catacaaatc
28800
gggctgctgt aacgtccaca tggtgaatgc atcttactca aagtccatca attcgtacgc
28860
gtttgtgtcc aggtcgggcg ttgaaaaatt gtagcttgcc attagatcgg atagcgattc
28920
aaattttgta agcgtttgta gcgcacgttt ggcatcttgt ttaaaattac acgacgacag
28980
acagtaaaaa tattcctcga taagcatgac tacacccata tcactgttta agtgctcgac
29040
gtagttgttg catgttatgt cgcgtgtgcc gcgatacgcg tgatttcggt gaaaatcaca
29100
ccacaaccag tcggcgtgcg tgtaacaaag tcgacagcga aacaatttat cgttttccaa
29160
aaaatttaaa tactcgacag ttttgcagct tagattccgc gtttgattca ccttaaaatc
29220
gtcgtcagcc tctataatct cgggcaacag cttgccttgt tgccccatcg tatcgatcac
29280
ctcccccaag tggcccggtg ttatattaag tcgtttaaaa tcatttattg cttcctgcac
29340
gtcggcctgg taatttttga ccacgggcgt ggaaatcaat tgccgttgaa gggaaataat
29400
tcgtggtgtg ggtatcggcc gcctgttgca caattccacc agcggtggag gcaagggcgc
29460
attcacagca accgttgtca tttataagta atagtgtaaa aatgcaaata ttcatcaaaa
29520
cattgacggg caaaaccatt accgccgaaa cggaacccgc agagacggtg gccgatctta
29580
agcaaaaaat tgccgataaa gaaggtgtgc ccgtagatca acaaagactt atctttgcgg
29640
gcaaacaact ggaagattcc aaaactatgg ccgattacaa tattcagaag gaatctactc
29700
ttcacatggt gttacgatta cgaggagggt attaataata acaataataa aaaccattaa
29760
atatacataa aagtttttta tttaatctga catatttgta tcttgtgtat tatcgctaac
29820
cattaaaagt gctggagcca cagtgttgcg gcgagtcttt atagaagatc gttgtttggc
29880
tggaactgag cttttccttt tcctgctgcc gctaatggga gtgggcacgt actctgtagt
29940
agacggtgca acgggcaact tgagcgctac cgtcttaaat ttggccatac ttttagtgat
30000
gaaatcgcgc gttaacactt cgtcgtaaat gttacttagc agaggcgcaa cattgtgatt
30060
aaatgtctcg tttaacaagc tgtaaaactc cgaataaagc ttatcgcgca tttcgcagct
30120
ctccttcaat tctgccaaat ttgcgttggt aagcaccaca gtctgtcttt ttttgctcgc
30180
tggaattgct gcgttctcgc ttgaagacga cgatgtcgat cggtcggcca tttttttgcc
30240
cagcttttca gtgtgatcaa aaatgaacac aaaatctgcc aattcgggct tgtttttcac
30300
caaatcccac atggccgggc tactaggcca ctcgggctgc ttgatcttag tgtaccaact
30360
gttaaacaaa atgtatttat tgttgttaat cactttcttc ttgcgtttgg acattttgcg
30420
ttcgtcttgc atgacaggca ccacgttaag gatatagtta atgttctttc tttccaagaa
30480
atttacaata acggccagct ggtccatgtt ggatttgttg taagagctcg attccagttt
30540
attcaacagc ttttcatttt tgcacacggc cgcagtctcc ggagattgtt gctccggcac
30600
gtttaccatg tttgcttctt gtaaaccttt gaaacaaccc gtttgtattc ttgatgatat
30660
atttttttaa tgcccaacaa cctggcaatt cgtttgtgat gaagacacac cttacgcttc
30720
gaacatttgt cggtgattac tgtgaaatgg cctaaattag ctcttatata ttcttttata
30780
cgctcaaacg acacgatgtc caacatgtgc gcgcagacgt tttctgtgtt catcgtgtgc
30840
ttgagcgtgt tgatggcttc cctgaacagc gcttgtattt cgctgcgagt caagcagtcc
30900
gaatcacacc cgcctaagtg cgtgcaattt ttggggggca tcgttgtcta tctttttcag
30960
agtggcgtag aaaaagtcct gcaattgcct attatcaaaa cgcgccttga cgctgcgcac
31020
aaaatcaaaa aattcaatgt aattgctgta atcgtacgtg atcagttgtt tgtcgttcat
31080
ataattaaag tatttgttga gcggcacgat ggccaggctg cgcgctattt cgcaattgaa
31140
gcgtcgcggt tttaacatta tacggtagtc attgccaaac gtgcccggca acaacttcac
31200
ggtgtacgtg ttgggtttgg cgttcacgtt aatcaagttg ccgcgcacga cgcctacgta
31260
tatcaaatac ttgtaggtga cgccgtcatc tttccattgt aacgtaaatg gcaacttgta
31320
gatgaacgcg ctgtcaaaaa accggccagt ttcttccaca aactcgcgca cggctgtctc
31380
gtaaactttt gcgtcgcaac aatcgcgatg acctcgtggt atggaaattt tttctaaaaa
31440
agtgtcgttc atgtcggcgg cgggcgcgtt cgcgctccgg tacgcgcgac gggcacacag
31500
caggacagcc ttgtccggct cgattatcat aaacaatcct gcagcgtttc gcattttaca
31560
tatttgacac ttaaaaaatt gcgcacacga gcaccatcgt ttgataccta attgcaacta
31620
tttacaattt atcagtttac gttgaacccg ttttaatttt ttagatccgt ccttgttcag
31680
ttgcaagttg actaaatgac aaaatttttc ggttctgcaa aaccgccctt gtctgttcca
31740
cccgttgtat ttgaaaaaac tttttttcac gcggcgacaa ctgcttgtat aatattgccc
31800
aatgtaaaca tgcaaaattt tgttactctc gtcaaaacag cggttggcgt tccattccat
31860
aattttttta ttatttatca acgatggcca ttgtaaattg tcgtcattta tacgcatcat
31920
atgatttaac aaaagctttt cgtatagcgg aacttcaatt cccttggaac atttttcaaa
31980
cgataattta atttgtttct cggttggcag catttcatgc ttgattaaca atcgcctgac
32040
ttttatagcc acgtttatgt ctttgcacag caaatgtggg ttgtcgacaa tgtaatagtg
32100
caaagcattt gttacggcaa atgcgtagtt tgatttgacg acgccctttt tcttgacggg
32160
cattgcggct tttaaaatta cttgcaagca ttgtacgaat acctctttgt gtttaaacaa
32220
taatatggac aaacatcggc gaaacaattt gtaataatta tgaaatccca aattgcaggt
32280
tttaaacttc tttgttactt gttttataat aaataaaatt tgctgaccca tgtctgcgcc
32340
cacaacttta attaaccatt tgtgcgcata ttgattgtct cgttgttccc aaccggaaaa
32400
ttgattgatc tcgagccacc ggcattggtc gtttgatacc gtcgttaacg ccgacgctcc
32460
tgcctgtttg attacgggtt ctaaaagacg aaacagcagc gtaaatttgt ttttgcgtcg
32520
gtagtatttt ggcaggcaat aatcaaaaaa atccgtaagc aattctctgc atctattaat
32580
attcgttgcg tacgaatcga gtttttcaaa aattactttg tttgtatgaa aataacgttt
32640
gggcttctca caataataat cttcgttgta gaacagaaac ggtttgcgag aattggcacg
32700
tttgtccatg attggctcag tgtaacgatt gattcaaatc aaaattgaca acacgtttgc
32760
cgtaatgtgc accggttcgc acacgtttgc cgcgtatgta atccatgttt atttcgctgt
32820
cgcaattgat tacacgattg tgttgggcgg cgcgttttat tgaatttagg cgacgcgtcg
32880
acaactccaa aggattgtaa agcgcagatt tttccagagt aaacgagttt aagtggccac
32940
cgttgaacca ttccagagcc acgattgtgt acagcaaaaa gaatatttct ttgtcgacgt
33000
tttcaaacgc aaacttgttt tttaggcaat agtagtaaaa ttttaacgaa ttgtataaat
33060
aaaacataaa attgccattt ttaaagtaaa attctacatc cgtgacgaac aaaaggttta
33120
ctattttgtt ctccaacaag tgtgccaatt ttcttaagta caccattgaa tttttgtcgt
33180
cgtccatctc gatcaacaac acgtacggcg ttttggaatt taaaattatt ctaaaatttt
33240
cctgttgcaa cgattccaca gcgtccgacc aatatgacgc tgccacctct agacagatgt
33300
atttcttgga aaacacgtgt cgtttgataa cctcgctgat ggacgtgatc gattgtaaat
33360
acttttcaaa cgtcgcgtct tcccaaccac gcaccgacac gggcgctgtc gtgtcgggct
33420
gatgtttgaa atccaaacca ctctgaatta acttggttgt gattcgtatg ctcaactgtt
33480
gacccaacgt gtagtgatct tcgtaggcgc gctcccacat cacgttacac acaaatttga
33540
cgagatcatc aacgtctttc tgttgcaaaa ttcgccgcaa acgcgccaca tcgcccttgt
33600
accaccgatc tcggcacaca agctgtagca tttttaaatc gtgatcgctc aagctattaa
33660
ttctggttag atttatatag tcgtcaatat cctcgggcgt ggtttgcgtc atgtctgtaa
33720
aacgtgcaaa atcaaacatt tttatgttgt agtcgaatct aacaaatcca tcggcgttca
33780
cttgcacttc gcgctttaca aaacgaggta gcgtgtaatc gaacccgttt aaatagattg
33840
cgtacaaaac cagcacttca tcttccagtt tgcacgcttg cggcaaaaat tgtgtggtgt
33900
gctccaaccg ggtgacaaac atgactatgg aaaataacgc ggaattcaac agacgactag
33960
agtacgtggg cacgatcgcc acaatgatga aacgaacatt gaacgtttta cgacagcagg
34020
gctattgcac gcaacaggat gcggattctt tgtgcgtgtc agacgacacg gcggcctggt
34080
tatgcggccg tttgccgacc tgcaattttg tatcgttccg cgtgcacatc gaccagtttg
34140
agcatccaaa tccggcgttg gaatatttta aatttgaaga aagtctggcg caacgccaac
34200
acgtgggccc gcgttacacg tacatgaatt acacgctttt taaaaacgtc gtggccctca
34260
aattggtcgt gtacacgcgc acgctacaag ctaacatgta cgcggacggg ttgccgtatt
34320
ttgtgcaaaa tttttcagaa acaagctaca aacatgttcg tgtgtatgtt agaaaacttg
34380
gtgcgataca agtagcgaca ttatcagttt acgaacaaat tattgaagat acaataaatg
34440
aactcgtcgt caatcacgtt gattagataa tgtccgtgtt aaatgtgata tcttagatta
34500
cgagcgcgca ataaccatag tttaatcgaa gagaatagcc gtcgccacaa tggataatta
34560
caaattgcaa ttgcaagaat tttttgacca agcgcccgac aacgacgatc ccaactttga
34620
acatcaaacg cccaatctat tggcgcatca gaaaaaaggc atacagtgga tgattaacag
34680
agaaaaaaac ggccggccca acggcggcgt gcttgccgac gacatgggac tcggcaaaac
34740
gctctctgtg ctaatgttaa tcgcaaaaaa caactctcta caattgaaaa ctctaatagt
34800
gtgtcctttg tctttaatca atcattgggt aaccgaaaac aagaagcata atttaaattt
34860
taacatttta aagtattaca aatctttgga tgccgacacg tttgagcatt accacattgt
34920
ggtgaccacg tacgacgttt tattggcaca tttcaaattg atcaaacaaa ataaacagtc
34980
aagtctgttt tcaacccgct ggcatcgagt tgttctagat gaagcgcata ttatcaaaaa
35040
ctgcaagacg ggcgtgcaca acgccgcgtg cgctttgacc gcaacaaacc gatggtgcat
35100
taccggcaca ccgatccaca acaagcattg ggacatgtac tcgatgatta attttttgca
35160
atgtcgtcct tttaacaatc caagagtgtg gaaaatgtta aataaaaaca acgactctac
35220
aaatcgcata aaaagtatta ttaaaaaaat tgttttaaaa cgcgacaaat ctgaaatttc
35280
ttctaacatt cctaaacaca cggttgagta tgtacatgtt aattttaatg aagaagaaaa
35340
aacgttgtac gataaattaa agtgtgaatc ggaagaggcg tatgtgaagg ctgtggcagc
35400
gcgtgaaaac gaaaacgcac taagccgatt gcagcaaatg cagcacgtgt tatggctaat
35460
actgaaattg aggcaaatct gctgccaccc gtatttggcc atgcacggta aaaatatttt
35520
ggaaacaaac gactgtttta aaatggatta tatgagcagc aagtgcaaac gagtgctcga
35580
cttggtagac gacattttga acacaagcaa cgacaagata atattggttt cgcaatgggt
35640
ggaatattta aaaatatttg aaaacttttt taaacaaaaa aacattgcta cgttaatgta
35700
cacgggccaa ttaaaagtgg aagacaggat tttggccgag acgacattca atgatgctgc
35760
caatactcaa catcgaattt tgctgctttc cattaagtgc ggcggcgtcg ggttaaactt
35820
aataggcgga aaccacattg taatgttgga gcctcattgg aacccgcaaa ttgaattgca
35880
ggcgcaagac cgaatcagtc gtatgggaca aacaaaaaac acgtacgtgt acaagatgct
35940
aaatgtggaa gacaacagca tcgaaaaata cattaaacaa cgccaagaca aaaagattgc
36000
gtttgtcaac acggtctttg aagagactct gctcaattac gaagacatta aaaaattttt
36060
caacttgtag ctggtaagtc gtcatgaaca cccgatatgc tacttgctat gtttgcgacg
36120
agttggtgta cttgtttaag aaaacgttta gtaacatgtc cccttcggcc gctgcgtttt
36180
accaacggcg catggccatt gttaaaaacg gtatcgtgct gtgcccacgt tgttcgtcgg
36240
aactaaaaat tggcaacggc gtttcgattc caatttaccc ccaccgcgct caacaacatg
36300
cacgacggtc gcgttaagac gcaagcgctt cgagttttgg cccgctcgct acctccgctg
36360
tacgactcga ccgtcgatcg acacggctgc aaggtgttca cggtgcggcg ctacaacaga
36420
cgcgtaatcg actttgcggg cattcgcaac aaaacgctgg aaatcattaa aacggataga
36480
aacttgccgc tcaacacaga atgcaatgtg aaagttgtcg acagtgcatg catgcgttgc
36540
agaaaaagtt tcgcagttta ccccgccgtt acctatctgc attgcggaca ttcgtgtctg
36600
tgcaccgact gcgacgaaac ggtaaacgtg gacaacacgt gtcctaaatg taaaagcggc
36660
attagatata aattaaaata caaaactttg taacatgttg ccctacgaaa tggtgattgc
36720
cgtgttggtt tacttgtcgc cggcgcagat tctaaattta aaccttcctt ttgcatacca
36780
aaaaagtgtg ctgtttgcca gcaactctgc aaaagttaac gaacgcatca ggcggcgagc
36840
gcgtgacgac aacgacgacg acccctattt ttactacaaa cagttcataa agattaattt
36900
tttaactaaa aaaataataa atgtttataa taaaactgaa aagtgtatta gagcgacgtt
36960
tgatggtcgg tatgtggtta cacgcgacgt tttaatgtgc tttgtaaaca agagttatat
37020
gaagcaattg ctgcgcgagg ttgacactcg cattacacta cagcaacttg ttaaaatgta
37080
tagtccagaa tttggttttt atgtaaatag caaaattatg tttgtgttaa ctgaatcggt
37140
gttggcgtct atttgtttaa aacactcgtt cggcaaatgc gagtggttgg acaaaaatat
37200
aaaaactgtg tgtttacaat taagaaaaat ttgtattaat aataagcaac attcgacatg
37260
tctatcgtat tgattattgt catagttgta atatttttaa tatgtttttt gtacctatca
37320
aatagcaata ataaaaatga tgccaataaa aacaatgctt ttattgatct caatcccttg
37380
ccgctcaatg ctacaaccgc tactactacc actgccgttg ctaccaccac taccaacaac
37440
aacaacagca tagtggcctt tcggcaaaac aacattcaag aactacaaaa ctttgaacga
37500
tggttcaaaa ataatctctc atattcgttt agccaaaaag ctgaaaaggt ggtaaatccc
37560
aatagaaatt ggaacgacaa cacggtattt gacaatttga gtccgtggac aagcgttccg
37620
gactttggta ccgtgtgcca cacgctcata gggtattgcg tacgctacaa caacaccagc
37680
gacacgttat accagaaccc tgaattggct tacaatctca ttaacgggct gcgcatcatt
37740
tgcagcaaac tgcccgatcc gccgccgcac caacaagcgc cctggggccc ggtcgccgat
37800
tggtaccatt tcacaatcac aatgcccgag gtgtttatga acattaccat tgtgctaaac
37860
gaaacgcagc attacgacga agctgcgtcc ctcacgcgtt actggctcgg cttgtatctg
37920
cccacggccg tcaactcgat gggctggcac cggacggcag gcaactcaat gcgcatgggt
37980
gtgccctaca cgtacagtca aatgttgcgc ggatattcat tggcgcaaat taggcaagag
38040
cagggaatac aagaaatcct aaacacgatc gcgtttccgt acgtgactca aggcaacggc
38100
ttgcacgtcg attcgatata catcgatcac attgacgtgc gcgcttacgg ctatttgata
38160
aattcatact ttacgtttgc ctattacacg tactattttg gagacgaggt aatcaacacg
38220
gtgggtttga cgagagccat cgaaaacgtg ggcagtcccg agggagttgt ggtgccaggc
38280
gtcatgtctc gaaacggcac gttgtactcc aacgtgatag gcaactttat tacgtatccg
38340
ttggccgtcc attcggccga ttactccaaa gtgttgacca aactttcaaa aacatattac
38400
ggttcggttg tgggcgtaac gaataggttg gcttactacg aatccgatcc cacaaacaac
38460
attcaagcgc ccctgtggac catggcgcgg cgcatttgga atcggcgcgg cagaattatc
38520
aactataatg ccaacacggt gtcgtttgag tcgggtatta ttttgcaaag tttgaacgga
38580
atcatgcgca tcccgtcggg caccacgtcc acgcagtcgt tcagaccgac cattggccaa
38640
acggctatag ccaaaaccga cacggccggc gccattttgg tgtacgccaa gtttgcggaa
38700
atgaacaatt tgcaatttaa atcgtgcacg ttgttctacg atcacggcat gttccagcta
38760
tattacaaca ttggcgtgga accaaactcg ctcaacaaca caaacgggcg ggtgattgtg
38820
ctaagcagag acacgtcggt caacaccaac gatttgtcat ttgaagcgca aagaattaac
38880
aacaacaact cgtcggaagg caccacgttc aacggtgtgg tctgtcatcg cgttcctatc
38940
acaaacatca acgtgccttc tctgaccgtt cgaagtccca attctagcgt cgaactagtc
39000
gagcagataa ttagttttca aacaatgtac acggccacgg cttcggcctg ttacaaatta
39060
aacgtcgaag gtcattcgga ttccctgaga gcttttagag ttaattccga cgaaaacatt
39120
tatgtaaacg tgggcaacgg cgttaaagcc ctgtttaatt atccctgggt aatggtcaaa
39180
gaaaataaca aagtgtcttt catgtcggct aacgaagaca ctactatacc atttagcgtt
39240
ataatgaatt ccttcacctc tatcggcgaa ccagctttgc aatactctcc atcaaattgc
39300
tttgtgtatg gaaacggttt caaattgaac aacagcacgt ttgatttaca atttattttt
39360
gaaattgtgt aattatattt agggagaatg tgatattcaa aagactgact gttaacacaa
39420
aagactgata ttgttgttgt tacaaaatag ataataaaac aaaaaataaa ttaaatatta
39480
tttatttatt aaactgttta attttaatgc taacgcgtac aaatcacgct gttccgacgt
39540
ggacatggaa ttgcgcagaa aagtcttgat agtgtcgatt tcttcgccgt catccacttc
39600
catatatttg atttcttcct cgatttgcat ttccaagttt gcgtattctt gcaaataata
39660
atctagtcgt tgggcgacct cgccaatttt aaataataca ttatccgaca ccaaatgcca
39720
gcgagtgact gtgcgctcca tcatcctggc actttttaat gtgaatatta aaaggttgtt
39780
gcatatatat cgttaaacgt ttatgtttac tttcacgtta gctcgtttca ttgatgtaaa
39840
catttagttt tataacagcg tcggtaattt tattttttaa agtaaacaga ccaaaatcaa
39900
aggtgtcttc gacaggtacg attattttcc cattgacact gttttcgtgc acagatataa
39960
ttttatcacc gtttattatt ttgcccaaac acacgtactc gtttcttctc aagccaacta
40020
tttctaaaca attcactttt ctattatcgt gtacgcaatt aaaagtaaac gaagcgctac
40080
aattgtcgta ttctattaca attctgcggc atttataaaa tttattaatg ttgacgcaaa
40140
ttccatgcag cgcatccatt tcgtactgca aatgcggcgc aattaaaaaa tttcctcgtc
40200
gttgttaaca atcttgggcg ctaaaaagca cgccaacacg cccacgtctt taatgcaata
40260
ttccaatttg aacggcagtt cctcggacat gtatattgtc acggtgggcg ccaaaggagc
40320
ggctttagca aaatgacaca agtaatcgcc cgcaaaagtg tgcgttacgg tttgctttgc
40380
tttgagaacg gaaaagtttt cgttgtccgc gctcatctgc acgtccgccg agccaatgtc
40440
gccatttgct ctaaactgca gacccttctt ggaacacgac acaataatat cgtggtcgaa
40500
ttgcgtcatg tctttgcaca cctgcgcaaa ctcgacgctc gacatgtgga cgacgcaatc
40560
gtaatcgcta tccggaattc ccaaatgttc cacgtcgatg cacatcaact tgagcgtgta
40620
cgtgcagatt ctattgtcgt tgttgaacac gaacgccatc acatcgccct gatcttccgc
40680
tttcatcagt acagagctgc gctcgttaac gcatttgaca attttactta aactgtttat
40740
ggacacgttg agcggcacgt tgcggtcaca tctatatttt ttgaaaccct cggcgtgtag
40800
ttgcaacgac acgagcgcga catgcgaggt gtccataacc tgcatgctta cgcctcgatt
40860
atcacaatca aaagtagcgt gcggcagcag atccttaaaa gtttccacca gcctcttcaa
40920
aactgcgccg gttttaaatt ccgcttcgaa catttttagc agtgattcta attgcagctg
40980
ctctttgata caactaattt tacgacgacg atgcgagctt ttattcaacc gagcgtgcat
41040
gtttgcaatc gtgcaagcgt tatcaatttt tcattatcgt attgttgcac atcaacaggc
41100
tggacaccac gttgaactcg ccgcagtttt gcggcaagtt ggacccgccg cgcatccaat
41160
gcaaactttc cgacattctg ttgcctacga acgattgatt ctttgtccat tgatcgaagc
41220
gagtgccttc gactttttcg tgtccagtgt ggcttgtttt aataaattct ttgaaaatat
41280
tgtcgggtgt attattaaat agcatgtatg gtatgttgaa gatgggataa cgcttggcgt
41340
gcgggtcgtc atgatttcca ccgcgcacca catatttgcg ctcaatttta tcaaaattgg
41400
actggcgaga caaaaacgag acgggcgaca ggcatatttg ggcgtgcgta ccatcttcgg
41460
ccatccactc ggtcaggtct tcgctgcggt taaacacacc tttctgaccg tgaatgccac
41520
atatttttat tccttccaaa tcgttggtgg acgtgactat gactatttta agcataacgt
41580
tgtcgccgtt aaccaccatg ctggcgtcga gtttttcaat tttttgattt ttaatttgtc
41640
taaagtaaac gtacactttg taaacgttaa aattgccgtt ggtgcacgtt tcaattttgt
41700
accgtcggcc gtcgtacacc caattaatct ttgcgttgct caccaacaca ccggccatgt
41760
acagcacaag tccgtcgtct agcgcaacgt aatttttgtc gctactattc gtaaacttta
41820
ctaaacacga ctgcttgggg ccgaccacaa gcttgccctt caatttgttc actttgttgt
41880
tgtataaaca aatgggcagc gcaatgtgcg gaatgtacgg atcttcggcg gtcatgagtt
41940
tattgtctcg caccaacgtc cacaatttaa acattttatt gttgagcaaa atggacttgt
42000
ttaccgccac agagtagcca tttggtaaac ccgatacgca attttcctct ttgtactcaa
42060
acacgggcat ggcattcttt agattggtta gggacacaat caatttgggt acgggcgtgg
42120
tatgaaataa atgtataaaa ttacgataat aatactgctc caacttggac atgagcgatt
42180
tgacgtcatc gttttctacg atcgtacact gaataatggg attatagtat atagaatgtt
42240
tatagtggta ttcgtagggt gtcaacaata cgttaatgtc ggcttcgttg ttcacccgca
42300
actttttttt gatgcatatc attccttcgt gatgattaac gtaaagtatt ctgtctgtaa
42360
tcttcaattc gatgggcgcc atgtttcttt tcatagtgta cacgataaac gacgtgtttg
42420
attttaaaca ttttaaattt gtgggtctat cattaaacgc gatcagcaac gagtcgtctt
42480
gaacgtcgtt gaggtcgtcc acgaacgcga ccagattgtg ttttagcaaa tattgaaatt
42540
tttgcgcaac catttcgtag tccacgttgg gcaaacatgc gttgcggcaa aggaaaaact
42600
ttttgcccgc cacggtcatt tcgccgtgaa aaaaactgcc aataaatttc acaaaatcct
42660
ttttttgctt caacattttc tggcgcatgc tgtcgttggt gattcgcgcc acctcgttgc
42720
cgacgcgata ttttaacacg ggcaacgaaa tttcaatatt gttattgctg ctgttgtcct
42780
gttgattggg aaagactttg cgttgcttgc taaaagtttt cgatacgcaa tatatgagac
42840
gcccgttgac tatacaatcg acaatctttt tcgactcttt gttgtacaag acgctttgaa
42900
ttttacgacg cttgttcgcc accgtgtacg cgtcgtcgtc ggccgtcttg tcgagaactc
42960
gttgatagtt ttgcaaaatt gtcgaagtta ataacagttc tatcaaatag gcgtgcttgt
43020
atacaatttt gttggccaaa ctgtctatag aatagtttat gtcgtgattc ataataattt
43080
ttatgtgttc cacgagttgt tgcttgtgaa gcgtgttgta ttcgaagaga aaatcgagcg
43140
gtttccattt gccgctgttg gccagatatg tttccagcac agaatttaaa tcttccgtca
43200
ctacgtaatc gctagcgtac acgtctcgag caaacaggac gtcgtcttgt ttgtcgtaaa
43260
ctagttggat tgcgcgattg atgtgcttct cttgatccac gttgccgtac aaaaacatgc
43320
gtttgcaatg tttggcgtat agcttgtcgt agaaattgtg caccaaaacg ttgttgttca
43380
tcattatgtt gggaaaactc aaaaatctgc cgtccagcat aaaagttccg ttaatattgt
43440
tgtttgcgtc gacatcgtcc gtttctctaa attgcttgtc taagcgcgtg ccgaatataa
43500
cgggcacaca tttatgcatt acgcaactga gctgttcatt aagagcgcaa cacaaataag
43560
acttgcgttc ttgaatagcg caaaaaagca tacgttcatt gctgtttgta gcgcaatcaa
43620
aagtatattt taatttgtat ttattttcaa ttctatcgta caactcgttg aaatcttgaa
43680
ccacgtccgt catcgtgaag cgattactgc gcactaatta tgtctaaacg tgttcgtgaa
43740
cggtcggttg tttcggatga aacggccaaa cgcattcgac aaaacgaaca ctgtcatgcc
43800
aaaaatgaat cttttttggg gttttgcaac ttggaagaaa ttgattatta tcaatgttta
43860
aaaatgcaat acgttccgga ccaaaagttt gacaacgatt ttattttaac agtgtacaga
43920
atggccaacg tggtgacgaa acaagttaga ccgtataaca gtatcgacga aaagcaccat
43980
tacaacacgg tgcgtaacgt gttgatttta ataaaaaatg cgcgtttagt gcttagtaat
44040
agtgtcaaaa agcaatacta tgacgatgtg ttaaaattga aaaaaaatac agacttggaa
44100
tcgtacgatc cattgattac ggtcttttta caaattggcg aatctgtaaa tgaagaaata
44160
caaaaactca gaaaagcttt ggtcaatttt tttactaata aacccgacaa gtcggatata
44220
aacaacccag atgtagtttc gtatcaattt atttttggca gagtacaaaa attgtataac
44280
agggcaatta aacaaaaaac taaaactata attgtaaaac gtcctacaac tatgaacaga
44340
attcaaatag attggaaaac tctttccgaa gacgaacaaa aaatgactag acaagaaatt
44400
gccgaaaaaa ttgtaaagcc ttgttttgag caatttggca ctatattaca catatacgta
44460
tgtcctttaa aacacaaccg aattattgtc gagtatgcaa actcagagtc ggtacaaaaa
44520
gccatgactg taaatgacga cactcgattt acagttacag agttttccgt ggttcagtac
44580
tacaacgtgg ccaaaacaga aatggtgaac cagcgaattg acataataag caaggacatt
44640
gaggatttaa gaaacgcttt aaaatcttac acataaatta aaatatcgaa caaaggaaaa
44700
aaacaattgt aacaaaaata atttacatta aaatttacaa gtttttttct agtgtcgtac
44760
ttttttacaa tgcgtctgtt gtccgtcgag cattgcaaac atattgtgga cggcgcaaaa
44820
tagcaaacaa aaggcacgtc cgcgctctcc cacgctattc taaaacgatg aatccatatt
44880
aatttttcat tgtcgccaaa cgtcgctccg ctggcctcct tccaataaca aatactcaga
44940
aacacaaaca tgtacaattg ctgtcgcggc gttaattgtc gctgtttttc caaatagtct
45000
attatgggaa acaaacactt gtcacaacac aaatactcgt taattgtcac aaccgacaag
45060
cacatttggc aaaatgcgtc gcaatttttg tacggacgag attctatgcg aagttcgttg
45120
tccatgacgt cttgggtcca ctttttcaac aagacacttt tatatttgtg atttgtacaa
45180
ctttggtacg tgttagagtg tttttgataa gctttgataa gtttaaaact gttggagtaa
45240
ggccacgtca ttatgttctg caccttttgt ttaaaagaca gaaattacta tatgttcaaa
45300
ctatttaaag attattggcc aacgtgcacg acagaatgcc agatatgtct tgagaaaatt
45360
gacgataacg ggggcatagt ggcaatgccc gacactggca tgttaaactt ggaaaagatg
45420
tttcacgaac aatgtattca gcgttggcgt cgcgaacata ctcgagatcc ctttaatcgt
45480
gttataaaat attattttaa ctttccccca aaaacactag aggagtgcaa cgtgatgctt
45540
cgagaaacta aagggtttat aggcgatcac gaaattgatc gcgtttacaa acgcgtttat
45600
caacgcgtta cacaggaaga cgccctggac attgaactcg attttaggca tttttttaaa
45660
atgcaatcat gacgaacgta tggttcgcga cggacgtcaa cctgatcaat tgtgtactga
45720
aagataattt atttttgata gataataatt acattatttt aaatgtgttc gaccaagaaa
45780
ccgatcaagt tagacctctg tgcctcggtg aaattaacgc ccttcaaacc gatgcggccg
45840
cccaagccga tgcaatgctg gatacatcct cgacgagcga attgcaaagt aacgcgtcca
45900
cgtaacaatt attcagatcc cgataacgaa aacgacatgt tgcacatgac cgtgttaaac
45960
agcgtgtttt tgaacgagca cgcgaaattg tattatcggc acttgttgcg caacgatcaa
46020
gccgaggcga gaaaaacaat tctcaacgcc gacagcgtgt acgagtgcat gttaattaga
46080
ccaattcgta cggaacattt tagaagcgtc gacgaggctg gcgaacacaa catgagcgtt
46140
ttaaagatca tcatcgatgc ggtcatcaag tacattggca aactggccga cgacgagtac
46200
attttgatag cggaccgcat gtatgtcgat ttaatctatt ccgaatttag ggccattatt
46260
ttgcctcaaa gcgcgtacat tatcaaagga gattacgcag aaagcgatag tgaaagcggg
46320
caaagtgtcg acgtttgtaa tgaactcgaa tatccttgga aattaattac ggcgaacaat
46380
tgtattgttt ctacggacga gtcacgtcag tcgcaataca tttatcgcac ttttcttttg
46440
tacaatacag tcttgaccgc aattcttaaa caaaacaatc cattcgacgt aattgccgaa
46500
aatacttcta tttcaattat agtcaggaat ttgggcagct gtccaaacaa taaagatcgg
46560
gtaaagtgct gcgatcttaa ttacggcggc gtcccgccgg gacatgtcat gtgcccgccg
46620
cgtgagatca ccaaaaaagt ttttcattac gcaaagtggg ttcgaaatcc caacaagtac
46680
aaacgataca gcgagttaat cgcgcgccaa tcagaaaccg gcggcggatc tgcgagttta
46740
cgcgaaaacg taaacaacca gctacacgct cgagatgtgt ctcaattaca tttattggat
46800
tgggaaaact ttatgggtga attcagcagt tattttggtc tgcacgcaca caacgtgtag
46860
catcgccagt atttaacagc tgacctattt gttaaacaag cattcttatc tcaataattg
46920
gtccgacgtg gtgacaattg tatccacaat catgaaaaaa gtagcgcttg gaaaaattat
46980
cgaaaacaca gtagaaagca aatataaaag caacagtgtg tcgtcgtcat tgtcaacggg
47040
cgccagtgca aaattgagtt taagcgaata ttacaaaact tttgaagcaa ataaagtggg
47100
ccagcacact acgtacgacg tggtcggcaa gcgagattac acgaaatttg acaaattggt
47160
gaaaaaatat tgacatgctg cgatcaatca tgcgacgttt caagagtaca aacaatctca
47220
gcaaaaaacc ctccgattat tatgtagtgt tatgtccaaa gtgttatttt gtgacgtcgg
47280
ccgaagtgag cgtggctgaa tacatagaaa tgcataaaaa ttttaacacg aaattcgccg
47340
atcggtgccc taacgatttt attgtgacca actctaaaag ttggaataat catgaaaatt
47400
gttctgccct attttaccct ctgtgttaat aaagtttgtt gtttgtattt tgtggtttta
47460
tttatttacg ctagatattg ggtttaaggt tcttagaaat agagttgtat tttccctacc
47520
aaaagggatt tgagcttcat ataaatacaa ttttcgctcg acaagcggtt tatttcactc
47580
ggaggtatta tatcaggcag tcgaacgtgc gcgatgaaac atcccgttta cgctagatat
47640
ttggagtttg atgatgtagt gttagatttg actagtttaa tatttttaga gtttgataac
47700
gctcaaaatg aagagtacat tatttttatg aatgtaaaaa aggcgtttta caaaaacttt
47760
cacattactt gtgatttgtc gcttgaaacg ctgaccgtgt tggtgtacga aaaagctcgc
47820
ctaattgtga aacaaatgga gtttgagcag ccgccaaact ttgttaattt tatcagtttc
47880
aacgcgaccg acaacgacaa ctccatgata atagacttgt gttccgacgc gcgcataatc
47940
gtggccaaga agctgacgcc cgacgaaacg tatcatcagc gcgtgtccgg atttttggat
48000
tttcaaaaac gtaactgcat acctcggccc ccaatcgagt cggacccaaa agtgcgagac
48060
gccttggatc gtgaactaga aataaaacta tacaagtaga aaaaaattaa tttattaata
48120
gttgtaataa ttatcttcgt cctcatcttc gctggtgtca taatgcggtg gtgtgtttgt
48180
gttttgtttt aatcgtttgc gcgtcgacac cacttcgccg ataggaaatt ttttggattt
48240
cgcattaaat gcccgcttag cgacgcgccg tttacgacta ctaaacatgt tgacgcgctc
48300
gtcgtcttca gtgtcataat ccgtgctagt gttttcgttg ttattttcta tgagacgatc
48360
gtttgattta gttttcgtag aattgtccgc gttatcgtcg ctttcgtcga tgtcgtccct
48420
aactatctcg taggcggctt tgcgcggaat ccaagaattt tgcaatgtat ctattttaac
48480
gtacttttct tcgagcgctt ttctagcttt atgcatagca atgtcttcgt cgccgccgtt
48540
cattttatga tactttgtaa acgtctcgac gaataacttt ttggcgcgag gaggcatttt
48600
ttcattgtat aacatatcgg gaatttgata cattgtaatt agaattaagc aagttcgtct
48660
tcggttgtac tgtattcggt ttctgtatct gtagtggaat cctctgtact agtagtagtg
48720
tcgctattgt tggcgtcagg ccttggctgc catttaccgt ctatcaacat gtattttttc
48780
ctaacagcac aacatgctag cttggtagct atctgtgtcg acttatattt ttgtaaacta
48840
cgatcgtaga atttttcaaa tatcctctta ccgttatagg gaaggttttg ataatattta
48900
ggcaacatat caataaaaga caatataaaa actttgtgtt tgtgttttat ttatcacata
48960
aaatggacgt ctggcaagaa tcacaaccaa tattagtgtt ttttttctta cattacgaga
49020
ttcaacttga tactaaaatt aattattaat taaattaaat taaattttga agcatttttt
49080
cgctatcgtt ttcagactca aaattatcga cgctatcgct atgaaaagcg taatatttgt
49140
tggctttgag atattctata ttttgctcat ttttaacaat aaacacgcga ctcttttcgt
49200
cgcgtctcac cataacaccg tttttacaaa tggaaatgta tttgtaaaac ggcaacagag
49260
cgtcgcgagt ttttttaagt aacagctttt gctccgctgt ggcggccaca aatattttta
49320
cgggcccgtc gtaattaatg tttaaattaa aatttttaag tcgacgctcg cgcgacttgg
49380
tttgccattc tttagcgcgc gtcgcgtcac acagcttggc cacaatgtgg tttttgtcaa
49440
acgaagattc tatgacgtgt ttaaagttta ggtcgagtaa agcgcaaatc ttttttaaat
49500
aatagtttct aattttttta ttattcagcc tgctgtcgtg aataccgtat atctcaacgc
49560
tgtctgtgag attgtcgtat tctagccttt ttagtttttc gctcatcgac ttgatattgt
49620
ccgacacatt ttcgtcgatt tgcgttttga tcaacgactt gagcagagac acgttaatca
49680
actgttcaaa ttgatccata ttaactatat caacccgatg cgtatatggt gcgtaaaata
49740
tattttttaa ccctcttata ctttgcactc tgcgttaata cgcgttcgtg tacagacgta
49800
atcatgtttt cttttttgga taaaactcct actgagtttg acctcatatt agaccctcac
49860
aagttgcaaa acgtggcatt ttttaccaat gaagaattta aagttatttt aaaaaatttc
49920
atcacagatt taaagaagaa ccaaaaatta aattatttca acagtttaat cgaccaatta
49980
atcaacgtgt acacagacgc gtcggtgaaa aacacgcagc ccgacgtgtt ggctaaaatt
50040
atcaaatcaa cttgtgttat agtcacagat ttgccgtcca acgtgtttct caaaaagttg
50100
aagaccaaca agtttacaga cactattaat tatttaattt tgccccactt tattttgtgg
50160
gatcacaatt ttgttatatt tttaaacaaa gctttcaatt ctaaacatga aaacaatctg
50220
gttgacattt cgggcgctct gcagaaaatc aaacttacac acggtgtcat caaagatcag
50280
ttgcagagca aaaacgggta cgcggtccaa tacttgtact cgacgtttct caacacggcc
50340
tcgttctacg ccaacgtgca atgtttaaat ggtgtcaacg aaattatgcc gccgcggagc
50400
agcgtaaagc gctattatgg acgtgatgtg gacaacgtgc gtgcatggac cacgcgtcat
50460
cccaacatta gccagctgag tacgcaagtc tcggacgtcc acattaacga gtcatctacc
50520
gactggaatg taaaagtggg tctgggaata tttcccggcg ctaacacaga ctgcgacggt
50580
gacaaaaaaa ttattacatt tttacccaaa cctaattccc taatcgactc ggaatgcctt
50640
ttgtacggcg accctcggtt taatttcatt tgctttgaca aaaaccgttt gtcgtttgtg
50700
tcacaacaaa tttattattt gtacaaaaat attgacgcaa tggaggcgtt gtttaaatct
50760
acaccattgg tttacgcgct gtggcaaaaa cataaacatg agcagtttgc acagaggcta
50820
gagatgttgt tgcgtgattt ttgcttaatt gccagttcaa acgctagtta tttacttttt
50880
aaacagctta cacagctcat agctaacgaa gaaatggtgt gcggagatga agaaatattc
50940
aatttaggcg gccaatttgt agacatgatt aaaagcggtg ctaaaggcag tcaaaatctg
51000
attaaaagca cgcaacaata ccgacagact ttaaatacag atattgaaac tgtgtcttca
51060
cgagccacca ccagtttaaa tagttacata tcttctcaca ataaggtaaa agtgtgtggc
51120
gccgacatat atcataacac ggttgtgtta cagagcgtgt ttattaaaaa taactatgtt
51180
tgttacaaaa acgacgaacg tacaatcatg aatatttgcg ctttgccctc tgagtttctg
51240
tttccagaac atttgctcga catgttcatt gaatgataat ataaatagag cgcatttgat
51300
tgcatgcaat cagtgtttta ttaattttag agcaacatgt acgataaatt tatgatctat
51360
cttcacttga atgggctgca cggagaagca aaatactaca aatatttaat gtctcaaatg
51420
gattttgaaa atcaagtagc cgatgaaatc aagcggtttt gtgaaactcg tctgaaaccg
51480
gcaatcagtt gcaacacttt aactgcggaa agtctcaata cgctcgtaga cagcgtagtc
51540
tgcaaaaatg gactgttaaa tccttacgcc aaagaagtac agtttgcttt gcaatatctt
51600
tttgacgatg acgaaatatc caaacgagat caagatggct ttaaactatt tttattacat
51660
aattatgaca ggtgtgaaaa tatggaagaa tattttttaa ttaacaattt tagcatagca
51720
gactacgaat ttgaagacat gtttgaaatt gttcgtattg attgtagaga tctgttatta
51780
cttcttgcta aatataatat gtaattaaaa ttttgtttgt tttattaaaa tcctggatta
51840
aaaaatgacg aataatttga tttgcgtgca cgccaacaag attcttcgtc attatgatca
51900
atgcgtgcat caagtttatg cttttgtaat tggcttctga ccactttagc catttgagcg
51960
tatctgcatt cgtcgtctag agtttcaaac accagatcgg cgcaattata aaatccttca
52020
cccacgggat ctatgcgctg ccaacgcaca tacattacaa attgatttga cctgtacggt
52080
attactacgg gtatagaata gactagactg ttgtcacata atgaatcgcc cggatttgga
52140
attaaatttg aatcgttacc acctatgtat tctaattcgt tccaagttat tggattgcga
52200
cgatcccagt ttgatttagt aataaacact tcaaaataac tgggctcgtg tatggctgtt
52260
ggacaaaaat gaacattcat ctgataaacc ggttgatagc gatttaaata tagcgtattt
52320
ggcctccagt tgttaaaagg ttcgtccatt ccgcttttat caccaaacac agaattgcga
52380
tcgtttgaac cggcaccgca aagtgtgtgc ggcacaaccc tttgttcgat taggtcaaaa
52440
tcgtcataat taggaccggc cacagccgcg tattccatat actgttgaaa catgtattgc
52500
gctgtggaag cggccgcccc ggattctaaa tcgagagctc gatatttata atagactgat
52560
ttgtaagcat tgcggcacgc ggcgtcggga atgttatcgc cattgtcggg ccaataaaag
52620
tttccatctt taaaacattt atattgacgg gccgtcggca cggacaaata gccgtgagag
52680
cgcactgccg gcgcgtgaat cgcagcaaac aatgcaatta ataatgcaat cattatgatt
52740
atacttatag aacactaatc ggaataataa ccgctgtcgt aatcttggtc aaaaacgtta
52800
tgttgaaaca taataacacc ttacagtaac atacaataaa acaacatagt atcgtatata
52860
attataaact ttattttttc attttataca aacaaaattt atacgtattg ttagcacatt
52920
gagtgtcatt ttcgctgtct gaactatcac aatcatcgtc atcatcatca tcattgtcat
52980
cgtcgtcgtc acgtttgcgt ttgacactgc attttttttg gttaattttc actaacactg
53040
gttcttttcg atcgtacaat tgattctgca tgtacttttg catgatcgcg gtaaaacact
53100
ttgcaatttt atccttttgt tcgtcgccaa atatttccag caactcgttc ataaatgtgc
53160
acaaaatgcc catgtgtttt atccagctga ttcgcatttt cactggatcg aacaaacgca
53220
aggggtacgc tttttctgtt accttgcctt cgatgtctat caaaaggtac gggatacgat
53280
ctccgttgcc gggcacaaaa tccgtgcctt tgttaaccaa aatttctcta caatgcctag
53340
ccaccgtaat cacgcgtctt ttgggtgacg gaccctcatt atcgtcagtt gatttgcgtt
53400
ttttgcccgg gttatcgtta taggtcatac taaagctgta gtcggtcaac gattttgatt
53460
tggcaaactc atcatagtat tcataaaaac tagtctgtaa actttgcaaa catttgtcca
53520
tgtccaaatg acgcaatatt tgttccactg ccgtcctaaa cgcgattctc ataaaaacgg
53580
gcatatcctt tttaactaac caacccttgt atacgatttt attctcactg ttgagatagc
53640
aatatttttt cttttttaat agtattaaaa ctttcattaa attttcaaat gccattttgt
53700
aaccgtccgt gaatgagtta ttaacgcgtg tctcaacatg tgtgcatatt tgttttaatg
53760
tgtcggtttc gttggatatt tcgttatagt taaatgtggg caaaacaaat gtagaatctg
53820
tgtcgccgta cacaacttta aaagtgatgc tgcccagatt gaatttttct aaaatctcag
53880
ggtcgttgct caaaccttca atcagagaaa tggccagccg caactgattg cgaccaactc
53940
tagtgatgta gtttgcaagc actttgtaaa aaatgccata ataaccgtat atgctattgg
54000
cggtgcgctt cacggaattt tgtttttgat cgtacagatc gtacaagaat gccgattcgc
54060
tttgattgtc gcgattcttt ttaaatttgc acctttcgct taacaatttt aatagcaatt
54120
taacaactat tgcacgcgaa ttgtggttca aatacacgtt gccgtcttcg cataaaatta
54180
aattggacaa acaagcacaa atggctatca ttatagtcaa gtacaaagaa ttaaaatcga
54240
gagaaaacgc gttcttgtaa atgcctgcac gaggttttaa cactttgccg cctttgtact
54300
tgaccgtttg attggcgggt cccaaattga tggcatcttt aggtatgttt tttagaggta
54360
tcaattttct tttgagatta gaaatacccg ctgcggcttt gtcggctttg aattggcccg
54420
atattattga cagatcgttt ttgttaaaaa aatacgggtc aggctcctct ttgccggtgc
54480
tctcgttaat gcgcgtgttt gtgatggctg cgtaaaagca cgccacgcta atcaaatgcg
54540
aaatattaca tatcacgtcg tctgtacaca aacgatgcaa tatacattgc gaatatacag
54600
aatcggccat tttcaatttg acaaacaatt ttatcggcaa catgcaatcc tgcacgttgt
54660
acttggcaat cacgtccagc cgtcgagtgt tgtacatctt gaccatttcg gtccaaggca
54720
aatcgatttt gttttcaccc aaatagtaac tactgattgt gttcaattga aagttttcaa
54780
ctttatgctg attagaatcg ctgctgaaaa atttatacaa atcaatgtga atgtaatagt
54840
taaaataata cgtgtccact ttgttgccca acttgtttat aaacagcttt gtcgtcggcg
54900
ccgcagccgg caaatcgtaa cgctttaata gcattttggt tttattcaat cgtccaagta
54960
tatagggcag atcaaatacg tctccgttaa aatccaaaat cacatcggga tttgtaattt
55020
ttatcatgtc aaaaaacgct gtaatcatgt cgatttcatt ttgaaacatg accacatacg
55080
tgtcatcgtc ataggtctct ggaatctggg tcggcagctt gtgatacata aaacaaaatt
55140
ttgcatactc gtcgtttttg tacaccacaa atcctataga cattatgcaa tcaaccgatg
55200
ctttcgacat gttgtggccg tccgaatgag tctcaatgtc atagcacgac aaaacgggca
55260
tgatgccgct ggttaaagtc atttcatcga ccaactcaaa gtcttcatta aaatgttgca
55320
aattaaacat gcgcgtcgtc gatccaccga catagttatt ttggcagcgt tgtgttttct
55380
tgaatcgcat ataggcgcct tccacaaacg gcgtttgcat gtgtacgcga ttaacgttgt
55440
gaagaaactt gtccaaacac gccgcgttgt ccgatggcgc tgctttgttt ctttcgtatt
55500
taatcacgtt tatcttgttc aaataatttc cttccacgcc cggcgccaca aacgtggtgt
55560
agctgatgca cttgttgcgg caagacggaa atatgtgctt gtcgtagcat tgtttgtaag
55620
aatacaaatt tagttttact ttaaagtaaa actgcagcac tcgttctttg atatttgtat
55680
tacaaaatgc aaacaagcaa ccttgttttt catcgtaatg caaacgaatg atacgaaacg
55740
tatcggctga agtaatattg aattctcctg gttttgcata ttctgcaaag cgcgttttga
55800
gttcattgta aggatatatt ttcattttta aatatgcagc gatggcccaa atatggaggc
55860
acagacgtca acacgcgcac tgtacacgat ttgttaaaca ccataaacac catgagtgct
55920
cgaatcaaaa ctctggagcg gtatgagcac gctttgcgag agattcacaa agtcgttgta
55980
attttgaaac cgtccgcgaa cacacatagc tttgaacccg acgctctgcc ggcgttgatt
56040
atgcaatttt tatcggattt cgccggccga gatatcaaca cgttgacgca caacatcaac
56100
tacaagtacg attacaatta tccgccggcg cccgtgcccg cgatgcaacc accgccaccg
56160
cctcctcaac cccccgcgcc acctcaacca ccgtattaca acaattatcc gtattatccg
56220
ccgtatccgt tttcgacacc gccgccaaca cagccgccag aatcgaacgt cgcgggcgtc
56280
ggcggctcgc aaagtttgaa tcaaatcacg ttgactaacg aggaggagtc tgaactggcg
56340
gctttattta aaaacatgca aacgaacatg acttgggaac ttgttcaaaa tttcgttgaa
56400
gtgttaatca ggatcgtacg cgtgcacgta gtaaacaacg tgaccatgat taacgttata
56460
tcgtctataa cttccgttcg aacattaatt gattacaatt ttacagaatt tattagatgc
56520
gtataccaaa aaacaaacat acgttttgca atagatcagt atctgtgcac taacatagtt
56580
acgtttatag atttttttac tagagtcttt tatttggtga tgcgaacaaa ttttcagttc
56640
accacttttg accaattgac ccaatactct aacgaacttt acacaagaat tcaaacgagc
56700
atacttcaaa gcgcggctcc tctttctcct ccgaccgtgg aaacggtcaa cagcgatatc
56760
gtcatttcaa atttgcaaga acaattaaaa agagaacgcg ctttgatgca acaaatcagc
56820
gagcaacata gaattgcaaa cgaaagagtg gaaactctgc aatcgcaata cgacgagttg
56880
gatttaaagt ataaagagat atttgaagac aaaagtgaat tcgcacaaca aaaaagtgaa
56940
aacgtgcgaa aaattaaaca attagagaga tccaacaaag aactcaacga caccgtacag
57000
aaattgagag atgaaaatgc cgaaagattg tctgaaatac aattgcaaaa aggcgatttg
57060
gacgaatata aaaacatgaa tcgccagttg aacgaggaca tttataaact caaaagaaga
57120
atagaatcga catttgataa agattacgtc gaaaccttga acgataaaat tgaatcgttg
57180
gaaaagcaat tggatgataa acaaaattta aaccgggaac taagaagcag catttcaaaa
57240
atagacgaaa ctacacagag gtacaaactt gacgccaaag atattatgga actcaaacag
57300
tcggtatcga ttaaagatca agaaattgcc atgaaaaacg ctcaatattt agaattgagt
57360
gctatatatc aacaaactgt aaatgaatta actgcaacta aaaatgaatt gtctcaagtc
57420
gcgacaacca atcaaagttt atttgcagaa aatgaagaat ctaaagtgct tttagaaggc
57480
acgttggcgt ttatagatag cttttatcaa ataattatgc agattgaaaa acctgattac
57540
gtgccgattt ctaaaccaca gcttacagca caagaaagta tatatcaaac ggattatatc
57600
aaagattggt tgcaaaaatt gaggtctaaa ctgtcaaacg ccgacgttgc caatttgcaa
57660
tcagtttccg aattgagtga tttaaaaagt caaataattt ctattgtacc acgaaatatt
57720
gtaaatcgaa ttttaaaaga aaattataaa gtaaaagtag aaaatgtcaa tgcagaatta
57780
ctggaaagtg ttgctgtcac aagtgctgta agcgctttag tacagcaata tgaacgatca
57840
gaaaagcaaa acgttaaact tagacaagaa ttcgaaataa aattaaacga tttacaaaga
57900
ttattggagc aaaatcagac tgattttgag tcaatatcag agtttatctc acgagatccg
57960
gctttcaaca gaaatttaaa tgacgagcga ttccaaaact tgaggcaaca atacgacgaa
58020
atgtctagta aatattcagc cttggaaacg actaaaatta aagagatgga gtctattgca
58080
gatcaggctg tcaaatctga aatgagtaaa ttaaacacac aactagatga attaaactct
58140
ttatttgtta aatataatcg taaagctcaa gacatatttg agtggaaaac tagcatgctt
58200
aaaaggtacg aaacgttggc gcgaacaaca gcggccagcg ttcaaccaaa cgtcgaatag
58260
aattacaaaa atttatattc attttcatct tcgtcatact tcaacagtcc caacacgttc
58320
atgttgtgat tctcgccgtt ttcgacagtt acgtaaatag ttactttgat taaattatct
58380
tccagcagca ttgagatttg attgaaatcc gcacatagct tttgtagcga atccgcttct
58440
ttttttttat ttgtgttgac gtagaaaaca gatttgttcc atttgcccaa gtcggaagag
58500
gtagaacagt catccgaatc ggcaatgttc aactcgtcgc ttttaaactg cacaataaac
58560
ttgttatcgc ccatgtcatt ttcttccaat tcgcttttta acacatttac attgtacgaa
58620
gcaacgtgtt tgttcgatcg actaatgttg atctttgcgt ttgtgcaatt ttgcaaattt
58680
gaatatgctt cgctttcttt agcctcgcac aattcgatgc gcgtagagtt gaccacgttc
58740
caattcatgt acacgtttga tccattaaaa atttgttgac actttatact gtaaatggta
58800
aagatttggt tttcattgtc ttttaaatat ttaaacacct cattgatgtc gtcagacccc
58860
tttatattgt tcttgaatag atttattagt gttttcgcat tgacagaaca ttccacttga
58920
accacgtcgg gatcgtcgtt gagatttttg tacacaacct caaaaacaac tttgtacaaa
58980
ccgctgttga ttttcttgta gataaatttg tactttacaa taatattgac gccatcttca
59040
ttttcaaaat gtttgttagt caaatagtcg ctcatggggg ttgcagtttc aatttccatt
59100
tcacattctt tgtattcgtt gatctgaatc atttgactaa actttgtttt cacataattt
59160
aaactaatgt catagcactt gccttcttcc atgtctttga aagattgcga atcgccgtag
59220
tattcttgaa ttttgttgtc ggacattatt cgaaaagtgt aatggtattc attatcgata
59280
ctcaacgtca ttttgctcat caatttacca ctaatccttt tgtaattttc tctaatcttc
59340
ttggggctac tggccatagc catgcgtttt ataagcggct caccgctact ttctccagac
59400
aaagatcttt tggtcgccat attgctgttg tcgatatgtg ggaatctatc cgatggcaaa
59460
tactgaatgg cgacgaaatc gaagtgtcgc cagagcaccg ttcgttagcg tggagggagt
59520
tgattataaa cgtggccagc aacacgccgc tcgacaacac gttcagaaca atgtttcaaa
59580
aagccgattt tgaaaatttc gactacaaca cgccgattgt gtacaattta aaaacaaaaa
59640
ctttaacaat gtacaacgag agaataagag cggctctgaa cagacccgtc cgatttaacg
59700
atcaaacggt caatgttaat attgcgtacg tatttttgtt ctttatttgt atagttttgc
59760
tgagcgtgtt ggccgtcttt ttcgacacaa acattgcgac cgacacgaag agtaaaaatg
59820
ttgcagcaaa aattaaataa actcaaagat ggtttgaaca cgttcagcag caagtcggtg
59880
gtttgcgctc gctcaaaatt atttgacaaa cgcccaacgc gcagacctag atgttggcga
59940
aaactatcag agatcgacaa aaagtttcac gtttgccgac acgttgacac gtttttggat
60000
ttgtgcggcg gaccgggcga gtttgccaac tataccatgt cgttgaaccc gctttgcaaa
60060
gcgtatggcg tcacgttgac aaacaactcg gtgtgcgtgt acaaaccgac agtgcgcaaa
60120
cgcaaaaatt tcacaaccat tacggggccc gacaagtcag gcgacgtgtt tgataaaaat
60180
gttgtatttg agattagcat caagtgtggc aacgcgtgcg atctggtgtt ggcagatggc
60240
tcggttgacg ttaatggacg cgaaaacgaa caagaacgtc tcaactttga tttgatcatg
60300
tgcgagacgc agctaatttt aatttgcctg cgtcccggcg gcaattgcgt tttaaaagtt
60360
ttcgacgcgt ttgaacacga aacgatccaa atgctaaaca agtttgttaa ccatttcgaa
60420
aaatgggttt tatacaaacc gccttcttct cggcctgcca attccgaacg ctatttaatt
60480
tgtttcaata aattagttag accgtattgt aacaattatg tcaacgagtt ggaaaaacag
60540
tttgaaaaat attatcgcat acaattaaaa aacttaaaca agttgataaa cttgttgaaa
60600
atataacgtg tgtataaaaa gccagcggct tcaaatcagg catcattcaa catggattcg
60660
ctagccaatt tgtgcttgaa aaccctgcct tacaagtttg agccgcctaa gtttttacga
60720
acaaaatatt gcgacgcatg tcgctacaga tttttaccaa aattttctga tgaaaaattt
60780
tgtggacaat gcatatgcaa catatgcaac aatccaaaaa atatagattg tccatcatca
60840
tatatatcga aaattaaacc gaagaaagaa aacaaagaaa tatatattac cagcaacaag
60900
tttaataaaa cgtgcaaaaa cgaatgtaat caacaatcaa accggagatg tttaatttcc
60960
tattttacaa atgaaagttg taaagagctc aattgttgtt ggtttaataa aaactgttac
61020
atgtgtttgg aatataaaaa gaatttatac aatgtaaatt tgtatacgat tgatggtcat
61080
tgtccttcgt ttaaagccgt ttgtttttca tgtataaaaa gaatcaaaac gtgccaagtt
61140
tgcaatcaac ctttattgaa aatgtacaaa gagaagcaag aagagcgttt gaagatgcag
61200
tcgctgtacg caacgttggc cgatgtagat ttaaaaatat tagacattta cgatgtcgac
61260
aattattcta gaaaaatgat attgtgtgct caatgtcata tatttgcacg ctgtttttgt
61320
accaatacca tgcaatgttt ttgtcctcga cagggttata agtgtgaatg tatatgccga
61380
cgatctaaat attttaaaaa taatgtattg tgtgttaaaa gtaaagcggc ttgttttaat
61440
aaaatgaaaa taaaacgtgt tccaaaatgg aagcatagtg tagattatac tttcaaaagt
61500
atatacaagt taataaatgt ttaattttaa ggatattgtt atggaataaa ctataaaatg
61560
aatttgatgc aatttaattt tttgatactt tccacagacg gtagattcag aacgatggca
61620
aacatgtcgc tagacaatga gtacaaactt gaattggcca aaacggggct gttttctcac
61680
aataacctga ttaaatgtat aggctgtcgc acgattttgg acaagattaa cgccaagcaa
61740
attaaacgac acacgtattc gaattattgc atatcgtcaa ccaacgcgtt gatgttcaat
61800
gaatcgatga gaaaaaaatc atttacgagt tttaaaagct ctcggcgtca gtttgcatca
61860
caatccgtgg tcgttgacat gttggctcgt cgcggcttct attattttgg caaagccggc
61920
catttgcgtt gttccggatg ccatatagtt tttaaatata aaagcgtaga cgacgcccaa
61980
cgccggcaca aacaaaattg caagtttctc aacgcaatag aagactattc cgtcaatgaa
62040
caatttggca aactcgatgt tgcggaaaaa gaaatactgg ctgccgattt gattcctccg
62100
cggctaagcg ttaaaccttc ggcgccgccc gccgaaccgc taactcaaca ggtctccgaa
62160
tgcaaagttt gttttgatag agaaaaatcg gtgtgtttca tgccgtgccg tcacctggct
62220
gtgtgcacgg aatgttcgcg tcggtgcaag cgttgttgtg tgtgcaacgc aaaaattatg
62280
cagcgcatcg aaacattacc tcagtaaaca ttgcaaacga ctacgacatt ctttaaaaat
62340
aagctatata taaatattgc attgtatgac aaaaaaatta ttaacctact gcaaagtaaa
62400
acttgtaaaa ggcttttcaa aaaaatttgc gagtttattt tgtcgctgcg tcgtgtcgca
62460
tctaagcgac gaagacgaca gcgacggtga tcgctattat cagtataata acaattgtaa
62520
tttcatatac ataaatattg taaaataaaa gacatattat tgtacataat gttttattgt
62580
aattaaatta atacaccaat ttaaacacat gttgatgttg ttgtgaataa tttttaaatt
62640
tttacttttt tcgtcaaaca ctatggcgtt gctttcgatt agttttttcg ttagcatttc
62700
atctaaaaaa tcaaactgtt tgcccggcgc gtttagggat tctatggtgt agtcgggcgt
62760
gtcgctgttt agatattggt ccacttcgcg cattatgtcc aagacgttgt tctgcaaatg
62820
aatgagcttt gtcaccacgt ccacggacgt gttcatgttt cttttttgaa aactaaattg
62880
caacaattgt acgtgtccac tatacaattc ggcttaatat actcgtcggc gcaatcgtat
62940
ttgcaatcca atttcgtgtt caacaaattg gtgatgatat ctttgaacgt gcacgttttc
63000
aatttgtcct tatcggccaa cgcaagtttc aattcgctct gtaaagtttc taaaattttg
63060
tctttattgt tgtcaaattc gtgcgtgttg cgttccaacc acaatttgaa cggctcgtcg
63120
acaaaaatgc tgcgcaacac ctcgtacaac tgtctgccta acgtgtacac ttgctcgtat
63180
tctttcatgc tgacctcttt gctaacgtac attactaaaa aatctacaag tattttcaaa
63240
catttgtaat aggcgacgta ttttgattta agttttaaac cgtccaccgt gtattcgtcc
63300
acgttcgcat cgaccacttt tcgattatta tcgccgcttg ttgccggcgc gtcggcctgt
63360
tcggttttaa ctatatccgg ttcaatattt aaagtttcaa aagatttaat ggcattcata
63420
aaatcatctt tttgctttgg cgtggtcaat ggtaaatcta tcgaggagtt gtcgtccgtg
63480
tgctcttcgg gcacgctgtt cagacgtaac gtaatctttt tgggatcgtc ttcatcgggt
63540
atcaaatcgg ctttaatttt attagaattg agcaacgaca tggtggtcgc ttgtaaattt
63600
aataaattaa ttaaagactg aaattgtata ttgcacaaat ttattttcat ttttattgat
63660
cttactatta atacgctggc agttggtatg cttcatccat ttttgtgact agaaaatttg
63720
ctaaaaaact gagctcgtcc tgtgttaaaa cgttgtcgtc cacgaatcta tgcaatgtaa
63780
atgttacact gacattgttt aacaatgcat gtattaaaaa atcaacctgt cgcctactga
63840
gtttattaga agagtcgacc gtttctacta gtttgtagat tttgttattt tcaatttcat
63900
tgtttaaaaa catgttaact actcgtttga gtttaagcga aaaatccttg tccggataga
63960
cttgttcgca cagccaattg ctaagagtgg ttttgaccac ggacaccttg gtggtgaacg
64020
tcgtcgattt gaccagttcg gtgaaaaagt ttttcattaa attggacatt ttaacaaaca
64080
cttatcaatc tattgagctg gtatttttgt ttagaatcgc atcaagcgct tgctcgatct
64140
ccaatttttt tcggacgctc ttagctttat gactcggtat gtcttctacg gtagactcgg
64200
tgttcttact tataatggcc gggctgacga taataaacac gagaaacaat atgagcagat
64260
acaaaaagat gctgttttcc tttttgtcat acactaggct aaatatggcc agtgcgccca
64320
acaacaaata taaattcatt tttattccct tactctattc gttgcgatag tacaacaacg
64380
attctcccga cgaaccggac gaattgcgat tatgctgcgc gtcgtcgtcg tcgttgttgt
64440
tctcctcttc gctgctcgtt tcgtctaaac ctatattgta tttgttcaag taatgtttgg
64500
tgcttgcgga ggattcgtgg ttcattaatt tggccacttt ttgtaaaggc acgccgctat
64560
tgtataggtt actgctcaaa taatgtctta tcatgttgct gcgcggccgt tccatctcga
64620
cgcccgactc ttcaaggagt cgcctgaaat ctttgaaggg cgtcgaggtg tttttagata
64680
tttgcaaaat ggtcgggttt cgtgaataaa tctcgcgtgc caattccaac ggtttcattt
64740
tgatgttgtt gagtgtgtta ttacgactgc gttttcgctt taaattaatc gtgtcgctgt
64800
gcagttttcc tcttttaatt agcacgttga gatcgtccac gctgagttgg cgcgcttcgt
64860
tgattcgcat acccgtccct aacatgatgc aaaacactat cgcgccccta attagaccgc
64920
ggtcgtgaac ataatcgctg ttgagcattt taattttatc attaataaaa tttaatatgg
64980
tatctattac gtttttaagc attaaattct tttccttttc cctgatattt ttgagctcct
65040
tgtcgcgcgg cagcataacc atgcggggaa ttttgtattc gggcaagttc atcatgttgg
65100
tgtaaaagtt tatagtcaac tgtagtgttt ctttggtgac cgagcgaagt tcgagcatgc
65160
gcctgcacag ttcttgggga tcaatgagaa gtgtttggtt ttctatcgag tcaaactcct
65220
tgtccaacga gtacgacatg tcttccaggt gaacatcgtc taccgagcag tacacaattt
65280
taatgaatcg agacttgtaa ctttttaaag tggtgggcgc aaacggtttg gggaacatgt
65340
acttgctcca cagactgttg tttttcacct cgtcgggcgt gcatcgttgc cgatcggtgg
65400
ccaaatcgaa cacggactcg aaccggggag cggattgaat ttttattttc caagaattaa
65460
aattgttttc gttgcgaaca ttaaaaccgt tcattgtggt taatcaaatt tattaaaaac
65520
aaaaggagaa tcggtgtcaa tactatccga atattgttgt tgttctctta atattacgaa
65580
ataatatatt acatacagca gtaagaataa agctataaaa gcgactacac taattaaaat
65640
tataattccc gccgacacgt tgctcgtcgt gttgtcatag cccaccatgt cgtttattgg
65700
cattttgtga acgggctcgc taaattgttg cggttcgctg gcagtatcgt cgttgagcgc
65760
caatttcaac gggatgtatt ccaccttttc gtggttgccc aaccgatagt agggcacgtc
65820
caaattcatg tttacaactt atttgctaac aggaatttat gcaacaaaag tggtttggct
65880
ttgatgagac gcaatttgaa atacttgctg catttacgct taagattgta ttccatgcgg
65940
gcggcggtct tgtagtcgta cgcgctcgcg ctgtgataca cgagccgtaa attggttgcg
66000
ttgcgcaaac acttggcgcc ttgtttgttc gaatgctgtt ttatgcgtct gttaagattg
66060
ctcgtgatgc ccgtgtacaa ttttccattg tcttgccgca gaatgtacac gcaccacacc
66120
ttgttggtgt acagagtcgt cgccatgatt atgcagtgcg ccctttcgtg ttcggccgag
66180
tggcgttagg cgcagccgcg gcaataatcg cgttggcgtc cttgttgtaa tttatttgtt
66240
gaaaaataaa acgtcttaga gtttcgtttt ggaacgccaa ttcggtcaag ctctcctggc
66300
aagcgctttt ggtcaaatga gcggccggcg aattgaccgc gttggcggcc gacgttaaga
66360
aggtggcgtt ctggaacatg ctgggctgct tgccggctcg cgtcgccagc tcggccatgt
66420
aattgaatat gttggcagac gcagatagcg gcgccaaaaa cgcaacgttc tcttttaaac
66480
tcatgactcg cgccctgttt ttttcgttca gcacgtagtg gtagtaatcg ccgccgccgg
66540
caaacagatc gtcaatcacg gcgttgatca gatcgttgat catgttgatg tgcggaaagc
66600
gacgcgactc gactgcgctc tgtatgtttg gcggcagagt ggcgtgcttg agcaacagag
66660
tcatgtaatt gttggccagc tgctgattga aaggtaacgg aatgggaatg ttgcacgtca
66720
ccgcttccgc caccatgtac tggacggcca gactgagttg tttggcggcc tcggccaaag
66780
cgtctttgcc caacatatca gcgccaccgt tgtaaaactt ttgcgcgtac gccggcagcg
66840
aatttagcac aaacgatggc tgaaatatat ttgaatcgct cgacagggac tcggccgcgt
66900
tgctctgtcc caactctttt tgcaaccgaa tcaggtggcg tatcatggtt tcctccgatt
66960
caaaccgctt taccacgttt acgctgattg ggttcgtgtc gatgcacatg tcacgaatag
67020
tgtttataaa aagaatcatg agaggactaa gttctgacat gtcattgcac ctgtaatatc
67080
taataatctt ttgaacaaaa tccacacatt tgttgtacca aatagattca ccggcgtcga
67140
gcgtcggttc tttgctcttg ttgtacggtg caatcgctac cgagtttgtg ctgttgctgc
67200
ggctcgtgta atccatcctg ttgtcgcgcg tggcgacggt cgtaggcacc gtcgccggcg
67260
gcacgtaccc gggcgcgttg taagtttgcg cgctggtgaa tatggccgtt gccggattag
67320
agggatacct cagcggcgga ggggtgttgt aataaaaatt gccacgttca tctgtcatac
67380
tttttatttg tactcttatg attacaaaac tcaatatacg gattacttat aatatagttg
67440
ttgtgacaaa aaagcgataa taaaattaac aaaattatca acaagttaat catggaaaat
67500
ttttcaacgt tgaataacaa caacaaaatg gcgcaggtca acagcaccgt ttgaaaactg
67560
acgcgccgac acaaaatgct ttcgcaattt ctaaaagcca cattaaacga attttcacct
67620
ttgatataat cacgcagttc ttttttacaa cattcgtcgc acaaaattaa cacctttata
67680
atgaggccgt cggtgtgtat cgtttgaaat gtccgcggtt gactgcctgg atgaaattca
67740
aacgagtacc cagtggacac gtgtatctgt gcaaaataat gggctaatat cgaggcgccc
67800
gtttttttaa cctttacttt tgatatttta ataacattaa tgttgttatt tgcgtaatca
67860
gagtttttat tgtggtgatc atcgtacaaa taatgaagca acagttcact atcgtattta
67920
atcttgttta gcgttgtcaa gtttttgttt cttaggcgtt ggagcgtctc cgtcgtcgat
67980
attttcttcg aaatcgagtc caacaacgtc ggcgtttcct tcttgctcat cgatagcggc
68040
ggcggaggcg gcctctccgt cgtcgtcatt ctcggtttct acagtgcgtt tgggcgacga
68100
cgtgtgtaca gcagcgtccg tcttactatt atcggaccgc caaatttttg tttgaaataa
68160
catttggccc ttgttcaact ttatttcggc gcagttaaac attattgcat taagatcata
68220
ttcgccgttt tgcaccaaat tgcacaaaac accatagttg ccgcacgaca ctgtagaata
68280
ggcgtttttg tacaacaatc tgagttgcgg cgagctagcc accttgataa tatgggcgcc
68340
aacgccccgt ttttttaagt aatattcgtc ttcaattata aaatctagta cgttttcatc
68400
ttcactgttg atttgggcgt tcacgatgat gtctggcgta atgttgctca tgcttgccat
68460
ttttcttata atagcgttta ctttaatgta tttggcaatt tattttgaat ttgacgaaac
68520
gactttcacc aagcggctcc aagtgatgac tgaatatgtg aagcgcacca acgcagacga
68580
acccacaccc gacgtaatag gctacgtgtc ggatattatg caaaacactt atattgtaac
68640
gtggttcaac accgtcgacc tttccaccta tcacgaaagc gtgcatgatg accggattga
68700
aatttttgat ttcttaaatc aaaaatttca acctgttgat cgaatcgtac acgatcgcgt
68760
tagagcaaat gatgaaaatc ccaacgagtt tattttgagc ggcgacaagg ccgacgtgac
68820
catgaaatgc cccgcatatt ttaactttga ttacgcacaa ctaaaatgtg ttcccgtgcc
68880
gccgtgcgac aacaagtctg ccggtcttta tcccatggac gagcgtttgc tggacacgtt
68940
ggtgttgaac caacacttgg acaaagatta ttctaccaac gcgcacttgt atcatcccac
69000
gttctatctt aggtgttttg caaacggagc gcacgcagtc gaagaatgtc cagataatta
69060
cacgtttgac gcggaaaccg gccagtgtaa agttaacgaa ttgtgtgaaa acaggccaga
69120
cggctatata ctatcatact ttccctccaa tttgctcgtc aaccagttta tgcagtgcgt
69180
aaatgggcgc cacgtggtgg gcgaatgccc cgcgaataaa atatttgatc gcaacttaat
69240
gtcgtgcgtg gaagcgcatc cgtgcgcgtt taacggcgcc ggacacacgt acataacggc
69300
cgatatcggc gacacgcaat atttcaaatg tttgaataat aacgagtcac aactgataac
69360
gtgcatcaac cggatcagaa actctgacaa ccagtacgag tgttccggcg actccagatg
69420
catagattta cccaacggta cgggccaaca tgtattcaaa cacgttgacg acgatatttc
69480
gtacaacagt ggccaattgg tgtgcgataa ttttgaagtt atttccgaca tcgaatgtga
69540
tcaatcaaac gtgtttgaaa acgcgttgtt tatggacaaa tttagattaa acatgcaatt
69600
cccaactgag gtgtttgacg gcaccgcgtg cgtgccagcc accgcggaca atgtcaactt
69660
tttacgttcc acgtttgcca ttgaaaatat tccaaaccat tatggcatcg acatgcaaac
69720
ctccatgttg ggcacgaccg aaatggttaa acagttggtt tccaaagatt tgtcgttaaa
69780
caacgacgcc atctttgctc aatggctttt gtatgcgaga gacaaagacg ccatcgggct
69840
taacccgttc accggcgagc ctatcgactg ttttggagac aacttgtacg atgtgtttga
69900
cgctagacgc gcaaacattt gtaacgattc gggaacgagc gttttaaaaa cgctcaattt
69960
tggcgatggc gagtttttaa acgtattgag cagcacgctg accggaaaag atgaggatta
70020
tcgccaattt tgtgctatat cctacgaaaa cggccaaaaa atcgtagaaa acgaacattt
70080
tcagcgacgt atattgacaa atatactaca gtcggacgtt tgtgccgacc tatatactac
70140
actttaccaa aaatatacta cactaaactc taaatatact acaactccac ttcaatataa
70200
ccacactctc gtaaaacggc ccaaaaatat cgaaatatat ggggcaaata cacgtttaaa
70260
aaacgctacg attccaaaaa acgctgcaac tattccgccc gtgtttaatc cctttgaaaa
70320
ccagccaaat aacaggcaaa acgattctat tctacccctg tttaaccctt ttcaaacgac
70380
cgacgccgta tggtacagcg aaccaggtgg cgacgacgac cattgggtag tggcgccgcc
70440
aaccgcacca cctccaccgc ccgagccaga accagagcca gaacccgagc cagaacccga
70500
gccagagtta ccgtcaccgc taatattaga caacaaagat ttattttatt catgccacta
70560
ctcggttccg tttttcaagc taaccagttg tcatgcggaa aatgacgtca ttattgatgc
70620
tttaaacgag ttacgcaaca acgttaaagt ggacgctgat tgcgaattgg ccaaagacct
70680
atcgcacgtt ttgaacgcgt acgcttatgt gggcaatggg attggttgta gatccgcgta
70740
cgacggagat gcgatagtgg taaaaaaaga agccgtgcct agtcacgtgt acgccaacct
70800
gaacacgcaa tccaacgacg gcgtcaaata caaccgttgg ttgcacgtca aaaacggcca
70860
atacatggcg tgtcccgaag aattgtacga taacaacgaa tttaaatgta acatagaatc
70920
ggataaatta tactatttgg ataatttaca agaagattcc attgtataaa cattttatgt
70980
cgaaaacaaa tgacatcatt ccggatcatg atttacgcgt agaattctac ttgtaaagca
71040
agttaaaata agccgtgtgc aaaaatgaca tcagacaaat gacatcatct acctatcatg
71100
atcatgttaa taatcatgtt ttaaaatgac atcagcttat gactaataat tgatcgtgcg
71160
ttacaagtag aattctactc gtaaagcgag tttagttttg aaaaacaaat gagtcatcat
71220
taaacatgtt aataatcgtg tataaaggat gacatcatcc actaatcgtg cgttacaagt
71280
agaattctac tcgtaaagcg agttcggttt tgaaaaacaa atgacatcat ttcttgattg
71340
tgttttacac gtagaattct actcgtaaag tatgttcagt ttaaaaaaca aatgacatca
71400
ttttacagat gacatcattt cttgattatg ttttacaagt agaattctac tcgtaaagca
71460
agtttagttt taaaaaacaa atgacatcat ctcttgatta tgttttacaa gtagaattct
71520
actcgtaaag cgagtttagt tttgaaaaac aaatgacatc atctcttgat tatgttttac
71580
aagtagaatt ctactcgtaa agcgagttta gttttcaaaa acaaatgaca tcatcccttg
71640
atcatgcgtt acaagtagaa ttctactcgt aaagcgagtt gaattttgat tacaaatatt
71700
ttgtttatga tagcaagtat aaataaccga acaaagttaa atttttttca tttacttgtc
71760
accatgtttc gaatataccc taataacaca actgtgcccg gttgtttagt gggtgacatt
71820
attcaagttc gttataaaga tgtatcacat attcgctttt tgtcagatta tttatctttg
71880
atgcctaacg ttgcgattgt aaacgaatat ggacctaaca accagttagt aataaaacgc
71940
aaaaacaaat cgctgaaaag cttgcaagat ttgtgtctgg acaaaatagc cgtttcgctc
72000
aagaaacctt ttcgtcagtt aaaatcgtta aatgctgttt gtttgatgcg agacattata
72060
ttttcgctgg gtttaccaat tatttttaat ccggctttgc tacaaagaaa agtgccgcag
72120
cgcagcgtgg gatatttcat gaattcaaaa ttggaaaggt ttgccaattg tgatcggggt
72180
catgtcgttg aagagaaaca attgcagagt aatttgtata tagattattt ttgtatgatt
72240
tgtggtttaa atgtttttaa aataaaagaa taacaattta cacattgttt tattacatgg
72300
ataatgttgt ttgtttgaca ttaaaggtta tcatggtgca atgattaata ataaaacaat
72360
attatgacat tattttcctg ttattttaca atataaaatc acaccaattg tgcaaagttt
72420
tattatttgt ttgtcgacgg tcgaggggtc agcggcgtgt gcaacaataa aaaacatgaa
72480
gctgttaaca attttgattt tattttattc attttttatg aatttgcaag cgctaccaga
72540
ttaccatcaa gcaaataggt gtgtgttgct gggaactcgc attggatgga acgatgacaa
72600
tagccaagat cccaacgtat attggaaatg gtgttaaata aaagtgaata tattttttat
72660
aaaatttttt atttaaaatt ccaagtaatc cctgcaaaca ttaaacactg taggtatttt
72720
taaatcttgc cacatgcgaa caacgcacgg cctgtcgtcg aacaccgcta ttacattata
72780
ttttcctctg atatagttgt taaacaattt taattttaat aaataatctt tacaagtatc
72840
gtctgaaggc ctcataaaca atttatatga tttaatatca aaatactttt caatccagtt
72900
tcgagtgggc tgttcacaaa ttacgcttct cccgctcata aacacgataa ttgcgtcgtg
72960
gcaatttgcc aaatacttaa cgcaagtaat aacgtctaag cgggcttcat cttgagcaac
73020
tctattatca aaatcataaa acgatctatt tgtgggcaaa gctactgtac cgtctaaatc
73080
acataataca gcgcggggaa atttgtcgcc gacaggaacg taatattcga aattatttac
73140
ctttagaaac tttttatatt gctttttaat agtttctgga tttaatggaa atttatcaga
73200
gcgtttataa ttgcgttcaa gagccgtttc caaagaaacg tccatcaaac gcgttaaaaa
73260
atggtaatta tgcgttgcgg ccattttttg ccacatgtcc accgattgag tgttcaaatt
73320
agtgtcgctg acaaccacgt tggcaccaca ttttgcggct tttaaaaact gttcaatgca
73380
cattttggta atttgttctt ctttagtttg tctacatttc cgcgattggt tatagaaagc
73440
gttcagtttt gtataatcgc cgtttaaaaa caacttaacg cgcacgtcgt ctctgttgat
73500
ttctgtatag ccttttaaac ttttggcata cgtgcttttg cccgaacccg aaatgcctat
73560
caacaccaac aattgttttg aagaaggcaa tttaattgtt ggagcaagtt tattatttaa
73620
tgcctgctta gtcgatacaa attttataat atttttgatc attttaattt tttcaggctc
73680
ggttaatttt aaaaattcgc tctccacatc gatcgtttgt gctttacgac atctgtacgc
73740
taaacatttc cacggcaaag tttgcaccag ttcgttgaaa cgctgttgat tcaaagtcaa
73800
acccgacacc ataatattta ttgtagactc gttggtgaac gtgtttctag catcaacgta
73860
cggtttaatg acacttttta aatgcgggaa aagagctaga aagtcatcgt gttcgccatt
73920
tataacaagc tgcgccaatt tagtaggatt ttcagcacgg ctctgatttt tgtgcatgtt
73980
caaatacacg tcgcttttaa tcttgcatag tggcgcgttg tttttatcgt aaactacaaa
74040
tccttcttcc aaatttttca actgggccgc gtgttcgaca cattcttgca cagacgtaaa
74100
ctcgtaacat ttggggtatt tgcaaaacgg caaattggaa cagtaaaaat aatcgcccgt
74160
ttcgttgttt ctgcttgcca aataccacaa cgttggctgt tcatcgtaaa cggttacaat
74220
tctgttgtgt ttgcttgtta actcaaacat gtgagtcgac gcgcagtcta aatattcgtt
74280
acacaacgct tgaaattgat tgtgggcctc gtcaagttga agagcttgca aaactaaacg
74340
tttaaacgtc acgtctgaca cgcaaaggtt ttctgcaaaa gcacttcctc gggtgctggc
74400
atgccattcg ccgttgtact tgtagatttt aattaaactt ccgtcgattt tttcgtaaaa
74460
cttaaaattc tccttcgatt ggaacagttt gtgatgagca tcttcgccgc cgatattttg
74520
tagcaattct tgaaaattaa agaaacgatc gaaagaacgc gacacaacgg cgtacgtgcg
74580
gctgttaaga attaaaccgc gacattccac gaccacagga tgatctcgat cgcgttcaaa
74640
cgattcgtaa ttaagaacca tcaaatcgtg ttcggtataa tttttaattt tgactttaaa
74700
cttgtcacaa agatttttca ctccgccgtt tgcaagtaga cgcgaaacgt gcaacatgat
74760
tgctgtttaa taatgcatac caatgctaaa ctgtctatta tataaagtgc agtgataact
74820
ttgttatcaa cgcgttcgat gccgacatat ataaacgcaa tgtaacagtt tttgctagta
74880
ccatcgcata caacattatg aatacaaggg gttgtgttaa taataataaa atgatattta
74940
tgaatgcttt gggcttgcaa cctcaaagta aattgaaaat tattgcacat aaaatactag
75000
aaaaatgtaa acgtgacgcg tacacgcgtt tcaagggcgt aaaggcgatc aagaatgaac
75060
taaaaacata caatcttacg ttgcaacaat acaacgaggc gctcaatcag tgcgctttaa
75120
acgatagccg atggcgcgac acaaataatt ggcatcacga tattgaagaa ggtgtgaaaa
75180
taaacaagag acatatatat agagttaatt ttaattctaa aacccaagaa attgaagaat
75240
attattacat taaagtagaa tgttatgtaa acagttaatt aatctacatt tattgtaaca
75300
tttgtggtaa tagtggcgtt ggttatacat ttatatgatt gtaatgttgt gtactcgttt
75360
tgtaataaat ttttgtgttt aatcaattca atatttttat ttgataaaac cttattttcg
75420
ctactcaatt tggcgttttt agacgcaagt tttgcgtaat cgtcattgag cgattttagc
75480
gccttttcag ttgtaattcg tttcagttgc aattctttaa aagatttatg catgttgttg
75540
tagtcgcttt taattttgtc taacttttct tgcatagaaa cgcttgtttg ttgtaatttg
75600
tctaaatcta attgttgttt aatgttgagc tgcgtttgtt cggcaatgtc tacctgtagt
75660
ttttttagta tcgcttgtgc ttcagacagc atagtgtcgt cggcatttgc gttgttgtct
75720
tctgcgtcgt ccaacagact tttttcaaac aacacactgg ccaaagaggc cgcatcaaaa
75780
ttagcgttta ttttattcca ttgtgcgaca ctcgacgcgc tgcatttaat cacatccaca
75840
acgtttcggt ttacgctgta aacgttgaaa tgcaaacttt caaccctaca caagggacat
75900
ggtacttttt ttcgttttct aatcttgcgt atacacattg agcataattg atgtttgcac
75960
gtgtctagtt ctaatacggg tattatagtc aatctgtcta ttggttgcag aaaataattt
76020
ttaatttctg caaccgaaaa acaaatgttg cattgcaatt taacaaactc catttttaga
76080
cggctattcc tccacctgct tcgcctgcaa caccaggcgc aggacctgcc actgcgccgc
76140
cgcccagagt agcgttagga tttgctcttg gtataaagtc gttgcgcaaa aagttgtttt
76200
ctgaattgat tatttggtat cccaaaaaca gcggaacgta cgtcgggtat tcttcgtatc
76260
cgctaagcgt tctgtccagc tcacgtgtgt cgccttcaaa tttcaaaacg tttctaattt
76320
gcaaacgatt gggttgactt ctcataatgt cactgcttct tatcgggttg tacaactcgg
76380
ggccgtcggg cacagacgcg accagacccg tttcgtcaat tatacacgtg gcgcaatttc
76440
taaacctcaa ttcctccgtg tcgatttgca agtactcggg cgctactgcg cgtcgaatca
76500
aattttgcaa aaatccactg taattgttaa ataattgatc gccagcaccg cctcgaagcg
76560
ctcgggcgtt ggtcacgtca aagaaacgca attcgtctcg cgacacccgc gaacaaaacg
76620
tgttcgggtt tgtggtgtcc agaatgcttt ttgtagttgc gtaaacgctg tgtataacgc
76680
gttgcgtgtt gcttgtgaaa ccttcggtat attttagatt gtcgcatata gtgttaactg
76740
cgttttcgtt gttatatatc aaatgaaaga ttagctgttc ggcttgcatc atactgttta
76800
gattaaacac gtcttggtaa ttggttgcgc ttggaattaa aattcgcttg atacctcttt
76860
ctttatttcc aactaaatgc ctagcgatcg tcattttgaa ttgattgtcg tcttcgtcga
76920
aaatgggcaa aaccattttt gacattttaa aacgttttat gaggtggttg ttgcaaataa
76980
accatccatc gtcatgatac gcgtcgggcg aacacggcga tttgtatgtt atgcacgcgt
77040
cgaacgacac gatggacgcg aaaatgcagc gattaactct catttgtcgc ggcgccatac
77100
ccacgggcac tagcgccata ttgttgccgt tataaatatg gactacggcg attttgtgat
77160
tgagaaagaa atctcttatt caataaattt tagccaagat ttgttgtata aaattttaaa
77220
ttcttatatt gttcctaatt attcgctggc acaacaatat ttcgatttgt acgacgaaaa
77280
cggctttcgc actcgtatac ctattcagag cgcttgcaat aacataatat caagcgtgaa
77340
aaagactaat tccaaacaca aaaaatttgt ttattggcct aaagatacca acgcgttggt
77400
gccgttggtg tggagagaaa gcaaagaaat caaactgcct tacaagactc tttcgcacaa
77460
cttgagtaaa ataattaaag tgtacgttta ccaacacgat aaaattgaaa tcaaatttga
77520
acatgtatat ttttcgaaaa gtgacattga tctatttgat tccacgatgg cgaacaagat
77580
atccaaactg ctgactttgt tggaaaatgg ggacgcttca gagacgctgc aaaactcgca
77640
agtgggcagc gatgaaattt tggcccgcat acgtctcgaa tatgaatttg acgacgacgc
77700
gcccgacgac gcgcagctaa acgtgatgtg caacataatt gcggacatgg aagcgttaac
77760
cgacgcgcaa aacatatcac cgttcgtgcc gttgaccacg ttgattgaca agatggcccc
77820
tcgaaaattt gaacgggaac aaaaaatagt gtacggcgac gacgcgttcg acaacgcgtc
77880
cgtaaaaaaa tgggcgctca aattggacgg tatgcggggc agaggtctgt ttatgcgcaa
77940
tttttgcatt attcaaaccg acgatatgca attctacaaa accaaaatgg ccaatctgtt
78000
tgcgctaaac aacattgtgg cctttcaatg cgaggttatg gacaaacaaa agatttacat
78060
tacagatttg ctgcaagtgt ttaaatacaa atacaacaat cgaacacagt acgaatgcgg
78120
cgtgaacgcg tcatacgcta tagatccggt gacggccatc gaatgtataa actacatgaa
78180
caacaacgtg caaagcgtca cgttgaccga cacttgcccc gcaattgaat tacggtttca
78240
gcaatttttt gatccaccgc tacagcagag caattacatg accgtgtccg tggacgggta
78300
tgtcgtgctc gacaccgagt tgagatacgt caaatataaa tggatgccaa caaccgagtt
78360
agagtatgac gccgtgaata agtcgtttaa cacactcaat gggccattga acggtctcat
78420
gattttaacc gacttgccgg agttactgca cgaaaacatt tacgaatgtg taatcacgga
78480
cacgacaata aacgtgttga aacatcgtcg cgaccgaatc gtgccaaatt aaagcacgtt
78540
aagcggatac aacgggcagt ccgagctgtt aaagtcaata caaccatcgt taacaaacga
78600
atacgcattg ttgtgacagc tgaggatata aaaaggaata gagaagtaat tgcaatgaaa
78660
tatcccgtta caattccacg gcacagcgta tgttgctcga gttctatcag ttgcacacaa
78720
cggcctaaga aaatttatta atgcttcatt tgtatctata ttagaaggat aatacatagg
78780
ttcgcccaaa ggactgggag aaggcggcgg cgaaggtgta ggtgtaggag gaataggaga
78840
aggcggcggc gaaggtgtag gtgttggagg aataggagaa ggcggcggcg aaggtgtagg
78900
tgtaggagga ataggagaag gtggaggtgt aggtgtaggt gttggaggta taggtgttgg
78960
aggaggtgta ggtgtaggtg ttggaggtat aggtgttgga ggaggtgtag gcgaaggtgg
79020
agaaggtgta ggagtaggtg gaggtgtagg taacggtaca attggtggag atgtaggtgg
79080
tggtacaatt ggtggatttg gatacaattc ctgaatgtcg tctaatattt ttaaagttaa
79140
taaaattatt ataaataaat ttaatattat tattattatt attatcacaa taatgtacca
79200
catgttgctt aaatataaaa attaaacaaa gaatgttgta ttattgcaaa tttaacaatt
79260
ttttgtattc tccccatgtc atgcgttcgt aatgagcggg cggtttttta tttctttgta
79320
tccacttgta atcgttaatg tggttgtgaa aagtcatact gacgtaggcc attaaatttt
79380
tcatgagcat attatttgac acaactgcaa catctgcgcc tgccgtttct tgctggtacg
79440
aatcgacaaa cgtaatgtct gtgccgtatt tttctttgtc aagtgcaatt tctataagct
79500
caatgtggta aatgatgaaa cctttgacgt tcatataatg atcgcggcac atggcgcact
79560
gtagtatgaa aaatacgttg taaaatagca ccttcattgt tttcaactgc tgcatgacaa
79620
aatctaaact gcttttgtct cgcgtataca ccatatcgtc gatgatgaga ctgagaaagt
79680
gcatggtgtc ccatatggta gtaaacgtgt aagtaaaact cttgggctgg cacgaacgca
79740
aattgagttc tgtggttttg tccataaatt ctatgcgaaa ctgttgcaag tccatgtcgg
79800
gggatgcgtt aatggcccat tcgatcaact gctgcacctc gtacttttga atgtctttgt
79860
atttcatcaa acacgcaaaa tggtataagt aagttgcttg cgaagacaac agtttggtga
79920
ggtgcgtcga tttagaggct cgcaaaaggt ctatgagacg aaacgaatac aacagatagc
79980
tgtctttgta acgagaaaaa agcggcgtca gcggtatcat ggcgactagc aaaacgatcg
80040
tgctgtactt gtgtcaggcg ccggccacag cgtcgttgta cgttagcgca gacacggacg
80100
ccgacgagcc tattatttat ttcgaaaata ttacagaatg tcttacggac gaccaatgcg
80160
acaagtttac ttattttgct gaactcaaac aggagcaagc cttatttatg aaaaaagtat
80220
acaaacactt ggtgcttaaa aacgagggtg cttttaacaa acaccacgta ttgttcgatg
80280
caatgattat gtataagaca tatgtgcatt tggtcgacga gtctgcgttc ggaagcaacg
80340
ttatcaacta ttgcgaacag tttatcacgg ccatttttga aatttttacg ctcagcagta
80400
aaatcgtcgt ggccgtgccc gtcaattggg aaaacgataa tttaagtgta cttttgaaac
80460
atttgcacaa cctaaatctc attggaattg aaattgtaaa ttaaaacaaa tcatgtgggg
80520
aatcgtgtta cttatcgttt tgctcatact gttttatctt tattggacga atgcattaaa
80580
tttcaattcc ttaaccgagt cgtcgcccag tttagggcag agcagcgact cggtggaatt
80640
agacgagaac aaacaattaa acgtaaagct gaataacggc cgggtggcca acttgcgcat
80700
cgcacacggc gataataaat tgagccaagt gtatattgcc gaaaaaccgc tatctataga
80760
cgacatagtc aaagagggct ccaacaaggt gggcactaac agcgtttttc tgggcaccgt
80820
atacgactat ggaatcaaat caccaaacgc ggccagcaca tctagtaatg taaccatgac
80880
gcgcggcgcc gcaaactttg atatcaagga attcaagtcc atgtttatcg tattcaaggg
80940
tgtgacgccc actaaaactg tagaggacaa tggcatgttg cgattcgaag tcgacaacat
81000
gattgtgtgt ttgatcgacc ccaacacggc gccgctgtcc gaacgagagg tgcgcgaatt
81060
gcgcaaatct aattgcactt tggtgtacac aagaaacgcg gcagctcagc aagttttatt
81120
ggaaaataac tttaccgtca ttaatgctga acaaaccgcc tatctcaaaa actataaatc
81180
atacagagaa atgaattaat aaaacaaaaa gtctatttat ataatatatt atttattaac
81240
atacaaaatt tggtacacta gtgttcaaat cgtttctgtt caacgccatt gtcatgttat
81300
aaaacacatt tgtagtttta ttgtaattat ttttaaattt atttttaatt tgctgtaata
81360
aaacttgttc attaaataca aaagactttg aactacttgc gtttatattc tttttataat
81420
tgtactgaac aaacgagggg tgcaaaaagt ttttcaaatg ctgcacggca atacctatca
81480
tctcctccat tttgtcctct cctattgtaa tagtggcact gcgcaccgtt ttaatgttta
81540
gaatgtaaat gagcgcatac agcggactat tgttggtgct caagcacatt aggttgtgct
81600
tatgcatagg gtcgttgctc agcagcgttt tgtatactac aaagcccgtt ttggggtcgc
81660
gtctgtacat tagtacgtgc gacaaaaaca aacgcaccgg cgtcacaagc gactcgtaat
81720
acatgctttc tatcggaaac tgtttggact tgatgtgttc gtacacggag ccggcaaact
81780
tgacgctgtc tacaaactta tggttcgtgt aaacaatcaa aaatctgtct tgtacaccgt
81840
cgtcataatc gtccacgtac agcggcttgt tgttaacaat taacattttg tagttggctt
81900
catactttag cagcccttgg tattttctgc tcttggaatc gctcttgctc gaatcggcat
81960
gcttcttaaa gtacgactcg ctgcattgtt tcaactcgtt gatagtgtac aactgcgagt
82020
tgagtttgct cacttccttg tcgctcgttt ccttgttgga ctctccgctg tggttgtcat
82080
cgtcaaactt gtgcatcaac accaaatagt ccaacagctc aaaaaacgac gacttgcccg
82140
aacccggttc gccgggcatg taaatagcct tctttccgta atctacggga atggccaaac
82200
tagcggcgaa atgcatcaac ataatcgcgt tcgcgtgatt aaaattggtg aagcgtttaa
82260
agtacaaata gccttcgaca atctttttca aataattgta cgagtactcc ttcaagtcca
82320
ctttggacat gatgatgcgc atgtagaatc gagtcagcca agtgggcaaa tcgtccgtgc
82380
tgcgcgccaa tatgattttg tcccaccaca cattgtactt cttcaagatc attaacgcgt
82440
cggcgtggtg cgtgtaaaat ttggaaatgt tatccgattc ttcaaactga acatcgggtt
82500
cacgtgcaac atcatcgcgc aattcggtta aaaacaaacg tttatcatta aacttgtcca
82560
tcaacatgtc gacatattcg attttgtgaa ttgttcgata caagtactga ataattttgt
82620
tgtgttcttt ggaaaaaaac tctccgtgtt ggttaacaaa ttcgctgttc gtgcgaatca
82680
acgtggtcga cacgtacgtt ttgttagtaa aaattagcat ccaaatcaat tcgctcaatt
82740
ctgcatcgtt accgaacatg tccgccatca agcagacttt tagcgctttt ctattgatct
82800
ttattttctt gtagcatttg cattttggtc gagatcccga taccgttgac cgacacggtt
82860
tgcattttag gttgtgcaac atgtcggaaa ccctgttctt gtttacgtac agagcgagcg
82920
taatcagatt ttcatcgtcc aaattccaca aatcgcgaaa caggttgttt aacgcgactc
82980
gcatatcggc ttggcatgtg ttgcaattgc ccatgtagtt aactatggcc gtgttagttt
83040
ttagcatttt tacatctcgg cacattttgg cgatgtgata agttctataa atgctgagct
83100
cgtcggcgct agtagatagc atgtaattaa acgcgtcctc gggcaaatac ttttcgtcgg
83160
tgggcttctt gaatgtctgc ggcaacgtgg tgcccaacaa aaatggacag ctcgaatgaa
83220
agctgttggt gaacacgttg tacacaccgt gcgttgtcaa gtacaagtat ttccaattgt
83280
taaattttat gttgctcaac ttgtaacaat tgcttttggt caatttgaat aggtcatcct
83340
ctttctttac aatttgataa tgtttgccgt tgaaaaccaa attgactccg gtcactacgt
83400
tttccaattt tctaaagaat cctttacaca caatgtcagg cggcaagttt agcgccatca
83460
cattctcgta cgtgtacgcc cacaattcat cgtgatccaa aatttcgttt ttagccgact
83520
gagtcaaata tatcatgtag tgtatgccaa aataatagcc caacgatacg cacaatttgg
83580
tatcgtcaaa gtcaaaccaa tgattgcagg ccctattaaa cactattttc tcttgttttt
83640
tgtaaggctc acatcgcttc aaagcttcat tcaaagcttc tttgtcgcag gcaaataatg
83700
attcacacaa aagttccaaa aacagtttga tgtcggtttc tctgtacgag aaattttcgt
83760
tcttggtcaa tatcttccac agtacataga ttaaaaaatc aaaattttta aatttgcttt
83820
tttcaaagta ttgttgtaga aggtttggat cgttggctcg ttcgtgggtc gccaaaactt
83880
taaccatgtt ctcgtgaatt gctataagcc ccaaattgat ttgcgtttga atgtagtctg
83940
cattttcgct gctcgccgat ataatgggta cgatgcgcgg ttttctggaa cgcgtgtcgc
84000
tcaagtccac gtcgtttttg tcaaaattgt tgttctcgaa cactctgagg cttttgaggt
84060
tgacgttgac gatatgcttg tacttgggca ccgtaatgca ttcctccaaa ttaatgtcgt
84120
ccctaatgta attgaaaaaa tttttatccg aattgaccag ctcgccatta actttgcacg
84180
tggccacagt gccgtcggcc attttgagta taaacaagtc ttcgtgagaa tcgtcaaact
84240
tggtttttcc atttacaaac agcgtttgcg gcggatcgtg attcgtgcgc aggctgagct
84300
cgacgttgag aaaacattta gggtcaaaca caaacaaatc cacagggcct agttttttgt
84360
tgtgtatgat tggtatcgtg ggttcgatga caattccaaa ttttatattt aaaaacagct
84420
gccatccgtt aaaagagaaa gcttgctttt tgggccagtt gggccaataa tagtaatcgc
84480
ccgcttgcac gcatttgtta atgtatccag ggtcggtgct cttgaaaaaa tcttcaaaat
84540
taatatactt ttgtatgatg tcatagtgct tcttcaaaat gaaaggtttt acaaaaatgc
84600
aaaaatcgtt actttccaac acccagtcgt ggccgtctaa tgtttgagct gcgtgtttct
84660
ctgcaggttc ttcggtgtct tcgcaagatg cgcccatgtc gtgtttcgcg cacggaccgt
84720
taaagttgtt tctaattgtg tttaagaact gttgaaagtt gttgacgtac tcaaacaatc
84780
tacgtgttcc tgttcgcgtg tttctaatga ttaaatgatt tgcatcttgc aagttgttaa
84840
tctcgtacgt tttgtcttga ggcacgtttt tcaaaaaaaa ttgtaaaatg ttgtcaatca
84900
tgttggctat cgtgtttgta cttttcgtgt taatttattt aataatttcg atcaaaaatc
84960
accatccatt cttacataga atagaaacgc taatacaaga tttcaacaac acattgttgt
85020
ttggcgcgta tgtacagatt tacgatttaa gcacgcccgc ccgcaccgaa cgattgttta
85080
ttattgcgcc cgaaaatgtg gtgttgtata attttaacaa aacgctctat tattacttgg
85140
actcggcgaa cgtgttttgt cccaacgagt ttagcgtgac cacgttcacg caatccacta
85200
ttaaaacgat caacgagacg ggaatatatg ccaccgcatg cacgccggtc agcagcttga
85260
cgctaattga acattttgca acattaaaaa ataacgtgcc cgatcacacg ctcgttctcg
85320
atgtggtcga ccaacagatt cagttttcaa tactcgacat tatcaattat ttgatttaca
85380
atggctacgt ggatttgttg gccgaataac gcgtatatag acgcttgtac gttcatcgta
85440
gtaatcattt taatacattt gattgaacta aacatacatc tgcaatgggt gaaagagtca
85500
ctaaattttg caatggaaaa cggcgataaa gaagacagcg acaatgaata gagtttatat
85560
ttttatttaa taaaatattg ttcgtaatcc ataatgtttt gtattatttc attgtgataa
85620
tgttcccaat cttgcacggg ggtggggcat cgtttgactt tgacgtagaa atcgtacgcg
85680
tagttattag ttggcagatc gtcgacaagt gtgatcgact tgaaaaagtt tacattttta
85740
tcgctcaaat atttaattac aatttttggc gatttgggta tattgttgtc ggatcgatga
85800
ttgtgaatgt caaaaacaaa tttattttca atgaaacgct tttttaaatt gtaatctaca
85860
atagcgttgt gtgaattttg aactaaatca gagcgttctt cttgaacggt ggaaccttcg
85920
ctgataatga tatcaaaata gccttccaaa tcgacgtctc gcatcgagtg tgctacatga
85980
tctctactgc catacgacca caagactaaa acgcaaccca tctcgtgcaa ctcctgcaag
86040
ctgtcataca caaacggatc tcgaatctca acttgctcct cttcggttat gagagtgctg
86100
tccaaatcaa acacgaccac gtgcggaaat ccccacgtca aagattcgct tttgagagag
86160
accactttgt agtgtggcaa tagaaaccat tctttaagaa acgaatacat tggcggtttg
86220
ttgctaagca cgcacatgtg gcccaacact ggcgttttga atgcgcgttt aatattgtgc
86280
ctgatgtcgc gcatgtcgtc ggcgggcgct ttgaatattt gcatacagta attgtaattg
86340
ttttctatga tcttgcacag ctgcgggtcg ttgcaaaatt gaaatattac atattcaaaa
86400
aatttatact tttcaaagcc aaggtatttg aggtcggcgt actcgcttaa aacgagaaca
86460
tgtcgtttga tgatggcgtc gttaaggcgc aaacagatcc atttgctttg aagcgaggag
86520
gccataatgt acaaaaatgg accagttacg ccttatttaa actgtttaaa gagtttcgta
86580
taaacaaaaa ctactctaaa ctaatagatt tcttaacaga aaattttccc aacaacgtca
86640
aaaacaaaac gttcaacttt tcgtctaccg gccatctgtt tcactcgttg cacgcgtacg
86700
tgcccagcgt cagtgatttg gtgaaagagc gcaaacaaat tcgattgcag acagaatatt
86760
tggcaaagct gttcaacaac acaataaacg atttcaaact gtacactgag ctgtacgagt
86820
ttatcgaacg gaccgaaggc gtcgattgct gttgtccgtg ccagctattg cacaagagtc
86880
tactcaacac caaaaattac gtggaaaact taaattgcaa actgtttgac ataaagccgc
86940
ccaaatttaa aaaaaaacct tttgacaaca ttctttacaa gtattcccta aattacaaaa
87000
gtttgttgtt gaaaaataag gaaaaacata ccagcactgg gtgtacacgc aaaaagaaaa
87060
tcaaacacag gcaaatattg aatgataaag ttatttattt acaaaacagt aataaaaata
87120
aactatttga gcttagcggg cttagtttaa aatcttgcag acatgatttt gtaacagtcg
87180
aaagccaaac gagggcaggc gacgaaatcg cttcgttcat tcgctactgt cggctgtgtg
87240
gaatgtctgg ttgttaatag tagcgtgttc tgtaacttcg gcgacctgtc gatgaacggc
87300
tcctggatct tctgtatgtg cggggtctac ccgggcggcg tctgtaaccc gagcttctgc
87360
gcctgcgtgt cgaaccatat gtggtaccgg ttgaagaacg gcgacggcga cgataaacca
87420
tgtttaaatt gtgtaattta tgtagctgta atttttacct tattaatatt ttttacgctt
87480
tgcattcgac gactgaactc ccaaatatat gtttaactcg tcttggtcgt ttgaattttt
87540
gttgctgtgt ttcctaatat tttccatcac cttaaatatg ttattgtaat cctcaatgtt
87600
gaacttgcaa ttggacacgg catagttttc catagtcgtg taaaacatgg tattggctgc
87660
attgtaatac atccgactga gcgggtacgg atctatgtgt ttgagcagcc tgttcaaaaa
87720
ctctgcatcg tcgcaaaacg gaatttcggt accgctgttg atgtattgtt gcggctgcaa
87780
catttgtatc ttttcgccgc gctcgatcaa caattcttca agagtggtgc gtttgtcgcg
87840
ctgtaaagcc acgttttgta acagcactat tttcgcatat ctcataatcg gactgttgaa
87900
acagcgtgca aacgacgacc gcataatatc gacggtcgtc aagtcgattg tggtcgaagg
87960
catctccaac agagatcgca cggcgtccaa cagcgtgtcc gtttgaacct gcgtcatttg
88020
cggtctgcac gtgtagtcgt caaacgtggt ttcgagcagt ttgaacaacg aatgatactt
88080
ttccgatcgc agcaaaaata tcatggtcat gaccacgtcg ctgattttgt attctgtaga
88140
actggtgctg ttcaacgaat agtgatggat tagtttgcga gcagcatttc tgtatcggcg
88200
catgttgatc aactcttcgg aaggctgcgc gggcgcggcg gcgttggctc gcgcaaacaa
88260
atttattacg ggacgcggcg taggctgcgc ggacgctggc gcggcgacga cgtccgcgtt
88320
tcccgccgcg tactgagacg ctatggcagc gttgttattt aaaattgtgt tttgcgattt
88380
gcgagccacg tgcatcataa aatttatcaa cacgtcggtg ttcaactgca cgctttgatg
88440
ttcgtcgcag agcaaaggaa atagctgggg ccatatcgcc aattgcatag gctcgtctat
88500
ttttaaccgc aatttgttta tttccaaata caacgcgata gcgctcatcg tgaccgacga
88560
cgcacactta ctctgtaact atcacttgga tcgtgttgtc gtaaacgctt cccaaaaagt
88620
ctaacacgtt gaccgtttcg attctattca acttaattgt ggacgcgttg gcttgcatcg
88680
gttccaacag actgcgcgct ccgacagatt gagtagacaa aatttttaaa ctttccgtct
88740
tattgggcgt aatgtcgttg attaacaacg acgcagccgt ttgagaggcc gcagtgttga
88800
tggtttgcaa catgtcgacg gccgccattt gcgtttgcgc cgaaggtctt gctggcggcc
88860
tgttgcggcg gtttcttcgt gcttgcgaca tgttgtcgtc agtgtccata tcggtatcat
88920
ttattgaagc aatcatggtt gagttcgata agcagagata tttcgttgtc caattggtac
88980
ttggtaatga tgtgccttat aaatgtttcg ggcacaatca tttctgtcat tagcacgtta
89040
caaatatcta ttttgatcaa tttcaattta tgaattaaca gattaatgtt ttcgtccgag
89100
tacttgctca tgatgaaacg acaaacgttg cggagttcca actccgctac cggatacgct
89160
ttgttgggca aactctctaa atagtgtctc aaataaaagc cgatcaatac ggtggacgct
89220
attttgttaa cctttttcat tttagtattg cggcccattt ctatcatgaa gtttttaaac
89280
ggtagcaaca gcctgtctcc gttagcaaca gtggagcagc cgttgcattg cgcgctcaaa
89340
atactcaaca cgcgctcgtg atcttcttgg cgcaatccga cggttgcttt tttgcattct
89400
ttgacaaatg gcacgcacat gtcgcgtttc gtgtacaaag aatacgcttt gtcgcaaatc
89460
aagttataga aaaattgcac aaatatctgc gtaatcaagt tgttttcgtt aataatgtca
89520
ctttcgtttt tgtaatcggt tcgaagcaac acgtacaaca tcagaggcat gccgaacatg
89580
ggtcttaaaa aaatgtccca accattttgc aagcccgcgt cgagggtgct cagcgaggac
89640
gccaagtatt tgcatttgca ctcaaaacat tgaattttgt ttgcgggctt gcacgactga
89700
cacatgatcg catccacgtc gggtgccggc gtcggattgt aatatttttg caagtattgc
89760
ataatggtcc taaaatgggg tacctgtttg ataaactcgt cgcgcaaaaa tatcgaaaaa
89820
atgtttttta cattgtgtat gttgtctgtg ttgttggctt gattctcaaa actactcttt
89880
atggaaacaa tacatttgtt aaattctgtg aaaaaagtaa gacctttact gtccacgatc
89940
aagctttggt tgaaatattt tgaaaataaa aaacacaacg aatcgatttc atcttgtaac
90000
aattgcgctt caaaacacac gttttcaaag cggtcgtaaa tgttaaacct taaactgtat
90060
tgtaatctgt aagcgcacat ggtgcattcg atataacctt ataatatgaa cgattccaat
90120
tctctgttga ttacgcgttt ggcagcgcaa atactgtcca gaaacatgca aacggtggat
90180
gtgattgttg acgacaaaac gctcagtttg gaagaaaaaa tagacacgtt gaccagcatg
90240
gtgttggctg taaatagccc gccgcaatcg ccgccgcggg taacatccag cgacctggcc
90300
gcatcgatca ttaaaaataa cagcaaaatg gtgggcaacg attttgaaat gcgatacaac
90360
gtgttgcgta tggccgtcgt ttttgttaag cattatccca agtattacaa cgagacgacc
90420
gccggtttag ttgccgaaat agaaagtaat ctgttgcaat atcaaaatta tgtaaaccaa
90480
ggcaattatc agaacattga gggttacgat agtttattaa ataaggcgga agagtgttat
90540
gttaaaattg atagactatt taaagagagc attaaaaaaa tcatggacga cacggaagcg
90600
ttcgaaagag aacaggaagc ggagagattg agggccgaac aaactgccgc aaacgctctt
90660
ctggagaggc gagcgcagac gtccgcagac gatgtcgtta atcgtgccga cgccaatatt
90720
cccacggcat ttagcgatcc gcttccaggc cccagcgcgc cgcggtacat gtacgaaagt
90780
tcagagtcgg acacgtacat ggaaaccgcc cgacgtaccg ccgaacatta caccgatcag
90840
gacaaagact acaacgcggc gtacactgcc gacgagtaca attccctggt caagacggtt
90900
cttttgcgtt taatcgaaaa ggcgctggcc actctaaaaa atcggttgca cataacaact
90960
attgatcaat tgaaaaagtt tagagattat ctgaatagcg atgctgatgc tggagaattt
91020
caaatatttt taaaccagga agattgtgtg atactgaaaa atttgtcaaa tttagcgtca
91080
aagtttttca acgttcgttg cgtggccgac acgttagagg taatgttgga agcgcttcgc
91140
aataatattg agttggtgca gcctgaaagc gatgccgtac ggcgaatagt cataaaaatg
91200
acgcaagaaa ttaaagattc gagcacgccg ctgtacaaca ttgccatgta caaaagcgat
91260
tatgacgcca taaaaaacaa aaacattaaa accttgttcg acttgtacaa cgacaggctg
91320
ccaatcaatt tcttggacac gtccgcaacc agtccagttc gcaaaacttc cggcaagaga
91380
tctgcggaag acgacttgtt gccgactcgc agcagcaaac gtgccaatag acccgaaatt
91440
aatgtaatat cgtcagaaga cgagcaggaa gatgatgacg ttgaagatgt cgactacgaa
91500
aaagaaagta aacgcagaaa attagaagac gaagattttc tcaaattaaa agcattagaa
91560
tttagcaagg acattgtcaa cgaaaagctt caaaaaatta ttgtggtcac cgacggtatg
91620
aaacggctgt acgaatactg caactgcaaa aattctttag agactttacc gagcgccgct
91680
aactatggca gcttgctcaa aaggctaaac ctgtacaatc tcgatcatat cgaaatgaat
91740
gtaaattttt acgagttgct gtttccattg acactgtaca atgacaatga taacagtgac
91800
aaaacgcttt ctcatcaatt ggtaaattac atatttttgg ccagtaacta ttttcaaaac
91860
tgcgctaaaa acttcaacta tatgcgcgaa acttttaacg tgtttggccc gtttaaacaa
91920
atcgacttta tggtcatgtt tgttataaaa tttaactttt tatgcgacat gcgtaatttt
91980
gccaaattaa tcgacgagct ggtgcccaac aaacagccca acatgagaat tcacagcgtg
92040
ttggtcatgc gggataaaat tgttaaacta gcttttagta atttacaatt tcaaaccttt
92100
tcaaagaaag acaagtcgcg caacacaaaa catttgcaaa gactaataat gttgatgaac
92160
gcaaactaca atgttatata ataaaaaatt ataaaatatt tttaattttt atttatattc
92220
agtacattta cacatattaa catattgttt atacaaattc ttataatcat tatgatttaa
92280
attgaattgt tgtctaaaca aattaaacac tttattaaac aataactttt cgttgtaatt
92340
ttttactttg cacatgttat aacaaaaaat taaaattttc atcatgtctg atttgtctat
92400
ggcgtcacag ttgcttttaa tgtaatcgca agttaaccac tcaaaaggac ccttttctat
92460
ttttaatttg tttaaatctt tataatcaga cttcagtttg taaattagat ttccacatcg
92520
aataataaat ccttccagcg ggctttgggg aaacattaaa gacttgaaat ttaacctttc
92580
tacaaaatcg ttgtacaaat atttgtgaca cggaatagta ttaaacccca cgttagtcaa
92640
caactcttgc gcctccacaa agggcacaaa ctccccgccg tataattgaa tttcgtaagc
92700
gtagtatttc aaactctctt tctggtccac gtagttaatt acgttaatgg gtgtcgtttt
92760
tgcgtcgtct ttccaaccca ttaattcgcc gtagacaata aaaccgtcat tgaaccgcgc
92820
ctgaagcgat cgcatgcacg tttctaaatc ttttcgaatg cggtaataat tcataaaatt
92880
gccgtccggt ctgtaagtgt ttcttgaccc gtacgtaatt ttattttggt tgcaaatgat
92940
tctgaaatta caaccgtcca acttttcttg aacaataatt tctttgtcgg ccaacgtacc
93000
ttttttacct tgatctagat gcgacacaga tggataaatt tgatacacaa ttttattctc
93060
atcttcgggc attacgggtc cgcgttcatt taacgcgtac atgacaatgt tgtggcgaat
93120
gtcggtgcgc tccggcggtt ctggcacgtg gtgcagtctg tcctgcaatt gttgcttcca
93180
ttgttgaaaa tattcggtcc attcttgttg atactcgccg cgttgcatga gttttacgta
93240
cagttttaaa agtttgacat tctttacaaa taacgttaga gtttcgtcga ttttgtatcc
93300
tccattattt ttgtttaaat ccaatacatt taaatcgttc actaccagtt gattgttttt
93360
atccatcgta atttttatct catcgcccac gttgaacaac atgtttaaaa ttttggtgga
93420
tttcggcgca cgtttataat ctaaataata ttcaacgtac acgtaattga acatgagctg
93480
caacaatcct ttggcattgt tcaaaatttt gtatctcatc aaagtataaa taattttcac
93540
catcgacacc gtcatcaact tggttacaaa ctcgtacaat tgcaagtttt caataccgta
93600
tttgtcttta aaatcttcac gtttactgaa catgcttaat tcgggagatt ttccagtcaa
93660
aatgccaatt aatcccgtgt acaagtcaac gtatttgaca tcgttgcccg attcatcttt
93720
tgcatgtcga tttttcaaaa gctctttatt gtcgataaat ttttcaaagg tctctcgatc
93780
acatttagtg taaatatggt agtcagtgtc gctgctttcg accgcgtatc ccttggcatg
93840
gctgcccgta tcaatgcaaa tgtacaccat gttagaatgt gctgcttact gtgcctgtat
93900
caagccttat atacctcaaa atatttcaca tttttgcatc atcgtaaaat atacatgcat
93960
ataattgtgt acaaaatatg actcattaat cgatcgtgcg ttacaagtag aattctactg
94020
gtaaagcaag ttcggttgtg agccgtgtgc aaaacatgac atcataacta atcatgttta
94080
taatcatgtg caaaatatga catcatccga cgattgtgtt ttacaagtag aattctactc
94140
gtaaagcgag tttaaaaatt ttgtgacgtc aatgaaacaa cgtgtaatat tttttacaat
94200
atttaagtga aacattatga cttccaataa ttttgtggat gtggatacgt ttgcaagaca
94260
attgattaca gataaatgta gtgctctaat caaaagtgcg gatctgttgc cggcaaacat
94320
tttagagatt gtagagaagg ccagagacaa gtattttgag gagccaactc aaaaaaacta
94380
tgaatacatt aaaaaattat ttttacgaac aaaatatatg gacgattcga tagattataa
94440
agattttaac agacgcatcc tattgatagt ttttaaattc gctttaaaca agagcaccaa
94500
ctactttcca tcgtacaaag agatcatcga ggtggccatt aaacgtttaa acaaaattaa
94560
ccccgattta aagagttctc cgcgcgcaat gcttcagcat tacaatgaat gtttggaaaa
94620
tctagacaat ccagtcacgg acgaacatca tttgttaaca tttggaaaag aagttgctac
94680
aaaaatattt atcgaagcgt ttgaatacag ttacaccaac actaatgcca tcagcatgga
94740
caaaacagat gaatttgatt ttattaaacc ggcattgaaa cctttgccag atgcaagacc
94800
gccatcgctt ttggccaacg tgatgaacga acgtaaaaga aaattacaaa acaccaactc
94860
aacggcaaaa tgtttgctac cagcaccacc gccacaattg cgtaaacttg aaaaaaagaa
94920
tcatttattg cctttgtttt ctttgtaatt atattgttgc atttctattt ctaatatcat
94980
agttttctaa taaagtagtt tcatattttt gtttttgtac agtaattgtt tcttggttta
95040
acaagatcac aaccaataac ataaagaata acacaatcat aacaaaaatt aaaaagccgc
95100
atactactag aacaaattct ttaattagcg atcggtttct atttacaaat tggccgagct
95160
gatcgccttc agtcggcgag ttgtgggctt ggatgatgtc gacgatattg ttgccggcgc
95220
gaccgcctgt cgctctcgat ataatgtcgg ccgccgtcgg tttcatgatg tgcttaacta
95280
caaataatag ttgtacttga cgggcgtcac cgtgatgccg ctgctaaaac ctccgtccgt
95340
taagacgcgt tgcgttacaa aattaatgtt tgtccgatta gcgtagtcgg aataatcaaa
95400
cgtgttgggc ggactaaaat cgggcatgtt gatgggcaca atgccgctgg agctgatagc
95460
aatgctgtcg ttcttgcaaa acagccgaat ttttttgtag ggctctgctt tattcggcgc
95520
agacgacacc atctggtcaa agttgttcaa ttttatgatt acgttgggta ccaattgata
95580
ggggaaaatt attttctgga acattttgac aaagtccaca accgtttggc tatagtcggg
95640
aatgccgagc aaagactgcg cctgtttaat gtatttgaga ctggagcggt ttactgtagc
95700
gcaattggat ggcacgtcgc ccttcataag ccggcgcgtt ctctcccaat tcaatttgtt
95760
gtacaaatta tcaatctcct cgtgcggcag attgattaca tagcgcgcgg gctgtttgcg
95820
atattgaaag atgcaaaaaa tgcgtttcaa cgacaatatc ttcaccatgg tggacgtttc
95880
cagattgaaa cataacaaaa agtcattgct ttccaccaat tctttaaaat gagacagcgg
95940
aatttcacaa gcgatcggtc gcaaattgct ttttattgga ggcggaacgc tttgaccgtt
96000
gcggtttttt agtaacgcgc tgcacgcaga ttgcatgtcc gtttcgggat acgtaaactc
96060
gatgggacat ttggggtttt catggtgaac gatcatagtg ttgcaataaa acaagttgtt
96120
ggtcaggagc acgctaaaaa cacgcgtttc gcccgcaccg atttcggtga tgggtaccaa
96180
cgggttccag tagactatgg tggcggacgc tgtttttttt ggcgatcgac tgtctatgtt
96240
aacatcatgc tcgtgcctgt acactagcac agaattgaat tttggaaatt gttttttgtc
96300
aatgtacaac cggtcgtcgt ctgtgggcac gtacacgatc aagttttcga ttaatttgtt
96360
gcctacgtcg ctttgcggtt ccaccaaatt gtgagggaac gcaaaaaagc gatcgctaat
96420
acaaacttga atctgaaacg ggcactccat cgtgatgtat atgtcttact tcattagact
96480
ttagattatt ttaatttgtg aactcgtacc gtattcaata gggtgtcggg cacgtaattg
96540
taatggtaaa acagatcctg ttgaacacgt gcgttgttca ctacgattga aatgcaaaaa
96600
tacatcaagt acataaacac tatgattaga aaggtagcag acagaaaata tttcatcttt
96660
aaatcttatg ctagttgaat aaaatacata gtacttttat acgtttattt atatttgttt
96720
tctttgttat aaccgtaatt gtaaaacttg tgatcgtgct cgccaggcat aatttctttg
96780
cacatcagct tgcgaatata tgtgacatct tcgtacaccg atttcttgat gttaccatcg
96840
tgaagcgttg tcggcttgag aggtttgcgg tcgttgttgt aaaaattttg caccgaataa
96900
ttatccatag tgcagcacag gcaatgtcac tgatgcatat gctttaattt tttattgcat
96960
tcagttatta tatgatttaa taaacgtaca caatagcacg tttatcggtt aaagataact
97020
ttcaatatat aaaagtgttt gaattgcgag accgtcaaca taacgtttat caacgcgatg
97080
actaaacgac aatttgcttt gctgtttgtg tggcaccacg acaaccaatt tgtttgcaac
97140
acggacgaat acccgttttg gcacaacatt gaataccatg cacggcgcta taaatgcatc
97200
gttttgtact gtgtggaaaa cgacggatcg ctacaactgc ccgtttgcaa aaacataaat
97260
ctcataaatt ataaaaaagc gtatcctcat tattatggaa actgtgttga cagtatagtg
97320
aaacgtgctg gcaaaattga ttatatgaaa gtaactgcaa tgttaaaccc ccacctgttg
97380
gacgtcgcgt acaattattt gctgttgatg gacatggatt gtgtggtgca aagcgtgcaa
97440
tggaaacaat tgtcaaccga cacgtattgt tttgagccgt tttacgactc tcaaattaaa
97500
tggttgtacg cgcccaaaag cggacaaagt tttgatagtt atcttgaaaa ctatgcaact
97560
ctaattcgag tcaaacaagt gcagcaacat cgaaaagaat taatactgca ttgtgtggat
97620
tttcttacaa tgaaagcaaa tgacaatttt atggtgttca aaaattatat taacatgatt
97680
ataaaagtgt atttgcaatt ttacaattac agatttccca tcaattttga ggacaacacg
97740
atgaaacctt gtgtaaattt aacttttaga cgtggcggca gttggaaaac tcaactgcaa
97800
cccgtatgca attatgttta caaaagtaaa aatatgccaa aatttattaa ataaaacaaa
97860
ttaatttaaa caagcgtttt tattgacaat actcacattt gatattattt ataatcaaga
97920
aatgatgtca tttgttttca aaattgaact ggctttacga gtagaatttt acttgtaaaa
97980
cacaatcaag aaatgatgtc atttttgtac gtgattataa acatgtttaa acatggtaca
98040
ttgaacttaa tttttgcaag ttgataaaca tgattaatgt acgactcatt tgtttgtgca
98100
agttgataaa cgtgattaat atatgactca tatgtttgtg caaaaatgat gtcatcgtac
98160
aaactcgctt tacgagtaga attctacttg taacgcatga tcaagggatg atgtcatttg
98220
tttttttaaa attcaactcg ctttacgagt agaattctac ttgtaaaaca caatcgaggg
98280
atgatgtcat ttgtagaatg atgtcatttg tttttcaaaa ccgaactcgc tttacgagta
98340
gaattctact tgtaacgcaa gatcggtgga tgatgtcatt ttaaaaatga tgtcatcgta
98400
caaactcgct ttacgagtag aattctacgt gtaaaacacg attacagcac ttcgtagttg
98460
tatcgaaaat tgttcaatgg ctctttgtta atgtcgtaat tgattaatat gtcgtacaat
98520
ttggcggcgt tgtgtttgca cacgaccgtt tttagttctt gaaacatttt ttcgtgtatg
98580
tttagcatgt tgtatttcag agtgcgatgt gtaatgctgg tgacgagcat caaaatgata
98640
aaatctaaag cggctaattt gtaatcccgt tcatacgctc tgtaatcgcc aacaactctg
98700
tggccagatc tttttagatt ttgacaggcg ttatggtacg aattgataat atttactata
98760
gtttctcttg ttatcggttt gtcgattaaa ctgttaacaa acatcacgtt gcccaagcgc
98820
gacggtttag acaccgactt gttttttgtc tgttcaaatt tgtacaaatt aaaaacgctc
98880
atagactggt cgtcaggcag tgtgtcgtta tacaaacaaa atggtaaaac gtttaattcg
98940
acaaacgacg agcacattaa agtttgttgg ctgttaacgt cctggggatg taaactgtta
99000
ttcataacgt aacacacttc aatgtcggaa tgcttgtttt caaatttgtc cttgtctaca
99060
gtttcaatgg tgattgagcg aggtttgagt ttattttgta aattcatttg gatattttca
99120
atatggtata ccaccgacac gttgtgagcc agcgatcctt gattggtttt aatcatattc
99180
aaaatattca tgatatggtt gaaaaaagag tctgtcaaaa cgtttgtgtc gttgttaaat
99240
atcgctttcc agggtttact gttgcgtgac tcaacgacgg ccgtgtaaca taacaagcgc
99300
gccagttgca tgtgcgacaa cttaatgtta tcaatgtcgg tgatgtttgg caccagattt
99360
tcattgccgt cttccagtag cgtgctcagt tcggtcgagt agttattcaa cgatcgattg
99420
tgcgattcaa acaagtttac tatcgcaggt tgtacatagt tttttatgtc gtcaaattga
99480
attatatcga tcttgtcctt gttctccagc ataaacgaca aattttttag gtcgaattta
99540
atatttggcg cgttttcgtt ggactttttg taatttaaca acatcgccaa cagtttgtgt
99600
aactcgccgt tagcttgatc tttgctaaac agtttattgg tagcgtaatt cacgttgtcg
99660
ttcaaaaaca gcaactcgtt gatgatcatt ttttgtaaaa gcgcgtactt gctcatgttg
99720
acagaatctc ttacatttca gttgtaaacg cgtctgtaca aattggccat gcgattcgga
99780
atgcacacgg ggatcgtgcg agccagtgcc gtttggcgaa atagcatttt ttcatagccg
99840
ctcgaacaat cgcacgcgtc cggcgaaaat tgcaccgtgt tcaaattcat attcaaccgg
99900
ccgtcgttgc atagataagg cctcggtgtt cccgtatcgt ccaccaagtc tctgtacgtg
99960
ctcacgcatg tttgagacac gacaaaatct ccgccggcgg agaaaacgtg aaccaagccc
100020
agtgcgggat cgcattctat caagtccgga gcctgcgcgt ttaccaaagc gtcggaggcg
100080
ttgcaaaagc catcctggca ggtcaactcg tttgcagcgc tggagatcac gcagttgtct
100140
ctacactgct gatccgtcac gcacggtaac cggttcaatg aacaatctac gcctcgattg
100200
cgctgaaacg taaaatttaa cggcggcgct tccaactcgt taatgtgcat gtatgcatct
100260
tgcaaaataa atttttgaac aaatttaaac gtgtacatgt acacgattag tataattacc
100320
agtagaataa gtatttgcca aaagttcaac atgatcgtct taactgagtg tgaaaagcgt
100380
ggtgtgacgc acgaaatgac tggttgcgca aaaaataaac cggggtctat ataactcggc
100440
gtcgaccgcg ttcattttta ccgtcatgca tctgacggct aatgtattgc tcgttcctaa
100500
cgcgctcaaa aagcgggacg tgaaatacat ttataatacc tatttgaaaa attacagtgt
100560
aattgaaggt gtgatgtgtt gcaatggcga ttgtttggcc gtggtggtgt tggaccgaaa
100620
tcagctgcaa aacacggaca tggaagtgtt ggagagttta gaatacacta gtgacaacat
100680
tgaactgtta tgcgaaaaaa tatgtgtgat agttgataat tacgacaagt attaccaaaa
100740
aaattgtgta taaataaaat accaaatttt attatatcat tttgttttat ttaataatta
100800
aagaatacaa cgccacatct attcctagta caacaaataa tttgattatt atttttgagt
100860
gcacattaaa aaataacaaa cagtgtaaaa atactacaga ataatacaat acataaatat
100920
tatagtaaat agctgcaatt ttgatagcgt aatttatact ttgatatttt tcaacgtaca
100980
acgttaaatg ttgatacgca ttattcacaa ataacaaaat ttttctaata tgccatttgt
101040
ccgcaattgt ttttgcgata tcaaagcctt tttcaaacaa ttgaaaaatt gcaaacaaaa
101100
ccacgtacat gacgttatac atagtgttaa agtttttaca taacaattct ataatgaaga
101160
aaattgctaa acacggcatg agcgcgcaca taatcgcgtt ggccgcaaat atctcgtacg
101220
tacaaaaata ctcggacatt ctccaataag taaaatgcat tttgctatta tactgttgtt
101280
tcttctagtg attattgcaa tagtgtacac gtatgtagac ttgatagatg tgcaccatga
101340
agaggtgcgt tatcctatta cggtttttga caacacacgc gcgccgctta ttgaaccgcc
101400
gtccgaaata gtaatcgaag gcaatgcaca cgaatgtcac aaaactttga cgccgtgctt
101460
cacacacggc gattgcgatc tgtgccgcga aggattagcc aactgccagt tgtttgacga
101520
agatacaata gtcaagatgc gtggagatga cggccaagaa cacgagacgc ttattcgagc
101580
gggagaagcg tactgcttgg ctttggatcg agaacgcgcc cgatcgtgta accccaacac
101640
gggtgtgtgg ttgttggccg aaactgaaac tggtttcgct cttttgtgca actgcttacg
101700
gcccggactt gttacgcagc tcaacatgta cgaagactgc aacgtgcccg tgggctgcgc
101760
gcctcacggc cgtatcgaca atatcaacag cgcttcgatc cggtgcgtgt gcgacgacgg
101820
gtacgtgagc gactataacg ccgacaccga aactccgtat tgccgtccgc gcaccgtgcg
101880
cgacgtaatg tacgacgaga gtttttttcc gcgggcgcca tgcgcagacg gccaagttcg
101940
tctggatcat ccggcgctca atgattttta ccgcagacac tttagactcg aagacatttg
102000
cgtgatcgac ccttgctcgg tggacccgat tagcgggcaa cgcacatcgg gacgcttatt
102060
tcaccaacca accgtaaatg gtgtgggaat caacggatgc aattgtccgg ccgatgacgg
102120
gttactgccc gtgtttaatc gacacaccgc cgacacgggc atggttagac aaagcgaccg
102180
caccgtcgcg aacgcttgct tgcagccgtt taacgtgcac atgttatcgt tgcgtcatgt
102240
ggattacaaa tttttctggg gccgcagcga ccacaccgag tttgccgacg cggacatggt
102300
gtttcaagcg aatgtcaacc aactcagtca cgaacggtat cgagcgattt tgtactcgtt
102360
gctcgagtcg cacccggacg taacagaaat cgtaacagtc aacatgggtg tcatgaaaat
102420
ttccgtgtca tacgatacca cattgaaaaa tatactatta ccatcttctg tttttaggct
102480
atttagattt aaagaaagtg gcactgctca gccggtatgc ttctttccag gcgtaggacg
102540
gtgcataacc gtcaattccg attcgtgcat caggcgacac gctggtggtc aagtgtggac
102600
cgcagaaacg ttcaccaact cgtggtgtgt actgagtcgt gaaggtacgc atataaaagt
102660
ttggagtcgc gcgtcacgat atccacgcgg agacgcgcct gcagcgttaa gattgcgcgg
102720
cttctttctg aacaacgatc gcgaacgaaa cacaataaga gcggtcacta caggcgacat
102780
gacccaaggg caacaaatag acgcattaac ccaaatactt gaaacttacc ccaactactc
102840
tgtataacaa catgagcatt ttaaaagttg tagaagcgtg cgatttggca cacacttttt
102900
tgaaattggg ttatttattt agggccaaga cttgtttgga tatcgcttta gataatttgg
102960
aactattgcg tcgaaagact aacataaaag aagtggcagt catgttaaac aagaaaacta
103020
cagagtgttt gcaattgaaa cgaaaaatag ataaaaaaat tgcacaacgt gttttaataa
103080
aaatttacac tatcaaatga tgacatcata acgggttcaa tattctgtgt gcaaaaataa
103140
atgacatcat atttcaaact tgttttacgc gtaaaattct actggtaaaa caagtttgag
103200
atatgatgtc atcatcacaa ataatagtat gtaataaaat aaacatattt gtgtgtaaat
103260
ataatttatt acaaataaat tttacattga atcaatctgt cttcgtgttt gttgtaaggt
103320
cttcgaatct tgtgtttcag cccctcggga tggtcaaaat gcgccgtagt aattgttaat
103380
ggatctttca acgatttttt gcccatggcg agtgtgacaa acgcggccac gacaaacagc
103440
aggataatca gtttcatggt gttctatatt tgacaatata tgggtcgctt ctaaatcacc
103500
ttgtccccaa aagcctcttt tatagttttt tagaacacgt tgtgtattcc aacagtaatt
103560
gttccatctc tttcaacagc cattcagcat ccggtcgttg actgtaatca tgctgaatta
103620
atttacaaac aatttcggtc aatttaggat ggccttggga taaacttgcc ggcatttgct
103680
gtacattgtt tctaaagtta gttagcgtag tttcgcgttc caaagcagtc ttgaagggca
103740
ttatcaattc gaataaaaca atgcccaaac tatacatgtc atttttgggg gtgtacactt
103800
ttttgatttg ttctggtgca gcgtacaaag ttatattttg agggttgttt ttgataaacg
103860
ttttgtatag actgccaaac atgccgccca catacaaatc aaagtcgggc ccagtcatga
103920
aaatatcttc gggattaata ttgtggtgca cgatatttac ggaatgaatc gctttcacgg
103980
cgctcaccaa atcaacaaac ttgctaatat aaaagccaaa atccgccgga actttaatgt
104040
tggtctttgc aaaagtttgc aaattgcgtt gtttcaaata gtcgctcaac atgtactcgt
104100
ttagaggcga cgcaaaatat atgcggtgct gccgcggatt caaataaacc aattgttcgg
104160
gtttcatggt atacagttaa gtgttaacgc gtcactaaat tcagacacga gcgcacgccc
104220
tatatacata caatttatcg cacaagatgc ttaacgcgat ctgtttataa actaaaacgc
104280
actgcaataa attttagcaa gcatttgtat ttaatcaatc gaaccgtgca ctgatataag
104340
aattaaaaat gggtttgttt gcgtgttgca caaaatacac aaggctgtcg accgacacaa
104400
aaatgaagtt tccctatgtt gcgttgtcgt acatcaacgt gacgctgtgc acctacaccg
104460
ccatgttggt gggatacatg gtaacattca atgactccag cgaattgaaa tatttacaat
104520
actggttgct gttgtcgttt ttgatgtccg tggtgctaaa cgctccgact ctgtggacga
104580
tgctcaaaac cacagaagcc catgaagtaa tttacgaaat gaagctgttc cacgccatgt
104640
actttagtaa cgtgctgttg aattatgtgg tgtttttgga caatcaaatg ggtacaaatt
104700
ttgtttttgt taacaattta attcactgtt gtgtactttt tatgatattt gttgaattgc
104760
ttatcctgtt gggccacaca atgggcacgt acacggatta tcaatatgtc aaatcgtgtt
104820
atatggttat attgtttgtt tcagttatga gtgttactat tgttatgggt ttagagtgtt
104880
tgaaaacgaa actaattgat aacagtttga tgtttaacgc gtttgtgtgc gctttgtaca
104940
ttgtgattgc aataatgtgg tctttaaaaa ataatttgac tagttattac gtttcaaatt
105000
tacaaagtat tcaagttgtt ccgttttcat acaacgatcc gccgccaccg ttctctaaca
105060
ttgtaatgga tgacataaaa aataaaaaat aatttataaa aatgtttttt attctttcac
105120
aattctgtaa attctaaaca aaaaatataa atacaaactt attatgttgt cgtctaaata
105180
aacatcaatt tgtaaatctg gacacctatt catatcattg atattacagt ctactataca
105240
acaattaaaa ctaaccaaat tatctttaca acaattaaag caattaaaac aatttaaata
105300
atcttcattg tcgtcgtata agtttatttg cactgtagac ggtgttacac agcgatccat
105360
tcgacgttcg tgttcgatca actttctcgc caacttgtac cataaaaatt gtttggacaa
105420
aaagttttcc aacaatggta acggccaatt caacgtgacg atgcgcacgt cctcgggtat
105480
gcatttgtta aaaaacacac agctcgcttt accaaacgaa agcaaaggta ctaaatatgg
105540
cgccattggc tgatttgtta ttccaagata attacaaata aactgatccg tcgtggggtg
105600
ataactggca ggtgtcagct ttaaataatc ttcaacgttg ttgtcgcgca aaagtctgca
105660
ttttacacgc gttgttaatc ccacgacttt tgcatgtaaa atcggatcca aatactgcag
105720
aatcgtgtct ataatttcta atggtaaacg tatgcgtttt gctcgtgggc gctttgtaac
105780
gctcgacatc ctaataacaa ctaacacaaa actaaaatga tactcaatat attgctttta
105840
cagttcatct ttaggtttaa actgtgcgtt tatcgcgttg agcaagtcgc cgttatcggc
105900
atcaatctcc caagcaaaca ggccgcccaa tttatttcgg tcgacatatt taacttttcc
105960
taacacagag tcgacgctgt caaacgaaat caaatcacct ttacttttat cgaaaacgta
106020
cgacgcttga gcggcgctgt caaacgtgta cacataattg ttgagatctt tttgaatttg
106080
acgataatct acaacaccgt cctcccacgt gcccgacacc ggcccgttgc cagtgccgga
106140
aaaatagttg tcattcgtat aatttgttac gccggtccag ccgcggccgt acatggcgac
106200
gcccacaatt attttgttgg gatcgacgcc ttgtttcagt aacgcatcga cagcgtagtg
106260
tgtagtgtat agctcttccg agttccaact tggcgcgtag actgttgttt ggtagcccaa
106320
atccgtgttt gaccaagccc ctttaaaatc gtaactcatg agaaatattt tgcctaatga
106380
cttttgcgct tcggcgtagt ttaccacggc aatcttgtcg taacccgcgc ttatagcgct
106440
tgttaattcg taaaccctgc cggtttgcgc ttcgaggtcg tctagcattg cgcgcagctc
106500
ctccaacaac aaaatgtatg ttttggcgtc acgctccgca tcgcccaacg acgggttagc
106560
ccctttgccg cccggaaact cccaatcgat gtctacaccg tcaaagaatt tccacacttg
106620
cagaaattcc ttaaccgaat ctacaaaaac gtttcttttt tcaacatcgt gcataaaata
106680
aaatgggtct gatagagtcc agcctcctat tgaaggaaga atttttaaat gggggtttgc
106740
taattttgcc gccatcaact gtccaaaatt gcctttatac ggctcgttcc aagcggacac
106800
acctttttgg ggtttttgta cggcggccca cggatcgtga atggcaactt tgaaatcttc
106860
gcgtcccttg cacgatcttt gcaaagattc aaagcttccg ggtatcgttt tgagggcgtc
106920
gtttattcca tcgccgccgc agatgggtat gaaaccatac aacaagtgtg ataaatttgg
106980
caagggaact ttgtctacgg gaaagttgcg cccgtacaca ccccactcaa caaagtacgc
107040
agcgacaatt ttatcctctc tcctgccagg tttgttgttt tccagccatg tgtattcgag
107100
cggtgccaga tggccgccgt cggtgtctgc gactttgacc aacacgggat cgctcacgga
107160
acagccgtcc tcattgcaaa gtttgacacg catgttaaat tgcccgctca caagaacttt
107220
aatggtagcc cttttacttt cggcgtcgcc tttccatacc tgctgctcgt caaacaacac
107280
gtacgctatg tcgccaatgt cgccgttcca gacgttccaa ctgacttgaa cgtcgacttg
107340
ttctttaggc tttattaaat tttcgtaagc ggtggcctcg taatttattt ctacgagcgc
107400
ataattgcga tcggcccaat cgatcaccgg cgtgccggga atcgcgttag aaacggcgac
107460
caaccacaaa acgtttaaca atttgtacaa cattttaatt tatcttaatt ttaagttgta
107520
attattttat gtaaaaaaat gaacaaaatt ttgttttatt tgtttgtgta cggcgttgta
107580
aacagcgcgg cgtacgacct tttgaaagcg cctaattatt ttgaagaatt tgttcatcga
107640
ttcaacaaag attatggtag cgaagttgaa aaattgcgaa gattcaaaat tttccaacac
107700
aatttaaatg aaattattaa taaaaaccaa aacgattcgg ccaaatatga aataaacaaa
107760
ttctcggatt tgtccaaaga cgaaactatc gcaaaataca caggtttgtc tttgcctatt
107820
cagactcaaa atttttgcaa agtaatagtc ctagaccagc caccgggcaa agggcccctt
107880
gaattcgact ggcgtcgtct caacaaagtc actagcgtaa aaaatcaggg catgtgtggc
107940
gcctgctggg cgtttgccac tctggctagt ttggaaagtc aatttgcaat caaacataac
108000
cagttgatta atctgtcgga gcagcaaatg atcgattgtg attttgtcga cgctggctgt
108060
aacggcggct tgttgcacac agcgttcgaa gccatcatta aaatgggcgg cgtacagctg
108120
gaaagcgact atccatacga agcagacaat aacaattgcc ttatgaactc caataagttt
108180
ctagttcaag taaaagattg ttatagatac attaccgtgt acgaggaaaa acttaaagat
108240
ttgttacgcc ttgtcggccc tattcctatg gccatagacg ctgccgacat tgttaactat
108300
aaacagggta ttataaaata ttgtttcaac agcggtctaa accatgcggt tcttttagtg
108360
ggttatggtg ttgaaaacaa cattccatat tggaccttta aaaacacttg gggcacggat
108420
tggggagagg acggattttt cagggtacaa caaaacataa acgcctgtgg tatgagaaac
108480
gaacttgcgt ctactgcagt catttattaa tctcaacaca ctcgctattt ggaacataat
108540
catatcgtct cagtagctca aggtagagcg tagcgctctg gatcgtatag atcttgctaa
108600
ggttgtgagt tcaagtctcg cctgagatat taaaaaactt tgtaatttta aaaattttat
108660
tttataatat acaattaaaa actatacaat tttttattat tacattaata atgatacaat
108720
ttttattatt acatttaata ttgtctatta cggtttctaa tcatacagta caaaaataaa
108780
atcacaatta atataattac aaagttaact acatgaccaa acatgaacga agtcaattta
108840
gcggccaatt cgccttcagc catggaagtg atgtcgctca gactggtgcc gacgccgcca
108900
aacttggtgt tctccatggt ggttatgagg ttgctttttt gttgggcaat aaacgaccag
108960
ccgctggcat ctttccaact gtcgtgatag gtcgtgttgc cgatggtcgg gatccaaaac
109020
tcgacgtcgt cgtcaattgc tagttccttg tagttgctaa aatctatgca ttgcgacgag
109080
tccgtgttgg ccacccaacg cccttctttg tagatgctgt tgttgtagca attactggtg
109140
tgtgccggcg gattggtgca cggcatcagc aaaaacgtgt cgtccgacaa aaatgttgaa
109200
gaaacagagt tgttcatgag attgccaatc aaacgctcgt ccaccttggc cacggagact
109260
atcaggtcgt gcagcatatt gtttagcttg ttgatgtgcg catgcatcag ctcaatgttc
109320
attttcagca aatcgttttc gtacatcagc tcctcttgaa tatgcatcag gtcgcctttg
109380
gtggcagtgt ctccctctgt gtacttggct ctaacgttgt ggcgccaagt gggcggccgc
109440
ttcttgactc ggtgctcgac tttgcgttta atgcatctgt taaacttgca gttccacgtg
109500
tttttagaaa gatcatatat atcattgtca atcaaacagt gttcgcgtgt caccgactcg
109560
gggttatttt tgtcatcttt aatgagcaga cacgcagctt ttatttggcg cgtggtgaac
109620
gtagactttt gtttgagaat catactcacg ccgtctcgat gaagcacagt gtccacggtc
109680
acgttgatgg ggttgccctc agcgtccaaa atgtatacct ggcactcgtc cgtgtcgtcc
109740
tggcactcga gcctgctgta cattttcgaa gtggaaatgc cgcatcgcca cgatttgttg
109800
cacgtgtggt gcgcaaagtg attgttattc tgccgcttca ccaactcttt gcctttgacc
109860
cactggccgc ggccctcgtt gtcgcgaaaa cagtcgtcgc tgtcactgcc ccaacggtcg
109920
atcagctctt cgcccacctc gcactgctgc ctgatgctcc acataagcaa atcctctttg
109980
cccacattca gcgttttcat ggtttcttcg acgcgtgtgt tgggatccag cgagccgccg
110040
ttgtacgcat acgcctggta gtaccccttg tagccgataa tcacgttttc gttgtagtcc
110100
gtctccacga tggtgatttc cacgtccttt tgcagcgttt ccttgggcgg ggtaatgtcc
110160
aagtttttaa tcttgtacgg acccgtcttc atttgcgcgt tgcagtgctc cgccgcaaag
110220
gcagaatgcg ccgccgccgc caaaagcaca tataaaacaa tagcgcttac catcttgctt
110280
gtgtgttcct tattgaagcc ttggtgtgac tgatttacta gtagcattga ggcatcttat
110340
atacccgacc gttatctggc ctacgtgaca caaggcacgt tgttagatta ataatcttat
110400
ctttttatct taattgataa gattattttt atctggctgt tataaaaacg ggatcatgaa
110460
cacggacgct cagtcgacat cgaacacgcg caacttcatg tactctcccg acagcagtct
110520
ggaggtggtc atcattacca attcggacgg cgatcacgat ggctatctgg aactaaccgc
110580
cgccgccaaa gtcatgtcac cttttcttag caacggcagt tcggccgtgt ggaccaacgc
110640
ggcgccctcg cacaaattga ttaaaaacaa taaaaattat attcatgtgt ttggtttatt
110700
taaatatctg tcaaattaca atttaaataa taaaaagcgt cctaaagagt attacaccct
110760
taaatcgatt attagcgact tgcttatggg cgctcaaggc aaagtatttg atccgctttg
110820
cgaagtaaaa acgcaactgt gtgcgattca ggagagtctc aacgaggcta tttcgatttt
110880
gaacgttcat agcaacgatg cggccgccaa cccgcctgcg ccagacatta acaagttgca
110940
agaactgata caagatttgc agtctgaata caataaaaaa attaccttta ccactgatac
111000
aattttggag aatttaaaaa atataaagga tttaatgtgc ctgaataaat aataataagg
111060
gttttgtacg atttcaacaa tgaacttttg ggccacgttt agcatttgtc tggtgggtta
111120
tttggtgtac gcgggacact tgaataacga gctacaagaa ataaaatcaa tattagtggt
111180
catgtacgaa tctatggaaa agcatttttc caatgtggta gacgaaattg attctcttaa
111240
aacggacacg tttatgatgt tgagcaactt gcaaaataac acgattcgaa cgtgggacgc
111300
agttgtaaaa aatggcaaaa aaatatccaa tctcgacgaa aaaattaacg tgttattaac
111360
aaaaaacggg gtagttaaca acgtgctaaa cgttcaataa acgcttatca ctaagttaat
111420
atactaaaaa tcacatagtc actacaatat ttcaaaatat gaagccgacg aataacgtta
111480
tgttcgacga cgcgtcggtc ctttggatcg acacggacta catttatcaa aatttaaaaa
111540
tgcctttgca ggcgtttcaa caacttttgt tcaccattcc atctaaacat agaaaaatga
111600
tcaacgatgc gggcggatcg tgtcataaca cggtcaaata catggtggac atttacggag
111660
cggccgttct ggttttgcga acgccttgct cgttcgccga ccagttgttg agcacattta
111720
ttgcaaacaa ttatttgtgc tacttttacc gtcgtcgccg atcacgatca cgctcacgat
111780
cacgctcgcg atcacgttct cctcattgca gacctcgttc gcgctctcct cattgcagac
111840
ctcgttcgcg atctcggtcc cggtctagat cgcggtcacg ttcatcgtct cccaggcgag
111900
ggcgtcgaca aatattcgac gcgctggaaa agattcgtca tcaaaacgac atgttgatga
111960
gcaacgtcaa ccaaataaat ctcaaccaaa ctaatcaatt tttagaattg tccaacatga
112020
tgacgggcgt gcgcaatcaa aacgtgcagc tcctcgcggc gttggaaacc gctaaagatg
112080
ttattttgac cagattaaac acattgcttg ccgagattac agactcgtta cccgacttga
112140
cgtccatgtt agataaatta gctgaacaat tgttggacgc catcaacacg gtgcagcaaa
112200
cgctgcgcaa cgagttgaac aacaccaact ctattttgac caatttagcg tcaagcgtca
112260
caaacatcaa cggtacgctc aacaatttgc tagccgctat cgaaaactta gtaggcggcg
112320
gcggcggtgg caattttaac gaagccgaca gacaaaaact ggacctcgtg tacactttgg
112380
ttaacgaaat caaaaatata ctcacgggaa cgctgacaaa aaaataagca tgtccgacaa
112440
aacaccaaca aaaaagggtg gcagccatgc catgacgttg cgagagcgcg gcgtaacaaa
112500
acccccaaaa aagtctgaaa agttgcagca atacaagaaa gccatcgctg ccgagcaaac
112560
gctgcgcacc acagcagatg tttcttcttt gcagaacccc ggggagagtg ccgtttttca
112620
agagttggaa agattagaga atgcagttgt agtattagaa aatgaacaaa aacgattgta
112680
tcccatatta gatacgcctc ttgataattt tattgtcgca ttcgtgaatc cgacgtatcc
112740
catggcctat tttgtcaata ccgattacaa attaaaacta gaatgtgcca gaatcagaag
112800
cgatttactt tacaaaaaca aaaacgaagt cgctatcaac aggcctaaga tatcgtcttt
112860
taaattgcaa ttgaacaacg taattttaga cactatagaa actattgaat acgatttaca
112920
aaataaagtt ctcacaatta ctgcacctgt tcaagatcaa gaactaagaa aatccattat
112980
ttattttaat attttaaata gtgacagttg ggaagtacca aagtatatga aaaaattgtt
113040
tgatgaaatg caattggaac ctcccgtcat tttaccatta ggtctttaga tttggtaagg
113100
ctagcacgtc gacatcatgt ttgcgtcgtt gacctcagag caaaagctgt tattaaaaaa
113160
atataaattt aacaattatg tgaaaacgat cgagttgagt caagcgcagt tggctcattg
113220
gcgttcaaac aaagatattc agccaaaacc tttggatcgt gcagaaattt tacgtgtcga
113280
aaaggccacc aggggacaaa gcaaaaatga gctgtggacg ctattgcgtt tggatcgcaa
113340
cacagcgtct gcatcgtcca actcgtccgg caacatgtta caacgaccag cgcttttgtt
113400
tggaaacgcg caagaaagtc acgtcaaaga aaccaacggc atcatgttag accacatgcg
113460
cgaaatcata gaaagtaaaa ttatgagcgc ggtcgttgaa acggttttgg attgcggcat
113520
gttctttagc cccttgggtt tgcacgccgc ttcgcccgat gcgtattttt ctctcgccga
113580
cggaacgtgg atcccagtgg aaataaaatg tccgtacaat taccgagaca cgaccgtgga
113640
gcagatgcgt gtcgagttgg ggaacggcaa tcgcaagtat cgcgtgaaac acaccgcgct
113700
gttggttaac aagaaaggca cgccccagtt cgaaatggtc aaaacggatg cgcattacaa
113760
gcaaatgcaa cggcagatgt atgtgatgaa cgcgcctatg ggcttttacg tggtcaaatt
113820
caaacaaaat ttggtggtgg tttctgtgcc gcgcgacgaa acgttctgca acaaagaact
113880
gtctacggaa aacaacgcgt acgtggcgtt tgccgtggaa aactccaact gcgcgcgcta
113940
ccaatgcgcc gacaagcgac ggctttcatt caaaacgcac agctgcaatc acaactatag
114000
tggtcaagaa atcgatgcta tggtcgatcg cggaatatat ttagattatg gacatttaaa
114060
atgtgcgtac tgtgatttta gctcagacag tcgggaaacg tgcgattctg ttttaaaacg
114120
cgagcacacc aactgcaaaa gttttaactt gaaacataaa aactttgaca atcctacata
114180
ctttgattat gttaaaagat tgcaaagttt gctaaagagt caccacttta gaaacgacgc
114240
taaaacactt gcctattttg gttactattt aactcataca ggaaccctga agaccttttg
114300
ctgcggatcg caaaactcgt cgcccaccaa acacgatcat ttaaacgact gtgtatatta
114360
tttggaaata aaataaacct ttatattata tataattctt ttatttatac atttgtttat
114420
acaattttat ttacgacaaa tattgactcg ttgttcagaa agtttaataa gcttgtcaat
114480
ttcttcggct tgcaaagggc tgccaacgcg ttcgttttga atgcgcgtaa tccggtttac
114540
ggtattgttg gcgcgaacaa taaactcctc aactggcaaa ttaacaattt tgtttgcgta
114600
ctcattgtgc actgcggcca ggttttgtag aatgttttcg ggaaaaatgg caattctatt
114660
aaatttgaca tgtttttgat tgtatacata gttttgatat tcttccagcg taggatattt
114720
gtttaaactc ttgacgcatt caatgtacaa tttgtgcagt gacaaaattc tgttaaaatc
114780
caaacgagaa catttctcaa aagttatttc ttgaccgttg aaatgtacac tttgcaattg
114840
tttcaataaa ctgtcgtaaa aagtttttcc ttcttcaagc acaaacgcgg ggcgcatcgt
114900
gttatctaca acgcttatgt acttgtcaaa atcttcaatt atatgataga aatacaaata
114960
tctctccgcg tttatggacg tgtcgtttaa aacatgttcg tcaacaactc cgttatgatt
115020
tactttcaaa aatttcaaat cttgcaaagc gtccgcgttg gtcaacttgt tgataataaa
115080
tttgtctttg cattcaaacg ctctgtttgc aatccactcc acagcgtcca aaacggacat
115140
gcgtttaaac atgttgatac gttttagaca atacgctcgt ttttttaccg cctcaacgtt
115200
cacgtccgtg tagtcgcacc attgcaggat ttgcaacatg tcctcggcaa aatgcgcgaa
115260
ctgccgcagc ttttcctttc caaaatgttg attgtcgtgt ttaaaaagca acgttgaaat
115320
ttccgagaca taccacaaag ccgtgggcaa ttttactttg atcagcggct ccatagccag
115380
gttgctgaac ccgatcatgc attccgtgtt gttaatgcgg taaatgacat agcgtttaaa
115440
gtagtccttt acattatcgt caatgtattc tgcgtcgttt atgtgcttgt acagcaaata
115500
gtacataagg cccgcgttaa acgcgacctt tttagcgtca aaatacgtgc acgccaacac
115560
gtaatcgttg tattcgtcga attgctcgtt gggcactatg gcgcccgtaa aagggcgtct
115620
gctgcgcggt gacaaacgcg ttccatgctg aatcaactgc ttcaaacttt ccaaattata
115680
acaatattca attgaatttt taatctcttt attttggctc cataaaagag gaaactcgag
115740
tcggctttta aacttggtca aactgccctg aattgtttca aacaagttgt aatgtgttaa
115800
caatatggcc ggcacaccgc tatcgttggc taaaatacaa tcggggaatc gaatattttc
115860
tacgttgctg taatcgtacg cttcgtcgtc gtcgttggca acaacatcgt cggtttcggc
115920
gtccacgctc gctaacttgt tctgatagtg taaatttttc attacatcaa aagcgtatga
115980
cttgttgcga ttgtgcaaat aatttatggc cgtgctaatg gtgctgtcga taattttatc
116040
aaaattgaga acatcggcgt tatacaacgt tttataaaat tctgttgact tgaacgtgtt
116100
tacaaactca tttttatttt taatctggtc aaaattcata ctagaattgt tagtttgttt
116160
gatttcgctg aatagccgct ggcggagacg cttcagcttg tccacctcgt ttaacacgtt
116220
ggcgtccgtc ggcatggaat tgataaattt gaaccgaaca aaagacagca gttcatcttt
116280
tttcgatata aaattttcgg ttgtaatgat atcgtagtta aattctttgg ttaaattgac
116340
ccattcgacc atttcatcgt tgcgataaat cttgcagtcc gagttgttga caaacgccga
116400
ggcaacggac aaatcaatct gttccgtgtt attattgatg gcataaaaca caatgcgttc
116460
gaaactaaac ggtttttcgt ttagcaaatt tttgcaaacg tttgcctcat ttttggaaat
116520
ttggccgtcg gtcaccatgt acaaaagttt caacttgccg tcgagcaagt ttatattctt
116580
gtgaatccac tttatgaatt cgctgggcct ggtgtcagta ccctcgccat tgcggcgcaa
116640
ataacgactc ttgacgtctc cgatttcttt ttggcggcaa taagcactcc aatgcaaata
116700
caaaactttg tcgcaactac tgatgttttc gatttcattc tgaaattgtt ctaaagtttg
116760
taacgcgttc ttgttaaagt aatagtccga gtttgtcgac aaggaatcgt cggtggcgta
116820
cacgtagtag ttaatcatct tgttgattga tatttaattt tggcgacgga tttttatata
116880
cacgagcgga gcggtcacgt tctgtaacat gagtgatcgt gtgtgtgtta tctctggcag
116940
cgcgatagtg gtcgcgaaaa ttacacgcgc gtcgtaacgt gaacgtttat attataaata
117000
ttcaacgttg cttgtattaa gtgagcattt gagctttacc attgcaaaat gtgtgtaatt
117060
tttccggtag aaatcgacgt gtcccagacg attattcgag attgtcaggt ggacaaacaa
117120
accagagagt tggtgtacat taacaagatt atgaacacgc aattgacaaa acccgttctc
117180
atgatgttta acatttcggg tcctatacga agcgttacgc gcaagaacaa caatttgcgc
117240
gacagaataa aatcaaaagt cgatgaacaa tttgatcaac tagaacgcga ttacagcgat
117300
caaatggatg gattccacga tagcatcaag tattttaaag atgaacacta ttcggtaagt
117360
tgccaaaatg gcagcgtgtt gaaaagcaag tttgctaaaa ttttaaagag tcatgattat
117420
accgataaaa agtctattga agcttacgag aaatactgtt tgcccaaatt ggtcgacgaa
117480
cgcaacgact actacgtggc ggtatgcgtg ttgaagccgg gatttgagaa cggcagcaac
117540
caagtgctat ctttcgagta caacccgatt ggtaacaaag ttattgtgcc gtttgctcac
117600
gaaattaacg acacgggact ttacgagtac gacgtcgtag cttacgtgga cagtgtgcag
117660
tttgatggcg aacaatttga agagtttgtg cagagtttaa tattgccgtc gtcgttcaaa
117720
aattcggaaa aggttttata ttacaacgaa gcgtcgaaaa acaaaagcat gatctacaag
117780
gctttagagt ttactacaga atcgagctgg ggcaaatccg aaaagtataa ttggaaaatt
117840
ttttgtaacg gttttattta tgataaaaaa tcaaaagtgt tgtatgttaa attgcacaat
117900
gtaactagtg cactcaacaa aaatgtaata ttaaacacaa ttaaataaat gttaaaattt
117960
attgcctaat attattttgt cattgcttgt catttattaa tttggatgat gtcatttgtt
118020
tttaaaattg aactggcttt acgagtagaa ttctacgcgt aaaacacaat caagtatgag
118080
tcataatctg atgtcatgtt ttgtacacgg ctcataaccg aactggcttt acgagtagaa
118140
ttctacttgt aatgcacgat cagtggatga tgtcatttgt ttttcaaatc gagatgatgt
118200
catgttttgc acacggctca taaactcgct ttacgagtag aattctacgt gtaacgcacg
118260
atcgattgat gagtcatttg ttttgcaata tgatatcata caatatgact catttgtttt
118320
tcaaaaccga acttgattta cgggtagaat tctacttgta aagcacaatc aaaaagatga
118380
tgtcatttgt ttttcaaaac tgaactcgct ttacgagtag aattctacgt gtaaaacaca
118440
atcaagaaat gatgtcattt gttataaaaa taaaagctga tgtcatgttt tgcacatggc
118500
tcataactaa actcgcttta cgggtagaat tctacgcgta aaacatgatt gataattaaa
118560
taattcattt gcaagctata cgttaaatca aacggacgtt atggaattgt ataatattaa
118620
atatgcaatt gatccaacaa ataaaattgt aatagagcaa gtcgacaatg tggacgcgtt
118680
tgtgcatatt ttagaaccgg gtcaagaagt gttcgacgaa acgctaagcc agtaccacca
118740
atttcctggc gtcgttagtt cgattatttt cccgcaactc gtgttaaaca caataattag
118800
cgttttgagc gaagacggca gtttgctcac gttgaaactc gaaaacactt gttttaattt
118860
tcacgtgtgc aataaacgct ttgtgtttgg caatttgcca gcggcggtcg tgaataatga
118920
aacgaagcaa aaactgcgca ttggagctcc aatttttgcc ggcaaaaagc tggtttcggt
118980
cgtgacggcg tttcatcgtg ttggcgaaaa cgaatggctg ttaccggtga cgggaattcg
119040
agaggcgtcc cagctgtcgg gacatatgaa ggtgctgaac ggcgtccgtg ttgaaaaatg
119100
gcgacccaac atgtccgtct acgggactgt gcaattgccg tacgataaaa ttaaacagca
119160
tgcgctcgag caagaaaata aaacgccaaa cgcgttggag tcttgtgtgc tattttacaa
119220
agattcagaa atacgcatca cttacaacaa gggggactat gaaattatgc atttgaggat
119280
gccgggacct ttaattcaac ccaacacaat atattatagt taaataagaa ttattatcaa
119340
atcatttgta tattaattaa aatactatac tgtaaattac attttattta caatcatgtc
119400
aaagcctaac gttttgacgc aaattttaga cgccgttacg gaaactaaca caaaggttga
119460
cagtgttcaa actcagttaa acgggctgga agaatcattc cagcttttgg acggtttgcc
119520
cgctcaattg accgatctta acactaagat ctcagaaatt caatccatat tgaccggcga
119580
cattgttccg gatcttccag actcactaaa gcctaagctg aaaagccaag cttttgaact
119640
cgattcagac gctcgtcgtg gtaaacgcag ttccaagtaa atgaatcgtt tttaaaataa
119700
caaatcaatt gttttataat attcgtacga ttctttgatt atgtaataaa atgtgatcat
119760
taggaagatt acgaaaaata taaaaaatat gagttctgtg tgtataacaa atgctgtaaa
119820
cgccacaatt gtgtttgttg caaataaacc catgattatt tgattaaaat tgttgttttc
119880
tttgttcata gacaatagtg tgttttgcct aaacgtatac tgcataaact ccatgcgagt
119940
gtatagcgag ctagtggcta acgcttgccc caccaaagta gattcgtcaa aatcctcaat
120000
ttcatcaccc tcctccaagt ttaacatttg gccgtcggaa ttaacttcta aagatgccac
120060
ataatctaat aaatgaaata gagattcaaa cgtggcgtca tcgtccgttt cgaccatttc
120120
cgaaaagaac tcgggcataa actctatgat ttctctggac gtggtgttgt cgaaactctc
120180
aaagtacgca gtcaggaacg tgcgcgacat gtcgtcggga aactcgcgcg gaaacatgtt
120240
gttgtaaccg aacgggtccc atagcgccaa aaccaaatct gccagcgtca atagaatgag
120300
cacgatgccg acaatggagc tggcttggat agcgattcga gttaacgctt tggcagtcac
120360
ggtcagcgtt ttgatggcga tcacgttgag cgagtgcact aacgcggctt tgtaagtctc
120420
tcccaacatg cgcacggtca cgcgccgagt cgtgctaagc aacatgtgtt tcatggccgg
120480
aatgagagaa gtgttaattt ttttcaacat gcttttaaac ccggacatta gcatatcaaa
120540
gccaatgtcc gtagcaatac cgaaaacgag cgcgtaatct tccaaaaacg atgttataat
120600
tgactccaag tcttggtcgc tgattgaacg gtcgagcgcc tcgaaatgtt cgacacgtgc
120660
acgttcgtta ccgcggtaat tgtatgcgat cggagtttta gtaaagccgg tttcggccgt
120720
gtacgtgatc tggacgggcg acccgttgac gatcatgccc aaatcgttta gtgttggatt
120780
tttgttaaaa agtttttcaa attccaagtc tgtggcgtta tcgcgcacgc tgcgccattg
120840
cgctagtatt gcgttggagt ccacgttggg tcgtggcggt agtatgctgg aaggcgcttt
120900
gtaatcaaaa tcgcgcagtt cgctaaaaat gttgttggcc agcattttga aagtgacaaa
120960
gatcgtgtcg cccagcacga atccgatgag cgattcccac catctaaacg aacaaccgcc
121020
gttgaatagc tctctgccga aacgtcgaca gtaggcttcg ttgaattcgc ctttaaagcg
121080
ttcgggaaac aaggggtcgg gatcgggccg aacgttaaaa gccggcacat cgtccacgcc
121140
catgatcgtg tgttcttcgg tgcgcaagta tgggctgtta aagtacattt tggacagcga
121200
gtccactaag atgcatttgt tgtcgagcgt gtatctaaac tcggcagact gaacttgggt
121260
ttcggcgcct tcacgcatgg ccgccgccct gtccaggtgg tagcacgcgg gctgcgcgta
121320
acccacgcta gtctcggagg tctgcgtgta catgaacggc gtcgtgttgg acacgacgcc
121380
ggtttcgtga aacggatagc agctcatgct ttcacacccg cgcttgctga aagccagttt
121440
gacggccagc gctttgtcgg ccaatttcgg cggcacataa taatcgtcgt cacttgacgc
121500
gggacgcagc gtgtagtcga ttagtatatg cggaaacctg gtgcgccatc tcgaaataaa
121560
ctcgagacga tgcatatgta tggcatacct actggcatta gttaaatcga cggctgttaa
121620
aaccgccatg ttatatagga cttaaaataa acaacaatat ataatgaaat atttattaga
121680
ttatattata gcaatacatt tacatttatt ataacaatac tttttattta atctgattat
121740
attataacga tacattttta tttagacatt gttatttaca atattaatta actttttata
121800
catttttaaa tcataatata taatcatttc gttgtgcatt tcaaagcttt tgatagcttc
121860
aaagtaatac atgaatttag agtattcagg aaaatgataa acgttggtaa acccgcattt
121920
ggtacaatat aacacgggat ttttataata cagtttagtt tttttacaca atttgcaata
121980
gttgttagtt gtaggtttca aaggaaacgt gattgcgccg tccaatacct gggtaaactt
122040
tttgacttta acagtggcaa acacggttcc tttgataccc gaaaatcggt tgtcttgcag
122100
agcggccatc atttcgcttg gctcttgaag tataaaacag ttgacgtcat ccaccacgtc
122160
gggtctggtg cacatgcttc ggtagcgctg caacactata ttggtgtatg tttccctgag
122220
aacgagaccg ccggtggtgc taagatcgat tgtttgaatg cgctcgttgg gctctttgtg
122280
atttcgaatt atgcgccgaa ttatttcaaa cactttgcag ttgtgatcgt caattctcaa
122340
ttctttaact tccgtcgtgt gctctaaact tacagggaaa atgtattggt aaaaaaacct
122400
ctctctggct aaatagctga ggtcgaccaa attgatagaa ggatatattt cgtacgaggt
122460
ttttggaacg ttgtgatata gatagcattt ttgacagcag atgtctatgc ggtcaggatc
122520
gtccaacggc ttttcgatgt gaaccacaac atacaaaaac cattcgcgcg tgttgtcttt
122580
gaatctataa ttgcaagtgg tgcatcgcga atcgctcatg tgctccatag tcttcttgta
122640
tttcacaggc ctgcttgcaa atttgcccgt catgcgcata tctttgctgt ttatgtagcc
122700
cataatgtaa ttggtggaaa attttagcgt ggctttcatg atgtcgcgtt ctaaatcgct
122760
catgaaatgc atacgtagat cgcgctcttg tttgaaatcc agtttgtcgc tgtacgcggg
122820
caaaccttca aacttgttcc caaactcggg cggcacaaaa tatccatctt ttctgttgac
122880
gactggtttt ttacttacaa tgctgctgtg ctccaacggc ttggccggag aggtgcgcgt
122940
aggctgttta ggcggagaga tgcgcgtagg tggtttgatg ttagattttg gcggcggacg
123000
aacaggcgac ggcggcgagt tggcggcagg cgctggcaaa gatttggcac gacccttgcc
123060
cccggtcctt ggcgcgtcaa aaatgttatt ctctcgaaaa aaacggttca ttgtaactgt
123120
tagttagcac tcagaaatca acacgatact gtgcacgttc agccatcgag aggctttata
123180
tatggaaacc ttatctatag agataagatt gtatatgcgt aggagagcct ggtcacgtag
123240
gcactttgcg cacggcacta gggctgtgga ggggacaggc tatataaagc ccgtttgccc
123300
aactcgtaaa tcagtatcaa ttgtgctccg gcgcacacgc tcgcttgcgc gccggatagt
123360
ataagtaatt gataacgggc aacgcaacat gataagaacc agcagtcacg tgctgaacgt
123420
ccaggaaaat ataatgacgt caaactgtgc gtcatcgcca tattcgtgcg aggcaacgtc
123480
cgcttgcgca gaagctcaac aggtaatgat cgataacttt gttttctttc acatgtacaa
123540
cgccgacata caaattgacg caaagctgca atgcggcgtg cgctcggccg cgtttgcaat
123600
gatcgacgat aaacatttgg aaatgtacaa gcatagaata gagaataaat ttttttatta
123660
ctatgatcaa tgtgccgaca ttgccaaacc cgaccgtctg cccgatgacg acggcgcgtg
123720
ctgtcaccat tttatttttg atgcccaacg tattattcaa tgtattaaag agattgaaag
123780
cgcgtacggc gtgcgtgatc gcggcaatgt aatagtgttt tatccgtact tgaaacagtt
123840
gcgagacgcg ttgaagctaa ttaaaaactc ttttgcgtgt tgttttaaaa ttataaattc
123900
tatgcaaatg tacgtgaacg agttaatatc aaattgcctg ttgtttattg aaaagctgga
123960
aactattaat aaaactgtta aagttatgaa tttgtttgta gacaatttgg ttttgtacga
124020
atgcaatgtt tgtaaagaaa tatctacgga tgaaagattt ttaaagccaa aagaatgttg
124080
cgaatacgct atatgcaacg cgtgctgcgt taacatgtgg aagacggcca ccacgcacgc
124140
aaaatgtcca gcgtgcagga catcgtataa ataagcacgc aacgcaaaat gagtggtggc
124200
ggcaacttgt tgactctgga aagagatcat tttaaatatt tatttttgac cagctatttt
124260
gatttaaaag ataatgaaca tgttccttca gagcctatgg catttattcg caattacttg
124320
aattgcacgt ttgatttgct agacgatgcc gtgctcatga actatttcaa ttacttgcaa
124380
agcatgcaat tgaaacattt ggtgggcagc acgtcgacaa acattttcaa gtttgtaaag
124440
ccacaattta gatttgtgtg cgatcgcaca actgtggaca ttttagaatt tgacacgcgc
124500
atgtacataa aacccggcac gcccgtgtac gccacgaacc tgttcacgtc caatccccgc
124560
aagatgatgg ctttcctgta cgctgaattt ggcaaggtgt ttaaaaataa aatattcgta
124620
aacatcaaca actacggctg cgtgttggcg ggcagtgccg gtttcttgtt cgacgatgcg
124680
tacgtggatt ggaatggtgt gcgaatgtgt gcggcgccgc gattagataa caacatgcat
124740
ccgttccgac tgtatctact gggcgaggac atggctaagc actttgtcga taataatata
124800
ctaccgccgc acccttctaa cgcaaagact cgcaaaatca acaattcaat gtttatgctg
124860
aaaaactttt acaaaggtct gccgctgttc aaatcaaagt acacggtggt gaacagcact
124920
aaaatcgtga cccgaaaacc caacgatata tttaatgaga tagataaaga attaaatggc
124980
aactgtccgt ttatcaagtt tattcagcgc gactacatat tcgacgccca gtttccgcca
125040
gatttgcttg atttgctaaa cgaatacatg accaaaagct cgatcatgaa aataattacc
125100
aagtttgtga ttgaagaaaa ccccgctatg agcggtgaaa tgtctcgcga gattattctt
125160
gatcgctact cagtagacaa ttatcgcaag ctgtacataa aaatggaaat aaccaaccag
125220
tttcctgtca tgtacgatca tgaatcgtcg tacatttttg tgagcaaaga ctttttgcaa
125280
ttgaaaggca ctatgaacgc gttctacgcg cccaagcagc gtatattaag tattttggcg
125340
gtgaatcgtt tgtttggcgc cacggaaacg atcgactttc atcccaacct gctcgtgtac
125400
cggcagagtt cgccgccggt ccgtttgacg ggcgacgtgt atgttgttga taagaacgaa
125460
aaagtttttt tggtcaaaca cgtgttctca aacacggtgc ctgcatatct tttaataaga
125520
ggtgattacg aaagttcgtc tgacttgaaa tcccttcgcg atttgaatcc gtgggttcag
125580
aacacgcttc tcaaattatt aatccccgac tcggtacaat aatatgattt acactgatcc
125640
cactactggc gctacgacta gcacagacgc gccgtccaca aactatttaa acaggctaac
125700
tccaaacatg ttcttgacca tcttggctgt agtagtaatt attgctttaa taattatatt
125760
tgttcaatct agcagtaatg gaaacagctc ggggggtaat gtacctccaa acgccctggg
125820
gggttttgta aatcctttaa acgctaccat gcgagctaat ccctttatga acacgcctca
125880
aaggcaaatg ttgtagataa gtgtataaaa aatgaaacgt atcaaatgca acaaagttcg
125940
aacggtcacc gagattgtaa acagcgatga aaaaatccaa aagacctacg aattggctga
126000
atttgattta aaaaatctaa gcagtttaga aagctatgaa actctaaaaa ttaaattggc
126060
gctcagcaaa tacatggcta tgctcagcac cctggaaatg actcaaccgc tgttggaaat
126120
atttagaaac aaagcagaca ctcggcagat tgccgccgtg gtgtttagca cattagcttt
126180
tatacacaat agattccatc cccttgttac taattttact aacaaaatgg agtttgtggt
126240
cactgaaacc aacgacacaa gcattcccgg agaacccatt ttgtttacgg aaaacgaagg
126300
tgtgctgctg tgttccgtgg acagaccgtc tatcgttaaa atgctaagcc gcgagtttga
126360
caccgaggct ttagtaaact ttgaaaacga caactgcaac gtgcggatag ccaagacgtt
126420
tggcgcctct aagcgcaaaa acacgactcg cagcgatgat tacgagtcaa ataaacaacc
126480
caattacgat atggatttga gcgattttag cataactgag gttgaagcca ctcaatattt
126540
aactctgttg ctgaccgtcg aacatgccta tttacattat tatattttta aaaattacgg
126600
ggtgtttgaa tattgcaaat cgctaacgga ccattcgctt tttaccaaca aattgcgatc
126660
gacaatgagc acaaaaacgt ctaatttact gttaagcaaa ttcaaattta ccattgaaga
126720
ttttgacaaa ataaactcaa attctgtaac atcagggttt aatatatata attttaataa
126780
ataattaaat aatatacaat gtttttatta attatatttt taatattaat taaagtatta
126840
atatttaaaa aaatgaatca aattcatcta aagtgtcaca gcgataaaat ttgtcctaaa
126900
gggtattttg gcctcaacgc cgatccctat gattgcacgg cgtattatct gtgtccgcat
126960
aaagtgcaaa tgttttgcga attaaatcac gaatttgact tggactccgc cagctgcaag
127020
cctatcgtgt acgatcacac gggcagcggg tgtacggctc gcatgtatag aaacttgtta
127080
ctatgaagag cgggtttcca gttgcacaac actattatcg atttgcagtt cgggacataa
127140
atgtttaaat atatcgatgt ctttgtgatg cgcgcgacat ttttgtaggt tattgataaa
127200
atgaacggat acgttgcccg acattatcat taaatccttg gcgtagaatt tgtcgggtcc
127260
attgtccgtg tgcgctagca tgcccgtaac ggacctcgta cttttggctt caaaggtttt
127320
gcgcacagac aaaatgtgcc acacttgcag ctctgcatgt gtgcgcgtta ccacaaatcc
127380
caacggcgca gtgtacttgt tgtatgcaaa taaatctcga taaaggcgcg gcgcgcgaat
127440
gcagctgatc acgtacgctc ctcgtgttcc gttcaaggac ggtgttatcg acctcagatt
127500
aatgtttatc ggccgactgt tttcgtatcc gctcaccaaa cgcgtttttg cattaacatt
127560
gtatgtcggc ggatgttcta tatctaattt gaataaataa acgataaccg cgttggtttt
127620
agagggcata ataaaagaaa tattgttatc gtgttcgcca ttagggcagt ataaattgac
127680
gttcatgttg gatattgttt cagttgcaag ttgacactgg cggcgacaag atcgtgaaca
127740
accaagtgac tatgacgcaa attaatttta acgcgtcgta caccagcgct tcgacgccgt
127800
cccgagcgtc gttcgacaac agctattcag agttttgtga taaacaaccc aacgactatt
127860
taagttatta taaccatccc accccggatg gagccgacac ggtgatatct gacagcgaga
127920
ctgcggcagc ttcaaacttt ttggcaagcg tcaactcgtt aactgataat gatttagtgg
127980
aatgtttgct caagaccact gataatctcg aagaagcagt tagttctgct tattattcgg
128040
aatcccttga gcagcctgtt gtggagcaac catcgcccag ttctgcttat catgcggaat
128100
cttttgagca ttctgctggt gtgaaccaac catcggcaac tggaactaaa cggaagctgg
128160
acgaatactt ggacaattca caaggtgtgg tgggccagtt taacaaaatt aaattgaggc
128220
ctaaatacaa gaaaagcaca attcaaagct gtgcaaccct tgaacagaca attaatcaca
128280
acacgaacat ttgcacggtc gcttcaactc aagaaattac gcattatttt actaatgatt
128340
ttgcgccgta tttaatgcgt ttcgacgaca acgactacaa ttccaacagg ttctccgacc
128400
atatgtccga aactggttat tacatgtttg tggttaaaaa aagtgaagtg aagccgtttg
128460
aaattatatt tgccaagtac gtgagcaatg tggtttacga atatacaaac aattattaca
128520
tggtagataa tcgcgtgttt gtggtaactt ttgataaaat taggtttatg atttcgtaca
128580
atttggttaa agaaaccggc atagaaattc ctcattctca agatgtgtgc aacgacgaga
128640
cggctgcaca aaattgtaaa aaatgccatt tcgtcgatgt gcaccacacg tttaaagctg
128700
ctctgacttc atattttaat ttagatatgt attacgcgca aaccacattt gtgactttgt
128760
tacaatcgtt gggcgaaaga aaatgtgggt ttcttttgag caagttgtac gaaatgtatc
128820
aagataaaaa tttatttact ttgcctatta tgcttagtcg taaagagagt aatgaaattg
128880
agactgcatc taataatttc tttgtatcgc cgtatgtgag tcaaatatta aagtattcgg
128940
aaagtgtgca gtttcccgac aatcccccaa acaaatatgt ggtggacaat ttaaatttaa
129000
ttgttaacaa aaaaagtacg ctcacgtaca aatacagcag cgtcgctaat cttttgttta
129060
ataattataa atatcatgac aatattgcga gtaataataa cgcagaaaat ttaaaaaagg
129120
ttaagaagga ggacggcagc atgcacattg tcgaacagta tttgactcag aatgtagata
129180
atgtaaaggg tcacaatttt atagtattgt ctttcaaaaa cgaggagcga ttgactatag
129240
ctaagaaaaa caaagagttt tattggattt ctggcgaaat taaagatgta gacgttagtc
129300
aagtaattca aaaatataat agatttaagc atcacatgtt tgtaatcggt aaagtgaacc
129360
gaagagagag cactacattg cacaataatt tgttaaaatt gttagcttta atattacagg
129420
gtctggttcc gttgtccgac gctataacgt ttgcggaaca aaaactaaat tgtaaatata
129480
aaaaattcga atttaattaa ttatacatat attttgaatt taattaatta tacatatatt
129540
ttatattatt tttgtctttt attatcgagg ggccgttgtt ggtgtggggt tttgcataga
129600
aataacaatg ggagttggcg acgttgctgc gccaacacca cctcctcctc ctcctttcat
129660
catgtatctg tagataaaat aaaatattaa acctaaaaac aagaccgcgc ctatcaacaa
129720
aatgataggc attaacttgc cgctgacgct gtcactaacg ttggacgatt tgccgactaa
129780
accttcatcg cccagtaacc aatctagacc caagtcgcca actaaatcac caaacgagta
129840
aggttcgatg cacatgagtg tttggcccgc aggaagatcg ctaatatcta cgtattgagg
129900
cgaatctggg tcggcggacg gatcgctgcc gcgacaaact gttttttcta cttcatagtt
129960
gaatccttgg cacatgttgg ttagttcggg cggattgtta ggcaacaagg ggtcgaatgg
130020
gcaaatggta acatccgact gatttagatt ggggtcttga cgacaagtgc gctgcaataa
130080
caagcaggcc tcggcgattt ctccggcgtc tttaccttgc acataataac ttccgccggt
130140
gttattgatg gcgttgatta tatcttgtac tagtgtggcg gcgctaaaca agaaatagcc
130200
gccggtggcc aagagtatgc ccgttcctcc tacttttaag ctttgcatgt aactatgtag
130260
acgggggttt tgctgcagtg cgttttgaac accttcgggc gtgcgcacgt tggtttccgg
130320
gaagttttgt ttgactgcat tggatcgcgt ctgcttggtg tggtaattaa agtctggcac
130380
gttgtccacg cgccgcaatt ggctcaatga gtttatttga gggtctgaaa tgccctgaaa
130440
tactccgcgt atgttgggga catcattgtt acgagtaatt ctgtttatgt ctgaagtgct
130500
cacaaactgg ttgttagata gttgatagcc cggctgaaat ctgttgtttc caatgttgcg
130560
tacactgggc gcgttgagca catttgtgaa accggcggga gtgcttgtta aaagacgcgt
130620
attatcagta ataaaactgg cctgattagg atacaattta ttgactgcgc gaagatttga
130680
aaaaaaactc attttaaagc aaacttattt aataaatata tcacagtaaa ggttttgcaa
130740
aactgccgtc gtcaatacaa cacggcagcg gcgtcatgtt ggtaaaatct aatcttctcc
130800
ttgctttaga ttctgggcga gaaggcgcat ttgttgtgta agttatttcg acgtctgcat
130860
tatttgttgt gtaaggtatc tcgacgtatg aagcaacttt aacattgtta taattttttt
130920
taaatattga tgcgctccac ggcgcgcgtt gatacggatg atatctctcc attgtatgat
130980
cgctaaattt atataccgtt tcaataaata tgttaaaacc caacatgtta attataatat
131040
tcataatagt ttgtttgttt tcaataatta tttttactgt tttgaaatct aaaagaggtg
131100
acgatgacga atcagacgac gggttcagtt gctataacaa accaattgga gtaaattttc
131160
cgcatcctac tagatgtgac gctttctaca tgtgtgtcgg tttaaatcaa aaattagagt
131220
taatctgccc tgaaggattt gaatttgatc cagatgttaa aaattgtgtt cctatatcag
131280
attatggatg taccgctaac caaaactaaa aataaaataa aatttatata gattaatgaa
131340
ataaaattta tatagattaa taaaataaaa tttatttaat atattatact atttatatta
131400
tttacaacac ttaacgtcta gacataacag tttgtaactt agaaactaaa tcagagttac
131460
tgcgctcaaa ctctgaaaat ttggcttgag actcggccac ctgcttacgc aattgttctt
131520
gcagattatt cacagtcgat tgcaactctt ctgatttctt ggtagattct tgcaagtcat
131580
agtttgcctt ttgtaaatct aattcggcga cagcatgctt gtgtttaagc ataatgtagt
131640
cgctgtttaa catggtcatt ttatgttcaa cttggctggt cttggctcgc agctcggaca
131700
gttctttttg caattgctcc acatagttca agtccgtggt gtgattgttg accgtgttat
131760
tttctaaaag ctcgcgccaa tgctgtttga tggaatcctg gttacgagtg acgttaatgg
131820
gcataaattc tacatacccg tgcttattgt acacgcgaca atctgatgaa gtagcgctgc
131880
aaaaacattt gtacacagaa ttgtccataa ttatcttgac ataacacttg aaacacacag
131940
catggttaca atgaatcgaa gtcacaaacg aggaatttac gtttttagtg tctttaaaag
132000
tagtaaaaca aatattacac gaaacctcta cttcttcttc gggttctgat tgctgctgct
132060
gctgctgctg cggctgcgga gactgcggcg aggcaaacaa atctggcgac tgtggtatta
132120
cgtaattcgg cgaataagat ggactataag tgggagacct tggggcaatc tcattcatca
132180
gctgagcctc aagatctaaa cctcgttgca gagccctctg cgcagctgtc tccgacgcaa
132240
tgttatcctg gtactgctgg gcagtgatgt cgggaaaccg ttcacgatcc acattttcac
132300
tattaattag tatgacgtca tcctcttgac ttaatagcgg atcgtcattg ctaatgttaa
132360
cctgaccgtg cacgtaatac gtgacaccct gacgatggta ggtgcgcgtc aacggctcgt
132420
tgacgttccc gataatctgc acgttttctt cgctgacacg ctgctcctga cgccgctcct
132480
gacggcgatg gctgcgactg cttgaagacg gctggctgcg actgcttgaa gacggctggg
132540
cttcgggaga tgttgtaaag ttgatgcggc gacggctgag agacagcctg tggcggcggc
132600
tgctgctggg agtggcggcg ttgatttggc gactcatggc tgggctggta ggatactgtt
132660
cactaggctg tgaggcttga actgtgctta cgagtagaac ggcagctgta tttatactgt
132720
ttatcagtac tgcacgactg ataagacaat agtggtgggg gaacttgcca ggcaaaaatg
132780
aacttttttg taatgcaaaa aagttgatag tgtagtagta tattgggagc gtatcgtaca
132840
gtgtagacta ttctaataaa atagtctacg atttgtagag attgtactgt atatggagtg
132900
tcaggcaaaa gtgaactttt ttgcattgca aaaaaattca ttttaaattt atcatatcac
132960
aggctgcagt ttctgttatc tgtcccccac tcaggcgtgc agctataaaa gcaggcactc
133020
accaactcgt aagcacagtt cgttgtgaag tgaacacgga gagcctgcca ataagcaaaa
133080
tgccaaggga caccaacaat cgccaccggt ctacgccata tgaacgtcct acgcttgaag
133140
atctccgcag acagttgcaa gacaatttgg acagcataaa cccccgagac agaatgcaag
133200
aagaacaaga agaaaacctg cgctatcaag tgcgtagaag gcagcgtcaa aaccagctcc
133260
gctccataca aatggaacag cagcgaatga tggcggaatt aaacaacgag ccggtgatta
133320
attttaaatt tgagtgtagt gtgtgtttag aaacatattc ccaacaatct aacgatactt
133380
gtcctttttt gattccgact acgtgcgacc acggtttttg tttcaaatgc gtcatcaatc
133440
tgcaaagcaa cgcgatgaat attccgcatt ccactgtgtg ctgtccattg tgcaataccc
133500
aggtaaaaat gtggcgttcc ttaaagccta acgctgttgt gacgtgtaag ttttacaaga
133560
aaactcaaga aagagttccg cccgtgcagc agtataaaaa cattattaaa gtgctacaag
133620
aacggagcgt gattagtgtc gaagacaacg acaataattg tgacataaat atggagaatc
133680
aggcaaagat agctgctttg gaagctgaat tggaagaaga aaaaaatcac agtgatcaag
133740
tagcttctga aaaccgacag ctgatagaag aaaatactcg tctcaatgaa cagattcaag
133800
agttgcagca tcaggtgagg acattggtgc cgcaacgtgg cattacggtt aatcagcaaa
133860
ttggccgtga cgacagtgcg ccagccgagc tgaacgagcg ttttcgctca cttgtctatt
133920
cgactatttc agagctgttt attgaaaatc gcgttcatag tattcaaaat tatgtttatg
133980
ccggaacttc tgctgctagt tcatgtgatg taaatgttac tgttaatttt gggtttgaaa
134040
attaatgtga tatgaaatgt atatataaaa atgatggaat aaataataaa catttttata
134100
ctttttatgt tttttttatt tcatgtgatt aagaaacttt taagatggat agtagtaatt
134160
gtattaaaat agatgtaaaa tacgatatgc cgttacatta tcaatgtgac aataacgcag
134220
ataaagacgt tgtaaatgcg tatgacacta tcgatgttga ccccaacaaa agatttataa
134280
ttaatcataa tcacgaacaa caacaagtca atgaaacaaa taaacaagtt gtcgataaaa
134340
cattcataaa tgacacagca acatacaatt cttgcataat aaaaatttaa atgacatcat
134400
atttgagaat aacaaatgac attatccctc gattgtgttt tacaagta 134448
<210>3
<211>296
<212>PRT
<213>Porcine circovirus
<400>3
Val Arg Arg Glu Ser Pro Lys His Arg Trp Cys Phe Thr Ile Asn Asn
1 5 10 15
Trp Thr Pro Thr Glu Trp Glu Ser Ile Val Glu Cys Gly Gly Ser Ile
20 25 30
Ala Arg Tyr Leu Ile Ile Gly Lys Glu Val Gly Lys Gly Gly Thr Pro
35 40 45
His Leu Gln Gly Tyr Val Asn Phe Lys Asn Lys Arg Arg Leu Ser Ser
50 55 60
Val Lys Arg Leu Pro Gly Phe Gly Arg Ala His Leu Glu Pro Ala Arg
65 70 75 80
Gly Ser His Lys Glu Ala Ser Glu Tyr Cys Lys Lys Glu Gly Asp Tyr
85 90 95
Leu Glu Ile Gly Glu Asp Ser Ser Ser Gly Thr Arg Ser Asp Leu Gln
100 105 110
Ala Ala Ala Arg Ile Leu Thr Glu Thr Ser Gly Asn Leu Thr Glu Val
115 120 125
Ala Glu Lys Met Pro Ala Val Phe Ile Arg Tyr Gly Arg Gly Leu Arg
130 135 140
Asp Phe Cys Gly Val Met Gly Leu Gly Lys Pro Arg Asp Phe Lys Thr
145 150 155 160
Glu Val Tyr Val Phe Ile Gly Pro Pro Gly Cys Gly Lys Thr Arg Glu
165 170 175
Ala Cys Ala Asp Ala Ala Ala Arg Glu Leu Gln Leu Tyr Phe Lys Pro
180 185 190
Arg Gly Pro Trp Trp Asp Gly Tyr Asn Gly Glu Gly Ala Val Ile Leu
195 200 205
Asp Asp Phe Tyr Gly Trp Val Pro Phe Asp Glu Leu Leu Arg Ile Gly
210 215 220
Asp Arg Tyr Pro Leu Arg Val Pro Val Lys Gly Gly Phe Val Asn Phe
225 230 235 240
Val Ala Lys Val Leu Tyr Ile Thr Ser Asn Val Val Pro Glu Glu Trp
245 250 255
Tyr Ser Ser Glu Asn Ile Arg Gly Lys Leu Glu Ala Leu Phe Arg Arg
260 265 270
Phe Thr Lys Val Val Cys Trp Gly Glu Gly Gly Ile Lys Lys Asp Met
275 280 285
Glu Thr Val Tyr Pro Ile Asn Tyr
290 295
<210>4
<211>214
<212>PRT
<213>Porcine circovirus
<400>4
Met Arg His Arg Ala Ile Phe Arg Arg Lys Pro Arg Pro Arg Arg Arg
1 5 10 15
Arg Arg His Arg Arg Arg Tyr Val Arg Arg Lys Leu Phe Ile Arg Arg
20 25 30
Pro Thr Ala Gly Thr Tyr Tyr Thr Lys Lys Tyr Ser Thr Met Asn Val
35 40 45
Ile Ser Val Gly Thr Pro Gln Asn Asn Lys Pro Trp His Ala Asn His
50 55 60
Phe Ile Thr Arg Leu Asn Glu Trp Glu Thr Ala Ile Ser Phe Glu Tyr
65 70 75 80
Tyr Lys Ile Leu Lys Met Lys Val Thr Leu Ser Pro Val Ile Ser Pro
85 90 95
Ala Gln Gln Thr Lys Thr Met Phe Gly His Thr Ala Ile Asp Leu Asp
100 105 110
Gly Ala Trp Thr Thr Asn Thr Trp Leu Gln Asp Asp Pro Tyr Ala Glu
115 120 125
Ser Ser Thr Arg Lys Val Met Thr Ser Lys Lys Lys His Ser Arg Tyr
130 135 140
Phe Thr Pro Lys Pro Ile Leu Ala Gly Thr Thr Ser Ala His Pro Gly
145 150 155 160
Gln Ser Leu Phe Phe Phe Ser Arg Pro Thr Pro Trp Leu Asn Thr Tyr
165 170 175
Asp Pro Thr Val Gln Trp Gly Ala Leu Leu Trp Ser Ile Tyr Val Pro
180 185 190
Glu Lys Thr Gly Met Thr Asp Phe Tyr Gly Thr Lys Glu Val Trp Ile
195 200 205
Arg Tyr Lys Ser Val Leu
210
<210>5
<211>2000
<212>DNA
<213>Porcine circovirus
<400>5
tagtattacc cggcacctcg gaacccggat ccacggaggt ctgtagggag aaaaagtggt 60
atcccattat ggatgctccg caccgtgtga gtggatatac cgggcagtgg atgatgaagc
120
ggcctcgtgt tttgatgccg caggacgggg actggataac tgagtttttg tggtgctacg
180
agtgtcctga agataaggac ttttattgtc atcctattct aggtccggag ggaaagcccg
240
aaacacaggt ggtgttttac gataaacaac tggaccccga ccgagtggga atctattgtg
300
gagtgtggag gcagtatagc gagatacctt attatcggca aagaggttgg aaaaggcggt
360
accccacact tgcaagggta cgtgaatttc aagaacaaaa ggcgactcag ctcggtgaag
420
cgcttacccg gatttggtcg ggcccatctg gagccggcga gggggagcca caaagaggcc
480
agcgagtatt gcaagaaaga gggggattac ctcgagattg gcgaagattc ctcttcgggt
540
accagatcgg atcttcaagc agcagctcgg attctgacgg agacgtcggg aaatctgact
600
gaagttgcgg agaagatgcc tgcagtattt atacgctatg ggcggggttt gcgtgatttt
660
tgcggggtga tggggttggg taaaccgcgt gattttaaaa ctgaagttta tgtttttatt
720
ggtcctccag gatgcgggaa aacgcgggaa gcttgtgcgg atgcggctgc gcgggaattg
780
cagttgtatt tcaagccacg ggggccttgg tgggatggtt ataatgggga gggtgctgtt
840
attctggatg atttttatgg gtgggttcca tttgatgaat tgctgagaat tggggacagg
900
taccctctga gggttcctgt taagggtggg tttgttaatt ttgtggctaa ggtattatat
960
attactagta atgttgtacc ggaggagtgg tattcctcgg agaatattcg tggaaagttg
1020
gaggccttgt ttaggaggtt cactaaggtt gtttgttggg gggagggggg gataaagaaa
1080
gacatggaga cagtgtatcc aataaactat tgattttatt tgcacttgtg tacaattatt
1140
gcgttggggt gggggtattt attgggtggg tgggtgggca gccccctagc cacggcttgt
1200
cgcccccacc gaagcatgtg ggggatgggg tccccacatg cgagggcgtt tacctgtgcc
1260
cgcacccgaa gcgcagcggg agcgcgcgcg aggggacacg gcttgtcgcc accggagggg
1320
tcagatttat atttattatc acttagagaa cggacttgta acgaatccaa acttctttgg
1380
tgccgtagaa gtctgtcatt ccagtttttt ccgggacata aatgctccaa agcagtgctc
1440
cccattgaac ggtggggtca tatgtgttga gccatggggt gggtctggag aaaaagaaga
1500
ggctttgtcc tgggtgagcg ctggtagttc ccgccagaat tggtttgggg gtgaagtaac
1560
ggctgtgttt ttttttagaa gtcataactt tacgagtgga actttccgca taagggtcgt
1620
cttggagcca agtgtttgtg gtccaggcgc cgtctagatc tatggctgtg tgcccgaaca
1680
tagtttttgt ttgctgagct ggagaaatta cagggctgag tgtaactttc atctttagta
1740
tcttataata ttcaaagcta attgcagttt cccattcgtt taggcgggta atgaagtggt
1800
tggcgtgcca gggcttatta ttctgagggg ttccaacgga aatgacgttc atggtggagt
1860
atttctttgt gtagtatgtg ccagctgtgg gcctcctaat gaatagtttt cttctgacat
1920
agcgccttct gtggcgtcgt cgtctccttg ggcggggttt tcttctgaat atagctctgt
1980
gtctcatttt ggtgccgggc 2000
<210>6
<211>645
<212>DNA
<213>Porcine circovirus
<400>6
atgcgccacc gtgctatctt caggcgtagg cctaggccca gaaggaggag gagacaccgc 60
cgtcgttacg ctagacgccg tctgttcatc aggagaccaa ccgccggtac ttactacacc
120
aagaagtact ccactatgaa cgtgatcagc gtcggcaccc cacagaacaa caagccttgg
180
cacgctaacc acttcatcac tcgcctgaac gagtgggaaa ctgccatcac cttcgagtac
240
tacaagatcc tgaagatgaa ggtgaccctg tcccctgtca tcagccccgc tcagcagacc
300
aagactatgt tcggccacac tgctatcgac ctggacggag cctggaccac taacacctgg
360
ctgcaggacg acccctacgc cgaatccagc actaggaagg tcatgaccca gccattctct
420
cactcaagat acttcactcc aaagcctctg ctggctggaa ccacttccgc ccaccctgga
480
cagtctctgt tcttcttctc ccgccccacc ccatggctga acacttacga ccctaccgtg
540
cagtggggtg ccctgctgtg gtctatctac gtccccgaga agactggtat gaccgacttc
600
tacggcacca aggaagtgtg gatcaggtac aagtcagtcc tgtga 645
<210>7
<211>735
<212>DNA
<213>Porcine circovirus
<400>7
atgcgccacc gtgctatctt ccgccgtagg ccaaggccta gacgccgtag gagacaccgc 60
cgtcgttacg ctagacgccg tctgttcatc aggagaccta ccgccggaac ttactacacc
120
aagaagtact ctactatgaa cgtgatctca gtcggtaccc ctcagaacaa caagccatgg
180
cacgctaacc acttcatcac tcgcctgaac gagtgggaaa ctgccatcac cttcgagtac
240
tacaagatcc tgaagatgaa ggtgaccctg tctccagtca tctcacctgc tcagcagacc
300
aagactatgt tcggtcacac tgctatcgac ctggacggcg cctggaccac taacacctgg
360
ctgcaggacg acccctacgc cgaatccagc actaggaagg tcatgacctc caagaagaag
420
cactcaagat acttcactcc caagccactg ctggctggca ccacttctgc ccacccagga
480
cagtccctgt tcttcttctc ccgccctacc ccctggctga acacttacga ccctactgtg
540
cagtggggcg ccctgctgtg gtccatctac gtccctgaga agactggaat gaccgacttc
600
tacggtacca aggaagtctg gatcaggtac aagagcgtgc tggtcaagat caacatcaac
660
ctgactcctc ccgtggctac ttctcgtgtg ccaagcagag ctctgccact gaggttcggt
720
tgcggccacc gttga 735
<210>8
<211>214
<212>PRT
<213>Porcine circovirus
<400>8
Met Arg His Arg Ala Ile Phe Arg Arg Arg Pro Arg Pro Arg Arg Arg
1 5 10 15
Arg Arg His Arg Arg Arg Tyr Ala Arg Arg Arg Leu Phe Ile Arg Arg
20 25 30
Pro Thr Ala Gly Thr Tyr Tyr Thr Lys Lys Tyr Ser Thr Met Asn Val
35 40 45
Ile Ser Val Gly Thr Pro Gln Asn Asn Lys Pro Trp His Ala Asn His
50 55 60
Phe Ile Thr Arg Leu Asn Glu Trp Glu Thr Ala Ile Thr Phe Glu Tyr
65 70 75 80
Tyr Lys Ile Leu Lys Met Lys Val Thr Leu Ser Pro Val Ile Ser Pro
85 90 95
Ala Gln Gln Thr Lys Thr Met Phe Gly His Thr Ala Ile Asp Leu Asp
100 105 110
Gly Ala Trp Thr Thr Asn Thr Trp Leu Gln Asp Asp Pro Tyr Ala Glu
115 120 125
Ser Ser Thr Arg Lys Val Met Thr Gln Pro Phe Ser His Ser Arg Tyr
130 135 140
Phe Thr Pro Lys Pro Leu Leu Ala Gly Thr Thr Ser Ala His Pro Gly
145 150 155 160
Gln Ser Leu Phe Phe Phe Ser Arg Pro Thr Pro Trp Leu Asn Thr Tyr
165 170 175
Asp Pro Thr Val Gln Trp Gly Ala Leu Leu Trp Ser Ile Tyr Val Pro
180 185 190
Glu Lys Thr Gly Met Thr Asp Phe Tyr Gly Thr Lys Glu Val Trp Ile
195 200 205
Arg Tyr Lys Ser Val Leu
210
<210>9
<211>244
<212>PRT
<213>Porcine circovirus
<400>9
Met Arg His Arg Ala Ile Phe Arg Arg Arg Pro Arg Pro Arg Arg Arg
1 5 10 15
Arg Arg His Arg Arg Arg Tyr Ala Arg Arg Arg Leu Phe Ile Arg Arg
20 25 30
Pro Thr Ala Gly Thr Tyr Tyr Thr Lys Lys Tyr Ser Thr Met Asn Val
35 40 45
Ile Ser Val Gly Thr Pro Gln Asn Asn Lys Pro Trp His Ala Asn His
50 55 60
Phe Ile Thr Arg Leu Asn Glu Trp Glu Thr Ala Ile Thr Phe Glu Tyr
65 70 75 80
Tyr Lys Ile Leu Lys Met Lys Val Thr Leu Ser Pro Val Ile Ser Pro
85 90 95
Ala Gln Gln Thr Lys Thr Met Phe Gly His Thr Ala Ile Asp Leu Asp
100 105 110
Gly Ala Trp Thr Thr Asn Thr Trp Leu Gln Asp Asp Pro Tyr Ala Glu
115 120 125
Ser Ser Thr Arg Lys Val Met Thr Ser Lys Lys Lys His Ser Arg Tyr
130 135 140
Phe Thr Pro Lys Pro Leu Leu Ala Gly Thr Thr Ser Ala His Pro Gly
145 150 155 160
Gln Ser Leu Phe Phe Phe Ser Arg Pro Thr Pro Trp Leu Asn Thr Tyr
165 170 175
Asp Pro Thr Val Gln Trp Gly Ala Leu Leu Trp Ser Ile Tyr Val Pro
180 185 190
Glu Lys Thr Gly Met Thr Asp Phe Tyr Gly Thr Lys Glu Val Trp Ile
195 200 205
Arg Tyr Lys Ser Val Leu Val Lys Ile Asn Ile Asn Leu Thr Pro Pro
210 215 220
Val Ala Thr Ser Arg Val Pro Ser Arg Ala Leu Pro Leu Arg Phe Gly
225 230 235 240
Cys Gly His Arg
<210>10
<211>244
<212>PRT
<213>Porcine circovirus
<400>10
Met Arg His Arg Ala Ile Phe Arg Arg Arg Pro Arg Pro Arg Arg Arg
1 5 10 15
Arg Arg His Arg Arg Arg Tyr Ala Arg Arg Arg Leu Phe Ile Arg Arg
20 25 30
Pro Thr Ala Gly Thr Tyr Tyr Thr Lys Lys Tyr Ser Thr Met Asn Val
35 40 45
Ile Ser Val Gly Thr Pro Gln Asn Asn Lys Pro Trp His Ala Asn His
50 55 60
Phe Ile Thr Arg Leu Asn Glu Trp Glu Thr Ala Ile Thr Phe Glu Tyr
65 70 75 80
Tyr Lys Ile Leu Lys Met Lys Val Thr Leu Ser Pro Val Ile Ser Pro
85 90 95
Ala Gln Gln Thr Lys Thr Met Phe Gly His Thr Ala Ile Asp Leu Asp
100 105 110
Gly Ala Trp Thr Thr Asn Thr Trp Leu Gln Asp Asp Pro Tyr Ala Glu
115 120 125
Ser Ser Thr Arg Lys Val Met Thr Gln Pro Phe Ser His Ser Arg Tyr
130 135 140
Phe Thr Pro Lys Pro Leu Leu Ala Gly Thr Thr Ser Ala His Pro Gly
145 150 155 160
Gln Ser Leu Phe Phe Phe Ser Arg Pro Thr Pro Trp Leu Asn Thr Tyr
165 170 175
Asp Pro Thr Val Gln Trp Gly Ala Leu Leu Trp Ser Ile Tyr Val Pro
180 185 190
Glu Lys Thr Gly Met Thr Asp Phe Tyr Gly Thr Lys Glu Val Trp Ile
195 200 205
Arg Tyr Lys Ser Val Leu Val Lys Ile Asn Ile Asn Leu Thr Pro Pro
210 215 220
Val Ala Thr Ser Arg Val Pro Ser Arg Ala Leu Pro Leu Arg Phe Gly
225 230 235 240
Cys Gly His Arg
<---

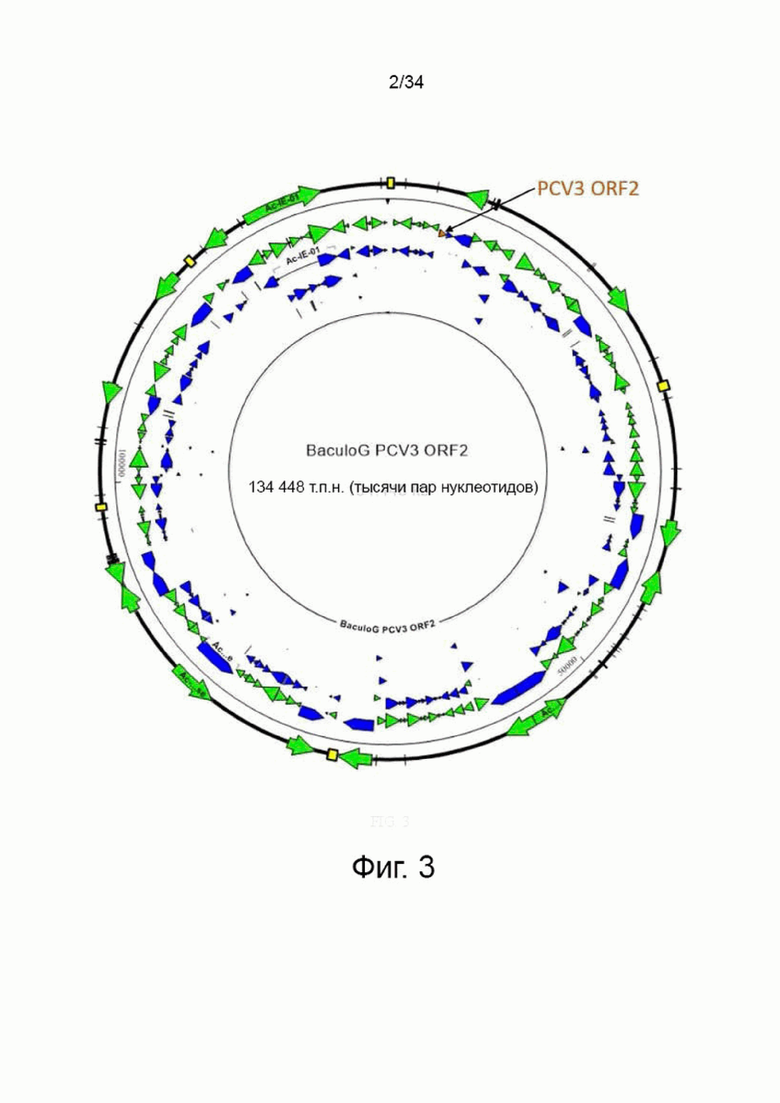
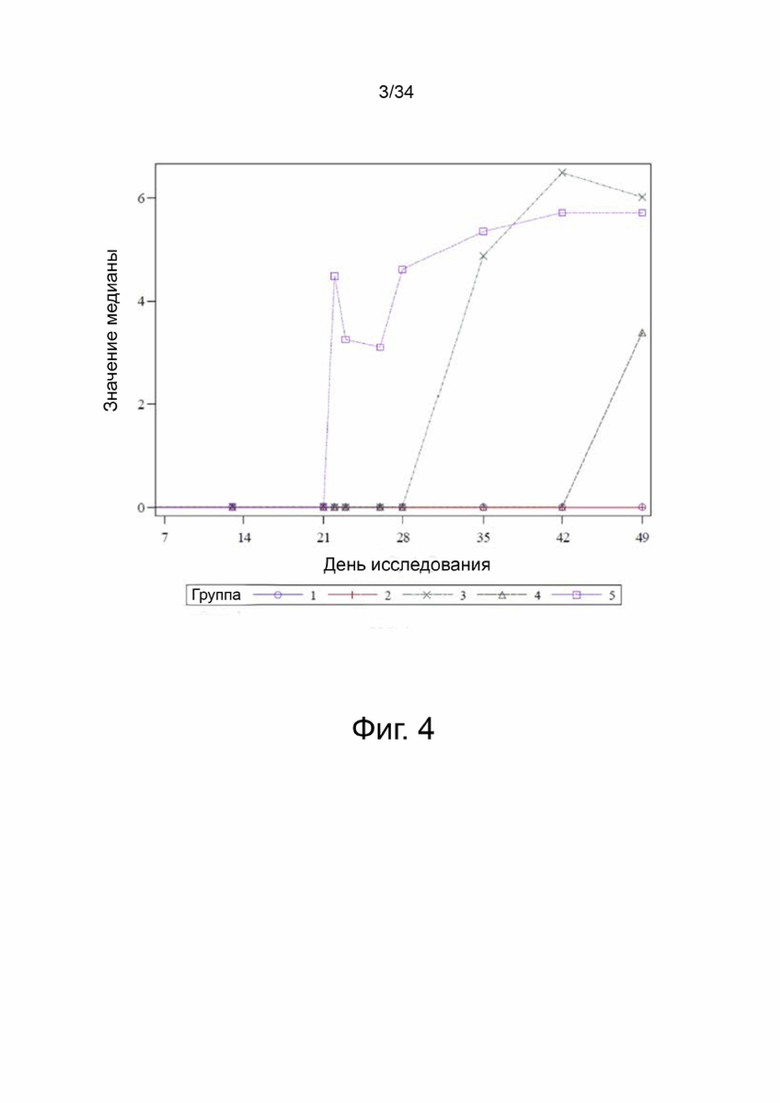
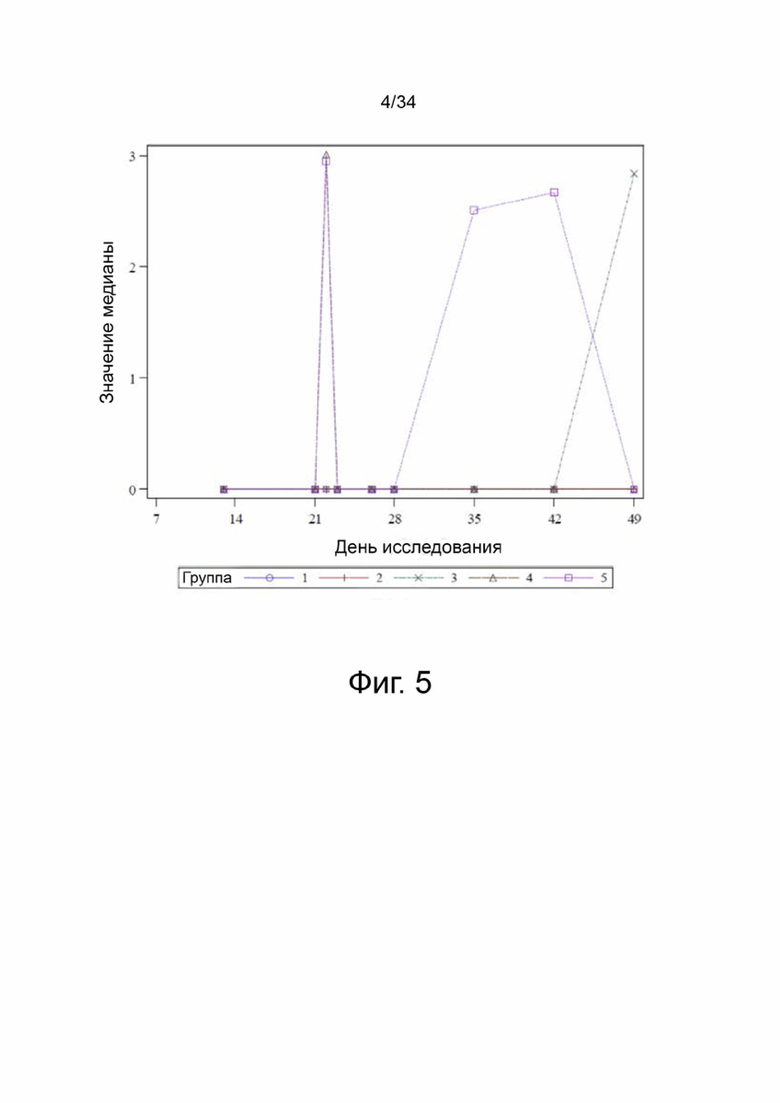
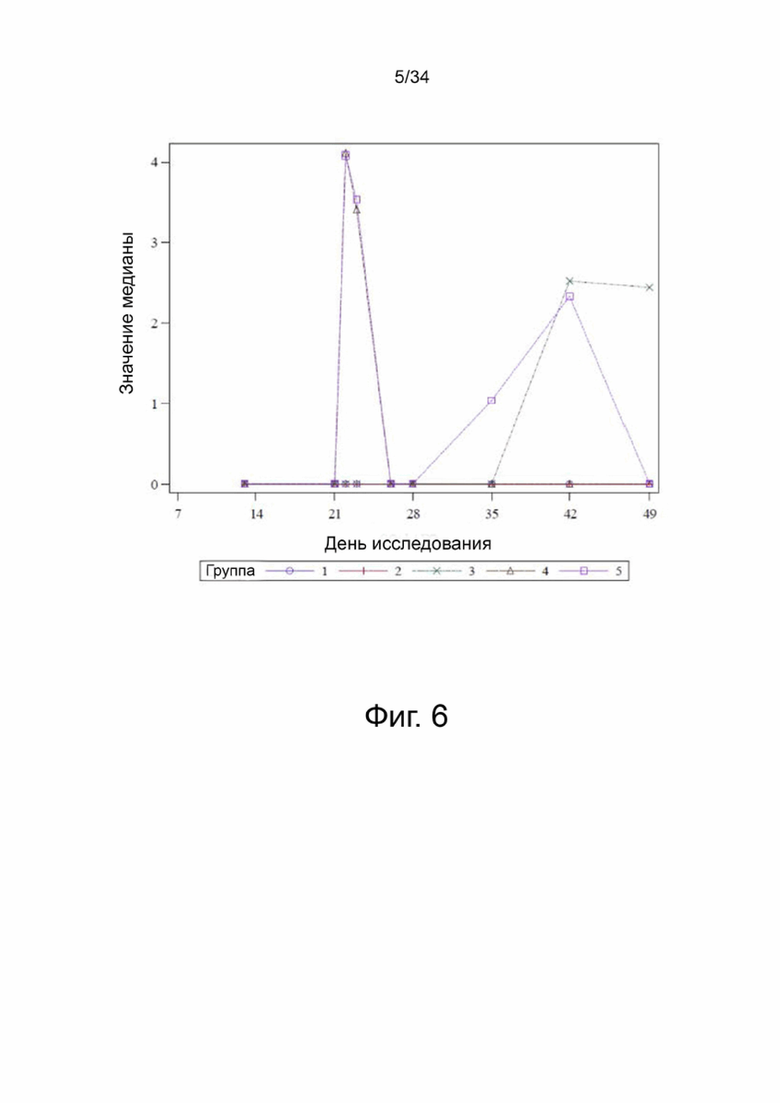
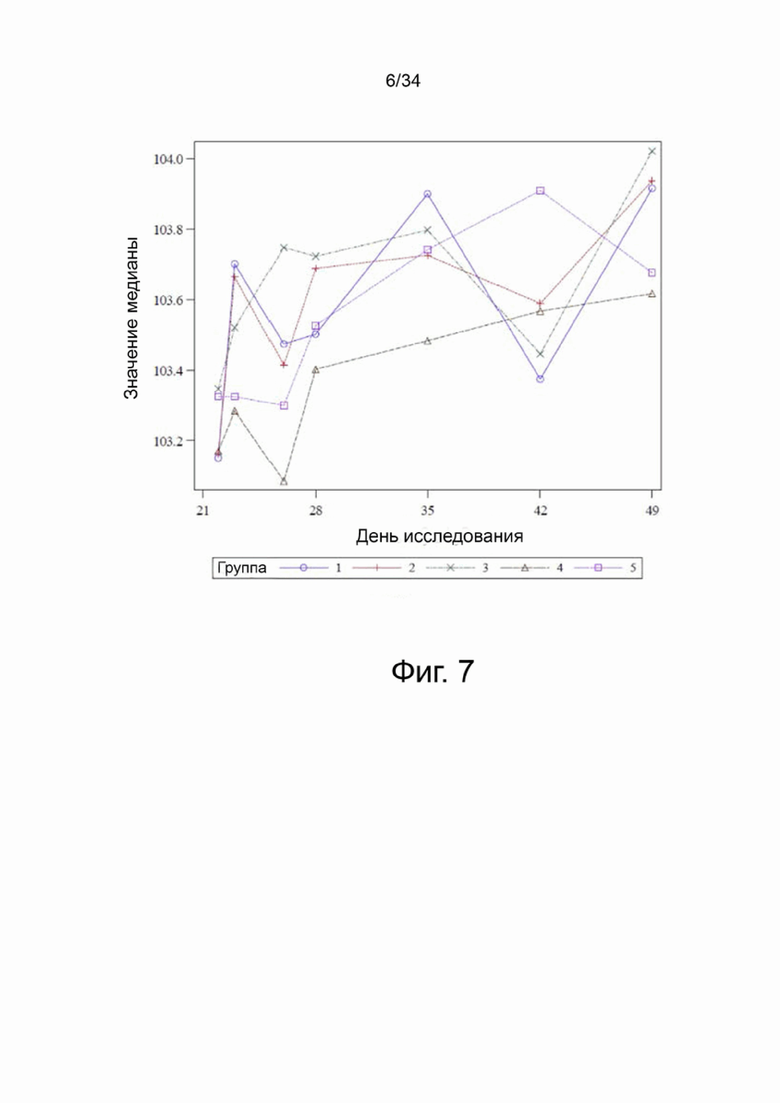
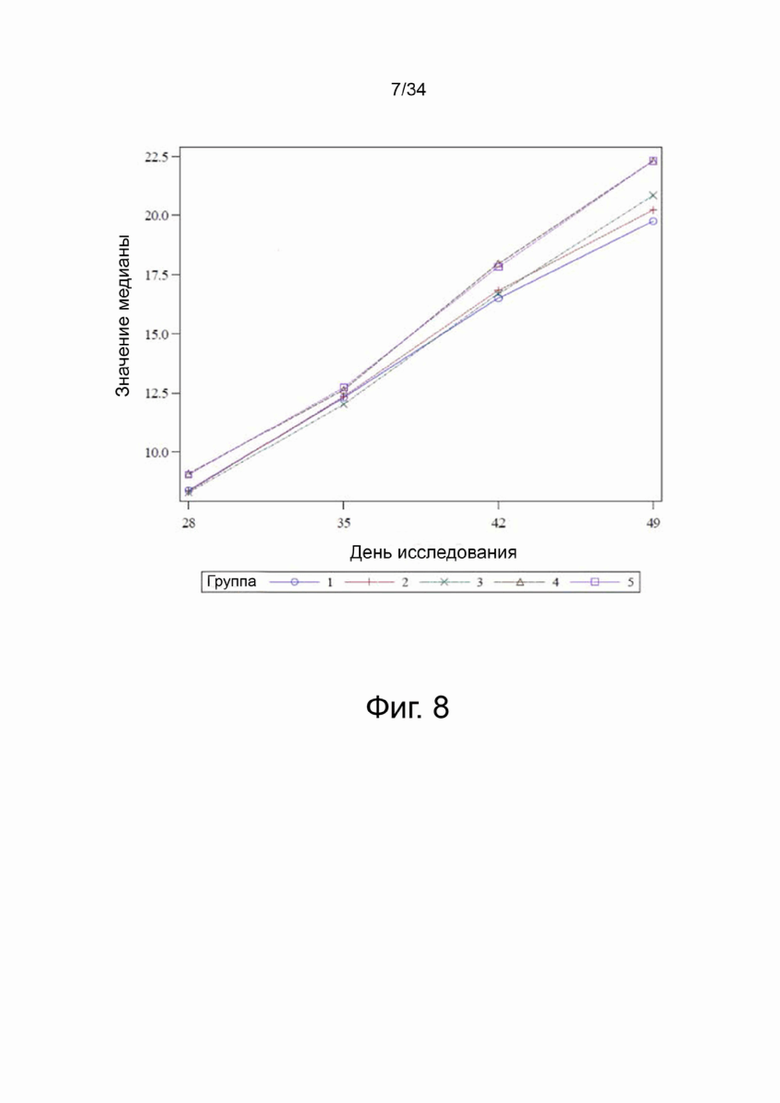
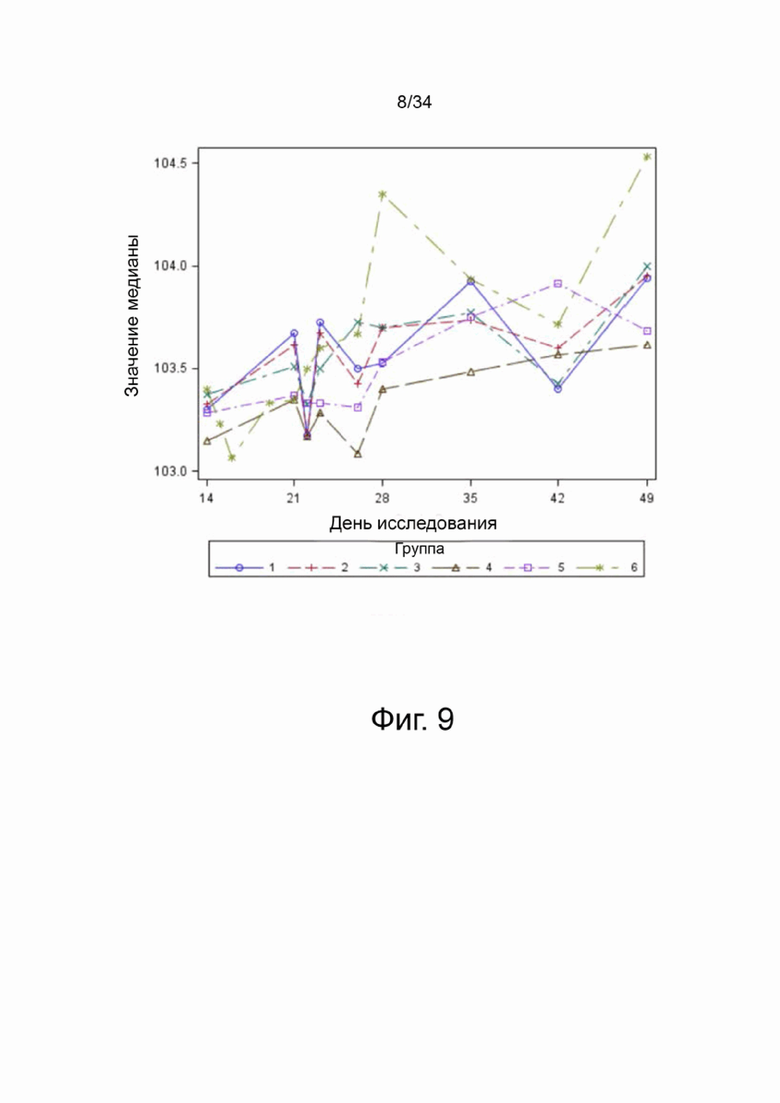



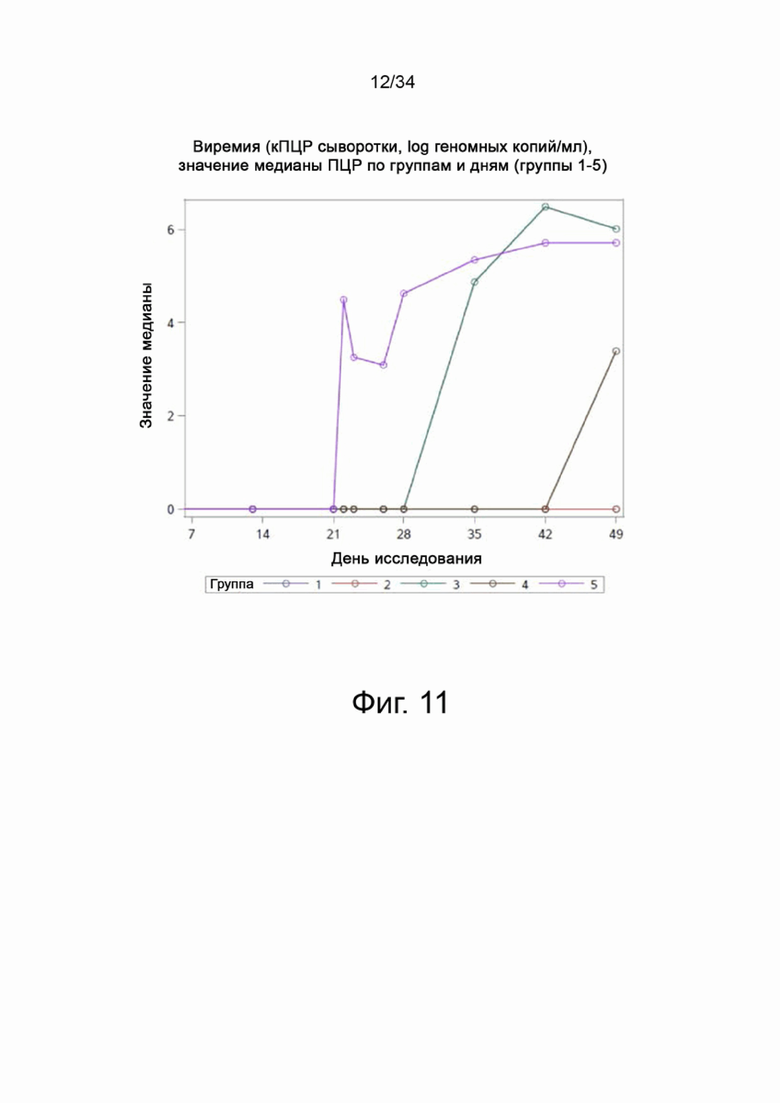
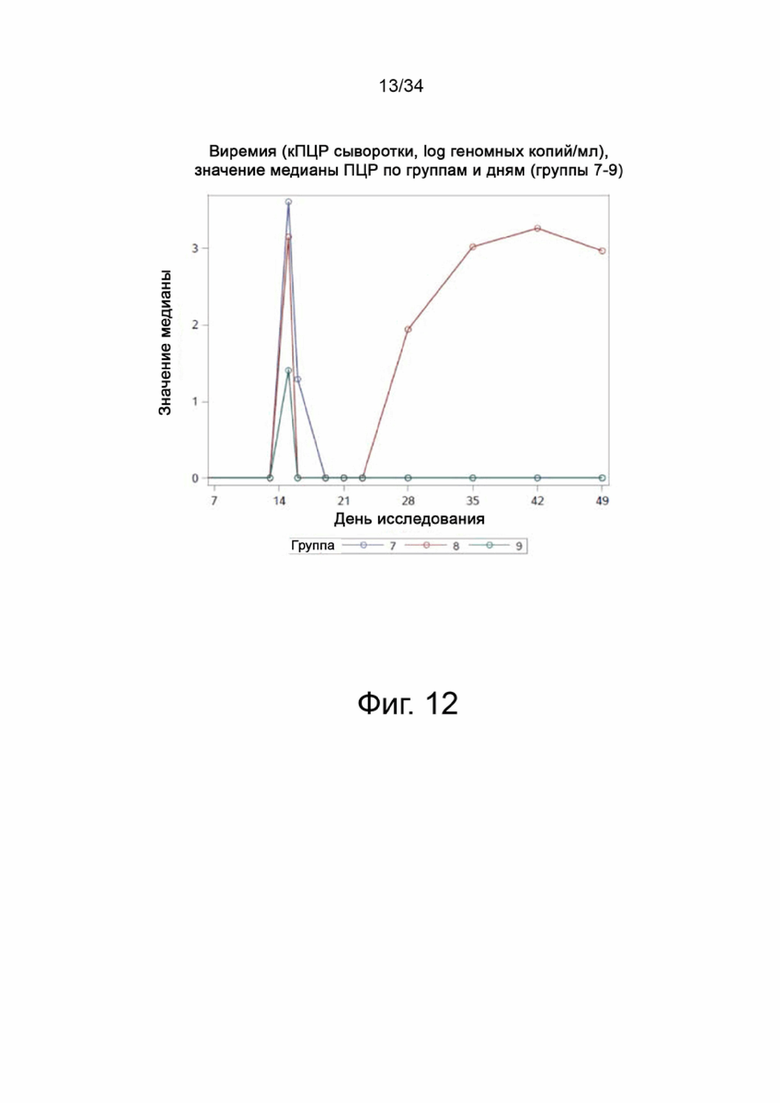
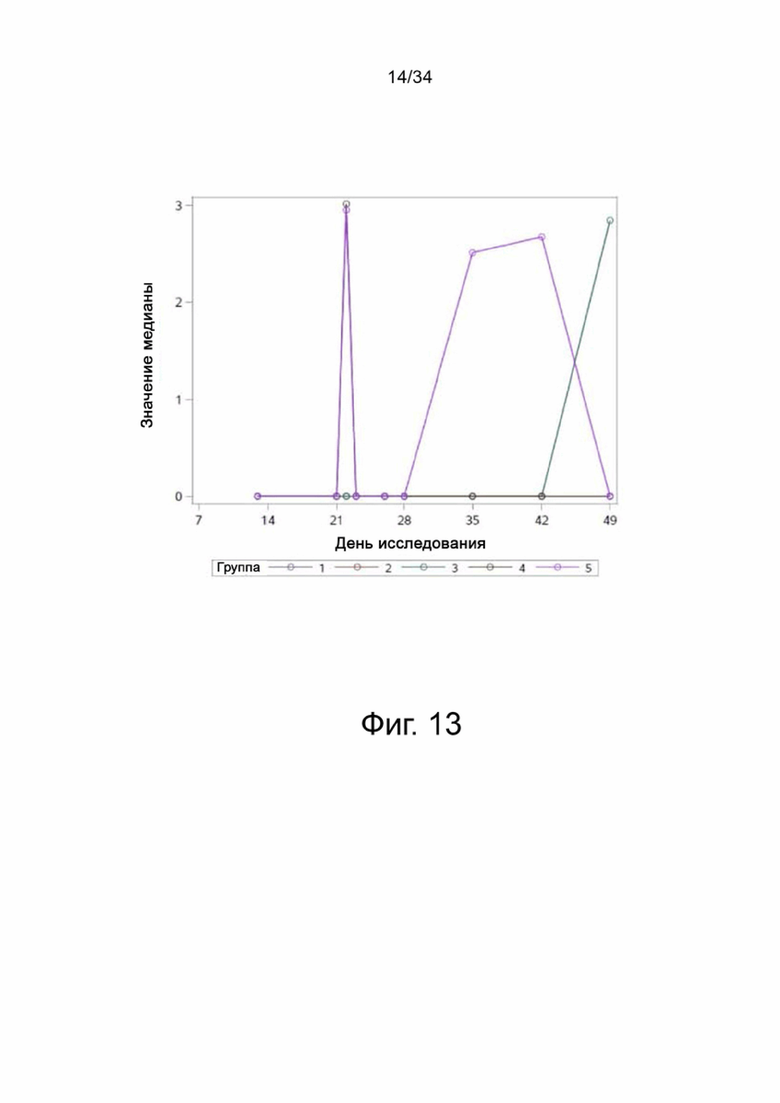
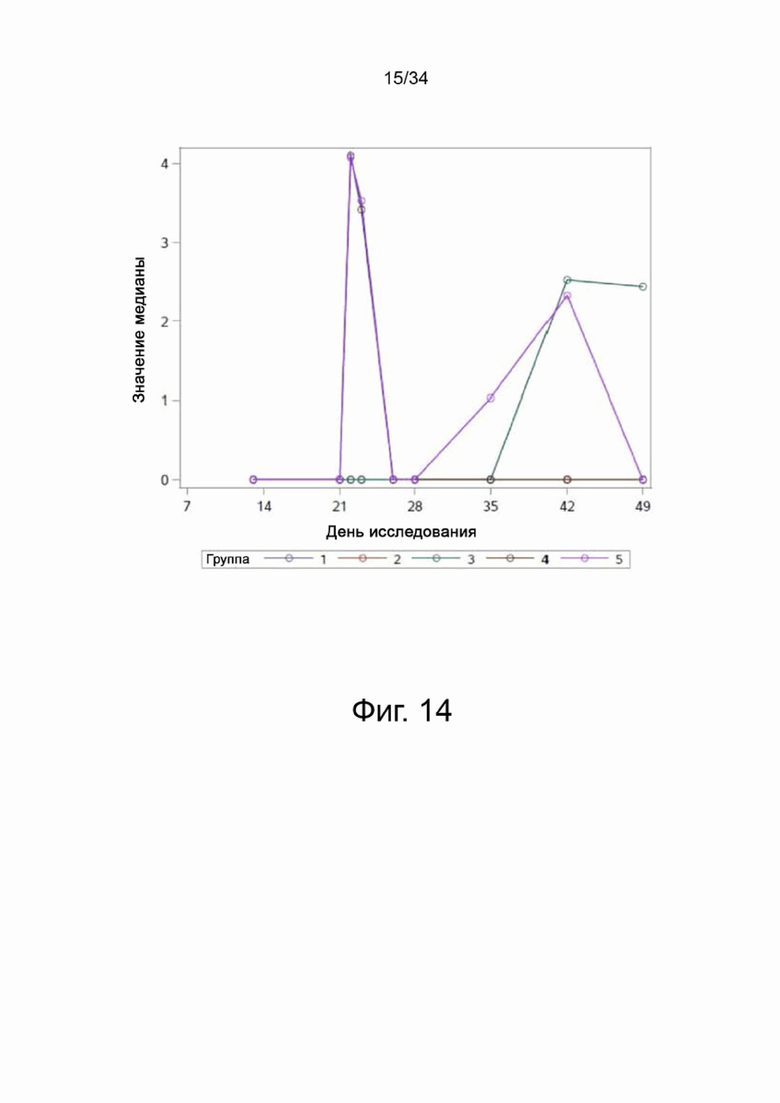
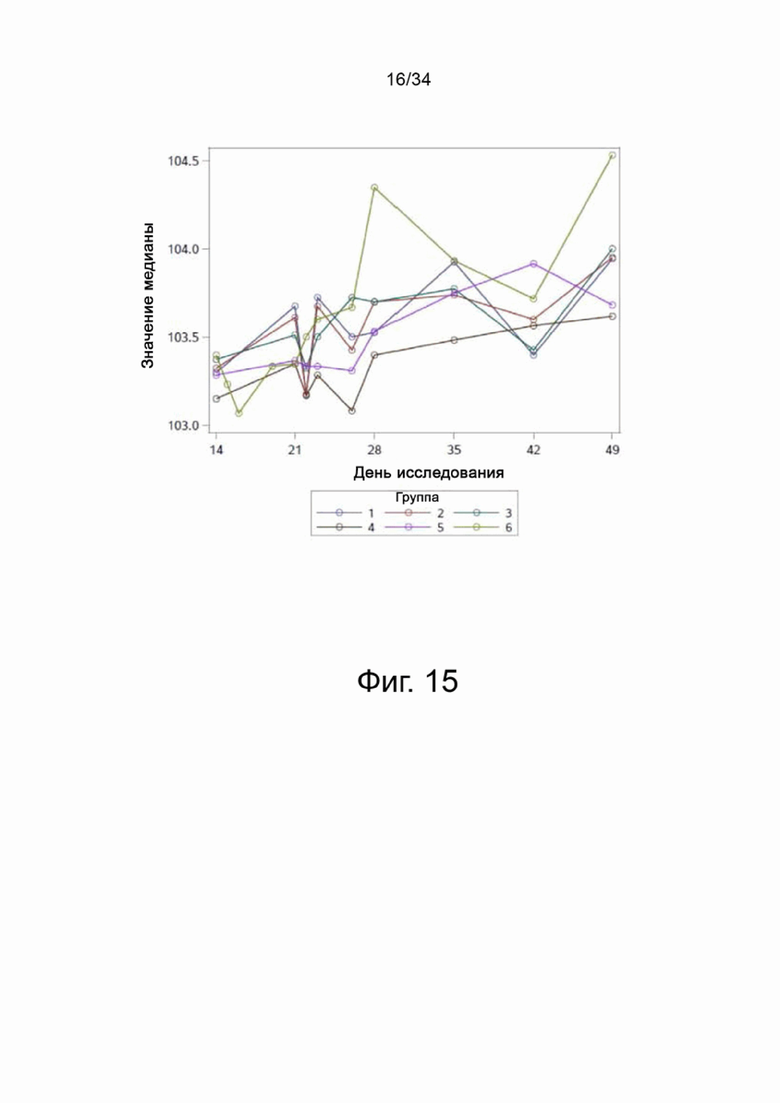
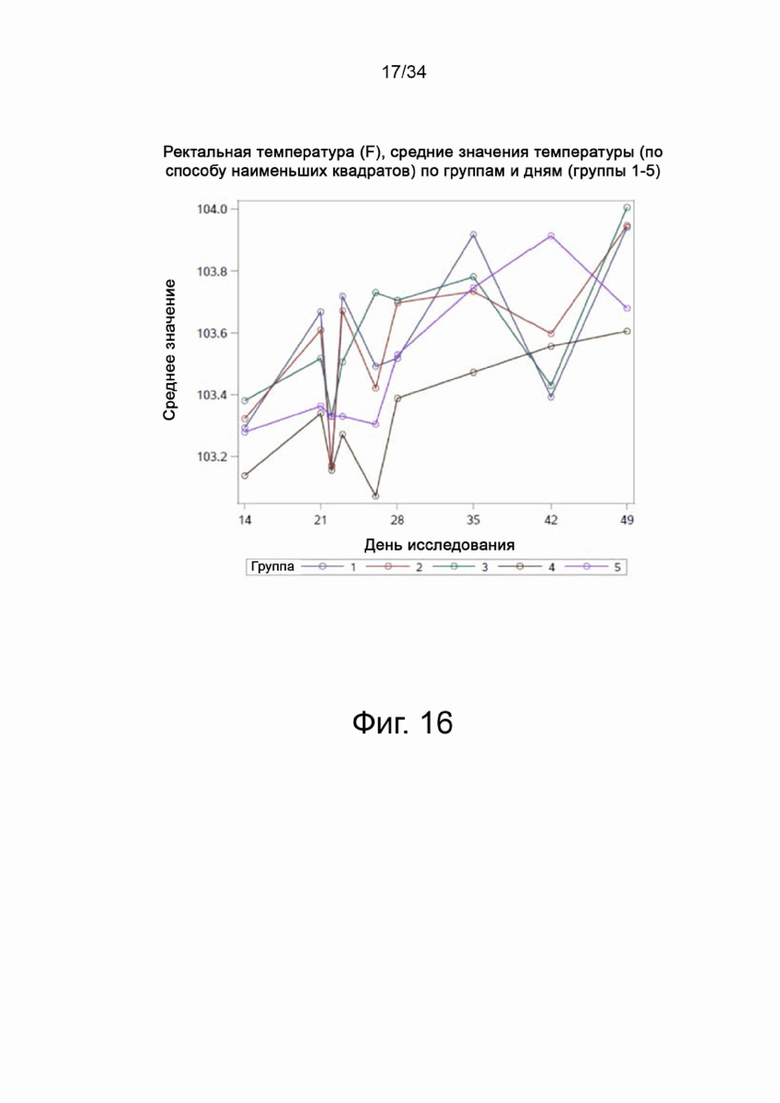
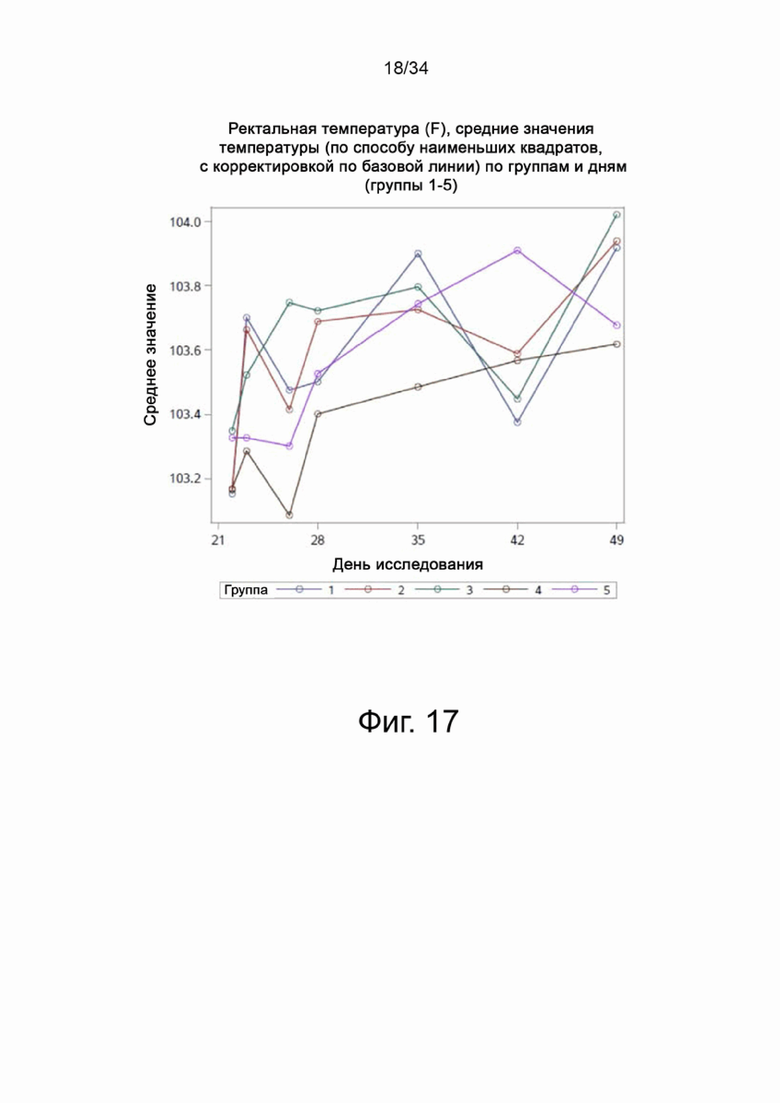
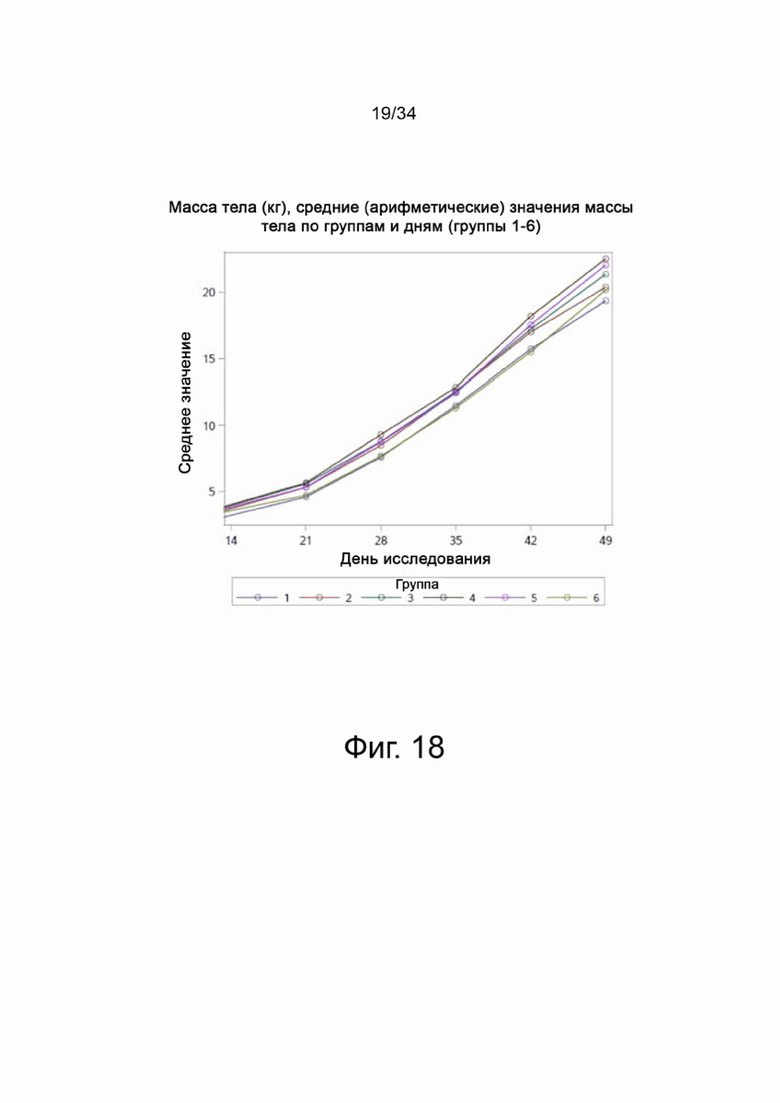
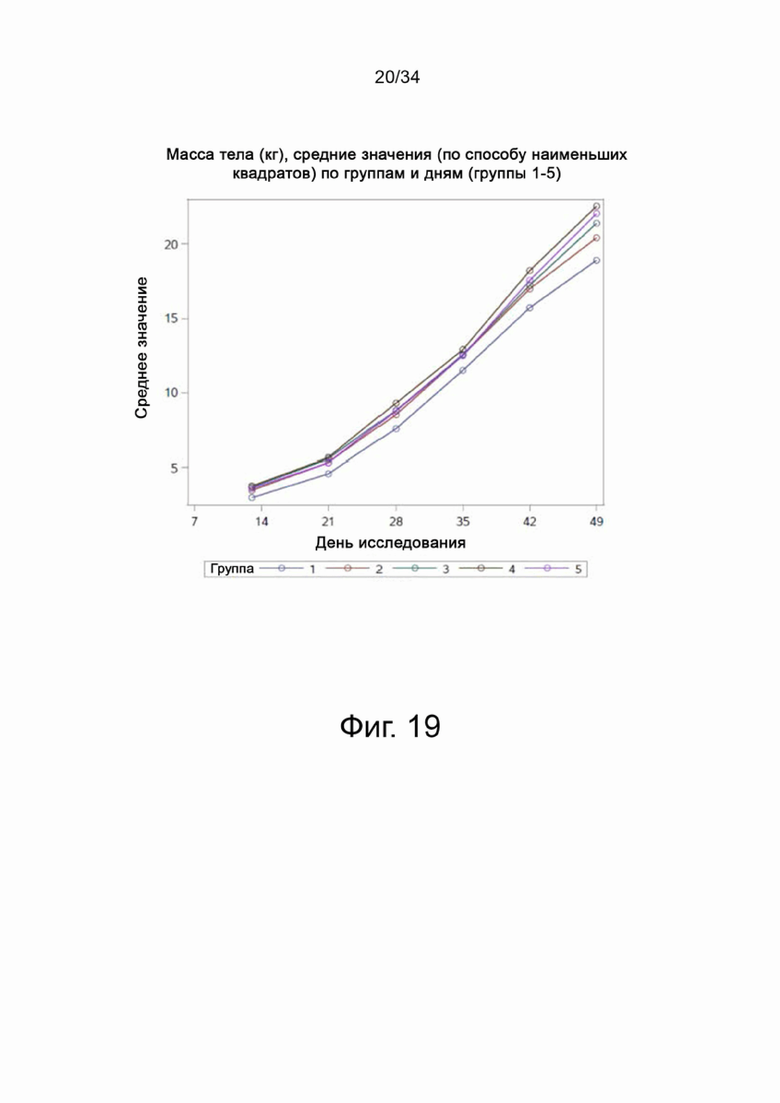
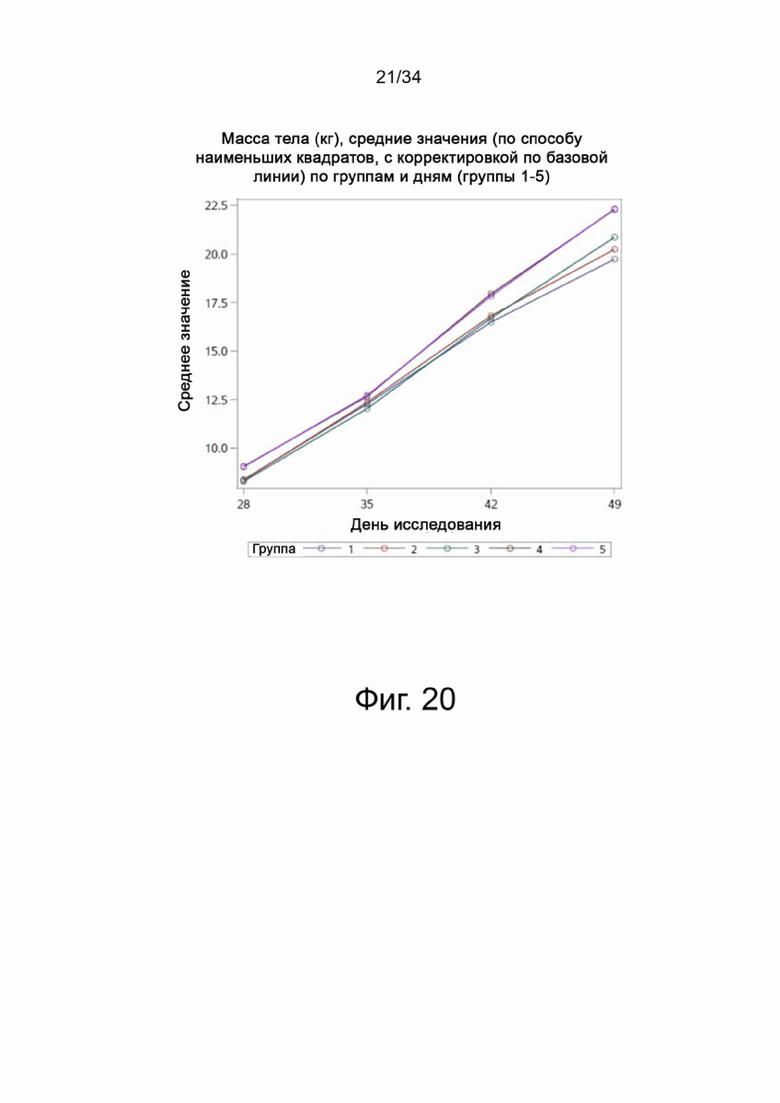
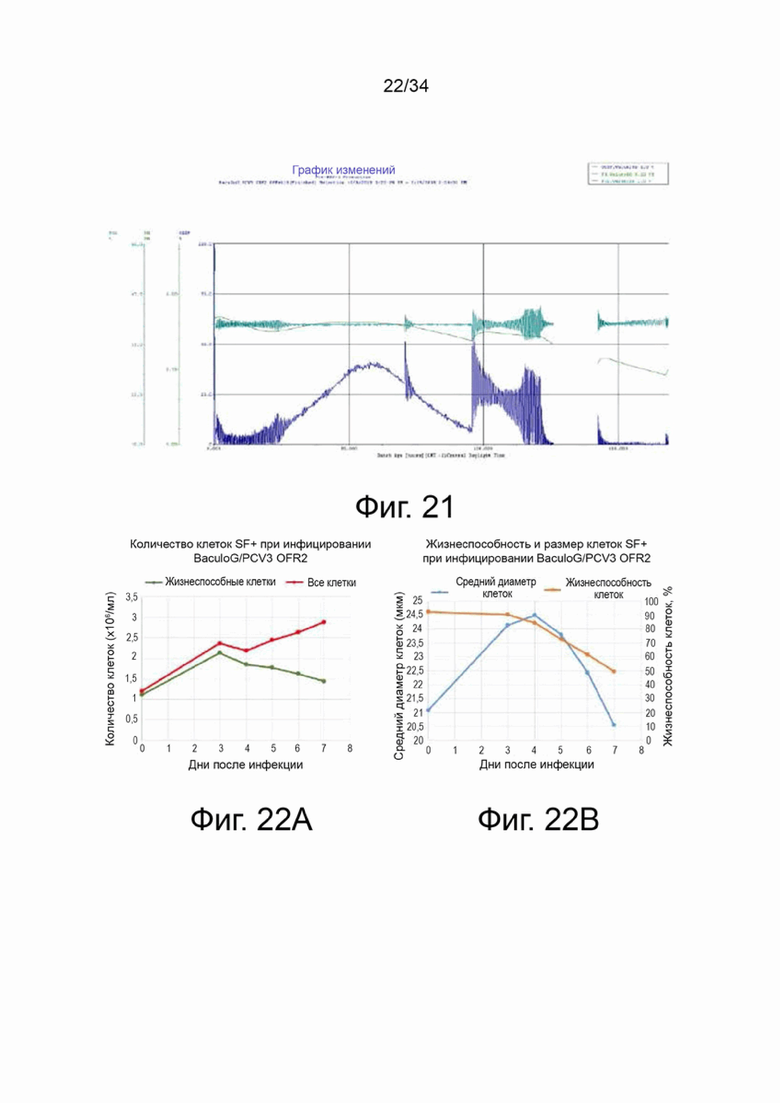
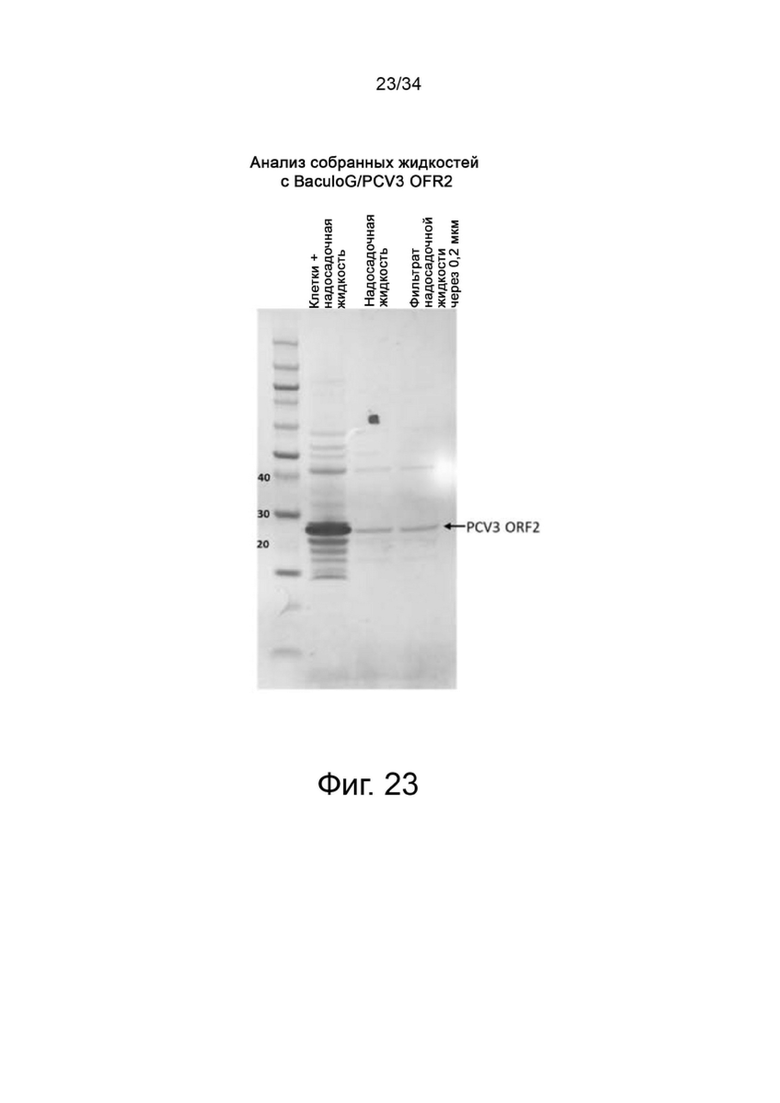

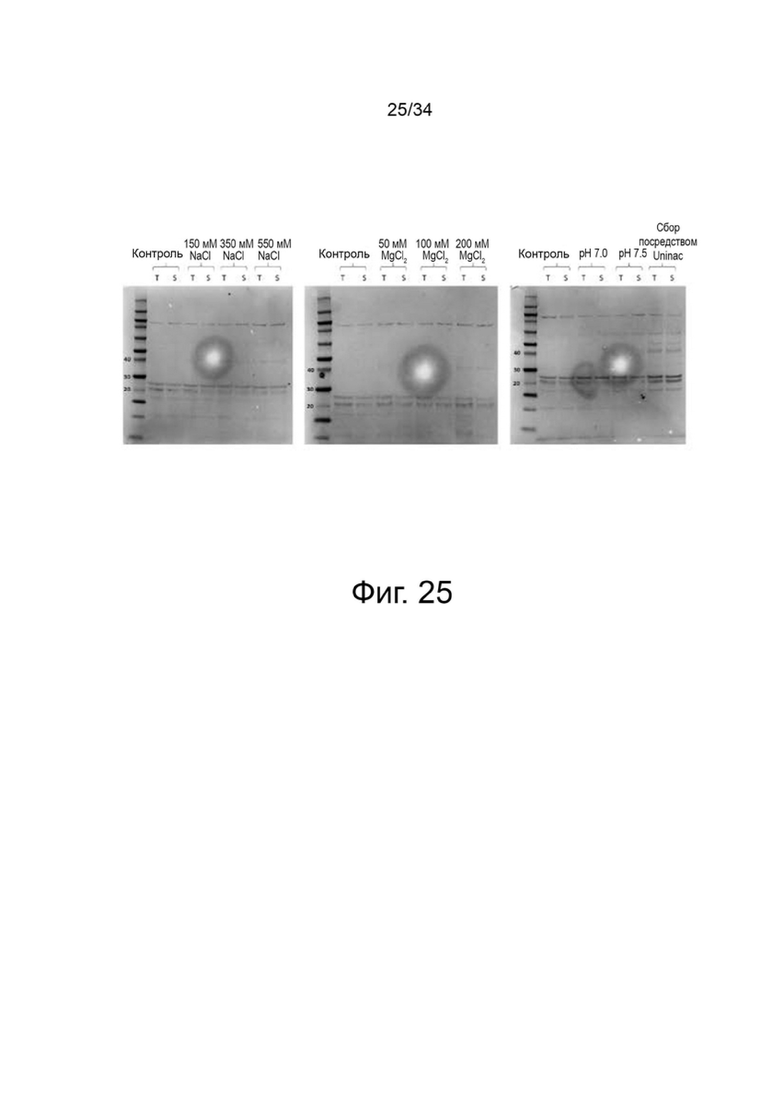
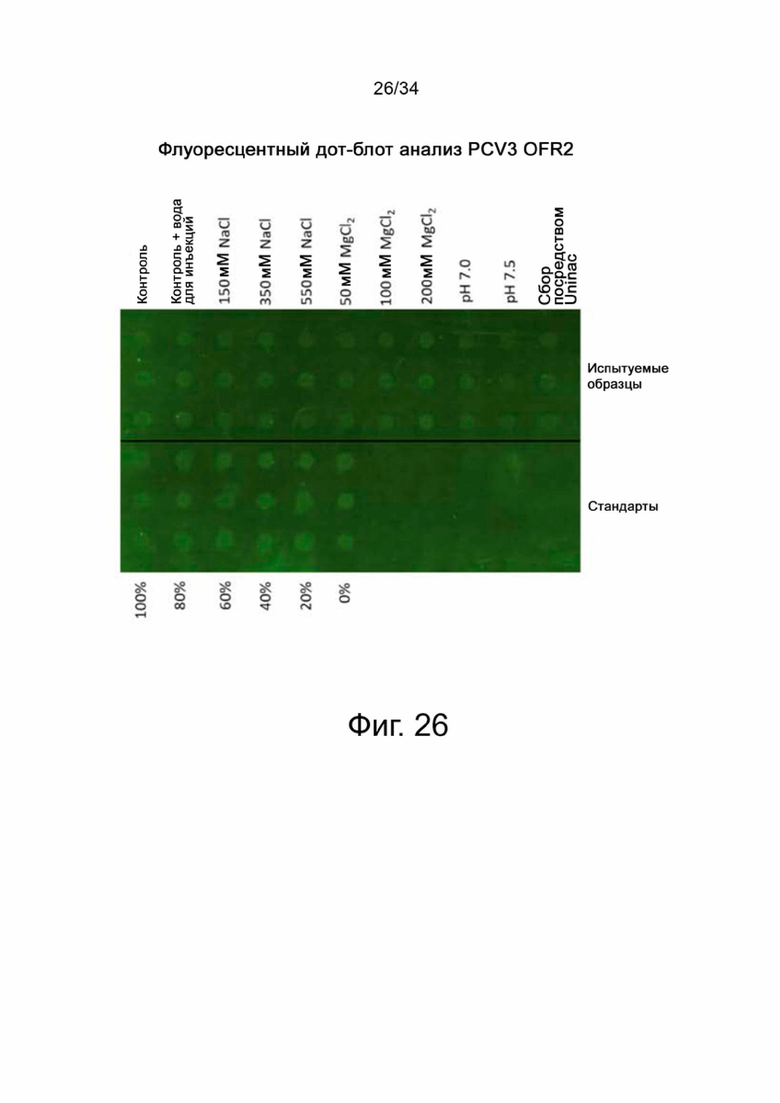
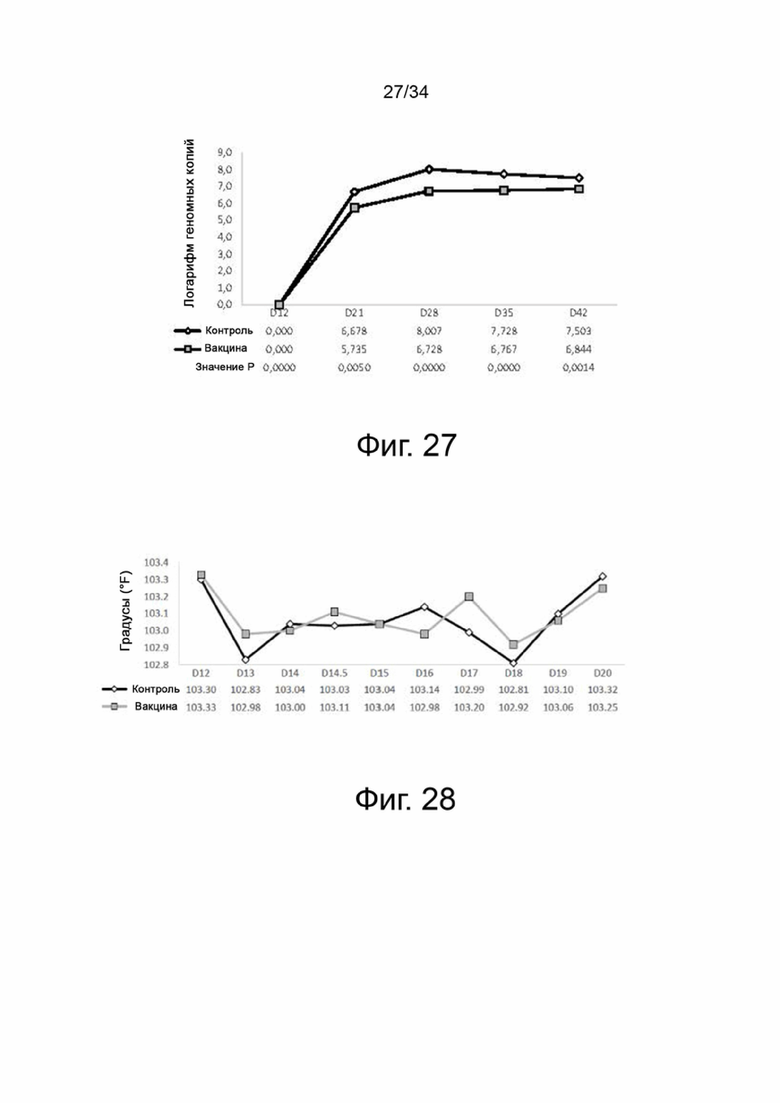
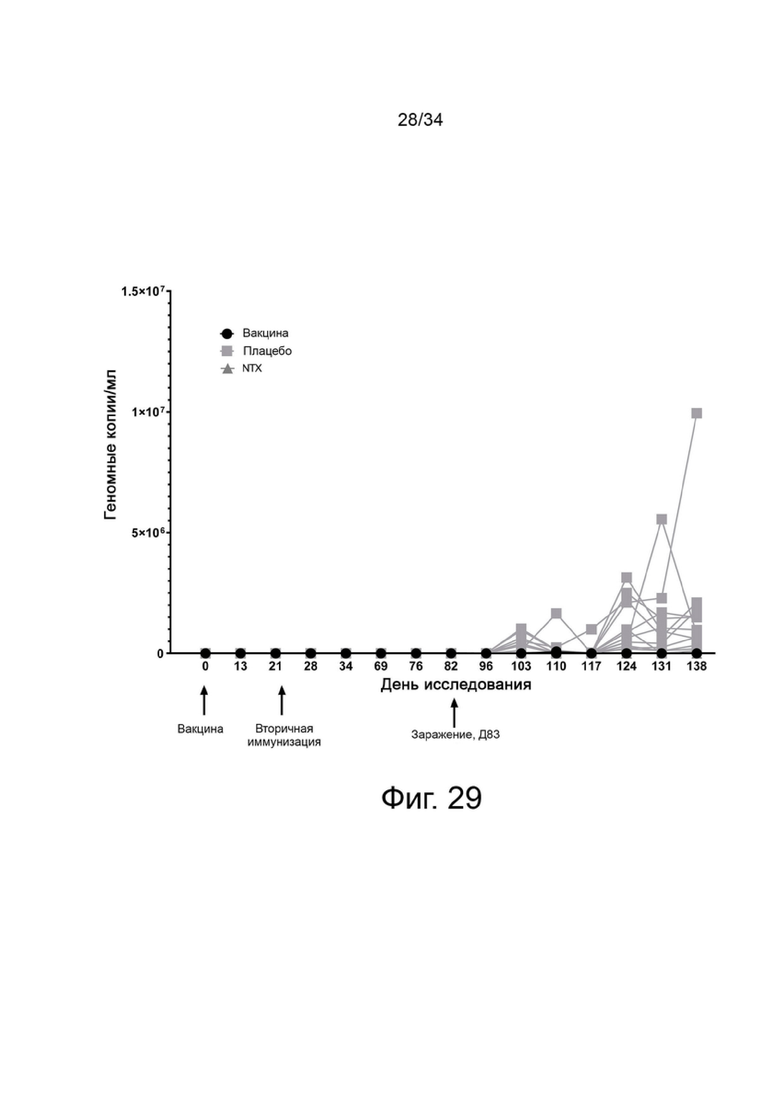
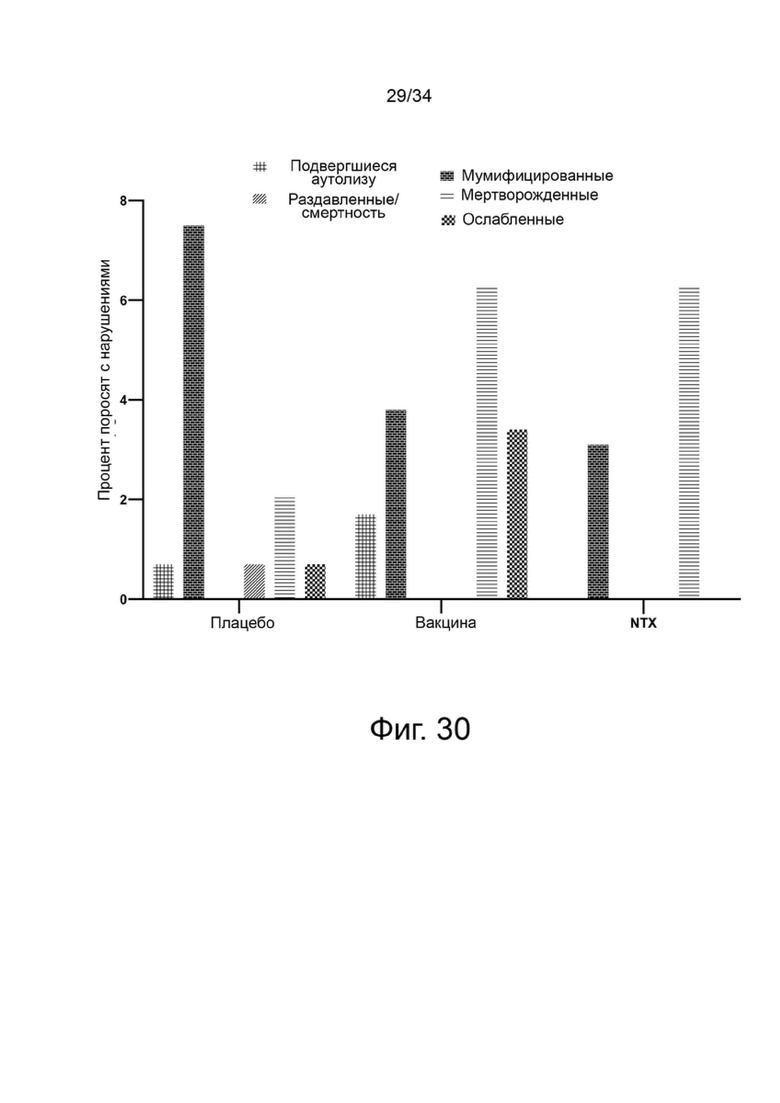
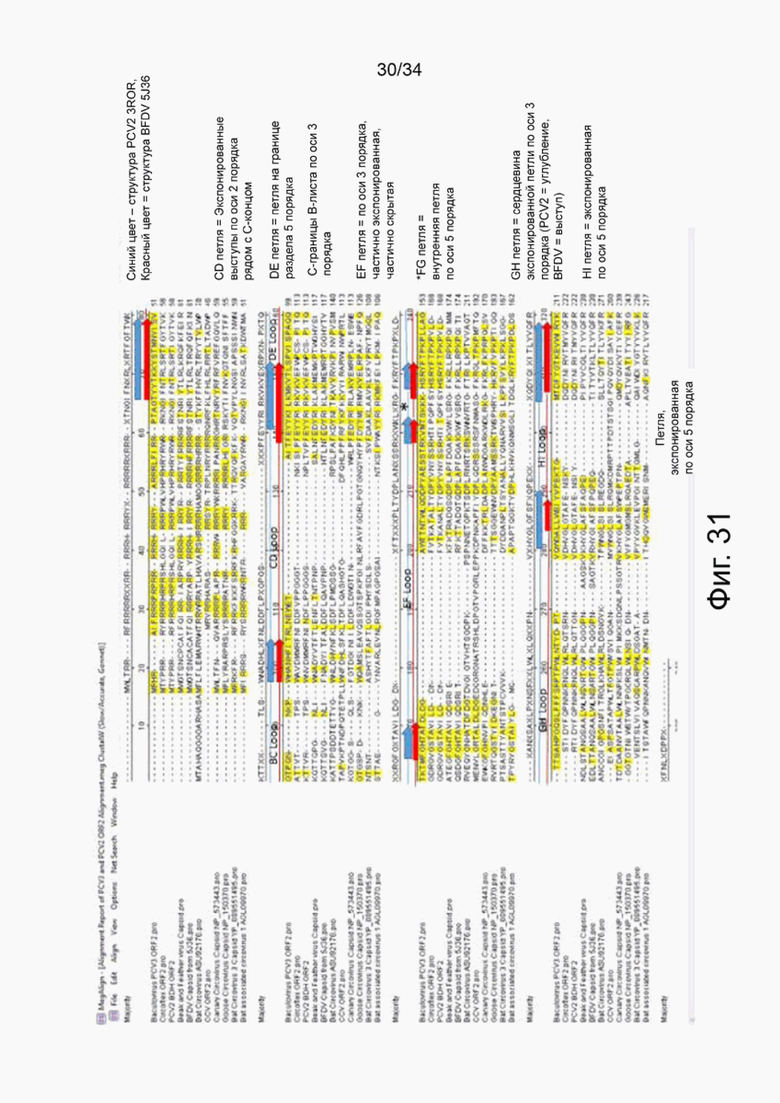

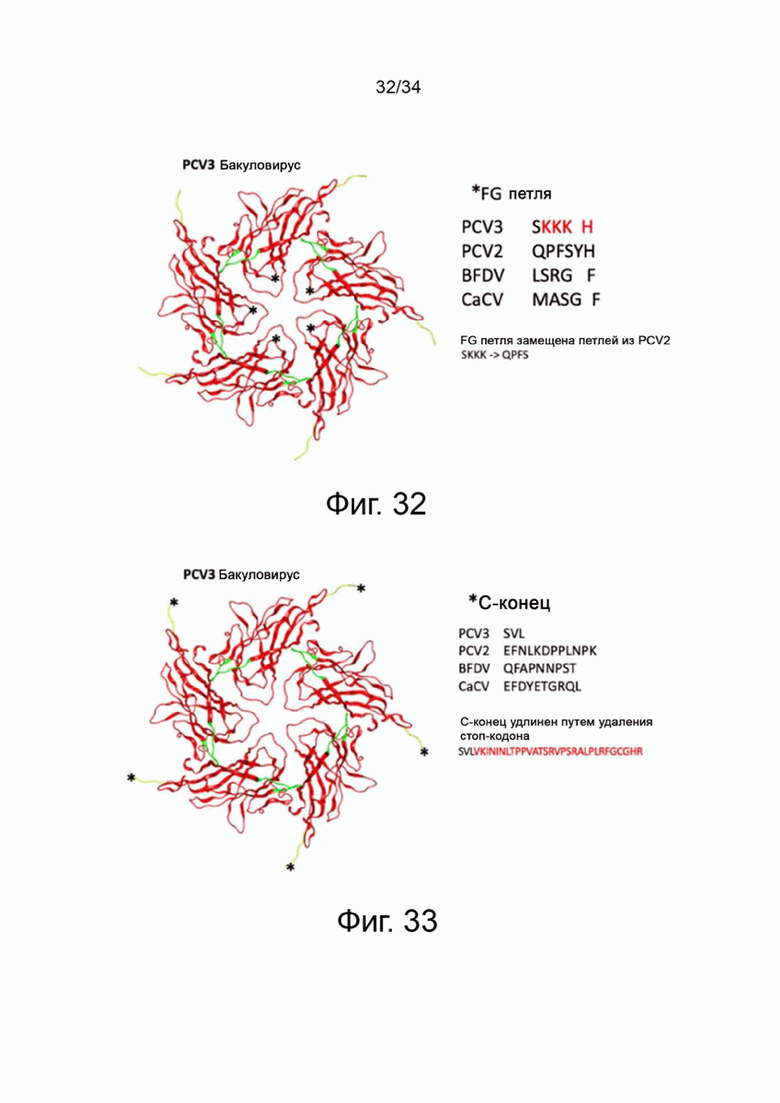
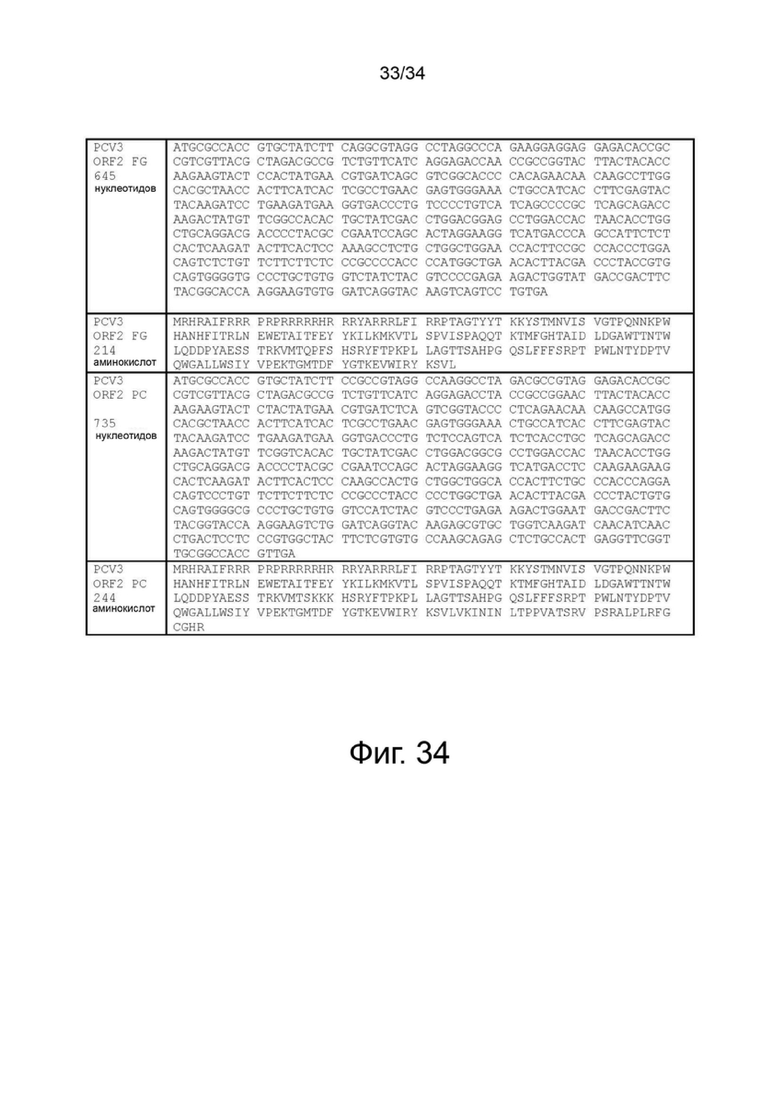

Изобретение относится к биотехнологии. Описан способ профилактики виремии цирковируса свиней 3 типа (PCV3) у поросенка, где способ включает введение композиции свинье, где свинья является беременной свиньей до первого опороса или свиноматкой и где беременная свинья до первого опороса или свиноматка рождает данного поросенка, где композиция содержит белок ORF2 PCV3, где белок ORF2 PCV3 содержит аминокислотную последовательность, имеющую по меньшей мере 97% идентичности последовательности с последовательностью SEQ ID NO: 4, и где белок ORF2 PCV3 представляет собой рекомбинантный экспрессируемый бакуловирусом белок ORF2 PCV3. Также описан способ профилактики виремии PCV3 у поросенка, где способ включает введение композиции свинье, где свинья является свиньей до первого опороса или свиноматкой до беременности поросенком, где свинья до первого опороса или свиноматка становится беременной указанным поросенком и беременная свинья до первого опороса или свиноматка рождает данного поросенка, где композиция содержит белок ORF2 PCV3, где белок ORF2 PCV3 содержит аминокислотную последовательность, имеющую по меньшей мере 97% идентичности последовательности с последовательностью SEQ ID NO: 4, и где белок ORF2 PCV3 представляет собой рекомбинантный экспрессируемый бакуловирусом белок ORF2 PCV3. Изобретение расширяет арсенал средств для лечения PCV3. 2 н. и 5 з.п. ф-лы, 35 ил., 154 табл., 16 пр.
1. Способ профилактики виремии цирковируса свиней 3 типа (PCV3) у поросенка, где способ включает введение композиции свинье, где свинья является беременной свиньей до первого опороса или свиноматкой и где беременная свинья до первого опороса или свиноматка рождает данного поросенка,
где композиция содержит белок ORF2 PCV3, где белок ORF2 PCV3 содержит аминокислотную последовательность, имеющую по меньшей мере 97% идентичности последовательности с последовательностью SEQ ID NO: 4, и
где белок ORF2 PCV3 представляет собой рекомбинантный экспрессируемый бакуловирусом белок ORF2 PCV3.
2. Способ по п.1, где свиноматка кормит указанного поросенка.
3. Способ по п.1, где композицию вводят свинье используя режим многократного или многодозового введения или где композицию вводят используя режим двудозового или двукратного введения.
4. Способ профилактики виремии PCV3 у поросенка, где способ включает введение композиции свинье, где свинья является свиньей до первого опороса или свиноматкой до беременности поросенком, где свинья до первого опороса или свиноматка становятся беременными указанным поросенком и беременная свинья до первого опороса или свиноматка рождает данного поросенка,
где композиция содержит белок ORF2 PCV3, где белок ORF2 PCV3 содержит аминокислотную последовательность, имеющую по меньшей мере 97% идентичности последовательности с последовательностью SEQ ID NO: 4, и
где белок ORF2 PCV3 представляет собой рекомбинантный экспрессируемый бакуловирусом белок ORF2 PCV3.
5. Способ по п.4, где введение осуществляют до спаривания/осеменения свиньи.
6. Способ по п.4, где свиноматка кормит указанного поросенка.
7. Способ по п.4, где композицию вводят свинье используя режим многократного или многодозового введения или где композицию вводят используя режим двудозового или двукратного введения.
| CN 109053896 А, 21.12.2018 | |||
| CN 109550045 A, 02.04.2019 | |||
| WO 2017066772 A1, 20.04.2017 | |||
| WO 2018233264 A1, 27.12.2018 | |||
| SUJIAO ZHANG ET AL, "Development and application of a baculovirus-expressed capsid protein-based indirect ELISA for detection of porcine circovirus 3 IgG antibodies", BMC VETERINARY RESEARCH,Vol | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ПОЛИВАЛЕНТНЫЕ ИММУННОГЕННЫЕ КОМПОЗИЦИИ PCV2 И СПОСОБЫ ПОЛУЧЕНИЯ ТАКИХ КОМПОЗИЦИЙ | 2006 |
|
RU2577127C9 |
Авторы
Даты
2024-02-21—Публикация
2020-04-06—Подача