Изобретение относится к медицине, а именно к хирургии, основной целью использования следует считать профилактику лимфореи при выполнении подмышечно-подключично-подлопаточной лимфодиссекции у пациентов онкологического профиля.
Рак молочной железы социально значимая патология, занимающая лидирующую позицию в структуре онкологической заболеваемости среди женского населения составляя, по данным исследователей 20,9% от общей онкологической заболеваемости. (Д. Каприна, В.В. Старинского, А.О. Шахзадовой: «Злокачественные новообразования в России в 2020 году (заболеваемость и смертность)» // – М.: МНИОИ им. П.А. Герцена − филиал ФГБУ «НМИЦ радиологии» Минздрава России, − 2021). Это приковывает внимание медицинской коллегии, как к вопросам выявления, так и лечебной тактики в отношении злокачественных новообразований молочных желез. Несмотря на успехи в области разработки новых препаратов лекарственной терапии, основным методом лечения остается хирургический.
Деэскалация объемов лечения находит все больше приверженцев в медицинской среде, в связи с меньшим количеством осложнений. Однако велика доля пациентов, которым необходим классический объем хирургического пособия. Операции на лимфатическом аппарате в подавляющем большинстве случаев сопряжены с таким явлением, как лимфорея. В зависимости от объема проведенного лечения (биопсия сигнального лимфатического узла, подмышечная лимфодиссекция I-III уровней), а так же конституциональных особенностей, доказана корреляция объёмов лимфореи и величины ИМТ (Богданов А.В., Куракина И.С., Нохрин Д.Ю.: "Профилактика длительной и обильной лимфореи при раке молочной железы" Журнал: Онкология. Журнал им. П.А. Герцена. 2020;9(3): 34 40. DOI: 10.17116/onkolog2020903134), выраженность этого осложнения может серьезно сказаться на сроках начала второго этапа лечения, что, безусловно, влияет на прогноз (по данным исследований и рекомендаций АОР наиболее оптимальным считается начало дистанционной лучевой терапии не позднее, чем через 12 недель от проведения операции, начало адъювантной химиотерапии - около двух недель.) Присоединение же инфекции, обусловленной длительным сохранением дренажа, а так же несвоевременной эвакуацией лимфоцеле, может повлечь необходимость хирургического пособия и отказ от проведения специального противоопухолевого лечения, что, безусловно, сказывается на показателях общей и безрецидивной выживаемости у пациентов с раком молочной железы. Наличие очага воспаления увеличивает риск инвалидизации в связи с увеличенной частотой возникновения лимфедемы и WEB-синдрома (Корнеев К. В., Солодкий В. А.: "Комбинация лимфаденэктомии с использованием ультразвукового скальпеля и миопластики как метод профилактики лимфореи у больных раком молочной железы после радикальных мастэктомий // Человек и его здоровье. 2013. №1.") Разработка эффективных методов борьбы с лимфореей до сих пор остается краеугольным камнем современной хирургии лимфоколлекторов. Обилие вариантов возможных методов профилактики позволяет подобрать оптимальный подход к каждому пациенту. Использование новых технологий развивает и совершенствует существующие тактики, позволяя добиться большей эффективности, в том числе, экономической.
Все методики по профилактике лимфореи целесообразно разделить на группы:
- использование системных лекарственных средств в послеоперационном периоде (октреотид, транексамовая кислота и т.д.)
- интрооперационное применение герметиков (различные коллагеновые пластинки, фибриновый клей и т.п.)
- сопоставление лоскутов с использованием лигирующих техник, мышечных и кожно-жировых трансплантатов, а также способов послеоперационного компрессионного бинтования.
- использование щадящих операционных техник (ультразвуковой скальпель, использование электрокоагуляции низкой выходной мощности), а так же методы физического воздействия на послеоперационное поле (фотодинамическая терапия, лазерное излучение, плазменная коагуляция)
- селективная перевязка лимфатических сосудов (с использованием контрастной и микрохирургической методик)
В современной литературе недостаточно данных для оценки сочетанного использования способов профилактики, что связанно с ростом экономических затрат, при статистически незначимой клинической выгоде. Исходя из этого, при разработке методики мы учитывали факторы доступности в клинической практике, а так же профиль безопасности.
Manouras A. et al. (Modified radical mastectomy with axillary dissection using the electrothermal bipolar vessel sealing system. Arch Surg. 2008 Jun;143(6):575-80). Описывает методику электролигирования лимфатических сосудов с использованием биполярной системы коагуляции. Схожим с настоящим изобретением, является факт использования биполярной системы для электрокоагулирования лимфатических сосудов. Однако изобретение отличается применением оптического бинокулярного увеличения для выделения лимфатических сосудов. * Также близким к указанному изобретению следует считать патент RU20090135302. Принципиальным отличием же является отсутствие необходимости прицельной перевязки указанных сосудов и формирования кожно-мышечных тоннелей в области подмышечной впадины, что, в свою очередь, позволяет уменьшить экономические затраты на проведение каждого вмешательства за счет сокращения использования шовного материала, так же исключается возможность непреднамеренного включения в состав образованной муфты нервных окончаний, кровеносных сосудов небольшого калибра, сохраненных лимфатических сосудов, пересечение которых, не входит в объем стандартного оперативного вмешательства. Способ позволяет сократить время операции, что, по данным исследователей, дополнительно влияет на вероятность возникновения послеоперационной лимфореи, кроме того, методика двойной лигирующей коагуляции не влияет на пропускную способность хирургического стола и не увеличивая нагрузку на исполнителей операции. Способ одинаково эффективен в отношении борьбы с послеоперационной лимфореей при использовании во время выполнения лимфодиссекции совместно с мастэктомией или радикальной резекцией молочной железы, в связи с одинаковым рекомендованным объемом операций на лимфоколлекторах в обоих указанных случаях. Авторы обращают внимание на функционально-щадящие особенности использования изобретения. Эффективным, в плане защиты от избыточного влияния повышенных температур, является аппарат Force Triad Liga Sure, в связи с наличием возможности автоматического подбора мощности, однако достижение схожих результатов при реализации способа возможно при использовании биполярной коагуляции с выходной мощностью не более 30 Вт. Во время проведения диссекционного этапа, мы обращали особое внимание на сохранение анатомических образований, которые, зачастую, могут быть повреждены при недостаточной прецизионности работы. К ним относятся a. et v. thoracicus lateralis, v. thoracoepigastrica, rr. ventrales (nn. intercostales), n. intercostobrachialis. (Олексенко В.В., Алиев К.А., Ефетова Т.С., Телькиева Г.Н.: "Анатомо-морфологическое обоснование нервосберегающей лимфодиссекции при раке молочной железы." Хирургия. Журнал им. Н.И. Пирогова. 2017;(6):79 83. https://doi.org/10.17116/hirurgia2017679-83. Melhem J, Amarin M, Odeh G, Al-Bustami N, Al-Lauzy H, Ayoub R. Intercostobrachial Nerve (ICBN) Preservation Versus Sacrifice in Axillary Dissection: Randomized Controlled Trial. Am J Clin Oncol. 2021 May 1;44(5):206-209. doi: 10.1097/COC.0000000000000809.) Конец формы
Сохранение указанных структур, по данным исследователей, позволяет уменьшить проявления постмастэктомического синдрома у пациентов после подмышечно-подключично-подлопаточной лимфодиссекции. Эмпирически установлено, что выраженность постмастэктомического синдрома зависит от типа сохраняемых структур, так наибольшую эффективность в его профилактике показывает сохранение указанных нервов. Подгрупповой анализ выявления точного процента вероятности развития постмастэктомического синдрома при повреждении того или иного нерва нецелесообразен в виду этических соображений. Сохранение указанных артериальных и венозных структур, по нашим данным, оказывает положительное влияние на скорость заживления п/о раны, а также показывает слабую корреляцию с уменьшением риска развития лимфедемы верхней конечности.
Фиксация кожных лоскутов шовным материалом создает дополнительный риск травматизации указанных образований. В заявленном способе для дополнительного сокращения мертвого пространства после радикальной мастэктомии предлагается использовать эластичное бинтование грудной стенки. С учетом данных литературы, стоит рассматривать эффективность бинтования только в совокупности с микрохирургическим лигированием лимфатических сосудов в виду отсутствия статистически значимой пользы при использовании изолированно бинтования. При выполнении радикальной резекции молочной железы использование эластического бинтования не показывает корреляционной связи с объемом п/о лимфореи.
Авторами установлено и статистически подтверждено, что использование изобретения позволяет снизить длительность и объем лимфореи по сравнению с контрольной группой стандартной лимфаденэктомии: длительность лимфореи - 9 дней против 18 дней контрольной группы, средние потери лимфы за 7 дней - 300 мл против 760 мл контрольной группы, частота формирования лимфоцеле - 5% против 17%. Преимущества сохранялось в группах как мастэктомии, так и радикальной резекции молочной железы.*** При сравнении с наиболее близким по технике способом RU20090135302, не было выявлено статистических различий в длительности лимфореи. Отсутствие необходимости тунелирования лимфатических сосудов, а так же фиксации кожного лоскута приводили к уменьшению времени операции и ее стоимости. Выраженность болевого синдрома оценивалась в соответствии с визуальной аналоговой шкалой боли и была меньше в группе коагуляционного лигирования.
Заявленный способ осуществляется следующим образом.
При выполнении радикальной мастэктомии с подмышечной-подключичной-подлопаточной лимфаденэктомией, либо радикальной резекции молочной железы во время проведении диссекционного этапа, используется бинокулярное оптическое усиление для выделения лимфатических сосудов в проекции удаляемой клетчатки, с сохранением анатомических образований мелкого калибра, пересечение которых, при наличии технической возможности, не подразумевается объемами выполняемой диссекции, к ним относятся латеральные грудные артерии и вены, грудонадчревная вена, межреберноплечевой нерв, передние ветви межреберных нервов. После обнаружения основных крупных лимфатических сосудов последние лигируются методикой двойной коагуляции при помощи электрогенератора Force Triad Liga Sure. Альтернативой стоит считать использование биполярной электрокоагуляции с выходной мощностью не более 30Вт, с соблюдением величины угла между линиями коагуляционного шва более 90о. (рис.1). Лимфатические сосуды меньшего калибра обнаруживаются следующим этапом, лигируются идентичным способом. После контроля гемостаза, при отсутствии подтекания лимфы, подмышечную область дренируют трубчатым силиконовым дренажем по Редону. Послеоперационную рану ушивают. При выполнении радикальной мастэктомии, после окончания операции, производят эластичное бинтование грудной клетки для лучшей адгезии лоскутов. Использование оптического усиления позволяет выделить лимфотические сосуды и превентивно их коагулировать. Методика двойной коагуляции создает крупный, по отношению к площади сосуда, коагуляционный блок, что исключает вероятность его несостоятельности. Применение в работе электрогенератора Force Triad Liga Sure, либо ограничение выходной мощности биполярного коагулятора, совместно с сохранением указанных анатомических образований уменьшает проявления постмастэктомического синдрома. Использование эластического бинтования после выполнения мастэктомии с подмышечной-подключичной-подлопаточной лимфаденэктомией, позволяет мягко сопоставить лоскуты для ликвидации мертвого пространства в области передней грудной стенки и подмышечной впадины без риска дополнительного травмирования сохраняемых сосудистых и нервных образований. Совокупность описанных методик является способом борьбы с лимфореей и уменьшает сроки заживления раны.
Пример выполнения.
Больная А. 61 год. Диагноз: рак правой молочной железы Т2N1М0, 2в cт.
Двумя полуовальным горизонтальным линиями, окаймляющими молочную железу, рассечена кожа до подкожной жировой клетчатки. Мобилизация кожных лоскутов с прилежащей подкожной жировой клетчаткой в краниальном и каудальном направлениях до фасции большой грудной мышцы. Фасция отделена от мышцы. Диссекция ткани молочной железы, вместе с фасцией большой грудной мышцы, до подмышечной впадины. После отведения края большой грудной мышцы, удалена межмышечная клетчатка с лимфоузлами и фасцией малой грудной мышцы. Диссекция продолжена в подмышечную впадину. Клетчатка отделена от подключичной, подмышечной вен. Выделены и сохранены торако-дорзальный сосудисто-нервный пучок, длинный грудной нерв, латеральные грудные артерия и вена, грудонадчревная вена, межреберноплечевой нерв, переднее ветки межреберных нервов. Клетчатка с лимфоузлами отделена от передней поверхности широчайшей мышцы спины и удалена в едином блоке с тканью молочной железы. Контроль гемостаза – сухо. Обработка послеоперационной раны растворами антисептиков. Следующим этапом, с использованием оптического бинокулярного увеличения, выделены стволы пересеченных лимфатических сосудов в проекции удаляемой клетчатки подмышечной, подключичной, подлопаточной областей. С использованием электрогенератора Force Triad Liga Sure, крупные лимфатические стволы лигированы методикой двойной коагуляции. Лимфатические сосуды маленького калибра коагулированы обычным способом. При контрольном осмотре: признаков подтекания лимфы не выявлено. Установлен активный дренаж по Редону в подмышечную область. Шов раны. Асептическая повязка. Активизация пациентки через 3 часа, после завершения операции. В дополнение к заявленному способу по пункту 1, дополнительно произведено бинтование эластичным бинтом (10 см\5 м) с наложением туров вокруг грудной клетки. Послеоперационный период - без особенностей. Заживление раны - первичным натяжением. Объем отделяемого по дренажу: 1сутки - 50мл серозно\сукровичного характера; 2 сутки – 50 мл лимфы; 3 сутки – 30 мл лимфы, дренаж удален.; 4 сутки - пункционно получено около 30 мл лимфы; 5 сутки - пункционно получено около 15 мл лимфы, 6 сутки - пункционно получено около 20 мл лимфы, 7 сутки - пункционно получено около 10 мл лимфы, 8 сутки - пункционно получено около 10 мл лимфы. 9 сутки - при попытке пункции, отделяемое отсутствует. Общий объем лимфореи: 215мл. Срок госпитализации 11 суток.
Заявляемый способ обладает техническими и экономическими преимуществами и, на наш взгляд, отвечает критериям патентоспособности.
Использованная литература:
RU 2410034 C1, RU2385673 C1
Богданов А.В., Куракина И.С., Нохрин Д.Ю.: "Профилактика длительной и обильной лимфореи при раке молочной железы" Журнал: Онкология. Журнал им. П.А. Герцена. 2020;9(3): 34 40. DOI: 10.17116/onkolog2020903134
Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой: «Злокачественные новообразования в России в 2020 году (заболеваемость и смертность)» // – М.: МНИОИ им. П.А. Герцена − филиал ФГБУ «НМИЦ радиологии» Минздрава России, − 2021 − илл.− 252 с.
Корнеев К. В., Солодкий В. А.: " Комбинация лимфаденэктомии с использованием ультразвукового скальпеля и миопластики как метод профилактики лимфореи у больных раком молочной железы после радикальных мастэктомий // Человек и его здоровье. 2013. №1."
Олексенко В.В., Алиев К.А., Ефетова Т.С., Телькиева Г.Н.: "Анатомо-морфологическое обоснование нервосберегающей лимфодиссекции при раке молочной железы." Хирургия. Журнал им. Н.И. Пирогова. 2017;(6):79 83. https://doi.org/10.17116/hirurgia2017679-83.
Boccardo FM, Ansaldi F, Bellini C, Accogli S, Taddei G, Murdaca G, Campisi CC, Villa G, Icardi G, Durando P, Puppo F, Campisi C. Prospective evaluation of a prevention protocol for lymphedema following surgery for breast cancer. Lymphology. 2009 Mar;42(1):1-9. Erratum in: Lymphology. 2009 Sep;42(3):149. PMID: 19499762.
Manouras A. et al. Modified radical mastectomy with axillary dissection using the electrothermal bipolar vessel sealing system. Arch Surg. 2008 Jun;143(6):575-80; discussion 581
Melhem J, Amarin M, Odeh G, Al-Bustami N, Al-Lauzy H, Ayoub R. Intercostobrachial Nerve (ICBN) Preservation Versus Sacrifice in Axillary Dissection: Randomized Controlled Trial. Am J Clin Oncol. 2021 May 1;44(5):206-209. doi: 10.1097/COC.0000000000000809.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ интраоперационной профилактики лимфореи при выполнении радикальной мастэктомии у пациенток с раком молочной железы | 2021 |
|
RU2755698C1 |
| СПОСОБ ИНРАОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПРИ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2009 |
|
RU2410034C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПРИ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2009 |
|
RU2427333C1 |
| СПОСОБ ПРОФИЛАКТИКИ ДЛИТЕЛЬНОЙ ЛИМФОРЕИ ПОСЛЕ ПОДКЛЮЧИЧНО-ПОДМЫШЕЧНО-ПОДЛОПАТОЧНОЙ ЛИМФАДЕНЭКТОМИИ | 2013 |
|
RU2527836C2 |
| СПОСОБ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПОСЛЕ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2007 |
|
RU2334485C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПОСЛЕ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2005 |
|
RU2276582C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПОСЛЕ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2012 |
|
RU2502480C1 |
| Способ профилактики послеоперационных осложнений при подмышечной лимфаденэктомии | 2024 |
|
RU2832797C1 |
| СПОСОБ МИОПЛАСТИКИ ПОСЛЕ РАДИКАЛЬНЫХ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЙ НА МОЛОЧНОЙ ЖЕЛЕЗЕ | 2010 |
|
RU2436521C1 |
| Способ профилактики постматэктомической лимфореи | 2022 |
|
RU2792853C1 |
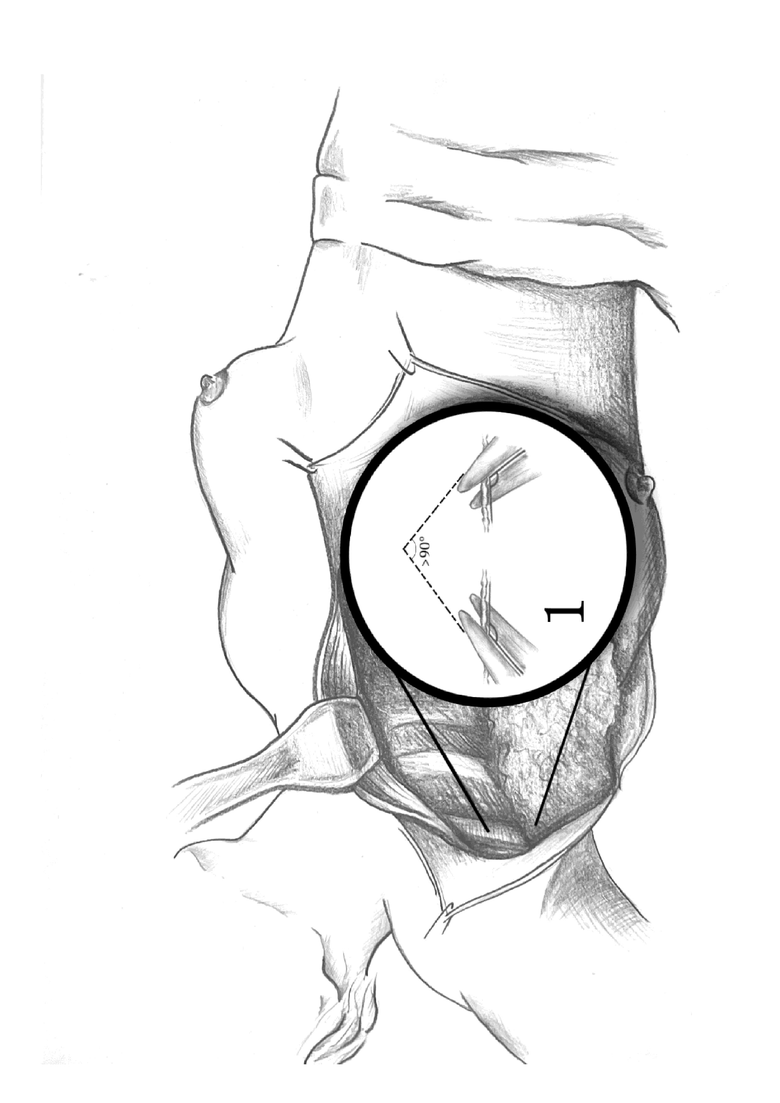
Изобретение относится к медицине, а именно к торакальной хирургии, онкологии. Выполняют диссекцию клетчатки с лимфоузлами в подмышечной, подключичной и подлопаточной областях с сохранением латеральных грудных артерии и вены, грудонадчревной вены, межреберноплечевого нерва, передних ветвей межреберных нервов. Под бинокулярным оптическим увеличением выделяют лимфатические сосуды в проекции удаленной клетчатки. Последовательно проводят двойную коагуляцию выделенных лимфатических сосудов с помощью электрогенератора Force Triad LigaSure или биполярной электрокоагуляции с низкой выходной мощностью не более 30 Вт с соблюдением угла между линиями коагуляционного шва более 90°. Способ позволяет выявить все возможные источники лимфореи и превентивно их коагулировать, сохранить нервные окончания, кровеносные сосуды небольшого калибра, не входящие в объем диссекции, что позволяет уменьшить проявления постмастэктомического синдрома у пациентов после подмышечно-подключично-подлопаточной лимфодиссекции; не требует формирования кожно-мышечных тоннелей в области подмышечной впадины, что сокращает травматичность и длительность оперативного вмешательства. 1 з.п. ф-лы, 1 ил., 1 пр.
1. Способ интраоперационной профилактики лимфореи при выполнении радикальной мастэктомии или радикальной резекции молочной железы, включающий подмышечно-подлопаточно-подключичную лимфодиссекцию, отличающийся тем, что выполняют диссекцию клетчатки с лимфоузлами в подмышечной, подключичной и подлопаточной областях с сохранением латеральных грудных артерии и вены, грудонадчревной вены, межреберноплечевого нерва, передних ветвей межреберных нервов; под бинокулярным оптическим увеличением выделяют лимфатические сосуды в проекции удаленной клетчатки; последовательно проводят двойную коагуляцию выделенных лимфатических сосудов с помощью электрогенератора Force Triad LigaSure или биполярной электрокоагуляции с низкой выходной мощностью не более 30 Вт с соблюдением угла между линиями коагуляционного шва более 90°.
2. Способ по п.1, характеризующийся тем, что дополнительно производят эластичное бинтование грудной клетки.
| MANOURAS A | |||
| et al | |||
| Modified radical mastectomy with axillary dissection using the electrothermal bipolar vessel sealing system | |||
| Arch Surg | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| СПОСОБ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПОСЛЕ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2007 |
|
RU2334485C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ ЛИМФОРЕИ ПРИ РАДИКАЛЬНОЙ МАСТЭКТОМИИ | 2009 |
|
RU2427333C1 |
| US 20200029632 A1, 30.01.2020 | |||
| Способ подпочвенного орошения с применением труб | 1921 |
|
SU139A1 |
| БОГДАНОВ А.В | |||
| др | |||
| Профилактика длительной и обильной | |||
Авторы
Даты
2024-05-07—Публикация
2023-05-02—Подача