Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно хирургии и трансплантации печени, и может быть использовано для стабилизации положения трансплантата печени в брюшной полости и сохранения проходимости кава-кавального (далее по тексту кавального) анастомоза посредством установки силиконового устройства, выполненного в виде баллон-катетера, в позадипеченочное поддиафрагмальное пространство.
Уровень техники
Трансплантация печени в настоящее время является единственным радикальным методом лечения пациентов в терминальной стадии различных диффузных заболеваний печени. При трансплантации печени особое внимание уделяют обеспечению гемодинамической стабильности, нарушение которой приводит к ишемическим повреждениям трансплантата, и, как следствие, к его дисфункции в раннем послеоперационном периоде, а также в отдаленные сроки. Одной из причин нарушения гемодинамической стабильности является нарушение оттока по венам печени после сосудистой реконструкции. На сегодняшний день в клинической практике широко используются три способа кавальной реконструкции: бок-в-бок, конец-в-конец и классический способ с пережатием НПВ. Ключевым фактором гемодинамической стабильности трансплантата является сохранение полной проходимости по созданному анастомозу. Венозный отток после трансплантации печени может быть затруднен деформацией (перегибом) или перекрутом кавального анастомоза, что приводит к обструкции, являющейся причиной наиболее серьезного осложнения - острого синдрома Бадда-Киари (СБК), который может привести к потере органа. Острый СБК - раннее послеоперационное сосудистое осложнение, на долю которого приходится около 3% случаев ортотопической трансплантации печени (ОТП). Это осложнение обычно возникает при сохранении полой вены реципиента при выполнении ОТП с использованием метода piggy-back из-за подвижности трансплантата в двух ортогональных плоскостях - сагиттальной и фронтальной. При технике формирования кавального анастомоза по Belgitti, особенно при широком анастомозе, подвижность трансплантата допускается только в боковой плоскости. Кавальный анастомоз ограничивает подвижность трансплантата по сагиттальной оси.
Таким образом, нарушение проходимости по созданному анастомозу может быть вызвано техническим дефектом при формировании кавального анастомоза, приводящим к стенозу анастомоза, а также анатомическими особенностями трансплантата и/или реципиента, приводящими к неправильному расположению трансплантата. Несоответствие массы тела донора и реципиента - относительно небольшой трансплантат, помещенный в большую брюшную полость (глубокую печеночную ямку) - вызывает подвижность трансплантата в образовавшемся широком пустом поддиафрагмальном пространстве, его смещение в правое подреберье, тем самым вызывая ротацию (перекручивание) или перегиб (деформацию) венозного анастомоза, приводящие к обструкции печеночного венозного оттока. Частота обструкции печеночного венозного оттока после имплантации печеночного трансплантата по классической методике достигает до 2%, при использовании техники piggyback - до 3-4%, и split - до 5-13%. В связи с изложенным актуальным является разработка средств и методов стабилизации трансплантата печени, устраняющих перечисленные выше проблемы, связанные с механической обструкцией выполненного анастомоза, препятствующей восстановлению венозного оттока из печени после ее трансплантации.
Из уровня техники известен способ стабилизации трансплантата печени посредством установки грудного имплантата в позадипеченочное поддиафрагмальное пространство (DOI: 10.1111/j.1399-0012.2011.01423.x Gastaca M, Valdivieso A, Ruiz P, Gonzalez J, Ventoso A, Ortiz de Urbina J. Venous outflow obstruction after orthotopic liver transplantation: use of a breast implant to maintain graft position. Clin Transplant 2011: 25: E320–E326. a 2011 John Wiley & Sons A/S). Стабилизация трансплантата с помощью данного средства с обеспечением постоянного правильного венозного оттока трансплантата является простой в реализации. Грудной имплантат представляет собой сложное высокотехнологичное изделие, которое состоит из капсулы и внутреннего наполнителя. Капсула обычно изготавливается из прочной силиконовой оболочки, которая может быть гладкой или шероховатой. Внутренний наполнитель может быть различным: солевым, силиконовым, гидрогелевым и другим. Грудной имплантат устанавливают после выполнения анастомозов. Однако извлечение данного средства после стабилизации положения трансплантата, которое может продолжаться до 2 месяцев после ОТП, связано с необходимостью повторной операции, которая является технически сложной в связи с заживлением и обтурацией области установки грудного имплантата. Кроме того, данное средство не позволяет удалять застойное содержимое из поддиафрагмального пространства после ОТП. Форма грудного имплантата не обеспечивает конгруэнтности с подлежащими анатомическими структурами и может вызывать пролежни в подлежащих тканях.
Известен способ стабилизации трансплантата печени после его имплантации посредством размещения в позадипеченочном пространстве стерильной перчатки, заполненной физраствором (D. Donataccio, S. Grosso, M. Donataccio, A simple and new device to avoid hepatic venous outflow obstruction in adult liver transplantation, Surg. Sci. 2 (2011) 485–487.). Однако данный способ также связан с необходимостью проведения повторной операции для удаления средства, поддерживающего положение трансплантата. Кроме того, в известном способе отсутствует возможность управления изменением объема используемого средства для обеспечения надежной фиксации трансплантата в его ложе. Кроме того, использование для стабилизации трансплантата печени медицинской перчатки в постоперационном периоде представляет существенную угрозу возникновения инфекционных осложнений в связи с возможным нарушением условий асептики-антисептики. Кроме того, известное средство не позволяет удалять застойное содержимое из поддиафрагмального пространства после ОТП.
Известен способ стабилизации трансплантата печени с помощью урологического катетера Фолея. (Wahab MA, Shehta A, Hamed H, Elshobary M, Salah T, Sultan AM, Fathy O, Elghawalby A, Yassen A, Shiha U. Hepatic venous outflow obstruction after living donor liver transplantation managed with ectopic placement of a foley catheter: A case report. Int J Surg Case Rep. 2015;10:65-8. doi: 10.1016/j.ijscr.2015.03.017. Epub 2015 Mar 12. PMID: 25805611; PMCID: PMC4429842.). Катетер Фолея наполняют физиологическим раствором и размещают между трансплантатом, диафрагмой и грудной стенкой. Постепенное опорожнение катетера начинают через неделю после его установки. Способ является простым и безопасным, позволяет контролировать процесс установки катетера Фолея и его удаление с помощью ультразвуковой допплерографии. Однако известный способ должным образом не стабилизирует расположение трансплантата в связи с малыми размерами баллона (до 50 мл), которые в большинстве случаев не обеспечивают заполнение им требуемого объема, образованного в позадипеченочной области после имплантации трансплантата для надежного позиционирования пересаженного органа, особенно в случае использования для трансплантации органа меньшего размера. Кроме того, использование катетера Фолея не позволяет адекватно дренировать поддиафрагмальное пространство, что может вызывать образование гематом, а в случае присоединения инфекции – абсцесса.
Для стабилизации трансплантата печени известно также использование зонда Блэкмора (Steinbrück K, Fernandes RA Jr, Enne M, da Silva Gomes Martinho JM, da Silva Alves JA, Pacheco-Moreira LF. Ectopic placement of Sengstaken-Blakemore device to correct outflow obstruction in liver transplantation: case reports. Transplant Proc. 2010 Mar;42(2):597-8. doi: 10.1016/j.transproceed.2010.01.048. PMID: 20304201.). Зонд Блэкмора оснащен двумя раздувными баллонами - круглым и овальным, сконфигурирован изначально для остановки кровотечения из расширенных вен пищевода и кардиального отдела желудка, а также для предотвращения забрасывания желудочного содержимого в пищевод и ротовую полость. Данный зонд является инструментом, который может быть использован при трансплантации печени, и который можно безопасно удалить через несколько недель после трансплантации. Однако недостаточный объем баллонов и наличие второго баллона делает его неподходящим для эффективной и надежной стабилизации трансплантата. Кроме того, известное средство при его использовании для стабилизации трансплантата печени не позволяет удалять застойное содержимое из поддиафрагмального пространства после ОТП.
Наиболее близким к заявленному изобретению является способ стабилизации трансплантата печени с помощью внутриматочного баллона (Tolan HK, Barut B, Kutlutürk K, Kayaalp C, Yilmaz S. Ectopic Balloon Device Placement to Correct the Positional Hepatic Venous Outflow Obstruction in Liver Transplantation. Exp Clin Transplant. 2020 Feb;18(1):89-92. doi: 10.6002/ect.2018.0125. Epub 2019 Jan 29. PMID: 30696392.), который содержит тонкий катетер с эластичным баллоном на конце. Катетер в большинстве случаев выполняют из силикона, который плотнее прилегает к тканям, обеспечивая лучшую фиксацию катетера в месте установки, препятствуя его миграции. Катетер имеет мягкий кончик с отверстиями и трубку для дренирования, через которую также возможно введение растворов в операционную рану. Баллон наполняют стерильной жидкостью до необходимого объема. Конструкция баллона обеспечивает возможность легкой и быстрой его установки, а также контролируемого постепенного удаления через небольшой дренажный разрез в течение нескольких недель без необходимости проведения повторной операции; характеризуется отсутствием реакции отторжения, связанной с материалом изделия, регулируемым диаметром баллона и наличием отверстия для дренирования полости. Однако внутриматочные баллонные катетеры сконфигурированы для специального применения - остановки послеродового кровотечения, проведения баллонной тампонады матки при раннем послеродовом кровотечении. При выполнении ОТП данные катетеры не обеспечивают надежной стабилизации трансплантата печени в связи с несоответствием геометрии раздуваемого баллона геометрии позадипеченочного пространства, которое является изогнутым и щелевидным, в отличие от полости матки, которая имеет более простую форму. Внутриматочный баллон расположен на катетере ближе к дистальному концу, в связи с чем не обеспечивает хорошего прилегания его к брюшной стенке с целью стабилизации трансплантата печени, а наличие мягкого кончика не позволяет зафиксировать катетер в анатомических структурах верхнего этажа брюшной полости после его заведения в позидипеченочное пространство. Перечисленные недостатки создают неудобство для хирургов при использовании внутриматочного баллона для стабилизации трансплантата печени, связанные с его проведением и фиксацией позади печени в верхнем отделе брюшной полости под диафрагмой, снижают эффективность проведенного хирургического лечения.
Технической проблемой, решаемой изобретением, является разработка способа стабилизации трансплантата печени, устраняющего перечисленные выше недостатки, характерные для аналогов, с использованием средства, сконфигурированного для размещения в поддиафрагмальном позадпеченочном пространстве после имплантации трансплантата.
Раскрытие изобретения
Технический результат заключается в обеспечении надежной фиксации трансплантата в одном положении для стабилизации кавального анастомоза со снижением риска его ротации при одновременном обеспечении активного дренажа (эвакуации) застойного содержимого из поддиафрагмального пространства.
Технический результат достигается способом стабилизации положения трансплантата печени в брюшной полости после гепатэктомии, включающим размещение трансплантата в поддиафрагмальном пространстве брюшной полости реципиента с последующим формированием сосудистых анастомозов, включая кавальный анастомоз, согласно которому, после формирования сосудистых анастомозов оценивают состояние венозного оттока, при этом оценивают факторы, вызывающие нарушение венозного оттока, включая наличие зоны демаркации, соответствующей бассейну оттока печеночной вены, наличие перекрута (ротации) относительно саггитальной оси трансплантата, наличие деформации кавального анастомоза;
при выявлении, по меньшей мере, одного из перечисленных факторов нарушения венозного оттока осуществляют имплантацию баллона-катетера в виде гибкой трубки, имеющей рабочую часть, выполненную с возможностью размещения в поддиафрагмальном пространстве реципиента, и проксимальную часть, выполненную с возможностью фиксации на коже реципиента, где рабочая часть снабжена раздуваемым под действием среды баллоном до объема 300 мл и Т-образным разветвлением, расположенным на дистальном конце трубки и содержащим дренажные отверстия,
при этом баллон-катетер дистальным Т-образным концом проводят снаружи через разрез в боковой области живота в брюшной стенке, устанавливают в позадипеченочном поддиафрагмальном пространстве, позиционируя трубку баллона-катетера за 6 и 7 сегментом трансплантата, после установки баллона-катетера его проксимальную часть фиксируют на коже реципиента, затем под интраоперационным контролем УЗИ осуществляют раздувание баллона до размеров, обеспечивающих наличие адекватного кровотока в сосудах трансплантата, после чего производят послойное ушивание раны;
начиная с 10 суток баллон-катетер сдувают под УЗИ контролем, при этом в случае выявления смещения трансплантата, вызывающего деформацию портального анастомоза, баллон снова раздувают до объема, обеспечивающего первоначальное расположение трансплантата, пробу повторяют не менее чем через 2 дня, и при отсутствии смещения трансплантата, баллон-катетер извлекают.
Заявленный способ стабилизации трансплантата является эффективным и безопасным, позволяет поддерживать положение печени или ее части при сплит-трансплантациях с помощью разработанного средства для этих целей и оригинальной техники проведения и размещения средства в поддиафрагмальном пространстве с возможностью его последующего удаления без проведения повторной операции. Баллон-катетер после ОТП может длительное время находиться в брюшной полости (до 2 месяцев, в среднем 10 – 20 дней) до полной стабилизации трансплантата.
Изобретение позволяет исключить обструкцию печеночного венозного оттока после имплантации печеночного трансплантата, связанную со смещением трансплантата в операционной ране и перекрутом, перегибом или деформацией венозного анастомоза, которые могут быть вызваны несоответствием массы тела донора и реципиента, использованием относительно небольшого трансплантата, помещенного в большую брюшную полость, и др. Использование позиционирующего баллона обеспечивает плотное прилегание трансплантата к поддиафрагмальному пространству реципиента, что позволяет трансплантату быстро достичь стабильности, таким образом преодолевая обструкцию венозного оттока. После трансплантации печени в случае интраоперационной диагностики обструкции венозного оттока, не связанной с наложением швов, простая объемная опора может позволить трансплантату адаптироваться к доступному пространству и преодолеть критическую перегрузку. Совмещение в разработанном устройстве функции удержания трансплантата в заданном положении с функцией дренирования поддиафрагмального пространства при трансплантации печени позволяет повысить эффективность лечения, сократить сроки госпитализации.
Таким образом, заявленное изобретение обеспечивает эффективную и безопасную стабилизацию трансплантата, а именно, стабильное и фиксированное расположение трансплантата в поддиафрагмальном пространстве, отсутствие перекрута порто-портального анастомоза, отсутствие зоны демаркации, что положительно влияет на гемодинамическую стабильность (сохранность кровоснабжения по правой печеночной вене) по данным УЗИ интраоперационно и в динамике, снижает риски дисфункции трансплантата в раннем послеоперационном периоде, а также в отдаленные сроки, повышая эффективность проведенной трансплантации печени.
Краткое описание чертежей
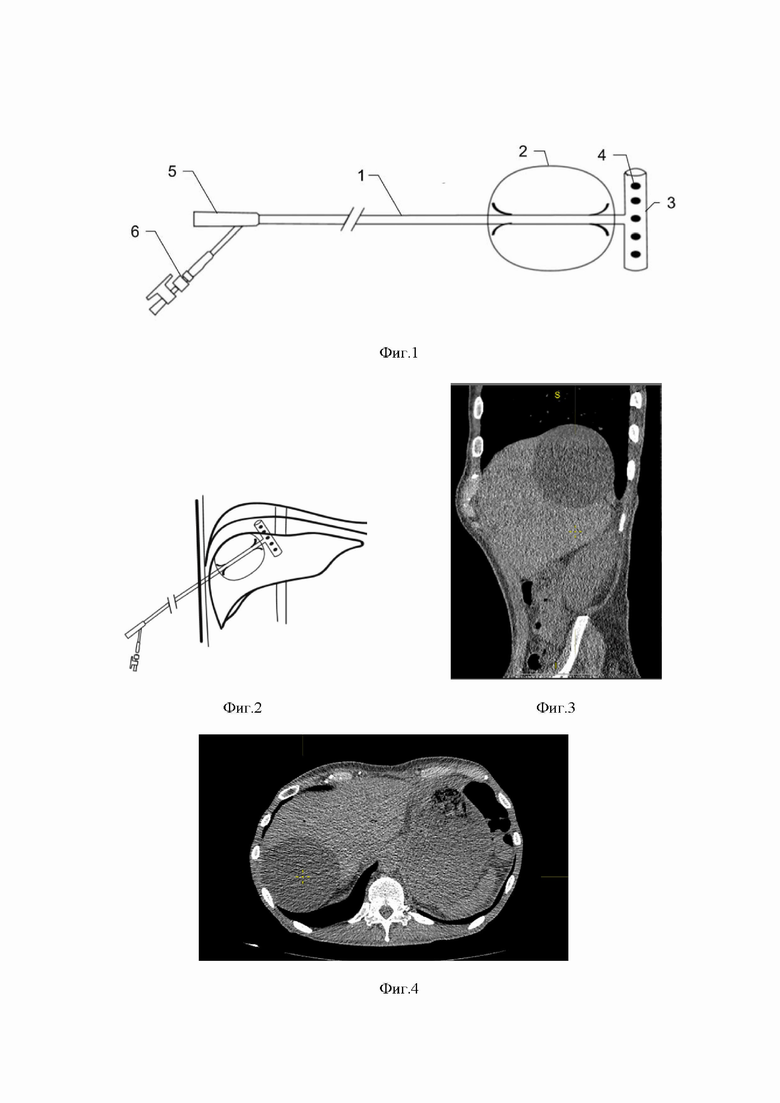
Изобретение поясняется чертежами и фотографиями, где на фигуре 1 схематично представлен разработанный баллон-катетер: 1 - гибкая трубка, 2 – баллон, 3 - Т-образное разветвление, 4 - дренажные отверстия, 5 - дренажный канал, 6 - канал для подведения рабочей среды; на фигуре 2 представлена схема установки баллона-катетера в поддиафрагмальное пространство, на фигуре 3 представлено интраоперационное УЗИ с установленным баллоном-катетером, на фигуре 4 - КТ пациента после операции на 1 сутки.
Осуществление изобретения
Выполняют ортотопическую трансплантацию печени (ОТП). ОТП может быть выполнена с использованием известных методик, например, Starzl, T. E., Iwatsuki, S., Esquivel, C. O., Todo, S., Kam, I., Lynch, S., ... & Shaw, B. W. (1985, November). Refinements in the surgical technique of liver transplantation. In Seminars in liver disease (Vol. 5, No. 04, pp. 349-356). При ОТП выполняют гепатэктомию, размещают трансплантат в поддиафрагмальном пространстве и формируют анастомоз по Бельгитти, Тзакису или Старзлу. Формируют портальный анастомоз и производят венозную реперфузию. После сосудистой реконструкции оценивают состояние трансплантата и венозного оттока. При выявлении нарушения венозного оттока оценивают факторы, характеризующие состояние кавального анастомоза, которые могут быть причиной такого нарушения, связанные с подвижностью трансплантата. Подвижность трансплантата может быть вызвана несоответствием антропометрических параметров донора и реципиента, наличием в позадипеченочной области свободного пространства после имплантации трансплантата.
Смещение печеночного трансплантата после репозиции в брюшную полость может приводить к появлению зоны демаркации, соответствующей бассейну оттока печеночной вены, ротации трансплантата и деформации вен в области кавального анастомоза. При выявлении зоны демаркации, соответствующей бассейну оттока печеночной вены, ротации трансплантата на угол более 15 градусов относительно сагиттальной оси трансплантата, или деформации кавального анастомоза, вызывающие нарушение венозного оттока, принимают решение об имплантации разработанного баллон-катетера.
Баллон-катетер выполнен в виде гибкой трубки, которая содержит:
- рабочую часть (внутреннюю часть), выполненную с возможностью размещения в поддиафрагмальном пространстве реципиента, снабженную эластичным баллоном, раздуваемым под воздействием среды (например, физиологическим раствором) до 300 мл, и Т-образным разветвлением (содержащим поперечный элемент), размещенным на дистальном конце трубки;
- проксимальную часть (наружную часть), выполненную с возможностью фиксации на коже реципиента.
Трубка снабжена дренажным каналом и каналом для подведения рабочей среды, используемой для раздувания баллона. На Т-образном конце выполнены сквозные аспирационные (дренажные) отверстия. В предпочтительном варианте реализации на Т-образном конце баллона-катетера выполнено 5 дренажных отверстий, одно отверстие расположено на поперечном элементе в его центральной части, совпадающей с осью трубки, а по два отверстия из оставшихся четырех расположены на поперечных элементах Т-образного разветвления с противоположных сторон от центрального отверстия. Выполнение на поперечном элементе трубки центрального отверстия облегчает введение баллона-катетера через разрез в брюшной полости для установки дренажа и его удаление из брюшной полости после стабилизации трансплантата путем простого нехирургического извлечения. При проведении баллона-катетера через разрез в брюшной стенке поперечный элемент за счет использования гибкой трубки и центрального отверстия занимает соосное с трубкой положение. Поперечный элемент трубки выполнен с открытыми атравматичными концами. Дренажные отверстия предпочтительно выполнены диаметром 0,2 мм, позволяют осуществить адекватный отток внутрибрюшного содержимого.
Трубка баллона-катетера выполнена из материала, подходящего для внутрибрюшного расположения, например, из силикона, характеризующегося твердостью по Шор А:14-16. Баллон-катетер предпочтительно имеет следующие габаритные размеры: длина трубки 45 – 50 см, диаметр 22F, при этом длина рабочей части трубки (баллона катетера) составляет 20 – 25 см, вдоль которой расположен эластичный баллон длиной примерно 15 см, раздуваемый до диаметра примерно от 5 см до 14 см, предпочтительно от 5 до 7 см; длина поперечного элемента Т-образной части составляет 10 - 12 см.
Баллон-катетер заводят в операционную рану «сложенным» Т-образным концом (с соосным расположением трубки и поперечных элементов Т-образного разветвления) через небольшой разрез в брюшной стенке по срединной подмышечной линии. Рабочую часть баллона-катетера располагают поддиафрагмально. Далее проксимальную часть баллона-катетера фиксируют на коже реципиента и производят раздувание баллона катетера путем нагнетания в него рабочей среды через соответствующий канал до исчезновения зоны демаркации, восстановления кровотока по всем печёночным венам, устранения ротации трансплантата. Для раздувания баллона катетера к наружному проксимальному концу трубки присоединяют устройство с емкостью для рабочей среды (в качестве такого устройства может быть использован шприц 50 мл). В качестве рабочей среды предпочтительно используют стерильный физиологический раствор комнатной температуры, как правило, в количестве, не более 250 мл (обычно не превышает 200-300 мл). Наличие Т-образного разветвления баллон-катетера обеспечивает его дополнительную фиксацию в операционной ране. Раздувание баллона-катетера проводят под интраоперационным УЗИ контролем с оценкой состояния оттока по печеночной вене. Баллон раздувают до объема, обеспечивающего плотное прилегание трансплантата к поддиафрагмальному пространству реципиента, до полного расправления кава-кавального анастомоза, что позволяет трансплантату быстро достичь стабильности, таким образом преодолевая обструкцию венозного оттока. Баллон заполняет полость между трансплантатом и диафрагмой, прижимая трансплантат сзади и латерально к диафрагме и передней брюшной стенке, удерживая печень в печеночной ямке в неподвижном положении с контролируемым положением анастомозов. Критерием правильности установки баллона является наблюдаемая УЗИ картина стабильного оттока по венам печени.
Начиная с 10 суток после выполнения ОТП, баллон-катетер сдувают под УЗИ контролем, при этом в случае выявления смещения трансплантата, вызывающего деформацию портального анастомоза, баллон снова раздувают до объема, обеспечивающего первоначальное положение трансплантата, через каждые два - три дня пробу повторяют, и при отсутствии смещения трансплантата, баллон-катетер извлекают. Баллон-катетер может быть извлечен на 10-20 сутки после фиксации печени спайками в её ложе.
Сдувание баллона может выполняться поэтапно и постепенно: на первом этапе на 10 сутки из баллона убирают ¼ часть рабочей среды от общего введенного объема под контролем УЗИ. При сохранении гемодинамики по печеночным венам далее в течение недели (например, через каждые 2 дня) из баллона продолжают убирать примерно по ¼ части рабочей среды. Контролируют отсутствие смещения трансплантата печени и отсутствие нарушения венозного оттока при помощи УЗИ. Если фиксация печени не произошла, раздувают баллон снова и повторяют сдувание через 2-3 дня. Если сдувание баллона не сопровождается изменениями кровотока или смещением трансплантата, полностью его опорожняют и извлекают баллон.
Возможность осуществления заявленного изобретения продемонстрирована следующими клиническими примерами.
Клинический пример №1
Пациент К., 36 лет находился в листе ожидания трансплантации печени с диагнозом «Цирроз печени HCV-этиологии, класс Чайлд-Пью С. MELD 32. Острая печеночная недостаточность на фоне хронической (ACLF-синдром), 2 типа. Синдром портальной гипертензии: ВРВП 3 ст, ЭЛ в 2019,2020, 2021, 2023, гепатоспленомегалия, тромбоз ВВ M0L1T1Rl2. Печеночно-клеточная недостаточность: коагулопатия, гипоальбуминемия, латентная энцефалопатия». С учётом отрицательной динамики состояния включен в экстренный лист ожидания, и в связи с наличием совместимого пригодного донорского органа оперирован. С учётом необходимости в срочной трансплантации, было допущено несоответствие антропометрии донора и реципиента. Так, масса тела донора составляла 72 кг, реципиента 104 кг. После имплантации небольшой донорской печени в большую полость реципиента отмечена дислокация печени направо. Трансплантат смещался в правое поддиафрагмальное пространство, от чего происходило перекручивание кавальных ворот печени, сдавление правой печеночной вены. На трансплантате появлялась зона демаркации, синюшный участок, соответствующий зоне оттока в правую печеночную вену. Интраоперационное УЗИ – правая печеночная вена сужена до 2-3 мм, линейный кровоток до 1,5 м/с, объёмный 20-30 мл/мин. Принято решение установить баллон-катетер разработанной конструкции. Был использован двухпросветный баллон-катетер длиной 30 см, толщиной 1 см, длиной поперечной Т-образной частью – 4 см, содержащий расширяющийся баллон объемом до 300 мл за счет введения физраствора, пять отверстий диаметром 0,2 см для дренирования, расположенные на дистальном Т-образном конце баллона-катетера, как показано на фиг.1.
Баллон-катетер заведен в операционную рану «сложенным» Т-образным концом через разрез в брюшной стенке по срединной подмышечной линии, установлен в позадипеченочном поддиафрагмальном пространстве с расположением трубки баллона-катетера за 6 и 7 сегментом трансплантата, раздут до 180 мл физиологического раствора. Контроль кровотока – перекрут вены в меньшей степени, по правой печеночной вене объемный кровоток снижен. Баллон дораздут до 300 мл – полная коррекция положения печени, кровоток по правой печеночной вене восстановился. На 10 сутки после операции выполнено пробное сдувание баллона до 250 мл – трансплантат печени смещается, с нарушением кровотока. На 13 сутки – сдувание баллона выполнено повторно, влияние на позиционирование трансплантата отсутствовало, в связи с чем произведено сдувание баллона-катетера в три этапа, на первом и втором этапах производили удаление физраствора по 50 мл, на третьем этапе проведено удаление оставшейся жидкости и удаление баллона-катетера через контрапертуру. Пациент выписан на 20 сутки в удовлетворительном состоянии. Контроль КТ через 6 месяцев – трансплантат позиционирован без смещений, сохранный кровоток в венах печени.
Таким образом, использование заявленного способа позволило стабилизировать положение трансплантата печени в поддиафрагмальном пространстве с помощью баллон-катетера без проведения повторной операции по его извлечению, улучшить кровоснабжение трансплантата печени посредством исключения перекрутов и перегибов венозного анастомоза, обеспечило отсутствие зоны ишемии в области кава-кавального анастомоза, более раннюю активизацию и более полную реабилитацию пациента, сократить срок его стационарного лечения.
Заявленный способ имеет широкие перспективы применения в клинической практике, может быть воспроизведен и тиражирован в хирургических клиниках, выполняющих операции по трансплантации печени.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ тромбэктомии при окклюзии оттока по собственным печеночным венам после ортотопической трансплантации печени | 2017 |
|
RU2675028C1 |
| Способ гепатэктомии при ортотопической трансплантации печени | 2017 |
|
RU2661733C1 |
| СПОСОБ ПЕРЕСАДКИ ПРАВОЙ ДОЛИ ПЕЧЕНИ ОТ ЖИВОГО РОДСТВЕННОГО ДОНОРА | 2000 |
|
RU2174826C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КРОВООБРАЩЕНИЯ ПРИ ТРАНСПЛАНТАЦИИ ПЕЧЕНИ ПРИ АНОМАЛЬНОМ СТРОЕНИИ АРТЕРИАЛЬНОГО РУСЛА ТРАНСПЛАНТАТА ПЕЧЕНИ | 2018 |
|
RU2691525C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2021 |
|
RU2760537C1 |
| Способ гипотермической оксигенированной двойной машинной перфузии трансплантата печени от посмертного донора | 2023 |
|
RU2830104C1 |
| Способ лечения больных циррозом печени, осложненным портальной гипертензией и гиперспленизмом | 2021 |
|
RU2783657C1 |
| СПОСОБ ОЦЕНКИ ТРАНСПЛАНТАТА ПЕЧЕНИ EX SITU С ИСПОЛЬЗОВАНИЕМ МНОГОСРЕЗОВОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ ДЛЯ ОПРЕДЕЛЕНИЯ ВОЗМОЖНОСТИ ВЫПОЛНЕНИЯ СПЛИТ-ТРАНСПЛАНТАЦИИ | 2019 |
|
RU2710609C1 |
| Способ профилактики ишемических осложнений в посттрансплантационном периоде при ортотопической трансплантации печени | 2020 |
|
RU2723465C1 |
| СПОСОБ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ ТРУПНОЙ ПЕЧЕНИ | 2013 |
|
RU2537768C2 |
Изобретение относится к области медицины, а именно хирургии и трансплантации печени. Размещают трансплантат печени в поддиафрагмальном пространстве брюшной полости реципиента. Формируют сосудистые анастомозы, включая кавальный анастомоз. После формирования сосудистых анастомозов оценивают состояние венозного оттока, оценивают факторы, вызывающие нарушение венозного оттока: наличие зоны демаркации, соответствующей бассейну оттока печеночной вены; наличие перекрута - ротации относительно сагиттальной оси трансплантата; наличие деформации кавального анастомоза. При выявлении по меньшей мере одного из перечисленных факторов нарушения венозного оттока осуществляют имплантацию баллона-катетера в виде гибкой трубки, имеющей рабочую часть, выполненную с возможностью размещения в поддиафрагмальном пространстве реципиента, и проксимальную часть, выполненную с возможностью фиксации на коже реципиента. Рабочая часть баллона-катетера снабжена раздуваемым под действием среды баллоном до объема 300 мл, в качестве среды используют физиологический раствор, и Т-образным разветвлением на дистальном конце трубки, содержащим дренажные отверстия. Баллон-катетер заводят в операционную рану «сложенным» Т-образным концом через разрез в брюшной стенке по срединной подмышечной линии, устанавливают в позадипеченочном поддиафрагмальном пространстве. Позиционируют трубку баллона-катетера за 6 и 7 сегментом трансплантата. После установки баллона-катетера его проксимальную часть фиксируют на коже реципиента. Под интраоперационным контролем УЗИ осуществляют раздувание баллона до размеров, обеспечивающих наличие адекватного кровотока в сосудах трансплантата. Производят послойное ушивание раны. Начиная с 10 суток баллон-катетер сдувают под УЗИ контролем. В случае выявления смещения трансплантата, вызывающего деформацию портального анастомоза, баллон снова раздувают до объема, обеспечивающего первоначальное положение трансплантата. Пробу повторяют не менее чем через 2 дня, и при отсутствии смещения трансплантата баллон-катетер извлекают. Способ позволяет обеспечить надежную фиксацию трансплантата в одном положении для стабилизации кавального анастомоза, снизить риск его ротации, одновременно обеспечить активный дренаж застойного содержимого из поддиафрагмального пространства. 4 ил., 1 пр.
Способ стабилизации положения трансплантата печени в брюшной полости после гепатэктомии, включающий размещение трансплантата в поддиафрагмальном пространстве брюшной полости реципиента с последующим формированием сосудистых анастомозов, включая кавальный анастомоз, отличающийся тем, что после формирования сосудистых анастомозов оценивают состояние венозного оттока, при этом оценивают факторы, вызывающие нарушение венозного оттока, включая наличие зоны демаркации, соответствующей бассейну оттока печеночной вены, наличие перекрута - ротации относительно сагиттальной оси трансплантата, наличие деформации кавального анастомоза,
при выявлении по меньшей мере одного из перечисленных факторов нарушения венозного оттока осуществляют имплантацию баллона-катетера в виде гибкой трубки, имеющей рабочую часть, выполненную с возможностью размещения в поддиафрагмальном пространстве реципиента, и проксимальную часть, выполненную с возможностью фиксации на коже реципиента, где рабочая часть снабжена раздуваемым под действием среды баллоном до объема 300 мл, в качестве среды используют физиологический раствор, и Т-образным разветвлением на дистальном конце трубки, содержащим дренажные отверстия,
баллон-катетер заводят в операционную рану «сложенным» Т-образным концом через разрез в брюшной стенке по срединной подмышечной линии, устанавливают в позадипеченочном поддиафрагмальном пространстве, позиционируя трубку баллона-катетера за 6 и 7 сегментом трансплантата, после установки баллона-катетера его проксимальную часть фиксируют на коже реципиента, после чего под интраоперационным контролем УЗИ осуществляют раздувание баллона до размеров, обеспечивающих наличие адекватного кровотока в сосудах трансплантата, после чего производят послойное ушивание раны,
начиная с 10 суток баллон-катетер сдувают под УЗИ контролем, при этом в случае выявления смещения трансплантата, вызывающего деформацию портального анастомоза, баллон снова раздувают до объема, обеспечивающего первоначальное положение трансплантата, пробу повторяют не менее чем через 2 дня, и при отсутствии смещения трансплантата баллон-катетер извлекают.
| Tolan HK et al | |||
| / Ectopic Balloon Device Placement to Correct the Positional Hepatic Venous Outflow Obstruction in Liver Transplantation | |||
| Exp Clin Transplant | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Котенко О.Г | |||
| и др | |||
| / Реконструкция венозного оттока при родственной трансплантации печени у детей // Трансплантология | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ предохранения аэростатов и дирижаблей от атмосферных разрядов | 1925 |
|
SU1957A1 |
| US | |||
Авторы
Даты
2024-07-29—Публикация
2024-01-03—Подача