Изобретение относится к области извлечения веществ органическими экстрагентами из водных растворов, в частности, к способам получения редкоземельных металлов (РЗМ) из бедного или техногенного сырья с помощью экстракции.
Известен способ извлечения редкоземельных металлов из водных растворов (патент RU №2484163, опубл. 10.06.2013), в котором в качестве экстрагента используют нафтеновую кислоту, а в качестве инертного растворителя используют керосин. При этом соотношение объемов органической и водной фаз составляло 1:(9-11). Процесс ведут при рН 5,0-5,1. Максимальный коэффициент распределения составил 65 при рН=5,5.
Недостатком способа является неполное извлечение церия из раствора. Извлечение церия ведется в слабокислой среде, и при этом необходимо четкое выполнение условия соотношения водной и органической фаз.
Известен способ извлечения церия (III) экстракцией олеиновой кислотой из нитратных сред (Журнал прикладной химии. 2007. Т. 80. Вып. 2. С. 187-190). Концентрация экстрагента равнялась 0,5 моль/л. Коэффициент распределения церия (III) при экстракции олеиновой кислотой в интервале pH 3-5 возрастает от 1 до 100, при рН=5,5 коэффициент распределения достигает величины 235.
Недостатками способа являются низкое извлечение церия (III) при pH<5 и зависимость от концентрации экстрагента.
Известен способ извлечения тория (IV) экстракцией при утилизации растворов солянокислотного вскрытия перовскита (Журнал прикладной химии. 2004. Т. 77. Вып. 5. С. 715-719). в котором в качестве экстрагента использовали трибутилфосфат ТБФ в солянокислых растворах перовскита. Извлечение тория (IV) происходит при точном соотношении органической и водной фазы 3:1 при рН раствора от 2 до 4. Максимальное извлечение тория (IV) составляет 84%.
Недостатками способа являются неполное извлечение тория из солянокислых растворов и зависимость эффективности процесса от соотношения органической и водной фаз.
Известен способ извлечения металлов из водных растворов (патент RU №2009228, опубл. 15.03.1994), включающий экстракцию металлов растворами азотсодержащих анионитов, содержащих, по крайней мере, два органических радикала в органическом инертном разбавителе. Экстракцию металлов ведут растворами аминов и/или четвертичных аммониевых оснований, два органических радикала в каждом из которых представляют 2,4-диэтилоктилы.
Недостатком способа является использование концентрированных растворов аминов и солей четвертичных аммониевых оснований, являющихся токсичными соединениями и требующих применения высаливателей.
Известен способ извлечения церия (патент RU №2530081, опубл. 10.10.2014) экстракцией из производственных растворов сложного солевого состава. Экстракцию ведут из сульфатных растворов концентрацией 0,5-2,0 М сложным органическим реагентом: используют раствор 2-метил-8,9-дигидро[1,2,4]триазоло[1,5-α]хиназолин-6(7Н)-она, в качестве растворителя применяют метиленхлорид. Процесс ведут в течение 15 минут при рН от 2 до 3. После расслоения органическую фазу отделяют и проводят реэкстракцию.
Недостатком способа является специфичность экстрагента, необходимость его применения в точной концентрации, равной 0,32%. Экстрагент относится к конденсированным гетероциклическим соединениям, для которого остаются невыясненными вопросы о механизмах и региоселективности превращений и дальнейшей модификации используемых соединений. Для более эффективного извлечения требуется использование растворителя - метиленхлорида.
Известен способ экстракции РЗЭ иттрия (III), церия (III) и эрбия (III) из водных растворов (патент RU 2441087, опубл. 27.01.2012), принятый за прототип. Экстракцию ведут из водных растворов в две стадии при рН 4,5-5,5 в течение 10-15 минут. В качестве экстрагента используют олеиновую кислоту и инертный разбавитель - керосин. Соотношение объемов экстрагента и водного раствора составляет 1:10. Причем содержание олеиновой кислоты в экстрагенте составляет для первой стадии 5-7 об. %, а для второй стадии содержание олеиновой кислоты составляет 15-17 об. %.
Недостатком способа является необходимость добавления инертного разбавителя - керосина, довольно узкий интервал концентрации содержания олеиновой кислоты. Наибольшая степень извлечения РЗЭ соответствует максимальной концентрации олеиновой кислоты и наблюдается при рН среды, равной 5.
Техническим результатом является увеличение степени извлечения катионов церия (III) из производственных растворов сложного солевого состава.
Технический результат достигается тем, что водный раствор помещают в реактор и при перемешивании добавляют серную кислоту при соотношении объема кислоты к объему раствора 1:2 с получением двойных сульфатов, их фильтрацию с получением твердой фазы и водной фазы, которую помещают в реактор, добавляют щелочь и перемешивают, полученную смесь отправляют на фильтрацию с получением водной фазы и твердой фазы в форме гидроксидов, которую переносят в реактор и добавляют азотную кислоту до полного ее растворения, с получением раствора, содержащего нитрат церия (III), к которому после добавление ПАВ добавляют хлорид натрия в количестве от 0,0025 до 0,25 моль/л, далее доводят рН от 3,0 до 7,0 путем добавления азотной кислоты, термостатируют при температуре от 20 до 250С, добавляют изооктиловый спирт и перемешивают в течение не более 30 минут, при этом органическую фазу отделяют и проводят инфракрасный спектроскопический анализ на содержание катионов церия (III), после этого ее сушат в сушильном шкафу с получением оксида церия, а водную фазу анализируют фотометрическим методом на содержание катионов церия (III), при этом полученные значения концентраций катионов церия (III) используют при расчете степени его извлечения в органическую фазу, и отправляют водную фазу на утилизацию.
Способ поясняется следующей фигурой:
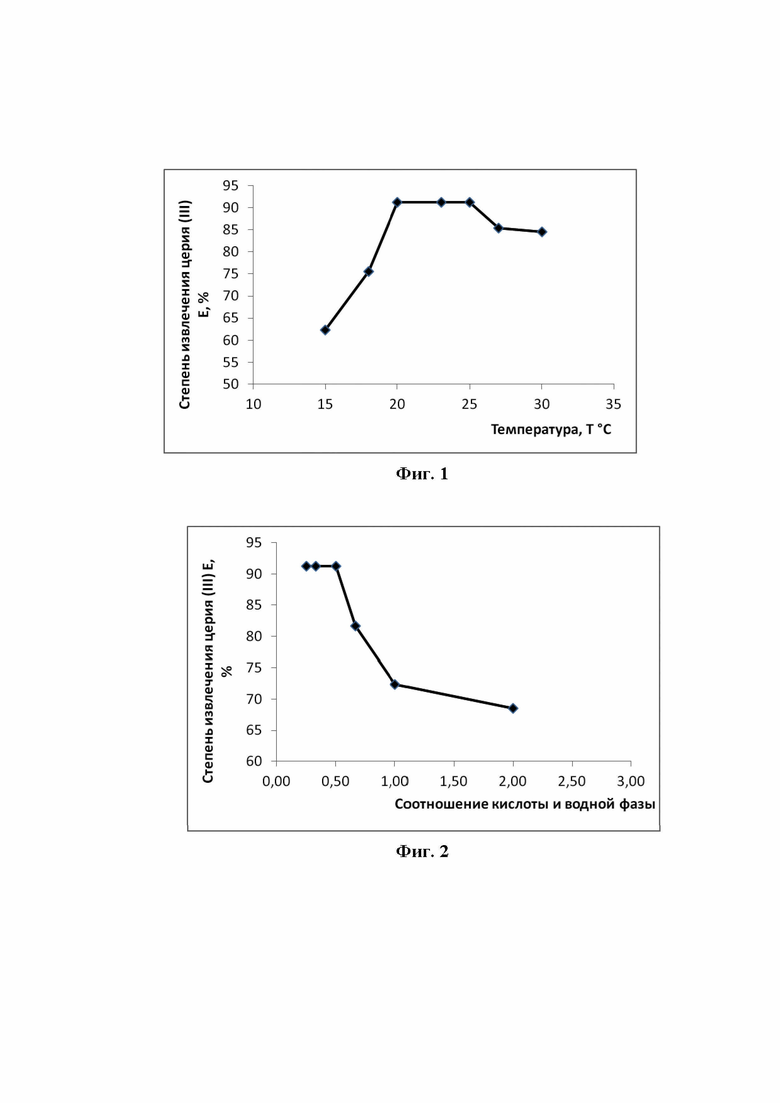
фиг. 1 - график зависимости максимального извлечения катионов церия (III) между водной и органической фазами от температуры;
фиг. 2 - график зависимости максимального извлечения катионов церия (III) от соотношения серной кислоты и водной фазы.
Способ осуществляют следующим образом. Исходным сырьем являются производственные растворы сложного солевого состава, которые используют для извлечения, в частности Ce+3. Раствор сложного солевого состава помещают в реактор и при перемешивании добавляют серную кислоту в соотношении объема кислоты к объему раствора 1:2 с получением двойных сульфатов. Далее двойные сульфаты отфильтровывают на делительной воронке с фильтром «синяя лента» с получением твердой фазы, которую отправляют на дальнейшую переработку, и водной фазы. Водную фазу помещают в реактор, добавляют щелочь для осаждения гидроксидов и перемешивают. Полученную смесь отправляют на фильтрацию на делительной воронке с фильтром «синяя лента» с получением твердой фазы, в форме гидроксидов и водной фазы, которую отправляют на дальнейшую переработку. Твердую фазу в форме гидроксидов переносят в реактор и добавляют азотную кислоту до полного растворения осадка. Полученный таким образом раствор, содержащий нитрат церия (III), помещают в реактор, добавляют поверхностно-активное вещество (ПАВ) анионного типа и перемешивают на магнитной мешалке. В качестве ПАВ анионного типа используют додецилсульфат натрия массой 0,17 г, что соответствует стехиометрии указанной реакции:
Ce3++3C12H25OSO3-=Ce(C12H25OSO3)3,
где Ce3+ - катион металла,
C12H25OSO3- - додецилсульфат-ион,
Ce[C12H25OSO3]3 - сольват.
Затем в водный раствор нитрата церия (III) добавляют хлорид натрия в количестве от 0,0025 до 0,25 моль/л. Доводят рН раствора до значения от 3,0 до 7,0 добавлением азотной кислоты и перемешивают на магнитной мешалке. Полученный раствор помещают в термостат и термостатируют при температуре от 20 до 25°С. Затем добавляют изооктиловый спирт и перемешивают в течение не более 30 минут. При этом происходит извлечение катионов церия (III) собирателем додецилсульфатом натрия в виде хлорокомплексов. Образовавшуюся смесь оставляют для расслаивания, после расслоения образуются органическая и водная фазы. Органическую фазу отделяют и проводят инфракрасный спектроскопический анализ на атомно-эмиссионном спектрометре на содержание катионов церия (III). Водную фазу анализируют фотометрическим методом на концентрационном фотоколориметре на содержание катионов церия (III). Полученные значения концентраций катионов церия (III) используют при расчете степени его извлечения в органическую фазу. Органическую фазу с извлеченными в нее катионами церия (III) направляют в сушильный шкаф для термического разложения с получением оксида церия, который является готовым продуктом. Водную фазу, содержащую следовые количества церия (III), отправляют на утилизацию.
Способ поясняется следующим примером.
В реактор помещали производственный раствор сложного солевого состава объемом 0,2 л с содержанием катионов церия (III) 0,001 моль/л. Далее при перемешивании добавляли серную кислоту в соотношении объема кислоты к объему раствора 1:2. Выбор соотношения серной кислоты и водной фазы 1:2 поясняется графиком зависимости максимального извлечения катионов церия (III) от соотношения серной кислоты и водной фазы (фиг. 2), при данном соотношении достигается максимальная степень извлечения. При меньшем и большем соотношениях серной кислоты и водной фазы степень извлечения понижается. В результате этого процесса получают двойные сульфаты, которые отправляли на дальнейшую переработку, и водную фазу, в которую добавляли щелочь для осаждения гидроксидов. Далее проводили процесс фильтрации с получением твердой фазы в виде гидроксидов церия (III). Гидроксиды церия (III) растворяли в азотной кислоте с получением раствора, содержащего нитрат церия (III). К водному раствору нитрата церия (III) при перемешивании добавляли поверхностно-активное вещество (ПАВ) анионного типа - додецилсульфат натрия, массой 0,17 г. В данном случае ПАВ выполнял функцию собирателя, что отражается на стехиометрии указанной реакции, которая может быть представлена следующим образом:
Ce3++3C12H25OSO3-=Ce(C12H25OSO3)3,
где Ce3+ - катион металла,
C12H25OSO3- - додецилсульфат-ион.
Использование в качестве экстрагента изооктилового спирта и ПАВ анионного типа додецилсульфата натрия обеспечивало значительное расширение спектра применяемых экстрагентов.
Затем в водном растворе нитрата церия (III) увеличивали содержание хлорид-ионов путем добавления хлорида натрия в виде порошка в количестве от 0,0025 до 0,25 моль/л. Выбор количества хлорид-ионов поясняется таблицей 1. При концентрации хлоридов менее 0,0025 М и более 0,25 М степень извлечения катионов церия (III) существенно понижается.
Таблица 1 - Экспериментальные данные по извлечению катионов церия (III) при различных концентрациях хлорид-ионов.
рН полученной смеси регулировали добавлением азотной кислоты до значения от 3,0 до 7,0. Выбор рабочего интервала рН поясняется таблицей 2. При значениях рН менее 3,0 и более 7,0 степень извлечения катионов церия (III) существенно понижается.
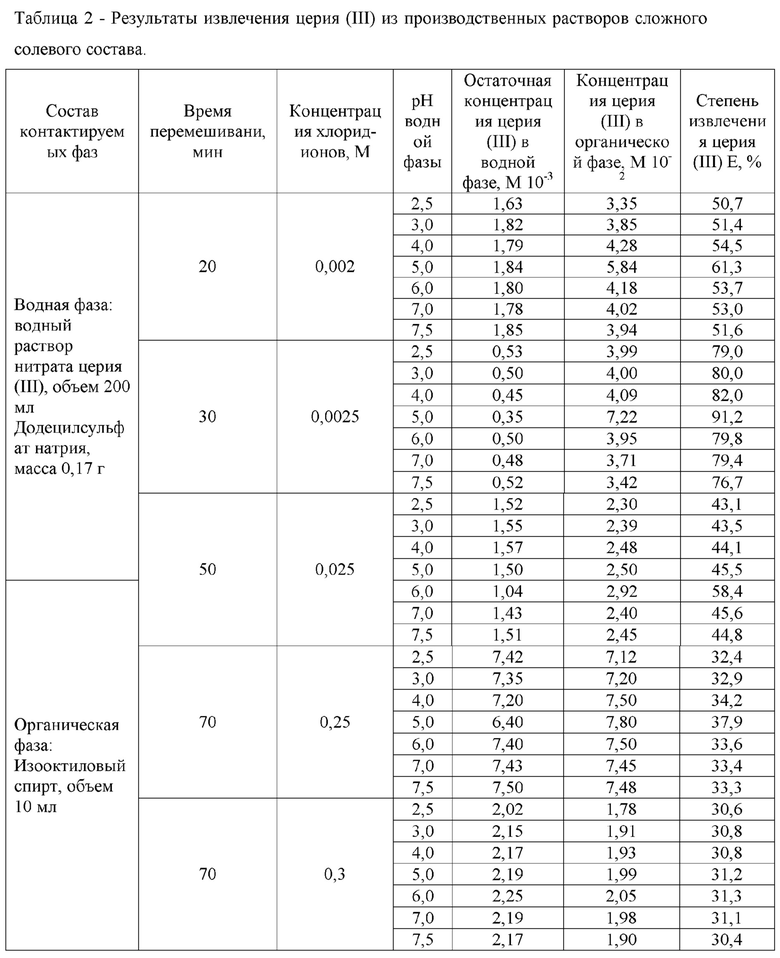
Полученную смесь помещали в реактор и перемешивали ее на магнитной мешалке типа ПЭ-6110. Затем рассматриваемую систему термостатировали в термостате при температуре от 20 до 25°С. Выбор температуры перемешивания от 20°С до 25°С поясняется графиком зависимости максимального извлечения катионов церия (III) между водной и органической фазами от температуры (фиг. 1), при такой температуре перемешивания достигаются максимальные значения степени извлечения. При температуре перемешивания менее 20°С и более 25°С значения степени извлечения существенно понижаются.
В качестве органического экстрагента использовали 10 мл изооктилового спирта, в слой которого переходили образовавшиеся сольваты. Сольваты ориентированы полярной группой к катиону церия (III) и экранированы неполярными радикалами с внешней стороны. Это обеспечивает взаимодействие сольвата с изооктиловым спиртом и переносом его в органическую фазу. Далее проводили перемешивание в течении 30 минут. Выбор времени перемешивания поясняется таблицей 2. При времени перемешивания органической и водной фаз менее и более 30 минут степень извлечения катионов церия (III) существенно понижается. При этом происходило извлечение катионов церия (III) собирателем додецилсульфатом натрия в виде хлорокомплексов из водной фазы в слой органической фазы. Образовавшуюся смесь отстаивали для расслоения, после чего образовывались две фазы - органическая и водная. Водную фазу анализировали на содержание церия (III) фотометрическим методом на приборе КФК - 3 КМ. Органическую фазу отправляли на инфракрасный спектроскопический анализ на атомно-эмиссионном спектрометре «ICPE-9000» на содержание катионов церия (III). Затем проводили расчет степени извлечения катионов церия (III), при котором использовали полученные значения концентраций катионов церия (III) в водной и органической фазах. Затем проводили процесс сушки в сушильном шкафу с получением готового продукта - оксида церия. Водную фазу, содержащую следовые количества церия (III), отправляли на утилизацию.
Способ позволяет достичь повышения степени извлечения катионов церия (III) из производственных растворов сложного солевого состава за счет увеличения времени перемешивания водной и органической фаз и увеличения концентрации хлорид-ионов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗВЛЕЧЕНИЯ СОЛЕЙ ГОЛЬМИЯ (III) ИЗ ВОДНЫХ РАСТВОРОВ | 2015 |
|
RU2616748C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ КАТИОНОВ САМАРИЯ (III) | 2011 |
|
RU2481141C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЭРБИЯ (III) ЭКСТРАКЦИЕЙ | 2016 |
|
RU2624269C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ La (III) ИЗ ВОДНОГО РАСТВОРА НИТРАТА ЛАНТАНА (III), ПОЛУЧЕННОГО ПРИ ПЕРЕРАБОТКЕ МОНАЦИТА | 2021 |
|
RU2760693C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ КАТИОНОВ Еu ИЗ ВОДНО-СОЛЕВЫХ РАСТВОРОВ | 2013 |
|
RU2548353C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ГОЛЬМИЯ (III) И ЦЕРИЯ (III) АНИОННЫМ ПОВЕРХНОСТНО-АКТИВНЫМ ВЕЩЕСТВОМ (ПАВ) ИЗ ВОДНОГО РАСТВОРА ИХ НИТРАТОВ | 2020 |
|
RU2735017C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ КАТИОНОВ САМАРИЯ (III) ИЗ ВОДНЫХ ФАЗ | 2013 |
|
RU2548836C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГОЛЬМИЯ (III) ИЗ РАСТВОРОВ СОЛЕЙ | 2014 |
|
RU2584626C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЛАНТАНА(III) ИЗ РАСТВОРОВ СОЛЕЙ | 2015 |
|
RU2602112C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦЕРИЯ ИЗ РАСТВОРОВ СОЛЕЙ | 2011 |
|
RU2456359C1 |
Изобретение относится к получению редкоземельных металлов, в частности к получению церия (III) экстракцией из техногенного сырья сложного солевого состава в виде водного раствора. Способ включает помещение водного раствора в реактор и при перемешивании добавление серной кислоты при соотношении объема кислоты к объему раствора 1:2 с получением двойных сульфатов, их фильтрацию с получением твердой фазы и водной фазы. Затем помещение водной фазы в реактор, добавление к ней щелочи, перемешивание, с получением смеси, которую отправляют на фильтрацию с получением водной фазы и твердой фазы в форме гидроксидов. Далее перенос полученной твердой фазы в реактор и добавление азотной кислоты до полного ее растворения, с получением раствора, содержащего нитрат церия (III), к которому после добавления поверхностно-активного вещества анионного типа, в качестве которого используют додецилсульфат натрия, добавляют хлорид натрия в количестве от 0,0025 до 0,25 моль/л, далее доводят рН от 3,0 до 7,0 путем добавления азотной кислоты, термостатируют при температуре от 20 до 25°С. Далее добавляют изооктиловый спирт в качестве экстрагента и перемешивают в течение не более 30 мин, при этом органическую фазу отделяют и сушат с получением оксида церия. Обеспечивается увеличение степени извлечения катионов церия (III). 2 ил., 2 табл., 1 пр.
Способ извлечения церия (III) из техногенного сырья сложного солевого состава в виде водного раствора, включающий добавление к упомянутому водному раствору, содержащему нитрат церия (III), поверхностно-активного вещества (ПАВ) анионного типа, в качестве которого используют додецилсульфат натрия, приведение в контакт водного раствора с экстрагентом, в качестве которого используют изооктиловый спирт, перемешивание смеси, отстаиваивание до образования органической и водной фаз и их разделение, отличающийся тем, что водный раствор помещают в реактор и при перемешивании добавляют серную кислоту при соотношении объема кислоты к объему раствора 1:2 с получением двойных сульфатов, их фильтрацию с получением твердой фазы и водной фазы, которую помещают в реактор, добавляют щелочь и перемешивают, полученную смесь отправляют на фильтрацию с получением водной фазы и твердой фазы в форме гидроксидов, которую переносят в реактор и добавляют азотную кислоту до полного ее растворения, с получением раствора, содержащего нитрат церия (III), к которому после добавления ПАВ добавляют хлорид натрия в количестве от 0,0025 до 0,25 моль/л, далее доводят рН от 3,0 до 7,0 путем добавления азотной кислоты, термостатируют при температуре от 20 до 25°С, добавляют изооктиловый спирт и перемешивают в течение не более 30 мин, при этом органическую фазу отделяют и проводят инфракрасный спектроскопический анализ на содержание катионов церия (III), после этого ее сушат в сушильном шкафу с получением оксида церия, а водную фазу анализируют фотометрическим методом на содержание катионов церия (III), при этом полученные значения концентраций катионов церия (III) используют при расчете степени его извлечения в органическую фазу, и отправляют водную фазу на утилизацию.
| LOBACHEVA O.L | |||
| et al | |||
| Solvent sublation of cerium ions from dilute aqueous solutions | |||
| Russian Chemical Bulletin, International Edition, Vol | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ гидрогенизации жиров, масел, жирных кислот из них и других непредельных органических соединений | 1913 |
|
SU962A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦЕРИЯ ИЗ РАСТВОРОВ СОЛЕЙ | 2011 |
|
RU2456359C1 |
| LOBACHEVA O.L | |||
| et al | |||
| Method for removing valuable components from technogenic solutions by the example of rare earth elements | |||
| Journal of | |||
Авторы
Даты
2024-08-06—Публикация
2023-12-18—Подача