ОБЛАСТЬ ТЕХНИКИ
[0001]
Настоящее изобретение относится к ингибитору фиброза для ткани после хирургической операции. Более конкретно, настоящее изобретение относится к ингибитору фиброза, характеризующемуся использованием биосовместимого полимера, который также может использоваться для ингибирования возникновения спаечного процесса в тканях.
УРОВЕНЬ ТЕХНИКИ
[0002]
Фиброз представляет собой явление, при котором соединительные ткани накапливаются в ткани, и он возникает в результате чрезмерного продуцирования и накопления в ткани соединительных тканей, таких как внеклеточный матрикс, в основном состоящий из коллагена. Фиброз наблюдается в сердце, легком, печени, поджелудочной железе, почке и т.п. Среди них, фиброз в сердце вызывает уплотнение сердечной мышцы и нарушает функцию сердца, хотя фиброз может препятствовать разрыву сердца после гибели клеток сердечной мышцы. Когда снижение функции сердца становится стойким, происходит увеличение сердца для компенсации снижения функции сердца. Таким образом, является довольно важным контроль фиброза. Когда физический стресс, такой как аутологичная ткань и искусственный объект или химическая реакция, воздействуют на поверхность органа, такую как эпикард (поверхность сердца), или ткани, на поверхности ткани возрастает образование волокон, что приводит к увеличению ткани в размере. В при повторной хирургической операции, в частности, при повторной операции на сердце, видимость эпикарда значительно ухудшается вследствие фиброза, ход коронарной артерии становится нечетким, и, таким образом, существует риск возникновения повреждения органа, такого как сердце или кровеносный сосуд, или ткани. Еще не был выявлен какой-либо ингибитор фиброза, который может удовлетворять потребностям хирургов. Таким образом, существует потребность в получении ингибитора фиброза, который может ингибировать фиброз поверхности органа или ткани, в частности, поверхности эпикарда.
[0003]
Помимо фиброза, другим риском, который может вызывать повреждение органа или ткани, является спаечный процесс в ткани после хирургической операции. Спаечный процесс в ткани после хирургической операции возникает в различных областях, включая кардиологию, а также хирургию пищеварительной системы, ортопедическую хирургию, гинекологию и акушерство, офтальмологию и т.п. Например, спаечный процесс в брюшной полости после абдоминальной хирургической операции является физиологической реакцией биологической репарации, и возникновение спаек трудно абсолютно предотвратить. Спаечный процесс, возникший после хирургической операции, с некоторой частотой вызывает адгезионную обструкцию кишечника. Полагают, что эта частота в некоторой степени пропорциональна длительности хирургической операции и степени кровотечения. Для предотвращения или снижения возникновения спаечного процесса требуется минимизация отслоения/кровотечения и длительности операции, чтобы предотвратить заражение в ходе операции, и минимизация остаточных чужеродных материалов путем аккуратного проведения хирургической операции хирургом, использование рассасывающихся шовных нитей, проведение надлежащего дренажа, предотвращение инфицирования, ранняя послеоперационная способность передвигаться и т.д. При неотложной операции с заражением также требуется проведение достаточного внутрибрюшинного промывания и изменение положения тела, и применение антибиотиков после операции. Однако, хотя эти контрмеры являются эффективными до некоторой степени в отношении предупреждения спаечной обструкции кишечника, является невозможным полностью предотвратить возникновение обструкции кишечника посредством этих контрмер (непатентный документ 1).
[0004]
Согласно последним исследованиям, предполагается, что: мезотелиальные клетки, которые представляют собой подобные пленки ткани, которые покрывают поверхность полости тела, такой как грудная полость, перикард и брюшную полость, продуцируют интерлейкин-6 в области операционного стресса; нейтрофилы продуцируют фактор некроза опухоли TNF-α и трансформирующий фактор роста TGF-β под действием интерлейкина-6; и мезотелиальные клетки вытесняются фиброзом под действием этого TGF-β, выступая в качестве основы для формирования спайки (непатентный документ 2).
[0005]
В области кардиологии спайка эпикарда со стенкой грудной клетки или спайка перикарда с эпикардом после хирургической операции повышает риск повреждения сердца или крупного кровеносного сосуда в ходе повторной хирургической операции (непатентный документ 3).
[0006]
При кардиологических хирургических операциях используют аутологичный перикард. Однако, когда закрытие не может быть достигнуто с использованием только аутологичного перикарда, используют различные типы заменителей перикарда. Примеры заменителя перикарда включают бычий перикард, покрытую силиконом полиэфирную ткань и лист политетрафторэтилена (PTFE) (непатентный документ 4).
[0007]
В области дефекта перикарда у человека после хирургической операции на открытом сердце, чтобы избежать возникновения повреждения сердца и крупного кровеносного сосуда в ходе тампонады сердца в острой послеоперационной фазе и стернотомии при повторной хирургической операции в поздней послеоперационной фазе, часто в качестве заменителя перикарда используют лист PTFE, имеющий толщину 0,1 мм. Результаты повторной хирургической операции в долговременной поздней послеоперационной фазе значительно отличаются от результатов, когда сердце покрывают аутологичным перикардом. Не рассасывающийся лист PTFE, который имеет структуру, в которую не может вторгаться биологическая ткань, может быть без труда удален в ходе повторной хирургической операции. Однако обе из обращенной к сердцу стороны и обращенной к грудине стороны листа PTFE покрываются фиброзными тканями в такой степени, что анатомическая структура каждой из фиброзных тканей не может быть подтверждена. В частности, в случае, когда обнаруживается нагрузка вследствие остаточного очага повреждения, возникает значительное утолщение фиброзных тканей. Когда широкую площадь поверхности сердца дополняют листом в ходе первоначальной хирургической операции, не удивительно, что наблюдают некоторую диастолическую недостаточность, даже если диагноз констриктивного перикардита (CP) не поставлен (непатентный документ 5). Более того, экспериментальные данные для этого случая также являются общеизвестными (непатентные документы 6-8).
[0008]
Когда лист PTFE трансплантируют в качестве заменителя перикарда, неизменно наблюдают признаки воспаления, индуцированного реакцией на чужеродное тело, воспалительная реакция становится выраженной через 4 недели после трансплантации и снижается через 12 недель после трансплантации. В результате трансплантации образуется очень толстая пленка соединительной ткани на обращенной к эпикарду стороне листа PTFE. Этот лист PTFE является пригодным, поскольку лист покрывает сердце и крупный кровеносный сосуд, так что сердце и крупный кровеносный сосуд не повреждаются в ходе стернотомии, которую проводят, когда повторная хирургическая операция становится необходимой. Однако в случае листа PTFF существует проблема влияния реакции на чужеродное тело в виде листа PTFE, когда повторная хирургическая операция не является необходимой, в частности, диастолической недостаточности, включающей CP. Когда лист PTFE удаляют, область, соединяемая листом, может быть отделена, и, таким образом, часто полагают, что лист PTFE редко вызывает воспаление окружающих тканей. Однако, на самом деле, лист PTFE вероятно будет вызывать воспалительную реакцию (непатентный документ 5). Более того, часто сообщают, что фиброз эпикарда, который вызывается листом PTFE, снижает видимость сердца (непатентный документ 9).
[0009]
Фиброз эпикарда индуцируется не только листом PTFE, но также случаем дефекта перикарда, когда проводят резекцию аутологичного перикарда, и случаем закрытия аутологичным перикардом. В эксперименте с использованием модели на кроликах описан рецидив фиброза в случае обширного закрытия политетрафторэтиленом (ePTFE) и в случае дефекта перикарда, где проводят резекцию аутологичного перикарда (непатентный документ 10). В эксперименте с использованием модели на собаках описано возникновение фиброза в случае закрытия ePTFE и в случае закрытия аутологичным перикардом (непатентный документ 11).
Между тем, также описан случай, где используют фибриновый клей, который представляет собой биологическое средство для склеивания тканей (непатентные документы 12 и 13). Однако фибриновый клей не может ингибировать спаечный процесс в тканях полностью (патентные документы 1-3), и, таким образом, серьезные проблемы, которые беспокоят хирургов, еще не решены.
[0010]
Децеллюляризованная биологическая ткань и децеллюляризованный орган (которые в совокупности называют далее в настоящем описании "децеллюляризованной тканью") представляют собой матрикс, получаемый путем удаления клеточных компонентов из биологической ткани или органа в организме человека или животного другого вида, и они привлекают внимание в качестве материала клеточного каркаса или материала, способствующего заживлению ран, который может использоваться для трансплантации или в регенеративной медицине. Компонент, отличный от клеток в биологической ткани, т.е. внеклеточный матрикс (ECM), является консервативным в отношении его структуры и состава среди видов организмов, и отчетливо обнаружено, что этот компонент не индуцирует иммунное отторжение среди практически всех видов организмов. Более того, также широко известно, что ECM вовлечен в дифференцировку клеток, и описано, что клетки, культивируемые на ECM в конкретной ткани, дифференцируются в клетки организма. Из этих данных, децеллюляризованная ткань, составляющая ECM, не подвергается иммунному отторжению после трансплантации и ожидается, что она будет регенерироваться клетками реципиента (непатентный документ 14).
ДОКУМЕНТЫ УРОВНЯ ТЕХНИКИ
ПАТЕНТНЫЕ ДОКУМЕНТЫ
[0011]
Патентный документ 1: JP-T-11-502431
Патентный документ 2: JP-A-2001-327592
Патентный документ 3: JP-T-2003-500170
Патентный документ 4: JP-4092397
Патентный документ 5: JP-A1-2008-111530
Патентный документ 6: JP-A-2009-50297
НЕПАТЕНТНЫЕ ДОКУМЕНТЫ
[0012]
Непатентный документ 1: Tsuneo Fukushima, et al., Surgical Therapy, 2006; 94(6):919-924
Непатентный документ 2: Uyama N. et al., Sci Rep. 2019; 26;9(1):17558
Непатентный документ 3: Dobell AR., et al., Ann Thorac Surg.1984; 37:273-8
Непатентный документ 4: Ozeren M. et al., Cardiovasc. Surg. 2002; 10(5):489-493
Непатентный документ 5: Tetsuya Kitagawa, PEDIATRIC CARDIOLOGY AND CARDIAC SURGERY. 2004; 20(6):632-633
Непатентный документ 6: Liermann A. et al., Helv Chir Acta. 1992; 58:515-519
Непатентный документ 7: Muralidharan S. et al., J Biomed Mater Res. 1991; 25:1201-1209
Непатентный документ 8: Bunton RW. et al., J Thorac Cardiovasc Surg. 1990; 100:99-107
Непатентный документ 9: Jukka T. et al., Interactive cardiovascular and thoracic surgery. 2011; 12(2):270-272
Непатентный документ 10: Kaushal S. et al., Thorac Cardiovasc Surg. 2011; 141:789-795
Непатентный документ 11: Naito Y. et al., J Thorac Cardiovasc Surg. 2008; 135:850-856
Непатентный документ 12: Takamichi Sato et al., Obstetrics and Gynecology, 1990; 57(12):2398-2404
Непатентный документ 13: Kiyoshi Okuda et al., The World of Obstetrics and Gynecology, 1993; 45(9):759-764
Непатентный документ 14: Akio Kishida, Organ Biology, 2018; 25(1):27-34
Непатентный документ 15: Singelyn J.M., et al., Biomaterials, 2009, 30, 5409-5416
Непатентный документ 16: Singelyn J.M,, et al., J. Am. Coll. Cardiol., 2012, 59, 751-763
Непатентный документ 17: Sonya B., et al., Sci. Transl. Med., 2013, 5, 173ra25
Непатентный документ 18: Sasaki S., et al., Mol. Vis., 2009, 15, 2022-2028
Непатентный документ 19: Yoshihide H., et al., Biomaterials, 2010, 31, 3941-3949
Непатентный документ 20: Seiichi F., et al., Biomaterials, 2010, 31, 3590-3595
Непатентный документ 21: Negishi J., et al., J. Artif. Organs, 2011, 14, 223-231
Непатентный документ 22: Hirashima M., et al., J. Biochem., 2016, 159, 261-270
Непатентный документ 23: Meta A., et al., J. Biosci. Bioeng, 2015, 120, 432-437
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ПРОБЛЕМЫ, РЕШАЕМЫЕ ИЗОБРЕТЕНИЕМ
[0013]
Проблемами, решаемыми настоящим изобретением, являются (1) ингибирование фиброза поверхности органа или ткани, в частности (2) ингибирование фиброза поверхности эпикарда, и они решаются предоставлением ингибитора фиброза, который может решить эти проблемы. Другой проблемой является предупреждение и снижение возникновения последующего спаечного процесса посредством ингибирования фиброза, чтобы избежать повреждения органа или ткани в ходе повторной хирургической операции.
РЕШЕНИЯ ПРОБЛЕМ
[0014]
Авторы настоящего изобретения провели обширные и тщательные исследования. В результате, авторы настоящего изобретения обнаружили ингибитор фиброза, посредством которого биосовместимый полимер фиксируют к ткани, фиброз которой подлежит ингибированию, тем самым вызывая ингибирование фиброза ткани, и они обнаружили, что ингибитор фиброза может решить указанные проблемы.
[0015]
Настоящее изобретение включает следующие аспекты:
(1) Ингибитор фиброза тканей, содержащий биосовместимый полимер.
(2) Ингибитор фиброза согласно (1), где биосовместимый полимер представляет собой фибрин или декстриновый гель.
(3) Набор для ингибирования фиброза тканей, содержащий комбинацию биосовместимого полимера и материала клеточного каркаса.
(4) Набор для ингибирования фиброза согласно (3), где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез для области дефекта ткани с использованием материала клеточного каркаса.
(5) Набор для ингибирования фиброза согласно (3) или (4), где биосовместимый полимер представляет собой фибрин или декстриновый гель.
(6) Набор для ингибирования фиброза согласно любому из (3)-(5), где материал клеточного каркаса представляет собой децеллюляризованную ткань.
(7) Набор для ингибирования фиброза согласно (6), где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда, мочевого пузыря, амниона, твердой мозговой оболочки, брюшины, большого сальника, грудной диафрагмы, фасции, дермы и кожи.
(8) Набор для ингибирования фиброза согласно любому из (3)-(7), который способствует самоорганизации материала клеточного каркаса.
(9) Набор для ингибирования фиброза согласно любому из (3)-(8), где ткань, фиброз которой подлежит ингибированию, представляет собой эпикард.
(10) Набор для ингибирования фиброза тканей, содержащий комбинацию биосовместимого полимера и заменителя перикарда.
(11) Набор для ингибирования фиброза согласно (10), где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез с использованием заменителя перикарда для области дефекта ткани.
(12) Набор для ингибирования фиброза согласно (10) или (11), где биосовместимый полимер представляет собой фибрин или декстриновый гель.
(13) Набор для ингибирования фиброза согласно любому из (10)-(12), где заменитель перикарда представляет собой децеллюляризованную ткань.
(14) Набор для ингибирования фиброза согласно (13), где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда, мочевого пузыря, амниона, твердой мозговой оболочки, брюшины, большого сальника, грудной диафрагмы, фасции, дермы и кожи.
(15) Набор для ингибирования фиброза согласно любому из (10)-(14), который способствует самоорганизации заменителя перикарда.
(16) Набор для ингибирования фиброза согласно любому из (10)-(15), где ткань, фиброз которой подлежит ингибированию, представляет собой перикард.
(17) Набор для предотвращения спаечного процесса, где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез с использованием материала клеточного каркаса или заменителя перикарда для области дефекта ткани.
(18) Набор для предотвращения спаечного процесса согласно (17), где биосовместимый полимер представляет собой фибрин или декстриновый гель.
(19) Набор для предотвращения спаечного процесса согласно (17), где материал клеточного каркаса или заменителя перикарда представляет собой децеллюляризованную ткань.
(20) Набор для предотвращения спаечного процесса согласно (19), где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда, мочевого пузыря, амниона, твердой мозговой оболочки, брюшины, большого сальника, грудной диафрагмы, фасции, дермы и кожи.
(21) Набор для предотвращения спаечного процесса согласно любому из (17)-(20), который способствует самоорганизации материала клеточного каркаса или заменителя перикарда.
(22) Набор для предотвращения спаечного процесса согласно любому из (17)-(21), где ткань, подлежащая ингибированию спаечного процесса, представляет собой эпикард.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[0016]
Ингибитор фиброза в соответствии с настоящим изобретением имеет эффект ингибирования фиброза поверхности органа или ткани. Ингибитор фиброза по настоящему изобретению ингибирует фиброз поверхности органа или ткани, в частности, поверхности эпикарда, для повышения видимости эпикарда, и, тем самым, он может снижать повреждения сердца или кровеносного сосуда в ходе повторной хирургической операции. Более того, ингибитор фиброза по настоящему изобретению может ингибировать воспалительную реакцию, которая индуцирует фиброз. Таким образом, также ожидается, что ингибитор фиброза будет иметь эффект снижения спаечного процесса, ассоциированного с воспалительной реакцией, и может использоваться как ингибитор спаечного процесса.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0017]
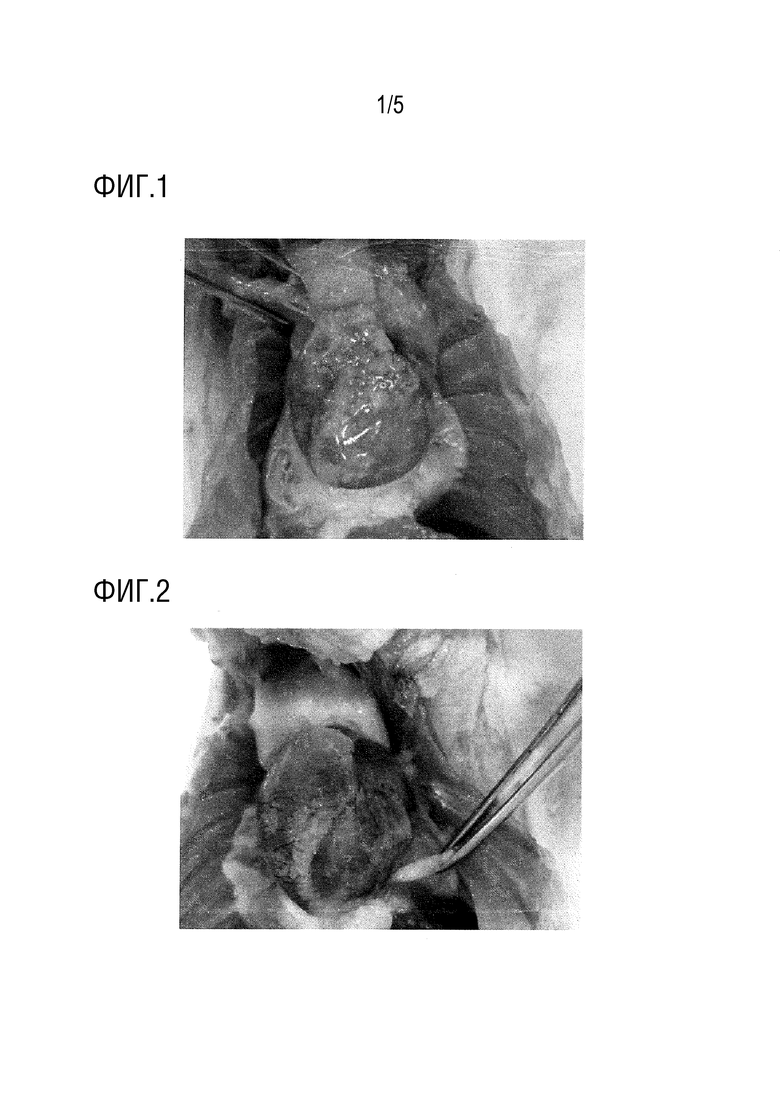
На фиг.1 представлена фотография, демонстрирующая оценку модели фиброза сердца кролика (группа ингибитора фиброза) после наблюдения в течение трех месяцев.
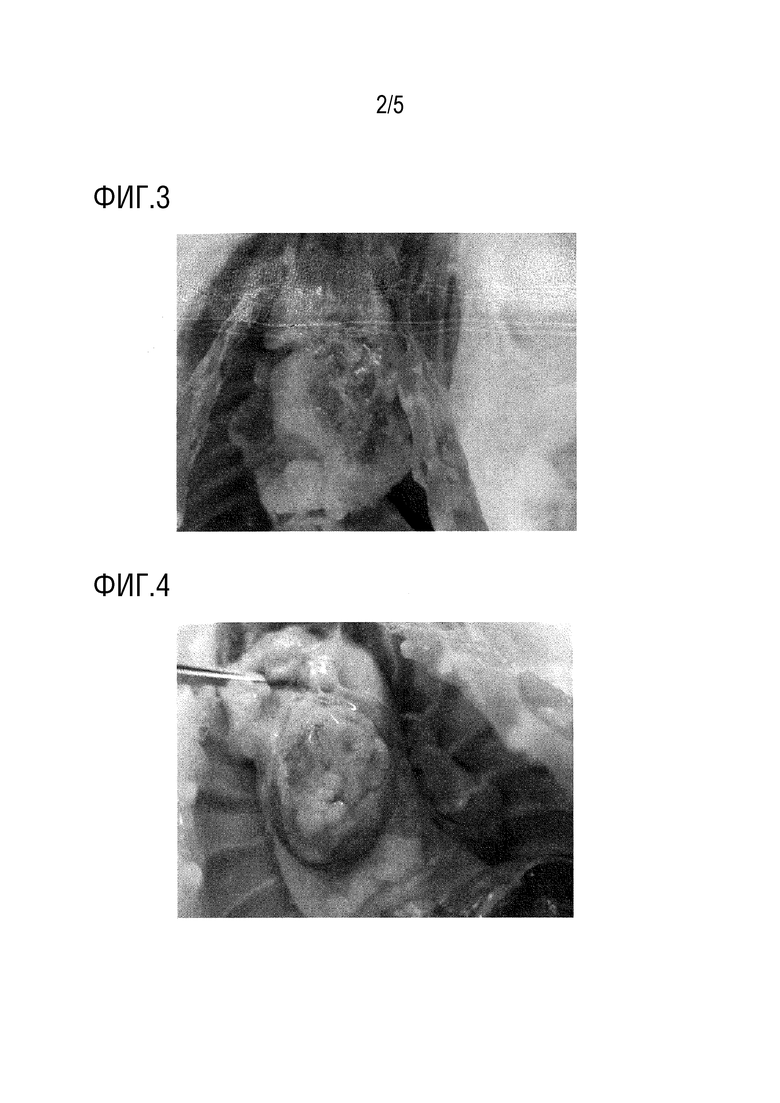
На фиг.2 представлена фотография, демонстрирующая оценку модели фиброза сердца кролика (группа набора ингибирования фиброза) после наблюдения в течение трех месяцев.
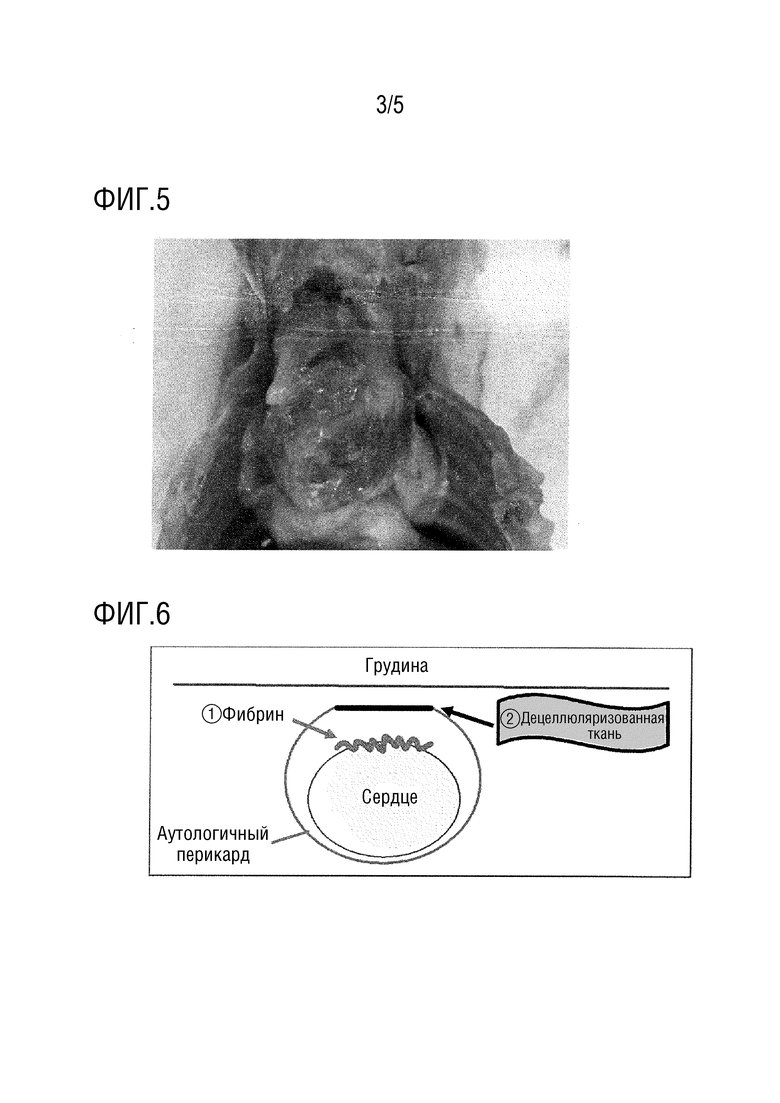
На фиг.3 представляет собой фотографию, демонстрирующую оценку модели фиброза сердца кролика (контрольная группа/дефект перикарда) после наблюдения в течение трех месяцев.
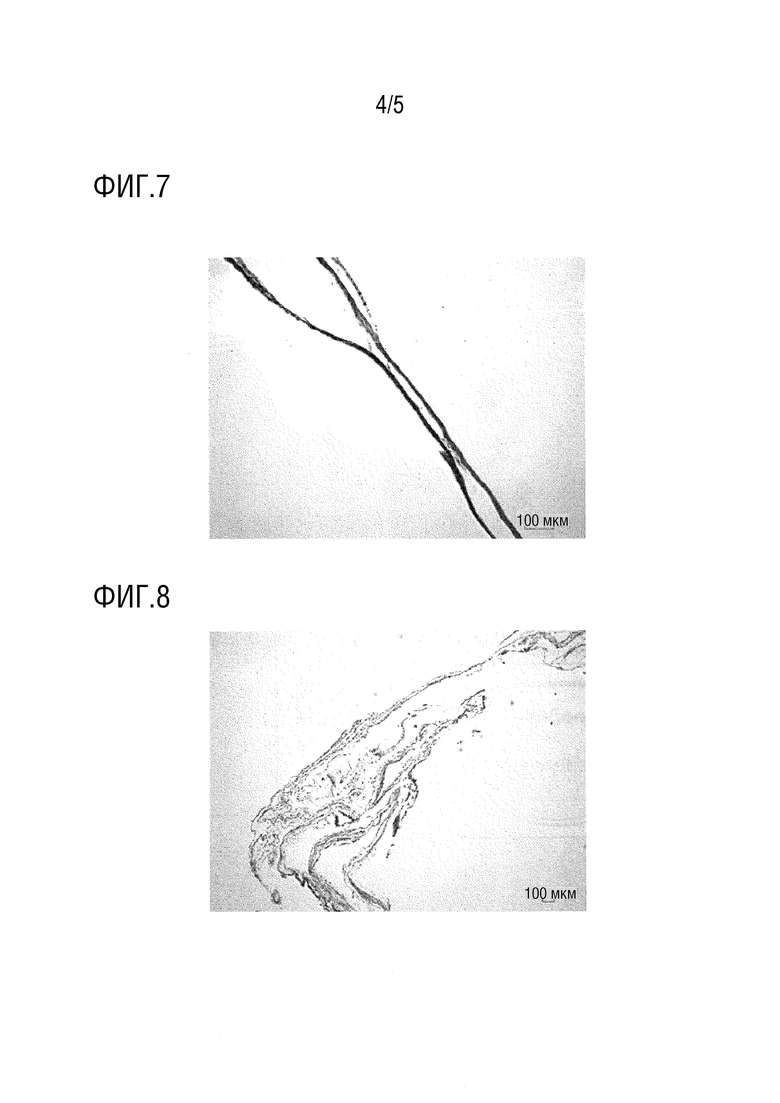
На фиг.4 представлена фотография, демонстрирующая оценку модели фиброза сердца кролика (контрольная группа/закрытие аутологичным перикардом) после наблюдения в течение трех месяцев.
На фиг.5 представлена фотография, демонстрирующая оценку модель фиброза сердца кролика (группа только децеллюляризованной ткани) после наблюдения в течение трех месяцев.
На фиг.6 представлен пример способа с использованием набора для ингибирования фиброза и набора для предотвращения спаечного процесса (случай, где (1) фибрин наносят и фиксируют к эпикарду в сердце, а затем (2) децеллюляризованную ткань пришивают и фиксируют к области дефекта перикарда, находящейся между эпикардом и грудиной).
На фиг.7 представлена фотография, демонстрирующая патологию в модели на сердце кролика (группа набора для ингибирования фиброза и набора для предотвращения спаечного процесса) после наблюдения в течение трех месяцев.
На фиг.8 представлена фотография, демонстрирующая патологию в модели на сердце кролика (группа только децеллюляризованной ткани) после наблюдения в течение трех месяцев.
На фиг.9 представлена фотография, демонстрирующая патологию в модели на сердце кролика (группа комплекса фибрин-(децеллюляризованная ткань)) после наблюдения в течение трех месяцев.
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0018]
Настоящее изобретение относится к: биосовместимому полимеру, который может использоваться в качестве ингибитора фиброза; и материалу клеточного каркаса.
[0019]
Термин "биосовместимый полимер", как используют в рамках изобретения, относится к полимеру, который демонстрирует меньшие иммунные реакции in vivo. Примеры биосовместимого полимера включают, но не ограничиваются ими, альгиновую кислоту, хитин, хитозан, гликозаминогликан, коллаген, хондроитинсульфат, целлюлозу, желатин, декстран, декстрин, гликопротеин, гиалуроновую кислоту, фибриноген, фибрин, фибронектин, гепарин и гепаран. В качестве биосовместимого полимера, особенно предпочтительным является фибрин или декстриновый гель.
[0020]
Термин "материал клеточного каркаса", как используют в рамках изобретения, относится к материалу, который способствует адгезии/пролиферации клеток.
[0021]
Децеллюляризованная ткань может быть получена путем получения биологической ткани от животного (донора), а затем проведения обработки для децеллюляризации биологической ткани. Путем проведения обработки для децеллюляризации биологической ткани из биологической ткани могут быть удалены клетки или патогены (вирусы, бактерии) из донора. В результате, даже когда биологическую ткань трансплантируют животному вида, отличного от донора, возникновение гетерологичной иммунной реакции может ингибироваться. По этим причинам тип животного, из которого может быть получена биологическая ткань, конкретно не ограничен. Между тем, является предпочтительным легкое получение биологической ткани. Таким образом, животное предпочтительно является не являющимся человеком животным, особенно предпочтительно домашними млекопитающими или домашними птицами. Примеры домашних млекопитающих включают крупный рогатый скот, лошадь, верблюда, ламу, осла, яка, овцу, свинью, козу, оленя, альпаку, собаку, енотовидную собаку, горностая, лису, кошку, кролика, хомячка, морскую свинку, крысу, белку и енота. Примеры домашних птиц включают мелкого попугайчика, попугая, курицу, утку, индейку, гуся, цесарку, фазана, страуса и перепела. Среди этих животных, с точки зрения доступности, предпочтительной является свинья.
[0022]
Примером биологической ткани является ткань, которая имеет структуру внеклеточного матрикса и может быть подвергнута обработке для децеллюляризации. Примером этой ткани является ткань, выбранная из группы, состоящей из подслизистой оболочки тонкого кишечника, мочевого пузыря, амниона, твердой мозговой оболочки, брюшины, грудной диафрагмы, фасции, дермы, кожи, печени, почки, мочевыводящих путей, уретры, языка, миндалевидной железы, пищевода, желудка, большого сальника, тонкого кишечника, толстого кишечника, ануса, поджелудочной железы, сердца, перикарда, кровеносного сосуда, селезенки, легкого, головного мозга, кости, спинного мозга, хряща, семенника, матки, маточной трубы, яичника, плаценты, роговицы, скелетной мышцы, сухожилия, нерва и т.п. Когда децеллюляризованная ткань имеет подобную листу форму, децеллюляризованная ткань может быть без труда применена в живом организме. Таким образом, одним предпочтительным примером ткани является ткань, выбранная из группы, состоящей из подслизистой оболочки тонкого кишечника, мочевого пузыря, амниона, твердой мозговой оболочки, брюшины, большого сальника, грудной диафрагмы, фасции, дермы и кожи. Децеллюляризованная ткань, которая не имеет подобной листу формы, является неприемлемой, поскольку децеллюляризованная ткань должна быть преобразована в подобную листу форму.
[0023]
В качестве способа сбора биологической ткани из животного можно использовать способ, походящий для вида животного донора или биологической ткани. Биологическую ткань, полученную от животного, подвергают обработке для децеллюляризации. Обработка для децеллюляризации конкретно не ограничена при условии, что клетки или патогены, происходящие из донора, могут быть удалены. Примеры способа включают обработку поверхностно-активным веществом (непатентные документы 15-21, патентные документы 4-6), и способ может быть выбран соответствующим образом в зависимости от вида животного донора и типа биологической ткани.
[0024]
Когда биосовместимый полимер комбинируют с децеллюляризованной тканью, фиксирование биосовместимого полимера к ткани, фиброз которой подлежит ингибированию, может быть достигнуто путем собственного гелеобразования биосовместимого полимера. Примеры способа фиксации фибрина, который является одним из биосовместимых полимеров, включают: способ, при котором фибрин фиксируют к ткани, фиброз которой подлежит ингибированию, путем нанесения фибрина на ткань; и способ, при котором фибрин фиксируют к ткани путем распыления порошка, который представляет собой составляющий компонент фибрина (порошок фибриногена, порошок тромбина) на ткань. Например, когда перикард повреждается в ходе хирургической операции на сердце, фиброз эпикарда и т.п. становится проблемой. Для ингибирования фиброза эпикарда в качестве примера фибрин фиксируют на эпикарде, в то время как децеллюляризованную ткань пришивают и фиксируют на аутологичном перикарде, который остается для цели снижения контакта с грудиной. Фибрин фиксируют на ткани, фиброз которой подлежит ингибированию, более конкретно эпикарде, в то время как для области дефекта перикарда, находящейся между эпикардом и грудиной создают протез с использованием децеллюляризованной ткани. Таким образом, может быть достигнут эффект в качестве набора для ингибирования фиброза. При фиксации фибрина может быть возможным нанесение либо одного из фибриногена или тромбина сначала, а затем нанесение другого, или также может быть возможным нанесение обоих из них одновременно. Также может быть выбрано применение путем распыления с использованием устройства для распыления. Фиксация фибрина завершается, когда наблюдают небольшое помутнение прозрачного геля. Примером ткани, фиброз которой подлежит ингибированию, является эпикард, как упоминалось выше. Однако примеры ткани не ограничиваются эпикардом. Полагают, что в дополнение к эпикарду возникновение фиброза может ингибироваться в ткани легкого и т.п.
[0025]
Концентрация фибриногена или тромбина в момент применения фибрина конкретно не ограничена при условии, что фибрин может образовываться. Например, концентрация фибриногена составляет от 4 мг/мл до 160 мг/мл, предпочтительно от 10 мг/мл до 80 мг/мл. Например, концентрация тромбина составляет от 1 Е/мл до 1200 Е/мл, предпочтительно от 60 Е/мл до 600 Е/мл.
[0026]
Фибрин представляет собой похожий на клей коагулят, образованный в результате взаимодействия фибриногена с тромбином, который является ферментом, и он представляет собой лекарственный продукт, который может использоваться для закрытия ткани, склеивания поврежденной области в органе, остановки кровотечения и т.п. Тип фибрина конкретно не ограничен, и он может представлять собой фибрин, в котором составляющие компоненты, такие как фибриноген и тромбин, происходят из крови или могут быть получены способом рекомбинации. Предпочтительным примером является BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.).
[0027]
Настоящее изобретение также относится к набору для ингибирования фиброза, в котором фибрин и децеллюляризованная ткань получены по отдельности. Этот набор составлен так, чтобы врач использовал фибрин и децеллюляризованную ткань при применении. Когда децеллюляризованная ткань является лиофилизированной, децеллюляризованную ткань пропитывают растворителем для восстановления децеллюляризованной ткани и восстановленную децеллюляризованную ткань применяют на пораженной области. Таким образом, набор может включать растворитель применения с восстановлением.
[0028]
Животное, используемое для модели фиброза сердца, конкретно не ограничено и предпочтительно представляет собой кролика, более предпочтительно японского белого кролика в возрасте 5-6 месяцев. При создании модели грудную клетку животного открывают путем разреза под анестезией, а затем металлический распатор приводят в контакт с сердцем или эпикардом. Длительность контакта с металлическим распатором конкретно не ограничена и составляет, например, от 10 до 20 минут. После воздействия металлического распатора сердце можно сушить сушкой (путем подачи воздуха).
[0029]
Примером способа оценки ингибирования фиброза является оценка путем визуального изучения. Например, в случае оценки ингибирования фиброза в эпикарде оценку можно проводить путем оценки в качестве степени фиброза 0 (фиброз не наблюдается), степени фиброза 1 (перикард может визуально наблюдаться) и степени фиброза 2 (эпикард не может визуально наблюдаться). В этом способе оценки определение может быть проведено в зависимости от того, могут ли визуально наблюдаться кровеносные сосуды эпикарда. Когда эпикард является побелевшим и кровеносные сосуды не могут наблюдаться, может быть определено, что фиброз не ингибируется удовлетворительным образом. Кроме того, также можно предпочтительно использовать способ, в котором область с фиброзом степени 2 сравнивают с контрольной группой для оценки эффекта ингибирования фиброза.
[0030]
Формулировка "самоорганизация материала клеточного каркаса или заменителя перикарда", как используют в рамках изобретения, относится к реконструированию искусственного материала и т.п. в ткань, подобную аутогенной ткани, со сниженной иммунной реакцией после трансплантации искусственного материала и т.п. в живой организм.
ПРИМЕРЫ
[0031]
Далее в настоящем описании настоящее изобретение описано более подробно с помощью примеров, которые, однако, никоим образом не предназначены для ограничения объема настоящего изобретения.
ПРИМЕР 1
[0032]
Эффект ингибирования фиброза посредством ингибитора фиброза и набора для ингибирования фиброза:
В качестве децеллюляризованных тканей использовали децеллюляризованную подслизистую оболочку тонкого кишечника свиньи, децеллюляризованную фетальную кожу кролика и децеллюляризованный перикард кролика.
[0033]
В качестве биосовместимого полимера использовали фибрин. Что касается происходящего из крови фибрина, раствор фибриногена получали с использованием лиофилизированного порошка фибриногена и раствора фибриногена в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Раствор тромбина получали с использованием лиофилизированного порошка тромбина и раствора тромбина в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Рекомбинантный фибрин получали с использованием рекомбинантного фибриногена (непатентный документ 22) и рекомбинантного тромбина (непатентный документ 23), оба из которых были произведены способами генной инженерии в KM Biologics Co., Ltd. В качестве декстринового геля использовали AdSpray (зарегистрированный торговый знак, Terumo Corporation). Завершение фиксации фибрина подтверждали, когда прозрачный гель становился немного замутненным, и завершение фиксации декстрина подтверждали, когда образовывался белый гель, содержавший микропузырьки.
[0034]
Модель фиброза сердца создавали с использованием самцов японского белого кролика в возрасте 5-6 месяцев. Эндотрахеальную трубку устанавливали в трахею под анестезией ксилазином и кетамина гидрохлоридом, а затем соединяли с дыхательным аппаратом. Часть (5 см) грудины разрезали в области выемок хрящей со второго по пятое ребра. Перикард (2,0 см × 1,5 см) непосредственно ниже разрезанной части грудной клетки разрезали. Эпикард приводили в контакт с металлическим распатором на 10 минут. Грудину и кожу раны грудной клетке с надрезом зашивали и закрывали. Считалось, что надлежащим временем для оценки было время после окончания воспаления ткани и завершения фиброза. Затем проводили долговременную оценку так, что животное содержали в обычных условиях в течение 3 месяцев, а затем подвергали разрезу грудной клетки и степень фиброза эпикарда оценивали невооруженным глазом.
Фиброз оценивали в соответствии со следующими критериями:
Степень фиброза 0: фиброз не наблюдался.
Степень фиброза 1: эпикард мог визуально наблюдаться.
Степень фиброза 2: эпикард не мог визуально наблюдаться.
Эффект ингибирования фиброза наблюдали путем сравнения площади фиброза степени 2 с контрольной группой. Область (%) фиброза степени 2 вычисляли по формуле:
(площадь фиброза степени 2)/(площадь области дефекта перикарда) × 100.
[0035]
В примере 1 следующие тестовые группы сравнивали и оценивали.
(1) Группа ингибитора фиброза (происходящий из крови фибрин),
(2) группа набора для ингибирования фиброза (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(3) группа набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(4) группа набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика),
(5) группа набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованный перикард кролика),
(6) группа набора для ингибирования фиброза (декстриновый гель и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(7) контрольная группа (дефект перикарда),
(8) контрольная группа (закрытие аутологичным перикардом),
(9) группа только децеллюляризованной ткани (децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(10) группа комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи).
[0036]
Группы (1)-(6) представляли собой группы по изобретению, и группы (7)-(10) представляли собой контрольные группы. Что касается способа применения фибрина для (1)-(5), раствор фибриногена и раствор тромбина смешивали и полученную смесь наносили на эпикард в области дефекта перикарда с использованием устройства для нанесения, где конечные концентрации раствора фибриногена и раствора тромбина составляли 40 мг/мл и 125 Е/мл, соответственно, и нанесенные растворы фиксировали. Способ получения декстринового геля и способ нанесения декстринового геля для (6) проводили, как описано на вкладыше в упаковку для AdSpray. Что касается способа нанесения децеллюляризованной ткани для (2)-(6) и (9), децеллюляризованную ткань зашивали и фиксировали (протез) к остальной части аутологичного перикарда таким образом, чтобы децеллюляризованная ткань была фиксирована к области дефекта перикарда, находящейся между эпикардом и грудиной. Что касается порядка применения для (2)-(6), фибрин или декстриновый гель фиксировали на эпикарде, а затем децеллюляризованную ткань пришивали и фиксировали (протез) к аутологичному перикарду. Группы (7)-(10) представляли собой группы, в каждой из которых не применяли ингибитор фиброза. Группа (10) представляла собой группу, в которой фибрин был в комплексе с децеллюляризованной тканью. Раствор фибриногена и раствор тромбина смешивали и полученную смесь наносили на обе поверхности децеллюляризованной ткани для образования комплекса между этими компонентами, и полученный продукт пришивали и фиксировали (протез) к оставшемуся аутологичному перикарду таким образом, чтобы полученный продукт фиксировался на области дефекта перикарда, находящейся между эпикардом и грудиной. Результаты оценки представлены в таблице 1.
[0037]
[Таблица 1]
[0038]
Как видно из вышеуказанных результатов, превосходный эффект ингибирования фиброза подтверждался, когда использовали ингибиторы фиброза и наборы для ингибирования фиброза, которые были продуктами по настоящему изобретению. Для каждого из ингибиторов фиброза по настоящему изобретению было подтверждено значимое отличие (p < 0,01) посредством критерия суммы рангов Уилкоксона, когда (3) группу набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (7) контрольной группой (дефект перикарда). Когда каждую из (1) группы ингибитора фиброза (происходящий из крови фибрин), (2) группы набора для ингибирования фиброза (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи), (4) группы набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика) и (5) группы набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованный перикард кролика) сравнивали с (7) контрольной группой (дефект перикарда), было подтверждено значимое отличие (p < 0,05). Когда (3) группу набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (8) контрольной группой (закрытие аутологичным перикардом), было подтверждено значимое отличие (p < 0,05). Когда каждую из (2) группы набора для ингибирования фиброза (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи), (3) группы набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи), (4) группы набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика) и (5) группы набора для ингибирования фиброза (рекомбинантный фибрин и децеллюляризованный перикард кролика) сравнивали с (10) группой комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи), было подтверждено значимое отличие (p < 0,01). Когда каждую из (1) группы ингибитора фиброза (происходящий из крови фибрин) и (6) группы набора для ингибирования фиброза (декстриновый гель и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (10) группой комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи), было подтверждено значимое отличие (p < 0,05).
ПРИМЕР 2
[0039]
Эффект ингибирования спаечного процесса посредством набора для предотвращения спаечного процесса:
В качестве децеллюляризованных тканей использовали децеллюляризованную подслизистую оболочку тонкого кишечника свиньи, децеллюляризованную фетальную кожу кролика и децеллюляризованный перикард кролика.
[0040]
В качестве биосовместимого полимера использовали фибрин. Что касается происходящего из крови фибрина, раствор фибриногена получали с использованием лиофилизированного порошка фибриногена и раствора фибриногена в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Раствор тромбина получали с использованием лиофилизированного порошка тромбина и раствора тромбина в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Рекомбинантный фибрин получали с использованием рекомбинантного фибриногена (непатентный документ 22) и рекомбинантного тромбина (непатентный документ 23), оба из которых были произведены способами генной инженерии в KM Biologics Co., Ltd. В качестве декстринового геля использовали AdSpray (зарегистрированный торговый знак, Terumo Corporation). Завершение фиксации фибрина подтверждали, когда прозрачный гель становился немного замутненным, и завершение фиксации декстрина подтверждали, когда образовывался белый гель, содержавший микропузырьки.
[0041]
Модель спаечного процесса сердечной ткани создавали с использованием самцов японского белого кролика в возрасте 5-6 месяцев. Эндотрахеальную трубку устанавливали в трахею под анестезией ксилазином и кетамина гидрохлоридом, а затем соединяли с дыхательным аппаратом. Часть (5 см) грудины разрезали в области выемок хрящей со второго по пятое ребра. Перикард (2,0 см × 1,5 см) непосредственно ниже разрезанной части грудной клетки разрезали. Эпикард приводили в контакт с металлическим распатором на 10 минут. Грудину, ребра, мышцу и кожу раны грудной клетке с надрезом зашивали и закрывали. Считалось, что надлежащим временем для оценки было время после окончания воспаления ткани и завершения спаечного процесса. Затем проводили долговременную оценку так, что животное содержали в обычных условиях в течение 3 месяцев, а затем подвергали разрезу грудной клетки и степень спаечного процесса поврежденной области эпикарда оценивали невооруженным глазом.
[0042]
Спаечный процесс оценивали в соответствии с критериями, представленными ниже, в зависимости от уровня отделения спайки в поврежденной области эпикарда.
Спаечный процесс степени 0: отсутствие спаек
Спаечный процесс степени 1: мягкие спайки (спайки, которые не требуют тупой диссекции для разделения пространства между реконструированным перикардом и грудиной и эпикардом).
Спаечный процесс степени 2: умеренные спайки (спайки, требующие тупой диссекции для разделения пространства между реконструированным перикардом и грудиной или эпикардом).
Спаечный процесс степени 3: тяжелые спайки (спайки, требующие острой диссекции для разделения пространства между реконструированным перикардом и грудиной или эпикардом).
Эффект ингибирования спаечного процесса определяли путем сравнения области в эпикарде, которая имела степень 0 спаечного процесса, и области в эпикарде, которая имела степени 3 спаечного процесса, с контрольными группами. область (%) в эпикарде, которая имела степень 0 спаечного процесса, вычисляли в соответствии с формулой:
(площадь эпикарда, которая имел степень 0 спаечного процесса)/(площадь области дефекта перикарда) × 100.
Область (%) в эпикарде, которая имела степень 3 спаечного процесса, вычисляли в соответствии с формулой:
(площадь эпикарда, которая имела степень 3 спаечного процесса)/(площадь области дефекта перикарда) × 100.
[0043]
В примере 2 следующие тестовые группы сравнивали и оценивали.
(1) Группа набора для предотвращения спаечного процесса (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(2) группа набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(3) группа набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика),
(4) группа набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованный перикард кролика),
(5) группа набора для предотвращения спаечного процесса (декстриновый гель и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(6) контрольная группа (дефект перикарда),
(7) контрольная группа (закрытие аутологичным перикардом),
(8) группа комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи).
[0044]
Группы (1)-(5) представляли собой группы по изобретению, и группы (6)-(8) представляли собой контрольные группы. Что касается способа применения фибрина для (1)-(4), раствор фибриногена и раствор тромбина смешивали и полученную смесь наносили и фиксировали на эпикарде в области дефекта перикарда с использованием устройства для нанесения, где конечные концентрации раствора фибриногена и раствора тромбина составляли 40 мг/мл и 125 Е/мл, соответственно. Способ получения декстринового геля и способ нанесения для (5) проводили, как описано на вкладыше в упаковку для AdSpray. Что касается способа применения децеллюляризованной ткани для (1)-(5), децеллюляризованную ткань пришивали и фиксировали (протез) к оставшемуся аутологичному перикарду, так чтобы она была фиксирована к области дефекта перикарда, находящейся между эпикардом и грудиной. Что касается порядка применения для (1)-(5), фибрин или декстриновый гель фиксировали на эпикарде, а затем децеллюляризованную ткань пришивали и фиксировали к аутологичному перикарду. Группы (6)-(8) представляли собой группы, в каждой из которых не применяли набор для предотвращения спаечного процесса. Группа (8) представляла собой группу, в который фибрин был в комплексе с децеллюляризованной тканью. Раствор фибриногена и раствор тромбина смешивали и полученную смесь наносили на обе поверхности децеллюляризованной ткани для образования комплекса между этими компонентами, и полученный продукт пришивали и фиксировали (протез) к оставшемуся аутологичному перикарду таким образом, чтобы полученный продукт фиксировался к области дефекта перикарда, находящейся между эпикардом и грудиной. Результаты оценки представлены в таблице 2.
[0045]
[Таблица 2]
[0046]
Как видно из вышеупомянутых результатов, когда использовали наборы для предотвращения спаечного процесса, которые представляли собой продукты по настоящему изобретению, был подтвержден долговременный превосходный эффект ингибирования спаечного процесса. Сравнивали области (%) степени 0 спаечного процесса в эпикарде. В результате было подтверждено значимое отличие (p < 0,01) для набора для предотвращения спаечного процесса по настоящему изобретению посредством критерия суммы рангов Уилкоксона, когда проводили сравнение между (3) группой набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика) с (6) контрольной группой (дефект перикарда). Когда каждую из (1) группы набора для предотвращения спаечного процесса (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) и (2) группы набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (6) контрольной группой (дефект перикарда), было подтверждено значимое отличие (p < 0,05). Когда (3) группу набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика) сравнивали с (7) контрольной группой (закрытие аутологичным перикардом), было подтверждено значимое отличие (p < 0,05). Когда каждую из (1) группы набора для предотвращения спаечного процесса (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) и (2) группы набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (8) группой комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи), было подтверждено значимое отличие (p < 0,05). Проводили сравнение областей (%) степени 3 спаечного процесса. В результате, значимое отличие (p < 0,01) было подтверждено для наборов для предотвращения спаечного процесса по настоящему изобретению посредством критерия суммы рангов Уилкоксона, когда каждую из (1) группы набора для предотвращения спаечного процесса (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи), (2) группы набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи), (3) группы набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная фетальная кожа кролика), (4) группы набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованный эпикард кролика) и (5) группы набора для предотвращения спаечного процесса (декстриновый гель и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (6) контрольной группой (дефект перикарда). Когда (2) группу набора для предотвращения спаечного процесса (рекомбинантный фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи) сравнивали с (7) контрольной группой (закрытие аутологичным перикардом), было подтверждено значимое отличие (p < 0,05).
ПРИМЕР 3
[0047]
Способствование самоорганизации децеллюляризованной ткани посредством набора для ингибирования фиброза и набора для предотвращения спаечного процесса:
В качестве децеллюляризованной ткани использовали децеллюляризованную подслизистую оболочку тонкого кишечника свиньи.
[0048]
В качестве биосовместимого полимера использовали фибрин. Что касается происходящего из крови фибрина, раствор фибриногена получали с использованием лиофилизированного порошка фибриногена и раствора фибриногена в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Раствор тромбина получали с использованием лиофилизированного порошка тромбина и раствора тромбина в BOLHEAL для склеивания тканей (зарегистрированный торговый знак, KM Biologics Co., Ltd.). Рекомбинантный фибрин получали с использованием рекомбинантного фибриногена (непатентный документ 22) и рекомбинантного тромбина (непатентный документ 23), оба из которых были произведены способами генной инженерии в KM Biologics Co., Ltd. В качестве декстринового геля использовали AdSpray (зарегистрированный торговый знак, Terumo Corporation). Завершение фиксации фибрина подтверждали, когда прозрачный гель становился немного замутненным, и завершение фиксации декстрина подтверждали, когда образовывался белый гель, содержавший микропузырьки.
[0049]
Самоорганизацию децеллюляризованной ткани оценивали с использованием модели на сердце кролика. Использовали самцов японского белого кролика в возрасте 5-6 месяцев. Эндотрахеальную трубку устанавливали в трахею под анестезией ксилазином и кетамина гидрохлоридом, а затем соединяли с дыхательным аппаратом. Часть (5 см) грудины разрезали в области выемок хрящей со второго по пятое ребра. Перикард (2,0 см × 1,5 см) непосредственно ниже разрезанной части грудной клетки разрезали. Эпикард приводили в контакт с металлическим распатором на 10 минут. Грудину, ребра, мышцу и кожу раны грудной клетке с надрезом зашивали и закрывали. Для долговременной оценки кролика содержали в обычных условиях в течение 3 месяцев, а затем подвергали разрезу, который открывал грудную клетку, для извлечения децеллюляризованной ткани. Проводили оценку прочности децеллюляризованной ткани, разрывов децеллюляризованной ткани при извлечении. Частоту возникновения разрывов (%) вычисляли по следующей формуле:
(количество индивидуумов, у которых произошел разрыв децеллюляризованной ткани при извлечении)/(количество индивидуумов в каждой тестируемой группе) × 100.
Получали гистопатологический образец извлеченной децеллюляризованной ткани, а затем подвергали окрашиванию HE. Таким образом, оценивали степень самоорганизации. Фотографии патологии для результатов представлены на фиг.7-9.
[0050]
В примере 3 оценивали следующие тестируемые группы.
(1) Группа ингибирования фиброза и набора для предотвращения спаечного процесса (происходящий из крови фибрин и децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(2) группа только децеллюляризованной ткани (децеллюляризованная подслизистая оболочка тонкого кишечника свиньи),
(3) группа комплекса фибрин-децеллюляризованная ткань (происходящий из крови фибрин был в комплексе с децеллюляризованной подслизистой оболочкой тонкого кишечника свиньи).
Что касается способа применения децеллюляризованной ткани в (1) и (2), децеллюляризованную ткань пришивали и фиксировали (протез) к оставшемуся аутологичному перикарду, так что децеллюляризованная ткань фиксировалась к области дефекта перикарда, находящейся между эпикардом и грудиной. Группа (3) представляла собой группу, в которой фибрин был в комплексе с децеллюляризованной тканью. Комплексный продукт пришивали и фиксировали (протез) к оставшемуся аутологичному перикарду таким образом, чтобы комплексный продукт был фиксирован к области дефекта перикарда, находящейся между эпикардом и грудиной. Результаты оценки представлены в таблице 3.
[0051]
[Таблица 3]
[0052]
Как понятно из вышеупомянутых результатов, было подтверждено, что набор для ингибирования фиброза и для предотвращения спаечного процесса, который представлял собой продукт по настоящему изобретению, может способствовать самоорганизации децеллюляризованной ткани для реконструирования аутологичной подобной перикарду ткани, имеющей надлежащую прочность.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
[0053]
Настоящее изобретение может использоваться в качестве ингибитора фиброза для поверхности органа или ткани, и также может использоваться для ингибирования спаечного процесса в тканях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВОССТАНОВЛЕНИЯ СВЯЗКИ ИЛИ СУХОЖИЛИЯ | 2013 |
|
RU2629809C2 |
| СПОСОБ ОБЕСПЕЧЕНИЯ УЛУЧШЕННОГО УПЛОТНЕНИЯ С ПОМОЩЬЮ ФИБРИНА | 2011 |
|
RU2556960C2 |
| Композиция для профилактики рубцово-спаечных осложнений в кардиохирургии и способ её применения | 2023 |
|
RU2836397C2 |
| СПОСОБ РЕГЕНЕРАЦИИ ТКАНИ | 2004 |
|
RU2542391C2 |
| СПОСОБ РЕГЕНЕРАЦИИ ТКАНИ | 2004 |
|
RU2392314C2 |
| УМЕНЬШЕНИЕ ОБЪЕМА ТКАНИ | 2000 |
|
RU2308967C2 |
| Способ изготовления аутологичного фибрина с регулируемым содержанием фибриногена без использования экзогенного тромбина | 2020 |
|
RU2758260C1 |
| СПОСОБ ФОРМИРОВАНИЯ ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА | 2008 |
|
RU2364353C1 |
| ТВЕРДАЯ ПОВЯЗКА ДЛЯ ЛЕЧЕНИЯ ТРАВМИРОВАННОЙ ТКАНИ | 2007 |
|
RU2480191C2 |
| БИОИНЖЕНЕРНЫЙ КОЛЛАГЕНОВЫЙ КОНСТРУКТ, МОДИФИЦИРОВАННЫЙ КИШЕЧНЫЙ КОЛЛАГЕНОВЫЙ СЛОЙ, ПЕРЕРАБОТАННЫЙ ТКАНЕВЫЙ МАТРИКС И СПОСОБ ВОССТАНОВЛЕНИЯ ИЛИ ЗАМЕЩЕНИЯ ПОВРЕЖДЕННОЙ ТКАНИ | 2006 |
|
RU2481114C2 |

Группа изобретений относится к способу ингибирования фиброза тканей, включающему применение биосовместимого полимера и материала клеточного каркаса, где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез для области дефекта ткани с использованием материала клеточного каркаса, где биосовместимый полимер представляет собой фибрин или декстриновый гель, где материал клеточного каркаса представляет собой децеллюляризованную ткань, и где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда и кожи, также относится к способу ингибирования фиброза тканей, включающему применение биосовместимого полимера и заменителя перикарда, где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез с использованием заменителя перикарда для области дефекта ткани, где биосовместимый полимер представляет собой фибрин или декстриновый гель, где заменитель перикарда представляет собой децеллюляризованную ткань, и где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда и кожи. Группа изобретений обеспечивает превосходный эффект ингибирования фиброза и самоорганизацию децеллюляризированной ткани для реконструирования аутологичной ткани. 2 н. и 4 з.п. ф-лы, 9 ил., 3 табл., 3 пр.
1. Способ ингибирования фиброза тканей, включающий применение биосовместимого полимера и материала клеточного каркаса, где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез для области дефекта ткани с использованием материала клеточного каркаса, где биосовместимый полимер представляет собой фибрин или декстриновый гель, где материал клеточного каркаса представляет собой децеллюляризованную ткань, и где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда и кожи.
2. Способ по п.1, который способствует самоорганизации материала клеточного каркаса.
3. Способ по п.1, где ткань, фиброз которой подлежит ингибированию, представляет собой эпикард.
4. Способ ингибирования фиброза тканей, включающий применение биосовместимого полимера и заменителя перикарда, где биосовместимый полимер фиксируют к одной ткани, фиброз которой подлежит ингибированию, и в другой ткани создают протез с использованием заменителя перикарда для области дефекта ткани, где биосовместимый полимер представляет собой фибрин или декстриновый гель, где заменитель перикарда представляет собой децеллюляризованную ткань, и где децеллюляризованная ткань представляет собой ткань, полученную посредством децеллюляризации биологической ткани, выбранной из группы, состоящей из подслизистой оболочки тонкого кишечника, перикарда и кожи.
5. Способ по п.4, который способствует самоорганизации заменителя перикарда.
6. Способ по п.4, где ткань, фиброз которой подлежит ингибированию, представляет собой перикард.
| US 2018078679 A1, 22.03.2018 | |||
| US 6417173 B1, 09.07.2002 | |||
| WO 9958168 A1, 18.11.1999. |
Авторы
Даты
2024-10-31—Публикация
2020-07-31—Подача