Предлагаемое изобретение относится к области медицины и касается композиций для профилактики рубцово-спаечных осложнений при операциях на сердце и способа их применения.
В настоящее время наблюдается рост количества операций на сердце. Известно, что спайки образуются при любом хирургическом вмешательстве, затрагивающем серозные оболочки. Чрезмерный рост соединительной ткани в условиях хирургических вмешательств на сердце может иметь крайне негативные последствия: страдает центральная гемодинамика, резко осложняется техническое выполнение оперативных вмешательств при повторных операциях.
Известно, что к профилактике послеоперационных спаек относится «бережная хирургическая техника, направленная на минимизацию травмы тканей», однако этого явно недостаточно для эффективной профилактики спаечного процесса.
Также известно, что для предупреждения развития спаечного процесса используют нестероидные противовоспалительные средства, гормональные препараты, которые при системном применении имеют очень ограниченный противоспаечный эффект, т.к. вновь образующиеся соединительнотканные тяжи на месте операционного повреждения не имеют васкуляризации и, следовательно, проникновение парентерально вводимых препаратов в эти зоны затруднено (Бокерия Л.А., Сивцев B.C. Послеоперационный спаечный перикардит: факторы риска, патогенез и методы профилактики. Анналы хирургии. 2014; 6: 7-15).
Известны средства, выполненные в форме гелей, которые могут быть использованы для профилактики спаечного процесса в перикарде.
Так, известен препарат на основе полиэтиленгликоля - Coseal (Baxter Healthcare, Fremont, CA). Рабочий раствор готовят из двух растворов полиэтиленгликоля, присутствующих в наборе, изготовленном производителем. Перед применением эти два раствора ex tempore смешивают, в результате чего формируется сополимер. После смешивания объем композиции увеличивается в 4 раза (Hendrikx М, Mees U, Hill AC, Egbert В, Coker GT, Estridge TD. Evaluation of a novel synthetic sealant for inhibition of cardiac adhesions and clinical experience in cardiac surgery procedures. Heart Surg Forum. 2001; 4 (3): 204-209).
Проведенные исследования показали, что использование Coseal снижает образование спаек средостения при операциях у детей по поводу врожденных пороков сердца. Однако применение Coseal, кроме положительного эффекта, в некоторых случаях приводит и к негативным последствиям - к тампонаде сердца и окклюзии верхней полой вены, вследствие увеличения объема формирующегося сополимера (Cannata A, Petrella D, Bruschi G, Fratto P, Gambacorta M, Martinelli L. Postsurgical intrapericardial adhesions: mechanisms of formation and prevention. Ann Thorac Surg. 2013; 95 (5): 1818-1826. DOI: 10.1016/j.athoracsur.2012.11.020). Так, среди 79 педиатрических пациентов выявлено шесть (5 серьезных) нежелательных явлений, обусловленных применением средства CoSeal (Napoleone CP, Valori A, Crupi G, Ocello S, Santoro F, Vouhe P, et al. An observational study of CoSeal for the prevention of adhesions in pediatric cardiac surgery. Interact Cardiovasc Thorac Surg. 2009; 9 (6): 978-982. DOI: 10.1510/icvts.2009.212175).
Также известно вещество с антиадгезивным действием, включающее биологически активный компонент: «Anti-adhesion polymer composition able to load growth factors» (Patent KR101330652B1, дата приоритета 28.02.2012, классы A61L24/046). Средство включает полиэтиленгликоль, который составляет от 65 до 85 мас.% с молекулярной массой 6000 ~ 20000 Да, полиэтиленгликоль-полипропиленгликоль-полиэтиленгликоль сополимер от 24 до 50 мас.%; желатин от 0,03 до 5% по весу; фактор роста (эпидермальный фактор роста, гепарин-связывающий эпидермальноподобный фактор роста, трансформирующий фактор роста - α, либо факторы роста фибробластов.
Недостатком известного средства является включение в его состав веществ, усиливающих пролиферацию фибробластов, т.е. потенциально усиливающих фиброз.
Наиболее близкое по технической сущности к заявляемому является средство, содержащее гелевую композицию биосовместимого полимера и блокатора р38 MAP киназы (US 2019/0240296 А1, 08.08.2019 «TREATMENT OF DISEASES MEDIATED BY VASCULAR HYPERPERMEABILITY» (https://patentimages.storage.googleapis.eom/97/2e/0e/1d0c2210babb57/US20190240296A1.pdf, дата обращения 20.03.23).
Известное средство получают путем удаления альбумина из композиции сывороточного альбумина человека и добавления одного или нескольких ингибиторов р38 МАР киназы, при этом ингибитор р38 МАР киназы выбирают из группы, состоящей из SB 203580, SB 203580 гидрохлорида, SB 202190, SB 239063, SB 706504, AL 8697, AMG 548, CMPD-1, DBM 1285 дигидрохлорида, EO 1428, JX 401, ML 3403, RWJ 67657, SCIO 469 гидрохлорида, SKF 86002 дигидрохлорида, SX 011, ТА 01, ТА 02, ТАК 715, VX 702, VX 745, p38 МАР киназы блокатор TOCRISET™ и их комбинации.
Известное средство обеспечивает ингибирование гиперпроницаемости сосудов у нуждающегося в этом субъекта, его применяют для лечения уже развившегося заболевания или состояния - для лечения сосудистых осложнений сахарного диабета и состояний, связанных с гиперпроницаемостью сосудов.
К недостаткам этого известного средства следует отнести отсутствие подавления роста соединительной ткани в перикарде при операциях на сердце после однократного применения, не соответствие вязкости жидкости для полости перикарда, а также использование компонентов человеческой плазмы крови, что не предназначено для применения при оперативных вмешательствах, в том числе на сердце.
До настоящего времени ни одно из средств не обладает всеми необходимыми качествами для предотвращения спаечного процесса в перикарде:
- прерывать процесс активации разрастания фиброзных тканей в зоне оперативного вмешательства на перикарде;
-подавлять рост соединительной ткани после однократного применения;
- не нарушать процесс ранозаживления в области операционной раны кожи и паренхимы органов;
- не обладать системным действием;
- отсутствие раздражающего действия;
- отсутствие необходимости фиксации;
- обладать биосовместимостью.
Задачей заявляемого изобретения является разработка композиций для профилактики рубцово-спаечных осложнений при операциях на сердце и способа их применения.
Техническим результатом настоящего изобретения является создание оригинальной композиции, обладающей эффектом предотвращения образования послеоперационных спаек в полости перикарда, а также сохранение стабильности свойств композиции при ее длительном хранении (12 месяцев и более).
Указанный технический результат достигается тем, что композиция для профилактики рубцово-спаечных осложнений при операциях на сердце содержит поливиниловый спирт, поливинилимидазол, блокатор р38 MAP киназы: SB203580, SB239063, VX-745 или AL 8697, глицерин, воду очищенную при следующем соотношении компонентов, мас.%:
Поливиниловый спирт – 3.1 - 8.0
Поливинилимидазол – 0.008 - 0.02
Глицерин – 7.7 - 13.3
Блокатор р38 МАР киназы – 0.00065 - 0.002
Вода очищенная до 100,0
рН композиции = 7,2 - 7,6.
В заявляемой композиции в качестве блокатора р38 MAP киназы она содержит одно из следующих веществ:
- SB203580 (4-(4'-фторфенил)-2-(4'-метилсульфинилфенил)-5-(4'-пиридил)-имидазол);
- SB239063 (транс-4-[4-(4-фторфенил)-5-(2-метокси-4-пиримидинил)-1H-имидаол-1-ил]циклогексанол);
- VX-745 (5-(2,6-дихлорфенил)-2-[2,4-дифторфенил)тио]-6H-пиримидо[1,6-b]пиридазин-6-он);
- AL 8697 (N-циклопропил-3-[3-(1,1-диметилэтил)-6,8-дифтор-1,2,4-триазоло[4,3-a]пиридин-7-ил]-5-фтор-4-метилбензамид).
Заявляемое средство содержит гелевую композицию биосовместимых полимеров с межмолекулярными связями через молекулы-производные имидазолиния или пиридиния со свойствами блокатора р38 MAP киназы, что приводит к подавлению роста соединительной ткани в перикарде, при этом композиция легко наносится и обладает биосовместимостью.
Заявляемая композиция по п.1 формулы изобретения дополнительно может содержать поливинилпирролидон в количестве 0 - 4.6 мас.%, хлорид натрия в количестве 0 - 0.9 мас.%, бисульфит натрия в количестве 0 - 0.009 мас.%.
Введение этих компонентов позволяет сохранить стабильность реологических свойств композиции при более длительном хранении (более 21 месяцев).
Способ применения заявляемой композиции для профилактики рубцово-спаечных осложнений при операциях на сердце у нуждающегося субъекта заключается в том, что композицию вводят в зону повреждения во время оперативного вмешательства в виде стерильного геля, однократно.
Проведенный сопоставительный анализ показал, что предлагаемое средство для профилактики рубцово-спаечных осложнений при операциях на сердце и способ его применения отличаются от известного и, следовательно, соответствуют критерию изобретения «новизна».
Экспериментальные исследования авторов заявляемого технического решения свидетельствуют о том, что предлагаемая композиция и способ ее введения обеспечивают получение технического результата, а именно: подавляет рост соединительной ткани в перикарде при операциях на сердце после однократного применения, легко наносится, обладает биосовместимостью и отсутствием раздражающего действия, не имеет системного действия, не нарушает процесс ранозаживления в области операционной раны.
Изложенное позволяет сделать вывод о соответствии заявляемого изобретения критерию «изобретательский уровень».
Реологические и физико-химические свойства композиции (вязкость, значение рН, зависимость вязкости от температуры) являются оптимальными как для непосредственного использования - не требуют значительных физических усилий для внесения в полость перикарда, так и для изготовления предзаполненных шприцев на распространенном для их производства оборудовании.
Заявляемое средство для профилактики рубцово-спаечных осложнений при операциях на сердце и способ его применения предназначены для использования в здравоохранении. Осуществление его возможностей подтверждают описанные в заявке средства и приемы, следовательно, предлагаемое изобретение соответствует условию патентоспособности «промышленная применимость».
Предлагаемая композиция и способ ее применения поясняется примерами конкретного применения.
Пример № 1. Изготовлена композиция следующего состава, мас.%:
Поливиниловый спирт марки 8-88 - 2,3
Поливиниловый спирт марки 18-88 - 0,8
Хлорид натрия - 0,5
Поливинилпирролидон - 4,6
Глицерин - 7,7
SB239063 - 0,00065
Поливинилимидазол - 0,008
Бисульфит натрия - 0,009
Вода очищенная до 100,0
1 М раствором NaOH рН композиции доведен до 7.2.
Получен гель, прозрачный, желтоватого оттенка, вязкость 38,20; стабильный при хранении в течение 12 месяцев - через 12 месяцев - прозрачный гель, желтоватого цвета, рН - 7.2, вязкость 38,25.
Пример № 2. Изготовлена композиция следующего состава, мас.%:
Поливиниловый спирт марки 18-88 - 5,3
Хлорид натрия - 0,9
Поливинилпирролидон - 1,6
Глицерин - 13,3
VX-745 -0,001
Поливинилимидазол - 0,02
Вода очищенная до 100,0
рН композиции доведен до 7.2 1 М раствором NaOH.
Получен гель, прозрачный, желтоватого оттенка, вязкость 48,15, стабильный при хранении в течение 12 месяцев - через 12 месяцев - прозрачный гель, желтоватого цвета, рН - 7.2, вязкость 48,13.
Пример № 3. Изготовлена композиция следующего состава, мас.%:
Поливиниловый спирт марки 8-88 - 2,0
Поливиниловый спирт марки 18-88 - 6,0
Хлорид натрия - 0,9
Поливинилпирролидон - 1,6
Глицерин - 13,3
AL 8697-0,001
Поливинилимидазол - 0,02
Вода очищенная до 100,0
рН композиции доведен до 7.6 1 М раствором NaOH.
Получен гель, прозрачный, желтоватого оттенка, вязкость 76,15, стабильный при хранении в течение 12 месяцев - через 12 месяцев - прозрачный гель, желтоватого цвета, рН - 7.6, вязкость 76,20.
Пример № 4. Изготовлена композиция следующего состава, мас.%:
Поливиниловый спирт марки 8-88 - 1,3
Поливиниловый спирт марки 18-88 - 4,0
Хлорид натрия - 0,9
Поливинилпирролидон - 1,6
Глицерин - 13,3
SB203580 - 0,002
Поливинилимидазол - 0,02
Вода очищенная до 100,0
рН композиции доведен до 7.6 1 М раствором NaOH.
Получен гель, прозрачный, желтоватого оттенка, вязкость 58,60, стабильный при хранении в течение 12 месяцев - через 12 месяцев - прозрачный гель, желтоватого цвета, рН - 7.6, вязкость 58,59.
Пример № 5. Изготовлена композиция следующего состава, мас.%:
Поливиниловый спирт марки 8-88 - 2
Поливиниловый спирт марки 18-88 - 4,9
Хлорид натрия - 0
Поливинилпирролидон -0
Глицерин - 13,3
SB203580 - 0,001
Поливинилимидазол - 0,02
Вода очищенная до 100,0
рН композиции доведен до 7.6 1 М раствором NaOH.
Получен гель, прозрачный, бесцветный, вязкость 73,23, стабильный при хранении в течение 12 месяцев - через 12 месяцев - прозрачный гель, желтоватого цвета, рН - 7.6, вязкость 73,25.
Все исследования изготовленных композиций были проведены с использованием экспериментальных животных и в соответствии с правилами, принятыми Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и иных целей (Страсбург, 1986) и требованиями «Правил проведения работ с использованием экспериментальных животных» (Приложение к Приказу Минздрава СССР от 12.08.1977 г. №755). Исследование одобрено Комитетом по этике ФГБНУ ИНЦХТ.
Пример №6.
Проведен хронический эксперимент на 10 самцах кроликов породы Шиншилла в возрасте 6 месяцев. Животные были разделены поровну на две группы: опытная и контрольная.
Всем животным в качестве наркоза внутривенно вводили Золетил-100 из расчета 7,5 мг/кг, раствор медитина 0,1% - 0,15 мл/кг. Через 10 мин после дачи наркоза кролика фиксировали на операционном столе за лапы брюшком вверх с разворотом тазового пояса на 90°, что позволяло получить удобный доступ к левой половине грудной клетки. Операционное поле после удаления шерсти дважды обрабатывали раствором кожного антисептика (Дезомакс). Далее выполняли интубацию трахеи и подключали к аппарату искусственной вентиляции легких (ИВЛ). Левостороннюю торакотомию осуществляли по 4 межреберью, края раны разводили с помощью ранорасширителей Кохера. Спавшееся левое легкое отводили в сторону для обеспечения доступа к сердцу. С помощью микрохирургических пинцета и ножниц приподнимали и рассекали париетальный листок перикарда. Длина надреза составляла 1 см. Затем на рассеченный париетальный листок перикарда накладывали непрерывный шов нитью нейлон Prolene 5.0. Перед последним стежком в полость перикарда, между висцеральным и париетальным листками, животным опытной группы (n=5) вводили 0.4 мл испытуемой композиции, изготовленной в соответствие с ПРИМЕРОМ №1 и такое же количество физиологического раствора вводили группе контроля (n=5). После ушивания рассеченного перикарда выполняли герметизацию грудной клетки и восстанавливали отрицательное давление с помощью шприца «Luer» объемом 20 мл. Ушивание раны выполняли непрерывным швом послойно нитью Prolene 3.0. По завершению операции каждому животному вводили раствор антимедина 0,05% в дозе, соответствующей количеству, введенного раствора медитина. Животных выводили из эксперимента на 28 сутки раствором хлороформа. В процессе выведения животных из эксперимента на каждого кролика заполняли протокол оценки тяжести спаечного процесса, подсчитывали баллы по шкале:
0 баллов - нет спаек;
1 балл - спайка пленчатая только в области шва;
2 балла - спайка рыхлая только в области шва;
3 балла - спайка плотная только в области шва;
4 балла - спайка пленчатая в области шва и за его пределами;
5 баллов - спайка рыхлая в области шва и за его пределами;
6 баллов - спайка плотная в области шва и за его пределами.
При этом проводили забор материала из зоны оперативного вмешательства для гистологических, исследований, фиксировали раствором FineFix (Milestone, Италия). Осуществляли заливку в Histomix. Гистологические срезы выполняли на ультратоме LEICA SM 2000R. Гистологические срезы окрашивали красителями гематоксилин-эозином и по Ван-Гизон. Морфологический анализ и фото документирование окрашенных гистологических препаратов выполняли с помощью биологического инвертированного микроскопа для лабораторных исследований ZEISS AxioVert. A1 А1 или микроскопа Nikon 80i.
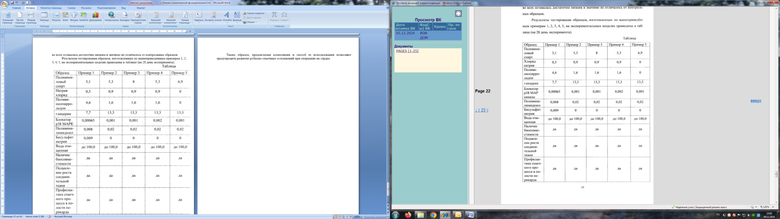
На Фигуре 1 показано сравнение выраженности спаечного процесса через 28 суток после оперативного вмешательства (U критерий Манна-Уитни) в опытной и контрольной группах, выраженное в баллах.
Выраженность спаечного процесса в опытной группе оказалась в 2 раза ниже, чем в контрольной группе.
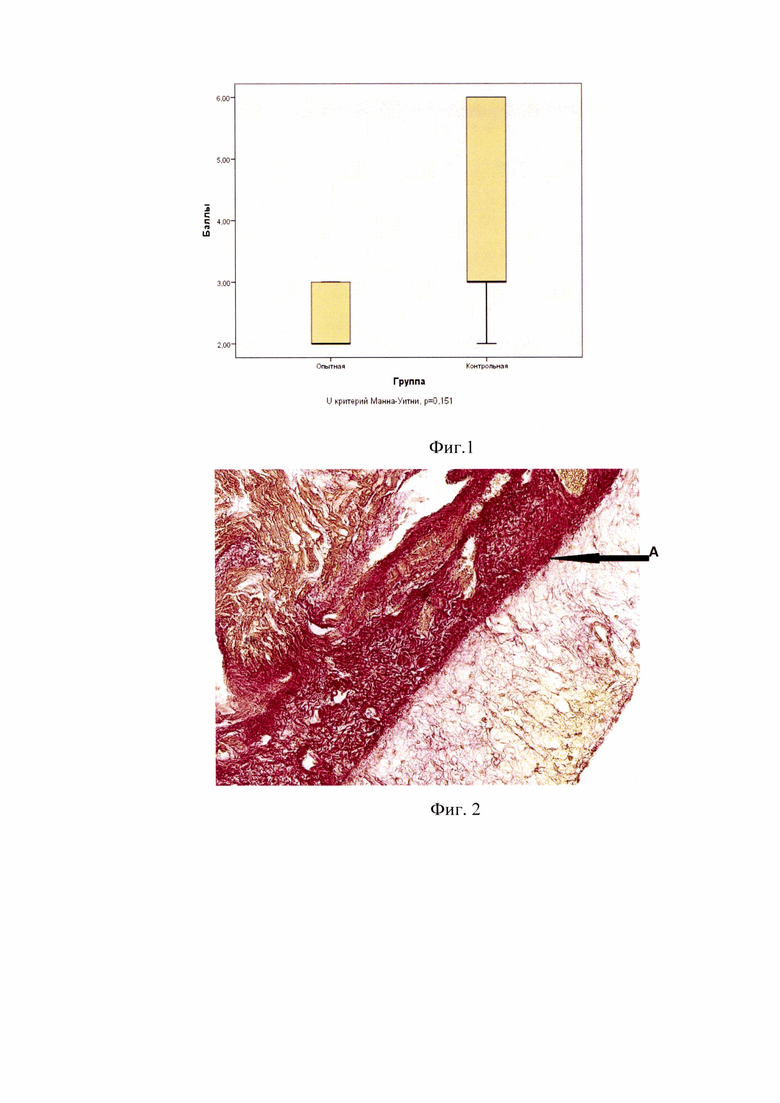
При гистологическом исследовании перикарда на 28 сутки у контрольной группы наблюдался выраженный спаечный процесс, в зоне повреждения между висцеральным и париетальным листками перикарда пространство полностью заполнено соединительной тканью с толстыми сформированными коллагеновыми волокнами. Так на Фигуре 2 позиция А показан выраженный спаечный процесс в перикарде, контрольная группа, 28 сутки, окраска по Ван Гизон.
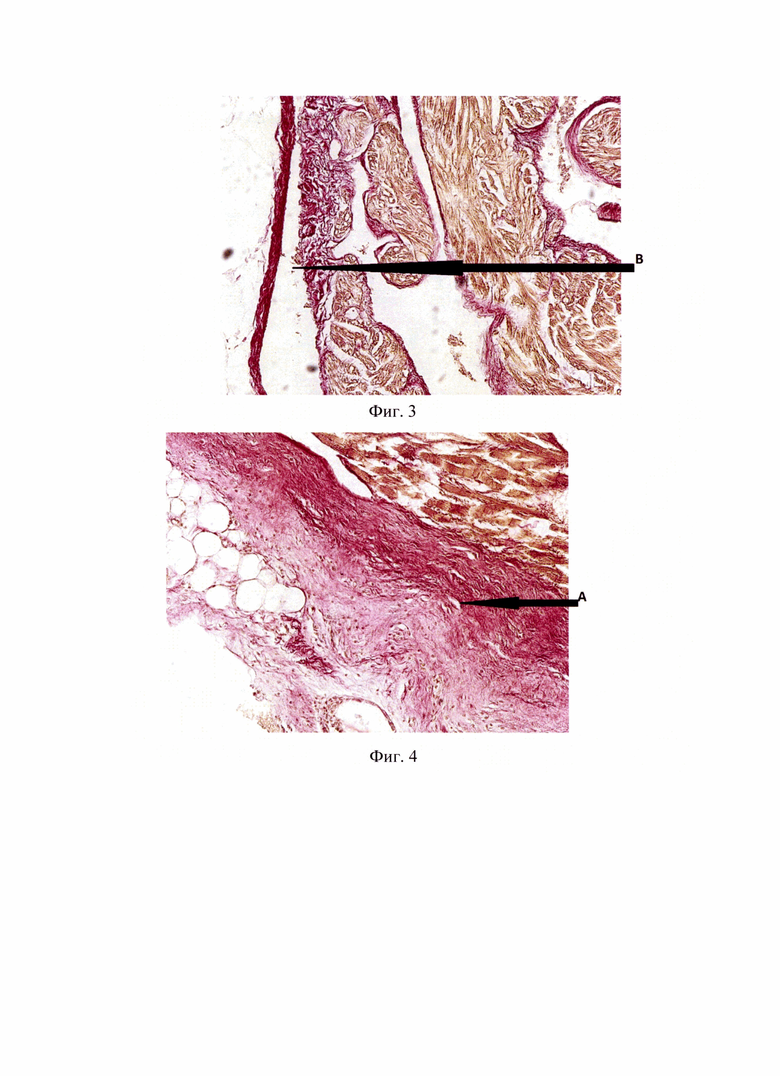
В опытной группе в зоне повреждения наблюдалось утолщение париетального листка перикарда, при этом полость между париетальным и висцеральным листками перикарда полностью свободна от коллагеновых волокон. Так, на Фигуре 3 позиция В показано отсутствие спаечного процесса в перикарде (свободная полость между висцеральным и париетальным листками), опытная группа, 28 сутки, окраска по Ван Гизон
Пример №7.
Для оценки эффективности заявляемой композиции также было проведено моделирование повреждения перикарда у лабораторных животных. В качестве модельных животных использовали крыс линии Wistar, самцы, возраст 3-4 месяца. В качестве наркоза применяли 0,1% медитин, Золетил. В конце операции вводили антимедин 0,5%. На грудной клетке по средней линии до подмышечной области слева удаляли шерсть, кожу обрабатывали 70%-м спиртом, йодопироном. Проводили интубацию трахеи. Выполняли разрез кожи по 4-5-му межреберью, вскрытие грудной клетки, доступ к перикарду. На перикард накладывали швы нитью нейлон №8/0. В полость перикарда каждому животному вводили 0,1 мл испытуемой композиции, изготовленной по Примеру №4 (основная группа, n=30), либо физиологический раствор (контрольная группа, n=30). Проводили герметизацию грудной клетки. Ушивание раны послойно нитью №3/0 непрерывным швом. Сроки выведения: 1-е, 3-й, 7-е, 14-е, 28-е сутки от начала эксперимента.
Для гистологических, исследований проводили забор материала из зоны оперативного вмешательства, который фиксировали раствором FineFix (Milestone, Италия). Осуществляли заливку в Histomix. Гистологические срезы выполняли на ультратоме LEICA SM 2000R, срезы окрашивали красителями гематоксилин-эозином и по Ван-Гизон. Морфологический анализ и фо-
тодокументирование окрашенных гистологических препаратов выполняли с помощью биологического инвертированного микроскопа для лабораторных исследований ZEISS AxioVert. А1 или микроскопа Nikon 80i.
У животных контрольной группы в сроки 1-е сутки в зоне травмы наблюдался выраженный отек, умеренная нейтрофильная инфильтрация, отложение фибрина. У основной группы в этот срок отмечалось только отложение фибрина с минимальной нейтрофильной инфильтрацией.
На 3-й сутки в контрольной группе отмечалась выраженная нейтрофильная инфильтрация в зоне травмы перикарда и прилегающих областях на большом протяжении. В основной группе в этот срок наблюдалась только минимальная нейтрофильная инфильтрация и только в зоне повреждения перикарда.
На 7-е сутки в контрольной группе отмечено нарастание нейтрофильной инфильтрации, рост соединительной ткани в зоне травмы перикарда и на большом протяжении в прилегающих областях, начало формирования спаек в полости перикарда. У основной группы в этот срок нейтрофильной инфильтрации нет, минимальный рост соединительной ткани только непосредственно в зоне травмы.
На 14-е сутки в контрольной группе прогрессировало формирование спаечного процесса на большой протяженности, облитерация полости перикарда. В основной группе отмечен минимальный рост соединительной ткани только в зоне травмы.
У животных контрольной группы к 28-м суткам формировался выраженный спаечный процесс в полости перикарда с полной облитерацией полости перикарда в зоне травматического воздействия, полость межу париетальным и висцеральным листка перикарда заполнена сформированной соединительной тканью с толстыми коллагеновыми волокнами. Так, на Фигуре 4 позиция А показан выраженный спаечный процесс в полости перикарда у животного контрольной группы. Окраска по Ван Гизон.
У животных основной группы на 28-е сутки спаечного процесса между висцеральным и париетальным листками перикарда не отмечено. На Фигуре 5 позиция В показано отсутствие спаечного процесса в перикарде, основная группа, 28-е сутки, окраска по Ван Гизон
Проведенные исследования показали противовоспалительный и выраженный противоспаечный эффект заявляемой композиции.
Пример №8.
Проведен хронический эксперимент на 30 самцах крыс линии Wistar в возрасте 4 месяцев с целью определить влияние (исключить негативное воздействие) композиции на ткани in vivo, определить безопасность и биологическую совместимость in vivo. Животные были разделены на 2 группы - контрольная - без введения композиции и опытная - с введением композиции, изготовленной по ПРИМЕРУ №4. В качестве наркоза использовали 0,1% раствор медитина, Золетил-100. После операции вводили раствор антимедина 0,5% в дозе 0,05 мг на 100 г массы животного. После дачи наркоза животное фиксировали за лапы на операционном столе вверх спинкой. В области операционного поля шерсть удаляли лезвием, операционное поле обрабатывали двукратно кожным антисептиком Дезомакс.Далее одноразовым лезвием скальпеля №15 наносили рану по паравертебральной линии, проникающую через кожу и подкожную клетчатку длиной 5 см. Затем рассекали собственную фасцию и в продольном направлении мышечные волокна длинной мышцы спины раздвигали тупым путем с помощью прямого гемостатического зажима типа Москит.Кровотечение в процессе операции тщательно останавливали. После этого кожу и подкожную клетчатку ушивали однорядным узловым швом нитью нейлон 3/0 (ООО ПТО «Медтехника») на атравматиче-ской круглой игле с интервалом между стежками 1 см. Перед наложением последнего стежка опытной группе в рану вводили исследуемую композицию в объеме 0.3 мл.
В сроки 1, 3, 7, 14 и 28 суток животных выводили из эксперимента с помощью подачи хлороформа ингаляционно. Для дальнейших гистологических исследований ткани из области раны иссекали и помещали гистологические кассеты с образцами в фиксирующий раствор FineFix (Milestone, Италия). После тщательной фиксации осуществляли проводку гистологических образцов в парафиновые блоки. Гистологические срезы выполняли на уль-тратоме LEICA SM 2000R и окрашивали красителями гематоксилин-эозин (Г-Э) и по Ван-Гизон (В-Г). Морфологический анализ и фотодокументирование окрашенных гистологических препаратов выполняли с помощью микроскопа для лабораторных исследований Nikon 80i, проводили фотодокументирование изображений.
У контрольной группы животных процесс формирования соединительнотканного рубца на месте кожно-мышечной раны соответствовал канонам развития воспалительного ответа в условиях асептической раны. К 1-м суткам после начала эксперимента отмечалась умеренная нейтрофильная инфильтрация в зоне повреждения, к 3-м суткам эпителизации раны не отмечено, сохранялась нейтрофильная инфильтрация, к 7-м суткам закономерно начиналось образование молодой грануляционной ткани. К 14-м суткам наблюдалась полная эпителизация раны, начиналось созревание соединительной ткани. К 28-м суткам плотность клеточных элементов фибробласти-ческого ряда в области раны снижалась. Формировался широкий, хорошо выраженный рубец с высокой плотностью коллагеновых волокон.
В основной группе через 1 сутки после начала эксперимента нейтрофильная инфильтрация в области раны была слабо выраженной, отек тканей не отмечался. К 3-м суткам инфильтрация практически не наблюдалась, отмечалась эпителизация раны. К 7-м суткам наблюдалась полная эпителизация раны, формировался узкий рубец. К 14-м суткам картина существенно не поменялась. К 28-м суткам наблюдалось созревание рубцовой ткани, рубец становился малозаметным. За все время эксперимента в основной группе не отмечены: замедление эпителизации раны, некрозы, эозинофилия, реакция на инородное тело в виде образования гранулем, появление в зоне раны клеток Пирогова-Ланхганса, инкапсуляция. В основной группе отмечено снижение воспалительной инфильтрации, ранняя эпителизация раны, резкое уменьшение зоны формирования рубцовой ткани. Следовательно, тестируемый образец у лабораторных животных показал безопасность и биологическую совместимость.
Пример 9.
Проводили пересев фибробластов в среду DMEM, содержащую 10% FBS, 1%о антибиотика/антимикотика при температуре 37°С, влажности 80%) и 5% CO2 в Biostation СТ, (Nikon), после образования монослоя клеток удаляли инкубационную среду, в лунки вносили исследуемые композиции в среде культивирования в количестве 10, 30% от вносимого объема. В контрольных образцах культуральную среду заменяли на свежую DMEM, содержащую 10% FBS и 1% антибиотик/антимикотик. Проводили фотодокументирование через каждые 12 часов в течение 3-х суток. Оценку воздействия на клеточную культуру и морфологические изменения производили с использованием программного продукта Nis-Elements AR, 4.1. Для анализа апоптотической и некротической гибели клеток на конечной точке эксперимента клетки окрашивали флуоресцентными красителями Annexin V, FITC conjugate (Invitrogen, cat. A13199) и Propidium iodide (Sigma-Aldrich, cat. P4864) соответственно.
На испытание получены образцы, изготовленные по вышеприведенным примерам 1, 2, 3, 4, 5.
В результате проведенного исследования было показано, что культивирование фибробластов с тестируемыми средствами в концентрации 10% и 30%о от объема среды не приводило к значимому повышению уровня некротической гибели клеток, количество окрашенных йодидом пропидия клеток во всех оставалась достаточно низким и значимо не отличалось от контрольных образцов.
Результаты тестирования образцов, изготовленных по вышеприведенным примерам 1, 2, 3, 4, 5, на экспериментальных моделях приведены в таблице (на 28 день эксперимента).
Таким образом, предлагаемая композиция и способ ее использования позволяют предупредить развитие рубцово-спаечных осложнений при операциях на сердце.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ЭПИДУРАЛЬНОГО ФИБРОЗА И СПОСОБ ЕЁ ПРИМЕНЕНИЯ | 2021 |
|
RU2796371C2 |
| СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СПАЕЧНОГО ПРОЦЕССА | 2012 |
|
RU2582975C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ СПАЙКООБРАЗОВАНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СПАЕЧНОГО ПРОЦЕССА | 2016 |
|
RU2624228C1 |
| СПОСОБ ЛЕЧЕНИЯ РАСПРОСТРАНЕННОГО ПЕРИТОНИТА | 2007 |
|
RU2339368C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВА СПАЙКООБРАЗОВАНИЯ БРЮШНОЙ ПОЛОСТИ | 2001 |
|
RU2221495C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННОГО РУБЦОВО-СПАЕЧНОГО ЭПИДУРИТА | 2013 |
|
RU2541828C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИНТРАОПЕРАЦИОННОГО ВЫСЫХАНИЯ БРЮШИНЫ ПРИ ОПЕРАЦИЯХ НА ОРГАНАХ БРЮШНОЙ ПОЛОСТИ | 2001 |
|
RU2199325C2 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ВЕНОЗНОЙ НЕДОСТАТОЧНОСТИ | 2013 |
|
RU2541808C1 |
| СПОСОБ КОРРЕКЦИИ ПЛОТНОСТИ СОЕДИНИТЕЛЬНОЙ ТКАНИ | 2008 |
|
RU2392960C1 |
| СПОСОБ ХИМИЧЕСКОГО ПЛЕВРОДЕЗА | 2016 |
|
RU2616271C1 |

Группа изобретений относится к химии, медицине и фармацевтике, а именно к композиции для профилактики рубцово-спаечных осложнений при операциях на сердце и к способу ее применения для профилактики рубцово-спаечных осложнений при операциях на сердце у нуждающегося субъекта. Предложенная композиция содержит, мас.%: 3,1-8,0 поливинилового спирта; 0,008-0,02 поливинилимидазола; 0,00065-0,002 блокатора р38 MAP киназы, представляющего собой SB203580, SB239063, VX-745 или AL 8697; 7,7-13,3 глицерина; воду очищенную до 100,0, при этом рН композиции составляет 7,2-7,6. В соответствии с предложенным способом указанную композицию вводят однократно в виде стерильного геля в зону повреждения во время оперативного вмешательства. Группа изобретений обеспечивает предотвращение образования послеоперационных спаек в полости перикарда, а также сохранение стабильности свойств композиции при ее длительном хранении (12 месяцев и более). 2 н. и 1 з.п. ф-лы, 5 ил., 1 табл., 9 пр.
1. Композиция для профилактики рубцово-спаечных осложнений при операциях на сердце, характеризующаяся тем, что содержит поливиниловый спирт, поливинилимидазол, блокатор р38 MAP киназы: SB203580, SB239063, VX-745 или AL 8697, глицерин, воду очищенную при следующем соотношении компонентов, мас.%:
рН композиции = 7,2-7,6.
2. Композиция по п. 1, характеризующаяся тем, что дополнительно содержит поливинилпирролидон в количестве 0-4.6 мас.%, хлорид натрия в количестве 0-0.9 мас.%, бисульфит натрия в количестве 0-0.009 мас.%.
3. Способ применения композиции по п. 1 для профилактики рубцово-спаечных осложнений при операциях на сердце у нуждающегося субъекта, характеризующийся тем, что композицию по п. 1 вводят в зону повреждения во время оперативного вмешательства в виде стерильного геля однократно.
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ СПАЙКООБРАЗОВАНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СПАЕЧНОГО ПРОЦЕССА | 2016 |
|
RU2624228C1 |
| Aritra Das et al | |||
| Compositional synergy of poly-vinyl alcohol, starch, glycerol and citric acid concentrations during wound dressing films fabrication / International Journal of Biological Macromolecules, 2020, V | |||
| Приспособление, увеличивающее число оборотов движущихся колес паровоза | 1919 |
|
SU146A1 |
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| EP 4151246 A1, 22.03.2023 | |||
| БИОРЕЗОРБИРУЕМАЯ ГИДРОГЕЛЕВАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ С БИОЛОГИЧЕСКИ АКТИВНЫМИ ВЕЩЕСТВАМИ (ВАРИАНТЫ) | 2012 |
|
RU2519103C2 |
| Шурыгин М.Г | |||
| и др | |||
| Перспективы | |||
Авторы
Даты
2025-03-14—Публикация
2023-06-06—Подача