ВВЕДЕНИЕ
Описан способ лечения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения, являющегося ингибитором полимеризации тубулина. Более конкретно, описан способ лечения протоковой аденокарциномы поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества только одного соединения замещенного пиримидина, являющегося обратным ингибитором полимеризации тубулина, или в комбинации с другими химиотерапевтическими средствами.
УРОВЕНЬ ТЕХНИКИ
По оценкам, в 2018 году рак поджелудочной железы может быть диагностирован у 55440 американцев, смертность от которого занимает пятое место среди общей смертности, вызываемой раком, и, в соответствии с прогнозом, эти цифры в течение ближайших десяти лет будут расти. Протоковая аденокарцинома поджелудочной железы (PDA) представляет собой рак с высокой резистентностью к химиотерапии, от которой ежегодно умирают более 45000 человек, и на нее приходится приблизительно 93% всех опухолей поджелудочной железы. Несмотря на то, что за последние годы наблюдается некоторый заметный прогресс в лечении протоковой аденокарциномы поджелудочной железы, это заболевание все еще остается раком, в основном неподдающимся лечению, с медианой выживаемости менее шести месяцев и уровнем выживаемости в течение 5 лет всего 8,7%.
Этот неблагоприятный прогноз обусловлен несколькими факторами. Большинство пациентов (85%) поступают с заболеванием на поздней стадии, что исключает возможность применения единственной эффективной терапии, а именно хирургического удаления опухоли. Однако даже среди пациентов с локализованным заболеванием, перенесших хирургическое вмешательство, уровень выживаемости в течение 5 лет и 10 лет составляют всего 25% и 8%, соответственно, из-за высокой частоты рецидивов (A. Richter et al., World J Surg 27, 324, Mar 2003). Для остальных 85% пациентов, а также пациентов с рецидивирующим заболеванием, доступно несколько способов лечения. В национальном стандарте лечения гемцитабин незначительно увеличивает выживаемость всего на несколько недель, и он рекомендован в первую очередь для улучшения показателей качества жизни (H. A. Burris, 3rd et al., J Clin Oncol 15, 2403, Jun 1997). Единственным другим препаратом, одобренным Управлением по надзору за пищевыми продуктами и медикаментами США (FDA) для лечения протоковой аденокарциномы поджелудочной железы на поздней стадии, является тарцева (Tarceva), который в комбинации с гемцитабином дает дополнительный положительный эффект, характеризующийся увеличением выживаемости в среднем всего на 10 дней. Несмотря на то, что было проведено более чем 60 клинических испытаний различных лекарственных средств и их комбинаций (H. Q. Xiong, K. Carr, J. L. Abbruzzese, Drugs 66, 1059, 2006), никаких других эффективных способов лечения не было найдено.
Среди наиболее важных характерных особенностей протоковой аденокарциномы поджелудочной железы необходимо отметить наличие распространяющейся десмопластической стромы, которая обуславливает локальное микроокружение, приводящее к высокому давлению интерстициальной жидкости, низкой васкуляризации и пониженной тканевой перфузии и диффузии. Вследствие этого, доставка лекарственного средства к опухолям поджелудочной железы является менее эффективной, чем в нормальных тканях, что приводит к широко распространенной первичной резистентности к химиотерапии, являющейся характерной для этого заболевания. Широко распространенная резистентность протоковой аденокарциномы поджелудочной железы к цитотоксической терапии частично обусловлена этим биофизическим барьером, препятствующим доставке лекарственного средства.
Доклинические испытания химиотерапевтических средств в экспериментальной модели на генетически-модифицированных мышах KPC (KrasLSL.G12D/+; p53R172H/+; PdxCretg/+) позволяют сделать предположение, что для того, чтобы повысить эффективность воздействия лекарственного средства на организм, усилия по разработке лекарственных средств для лечения протоковой аденокарциномы поджелудочной железы должны быть направлены на лекарственные средства с длительным периодом полувыведения и высоким значением терапевтического индекса (с широким интервалом между концентрацией, при которой достигается требуемый эффект, и концентрацией, при которой проявляется токсичность). Кроме того, при разработке новых схем лечения протоковой аденокарциномы поджелудочной железы следует учитывать стабильность и удерживание лекарственного средсьва внутри опухолевых клеток.
К сожалению, большинство традиционных цитотоксических средств быстро выводятся из кровотока, являются очень токсичными для нормальных пролиферирующих тканей, быстро метаболизируются или активно выводятся из опухолевых клеток. Важным с информативной точки зрения контрпримером является наб-паклитаксел (абраксан, фирмы Celgene), связанная с альбумином форма паклитаксела, стабилизирующего микротрубочки, который одобрен Управлением по надзору за пищевыми продуктами и медикаментами США (FDA) для применения в комбинации с гемцитабином для лечения пациентов с метастатическим раком поджелудочной железы. Наб-паклитаксел имеет конечный период полувыведения из кровотока 27 часов и менее токсичен, чем немодифицированный паклитаксел. Успех этой схемы помог подтвердить важность учета фармакологических аспектов в разработке лекарственных средств для лечения рака поджелудочной железы и продемонстрировал преимущества комбинирования гемцитабина (аналога дезоксицитидина) с лекарственным средством, действие которого направлено на микротрубочки.
В связи с этим, сохраняется потребность в химиотерапевтических средствах, которые позволяли бы преодолевать биофизический барьер при протоковой аденокарциноме поджелудочной железы для достижения эффективного биораспределения в опухолевых тканях, обладали бы необходимыми фармакодинамическими свойствами и позволяли бы достигать синергического эффекта в комбинации с другими химиотерапевтическими средствами для лечения рака поджелудочной железы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соединение 1 представляет собой синтетическое противораковое средство, используемое для ингибирования полимеризации тубулина и функции белка BMI-1 (смотрите патентный документ WO2014/081906), именуемое 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4-[4-(трифторметил)фенил]пиримидин-4,6-диамином, которое имеет структурную формулу (I):
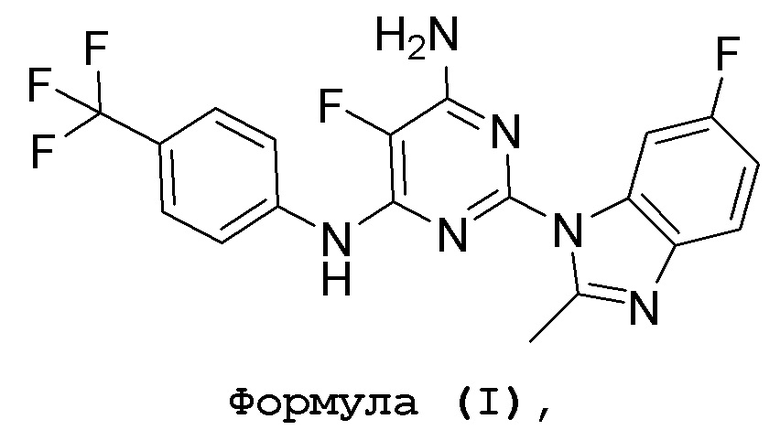
или его фармацевтически приемлемая соль или его фармацевтическая композиция.
Соединение 1 продемонстрировало фармакологические свойства, которые включают длительный период полувыведения из системы кровообращения и отсутствие активности субстрата P-гликопротеина (PGP) и эффективное биораспределение в опухолевых тканях. Кроме того, было обнаружено, что соединение 1 индуцирует митотический блок и апоптоз во многих линиях клеток протоковой аденокарциномы поджелудочной железы (PDA).
В результате проведения исследований механизма действия, но не выдвигая в качестве обоснования какую-либо конкретную теорию, было показано, что соединение 1 действует как ингибитор полимеризации микротрубочек. Кроме того, соединение 1 может применяться с синергическим эффектом в комбинации со стандартными схемами лечения такими препаратами, как гемцитабин и наб-паклитаксел, либо с любым одним из двух, либо с обоими вместе, с целью повышения эффективности в полученных от пациента ксенотрансплантатных моделей (PDX), что позволяет достигать мощной и продолжительной ремиссии рака. Кроме того, соединение 1 продемонстрировало эффективность в комбинации с гемцитабином в экспериментальной модели протоковой аденокарциномы поджелудочной железы (PDA) на генетически-модифицированных мышах KPC с высокой степенью резистентности к химиотерапии.
Эти данные и результаты исследования безопасности соединения 1 в качестве противоракового средства при клинических испытаниях являются убедительным обоснованием для исследования применения соединение 1 в комбинации со стандартной химиотерапией для лечения протоковой аденокарциномы поджелудочной железы (PDA).
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Один описанный в изобретении аспект включает способ лечения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1, 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4-[4-(трифторметил)фенил]пиримидин-4,6-диамина, имеющего структурную формулу (I):

или его фармацевтически приемлемой соли или его фармацевтической композиции.
Другой аспект включает способ лечения протоковой аденокарциномы поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции.
Один описанный в изобретении аспект включает способ лечения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции в комбинации с эффективным количеством одного или более химиотерапевтических средств.
Другой аспект включает способ лечения протоковой аденокарциномы поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции в комбинации с эффективным количеством одного или более химиотерапевтических средств.
Один описанный в изобретении аспект включает способ лечения протоковой аденокарциномы поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции в комбинации с эффективным количеством гемцитабина и наб-паклитаксела, либо с любым одним из двух, либо с обоими вместе.
Другой аспект включает способ лечения протоковой аденокарциномы поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции в комбинации с эффективным количеством гемцитабина и наб-паклитаксела, либо с любым одним из двух, либо с обоими вместе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1a в графическом виде представлены данные по относительной жизнеспособности клеток Aspc1 в течение времени после воздействия на них плацебо или соединения 1 (0,1 мкM или 1,0 мкM). Результаты показывают, что по сравнению с плацебо, соединение 1 вызывает зависимое от дозы и от времени снижение жизнеспособности клеток протоковой аденокарциномы поджелудочной железы (PDA) человека.
На фигуре 1b изображены типичные гистограммы содержания ДНК, измеренного методом проточной цитометрии по флуоресценции красителя 7-AAD из клеток Aspc1, подвергнутых воздействию плацебо или соединения 1 (0,1 мкМ или 1,0 мкМ).
На фигуре 1c в графическом виде представлены данные по проценту клеток Aspc1 в фазе G0/G1, фазе S и фазе G2/M через 24 часа после воздействия плацебо (DMSO), соединения 1 (0,1 мкМ, 1,0 мкМ) или 0,1 мкМ нокодазола (NOC, положительный контроль).
На фигуре 1d в графическом виде представлены данные по проценту клеток Aspc1 при непрямом делении (содержание ДНК 4N в клетках PH3+) после воздействия в течение 24 часов DMSO, соединения 1 (0,1 мкМ или 1,0 мкМ) или 0,1 мкM нокодазола (NOC). Данные, приведенные на фигурах 1b, 1c и 1d, показывают, что соединение 1 оказывает зависимое от дозы и времени воздействие на блок клеточного цикла клеток протоковой аденокарциномы поджелудочной железы (PDA) человека.
На фигуре 2a изображены типичные гистограммы содержания ДНК, измеренного по флуоресценции красителя DAPI в клетках Aspc1, подвергнутых воздействию плацебо или соединения 1 (1,0 мкМ), в моменты времени через 24 часа, через 48 часов и через 72 часа.
На фигуре 2b в графическом виде представлены данные по проценту клеток Aspc1 с содержанием ДНК >4N после воздействия DMSO или соединения 1 (0,1 мкМ или 1,0 мкМ) в моменты времени через 24 часа, через 48 часов и через 72 часа. Данные, приведенные на фигурах 2a и 2b, показывают, что соединение 1 вызывает зависимое от дозы и времени увеличение количества полиплоидных клеток протоковой аденокарциномы поджелудочной железы (PDA) человека.
На фигуре 3a представлены полученные методом проточной цитометрии типичные диаграммы рассеяния, демонстрирующие индуцирование апоптоза клеток Aspc1 после воздействия DMSO через 24 часа или 1,0 мкМ соединения 1 через 72 часа. В нефиксированных клетках окрашивали активную каспазу 3 с помощью красителя DAPI для того, чтобы различать жизнеспособные клетки (слева внизу) от клеток на стадии раннего апоптоза (слева вверху), на стадии позднего апоптоза (справа вверху) и на стадии некроза (справа внизу).
На фигуре 3b в графическом виде представлены данные по суммарному числу апоптозных клеток Aspc1 (активная каспаза 3+), определенному для DMSO или для соединения 1 в моменты времени через 24 часа, через 48 часов и через 72 часа. Данные, приведенные на фигурах 3a и 3b, показывают, что, по сравнению с плацебо, соединение 1 вызывает зависимое от времени увеличение клеточных биомаркеров, что указывает на соответствующий рост апоптоза клеток.
На фигуре 4a в графическом виде представлены данные по уровням соединения 1 в плазме мышей, определенным методом масс-спектроскопии, в начальный момент времени или через 2, 4, 7, 24 или 48 часов после перорального введения разовой дозы соединения 1 (10 мг/кг). На фигуре 4a показано, что соединение 1 характеризуется длительным периодом полувыведения из плазмы крови и проникает в центральную нервную систему и распределяется в тканях головного мозга.
На фигуре 4b в графическом виде представлены данные по отношениям величин CC50 при воздействии на клетки MDCK-P-gp при сравнении с воздействием на клетки MDCK-WT соединения 1, соединения 2, хлорпромазина, пуромицина, винбластина, доксорубицина, паклитаксела и винкристина. На фигуре 4b показано, что, по сравнению с другими химиотерапевтическими средствами, которые вызывают блок клеточного цикла, соединение 1, соединение 2 и хлорпромазин не действуют в качестве субстрата P-гликопротеина.
На фигуре 5a в графическом виде представлены данные по концентрациям соединения 1 в плазме, четырехглавой мышце и тканях протоковой аденокарциномы поджелудочной железы (PDA) мышей KPC через 24 часа после перорального введения разовой дозы соединения 1 (10 мг/кг) отдельно или в комбинации с гемцитабином (100 мг/кг). На фигуре 5a показано, что повышенная эффективность комбинации не обусловлена фармакокинетическим взаимодействием лекарственное средство-лекарственное средство.
На фигуре 5b представлены результаты вестерн-блоттинга для циклина B1 на опухолях мышей KPC, подвергнутых воздействию 10 мг/кг соединения 1. Проводили взятие биоптатов опухоли (Bx) за 48 часов до введения первой дозы и сравнивали с биоптатами, взятыми при некропсии (Nx) через 24 часа после введения третьей дозы.
На фигуре 5c в графическом виде представлены данные по определению количества циклина B1 (CycB1) из фигуры 5b, отнесенного к количеству винкулина (Vinc). На фигуре 5a показано, что соединение 1 распределяется в тканях протоковой аденокарциномы поджелудочной железы (PDA); и на фигурах 5b и 5c показано, что соединение 1 приводит к соответствующему снижению количества циклина B1 относительно винкулина, что позволяет предположить, что снижение прогрессирования митоза клеток протоковой аденокарциномы поджелудочной железы (PDA), индуцированное снижением количества циклина B1 относительно винкулина, индуцировало апоптоз.
На фигуре 6a в графическом виде представлены данные по изменениям во времени массы тела мышей KPC, подвергнутых воздействию комбинации соединения 1 и гемцитабина.
На фигуре 6b в графическом виде представлены данные по выживаемости с течением времени мышей KPC, подвергнутых воздействию плацебо (VEH), гемцитабина (GEM, 100 мг/кг два раза в неделю), соединения 1 (Cpd 1, 17 мг/кг два раза в неделю) или комбинации соединения 1 и гемцитабина (Cpd/GEM).
На фигуре 6c в графическом виде представлены данные по расчетам скорости роста опухоли, проведенным на основе длительного исследования объемов опухоли у мышей KPC, подвергнутых воздействию плацебо (VEH), гемцитабина (GEM), соединения 1 (Cpd 1) или комбинации соединения 1 и гемцитабина (Cpd/GEM).
На фигуре 6d в графическом виде представлены данные по количественному описанию иммуногистохимии для клеток с фосфорилированным гистоном H3 (PH3), которые демонстрируют среднее число положительных клеток в поле зрения микроскопа при 40 кратном увеличении для 10 полей зрения для одной опухоли после некропсии у мышей KPC, подвергнутых воздействию плацебо (VEH), гемцитабина (GEM), соединения 1 (Cpd 1) или комбинации соединения 1 и гемцитабина (Cpd/GEM).
На фигуре 6e в графическом виде представлены данные по количественному описанию иммуногистохимии для клеток с фосфорилированной расщепленной каспазой-3 (CC3), которые демонстрируют среднее число положительных клеток в поле зрения микроскопа при 40 кратном увеличении для 10 полей зрения для одной опухоли после некропсии у мышей KPC, подвергнутых воздействию плацебо (VEH), гемцитабина (GEM), соединения 1 (Cpd 1) или соединения 1 и гемцитабина (Cpd 1/GEM). На фигурах 6a, 6b, 6c, 6d и 6e показано, что соединение 1 в комбинации с гемцитабином синергически повышает общую выживаемость в экспериментальной модели на мышах KPC; где на фигуре 6a показано, что соединение 1 в комбинации с гемцитабином позволяет поддерживать относительно постоянной величину массы тела мышей KPC; на фигуре 6b показано, что, по сравнению с плацебо, с применяемым отдельно гемцитабином или применяемым отдельно соединением 1, соединение 1 в комбинации гемцитабином одновременно уменьшает объем опухоли и при этом синергически повышает общую выживаемость по сравнению с применением каждого лекарственного средства по отдельности; на фигурах 6c, 6d и 6e показано, что, по сравнению с плацебо, с применяемым отдельно гемцитабином или применяемым отдельно соединением 1, соединение 1 в комбинации гемцитабином вызывает общее снижение скорости роста клеток протоковой аденокарциномы поджелудочной железы (PDA) и конкретных клеточных биомаркеров.
На фигуре 7a в графическом виде представлены данные по объемам опухоли, измеренным методом 3D ультразвуковой визуализации высокого разрешения, для мышей KPC, подвергнутых воздействию плацебо (veh) или соединения 1 (Cpd 1).
На фигуре 7b в графическом виде представлены данные по объемам опухоли, измеренным методом 3D ультразвуковой визуализации высокого разрешения, для мышей KPC, подвергнутых воздействию плацебо (veh) или комбинации соединения 1 и гемцитабина (Cpd 1/gem). На фигуре 7a показано, что, по сравнению с плацебо, соединение 1 вызывает зависимое от времени уменьшение объема опухоли в экспериментальной модели протоковой аденокарциномы поджелудочной железы (PDA) на мышах KPC; и на фигуре 7b показано, что, по сравнению с применением только одного гемцитабина или только одного соединение 1, соединение 1 в комбинации с гемцитабином вызывает дополнительное зависимое от времени уменьшение объема опухоли в экспериментальной модели протоковой аденокарциномы поджелудочной железы (PDA) на мышах KPC.
На фигуре 8a в графическом виде представлены данные по росту опухоли, измеренному по проценту изменения объема опухоли, в течение 7 дней у мышей KPC, подвергнутых воздействию плацебо (VEH), соединения 1 (Cpd 1), гемцитабина (GEM) или комбинации соединения 1 и гемцитабина (Cpd 1/GEM).
На фигуре 8b в графическом виде представлены данные по проценту мышей, имеющих метастазы в печени, в случае мышей KPC, подвергнутых воздействию плацебо (V), соединения 1 (Cpd 1+V), гемцитабина (G) или комбинации соединения 1 и гемцитабина (Cpd 1+G). На фигуре 8a показано, что, по сравнению с применением плацебо, только одного гемцитабина или только одного соединения 1, применение соединения 1 в комбинации с гемцитабином вызывает снижение роста опухоли в экспериментальной модели протоковой аденокарциномы поджелудочной железы (PDA) на мышах KPC; и на фигуре 8b показано, что, по сравнению с применением плацебо и только одного гемцитабина, применение соединения 1 в комбинации с гемцитабином вызывает снижение количества метастазов в печени у мышей KPC, обусловленных протоковой аденокарциномой поджелудочной железы (PDA).
На фигуре 9a приведено изображение окрашенного гистологического среза опухоли мышей KPC, подвергнутых воздействию гемцитабина (GEM).
На фигуре 9a приведено изображение окрашенного гистологического среза опухоли мышей KPC, подвергнутых воздействию комбинации соединения 1 и гемцитабина (Cpd 1/GEM). На фигуре 9a показана индуцированная гемцитабином популяция апоптозных клеток; и на фигуре 9b показана популяция апоптозных клеток, индуцированная соединением 1 в комбинации с гемцитабином; где соединение 1 в комбинации с гемцитабином вызывает значительное увеличение популяции апоптозных клеток, что позволяет предположить наличие синергического эффекта по увеличению индуцированного апоптоза.
На фигуре 10a представлен ряд результатов вестерн-блоттинга, характеризующих уровни BMI-1 в клетках Aspc1, MiaPaCa-2 и Panc1, подвергнутых воздействию в течение 24 часов плацебо (VEH), 0,1 мкM нокодазола (NOC), 0,1 мкМ соединения 1 (0,1) или 1,0 мкМ соединения 1 (1,0) при сравнении с введением винкулина (VINC) в качестве контроля. На фигуре 10a показано, что, по сравнению с экспрессией в случае применения плацебо и винкулина, соединение 1 вызывает стабильное снижение экспрессии белка BMI-1 в различных типах клеток.
На фигуре 10b в графическом виде представлены данные по относительной жизнеспособности клеток J1002VEH и J1002TAM, подвергнутых воздействию плацебо (VEH), 0,1 мкМ соединения 1 (Cpd 1) или 1,0 мкМ соединения 1 (Cpd 1), в течение 96 часов. На фигуре 10b показано, при сравнении с плацебо и в присутствии J1002, что соединение 1 вызывает зависимое от дозы и от времени снижение жизнеспособности клеток, зависимых от экспрессии белка BMI-1.
На фигуре 10c представлены кривые зависимости "доза-эффект" для клеток J1002VEH и J1002TAM, подвергнутых воздействию соединения 1, в течение 72 часов. На фигуре 10c показано, по сравнению с клетками, подвергнутых воздействию плацебо, что соединение 1 в диапазоне концентраций ниже мкM характеризуется активностью в отношении снижения экспрессии белка BMI-1 в присутствии J1002.
На фигуре 10d представлены типичные гистограммы ДНК для клеток J1002VEH, подвергнутых в течение 24 часов воздействию плацебо (VEH) или 1,0 мкМ соединения 1 (Cpd 1).
На фигуре 10e в графическом виде представлены данные по проценту клеток J1002VEH в фазе G0/G1, фазе S и фазе G2/M через 24 часа после воздействия плацебо (VEH) или 1,0 мкМ соединения 1 (Cpd 1).
На фигуре 10f представлены типичные гистограммы ДНК для клеток J1002TAM, подвергнутых в течение 24 часов воздействию плацебо (VEH) или 1,0 мкМ соединения 1 (Cpd 1).
На фигуре 10g в графическом виде представлены данные по проценту клеток J1002TAM в фазе G0/G1, фазе S и фазе G2/M через 24 часа после воздействия плацебо (VEH) или 1,0 мкМ соединения 1 (Cpd 1). На фигурах 10d, 10e, 10f и 10g показано, при сравнении с плацебо и в присутствии J1002, что соединение 1 вызывает зависимое от дозы и времени увеличение количества BMI-1 зависимых полиплоидных клеток; где взятые вместе полученные данные позволяют предположить, что соединение 1 индуцирует опосредовано гиперфосфорилирование BMI-1 в результате митотического блока.
На фигуре 11a в графическом виде представлены данные по дифференциально экспрессированным генам, измеренным методом секвенирования РНК, на клетках Aspc1, подвергнутых воздействию DMSO или 1 мкM соединения 1 (Cpd 1), проинтегрированные в течение 8, 16 и 24 часов.
На фигуре 11b представлены результаты вестерн-блоттинга, указывающие на свободный тубулин из клеток Aspc1, подвергнутых воздействию плацебо (VEH), 3,0 мкМ соединения 1 (Cpd 1), 1,0 мкМ колхицина (COL) или 1,0 мкМ паклитаксела (TAX) в течение 2 часов. После обработки, клеточные лизаты фракционировали путем центрифугирования с целью отделения свободного тубулина от микротрубочек. LSP=осадок при низкой скорости вращения (1000 x g, 5 минут), HSP=осадок при высокой скорости вращения (100000 x g, 1 час), HSS=надосадочная жидкость при высокой скорости вращения (100000 x g, 1 час). На фигурах 11a и 11b показано, при сравнении с плацебо, COL (карбоплатином) и TAX (тамоксифеном), что применение соединения 1 приводит к значительному кратному изменению повышения степени предотвращения образования тубулина.
На фигуре 11c представлено изображение тубулина и DAPI в клетках Aspc1, подвергнутых воздействию плацебо (VEH) в течение 24 часов.
На фигуре 11d представлено изображение тубулина и DAPI в клетках Aspc1, подвергнутых воздействию соединения 1 (Cpd 1) в течение 24 часов. На фигурах 11c и 11d показано, при сравнении с плацебо, что соединение 1 вызывает значительное снижение образования тубулина.
На фигуре 11e в графическом виде представлены данные по исследованию зависимости полимеризации тубулина от времени для клеток, подвергнутых воздействию плацебо (DMS), тамоксифена (TAX), карбоплатина (COL) и соединения 1 (0,12 мкМ, 0,37 мкМ, 1,11 мкМ, 3,33 мкМ и 10 мкМ).
На фигуре 11f в графическом виде представлены данные, выраженные в относительных единицах флуоресценции в минуту, которые приведены на фигуре 11e. На фигурах 11e и 11f показано, при сравнении с плацебо, COL (карбоплатином) и TAX (тамоксифеном), что соединение 1 вызывает зависимое от дозы снижение полимеризации тубулина; где взятые вместе полученные данные позволяют предположить, что соединение 1 непосредственно ингибирует образование микротрубочек.
На фигуре 12a в графическом виде представлены данные по средней величине объемов опухоли в зависимости от времени в полученных от пациента подкожных ксенотрансплантатных моделей протоковой аденокарциномой поджелудочной железы (PDA) человека, подвергнутых воздействию плацебо (veh), гемцитабина (gem), наб-паклитаксела (nabP), комбинации гемцитабина и наб-паклитаксела (gm/nabP), соединения 1 (Cpd 1), комбинации соединения 1 и гемцитабина (Cpd 1/gem), комбинации соединения 1 и наб-паклитаксела (Cpd 1/nabP) и комбинации соединения 1, гемцитабина и наб-паклитаксела (Cpd 1/gem/nabP).
На фигуре 12b в графическом виде представлены данные по массе тела мышей в зависимости от времени, подвергнутых воздействию плацебо (veh), гемцитабина (gem), наб-паклитаксела (nabP), комбинации гемцитабина и наб-паклитаксела (gm/nabP), соединения 1 (Cpd 1), комбинации соединения 1 и гемцитабина (Cpd 1/gem), комбинации соединения 1 и наб-паклитаксела (Cpd 1/nabP) и комбинации соединения 1, гемцитабина и наб-паклитаксела (Cpd 1/gem/nabP).
На фигуре 12c в графическом виде представлены константы скорости роста и распада опухоли для опухолей, подвергнутых воздействию гемцитабина (gem), наб-паклитаксела (nabP) и соединения 1 (Cpd 1).
На фигуре 12d в графическом виде представлены данные по ответу опухоли для каждой мыши, подвергнутой воздействию плацебо (veh), гемцитабина (gem), наб-паклитаксела (nabP), комбинации гемцитабина и наб-паклитаксела (gm/nabP), соединения 1 (Cpd 1), комбинации соединения 1 и гемцитабина (Cpd 1/gem), комбинации соединения 1 и наб-паклитаксела (Cpd 1/nabP) и комбинации соединения 1, гемцитабина и наб-паклитаксела (Cpd 1/gem/nabP). На фигурах 12a, 12b, 12c и 12d показано, что соединение 1 либо в двухкомпонентной комбинации с наб-паклитакселом, либо в трехкомпонентной комбинации с гемцитабином и наб-паклитакселом, синергически уменьшает объем опухоли и общий рост опухоли в полученной от пациента ксенотрансплантатной модели протоковой аденокарциномой поджелудочной железы (PDA) человека; где, на фигуре 12a показано, при сравнении с применением плацебо, только одного гемцитабина, только одного соединения 1, только одного наб-паклитаксела, гемцитабина в комбинации с наб-паклитакселом и гемцитабина в комбинации с соединением 1, что соединение 1 либо в двухкомпонентной комбинации с наб-паклитакселом, либо в трехкомпонентной комбинации с гемцитабином и наб-паклитакселом, синергически уменьшает объем опухоли; на фигуре 12b показано, при сравнении с применением плацебо, только одного гемцитабина, только одного соединения 1, только одного наб-паклитаксела, гемцитабина в комбинации с наб-паклитакселом и гемцитабина в комбинации с соединением 1, соединения 1 в синергетической комбинации с наб-паклитакселом, и соединения 1 в синергетической комбинации с гемцитабином и наб-паклитакселом, что в случае всех комбинаций поддерживается относительная масса тела мышей KPC; на фигуре 12c показано, при сравнении со случаем присутствия или отсутствия любого из гемцитабина, соединения 1 и наб-паклитаксела, что соединение 1 в комбинации либо с одним, либо с обоими гемцитабином и наб-паклитакселом, значительно снижает общую скорость роста опухоли, увеличивая при этом скорость распада опухоли; и на фигуре 12d показано, при сравнении со случаем присутствия или отсутствия любого из гемцитабина, соединения 1 и наб-паклитаксела, что соединение 1 в комбинации либо с одним, либо с обоими гемцитабином и наб-паклитакселом, значительно снижает начальный объем опухоли.
Определения
Используемый в изобретении термин "приблизительно" обозначает диапазон для данной величины, в котором полученная величина является практически такой же, что и указанная в явной форме величина. В одном аспекте, "приблизительно" означает отклонение в пределах 25% от данной величины или диапазона. Например, фраза "приблизительно 70% по массе" включает, по меньшей мере, все величины от 52% до 88% по массе. В другом аспекте, термин "приблизительно" означает отклонение в пределах 10% от данной величины или диапазона. Например, фраза "приблизительно 70% по массе" включает, по меньшей мере, все величины от 63% до 77% по массе. В другом аспекте, термин "приблизительно" означает отклонение в пределах 7% от данной величины или диапазона. Например, фраза "приблизительно 70% по массе" включает, по меньшей мере, все величины от 65% до 75% по массе.
Концентрации, количества, число клеток, проценты и другие численные значения могут быть представлены в изобретении в формате их диапазона. Следует иметь в виду, что такой формат диапазона используется только из соображений удобства и краткости, и его следует толковать в более широком смысле в том смысле, что он включает не только численные значения, указанные в явном виде в форме пределов диапазона, но также включает все индивидуальные численные значения или поддиапазоны, входящие в этот диапазон, как если бы в явном виде было бы указаны каждое численное значение и каждый поддиапазон.
Используемые в изобретении термины "терапии" и "терапия" могут относится к любому протоколу (протоколам), способу (способам), композициям, лекарственным формам и/или лекарственному средству (лекарственным средствам), которые могут применяться для предотвращения, лечения, тактики лечения или облегчения состояния или нарушения или одного или более их симптомов (например, рака поджелудочной железы или одного или более его симптомов или одного или более ассоциированных с ним состояний).
В конкретных аспектах, термины "терапии" и "терапия" относятся к медикаментозной терапии, такой как химиотерапия, вспомогательной терапии, лучевой терапии, хирургическому вмешательству, биологической терапии, поддерживающей терапии, антивирусной терапии и/или к другим видам терапий, применяемым для лечения, тактики лечения, предотвращения или облегчения состояния или нарушения или одного или более их симптомов (например, рака поджелудочной железы или одного или более его симптомов или одного или более ассоциированных с ним состояний). В некоторых аспектах, термин "терапия" относится к терапии, не являющейся применением соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции. В конкретных аспектах, "дополнительная терапия" и "дополнительные терапии" относятся к терапии, которая не является лечением с применением соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции. В конкретном аспекте, терапия включает применение соединения 1 в качестве вспомогательной терапии. Например, применение соединения 1 в сочетании с медикаментозной терапии, такой как химиотерапия, биологической терапией, хирургическим вмешательством, поддерживающей терапией, антивирусной терапией и/или другими видами терапий, может использоваться для лечения, тактики лечения, предотвращения или облегчения состояния или нарушения или одного или более их симптомов (например, рака поджелудочной железы или одного или более его симптомов или одного или более ассоциированных с ним состояний).
Используемый в изобретении термин "младенец" относится к новорожденному человеку в возрасте до 1 года.
Используемый в изобретении термин "ребенок преддошкольного возраста" относится к человеку в возрасте от 1 года до 3 лет.
Используемый в изобретении термин "ребенок" относится к человеку в возрасте от 1 года до 18 лет.
Используемый в изобретении термин "взрослый человек" относится к человеку в возрасте 18 или старше.
Используемый в изобретении термин "человек среднего возраста" относится к человеку в возрасте от 30 до 64 лет.
Используемый в изобретении термин "человек пожилого возраста" относится к человеку в возрасте 65 или старше.
Используемый в изобретении термин "субъект" относится к индивидууму, которого подвергают описанной в изобретении терапии. В конкретном аспекте, индивидуумом является человек.
Используемый в изобретении термин "рак поджелудочной железы" относится в целом к описанному в изобретении раку поджелудочной железы. В конкретном аспекте, общий термин "рак поджелудочной железы" может относится к протоковой аденокарциноме поджелудочной железы (PDA) без конкретного использования этого термина.
Используемый в изобретении термин "эффективное количество" применительно к введению соединения 1 субъекту, имеющему рак поджелудочной железы, относится к дозе соединения 1, которая позволяет достигать положительного или терапевтического эффекта. В конкретных аспектах, "эффективное количество" соединения 1 относится к количеству соединения 1, которое является достаточным для достижения, по меньшей мере, одного, двух, трех, четырех или более из следующих положительных или терапевтических эффектов: (i) торможение развития рака поджелудочной железы; (ii) ослабление симптомов рака поджелудочной железы; (iii) ликвидация, устранение или полная ремиссия рака поджелудочной железы; (iv) предотвращение развития или проявления одного или более симптомов, ассоциированных с раком поджелудочной железы; (v) уменьшение или облегчение тяжести одного или более симптомов, ассоциированных с раком поджелудочной железы; (vi) снижение числа одного или более симптомов, ассоциированных с раком поджелудочной железы; (vii) облегчение тяжести одного или более симптомов, ассоциированных с раком поджелудочной железы; (viii) снижение продолжительности проявления одного или более симптомов, ассоциированных с раком поджелудочной железы; (ix) предотвращение повторной пролиферации или одного или более симптомов, ассоциированных с раком поджелудочной железы; (x) снижение летальности; (xi) повышение выживаемости субъектов; (xii) повышение безрецидивной выживаемости; (xiii) увеличение числа субъектов с раком поджелудочной железы в состоянии ремиссии; (xiv) уменьшение количества госпитализаций субъекта; (xv) снижение продолжительности госпитализации; (xvi) снижение частоты госпитализаций; (xvii) повышение периода выживания субъекта; (xviii) повышение периода бессимптомного выживания субъекта с раком поджелудочной железы; (xix) повышение продолжительности периода ремиссии рака поджелудочной железы у субъекта; (xx) повышение качества жизни (QOL), оцениваемое известными методами, например, с помощью опросного листа по оценке QOL и другими подобными методами; (xxi) снижение пролиферации в результате введения соединения 1 перед проведением лечения с помощью другого химиотерапевтического средства; (xxii) снижение пролиферации в результате введения соединения 1 после проведения лечения с помощью другого химиотерапевтического средства; (xxiii) снижение пролиферации при применении комбинированной терапии в результате введения соединения 1 с другим химиотерапевтическим средством; (xxiv) аддитивный антипролиферативный эффект при применении комбинированной терапии в результате введения соединения 1 с другим химиотерапевтическим средством; (xxv) синергический антипролиферативный эффект при применении комбинированной терапии в результате введения соединения 1 с другим химиотерапевтическим средством; (xxvi) снижение пролиферации в результате введения соединения 1 перед проведением лучевой терапии; (xxvii) снижение пролиферации в результате введения соединения 1 после проведения лучевой терапии; (xxviii) снижение пролиферации в результате введения соединения 1 при проведении комбинированной терапии с лучевой терапией; (xxix) снижение пролиферации в результате введения соединения 1 перед хирургическим вмешательством; (xxx) снижение пролиферации в результате введения соединения 1 при проведении комбинированной терапии с хирургическим вмешательством; (xxxi) усиление или улучшение терапевтического эффекта в результате введения соединения 1 с проведением паллиативной терапии; (xxxii) снижение концентрации BMI-1 в плазме у субъекта, имеющего рак поджелудочной железы; (xxxiii) снижение количества циркулирующих в периферической крови пролиферативных клеток в плазме субъекта, имеющего рак поджелудочной железы; (xxxiv) изменение (например, снижение или повышение) концентрации биомаркера рака поджелудочной железы в плазме у субъекта, имеющего рак поджелудочной железы (например, BMI-1, полимеризация тубулина, маркеры апоптоза или ткань и другие подобные биомаркеры); (xxxv) снижение концентрации BMI-1 в биологическом образце (например, в плазме, сыворотке, моче или любых других биожидкостях), взятом у субъекта, имеющего рак поджелудочной железы; (xxxvi) количество пролиферативных клеток поддерживается постоянным после применения описанной в изобретении терапии, измеряемое традиционными методами, доступными для использования любым специалистом в данной области, такими как магнитно-резонансная томография (MRI), магнитно-резонансная томография с улучшенным динамическим контрастированием (DCE-MRI), рентгеновский анализ, изображение, полученное методом компьютерной томографии (CT), изображение, полученное методом позитронно-эмиссионной томографии (PET), флуоресценция красителя 7-AAD или флуоресценция красителя DAPI ; (xxxvii) количество пролиферативных клеток снижается после применения описанной в изобретении терапии, измеряемое традиционными методами, доступными для использования любым специалистом в данной области, такими как магнитно-резонансная томография (MRI), магнитно-резонансная томография с улучшенным динамическим контрастированием (DCE-MRI), рентгеновский анализ, изображение, полученное методом компьютерной томографии (CT), изображение, полученное методом позитронно-эмиссионной томографии (PET), флуоресценция красителя 7-AAD или флуоресценция красителя DAPI ; или (xxxviii) количество пролиферативных клеток не увеличивается, или увеличивается, но на меньшую величину, чем можно было ожидать, после применения описанной в изобретении терапии, измеряемое традиционными методами, доступными для использования любым специалистом в данной области, такими как магнитно-резонансная томография (MRI), магнитно-резонансная томография с улучшенным динамическим контрастированием (DCE-MRI), рентгеновский анализ, изображение, полученное методом компьютерной томографии (CT), изображение, полученное методом позитронно-эмиссионной томографии (PET), флуоресценция красителя 7-AAD или флуоресценция красителя DAPI.
Используемый в изобретении термин "в течение периода продолжительностью 24 часа" относится к периоду времени, в течение которого поддерживается состояние на постоянном уровне; например, эффективное количество соединения 1 определяется, когда достигается средняя концентрация соединения 1 в плазме и поддерживается в течение множества периодов продолжительностью 24 часа. Другими словами, средняя концентрация соединения 1 в плазме может быть достигнута в соответствующее время, которое может быть большим или меньшим чем 24 часа.
Используемый в изобретении термин "описанная в изобретении терапия" относится к способу применения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции в качестве ингибитора функции BMI-1 путем нацеленного ингибирования полимеризации тубулина для лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения 1.
В одном аспекте, рак поджелудочной железы представляет собой протоковую аденокарциному поджелудочной железы. В другом аспекте описанной в изобретении терапии, способ применения соединение 1 или его фармацевтически приемлемой соли или фармацевтической композиции включает комбинацию с другим химиотерапевтическим средством, обладающим синергической антипролиферативной активностью. В одном аспекте, другое химиотерапевтическое средство ингибирует функциональную активность BMI-1. В другом аспекте, другое химиотерапевтическое средство ингибирует полимеризацию тубулина.
Используемый в изобретении термин "фармацевтически приемлемая соль (фармацевтически приемлемые соли)" относится к соли, приготовленной из фармацевтически приемлемой нетоксичной кислоты или фармацевтически приемлемого нетоксичного основания, включающих неорганическую кислоту и основание и органическую кислоту и основание; смотрите, например, монографии Remington’s Pharmaceutical Sciences, 18th eds., Mack Publishing, Easton PA (1990) или Remington: The Science and Practice of Pharmacy, 19 th eds., Mack Publishing, Easton PA (1995).
Используемый в изобретении термин "соединение 1" обычно относится к соединению 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]-имидазол-1-ил)-N4-[4-(трифторметил)фенил]пиримидин-4,6-диамина и его фармацевтически приемлемым солям. "Соединение 1" может быть практически чистым (например, иметь чистоту приблизительно 90%, приблизительно 95%, приблизительно 98%, приблизительно 99% или приблизительно 99,9%). В различных аспектах, термин "соединение 1" относится к соединению 109, раскрытому в патентном документе International Publication No. WO2014/081906, полное содержание которого включено в настоящее изобретение путем ссылки на него.
Способ применения
Как продемонстрировано в изобретении, соединение 1 или его фармацевтически приемлемая соль или фармацевтическая композиция представляет собой ингибитор полимеризации тубулина и функции BMI-1 для применения для лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включающего введение субъекту эффективного количества соединения 1 или его фармацевтически приемлемой соли или его фармацевтической композиции.
В одном аспекте, рак поджелудочной железы представляет собой протоковую аденокарциному поджелудочной железы.
В другом аспекте, способ применения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции включает комбинацию соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции с одним или более другими химиотерапевтическими средствами, где комбинация проявляет синергическую антипролиферативную активность. В одном аспекте, другое химиотерапевтическое средство ингибирует функциональную активность BMI-1. В другом аспекте, другое химиотерапевтическое средство ингибирует полимеризацию тубулина. Однако, неизвестны или не разрешены к применению в клинической практике ингибиторы либо функциональной активности BMI-1 или полимеризации тубулина, либо одновременно и функциональной активности BMI-1 или полимеризации тубулина, для применения при лечении видов рака поджелудочной железы. В связи с этим, высокая и селективная активность, благоприятные фармацевтические свойства и большой опыт клинического применения соединение 1 позволяет предположить, что соединение 1 является подходящим лекарственным средством для лечения рака поджелудочной железы.
В одном аспекте, в изобретении описаны способы ингибирования или снижения полимеризация тубулина и функции BMI-1 для индуцирования блока клеточного цикла в пролиферирующих клетках или клеточных линиях.
В другом аспекте, способ ингибирования или снижения полимеризация тубулина и функции BMI-1 для индуцирования блока клеточного цикла в пролиферирующих клетках или клеточных линиях включает контактирование соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции с пролиферирующими клетками или клеточными линиями, где пролиферирующие клетки или клеточные линии ранее могли не подвергаться какому-либо воздействию, или было установлено, что они уже подвергались воздействию с целью ингибирования или снижения полимеризации тубулина и функции BMI-1.
В другом аспекте, неограничивающие примеры таких клеток или клеточных линий выбирают из клеток HL-60, HeLa, HT1080, HCT116, HEK293, NCI H460, U-87MG, ASPC-1, PL-45, HPAF-2, PC-3, MDA-MB-231, MDA-MB-468, A431, SNU-1, AGS, Kato III, A549, Calu-6, A375, SY5Y, SKOV3, Capan-1, sNF96.2, TIVE-L1, TIVE-L2, LNCaP и других подобных клеток. В более конкретном аспекте, клетки или клеточные линии могут представлять собой клетки рака поджелудочной железы.
В одном аспекте, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 у субъекта, имеющего рак поджелудочной железы и нуждающегося в лечении, включает введение эффективного количества соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту.
В конкретном аспекте, у субъекта диагностирован рак поджелудочной железы, поддающийся лечению путем ингибирования или снижения полимеризации тубулина и функции BMI-1.
В конкретном аспекте, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 позволяет ингибировать или снижать полимеризацию тубулина и функцию BMI-1 приблизительно на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 80%, 85%, 90%, 95% или 100% по сравнению с полимеризацией тубулина и функцией BMI-1 до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В конкретном аспекте, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 позволяет ингибировать или снижать полимеризацию тубулина и функцию BMI-1 на величину в диапазоне от приблизительно 5% до приблизительно 20%, от приблизительно 10% до приблизительно 30%, от приблизительно 15% до приблизительно 40%, от приблизительно 15% до приблизительно 50%, от приблизительно 20% до приблизительно 30%, от приблизительно 20% до приблизительно 40%, от приблизительно 20% до приблизительно 50%, от приблизительно 30% до приблизительно 60%, от приблизительно 30% до приблизительно 70%, от приблизительно 30% до приблизительно 80%, от приблизительно 30% до приблизительно 90%, от приблизительно 30% до приблизительно 95%, от приблизительно 30% до приблизительно 99%, или от приблизительно 40% до приблизительно 100%, или в любом промежуточном диапазоне, по сравнению с полимеризацией тубулина и функцией BMI-1 до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В конкретном аспекте, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 позволяет ингибировать пролиферацию или снижать in vitro или in vivo популяцию пролиферирующих клеток или клеточных линий приблизительно на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 80%, 85%, 90%, 95% или 100%, по сравнению с in vitro или in vivo популяцией пролиферирующих клеток или клеточных линий до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В конкретном аспекте, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 позволяет ингибировать пролиферацию или снижать in vitro или in vivo популяцию пролиферирующих клеток или клеточных линий на величину в диапазоне от приблизительно 5% до приблизительно 20%, от приблизительно 10% до приблизительно 30%, от приблизительно 15% до приблизительно 40%, от приблизительно 15% до приблизительно 50%, от приблизительно 20% до приблизительно 30%, от приблизительно 20% до приблизительно 40%, от приблизительно 20% до приблизительно 50%, от приблизительно 30% до приблизительно 60%, от приблизительно 30% до приблизительно 70%, от приблизительно 30% до приблизительно 80%, от приблизительно 30% до приблизительно 90%, от приблизительно 30% до приблизительно 95%, от приблизительно 30% до приблизительно 99%, или от приблизительно 40% до приблизительно 100%, или в любом промежуточном диапазоне, по сравнению с in vitro или in vivo популяцией пролиферирующих клеток или клеточных линий до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В различных аспектах, описанный в изобретении способ ингибирования или снижения полимеризация тубулина и функции BMI-1 позволяет снижать концентрацию BMI-1 в плазме у субъекта, что оценивается с помощью хорошо известных методов, например, методом ELISA (твердофазным иммуноферментным анализом).
В одном аспекте, в изобретении описан способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение количества соединения 1, эффективного для ингибирования или снижения полимеризации тубулина и функции BMI-1 у субъекта.
В конкретном аспекте, в изобретении описан способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяющий ингибировать или снижать полимеризации тубулина и функцию BMI-1 приблизительно на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 80%, 85%, 90%, 95% или 100% по сравнению с полимеризацией тубулина и функцией BMI-1 до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В конкретном аспекте, описанный в изобретении способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяющий ингибировать или снижать полимеризации тубулина и функцию BMI-1 на величину в диапазоне от приблизительно 5% до приблизительно 20%, от приблизительно 10% до приблизительно 30%, от приблизительно 15% до приблизительно 40%, от приблизительно 15% до приблизительно 50%, от приблизительно 20% до приблизительно 30%, от приблизительно 20% до приблизительно 40%, от приблизительно 20% до приблизительно 50%, от приблизительно 30% до приблизительно 60%, от приблизительно 30% до приблизительно 70%, от приблизительно 30% до приблизительно 80%, от приблизительно 30% до приблизительно 90%, от приблизительно 30% до приблизительно 95%, от приблизительно 30% до приблизительно 99%, или от приблизительно 40% до приблизительно 100%, или в любом промежуточном диапазоне, по сравнению с полимеризацией тубулина и функцией BMI-1 до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В различных аспектах, описанный в изобретении способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяет снижать концентрацию BMI-1 у субъекта, что оценивается с помощью хорошо известных методов, например, методом ELISA.
В одном аспекте, в изобретении описан способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение количества соединения 1, эффективного для ингибирования пролиферации или снижения in vitro или in vivo популяции пролиферирующих клеток или клеточных линий у субъекта.
В конкретном аспекте, описанный в изобретении способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяет ингибировать пролиферацию или снижать in vitro или in vivo популяцию пролиферирующих клеток или клеточных линий у субъекта приблизительно на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 80%, 85%, 90%, 95% или 100% по сравнению пролифераций или in vitro или in vivo популяцией пролиферирующих клеток или клеточных линий у субъекта до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В конкретном аспекте, описанный в изобретении способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяет ингибировать пролиферацию или снижать in vitro или in vivo популяцию пролиферирующих клеток или клеточных линий у субъекта на величину в диапазоне от приблизительно 5% до приблизительно 20%, от приблизительно 10% до приблизительно 30%, от приблизительно 15% до приблизительно 40%, от приблизительно 15% до приблизительно 50%, от приблизительно 20% до приблизительно 30%, от приблизительно 20% до приблизительно 40%, от приблизительно 20% до приблизительно 50%, от приблизительно 30% до приблизительно 60%, от приблизительно 30% до приблизительно 70%, от приблизительно 30% до приблизительно 80%, от приблизительно 30% до приблизительно 90%, от приблизительно 30% до приблизительно 95%, от приблизительно 30% до приблизительно 99%, или от приблизительно 40% до приблизительно 100%, или в любом промежуточном диапазоне, по сравнению с пролиферацией или in vitro или in vivo популяцией пролиферирующих клеток или клеточных линий у субъекта до введения соединения 1 субъекту, что оценивается с помощью хорошо известных методов.
В различных аспектах, описанный в изобретении способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, позволяет ингибировать пролиферацию или снижать in vitro или in vivo популяцию пролиферирующих клеток или клеточных линий у субъекта, что оценивается с помощью хорошо известных методов, например, методом ELISA.
В одном аспекте, в изобретении описан способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение количества соединения 1, эффективного для ингибирования пролиферации или снижения in vitro или in vivo популяции пролиферирующих клеток или клеточных линий у субъекта, в комбинации с другой терапией (например, с одной или более дополнительными терапиями, при которых не применяют соединений 1, или при которых применяют другое антипролиферативное средство), субъекту, нуждающемуся в этом.
Такие способы могут включать введение соединения 1 до, одновременно или после применения дополнительной терапии. В конкретных аспектах, такие способы характеризуются наличием аддитивного или синергического эффекта.
В конкретном аспекте, в изобретении предлагается способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения 1 и эффективного количества эффективное количество другого лекарственного средства.
Конкретные примеры типов рака, которые могут быть предотвращены, подвергнуты лечению или облегчены с помощью предложенных в изобретении способов, включают, но этим не ограничивая, типы рака поджелудочной железы, такие как, но этим не ограничивая, протоковая аденокарцинома поджелудочной железы.
В конкретных аспектах, типы рака поджелудочной железы, которые могут быть предотвращены, подвергнуты лечению или облегчены с помощью предложенных в изобретении способов, выбирают из протоковой аденокарциномы поджелудочной железы.
В одном аспекте, в изобретении предложен способ профилактики, лечения или облегчения рака поджелудочной железы, включающий: (a) введение субъекту, нуждающемуся в этом, одной или более доз соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции; и (b) мониторинг концентрации конкретных биомаркеров до и/или после проведения стадии (a).
В конкретном аспекте, стадию мониторинга (b) проводят до и/или после определенного числа доз (например, 1, 2, 4, 6, 8, 10, 12, 14, 15 или 29 доз или более доз; от 2 до 4, от 2 до 8, от 2 до 20 или от 2 до 30 доз) или через определенный период времени (например, через 1, 2, 3, 4, 5, 6 или 7 дней; или через 1, 2, 3, 4, 5, 10, 15, 20, 30, 40, 45, 48 или 50 недель) введения соединение 1 или его фармацевтически приемлемой соли или фармацевтической композиции.
В конкретном аспекте, один или более из этих параметров мониторинга определяют до введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту.
В конкретном аспекте, снижение пролиферации in vitro или in vivo популяции пролиферирующих клеток или клеточных линий после введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции указывает, что курс лечения является эффективным с целью профилактики, лечения или облегчения рака поджелудочной железы.
В конкретном аспекте, изменение пролиферации in vitro или in vivo популяции пролиферирующих клеток или клеточных линий после введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции может указывать на то, что доза, частота и/или продолжительность введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции могут быть скорректированы (например, увеличены, уменьшены или сохранены на том же уровне).
В конкретном аспекте, мониторинг концентрации конкретных биомаркеров в биологических образцах субъекта проводят перед, в течение и/или после курса лечения рака поджелудочной железы, включающего введение соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту.
Доза, частота и/или продолжительность введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту могут быть изменены вследствие пролиферации in vitro или in vivo популяции пролиферирующих клеток или клеточных линий. В качестве варианта, изменения этих подвергаемых мониторингу параметров (например, концентрации конкретных биомаркеров) могут указывать на то, что курс лечения, включающий введение соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции, является эффективным для профилактики, лечения или облегчения рака поджелудочной железы.
Концентрация конкретных биомаркеров у субъекта может быть определена любым известным для специалиста в данной области методом. В конкретных аспектах, метод определения концентрации конкретных биомаркеров у субъекта включает получение биологического образца (например, образца ткани или жидкости) субъекта, и определение концентрации биомаркеров в биологическом образце (например, в плазме, сыворотке, моче или любых других биологических жидкостях), который был подвергнут конкретным типам обработки (например, центрифугированию), и определение с применением иммунологических методов, таких как твердофазный иммуноферментный анализ (ELISA).
В конкретном аспекте, описанный в изобретении способ твердофазного иммуноферментного анализа (ELISA) может быть использован для определения концентрации биомаркеров в биологическом образце (например, в плазме, сыворотке, моче или любых других биологических жидкостях), который был подвергнут конкретным типам обработки (например, центрифугированию). Другие известные методы, которые могут быть использованы для определения концентрации биомаркеров в биологическом образце, включают методы многоканального или протеомного анализа.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют облегчать или сдерживать развитие одного, двух или более симптомов, ассоциированных с раком поджелудочной железы. Облегчение или сдерживание развития одного, двух или более симптомов рака поджелудочной железы может быть использовано в качестве клинического результата по эффективности соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции для профилактики, лечения или облегчения рака поджелудочной железы. В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют снижать продолжительность и/или тяжесть одного или более симптомов, ассоциированных с раком поджелудочной железы. В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют ингибировать начало проявления, прогрессию и/или повторное проявление одного или более симптомов, ассоциированных с раком поджелудочной железы. В некоторых аспектах, предложенные в изобретении способы лечения рака поджелудочной железы позволяют уменьшать число симптомов, ассоциированных с раком поджелудочной железы.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют продлевать или задерживать фазу G1/S или последнюю фазу G1/S клеточного цикла (то есть, период между последней контрольной точкой (фазой покоя или предшествующей синтезу ДНК фазой) и фазой начального синтеза ДНК). В других аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют продлевать или задерживать фазу S или фазу G2/M клеточного цикла (то есть, период между синтезом ДНК и начальной фазой деления).
В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют уменьшать, облегчать или смягчать тяжесть рака поджелудочной железы и/или одного или более его симптомов. В других аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют снижать потребность в госпитализации (например, снижать частоту или продолжительность госпитализации) субъекта, у которого диагностирован рак поджелудочной железы.
В конкретных аспектах, предложенные в изобретении способы позволяют увеличивать срок выживания субъекта, у которого диагностирован рак поджелудочной железы. В конкретных аспектах, предложенные в изобретении способы позволяют увеличивать срок выживания субъекта, у которого диагностирован рак поджелудочной железы, приблизительно на 6 месяцев или более, приблизительно на 7 месяцев или более, приблизительно на 8 месяцев или более, приблизительно на 9 месяцев или более, или приблизительно на 12 месяцев или более.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют ингибировать или снижать прогрессирование рака поджелудочной железы или одного или более ассоциированным с ним симптомов. В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют усилить или улучшить терапевтический эффект от проведения другой терапии (например, применения противоракового средства, лучевой терапии, медикаментозной терапии, такой как химиотерапия, антиандрогенной терапии или хирургического вмешательства). В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы включают применение соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции в качестве вспомогательной терапии.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют понизить смертность субъектов, у которых диагностирован рак поджелудочной железы. В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличить число субъектов в состоянии ремиссии или уменьшить число случаев госпитализации. В других аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют предотвратить развитие, появление или прогрессирование одного или более симптомов, ассоциированных с раком поджелудочной железы.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличить выживаемость при отсутствии симптомов пациентов с раком поджелудочной железы. В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы не позволяют излечить рак поджелудочной железы у субъектов, но позволяют предотвратить прогрессирование или усугубление заболевания. В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют повысить качество жизни субъекта.
В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличивать число случаев выживаемости без признаков рака у субъектов, у которых диагностирован рак. В некоторых аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличить безрецидивную выживаемость. В конкретных аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличить число субъектов в состоянии ремиссии. В других аспектах, предложенные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы позволяют увеличивать продолжительность ремиссии у субъектов.
Подвергаемая лечению группа пациентов
В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, который имеет или у которого диагностирован рак поджелудочной железы. В других аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, который предрасположен или склонен к заболеванию раком поджелудочной железы. В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек с повышенным риском развития рака поджелудочной железы.
В одном аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является младенец. В другом аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является ребенок преддошкольного возраста. В другом аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является ребенок. В другом аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является взрослый человек. В другом аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек среднего возраста. В другом аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек пожилого возраста.
В конкретных аспектах, субъект, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, имеет рак поджелудочной железы, метастазирующий в другие области организма, такие как кости, легкое и печень. В конкретных аспектах, субъект, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами находится в состоянии ремиссии рака поджелудочной железы. В некоторых аспектах, субъект, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами имел рецидив рака поджелудочной железы. В конкретных аспектах, субъект, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами испытывает повторное проявление одного или более симптомов, ассоциированных с раком поджелудочной железы.
В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек в возрасте от приблизительно 1 до приблизительно 5 лет, от приблизительно 5 до приблизительно 10 лет, от приблизительно 10 до приблизительно 18 лет, от приблизительно 18 до приблизительно 30 лет, от приблизительно 25 до приблизительно 35 лет, от приблизительно 35 до приблизительно 45 лет, от приблизительно 40 до приблизительно 55 лет, от приблизительно 50 до приблизительно 65 лет, от приблизительно 60 до приблизительно 75 лет, от приблизительно 70 до приблизительно 85 лет, от приблизительно 80 до приблизительно 90 лет, от приблизительно 90 до приблизительно 95 лет или от приблизительно 95 до приблизительно 100 лет, или в возрасте в любом из промежутков между указанными диапазонами.
В конкретном аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек в возрасте 18 лет или старше. В конкретном аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является ребенок в возрасте от 1 года до 18 лет. В конкретном аспекте, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек в возрасте от 12 лет до 18 лет. В конкретном аспекте, субъектом является мужчина. В другом аспекте, субъектом является женщина. В одном аспекте, субъектом является женщина, которая не является беременной или которая в данный момент не кормит младенца грудью. В одном аспекте, субъектом является женщина, которая является беременной или будет/может стать беременной, или которая в данный момент кормит младенца грудью.
В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, который находится в состоянии нарушенного иммунитета или в состоянии ослабленного иммунитета. В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, в отношении которого проводят иммуносупрессивную терапию или который восстанавливается после иммуносупрессивной терапии. В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, который имеет рак поджелудочной железы или подвергаются риску развития у него рака поджелудочной железы. В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, в отношении которого проводятся, будут проводится или уже проведены хирургическое вмешательство, медикаментозная терапия, такая как химиотерапия, гормональная терапия и/или лучевая терапия.
В некоторых аспектах, субъекту, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, вводят соединение 1 или его фармацевтически приемлемую соль или фармацевтическую композицию, или проводят комбинированную терапию до развития нежелательных отрицательных эффектов или непереносимости к терапиям, которые не являются терапиями с применением соединения 1. В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является невосприимчивый к лечению субъект. В конкретных аспектах, невосприимчивым к лечению субъектом является субъект, невосприимчивый к лечению при применении стандартной терапии (например, хирургического вмешательства, лучевой терапии и/или медикаментозной терапии, такой как химиотерапия). В конкретных аспектах, субъект с раком поджелудочной железы является невосприимчивым к лечению при проведении терапии, когда рак поджелудочной железы не был в значительной степени устранен и/или не были в значительной степени облегчены один или более симптомов. Определение того, что субъект является невосприимчивым к лечению, может быть проведено либо in vivo, либо in vitro, любым известным методом анализа эффективности лечения рака поджелудочной железы, используя в таком контексте общепринятые значения термина "невосприимчивый к лечению".
В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, по поводу которого было доказано, что он является невосприимчивым к лечению с помощью терапий, которые не являются терапиями с применением соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции, и он более не подвергается лечению с помощью этих терапий. В конкретных аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, который уже был подвергнут лечению с помощью одной или более традиционных противораковых терапий, таких как хирургическое вмешательство, медикаментозная терапия, такая как химиотерапия, антиандрогенная терапия или лучевая терапия. К этим субъектам относятся невосприимчивые к лечению субъекты, субъекты, которые являются слишком молодыми для применения на них традиционных терапий, и субъекты с рецидивирующими видами рака поджелудочной железы несмотря на проведение лечения с помощью существующих терапий.
В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, у которого проведение традиционных терапий вызывает нежелательные побочные эффекты. В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, в отношении которого не проводилась терапия, например, медикаментозная терапия, такая как химиотерапия, хирургическое вмешательство, антиандрогенная терапия или лучевая терапия, до введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции. В других аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, в отношении которого была проведена терапия до введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции. В некоторых аспектах, субъектом, которого подвергают лечению по поводу рака поджелудочной железы в соответствии с предлагаемыми в изобретении способами, является человек, у которого предшествующая терапия вызывала нежелательные побочные эффекты или в отношении которого предшествующую терапию отменяли вследствие недопустимых уровней токсичности для человека.
Дозирование и введение
В соответствии с предложенными в изобретении способами профилактики, лечения или облегчения рака поджелудочной железы, соединение 1 или его фармацевтически приемлемая соль или фармацевтическая композиция могут быть введены субъекту, нуждающемуся в этом, различными способами в количествах, которые позволяют достигать положительного или терапевтического эффекта. Соединение 1 или его фармацевтически приемлемая соль или фармацевтическая композиция могут быть перорально введены субъекту, нуждающемуся в этом, в соответствии с предложенными в изобретении способами профилактики, лечения или облегчения рака поджелудочной железы. Пероральное введение соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции может облегчать субъектам, нуждающимся в таком лечении, соблюдать схему приема соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции. Так, например, в конкретном аспекте, соединение 1 или его фармацевтически приемлемую соль или фармацевтическую композицию перорально вводят субъекту, нуждающемуся в этом. В другом аспекте, предлагаемые в изобретении соединение 1 или его фармацевтически приемлемая соль или фармацевтическая композиция могут быть введены перорально вместе с пищей или водой или без пищи или воды.
Другие способы введения включают, но этим не ограничивая, внутривенное, интрадермальное, интратекальное, внутримышечное, подкожное, интраназальное, ингаляционное, трансдермальное, местное, трансмукозальное, интракраниальное, эпидуральное и интрасиновиальное введение. В одном аспекте, соединение 1 или его фармацевтически приемлемую соль или фармацевтическую композиции вводят системно (например, парентерально) субъекту, нуждающемуся в этом. В одном аспекте, соединение 1 или его фармацевтически приемлемую соль или фармацевтическую композицию вводят с помощью способа, который позволяет преодолеть соединение 1 или его фармацевтически приемлемой соли или фармацевтической композиции гематоэнцефалический барьер (например, перорально).
В соответствии с предложенными в изобретении способами профилактики, лечения или облегчения рака поджелудочной железы, которые включают введение соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции в комбинации с одной или более дополнительными терапиями, соединение 1 или его фармацевтически приемлемая соль или фармацевтическая композиция и одно или более дополнительных терапевтических средств могут быть введены одним и тем же способом или разными способами введения.
Доза и частота введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту, нуждающемуся в этом, в соответствии с предложенными в изобретении способами профилактики, лечения или облегчения рака поджелудочной железы, будут являться эффективными в случае минимизации любых побочных эффектов. Точная доза и частота введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции может быть определена лечащим врачом с учетом факторов, относящихся к субъекту, которому необходимо проведение лечения.
Факторы, которые могут быть приняты во внимание, включают тяжесть болезненного состояния, общее состояние здоровья субъекта, возраст, массу тела и пол субъекта, режим питания, время и частоту введения, комбинацию лекарственных средств (комбинации лекарственных средств), чувствительность к воздействию препаратов, и резистентность/восприимчивость к терапии. Доза и частота введения соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции могут быть скорректированы в течение некоторого времени с целью обеспечения эффективного количества соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции или с целью поддержания требуемого эффекта.
Как было описано выше, представленные в изобретении способы профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включают введение субъекту эффективного количества соединение 1 или его фармацевтически приемлемой соли или фармацевтической композиции, где эффективное количество представляет собой дозу, вводимую субъекту два раза в неделю в различные дни, где вторую дозу в неделю вводят после первой дозой через три дня, и где первую дозу на следующей неделе вводят после второй дозы, введенной на предшествующей неделе, через четыре дня.
В конкретном аспекте, эффективное количество представляет собой вводимую субъекту дозу, которая может быть увеличена или уменьшена в зависимости от ответа субъекта на лечение.
В конкретном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, выбранную из дозы в диапазоне от приблизительно 50 мг до приблизительно 200 мг, от приблизительно 100 мг до приблизительно 200 мг, от приблизительно 150 мг до приблизительно 200 мг, и другом подобном диапазоне, или в любом промежутке между ними, вводимую перорально два раза в неделю.
В конкретном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, выбранную из приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг, и другой подобной дозы, или в любом промежутке между ними, вводимую перорально два раза в неделю.
В конкретном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтически приемлемой соли или фармацевтической композиции субъекту, где эффективное количество представляет собой дозу приблизительно 50 мг, вводимую перорально два раза в неделю.
В некоторых аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая выражена в мг на квадратный метр (мг/м2). Доза, выраженная в мг/м2, для соединения 1 может быть определена, например, путем умножения коэффициента пересчета для животного на дозу для животного в мг на килограмм (мг/кг) с получением дозы в мг/м2, являющейся эквивалентной дозой для человека. Для регуляторных целей, могут быть использованы следующие коэффициенты пересчета: мышь=3, хомяк=4,1, крыса=6, морская свинка=7,7 (на основе публикации Freireich et al., Cancer Chemother. Rep. 50(4):219-244 (1966)). Рост и масса тела человека могут быть использованы для расчета площади поверхности тела человека, применяя формулу Бойда для расчета площади поверхности тела. В конкретных аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой количество в диапазоне от приблизительно 0,1 мг/м2 до приблизительно 1000 мг/м2, или в любом промежутке между этими величинами.
В одном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая позволяет достигать целевой средней концентрации соединения 1 в плазме у субъекта с раком поджелудочной железы или в экспериментальной модели предварительно ксенотрансплантированного рака поджелудочной железы на животном.
В конкретном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая позволяет достигать средней концентрации соединения 1 в плазме через 24 часа в диапазоне от приблизительно 3 час·мкг/мл до приблизительно 70 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 60 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 50 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 40 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 30 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 20 час·мкг/мл, от приблизительно 3 час·мкг/мл до приблизительно 10 час·мкг/мл, и в другом подобном диапазоне, или в любом диапазоне между ними, у субъекта с раком поджелудочной железы или в экспериментальной модели предварительно ксенотрансплантированного рака поджелудочной железы на животном.
В конкретном аспекте, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая позволяет достигать средней концентрации соединения 1 в плазме через 24 часа приблизительно 3 час·мкг/мл, приблизительно 10 час·мкг/мл, приблизительно 20 час·мкг/мл, приблизительно 30 час·мкг/мл, приблизительно 40 час·мкг/мл, приблизительно 50 час·мкг/мл, приблизительно 60 час·мкг/мл, приблизительно 70 час·мкг/мл, и другого подобного значения, или в любом диапазоне между ними, у субъекта с раком поджелудочной железы или в экспериментальной модели предварительно ксенотрансплантированного рака поджелудочной железы на животном.
Для достижения таких концентраций в плазме, может быть введена описанная в изобретении доза соединения 1 или его фармацевтической композиции. В конкретных аспектах, последующие дозы соединения 1 или его фармацевтической композиции могут быть скорректированы соответствующим образом на основе средних концентраций соединения 1 в плазме, достигаемых при вводимой пациенту дозы соединения 1 или его фармацевтической композиции.
В конкретных аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая позволяет достигать снижения средней целевой концентрации одного или более биомаркеров в плазме у субъекта с раком поджелудочной железы или в экспериментальной модели предварительно ксенотрансплантированного рака поджелудочной железы на животном.
В конкретных аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество представляет собой дозу, которая позволяет достигать требуемых отношений концентраций соединения 1 или его фармацевтической композиции в ткани к средним концентрациям в плазме, определяемых, например, с помощью любых известных методов визуализации, у субъекта с раком поджелудочной железы или в экспериментальной модели предварительно ксенотрансплантированного рака поджелудочной железы на животном.
В некоторых аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение эффективного количества соединения 1 или его фармацевтической композиции субъекту, где эффективное количество может быть или может не быть одинаковым для каждой дозы. В конкретных аспектах, первую (то есть, начальную) дозу соединения 1 или его фармацевтической композиции вводят субъекту, нуждающемуся в этом, в течение первого периода времени, затем вводят субъекту вторую (то есть, нагрузочную) дозу соединения 1 или его фармацевтической композиции в течение второго периода времени и, затем, вводят субъекту третью (то есть, поддерживающую) дозу соединения 1 или его фармацевтической композиции в течение второго периода времени. Первая доза может быть большей, чем вторая доза, или первая доза может быть меньшей, чем вторая доза. Аналогичным образом, третья доза соединения 1 или его фармацевтической композиции может быть большей или меньшей, чем вторая доза, и большей или меньшей, чем первая доза.
В некоторых аспектах, описанные в изобретении величины доз относятся к суммарно вводимым величинам; то есть, если вводят более чем одно соединение 1, то тогда, в некоторых аспектах, дозы соответствуют суммарно вводимой величине. В конкретном аспекте, пероральные композиции содержат от приблизительно 5% до приблизительно 95% соединения 1 по массе.
Продолжительность времени, в течение которого вводят соединение 1 или его фармацевтическую композицию субъекту, нуждающемуся в этом, в соответствии со способом профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, будет представлять собой период времени, который определяется выживаемостью без признаков рака или выживаемостью в отсутствии симптомов. В конкретных аспектах, представленный в изобретении способ лечения рака поджелудочной железы включает введение соединения 1 или его фармацевтической композиции в течение периода времени до тех пор, пока не снижается тяжесть и/или количество из одного или более симптомов, ассоциированных с раком поджелудочной железы.
В некоторых аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение соединения 1 или его фармацевтической композиции в течение вплоть до 48 недель. В других аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение соединения 1 или его фармацевтической композиции в течение вплоть до 4 недель, 8 недель, 12 недель, 16 недель, 20 недель, 24 недель, 26 недель (0,5 года), 52 недель (1 года), 78 недель (1,5 лет), 104 недель (2 лет) или 130 недель (2,5 лет) или более.
В конкретных аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение соединения 1 или его фармацевтической композиции в течение неопределенного периода времени. В некоторых аспектах, представленный в изобретении способ лечения рака поджелудочной железы включает введение соединения 1 или его фармацевтической композиции в течение периода времени, за которым следует период отдыха (то есть, период, в течение которого соединение 1 или его фармацевтическую композицию не вводят), и затем введение соединения 1 или его фармацевтической композиции возобновляют.
В конкретных аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение соединения 1 или его фармацевтической композиции циклами, например, циклами в 1 неделю, циклами в 2 недели, циклами в 3 недели, циклами в 4 недели, циклами в 5 недель, циклами в 6 недель, циклами в 8 недель, циклами в 9 недель, циклами в 10 недель, циклами в 11 недель или циклами в 12 недель. В таких циклах, соединение 1 или его фармацевтическая композиция могут быть введены один или два раза в неделю. В конкретном аспекте недельного цикла, соединение 1 или его фармацевтическая композиция могут быть введены два раза в неделю. В конкретном аспекте такого недельного цикла, соединение 1 или его фармацевтическая композиция могут быть введены один раз в день.
В конкретных аспектах, период времени введения соединения 1 или его фармацевтической композиции может быть обусловлен одним или более подвергаемых мониторингу параметров, например, концентрацией конкретных биомаркеров.
В конкретных аспектах, период времени введения соединения 1 или его фармацевтической композиции может быть скорректирован на основе одного или более подвергаемых мониторингу параметров, например, концентрации биомаркеров.
В конкретных аспектах, в соответствии со способом профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, соединение 1 или его фармацевтическую композицию вводят субъекту, нуждающемуся в этом, до принятия пищи, в процессе принятия пищи или после принятия пищи (например, до, в процессе или после завтрака, обеда или ужина). В конкретных аспектах, в соответствии с представленными в изобретении способами лечения рака поджелудочной железы, соединение 1 или его фармацевтическую композицию вводят субъекту, нуждающемуся в этом, утром (например, между 5 часами утра и 12 часами по полудню).
В конкретных аспектах, в соответствии со способом профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, соединение 1 или его фармацевтическую композицию вводят субъекту, нуждающемуся в этом, в полдень (то есть, 12 по полудню). В конкретных аспектах, в соответствии с представленными в изобретении способами лечения рака поджелудочной железы, соединение 1 или его фармацевтическую композицию вводят субъекту, нуждающемуся в этом, днем (например, между 12 часами и 17 по полудню), вечером (например, между 17 часами по полудню и временем отхода ко сну), и/или перед сном.
В конкретном аспекте, дозу соединения 1 или его фармацевтической композиции вводят субъекту один раз в сутки и два раза в неделю.
Комбинированные терапии
В изобретении представлены комбинированные терапии для лечения рака поджелудочной железы, которые включают введение соединения 1 или его фармацевтической композиции в комбинации с одним или более дополнительными терапевтическими средствами субъекту, нуждающемуся в этом. В конкретном аспекте, в изобретении представлены комбинированные терапии для лечения рака поджелудочной железы, которые включают введение эффективного количества соединения 1 или его фармацевтической композиции в комбинации с эффективным количеством другого терапевтического средства субъекту, нуждающемуся в этом.
Используемый в изобретении термин "в комбинации" применительно к введению соединения 1 или его фармацевтической композиции, относится к введению соединения 1 или его фармацевтической композиции до применения, одновременно с применением или после применения одной или более дополнительных терапий (например, лекарственных средств, хирургического вмешательства или лучевой терапии) для использования при лечении рака поджелудочной железы. Использование термина "в комбинации" не ограничивает порядок, в котором одно или более терапевтических средств и одну или более дополнительных терапий применяли в отношении субъекта. В конкретных аспектах, интервал времени между введением соединения 1 или его фармацевтической композиции и применением одной или более дополнительных терапий может составлять приблизительно 1-5 минут, 1-30 минут, от 30 минут до 60 минут, 1 час, 1-2 часа, 2-6 часов, 2-12 часов, 12-24 часа, 1-2 дня, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 7 недель, 8 недель, 9 недель, 10 недель, 15 недель, 20 недель, 26 недель, 52 недели, 11-15 недель, 15-20 недель, 20-30 недель, 30-40 недель, 40-50 недель, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 1 год, 2 года, или любой период времени между ними. В конкретных аспектах, соединение 1 или его фармацевтическую композицию и одну или более дополнительных терапий применяют раздельно с интервалом 1 день, 1 неделя, 2 недели, 3 недели, 4 недели, один месяц, 2 месяца, 3 месяца, 6 месяцев, 1 год, 2 года или 5 лет.
В некоторых аспектах, предложенные в изобретении комбинированные терапии включают введение соединения 1 или его фармацевтической композиции ежедневно и применение одной или более дополнительных терапий один раз в неделю, один раз каждые 2 недели, один раз каждые 3 недели, один раз каждые 4 недели, один раз каждый месяц, один раз каждые 2 месяца (например, приблизительно 8 недель), один раз каждые 3 месяца (например, приблизительно 12 недель) или один раз каждые 4 месяца (например, приблизительно 16 недель). В конкретных аспектах, соединение 1 или его фармацевтическую композицию и одну или более дополнительных терапий применяют циклически в отношении к субъекту. Циклически повторяющаяся терапия включает введение соединения 1 или его фармацевтической композиции в течение некоторого периода времени, затем применение одной или более дополнительных терапий в течение некоторого периода времени, и повторение этого последовательного применения. В конкретных аспектах, циклически повторяющаяся терапия может также включать период отдыха, когда соединение 1 или его фармацевтическую композиции или дополнительную терапию не применяют в течение некоторого периода времени (например, в течение 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 1 недели, 2 недель, 3 недель, 4 недель, 5 недель, 10 недель, 20 недель, 1 месяца, 2 месяцев, 3 месяцев, 4 месяцев, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 2 лет или 3 лет). В одном аспекте, число применяемых циклов составляет от 1 до 12 циклов, от 2 до 10 циклов или от 2 до 8 циклов.
В некоторых аспектах, способ профилактики, лечения или облегчения рака поджелудочной железы у субъекта, нуждающегося в этом, включает введение соединения 1 или его фармацевтической композиции в качестве монотерапии в течение некоторого периода времени перед введением соединения 1 или его фармацевтической композиции в комбинации с дополнительной терапией. В конкретных аспектах, предложенные в изобретении способы лечения рака поджелудочной железы включают применение только одной дополнительной терапии в течение некоторого периода времени перед введением соединения 1 или его фармацевтической композиции в комбинации с дополнительной терапией.
В некоторых аспектах, введение соединения 1 или его фармацевтической композиции и применение одной или более дополнительных терапий в соответствии с представленными в изобретении способами характеризуется аддитивным эффектом по сравнению с введением соединения 1 или его фармацевтической композиции или применения указанных одной или более дополнительных терапий по отдельности. В некоторых аспектах, введение соединения 1 или его фармацевтической композиции и применение одной или более дополнительных терапий в соответствии с представленными в изобретении способами характеризуется синергическим эффектом по сравнению с введением соединения 1 или его фармацевтической композиции или применения указанных одной или более дополнительных терапий по отдельности.
Используемый в изобретении термин "синергический" относится к эффекту, достигаемому при введении соединения 1 или его фармацевтической композиции в комбинации с одной или более дополнительными терапиями (например, с лекарственными средствами), при котором комбинация является более эффективной, чем аддитивные эффекты любых двух или более каждой в отдельности терапий (например, лекарственных средств).
В конкретном аспекте, синергический эффект комбинированной терапии позволяет использовать более низкие дозы (то есть, дозы ниже оптимальных) соединения 1 или его фармацевтической композиции или дополнительного терапевтического средства, и/или менее частое введение соединения 1 или его фармацевтической композиции или дополнительного терапевтического средства субъекту.
В конкретных аспектах, возможность использовать более низкие дозы соединения 1 или его фармацевтической композиции или дополнительного терапевтического средства, и/или вводить соединение 1 или его фармацевтическую композицию или указанное дополнительное терапевтическое средство менее часто позволяет снижать токсичность, ассоциированную с введением соединения 1 или его фармацевтической композиции или указанного дополнительного терапевтического средства, соответственно, субъекту без снижения эффективности соединения 1 или его фармацевтической композиции или указанного дополнительного терапевтического средства, соответственно, при лечении рака поджелудочной железы.
В некоторых аспектах, синергический эффект приводит к повышению эффективности соединения 1 или его фармацевтической композиции и каждой из указанных дополнительных терапий при лечении рака поджелудочной железы. В некоторых аспектах, синергический эффект комбинации соединения 1 или его фармацевтической композиции и одной или более дополнительных терапий предотвращает или снижает неблагоприятные или нежелательные побочные эффекты, ассоциированные с применением любой только одной единственной терапии.
Комбинация соединения 1 или его фармацевтической композиции и одного или более дополнительных терапевтических средств может быть введена субъекту в одной и той же фармацевтической композиции. В качестве варианта, соединение 1 или его фармацевтическая композиция и одно или более дополнительных терапевтических средств могут быть введены одновременно субъекту в раздельных фармацевтических композициях. Соединение 1 или его фармацевтическая композиция и одно или более дополнительных терапевтических средств могут быть введены последовательно субъекту в раздельных фармацевтических композициях. Соединение 1 или его фармацевтическая композиция и одно или более дополнительных терапевтических средств могут быть также введены субъекту одним и тем же или разными способами введения.
Предложенные в изобретении комбинированные терапии включают введение субъекту, нуждающемуся в этом, соединения 1 или его фармацевтической композиции в комбинации с традиционными или известными терапиями для лечения рака поджелудочной железы. Другие терапии для рака поджелудочной железы или ассоциированного с ним состояния предназначены для контроля или облегчения одного или более симптомов. Соответственно, в некоторых аспектах, предложенные в изобретении комбинированные терапии включают введение субъекту, нуждающемуся в этом, болеутоляющее лекарственное средство или другие терапевтические средства, направленные на облегчение или контролирование одного или более симптомов, ассоциированных с раком поджелудочной железы или ассоциированного с ним состояния.
Конкретные примеры противораковых средств, которые могут быть использованы в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают: гормональное средство (например, ингибитор ароматазы, селективный модулятор эстрогеновых рецепторов (SERM), и антагонист эстрогеновых рецепторов), химиотерапевтическое средство (например, ингибитор разборки микротрубочек, антиметаболит, ингибитор топоизомеразы и кросслинкер для ДНК или повреждающее ДНК средство), антиангиогенное средство (например, антагонист VEGF, антагонист рецептора, антагонист интегрина, средство для целенаправленного воздействия на кровеносные сосуды (vta)/средство для разрушения кровеносных сосудов (vda)), лучевую терапию и традиционное хирургическое вмешательство.
Неограничивающие примеры гормональных средств, которые могут быть использованы в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают ингибиторы ароматазы, селективные модуляторы эстрогеновых рецепторов (SERM) и антагонист эстрогеновых рецепторов. Гормональные средства, которые представляют собой ингибиторы ароматазы, могут быть стероидными или нестероидными. Неограничивающие примеры нестероидных гормональных средств включают летрозол, анастрозол, аминоглутетимид, фадрозол и ворозол. Неограничивающие примеры стероидных гормональных средств включают аромазин (эксеместан), форместан и тестолактон. Неограничивающие примеры гормональных средств, которые являются селективными модуляторами эстрогеновых рецепторов (SERM), включают тамоксифен (который продают под фирменным названием нолвадекс®), афимоксифен, арзоксифен, базедоксифен, кломифен, фемарелле, лазофоксифен, ормелоксифен, ралоксифен и торемифен. Неограничивающие примеры гормональных средств, которые являются антагонистами эстрогеновых рецепторов, включают фулвестрант. Другие гормональные средства включают, но этим не ограничивая, абиратерон и лонаприсан.
Неограничивающие примеры химиотерапевтических средств, которые могут быть использованы в комбинации с соединением 1 или его фармацевтической композицией для лечения рака, включают ингибитор разборки микротрубочек, антиметаболит, ингибитор топоизомеразы и кросслинкер для ДНК или повреждающее ДНК средство.
Химиотерапевтические средства, которые являются ингибиторами разборки микротрубочек, включают, но этим не ограничивая, таксены (например, паклитаксел (который продают под фирменным названием таксол®), доцетаксел, наб-паклитаксел (связанный с наночастицами альбумина паклитаксел, который продают под фирменным названием абраксан®), ларотаксел, ортатаксел и тезетаксел); эпотилоны (например, иксабепилон); и алкалоиды барвинка (например, винорелбин, винбластин, виндезин и винкристин (который продают под фирменным названием онковин®)).
Химиотерапевтические средства, которые являются антиметаболитами, включают, но этим не ограничивая, фолатные антиметаболиты (например, метотрексат, аминоптерин, пеметрексед, ралтитрексед); пуриновые антиметаболиты (например, кладрибин, клофарабин, флударабин, меркаптопурин, пентостатин, тиогуанин); пиримидиновые антиметаболиты (например, 5-фторурацил, капецитабин, гемцитабин (гемзар®), цитарабин, децитабин, флоксуридин, тегафур); и дезоксирибонуклеотидные антиметаболиты (например, гидроксимочевину).
Химиотерапевтические средства, которые являются ингибиторами топоизомеразы, включают, но этим не ограничивая, ингибиторы топоизомеразы класса I (камптотеки) (например, топотекан (который продают под фирменным названием гикамтин®) иринотекан, рубитекан и белотекан); ингибиторы топоизомеразы класса II (подофилла) (например, этопозид или VP-16, и тенипозид); антрациклины (например, доксорубицин, эпирубицин, доксил, акларубицин, амрубицин, даунорубицин, идарубицин, пирарубицин, валрубицин и зорубицин); и антрацендионы (например, митоксантрон и пиксантрон).
Химиотерапевтические средства, которые являются кросслинкерами для ДНК (или повреждающими ДНК средствами), включают, но этим не ограничивая, алкилирующие средства (например, циклофосфамид, мехлоретамин, ифосфамид (который продают под фирменным названием ифекс®), трофосфамид, хлорамбуцил, мелфалан, преднимустин, бендамустин, урамустин, эстрамустин, кармустин (который продают под фирменным названием BiCNU®), ломустин, семустин, фотемустин, нимустин, ранимустин, стрептозоцин, бусульфан, манносульфан, треосульфан, карбоквон, N, N'N'-триэтилентиофосфорамид, триазиквон, триэтиленмеламин); средства, подобные алкилирующим средствам (например, карбоплатин (который продают под фирменным названием параплатин®), цисплатин, оксалиплатин, недаплатин, триплатина тетранитрат, сатраплатин, пикоплатин); неклассические кросслинкеры для ДНК (например, прокарбазин, дакарбазин, темозоломид (который продают под фирменным названием темодар®), алтретамин, митобронитол); и интеркалирующие средства (например, актиномицин, блеомицин, митомицин и пликамицин).
Неограничивающие примеры антиангиогенных средств, которые могут быть использованы в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают антагонисты VEGF, антагонисты рецепторов, антагонисты интегрина (например, витаксин, циленгитид и S247) и средства для целенаправленного воздействия на кровеносные сосуды (vta)/средства для разрушения кровеносных сосудов (vda) (например, фосбретабулин). Антагонисты VEGF включают, но этим не ограничивая, антитела против VEGF (например, бевацизумаб (который продают под фирменным названием авастин®) и ранибизумаб (который продают под фирменным названием люцентис®)), ловушки VEGF (например, афлиберцепт), антисмысловая или миРНК или микроРНК VEGF и аптамеры (например, пегаптаниб (который продают под фирменным названием макуген®)). Антиангиогенные средства, которые являются антагонистами рецепторов, включают, но этим не ограничивая, антитела (например, рамуцирумаб) и ингибиторы киназ (например, сунитиниб, сорафениб, цедираниб, панзопаниб, вандетаниб, акситиниб и AG-013958), такие как ингибиторы тирозинкиназы. Другие неограничивающие примеры антиангиогенных средств включают ATN-224, анекортав ацетат (который продают под фирменным названием ретаан®), ингибитор деполимеризации микротрубочек, такой как пролекарство комбретастатин A4, и белок или белковый фрагмент, такой как коллаген 18 (эндостатин).
Неограничивающие примеры других терапевтических средств, которые могут быть введены субъекту в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают:
(1) статин, такой как ловостатин (например, который продают под фирменным названием мевакор®);
(2) ингибитор mTOR, такой как сиролимус, который известен также как рапамицин (например, который продают под фирменным названием рапамун®), темсиролимус (например, который продают под фирменным названием торисел®), эверолимус (например, который продают под фирменным названием афинитор®), и дефоролимус;
(3) ингибитор фарнезилтрансферазы, такой как типифарниб (например, который продают под фирменным названием зарнестра®);
(4) противофиброзное средство, такое как пирфенидон;
(5) пегилированный интерферон, такой как PEG-интерферон альфа-2b;
(6) стимулятор ЦНС, такой как метилфенидат (который продают под фирменным названием риталин®);
(7) антагонист HER-2, такой как антитело против HER-2 (например, трастузумаб) и ингибитор киназ (например, лапатиниб);
(8) антагонист IGF-1, такой как антитело против IGF-1 (например, AVE1642 и IMC-A11) или ингибитор киназы IGF-1;
(9) антагонист EGFR/HER-1, антитело против EGFR (например, цетуксимаб, панитумумаб) или ингибитор киназы EGFR (например, эрлотиниб (например, который продают под фирменным названием тарцева ®), гефитиниб);
(10) антагонист SRC, такой как босутиниб;
(11) ингибитор циклинзависимой киназы (CDK), такой как селициклиб;
(12) ингибитор Янус-киназы 2, такой как лестауртиниб;
(13) ингибитор протеасомы, такой как бортезомиб;
(14) ингибитор фосфодиэстеразы, такой как анагрелид;
(15) ингибитор инозинмонофосфатдегидрогеназы, такой как тиазофурин;
(16) ингибитор липоксигеназы, такой как масопрокол;
(17) антагонист эндотелина;
(18) антагонист ретиноидного рецептора, такой как третиноин или алитретиноин;
(19) иммуномодулятор, такой как леналидомид, помалидомид или талидомид (например, который продают под фирменным названием талидомид®);
(20) ингибитор киназы (например, тирозинкиназы), такой как иматиниб (например, который продают под фирменным названием гливек®), дазатиниб, эрлотиниб, нилотиниб, гефитиниб, сорафениб, сунитиниб (например, который продают под фирменным названием сутент®), лапатиниб, AEE788 или TG100801;
(21) нестероидное противовоспалительное средство, такое как целекоксиб (который продают под фирменным названием целебрекс®);
(22) человеческий гранулоцитарный колониестимулирующий фактор (G-CSF), такой как филграстим (который продают под фирменным названием нейпоген®);
(23) фолиниевая кислота или лейковорин кальция;
(24) антагонист интегрина, такой как α5β1-антагонист интегрина (например, JSM6427);
(25) антагонист ядерного фактора каппа-бета (NF-κβ), такой как OT-551, который является также антиоксидантом;
(26) ингибитор сигнального пути hedgehog, такой как CUR61414, циклопамин, GDC-0449, или антитело против hedgehog;
(27) ингибитор гистондеацетилазы (HDAC), такой как SAHA (также называемый вориностатом (который продают под фирменным названием золинза®)), PCI-24781, SB939, CHR-3996, CRA-024781, ITF2357, JNJ-26481585 или PCI-24781;
(28) ретиноид, такой как изотретиноин (например, который продают под фирменным названием аккутан®);
(29) антагонист фактор роста гепатоцитов/рассеивающего фактора (HGF/SF), такой как HGF/SF моноклональное антитело (например, AMG 102);
(30) синтетическое химическое вещество, такое как антинеопластон;
(31) противодиабетическое средство, такое как росиглитазона малеат (например, который продают под фирменным названием авандия®);
(32) противомалярийное и амебоцидное средство, такое как хлорохин (например, который продают под фирменным названием арален®);
(33) синтетический брадикинин, такой как RMP-7;
(34) ингибитор рецептора фактора роста тромбоцитов, такой как SU-101;
(35) ингибиторы рецепторов тирозин киназы Flk-1/KDR/VEGFR2, FGFR1 и PDGFR бета, такие как SU5416 и SU6668;
(36) противовоспалительное средство, такое как сульфасалазин (например, который продают под фирменным названием азулфидин®); и
(37) TGF-бета антисмысловая терапия.
Неограничивающие примеры других терапевтических средств, которые могут быть введены субъекту в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают: синтетический нанопептидный аналог природного гонадотропин-высвобождающего гормона, такой как лейпролид ацетат (который продают под фирменным названием люпрон®); нестероидный антиандроген, такой как флутамид (который продают под фирменным названием эулексин®) или нилутамид (который продают под фирменным названием ниландрон®); нестероидный ингибитор андрогенового рецептора, такой как бикалутамид (который продают под фирменным названием касодекс®); стероидный гормон, такой как прогестерон; противогрибковой средство, такое как кетоконазол (который продают под фирменным названием низорал®); глюкокортикоид, такой как преднизон; эстрамустин фосфат натрий (который продают под фирменным названием эмцит®); и бисфосфонат, такой как памидронат, алендронат и ризедронат.
Дополнительные конкретные примеры терапевтических средств, которые могут быть использованы в комбинации с соединением 1 или его фармацевтической композицией для лечения рака поджелудочной железы, включают, но этим не ограничивая, средства, ассоциированные с противораковой иммунотерапией (например, цитокины, интерлейкины и противораковые вакцины).
Конкретные примеры средств, снижающих побочные эффекты, ассоциированные с раком поджелудочной железы, которые могут быть использованы в качестве терапевтических средств в комбинации с соединением 1 или его фармацевтической композицией, включают, но этим не ограничивая: противорвотные средства, например, ондансетрон гидрохлорид (который продают под фирменным названием зофран®), гранисетрона гидрохлорид (который продают под фирменным названием китрил®), лоразепам (который продают под фирменным названием ативан®) и дексаметазон (который продают под фирменным названием декадрон®).
В конкретных аспектах, предложенные в изобретении комбинированные терапии для лечения рака поджелудочной железы включают введение соединения 1 или его фармацевтической композиции в комбинации с одним или более средствами, используемыми для лечения и/или сдерживания развития побочного эффекта, такого как, кровотечение (обычно кратковременное незначительное кровотечение из носа), артериальный или венозный тромбоз, гипертензия, замедленное заживание раны, бессимптомная протеинурия, перфорация носовой перегородки, синдром задней обратимой лейкоэнцефалопатии в связи с гипертензией, головокружение, атаксия, головная боль, охриплость голоса, тошнота, рвота, диарея, высыпание, подногтевое кровоизлияние, миелодиспластические синдромы, миелосупрессия, утомляемость, гипотиреоидизм, удлинение интервала QT или сердечная недостаточность.
В конкретных аспектах, соединение 1 или его фармацевтическую композицию не используют в комбинации с лекарственным средством, которое метабилизируется в основном под воздействием CYP2D6 (таким как антидепрессант (например, трициклический антидепрессант, селективный ингибитор обратного захвата серотонина, и другие подобные лекарственные средства, антипсихотическое средство, блокатор бета-адренергического рецептора или конкретные типы антиаритмических средств), для лечения рака поджелудочной железы.
Наборы
В изобретении предлагается фармацевтическая упаковка или набор, включающие один или более контейнеров, наполненных соединением 1 или его фармацевтической композицией. Кроме того, в фармацевтическую упаковку или набор могут быть также включены одно или более других терапевтических средств, применяемых для лечения рака поджелудочной железы, или других соответствующих лекарственных средств. Кроме того, в изобретении также предлагается фармацевтическая упаковка или набор, включающие один или более контейнеров, наполненных одним или более из градиентов описанных в изобретении фармацевтических композиций. В такие наборы может быть необязательно вложено уведомление по форме, установленной правительственным агентством, регулирующим производство, использование или продажу фармацевтических или биологических продуктов, причем в этом уведомлении отражено одобренное агентством производство, использование или продажа этого набора для применения на людях.
Независимо от того, было ли специально и индивидуально указано, что содержание цитируемого в изобретении документа включено в изобретение путем ссылки на него, содержание всех упомянутых в изобретении документов включено в изобретение путем ссылок на них с какой бы то ни было целью в равной мере, как если бы каждая отдельная ссылка на документ означала включение в изобретение полного его содержания.
После ознакомления с подробно описанным предметом изобретения, для специалистов в данной области станет очевидным, что то же самое может быть осуществлено в широком диапазоне эквивалентов, не выходя за рамки описанных в изобретении предмета или аспектов изобретения. Предполагается, что прилагаемая формула изобретения включает в себя все эти эквиваленты.
ПРИМЕРЫ
Следующие далее примеры приведены только с целью иллюстрации различных способов изобретения, и они никоим образом не ограничивают объем изобретения.
Материалы и методы, используемые в представленных далее примерах, были либо доступны из коммерческих источников, либо были получены известными специалистам в данной области методами в соответствии с известными методиками или методиками, описанными в указанных публикациях.
Соединение 1 получали в соответствии с методикой, описанной в патентном документе International Publication No. WO2014/081906.
Соединение 2 относится к 6-(5,6-дифтор-2-метил-1H-бензо[d]имидазол-1-ил)-N-(4-(трифторметил)фенил)пиразин-2-амину, известному ингибитору функции BMI-1, полученному в соответствии с методикой, описанной в патентном документе International Publication No. WO2015/076800.
Клеточные линии, культуры клеток, и исследования жизнеспособности
Аутентифицированные линии клеток человека приобретали у Американской коллекции типовых культур (ATCC), и для исходных клеток проводили совокупно 30 пассажей. Генерировали клеточные линии мышей KPC и проводили для них совокупно 30 пассажей. Получали клетки J1002 от мышей KPBBR и проводили для них совокупно 15 пассажей. На протяжении всего периода проведения эксперимента, все клеточные линии постоянно тестировали на отсутствие микоплазмы с использованием набора для обнаружения микоплазм MycoAlert Mycoplasma Detection Kit (Lonza; LT07-318). Клетки содержали в стандартных условиях при 37°C и 5% CO2 и выращивали в среде DMEM (Life Technologies, 12430-054), дополненной пенициллином и стрептомицином (Corning, 30-003-CI) и 10% FBS (Life Technologies, 10438- 034).
Для получения кривых пролиферации клеток, клетки высевали в 96-луночных планшетах (Corning, 3603) и выращивали в течение ночи. В планшетах для репликации проводили посев клеток для каждого момента времени, так как измерения жизнеспособности клеток являлись процедурой для получения конечных результатов исследования. На следующий день клетки подвергали воздействию соединения в указанных концентрациях и воздействию DMSO при самой высокой используемой концентрации (всегда ниже 0,003%). Клетки подвергали воздействию в течение 96 часов, и жизнеспособность определяли каждые 24 часа с использованием реагента AlamarBlue (BioRad, BUF012B). Вкратце, в каждую лунку (100 мкл) добавляли 10 мкл реагента AlamarBlue, недолго перемешивали и инкубировали при 37°C и 5% CO2 в течение 4 часов. После инкубации, измеряли флуоресценцию на многорежимном планшет-ридере Promega. Для анализа, из полученных необработанных результатов вычитали уровни фона, и затем проводили нормализацию для представления результатов в форме кратности изменения по сравнению с клетками, подвергнутыми воздействию DMSO в день 0. Все анализы проводили, по меньшей мере, по три раза с 4-8 техническими репликациями на одну подвергаемую воздействию группу на один эксперимент. (фигура 1а и фигура 10b).
Для получения кривых зависимости "доза-эффект", клетки высевали в 96-луночных планшетах (Corning, 3603) и выращивали в течение ночи. На следующий день, клетки подвергали воздействию соединения 1. Построение кривых зависимости "доза-эффект" начинали при концентрации 10 мкМ, уменьшали концентрацию на каждом этапе разведения в 3 раза, и заканчивали построение кривых при самой высокой используемой концентрации DMSO (всегда ниже 0,03%). Клетки подвергали воздействию в течение 72 часов, и затем определяли жизнеспособность с использованием реагента AlamarBlue (BioRad, BUF012B). Вкратце, в каждую лунку (100 мкл) добавляли 10 мкл реагента AlamarBlue, недолго перемешивали и инкубировали при 37°C и 5% CO2 в течение 4 часов. После инкубации, измеряли флуоресценцию на многорежимном планшет-ридере Promega. Для анализа, из полученных необработанных результатов вычитали уровни фона, и затем проводили нормализацию для представления результатов в форме процента клеток, подвергнутых воздействию DMSO. Все анализы проводили, по меньшей мере, по три раза с 4-8 техническими репликациями на один эксперимент (рисунок 10c).
Анализ клеточного цикла
Клетки высевали в 12-луночные или 6-луночные планшеты, для того чтобы через 16 часов они были бы приблизительно на 30-50% конфлюэнтными. Затем клетки подвергали воздействию в течение 24 часов либо DMSO (<0,003%), либо соединения 1 (100 нМ или 1 мкМ), либо 100 нМ нокодазола (Sigma, M1404). После обработки, клетки собирали и фиксировали в ледяном 70% этаноле в течение, как минимум, одного часа. После фиксации, клетки повторно суспендировали в PBS+2% FBS+3 мкМ DAPI (BioLegend, 422801) или 0,25 мкг 7-AAD (BD Pharmingen, 559925) и анализировали на проточный цитометре MACSQuant® Analyzer 10 (Miltenyi Biotec) или на проточном цитометре BD LSR IITM. Для экспериментов по определению зависимости клеточного цикла от времени, клетки получали, как описано выше, за исключением того, что подвергали их воздействии в течение 24, 48 или 72 часов. Данные анализировали с помощью программного обеспечения FlowJo. Проценты популяций клеток в фазе G2/M идентифицировали с использованием платформы одномерного клеточного цикла, предлагаемой программным обеспечением FlowJo. Проценты популяций клеток > 4N определяли путем селекции выше 4N популяции клеток, подвергнутых воздействию DMSO. (фигура 1b, фигура 1c, фигура 2a, фигура 2b, фигура 10e и фигура 10g).
Проточная цитометрия для внутриклеточных белков
Для окрашивания фосфогистоном H3 (PH3), клетки фиксировали и пермеабилизировали в соответствии с инструкциями фирмы-производителя с использованием набора eBioscience Foxp3/Transcription Factor Staining Buffer Set (ThermoFisher, 00-5523-00). Клетки блокировали антителом Fc (BD Biosciences, 564220) и окрашивали с использованием антитела PH3 (Ser10) (BioLegend, 650805) из расчета 5 мкл на миллион клеток (45 мин, комнатная температура, в темноте). Образцы анализировали на проточном цитометре BD FortessaTM с использованием программного обеспечения FlowJo. (фигура 1d и фигура 3a).
Для окрашивания активной каспазы-3 (ActCasp3) использовали набор Caspase 3 (active) FITC Staining Kit (Abcam, ab65613) в соответствии с инструкциями фирмы-производителя. Клетки высевали в 12-луночные планшеты, для того чтобы через приблизительно 16 часов они были бы приблизительно на 50-60% конфлюэнтными. Затем клетки подвергали воздействию лекарственных средств в указанных концентрациях или DMSO в качестве плацебо в течение 24 часов, после чего их собирали, окрашивали с помощью FITC-DEVD-FMK (1 мкл/образец, 1 час, комнатная температура, в темноте), промывали и затем окрашивали с помощью красителя DAPI для анализа. Образцы анализировали на проточном цитометре BD LSR IITM с использованием программного обеспечения FlowJo (фигура 3а и фигура 3b).
Вестерн-блоттинг
Вестерн-блоттинг проводили на лизатах, выделенных из подвергнутых воздействию клеток. Клетки лизировали с использованием буфера RIPA (50 мМ Tris, pH 7,4, 150 мМ NaCl, 1% Nonidet P-40, 0,1% SDS, 0,5% дезоксихолат) с добавлением не содержащего EDTA коктейля ингибиторов протеазы cOmplete™ EDTA-free Protease Inhibitor Cocktail (Sigma, 11836170001) и коктейля ингибиторов фосфатазы HaltTM (ThermoFisher, 78420). Лизаты количественно определяли с использованием набора для анализа белка Pierce BCA Protein Assay Kit (ThermoFisher, 23227), разбавляли в буфере для образцов SDS, разделяли с помощью SDS-PAGE (15-30 мкг/образец) и переносили на мембраны из поливинилиденфторида (PVDF). Мембраны блокировали с помощью 5% масс/об обезжиренного сухого молока в TBS-T (0,1% Tween20), и первичные антитела инкубировали в течение ночи при 4°C, разбавленные в 5% BSA в TBS-T до указанных концентраций. Вторичные антитела, конъюгированные с HRP, инкубировали в блокирующем буфере в течение 1 часа при комнатной температуре, затем проводили детекцию с использованием раствора субстрата Super Digital-ECLTM (Kindle Biosciences, R1002). (фигура 5b, фигура 10a и фигура 11b)
Вестерн-блоттинг для антител:
Bmi1: Cell Signaling, # 5856, 1:1000
Винкулин: Cell Signaling, # 4650S, 1:1000
Бета-тубулин: Cell Signaling, # 2146S, 1:1000
Эксперимент по определению активности субстрата P-гликопротеина
Клетки линии MDCKII-mdr1 и MDCKII-wt приобретали у Нидерландского института рака, NKI-AVL. Клетки культивировали в модифицированной эссенциальной среде Дульбекко (DMEM), дополненной 10% FBS и 1% пенициллина-стрептоцида, и использовали их между пассажами 3-9. Клетки высевали при плотности 3 × 103 клеток/лунка в 96-луночные планшеты с обработанной поверхностью для исследования тканевых культур. Через 4 часа, в течение которых клеткам давали возможность прикрепиться, клетки подвергали воздействию тестируемого соединения в присутствии или в отсутствие ингибитора Р-гликопротеина валсподара. Планшеты инкубировали при 37° C, 5% CO2 в течение 72 часов и измеряли АТФ по люминесценции с использованием реагента CellTiter-Glo® (Promega) (фигура 4b).
Секвенирование РНК
Приблизительно 1,75 мкг тотальной РНК на образец подвергали вытяжке полиадениловой кислоты для обогащения мРНК, которую затем использовали в качестве входных данных для набора для приготовления РНК Illumina TruSeq RNA prep kit. Готовили образцы готовили для платформы Illumina HiSeq 4000 с использованием робота Beckmann-Coulter Roboter и набора SPRIworks Fragment Library Kit I. Проводили ПЦР с использованием набора для амплификации KAPA PCR Amplification Kit. Затем библиотеки секвенировали в Колумбийском центре генома с получением 30 миллионов односторонних считываний длиной 100 пар оснований (п.о.) (фигура 11a).
Анализ секвенирования РНК
Считывания были сопоставлены с эталонным геномом человека (NCBI/build 37.2) с использованием выравнивателя STAR (version 2.4.2) (Dobin A, Davis CA, Schlesinger F, et al. STAR: Ultrafast Universal RNA-Seq Aligner, Bioinformatics 2013;29:15-21) и количественно определены на уровне генов с использованием функции summarizeOverlaps из пакета R 'GenomicAlignments' (Lawrence M, Huber W, Pages H, et al. Software for computing and annotating genomic ranges, PLoS Computational Biology 2013;9:e1003118) с информацией об аннотациях генов из пакета R ‘TxDb.Hsapiens.UCSC.hg19.knownGene’ (Carlson M, Maintainer BP. TxDb.Hsapiens.UCSC.hg19.knownGene:Annotation Package for TxDb Object(s). 2015). Данные по секвенированию РНК были депонированы в GEO (ID: GSE118441) (фигура 11a).
Дифференциальная экспрессия генов (DEG)
Анализ дифференциальной экспрессии генов между указанными условиями проводили с использованием каркасов voom-limma, реализованных в пакете R ‘limma’ (Ritchie ME, Phipson B, Wu D, et al. Limma powers differential expression analyses for RNA-sequencing and microarray studies, Nucleic Acids Research 2015;43:e47). Общий эффект воздействия соединения 1 по сравнению с DMSO оценивали с использованием многомерного плана с учетом как воздействия, так и момента времени.
Обогащение набора генов
Использовали реализацию R для одного образца для анализа обогащения набора генов (GSEA): анализ вариации набора генов с параметрами по умолчанию (Hanzelmann S, Castelo R, Guinney J. GSVA: gene set variation analysis for microarray and RNA-seq data, BMC Bioinformatics 2013;14:7). Необработанные результаты подсчетов секвенирования РНК нормализовали с целью учета различных размеров библиотек, и величину отклонения стабилизировали путем подгонки дисперсии под отрицательно-биномиальное распределение, как это реализуется в пакете DESeq2 R (Love MI, Huber W, Anders S. Moderated estimation of fold change and dispersion for RNA-seq data with DESeq2, Genome Biol 2014;15:550). Наборы генов получали из модулей HALLMARK MSigDb v6.0, канонических путей C2 и онкогенных сигнатур C6 (Subramanian A, Tamayo P, Mootha VK, et al. Gene set enrichment analysis: a knowledge-based approach for interpreting genome-wide expression profiles, Proc Natl Acad Sci U S A 2005;102:15545-50 and Liberzon A, Subramanian A, Pinchback R, et al. Molecular signatures database (MSigDB) 3.0, Bioinformatics 2011;27:1739-40). Анализ дифференциального обогащения этих наборов генов между воздействием DMSO и соединения 1 проводили с использованием пакета limma R (Ritchie ME, Phipson B, Wu D, et al. limma powers differential expression analyses for RNA-sequencing and microarray studies, Nucleic Acids Res 2015;43:e47), и уровень ложноположительных результатов (FDR) < 0,1 считали значимым. Результаты по обогащению одного образца для выбранных биологических путей отображали на тепловой карте с использованием пакета pheatmap R (http://CRAN R-project org/package= pheatmap R package version 2017;1:2) (фигура 11a) .
Сигнатуры наборов генов:
*REACTOME - онлайн-база данных биологических путей
Исследование бесклеточной полимеризации тубулина
Анализы проводили в соответствии с рекомендациями фирмы-производителя с использованием набора для флуоресцентного анализа полимеризации тубулина фирмы Cytoskeleton (#BK011P), в котором используется тубулин с чистотой > 99% из головного мозга свиньи. Все используемые лекарственные средства растворяли в DMSO и затем разбавляли в 10 раз в сверхчистой воде до конечной концентрации. Конечная процентное содержание DMSO поддерживали постоянным для всех образцов. Тубулин получали путем ресуспендирования в дозе 2 мг/мл в смеси 80 мМ PIPES pH 6,9, 2,0 мМ MgCl2, 0,5 мМ EGTA, 1,0 мМ GTP, 15% глицерина и 10 мкМ флуоресцентного репортера. Все образцы лекарственных средств (10X) добавляли в предварительно подогретую половину площади 96-луночного планшета (Corning Costar, 3686) в двух экземплярах, и затем нагревали до 37° C в течение 1 мин. Затем во все лунки добавляли тубулин (50 мкл/лунку), и планшет помещали в планшет ридер, предварительно подогретый до 37°C. Среду в планшете перемешивали путем орбитального встряхивания в течение 5 секунд, и флуоресценцию измеряли каждые 60 секунд в течение 90 минут (возбуждение: 340-360+/-20 нм, эмиссия: 410-460+/-20 нм) в планшет-ридере BioTek Synergy 2. Скорости полимеризации (относительные единицы флуоресценции/минута) определяли путем измерения максимального угла наклона (путем линейной регрессии) линейного участка фазы роста кривой полимеризации. (фигура 11e и фигура 11f)
Анализ содержания свободного тубулина
Свободный гетеродимер тубулина отделяли от тубулина, включенного в микротрубочки, в соответствии с рекомендациями фирмы-производителя, с использованием набора Microtubule/Tubulin In Vivo Assay Biochem Kit (Cytoskeleton, #BK038). Клетки высевали в 12-луночные планшеты, для того чтобы через приблизительно 16 часов они были приблизительно на 50-60% конфлюэнтными. Клетки подвергали воздействию лекарственных средств в указанных концентрациях или DMSO в качестве плацебо в течение 2 часов, после чего их один раз промывали с помощью PBS и собирали. Все этапы этого анализа проводили при 37°C, для того чтобы сохранить массу микротрубочек. Клетки лизировали в буфере для стабилизации клеточного скелета при лизисе и стабилизации микротрубочек (LMS01), дополненном 0,1 мМ ГТФ, 1,0 мМ АТФ и коктейлем ингибиторов протеаз 1X (#PIC02). Образцы центрифугировали при 1000 x g в течение 5 минут при 37°C. Надосадочную жидкость тщательно собирали для ультрацентрифугирования, а полученный при низкой скорости центрифугирования осадок (LSP) суспендировали в буфере для образцов SDS (SDS01) и замораживали при -20°C для последующего анализа вестерн-блоттингом. Полученную при низкой скорости центрифугирования надосадочную жидкость центрифугировали при 100000 x g в течение 60 минут при 37°C. Надосадочную жидкость (полученную при высокой скорости центрифугирования надосадочную жидкость HSS) осторожно собирали, ресуспендировали в буфере для образцов SDS и замораживали при -20°C для последующего анализа вестерн-блоттингом. Осадок (полученный при высокой скорости центрифугирования осадок, HSP) сначала растворяли в 1X буфере для деполимеризации микротрубочек (BUF01) в течение 15 минут, ресуспендировали в буфере для образца SDS и замораживали при -20°C для последующего анализа вестерн-блоттингом. (фигура 11b)
Иммуноцитохимия
Клетки высевали на покровных стеклах в 12-луночных планшетах. Покровные стекла готовили путем замачивания в 1 н. HCl (60°C, 6 часов), промывания в 70% этаноле и наносили слой покрытия из поли-L-лизина (Sigma, P5899) в соответствии с инструкциями фирмы-производителя. Клетки высевали, для того чтобы на следующий день они были приблизительно на 50% конфлюэнтными. Затем клетки подвергали воздействию плацебо (DMSO, <0,003%) или 1 мкМ соединения 1 и инкубировали в течение 24 часов. После воздействия, клетки промывали с помощью TBS, и свободный тубулин экстрагировали буфером Brinkley Buffer 1980 (80 мМ PIPES pH 6,8, 1 мМ MgCl2, 1 мМ EGTA), дополненным 4 мМ EGTA и 0,5% Triton-X (30 секунд). После экстракции, клетки фиксировали в течение 20 минут в 4% формальдегиде, разведенном в цитоскелетном буфере (10 мМ MES pH 6,1, 138 мМ KCl, 3 мМ MgCl2, 2 мМ EGTA), дополненном 0,32 М сахарозы. После фиксации, клетки промывали с помощью TBS, и затем блокировали в TBS-T (0,1% Triton-X) + 2% BSA+22,52 мг/мл глицина в течение 30 минут. Антитело против бета-тубулина инкубировали в течение ночи при 4°C (Abcam179513, 1:1000) с последующей инкубацией со вторичным антителом в течение одного часа при комнатной температуре с использованием козьего против кроличьего вторичного антитела 594 (Life Technologies, A11012) при 1:500. Все промывки проводили с помощью TBS-T, а все блокирования и инкубации антител проводили в TBS-T (0,1% Triton-X) + 2% BSA+22,52 мг/мл глицина. После окрашивания, клетки инкубировали с красителем DAPI (BioLegend, 422801) при 300 нМ в течение 5 минут, промывали и закрепляли на стеклах с помощью среды ProLong Diamond Antifade Mountant (Invitrogen, P36965). Микроскопические препараты сушили в течение 24 часов при комнатной температуре, и затем хранили при 4°C в темноте до получения изображения.
Конфокальную визуализацию проводили с использованием конфокальной насадки для лазерного сканирования A1 на подставке для микроскопа Eclipse Ti с масляно-иммерсионным объективом 60x/1.49 ApoTIRF, и с использованием стандартных лазеров и наборов фильтров (Nikon Instruments, Melville, NY). Диаметр точечного отверстия был установлен на 1 единицу Эйри, и отдельные оптические получали вблизи базальной поверхности клеток для максимального обнаружения микротрубочек. Все условия визуализации поддерживали постоянными. Изображения визуализировали, анализировали и готовили к публикации с использованием дистрибутива Fiji для ImageJ (Schindelin J, Arganda-Carreras I, Frise E, et al. Fiji: an open-source platform for biological-image analysis. Nature Methods 2012;9:676-682) (фигура 10d и фигура 10f).
Выведение животных и генотипирование
Генетически модифицированные модели создавали путем скрещивания следующих модифицированных штаммов смешанного генетического фона:
KrasLSL.G12D - описан в публикации Tuveson DA, Shaw AT, Willis NA, et al. Endogenous oncogenic K-ras(G12D) stimulates proliferation and widespread neoplastic and developmental defects, Cancer Cell 2004;5:375-87.
Tp53LSL.R172H - описан в публикации Olive KP, Tuveson DA, Ruhe ZC, et al. Mutant p53 gain of function in two mouse models of Li-Fraumeni syndrome, Cell 2004;119:847-60.
Pdx1-Cretg - описан в публикации Hingorani SR, Petricoin EF, Maitra A, et al. Preinvasive and invasive ductal pancreatic cancer and its early detection in the mouse, Cancer Cell 2003;4:437-50.
Tp53Flox - описан в публикации Jonkers J, Meuwissen R, van der Gulden H, et al. Synergistic tumor suppressor activity of BRCA2 and p53 in a conditional mouse model for breast cancer, Nat Genet 2001;29:418-25.
KrasFSF.G12D - Jackson Laboratory, Stock No. 008653.
Tp53R172H - этот штамм получали путем скрещивания штамма Tp53LSL.R172H с Deleter-Cre для индуцирования рекомбинации зародышевой линии, и затем удаления аллеля Cre. Это индуцировало рекомбинацию кассеты Lox-STOP-LOX в аллеле Tp53LSL.R172H, что приводило к появлению аллеля зародышевой линии Tp53R172H с единственным экзогенным сайтом LoxP в интроне 1.
Pdx1-FlpOtg - проксимальный промотор 6 тысяч нуклеотидов (т.н.) трансгена Pdx1-Cre сливали с инициирующий кодоном оптимизированной по кодонам термостабильной рекомбиназы Flp (FlpO) млекопитающих с последующим слиянием 5'-конца открытой рамки считывания FlpO с сигнальной последовательностью полиаденилирования hGH.
Bmi1Flox - описан в публикации Mich JK, Signer RA, Nakada D, et al. Prospective identification of functionally distinct stem cells and neurosphere-initiating cells in adult mouse forebrain, Elife 2014;3:e02669.
Rosa26Cre-ERT2 - описан в публикации Ventura A, Kirsch DG, McLaughlin ME, et al. Restoration of p53 function leads to tumour regression in vivo, Nature 2007;445:661-5.
Использовали экспериментальные модели на мышах KrasLSL.G12D/+; p53LSL.G12D/+; Pdx1-Cretg/+ (KPC) и родственные модели, как описано в публикации Hingorani SR, Wang L, Multani AS, et al. Объединяли Trp53R172H и KrasG12D для промотирования хромосомной нестабильности и развитию протоковой аденокарциномы поджелудочной железы с метастазированием у мышей, Cancer Cell 2005; 7: 469-83. Клетки J1002 получали из находящейся на месте своего образования опухоли поджелудочной железы у KrasFSF.G12D/+; p53R172H/+; Pdx1-FlpOtg/+; Bmi1Fl/Fl; Rosa26CreERT2/+ (KPFBR) мыши, которая возникла после воздействия cerulean (для ускорения развития опухоли), но до лечения тамоксифеном. Генотипирование выполнялось компанией Transnetyx (Cordova, TN). В исследованиях использовали как самцов, так и самок. Животным давали стандартный корм и содержали в условиях 12-часового цикла свет/темнота.
Генерация первичных опухолевых клеточных линий KPFBR
Небольшой кусочек опухоли (~30 мг) механически разрушали путем измельчения стерильными ножницами в течение минимум пяти минут в охлажденном льдом буфере для ферментативного расщепления ткани опухоли (5 мл/образец). Буфер для ферментативного расщепления ткани опухоли состоял из 75 мкг/мл ДНКазы I (ThermoScientific, EN0521), 80 мкг/мл диспазы II (ThermoFisher, 17105041) и 1 мг/мл коллагеназы V (Sigma Aldrich, C9263), разбавленных в стерильном забуференном фосфатом физиологическом растворе (PBS). После измельчения, разрушенную опухоль инкубировали в буфере для ферментативного расщепления при 37°C в течение 20 минут. После ферментативного расщепления, для разбавления ферментативно расщепленной опухоли использовали 40 мл охлажденного льдом PBS, и все 45 мл фильтровали через стерильный сетчатый фильтр с размером пор 70 мкм. Суспензию отдельных клеток центрифугировали (300 х g, 5 мин), один раз промывали с помощью PBS, ресуспендировали в бессывороточной дуктальной среде (SFDM, состав приведен ниже) и высевали в 1-2 лунки покрытого коллагеном 6-луночного планшета (Corning, 354400). Клетки размножали в SFDM на покрытых коллагеном планшетах и переносили в стандартную среду DMEM (10% FBS, 1% Pen-Strep, 1% L-глутамин) и стандартные планшеты для тканевых культур (без коллагена).
Состав SFDM:
Среда DMEM/F-12 (ThermoFisher, 12634010)
1,22 мг/мл никотинамида (Sigma, N3376)
5 мг/мл глюкозы (Sigma, G6152)
5% ITS+ (BD Biosciences, 354352)
2,5 мкг/мл амфотерицина B (ThermoFisher, 15290018)
5% Nu-serum IV (Corning, 392-0321)
25 мкг/мл экстракта бычьего гипофиза (Sigma, 1476)
20 нг/мл EGF (ThermoFisher, PMG8041)
50 нМ 3,3’5-трийод-L-тиронина (Sigma, 564605)
1 мкм дексаметазона (Sigma, D1756)
100 нг/мл холерного токсина (Quadratech, 100)
Оценка делеции Bmi1
Для оценки рекомбинации условного аллеля Bmi1 в клетках J1002, проводили ПЦР на ДНК, выделенной экстракцией смесью фенол-хлороформ-изоамиловый спирт. Клетки подвергали ферментативному расщеплению в течение ночи при 55°C в буфере для лизиса (10 мМ Tris pH 7,5, 10 мМ EDTA, 10 мМ NaCl и 0,5% саркозила), дополненном 1 мг/мл протеиназы K (New England BioLabs, P8107S). На следующий день, ДНК выделяли путем объединения лизатов со смесью 50% фенола, 48% хлороформа и 2% изоамилового спирта и центрифугирования при 16000 x g в течение 30 минут. Верхний слой, содержащий ДНК, отделяли, осаждали и промывали 2,5 объемами 100% этанола. Концентрации ДНК измеряли на спектрофотометре ThermoScientificTM NanoDrop 2000. Реакции ПЦР проводили с использованием смеси GoTaq® Green Master Mix (Promega, M712B), 1 нг ДНК и 250 нМ каждого праймера. Использовали три праймера (DN437, DN438, DN946), которые амплифицируют Bmi1 дикого типа (Bmi1WT), Bmi1 со вставленными сайтами loxP (Bmi1fl/fl) и рекомбинированный Bmi1 (Bmi1Δ), все в одной реакции. После ПЦР, амплифицированную ДНК разделяли на 2% агарозном геле с добавлением красителя SYBRTM Safe DNA Gel Stain (ThermoFisher, S33102) и визуализировали с использованием УФ-света.
Праймеры:
DN437: gctagcattcctggttttgc
DN438: ggcacagtgatgaggtgttg
DN946: cacgaggtgcttctttcctc
Условия проведения циклов:
1. 95°C, 2 мин.
2. 95°C, 15 сек.
3. 51,4°C, 15 сек.
4. 68°C, 45 сек.
(Повторите стадии 2-4 30 раз)
5. 68°C, 5 мин.
6. 4°C, навсегда
Ожидаемые ампликоны:
Дикий тип Bmi1 (Bmi1WT) = 400 п.о.
Фланкированный Bmi1 (Bmi1fl/fl) = 500 п.о.
Рекомбинированный Bmi1 (Bmi1 Δ) = 300 п.о.
Интервенционное исследование на модели опухоли на бестимусных мышах, которым вводили полученные от пациента ксенотрансплантаты (PDX)
Фрагменты опухоли раннего пассажа из модели Champions CTG-1462 имплантировали подкожно бестимусным мышам (nu/nu), и затем мышей случайным образом распределяли по группам лечения, когда опухоли достигли объема 150-300 мм3. Мышей (n=5/группа) подвергали лечению в одной из семи групп: плацебо, гемцитабин (50 мг/кг, раз в неделю, интраперитонеально), наб-паклитаксел (10 мг/кг, внутривенно, раз в неделю x недели), соединение 1 (12,5 мг/кг, раз в две недели x 4 недели, перорально) или комбинации полных доз гемцитабин+наб-паклитаксел, гемцитабин+соединение 1, наб-паклитаксел+соединение 1, или гемцитабин+наб-паклитаксел+соединение 1. Конечными точками исследования были точки, когда опухоль достигала объема 1500 мм3 или после 90 дней проведения исследования. Длину (L) и ширину (W) диаметров опухолей измеряли с помощью цифровых штангенциркулей, и мышей взвешивали дважды в неделю. Объем опухоли рассчитывали по формуле (L x W2)/2. (фигура 12a и фигура 12b)
Интервенционное исследование/исследование выживаемости KPC мышей
Образование опухоли у мышей KPC постоянно контролировали путем еженедельной пальпации до тех пор, пока не обнаруживали опухолевидное образование. После положительного результата пальпации, опухолевидное образование постоянно контролировали путем проведения ультразвукового исследования дважды в неделю до тех пор, пока опухоль не достигла требуемого для включения в группу исследования размера со средним диаметром 4-7 мм. После того, как опухоль достигала требуемого размера, мышей KPC случайным образом распределяли по группам лечения интервенционного исследования. Мышей подвергали воздействию плацебо, соединения 1 (17 мг/кг, перорально, два раза в неделю), только гемцитабина (100 мг/кг, интраперитонеально, два раза в неделю) или соединения 1+гемцитабин. Мыши, которым вводили соединение 1, также вводили плацебо вместо гемцитабина (физиологический раствор, интраперитонеально, два раза в неделю) в объеме (мкл), рассчитанном от массы тела, умноженной на 50 (г). Мышам, получавшим гемцитабин, также вводили плацебо вместо соединения 1 (0,5% гидроксипропилметилцеллюлозы с 0,1% Tween80 (масс./об.), перорально, два раза в неделю) в объеме (мкл), рассчитанном от массы тела, умноженной на 5,7 (г). Все комбинации лекарственных средств и плацебо вводили одновременно.
Измерения уровней соединения 1 в образцах плазмы и тканей
Используемые для анализа образцы плазмы крови и ткани немедленно замораживали на сухом льду и хранили при -80°C до проведения анализа. Концентрации соединения 1 в образцах определяли количественно методом высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (LC-MS/MS). Соединение 1 и его внутренний стандарт (дейтерированное соединение 1) извлекали из образцов экстракцией и осаждением белков.
Для исследования фармакокинетической зависимости концентраций в плазме от времени, строили калибровочную кривую в диапазоне концентраций от 0,001 мкг/мл до 3,0 мкг/мл. Нижний предел количественного определения (LLOQ) соединения 1 (в любой форме) в плазме составлял 0,001 мкг/мл. (фигура 4а)
Для фармакокинетического исследования, в котором оценивали концентрацию соединения 1 в плазме, четырехглавой мышце и опухолевой ткани после введения однократной дозы соединения 1, условия анализа были следующими (фигура 5a).
Плазма. Калибровочную кривую строили для диапазона концентраций от 0,002 мкг/мл до 6,0 мкг/мл. Величина LLOQ для соединения 1 (в любой форме) в плазме составляла 0,001 мкг/мл.
Четырехглавая мышца. Калибровочную кривую строили для диапазона концентраций от 0,001 мкг/г влажной ткани до 3,0 мкг/г влажной ткани. Величина LLOQ для соединения 1 (в любой форме) в плазме составляла 0,01 мкг/г влажной ткани.
Опухолевая ткань. Калибровочную кривую строили для диапазона концентраций от 0,001 мкг/г влажной ткани до 3,0 мкг/г влажной ткани. Величина LLOQ для соединения 1 (в любой форме) в плазме составляла 0,02 мкг/г влажной ткани.
Ультразвуковое исследование
Ультрасонографию опухоли и количественную оценку ее объема проводили, как описано в публикации Sastra SA, Olive KP, Quantification of murine pancreatic tumors by high-resolution ultrasound, Methods Mol Biol 2013;980:249-66 (фигура 7а и фигура 7b).
Иммуногистохимия
Для подготовки образцов для иммуногистохимии, ткани сначала фиксировали в течение ночи в 10% забуференном фосфатом формалине, и затем хранили в 70% этаноле для обеспечения длительного хранения. Затем фиксированные ткани подвергали дегидратации в соответствии со стандартным протоколом и заключали в блоки парафина. Из ткани изготавливали срезы толщиной 5 мкм с помощью микротома Leica RM 2235, устанавливали на положительно заряженные предметные стекла и подвергали термической обработке при 60°C в течение 30 минут. Для подготовки к окрашиванию, микроскопические препараты сначала депарафинизировали в ксилоле, и затем повторно гидратировали в несколько стадий этанолом, затем споласкивали в дистиллированной воде. После чего проводили демаскирование антигена в экспериментально определенном антителоспецифическом буфере для демаскирования антигена (обычно 10 мМ цитрата, pH 6,0 или 10 мМ Tris, pH 10,0). Буфер для демаскирования антигена нагревали до кипения в автоклаве, после чего в него помещали микроскопические препараты на 5 минут. После охлаждения до комнатной температуры, микроскопические препараты погружали в 3% перекиси водорода в PBS на 20 минут, чтобы погасить эндогенные пероксидазы.
Затем микроскопические препараты блокировали в течение одного часа при комнатной температуре в TBS-T (0,1% Tween20) + 1,5% нормальной лошадиной сыворотки (Vector Laboratories, S-2000) + 2% блокатора, не содержащего белок животного происхождения (Vector Laboratories, SP-5030). Первичные антитела разбавляли в блокирующем растворе и инкубировали в течение ночи при 4°C в указанных концентрациях. На следующий день, проводили инкубацию вторичных антител при комнатной температуре в течение 30 минут с использованием набора для детекции ImmPRESS HRP Anti-Rabbit IgG (Peroxidase) Polymer Detection Kit (Vector Laboratories, MP-7401). Детекцию проводили с использованием субстрата пероксидазы ImmPACT DAB Peroxidase (HRP) Substrate (Vector Laboratories, SK-4105), и микроскопические препараты последовательно докрашивали гематоксилином, дегидратировали в ксилоле и заклеивали покровным стеклом Permount (Fisher, S70104) (фигура 6d и фигура 6e).
Антитела для иммуногистохимии:
PH3: Cell Signaling, #9701, 1:100
CC3: Cell Signaling, #9664S, 1:10
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО МИЕЛОИДНОГО ЛЕЙКОЗА | 2020 |
|
RU2812782C2 |
| СПОСОБ УМЕНЬШЕНИЯ МУЛЬТИЛЕКАРСТВЕННОЙ РЕЗИСТЕНТНОСТИ С ИСПОЛЬЗОВАНИЕМ ТРИПИРОФОСФАТА ИНОЗИТА | 2010 |
|
RU2563127C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2011 |
|
RU2605335C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2011 |
|
RU2743643C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2767664C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2757373C2 |
| КОМБИНИРОВАННАЯ ХИМИОТЕРАПИЯ | 2001 |
|
RU2284818C2 |
| МОДИФИЦИРОВАННЫЕ ЦИТОТОКСИНЫ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2721949C2 |
| СПОСОБЫ ЛЕЧЕНИЕ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2576609C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА, ИМЕЮЩЕГО ГЕМИЗИГОТНУЮ ПОТЕРЮ ТР53 | 2016 |
|
RU2721953C2 |
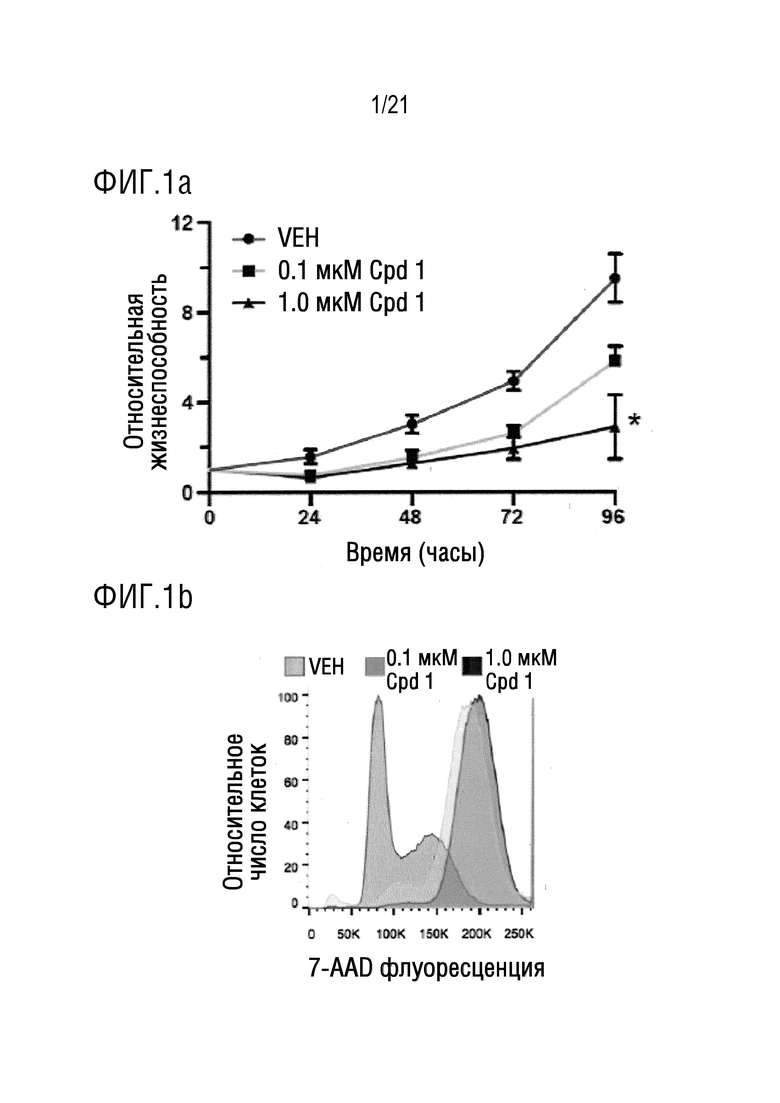
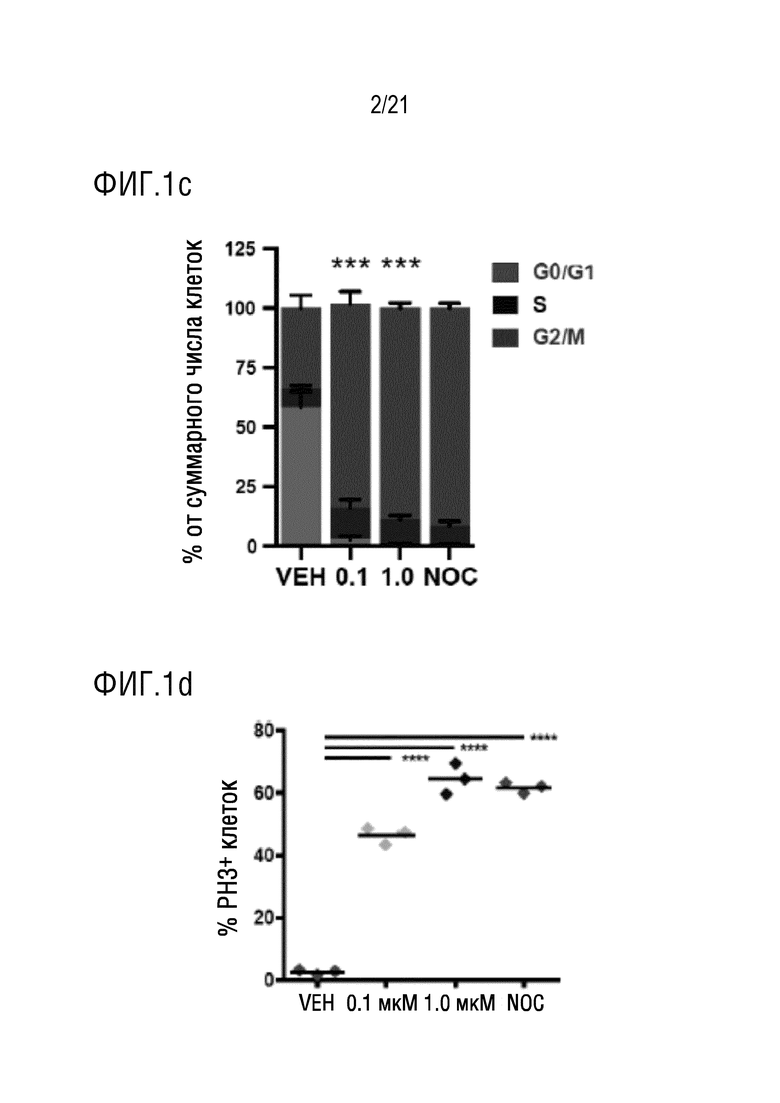
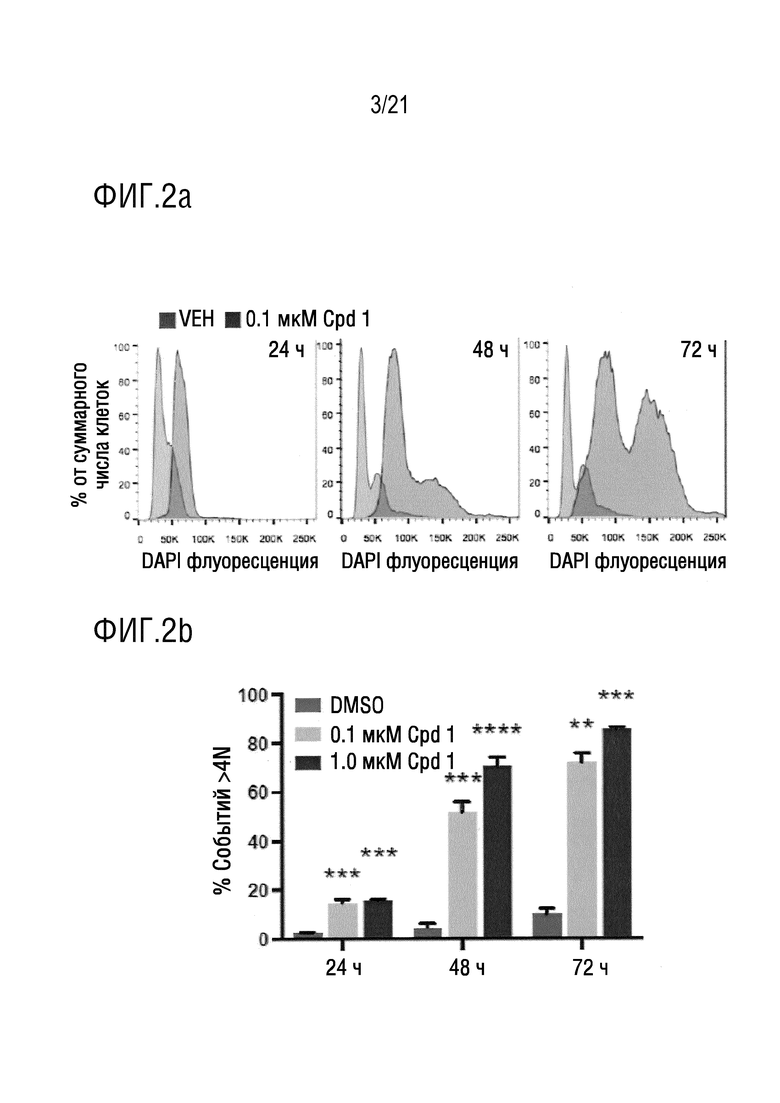
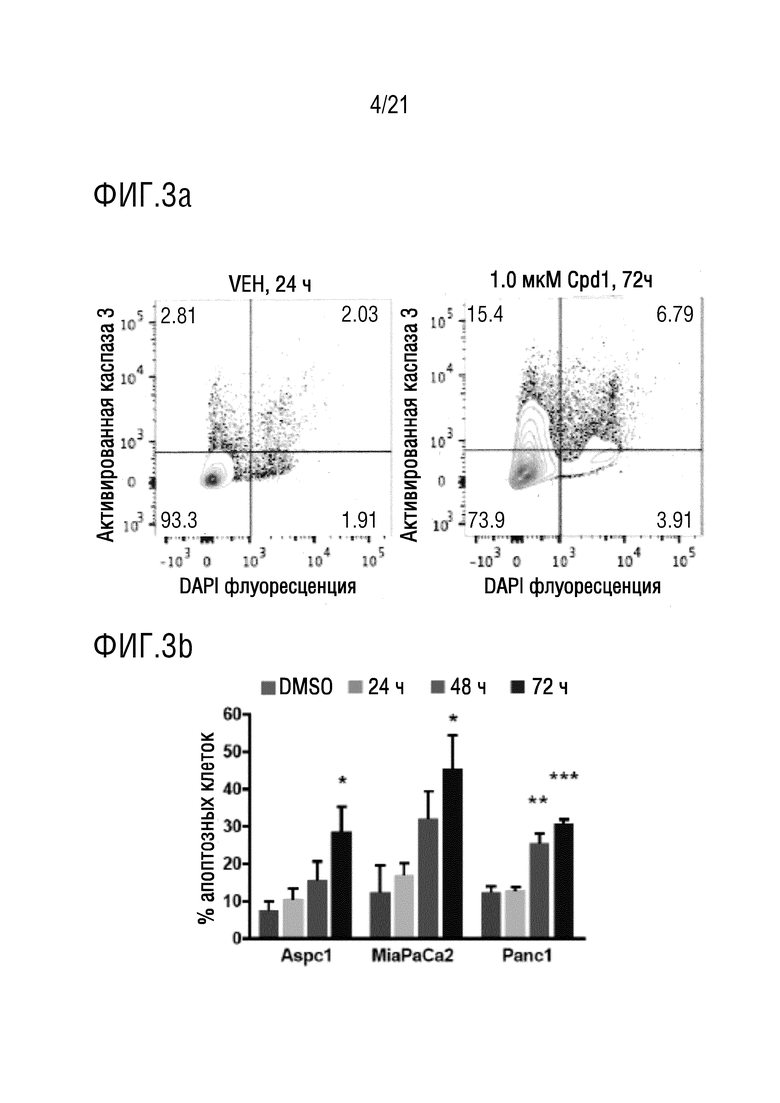
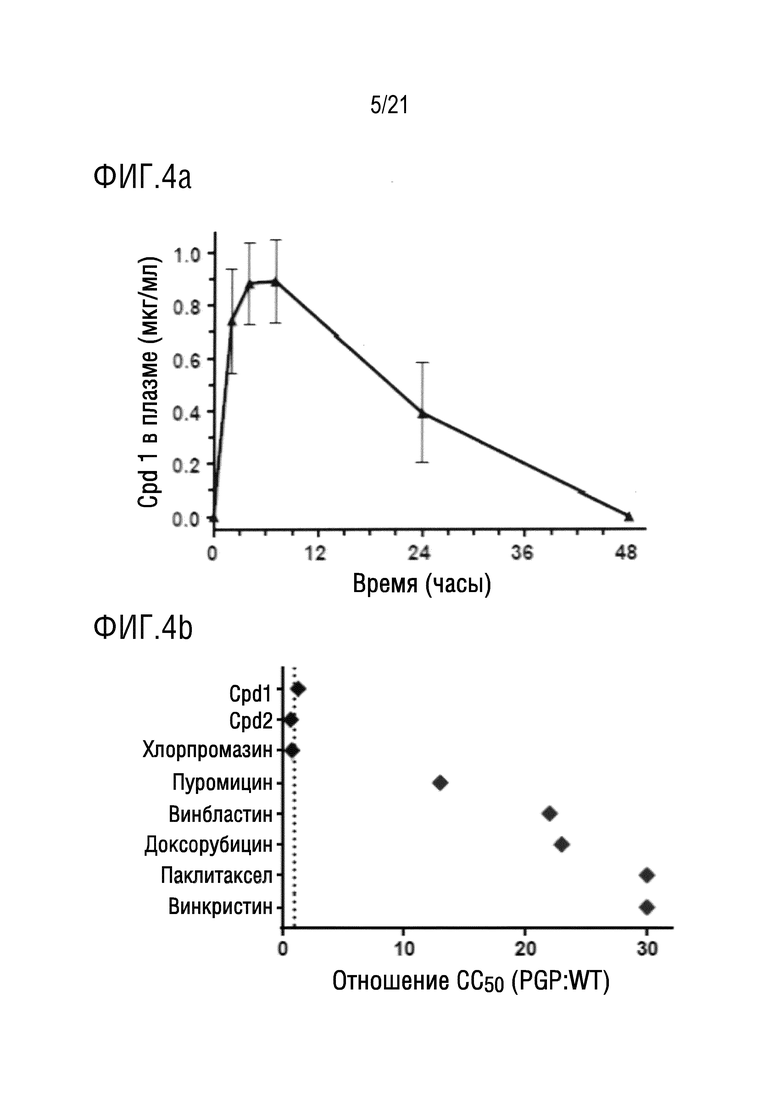
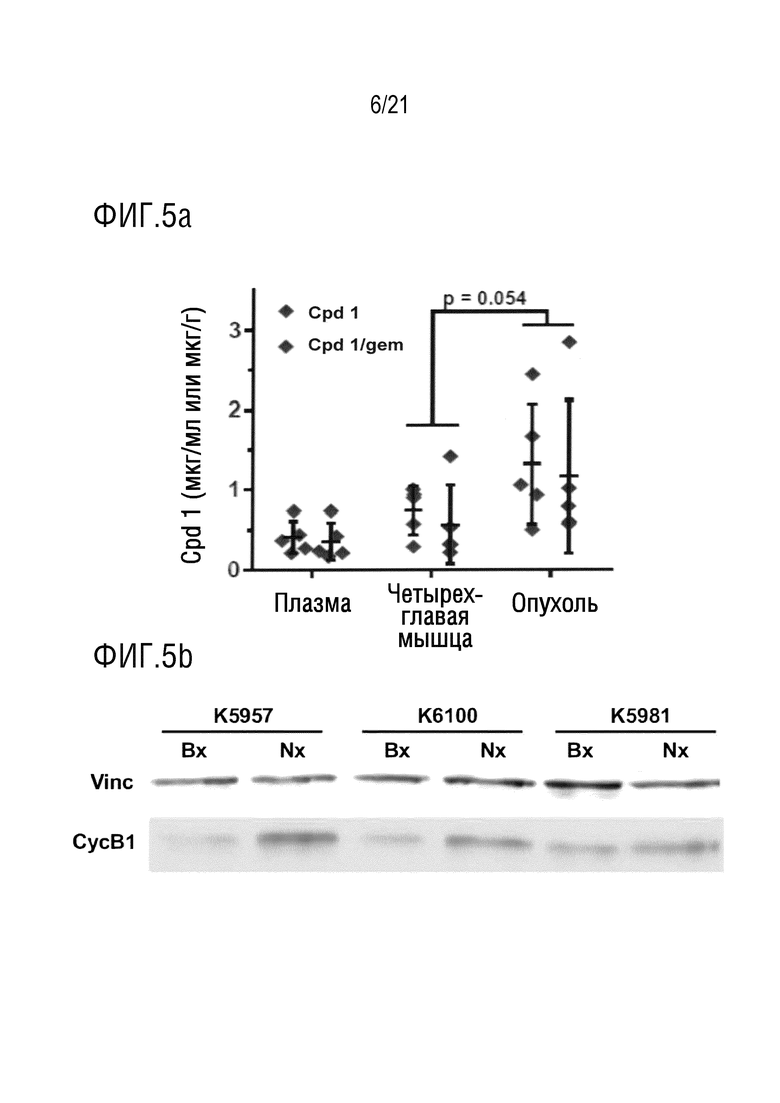
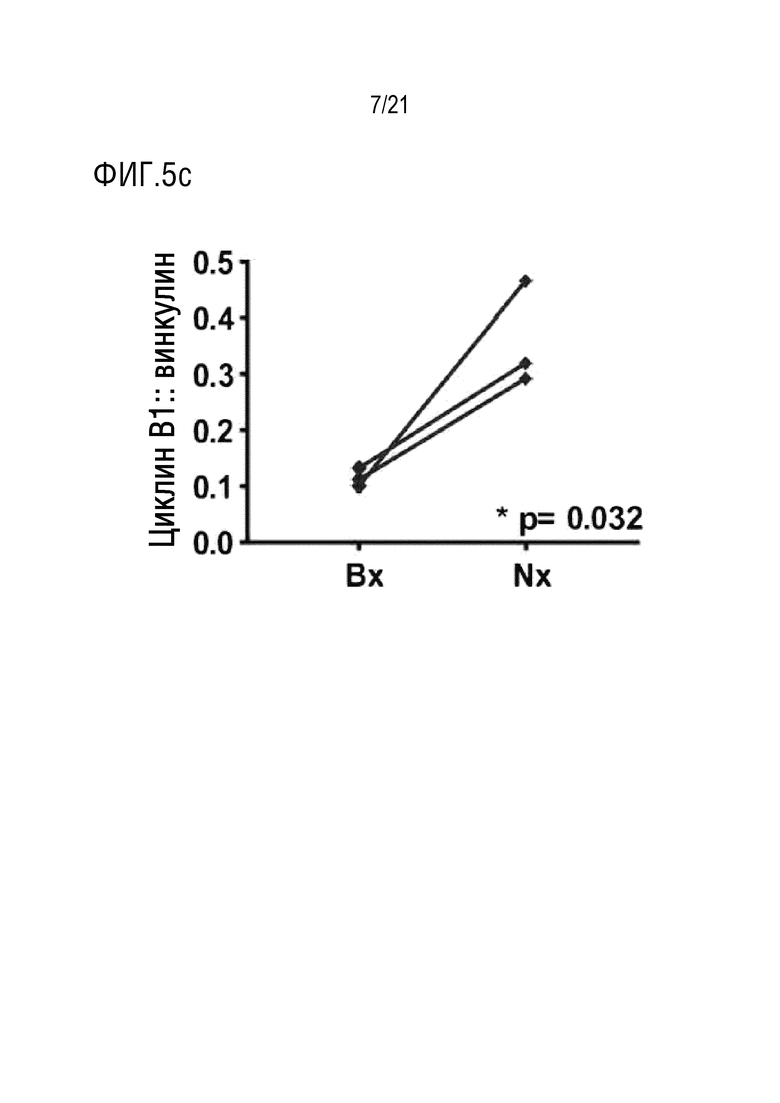
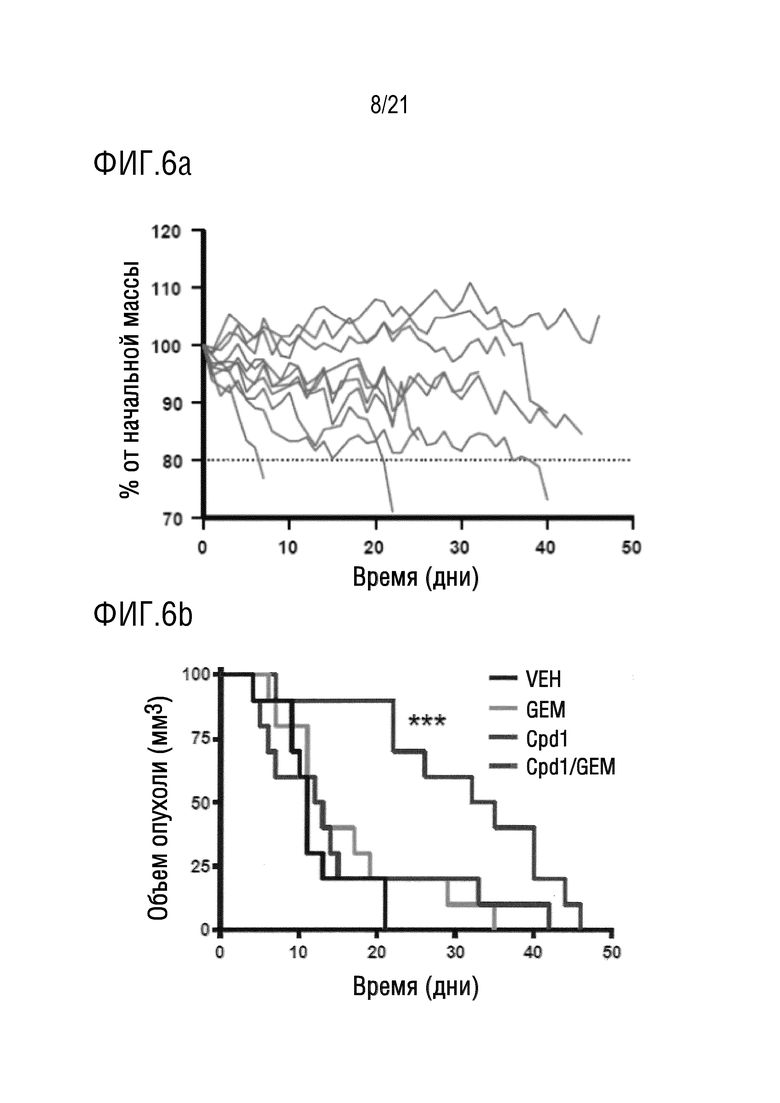
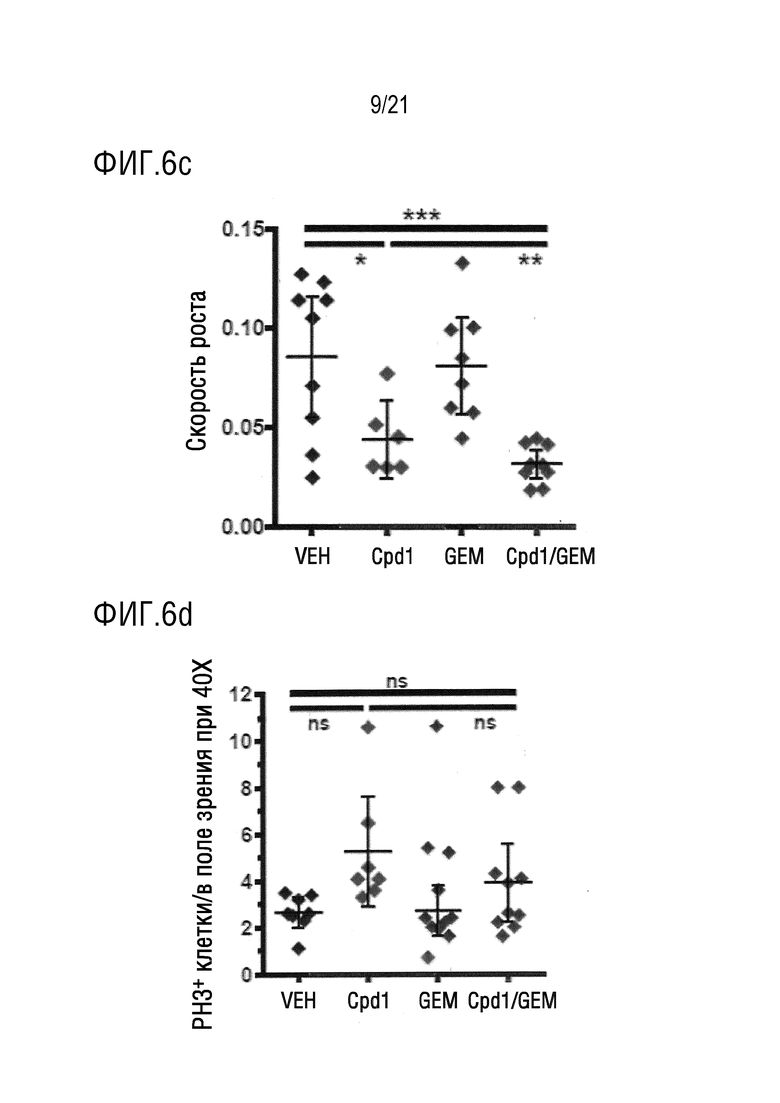
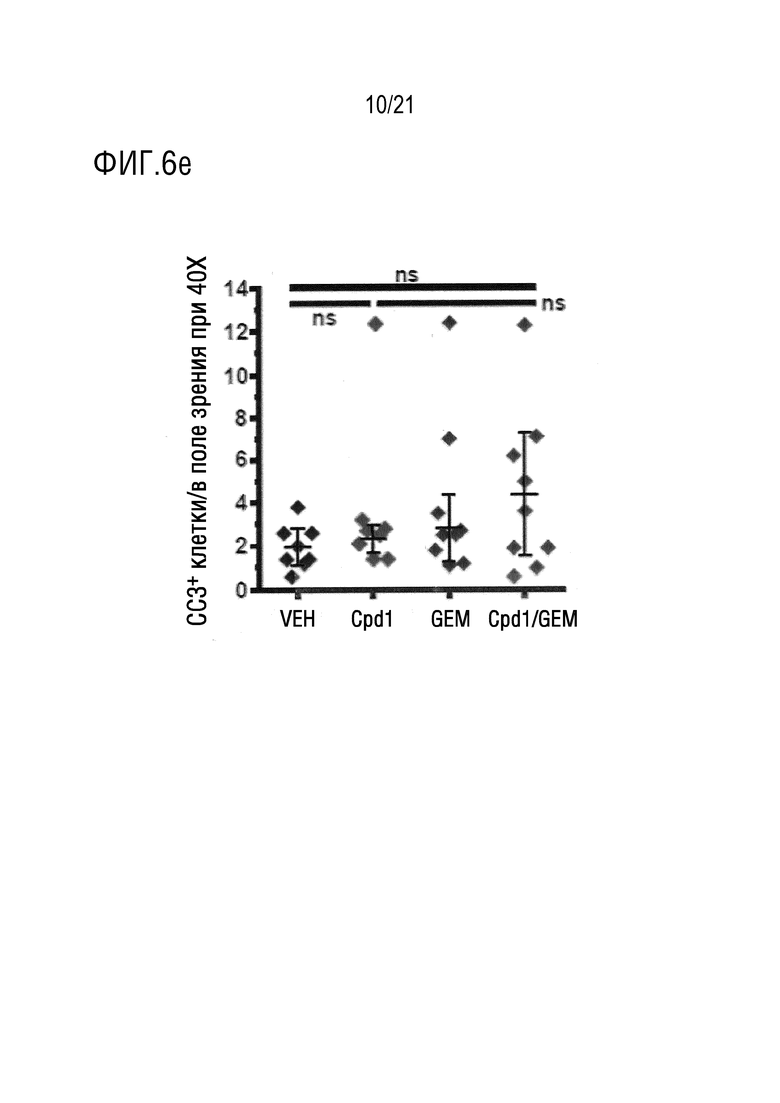
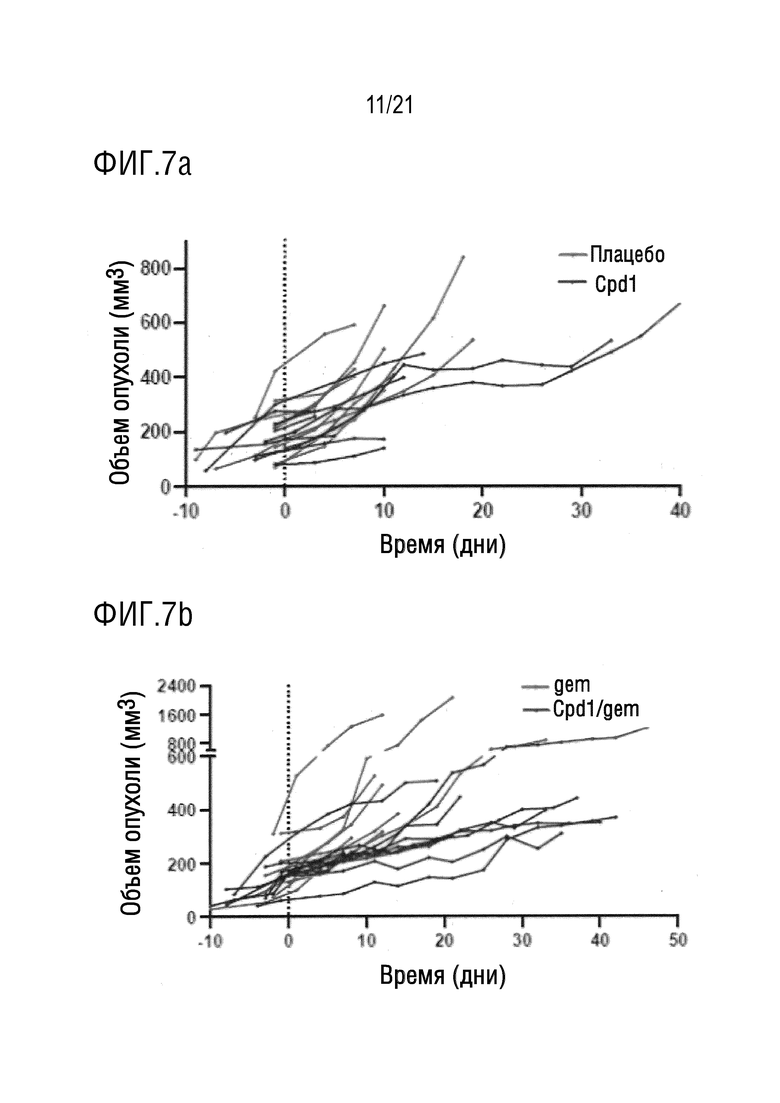
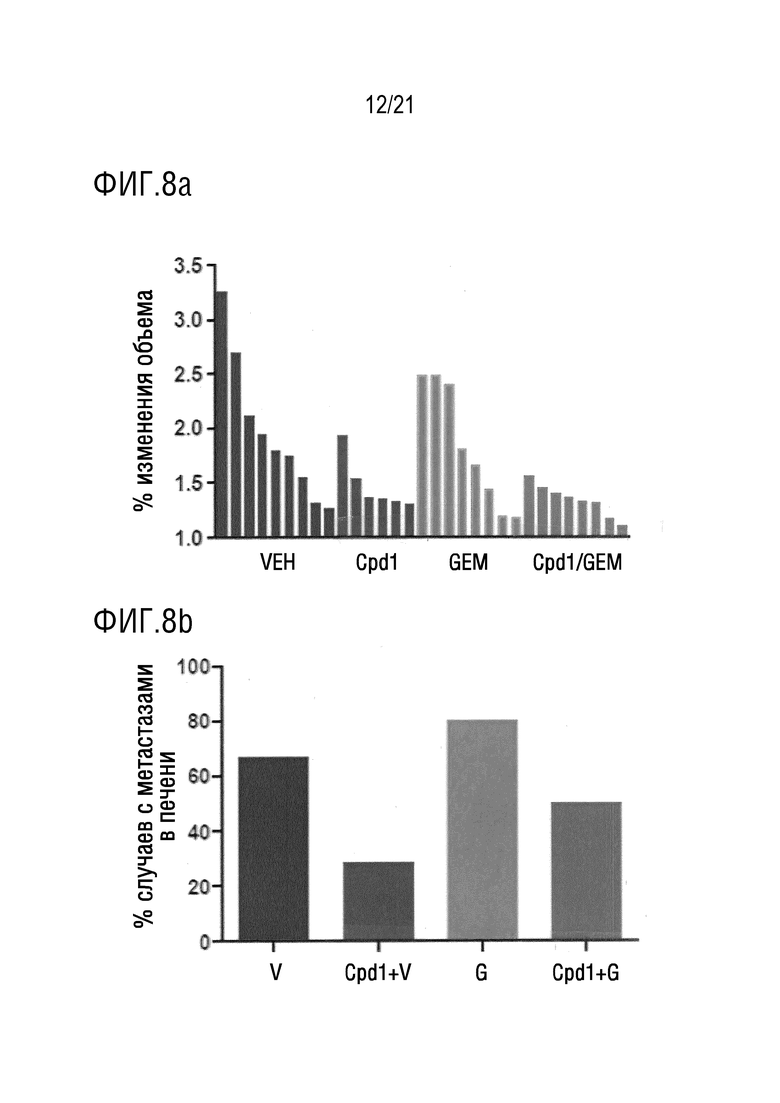
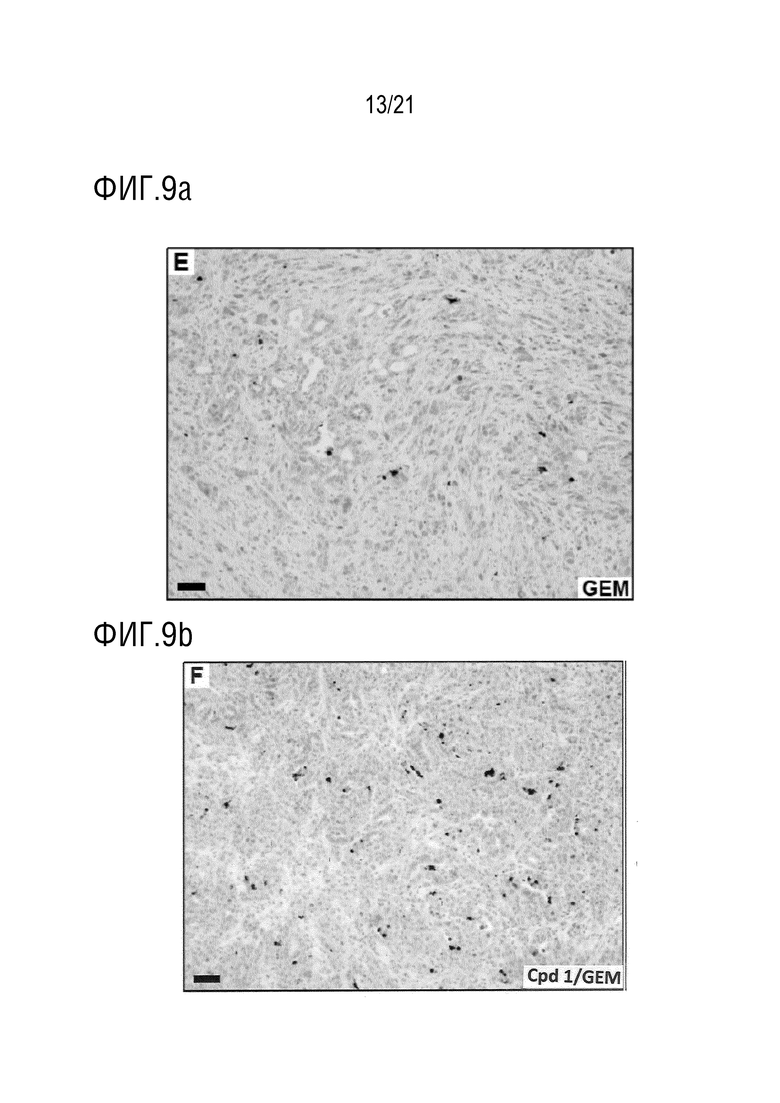
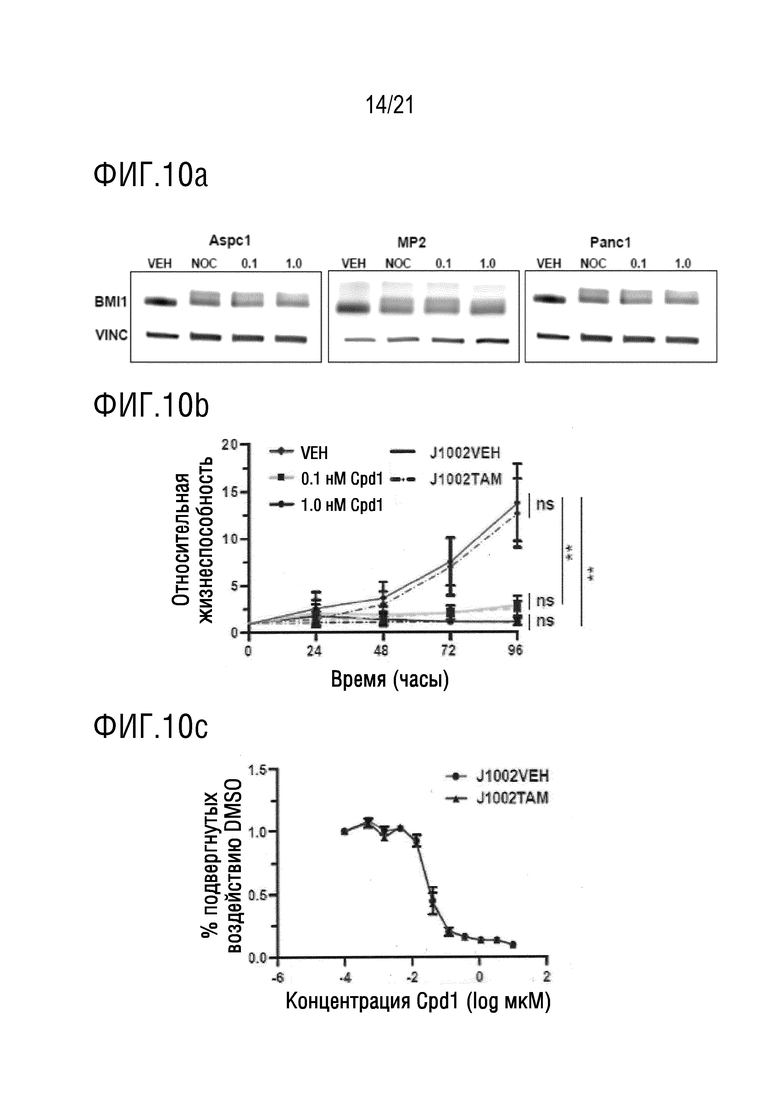
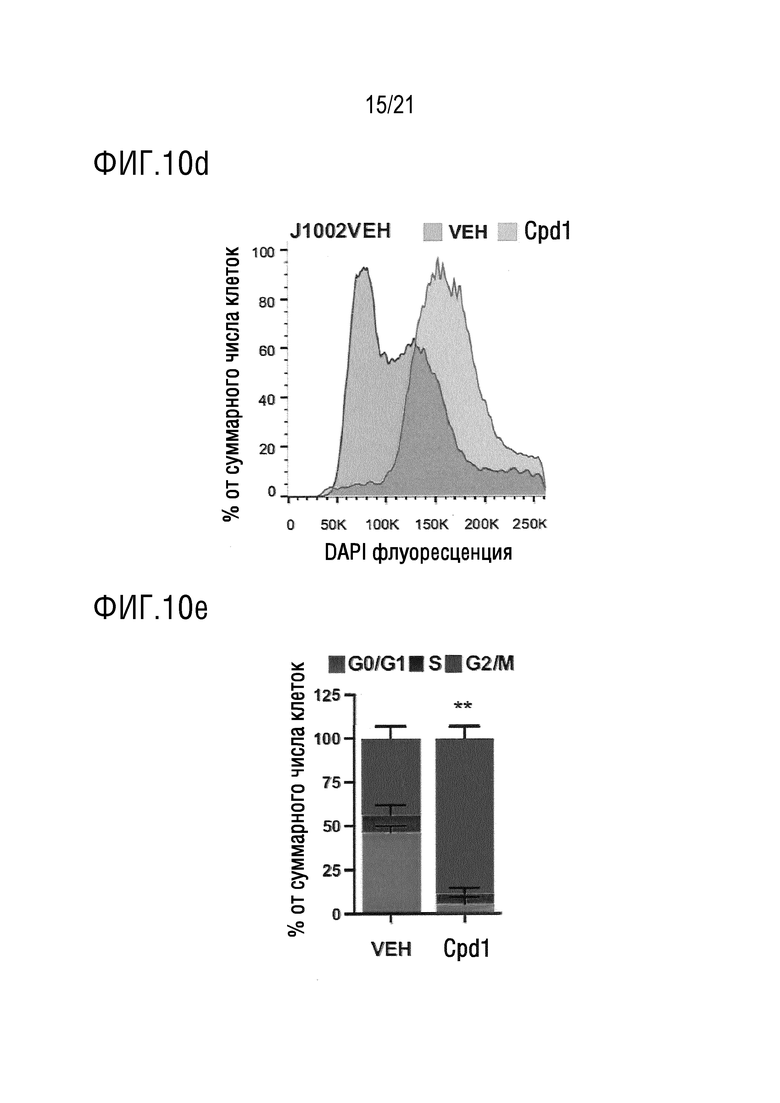
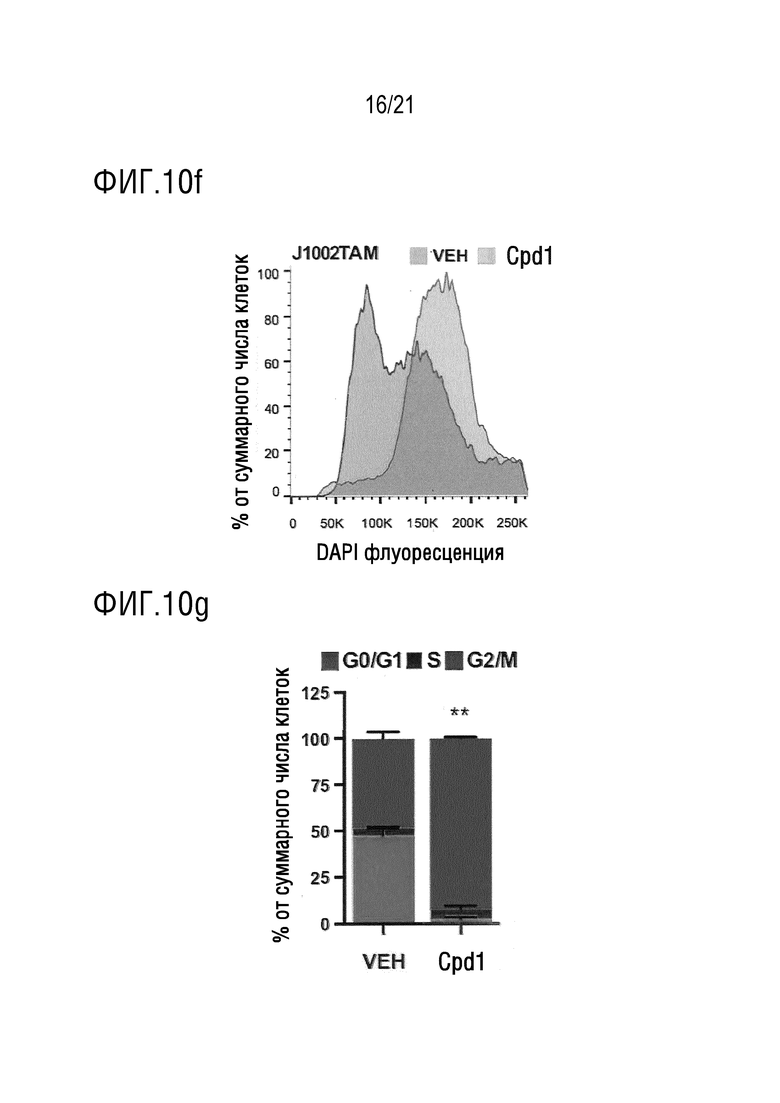
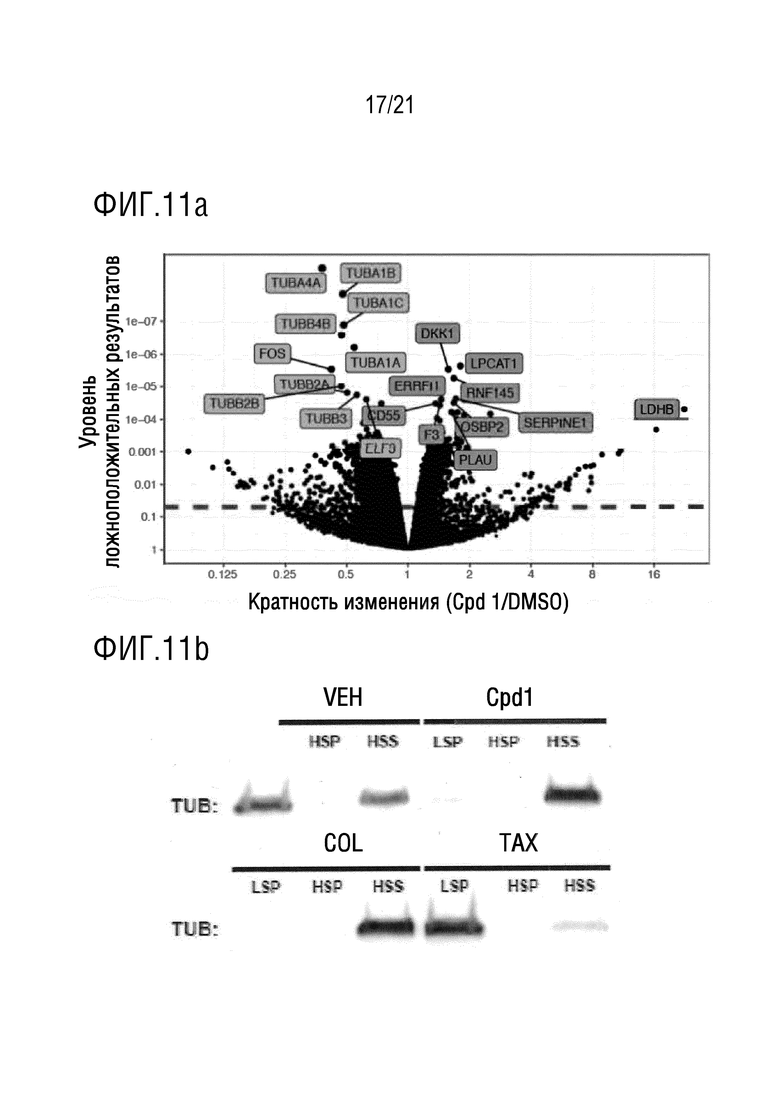
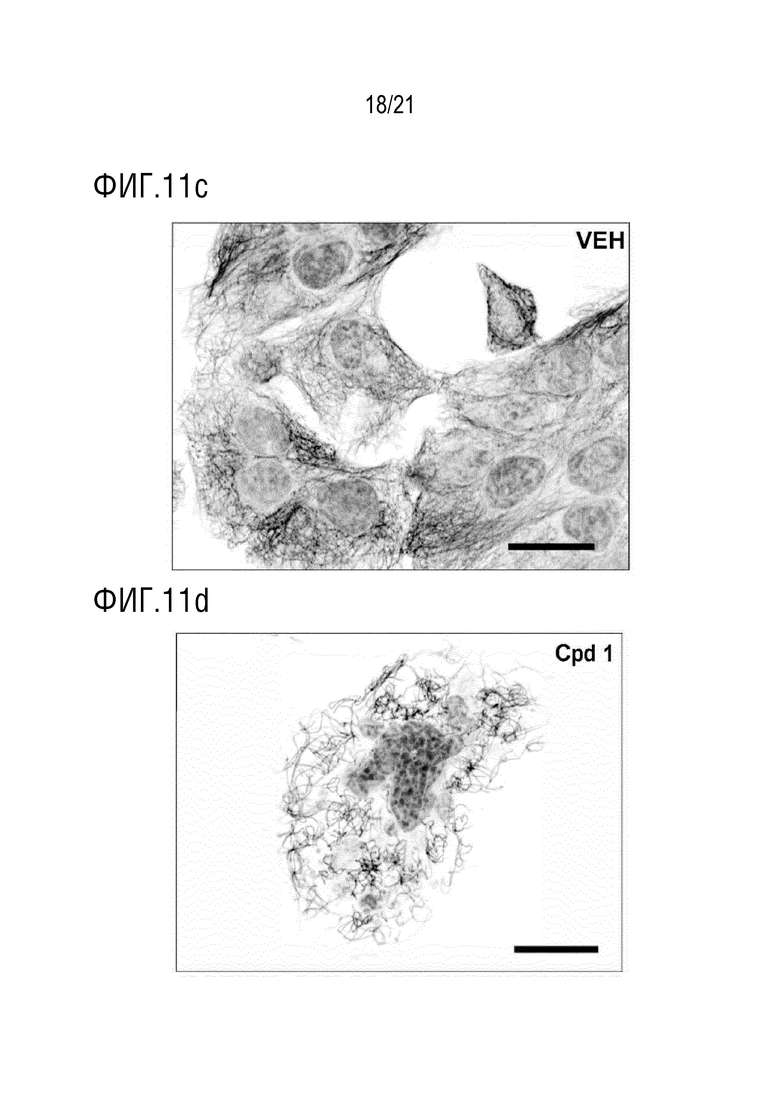
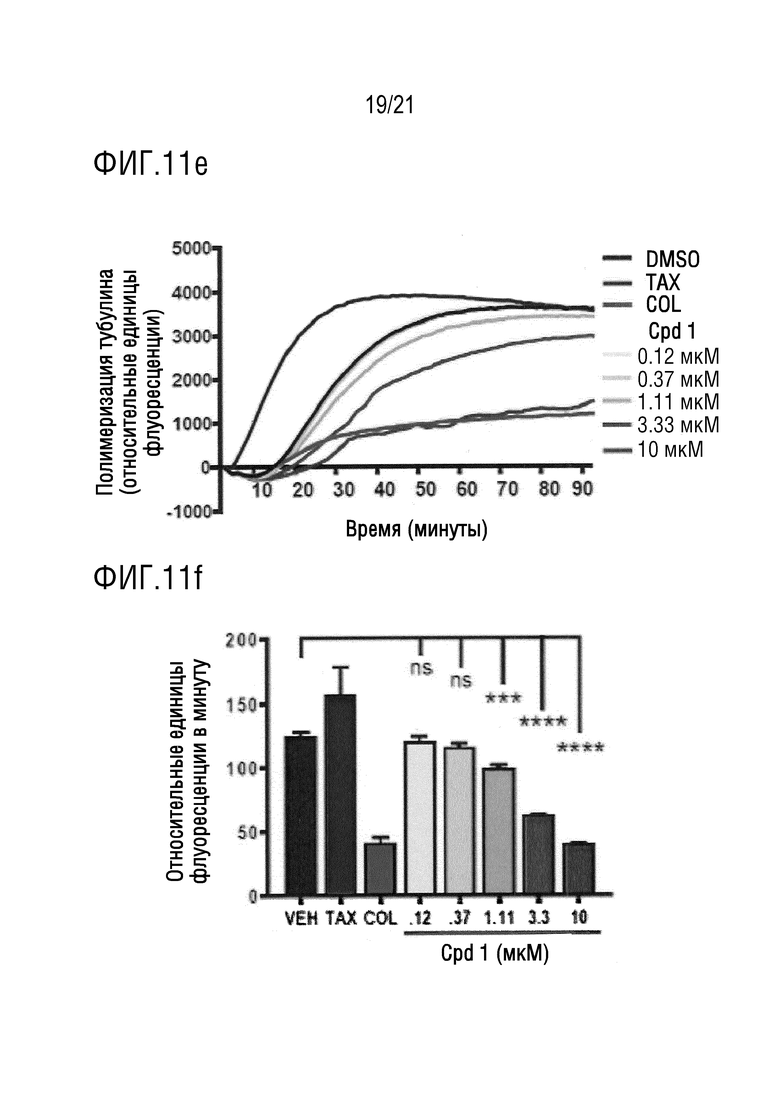
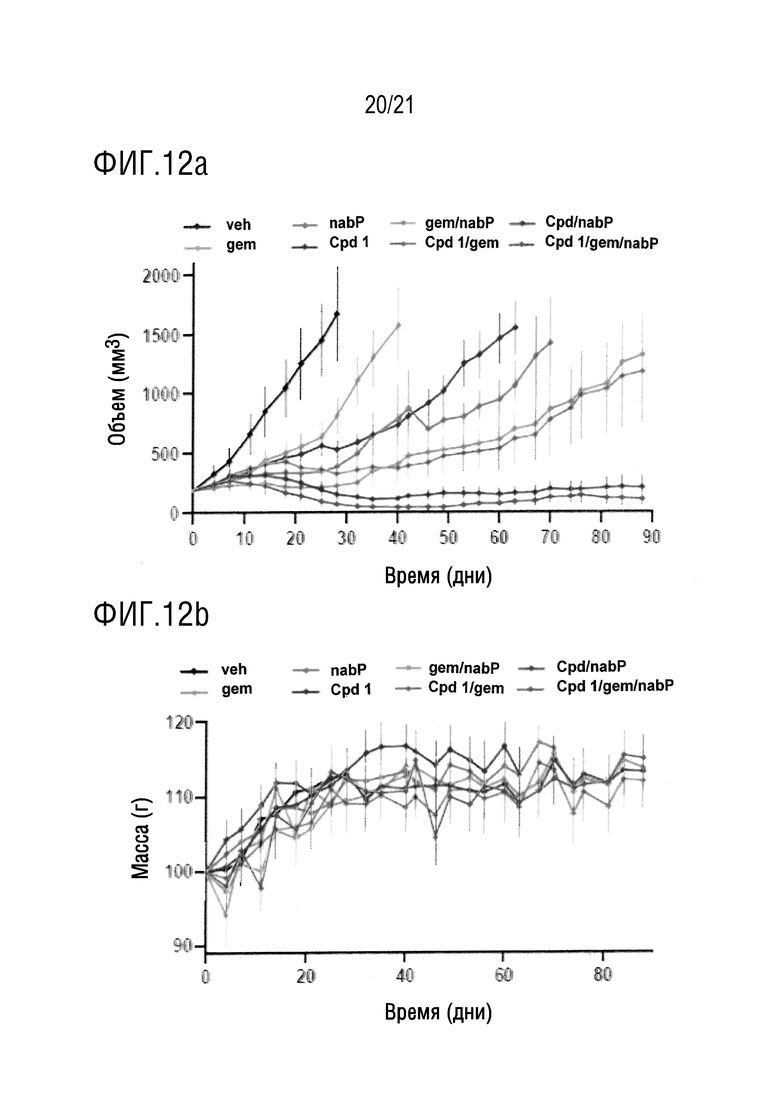
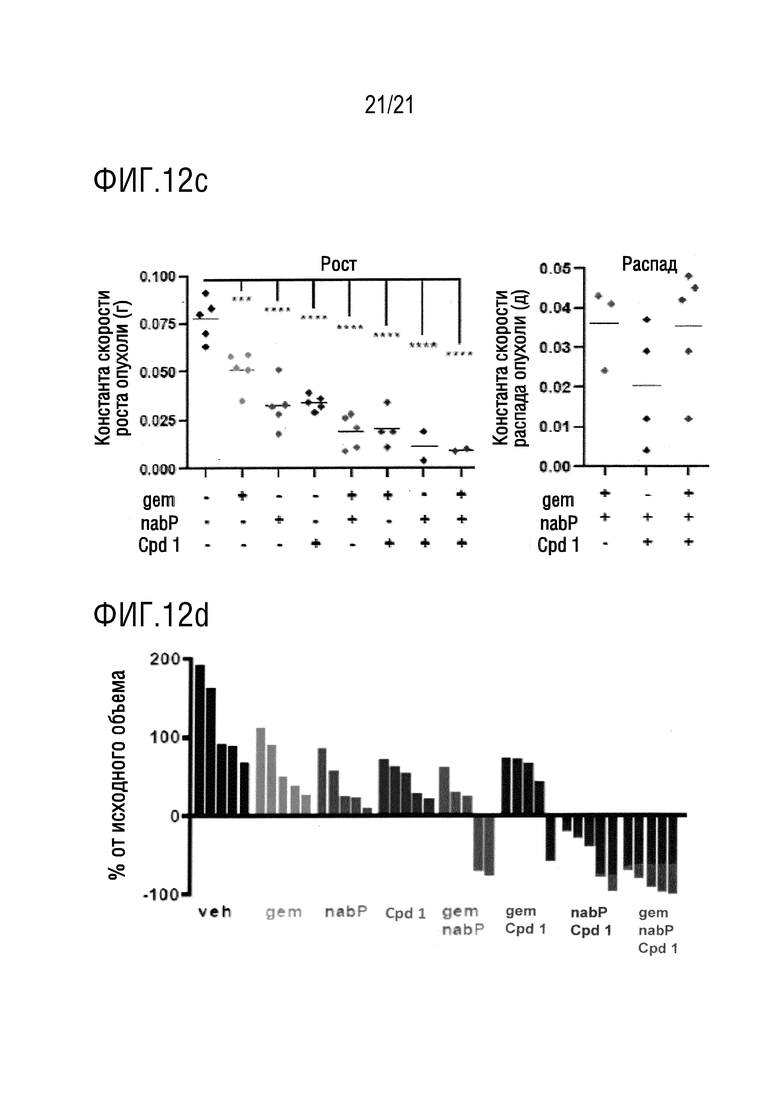
Группа изобретений относится к лечению рака поджелудочной железы. Предложено применение комбинации, состоящей по существу из соединения 5 фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4[4(трифторметил)фенил]пиримидин-4,6-диамина, имеющего структуру Формулы (I):
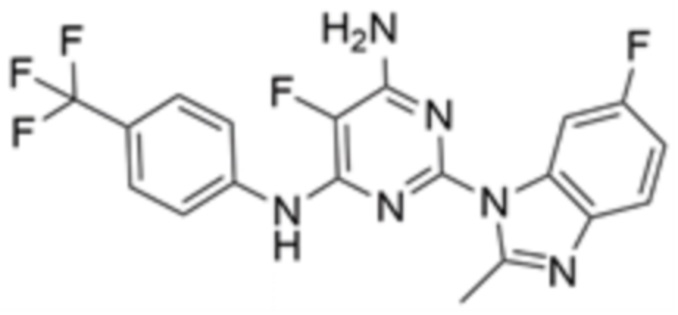
или его фармацевтически приемлемой соли, и наб-паклитаксела, для лечения рака поджелудочной железы, включающего введение субъекту, нуждающемуся в этом, эффективного количества указанного соединения и наб-паклитаксела. Предложено также применение указанной комбинации веществ в эффективном количестве в получении набора для лечения рака поджелудочной железы. Группа изобретений обеспечивает эффективное лечение и продолжительную ремиссию рака. 2 н. и 3 з.п. ф-лы, 12 ил.
1. Применение комбинации, состоящей по существу из соединения 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4[4(трифторметил)фенил]пиримидин-4,6-диамина, имеющего структуру Формулы (I):
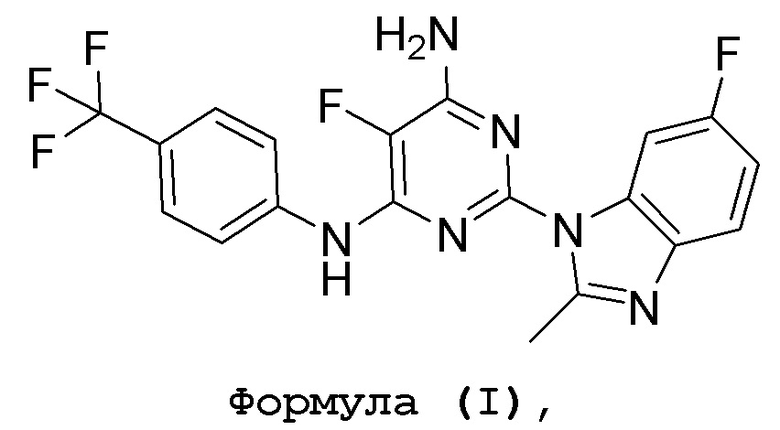
или его фармацевтически приемлемой соли, и наб-паклитаксела, для лечения рака поджелудочной железы, включающего введение субъекту, нуждающемуся в этом, эффективного количества указанного соединения и наб-паклитаксела.
2. Применение по п.1, где рак поджелудочной железы представляет собой аденокарциному протоков поджелудочной железы.
3. Применение по п.1, где фармацевтическая композиция содержит 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4[4(трифторметил)фенил]пиримидин-4,6-диамин или его фармацевтически приемлемую соль.
4. Применение комбинации, состоящей по существу из эффективного количества соединения 5-фтор-2-(6-фтор-2-метил-1H-бензо[d]имидазол-1-ил)-N4[4(трифторметил)фенил]пиримидин-4,6-диамина, имеющего структуру Формулы (I):

или его фармацевтически приемлемой соли, и эффективного количества наб-паклитаксела, в получении набора для лечения рака поджелудочной железы.
5. Применение по п.4, где рак поджелудочной железы представляет собой аденокарциному протоков поджелудочной железы.
| Jaime Eberle-Singh | |||
| Delineating the function, efficacy, and mechanism of a novel preclinical agent for the treatment of pancreatic ductal adenocarcinoma | |||
| COLIUMBIA UNIVERSITY | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Приспособление для записи начала и конца работы в устройствах для регистрации простоя и работы станков и Машин | 1929 |
|
SU28033A1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ИМИДАЗО[4,5-с]ПИРИДИНА, В КАЧЕСТВЕ АНТАГОНИСТА ПУТИ HEDGEHOG | 2010 |
|
RU2533825C2 |
| WO2013004332 A1, 10.01.2013. | |||
Авторы
Даты
2024-11-26—Публикация
2019-08-17—Подача