ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к применимой для ингаляции жидкой фармацевтической композиции, содержащей энсифентрин и гликопирролат. Изобретение также относится к небулайзеру, содержащему эту жидкую фармацевтическую композицию.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
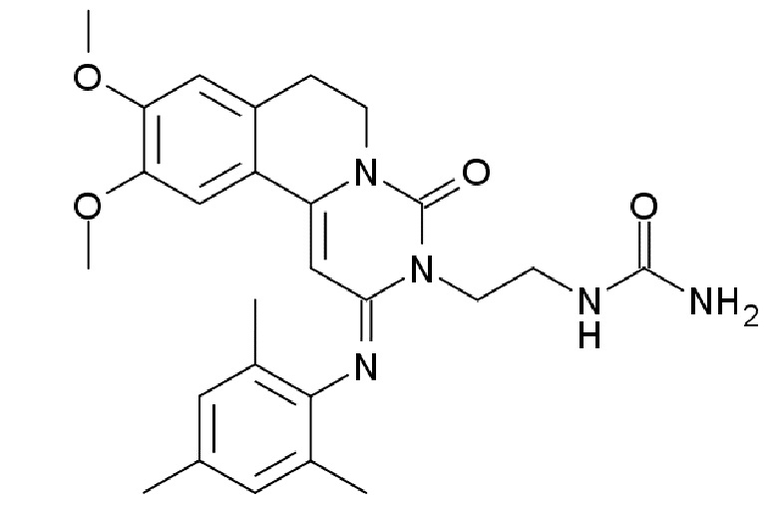
Энсифентрин (N-(2-{(2E)-9,10-диметокси-4-оксо-2-[(2,4,6-триметилфенил)имино]-6,7-дигидро-2H-пиримидо[6,1-a]изохинолин-3(4H)-ил}этил)мочевина, также известный как RPL554) представляет собой двойной ингибитор фосфодиэстеразы 3 и фосфодиэстеразы 4 (ФДЭ3/ФДЭ4) и описан в международной заявке WO 00/58308 A1.
В качестве комбинированного ингибитора ФДЭ3/ФДЭ4энсифентрин обладает как бронхолитической, так и противовоспалительной активностью и полезен при лечении респираторных заболеваний, таких как астма и хроническая обструктивная болезнь легких (ХОБЛ). Структура энсифентрина показана ниже.
Международная заявка WO 2016/042313 A описывает композиции энсифентрина в виде суспензии частиц в водном разбавителе.
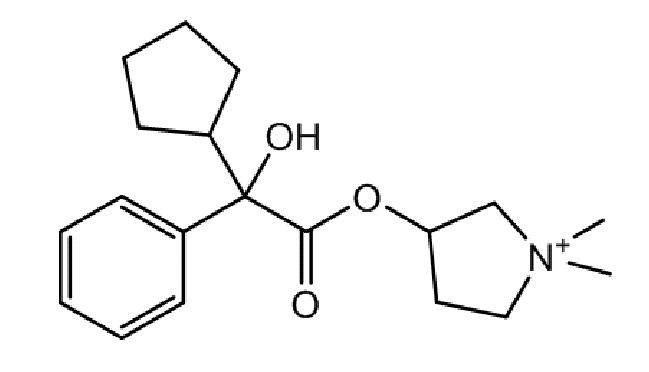
Энсифентрин можно использовать в сочетании с антагонистом мускариновых рецепторов гликопирролатом. Используемый здесь термин «гликопирролат» означает соль, содержащую катион гликопиррония. Гликопирроний имеет формулу (1,1-диметилпирролидин-1-ий-3-ил)-2-циклопентил-2-гидрокси-2-фенилацетат. Структура гликопиррония показана ниже.
Комбинация энсифентрина и гликопирролата, подходящая для лечения респираторных заболеваний, описана в международной заявке WO 2014/140648 A.
Комбинация фармацевтических соединений является сложной и непредсказуемой. Это особенно относится к случаю жидких фармацевтических композиций для введения путем ингаляции. Например, такие применимые для ингаляциижидкие фармацевтические композиции должны быть достаточно стабильными, чтобы во время ингаляции доставлялась подходящая постоянная доза, даже после хранения в течение определенного периода времени. Трудности, связанные с приготовлением применимой для ингаляции фармацевтической композиции усугубляются, когда эта композиция содержит два активных агента, например, как в случае комбинации энсифентрина и гликопирролата. Для такого комбинированиякомпозиций необходимо контролировать стабильность обоих фармацевтических соединений.
Существует потребность в разработке жидкой фармацевтической композиции, содержащей энсифентрин и гликопирролат, в которой оба соединения являются стабильными. Также желательно получать жидкую фармацевтическую композицию, которая пригодна для введения путем ингаляции.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Неожиданным открытием настоящего изобретения является то, что фармацевтическая композиция, в которой как энсифентрин, так и гликопирролат являются стабильными, может быть получена путем приготовления композиции энсифентрина в виде суспензии частиц и гликопирролата в виде раствора в водном разбавителе при низком рН и в которой концентрация гликопирролата является низкой по сравнению с концентрацией энсифентрина. Было показано, что эта конкретная композиция, в которой энсифентрин является суспендированным, а гликопирролат растворенным, стабильна в отношении химического разложения обоих активных агентов после хранения в течение по меньшей мере трех месяцев.
Соответственно изобретение представляет жидкую фармацевтическую композицию, пригодную для введения путем ингаляции, содержащую: (i) частицы энсифентрина, (ii) гликопирролат и (iii) разбавитель, и этот разбавитель содержит воду, причемгликопирролат растворен в разбавителе, концентрация гликопирролата меньше или равна 5,0 мг/мл, а рН этой жидкой фармацевтической композиции составляет от 3,0 до 6,0.
Изобретение также представляетнебулайзер, содержащий жидкую фармацевтическую композицию согласно изобретению.
Кроме того, изобретение представляет жидкую фармацевтическую композицию согласно изобретению для применения при лечении организма человека или животного.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Жидкая фармацевтическая композиция содержит гликопирролат. Гликопирролат обычно присутствует в жидкой фармацевтической композиции в виде фармацевтически приемлемой соли гликопиррония. Гликопирролат обычно представляет собой бромидную соль, бромид гликопиррония, но можно использовать и другие фармацевтически приемлемые соли гликопиррония, например хлорид гликопиррония. Гликопирролат предпочтительно представляет собой бромид гликопиррония.
Гликопирролат растворяют в разбавителе. Соответственно, из общей массы гликопирролата, присутствующего в жидкой фармацевтической композиции, по меньшей мере некоторая часть (например, по меньшей мере 50 % массовых) растворена в разбавителе. Обычно практически весь гликопирролат растворен в разбавителе. Например, по меньшей мере 99,0 % массовыхгликопирролата может быть растворено в разбавителе по отношению к общей массе гликопирролата в жидкой фармацевтической композиции. Термин «растворен» имеет свое обычное значение для данной области техники, например такое, что гликопирролат находится в растворе в разбавителе и не может быть выделен с помощью стандартной фильтрации.
Фармацевтическая композиция представляет собой жидкую фармацевтическую композицию и, как таковая, является жидкой в условиях окружающей среды (например, при температурах от 10 до 40°С).
рН жидкой фармацевтической композиции составляет от 3,0 до 6,0. Обычно рН жидкой фармацевтической композиции составляет от 3,5 до 5,0. Например, рН жидкой фармацевтической композиции может составлять от 4,3 до 4,7. pH жидкой фармацевтической композиции может составлять от 3,5 до 4,5, например, от 3,8 до 4,2.
рН жидкой фармацевтической композиции обычно представляет собой рН, который измерен при температуре 20°С. рН жидкой фармацевтической композиции можно измерить любым подходящим способом. Например, рН может быть измерен с использованием потенциометрического рН-метра.
Жидкая фармацевтическая композиция обычно дополнительно содержит буфер. Буфер можно использовать для контроля рН жидкой фармацевтической композиции. Буфер обычно содержит слабую кислоту и сопряженное с ней основание. Примеры буферов включают цитратный буфер, фосфатный буфер, ацетатный буфер и бикарбонатный буфер.
Предпочтительно, буфер представляет собой цитратный буфер. Цитратный буфер обычно содержит лимонную кислоту и цитратную соль. Например, цитратный буфер может содержать лимонную кислоту и тринатрийцитрат. Лимонная кислота может представлять собой моногидрат лимонной кислоты. Тринатрийцитрат может представлять собой дигидрат тринатрийцитрата.
Концентрация буфера обычно составляет от 10,0 до 40,0 мг/мл. Предпочтительно, концентрация буфера составляет от 20,0 до 30,0 мг/мл. Концентрация буфера включает как компоненты кислоты, так и компоненты сопряженного основания в буфере.
Концентрация гликопирролата в жидкой фармацевтической композиции меньше или равна 5,0 мг/мл. Например, концентрация гликопирролата может составлять от 0,001 до 5,0 мг/мл. Обычно концентрация гликопирролата составляет от 0,01 мг/мл до 2,0 мг/мл, например от 0,01 до 1,0 мг/мл.
Предпочтительно, концентрация гликопирролата составляет от 0,02 мг/мл до 0,25 мг/мл. Например, концентрация гликопирролата может составлять от 0,14 до 0,16 мг/мл. Концентрация гликопирролата может составлять от 0,02 до 0,03 мг/мл, например,примерно 0,025 мг/мл (25 мкг/мл).
Жидкая фармацевтическая композиция содержит частицы энсифентрина. Частицы энсифентрина содержат энсифентрин (то есть, свободное основание энсифентрина) или его фармацевтически приемлемую соль. Обычно, частицы энсифентрина содержат энсифентрин. Частицы энсифентрина обычно содержат по меньшей мере 90,0 % масс.энсифентрина или его фармацевтически приемлемой соли, более предпочтительно, по меньшей мере 95,0 % масс. Частицы энсифентрина могут состоять в основном из энсифентрина или его фармацевтически приемлемой соли или могут состоять из энсифентрина или его фармацевтически приемлемой соли. Например, частицы энсифентрина могут состоять из свободного основания энсифентрина.
Композиция, которая состоит в основном из какого-либо компонента, обычно содержит только этот компонент и другие компоненты, которые существенно не влияют на основные характеристики компонента, из которого в основном состоит композиция. Композиция, состоящая в основном из какого-либо компонента, может содержать по меньшей мере 99,5 % масс. этого компонента по отношению к общей массе композиции.
Частицы энсифентрина в жидкой фармацевтической композиции обычно суспендированы в разбавителе. Соответственно, жидкая фармацевтическая композиция обычно содержит суспензию частиц энсифентрина. Также может случиться так, что некоторые или все частицы энсифентрина в жидкой фармацевтической композиции осели на дно сосуда, содержащего эту жидкую фармацевтическую композицию, например, после хранения в течение определенного периода времени. Частицы энсифентрина можно повторно суспендировать любым подходящим способом, например, с помощью взбалтывания этой жидкой фармацевтической композиции.
Массовое соотношение энсифентрин:гликопирролат в жидкой фармацевтической композиции может составлять от 1:5 до 200:1. Например, на каждый 1 граммэнсифентрина в композиции может присутствовать от 0,005 до 5,0 граммовгликопирролата. Как правило, общая концентрация энсифентрина в жидкой фармацевтической композиции больше, чем общая концентрация гликопирролата в этой жидкой фармацевтической композиции. Предпочтительно, массовое соотношение энсифентрин:гликопирролат в жидкой фармацевтической композиции составляет от 5:1 до 150:1. Массовое соотношение энсифентрин:гликопирролат в жидкой фармацевтической композиции может составлять от 15:1 до 120:1, например, от 8:1 до 12:1.
Концентрация частиц энсифентрина в жидкой фармацевтической композиции может представлять собой любую подходящую концентрацию, например от 0,01 до 400 мг/мл. Обычно концентрация частиц энсифентрина составляет от 0,1 до 5,0 мг/мл. Предпочтительно, концентрация частиц энсифентрина составляет от 0,1 до 2,5 мг/мл. Например, концентрация частиц энсифентрина может составлять от 0,15 до 0,5 мг/мл или от 1,0 до 2,0 мг/мл.
Частицы энсифентрина обычно имеют Dv50 от 0,5 мкм до 5,0 мкм. Частицы энсифентрина предпочтительно имеют Dv50 от 1,0 мкм до 2,0 мкм. Обычно Dv10 частиц энсифентрина составляет от 0,2 мкм до 1,0 мкм, а Dv90 частиц энсифентрина составляет от 2,5 мкм до 6,0 мкм. Например, Dv10 частиц энсифентрина может составлять от 0,4 мкм до 0,6 мкм, а Dv90 частиц энсифентрина может составлять от 2,8 мкм до 3,8 мкм.
Размеры частиц в данном документе описаны со ссылкой на значение Dv50, которое представляет собой средний размер частиц для объемного распределения. Таким образом, половина объема частиц имеет диаметр меньше значения Dv50, а половина объема частиц имеет диаметр больше этого значения Dv50. Это хорошо известный способ для описания распределения частиц по размерам. Параметры Dv10 и Dv90 также можно использовать для характеристики распределения размера частиц в образце. 10 % объема частиц имеют диаметр меньше значения Dv10. 90% объема частиц имеют диаметр меньше значения Dv90.
Методика, используемая для измерения значений Dv50 (и Dv10 и Dv90), как указано в данном документе, обычно представляет собой лазерную дифракцию. Распределение частиц энсифентрина по размерам может быть измерено с помощью лазерной дифракции с использованием системы мокрого диспергирования порошка. Например, распределение частиц по размерам можно измерить с помощью лазерной дифракции, с помощьюприбора MalvernSpraytec в сочетании с кюветой для мокрого диспергирования. Обычно, параметры прибора для MalvernSpraytec представляют собой следующие:
• частица - стандартная непрозрачная частица;
• показатель преломления частицы - 1,50;
• показатель преломления (мнимый) - 0,50;
• плотность частицы - 1,00;
• показатель преломления диспергатора - 1,33;
• блок контроллера - 1000 об/мин;
• тип измерения - временной;
• время начала выборки - 30 с;
• затемнение - 20% - 30%;
• диспергатор - 1% полисорбата 20 в деионизированной воде.
Частицы энсифентрина могут быть получены с помощью любого фармацевтически приемлемого процесса уменьшения размера или процесса производства с контролируемым размером частиц. Например, эти частицы могут быть получены путем распылительной сушки раствора энсифентрина, путем контролируемой кристаллизации или путем уменьшения размера твердой формы энсифентрина, например, с помощью воздушно-струйного измельчения, механической микронизации или измельчения в среде.
Разбавитель содержит воду. Разбавитель может, например, содержать воду и вторичный растворитель, такой как этанол. Как правило, жидкая фармацевтическая композиция содержит по меньшей мере 50 % массовых воды, в пересчете на общую массу жидкой фармацевтической композиции. Предпочтительно, разбавитель представляет собой воду, а жидкая фармацевтическая композиция содержит по меньшей мере 80 % массовых разбавителя, в пересчете на общую массу жидкой фармацевтической композиции. Разбавитель обычно является стерильным. Жидкая фармацевтическая композиция обычно является стерильной.
Жидкая фармацевтическая композиция обычно дополнительно содержит регулятор тоничности. Примеры регуляторов тоничности включают хлорид натрия, хлорид калия, глюкозу, глицерин и маннит. Предпочтительно, регулятором тоничности является хлорид натрия.
Концентрация регулятора тоничности обычно больше или равна 1,0 мг/мл (например, от 1,0 до 50,0 мг/мл). Предпочтительно, концентрация регулятора тоничности составляет от 4,0 до 20,0 мг/мл, более предпочтительно, от 6,0 до 12,0 мг/мл.
Жидкая фармацевтическая композиция обычно дополнительно содержит одно или несколько поверхностно-активных веществ. Одно или несколько поверхностно-активных веществ могут включать неионогенное поверхностно-активное вещество, анионное поверхностно-активное вещество, катионное поверхностно-активное вещество, цвиттер-ионное поверхностно-активное вещество или их смесь. Как правило, одно или несколько поверхностно-активных веществ включают неионогенное поверхностно-активное вещество.
Примеры поверхностно-активных веществ включают лецитин, олеиновую кислоту, простые алкиловые эфиры полиоксиэтиленгликоля (например, PEG 300, PEG 600, PEG 1000, Brij 30, Brij 35, Brij 56, Brij 76 и Brij 97), полипропиленгликоль (например, PPG 2000), простые алкиловые эфиры глюкозида, простые полиоксиэтиленгликолевые эфирыоктилфенола, простые полиоксиэтиленгликолевые эфирыалкилфенола, сложные алкиловые эфиры глицерина, сложные алкиловые эфиры полиоксиэтиленгликоля и сорбитана (полисорбаты, например, полисорбат 20, полисорбат 40, полисорбат 60 и полисорбат 80), сложные алкиловые эфиры сорбитана (например, монолауратсорбитана (Span 20), моноолеатсорбитана (Span 80) и триолеатсорбитана (Span 85)), кокамид MEA, кокамид DEA, додецилдиметиламиноксид, блок-сополимеры полиэтиленгликоля и полипропиленгликоля (полоксамеры), блок-сополимеры полиэтиленгликоля и полипропиленоксида (например, поверхностно-активные вещества Pluronic), поливинилпирролидон K25, поливиниловый спирт, олигомолочную кислоту, диоктилсульфосукцинат натрия и полиэтоксилированный амин таллового жира (POEA).
Предпочтительно, одно или несколько поверхностно-активных веществ включают полисорбат и/или сложный алкиловый эфир сорбитана. Одно или несколько поверхностно-активных веществ могут, например, включать полисорбат 20 (полиоксиэтилен (20)сорбитанамонолаурата), полисорбат 40 (полиоксиэтилен (20)сорбитанамонопальмитата), полисорбат 60 (полиоксиэтилен (20) сорбитанамоностеарата) или полисорбат 80 (полиоксиэтилен(20)сорбитанамоноолеата). Одно или несколько поверхностно-активных веществ могут, например, включать сорбитанамонолаурат (Span 20), сорбитанамоноолеат (Span 80) или сорбитанатриолеат (Span 85). Предпочтительно, жидкая фармацевтическая композиция содержит полисорбат 20 и/или сорбитанамонолаурат (Span 20).
Жидкая фармацевтическая композиция может содержать два или более поверхностно-активных вещества или эта жидкая фармацевтическая композиция может содержать одно поверхностно-активное вещество. Например, композиция может содержать одно поверхностно-активное вещество, которое представляет собой полисорбат, например, полисорбат 20. Композиция может содержать два или более поверхностно-активных вещества. Например, жидкая фармацевтическая композиция может содержать полисорбат 20 и сорбитанамонолаурат (Span 20).
Общая концентрация одного или нескольких поверхностно-активных веществ обычно составляет от 0,01 до 2,0 мг/мл. Предпочтительно, общая концентрация поверхностно-активного вещества составляет от 0,1 до 1,0 мг/мл. Например, общая концентрация поверхностно-активного вещества в жидкой фармацевтической композиции может составлять от 0,25 до 0,75 мг/мл. Жидкая фармацевтическая композиция может, например, содержать полисорбат в концентрации от 0,1 до 1,0 мг/мл и при желаниисложный алкиловый эфир сорбитана в концентрации от 0,01 до 0,1 мг/мл.
Жидкая фармацевтическая композиция обычно содержит:
(i) частицы энсифентрина;
(ii) гликопирролат;
(iii) разбавитель;
(iv) полисорбатное поверхностно-активное вещество;
(v) цитратный буфер и
(vi) хлорид натрия.
Например, жидкая фармацевтическая композиция может содержать:
(i) от 0,1 до 2,5 мг/мл частиц энсифентрина, при желании от 0,5 до 2,5 мг/мл частиц энсифентрина;
(ii) от 0,01 мг/мл до 2,0 мг/мл бромида гликопиррония;
(iii) воду;
(iv) от 0,1 до 1,0 мг/мл полисорбата 20;
(v) от 5,0 до 15,0 мг/мл лимонной кислоты;
(vi) от 10,0 до 20,0 мг/мл тринатрия цитрата и
(vii) от 5,0 до 15,0 мг/мл хлорида натрия.
Жидкая фармацевтическая композиция может, например, содержать:
(i) частицы энсифентрина;
(ii) гликопирролат;
(iii) разбавитель;
(iv) полисорбатное поверхностно-активное вещество;
(v) поверхностно-активное вещество на основе сложного алкилового эфира сорбитана;
(vi) цитратный буфер и
(vii) хлорид натрия.
Например, жидкая фармацевтическая композиция может содержать:
(i) от 0,1 до 2,5 мг/мл частиц энсифентрина, при желании от 0,5 до 2,5 мг/мл частиц энсифентрина;
(ii) от 0,01 мг/мл до 2,0 мг/мл бромида гликопиррония;
(iii) воду;
(iv) от 0,1 до 1,0 мг/мл полисорбата 20;
(v) от 0,01 до 0,1 мг/мл монолауратасорбитана;
(vi) от 5,0 до 15,0 мг/мл лимонной кислоты;
(vii) от 10,0 до 20,0 мг/мл тринатрия цитрата и
(viii) от 5,0 до 15,0 мг/мл хлорида натрия.
Жидкая фармацевтическая композиция может состоять или в основном состоять из компонентов от (i) до (vi), компонентов от (i) до (vii) или компонентов от (i) до (viii).
Жидкая фармацевтическая композиция имеет преимущество стабильности. В частности, эта жидкая фармацевтическая композиция обычно стабильна по отношению к химическому разложению энсифентрина и гликопирролата в течение по меньшей мере одного месяца при хранении при температуре 25°С и относительной влажности 60%. Эта жидкая фармацевтическая композиция может, например, быть стабильной в этих условиях в течение по меньшей мере трех месяцев.
Жидкая фармацевтическая композиция может быть получена с помощью стандартных способов составления композиций. Жидкую фармацевтическую композицию обычно получают способом, включающим растворение гликопирролата в разбавителе для получения раствора гликопирролата и смешивание частиц энсифентрина с этим раствором гликопирролата для получения суспензии частиц энсифентрина. В качестве альтернативы, жидкая фармацевтическая композиция может быть получена способом, включающим смешивание частиц энсифентрина с разбавителем с получением суспензии частиц энсифентрина, а затем растворение гликопирролата в этой суспензии.
Жидкая фармацевтическая композиция пригодна для введения путем ингаляции. Как правило, эта жидкая фармацевтическая композиция подходит для введения с помощью небулайзера.
Изобретение представляетнебулайзер, содержащий жидкую фармацевтическую композицию согласно изобретению. В этот небулайзеробычно загружают жидкую фармацевтическую композицию. Небулайзер обычно содержит от примерно 1,0 мл до примерно 200 мл, более типично, от 1,0 мл до 20 мл жидкой фармацевтической композиции. Небулайзер предпочтительно содержит от 2,0 мл до 5,0 мл жидкой фармацевтической композиции, например, около 2,5 мл.
Небулайзеры распыляют жидкую фармацевтическую композицию до аэрозоля, который вдыхается в дыхательные пути субъекта. Примеры небулайзеров включают небулайзеры, продуцирующие мягкий аэрозоль, небулайзер на основе технологии вибрирующего сита, струйный небулайзер и ультразвуковой небулайзер. Подходящие приборы небулайзеры включают Philips I-neb™ (Philips), Philips SideStream (Philips), AeroNeb® (Philips), Philips InnoSpire Go (Philips), Pari LC Sprint (Pari GmbH), ингаляционную систему доставки AERxR™ (Aradigm Corp) и многоразовый небулайзер Pari LC Plus (Pari GmbH).
Энсифентрин полезен при лечении респираторных заболеваний и воспалительных заболеваний. Гликопирролат полезен при лечении респираторных заболеваний. Было обнаружено, что энсифентрин и гликопирролат взаимодействуют синергически, вызывая расслабление гладкой мускулатуры бронхов. Изобретение предоставляет жидкую фармацевтическую композицию согласно изобретению для применения при лечении организма человека или животного. Обычно эту жидкую фармацевтическую композицию вводят путем ингаляции.
Жидкая фармацевтическая композиция обычно предназначена для лечения или профилактики заболевания или состояния, выбранного из хронической обструктивной болезни легких (ХОБЛ), астмы, аллергической астмы, сенной лихорадки, аллергического ринита, бронхита, эмфиземы, бронхоэктатической болезни, респираторного дистресс-синдрома взрослых (ARDS), стероидорезистентной астмы, тяжелой астмы, детской астмы, муковисцидоза, фиброза легких, пневмофиброза, интерстициального заболевания легких, кожного заболевания, атопического дерматита, псориаза, воспаления глаз, церебральной ишемии, воспалительногозаболевания и аутоиммунного заболевания. Предпочтительно, заболевание или состояние представляет собой ХОБЛ или астму. Более предпочтительно, заболевание или состояние представляет собой хроническую обструктивную болезнь легких (ХОБЛ).
Эффективное количество энсифентрина обычно составляет примерно от 0,001 мг/кг до 50 мг/кг для однократной дозы, например, от 0,01 мг/кг до 1 мг/кг для однократной дозы. Эффективное количество энсифентрина может представлять собой дозу от примерно 0,1 мг до примерно 500 мг, или от примерно 0,1 мг до 100 мг, или от примерно 0,1 мг до примерно 6 мг. Разовая доза энсифентрина может составлять от 0,3 мг до 3 мг.
Эффективное количество гликопирролата обычно составляет примерно от 0,001 мг/кг до 25 мг/кг для однократной дозы, например, от 0,001 мг/кг до 0,5 мг/кг для однократной дозы. Эффективное количество гликопирролатаможет представлять собой дозуот примерно 0,01 мг до примерно 250 мг или от примерно 0,02 мг до 3 мг. Разовая доза гликопирролата может составлять от 0,02 мг до 2,0 мг.
Жидкую фармацевтическую композицию можно вводить один, два или три раза в день или можно вводить дважды, три раза, четыре раза или пять раз в неделю. Например, фармацевтическую композицию можно вводить два раза в день.
Изобретение также представляет применение жидкой фармацевтической композиции, как определено в данном документе, в производстве лекарственного средства для лечения заболевания или состояния, как определено в данном документе.
Изобретение описано более подробно с помощью следующих примеров.
ПРИМЕРЫ
Методы
Анализ и тестирование соответствующих веществ проводили с использованием высокоэффективной жидкостной хроматографии с подвижной фазой ацетонитрил:вода.
Пример 1 - приготовление композиций
Были приготовлены пять фармацевтических композиций (композиций от А до Е), содержащихэнсифентрин и бромид гликопиррония (GP).
Состав этих пяти композиций показан в Таблице 1.
В каждом случае сначала готовили суспензию частиц энсифентрина в концентрации 1,5 мг/мл в одном из двух носителей:
(i) водный раствор полисорбата 20, сорбитанамонолаурата, моногидрата мононатрийфосфата, безводного двухосновного фосфата натрия и хлорида натрия для композиций от А до С или
(ii) водный раствор полисорбата 20, моногидрата лимонной кислоты, дигидрата тринатрия цитрата и хлорида натрия для композиций D и E.
Затем бромид гликопиррония растворяли в суспензии энсифентрина в указанной концентрации (0,15 мг/мл, 1,5 мг/мл или 15,0 мг/мл). Полученные композиции имели вид бледно-желтых суспензий, которые не содержали видимых агломератов после повторного суспендирования.
Было определено, что рН композиций от А до С составляет 6,7. Было определено, что pH композиций D и E составляет 4,5.
Пример 2 - стабильность композиций
Оценивали стабильность композиций от А до Е по отношению к химическому разложению активных ингредиентов. Образцы композиций объемом 5 мл хранили в закрытых стеклянных флаконах при трех различных типах условий: (а) 25°C/60% относительной влажности (RH); (b) 40°С/75% RH; и (c) 60°С. Все композиции тестировали после хранения при этих условиях в течение двух недель. Композиции D и E дополнительно тестировали после хранения при этих условиях в течение трех месяцев.
Результаты оценки стабильности спустя две недели представлены в Таблице 2.
Можно увидеть, что композиции с фосфатным буфером с рН 6,7 (А, В и С) были нестабильны при всех условиях через две недели, с наблюдаемым разложением гликопиррония. Композиция С после хранения при 60°С значительно разложилась, и частицы энсифентрина не могли быть повторно суспендированы даже после энергичного встряхивания.
И напротив, композиции D и E (композиции с цитратным буфером с pH 4,5) были более стабильны спустя две недели, чем композиции от A до C. Для композиции D после хранения при 25°C/60% RH или 40°C/75% RH разложения не наблюдалось. Незначительное разложение гликопиррония наблюдали для композиции D после хранения при 60°C.
Для композиции Е наблюдался некоторый низкий уровень разложения гликопиррония после хранения при 25°С/60% RH или 40°С/75% RH и более значительное разложение после хранения при 60°С.
Ввиду нестабильности композиции от А до С дальнейшую оценку стабильности этих композиций не проводили. Стабильность композиций D и E снова была оцененаспустя 3 месяца, а результаты представлены в Таблице 3.
Было обнаружено, что композиция D оставалась стабильной после хранения в течение 3 месяцев как при 25°C/60% RH, так и при 40°C/75% RH. После хранения при 60°С в течение 3 месяцев наблюдалось незначительноеразложениегликопиррония.
Некоторое химическоеразложение наблюдалось после хранения композиции Е в течение 3 месяцев при 25°C/60% RH. Более значительноеразложение наблюдалось после хранения в течение 3 месяцев при 40°C/75% RH и 60°C.
Заключение
Было обнаружено, что из пяти протестированныхкомпозиций только композиция D имеет подходящие характеристики стабильности после хранения. Соответственно, авторы изобретения обнаружили, что низкий рН и низкая концентрация гликопирролата по сравнению с концентрацией энсифентринаявляются важными для стабильнойкомпозиции комбинации гликопирролата и энсифентрина для применения в качестве ингаляционногопродукта.
Настоящее изобретение относится к жидкой стабильной фармацевтической композиции, пригодной для введения путем ингаляции, содержащей: (i) частицы энсифентрина, (ii) гликопирролат и (iii) разбавитель, и этот разбавитель содержит воду, причем гликопирролат растворен в разбавителе, концентрация гликопирролата меньше или равна 5,0 мг/мл, и рН этой жидкой фармацевтической композиции составляет от 3,0 до 6,0. 3 н. и 17 з.п. ф-лы, 3 табл., 2 пр.
1. Жидкая фармацевтическая композиция, пригодная для введения путем ингаляции, содержащая:
(i) частицы энсифентрина,
(ii) гликопирролат и
(iii) разбавитель, где указанный разбавитель содержит воду,
где концентрация частиц энсифентрина составляет от 0,1 до 5,0 мг/мл;
гликопирролат растворен в разбавителе,
концентрация гликопирролата меньше или равна 5,0 мг/мл; и
рН указанной жидкой фармацевтической композиции составляет от 3,0 до 6,0.
2. Жидкая фармацевтическая композиция по п. 1, в которой рН указанной жидкой фармацевтической композиции составляет от 3,5 до 5,0.
3. Жидкая фармацевтическая композиция по п. 1 или 2, в которой указанная жидкая фармацевтическая композиция дополнительно содержит буфер, причем предпочтительно буфер представляет собой цитратный буфер.
4. Жидкая фармацевтическая композиция по любому из пп. 1-3, в которой концентрация буфера составляет от 10,0 до 40,0 мг/мл, предпочтительно от 20,0 до 30,0 мг/мл.
5. Жидкая фармацевтическая композиция по любому из пп. 1-4, в которой концентрация гликопирролата составляет от 0,01 мг/мл до 2,0 мг/мл, предпочтительно от 0,02 мг/мл до 0,25 мг/мл.
6. Жидкая фармацевтическая композиция по любому из пп. 1-5, в которой массовое соотношение энсифентрин:гликопирролат в жидкой фармацевтической композиции составляет от 1:5 до 200:1, предпочтительно от 15:1 до 120:1.
7. Жидкая фармацевтическая композиция по любому из пп. 1-6, причем концентрация частиц энсифентрина составляет от 0,15 до 2,5 мг/мл.
8. Жидкая фармацевтическая композиция по любому из пп. 1-7, в которой частицы энсифентрина имеют Dv50 от 0,5 до 5,0 мкм.
9. Жидкая фармацевтическая композиция по любому из пп. 1-8, в которой гликопирролат представляет собой фармацевтически приемлемую соль гликопиррония,
в которой предпочтительно гликопирролат представляет собой бромид гликопиррония или хлорид гликопиррония,
в которой более предпочтительно гликопирролат представляет собой бромид гликопиррония.
10. Жидкая фармацевтическая композиция по любому из пп. 1-9, в которой разбавитель представляет собой воду, и указанная жидкая фармацевтическая композиция содержит по меньшей мере 80 масс.% разбавителя в пересчете на общую массу жидкой фармацевтической композиции.
11. Жидкая фармацевтическая композиция по любому из пп. 1-10, в которой указанная жидкая фармацевтическая композиция дополнительно содержит регулятор тоничности, причем предпочтительно регулятор тоничности представляет собой хлорид натрия.
12. Жидкая фармацевтическая композиция по п. 11, в которой концентрация регулятора тоничности больше или равна 1,0 мг/мл, предпочтительно составляет от 4,0 до 20,0 мг/мл, более предпочтительно от 6,0 до 12,0 мг/мл.
13. Жидкая фармацевтическая композиция по любому из пп. 1-12, в которой указанная жидкая фармацевтическая композиция дополнительно содержит одно или более поверхностно-активное вещество, причем предпочтительно одно или более поверхностно-активное вещество выбирают из полисорбата и сложного алкилового эфира сорбитана.
14. Жидкая фармацевтическая композиция по п. 13, в которой общая концентрация одного или более поверхностно-активного вещества составляет от 0,01 до 2,0 мг/мл, предпочтительно от 0,1 до 1,0 мг/мл.
15. Жидкая фармацевтическая композиция по любому из пп. 1-14, в которой указанная жидкая фармацевтическая композиция содержит:
(i) частицы энсифентрина;
(ii) гликопирролат;
(iii) разбавитель;
(iv) полисорбатное поверхностно-активное вещество;
(v) необязательно поверхностно-активное вещество на основе сложного алкилового эфира сорбитана;
(vi) цитратный буфер и
(vii) хлорид натрия.
16. Жидкая фармацевтическая композиция по любому из пп. 1-15, в которой указанная жидкая фармацевтическая композиция содержит:
(i) от 0,1 до 2,5 мг/мл частиц энсифентрина, необязательно от 0,5 до 2,5 мг/мл частиц энсифентрина;
(ii) от 0,01 мг/мл до 2,0 мг/мл бромида гликопиррония;
(iii) воду;
(iv) от 0,1 до 1,0 мг/мл полисорбата 20;
(v) необязательно от 0,01 до 0,1 мг/мл монолаурата сорбитана;
(vi) от 5,0 до 15,0 мг/мл лимонной кислоты;
(vii) от 10,0 до 20,0 мг/мл тринатрия цитрата и
(viii) от 5,0 до 15,0 мг/мл хлорида натрия.
17. Жидкая фармацевтическая композиция по любому из пп. 1-16, в которой указанная жидкая фармацевтическая композиция пригодна для введения с помощью небулайзера.
18. Применение жидкой фармацевтической композиции по любому из пп. 1-17 для лечения или профилактики заболевания или состояния, выбранного из хронической обструктивной болезни легких (ХОБЛ) и астмы.
19. Применение по п. 18, в котором заболевание или состояние представляет собой хроническую обструктивную болезнь легких (ХОБЛ).
20. Способ лечения или профилактики заболевания или состояния, выбранного из хронической обструктивной болезни лёгких (ХОБЛ) и астмы, у нуждающегося в этом субъекта, где указанный способ включает введение указанному субъекту эффективного количества жидкой фармацевтической композиции по любому из пп. 1-17.
| WO 2014140648 A1, 2014.09.18 | |||
| ЖИДКАЯ ИНГАЛЯЦИОННАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ RPL 554 | 2015 |
|
RU2699995C2 |
| WO 2006008213 A1, 2006.01.26 | |||
| WO 2011157536 A1, 2011.12.22 | |||
| EP 1861361 A1, 2007.12.05 | |||
| US 2009215734 A1, 2009.08.27 | |||
| LUIGINO CALZETTA et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2024-12-05—Публикация
2021-02-26—Подача