Изобретение относится к полимерным композиционным материалам, точнее к биорезорбируемым композиционным материалам на основе волокон из хитозана и связующего из термопластичных биорезорбируемых полимеров на основе поли(α-гидроксиэфиров) для реконструкции костной ткани.
Изобретение предназначено для использования в медицине, в частности, в краниопластике. Изобретение может найти применение также в тканевой инженерии при получении тканеинженерных препаратов для лечения дефектов костной ткани различной этиологии.
Материал для реконструкции костной ткани должен обладать прочностными и упругими характеристиками, близкими к аналогичным параметрам нативной костной ткани, быть рентгенопрозрачным, устойчивым к инфекциям, обладать низкой теплопроводностью.
В настоящее время для реконструкции костей используют имплантаты различного состава и строения. Одним из основных материалов для изготовления имплантатов в настоящее время является титан и его сплавы, а также композиционные материалы, содержащие углеродные волокна, волокна природного происхождения, в частности, базальтовые. Кроме того, в качестве наполнителей применяют биорезорбируемые соли кальция - гидроксиапатит, трикальций фосфат в α и β модификациях, фосфат и карбонат кальция, альгинат натрия. В качестве связующего композиционных материалов используют коллаген, казеин, биоактивные стекла, гиалуроновую кислоту.
Для лечения дефектов костной ткани различной этиологии широко применяют аллотрансплантаты, которые получают из хрящевой и/или костной ткани человека или животных, а также компонентов кожи и сухожилий. (Ashammakhi N. et al. Spotlight on Naturally Absorbable Osteofixation Devices // Journal of Craniofacial Surgery. 2003. Vol. 14, № 2. P. 247-259. RU 2 702 520 C1, 2 702 520 C1). Костные фрагменты бедренной или большеберцовой кости измельчают до крошки размером от 1,0 мм до 500 мкм. Из полученной аутологичной костной ткани путем смешивания с β-трикальцийфосфатом готовят композит, который имплантируют в полость костного дефекта. Такие материалы должны быть подготовлены непосредственно перед трансплантацией, что доступно только крупным специализированным медицинским центрам, а, кроме того, наличие иммунологического барьера делает применение этих материалов весьма ограниченным.
В патенте RU 2813132 описан материал для стимуляции репаративных процессов в дефектах костной ткани, состоящий из коллагена и костной крошки. Материал содержит коллаген первого типа, выделенный из сухожилий тканевых доноров, в количестве 10-12 мас.%, костную крошку размером 250-630 мкм, полученную из тканевых доноров, в количестве 87-89 мас. %. Способ получения костно-пластического материала включает смешивание коллагена и костной крошки с последующей лиофилизацией. Для стимуляции репаративных процессов в дефектах костной ткани, применяют вымачивание материала в изотоническом растворе хлорида натрия не менее 30 мин. Метод обеспечивает гомогенность компонентов смеси, отсутствие сгустков крошки и коллагена во всем объеме смеси.
Деминерализация исходной кортикальной костной ткани является одним из способов получения материала для костной пластики. В патенте US 20170119927 A1 описана композиция для восстановления костной ткани, содержащая костные частицы и периостальную ткань (надкостницу). Костные частицы содержат деминерализованный кортикальный костный порошок, волокна или их комбинации. Периостальная ткань содержит микронизированный порошок надкостницы, кусочки надкостницы или их комбинации. Композиция для восстановления костей может быть гидратирована физиологически приемлемой жидкостью, ее можно вводить и в негидратированной форме.
Имплантат на основе деминерализованной кортикальной кости описан в патенте US 20120116515 A1. Материал имплантата содержит частицы размером 1-5 мм кортикальной кости человека, которые частично деминерализованы. Материал имплантата содержит физиологический раствор, гиалуронат натрия, гиалуроновую кислоту. Имплантаты можно использовать при лечении костей, в том числе при лечении заболеваний позвоночника, таких как как переломы тел позвонков, или дегенерация межпозвонковых дисков.
Материал для костной пластики получали методом децеллюляризации матрикса биологической ткани EP 3 338 818 B. Полученный матричный материал биологической ткани сохраняет естественное состояние сшивки органических компонентов, и, таким образом, химические сшивающие агенты не требуются. Матричный материал биологической ткани, описанный в этом изобретении, имеет микрофибриллярную форму и, таким образом, может быть использован для приготовления гомогенно диспергированного композиционного материала посредством физического смешивания матричного материала с неорганическими материалами, такими как фосфат кальция или методом биоминерализации. Недостатком полученного материала является наличие органических компонентов костной ткани донора, что может вызывать иммунную реакцию отторжения организма реципиента. Кроме того, способ получения материала содержит несколько стадий, которые достаточно сложно осуществить на практике.
Основными материалами для изготовления имплантатов в настоящее время являются металлы, в первую очередь, титан и его сплавы. Имплантаты на основе металлов обладают хорошими прочностными и упругими характеристиками (Schmutz P., Quach-Vu N.-C., Gerber I. Metallic Medical Implants: Electrochemical Characterization of Corrosion Processes // Electrochem Soc Interface. 2008. Vol. 17, № 2. P. 35-40. RU 2015112 424). В патенте RU 2715921 описан способ краниопластики при сложных дефектах костей черепа с использованием титанового имплантата в виде сферической сетки.
Существенным недостатком конструкций для костной пластики на основе титана является разница в прочностных и упругих характеристиках имплантата и нативной костной ткани. В процессе жизнедеятельности человека в месте контакта имплантата и кости происходит повышение концентрации напряжений (stress-shielding effect). Вследствие этого, в костной ткани возникают воспалительные процессы, приводящие к ее разрушению. Кроме того, за счет выделения из металлической конструкции токсических легирующих компонентов (никеля, хрома, тяжелых металлов и др.) также наблюдается воспаление в области имплантации. Воспалительные процессы приводят к необходимости дополнительного хирургического вмешательства. (Schlickewei W., Schlickewei C. The Use of Bone Substitutes in the Treatment of Bone Defects - the Clinical View and History // Macromol Symp. 2007. Vol. 253, № 1. P. 10-23. Bozkurt M. et al. Stability of a cannulated screw versus a kirschner wire for the proximal crescentic osteotomy of the first metatarsal: a biomechanical study // The Journal of Foot and Ankle Surgery. 2004. Vol. 43, № 3. P. 138-143).
Были предприняты попытки снижения жесткости имплантатов путем использования в имплантатах полимеров (Brown Stanley.A., Vandergrift J. Healing of Femoral Osteotomies with Plastic Plate Fixation // Biomater Med Devices Artif Organs. 1981. Vol. 9, № 1. P. 27-35), полимер-металлических систем (Szivek J.A. et al. A study of bone remodeling using metalpolymer laminates // J Biomed Mater Res. 1981. Vol. 15, № 6. P. 853-865.) и полимерных композиционных материалов, армированных волокнами (Gllet N. et al. The use of short carbon fibre reinforced thermoplastic plates for fracture fixation // Biomaterials. 1985. Vol. 6, № 2. P. 113-121). В работе (Nurettin D, Burak B. Feasibility of carbon-fiber-reinforced polymer fixation plates for treatment of atrophic mandibular fracture: A finite element method. J Craniomaxillofac Surg. 2018 Dec;46(12):2182-2189. doi: 10.1016/j.jcms.2018.09.030) приведены результаты исследования биомеханической стабильности пластин, изготовленных из титанового сплава и композиционного материала на основе полиэфирэфиркетона, армированного углеродным волокном. Показано, что композит характеризуется деформацией 2-10%, что способствует регенеративным процессам за счет образования костной мозоли в области перелома. Биомеханические параметры имплантата, их модуль упругости близки значению модуля упругости кортикальной кости, что позволило рекомендовать эти материалы для лечения атрофических переломов нижней челюсти.
Исключение повторных хирургических вмешательств, становится возможно, если имплантат состоит из биорезорбируемых материалов, таких как полимеры, биостекло, керамика (Gogolewski S. Bioresorbable polymers in trauma and bone surgery // Injury. 2000. Vol. 31. P. D28-D32; Daniels A.U., Chang M.K., Andriano K.P. Mechanical properties of bio-degradable polymers and composites proposed for internal fixation of bone. // J Appl Biomater. 1990. Vol. 1, № 1. P. 57-78; Vroman I., Tighzert L. Biodegradable Polymers // Materials. 2009. Vol. 2, № 2. P. 307-344; Gunatillake P. Biodegradable synthetic polymers for tissue engineering // Eur Cell Mater. 2003. Vol. 5. P. 1-16).
В патентах RU 2553368; US 8460686 предложен способ замещения дефектов костной ткани человека или млекопитающего материалом, содержащем биодеградируемые компоненты, такие, как биологический гидроксиапатит, фосфат магния, гидрофосфат кальция, гидроокись кальция, альгинат натрия, биоактивное стекло. В качестве связующего использовали казеин в виде аммиачного раствора или коллаген. Полученный композиционный материал содержал в качестве наполнителя частицы солей кальция и магния, а матрицей являлся казеин или биостекло. Такое сочетание компонентов не может обеспечить уровень прочностных и упругих характеристик, которые необходимы для реконструкции кортикальной костной ткани.
Наиболее близкими к заявленному материалу для реконструкции костной ткани является работа (Schliemann B. Arch Orthop Trauma Surg. 2017 Jan;137(1):63-71. doi: 10.1007/s00402-016-2620-8), и патенты RU 2741015 и US 9427495 B2.
В статье (Schliemann B. doi: 10.1007/s00402-016-2620-8) показано, что высокая жесткость металлических имплантатов осложняет процесс восстановления переломов проксимального отдела плечевой кости. Для снижения негативного влияния металлического имплантата на процесс регенерации костной ткани, предложены пластины из полиэфирэфиркетона, армированные углеродным волокном. Модуль упругости такого имплантата близок к модулю кортикальной кости человека. Показано, что область фиксации пластиной из полиэфирэфиркетона, содержащей углеродные волокна, имеет меньшую прочность и повышенную деформативность на границе раздела кость - имплантат по сравнению с титановой фиксирующей пластиной. Однако, описанный материал не обладает свойством биорезорбции.
Способ получения остеопластического дисперсного биокомпозита описан в патенте RU 2741015. Материал предназначен для лечения заболеваний и повреждений костной системы человека. Повышение биологической активности получаемого дисперсного остеопластического материала достигается введением в его состав волластонита и гидроксиапатита, а также равномерным распределением последнего в объеме композита.
В патенте US 9427495B2 приведено описание многофазного биодеградируемого, остеоинтегративного композитного материала для фиксации мягких тканей опорно-двигательного аппарата к кости. Материал может поддерживать рост и дифференцировку клеток разных типов тканей. Биорезорбируемый материал содержит фосфат кальция и обладает биомиметическими и/или остеоинтегративным свойствами.
Способ изготовления многофазного материала для реконструкции контакта между костной и мышечной тканями (патент US 9427495B2) включает формирование материала путем спекания сферических частиц на основе сополимера поли(лактида-гликолида); формирование композита из поли(лактида-гликолида) и биоактивного стекла. Материал обладает остеоиндуктивными свойствами, способствует пролиферации соматических клеток. Отметим, что все компоненты композиционных материалов, описанные в патенте, являются биорезорбируемыми, однако материалы на основе полилактида и его сополимеров с гликолидом характеризуются значениям прочности и модуля упругости ниже аналогичных значений кортикальной кости человека или млекопитающего. Поэтому они не могут быть использованы для реконструкции опорных костей, а также костей черепа.
Материалы для восстановления костной ткани на основе металлов, а также композиционные материалы, содержащие углеродные волокна или базальтовый волокнистый материал (RU 2749024) обладают необходимыми прочностными и упругими характеристиками, позволяющими их использовать для изготовления имплантатов костной ткани. Однако, в биологически активной среде они сохраняют свои свойства, форму и размеры в течение длительного времени, то есть не обладают свойством биорезорбции. Это существенно осложняет их использование в детской костной пластике, в частности, в краниопластике. В процессе развития детского организма происходит изменение размеров его костного аппарата, вследствие чего возникает необходимость в повторных хирургических вмешательствах для замены имплантатов.
Биорезорбируемые композиционные материалы для костной пластики, содержащие частицы гидроксиаптита, волластонита, фосфата кальция различного строения и размеров и биорезорбируемое связующее из полилактида и его сополимера с полигликолидом, а также биорезорбируемые стекла, не обладают прочностными и упругими характеристиками, позволяющими их применять в костной пластике, в частности, при реконструкции костей черепа и других кортикальных костных тканей человека или млекопитающего.
Таким образом, создание качественного биорезорбируемого имплантата для реконструкции костной ткани остается актуальной задачей.
Решением данной задачи является создание эффективного биорезорбируемого имплантата для реконструкции костной ткани.
Заявленный биорезорбируемый композиционный материал для реконструкции костной ткани отличается тем, что биорезорбируемый материал для реконструкции костной ткани содержит 50 - 60 мас. % волокон из хитозана и, или композиционных волокон из хитозана, содержащих 0,01-0,50 мас. % нанофибрилл хитина, и связующее из термопластичного биорезорбируемого полимера на основе поли(L-лактида), обладающий рентгенопрозрачностью, прочностью на изгиб 100-130 МПа, модулем упругости на изгиб 7-9 ГПа, деформацией на изгиб 2-3 %, где биорезорбируемый материал получен путем прессования при температуре Т=140℃ и давлении 2 МПа препрега, который получен каландрированием при температуре Т=185℃ ткани полотняного переплетения из волокон хитозана и/или композиционных волокон из хитозана, содержащих 0,01- 0,50 мас. % нанофибрилл хитина, и пленки из поли(L-лактида) толщиной 300 мкм, и состоит из восьми слоев ткани на основе волокон из хитозана и/или композиционных волокон из хитозана, содержащих 0,01- 0,50 мас. % нанофибрилл хитина, и восьми слоев пленки из поли(L-лактида).
Совокупность существенных признаков заявляемого биорезорбируемого композиционного материала для реконструкции костной ткани обеспечивает получение технического результата:
- композиционный материал является биорезорбируемым;
- имеет низкую по сравнению с металлами плотность композиционного материала обеспечивает рентгенопрозрачность имплантата на его основе;
- имеет физико-механические характеристики, такие как прочность на изгиб, модуль упругости, деформация на изгиб, которые сопоставимы с аналогичными характеристиками кортикальной костной ткани.
Анализ известного уровня техники не позволил обнаружить решение, полностью совпадающее по совокупности существенных признаков с заявляемым, что может указывать на новизну биорезорбируемого композиционного материала для реконструкции костной ткани.
Неочевидным из уровня техники является факт, что состав и способ получения обеспечивают сочетание прочностных и упругих характеристик и биорезорбируемость заявленного композиционного материала для реконструкции костной ткани.
Только совокупность существенных признаков заявляемого биорезорбируемого композиционного материала на основе волокон из хитозана и связующего на основе поли(L-лактида) для реконструкции костной ткани позволяет достичь указанного технического результата.
Ни в одном из аналогов не удалось при комбинации волокнистого наполнителя и полимерного связующего получить результат заявляемого изобретения. Это позволяет утверждать о соответствии заявляемого биорезорбируемого композиционного материала для реконструкции костной ткани условию патентоспособности «изобретательский уровень».
Сущность изобретения и подтверждение возможности его осуществления наиболее полно раскрываются в примере получения биорезорбируемого композиционного материала для реконструкции костной ткани.
Пример 1.
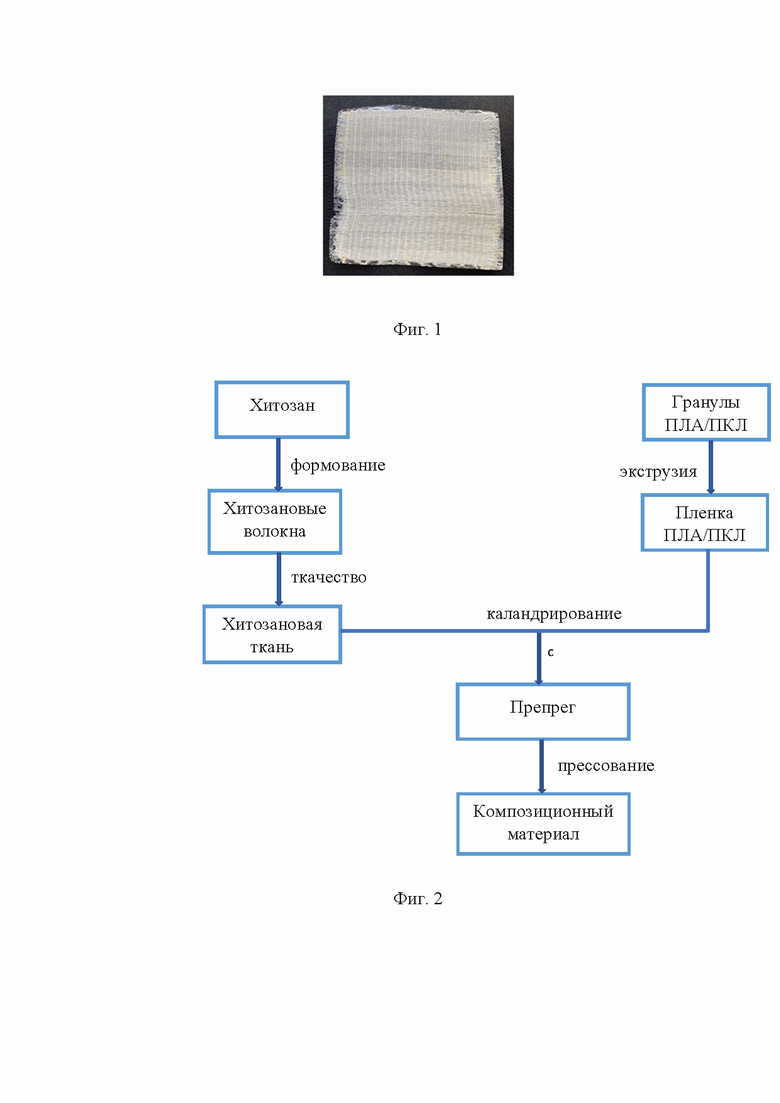
Биорезорбируемый композиционный материал (Фиг.1) получали по схеме (Фиг. 2). Метод включает прессование препрега (Фиг.3), состоящего из восьми слоев ткани (Фиг.4) на основе волокон из хитозана (Фиг.5), и восьми слоев пленки из поли(L-лактида) (Фиг.6) при Т=140°C и давлении 2 МПа. Хитозан для получения волокон мокрым способом имел молекулярную массу 203,0 кДа, степень деацетилирования 88,0 %, плотность 1,43 г/см3. Препрег получали каландрированием при температуре Т=185°C ткани полотняного переплетения из волокон хитозана и пленки из поли(L-лактида) толщиной 300 мкм (Фиг.6). Пленку из поли(L-лактида) с отношением L-лактида к D-лактиду - 96:4, молекулярной массой 180 кДа, плотностью 1.24 г/см3, получали методом экструзии при температуре Т=190°C. Толщина пленки составляла 300-350 мкм. Схема укладки препрега для прессования см. (Фиг.7).
Содержание волокнистого наполнителя в композиционном материале толщиной 1,5 мм, составляло 53,1 мас.%, Прочность композиционного материала при изгибе составляла σ=130±3,29 МПа, модуль упругости при изгибе Е= 9,1±0,08 ГПа, деформация до разрыва ε=2,5±0,9 %.
Пример 2.
Биорезорбируемый композиционный материал получали методом, описанным в примере 1. Ткань полотняного переплетения состояла из композиционных волокон на основе хитозана, содержащих в качестве наполнителя 0,3 мас. % нанофибрилл хитина. Содержание волокнистого наполнителя в композиционном материале составляло 58,5 мас. %, толщина материала 1,5 мм. Прочность композиционного материала при изгибе составляла σ=125±1,1 МПа, модуль упругости при изгибе Е=8,5±0,5 ГПа, деформация до разрыва ε=2,5±0,3 %.
Таким образом, примеры получения биорезорбируемого композиционного материала, содержащего в качестве армирующих элементов волокна хитозана, и в качестве связующего - термопластичные биорезорбируемые полимеры - поли(L-лактида), позволяют сделать вывод о технологичности процесса получения материала, его низкой экологической нагрузке. Результаты исследования прочностных и упругих характеристик заявленного композита показали близость указанных параметров к аналогичным параметрам нативной кортикальной костной ткани человека или животного. Миметические характеристики материала являются основой его высокой биосовместимости, отсутствия негативных последствий при имплантации в живой организм.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОРЕЗОРБИРУЕМЫЙ ИМПЛАНТАТ ДЛЯ РЕГЕНЕРАЦИИ ПЕРИФЕРИЧЕСКИХ НЕРВОВ | 2023 |
|
RU2805813C1 |
| БИОРЕЗОРБИРУЕМЫЙ ИМПЛАНТАТ КРОВЕНОСНЫХ СОСУДОВ НА ОСНОВЕ НАНОВОЛОКОН | 2023 |
|
RU2808880C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО БИОДЕГРАДИРУЕМОГО ПОРИСТОГО КОМПОЗИЦИОННОГО МАТЕРИАЛА | 2014 |
|
RU2568919C1 |
| Композиционное полимерное раневое покрытие на основе нановолокон | 2017 |
|
RU2647609C1 |
| БИОСОВМЕСТИМЫЙ КОМПОЗИТ И ЕГО ПРИМЕНЕНИЕ | 2010 |
|
RU2527340C2 |
| ПОЛИМЕРНАЯ КОМПОЗИЦИЯ БИОМЕДИЦИНСКОГО НАЗНАЧЕНИЯ | 2001 |
|
RU2197509C1 |
| ПОРИСТЫЕ КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ НА ОСНОВЕ ХИТОЗАНА ДЛЯ ЗАПОЛНЕНИЯ КОСТНЫХ ДЕФЕКТОВ | 2007 |
|
RU2376019C2 |
| Способ получения биорезорбируемого материала на основе магния и гидроксиапатита с защитным многокомпонентным покрытием | 2021 |
|
RU2763138C1 |
| ИМПЛАНТАТ ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2692578C1 |
| Способ получения композиции термопластичных биосовместимых и биодеградируемых привитых сополимеров на основе хитозана и полилактида | 2023 |
|
RU2830005C1 |


Изобретение относится к области полимерных композиционных материалов, которые могут быть использованы в медицине для реконструкции костной ткани, в частности в краниопластике. Предлагаемый биорезорбируемый композиционный материал для реконструкции костной ткани содержит 50-60 мас. % волокон из хитозана и/или композиционных волокон из хитозана, содержащих 0,01-0,50 мас. % нанофибрилл хитина, и связующее из термопластичного биорезорбируемого полимера на основе поли(L-лактида), обладает рентгенопрозрачностью, прочностью на изгиб 100-130 МПа, модулем упругости на изгиб 7-9 ГПа, деформацией на изгиб 2-3 %, причем биорезорбируемый материал получен путем прессования при Т=140°С и давлении 2 МПа препрега, который получен каландрированием при температуре Т=185°С ткани полотняного переплетения из волокон хитозана и/или композиционных волокон из хитозана, содержащих 0,01-0,50 мас. % нанофибрилл хитина, и пленки из поли(L-лактида) толщиной 300 мкм, и состоит из восьми слоев ткани на основе волокон из хитозана и/или композиционных волокон из хитозана, содержащих 0,01- 0,50 мас. % нанофибрилл хитина, и восьми слоев пленки из поли(L-лактида). Указанный материал является биорезорбируемым, имеет низкую по сравнению с металлами плотность композиционного материала, что обеспечивает рентгенопрозрачность имплантата на его основе; имеет физико-механические характеристики, такие как прочность на изгиб, модуль упругости, деформация на изгиб, которые сопоставимы с аналогичными характеристиками кортикальной костной ткани. 7 ил., 2 пр.
Биорезорбируемый материал для реконструкции костной ткани, отличающийся тем, что композиционный материал содержит 50-60 мас. % волокон из хитозана и/или композиционных волокон из хитозана, содержащих 0,01-0,50 мас. % нанофибрилл хитина, и связующее из термопластичного биорезорбируемого полимера на основе поли(L-лактида), обладающий рентгенопрозрачностью, прочностью на изгиб 100-130 МПа, модулем упругости на изгиб 7-9 ГПа, деформацией на изгиб 2-3 %, где биорезорбируемый материал получен путем прессования при температуре Т=140°С и давлении 2 МПа препрега, который получен каландрированием при температуре Т=185°С ткани полотняного переплетения из волокон хитозана и/или композиционных волокон из хитозана, содержащих 0,01- 0,50 мас. % нанофибрилл хитина, и пленки из поли(L-лактида) толщиной 300 мкм, и состоит из восьми слоев ткани на основе волокон из хитозана и/или композиционных волокон из хитозана, содержащих 0,01-0,50 мас. % нанофибрилл хитина, и восьми слоев пленки из поли(L-лактида).
| Токарный резец | 1924 |
|
SU2016A1 |
| US 6511511 B1, 28.01.2003 | |||
| RU 2019138446 A, 28.05.2021 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| CN 102580162 A, 18.07.2012 | |||
| ДОБРОВОЛЬСКАЯ И.П | |||
| и др | |||
| Структура и свойства одномерных матриц на основе хитозана и нанофибрилл хитина для клеточных технологий | |||
| Научно-технические ведомости СПбГПУ | |||
| Физико-математические науки, 2014, | |||
Авторы
Даты
2025-02-11—Публикация
2024-04-25—Подача