Область техники настоящего изобретения
Настоящее изобретение относится к замещенным тиофенкарбоксамидным производным, их применению для борьбы с фитопатогенными микроорганизмами и содержащим их композициям.
Предшествующий уровень техники настоящего изобретения
Хотя к настоящему времени было разработано множество микробиоцидных средств, сохраняется потребность в разработке новых микробиоцидных соединений для удовлетворения постоянно растущих экологических и экономических требований, предъявляемых к современным средствам и композициям для защиты растений. Это включает, например, улучшение спектра действия, профиля безопасности, селективности, нормы внесения, образования остатков и благоприятной способности препарата. Также может быть желательно предоставить новые соединения для предотвращения возникновения резистентности.
Настоящее изобретение обеспечивает новые соединения, которые имеют преимущества перед известными соединениями и композициями по меньшей мере в некоторых из этих аспектов.
В 450355 и JP 2009078991 описаны производные тиофенкарбоксамида, которые можно использовать для защиты растений от атак микроорганизмов, повреждающих растения.
В WO 2004/024692 раскрыты производные гетероциклических карбоновых кислот и их применение в качестве фунгицидов и бактерицидов для защиты растений или материалов, таких как древесина.
Краткое раскрытие настоящего изобретения
Настоящее изобретение относится к соединениям формулы (I) или формулы (II), раскрытым в настоящем документе, а также к их изомерам, полиморфам, солям, N-оксидам и сольватам.
Настоящее изобретение относится к композиции, содержащим по меньшей мере одно соединение формулы (I) или (II) или такое, как раскрыто в настоящем документе, и по меньшей мере один сельскохозяйственно приемлемый носитель.
Настоящее изобретение относится к способам получения соединений формулы (I) или (II), как раскрыто в настоящем документе, и их промежуточных соединений.
Настоящее изобретение относится к способу борьбы с фитопатогенными микроорганизмами, который включает стадию нанесения по меньшей мере одного соединения формулы (I) или (II), как определено в настоящем документе, или композиции, как определено в настоящем документе, на растения, части растений, семена, плоды или на почву в котором растут растения.
Определения
Термин «алкил», используемый в настоящем документе в контексте алкила или алкилсульфонила, алкилсульфинила, алкилтио, алкиламино, например, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкил, означающий, например, метил, этил, н-пропил, изо-пропил, н-бутил, изобутил, трет-бутил, втор-бутил, пентил, изо-пентил, гексил, гептил, октил, нонил и децил и их изомеры.
Термин «алкенил», используемый в настоящем документе, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкенил, например, винил, пропен-1-ил, пропен-2-ил, бут-1-ен-1-ил, бут-1-ен-2-ил, бут-2-ен-1-ил, бут-2-ен-2-ил, бут-1-ен-3-ил, 2-метил-проп-2-ен-1-ил, или 2-метил-проп-1-ен-1-ил.
Термин «алкинил», используемый в настоящем документе, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкинил, например, этинил, проп-1-ин-1-ил, бут-1-ин-1-ил, бут-2-ин-1-ил или бут-3-ин-1-ил.
Термин «гало» или «галогено» (например, галогеналкил, «C1-С6-галогеналкил» или «C1-С8-галогеналкил») обозначает необязательное присутствие одного или нескольких галогеновых заместителей, которые могут быть одинаковыми или разными.
Термин «галогеналкил», используемый в настоящем документе, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкил, как определено выше, в котором один или несколько водородных заместителей заменены галогеном одинаковым или различным. Особенно предпочтительно указанный галогеналкил представляет собой, например, хлорметил, фторпропил, фторметил, дифторметил, трихлорметил, 2,2,2-трифторэтил, пентафторэтил, бромбутил, трифторметил, йодэтил и их изомеры.
Термин «галогеналкенил», используемый в настоящем документе, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкенил, как определено выше, в котором один или несколько водородных заместителей заменены одинаково или различно на галоген.
Термин «галогеналкинил», используемый в настоящем документе, следует понимать как предпочтительно означающий разветвленный и неразветвленный алкинил, как определено выше, в котором один или несколько водородных заместителей заменены одинаково или различно на галоген.
Используемый в настоящем документе термин «алкокси» относится к группе формулы (алкил)-О-, в которой термин «алкил» имеет значение, определенное в настоящем документе. Примеры C1-С8-алкокси включают, но не ограничиваются ими, метокси, этокси, н-пропокси, 1-метилэтокси, н-бутокси, 1-метилпропокси, 2-метилпропокси, 1,1-диметилэтокси, н-пентокси, 1-метилбутокси, 2-метилбутокси, 3-метилбутокси, 2,2-диметилпропокси, 1-этилпропокси, 1,1-диметилпропокси, 1,2-диметилпропокси, н-гексилокси, 1-метилпентокси, 2-метилпентокси, 3-метилпентокси, 4-метилпентокси, 1,1-диметилбутокси, 1,2-диметилбутокси, 1,3-диметилбутокси, 2,2-диметилбутокси, 2,3-диметилбутокси, 3,3-диметилбутокси, 1-этилбутокси, 2-этилбутокси, 1,1,2-триметилпропокси, 1,2,2-триметилпропокси, 1-этил-1-метилпропокси и 1-этил-2-метилпропокси.
Используемый в настоящем документе термин «галогеналкокси» относится к алкоксигруппе, как определено выше, в которой один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными. Примеры C1-С8-галогеналкокси включают, но не ограничиваются ими, хлорметокси, бромметокси, дихлорметокси, трихлорметокси, фторметокси, дифторметокси, трифторметокси, хлорфторметокси, дихлорфторметокси, хлордифторметокси, 1-хлорэтокси, 1-бромэтокси, 1-фторэтокси, 2-фторэтокси, 2,2-дифторэтокси, 2,2,2-трифторэтокси, 2-хлор-2-фторэтокси, 2-хлор-2,2-дифторэтокси, 2,2-дихлор-2-фторэтокси, 2,2,2-трихлорэтокси, пентафторэтокси и 1,1,1-трифторпроп-2-окси.
Используемый в настоящем документе термин «алкилсульфанил» относится к насыщенной, линейной или разветвленной группе формулы (алкил)-S-, в которой термин «алкил» имеет значение, определенное в данном документе. Примеры C1-С8-алкилсульфанила включают, но не ограничиваются ими, метилсульфанил, этилсульфанил, пропилсульфанил, изопропилсульфанил, бутилсульфанил, втор-бутилсульфанил, изобутилсульфанил, трет-бутилсульфанил, пентилсульфанил, изопентилсульфанил, гексилсульфанил.
Используемый в настоящем документе термин «галогеноалкилсульфанил» относится к алкилсульфанилу, как определено выше, в котором один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными.
Используемый в настоящем документе термин «алкилсульфинил» относится к насыщенной, линейной или разветвленной группе формулы (алкил)-S(=O)-, в которой термин «алкил» имеет значение, определенное в данном документе. Примеры C1-С8-алкилсульфинила включают, но не ограничиваются ими, насыщенные алкилсульфинильные радикалы с прямой или разветвленной цепью, имеющие от 1 до 8, предпочтительно от 1 до 6 и более предпочтительно от 1 до 4 атомов углерода, например (но не ограничиваясь ими) метилсульфинил, этилсульфинил, пропилсульфинил, 1-метилэтилсульфинил, бутилсульфинил, 1-метилпропилсульфинил, 2-метилпропилсульфинил, 1,1-диметилэтилсульфинил, пентилсульфинил, 1-метилбутилсульфинил, 2-метилбутилсульфинил, 3-метилбутилсульфинил, 2,2-диметилпропилсульфинил, 1-этилпропилсульфинил, 1,1-диметилпропилсульфинил, 1,2-диметилпропилсульфинил, гексилсульфинил, 1-метилпентилсульфинил, 2-метилпентилсульфинил, 3-метилпентилсульфинил, 4-метилпентилсульфинил, 1,1-диметилбутилсульфинил, 1,2-диметилбутилсульфинил, 1,3-диметилбутилсульфинил, 2,2-диметилбутилсульфинил, 2,3-диметилбутилсульфинил, 3,3-диметилбутилсульфинил, 1-этилбутилсульфинил, 2-этилбутилсульфинил, 1,1,2-триметилпропилсульфинил, 1,2,2-триметилпропилсульфинил, 1-этил-1-метилпропилсульфинил и 1-этил-2-метилпропилсульфинил.
Используемый в настоящем документе термин «галогеноалкилсульфинил» относится к алкилсульфинилу, как определено выше, в котором один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными.
Используемый в настоящем документе термин «алкилсульфонил» относится к насыщенной, линейной или разветвленной группе формулы (алкил)-S(=O)2-, в которой термин «алкил» имеет значение, определенное в настоящем документе. Примеры C1-С8-алкилсульфонила включают, но не ограничиваются ими, метилсульфонил, этилсульфонил, пропилсульфонил, 1-метилэтилсульфонил, бутилсульфонил, 1-метилпропилсульфонил, 2-метилпропилсульфонил, 1,1-диметилэтилсульфонил, пентилсульфонил, 1-метилбутилсульфонил, 2-метилбутилсульфонил, 3-метилбутилсульфонил, 2,2-диметилпропилсульфонил, 1-этилпропилсульфонил, 1,1-диметилпропилсульфонил, 1,2-диметилпропилсульфонил, гексилсульфонил, 1-метилпентилсульфонил, 2-метилпентилсульфонил, 3-метилпентилсульфонил, 4-метилпентилсульфонил, 1,1-диметилбутилсульфонил, 1,2-диметилбутилсульфонил, 1,3-диметилбутилсульфонил, 2,2-диметилбутилсульфонил, 2,3-диметилбутилсульфонил, 3,3-диметилбутилсульфонил, 1-этилбутилсульфонил, 2-этилбутилсульфонил, 1,1,2-триметилпропилсульфонил, 1,2,2-триметилпропилсуль фонил, 1-этил-1-метилпропилсульфонил и 1-этил-2-метилпропилсульфонил.
Термин «галогеноалкилсульфонил», используемый в настоящем документе, относится к C1-С8-алкилсульфонилу, как определено выше, в котором один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными.
Термин «галогеноалкилкарбонил», используемый в настоящем документе, относится к алкилкарбонилу, как определено выше, в котором один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными.
Используемый в настоящем документе термин «алкоксикарбонил» относится к насыщенной, линейной или разветвленной группе формулы (алкокси)-С(=O)-, в которой термин «алкокси» имеет значение, определенное в данном документе.
Используемый в настоящем документе термин «галогеналкоксикарбонил» относится к алкоксикарбонилу, определенному выше, в котором один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или разными.
Термин «циклоалкил», используемый в настоящем документе, относится к неароматическому моноциклическому углеродсодержащему кольцу, имеющему от 3 до 8 атомов углерода. Примеры насыщенного циклоалкила включают, но не ограничиваются ими, циклопропильную, циклобутильную, циклопентильную, циклогексильную, циклогептильную, циклооктильную, циклононильную и циклодецильную группы.
Используемый в настоящем документе термин «гетероциклил» относится к четырех-, пяти- или шестичленным, насыщенным или частично ненасыщенным гетероциклам, содержащим от одного до четырех гетероатомов, независимо выбранных из группы кислорода, азота и серы. Если кольцо содержит более одного атома кислорода, они не являются непосредственно соседними.
Используемый в настоящем документе термин «арил» относится к ароматической углеводородной кольцевой системе, содержащей от 6 до 15 атомов углерода или от 6 до 12 атомов углерода, предпочтительно от 6 до 10 атомов углерода. Кольцевая система может быть моноциклической или конденсированной полициклической (например, бициклической или трициклической) ароматической кольцевой системой. Примеры арила включают, но не ограничиваются ими, фенил, азуленил, нафтил и флуоренил. Также следует понимать, что, когда указанная арильная группа замещена одним или несколькими заместителями, указанный(е) заместитель(и) может (могут) находиться в любом положении указанного(ых) арильного(ых) кольца(колец). В частности, в случае, когда арил представляет собой фенильную группу, указанный заместитель(и) может (могут) занимать одно или оба орто-положения, одно или оба мета-положения, или пара-положение, или любую комбинацию этих положений. Это определение также применимо к арилу как части составного заместителя (например, арилокси).
Используемый в настоящем документе термин «аралкил» относится к C1-С6-алкилу, замещенному арилом, как определено в настоящем документе. Пример аралкила включает бензильную группу (-СН2-С6Н5).
Термин «ароматический 5-14-членный гетероцикл» или «гетероарил», используемый в настоящем документе, относится к ароматической кольцевой системе, содержащей от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из кислорода, азота и серы. Ароматические гетероциклы включают ароматические 5- или 6-членные моноциклические гетероциклы и 6-14-членные полициклические (например, бициклические или трициклические) ароматические гетероциклы. 5-14-членный ароматический гетероцикл может быть связан с исходной молекулярной частью через любой атом углерода или атом азота, содержащийся в гетероцикле.
Используемый в настоящем документе термин «C1-С6», например, в контексте определения «C1-С6-алкил» или «C1-С6-алкокси», следует понимать как означающий группа, имеющая конечное число атомов углерода от 1 до 6, т.е. 1, 2, 3, 4, 5 или 6 атомов углерода.
Используемый в настоящем документе термин «C1-С8», например, в контексте определения «C1-С8-алкил» или «С1-С8-алкокси», следует понимать как означающий группа, имеющая конечное число атомов углерода от 1 до 8, т.е. 1, 2, 3, 4, 5, 6, 7 или 8 атомов углерода.
Используемый в настоящем документе термин «оксо» относится к атому кислорода, который связан с атомом углерода или атомом серы двойной связью.
Термин «уходящая группа», используемый в настоящем документе, следует понимать как означающий группу, которая замещается из соединения в реакции замещения или отщепления, например, атом галогена, трифторметансульфонатную («трифлатную») группу, алкокси, метансульфонат, п-толуолсульфонат и т.д.
Подробное раскрытие настоящего изобретения
Настоящее изобретение относится к соединению формулы (I):
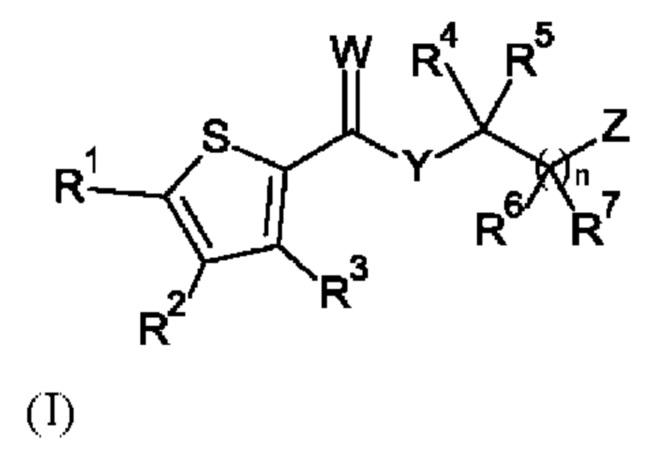
где
R1 и R2 независимо выбраны из группы, состоящей из галогена, циано, C1-С6-алкила или C1-С6-галоалкила, где по меньшей мере один из R1 или R2 представляет собой галоген;
R3 выбран из группы, состоящей из водорода, галогена, циано, C1-С6-алкила или C1-С6-галоалкила;
R4 и R5 независимо выбраны из группы, состоящей из водорода, галогена, циано, гидроксила, С1-С6-алкила, C1-С6-гидроксиалкила, C1-С6-алкокси, C1-С6-галоалкила, -О-С(=O)-С1-С6-алкила, C3-С6-карбоцикла, 4-, 5- или 6-ти членного не ароматического гетероциклила, -C(=O)-NH2, -С(=O)-NH(C1-С6-алкила), -С(=O)-N(С1-С6-алкила)2, -С(=O)-ОН, -С(=O)-O-C1-С6-алкила, арила, 5-9-ти членного гетероарила, -C1-С6-алкил-C1-С6-алкокси, -C1-С6-алкил-C1-С6-галоалкила, -C1-С6-алкил-C3-С6-карбоцикла, -C1-С6-алкил-4-, 5- или 6-ти членного неароматического гетероциклила, -C1-С6-алкил-арила, -C1-С6-алкил-гидроксиарила, -C1-С6-алкил-5-9-ти членного гетероарила, -C1-С6-алкил-S-C1-С6-алкила, -C1-С6-алкил-S-С(=O)-C1-С6-алкила, -C1-С6-алкил-O-(С=O)-C1-С6-алкила, -C1-С6-алкил-C(=O)-NH2, -C1-С6-алкил-С(=O)-NH(C1-С6-алкила), -C1-С6-алкил-С(=O)-N(C1-С6-алкила)2, -C1-С6-алкил-С(=O)-ОН, -C1-С6-алкил-С(=O)-O-C1-С6-алкила, -C1-С6-алкил-NH-C(=NH)-NH2, -S-C1-С6-алкила, -S-С(=O)-C1-С6-алкила, -S-С(=O)-O-C1-С6-алкила, -S-C(=S)-O-C1-С6-алкила, -S-C(=O)-S-C1-С6-алкила, -S-C(=O)-NH2, -S-C(=O)-NH(C1-С6-алкила), -S-C(=O)-NH(C1-С6-алкила)2, -S-C(=S)-NH2, -S-C(=S)-NH(C1-С6-алкила), -S-C(=S)-NH(C1-С6-алкила)2, -C1-С6-алкил-S-С(=O)-O-C1-С6-алкила, -C1-С6-алкил-S-С(=O)-S-C1-С6-алкила, -C1-С6-алкил-S-С(=O)-NH2, -C1-С6-алкил-S-С(=O)-NH(C1-С6-алкила), -C1-С6-алкил-S-С(=O)-NH(C1-С6-алкила)2, -C1-С6-алкил-S-C(=S)-NH2, -C1-С6-алкил-S-C(=S)-NH(C1-С6-алкила), -C1-С6-алкил-S-С(=S)-NH(C1-С6-алкила)2, где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, C1-С6-алкил или С3-C6-карбоцикл, или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл, где указанный С3-C6-карбоцикл и 3-6-ти членный гетероцикл могут быть замещены одним или несколькими Rx заместителями, где Rw независимо выбран из группы, состоящей из нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С3-С7циклоалкила, С3-С7 галогеноциклоалкила, имеющего от 1 до 5 атомов галогена,С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонила, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоил, где Rx независимо выбран из группы, состоящей из галогена, нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С1-С8-алкила, С3-С7 циклоалкила, С1-С8-галогеноалкила, имеющего от 1 до 5 атомов галогена, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена, С2-С8-алкенила, С2-С8-алкинила, С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонила, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоила;
R6 м R7 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С3-С6-карбоцикла, или R6 и R7 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл;
n представляет собой 0 или 1;
W представляет собой кислород или серу;
Y представляет собой NR8, где R8 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-галоалкила, С1-С6-цианоалкила, гидрокси, С1-С6-алкокси или С3-С6-карбоцикл;
Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, где Ra выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-галоалкила, С1-С6-цианоалкила, С2-С6-алкенила, С2-С6-алкинила, С3-С8-циклоалкила, арила, аралкила, 4-, 5- или 6-ти членного неароматического гетероциклила, -С1-С6-алкил-Si(С1-С6-алкила)3, -С1-С6-алкил-С3-С8-циклоалкила, 5-9-ти членного гетероарила и -С1-С6-алкил-5-9-ти членного гетероарила, или Ra может образовывать вместе с R4 и с атомами, к которым они присоединены, 4-7-ти членный гетероцикл, где Rb и Rc независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, гидроксила, С1-С6-алкокси, циано, С1-С6-цианоалкила, или Rb может образовывать вместе с R4 и с атомами, к которым они присоединены, 4-7-ти членный гетероцикл, где Rd и Re независимо выбраны из группы, состоящей из водорода, циано, гидроксила, С1-С6-алкила, С1-С6-гидроксиалкила, С1-С6-алкокси, -O-С(=O)-С1-С6-алкила, С3-С6-карбоцикла, -C(=O)-NH2, -С(=O)-NH(С1-С6-алкила),- С(=O)-N(С1-С6-алкила)2, -С(=O)-ОН, -C(=O)-O-С1-С6-алкила, арила, 5-9-ти членного гетероарила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-5-9-ти членного гетероарила, -С1-С6-алкил-S-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-С1-С6-алкила, -С1-С6-алкил-O-(С=O)-С1-С6-алкила, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил- С(=O)-N(С1-С6-алкила)2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-NH-С(=NH)-NH2, где по меньшей мере один из Rd и Re представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл, или Rd и Re образуют вместе с атомом водорода, к которому они присоединены, карбонил, С1-С6-карбоцикл или 3-6-ти членный гетероцикл;
при условии, что соединения формулы (I) со следующими комбинациями R1, R2 и R3
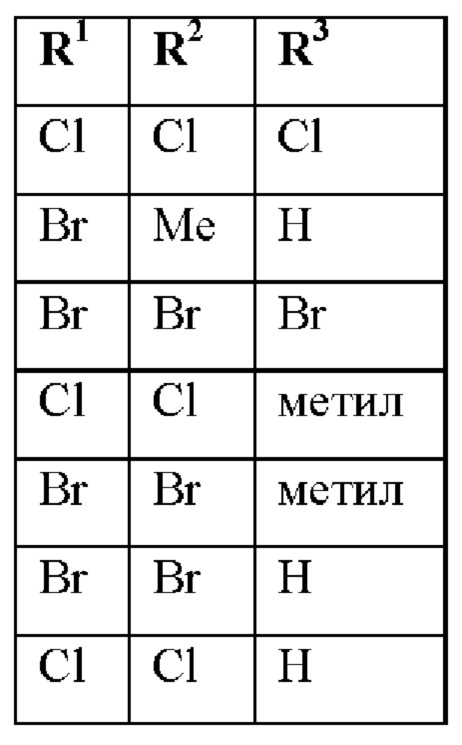
исключены;
при условии, что соединения формулы (I) со следующими комбинациями R1, R2 и R3
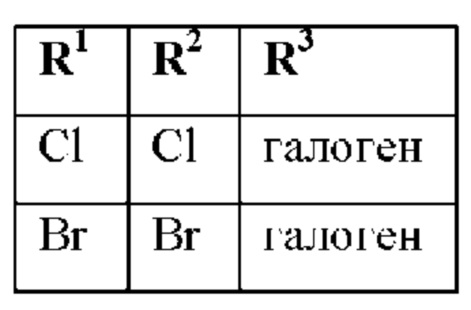
исключены, если R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NH, и Z представляет собой -С(=O)-ORa;
при условии, что соединения формулы (I) со следующими комбинациями R1, R2 и R3
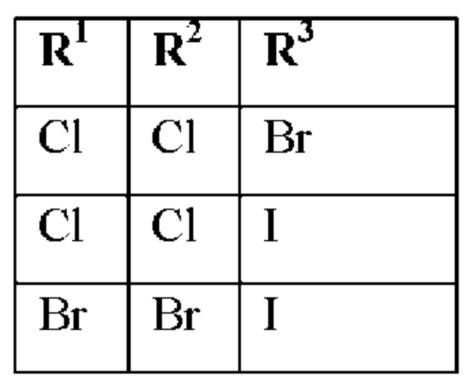
исключены, если R4 выбран из группы, состоящей из водорода, С1-С6-алкила, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила, и R5 представляет собой водород, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NH и Z представляет собой -С(=O)-ORa;
при условии, что N-[(4-бром-5-метил-2-тиенил)карбонил]-N-пропилглицин [2193740-02-0] и 4-бром-N-(1-циано-2,2-диметилциклопропил)-5-метилтиофен-2-карбоксамид [2192630-99-0] исключены из соединений формулы (I).
Предпочтительно, если R1 представляет собой С1-С6-галоалкил, или R2 представляет собой С1-С6-галоалкил, и R4 выбран из группы, состоящей из водорода, С1-С6-алкила, и R5 выбран из группы, состоящей из водорода, С1-С6-алкила, и n представляет собой 0, и W представляет собой кислород, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Также предпочтительно соединения формулы (I) исключены, где R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Предпочтительно, что R4 и R5 независимо выбраны из группы, состоящей из водорода, галогена, циано, гидроксила, С1-С6-алкила, С1-С6-гидроксиалкила, С1-С6-алкокси, С1-С6-галоалкила, -O-С(=O)-С1-С6-алкила, С3-С6-карбоцикла, 4-, 5- или 6-ти членного неароматического гетероциклила, -C(=O)-NH2, -С(=O)-NH(С1-С6-алкила), -С(=O)-N(С1-С6-алкила)2, -С(=O)-ОН, -С(=O)-O-С1-С6-алкила, арила, 5-9-ти членного гетероарила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-4-, 5- или 6-ти членного неароматического гетероциклила, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-5-9-ти членного гетероарила, -С1-С6-алкил-S-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-С1-С6-алкила, -С1-С6-алкил-O-(С=O)-С1-С6-алкила, -С1-С6-алкил-C(=O)-NH2, -С1-С6-алкил-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-С(=O)-N(С1-С6-алкила)2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-NH-C(=NH)-NH2, -S-С1-С6-алкила, -S-C(=O)-С1-С6-алкила, -S-С(=O)-O-С1-С6-алкила, -S-С(=S)-O-С1-С6-алкила, -S-С(=O)-S-С1-С6-алкила, -S-C(=O)-NH2, -S-C(=O)-NH(С1-С6-алкила), -S-C(=O)-NH(С1-С6-алкила)2, -S-C(=S)-NH2, -S-C(=S)-NH(С1-С6-алкила), -S-C(=S)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-S-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-NH2, -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=S)-NH2, -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила)2, где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл, или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С4-С6-карбоцикл или 3-6-ти членный гетероцикл, где указанный С4-С6-карбоцикл и 3-6-ти членный гетероцикл могут быть замещены одним или несколькими Rx заместителями, где Rw независимо выбран из группы, состоящей из нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С3-С7-циклоалкила, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена, С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонил, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоила, где Rx независимо выбран из группы, состоящей из галогена, нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С1-С8-алкила, С3-С7-циклоалкила, С1-С8-галогеноалкила, имеющего от 1 до 5 атомов галогена, С3-С7 галогеноциклоалкила, имеющего от 1 до 5 атомов галогена, С2-С8-алкенила, С2-С8-алкинила, С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонила, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоила.
Также предпочтительно, что R4 и R5 независимо выбраны из группы, состоящей из водорода, галогена, циано, гидроксила, С1-С6-алкила, С1-С6-гидроксиалкила, С1-С6-алкокси, С1-С6-галоалкила, -O-С(=O)-С1-С6-алкила, С3-С6-карбоцикла, 4-, 5- или 6-ти членного неароматического гетероциклила, -C(=O)-NH2, -С(=O)-NH(С1-С6-алкила), -С(=O)-N(С1-С6-алкила)2, -С(=O)-ОН, -С(=O)-O-С1-С6-алкила, арила, 5-9-ти членного гетероарила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-4-, 5- или 6-ти членного неароматического гетероциклила, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-5-9-ти членного гетероарила, -С1-С6-алкил-S-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-С1-С6-алкила, -С1-С6-алкил-O-(С=O)-С1-С6-алкила, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(-O)-NH(С1-С6-алкила), -С1-С6-алкил-С(=O)-N(С1-С6-алкила)2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-NH-C(=NH)-NH2, -S-С1-С6-алкила, -S-C(=O)-С1-С6-алкила, -S-С(=O)-O-С1-С6-алкила, -S-С(=S)-O-С1-С6-алкила, -S-C(=O)-S-С1-С6-алкила, -S-C(=O)-NH2, -S-С(=O)-NH(С1-С6-алкила), -S-С(=O)-NH(С1-С6-алкила)2, -S-C(=S)-NH2, -S-С(=S)-NH(С1-С6-алкила), -S-C(=S)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-S-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-NH2, -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=S)-NH2, -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила)2, где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл, или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, 3-6-ти членный гетероцикл, где 3-6-ти членный гетероцикл могут быть замещены одним или несколькими Rx заместителями, где Rw независимо выбран из группы, состоящей из нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С3-С7-циклоалкила, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена,С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонила, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоила, где Rx независимо выбран из группы, состоящей из галогена, нитро, гидроксила, циано, карбоксила, амино, сульфанила, пентафтор-l6-сульфанила, формила, карбамоила, карбамата, С1-С8-алкила, С3-С7-циклоалкила, С1-С8-галогеноалкила, имеющего от 1 до 5 атомов галогена, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена, С2-С8-алкенила, С2-С8-алкинила, С1-С8-алкиламино, ди-С1-С8-алкиламино, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонила, С1-С8-галогеноалкилкарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбамоила, ди-С1-С8-алкилкарбамоила, С1-С8-алкоксикарбонила, С1-С8-галогеноалкоксикарбонила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбонилокси, С1-С8-галогеноалкилкарбонилокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилкарбониламино, С1-С8-галогеноалкилкарбониламино, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфинила, С1-С8-галогеноалкилсульфинила, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфонила, С1-С8-галогеноалкилсульфонила, имеющего от 1 до 5 атомов галогена; С1-С8-алкил-сульфониламино, С1-С8-галогеноалкилсульфониламино, имеющего от 1 до 5 атомов галогена; сульфамоила; С1-С8-алкилсульфамоила и ди-С1-С8-алкилсульфамоила.
Также предпочтительно, что соединения исключены, где R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил.
Также предпочтительно, если R4 и R5 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, арила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С3-С6-карбоцикла, С1-С6-алкил-O-(С=O)-С1-С6-алкила, -С1-С6-алкил-С(=O)-ОН; -С1-С6-алкил-арила, -С1-С6-алкил-S-С1-С6-алкила, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NR8, где R8 выбран из группы, состоящей из водорода, С1-С6-алкила, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Согласно другому варианту осуществления предпочтительно, если R1 и R2 независимо выбраны из группы, состоящей из F, Cl, Br, I, Циано, СН3 и предпочтительно выбраны независимо друг от друга из группы, состоящей из F, Cl, Br, I.
Согласно другому варианту осуществления предпочтительно, если R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3 предпочтительно выбран из группы, состоящей из CN, Br, Cl, F.
Согласно другому варианту осуществления предпочтительно, если R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3.
Согласно другому предпочтительному варианту осуществления R3 выбран из группы, состоящей из водород, F, Cl, Br, I, циано, СН3, CHF2, CF3, и предпочтительно выбран из группы, состоящей из водорода, F, Cl, Br, I, циано, СН3.
Согласно другому предпочтительному варианту осуществления R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3.
Также предпочтительным является соединение формулы (I) со следующими комбинациями R1, R2 и R3
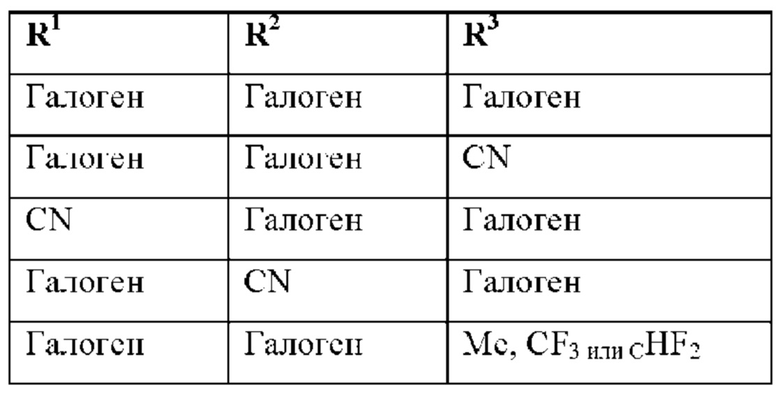
Также предпочтительно, если R3 не представляет собой водород.
Также предпочтительными являются соединения формулы (I), где R3 не представляет собой водород, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Также предпочтительно, если по меньшей мере один из R1, R2 и R3 представляет собой циано.
Согласно другому предпочтительному варианту осуществления R4 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, С(=O)-ОН, -С(=O)-O-С1-С6-алкила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, R5 выбран из группы, состоящей из водорода, С1-С6-алкила или С3-С6-карбоцикла; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл.
Также предпочтительно, если R6 и R7 независимо выбраны из группы, состоящей из водорода, С1-С3-алкила, С3-С6-карбоцикла.
Согласно другому предпочтительному варианту осуществления n представляет собой 0.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Также предпочтительно, если W представляет собой кислород.
Также предпочтительными являются соединения формулы (I) где W представляет собой кислород, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Кроме того, предпочтительно, если Y выбран из группы, состоящей из NH, N-ОСН3, N-OH, и наиболее предпочтительно NH.
Также предпочтительными являются соединения формулы (I) где Y представляет собой NH, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, и предпочтительно -C(=O)-ORa.
Согласно другому варианту осуществления Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc.
Согласно другому предпочтительному варианту осуществления R1 и R2 независимо выбраны из группы, состоящей из F, Cl, Br, I, циано, СН3 и предпочтительно выбраны независимо друг от друга из группы, состоящей из F, Cl, Br, I;
R3 выбран из группы, состоящей из водорода, F, Cl, Br, I, Циано, СН3, CHF2, CF3 и предпочтительно выбран из группы, состоящей из Водорода, F, Cl, Br, I, Циано, СН3;
R4 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, С(=O)-ОН, -С(=O)-O-С1-С6-алкила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, R5 выбран из группы, состоящей из представляет собой водорода, С1-С6-алкила или С3-С6-карбоцикла; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл;
R6 и R7 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С3-С6-карбоцикла, или R6 и R7 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл;
n представляет собой 0;
W представляет собой кислород;
Y выбран из группы, состоящей из NH, N-OCH3, N-OH, и предпочтительно NH;
Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, и предпочтительно -C(=O)-ORa. Согласно другому предпочтительному варианту осуществления
R1 и R2 независимо выбраны из группы, состоящей из F, Cl, Br, I;
R3 выбран из группы, состоящей из Водорода, F, Cl, Br, I, Циано, СН3;
R4 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, С(=O)-ОН, -С(=O)-O-С1-С6-алкила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, R5 выбран из группы, состоящей из водород, С1-С6-алкила или С3-С6-карбоцикла; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл;
R6 и R7 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С3-С6-карбоцикла, или R6 и R7 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл;
n представляет собой 0;
W представляет собой кислород;
Y представляет собой NH;
Z представляет собой -C(=O)-ORa.
Согласно другому варианту осуществления соединение формулы (I) является предпочтительным, где
R1, R2 и R3 имеют следующие комбинации
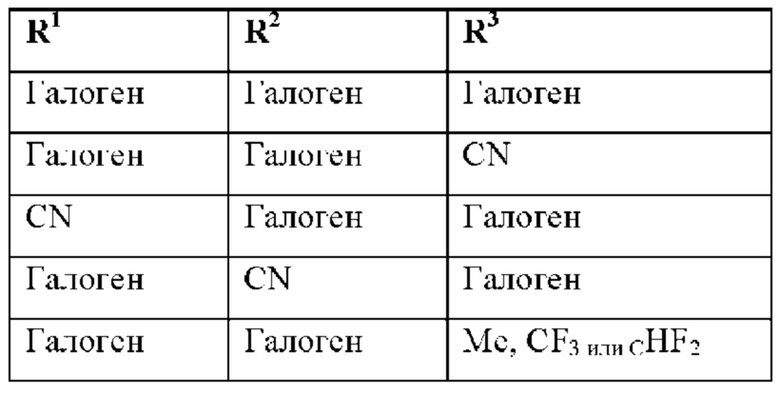
R4 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, С(=O)-ОН, -С(=O)-O-С1-С6-алкила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, R5 выбран из группы, состоящей из водорода, С1-С6-алкила или С3-С6-карбоцикла; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл.
R6 и R7 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С3-С6-карбоцикла, или R6 и R7 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл;
n представляет собой 0;
W представляет собой кислород;
Y выбран из группы, состоящей из NH, N-OCH3, N-OH, и предпочтительно NH; Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, и предпочтительно -C(=O)-ORa.
Согласно другому варианту осуществления, если R1=галоген, тогда R2=циано, С1-С6-алкил или С1-С6-галоалкил и R3=циано, С1-С6-алкил или С1-С6-галоалкил.
Согласно другим вариантам осуществления, если R1=галоген, тогда R2=циано, С1-С6-алкил или С1-С6-галоалкил и R3=водород или галоген. Согласно другому варианту осуществления, если R2=галоген, тогда R1=циано, С1-С6-алкил или С1-С6-галоалкил, и R3=циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, если R2=галоген, тогда R1=циано, С1-С6-алкил или С1-С6-галоалкил, и R3=водород или галоген. Согласно другому варианту осуществления, если R1 и R2=галоген, R2 отличен от R1, и R3=водород или галоген. Согласно другому варианту осуществления, если R1 и R2=галоген, R2 отличен от R1 и R3=циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, если R1 и R2=галоген, R3=циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, если R1 и R2=галоген, R3=водород или галоген. Согласно другому варианту осуществления, если R1 и R2=галоген, R3=водород. Согласно другому варианту осуществления, если R1 и R2=галоген, R3=галоген.
Согласно другому варианту осуществления, R1 представляет собой галоген, циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, R1 представляет собой галоген, циано, С1-С3-алкил или С1-С3-галоалкил. Согласно другому варианту осуществления, R1 представляет собой галоген, циано или С1-С3-алкил. Согласно другому варианту осуществления, R1 представляет собой С1-С3-галоалкил. Согласно другому варианту осуществления, R1 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно другому варианту осуществления R1 представляет собой галоген, циано или метил. Согласно другому варианту осуществления, R1 представляет собой трифторметил или дифторметил.
Согласно другому варианту осуществления, R2 представляет собой галоген, циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, R2 представляет собой галоген, циано, С1-С3-алкил или С1-С3-галоалкил. Согласно другому варианту осуществления, R2 представляет собой галоген, циано или С1-С3-алкил. Согласно другому варианту осуществления, R2 представляет собой С1-С3-галоалкил. Согласно другому варианту осуществления, R2 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно другому варианту осуществления, R2 представляет собой галоген, циано или метил. Согласно другому варианту осуществления, R2 представляет собой трифторметил или дифторметил.
Согласно другому варианту осуществления, R3 представляет собой водород, галоген, циано, С1-С6-алкил или С1-С6-галоалкил. Согласно другому варианту осуществления, R3 представляет собой водород, галоген, циано, С1-С3-алкил или С1-С3-галоалкил. Согласно другому варианту осуществления, R3 представляет собой водород, галоген, циано, метил, трифторметил или дифторметил.
Согласно другому варианту осуществления, R4 и R5 независимо выбраны из группы, состоящей из галогена, циано, гидроксила, С1-С6-алкокси, С1-С6-галоалкила, -О-С(=O)-С1-С6-алкила, 4-, 5- или 6-ти членного неароматического гетероциклила, -С(=O)-NH2, -С(=O)-NH(С1-С6-алкила), -С(=O)-N(С1-С6-алкила)2, -С(=O)-ОН, -С(=O)-O-С1-С6-алкила, 5-9-ти членного гетероарила, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-4-, 5 или 6-ти членного неароматического гетероциклила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-5-9-ти членного гетероарила, -С1-С6-алкил-S-С(=O)-С1-С6-алкила, -С1-С6-алкил-C(=O)-NH2, -С1-С6-алкил-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-С(=O)-N(С1-С6-алкила)2, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-NH-C(=NH)-NH2, -S-С1-С6-алкила, -S-С(=O)-С1-С6-алкила, -S-С(=O)-O-С1-С6-алкила, -S-C(=S)-O-С1-С6-алкила, -S-C(=O)-S-С1-С6-алкила, -S-C(=O)-NH2, -S-С(=O)-NH(С1-С6-алкила), -S-С(=O)-NH(С1-С6-алкила)2, -S-C(=S)-NH2, -S-C(=S)-NH(С1-С6-алкила), -S-C(=S)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-S-С(=O)-S-С1-С6-алкила, -С1-С6-алкил-S-C(=O)-NH2, -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила)2, -С1-С6-алкил-S-С(=S)-NH2, -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила)2; где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл. Согласно другому варианту осуществления, R4 и R5 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, арила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С3-С6-карбоцикла, С1-С6-алкил-O-(С=O)-С1-С6-алкила, -С1-С6-алкил-С(=O)-ОН; -С1-С6-алкил-арила, -С1-С6-алкил-S-С1-С6-алкила, где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл, где указанный С3-С6-карбоцикл и 3-6-ти членный гетероцикл могут быть замещены одним или несколькими Rx заместителями. Согласно другому варианту осуществления, R4 представляет собой водород, С1-С6-алкил, С1-С6-гидроксиалкил, С3-С6-карбоцикл, С(=O)-ОН, -C(=O)-O-С1-С6-алкил, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкил, -С1-С6-алкил-С3-С6-карбоцикл, -С1-С6-алкил-арил, -С1-С6-алкил-гидроксиарил, -С1-С6-алкил-S-С1-С6-алкил-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-ОН, -С1-С6-алкил-С(=O)-O-С1-С6-алкил, R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл. Согласно другому варианту осуществления, R4 представляет собой водород, С1-С6-алкил, С3-С6-карбоцикл, -С1-С6-алкил-С1-С6-галоалкил, -С1-С6-алкил-С3-С6-карбоцикл, -С1-С6-алкил-арил, -С1-С6-алкил-гидроксиарил, -С1-С6-алкил-S-С1-С6-алкил-, R5 представляет собой водород или С1-С6-алкил; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл. Согласно другому варианту осуществления, R4 представляет собой водород, С1-С6-алкил, С3-С6-карбоцикл, -С1-С6-алкил-С1-С6-галоалкил, -С1-С6-алкил-С3-С6-карбоцикл, -С1-С6-алкил-арил, -С1-С6-алкил-гидроксиарил, -С1-С6-алкил-S-С1-С6-алкил-, R5 представляет собой водород или С1-С6-алкил. Согласно другому варианту осуществления, R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-ти членный гетероцикл. Согласно другому варианту осуществления, R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл. Согласно другому варианту осуществления, R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил или Циклобутил.
Согласно другому варианту осуществления n представляет собой 0. Согласно другому варианту осуществления n представляет собой 1.
Согласно другому варианту осуществления W представляет собой кислород. Согласно другому варианту осуществления W представляет собой серу.
Согласно другому варианту осуществления n представляет собой 0 и W представляет собой кислород.
Также предпочтительными являются соединения формулы (I), где n представляет собой 0, и W представляет собой кислород, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород и R8 представляет собой Н.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород и R8 представляет собой Н, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галоген и С1-С6-алкил; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 не представляет собой Н.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 не представляет собой Н, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3 и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R1 выбран из группы, состоящей из CN, Br, Cl, F.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R1 выбран из группы, состоящей из CN, Br, Cl, F, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и С1-С6-алкил; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, и R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и C1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, и по меньшей мере один из R1,R2 и R3 представляет собой циано.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3, и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3, Me.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3 и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3, Me, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и C1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3 и R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3, Me.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, и R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3 и R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3, Me, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и C1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления n представляет собой 0, W представляет собой кислород, R8 представляет собой Н, R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3, R2 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3 и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3, Me.
Также предпочтительными являются соединения формулы (I) где n представляет собой 0, W представляет собой кислород, R8 представляет собой Н и R3 выбран из группы, состоящей из Br, Cl, F, CN, Me, CHF2, CF3, R22 выбран из группы, состоящей из Br, Cl, F, CHF2, CF3 и R1 выбран из группы, состоящей из CN, Br, Cl, F, CHF2, CF3, Me, и где соединения исключены, когда R1, R2 и R3 независимо выбраны из группы, состоящей из галогена и C1-С6-алкила; W представляет собой кислород; Y представляет собой NH; R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил; n представляет собой 0; и Z выбран из группы, состоящей из -C(=O)-ORa, -C(=O)-NRbRc.
Согласно другому варианту осуществления, Y представляет собой NR8, причем R8 представляет собой водород. Согласно другому варианту осуществления Y представляет собой NR8, причем R8 представляет собой C1-С6-алкил, C1-С6-галоалкил, C1-С6-цианоалкил, гидрокси, C1-С6-алкокси или C3-С6-карбоцикл.
Согласно другому варианту осуществления Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa. Согласно другому варианту осуществления Z представляет собой -C(=O)-ORa.
Согласно другому варианту осуществления, если R1 представляет собой C1-С6-галоалкил, или R2 представляет собой C1-С6-галоалкил, и R4 выбран из группы, состоящей из водорода, C1-С6-алкила, и R5 выбран из группы, состоящей из водорода, C1-С6-алкила, и n представляет собой 0, и W представляет собой кислород, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Согласно другому варианту осуществления, если R4 и R5 независимо выбраны из группы, состоящей из водорода, C1-С6-алкила, C1-С6-гидроксиалкила, C3-С6-карбоцикла, арила, -C1-С6-алкил-C1-С6-алкокси, -C1-С6-алкил-C3-С6-карбоцикла, C1-С6-алкил-O-(С=O)-C1-С6-алкила, -C1-С6-алкил-С(=O)-ОН; -C1-С6-алкил-арила, -C1-С6-алкил-S-C1-С6-алкила, где по меньшей мере один из R4 и R5 представляет собой водород, C1-С6-алкил или C3-С6-карбоцикл, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NR8, где R8 выбран из группы, состоящей из водорода, C1-С6-алкила, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Согласно другому варианту осуществления, если R1, R2 и R3 имеют следующие комбинации
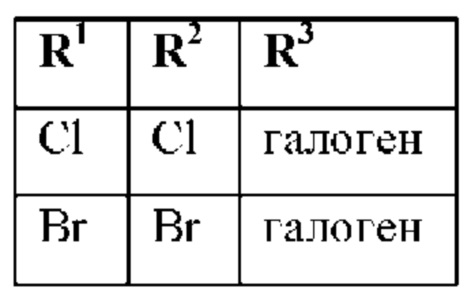
и R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, циклопропил, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NH, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Согласно другому варианту осуществления, если R1, R2 и R3 имеют следующие комбинации

и R4 выбран из группы, состоящей из водорода, C1-С6-алкила, -C1-С6-алкил-арила, -C1-С6-алкил-гидроксиарила, -C1-С6-алкил-S-C1-С6-алкила, R5 представляет собой водород, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NH тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
Также предпочтительными являются соединения I.0001-I.1070, раскрытые в таблицах I.1 и I.2 в экспериментальной части.
Другой аспект настоящего изобретения относится к композиции, содержащей по меньшей мере одно соединение формулы (I) согласно настоящему изобретению и по меньшей мере одно сельскохозяйственно приемлемое вспомогательное вещество.
Другой аспект настоящего изобретения относится к способу борьбы с бактериальными и/или грибковыми заболеваниями растений, включающему стадию нанесения по меньшей мере одного соединения формулы (I) согласно настоящему изобретению или композиции согласно настоящему изобретению на растения, части растения, семена, плоды или в почву, в которой растут растения.
Другой аспект настоящего изобретения относится к применению соединения согласно настоящему изобретению или композиции согласно настоящему изобретению для борьбы с бактериальными и/или грибковыми заболеваниями растений или частей растений. Предпочтительно их применяют для борьбы с грибковыми заболеваниями растений или частей растений.
Другой аспект настоящего изобретения относится к применению соединения согласно настоящему изобретению или композиции согласно настоящему изобретению для борьбы с нематодами на растениях или частях растений.
Другой аспект настоящего изобретения относится к применению соединения согласно настоящему изобретению или композиции согласно настоящему изобретению для борьбы с вирусами на растениях или частях растений.
Предпочтительно соединение или композицию согласно настоящему изобретению используют против: болезней, вызываемых возбудителями мучнистой росы, такими как виды Podosphaera (например, Podosphaera leucotricha), виды Sphaerotheca (например, Sphaerotheca fuliginea); заболевания, вызываемые возбудителями ржавчины, такими как виды Uromyces (например, Uromyces appendiculatus); болезни, вызываемые патогенами из группы оомицетов, такими как виды Peronospora (например, Peronospora parasitica), виды Phytophthora (например, Phytophthora infestans), виды Plasmopara (например, Plasmopara viticola), виды Pseudoperonospora (например, Pseudoperonospora humuli или Pseudoperonospora cubensis), виды Pythium (например, Pythium ultimum); болезни пятнистости листьев и болезни увядания листьев, вызываемые, например, видами Alternaria (например, Alternaria solani), видами Cercospora (например, Cercospora beticola), видами Colletotrichum (например, Colletotrichum lindemuthanium), видами Venturia (например, Venturia inaequalis); заболевания, вызываемые бактериальными патогенами, например, виды Xanthomonas (например, Xanthomonas campestris pv. campestris), виды Pseudomonas (например, Pseudomonas syringae pv. tomato), виды Erwinia (например, Erwinia amylovora), виды Liberibacter (например, Liberibacter Candidatus), виды Ralstonia (например, Ralstonia solanacearum).
Согласно еще одному аспекту настоящего изобретения соединение или композиция согласно настоящему изобретению применяют в качестве активатора защиты растений. Индуктор защиты растений согласно настоящему изобретению представляет собой соединение или композицию, которая стимулирует собственную защитную систему растения.
Настоящее изобретение также относится к применению соединения формулы (II) для защиты растений
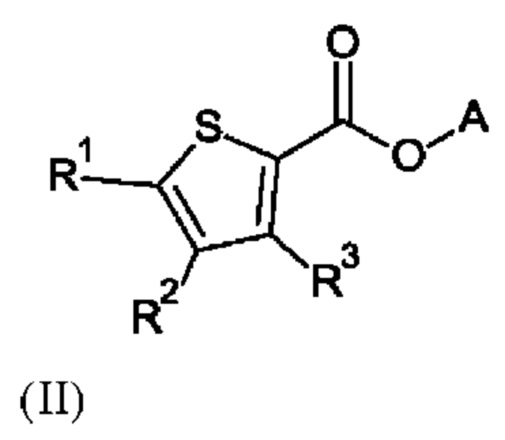
где
R1 и R2 независимо друг от друга выбраны из группы, состоящей из галогена, циано, C1-С3-алкила или C1-С3-галоалкила, где по меньшей мере один из R1 или R2 представляет собой галоген;
R3 выбран из группы, состоящей из водорода, галогена, циано, C1-С3-алкила или C1-С3-галоалкила;
А выбран из группы, состоящей из водорода и C1-С6-алкила;
при условии, что соединения формулы (II) со следующими комбинациями R1, R2 и R3
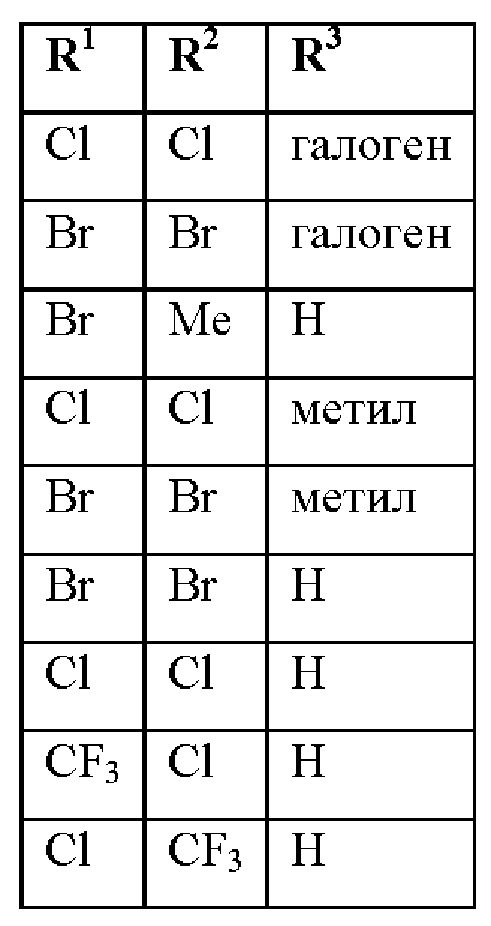
исключены.
Согласно варианту осуществления, R1 представляет собой галоген, циано, C1-С3-алкил или C1-С3-галоалкил. Согласно варианту осуществления, R1 представляет собой галоген, циано или C1-С3-алкил. Согласно варианту осуществления, R1 представляет собой C1-С3-галоалкил. Согласно варианту осуществления, R1 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно варианту осуществления, R1 представляет собой галоген, циано или метил. Согласно варианту осуществления, R1 представляет собой трифторметил или дифторметил.
Согласно варианту осуществления, R2 представляет собой галоген, циано, C1-С3-алкил или C1-С3-галоалкил. Согласно варианту осуществления, R2 представляет собой галоген, циано или C1-С3-алкил. Согласно варианту осуществления, R2 представляет собой C1-С3-галоалкил. Согласно варианту осуществления, R2 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно варианту осуществления, R2 представляет собой галоген, циано или метил. Согласно варианту осуществления, R2 представляет собой трифторметил или дифторметил.
Согласно варианту осуществления, R3 представляет собой водород, галоген, циано,
C1-С3-алкил или C1-С3-галоалкил. Согласно варианту осуществления, R3 представляет собой водород, галоген, циано, метил, трифторметил или дифторметил.
Согласно варианту осуществления, А представляет собой водород. Согласно варианту осуществления, А представляет собой водород или C1-С6-алкил. Согласно варианту осуществления, А представляет собой водород или C1-С3-алкил. Согласно варианту осуществления, А представляет собой водород, метил, этил или пропил.
Согласно предпочтительному варианту осуществления R1 и R2 независимо друг от друга выбраны из группы, состоящей из галогена, циано или C1-С3-алкила, где по меньшей мере один из R1 или R2 представляет собой галоген.
Также предпочтительными являются соединения II.001-II.104, раскрытые в Таблице II.1 в экспериментальной части.
Также предпочтительно, когда соединение формулы (II) применяют для борьбы с фитопатогенными грибами и/или бактериями на растениях или частях растения. Наиболее предпочтительно соединение формулы (II) применяют для борьбы с грибковыми заболеваниями растений или частей растений.
Также предпочтительно, когда соединение формулы (II) применяют для борьбы с нематодами на растениях или частях растений.
Также предпочтительно, когда соединение формулы (II) применяют для борьбы с вирусами на растениях или частях растений.
Предпочтительно соединение или композицию согласно настоящему изобретению используют против: болезней, вызываемых возбудителями мучнистой росы, такими как виды Podosphaera (например, Podosphaera leucotricha), виды Sphaerotheca (например, Sphaerotheca fuliginea); заболевания, вызываемые возбудителями ржавчины, такими как виды Uromyces (например, Uromyces appendiculatus); болезни, вызываемые патогенами из группы оомицетов, такими как виды Peronospora (например, Peronospora parasitica), виды Phytophthora (например, Phytophthora infestans), виды Plasmopara (например, Plasmopara viticola), виды Pseudoperonospora (например, Pseudoperonospora humuli или Pseudoperonospora cubensis), виды Pythium (например, Pythium ultimum); болезни пятнистости листьев и болезни увядания листьев, вызываемые, например, видами Alternaria (например, Alternaria solani), видами Cercospora (например, Cercospora beticola), видами Colletotrichum (например, Colletotrichum lindemuthanium), видами Venturia (например, Venturia inaequalis); заболевания, вызываемые бактериальными патогенами, например, виды Xanthomonas (например, Xanthomonas campestris pv. campestris), виды Pseudomonas (например, Pseudomonas syringae pv. tomato), виды Erwinia (например, Erwinia amylovora), виды Liberibacter (например, Liberibacter Candidatus), виды Ralstonia (например, Ralstonia solanacearum).
Согласно еще одному аспекту настоящего изобретения соединение формулы (II) настоящему изобретению применяют в качестве активатора защиты растений. Индуктор защиты растений согласно настоящему изобретению представляет собой соединение или композицию, которая стимулирует собственную защитную систему растения.
Настоящее изобретение также относится к соединению формулы (II-А):
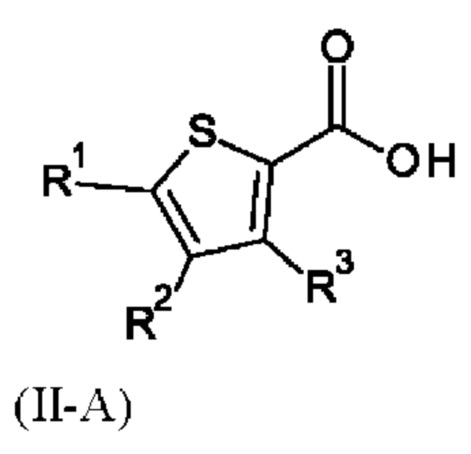
где
R1 выбран из группы, состоящей из галогена, циано, метила или C1-С2-галоалкила; R2 выбран из группы, состоящей из галогена, циано или C1-С2-галоалкила; R3 выбран из группы, состоящей из галогена, циано, метила или C1-С2-галоалкила; где по меньшей мере два из R1, R2 или R3 представляют собой галоген;
при условии, что соединения формулы (II-А) со следующими комбинациями R1, R2 и R3
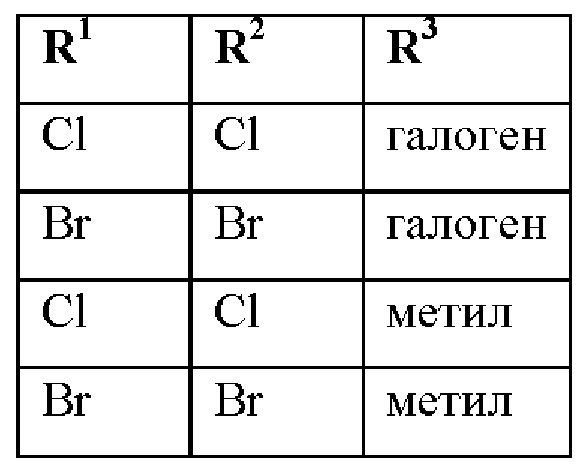
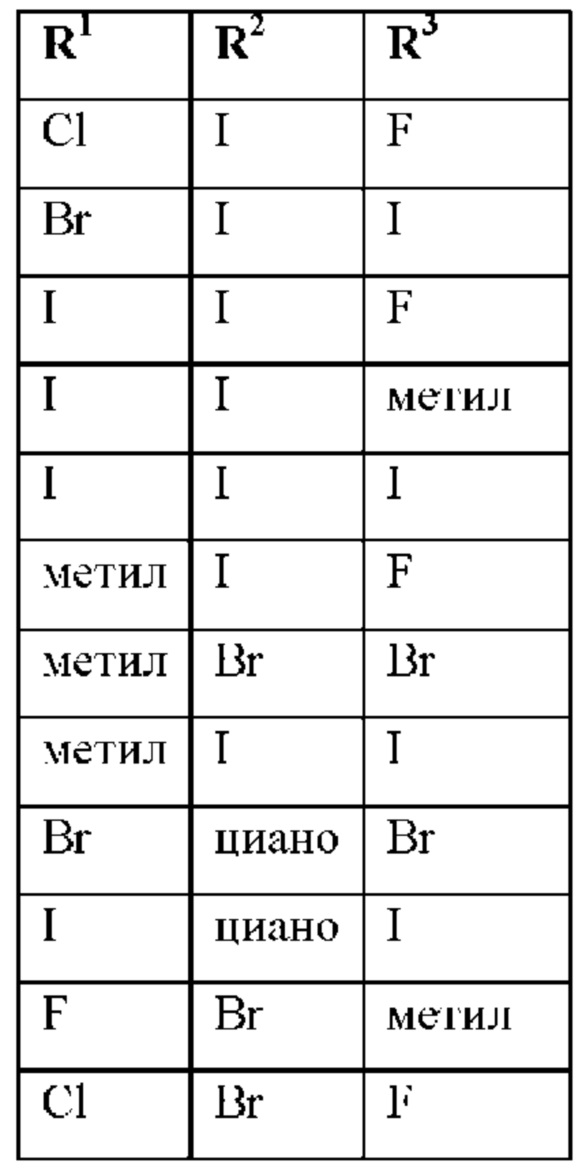
исключены.
WO 2020/079205 раскрывает 3-фтор-5-йодтиофен-2-карбоновую кислоту и 5-бром-4-хлор-3-фтортиофен-2-карбоновую кислоту; FR 3052451 описывает 5-хлор-3-фтор-4-метилтиофен-2-карбоновую кислоту и 4,5-дихлор-3-фтортиофен-2-карбоновую кислоту.; HULL JOHN W JR ET AL: "Development of potential manufacturing routes for substituted тиофенев - Preparation of halogenated 2- thiophenecarboxylic acid derivatives as building blocks for a new family of 2,6-dihaloaryl 1,2,4-triazole insecticides", BEILSTEIN JOURNAL OF ORGANIC CHEMISTRY, BIOMED CENTRAL, LONDON, GB, vol. 3, no. 1, 4 September 2007 (2007-09-04), page 23, XP021041099, ISSN: 1860-5397 раскрывает 3,5-дибром-4-метилтиофен-2-карбоновую кислоту; KOCHANNY ET AL: "Substituted thiophene-anthranilamides as potent inhibitors of human factor Xa", BIOORGANIC & MEDICINAL CHEMISTRY: A TETRAHEDRON PUBLICATION FOR THE RAPID DISSEMINATION OF FULL ORIGINAL RESEARCH PAPERS AND CRITICAL REVIEWS ON BIOMOLECULAR CHEMISTRY, MEDICINAL CHEMISTRY AND RELATED DISCIPLINES, ELSEVIER, NL, vol. 15, no. 5, 31 January 2007 (2007-01-31), pages 2127-2146, XP005867178, ISSN: 0968-0896, DOI: 10.1016/J.BMC.2006.12.019 раскрывает 3-хлор-5-(хлорметил)-4-метилтиофен-2-карбоновую кислоту и STEINKOPF W ET AL: "Thiophene series. XXXVII. Iodine derivatives of 3-thiotolene", JUSTUS LIEBIGS ANNALEN DER CHEMIE, VERLAG CHEMIE GMBH, DE, vol. 532, 1 January 1937 (1937-01-01), pages 236-249, XP009107181, ISSN: 0075-4617, DOI: 10.1002/JLAC.19375320120 раскрывает 4,5-дийод-3-метилтиофен-2-карбоновую кислоту. Однако ни одно из вышеупомянутых соединений предшествующего уровня техники не подпадает под объем настоящего изобретения, поскольку все они исключены по условию.
Согласно варианту осуществления, R1 представляет собой галоген, циано, метил или C1-С2-галоалкил. Согласно варианту осуществления, R1 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно варианту осуществления, R1 представляет собой галоген, циано или метил.
Согласно варианту осуществления, R1 представляет собой галоген или циано. Согласно варианту осуществления, R1 представляет собой C1-С2-галоалкил. Согласно варианту осуществления, R1 представляет собой трифторметил или дифторметил.
Согласно варианту осуществления, R2 представляет собой галоген, циано или C1-С2-галоалкил. Согласно варианту осуществления, R2 представляет собой галоген, циано, трифторметил или дифторметил. Согласно варианту осуществления, R1 представляет собой галоген или циано. Согласно варианту осуществления, R2 представляет собой C1-С2-галоалкил. Согласно варианту осуществления, R2 представляет собой трифторметил или дифторметил.
Согласно варианту осуществления, R3 представляет собой галоген, циано, метил или C1-С2-галоалкил. Согласно варианту осуществления, R3 представляет собой галоген, циано, метил, трифторметил или дифторметил. Согласно настоящему изобретению не охвачены соединения, полученные в результате комбинаций, которые противоречат законам природы и которые, следовательно, специалист в данной области исключил бы на основании своих экспертных знаний. Например, исключаются кольцевые структуры, имеющие три или более соседних атома кислорода.
В зависимости от природы заместителей соединение формулы (I) или (II) может присутствовать в виде различных стереоизомеров. Эти стереоизомеры представляют собой, например, энантиомеры, диастереомеры, атропоизомеры или геометрические изомеры. Соответственно изобретение охватывает как чистые стереоизомеры, так и любую смесь этих изомеров. Если соединение может находиться в двух или более таутомерных формах в равновесии, ссылка на соединение посредством одного таутомерного описания должна рассматриваться как включающая все таутомерные формы.
Любое из соединений согласно настоящему изобретению может также существовать в форме одного или нескольких геометрических изомеров в зависимости от количества двойных связей в соединении. Геометрические изомеры по природе заместителей у двойной связи или кольца могут находиться в цис-(=Z-) или транс-(=Е-) форме. Таким образом, изобретение в равной степени относится ко всем геометрическим изомерам и ко всем возможным смесям во всех соотношениях.
Соединение формулы (I) или (II) может находиться в свободной форме, в форме соли, в форме N-оксида или в форме сольвата (например, гидрата).
В зависимости от природы заместителей соединение формулы (I) или (II) может присутствовать в форме свободного соединения и/или его соли, такой как сельскохозяйственно активная соль.
Сельскохозяйственно активные соли включают кислотно-аддитивные соли неорганических и органических кислот, а также соли обычных оснований. Примерами неорганических кислот являются галогеноводородные кислоты, такие как фтористый водород, хлористый водород, бромистый водород и йодистый водород, серная кислота, фосфорная кислота и азотная кислота, и кислые соли, такие как бисульфат натрия и бисульфат калия. Полезные органические кислоты включают, например, муравьиную кислоту, угольную кислоту и алкановые кислоты, такие как уксусная кислота, трифторуксусная кислота, трихлоруксусная кислота и пропионовая кислота, а также гликолевую кислоту, тиоциановую кислоту, молочную кислоту, янтарную кислоту, лимонную кислоту, бензойную кислоту, коричную кислоту, щавелевую кислоту, насыщенные или моно- или диненасыщенные жирные кислоты, содержащие от 6 до 20 атомов углерода, сложные моноэфиры алкилсеры, алкилсульфокислоты (сульфокислоты, содержащие неразветвленные или разветвленные алкильные радикалы, содержащие от 1 до 20 атомов углерода), арилсульфокислоты или арилдисульфокислоты (ароматические радикалы, такие как фенил и нафтил, которые несут одну или две группы сульфоновой кислоты), алкилфосфоновые кислоты (фосфоновые кислоты, имеющие алкильные радикалы с прямой или разветвленной цепью, содержащие от 1 до 20 атомов углерода), арилфосфоновые кислоты или арилдифосфоновые кислоты (ароматические радикалы, такие как фенил и нафтил, которые несут один или два радикала фосфоновой кислоты), где алкильные и арильные радикалы могут иметь дополнительные заместители, например п-толуолсульфоновая кислота, салициловая кислота, п-аминосалициловая кислота, 2-феноксибензойная кислота, 2-ацетоксибензойная кислота и др.
Сольваты соединений формулы (I) или (II) или их солей представляют собой стехиометрические композиции соединений с растворителями.
Соединения формулы (I) или (II) могут существовать в нескольких кристаллических и/или аморфных формах. Кристаллические формы включают несольватированные кристаллические формы, сольваты и гидраты.
Способы получения соединений формулы (I)
Настоящее изобретение относится к способам получения соединений формулы (I). Соединения формулы (I) могут быть получены различными способами по аналогии с известными способами (см. ссылки в настоящем документе) и одним или несколькими из следующих способов синтеза, описанных в настоящем документе ниже и в экспериментальной части.
Общие синтетические способы получения соединений формулы (I)
Если не указано иное, далее R1, R2, R3, R4, R5, R6, R7, W, Y, Z и n имеют значения, указанные выше для соединений формулы (I).
Способ А1
Соединения формулы (Ia) могут быть получены способом А1, который включает стадию взаимодействия соединения формулы (III) или одной из его солей с соединением формулы (IV) или одной из его солей, как показано следующей реакцией схема:
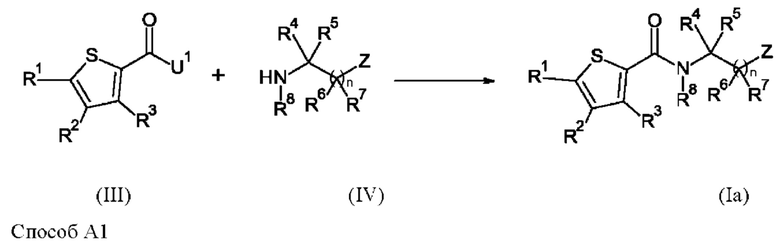
где U1 представляет собой галоген, гидрокси или C1-С6-алкокси.
Когда U1 представляет собой гидрокси, способ А1 целесообразно проводить в присутствии конденсирующего агента. Подходящие конденсирующие агенты могут быть выбраны из неограничивающего списка, состоящего из галогенангидрида, такого как фосген, трибромид фосфора, трихлорид фосфора, пентахлорид фосфора, оксид трихлорида фосфора, оксалилхлорид или тионилхлорид; ангидридный агент, такой как этилхлорформиат, метилхлорформиат, изопропилхлорформиат, изобутилхлорформиат или метансульфонилхлорид; карбодиимиды, такие как N,Nў-дициклогексилкарбодиимид (DCC), гидрохлорид N-(3-диметиламинопропил)-Nў-этилкарбодиимида (EDC) или другие обычные конденсирующие агенты, такие как пятиокись фосфора, полифосфорная кислота, бис(2-оксо-3-оксазолидинил)фосфинхлорид, 1-[бис(диметиламино)метилен]-1Н-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфат (HATU), 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния тетрафторборат (TBTU), (1-циано-2-этокси-2-оксоэтилиденаминоокси)диметиламиноморфолинокарбения гексафторфосфат, N,Nў-карбонилдиимидазол, 2-этокси-N-этоксикарбонил-1,2-дигидрохинолин (EEDQ), трифенилфосфин/тетрахлорметан, гидрат 4-(4,6-диметокси[1.3.5]-триазин-2-ил)-4-метилморфолиния хлорида, бис(2-оксо-3-оксазолидинил)фосфинхлорид (ВОР-Cl), бромтрипирролидинофосфонийгексафторфосфат (PyBroP), 2-хлор-1,3-диметилимидазолиния хлорид (DMC), пропанфосфоновый ангидрид (ТЗР) и 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он (DEPBT).
Когда U1 представляет собой галоген, способ А1 целесообразно проводить в присутствии кислотного связующего. Подходящими кислотными связующими для осуществления способа А1 являются в каждом случае все обычные для таких реакций неорганические и органические основания. Предпочтительны карбонаты щелочных металлов, такие как карбонат цезия, карбонат натрия, карбонат калия, бикарбонат калия, бикарбонат натрия, ацетаты щелочноземельных металлов, такие как ацетат натрия, ацетат калия, ацетат кальция, а также третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, трибутиламин, N,N-диметиланилин, N-метилпиперидин, N,N-диметилпиридин-4-амин, диазабициклооктан (DABCO), диазабициклононен (DBN) или диазабициклоундецен (DBU), или ароматические основания, такие как пиридин.
Когда U1 представляет собой C1-С6-алкокси, способ А1 можно проводить с избытком аминного компонента, необязательно в присутствии кислоты Льюиса, такой как триметилалюминий.
При необходимости способ А1 можно проводить в присутствии основания и при необходимости в присутствии растворителя, предпочтительно в безводных условиях.
Подходящие растворители для осуществления способа А1 конкретно не ограничены. Они могут быть обычными инертными органическими растворителями до тех пор, пока они не растворяют соединение для взаимодействия с ним или проявляют с ним какое-либо конкретное взаимодействие. Предпочтение отдается использованию необязательно галогенированных, алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, пентан, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол, декалин, ISOPARФ Е или ISOPARФ G, хлорбензол, дихлорбензол, дихлорметан, хлороформ, четыреххлористый углерод, 1,2-дихлорэтан или трихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил -трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 2-метилтетрагидрофуран, 1,2-диметоксиэтан, 1,2-диэтоксиэтан или анизол; нитрилы, такие как ацетонитрил, пропионитрил, н- или изо-бутиронитрил или бензонитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; мочевины, такие как 1,3-диметил-3,4,5,6-тетрагидро-2(1H)-пиримидинон; сложные эфиры, такие как метилацетат или этилацетат, сульфоксиды, такие как диметилсульфоксид, или сульфоны, такие как сульфолан; и их смесь
Способ А1 можно проводить в инертной атмосфере, такой как атмосфера аргона или азота. При осуществлении способа А1 на моль соединения формулы (IV) можно использовать 1 моль или избыток соединения формулы (III) и от 1 до 5 молей основания. Возможно также использование компонентов реакции в других соотношениях. Обработку проводят известными методами.
Соединения формулы (IV) имеются в продаже или могут быть получены хорошо известными способами (J. Med. Chem. 2018, 61, 8670-8692; Tetrahedron, 44(1), 195-202; 1988, WO 2009070485; WO 2019086142; Chem. Res. Toxicol. 1990, 3, 118-124; JP 49035334; JP 49000223; Journal of Organic Chemistry (1989), 54(12), 2940-2949).
Соединения формулы (IIIa), в которой U1 представляет собой гидрокси, являются коммерчески доступными, их можно получить из соединений формулы (IIIb), в которой U1 представляет собой C1-C6-алкокси с помощью хорошо известных способов, таких как основной гидролиз, или их можно получить путем известных способов (Beilstein J. Org. Chem. 2007, 3, No. 23)
Соединения формулы (IIIc), в которой U1 представляет собой галоген являются коммерчески доступными, их можно получить из соединений формулы (IIIa), где U1 представляет собой гидрокси, с помощью хорошо известных способов.
Соединения формулы (IIIb), в которой U1 представляет собой C1-С6-алкокси могут быть получены из соединений формулы (IIIa), где U1 представляет собой гидрокси с помощью хорошо известных способов.
Способ В1
Соединения формулы (Ib), где R1 представляет собой C1-С6-алкил, (Ic) где R2 представляет собой C1-С6-алкил, и (Id), где R3 представляет собой C1-С6-алкил, может быть получен способом В1, который включает стадию взаимодействия соединения формулы (Va), (Vb) или (Vc) или одной из его солей с соединением формулы (VIa), (VIb) или (VIc) или одной из его солей, как показано на следующей схеме реакции:
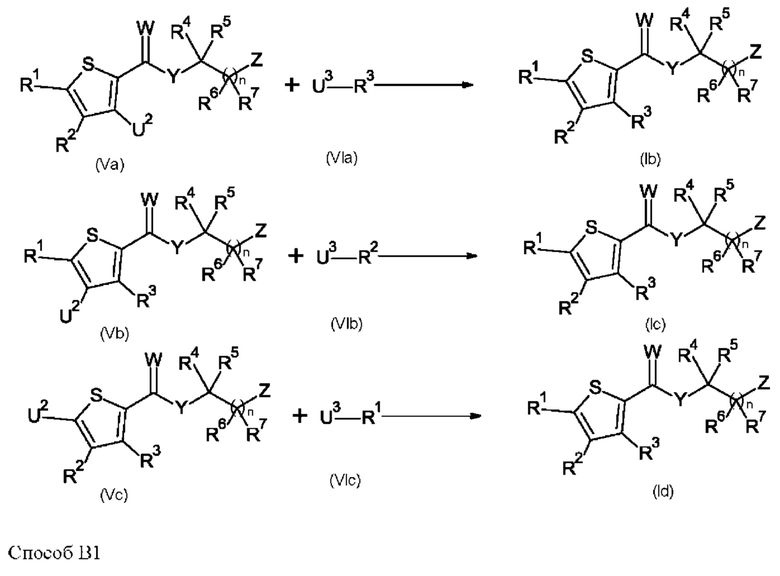
где U3 представляет собой производное бора, такое как бороновая кислота, производное сложного эфира бороновой кислоты, производное трифторбората калия или галогенометалл, который может образовывать комплексы с 1-2 лигандами, такими как галогеномагний или галогеноцинк,
и где:
для (Va), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу:
- R1 или R2 не представляет собой йод
-, когда R1 или R2 представляет собой бром, U2 не представляет собой бром для (Vb), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу, при условии, что:
- R1 или R3 не представляет собой йод
-, когда R1 или R3 представляет собой бром, U2 не представляет собой бром для (Vc), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу при условии, что:
- R2 или R3 не представляет собой йод
-, когда R2 или R3 представляют собой бром, U2 не представляет собой бром.
Способ В1 можно проводить в присутствии катализатора на основе переходного металла, такого как палладий, и, при необходимости, в присутствии фосфинового лиганда или N-гетероциклического карбенового лиганда, при необходимости в присутствии основания и, при необходимости, в присутствии растворителя в соответствии с известными способами (WO 2012054721, Angew. Chem. Int. Ed. 2017, 56, 1581, Angew. Chem. Int. Ed. 2017, 56, 7078, и процитированные в них источники).
Способ В1 можно проводить в присутствии катализатора, такого как соль или комплекс металла. Подходящими для этой цели производными металлов являются катализаторы на основе переходных металлов, такие как палладий. Подходящими солями или комплексами металлов для этой цели являются, например, хлорид палладия, ацетат палладия, тетракис(трифенилфосфин)палладий(0), бис(дибензилиденацетон)палладий(0), трис(дибензилиденацетон)дипалладий(0), бис(трифенилфосфин)палладий (II) дихлорид, [1,1ў-бис(дифенилфосфино)ферроцен]дихлорпалладий(II), бис(циннамил)дихлордипалладий(II), бис(аллил)-дихлордипалладий(II), [1,1ў-бис(ди-трет-бутилфосфино)ферроцен]дихлорпалладий(II), ди-m-йодобис(три-трет-бутилфосфино)дипалладий(I) или ди-m-бромбис(три-трет-бутилфосфино)дипалладий(I).
Также возможно образование комплекса палладия в реакционной смеси путем раздельного добавления в реакцию соли палладия и лиганда или соли, такой как триэтилфосфин, три-трет-бутилфосфин, три-трет-бутилфосфония тетрафторборат, трициклогексилфосфин, 2-(дициклогексилфосфино)бифенил, 2-(ди-трет-бутилфосфино)бифенил, 2-(дициклогексилфосфино)-2ў-(N,N-диметиламино)бифенил, 2-(трет-бутилфосфино)-2ў-(N,N-диметиламино)бифенил, 2-ди-трет-бутилфосфино-2ў,4ў,6ў-триизопропилбифенил 2-дициклогексилфосфино-2ў,4ў,6ў-триизопропилбифенил, 2-дициклогексилфосфино-2,6ў-диметоксибифенил, 2-дициклогексилфосфино-2ў,4ў,6ў-триизопропилбифенил, дициклогексилфосфино-2ў,6ў-диизопропоксибифенил, трифенилфосфин, трис-(о-толил)фосфин, 3-(дифенилфосфино)бензолсульфонат натрия, трис-2-(метоксифенил)фосфин, 2,2ў-бис(дифенилфосфино)-1,1ў-бинафтил, 1,4-бис(дифенилфосфино)бутан, 1,2-бис(дифенилфосфино)этан, 1,4-бис(дициклогексилфосфино)бутан, 1,2-бис(дициклогексилфосфино)этан, 2-(дициклогексилфос фино)-2ў-(N,N-диметиламино)-бифенил, 1,1ў-бис(дифенилфосфино)-ферроцен, (R)-(-)-1-[(S)-2-дифенил-фосфино)ферроценил]этилдициклогексилфосфин, трис-(2,4-трет-бутилфенил)фосфит, ди(1-адамантил)-2-морфолинофенилфосфин или хлорид 1,3-бис(2,4,6-триметилфенил)имидазолия.
Также выгодно выбирать соответствующий катализатор и/или лиганд из коммерческих каталогов, таких как "Metal Catalysts for Organic Synthesis" от Strem Chemicals или "Phosphorous Ligands and Compounds" от Strem Chemicals.
Подходящими основаниями для проведения способа В1 могут быть неорганические и органические основания, обычные для таких реакций. Предпочтительно используют гидроксиды щелочноземельных или щелочных металлов, такие как гидроксид натрия, гидроксид кальция, гидроксид калия или другие производные гидроксида аммония; фториды щелочноземельных металлов, щелочных металлов или аммония, такие как фторид калия, фторид цезия или фторид тетрабутиламмония; карбонаты щелочноземельных или щелочных металлов, такие как карбонат натрия, карбонат калия, бикарбонат калия, бикарбонат натрия или карбонат цезия; ацетаты щелочных или щелочноземельных металлов, такие как ацетат натрия, ацетат лития, ацетат калия или ацетат кальция; фосфат щелочного металла или щелочноземельного металла, такой как трикалийфосфат щелочного металла; алкоголяты щелочных металлов, такие как трет-бутоксид калия или трет-бутоксид натрия; третичные амины, такие как триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-дициклогексилметиламин, N,N-диизопропилэтиламин, N- -метилпиперидин, N,N-диметиламинопиридин, диазабициклооктан (DABCO), диазабициклононен (DBN) или диазабициклоундецен (DBU); а также ароматические основания, такие как пиридин, пиколины, лутидины или коллидины.
Подходящими растворителями для осуществления способа В1 могут быть обычные инертные органические растворители. Предпочтение отдается использованию необязательно атомизированных галогеном алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, пентан, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол или декалин; хлорбензол, дихлорбензол, дихлорметан, хлороформ, четыреххлористый углерод, дихлорэтан или трихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 2-метилтетрагидрофуран, 1,2-диметоксиэтан, 1,2-диэтоксиэтан или анизол; нитрилы, такие как ацетонитрил, пропионитрил, н- или изобутиронитрил или бензонитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; мочевины, такие как 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)-пиримидинон; сложные эфиры, такие как метилацетат или этилацетат, сульфоксиды, такие как диметилсульфоксид, или сульфоны, такие как сульфолан; и их смеси.
Также может быть выгодно проводить способ В1 с сорастворителем, таким как вода или спирт, такой как метанол, этанол, пропанол, изопропанол или трет-бутанол.
Способ В1 можно проводить в инертной атмосфере, такой как аргон или азот. При осуществлении способа B1, 1 моль или избыток соединения формулы (VIa), (VIb) или (VIc) и от 1 до 5 молей основания и от 0,01 до 20 мольных процентов комплекса палладия на моль соединения формулы (Va), (Vb) или (Vc). Возможно также использование компонентов реакции в других соотношениях. Обработку осуществляют известными методами.
Соединения формулы (VIa), (VIb) или (VIc) являются коммерчески доступными или могут быть получены хорошо известными способами.
Соединения формулы (Va), (Vb) или (Vc), где W представляет собой кислород, могут быть получены путем взаимодействия соединения формулы (VIIa), (VIIb) или (VIIc) с соединением формулы (IV) в условиях, описанных в связи со способом А1:
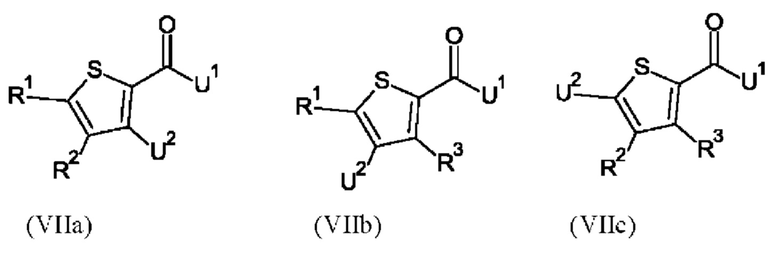
где U2 и U1 имеют значения, указанные выше.
Соединения формулы (VIIa), (VIIb) или (VIIc), где U2 представляет собой хлор, бром или йод, являются коммерчески доступными или могут быть получены хорошо известными способами с такими же реакционными условиями, как те, которые раскрыты для получения соединений формулы (III).
Соединения формулы (VIIa), (VIIb) или (VIIc), где U2 представляет собой мезилатную группу, тозилатную группу или трифлатную группу, могут быть получены хорошо известными способами из соответствующего соединения, содержащего гидроксильную группу в положении U2.
Способ С1
Соединения формулы (Ie) могут быть получены по способу С1 из соединения формулы (Ia) путем проведения реакции тионирования, как показано на следующей схеме реакции:
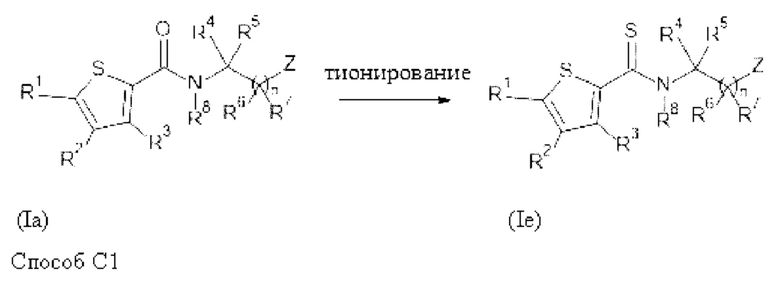
Способ С1 согласно изобретению осуществляют в присутствии тионирующего агента.
Подходящими тионирующими агентами для осуществления способа С1 согласно изобретению могут быть сера (S), сероводородная кислота (H2S), сульфид натрия (Na2S), гидросульфид натрия (NaHS), трисульфид бора (B2S3), бис(диэтилалюминий)сульфид ((AlEt2)2S), сульфид аммония ((NH4)2S), пентасульфид фосфора (P2S5), реактив Лавессона (2,4-бис(4-метоксифенил)-1,2,3,4-дитиадифосфетан-2,4-дисульфид) или тионирующий реагент на полимерном носителе, такой как описанный в Journal of the Chemical Society, Perkin 1 (2001), 358, необязательно в присутствии каталитического или стехиометрического или избыточного количества, количества основания, такого как неорганическое и органическое основание. Предпочтение отдается использованию карбонатов щелочных металлов, таких как карбонат натрия, карбонат калия, бикарбонат калия, бикарбонат натрия; гетероциклические ароматические основания, такие как пиридин, пиколин, лутидин, коллидин; а также третичные амины, такие как триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-диметилпиридин-4-амин или N-метилпиперидин.
Подходящими растворителями для осуществления способа С1 согласно изобретению могут быть обычные инертные органические растворители. Предпочтение отдается использованию необязательно галогенированных алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол или декалин, хлорбензол, дихлорбензол, дихлорметан, хлороформ, четыреххлористый углерод, дихлорэтан или трихлорэтан, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 1,2-диметоксиэтан или 1,2-диэтоксиэтан, нитрилы, такие как ацетонитрил, пропионитрил, н- или изо-бутиронитрил или бензонитрил, сернистые растворители, такие как сульфолан или сероуглерод.
При осуществлении способа С1 согласно изобретению, 1 моль или избыток эквивалента серы тионирующего агента и от 1 до 3 молей основания можно применять на моль амидного реагента (Ia).
Возможно также использование компонентов реакции в других соотношениях. Обработка проводят известными методами.
Способ D1
Соединения формулы (If), где R1 представляет собой циано, (Ig) где R2 представляет собой циано, м (Ih) где R3 представляет собой циано, могут быть получены способом D1, который включает стадию взаимодействия соединения формулы (Va), (Vb) или (Vc) или одной из его солей с цианирующим реагентом в соответствии с к известным процессам (Chem. Rev. 1987, 87, 4, 779-794; Chem. Soc. Rev., 2011,40, 5049-5067; WO 2012123471 и процитированные в них ссылочные источники).
Способ D1 можно проводить в присутствии катализатора на основе переходного металла, такого как соль или комплекс металла, и, при необходимости, в присутствии лиганда; при необходимости в присутствии основания и при необходимости в присутствии растворителя. Подходящими для этой цели производными металлов являются переходные металлы, такие как палладий или медь. Подходящие растворители для проведения способа D1 конкретно не ограничиваются. Они могут быть обычными инертными органическими растворителями до тех пор, пока они не растворяют соединение для взаимодействия с ним или проявляют какое-либо конкретное взаимодействие с ним. Подходящими растворителями могут быть, например, растворители, описанные в связи со способом А1. Примеры цианирующих агентов включают ферроцианид калия, цианид меди, цианид цинка, цианид натрия, цианид калия.
Способ Е1
Соединения формулы (I), как определено в настоящем документе, могут быть получены способом Е1 из соединения формулы (VIII) или одной из его солей путем проведения реакции галогенирования, как показано на следующей схеме реакции:

где U4, U5 и U6 независимо выбраны из перечня, состоящего из водорода, галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U4, U5 или U6 представляет собой по меньшей мере водород.
Способ Е1 можно проводить согласно известным способам (Angewandte Chemie, International Edition, 52(16), 4440-4444; 2013; ACS Catalysis, 6(11), 7839-7843; 2016; Journal of the American Chemical Society, 2017, 139, 888; Angewandte Chemie, International Edition, 2014, 53, 7928; Journal of the American Chemical Society, 2018, 140, 2789; WO 2008156879; WO 2012114285; WO 2008109786; WO 2007098356).
Способ El осуществляют в присутствии галогенирующего агента и, при необходимости, в присутствии растворителя.
Подходящие галогенирующие агенты для осуществления способа Е1 конкретно не ограничены при условии, что они используются для бромирования, хлорирования, йодирования или фторирования. Примеры агентов бромирования включают бром, N-бромсукцинимид, 1,2-дибромтетрахлорэтан и 1,3-дибром-5,5-диметил-2,4-имидазолидиндион. Примеры агентов хлорирования включают N-хлорсукцинимид, сульфурилхлорид, гексахлорэтан и 1,3-дихлор-5,5-диметил-2,4-имидазолидиндион. Примеры йодирующих агентов включают йод, N-йодосукцинимид, хлорид йода и 1,3-дийод-5,5-диметил-2,4-имидазолидиндион. Примеры агентов фторирования включают N фторбензолсульфонимид и 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан-бис (тетрафторборат).
Подходящие растворители для осуществления способа Е1 не ограничены конкретным образом. Они могут быть обычными инертными органическими растворителями до тех пор, пока они не растворяют соединение для взаимодействия с ним или проявляют с ним какое-либо конкретное взаимодействие. Подходящими растворителями могут быть, например, растворители, описанные в связи со способом А1. Для осуществления способа А1. Для осуществления способа Е1, также может быть выгодно использовать в качестве катализатора кислоту Льюиса, такую как хлорид цинка (II). Для осуществления способа Е1, также может быть выгодно использовать катализаторы на основе переходных металлов, такие как палладиевые катализаторы. Для осуществления способа Е1, также может быть выгодно использовать соответствующий металлоорганический реагент, такой как н-бутиллитий. Для осуществления способа Е1 в соответствии с известным способом (WO 2020079205) также может быть выгодно использовать подходящее основание перед галогенированием, такое как н-бутиллитий, диизопропиламин лития, тетраметилпиперидид лития, бис(триметилсилил)амин лития, метиллитий или хлор-(2,2,6,6-тетраметил-1-пиперидил)магний и т.п., предпочтительно в безводных условиях. Необязательно можно использовать хлорид лития в предварительно приготовленной комбинации с этими реагентами.
Способ F1
Соединения формулы (Ii), как определено в настоящем документе, где R3 представляет собой галоген, циано, C1-С6-алкил или C1-С6-галоалкил, могут быть получены способом F1, включающим стадию проведения диазотирования соединение формулы (IX) или одну из его солей с последующим ароматическим замещением с получением соединения формулы (Ii), как показано на следующей схеме реакции:
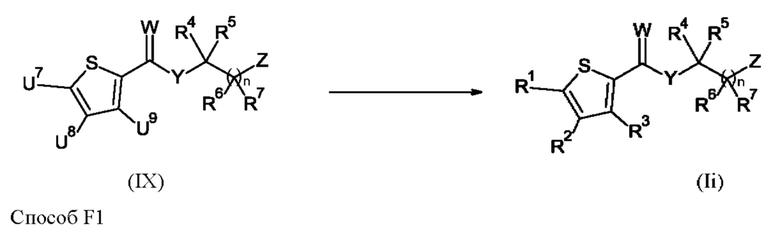
где U7, U8 и U9 независимо выбраны из перечня, состоящего из аминогруппы,
галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U7, U8 или U9 представляет собой по меньшей мере аминогруппу.
Способ F1 можно проводить в соответствии с известными способами (The Chemistry of diazonium and diazo groups; Saul Patai; Wiley-Interscience; 1978; 288-280 and 645-657; Account of Chemical Research (2018), 51, 496 и процитированные в них ссылки).
Соединения формулы (IX) или одна из их солей, как определено здесь, могут быть получены способом, включающим стадию восстановления нитрогруппы в соответствии с хорошо известными способами (Science of Synthesis: Catalytic Reduction in Organic Synthesis 2; J. G. de Vries, 2018, chapter 2.7: Reduction of Nitro Compounds to Amines, Azo Compounds, Hydroxylamines, and Oximes, and Reduction of N-Oxides to Amines, и ссылочные источники в них) или снятия защиты с защищенной аминогруппы в соответствии с известными методами.
Примеры защитных групп аминогруппы включают бензильную группу, 4-метоксибензильную группу, аллильную группу, незамещенный или замещенный C1-С6-алкилсульфонил, трифторметилсульфонил, незамещенный или замещенный фенилсульфонил, незамещенный или замещенный C1-С6-алококсикарбонил, незамещенный или замещенный бензилоксикарбонил, аллилоксикарбонил, ацетильную группу или трифторацетильную группу.
Процесс снятия защиты можно проводить в соответствии с известными способами удаления защитных групп (Greene's Protective Groups in Organic Synthesis; Peter G.M. Wuts; Wiley; Fifth Edition; 2014; 895-1194). Например, защитные группы третбутоксикарбонила и бензилоксикарбонила можно удалить в кислой среде (например, с помощью соляной кислоты или трифторуксусной кислоты). Бензильные защитные группы можно удалить гидрогенолитически водородом в присутствии катализатора (например, палладия на активированном угле). Трифторацетильную группу можно удалить щелочной средой (например, карбонатом калия или гидроксидом лития).
Соединения формулы (Ij), где Z представляет собой -C(=O)-ORa, где Ra выбран из группы, состоящей из C1-С6-алкила, C1-С6-галоалкила, C1-С6-цианоалкила, С2-С6-алкенила, С2-С6-алкинила, С3-С8-циклоалкила, арила, аралкила, 4-, 5- или 6-ти членного неароматического гетероциклила, -C1-С6-алкил-Si(C1-С6-алкила)3, -C1-С6-алкил-С3-С8-циклоалкила, 5-9-ти членного гетероарила и -C1-С6-алкил-5-9-ти членного гетероарила, могут быть получены из соединения формулы (Ik), где Z представляет собой -C(=O)-ORa, где Ra представляет собой водород и соответствующие спирты или одну из их солей, с помощью хорошо известного процесса сочетания в условиях, описанных в связи со способом А1.
Соединения формулы (Ik), где Z представляет собой -C(=O)-ORa, где Ra представляет собой водород, могут быть получены из соединения формулы (Ij), где Z представляет собой -C(=O)-ORa, где Ra выбран из группы, состоящей из C1-С6-алкила, C1-С6-галоалкила, C1-С6-цианоалкила, С2-С6-алкенила, С2-С6-алкинила, С3-С8-циклоалкила, арила, аралкила, 4-, 5- или 6-ти членного неароматического гетероциклила, -C1-С6-алкил-Si(C1-С6-алкила)3, -C1-С6-алкил-С3-С8-циклоалкила, 5-9-ти членного гетероарила и -C1-С6-алкил-5-9-ти членного гетероарила, хорошо известными способами, такими как гидролиз. Примеры реагентов гидролиза включают гидроксид лития, гидроксид калия, гидроксид натрия, гидроксид триметилолова. Гидролиз можно проводить, как описано в WO 2008157844; WO 2006002099; WO 20050256107; Angewandte Chemie, International Edition (2005), 44(9), 1378-1382.
Соединения формулы (Im), где Z представляет собой -C(=O)-SRa, -C(=O)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, могут быть получены из соединения формулы (Ik), где Z представляет собой -C(=O)-ORa, где Ra представляет собой водород, и соответствующие тиолы, амины или одну из их солей, с помощью хорошо известных способов сочетания в описанных условиях, в связи с процессом А1.
Способы получения соединений формулы (II)
Настоящее изобретение относится к способам получения соединений формулы (II). Соединения формулы (II) могут быть получены различными путями по аналогии с известными способами (см. ссылки в настоящем документе) и одним или несколькими из следующих способов синтеза, описанных в настоящем документе ниже и в экспериментальной части.
Общие синтетические пути получения соединений формулы (II) Настоящее изобретение относится к способам получения соединений формулы (II). Соединения формулы (II) могут быть получены различными путями по аналогии с известными способами, описанными в Beilstein Journal of Organic Chemistry (2007), 3, No. 23; WO 2008109786; Justus Liebigs Annalen der Chemie (1937), 532, 236-49; Justus Liebigs Annalen der Chemie (1938), 536, 135-42; WO 2017212010; WO 2012021696; WO 2003024961; Tetrahedron Letters (1997), 38(6), 1049-1052; WO 200302496; Journal of Agricultural and Food Chemistry (2007), 55(18), 7517-7526, WO 2020079205 и другие ссылки в нем, или одним или несколькими из следующих способов синтеза, описанных в настоящем документе ниже и в экспериментальной части.
Соединения формулы (II) могут быть получены различными путями, согласно способам, описанным ниже, в различных порядках.
Если не указано иное, далее R1, R2, R3 и А имеют те же значения, что и указанные выше для соединений формулы (II).
Способ А2
Соединения формулы (IIa), где R1 представляет собой C1-С3-алкил, (IIb) где R2 представляет собой C1-С3-алкил, и (IIc) где R3 представляет собой C1-С3-алкил, могут быть получен способом А2, который включает стадию взаимодействия соединения формулы (Ха), (Xb) или (Хс) или одной из его солей с соединением формулы (VIa), (VIb) или (VIc) или одной из его солей, как показано на следующей схеме реакции:
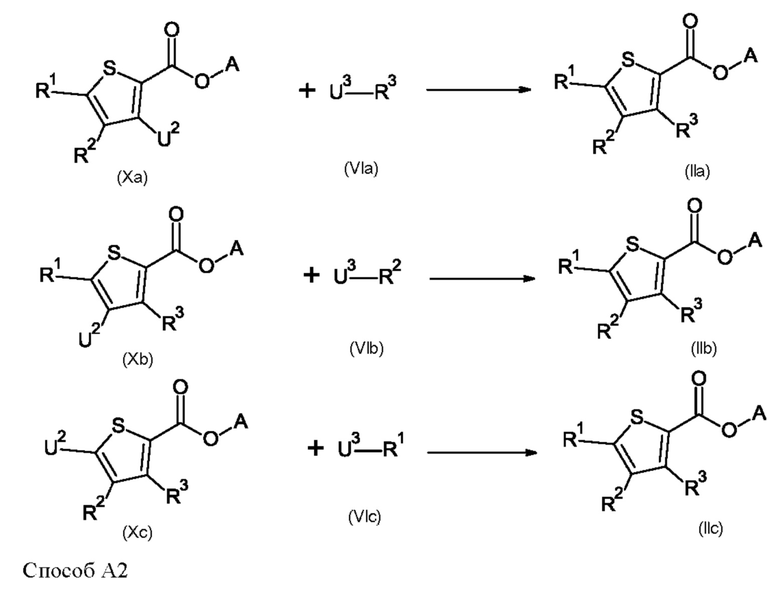
где U3 представляет собой производное бора, такое как бороновая кислота, производное сложного эфира бороновой кислоты, производное трифторбората калия или галогенометалл, который может образовывать комплексы с 1-2 лигандами, такими как галогеномагний или галогеноцинк,
и где:
для (Va), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу:
- R1 или R2 не представляет собой йод
- когда R1 или R2 представляет собой бром, U2 не представляет собой бром для (Vb), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу, при условии, что:
- R1 или R3 не представляет собой йод
-, когда R1 или R3 представляет собой бром, U2 не представляет собой бром для (Vc), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу при условии, что:
- R2 или R3 не представляет собой йод
-, когда R2 или R3 представляют собой бром, U2 не представляет собой бром.
Способ А2 можно проводить в присутствии катализатора на основе переходного металла, такого как палладий, и, при необходимости, в присутствии фосфинового лиганда или N-гетероциклического карбенового лиганда, при необходимости в присутствии основания и, при необходимости, в присутствии растворителя в соответствии с известными способами (WO 2012054721, Angew. Chem. Int. Ed. 2017, 56, 1581, Angew. Chem. Int. Ed. 2017, 56, 7078, и процитированные в них источники).
Способ А2 можно проводить в присутствии катализатора, такого как соль или комплекс металла. Подходящими для этой цели производными металлов являются катализаторы на основе переходных металлов, такие как палладий. Подходящими солями или комплексами металлов для этой цели являются, например, хлорид палладия, ацетат палладия, тетракис(трифенилфосфин)палладий(0), бис(дибензилиденацетон)палладий(0), трис(дибензилиденацетон)дипалладий(0), бис(трифенилфосфин)палладий(II) дихлорид, [1,1ў-бис(дифенилфосфино)ферроцен]дихлорпалладий(II), бис(циннамил)дихлордипалладий(II), бис(аллил)-дихлордипалладий(II), [1,1ў-бис(ди-трет-бутилфосфино)ферроцен]дихлорпалладий(II), ди-m-йодобис(три-трет-бутилфосфино)дипалладий(I) или ди-m-бромбис(три-трет-бутилфосфино)дипалладий(I).
Также возможно образование комплекса палладия в реакционной смеси путем раздельного добавления в реакцию соли палладия и лиганда или соли, такой как триэтилфосфин, три-трет-бутилфосфин, три-трет-бутилфосфония тетрафторборат, трициклогексилфосфин, 2-(дициклогексилфосфино)бифенил, 2-(ди-трет-бутилфосфино)бифенил, 2-(дициклогексилфосфино)-2ў-(N,N-диметиламино)бифенил, 2-(трет-бутилфосфино)-2ў-(N,N-диметиламино)бифенил, 2-ди-трет-бутилфосфино-2ў,4ў,6ў-триизопропилбифенил 2-дициклогексилфосфино-2ў,4ў,6ў-триизопропилбифенил, 2-дициклогексилфосфино-2,6ў-диметоксибифенил, 2-дициклогексилфосфино-2ў,4ў,6ў-триизопропилбифенил, дициклогексилфосфино-2ў,6ў-диизопропоксибифенил, трифенилфосфин, трис-(о-толил)фосфин, 3-(дифенилфосфино)бензолсульфонат натрия, трис-2-(метоксифенил)фосфин, 2,2ў-бис(дифенилфосфино)-1,1ў-бинафтил, 1,4-бис(дифенилфосфино)бутан, 1,2-бис(дифенилфосфино)этан, 1,4-бис(дициклогексилфосфино)бутан, 1,2-бис(дициклогексилфосфино)этан, 2-(дициклогексилфос фино)-2ў-(N,N-диметиламино)-бифенил, 1,1ў-бис(дифенилфосфино)-ферроцен, (R)-(-)-1-[(S)-2-дифенил-фосфино)ферроценил]этилдициклогексилфосфин, трис-(2,4-трет-бутилфенил)фосфит, ди(1-адамантил)-2-морфолинофенилфосфин или хлорид 1,3-бис(2,4,6-триметилфенил)имидазолия.
Также выгодно выбирать соответствующий катализатор и/или лиганд из коммерческих каталогов, таких как "Metal Catalysts for Organic Synthesis" от Strem Chemicals или "Phosphorous Ligands and Compounds" от Strem Chemicals.
Подходящими основаниями для проведения способа А2 могут быть неорганические и органические основания, обычные для таких реакций. Предпочтительно используют гидроксиды щелочноземельных или щелочных металлов, такие как гидроксид натрия, гидроксид кальция, гидроксид калия или другие производные гидроксида аммония; фториды щелочноземельных металлов, щелочных металлов или аммония, такие как фторид калия, фторид цезия или фторид тетрабутиламмония; карбонаты щелочноземельных или щелочных металлов, такие как карбонат натрия, карбонат калия, бикарбонат калия, бикарбонат натрия или карбонат цезия; ацетаты щелочных или щелочноземельных металлов, такие как ацетат натрия, ацетат лития, ацетат калия или ацетат кальция; фосфат щелочного металла или щелочноземельного металла, такой как трикалийфосфат щелочного металла; алкоголяты щелочных металлов, такие как трет-бутоксид калия или трет-бутоксид натрия; третичные амины, такие как триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-дициклогексилметиламин, N,N-диизопропилэтиламин, N-метилпиперидин, N,N-диметиламинопиридин, диазабициклооктан (DABCO), диазабициклононен (DBN) или диазабициклоундецен (DBU); а также ароматические основания, такие как пиридин, пиколины, лутидины или коллидины.
Подходящими растворителями для осуществления способа А2 могут быть обычные инертные органические растворители. Предпочтение отдается использованию необязательно атомизированных галогеном алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, пентан, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол или декалин; хлорбензол, дихлорбензол, дихлорметан, хлороформ, четыреххлористый углерод, дихлорэтан или трихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 2-метилтетрагидрофуран, 1,2-диметоксиэтан, 1,2-диэтоксиэтан или анизол; нитрилы, такие как ацетонитрил, пропионитрил, и- или изобутиронитрил или бензонитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; мочевины, такие как 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)-пиримидинон; сложные эфиры, такие как метилацетат или этилацетат, сульфоксиды, такие как диметилсульфоксид, или сульфоны, такие как сульфолан; и их смеси.
Также может быть выгодно проводить способ А2 с сорастворителем, таким как вода или спирт, такой как метанол, этанол, пропанол, изопропанол или трет-бутанол.
Способ А2 можно проводить в инертной атмосфере, такой как атмосфера аргона или азота. При проведении способа А1 моль или избыток соединения формулы (VIa), (VIb) или (VIc) и от 1 до 5 молей основания и от 0,01 до 20 мольных процентов комплекса палладия можно применять на моль соединения формулы (Ха), (Xb) или (Vc). Возможно также использование компонентов реакции в других соотношениях. Обработка осуществляется известными методами.
Соединения формулы (VIa), (VIb) или (VIc) имеются в продаже или могут быть получены хорошо известными способами.
Соединения формулы (Ха), (Xb) или (Хс) имеются в продаже или могут быть получены хорошо известными способами.
Способ В2
Соединения формулы (IId), где R1 представляет собой циано, (IIe) где R2 представляет собой циано, и (IIf) где R3 представляет собой циано, могут быть получены по способу В2, который включает стадию взаимодействия соединения формулы (Ха), (Xb) или (Хс) или одной из его солей с цианирующим реагентом в соответствии с известными способами (Chem. Rev. 1987, 87, 4, 779-794; Chem. Soc. Rev., 2011,40, 5049-5067; WO 2012123471 и процитированные в них источники).
Способ В2 можно проводить в присутствии катализатора на основе переходного металла, такого как соль или комплекс металла, и, при необходимости, в присутствии лиганда; при необходимости в присутствии основания и при необходимости в присутствии растворителя. Подходящими для этой цели производными металлов являются переходные металлы, такие как палладий или медь. Подходящие растворители для проведения способа В2 конкретно не ограничиваются. Они могут быть обычными инертными органическими растворителями до тех пор, пока они не растворяют соединение для взаимодействия с ним или проявляют какое-либо конкретное взаимодействие с ним. Подходящими растворителями могут быть, например, растворители, описанные в связи со способом А1. Примеры цианирующих агентов включают ферроцианид калия, цианид меди, цианид цинка, цианид натрия, цианид калия.
Способ С2
Соединения формулы (II), как определено в настоящем документе, могут быть получены способом С2 из соединения формулы (XI) или одной из его солей путем проведения реакции галогенирования, как показано на следующей схеме реакции:
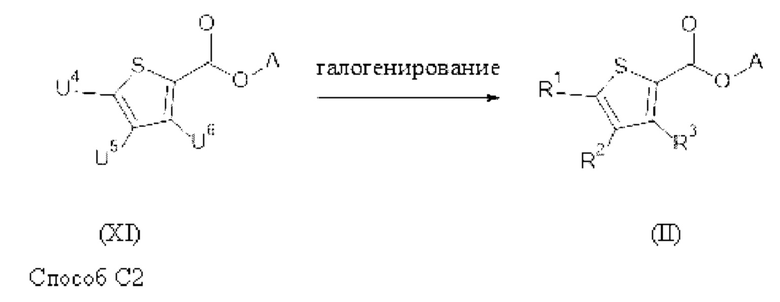
где U4, U5 и U6 независимо выбраны из перечня, состоящего из водорода, галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U4, U5 или U6 представляет собой по меньшей мере водород.
Способ С2 можно проводить согласно известным способам (Angewandte Chemie, International Edition, 52(16), 44404444; 2013; ACS Catalysis, 6(11), 7839-7843; 2016; Journal of the American Chemical Society, 2017, 139, 888; Angewandte Chemie, International Edition, 2014, 53, 7928; Journal of the American Chemical Society, 2018, 140, 2789; WO 2008156879; WO 2012114285; WO 2008109786; WO 2007098356).
Способ C2 осуществляют в присутствии галогенирующего агента и, при необходимости, в присутствии растворителя.
Подходящие галогенирующие агенты для осуществления способа Е1 конкретно не ограничены при условии, что они используются для бромирования, хлорирования, йодирования или фторирования. Примеры агентов бромирования включают бром, N-бромсукцинимид, 1,2-дибромтетрахлорэтан и 1,3-дибром-5,5-диметил-2,4-имидазолидиндион. Примеры агентов хлорирования включают N-хлорсукцинимид, сульфурилхлорид, гексахлорэтан и 1,3-дихлор-5,5-диметил-2,4-имидазолидиндион. Примеры йодирующих агентов включают йод, N-йодосукцинимид, хлорид йода и 1,3-дийод-5,5-диметил-2,4-имидазолидиндион. Примеры агентов фторирования включают N фторбензолсульф онимид и 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан-бис (тетрафторборат).
Подходящие растворители для осуществления способа С2 не ограничены конкретным образом. Они могут быть обычными инертными органическими растворителями до тех пор, пока они не растворяют соединение для взаимодействия с ним или проявляют с ним какое-либо конкретное взаимодействие. Подходящими растворителями могут быть, например, растворители, описанные в связи со способом А1. Для осуществления способа А1. Для осуществления способа С2, также может быть выгодно использовать в качестве катализатора кислоту Льюиса, такую как хлорид цинка(II). Для осуществления способа С2, также может быть выгодно использовать соответствующий металло органический реагент, такой как н-бутиллитий. Для осуществления способа С2 также может быть выгодно использовать катализаторы на основе переходных металлов, такие как палладиевые катализаторы.
Для осуществления способа С2 также может быть выгодно использовать соответствующий металло органический реагент, такой как н-бутиллитий. Для осуществления способа С2 в соответствии с известным способом (WO 2020079205) также может быть выгодно использовать подходящее основание перед галогенированием, такое как н-бутиллитий, диизопропиламин лития, тетраметилпиперидид лития, бис(триметилсилил)амин лития, метиллитий или хлор-(2,2,6,6-тетраметил-1-пиперидил)магний и т.п., предпочтительно в безводных условиях. Необязательно можно использовать хлорид лития в предварительно приготовленной комбинации с этими реагентами.
Способ D2
Соединения формулы (II), как определено в настоящем документе, могут быть получены способом D2, включающим стадию проведения диазотирования соединения формулы (XII) или одной из его солей с последующим ароматическим замещением с получением соединения формулы (II), как показано на следующей схеме реакции:
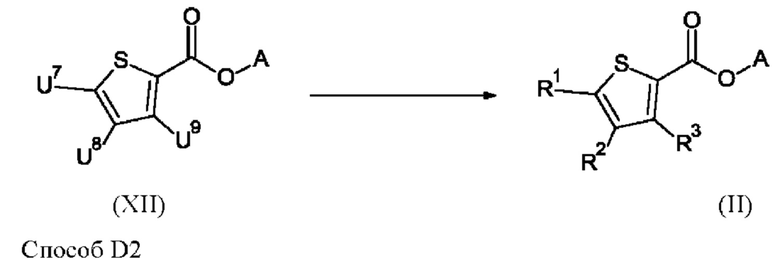
где U7, U8 и U9 независимо выбраны из перечня, состоящего из аминогруппы, галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U7, U8 или U9 представляет собой по меньшей мере аминогруппу.
Способ D2 можно проводить в соответствии с известными способами (The Chemistry of diazonium and diazo groups; Saul Patai; Wiley-Interscience; 1978; 288-280 and 645-657; Account of Chemical Research (2018), 51, 496 и процитированные в них источники; Journal of Medicinal Chemistry, 46(18), 3914-3929; 2003; WO 2012123471; Bioorganic & Medicinal Chemistry, 15(5), 2127-2146; 2007; WO 2016092556; Advanced Synthesis & Catalysis, 356(10), 2343-2348; 2014).
Соединения формулы (XII) или одна из их солей, как определено здесь, могут быть получены способом, включающим стадию восстановления нитрогруппы в соответствии с хорошо известными способами (Science of Synthesis: Catalytic Reduction in Organic Synthesis 2; J.G. de Vries, 2018, chapter 2.7: Reduction of Nitro Compounds to Amines, Azo Compounds, Hydroxylamines, and Oximes, and Reduction of N-Oxides to Amines, и ссылочные источники в них) или снятия защиты с защищенной аминогруппы в соответствии с известными методами.
Примеры защитных групп аминогруппы включают бензильную группу, 4-метоксибензильную группу, аллильную группу, незамещенный или замещенный C1-С6-алкилсульфонил, трифторметилсульфонил, незамещенный или замещенный фенилсульфонил, незамещенный или замещенный C1-С6-алококсикарбонил, незамещенный или замещенный бензилоксикарбонил, аллилоксикарбонил, ацетильную группу или трифторацетильную группу.
Процесс снятия защиты можно проводить в соответствии с известными способами удаления защитных групп (Greene's Protective Groups in Organic Synthesis; Peter G.M. Wuts; Wiley; Fifth Edition; 2014; 895-1194). Например, защитные группы третбутоксикарбонила и бензилоксикарбонила можно удалить в кислой среде (например, с помощью соляной кислоты или трифторуксусной кислоты). Бензильные защитные группы можно удалить гидрогенолитически водородом в присутствии катализатора (например, палладия на активированном угле). Трифторацетильную группу можно удалить щелочной средой (например, карбонатом калия или гидроксидом лития).
Способ Е2
Соединения формулы (IIg), как описано в настоящем документе, где R1, R2 или R3 представляют собой, по меньшей мере, соответственно C1-С3-дифторалкил или С1-С3-фторалкил, могут быть получены способом Е2, включающим стадию фторирования соответствующих соединений (XIII), как показано на следующей схеме реакции:
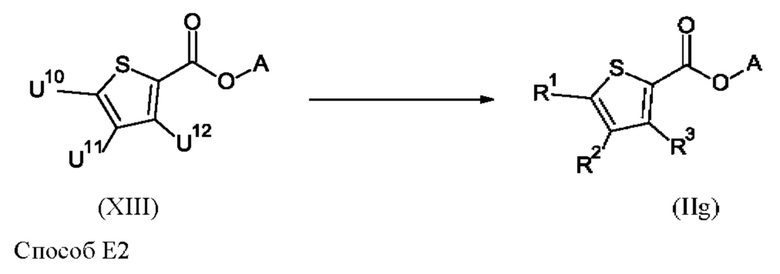
где U10, U11 и U12 независимо выбраны из группы, состоящей из соответственно C1-С3-оксоалкилалкила или C1-С3-гидроксиалкила, галогена, циано, C1-С3-алкила или С1-С3-галоалкила, при условии, что один из соответствующих U10, U11 или U12 представляет собой, по меньшей мере, соответственно C1-С3-оксоалкилалкил или C1-С3-гидроксиалкил.
Подходящие фторирующие агенты для осуществления способа Е2 конкретно не ограничены при условии, что они используются для фторирования. Примеры фторирующих агентов включают фториды серы, такие как тетрафторид серы, диэтиламиносеры трифторид, морфолиносеры трифторид, бис(2-метоксиэтил)аминосеры трифторид или 4-трет-бутил-2,6-диметилфенилсеру,
Способ Е2 может быть осуществлен, как описано в WO 1998042347; WO 2015005489; European Journal of Medicinal Chemistry, 159, 23-34; 2018.
Способ F2
Соединения формулы (II), как определено в настоящем документе, могут быть получены способом Е2, включающим стадию гидролиза соединений (XIV), как показано на следующей реакционной схеме:
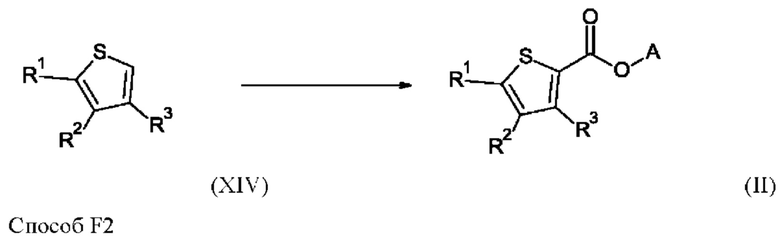
Способ F2 можно проводить как описано в них WO 2006086488; WO 2013170112; WO 2000021928; J. Org. Chem. 2019, 84, 16, 9869-9896; Comprehensive Organic Functional Group Transformations, Volume 5, 1995, chapter 5.02.1.2, Carbonation of Organometallic Reagents, 27-28 и ссылочных источниках в них.
Способ G2
Соединения формулы (Iih), как определено в настоящем документе, при условии,
что R1, R2 и R3 не являются циано, могут быть получены способом G2, включающим стадию гидролиза соответствующих соединений (XV), как показано на следующей реакционной схеме:
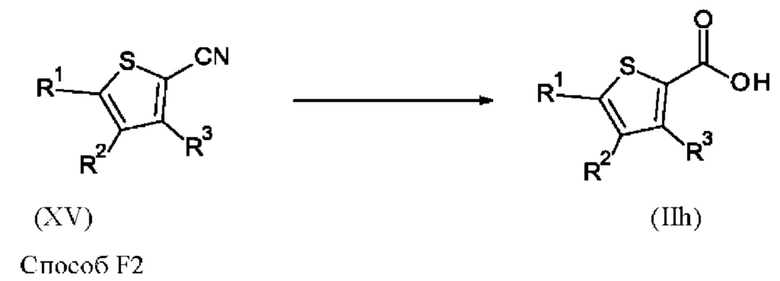
Способ G2 можно проводить, как описано в Beilstein Journal of Organic Chemistry, 3, No. 23, 2007; WO 2012075678.
Соединения формулы (XV) известны или могут быть получены известными способами.
Соединения формулы (IIi) где А представляет собой водород, могут быть получены из соединения формулы (IIj) где А представляет собой C1-С6-алкил, с помощью хорошо известных процессов, таких как гидролиз. Примеры реагентов гидролиза включают гидроксид лития, гидроксид калия, гидроксид натрия, гидроксид триметилолова. Гидролиз можно проводить, как описано в WO 2015043364; WO 2017212010; WO 2014140078; WO 2003024961; WO 2009154741; Angewandte Chemie, International Edition (2005), 44(9), 1378-1382.
Соединения формулы (IIj), где А представляет собой C1-С6-алкил, можно получить из соединения формулы (IIi), где А представляет собой водород, с помощью хорошо известных процессов, таких как этерификация. Такие способы могут быть выполнены, как описано в WO 2017202291; Chemical Communications (Cambridge, United Kingdom), 53(8), 1370-1373; 2017; WO 2010083145.
Способ Н2
Соединения формулы (IIi), как определено в настоящем документе, могут быть получены способом Н2, включающим стадию взаимодействия соединения (XVI), как определено в настоящем документе, и где М представляет собой щелочной металл, такой как литий, который может образовывать комплексы с 1-2 лигандами, или галогеномагний, который может образовывать комплекс от 1 до 2 лигандами с диоксидом углерода, как показано на следующей схеме реакции:
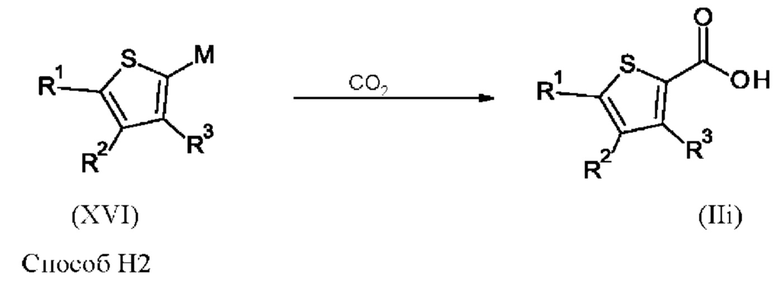
Способ I2
Соединения формулы (XVI), как определено в настоящем документе, могут быть получены способом Н2, включающим стадию металлирования соединения (XVII), где U13 выбирают из перечня, состоящего из хлора, брома или йода, как показано в следующей схеме:
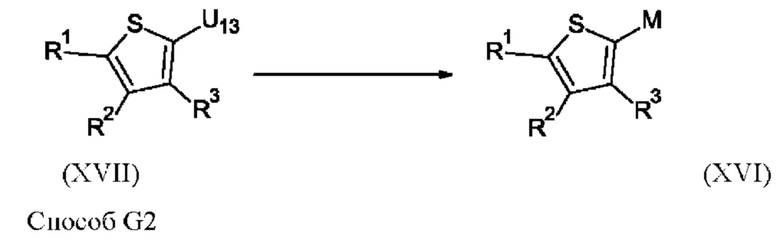
Способ I2 можно осуществлять с использованием металлического магния или металлического лития, или путем обмена галоген/металл с использованием алкиллитиевого реагента или реактива Гриньяра, или промышленного комплекса, полученного из алкиллитиевого реагента или реактива Гриньяра, предпочтительно в безводных условиях. Необязательно можно использовать хлорид лития в предварительно приготовленной комбинации с этими реагентами.
Способ I2 можно осуществлять, как описано в WO 2019209759, Angewandte Chemie, International Edition, 58(45), 16210-16216; 2019, New Journal of Chemistry, 41(19), 10929-10934; 2017, CN106518840, WO 2014090918 или WO 2013089087 и ссылочные источники в них.
Примеры алкиллитиевых реагентов, используемых в процессе литирования, включают метиллитий, фениллитий, н-бутиллитий, втор-бутиллитий, изобутиллитий, трет-бутиллитий и т.п.
Примеры реагентов Гриньяра, используемых в процессе комплексообразования магния, включают хлорид метилмагния, хлорид этилмагния, хлорид н-бутилмагния, хлорид изопропилмагния, хлор-(2,2,6,6-тетраметил-1-пиперидил)магний и т.п. Можно также использовать промышленный комплекс, полученный из хлорида н-бутилмагния и н-бутиллития.
Примеры лигандов, используемых в процессе литирования или в процессе комплексообразования магния, включают тетраметилэтилендиамин,
гексаметилфосфотриамид, (+) или (-)-спартеин или 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)-пиримидинон.
Растворитель, используемый в литировании или комплексообразовании магния, не ограничивается особым образом, пока он образует безводную реакционную систему без растворения соединения для взаимодействия с ним или проявления какого-либо конкретного взаимодействия с ним. Предпочтение отдается использованию негалогенированных алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, пентан, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол, декалин, ISOPAR (зарегистрированная торговая марка) Е или ISOPAR (зарегистрированная торговая марка) G; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 2-метилтетрагидрофуран, 1,2-диметоксиэтан или 1,2-диэтоксиэтан; и их смесь.
Цитирование или комплексообразование магния можно проводить в инертной атмосфере и готовить при температуре от 0°С до -78°С.
Соединения формулы (XVII) известны или могут быть получены известными способами.
Способ J2
Альтернативно, соединения формулы (XVI), как определено в настоящем документе, могут быть получены способом J2, включающим стадию металлирования соединения (XVIII), как показано на следующей реакционной схеме:
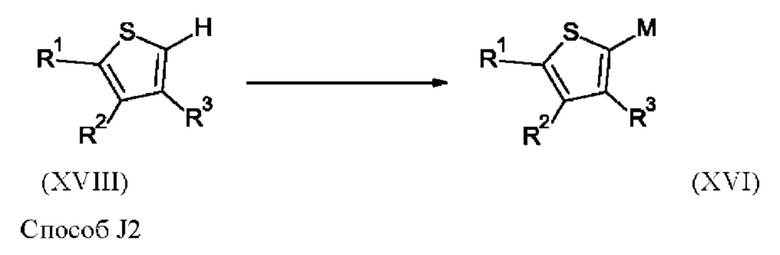
Способ J2 можно осуществлять с использованием основания, такого как н-бутиллитий, диизопропиламин лития, тетраметилпиперидид лития, бис(триметилсилил)амин лития, метиллитий или хлор-(2,2,6,6-тетраметил-1-пиперидил)магний и т.п., предпочтительно в безводных условиях. Необязательно можно использовать хлорид лития в предварительно приготовленной комбинации с этими реагентами.
Растворитель, используемый в реакции соединения (XVIII) с основанием, конкретно не ограничивается, пока он образует безводную реакционную систему без растворения соединения для взаимодействия с ним или проявления какого-либо конкретного взаимодействия с ним. Предпочтение отдается использованию негалогенированных алифатических, алициклических или ароматических углеводородов, таких как петролейный эфир, пентан, гексан, гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол, декалин, ISOPAR (зарегистрированная торговая марка) Е или ISOPAR (зарегистрированная торговая марка) G; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 2-метилтетрагидрофуран, 1,2-диметоксиэтан или 1,2-диэтоксиэтан; и их смесь.
Реакцию можно проводить в инертной атмосфере и готовить при температуре от 0°С до -78°С.
Способ J2 можно осуществлять, как описано в WO 2006086488; WO 2013170112; WO 2000021928; J. Org. Chem. 2019, 84, 16, 9869-9896; Comprehensive Organic Functional Group Transformations, Volume 5, 1995, chapter 5.02.1.2, Carbonation of Organometallic Reagents, 27-28 и ссылочные источники в них.
Соединения формулы (XVIII) известны или могут быть получены известными способами.
В качестве альтернативы, соединения формулы (IIj), где А представляет собой C1-С6-алкил, могут быть получены из соединений формулы (XVII) известными способами, такими как фото каталитическое карбоксилирование четырехбромистым углеродом и C1-С6-алкиловыми спиртами, такими как описано в Journal of Organic Chemistry, 84(16), 9869-9896; 2019 или прямое алкоксикарбонилирование посредством Cu-опосредованного трихлорметилирования и алкоголиза in situ, как описано в organic Letters, 22(5), 2093-2098; 2020, или металлирование с последующей реакцией с C1-С6-алкилхлорформиатом, как описано в MedChemComm, 9(3), 583-589; 2018.
Промежуточные соединения для получения соединения формулы (I)
Настоящее изобретение относится к промежуточным соединениям для получения соединений формулы (I)
Если не указано иное далее R1, R2, R3, R4, R5, R6, R7, n, W, Y и Z имеют значения, указанные выше для соединений формулы (I).
Соединения формул (Va), (Vb) и (Vc) предоставлены:
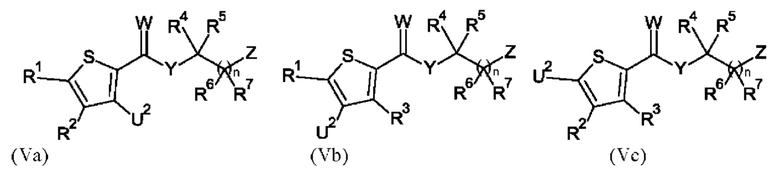
где
для (Va), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу:
- R1 или R2 не представляет собой йод
-, когда R1 или R2 представляет собой бром, U2 не представляет собой бром для (Vb), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу, при условии, что:
- R1 или R3 не представляет собой йод
-, когда R1 или R3 представляет собой бром, U2 не представляет собой бром для (Vc), U2 представляет собой бром, йод, мезилатную группу, тозилатную группу или трифлатную группу при условии, что:
- R2 или R3 не представляет собой йод
-, когда R2 или R3 представляют собой бром, U2 не представляет собой бром. Соединения формулы (VIII) предоставлены:
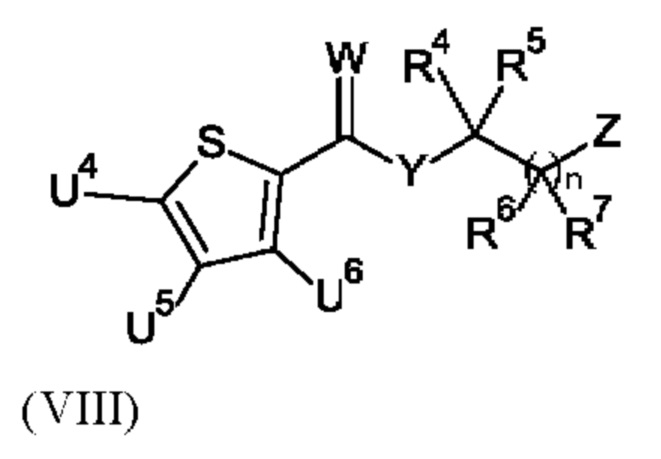
где U4, U5 и U6 независимо выбраны из группы, состоящей из водорода, галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U4, U5 или U6 представляет собой по меньшей мере водород.
Соединения формулы (IX) предоставлены:
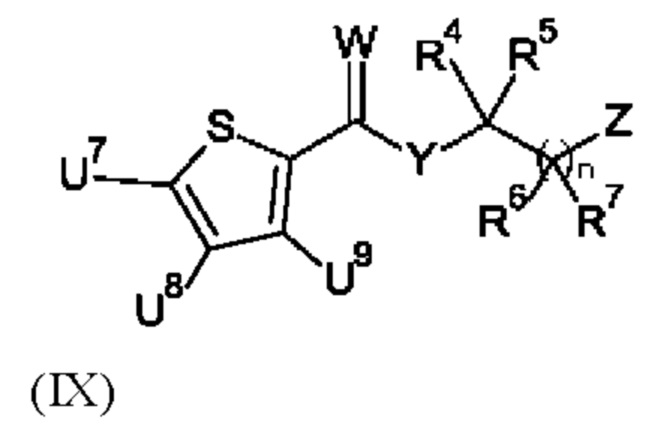
где U7, U8 и U9 независимо выбраны из группы, состоящей из аминогруппы, галогена, циано, C1-С6-алкила или C1-С6-галоалкила, при условии, что один из U7, U8 или U9 представляет собой по меньшей мере аминогруппу.
Композиции и составы
Настоящее изобретение, кроме того, относится к композиции, в частности композиции для борьбы с нежелательными микроорганизмами, содержащей одно или более соединений формулы (I) или (II). Композицией предпочтительно является фунгицидная композиция.
Композиция, как правило, содержит одно или более соединений формулы (I) или (II) и один или более приемлемых носителей, в частности один или более сельскохозяйственно приемлемых носителей.
Носитель представляет собой твердое или жидкое, природное или синтетическое, органическое или неорганическое вещество, которое в общем инертно. Носитель в общем улучшает нанесение соединений, например, на растения, части растений или семена. Примеры подходящих твердых носителей включают, но не ограничиваются ими, соли аммония, муку из природных горных пород, таких как каолины, глины, тальк, мел, кварц, аттапульгит, монтмориллонит и диатомитовая земля, а также муку из синтетических горных пород, таких как мелкодисперсный диоксид кремния, глинозем и силикаты. Примеры обычно используемых твердых носителей для приготовления гранул включают, но не ограничиваются ими, измельченные и фракционированные природные породы, такие как кальцит, мрамор, пемза, сепиолит и доломит, синтетические гранулы неорганической и органической муки и гранулы органического материала, такого как бумага, опилки, скорлупа кокоса, кукурузные початки и стебли табака. Примеры подходящих жидких носителей включают, но не ограничиваются ими, воду, органические растворители и их комбинации. Примеры подходящих растворителей включают полярные и неполярные органические химические жидкости, например, из классов ароматических и неароматических углеводородов (таких как циклогексан, парафины, алкилбензолы, ксилол, толуол, алкилнафталины, хлорированные ароматические соединения или хлорированные алифатические углеводороды, такие как хлорбензолы, хлорэтилены или метиленхлорид), спирты и полиолы (которые необязательно также могут быть замещены, этерифицированы и/или этерифицированы, такие как бутанол или гликоль), кетоны (такие как ацетон, метилэтилкетон, метилизобутилкетон или циклогексанон), сложные эфиры (включая жиры и масла) и простые (поли)эфиры, незамещенные и замещенные амины, амиды (такие как диметилформамид), лактамы (такие как N-алкилпирролидоны) и лактоны, сульфоны и сульфоксиды (такие как диметилсульфоксид). Носителем также может быть сжиженный газовый наполнитель, т.е. жидкость, которая является газообразной при стандартной температуре и стандартном давлении, например, аэрозольные пропелленты, такие как галогенуглеводороды, бутан, пропан, азот и диоксид углерода. Количество носителя обычно находится в диапазоне от 1 до 99,99 мас. %, предпочтительно от 5 до 99,9 мас. %, более предпочтительно от 10 до 99,5 мас. % и наиболее предпочтительно от 20 до 99 мас. % от композиции.
Композиция может дополнительно содержать одно или более приемлемых вспомогательных веществ, которые являются обычными для составления композиций (например, агрохимических композиций), такие как одно или более поверхностно-активные вещества.
Поверхностно-активное вещество может быть ионным (катионным или анионным) или неионным поверхностно-активным веществом, таким как ионный или неионный эмульгатор (эмульгаторы), пенообразователь (пенообразователи), диспергатор (диспергаторы), смачивающий агент (агенты) и любые их смеси. Примеры подходящих поверхностно-активных веществ включают, но не ограничиваются ими, соли полиакриловой кислоты, соли лигносульфоновой кислоты, соли фенолсульфоновой кислоты или нафталинсульфоновой кислоты, поликонденсаты этилена и/или пропиленоксида с жирными спиртами, жирными кислотами или жирными аминами (сложные эфиры полиоксиэтилена и жирных кислот, простые эфиры полиоксиэтилена и жирных спиртов, например алкиларилполигликолевые простые эфиры), замещенные фенолы (предпочтительно алкилфенолы или арилфенолы), соли сложных эфиров сульфоянтарной кислоты, производные таурина (предпочтительно алкилтаураты), сложные эфиры фосфорной кислоты и полиэтоксилированных спиртов или фенолов, жирные сложные эфиры полиолов и производные соединений, содержащие сульфаты, сульфонаты, фосфаты (например, алкилсульфонаты, ал кил сульфаты, арилсульфонаты) и гидролизаты белков, отработанные растворы лигносульфитов и метилцеллюлоза. Поверхностно-активное вещество обычно используют, когда соединение формулы (I) или (II) и/или носитель нерастворимы в воде, а нанесение проводят с водой. Затем количество поверхностно-активных веществ обычно составляет от 5 до 40 мас. % от композиции.
Другие примеры вспомогательных веществ, которые обычно используются для составления агрохимических композиций, включают водоотталкивающие средства, сиккативы, связующие (адгезив, повышающее клейкость средство, фиксирующий агент, такой как карбоксиметилцеллюлоза, природные и синтетические полимеры в форме порошков, гранул или латексов, такие как гуммиарабик, поливиниловый спирт и поливинилацетат, природные фосфолипиды, такие как цефалины и лецитины, и синтетические фосфолипиды, поливинилпирролидон, поливинилацетат, поливиниловый спирт и тилоза), загустители, стабилизаторы (например, холодные стабилизаторы, консерванты, антиоксиданты, светостабилизаторы или другие вещества, улучшающие химическую и/или физическую стабильность), красители или пигменты (например, неорганические пигменты, например, оксид железа, оксид титана и берлинская лазурь; органические красители, например, ализарин, азо и металлофталоцианиновые красители), пеногасители (например, силиконовые пеногасители и стеарат магния), консерванты (например, дихлорфен и полуформиаль бензилового спирта), вторичные загустители (производные целлюлозы, производные акриловой кислоты, ксантан, модифицированные глины и тонкоизмельченный диоксид кремния), клейкие вещества, гиббереллины и технологические вспомогательные вещества, минеральные и растительные масла, ароматизаторы, воски, питательные вещества (включая микроэлементы, такие как соли железа, марганца, бора, меди, кобальт, молибден и цинка), защитные коллоиды, тиксотропные вещества, пенетранты, связывающие агенты и комплексообразователи.
Выбор вспомогательных веществ зависит от предполагаемого способа применения соединения формулы (I) или (II) и/или от физических свойств. Кроме того, вспомогательные вещества могут быть выбраны для придания конкретных свойств (технических, физических и/или биологических свойств) композициям или формам применения, полученным из них. Выбор вспомогательных веществ может позволить адаптировать композиции для конкретных нужд.
Композиция согласно настоящему изобретению может быть в любой обычной форме, такой как растворы (например, водные растворы), эмульсии, смачиваемые порошки, суспензии на водной и масляной основе, порошки, пыли, пасты, растворимые порошки, растворимые гранулы, гранулы для разбрасывания, суспоэмульсионные концентраты, природные или синтетические продукты, пропитанные соединением согласно настоящему изобретению, удобрения, а также микрокапсулы в полимерных веществах. Соединение согласно настоящему изобретению может присутствовать в суспендированной, эмульгированной или растворенной форме.
Композиция согласно настоящему изобретению может быть предоставлена конечному пользователю в виде готовой к применению композиции, т.е. композиции можно наносить непосредственно на растения или семена с помощью подходящего устройства, такого как устройство для опрыскивания или опудривания. Альтернативно, композиции могут быть предоставлены конечному пользователю в форме концентратов, которые перед использованием необходимо разбавлять, предпочтительно водой.
Композиция согласно настоящему изобретению может быть приготовлена обычными способами, например, путем смешивания соединения формулы (I) или (II) с одним или более подходящими вспомогательными веществами, такими как раскрытые в настоящем документе выше.
Композиция согласно настоящему изобретению может содержать в общем от 0.01 до 99 мас. %, от 0.05 до 98 мас. %, предпочтительно от 0.1 до 95 мас. %, более предпочтительно от 0.5 до 90 мас. %, наиболее предпочтительно от 1 до 80 мас. % соединения формулы (I) или (II).
Соединение (соединения) и композиция (композиции) согласно настоящему изобретению может быть смешана с другими активными ингредиентами, такими как фунгициды, бактерициды, акарициды, нематициды, инсектициды, гербициды, удобрения, регуляторы роста, защитные средства или полухимические вещества. Это может позволить расширить спектр активности или предотвратить развитие резистентности. Примеры известных фунгицидов, инсектицидов, акарицидов, нематоцидов и бактерицидов раскрыты в the Pesticide Manual, 17th Edition.
Активные ингредиенты, указанные в настоящем документе под их общим названием, известны и описаны, например, в The Pesticide Manual (16th Ed. British Crop Protection Council) или могут быть найдены в Интернете (например, www.alanwood.net/pesticides).
Если соединение (А) или соединение (В) может присутствовать в таутомерной форме, такое соединение понимается здесь выше и ниже также как включающее, где применимо, соответствующие таутомерные формы, даже если они конкретно не упоминаются в каждом случае.
Примерами фунгицидов, которые могут быть смешаны с соединением формулы (I) или (II) и композицией согласно настоящему изобретению, являются:
1) Ингибиторы биосинтеза эргостерина, такие как, например, (1.001) ципроконазол, (1.002) дифеноконазол, (1.003) эпоксиконазол, (1.004) фенгексамид, (1.005) фенпропидин, (1.006) фенпропиморф, (1.007) фенпиразамин, (1.008) флуквинконазол, (1.009) флутриафол, (1.010) имазалил, (1.011) имазалил сульфат, (1.012) ипконазол, (1.013) метконазол, (1.014) миклобутанил, (1.015) паклобутразол, (1.016) прохлораз, (1.017) пропиконазол, (1.018) протиоконазол, (1.019) пиризоксазол, (1.020) Спирохамин, (1.021) тебуконазол, (1.022) тетраконазол, (1.023) триадименол, (1.024) тридеморф, (1.025) тритиконазол, (1.026) (1R,2S,5S)-5-(4-хлорбензил)-2-(хлорметил)-2-метил-1-(1Н-1,2,4-триазол-1-илметил)циклопентанол, (1.027) (1S,2R,5R)-5-(4-хлорбензил)-2-(хлорметил)-2-метил-1-(1Н-1,2,4-триазол-1-илметил)циклопентанол, (1.028) (2R)-2-(1-хлорциклопропил)-4-[(1R)-2,2-дихлорциклопропил]-1-(1Н-1,2,4-триазол-1-ил)бутан-2-ол (1.029) (2R)-2-(1-хлорциклопропил)-4-[(1S)-2,2-дихлорциклопропил]-1-(1Н-1,2,4-триазол-1-ил)бутан-2-ол, (1.030) (2R)-2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1H-1,2,4-триазол-1-ил)пропан-2-ол, (1.031) (2S)-2-(1-хлорциклопропил)-4-[(1Н)-2,2-дихлорциклопропил]-1-(1Н-1,2,4-триазол-1-ил)бутан-2-ол, (1.032) (2S)-2-(1-хлорциклопропил)-4-[(1S)-2,2-дихлорциклопропил]-1-(1H-1,2,4-триазол-1-ил)бутан-2-ол, (1.033) (2S)-2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1Н-1,2,4-триазол-1-ил)пропан-2-ол, (1.034) (R)-[3-(4-хлор-2-фторфенил)-5-(2,4-дифторфенил)-1,2-оксазол-4-ил](пиридин-3-ил)метанол, (1.035) (S)-[3-(4-хлор-2-фторфенил)-5-(2,4-дифторфенил)-1,2-оксазол-4-ил](пиридин-3-ил)метанол, (1.036) [3-(4-хлор-2-фторфенил)-5-(2,4-дифторфенил)-1,2-оксазол-4-ил](пиридин-3-ил)метанол, (1.037) 1-({(2R,4S)-2-[2-хлор-4-(4-хлорфенокси)фенил]-4-метил-1,3-диоксолан-2-ил}метил)-1Н-1,2,4-триазол, (1.038) 1-({(2S,4S)-2-[2-хлор-4-(4-хлорфенокси)фенил]-4-метил-1,3-диоксолан-2-ил}метил)-1Н-1,2,4-триазол, (1.039) 1-{[3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1Н-1,2,4-триазол-5-ил-тиоцианат, (1.040) 1-{[rel(2R,3R)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1Н-1,2,4-триазол-5-ил-тиоцианат, (1.041) 1-{[rel(2R,3S)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1H-1,2,4-триазол-5-ил-тиоцианат, (1.042) 2-[(2R,4R,5R)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.043) 2-[(2R,4R,5S)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.044) 2-[(2R,4S,5R)-l-(2,4-дихлорофенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.045) 2-[(2R,4S,5S)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.046) 2-[(2S,4R,5R)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.047) 2-[(2S,4R,5S)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.048) 2-[(2S,4S,5R)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.049) 2-[(2S,4S,5S)-1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.050) 2-[1-(2,4-дихлорфенил)-5-гидрокси-2,6,6-триметилгептан-4-ил]-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.051) 2-[2-хлор-4-(2,4-дихлорофенокси)фенил]-1-(1Н-1,2,4-триазол-1-ил)пропан-2-ол, (1.052) 2-[2-хлор-4-(4-хлорфенокси)фенил]-1-(1Н-1,2,4-триазол-1-ил)бутан-2-ол, (1.053) 2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1Н-1,2,4-триазол-1-ил)бутан-2-ол, (1.054) 2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1Н-1,2,4-триазол-1-ил)пентан-2-ол, (1.055) 2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1Н-1,2,4-триазол-1-ил)пропан-2-ол, (1.056) 2-{[3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.057) 2-{[rel(2R,3R)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.058) 2-{[rel(2R,3S)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-2,4-дигидро-3Н-1,2,4-триазол-3-тион, (1.059) 5-(4-хлорбензил)-2-(хлорметил)-2-метил-1-(1Н-1,2,4-триазол-1-илметил)циклопентанол, (1.060) 5-(аллилсульфанил)-1-{[3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1Н-1,2,4-триазол, (1.061) 5-(аллилсульфанил)-1-{[rel(2R,3R)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1Н-1,2,4-триазол, (1.062) 5-(аллилсульфанил)-1-{[rel(2R,3S)-3-(2-хлорфенил)-2-(2,4-дифторфенил)оксиран-2-ил]метил}-1Н-1,2,4-триазол, (1.063) Nў-(2,5-диметил-4-{[3-(1,1,2,2-тетрафторэтокси)фенил]сульфанил}фенил)-N-этил-N-метилимидоформамид, (1.064) Nў-(2,5-диметил-4-{[3-(2,2,2-трифторэтокси)фенил]сульфанил}фенил)-N-этил-N-метилимидоформамид, (1.065) Nў-(2,5-диметил-4-{[3-(2,2,3,3-тетрафторпропокси)фенил]сульфанил}фенил)-N-этил-N-метилимидоформамид, (1.066) Nў-(2,5-диметил-4-{[3-(пентафторэтокси)фенил]сульфанил}фенил)-N-этил-N-метилимидоформамид, (1.067) Nў-(2,5-диметил-4-{3-[(1,1,2,2-тетрафторэтил)сульфанил]фенокси}фенил)-N-этил-N-метилимидоформамид, (1.068) Nў-(2,5-диметил-4-{3-[(2,2,2-трифторэтил)сульфанил]фенокси}фенил)-N-этил-N-метилимидоформамид, (1.069) Nў-(2,5-диметил-4-{3-[(2,2,3,3-тетрафторпропил)сульфанил]фенокси}фенил)-N-этил-N-метилимидоформамид, (1.070) Nў-(2,5-диметил-4-{3-[(пентафторэтил)сульфанил]фенокси}фенил)-N-этил-N-метилимидоформамид, (1.071) Nў-(2,5-диметил-4-феноксифенил)-N-этил-N-метилимидоформамид, (1.072) Nў-(4-{[3-(дифторметокси)фенил]сульфанил}-2,5-диметилфенил)-N-этил-N-метилимидоформамид, (1.073) Nў-(4-{3-[(дифторметил)сульфанил]фенокси}-2,5-диметилфенил)-N-этил-N-метилимидоформамид, (1.074) Nў-[5-бром-6-(2,3-дигидро-1Н-инден-2-илокси)-2-метилпиридин-3-ил]-N-этил-N-метилимидоформамид, (1.075) Nў-{4-[(4,5-дихлор-1,3-тиазол-2-ил)окси]-2,5-диметилфенил}-N-этил-N-метилимидоформамид, (1.076) Nў-{5-Бром-6-[(1R)-1-(3,5-дифторофенил)этокси]-2-метилпиридин-3-ил}-N-этил-N-метилимидоформамид, (1.077) Nў-{5-бром-6-[(1S)-1-(3,5-дифторфенил)этокси]-2-метилпиридин-3-ил}-N-этил-N-метилимидоформамид, (1.078) N-{5-бром-6-[(цис-4-изопропилциклогексил)окси]-2-метилпиридин-3-ил}-N-этил-N-метилимидоформамид, (1.079) Nў-{5-бром-6-[(транс-4-изопропилциклогексил)окси]-2-метилпиридин-3-ил}-N-этил-N-метилимидоформамид, (1.080) Nў-{5-бром-6-[1-(3,5-дифторфенил)этокси]-2-метилпиридин-3-ил}-N-этил-N-метилимидоформамид, (1.081) ипфентрифлуконазол, (1.082) 2-[4-(4-хлорфенокси)-2-(трифторметил)фенил]-1-(1Н-1,2,4-триазол-1-ил)пропан-2-ол, (1.083) 2-[6-(4-бромфенокси)-2-(трифторметил)-3-пиридил]-1-(1,2,4-триазол-1-ил)пропан-2-ол, (1.084) 2-[6-(4-хлорфенокси)-2-(трифторметил)-3-пиридил]-1-(1,2,4-триазол-1-ил)пропан-2-ол, (1.085) 3-[2-(1-хлорциклопропил)-3-(3-хлор-2-фтор-фенил)-2-гидрокси-пропил]имидазол-4-карбонитрил, (1.086) 4-[[6-[rac-(2R)-2-(2,4-дифторфенил)-1,1-дифтор-2-гидрокси-3-(5-тиоксо-4Н-1,2,4-триазол-1-ил)пропил]-3-пиридил]окси]бензонитрил, (1.087) N-изопропил-Nў-[5-метокси-2-метил-4-(2,2,2-трифтор-1-гидрокси-1-фенилэтил)фенил]-N-метилимидоформамид, (1.088) N-{5-бром-2-метил-6-[(1-пропоксипропан-2-ил)окси]пиридин-3-ил}-N-этил-N-метилимидоформамид.
2) Ингибиторы комплекса I или II дыхательной цепи, такие как, например, (2.001) бензовиндифлупир, (2.002) биксафен, (2.003) боскалид, (2.004) карбоксин, (2.005) флуопирам, (2.006) флутоланил, (2.007) флуксапироксид, (2.008) фураметпир, (2.009) изофетамид, (2.010) изопирам (anti-эпимерный энантиомер 1R,4S,9S), (2.011) изопиразам (anti-эпимерный энантиомер 1S,4R,9R), (2.012) изопиразам (anti-эпимерный рацемат 1RS,4SR,9SR), (2.013) изопиразам (смесь syn-эпимерного рацемата 1RS,4SR,9RS и anti-эпимерного рацемата 1RS,4SR,9SR), (2.014) изопиразам (syn-эпимерный энантиомер 1R,4S,9R), (2.015) изопиразам (syn-эпимерный энантиомер 1S,4R,9S), (2.016) изопиразам (syn-эпимерный рацемат 1RS,4SR,9RS), (2.017) пенфлуфен, (2.018) пентиопирад, (2.019) пидифлуме-тофен, (2.020) пиразифлумид, (2.021) седаксан, (2.022) 1,3-диметил-N-(1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил)-1Н-пиразол-4-карбоксамид, (2.023) 1,3-диметил-N-[(3R)-1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил]-1Н-пиразол-4-карбоксамид, (2.024) 1,3-диметил-N-[(3S)-1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил]-1Н-пиразол-4-карбоксамид, (2.025) 1-метил-3-(трифторметил)-N-[2ў-(трифторметил)бифенил-2-ил]-1Н-пиразол-4-карбоксамид, (2.026) 2-фтор-6-(трифторометил)-N-(1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил)бензамид, (2.027) 3-(дифторметил)-1-метил-N-(1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил)-1Н-пиразол-4-карбоксамид, (2.028) инпирфлуксам, (2.029) 3-(дифторметил)-1-метил-N-[(3S)-1,1,3-триtriметил-2,3-дигидро-1Н-инден-4-ил]-1Н-пиразол-4-карбоксамид, (2.030) флуиндапир, (2.031) 3-(дифторметил)-N-[(3R)-7-фтор-1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил]-1-метил-1Н-пиразол-4-карбоксамид, (2.032) 3-(дифторметил)-N-[(3S)-7-фтор-1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил]-1-метил-1Н-пиразол-4-карбоксамид, (2.033) 5,8-дифтор-N-[2-(2-фтор-4-{[4-(трифторметил)пиридин-2-ил]окси}фенил)этил]хиназолин-4-амин, (2.034) N-(2-циклопентил-5-фторбензил)-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.035) N-(2-трет-бутил-5-метилбензил)-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1N-пиразол-4-карбоксамид, (2.036) N-(2-трет-бутилбензил)-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.037) N-(5-хлор-2-этилбензил)-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.038) изофлуципрам, (2.039) N-[(1R,4S)-9-(дихлорметилен)-1,2,3,4-тетрагидро-1,4-метанонафтален-5-ил]-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, (2.040) N-[(1S,4R)-9-(дихлорметилен)-1,2,3,4-тетрагидро-1,4-метанонафтален-5-ил]-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, (2.041) N-[1-(2,4-дихлорфенил)-1-метоксипропан-2-ил]-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, (2.042) N-[2-хлор-6-(трифторметил)бензил]-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1 N-пиразол-4-карбоксамид, (2.043) N-[3-хлор-2-фтор-6-(трифторметил)бензил]-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.044) N-[5-хлор-2-(трифторметил)бензил]-N-циклопропил-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.045) N-циклопропил-3-(дифторметил)-5-фтор-1-метил-N-[5-метил-2-(трифторметил)бензил]-1Н-пиразол-4-карбоксамид, (2.046) N-циклопропил-3-(дифторметил)-5-фтор-N-(2-фтор-6-изопропилбензил)-1-метил-1Н-пиразол-4-карбоксамид, (2.047) N-циклопропил-3-(дифторметил)-5-фтор-N-(2-изопропил-5-метилбензил)-1-метил-1Н-пиразол-4-карбоксамид, (2.048) N-циклопропил-3-(дифторметил)-5-фтор-N-(2-изопропилбензил)-1-метил-1Н-пиразол-4-саrbотиоамид, (2.049) N-циклопропил-3-(дифторометил)-5-фтор-N-(2-изопропилбензил)-1-метил-1Н-пиразол-4-карбоксамид, (2.050) N-циклопропил-3-(дифторметил)-5-фтор-N-(5-фтор-2-изопропилбензил)-1-метил-1Н-пиразол-4-карбоксамид, (2.051) N-циклопропил-3-(дифторметил)-N-(2-этил-4,5-диметилбензил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.052) N-циклопропил-3-(дифторметил)-N-(2-этил-5-фторбензил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.053) N-циклопропил-3-(дифторметил)-N-(2-этил-5-метилбензил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.054) N-циклопропил-N-(2-циклопропил-5-фторбензил)-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.055) N-циклопропил-N-(2-циклопропил-5-метил бензил)-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.056) N-циклопропил-N-(2-циклопропилбензил)-3-(дифторметил)-5-фтор-1-метил-1Н-пиразол-4-карбоксамид, (2.057) пирапропоин, (2.058) N-[rac-(1S,2S)-2-(2,4-дихлорфенил)циклобутил]-2-(трифторметил)никотинамид, (2.059) N-[(1S,2S)-2-(2,4-дихлорфенил)циклобутил]-2-(трифторметил)никотинамид.
3) Ингибиторы дыхания, действующие на комплекс III дыхательной цепи, например, (3.001) аметоктрадин, (3.002) амисулбром, (3.003) азокситробин, (3.004) коуметоксистробин, (3.005) коумоксистробин, (3.006) циазофамид, (3.007) ди-моксистробин, (3.008) эноксастробин, (3.009) фамоксадон, (3.010) фенамидон, (3.011) флуфеноксистробин, (3.012) флуоксастробин, (3.013) крезоксим-метил, (3.014) метоминостробин, (3.015) оризастробин, (3.016) пикоксистробин, (3.017) пираклостробин, (3.018) пираметостробин, (3.019) пираоксистробин, (3.020) три-флоксистробин (3.021) (2Е)-2-{2-[({[(1Е)-1-(3-{[(Е)-1-фтор-2-фенилвинил]окси}фенил)этилиден]амино}окси)метил]фенил}-2-(метоксиимино)-N-метилацетамид, (3.022) (2Е,3Z)-5-{[1-(4-хлорфенил)-1Н-пиразол-3-ил]окси}-2-(метоксиимино)-N,3-диметилпент-3-енамид, (3.023) (2R)-2-{2-[(2,5-диметилфенокси)метил]фенил}-2-метокси-N-метилацетамид, (3.024) (2S)-2-{2-[(2,5-диметилфенокси)метил]фенил}-2-метокси-N-метилацетамид, (3.025) фенпикоксамид, (3.026) мандестробин, (3.027) N-(3-этил-3,5,5 триметилциклогексил)-3-формамидо-2-гидроксибензамид, (3.028) (2Е,3Z)-5-{[1-(4-хлор-2-фторфенил)-1Н-пиразол-3-ил]окси}-2-(метоксиимино)-N,3-диметилпент-3-енамид, (3.029) метил {5-[3-(2,4-диметилфенил)-1Н-пиразол-1-ил]-2-метилбензил}карбамат, (3.030) метилтетрапрол, (3.031) флорилпикоксамид.
4) ингибитора митоза и клеточного деления, например, (4.001) карбендазим, (4.002) диэтофенкарб, (4.003) этабоксам, (4.004) флуопиколид, (4.005) пенцику-рон, (4.006) тиабендазол, (4.007) тиофанат-метил, (4.008) зоксамид, (4.009) пиридахлометил, (4.010) 3-хлор-5-(4-хлорфенил)-4-(2,6-дифторфенил)-6-метилпиридазин, (4.011) 3-хлор-5-(6-хлорпиридин-3-ил)-6-метил-4-(2,4,6-трифторфенил)пиридазин, (4.012) 4-(2-бром-4-фторфенил)-N-(2,6-дифторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.013) 4-(2-бром-4-фторфенил)-N-(2-бром-6-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.014) 4-(2-бром-4-фторфенил)-N-(2-бромфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.015) 4-(2-бром-4-фторфенил)-N-(2-хлор-6-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.016) 4-(2-бром-4-фторфенил)-N-(2-хлорфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.017) 4-(2-бром-4-фторфенил)-N-(2-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.018) 4-(2-хлор-4-фторфенил)-N-(2,6-дифторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.019) 4-(2-хлор-4-фторфенил)-N-(2-хлор-6-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.020) 4-(2-хлор-4-фторфенил)-N-(2-хлорфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.021) 4-(2-хлор-4-фторфенил)-N-(2-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.022) 4-(4-хлорфенил)-5-(2,6-дифторфенил)-3,6-диметилпиридазин, (4.023) N-(2-бром-6-фторфенил)-4-(2-хлор-4-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.024) N-(2-бромфенил)-4-(2-хлор-4-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.025) N-(4-хлор-2,6-дифторфенил)-4-(2-хлор-4-фторфенил)-1,3-диметил-1Н-пиразол-5-амин, (4.026) флуопимомид.
5) Соединения, имеющие мультинаправленную активность, например, (5.001) бордосская жидкость, (5.002) каптафол, (5.003) каптан, (5.004) хлорталонил, (5.005) гидроксид меди, (5.006) нафтенат меди, (5.007) оксид меди, (5.008) окси-хлорид меди, (5.009) меди(2+)-сульфат, (5.010) дитианон, (5.011) додин, (5.012) фолпет, (5.013) манкозеб, (5.014) манеб, (5.015) метирам, (5.016) метирам цинка, (5.017) оксин меди, (5.018) пропинеб, (5.019) сера и преараты серы, включая по-лисульфид кальция, (5.020) тирам, (5.021) зинб, (5.022) зирам, (5.023) 6-этил-5,7-диоксо-6,7-дигидро-5Н-пирроло[3ў,4ў:5,6][1,4]дитиино[2,3-с][1,2]тиазол-3-карбонитрил.
6) Соединения, которые способны вызвать защиту хозяина, например, (6.001) ацибензолар-8-метил, (6.002) изотианил, (6.003) пробеназол, (6.004) тиадинил.
7) Ингибиторы биосинтеза аминокислот и/или белков, такие как, например, (7.001) ципродинил, (7.002) касугамицин, (7.003) касугамицин гидрохлорид ги-дарт, (7.004) Окситетрациклин (7.005) пириметанил, (7.006) 3-(5-фтор-3,3,4,4-тетраметил-3,4-дигидроизохинолин-1-ил)хинолин.
(8) Ингибиторы продукции АТФ, такие как, например, (8.001) силтиофам.
9) Ингибиторы синтеза клеточных стенок, такие как, например, (9.001) бентиава-ликарб, (9.002) диметоморф, (9.003) флуморф, (9.004) ипроваликарб, (9.005) ман-дипропамид, (9.006) пириморф, (9.007) валифеналат, (9.008) (2Е)-3-(4-трет.-бутилфенил)-3-(2-хлорпиридин-4-ил)-1-(морфолин-4-ил)проп-2-ен-1-он, (9.009) (2Z)-3-(4-трет.-бутилфенил)-3-(2-хлорпиридин-4-ил)-1-(морфолин-4-ил)проп-2-ен-1-он.
10) Ингибиторы липидного и мембранного синтеза, такие как, например, (10.001) пропамокарб, (10.002) пропамокарб гидрохлорид, (10.003) токлофос-метил.
11) Ингибиторы биосинтеза меланина, например, (11.001) трициклазол, (11.002) толпрокарб.
12) Ингибиторы синтеза нуклеиновых кислот, такие как, например, (12.001) беналаксил, (12.002) беналаксил-М (киралаксил), (12.003) Металаксил, (12.004) Металаксил-М (мефеноксам).
13) Ингибиторы сигнальной трансдукции, такие как, например, (13.001) флудиоксонил, (13.002) ипродион, (13.003) процимидон, (13.004) проквиназид, (13.005) квиноксифен, (13.006) винклозолин.
14) Соединения, которые могут действовать в качестве разобщителей, например, (14.001) флуазинам, (14.002) мептилдинокап.
15) Дополнительные фунгициды, выбранные из группы, включающей (15.001) абсцизовую кислоту, (15.002) бентиазол, (15.003) бетоксазин, (15.004) капсимицин, (15.005) карвон, (15.006) хинометионат, (15.007) куфранеб, (15.008) цифлуфенамид, (15.009) цимоксанил, (15.010) ципросульфамид, (15.011) флутианил, (15.012) фосетил-алюминий, (15.013) фосетил-кальций, (15.014) фосетил-натрий, (15.015) метилизотиоцианат, (15.016) метрафенон, (15.017) милдиомицин, (15.018) натамицин, (15.019) диметилдитиокарбамат никеля, (15.020) нитротал-изопропил, (15.021) оксамокарб, (15.022) оксатиапипролин, (15.023) оксифентиин, (15.024) пентахлорфенол и его соли, (15.025) фосфористая кислота соли, (15.026) пропамокарб-фосетилат, (15.027) пириофенон (хлазафенон), (15.028) тебуфлохин, (15.029) теклофталам, (15.030) толнифанид, (15.031) 1-(4-{4-[(5R)-5-(2,6-дифторфенил)-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)-2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]этанон, (15.032) 1-(4-{4-[(5S)-5-(2,6-дифторфенил)-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)-2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]этанон, (15.033) 2-(6-бензилпиридин-2-ил)хиназолин, (15.034) дипиметитрон, (15.035) 2-[3,5-бис(дифторметил)-1Н-пиразол-1-ил]-1-[4-(4-{5-[2-(проп-2-ин-1-илокси)фенил]-4,5-дигидро-1,2-оксазол-3-ил}-1,3-тиазол-2-ил)пиперидин-1-ил]этанон, (15.036) 2-[3,5-бис(дифторметил)-1Н-пиразол-1-ил]-1-[4-(4-{5-[2-хлор-6-(проп-2-ин-1-илокси)фенил]-4,5-дигидро-1,2-оксазол-3-ил}-1,3-тиазол-2-ил)пиперидин-1-ил]этанон, (15.037) 2-[3,5-бис(дифторметил)-1Н-пиразол-1-ил]-1-[4-(4-{5-[2-фтор-6-(проп-2-ин-1-илокси)фенил]-4,5-дигидро-1,2-оксазол-3-ил}-1,3-тиазол-2-ил)пиперидин-1-ил]этанон, (15.038) 2-[6-(3-фтор-4-метоксифенил)-5-метилпиридин-2-ил]хиназолин, (15.039) 2-{(5R)-3-[2-(1-{[3,5-бис(дифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-4,5-дигидро-1,2-оксазол-5-ил}-3-хлорфенилметансульфонат, (15.040) 2-{(5S)-3-[2-(1-{[3,5-бис(дифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-4,5-дигидро-1,2-оксазол-5-ил}-3-хлорфенилметансульфонат, (15.041) ипфлуфенохин, (15.042) 2-{2-фтор-6-[(8-фтор-2-метилхинолин-3-ил)окси]фенил}пропан-2-ол, (15.043) флуоксапипролин, (15.044) 2-{3-[2-(1-{[3,5-бис(дифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-4,5-дигидро-1,2-оксазол-5-ил}фенилметансульфонат, (15.045) 2-фенилфенол и соли, (15.046) 3-(4,4,5-трифтор-3,3-диметил-3,4-дигидроизохинолин-1-ил)хинолин, (15.047) хинофумелин, (15.048) 4-амино-5-фторпиримидин-2-ол (таутомерная форма: 4-амино-5-фторпиримидин-2(1Н)-он), (15.049) 4-оксо-4-[(2-фенилэтил)амино]бутановая кислота, (15.050) 5-амино-1,3,4-тиадиазол-2-тиол, (15.051) 5-хлор-Nў-фенил-Nў-(проп-2-ин-1-ил)тиофен-2-сульфоногидразид, (15.052) 5-фтор-2-[(4-фторбензил)окси]пиримидин-4-амин, (15.053) 5-фтор-2-[(4-метилбензил)окси]пиримидин-4-амин, (15.054) 9-фтор-2,2-диметил-5-(хинолин-3-ил)-2,3-дигидро-1,4-бензоксазепин, (15.055) бут-3-ин-1-ил {6-[({[(Z)-(1-метил-1Н-тетразол-5-ил)(фенил)метилен]амино}окси)метил]пиридин-2-ил}карбамат, (15.056) этил (2Z)-3-амино-2-циано-3-фенилакрилат, (15.057) феназин-1-карбоновая кислота, (15.058) пропил 3,4,5-тригидроксибензоат, (15.059) хинолин-8-ол, (15.060) хинолин-8-олсульфат (2:1), (15.061) трет-бутил{6-[({[(1-метил-1Н-тетразол-5-ил)(фенил)метилен]амино}окси)метил]пиридин-2-ил}карбамат, (15.062) 5-фтор-4-имино-3-метил-1-[(4-метилфенил)сульфонил]-3,4-дигидропиримидин-2(1Н)-он, (15.063) аминопирифен, (15.064) (Nў-[2-хлор-4-(2-фторфенокси)-5-метилфенил]-N-этил-N-метилимидоформамид), (15.065) (Nў-(2-хлор-5-метил-4-феноксифенил)-N-этил-N-метилимидоформамид), (15.066) (2-{2-[(7,8-дифтор-2-метилхинолин-3-ил)окси]-6-фторфенил}пропан-2-ол), (15.067) (5-бром-1-(5,6-диметилпиридин-3-ил)-3,3-диметил-3,4-дигидроизохинолин), (15.068) (3-(4,4-дифтор-5,5-диметил-4,5-дигидротиено[2,3-с]пиридин-7-ил)хинолин), (15.069) (1-(4,5-диметил-1Н-бензимидазол-1-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин), (15.070) 8-фтор-3-(5-фтор-3,3-диметил-3,4-дигидроизохинолин-1-ил)хинолон, (15.071) 8-фтор-3-(5-фтор-3,3,4,4-тетраметил-3,4-дигидроизохинолин-1-ил)хинолон, (15.072) 3-(4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин-1-ил)-8-фторхинолин, (15.073) (N-метил-N-фенил-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид), (15.074) метил{4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил}карбамат, (15.075) (N-{4-[5-(трифторметил)-1,2,4-оксадиазол-3)-ил]бензил}циклопропанкарбоксамид), (15.076) N-метил-4-(5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.077) N-[(Е)-метоксииминометил]-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.078) N-[(Z)-метоксииминометил]-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.079) N-[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]циклопропанкарбоксамид, (15.080) N-(2-фторфенил)-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.081) 2,2-дифтор-N-метил-2-[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]ацетамид, (15.082) N-аллил-N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил)фенил]метил]ацетамид, (15.083) N-[(E)-N-метокси-С-метилкарбомидоил]-4-(5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.084) N-[(Z)-N-метокси-С-метилкарбомидоил]-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.085) N-аллил-N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пропанамид, (15.086) 4,4-диметил-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пирролидин-2-он, (15.087) N-метил-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензолкарботиоамид, (15.088) 5-метил-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пирролидин-2-он, (15.089) N-((2,3-дифтор-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]-3,3,3-трифторпропанамид, (15.090) 1-метокси-1-метил-3-[[4-[5-(триффторметил}-1,2,4-оксадиазол-3-ил]фенил]метил]мочевина, (15.091) 1,1-диэтил-3-[[4-[5-(трифторметил}-1,2,4-оксадиазол]-3-ил]фенил]метил]мочевина, (15.092) N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пропанамид, (15.093) N-метокси-N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]циклопропанкарбоксамид, (15.094) 1-метокси-3-метил-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]мочевина, (15.095) N-метокси-N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил)циклопропанкарбоксамид, (15.096) N,2-диметокси-N-[[4-[5-(трифторметил}-1,2,4-оксадиазол-3-ил]фенил]метил]пропанамид, (15.097) N-этил-2-метил-N-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил)фенил]метил]пропанамид, (15.098) 1-метокси-3-метил-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]мочевина, (15.099) 1,3-диметокси-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]мочевина, (15.100) 3-этил-1-метокси-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]мочевина, (15.101) 1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пиперидин-2-он, (15.102) 4,4-диметил-2-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]изооксазолидин-3-он, (15.103) 5,5-диметил-2-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]изоксазолидин-3-он, (15.104) 3,3-диметил-1-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]пиперидин-2-он, (15.105) 1-[[3-фтор-4-(5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]азепан-2-он, (15.106) 4,4-диметил-2-[[4-(5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]изоксазолидин-3-он, (15.107) 5,5-диметил-2-[[4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил]метил]изоксазолидин-3-он, (15.108) этил 1-{4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензил}-1Н-пиразол-4-карбоксилат, (15.109) N,N-диметил-1-{4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензил}-1Н-1,2,4-триазол-3-амин, (15.110) N-{2,3-дифтор-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензил}бутанамид, (15.111) N-(1-метилциклопропил)-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.112) N-(2,4-дифторфенил)-4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]бензамид, (15.113) 1-(5,6-диметилпиридин-3-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин, (15.114) 1-(6-(дифторметил)-5-метилпиридин-3-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин, (15.115) 1-(5-(фторметил)-6-метилпиридин-3-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин, (15.116) 1-(6-(дифторметил)-5-метоксипиридин-3-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин, (15.117) 4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенилдиметилкарбамат, (15.118) N-{4-[5-(трифторметил)-1,2,4-оксадиазол-3-ил]фенил}пропанамид, (15.119) 3-[2-(1-{[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-1,5-дигидро-2,4-бензодиоксепин-6-илметансульфонат, (15.120) 9-фтор-3-[2-(1-{[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-азол-4-ил]-1,5-дигидро-2,4-бензодиоксепин-6-ил метансульфонат, (15.121) 3-[2-(1-{[3,5-бис(дифторметил)-1 Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-1,5-дигидро-2,4-бензодиоксепин-6-ил метансульфонат, (15.122) 3-[2-(1-{[3,5-бис(дифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-1,3-тиазол-4-ил]-9-фтор-1,5-дигидро-2,4-бензодиоксепин-6-ил метансульфонат, (15.123) 1-(6,7-диметилпиразоло[1,5-а]пиридин-3-ил)-4,4-дифтор-3,3-диметил-3,4-дигидроизохинолин, (15.124) 8-фтор-N-(4,4,4-трифтор-2-метил-1-фенилбутан-2-ил)хинолин-3-карбоксамид, (15.125) 8-фтор-N-[(28)-4,4,4-трифтор-2-метил-1-фенилбутан-2-ил]хинолин-3-карбоксамид, (15.126) N-(2,4-диметил-1-фенилпентан-2-ил)-8-фторхинолин-3-карбоксамид и (15.127) N-[(28)-2,4-диметил-1-фенилпентан-2-ил]-8-фторхинолин-3-карбоксамид.
Все названные партнеры по смешиванию классов (1) - (15) могут, если это позволяют их функциональные группы, необязательно образовывать соли с подходящими основаниями или кислотами.
Другой аспект настоящего изобретения относится к одной или нескольким из следующих комбинаций соединений:
(1.0001)+(1.001), (1.0001)+(1.002), (1.0001)+(1.003), (1.0001)+(1.004), (1.0001)+(1.005), (1.0001)+(1.006), (1.0001)+(1.007), (1.0001)+(1.008), (1.0001)+(1.009), (1.0001)+(1.010), (1.0001)+(1.011), (1.0001)+(1.012), (1.0001)+(1.013), (1.0001)+(1.014), (1.0001)+(1.015), (1.0001)+(1.016), (1.0001)+(1.017), (1.0001)+(1.018), (1.0001)+(1.019), (1.0001)+(1.020), (1.0001)+(1.021), (1.0001)+(1.022), (1.0001)+(1.023), (1.0001)+(1.024), (1.0001)+(1.025), (1.0001)+(1.026), (1.0001)+(1.027), (1.0001)+(1.028), (1.0001)+(1.029), (1.0001)+(1.030), (1.0001)+(1.031), (1.0001)+(1.032), (1.0001)+(1.033), (1.0001)+(1.034), (1.0001)+(1.035), (1.0001)+(1.036), (1.0001)+(1.037), (1.0001)+(1.038), (1.0001)+(1.039), (1.0001)+(1.040), (1.0001)+(1.041), (1.0001)+(1.042), (1.0001)+(1.043), (1.0001)+(1.044), (1.0001)+(1.045), (1.0001)+(1.046), (1.0001)+(1.047), (1.0001)+(1.048), (1.0001)+(1.049), (1.0001)+(1.050), (1.0001)+(1.051), (1.0001)+(1.052), (1.0001)+(1.053), (1.0001)+(1.054), (1.0001)+(1.055), (1.0001)+(1.056), (1.0001)+(1.057), (1.0001)+(1.058), (1.0001)+(1.059), (1.0001)+(1.060), (1.0001)+(1.061), (1.0001)+(1.062), (1.0001)+(1.063), (1.0001)+(1.064), (1.0001)+(1.065), (1.0001)+(1.066), (1.0001)+(1.067), (1.0001)+(1.068), (1.0001)+(1.069), (1.0001)+(1.070), (1.0001)+(1.071), (1.0001)+(1.072), (1.0001)+(1.073), (1.0001)+(1.074), (1.0001)+(1.075), (1.0001)+(1.076), (1.0001)+(1.077), (1.0001)+(1.078), (1.0001)+(1.079), (1.0001)+(1.080), (1.0001)+(1.081), (1.0001)+(1.082), (1.0001)+(1.083), (1.0001)+(1.084), (1.0001)+(1.085), (1.0001)+(1.086), (1.0001)+(1.087), (1.0001)+(1.088), (1.0001)+(1.089), (1.0001)+(1.090), (1.0001)+(1.091), (1.0001)+(2.001), (1.0001)+(2.002), (1.0001)+(2.003), (1.0001)+(2.004), (1.0001)+(2.005), (1.0001)+(2.006), (1.0001)+(2.007), (1.0001)+(2.008), (1.0001)+(2.009), (1.0001)+(2.010), (1.0001)+(2.011), (1.0001)+(2.012), (1.0001)+(2.013), (1.0001)+(2.014), (1.0001)+(2.015), (1.0001)+(2.016), (1.0001)+(2.017), (1.0001)+(2.018), (1.0001)+(2.019), (1.0001)+(2.020), (1.0001)+(2.021), (1.0001)+(2.022), (1.0001)+(2.023), (1.0001)+(2.024), (1.0001)+(2.025), (1.0001)+(2.026), (1.0001)+(2.027), (1.0001)+(2.028), (1.0001)+(2.029), (1.0001)+(2.030), (1.0001)+(2.031), (1.0001)+(2.032), (1.0001)+(2.033), (1.0001)+(2.034), (1.0001)+(2.035), (1.0001)+(2.036), (1.0001)+(2.037), (1.0001)+(2.038), (1.0001)+(2.039), (1.0001)+(2.040), (1.0001)+(2.041), (1.0001)+(2.042), (1.0001)+(2.043), (1.0001)+(2.044), (1.0001)+(2.045), (1.0001)+(2.046), (1.0001)+(2.047), (1.0001)+(2.048), (1.0001)+(2.049), (1.0001)+(2.050), (1.0001)+(2.051), (1.0001)+(2.052), (1.0001)+(2.053), (1.0001)+(2.054), (1.0001)+(2.055), (1.0001)+(2.056), (1.0001)+(2.057), (1.0001)+(2.058), (1.0001)+(2.059), (1.0001)+(3.001), (1.0001)+(3.002), (1.0001)+(3.003), (1.0001)+(3.004), (1.0001)+(3.005), (1.0001)+(3.006), (1.0001)+(3.007), (1.0001)+(3.008), (1.0001)+(3.009), (1.0001)+(3.010), (1.0001)+(3.011), (1.0001)+(3.012), (1.0001)+(3.013), (1.0001)+(3.014), (1.0001)+(3.015), (1.0001)+(3.016), (1.0001)+(3.017), (1.0001)+(3.018), (1.0001)+(3.019), (1.0001)+(3.020), (1.0001)+(3.021), (1.0001)+(3.022), (1.0001)+(3.023), (1.0001)+(3.024), (1.0001)+(3.025), (1.0001)+(3.026), (1.0001)+(3.027), (1.0001)+(3.028), (1.0001)+(3.029), (1.0001)+(3.030), (1.0001)+(3.031), (1.0001)+(4.001), (1.0001)+(4.002), (1.0001)+(4.003), (1.0001)+(4.004), (1.0001)+(4.005), (1.0001)+(4.006), (1.0001)+(4.007), (1.0001)+(4.008), (1.0001)+(4.009), (1.0001)+(4.010), (1.0001)+(4.011), (1.0001)+(4.012), (1.0001)+(4.013), (1.0001)+(4.014), (1.0001)+(4.015), (1.0001)+(4.016), (1.0001)+(4.017), (1.0001)+(4.018), (1.0001)+(4.019), (1.0001)+(4.020), (1.0001)+(4.021), (1.0001)+(4.022), (1.0001)+(4.023), (1.0001)+(4.024), (1.0001)+(4.025), (1.0001)+(4.026), (1.0001)+(5.001), (1.0001)+(5.002), (1.0001)+(5.003), (1.0001)+(5.004), (1.0001)+(5.005), (1.0001)+(5.006), (1.0001)+(5.007), (1.0001)+(5.008), (1.0001)+(5.009), (1.0001)+(5.010), (1.0001)+(5.011), (1.0001)+(5.012), (1.0001)+(5.013), (1.0001)+(5.014), (1.0001)+(5.015), (1.0001)+(5.016), (1.0001)+(5.017), (1.0001)+(5.018), (1.0001)+(5.019), (1.0001)+(5.020), (1.0001)+(5.021), (1.0001)+(5.022), (1.0001)+(5.023), (1.0001)+(6.001), (1.0001)+(6.002), (1.0001)+(6.003), (1.0001)+(6.004), (1.0001)+(7.001), (1.0001)+(7.002), (1.0001)+(7.003), (1.0001)+(7.004), (1.0001)+(7.005), (1.0001)+(7.006), (1.0001)+(8.001), (1.0001)+(9.001), (1.0001)+(9.002), (1.0001)+(9.003), (1.0001)+(9.004), (1.0001)+(9.005), (1.0001)+(9.006), (1.0001)+(9.007), (1.0001)+(9.008), (1.0001)+(9.009), (1.0001)+(10.001), (1.0001)+(10.002), (1.0001)+(10.003), (1.0001)+(11.001), (1.0001)+(11.002), (1.0001)+(12.001), (1.0001)+(12.002), (1.0001)+(12.003), (1.0001)+(12.004), (1.0001)+(13.001), (1.0001)+(13.002), (1.0001)+(13.003), (1.0001)+(13.004), (1.0001)+(13.005), (1.0001)+(13.006), (1.0001)+(14.001), (1.0001)+(14.002), (1.0001)+(15.001), (1.0001)+(15.002), (1.0001)+(15.003), (1.0001)+(15.004), (1.0001)+(15.005), (1.0001)+(15.006), (1.0001)+(15.007), (1.0001)+(15.008), (1.0001)+(15.009), (1.0001)+(15.010), (1.0001)+(15.011), (1.0001)+(15.012), (1.0001)+(15.013), (1.0001)+(15.014), (1.0001)+(15.015), (1.0001)+(15.016), (1.0001)+(15.017), (1.0001)+(15.018), (1.0001)+(15.019), (1.0001)+(15.020), (1.0001)+(15.021), (1.0001)+(15.022), (1.0001)+(15.023), (1.0001)+(15.024), (1.0001)+(15.025), (1.0001)+(15.026), (1.0001)+(15.027), (1.0001)+(15.028), (1.0001)+(15.029), (1.0001)+(15.030), (1.0001)+(15.031), (1.0001)+(15.032), (1.0001)+(15.033), (1.0001)+(15.034), (1.0001)+(15.035), (1.0001)+(15.036), (1.0001)+(15.037), (1.0001)+(15.038), (1.0001)+(15.039), (1.0001)+(15.040), (1.0001)+(15.041), (1.0001)+(15.042), (1.0001)+(15.043), (1.0001)+(15.044), (1.0001)+(15.045), (1.0001)+(15.046), (1.0001)+(15.047), (1.0001)+(15.048), (1.0001)+(15.049), (1.0001)+(15.050), (1.0001)+(15.051), (1.0001)+(15.052), (1.0001)+(15.053), (1.0001)+(15.054), (1.0001)+(15.055), (1.0001)+(15.056), (1.0001)+(15.057), (1.0001)+(15.058), (1.0001)+(15.059), (1.0001)+(15.060), (1.0001)+(15.061), (1.0001)+(15.062). (1.0001)+(15.063). (1.0001)+(15.064). (1.0001)+(15.065), (1.0001)+15.066), (1.0001)+(15.067), (1.0001)+(15.068), (1.0001)+(15.069), (1.0001)+(15.070), (1.0001)+(15.071), (1.0001)+(15.072), (1.0001)+(15.073), (1.0001)+(15.074), (1.0001)+(15.075), (1.0001)+(15.076), (1.0001), (1.0001)+(15.077), (1.0001)+(15.078), (1.0001)+(15.079), (1.0001)+(15. 080), (1.0001)+(15.081), (1.0001)+(15.082), (1.0001)+(15.083), (1.0001)+(15.084), (1.0001)+(15.085), (1.0001)+(15.086), (1.0001)+(15.087), (1.0001)+(15.088), (1.0001)+(15.089), (1.0001)+(15.090), (1.0001)+(15.091), (1.0001)+(15.092), (1.0001)+(15.093), (1.0001)+(15.094), (1.0001)+(15.095), (1.0001)+(15.096), (1.0001)+(15.097), (1.0001)+(15.098), (1.0001)+(15.099), (1.0001)+(15.100), (1.0001)+(15.101), (1.0001)+(15.102), (1.0001)+(15.103), (1.0001)+(15.104), (1.0001)+(15.105), (1.0001)+(15.106), (1.0001)+(15.107), (1.0001)+(15.108), (1.0001)+(15.109), (1.0001)+(15.110), (1.0001)+(15.111), (1.0001)+(15.112), (1.0001)+(15.113), (1.0001)+(15.114), (1.0001)+(15.115), (1.0001)+(15.116), (1.0001)+(15.117), (1.0001)+(15.118), (1.0001)+(15.119), (1.0001)+(15.120), (1.0001)+(15.121), (1.0001)+(15.122), (1.0001)+(15.123), (1.0001)+(15.124), (1.0001)+(15.125), (1.0001)+(15.126), (1.0001)+(15.127).
В этих комбинациях первый компонент представляет собой соединение формулы (I), как определено в таблицах 1.1 и 1.2 (например, 1.001), а второй компонент представляет собой фунгицид, выбранный из групп 1-15, как определено в настоящем документе. Например, комбинация (1.001)+(1.001) соответствует комбинации, содержащей соединение 1.001 в таблицах 1.1 и 1.2 ципроконазол (1.001).
В некоторых других вариантах осуществления комбинации соединений соответствуют описанным выше комбинациям, в которых соединение (1.001) заменено любым из соединений, перечисленных в таблицах 1.1 и 1.2.
Соединения формулы (I) и фунгицид, выбранный из групп (1)-(15), могут присутствовать при массовом соотношении от 100:1 до 1:100 (соединение формулы (I): фунгицид, выбранный из группы (1)-(15)), или в пределах от 50:1 до 1:50, или в пределах от 20:1 до 1:20. Другие примеры диапазонов весового соотношения включают от 95:1 до 1:95, от 90:1 до 1:90, от 85:1 до 1:85, от 80:1 до 1:80, от 75:1 до 1:75, 70:1. до 1:70, 65:1 до 1:65, 60:1 до 1:60, 55:1 до 1:55, 45:1 до 1:45, 40:1 до 1:40, 35:1 до 1:35, 30:1 до 1:30, 25:1 до 1:25, 15:1 до 1:15, 10:1 до 1:10, 5:1 до 1:5, 4:1 до 1:4, от 3:1 до 1:3, от 2:1 до 1:2.
К комбинациям соединений может быть добавлен дополнительный фунгицид, выбранный из групп 1-15, как определено в настоящем документе.
Другой аспект настоящего изобретения относится к одной или нескольким из следующих комбинаций соединений:
(11.001)+(1.001), (11.001)+(1.002), (11.001)+(1.003), (11.001)+(1.004), (11.001)+(1.005), (11.001)+(1.006), (11.001)+(1.007), (11.001)+(1.008), (11.001)+(1.009), (11.001)+(1.010), (11.001)+(1.011), (11.001)+(1.012), (11.001)+(1.013), (11.001)+(1.014), (11.001)+(1.015), (11.001)+(1.016), (11.001)+(1.017), (11.001)+(1.018), (11.001)+(1.019), (11.001)+(1.020), (11.001)+(1.021), (11.001)+(1.022), (11.001)+(1.023), (11.001)+(1.024), (11.001)+(1.025), (11.001)+(1.026), (11.001)+(1.027), (11.001)+(1.028), (11.001)+(1.029), (11.001)+(1.030), (11.001)+(1.031), (11.001)+(1.032), (11.001)+(1.033), (11.001)+(1.034), (11.001)+(1.035), (11.001)+(1.036), (11.001)+(1.037), (11.001)+(1.038), (11.001)+(1.039), (11.001)+(1.040), (11.001)+(1.041), (11.001)+(1.042), (11.001)+(1.043), (11.001)+(1.044), (11.001)+(1.045), (11.001)+(1.046), (11.001)+(1.047), (11.001)+(1.048), (11.001)+(1.049), (11.001)+(1.050), (11.001)+(1.051), (11.001)+(1.052), (11.001)+(1.053), (11.001)+(1.054), (11.001)+(1.055), (11.001)+(1.056), (11.001)+(1.057), (11.001)+(1.058), (11.001)+(1.059), (11.001)+(1.060), (11.001)+(1.061), (11.001)+(1.062), (11.001)+(1.063), (11.001)+(1.064), (11.001)+(1.065), (11.001)+(1.066), (11.001)+(1.067), (11.001)+(1.068), (11.001)+(1.069), (11.001)+(1.070), (11.001)+(1.071), (11.001)+(1.072), (11.001)+(1.073), (11.001)+(1.074), (11.001)+(1.075), (11.001)+(1.076), (11.001)+(1.077), (11.001)+(1.078), (11.001)+(1.079), (11.001)+(1.080), (11.001)+(1.081), (11.001)+(1.082), (11.001)+(1.083), (11.001)+(1.084), (11.001)+(1.085), (11.001)+(1.086), (11.001)+(1.087), (11.001)+(1.088), (11.001)+(1.089), (11.001)+(1.090), (11.001)+(1.091), (11.001)+(2.001), (11.001)+(2.002), (11.001)+(2.003), (11.001)+(2.004), (11.001)+(2.005), (11.001)+(2.006), (11.001)+(2.007), (11.001)+(2.008), (11.001)+(2.009), (11.001)+(2.010), (11.001)+(2.011), (11.001)+(2.012), (11.001)+(2.013), (11.001)+(2.014), (11.001)+(2.015), (11.001)+(2.016), (11.001)+(2.017), (11.001)+(2.018), (11.001)+(2.019), (1.001)+(2.020), (1.001)+(2.021), (1.001)+(2.022), (1.001)+(2.023), (1.001)+(2.024), (1.001)+(2.025), (1.001)+(2.026), (11.001)+(2.027), (11.001)+(2.028), (11.001)+(2.029), (11.001)+(2.030), (11.001)+(2.031), (11.001)+(2.032), (11.001)+(2.033), (11.001)+(2.034), (11.001)+(2.035), (11.001)+(2.036), (11.001)+(2.037), (11.001)+(2.038), (11.001)+(2.039), (11.001)+(2.040), (11.001)+(2.041), (11.001)+(2.042), (11.001)+(2.043), (11.001)+(2.044), (11.001)+(2.045), (11.001)+(2.046), (11.001)+(2.047), (11.001)+(2.048), (11.001)+(2.049), (11.001)+(2.050), (11.001)+(2.051), (11.001)+(2.052), (11.001)+(2.053), (11.001)+(2.054), (11.001)+(2.055), (11.001)+(2.056), (11.001)+(2.057), (11.001)+(2.058), (11.001)+(2.059), (11.001)+(3.001), (11.001)+(3.002), (11.001)+(3.003), (11.001)+(3.004), (11.001)+(3.005), (11.001)+(3.006), (11.001)+(3.007), (11.001)+(3.008), (11.001)+(3.009), (11.001)+(3.010), (11.001)+(3.011), (11.001)+(3.012), (11.001)+(3.013), (11.001)+(3.014), (11.001)+(3.015), (11.001)+(3.016), (11.001)+(3.017), (11.001)+(3.018), (11.001)+(3.019), (11.001)+(3.020), (11.001)+(3.021), (11.001)+(3.022), (11.001)+(3.023), (11.001)+(3.024), (11.001)+(3.025), (11.001)+(3.026), (11.001)+(3.027), (11.001)+(3.028), (11.001)+(3.029), (11.001)+(3.030), (11.001)+(3.031), (11.001)+(4.001), (11.001)+(4.002), (11.001)+(4.003), (11.001)+(4.004), (11.001)+(4.005), (11.001)+(4.006), (11.001)+(4.007), (11.001)+(4.008), (11.001)+(4.009), (11.001)+(4.010), (11.001)+(4.011), (11.001)+(4.012), (11.001)+(4.013), (11.001)+(4.014), (11.001)+(4.015), (11.001)+(4.016), (11.001)+(4.017), (11.001)+(4.018), (11.001)+(4.019), (11.001)+(4.020), (11.001)+(4.021), (11.001)+(4.022), (11.001)+(4.023), (11.001)+(4.024), (11.001)+(4.025), (11.001)+(4.026), (11.001)+(5.001), (11.001)+(5.002), (11.001)+(5.003), (11.001)+(5.004), (11.001)+(5.005), (11.001)+(5.006), (11.001)+(5.007), (11.001)+(5.008), (11.001)+(5.009), (11.001)+(5.010), (11.001)+(5.011), (11.001)+(5.012), (11.001)+(5.013), (11.001)+(5.014), (11.001)+(5.015), (11.001)+(5.016), (11.001)+(5.017), (11.001)+(5.018), (11.001)+(5.019), (11.001)+(5.020), (11.001)+(5.021), (11.001)+(5.022), (11.001)+(5.023), (11.001)+(6.001), (11.001)+(6.002), (11.001)+(6.003), (11.001)+(6.004), (11.001)+(7.001), (11.001)+(7.002), (11.001)+(7.003), (11.001)+(7.004), (11.001)+(7.005), (11.001)+(7.006), (11.001)+(8.001), (11.001)+(9.001), (11.001)+(9.002), (11.001)+(9.003), (11.001)+(9.004), (11.001)+(9.005), (11.001)+(9.006), (11.001)+(9.007), (11.001)+(9.008), (11.001)+(9.009), (11.001)+(10.001), (11.001)+(10.002), (11.001)+(10.003), (11.001)+(11.001), (11.001)+(11.002), (11.001)+(12.001), (11.001)+(12.002), (11.001)+(12.003), (11.001)+(12.004), (11.001)+(13.001), (11.001)+(13.002), (11.001)+(13.003), (11.001)+(13.004), (11.001)+(13.005), (11.001)+(13.006), (11.001)+(14.001), (11.001)+(14.002), (11.001)+(15.001), (11.001)+(15.002), (11.001)+(15.003), (11.001)+(15.004), (11.001)+(15.005), (11.001)+(15.006), (11.001)+(15.007), (11.001)+(15.008), (11.001)+(15.009), (11.001)+(15.010), (11.001)+(15.011), (11.001)+(15.012), (11.001)+(15.013), (11.001)+(15.014), (11.001)+(15.015), (11.001)+(15.016), (11.001)+(15.017), (11.001)+(15.018), (11.001)+(15.019), (11.001)+(15.020), (11.001)+(15.021), (11.001)+(15.022), (11.001)+(15.023), (11.001)+(15.024), (11.001)+(15.025), (11.001)+(15.026), (11.001)+(15.027), (11.001)+(15.028), (11.001)+(15.029), (11.001)+(15.030), (11.001)+(15.031), (11.001)+(15.032), (11.001)+(15.033), (11.001)+(15.034), (11.001)+(15.035), (11.001)+(15.036), (11.001)+(15.037), (11.001)+(15.038), (11.001)+(15.039), (11.001)+(15.040), (11.001)+(15.041), (11.001)+(15.042), (11.001)+(15.043), (11.001)+(15.044), (11.001)+(15.045), (11.001)+(15.046), (11.001)+(15.047), (11.001)+(15.048), (11.001)+(15.049), (11.001)+(15.050), (11.001)+(15.051), (11.001)+(15.052), (11.001)+(15.053), (11.001)+(15.054), (11.001)+(15.055), (11.001)+(15.056), (11.001)+(15.057), (11.001)+(15.058), (11.001)+(15.059), (11.001)+(15.060), (11.001)+(15.061), (11.001)+(15.062). (11.001)+(15.063). (11.001)+(15.064). (11.001)+(15.065), (11.001)+15.066), (11.001)+(15.067), (11.001)+(15.068), (11.001)+(15.069), (11.001)+(15.070), (11.001)+(15.071), (11.001)+(15.072), (11.001)+(15.073), (11.001)+(15.074), (11.001)+(15.075), (11.001)+(15.076), (11.001), (11.001)+(15.077), (11.001)+(15.078), (11.001)+(15.079), (11.001)+(15.080), (11.001)+(15.081), (1.001)+(15.082), (1.001)+(15.083), (1.001)+(15.084), (1.001)+(15.085), (1.001)+(15.086), (1.001)+(15.087), (1.001)+(15.088), (1.001)+(15.089), (1.001)+(15.090), (1.001)+(15.091), (1.001)+(15.092), (1.001)+(15.093), (11.001)+(15.094), (11.001)+(15.095), (11.001)+(15.096), (11.001)+(15.097), (11.001)+(15.098), (11.001)+(15.099), (11.001)+(15.100), (11.001)+(15.101), (11.001)+(15.102), (11.001)+(15.103), (11.001)+(15.104), (11.001)+(15.105), (11.001)+(15.106), (11.001)+(15.107), (11.001)+(15.108), (11.001)+(15.109), (11.001)+(15.110), (11.001)+(15.111), (11.001)+(15.112), (11.001)+(15.113), (11.001)+(15.114), (11.001)+(15.115), (11.001)+(15.116), (11.001)+(15.117), (11.001)+(15.118), (11.001)+(15.119), (11.001)+(15.120), (11.001)+(15.121), (11.001)+(15.122), (11.001)+(15.123), (11.001)+(15.124), (11.001)+(15.125), (11.001)+(15.126), (11.001)+(15.127).
В этих комбинациях первый компонент представляет собой соединение формулы (II), как определено в таблице II.1 (например, II.001), а второй компонент представляет собой фунгицид, выбранный из групп 1-15, как определено в настоящем документе. Например, комбинация (II.001)+(1.001) соответствует комбинации, содержащей соединение II.001 в таблице II.1 и ципроконазол (1.001).
В некоторых других вариантах осуществления комбинации соединений соответствуют описанным выше комбинациям, в которых соединение (II.001) заменено любым из соединений, перечисленных в таблице II.1.
Соединения формулы (II) и фунгицид, выбранный из групп (1)-(15), могут присутствовать при массовом соотношении от 100:1 до 1:100 (соединение формулы (II): фунгицид, выбранный из группы (1)-(15)), или в пределах от 50:1 до 1:50, или в пределах от 20:1 до 1:20. Другие примеры диапазонов весового соотношения включают от 95:1 до 1:95, от 90:1 до 1:90, от 85:1 до 1:85, от 80:1 до 1:80, от 75:1 до 1:75, 70:1. до 1:70, 65:1 до 1:65, 60:1 до 1:60, 55:1 до 1:55, 45:1 до 1:45, 40:1 до 1:40, 35:1 до 1:35, 30:1 до 1:30, 25:1 до 1:25, 15:1 до 1:15, 10:1 до 1:10, 5:1 до 1:5, 4:1 до 1:4, от 3:1 до 1:3, от 2:1 до 1:2.
К комбинациям соединений может быть добавлен дополнительный фунгицид, выбранный из групп 1-15, как определено в настоящем документе.
Соединения формулы (I) или (II) и содержащие их композиции можно комбинировать с одним или несколькими агентами для биологической борьбы.
Примерами агентов биологической борьбы, которые можно комбинировать с соединениями формулы (I) или (II) и их композициями, являются:
(А) Противобактериальные агенты, выбранные из группы, состоящей из:
(А1) бактерий, таких как (A1.1) Bacillus subtilis, в частности штамм QST713/AQ713 (доступный как SERENADE OPTI или SERENADE ASO от Bayer CropScience LP, US, имеющий NRRL № доступа B21661 описанный в патенте США №6,060,051); (А1.2) Bacillus amyloliquefaciens, в частности штамм D747 (доступный как Double NickelФ от Certis, US, имеющий номер доступа FERM ВР-8234 и описанный в патенте США №7,094,592); (А1.3) Bacillus pumilus, в частности штамм BU F-33 (имеющий NRRL № доступа 50185); (А1.4) Bacillus subtilis var. amyloliquefaciens штамм FZB24 (доступный как TaegroТ от Novozymes, US); (А1.5) aPaenibacillus sp. штамм, имеющий №доступа NRRL В-50972 или № доступа NRRL В-67129, описанный в публикации международной заявки на патент WO 2016/154297; и
(А2) грибов, таких как (А2.1) Aureobasidium pullulans, в частности бластоспоры штамма DSM14940; (А2.2) Aureobasidium pullulans бластоспоры штамма DSM 14941; (А2.3) Aureobasidium pullulans, в частности смеси бластоспор штаммов DSM14940 и DSM14941;
(В) Фунгициды, выбранные из группы:
(В1) бактерий, например (B1.1) Bacillus subtilis, в частности штамм QST713/AQ713 (доступный как SERENADE OPTI или SERENADE ASO от Bayer CropScience LP, US, имеющий NRRL № доступа B21661 описанный в патенте США №6,060,051); (В1.2) Bacillus pumilus, в частности штамм QST2808 (доступный как SONATAТ от Bayer CropScience LP, US, имеющий № доступа NRRL В-30087 описанный в патенте США №6,245,551); (В1.3) Bacillus pumilus, в частности штамм GB34 (доступный как Yield ShieldТ от Bayer AG, DE); (B1.4) Bacillus pumilus, в частности штамм BU F-33 (имеющий NRRL № доступа 50185); (B1.5) Bacillus amyloliquefaciens, в частности штамм D747 (доступный как Double NickelФ от Certis, US, имеющий номер доступа FERM ВР-8234 и раскрытый в патенте США №7,094,592); (В1.6) Bacillus subtilis Y1336 (доступный как BIOBACТ WP от Bion-Tech, Taiwan, зарегистрирован как биологический фунгицид на Тайване под регистрационными номерами 4764, 5454, 5096 и 5277); (В1.7) Bacillus amyloliquefaciens штамм MBI 600 (доступный как SUBTILEX от BASF SE); (В1.8) Bacillus subtilis штамм GB03 (доступный как KodiakТ от Bayer AG, DE); (В1.9) Bacillus subtilis var. amyloliquefaciens штамм FZB24 (доступный от Novozymes Biologicals Inc., Salem, Virginia или Syngenta Crop Protection, LLC, Greensboro, North Carolina как фунгицид TAEGROТ или TAEGROТ ECO (EPA № регистрации 70127-5); (B1.10) Bacillus mycoides, изолят J (доступный как BmJ TGAI или WG от Certis USA); (B1.11) Bacillus licheniformis, в частности штамм SB3086 (доступный как EcoGuard ТМ Biofungicide и Green Releaf от Novozymes); (В1.12) Paenibacillus sp. Штамм, имеющий № доступа NRRL В-50972 или № доступа NRRL В-67129, описанный в публикации международной заявки на патент WO 2016/154297.
Согласно некоторым вариантам осуществления, агент для биологической борьбы представляет собой Bacillus subtilis или Bacillus amyloliquefaciens штамм, который продуцирует соединение типа фенгицина или плипастатина, соединение типа итурина и/или соединение типа сурфактина. Уровень техники можно найти в следующей обзорной статье: Ongena, М., et al., "Bacillus Lipopeptides: Versatile Weapons for Plant Disease Biocontrol," Trends in Microbiology, Vol 16, No. 3, March 2008, pp. 115-125. Bacillus штаммы, способные продуцировать липопептиды, включают Bacillus subtilis QST713 (доступный как SERENADE OPTI или SERENADE ASO от Bayer CropScience LP, US, имеющий NRRL № доступа B21661 описанный в патенте США №6,060,051), Bacillus amyloliquefaciens штамм D747 (доступный как Double NickelФ от Certis, US, имеющий номер доступа FERM ВР-8234 и раскрытый в патенте США 7,094,592); Bacillus subtilis MBI600 (доступный как SUBTILEXТ от Becker Underwood, US ЕРА Reg. No. 71840-8); Bacillus subtilis Y1336 (доступный как BIOBACТ WP от Bion-Tech, Taiwan, зарегистрирован как биологический фунгицид на Тайване под регистрационными номерами.4764, 5454, 5096 и 5277); Bacillus amyloliquefaciens, в частности штамм FZB42 (доступный как RHIZOVITALТ от ABiTEP, DE); и Bacillus subtilis var. amyloliquefaciens FZB24 (доступный от Novozymes Biologicals Inc., Salem, Virginia или Syngenta Crop Protection, LLC, Greensboro, North Carolina в качестве фунгицида TAEGROТ или TAEGROТ ECO (EPA № регистрации 70127-5); и
(B2) грибов, например: (В2.1) Coniothyrium minitans, в частности штамм CON/M/91-8 (№ доступа DSM-9660; например, ContansТ от Bayer); (В2.2) Metschnikowia fructicola, в частности штамм NRRL Y-30752 (например, ShemerТ); (В2.3) Microsphaeropsis ochracea (например, MicroxТ от Prophyta); (В2.5) Trichoderma spp., включая Trichoderma atroviride, штамм SCI, описанный в международной заявке №. PCT/IT2008/000196); (В2.6) Trichoderma harzianum rifai штамм KRL-AG2 (также известный как штамм Т-22, /АТСС 208479, например, PLANTSHIELD T-22G, RootshieldТ, и TurfShield от Bio Works, US); (В2.14) Gliocladium roseum, штамм 321U от W.F. Stoneman Company LLC; (B2.35) Talaromyces flavus, штамм V117b; (B2.36) Trichoderma asperellum, штамм ICC 012 от Isagro; (B2.37) Trichoderma asperellum, штамм SKT-1 (например, ECO-HOPEТ от Kumiai Chemical Industry); (B2.38) Trichoderma atroviride, штамм CNCM 1-1237 (например, EsquiveТ WP от Agrauxine, FR); (B2.39) Trichoderma atroviride, штамм № V08/002387; (B2.40) Trichoderma atroviride, штамм NMI № V08/002388; (B2.41) Trichoderma atroviride, штамм NMI № V08/002389; (B2.42) Trichoderma atroviride, штамм NMI № V08/002390; (B2.43) Trichoderma atroviride, штамм LC52 (например, Tenet от Agrimm Technologies Limited); (B2.44) Trichoderma atroviride, штамм АТСС 20476 (IMI 206040); (B2.45) Trichoderma atroviride, штамм T11 (IMI352941/CECT20498); (B2.46) Trichoderma harmatum; (B2.47) Trichoderma harzianum; (B2.48) Trichoderma harzianum rifai T39 (например, TrichodexТ от Makhteshim, US); (B2.49) Trichoderma harzianum, в частности, штамм KD (например, Trichoplus от Biological Control Products, SA (доступно от Becker Underwood)); (B2.50) Trichoderma harzianum, штамм ITEM 908 (например, Trianum-P от Koppert); (B2.51) Trichoderma harzianum, штамм TH35 (например, Root-Pro от Mycontrol); (B2.52) Trichoderma virens (также известен как Gliocladium virens), в частности штамм GL-21 (например, SoilGard 12G от Certis, US); (B2.53) Trichoderma viride, штамм TV1 (например, Trianum-Р от Koppert); (B2.54) Ampelomyces quisqualis, в частности штамм AQ 10 (например, AQ 10Т от hitrachemBio Italia); (B2.56) Aureobasidium pullulans, в частности бластоспоры штамма DSM14940; (В2.57) Aureobasidium pullulans, в частности бластоспоры штамма DSM 14941; (В2.58) Aureobasidium pullulans, в частности смеси бластоспор штаммов DSM14940 и DSM 14941 (например, BotectorТ от bio-ferm, СН); (В2.64) Cladosporium cladosporioides, штамм Н39 (от Stichting Dienst Landbouwkundig Onderzoek); (B2.69) Gliocladium catenulatum (синоним: Clonostachys rosea f. catenulate) штамм J1446 (например, PrestopТ от AgBio Inc. а также: например, PrimastopТ от Kemira Agro Oy); (B2.70) Lecanicillium lecanii (ранее известный как Verticillium lecanii) conidia штамма KV01 (например, VertalecТ от Koppert/Arysta); (B2.71) Penicillium vermiculatum; (B2.72) Pichia anomala, штамм WRL-076 (NRRL Y-30842); (B2.75) Trichoderma atroviride, штамм SKT-1 (FERM P-16510); (B2.76) Trichoderma atroviride, штамм SKT-2 (FERM P-16511); (B2.77) Trichoderma atroviride, штамм SKT-3 (FERM P-17021); (B2.78) Trichoderma gamsii (ранее Т. viride), штамм ICC080 (IMI CC 392151 CABI, например, BioDerma от AGROBIOSOL DE MEXICO, S.A. DE C.V.); (B2.79) Trichoderma harzianum, штамм DB 103 (например, T-Gro от Dagutat Biolab); (B2.80) Trichoderma polysporum, штамм IMI 206039 (например, Binab TF WP от BINAB Bio-Innovation AB, Sweden); (B2.81) Trichoderma stromaticum (например, Tricovab от Ceplac, Brazil); (B2.83) Ulocladium oudemansii, в частности штамм HRU3 (например, Botry-ZenТ от Botry-Zen Ltd, NZ); (B2.84) Verticillium albo-atrum (ранее V. dahliae), штамм WCS850 (CBS 276.92; например, Dutch Trig от Tree Care Innovations); (B2.86) Verticillium chlamydosporium, (B2.87) смеси Trichoderma asperellum штамм ICC 012 и Trichoderma gamsii штамм ICC 080 (продукт, известный как например, BIO-ТАМФ от Bayer CropScience LP, US).
Дополнительными примерами агентов для биологической борьбы, которые можно комбинировать с соединениями формулы (I) или (II) и композициями, содержащими их, являются:
Бактерии, выбранные из группы, состоящей из Bacillus cereus, в частности В. cereus штамм CNCM I-1562 и Bacillus firmus, штамм I-1582 (Номер доступа CNCM I-1582), Bacillus subtilis штамм OST 30002 (№ доступа NRRL B-50421), Bacillus thuringiensis, в частности В. thuringiensis подвид israelensis (подтип Н-14), штамм АМ65-52 (№ доступа АТСС 1276), В. thuringiensis subsp. aizawai, в частности штамм ABTS-1857 (SD-1372), В. thuringiensis subsp. kurstaki штамм HD-1, В. thuringiensis subsp. tenebrionis штамм NB 176 (SD-5428), Pasteuria penetrans, Pasteuria spp. (Rotylenchulus reniformis нематода)-PR3 (Номер доступа АТСС SD-5834), Streptomyces microflavus штамм AQ6121 (=QRD 31.013, NRRL В-50550), и Streptomyces galbus штамм AQ 6047 (Номер доступа NRRL 30232);
Грибы и дрожжи, выбранные из группы, состоящей из Beauveria bassiana, в частности штамм АТСС 74040, Lecanicillium spp., в частности штамм HRO LEC 12, Metarhizium anisopliae, в частности штамм F52 (DSM3884 или АТСС 90448), Paecilomyces fumosoroseus (сейчас: Isaria fumosorosea), в частности штамм IFPC 200613, или штамм Apopka 97 (№ доступа АТСС 20874), и Paecilomyces lilacinus, в частности Р. lilacinus штамм 251 (AGAL 89/030550);
Вирусы, выбранные из группы, состоящей из Adoxophyes orana (сетчатая листокрутка) вирус зернистости (GV), Cydia pomonella (яблоневая плодожорка) вирус зернистости (GV), Helicoverpa armigera (коробочный червь) вирус ядерного полиэдроза (NPV), Spodoptera exigua (совка малая) mNPV, Spodoptera frugiperda (совка травяная) mNPV, Spodoptera littoralis (гусеница, питающаяся листьями африканского хлопка) NPV.
Бактерии и грибы, которые могут быть добавлены в качестве «инокулянта» к растениям, частям растений или органам растений и которые благодаря своим особым свойствам способствуют росту растений и здоровью растений. Примерами являются:
Agrobacterium spp., Azorhizobium caulinodans, Azospirillum spp., Azotobacter spp., Bradyrhizobium spp., Burkholderia spp., в частности Burkholderia cepacia (ранее известен как Pseudomonas cepacia), Gigaspora spp., или Gigaspora monosporum, Glomus spp., Laccaria spp., Lactobacillus buchneri, Paraglomus spp., Pisolithus tinctorus, Pseudomonas spp., Rhizobium spp., в частности Rhizobium trifolii, Rhizopogon spp., Scleroderma spp., Suillus spp., и Streptomyces spp.
Растительные экстракты и продукты, образованные микроорганизмами, включая белки и вторичные метаболиты, которые могут использоваться в качестве агентов для биологической борьбы, такие как Allium sativum, Artemisia absinthium, azadirachtin, Biokeeper WP, Cassia nigricans, Celastrus angulatus, Chenopodium anthelminticum, хитин, Armour-Zen, Dryopteris filix-mas, Equisetum arvense. Fortune Aza, Fungastop, Heads Up (экстракт Chenopodium quinoa saponin), пиретрум/пиретрины, Quassia amara, дуб, Килайя, Регалия, "RequiemФ Инсектицид", ротенон, риания/рианодин, Symphytum officinale, Tanacetum vulgare, тимол, Triact 70, TriCon, Tropaeulum majus, Urtica dioica, Veratrin, Viscum album, экстракт Brassicaceae, в частности порошок мас-личного рапса или горчичный порошок.
Примерами инсектицидов, акарицидов и нематоцидов, соответственно, которые могут быть смешаны с соединениями формулы (I) или (II) и композициями, содержащими их, являются:
(1) Ингибиторы ацетилхолинэстеразы (AChE), например карбаматы, например, аланикарб, альдикарб, Бендиокарб, Бенфуракарб, Бутокарбоксим, Бутоксикарбоксим, Карбарил, Карбофуран, Карбосульфан, Этиофенкарб, Фенобукарб, Форметанат, Фуратиокарб, изопрокарб, Метиокарб, Метомил, Метолкарб, Оксамил, пиримикарб, пропоксур, тиодикарб, тиофанокс, триазамат, триметакарб, ХМС, и Ксилилкарб; или фосфорорганические соединения, например, ацефат, азаметифос, азинфосэтил, азинфосметил, Кадузафос, хлорэтоксифос, хлорфенвинфос, хлормефос, хлорпирифос, хлорпирифос-метил, Кумафос, цианофос, деметон-S-метил, диазинон, дихлорвос/DDVP, дикротофос, диметоат, диметилвинфос, дисульфотон, EPN, Этион, Этопрофос, Фамфур, Фенамифос, Фенитротион, Фентион, Фостиазат, гептенофос, Имициафос, изофенфос, изопропил-О-(метоксиаминотио-фосфорил)салицилат, изоксатион, Малатион, Мекарбам, Ме-тамидофос, Метидатион, Мевинфос, Монокротофосфос, Налед, Ометоат, Окси-деметон-метил, Паратион, Паратион-метил, Фентоат, Форат, Фосалон, Фосмет, Фосфамидон, Фоксим, пиримифос-метил, профенофос, пропетамфос, протиофос, пираклофос, пиридафентион, Хиналфос, Сульфотеп, Тебупиримфос, Темефос, Тербуфос, тетрахлорвинфос, тиометон, триазофос, трихлорфон и Вамидотион.
(2) Антагонисты GABA-зависимого хлоридного канала, например, циклодиеновые хлорорганические соединения, например, хлордан и Эндосульфан; или фенилпиразолы (фипролы), например, Этипрол и Фипронил.
(3) Модуляторы натриевого канала/Блокаторы потенциал-зависимого натриевого канала, например пиретроиды, например, акринатрин, аллетрин, d-цис-транс Ал-летрин, d-транс-аллетрин, Бифентрин, Биоаллетрин, Биоаллетрина S-циклопентенил-изомер, Биоресметрин, циклопротрин, цифлутрин, бета-цифлутрин, цигалотрин, лямбда-цигалотрин, гамма-цигалотрин, циперметрин, альфа-циперметрин, бета-циперметрин, тета-циперметрин, зета-циперметрин, цифенотрин [(1R)-транс-изомеры], дельтаметрин, Эмпентрин [(EZ)-(1R) изомеры), Эсфенвалерат, Этофенпрокс, Фенпропатрин, Фенвалерат, Флуцитринат, Флуметрин, тау-Флувалинат, галфенпрокс, Имипротрин, Кадетрин, Перметрин, Фенотрин [(1R)-транс-изомер), Праллетрин, пиретрин (пиретрум), Ресметрин, Силафлуофен, Тефлутрин, тетраметрин, тетраметрин [(1R) изомеры)], Траломет-рин, и Трансфлутрин; или дДТ; или метоксихлор.
(4) Агонисты никотинового ацетилхолинового рецептора (nAChR), например, неоникотиноиды, например, ацетамиприд, Клотианидин, динотефуран, Имида-клоприд, Нитенпирам, тиаклоприд, и Тиаметоксам; или Никотин; или Сульфок-сахлор или флупирадифурон.
(5) Аллостерические модуляторы никотинового ацетилхолинового рецептора (nAChR), например, спиносины, например, Спинеторам и Спиносад.
(6) Аллостерические модуляторы глутамат-зависимого хлоридного канала (GluCl), например, авермектины/мильбемицины, например, абамектин, Эмамек-тина бензоат, Лепимектин и Мильбемектин.
(7) Миметики ювенильного гормона, например, аналоги ювенильного гормона, например, гидропрен, Кинопрен и Метопрен; или Феноксикарб; или Пирипрок-сифен.
(8) Различные неспецифические (многосайтовые) ингибиторы, как например, алкилгалогениды, например, метилбромид и другие алкилгалогениды; или хлор-пикрин; или сульфурилфторид; или Боракс или винокислая сурьмянокалиевая соль или предшественник метилизоцианата, например, диазомет и метам.
(9) Модуляторы органа слуха у насекомых, например, пиметрозин; или Флоникамид.
(10) Ингибиторы роста клещей, например, Клофентезин, гекситиазокс, и дифловидазин; или Этоксазол.
(11) Микробные разрушители мембран средней кишки насекомых, например, Bacillus thuringiensis подвид israelensis. Bacillus sphaericus, Bacillus thuringiensis подвид aizawai. Bacillus thuringiensis подвид kurstaki. Bacillus thuringiensis подвид tenebrionis, и ВТ растительные белки: Cry1Ab, Cry1Ac, Cry1Fa, Cry2Ab, mCry3A, Cry3Ab, Cry3Bb, Cry34/35Ab1.
(12) ингибиторы митохондриального АТФ-синтеза, такие как АТР-дезинтеграторы, такие как, например; диафентиурон или оловоорганические митициды, например, азоциклотин, цигексатин, и Фенбутатина оксид; или Пропаргит; или тетрадифон.
(13) Средства, разобщающие окислительное фосфорилирование посредством разрушения протонового градиента, например, хлорфенапир, DNOC и Сульфлурамид.
(14) Блокаторы никотинергического ацетилхолинового рецептора, такие как, например, Бенсультап, Картапа гидрохлорид, тиоциклам и Тиосультап-натрий.
(15) Ингибиторы биосинтеза хитина, типа 0, например, Бистрифлурон, Хлофлуазурон, дифлубензурон, Флуциклоксурон, Флуфеноксурон, гексафлумурон, Луфенурон, Новалурон, Новифлумурон, Тефлубензурон и Трифлумурон.
(16) Ингибиторы биосинтеза хитина, типа 1, например, Бупрофезин.
(17) Ингибиторы линьки (в частности для двукрылых, т.е. мух), такие как, например, циромазин.
(18) Агонисты рецептора экдизона, например, Хромафенозид, галофенозид, метоксифенозид и Тебуфенозид.
(19) Октопаминергические агонисты, такие как, например, амитраз.
(20) Ингибиторы транспорта электронов митохондриального комплекса III, например, Гидраметилнон; или Ацехиноцил; или Флуакрипирим.
(21) Ингибиторы транспорта электронов митохондриального комплекса I, например, из группы METI акарицидов, например, Феназахин, Фенпироксимат, пиримидифен, пиридабен, Тебуфенпирад и Толфенпирад; или Ротенон (Деррис).
(22) Блокаторы потенциалзависимого натриевого канала, например, Индоксакарб; или Метафлумизон.
(23) Ингибиторы ацетил-КоА-карбоксилазы, например, производные тетроновой и тетраминовой кислоты, например, кетоенолы, такие как, в частности, Спиротетрамат, Спиромезифен и Спиродиклофен.
(24) Ингибиторы транспорта электронов митохондриального комплекса IV, например, фосфины, например, фосфид алюминия, фосфид кальция, Фосфин и фосфид цинка; или Цианид, цианид кальция, цианид калия и цианид натрия.
(25) Ингибиторы транспорта электронов митохондриального комплекса II, например, бета-кетонитрильная производная, например, циенопирафен и Цифлуметофен, и Карбоксанилид, как например, Пифлубумид.
(28) Модуляторы рианодинового рецептора, такие как, например, диамиды, например, хлорантранилипрол, циантранилипол и флубендиамид,
другие активные ингредиенты такие как, например, афидопиропен, афоксоланер, азадирахтин, бенклотиаз, бензоксимат, бифеназат, бромфланилид, бромпропилат, хинометионат, хлорпраллетрин, криолит, цикланилипрол, циклоксаприд, цигалодиамид, диклоромезотиаз, дикофол, эпсилон-метофлутрин, эпсилон-момфлутрин, флометоквин, флуазаиндолизин, флуенсульфон, флуфенерим, флуфеноксистробин, флуфипрол, флугексафон, флуопирам, флураланер, флуксаметамид, фуфенозид, гуадипир, гептафлутрин, имидаклотиз, ипродион, каппа-бифентрин, каппа-тефлутрин, лотиланер, меперфлутрин, паичонгдинг, пиридалил, пирифлуквиназон, пириминостробин, спиробудиклофен, тетраметилфлутрин, тетранилипрол, тетрахлорантранилипрол, тиголанер, тиоксазафен, тиофлуоксимат, трифлумезопирим и иодметан; кроме того, препараты на основе Bacillus firmus (I-1582, BioNeem, Votivo), а также следующие активные соединения: 1-{2-фтор-4-метил-5-[(2,2,2-трифторэтил)сульфинил]фенил}-3-(трифторметил)-1Н-1,2,4-триазол-5-амин (известный из WO 2006/043635) (CAS 885026-50-6), {1ў-[(2Е)-3-(4-хлорфенил)проп-2-ен-1-ил]-5-фторспиро[индол-3,4ў-пиперидин]-1(2Н)-ил}(2-хлорпиридин-4-ил)метанон (известный из WO 2003/106457) (CAS 637360-23-7), 2-хлор-N-[2-{1-[(2Е)-3-(4-хлорфенил)проп-2-ен-1-ил]пиперидин-4-ил}-4-(трифторметил)фенил]изоникотинамид (известный из WO 2006/003494) (CAS 872999-66-1), 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-метокси-1,8-диазаспиро[4.5]дец-3-ен-2-он (известный из WO 2010052161) (CAS 1225292-17-0), 3-(4-хлор-2,6-диметилфенил)-8-метокси-2-оксо-1,8-диазаспиро[4.5]дец-3-ен-4-ил-этилкарбонат (известный из ЕР 2647626) (CAS-1440516-42-6), 4-(бут-2-ин-1-илокси)-6-(3,5-диметилпиперидин-1-ил)-5-фторпиримидин (известный из WO 2004/099160) (CAS 792914-58-0), PF1364 (известный из JP 2010/018586) (CAS-Reg.No. 1204776-60-2), N-[(2Е)-1-[(6-хлорпиридин-3-ил)метил]пиридин-2(1Н)-илиден]-2,2,2-трифторацетамид (известный из WO 2012/029672) (CAS 1363400-41-2), (3Е)-3-[1-[(6-хлор-3-пиридил)метил]-2-пиридилиден]-1,1,1-трифторпропан-2-он (известный из WO 2013/144213) (CAS 1461743-15-6), N-[3-(бензилкарбамоил)-4-хлорфенил]-1-метил-3-(пентафторэтил)-4-(трифторметил)-1Н-пиразол-5-карбоксамид (известный из WO 2010/051926) (CAS 1226889-14-0), 5-бром-4-хлор-N-[4-хлор-2-метил-6-(метилкарбамоил)фенил]-2-(3-хлор-2-пиридил)пиразол-3-карбоксамид (известный из CN 103232431) (CAS 1449220-44-3), 4-[5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(цис-1-оксидо-3-тиетанил)бензамид, 4-[5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(транс-1-оксидо-3-тиетанил)бензамид и 4-[(5S)-5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(цис-1-оксидо-3-тиетанил)бензамид (известный из WO 2013/050317 A1) (CAS 1332628-83-7), N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид, (+)-N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид и (-)-N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид (известный из WO 2013/162715 А2, WO 2013/162716 А2, US 2014/0213448 A1) (CAS 1477923-37-7), 5-[[(2E)-3-хлор-2-пропен-1-ил]амино]-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[(трифторметил)сульфинил]-1Н-пиразол-3-карбонитрил (известный из CN 101337937 А) (CAS 1105672-77-2), 3-бром-N-[4-хлор-2-метил-6-[(метиламино)тиохометил]фенил]-1-(3-хлор-2-пиридинил)-1Н-пиразол-5-карбоксамид, (Liudaibenjiaxuanan, известный из CN 103109816 А) (CAS 1232543-85-9); N-[4-хлор-2-[[(1,1-диметилэтил)амино]карбонил]-6-метилфенил]-1-(3-хлор-2-пиридинил)-3-(фторметокси)-1Н-пиразол-5-карбоксамид (известный из WO 2012/034403 A1) (CAS 1268277-22-0), N-[2-(5-амино-1,3,4-тиадиазол-2-ил)-4-хлор-6-метилфенил]-3-бром-1-(3-хлор-2-пиридинил)-1Н-пиразол-5-карбоксамид (известный из WO 2011/085575 A1) (CAS 1233882-22-8), 4-[3-[2,6-дихлор-4-[(3,3-дихлор-2-пропен-1-ил)окси]фенокси]пропокси]-2-метокси-6-(трифторметил)пиримидин (известный из CN 101337940 А) (CAS 1108184-52-6); (2Е)- и 2(Z)-2-[2-(4-цианофенил)-1-[3-(трифторметил)фенил]этилиден]-N-[4-(дифторметокси)фенил]гидразинкарбоксамид (известный из CN 101715774 A) (CAS 1232543-85-9); циклопропанкарбоновая кислота-3-(2,2-дихлорэтенил)-2,2-диметил-4-(1Н-бензимидазол-2-ил)фениловый сложный эфир (известный из CN 103524422 А) (CAS 1542271-46-4); (4aS)-7-хлор-2,5-дигидро-2-[[(метоксикарбонил)[4-[(трифторметил)тио]фенил]амино]карбонил]индено[1,2-е][1,3,4]оксадиазин-4а(3Н)-карбоновая кислота метиловый сложный эфир (известный из CN 102391261 А) (CAS 1370358-69-2); 6-дезокси-3-O-этил-2,4-ди-O-метил-1-[N-[4-[1-[4-(1,1,2,2,2-пентафторэтокси)фенил]-1Н-1,2,4-триазол-3-ил]фенил]карбамат]-a-L-маннопираноза (известный из US 2014/0275503 A1) (CAS 1181213-14-8); 8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло [3.2.1] октан (CAS 1253850-56-4), (8-anti)-8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло[3.2.1]октан (CAS 933798-27-7), (8-syn)-8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло[3.2.1]октан (известный из WO 2007040280 A1, WO 2007040282 A1) (CAS 934001-66-8) и N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)тио]-пропанамид (известный из WO 2015/058021 A1, WO 2015/058028 A1) (CAS 1477919-27-9) и N-[4-(аминотиоксометил)-2-метил-6-[(метиламино)карбонил]фенил]-3-бром-1-(3-хлор-2-пиридинил)-1Н-пиразол-5-карбоксамид (известный из CN 103265527 А) (CAS 1452877-50-7), 5-(1,3-диоксан-2-ил)-4-[[4-(трифторметил)фенил]метокси]-пиримидин (известный из WO 2013/115391 A1) (CAS 1449021-97-9), 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-метокси-1-метил-1,8-диазаспиро[4.5]дец-3-ен-2-он (известный из WO 2010/066780 A1, WO 2011/151146 A1) (CAS 1229023-34-0), 3-(4-хлор-2,6-диметилфенил)-8-метокси-1-метил-1,8-диазаспиро[4.5]декан-2,4-дион (известный из WO 2014/187846 A1) (CAS 1638765-58-8), 3-(4-хлор-2,6-диметилфенил)-8-метокси-1-метил-2-оксо-1,8-диазаспиро[4.5]дец-3-ен-4-ил-карбоновой кислоты сложный этиловый эфир (известный из WO 2010/066780 A1, WO 2011151146 A1) (CAS 1229023-00-0), N-[1-[(6-хлор-3-пиридинил)метил]-2(1Н)-пиридинилиден]-2,2,2-трифтор-ацетамид (известный из DE 3639877 A1, WO 2012029672 A1) (CAS 1363400-41-2), [N(Е)]-N-[1-[(6-хлор-3-пиридинил)метил]-2(1Н)-пиридинилиден]-2,2,2-трифтор-ацетамид, (известный из WO 2016005276 A1) (CAS 1689566-03-7), [N(Z)]-N-[1-[(6-хлор-3-пиридинил)метил]-2(1Н)-пиридинилиден]-2,2,2-трифтор-ацетамид, (CAS 1702305-40-5), 3-эндо-3-[2-пропокси-4-(трифторметил)фенокси]-9-[[5-(трифторметил)-2-пиридинил]окси]-9-азабицикло[3.3.1]нонан (известный из WO 2011/105506 A1, WO 2016/133011 A1) (CAS 1332838-17-1).
Примерами защитных средств, которые могут быть смешаны с соединениями формулы (I) или (II), и содержащими их композициями, являются, например, беноксакор, клоквинтоцет (-мексил), циометринил, ципросульфамид, дихлормид, фенхлоразол (-этил), фенхлорим, флуразол, флуксофеним, фурилазол, изоксадифен (-этил), мефенпир (-диэтил), нафталевый ангидрид, оксабетринил, 2-метокси-N-({4-[(метилкарбамоил)амино]фенил}сульфонил)бензамид (CAS 129531-12-0), 4-(дихлорацетил)-1-окса-4-азаспиро[4.5]декан (CAS 71526-07-3), 2,2,5-триметил-3-(дихлорацетил)-1,3-оксазолидин (CAS 52836-31-4).
Примерами гербицидов, которые могут быть смешаны с соединениями формулы (I) или (II), и композициями, содержащими их, являются:
ацетохлор, ацифлуорфен, ацифлуорфен-натрий, аклонифен, алахлор, аллидохлор, аллоксидим, аллоксидим-натрий, аметрин, амикарбазон, амидохлор, амидосульфурон, 4-амино-3-хлор-6-(4-хлор-2-фтор-3-метилфенил)-5-фторпиридин-2-карбоновая кислота, аминоциклопирахлор, аминоциклопирахлор-калий, аминоциклопирахлор-метил, аминопиралид, амитрол, аммония сульфомат, анилофос, асулам, атразин, азафенидин, азимсульфурон, бефлубутамид, беназолин, беназолин-этил, бенфлуралин, бенфуресат, бенсулид, бенсульфурон, бенсульфурон-метил, бенсулид, бентазон, бензобициклон, бензофенап, бициклопирон, бифенокс, биланафос, биланафос-натрий, биспирибак, биспирибак-натрий, бромацил, бромобутид, бромофеноксим, бромоксинил, бромоксинил бутират, -калий, -гептаноат и октаноат, бузоксинон, бутахлор, бутафенацил, бутамифос, бутенахлор, бутралин, бутроксидим, бутилат, кафенстрол, карбетамид, карфентразон, карфентразон-этил, хлорамбен, хлорбромурон, хлорфенак, хлорфенак-натрий, хлорфенпроп, хлорфлуренол, хлорфлуренол-метил, хлоридазон, хлоримурон, хлоримурон-этил, хлорофталим, хлортолурон, хлортал-диметил, хлорсульфурон, цинидон, цинидон-этил, цинметилин, циносульфурон, клацифос, клетодим, клодинафоп, клодинафоп-пропаргил, кломазон, кломепроп, клопиралид, клорансулам, клорансулам-метил, кумилурон, цианамид, цианазин, цикланилид, циклоат, циклопириморат, циклосульфамурон, циклоксидим, цигалофоп, цигалофоп-бутил, ципразин, 2,4-D, 2,4-D-бутотил, -бутил, -диметиламмоний, -диоламин, -этил, -2-этилшексил, -изобутил, -изооктил, -изопропиламмоний, -калий, -триизопропаноламмоний и -троламин, 2,4-DB, 2,4-DB-бутил, -диметиламмоний, -изооктил, -калий и натрий, даймурон (димрон), далапон, дазомет, н-деканол, десмедифам, детосил-пиразолат (DTP), дикамба, дихлобенил, 2-(2,4-дихлорбензил)-4,4-диметил-1,2-оксазолидин-3-он, 2-(2,5-дихлорбензил)-4,4-диметил-1,2-лксазолидин-3-он, дихлорпроп, дихлорпроп-Р, диклофоп, диклофоп-метил, диклофоп-Р-метил, диклосулам, дифензокват, дифлуфеникан, дифлубензопир, дифлубензопир-натрий, димефурон, димепиперат, диметахлор, диметаметрин, диметенамид, диметенамид-Р, диметра-сульфурон, динитрамин, динотерб, дифенамид, дикват, дикват-дибромид, дитиопир, диурон, DNOC, эндотал, ЕРТС, эспрокарб, эталфлуралин, этаметсульфурон, этаметсульфурон-метил, этиозин, этофумезат, этоксифен, этоксифен, этоксифен-этил, этоксисульфурон, этобензанид, F-9600, F-5331, т.е. N-[2-хлор-4-фтор-5-[4-(3-фторпропил)-4,5-дигидро-5-оксо-1Н-тетразол-1-ил]-фенил]-этансульфон амид, F-7967, т.е. 3-[7-хлор-5-фтор-2-(трифторметил)-1Н-бензимидазол-4-ил]-1-метил-6-(трифторметил)пиримидин-2,4(1Н,3Н)-дион, феноксапроп, феноксапроп-Р, феноксапроп-этил, феноксапроп-Р-этил, феноксасульфон, фенквинотрион, фентразамид, флампроп, флампроп-М-изопропил, флампроп-М-метил, флазасульфурон, флорасулам, флуазифоп, флуазифоп-Р, флуазифоп-бутил, флуазифоп-Р-бутил, флукарбазон, флукарбазон-натрий, флуцетосульфурон, флухлоралин, флуфенацет, флуфенпир, флуфенпир-этил, флуметсулам, флумиклорак, флумиклорак-пентил, флумиоксазин; флуометурон, флуо-родифен, фторогликофен, фторогликофен-этил, флупоксам, флупропацил, флупропанат, флупирсульфурон, флупирсульфурон-метил-натрий, флуренол, флуренол-бутил, -диметиламмоний и метил, флуорогликофен, флуорогликофен-этил, флупропанат, флупирсульфурон, флупирсульфурон-метил-натрий, флуридон, флурохлоридон, флуроксипир, флуроксипир-метил, флурпримидол, флуртамон, флутиацет, флутиацет-метил, фомесафен, фомесафен-натрий, форамсульфурон, фосамин, глуфосинат, глуфосинат-аммоний, глуфосинат-Р-натрий глуфосинат-Р-аммоний, глуфосинат-Р-натрий, глуфосат, глуфосат-аммоний, -изопропиламмоний, -диаммоний, -диметиламмоний, -калий, -натрий и -трицезий, Н-9201, т.е. O-(2,4-диметил-6-нитрофенил)-O-этил-изопропилфосфорамидотиоат, галауксифен, галауксифен-метил, галосафен, галосульфурон, галосульфурон-метил, галоксифоп, галоксифоп-Р, галоксифоп-этоксиэтил, галоксифоп-Р-этоксиэтил, галоксифоп-метил, галоксифоп-Р-метил, гексазинон, HW-02, т.е. 1-(диметоксифосфорил)-этил-(2,4-дихлорфенокси)ацетат, имазаметабенз, имазаметабенз-метил, имазамокс, имазамокс-аммоний, имазапик, имазапик-аммоний, имазапир, имазапир-изопропиламмоний, имазахин, имазахин-аммоний, имазетапир, имазетапир-аммоний, имазосульфурон, инданофан, индазифлам, йодосульфурон, йодосульфурон-метил-натрий, иоксинил, иоксинил-октаноат, -калий и натрий, ипфенкарбазон, изопротурон, изоурон, изоксабен, изоксафлутол, карбутилат, KUH-043, т.е. 3-({[5-(Дифторметил)-1-метил-3-(трифторметил)-1Н-пиразол-4-ил]метил}сульфонил)-5,5-диметил-4,5-дигидро-1,2-оксазол, кетоспирадокс, лактофен, ленацил, линурон, МСРА, МСРА-метил, -этил и натрий, мекопроп, мекопроп-натрий и бутотил, мекопроп-Р, м мекопроп-Р-бутотил, -диметиламмоний, -2-этилгексил и -калий, мефенацет, мефлуидид, мезосульфурон, мезосульфурон-метил, мезотрион, метабензтиазурон, метам, метамифоп, метамитрон, метазахлор, метазасульфурон, метиозолин, метилизотиоцианат, метобромурон, метолахлор, S-метолахлор, метосулам, метоксурон, метрибузин, метсульфурон, метсульфурон-метил, молинат, монолинурон, моносульфурон, моносульфурон-сложный эфир, МТ-5950, т.е. N-[3-хлор-4-(1-метилэтил)-фенил]-2-метилпентан амид, NGGC-011, напроанилид, напропамид, напталам, NC-310, т.е. 4-(2,4-дихлоробензоил)-1-метил-5-бензилоксипиразол, небурон, никосульфурон, нонановая кислота (пералгоновая кислота), норфлуразон, олеиновая кислота (жирные кислоты), орбенкарб, ортосульфамурон, оризалин, оксадиаргил, оксадиазон, оксасульфурон, окса-зикломефон, оксифлуорфен, паракват, паракват-дихлорид, пебулат, пендиметалин, пенокссулам, пентанохлорфенол, пентоксамид, петролейные масла, фенмедифам, пиклорам, пиколинафен, пиноксаден, пиперофос, претилахлор, примисульфурон, примисульфурон-метил, продиамин, профоксидим, прометон, прометрин, пропахлор, пропанил, пропахизафоп, пропазин, профам, пропизохлор, пропоксикарбазон, пропоксикарбазон-натрия, пропирисульфурон, пропизамид, просульфокарб, просульфурон, принахлор, пираклонил, пирафлуфен, пирафлуфен-этил, пирасульфотол, пиразолинат (пиразолат), пиразосульфурон, пиразосульфурон-этил, пиразоксифен, пирибамбенз, пирибамбенз-изопропил, пирибамбенз-пропил, пирибензоксим, пирибутикарб, пиридафол, пиридат, пирифталид, пириминобак, пириминобак-метил, пиримисульфан, пиритиобак, пиритиобак-натрий, пироксасульфон, пироксулам, хинклорак, хинмерак, хинокламин, хизалофоп, хизалофоп-этил, хизалофоп-Р, хизалофоп-Р-этил, хизалофоп-Р-тефурил, римсульфурон, секбуметон, сетоксидим, сидурон, симазин, симетрин, SL-261, сулкотрин, сульфентразон, сульфометурон, сульфометурон-метил, сульфосульфурон, SYN-523, SYP-249, т.е. 1-Этокси-3-метил-1-оксобут-3-ен-2-ил-5-[2-хлор-4-(трифторметил)фенокси]-2-нитробензоат, SYP-300, т.е. 1-[7-Фтор-3-оксо-4-(проп-2-ин-1-ил)-3,4-дигидро-2Н-1,4-бензоксазин-6-ил]-3-пропил-2-тиоксоимидазолидин-4,5-дион, 2,4,6-ТВА, ТСА (трихлоруксусная кислота), ТСА-натрий, тебутиурон, тефурилтрион, темботрион, тепралоксидим, тербацил, тербукарб, тербуметон, тербутилазин, тербутрин, тенилхлор, тиазопир, тиенкарбазон, тиенкарбазонметил, тифенсульфурон, тифенсульфурон-метил, тиобенкарб, тиафенацил, толпиралат, топрамезон, тралкоксидим, триафамон, триаллат, триасульфурон, триазифлам, трибенурон, трибенурон-метил, триклопир, триэтазин, трифлоксисульфурон, трифлоксисульфурон-натрий, трифлудимоксазин, трифлуралин, трифлусульфурон, трифлусульфуронметил, тритосульфурон, сульфат мочевины, вернолат, XDE-848, ZJ-0862, т.е. 3,4-дихлор-N-{2-[(4,6-диметоксипиримидин-2-ил)окси]бензил} анилин, а также следующие соединения:
Примерами регуляторов роста растений являются:
Ацибензолар, ацибензолар-S-метил, 5-аминолевулиновая кислота, анцимидол, 6-бензиламинопурин, брассинолид, катехин, хлормекват хлорид, клопроп, цикланилид, 3-(циклопроп-1-енил) пропионовая кислота, даминозид-деканоломет, дазомет, дикегулак, дикегулак-натрий, эндотал, эндотал-дикалий, -динатрий и -моно(n,n-диметилалкиламмоний), этифон, флуметралин, флуренол, флуренол-бутил, флурпримидол, форхлорфенурон, гиббереллиновая кислота, инабенфид, индол-3-уксусная кислота (IAA), 4-индол-3-илмасляная кислота, изопротиолан, пробеназол, жасмоновая кислота, гидразид малеиновой кислоты, мепикватхлорид, 1-метилцикло пропей, метилжасмонат, 2-(1-нафтил)ацетамид, 1-нафтилуксусная кислота, 2-нафтилоксиуксусная кислота, смесь нитро фенолятов, паклобутразол, N-(2-фенилэтил)-бета-аланин, N-фенилфталаминовая кислота, прогексадион, прогексадион-кальций, прогидрожасмон, салициловая кислота, стриголактон, текназен, тидиазурон, триаконтанол, тринексапак, тринексапак-этил, цитодеф, униконазол, униконазол-Р.
Способы и применения
Соединения формулы (I) или (II) и содержащие их композиции обладают сильной микробиоцидной активностью. Их можно использовать для борьбы с нежелательными микроорганизмами, такими как нежелательные грибки и бактерии. Они могут быть особенно полезны для защиты растений (они контролируют микроорганизмы, вызывающие заболевания растений) или для защиты материалов (например, промышленных материалов, древесины, товаров на хранении), как более подробно описано ниже. Более конкретно, соединения формулы (I) или (II) и композиция согласно настоящему изобретению могут использоваться для защиты семян, прорастающих семян, проросших проростков, растений, частей растений, плодов, урожая и/или почвы, в которой растения растут, от нежелательных микроорганизмов.
Контроль или борьба, как используется в настоящем документе, включает защитную, лечебную и исключающую нежелательные микроорганизмы обработку. Нежелательные микроорганизмы могут быть патогенными бактериями, патогенными вирусами, патогенными оомицетами или патогенными грибами, более конкретно, фитопатогенными бактериями, фитопатогенным вирусом, фитопатогенными оомицетами или фитопатогенными грибами. Как подробно описано ниже, эти фитопатогенные микроорганизмы являются возбудителями широкого спектра заболеваний растений.
Более конкретно, соединение формулы (I) или (II) и композиция согласно настоящему изобретению могут использоваться в качестве фунгицидов. В контексте настоящего изобретения термин «фунгицид» относится к соединению или композиции, которые можно использовать для защиты растений для борьбы с нежелательными грибами, такими как плазмодиофоромицеты, хитридиомицеты, зигомицеты, аскомицеты, базидиомицеты и дейтеромицеты, и/или для борьбы с оомицетами, более предпочтительно для борьбы с Basidiomycetes (вызывающими заболевания ржавчины).
Настоящее изобретение также относится к способу борьбы с нежелательными фитопатогенными микроорганизмами, такими как фитопатогенные грибы, оомицеты и бактерии, включающему стадию нанесения по меньшей мере одного соединения формулы (I) или (II) или по меньшей мере одной композиции согласно настоящему изобретению на микроорганизмы и/или их среду обитания (на растения, части растений, семена, плоды или почву, на которой растения растут).
Как правило, когда соединение и композиция согласно настоящему изобретению используются в лечебных или защитных методах борьбы с фитопатогенными грибами и/или фитопатогенными оомицетами, их эффективное и совместимое с растениями количество наносят на растения, части растений, плоды, семена или на почву или субстраты, на которых растут растения. Подходящие субстраты, которые можно использовать для выращивания растений, включают субстраты на неорганической основе, такие как минеральная вата, в частности каменная вата, перлит, песок или гравий; органические субстраты, такие как торф, сосновая кора или опилки; и субстраты на нефтяной основе, такие как полимерные пены или пластиковые шарики. Эффективное и совместимое с растениями количество означает количество, которое достаточно для борьбы или уничтожения грибов, присутствующих или способных появиться на пахотных землях, и которое не влечет за собой каких-либо заметных симптомов фитотоксичности для указанных культур. Такое количество может варьироваться в широком диапазоне в зависимости от грибка, который необходимо контролировать, типа культуры, стадии роста культуры, климатических условий и соответствующего соединения или композиции согласно настоящему изобретению. Это количество может быть определено путем систематических полевых испытаний, которые находятся в пределах возможностей специалиста в данной области техники.
Растения и части растений
Соединения формулы (I) или (II) и содержащие их композиции наносят на любое из растений или частей растений.
Растения в контексте настоящего изобретения понимаются в значении все растения и популяции растений, такие как желательные и нежелательные дикорастущие растения или культурные растения (включая встречающиеся в природе культурные растения). Культурные растения могут быть растениями, которые могут быть получены традиционными методами селекции и оптимизации, или методами биотехнологии и генной инженерии, или комбинацией этих методов, включая генетически модифицированные растения (ГМО или трансгенные растения) и включая сорта растений, которые охраняются и не охраняются правами селекционеров.
Части растений понимаются в значении все части и органы растений, расположенных выше и ниже земли, такие как побег, лист, цветок и корень, примеры которых включают в себя листья, иглы, стебли, черешки, цветы, плодовые тела, плоды и семена, а также корни, клубни и корневища. Части растений также включают урожай, а также материал для вегетативного и генеративного размножения, например, черенки, клубни, корневища, отводки и семена
Растения, которые можно лечить (обрабатывать) в соответствии со способом согласно настоящему изобретению, включают следующие: хлопок, лен, виноградная лоза, фрукты, овощи, такие как Rosaceae sp. (например семечковые плоды, такие как яблоки и груши, а также косточковые фрукты, такие как абрикосы, вишни, миндаль и персики, и ягоды, такие как клубника), Ribesioidae sp., Juglandaceae sp., Betulaceae sp., Anacardiaceae sp., Fagaceae sp., Moraceae sp., Oleaceae sp., Actinidaceae sp., Lauraceae sp., Musaceae sp. (например, банановые деревья и плантации), Rubiaceae sp. (например, кофе), Theaceae sp., Sterculiceae sp., Rutaceae sp. (например, лимон, апельсин и грейпфрут); Solanaceae sp. (например, томаты), Liliaceae sp., Asteraceae sp. (например, салат-латук), Umbelliferae sp., Cruciferae sp., Chenopodiaceae sp., Cucurbitaceae sp. (например, огурец), Alliaceae sp. (например, лук-порей, лук), Papilionaceae sp. (например, горох); основные культурные растения, такие как Graminae sp. (например, кукуруза, торф, зерновые, такие как пшеница, рожь, рис, ячмень, овес, просо и тритикале), Asteraceae sp. (например, подсолнух), Brassicaceae sp. (например, белая капуста, красная капуста, брокколи, цветная капуста, брюссельская капуста, пекинская капуста, кольраби, редис и масленичный рапс, горчица, хрен и кресс-салат), Fabacae sp. (например, фасоль, арахис), Papilionaceae sp. (например, соя), Solanaceae sp. (например, картофель), Chenopodiaceae sp. (например, сахарная свекла, кормовая свекла, листовая свекла, свекла); полезные растения и декоративные растения для садов и лесистых мест; и генетически модифицированные сорта каждого из этих растений
Согласно некоторым предпочтительным вариантам осуществления растения дикого типа и сорта растений или растения, полученные обычными биологическими методами селекции, такими как скрещивание или слияние протопластов, а также их части, обрабатывают в соответствии со способами согласно настоящему изобретению.
Согласно некоторым предпочтительным вариантам осуществления трансгенные растения и сорта растений, полученные методами генной инженерии, при необходимости в комбинации с обычными методами (генетически модифицированные организмы), и их части обрабатывают в соответствии со способами согласно настоящему изобретению. Более предпочтительно, растения тех сортов растений, которые являются коммерчески доступными или используются, обрабатывают в соответствии с настоящим изобретением. Сорта растения представляют собой растения, обладающие новыми характеристиками ("особенностями"), которые придаются с помощью обычного скрещивания, мутагенеза или способа с использованием рекомбинантных ДНК. Ими могут быть культивары, биотипы или генотипы.
Способ согласно настоящему изобретению могут применяться при обработке генетически модифицированных организмов (ГМО), например, растений или семян. Генетически модифицированные растения (или трансгенные растения) представляют собой растения, в которых гетерологичный ген был стабильно интегрирован в геном. Выражение "гетерологичный ген" по существу означает ген, который обеспечивается или собирается вне растения, и при введении в ядерный, хлоропластный или митохондриальный геном придает трансформированному растению новые или улучшенные агрономические или другие свойства посредством экспрессии белка или полипептида, представляющего интерес, или посредством понижающей регуляции или сайленсинга других гена(генов), которые присутствуют в растении (с использованием, например, антисмысловой технологии, технологии косупрессии, технологии РНК-интерференции (РНКи) или технологии микроРНК (miPHK)). Гетерологичный ген, который располагается в геноме, также называют трансгеном. Трансген, который определяют по его конкретному расположению в геноме растения, именуют трансформационным или трансгенным событием.
Растения и сорта растений, которые, предпочтительно, подлежат обработке согласно изобретению, включают все растения, которые имеют генетический материал, который придает, в частности, преимущественные, полезные признаки этим растениям (вне зависимости от того получены ли они селекцией и/или биотехнологическими средствами).
Растения и сорта растений, которые также предпочтительно подлежат обработке в соответствии с настоящим изобретением, являются резистентными против одного или нескольких биотических стрессов, т.е. указанные растения показывают лучшую защиту против животных и микробных вредителей, как например, против нематод, насекомых, клещей, фитопатогенных грибков, бактерий, вирусов и/или вироидов.
Растения и сорта растений, которые также могут быть обработаны в соответствии с настоящим изобретением, представляют собой такие растения, которые являются резистентными к одному или более абиотическим стрессам. Условия абиотического стресса могут включать, например, засуху, воздействие холодной температуры, воздействие тепла, осмотический стресс, затопление, увеличенную соленость почвы, увеличенное минеральное воздействие, воздействие озона, воздействие высокой освещенности, ограниченную доступность азотных питательных компонентов, ограниченную доступность фосфорных питательных компонентов, избегание затененности.
Растения и сорта растений, которые также могут быть обработаны в соответствии с настоящим изобретением, представляют собой растения, характеризующиеся повышенными характеристиками урожайности. Повышенная урожайность у указанных растений может быть результатом, например, улучшенных физиологии, роста и развития растения, как например, эффективность использования воды, эффективность удерживания воды, улучшенное использование азота, повышенная ассимиляция углерода, улучшенный фотосинтез, повышенная эффективность прорастания и ускоренное созревание. На урожайность, кроме того, можно воздействовать посредством улучшенной архитектуры растения (в условиях стресса и отсутствия стресса), включая, но без ограничения к этому, раннее цветение, контроль цветения для получения гибридных семян, мощность проростков, размер растения, число междоузлий и расстояние, рост корня, размер семян, размер плодов, размер стручков, число стручков или колосков, число семян на стручок или колосок, масса семян, повышенное заполнение семенами, сниженный разброс семян, сниженное раскрывание стручка и резистентность к полеганию. Дополнительные признаки урожайности включают состав семян, такой как содержание углеводов, и состав, например, хлопка или крахмала, содержание белка, содержание и состав масла, пищевая ценность, снижение антипищевых соединений, улучшенная перерабатываемость и лучшая стабильность при хранении.
Растения, которые могут быть обработаны в соответствии с настоящим изобретением, представляют собой гибридные растения, которые уже экспрессируют характеристику гетерозиса или гибридную мощность, что приводит, в целом, к более высокой урожайности, жизненности, здоровью и резистентности к биотическим и абиотическим стрессам.
Растения или сорта растений (полученные посредством методов биотехнологии растений, таких как генетическая инженерия), которые могут быть обработаны в соответствии с настоящим изобретением, представляют собой гербицид о стойкие растения, т.е. растения, сделанные толерантными к одному или нескольким данным гербицидам. Такие растения могут быть получены либо посредством генетической трансформации, либо посредством селекции растений, содержащих приданную мутацию, такую как гербицидостойкость.
Растения или сорта растений (полученные посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением, представляют собой резистентные к насекомым трансгенные растения, т.е. растения, сделанные резистентными к нападению некоторых целевых насекомых. Такие растения могут быть получены посредством генетической трансформации, или посредством селекции растений, содержащих мутацию, придающую такую резистентность к насекомым.
Растения или сорта растений (полученные методами биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением, являются толерантными к абиотическим стрессам. Такие растения могут быть получены посредством генетической трансформации или посредством селекции растений, содержащих мутацию, придающую такую резистентность к стрессу.
Растения или сорта растений (полученные посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением показывают измененное количество, качество и/или стабильность при хранении собираемого продукта и/или измененные свойства конкретных ингредиентов собираемого продукта.
Растения или сорта растений (которые могут быть получены посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением, представляют собой растения, такие как хлопчатники, с измененными волокнистыми характеристиками. Такие растения могут быть получены посредством генетической трансформации или посредством селекции растений и содержат мутацию, придающую такую измененную волокнистую характеристику.
Растения или сорта растений (которые могут быть получены посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением представляют собой растения, такие как масличные рапсовые или родственные растения Brassica, с измененными характеристиками масличного профиля. Такие растения могут быть получены посредством генетической трансформации, или посредством селекции растений, содержащих мутацию, придающую такие измененные характеристики масличного профиля.
Растения или сорта растений (которые могут быть получены посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением представляют собой растения, такие как масличный рапс или растения Brassica, с измененными характеристиками осыпания семян. Такие растения могут быть получены посредством генетической трансформации, или посредством селекции растений, содержащих мутацию, придающую такие измененные характеристики осыпания семян, и включают растения, такие как масличного рапса с замедленной или уменьшенной осыпанием семян.
Растения или сорта растений (которые могут быть получены посредством методов биотехнологии растений, таких как генетическая инженерия), которые также могут быть обработаны в соответствии с настоящим изобретением представляют собой растения, такие как растения Tobacco, с измененными моделями посттрансляционной модификации белка.
Патогены и заболевания
Способы, раскрытые выше, могут применяться для борьбы с микроорганизмами, в частности фитопатогенными микроорганизмами, такими как фитопатогенные грибы, вызывающие заболевания, такие как:
заболевания, вызванные патогенами мучнистой росы, такими как виды Blumeria (например, Blumeria graminis), виды Podosphaera (например, Podosphaera leucotricha), виды Sphaerotheca (например, Sphaerotheca fuliginea), виды Uncinula (например, Uncinula necator);
заболевания, вызванные патогенами ржавчинного заболевания, такими как виды Gymnosporangium (например, Gymnosporangium sabinae), виды Hemileia (например, Hemileia vastatrix), вид Phakopsora (например, Phakopsora pachyrhizi или Phakopsora meibomiae), виды Puccinia (например, Puccinia recondita, Puccinia graminis или Puccinia striifbrmis), виды Uromyces (например, Uromyces appendiculatus);
заболевания, вызванные патогенами из группы Oomycetes, такими как виды Albugo (например, Albugo Candida), виды Bremia (например, Bremia lactucae), виды Peronospora (например, Peronospora pisi или Р. brassicae), виды Phytophthora (например, Phytophthora infestans), виды Plasmopara (например, Plasmopara viticola), виды Pseudoperonospora (например, Pseudoperonospora humuli или Pseudoperonospora cubensis), виды Pythium (например, Pythium ultimum);
болезни пятнистости листьев и заболевания увядания листьев, вызванные, например, видами Altemaria (например, Alternaria solani), видами Cercospora (например, Cercospora beticola), видами Cladiosporium (например, Cladiosporium cucumerinum), видами Cochliobolus (например, Cochliobolus sativus (кондиальная форма: Drechslera, syn: Helminthosporium) или Cochliobolus miyabeanus), видами Colletotrichum (например, Colletotrichum lindemuthanium), видами Cycloconium (например, Cycloconium oleaginum), видами Diaporthe (например, Diaporthe citri), видами Elsinoe (например, Elsinoe fawcettii), видами Gloeosporium (например, Gloeosporium laeticolor), видами Glomerella (например, Glomerella cingulata), видами Guignardia (например, Guignardia bidwelli), видами Leptosphaeria (например, Leptosphaeria maculans), видами Magnaporthe (например, Magnaporthe grisea), видами Microdochium (например, Microdochium nivale), видами Mycosphaerella (например, Mycosphaerella graminicola, Mycosphaerella arachidicola или Mycosphaerella fijiensis), видами Phaeosphaeria (например, Phaeosphaeria nodorum), видами Pyrenophora (например, Pyrenophora teres или Pyrenophora tritici repentis) видом Ramularia (например, Ramularia collo-cygni или Ramularia areola), видами Rhynchosporium (например, Rhynchosporium secalis), видами Septoria species (например, Septoria apii или Septoria lycopersici), видами Stagonospora (например, Stagonospora nodorum), видами Typhula (например, Typhula incarnate), видами Venturia (например, Venturia inaequalis),
заболевания корней и стеблей, вызванные, например, видами Corticium (например, Corticium gramineamm), видами Fusarium (например, Fusarium оксиsporum), видами Gaeumannomyces, (например, Gaeumannomyces graminis), видами Plasmodiophora, (например, Plasmodiophora brassicae), видами Rhizoctonia, (например, Rhizoctonia solani), видами Sarocladium, (например, Sarocladium oryzae), видами Sclerotium, (например, Sclerotium oryzae), видами Tapesia, (например, Tapesia acuformis), видами Thielaviopsis, (например, Thielaviopsis basicola);
заболевания початка и метелок (включая кукурузные початки), вызванные, например, видами Alternaria (например, Alternaria spp.), видами Aspergillus (например, Aspergillus flavus), видами Cladosporium (например, Cladosporium cladosporioides), видами Claviceps (например, Claviceps ригрмочевина), видами Fusarium, (например, Fusarium culmorum), видами Gibberella (например, Gibberella zeae), видами Monographella, (например, Monographella nivalis), видами Stagnospora (например, Stagnospora nodorum);
заболевания, вызываемые грибами головневых, например, видами Sphacelotheca (например, Sphacelotheca reiliana), видами Tilletia (например, Tilletia caries или Tilletia controversa), видами Urocystis (например, Urocystis occulta), видами Ustilago (например, Ustilago nuda);
гниль плодов, вызываемая, например, видами Aspergillus (например, Aspergillus flavus), видами Botrytis (например, Botrytis cinerea), видами Penicillium (например, Penicillium expansum или Penicillium purpurogenum), видами Rhizopus (например, Rhizopus stolonifer), видами Sclerotinia (например, Sclerotinia sclerotiorum), видами Verticilium (например, Verticilium alboatrum);
обсеменение и передающиеся через почву или с почвой гниение, а также болезни саженцев, вызванные, например, видами Alternaria (например, Alternaria brassicicola), видами Aphanomyces (например, Aphanomyces euteiches), видами Ascochyta (например, Ascochyta lentis), видами Aspergillus (например, Aspergillus flavus), видами Cladosporium (например, Cladosporium herbarum), видами Cochliobolus (например, Cochliobolus sativus (конидиальная форма: Drechslera, Bipolaris Syn: Helminthosporium)), видами Colletotrichum (например, Colletotrichum coccodes), видами Fusarium (например, Fusarium culmorum), видами Gibberella (например, Gibberella zeae), видами Macrophomina (например, Macrophomina phaseolina), видами Microdochium (например, Microdochium nivale), видами Monographella (например, Monographella nivalis), видами Penicillium (например, Penicillium expansum), видами Phoma (например, Phoma lingam), видами Phomopsis (например, Phomopsis sojae), видами Phytophthora (например, Phytophthora cactorum), видами Pyrenophora (например, Pyrenophora graminea), видами Pyricularia (например, Pyricularia oryzae), видами Pythium (например, Pythium ultimum), видами Rhizoctonia (например, Rhizoctonia solani), видами Rhizopus (например, Rhizopus oryzae), видами Sclerotium (например, Sclerotium rolfsii), видами Septoria (например, Septoria nodorum), видами Typhula (например, Typhula incarnate), видами Verticillium (например, Verticillium dahlia);
раковые заболевания, галлы и ведьмины метлы, вызванные, например, видами Nectria (например, Nectria galligena);
вилт заболевания, вызванные, например, видами Monilinia (например, Monilinia laxa);
деформации листьев, цветов и плотов, вызванные, например, видами Exobasidium (например, Exobasidium vexans), видами Taphrina (например, Taphrina deformans);
дегенеративные заболевания древесных растений, вызванные, например, видами Esca (например, Phaeomoniella chlamydospora, Phaeoacremonium aleophilum или Fomitiporia mediterranea), видами Ganoderma (например, Ganoderma boninense);
заболевания цветов и семян, вызванные, например, видами Botrytis (например, Botrytis cinerea);
заболевания клубней растений, вызванные, например, видами Rhizoctonia (например, Rhizoctonia solani), видами Helminthosporium (например, Helminthosporium solani);
заболевания, вызванные бактериальными патогенами, например, видами Xanthomonas (например, Xanthomonas campestris pv. Oryzae), видами Pseudomonas (например, Pseudomonas syringae pv. Lachrymans), видами Erwinia (например, Erwinia amylovora).
Обработка семян
Способ борьбы с нежелательными микроорганизмами может использоваться для защиты семян от фитопатогенных микроорганизмов, таких как грибы.
Термин "семя(семена)", как применяется в настоящем документе, включает покоящееся семя, грунтованное семя, предварительно проросшее семя и семя с появившимися корнями и листьями.
Таким образом, настоящее изобретение также относится к способу защиты семян и/или сельскохозяйственных культур от нежелательных микроорганизмов, таких как бактерии или грибы, который включает стадию обработки семян одним или более соединениями формулы (I) или (II) или композицией, содержащая их. Обработка семян соединением (соединениями) формулы (I) или (II) или композицией, содержащей их, защищает не только семена от фитопатогенных микроорганизмов, но также прорастающие растения, проросшие проростки и растения после появления всходов.
Обработку семян можно проводить перед посевом, во время посева или вскоре после него.
Когда обработка семян выполняется перед посевом (например, так называемые обработки на семе), обработка семян может быть выполнена следующим образом: семена могут быть помещены в смеситель с желаемым количеством соединения (соединений) формулы (I) или (II) или композиции, содержащей их (либо как таковой, либо после разбавления), семена и соединение (соединения) формулы (I) или (II) или композицию, содержащую их, смешивают до достижения гомогенного распределения на семенах. При необходимости семена можно высушить.
Настоящее изобретение также относится к семенам, обработанным одним или более соединениями (I) или композицией, содержащей их. Как было указано ранее, использование обработанных семян позволяет не только защищать семена до и после посева от нежелательных микроорганизмов, таких как фитопатогенные грибы, но также позволяет защитить прорастающие растения и молодые проростки, появляющиеся из указанных обработанных семян. Большая часть повреждений сельскохозяйственных культур, вызванных вредными организмами, вызвана заражением семян перед посевом или после прорастания растений. Эта фаза особенно важна, поскольку корни и побеги растущего растения особенно чувствительны, и даже небольшое повреждение может привести к гибели растения.
Следовательно, настоящее изобретение также относится к способу защиты семян, прорастающих растений и проросших проростков, в более общем плане к способу защиты сельскохозяйственных культур от фитопатогенных микроорганизмов, который включает стадию применения семян, обработанных одним или более соединениями формулы (I) или (II) или композицией, содержащей их.
Предпочтительно семя обрабатывают в состоянии, в котором оно достаточно устойчиво к повреждениям, которые могут случиться в процессе обработки. В общем, семена можно обработать в любое время в период от некоторого времени после посева до сбора урожая. Принято использовать семя, которое было отделено от растения и освобождено от початков, шелухи, стеблей, оболочек, волосков или мякоти плодов. Например, можно использовать семя, которое было собрано, очищено и высушено до содержания влаги менее чем 15 мас. %. В качестве альтернативы можно также использовать семя, которое после сушки, например, было обработано водой и затем снова высушено, или семена сразу после прайминга, или семена, хранящиеся в условиях прайминга, или предварительно проросшие семена, или семена, высеянные в брудерный лоток, ленты или бумагу.
Количество соединения (соединений) формулы (I) или (II) или содержащей их композиции, наносимое на семена, обычно является таким, что прорастание семян не ухудшается, или полученное растение не повреждено. Это должно быть обеспечено, в частности, в случае, если активные ингредиенты будут проявлять фитотоксические эффекты при определенных дозах применения. Присущие фенотипы трансгенных растений также следует принимать во внимание при определении количества соединения (соединений) формулы (I) или (II) или композиции, содержащей их, для нанесения на семена для получения оптимальной защиты семян и прорастающих растений с использованием минимального количества соединения (соединений формулы (I) или (II) или композиции, содержащей их.
Как указано выше, соединения формулы (I) или (II) могут наноситься как таковые, непосредственно на семена, т.е. без применения любых других компонентов и без разбавления, или может применяться композиция соединения формулы (I) или (II). Предпочтительно, композиции наносят на семена в любой подходящей форме. Примеры подходящих составов включают растворы, эмульсии, суспензии, порошки, пены, взвеси или в сочетании с другими композициями для покрытия семян, такими как пленкообразующие материалы, гранулирующие материалы, тонкоизмельченные порошки железа или других металлов, гранулы, материал для покрытия для инактивированных семян, а также ULV препараты. Составами могут быть готовые для применения составы или концентраты, которые необходимо разбавить перед применением.
Эти составы готовят известными методами, путем смешивания активных ингредиентов или комбинаций активных ингредиентов с обычными добавками, например, такими как обычные наполнители и растворители или разбавители, красители, смачивающие средства, диспергирующие средства, эмульгаторы, противовспениватели, консерванты, вторичные загустители, адгезивы, гиббереллины, а также вода.
Эти составы готовят известными методами, путем смешивания активных ингредиентов или комбинаций активных ингредиентов с обычными добавками, например, такими как обычные наполнители и растворители или разбавители, красители, смачивающие средства, диспергирующие средства, эмульгаторы, противовспениватели, консерванты, вторичные загустители, адгезивы, гиббереллины, а также вода.
Полезными красителями, которые могут присутствовать в композициях для протравливания семян являются любые красители, которые являются обычными для таких целей. Можно использовать либо пигменты, которые плохо растворимы в воде, либо красители, растворимые в воде. Примеры включают в себя красители, известные под названиями родамин В, C.I. Pigment Red 112 и C.I. Solvent Red 1. Полезные смачивающие средства, которые могут присутствовать в композициях для протравливания семян являются любые вещества, способствующие смачиванию, и которые обычно используются для композиций активных агрохимических ингредиентов. Предпочтение отдается использованию алкилнафталинсульфонатов, таких как диизопропил- или диизобутилнафталинсульфонаты. Полезные диспергирующие средства и/или эмульгаторы, которые могут присутствовать в композициях для протравливания семян представляют собой любые неионные, анионные и катионные диспергирующие средства, обычно используемые для композиции активных агрохимических ингредиентов. Предпочтительно используются неионные или анионные диспергирующие средства или смеси неионных или анионных диспергирующих средств. Подходящие неионные диспергирующие средства включают в частности блок-полимеры этиленоксид/пропиленоксид, алкилфенол-полигликолевые эфиры и тристирилфенол-полигликолевый эфир и их фосфатированные или сульфатированные производные. В качестве анионных диспергирующих средств особенно применяются лигносульфонаты, соли полиакриловой кислоты и конденсаты арилсульфонат/формальдегид. Противоспениватели, которые могут присутствовать в композициях для протравливания семян представляют собой любые ингибирующие пенообразование вещества, обычно используемые для композиции активных агрохимических ингредиентов. Предпочтительно могут быть использованы силиконовые пеногасители и стеарат магния. Консерванты, которые могут присутствовать в композициях для протравливания семян представляют собой любые вещества, используемые для таких целей в агрохимических композициях. Примеры включают дихлорофен и полуформаль бензилового спирта. В качестве вторичных загустителей, которые могут содержаться в композициях для протравливания семян, используют любые вещества, применяемые для подобной цели в агрохимических средствах. Предпочтительными являются производные целлюлозы, производные акриловой кислоты, ксантан, модифицированные глины и высокодисперсная кремниевая кислота. Адгезивы, которые могут присутствовать в композициях для протравливания семян представляют собой любые обычные связующие, используемые в продуктах для протравливания семян. Предпочтительные примеры включают поливинилпирролидон, поливинилацетат, поливиниловый спирт и тилозу.
Соединения формулы (I) или (II) и композиции, содержащие их, пригодны для защиты семян любого сорта растений, который используется в сельском хозяйстве, в теплицах, в лесах или в садоводстве и виноградарстве. В частности, это могут быть семена зерновых культур (таких как пшеница, ячмень, рожь, просо и овес), масличного рапса, кукурузы, хлопка, сои, риса, картофеля, подсолнечника, фасоли, кофе, свеклы (например, сахарная свекла и кормовая свекла), арахиса, овощей (таких как томаты, огурец, лук и салат-латук), травы для газонов и декоративных растений. Особое значение имеет обработка семян пшеницы, сои, масличного рапса, кукурузы и риса.
Соединения формулы (I) или (II) и композиции, содержащие их, могут применяться для протравливания семян трансгенных растений. В этом случае дополнительные синергетические эффекты могут также возникать при взаимодействии с веществами, образованными посредством экспрессии.
Нематоды
В данном контексте термин «нематоды» включает все виды типа Nematoda и, в частности, виды, действующие как паразиты на растениях или грибах (например, виды отряда Aphelenchida, Meloidogyne, Tylenchida и другие) или же на людях и животных (например, виды отрядов Trichinellida, Tylenchida, Rhabditina и Spinirida) и вызывающие повреждение этих живых организмов или на них, а также другие паразитические гельминты.
Нематоцид для защиты растений, как описано в настоящем документе, способен контролировать нематоды.
Термин "борьба с нематодами" означает уничтожение нематод или предотвращение или препятствование их развитию или их росту, или предотвращение или препятствование их проникновению в ткани растения или их присасыванию к ткани растения.
Здесь эффективность соединений определяют путем сравнения смертности, образования галлов, образования кист, плотности нематод на объем почвы, плотности нематод на корень, количества яиц нематод на объем почвы, подвижности нематод между растением или частью растения, обработанными соединением формулы (I) или (II), или обработанной почвой и необработанным растением или частью растения или необработанной почвой (100%). Предпочтительно достигаемое снижение составляет 25-50% по сравнению с необработанным растением, частью растения или необработанной почвой, особенно предпочтительно 51-79% и особенно предпочтительно полное уничтожение или полное предотвращение развития и роста нематод с помощью снижение от 80 до 100%. Борьба с нематодами, как описано в настоящем документе, также включает контроль размножения нематод (развитие цист и/или яиц). Соединения формулы (I) или (II) можно также использовать для поддержания здоровья растений или животных, и их можно применять в лечебных, профилактических или системных целях для борьбы с нематодами.
Специалисту в данной области техники известны способы определения смертности, галлообразования, цистообразования, плотности нематод на объем почвы, плотности нематод на корень, количества яиц нематод на объем почвы, подвижности нематод.
Применение соединения формулы (I) или (II) может поддерживать здоровье растения, а также включает снижение повреждений, вызванных нематодами, и повышение урожайности.
В данном контексте термин «нематоды» относится к нематодам растений, которые включают все нематоды, повреждающие растения. Нематоды растений включают фитопаразитические нематоды и почвенные нематоды. Фитопаразитические нематоды включают эктопаразитов, таких как Xiphinema spp., Longidoms spp. и Trichodonis spp.; полупаразиты, такие как Tyienchulus spp.; мигрирующие эндопаразиты, такие как Pratylenchus spp., Radopholus spp. и виды скутеллонемы; немигрирующие паразиты, такие как Heterodera spp., Globodera spp. и Meloidogyne spp., а также стеблевые и листовые эндопаразиты, такие как Ditylenchus spp., Aphelenchoides spp. и Hirschmaniella spp. Особенно вредными корневыми паразитическими почвенными нематодами являются, например, цистообразующие нематоды родов Heterodera или Globodera и/или корневые галловые нематоды рода Meloidogyne. Вредоносными видами этих родов являются, например, Meloidogyne incognita, Heterodera glycines (цистообразующая нематода соевых бобов), Globodera pallida и Globodera rostochiensis (желтоклеточная нематода картофеля), причем эти виды эффективно контролируются соединениями, описанными в настоящем тексте. Однако применение соединений, описанных в настоящем документе, никоим образом не ограничивается этими родами или видами, а также распространяется таким же образом на другие нематоды.
К растительным нематодам относятся, например, Aglenchus agricola, Anguina tritici, Aphelenchoides arachidis, Aphelenchoides fragaria, эндопаразиты стебля и листьев Aphelenchoides spp., Belonolaimus gracilis, Belonolaimus longicaudatus, Belonolaimus nortoni, Bursaphelenchus cocophilus, Bursaphelenchuppus eremus, Bursaphelenchus xylophilus, Cacopaums pestis, Criconemella curvata, Criconemella onoensis, Criconemella omata, Criconemella rusium, Criconemella xenoplax (=Mesocriconema xenoplax) и Criconemella spp., Criconemoides femiae, Criconemoides onoense, Criconemoides omatum и Criconemoides spp., Ditylenchus destructor, Ditylenchus dipsaci а также стеблевые и листовые эндопаразиты Ditylenchus spp., Dolichodorus heterocephalus, Globodera pallida (=Heterodera pallida), Globodera rostochiensis (желтая картофельная цистообразующая нематода), Globodera solanacearum, Globodera tabacum, Globodera Virginia и немигрирующие цистообразующие паразиты Globodera spp., Helicotylenchus digonicus, Helicotylenchus dihystera, Helicotylenchus erythrine, Helicotylenchus multicinctus, Helicotylenchus nannus, Helicotylenchus pseudorobustus и Helicotylenchus spp., Hemicriconemoides, Hemicycliophora arenaria, Hemicycliophora nudata, Hemicycliophora parvana, Heterodera avenae, Heterodera cruciferae, Heterodera glycines (цистовая нематода соевых бобов), Heterodera oryzae, Heterodera schachtii, Heterodera zeae и немигрирующих цистообразующих паразитов Heterodera spp., Hirschmaniella gracilis, Hirschmaniella oryzae, Hirschmaniella spinicaudata и стеблевых и листовых эндопаразитов Hirschmaniella spp., Hoplolaimus aegyptii, Hoplolaimus califomicus, Hoplolaimus colifomicus, Hoplolaimus califomicus, Hoplolaimus califomicus, Hoplolaimus califomicus Hoplolaimus galeatus, Hoplolaimus indicus, Hoplolaimus magnistylus, Hoplolaimus pararobustus, Longidorus africanus, Longidorus breviannulatus, Longidorus elongatus, Longidorus laevicapitatus, Longidorus vineacola и эктопаразиты Longidorus spp., Meloidogyne acronea, Meloidogyne afric ana, Meloidogyne arenaria, Meloidogyne arenaria thamesi, Meloidogyne artiella, Meloidogyne chitwoodi, Meloidogyne coffeicola, Meloidogyne ethiopica, Meloidogyne exigua, Meloidogyne fallax, Meloidogyne graminicola, Meloidogyne graminis, Meloidogyne hapla, Meloidogyne incognita, Meloidogyne incognita acrita, Meloidogyne javanica, Meloidogyne kikuyensis, Meloidogyne minor, Meloidogyne naasi, Meloidogyne paranaensis, Meloidogyne thamesi и немигрирующие паразиты Meloidogyne spp., Meloinema spp., Nacobbus aberrans, Neotylenchus vigissi, Paraphelenchus pseudoparietinus, Paratrichodorus allius, Paratrichodorus lobatus, Paratrichodorus minor, Paratrichodorus porosterosterus nanus, Paratrichodorus nanus, Paratrichodorus nanus и Paratrichodorus spp., Paratylenchus hamatus, Paratylenchus minutus, Paratylenchus projectus и Paratylenchus spp., Pratylenchus agilis, Pratylenchus alleni, Pratylenchus andinus, Pratylenchus brachyurus, Pratylenchus злаковый, Pratylenchus coffeae, Pratylenchus crenatus. Prat yienchus delattrei, Pratylenchus giibbicaudatus, Pratylenchus goodeyi, Pratylenchus hamatus, Pratylenchus hexincisus, Pratylenchus loosi, Pratylenchus neglectus, Pratylenchus penetrans, Pratylenchus pratensis, Pratylenchus scribneri, Pratylenchus teres, Pratylenchus thomei, Pratylenchus vulnus, Pratylenchus zeae и мигрирующие эндопаразиты Pratylenchus spp., Pseudohalenchus minutus, Psilenchus magnidens, Psilenchus tumidus, Punctodera chalcoensis, Quinisulcius acutus, Radopholus citrophilus, Radopholus similis, the migratory endoparasites Radopholus spp., Rotylenchulus borealis, Rotylenchulus parvus, Rotylenchulus reniformis и Rotylenchulus spp., Rotylenchus laurentinus, Rotylenchus macrodoratus, Rotylenchus robustus, Rotylenchus uniformis и Rotylenchus spp., Scutellonema brachyurum, Scutellonema bradys, Scutellonema clathricaudatum и мигрирующие эндопаразиты Scutellonema spp., Subanguina radiciola, Tetylenchus nicotianae, Trichodorus cylindricus, Trichodorus minor, Trich odorus primitivus, Trichodorus proximus, Trichodorus similis, Trichodorus sparsus и эктопаразиты Trichodorus spp., Tyienchorhynchus agri, Tyienchorhynchus brassicae, Tyienchorhynchus clams, Tyienchorhynchus claytoni, Tyienchorhynchus digitatus, Tyienchorhynchus ebriensis, Tyienchorhynchus maximus, Tyienchorhynchus nudus, Tyienchorhynchus vulgaris и Tyienchorhynchus spp., Tyienchulus semipenetrans и полупаразиты Tyienchulus spp., Xiphinema americanum, Xiphinema brevicolle, Xiphinema dimorphicaudatum, Xiphinema index и эктопаразиты Xiphinema spp.
Нематоды, для борьбы с которыми может быть использовано соединение формулы (I) или (II), включают нематоды рода Meloidogyne, такие как южная галловая нематода (Meloidogyne incognita), яванская галловая нематода (Meloidogyne javanica), северная галловая нематода - галловая нематода (Meloidogyne hapla) и галловая нематода арахисового корня (Meloidogyne arenaria); нематоды рода Ditylenchus, такие как нематода картофельной гнили (Ditylenchus destructor) и стеблевая и луковичная нематода (Ditylenchus dipsaci); нематоды рода Pratylenchus, такие как нематода, поражающая корни початка (Pratylenchus penetrans), нематода, поражающая корни хризантемы (Pratylenchus fallax), нематода из кофейного корня (Pratylenchus coffeae), нематода из чайного корня (Pratylenchus loosi) и корень грецкого ореха - поражение нематодой (Pratylenchus vulnus); нематоды рода Globodera, такие как желтая картофельная нематода (Globodera rostochiensis) и белая картофельная нематода (Globodera pallida); нематоды рода Heterodera, такие как соевая нематода (Heterodera glycines) и свекловичная нематода (Heterodera schachtii); нематоды рода Aphelenchoides, такие как рисовая белокрылая нематода (Aphelenchoides besseyi), хризантемная нематода (Aphelenchoides ritzemabosi) и земляничная нематода (Aphelenchoides fragariae); нематоды рода Aphelenchus, такие как грибоядная нематода (Aphelenchus avenae); нематоды рода Radopholus, такие как роющая нематода (Radopholus similis); нематоды рода Tyienchulus, такие как цитрусовая корневая нематода (Tyienchulus semipenetrans); нематоды рода Rotylenchulus, такие как почковидная нематода (Rotylenchulus renifbrmis); живущие на деревьях нематоды, такие как нематода из соснового леса (Bursaphelenchus xylophilus) и нематода с красным кольцом (Bursaphelenchus cocophilus) и им подобные.
Растения, для защиты которых может быть использовано соединение формулы (I) или (II), включают такие растения, как злаки (например, рис, ячмень, пшеница, рожь, овес, кукуруза и т.п.), бобы (соевые бобы, фасоль адуки, фасоль, бобы, горох, арахис и т.п.), фруктовые деревья/фрукты (яблоки, цитрусовые, груши, виноград, персики, японские абрикосы, вишня, грецкие орехи, миндаль, бананы, клубника и т.п.), виды овощей (капуста, помидоры, шпинат, брокколи, салат, лук, зеленый лук, перец и т.п.), корнеплоды (морковь, картофель, батат, редис, корень лотоса, репа и т.п.), растения для промышленного сырья (хлопок, конопля, бумага шелковица, митсумата, рапс, свекла, хмель, сахарный тростник, сахарная свекла, оливки, каучуконосы, пальмы, кофе, табак, чай и т.п.), тыквенные (тыква, огурец, арбуз, дыня и т.п.), луговые растения (ежа, сорго, тимофеевка, клевер, люцерна и т.п.), газонные травы (маскареновая трава, полевица и т.п.), пряные растения и т.п. (лаванда, розмарин, тимьян, петрушка, перец, имбирь и т.п.) и цветы (хризантемы, розы, орхидеи и т.п.).
Соединения формулы (I) или (II) особенно подходят для борьбы с кофейными нематодами, в частности, Pratylenchus brachyurus, Pratylenchus coffeae, Meloidogyne exigua, Meloidogyne incognita, Meloidogyne coffeicola, Helicotylenchus spp. и Meloidogyne paranaensis, Rotylenchus spp., Xiphinema spp., Tyienchorhynchus spp. и Scutellonema spp.
Соединения формулы (I) или (II) особенно подходят для борьбы с картофельными нематодами, в частности, Pratylenchus brachyurus, Pratylenchus pratensis, Pratylenchus scribneri, Pratylenchus penetrans, Pratylenchus coffeae, Ditylenchus dipsaci и of Pratylenchus alleni, Pratylenchus andinus, Pratylenchus cerealis, Pratylenchus crenatus, Pratylenchus hexincisus, Pratylenchus loosi, Pratylenchus neglectus, Pratylenchus teres, Pratylenchus thomei, Pratylenchus vulnus, Belonolaimus longicaudatus, Trichodoms cylindricus, Trichodoms primitivus, Trichodorus proximus, Trichodorus similis, Trichodoms sparsus, Paratrichodoms minor, Paratrichodorus allius, Paratrichodorus nanus, Paratrichodorus teres, Meloidogyne arenaria, Meloidogyne fallax, Meloidogyne hapla, Meloidogyne thamesi, Meloidogyne incognita, Meloidogyne chitwoodi, Meloidogyne javanica, Nacobbus aberrans, Globodera rostochiensis, Globodera pallida, Ditylenchus destructor, Radopholus similis, Rotylenchulus reniformis, Neotylenchus vigissi, Paraphelenchus pseudoparietinus, Aphelenchoides fragariae и Meloinema spp.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами томатов, в частности, с Meloidogyne arenaria, Meloidogyne hapla, Meloidogyne javanica, Meloidogyne incognita, Pratylenchus penetrans и Pratylenchus brachyurus, Pratylenchus coffeae, Pratylenchus scribneri, Pratylenchus vulnus, Paratrichodorus minor, Meloidogyne exigua, Nacobbus aberrans, Globodera solanacearum, Dolichodorus heterocephalus и Rotylenchulus reniformis.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами растений огурца, в частности, с Meloidogyne arenaria, Meloidogyne hapla, Meloidogyne javanica, Meloidogyne incognita, Rotylenchulus reniformis и Pratylenchus thomei.
Соединения формулы (I) или (II) особенно подходят для борьбы с хлопковыми нематодами, в частности, с Belonolaimus longicaudatus, Meloidogyne incognita, Hoplolaimus columbus, Hoplolaimus galeatus и Rotylenchulus reniformis.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами кукурузы, в частности, с Belonolaimus longicaudatus, Paratrichodorus minor и Pratylenchus brachyurus, Pratylenchus delattrei, Pratylenchus hexincisus, Pratylenchus penetrans, Pratylenchus zeae, (Belonolaimus gracilis), Belonolaimus nortoni, Longidorus breviannulatus, Meloidogyne arenaria, Meloidogyne arenaria thamesi, Meloidogyne graminis, Meloidogyne incognita, Meloidogyne incognita acrita, Meloidogyne javanica, Meloidogyne naasi, Heterodera avenae, Heterodera oryzae, Heterodera zeae, Punctodera chalcoensis, Ditylenchus dipsaci, Hoplolaimus aegyptii, Hoplolaimus magnistylus, Hoplolaimus galeatus, Hoplolaimus indicus, Helicotylenchus digonicus, Helicotylenchus dihystera, Helicotylenchus pseudorobustus, Xiphinema americanum, Dolichodorus heterocephalus, Criconemella omata, Criconemella onoensis, Radopholus similis, Rotylenchulus borealis, Rotylenchulus parvus, Tyienchorhynchus agri, Tyienchorhynchus clarus, Tyienchorhynchus claytoni, Tyienchorhynchus maximus, Tyienchorhynchus nudus, Tyienchorhynchus vulgaris, Quinisulcius acutus, Paratylenchus minutus, Hemicycliophora parvana, Aglenchus agricola, Anguina tritici, Aphelenchoides arachidis, Scutellonema brachyurum и Subanguina radiciola.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами сои, в частности, с Pratylenchus brachyurus, Pratylenchus pratensis, Pratylenchus penetrans, Pratylenchus scribneri, Belonolaimus longicaudatus, Heterodera glycines, Hoplolaimus columbus и Pratylenchus coffeae, Pratylenchus hexincisus, Pratylenchus neglectus, Pratylenchus crenatus, Pratylenchus alleni, Pratylenchus agilis, Pratylenchus zeae, Pratylenchus vulnus, (Belonolaimus gracilis), Meloidogyne arenaria, Meloidogyne incognita, Meloidogyne javanica, Meloidogyne hapla, Hoplolaimus columbus, Hoplolaimus galeatus и Rotylenchulus reniformis.
Соединения формулы (I) или (II) особенно подходят для борьбы с табачными нематодами, в частности, с Meloidogyne incognita, Meloidogyne javanica и Pratylenchus brachyurus, Pratylenchus pratensis, Pratylenchus hexincisus, Pratylenchus penetrans, Pratylenchus neglectus, Pratylenchus crenatus, Pratylenchus thomei, Pratylenchus vulnus, Pratylenchus zeae, Longidorus elongatu, Paratrichodorus lobatus, Trichodorus spp., Meloidogyne arenaria, Meloidogyne hapla, Globodera tabacum, Globodera solanacearum, Globodera virginiae, Ditylenchus dipsaci, Rotylenchus spp., Helicotylenchus spp., Xiphinema americanum, Criconemella spp., Rotylenchulus reniformis, Tyienchorhynchus claytoni, Paratylenchus spp. и Tetylenchus nicotianae.
Соединения формулы (I) или (II) особенно подходят для борьбы с цитрусовыми нематодами, в частности, с Pratylenchus coffeae и Pratylenchus brachyurus, Pratylenchus vulnus, Belonolaimus longicaudatus, Paratrichodorus minor, Paratrichodorus porosus, Trichodorus, Meloidogyne incognita, Meloidogyne incognita acrita, Meloidogyne javanica, Rotylenchus macrodoratus, Xiphinema americanum, Xiphinema brevicolle, Xiphinema index, Criconemella spp., Hemicriconemoides, Radopholus similis и Radopholus citrophilus, Hemicycliophora arenaria, Hemicycliophora nudata и Tyienchulus semipenetrans.
Соединения формулы (I) или (II) особенно подходят для борьбы с банановыми нематодами, в частности, с Pratylenchus coffeae, Radopholus similis и Pratylenchus giibbicaudatus, Pratylenchus loosi, Meloidogyne spp., Helicotylenchus multicinctus, Helicotylenchus dihystera и Rotylenchulus spp..
Соединения формулы (I) или (II) особенно подходят для борьбы с ананасовыми нематодами, в частности, с Pratylenchus zeae, Pratylenchus pratensis, Pratylenchus brachyurus, Pratylenchus goodeyi., Meloidogyne spp., Rotylenchulus renifbrmis и Longidoms elongatus, Longidorus laevicapitatus, Trichodorus primitivus, Trichodorus minor, Heterodera spp., Ditylenchus myceliophagus, Hoplolaimus califomicus, Hoplolaimus pararobustus, Hoplolaimus indicus, Helicotylenchus dihystera, Helicotylenchus nannus, Helicotylenchus multicinctus, Helicotylenchus erythrine, Xiphinema dimorphicaudatum, Radopholus similis, Tyienchorhynchus digitatus, Tyienchorhynchus ebriensis, Paratylenchus minutus, Scutellonema clathricaudatum, Scutellonema bradys, Psilenchus tumidus, Psilenchus magnidens, Pseudohalenchus minutus, Criconemoides femiae, Criconemoides onoense и Criconemoides omatum.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами виноградной лозы, в частности, с Pratylenchus vulnus, Meloidogyne arenaria, Meloidogyne incognita, Meloidogyne javanica, Xiphinema americanum, Xiphinema index и Pratylenchus pratensis, Pratylenchus scribneri, Pratylenchus neglectus, Pratylenchus brachyurus, Pratylenchus thomei и Tyienchulus semipenetrans.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами в древесных культурах - семечковых, в частности, с Pratylenchus penetrans и Pratylenchus vulnus, Longidorus elongatus, Meloidogyne incognita и Meloidogyne hapla.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами в древесных культурах - косточковых культурах, в частности, с Pratylenchus penetrans, Pratylenchus vulnus, Meloidogyne arenaria, Meloidogyne hapla, Meloidogyne javanica, Meloidogyne incognita, Criconemella xenoplax и Pratylenchus brachyurus, Pratylenchus coffeae, Pratylenchus scribneri, Pratylenchus zeae, Belonolaimus longicaudatus, Helicotylenchus dihystera, Xiphinema americanum, Criconemella curvata, Tyienchorhynchus claytoni, Paratylenchus hamatus, Paratylenchus projectus, Scutellonema brachyurum и Hoplolaimus galeatus.
Соединения формулы (I) или (II) особенно подходят для борьбы с нематодами в древесных культурах, сахарном тростнике и рисе, в частности, с Trichodorus spp., Criconemella spp. и Pratylenchus spp., Paratrichodoms spp., Meloidogyne spp., Helicotylenchus spp., Tyienchorhynchus spp., Aphelenchoides spp., Heterodera spp, Xiphinema spp. и Cacopaums pestis.
Нанесение
Соединение формулы (I) или (II) может быть нанесено как таковое или, например, в форме готовых к применению растворов, эмульсий, суспензий на водной или масляной основе, порошков, смачиваемых порошков, паст, растворимых порошков, пыли, растворимых гранул, гранул для разбрасывания, суспоэмульсионных концентратов, природных продуктов, пропитанных соединением формулы (I) или (II), синтетических веществ, пропитанных соединением формулы (I) или (II), удобрений, а также микроинкапсулирований в полимерных веществах.
Нанесение осуществляется обычным образом, например, путем полива, распыления, атомизации, разбрасывания, опыления, вспенивания, намазывания и т.п. Также возможно наносить соединение согласно формулы (I) или (II) методом сверхнизкого объема, с помощью системы капельного орошения или орошения, внести его в борозду или ввести в стебель почвы или ствол. Кроме того, возможно нанесение соединения согласно формулы (I) или (II) с помощью герметика для ран, краски или другой перевязки для ран.
Эффективное и совместимое с растениями количество соединения согласно настоящему изобретению, которое наносят на растения, части растений, плоды, семена или почву, будет зависеть от различных факторов, таких как применяемое соединение/композиция, объект обработки (растение, часть растения, плоды, семена или почва), тип обработки (опудривание, опрыскивание, протравливание семян), цель обработки (лечебная и защитная), тип микроорганизмов, стадия развития микроорганизмов, чувствительность микроорганизмов, стадия роста урожая и условия окружающей среды.
Когда соединение согласно формулы (I) или (II) применяют в качестве фунгицида, нормы нанесения могут варьироваться в относительно широком диапазоне, в зависимости от вида применения. Для обработки частей растений, таких как листья, норма нанесения может составлять от 0,1 до 10 000 г/Га, предпочтительно от 10 до 1000 г/Га, более предпочтительно от 50 до 300 г/Га (в случае применения поливом или орошением, можно даже уменьшить норму нанесения, особенно при использовании инертных субстратов, таких как минеральная вата или перлит). Для обработки семян норма нанесения может варьироваться от 0,1 до 200 г на 100 кг семян, предпочтительно от 1 до 150 г на 100 кг семян, более предпочтительно от 2,5 до 25 г на 100 кг семян, даже более предпочтительно от 2,5 до 12,5 г на 100 кг семян. Для обработки почвы норма нанесения может составлять от 0,1 до 10 000 г/Га, предпочтительно от 1 до 5000 г/Га.
Эти нормы нанесения являются просто примерами и не предназначены для ограничения объема настоящего изобретения.
Защита материалов
Соединение и композиция согласно настоящему изобретению могут быть также использованы для защиты материалов, особенно для защиты промышленных материалов от атаки и разрушения нежелательными микроорганизмами.
Кроме того, соединение и композиция согласно настоящему изобретению могут быть использованы в качестве противообрастающих композиций, отдельно или в комбинации с другими активными ингредиентами.
Промышленные материалы в данном контексте понимаются как неживая материя, которая была получена для использования в промышленности. Например, промышленные материалы, которые должны быть защищены активными ингредиентами по изобретению от микробного изменения или разрушения, могут быть адгезивами, клеями, бумагой, обоями и картоном/строительным картоном, текстилем, коврами, кожей, деревом, волокнами и тканями, красками и пластмассовыми изделиями, смазочно-охлаждающими жидкостями и другими материалами, которые могут быть инфицированы или уничтожены микроорганизмами. Части производственных установок и сооружений, например, контуры циркуляции охлаждающей воды, систем охлаждения и отопления и вентиляции и кондиционирования воздуха, которые могут быть нарушены в результате распространения микроорганизмов также могут быть упомянуты в пределах объема материалов, подлежащих защите. Промышленные материалы в пределах объема настоящего изобретения предпочтительно включают адгезивы, проклейки, бумага и картон, изделия из кожи, дерево, краски, смазки и смазывающе-охлаждающие жидкости, более предпочтительно древесину.
Соединение и композиция согласно настоящему изобретению могут предотвратить неблагоприятные эффекты, такие как гниение, разложение, изменение цвета, обесцвечивание или образование плесени.
В случае обработки древесины соединение и композиция согласно настоящему изобретению могут быть также использованы против грибковых заболеваний, которые могут расти на поверхности или внутри древесины.
Термин "древесина" означает любые типы видов древесины и любые виды переработки указанной древесины, предназначенной для строительства, например, массивная древесина, древесина высокой плотности, клееная древесина и фанера. Кроме того, соединение и композиция согласно настоящему изобретению могут быть использованы для защиты объектов, которые вступают в контакт с соленой водой или солоноватой водой, особенно корпуса, решетки водоприемника, сетки, здания, причалы и системы сигнализации от обрастания.
Соединение и композиция согласно настоящему изобретению также может применяться для защиты товаров на хранении. Под товарами на хранении понимаются природные вещества растительного или животного происхождения или продукты, полученных из них, которые имеют природное происхождение, и для которых требуется долговременная защита. Товары на хранении растительного происхождения, например, растения или части растений, таких как стебли, листья, клубни, семена, фрукты, зерновые, могут быть защищены как свежеубранные, так или после обработки посредством (предварительной) сушки, увлажнения, измельчения, гранулирования, прессования или обжаривания. Товары на хранении также включают древесину, как необработанную, такую как строительный лес, электрические столбы и изолирующие слои или в виде готовых изделий, таких как мебель. Товары на хранении животного происхождения представляют собой, например, шкуры, кожи, меха и шерсть. Композиции согласно настоящему изобретению могут предотвратить вредные эффекты, такие как гниение, разложение, изменение цвета, обесцвечивание или образование плесени.
Микроорганизмы, способные разрушать или изменять промышленные материалы включают в себя, например, бактерии, грибы, дрожжи, водоросли и слизевые организмы. Соединение и композиция согласно настоящему изобретению предпочтительно действуют против грибов, особенно плесени, изменяющих цвет дерева грибов и дереворазрушающих грибов (Ascomycetes, Basidiomycetes, Deuteromycetes и Zygomycetes), а также против слизевых организмов и водорослей. Примеры включают микроорганизмы следующих родов: Altemaria, такие как Altemaria tenuis; Aspergillus, таких как Aspergillus niger; Chaetomium, такие как Chaetomium globosum; Coniophora, такие как Coniophora puetana; Lentinus, такие как Lentinus tigrinus; Penicillium, такие как Penicillium glaucum; Polyporus, такие как Polyporus versicolor; Aureobasidium, такие как Aureobasidium pullulans; Sclerophoma, такие как Sclerophoma pityophila; Trichoderma, такие как trichoderma viride; Ophiostoma spp., Ceratocystis spp., Humicola spp., Petriella spp., trichurus spp., Coriolus spp., Gloeophyllum spp., Pleurotus spp., Poria spp., Serpula spp. и Tyromyces spp., Cladosporium spp., Paecilomyces spp. Mucor spp., Escherichia, такие как Escherichia coli; Pseudomonas, такие как Pseudomonas aeruginosa; Staphylococcus, такие как Staphylococcus aureus, Candida spp. и Saccharomyces spp., такие как Saccharomyces cerevisae.
Аспекты настоящего изобретения могут быть дополнительно поняты в свете следующих примеров, которые ни в коей мере не должны рассматриваться как ограничивающие объем настоящего изобретения.
ПРИМЕРЫ
Синтез соединений формулы (I)
Пример получения (I)-1: Получение этил N-[(4-бром-5-циано-3-метил-2-тиенил)карбонил]глицината (соединение I.0024)
Стадия 1: Получение 4-бром-5-циано-3-метилтиофен-2-карбоновой кислоты
К раствору 150 мг (0,86 ммоль) метил 4-бром-5-циано-3-метилтиофен-2-карбоксилата в 3,9 мл тетрагидрофурана добавляли по каплям 0,7 мл 1,1 М водного раствора гидроксида лития (0,7 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Полученную реакционную смесь осторожно подкисляли 1,0 М водным раствором соляной кислоты при 0°С и экстрагировали этилацетатом. Объединенные органические слои сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении с получением 142 мг (чистота 97%, выход 97%) указанного в заголовке соединения в виде белого твердого вещества. LogP=2.05. (М+Н)=246.
Стадия 2: Получение этил N-[(4-бром-5-циано-3-метил-2-тиенил)карбонил]глицината (соединение I.0024)
В 50 мл в круглодонной колбе в инертной атмосфере, раствор 402 мг (2,37 ммоль) хлорида 2-хлор-1,3-диметилимидазолидиния, растворенного в 5 мл дихлорметана, добавляли к раствору 450 мг (1,82 ммоль) 4-бром-5-циано-3-метилтиофен-2-карбоновой кислоты и 1,37 мл (7,86 ммоль) N,N-диизопропилэтиламина, растворенного в 7 мл дихлорметана. Через 5 мин перемешивания добавляли 333 мг (2,37 ммоль) гидрохлорида этилглицината (1:1) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Полученную реакционную смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 516 мг (чистота 100%, выход 86%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=2.40. (М+Н)=331.
Пример получения (I)-2: Получение N-[(4,5-дибром-3-фтор-2-тиенил)карбонил]глицина (соединение I.0227)
В первой круглодонной колбе к раствору 300 мг (0,98 ммоль) 4,5-дибром-3-фтортиофен-2-карбоновой кислоты в 6,5 мл сухого дихлорметана, добавляли при комнатной температуре 95 мкл (1,08 ммоль) оксалилхлорида и каплю N,N-диметилформамида. После 1 ч перемешивания при комнатной температуре реакционную смесь концентрировали при пониженном давлении и растворяли в 2,3 мл сухого 1,4-диоксана с получением раствора ацилхлорида. Во второй круглодонной колбе к раствору 220 мг (0,97 ммоль) гидрохлорида глицина (1:1) в 1,5 мл воды, добавляли 0,6 мл 0,5 М водного раствора гидроксида натрия (0,3 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов и затем медленно добавляли к предварительно приготовленному раствору ацилхлорида. Полученную реакционную смесь перемешивали при комнатной температуре в течение 60 часов, разбавляли водой и осторожно подкисляли 37% (мас./мас.) водным раствором соляной кислоты при 0°С. Образовавшийся осадок отфильтровывали и фильтрат концентрировали при пониженном давлении. Твердое вещество и фильтрат собирали и очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор муравьиной кислоты (1%)), получая 100 мг (чистота 96%, выход 27%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=1.97. (М+Н)=360.
Пример получения (I)-3: Получение S-этил 1-{[(4,5-дибром-3-iodo-2-тиенил)карбонил]амино}циклопропанкарботиоата (соединение I.0139)
В инертной атмосфере к раствору 100 мг (2,20 ммоль) 1-{[(4,5-дибром-3-йодо-2-тиенил)карбонил]амино}циклопропанкарбоновой кислоты в 2 мл сухого дихлорметана при комнатной температуре добавляли 106 мкл (0,60 ммоль) N,N-диизопропилэтиламина, а затем 115 мг (0,30 ммоль) 1-[бис(диметиламино)метилен]-1Н-1,2,3-триазоло[4,5-b]пиридиний-3-оксидгексафторфосфата. После 15 мин перемешивания при комнатной температуре, 19 мг (0,30 ммоль) этантиола добавляли и реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Добавляли насыщенный водный раствор бикарбоната натрия и полученную реакционную смесь дважды экстрагировали дихлорметаном. Объединенные органические слои фильтровали через картридж с силикагелем и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 53 мг (чистота 100%, выход 49%) указанного в заголовке соединения в виде белого твердого вещества. LogP=3.96. (М+Н)=538.
Пример получения (I)-4: Получение 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонил]амино}циклобутанкарбоновой кислоты (соединение I.0172)
К раствору 203 мг (0,47 ммоль) этил 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонил]амино}циклобутанкарбоксилата в 5 мл тетрагидроуфрана по каплям добавляли тетрагидрофуран 1,04 мл 1 М водного раствора гидроксида калия (1,04 ммоль).
Реакционную смесь перемешивали при комнатной температуре в течение 76 часов. Полученную реакционную смесь затем осторожно подкисляли до рН 1 с помощью 1,0 М водного раствора соляной кислоты при 0°С и трижды экстрагировали этилацетатом. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор муравьиной кислоты (1%)); получая 115 мг (чистота 98%, выход 59%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=2.57. (М+Н)=400.
Пример получения (I)-5: Получение метил 1-{[(4,5-дибром-3-фтор-2-тиенил)карботиоил]амино}циклопропанкарбоксилата (соединение I.0328)
Стадия 1: Получение метил 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонил]амино}циклопропанкарбоксилата
В 100 мл круглодонной колбе в инертной атмосфере, раствор 733 мг (4,33 ммоль) хлорида 2-хлор-1,3-диметилимидазолидиния, растворенного в 4,3 мл дихлорметана, добавляли к раствору 1,0 г (3,33 ммоль) 4,5-дибром-3-фтортиофен-2-карбоновой кислоты и 2,50 мл (14,3 ммоль) N,N-диизопропилэтиламина, растворенного в 35 мл дихлорметана. После 15 мин перемешивания добавляли 1,0 г (6,66 ммоль) гидрохлорида метил-1-аминоциклопропанкарбоксилата (1:1) и реакционную смесь перемешивали при комнатной температуре в течение 72 часов. Добавляли воду и полученную реакционную смесь дважды экстрагировали дихлорметаном. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент дихлорметан/этилацетат) с получением 1,24 г (чистота 100%, выход 93%) указанного в заголовке соединения в виде белого твердого вещества. LogP=2.77. (М+Н)=400.
Стадия 2; Получение метил 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонотиоил]амино}циклопропанкарбоксилата (соединение I.0328)
К раствору 265 мг (0,65 ммоль) метил 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонил]амино}циклопропанкарбоксилата в 5 мл 1,2-диметоксиэтана добавляли 267 мг (0,66 ммоль) реактива Лавессона. Реакционную смесь перемешивали при 50°С в течение 42 часов. Полученную реакционную смесь разбавляли дихлорметаном, фильтровали через основной картридж ChromabondТ Alumina и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 158 мг (чистота 100%, выход 57%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=3.91. (М+Н)=416.
Пример получения (I)-6: Получение 1-{[(4,5-дибром-3-фтор-2-тиенил)карбонотиоил]амино}циклопропанкарбоновой кислоты (соединение I.0329)
К раствору 271 мг (0,47 ммоль) метил 1-{[(4,5-дибром-3-фтор-2-тиенил)карботиоил]амино}циклопропанкарбоксилата в 7 мл 1,2-дихлорэтана добавляли 203 мг (0,47 ммоль) гидроксида триметилолова. Реакционную смесь перемешивали при 60°С в течение 18 часов. Полученную реакционную смесь концентрировали при пониженном давлении, растворяли в ацетилацетате и трижды промывали 1,0 М водный раствор соляной кислоты. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор муравьиной кислоты (1%)); получая 135 мг (чистота 100%, выход 54%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=2.95. (М+Н)=402.
Пример получения (I)-7: Получение этил N-[(4,5-дихлор-3-циано-2-тиенил)карбонил]лейцината (соединение I.0279)
Стадия 1: Получение этил N-[(4,5-дихлор-3-иод-2-тиенил)карбонил]лейцината
В микроволновом флаконе объемом 5 мл в инертной атмосфере, раствор 102 мг (0,60 ммоль) хлорида 2-хлор-1,3-диметилимидазолидиния, растворенного в 1 мл дихлорметана, добавляли к раствору 150 мг (0,46 ммоль) 4,5-дихлор-3-йодтиофен-2-карбоновой кислоты и 0,35 мл (2,00 ммоль) N,N-диизопропилэтиламина, растворенного в 2 мл дихлорметана. После 5 мин перемешивания добавляли 118 мг (0,60 ммоль) гидрохлорида DL- этиллейцината (1:1) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Полученную реакционную смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 183 мг (чистота 100%, выход 85%) целевого соединения в виде белого твердого вещества. LogP=5.04. (М+Н)=464.
Стадия 2: Получение этил N-[(4,5-дихлор-3-циано-2-тиенил)карбонил]лейцината (соединение I.0279)
В микроволновом флаконе объемом 5 мл в инертной атмосфере 183 мг (0,39 ммоль) этил N-[(4,5-дихлор-3-иодо-2-тиенил)карбонил]лейцината и 42 мг (0,47 ммоль) цианида меди(I) последовательно добавляли, а затем дегазированный N,N-диметилформамид (1,3 мл). Флакон закрывали и реакционную смесь перемешивали при 110°С в течение 5 часов. Полученную реакционную смесь гасили насыщенным водным раствором бикарбоната натрия и экстрагировали ацетилацетатом. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток растворяют в дихлорметане, фильтруют через патрон с силикагелем и концентрируют при пониженном давлении, получая 125 мг (чистота 98%, выход 85%) указанного в заголовке соединения в виде бесцветного масла. LogP=4.05. (М+Н)=363.
Пример получения (I)-8: Получение этил N-[(4,5-дибром-3-фтор-2-тиенил)карбонил]глицината (соединение I.0449)
К раствору 226 мг (0,72 ммоль) этил N-[(4-бром-3-фтор-2-тиенил)карбонил]глицината в 6 мл уксусной кислоты добавили 0,23 мл (4,37 ммоль) брома. Реакционную смесь перемешивали при 70°С в течение 2,5 часов. Полученную реакционную смесь гасили при 0°С со льдом, затем добавляли насыщенный водный раствор тиосульфата натрия и дважды экстрагировали дихлорметаном. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении =. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с выходом 102 мг (чистота 100%, выход 36%) указанного в заголовке соединения в виде твердого вещества желтого цвета. LogP=2.97. (М+Н)=388.
Пример получения (I)-9: Получение этил N-[(4-хлор-3-фтор-5-метил-2-тиенил)карбонил]глицината (соединение I.0793)
К раствору 50 мг (0,14 ммоль) этил N-[(5-бром-4-хлор-3-фтор-2-тиенил)карбонил]глицината в 1,5 мл дегазированного 1,4-диоксана добавляли 25 мг (0,41 ммоль) триметилбороксина, 71 мг (0,22 ммоль) карбоната цезия и 5,9 мг (7,2 мкмоль) (1:1) комплекса [1,1ў-бис(дифенилфосфино)ферроцен]дихлорпалладия(II) с дихлорметаном. Реакционную смесь перемешивали при 100°С для 5 часы. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические слои промывали соляным раствором, фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с выходом 40 мг (чистота 100%, выход 98%) целевого соединения в виде белого твердого вещества. LogP=2.54. (М+Н)=280.
Пример получения (I)-10: Получение N-(2-амино-2-оксоэтил)-4,5-дибром-3-фтортиофен-2-карбоксамида (соединение I.0894)
В инертной атмосфере к раствору 600 мг (1,66 ммоль) N-[(4,5-дибром-3-фтор-2-тиенил)карбонил] глицина в 30 мл N,N-диметилформамида при комнатной температуре, 133 мг (2,49 ммоль) хлорида аммония, 478 мг (2,49 ммоль) гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида, 225 мг (1,66 ммоль) 1-гидроксибензотриазола и 406 мг (3,32 ммоль) 4-(диметиламино)пиридина. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Полученную реакционную смесь экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор бикарбоната аммония [10]. ммоль/л]), чтобы получить 260 мг (чистота 99%, выход 43%) целевого соединения в виде белого твердого вещества. LogP=1.69. (М+Н)=359.
Пример получения (I)-11: N-(2-амино-2-сульфанилиденэтил)-4,5-дибром-3-фтортиофен-2-карбоксамид (соединение I.0896)
В инертной атмосфере к раствору 200 мкг (0,56 ммоль) N-(2-амино-2-оксоэтил)-4,5-дибром-3-фтортиофен-2-карбоксамида в 10 мл толуола добавили 270 мг г (0,67 ммоль) реактива Лавессона. Реакционную смесь перемешивали при 60°С в течение 5 часов. Полученную реакционную смесь концентрировали при пониженном давлении, разбавляли водой и экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор муравьиной кислоты (0,1%)), получая 80 мг (чистота 99%, выход 38%) целевого соединения в виде белого твердого вещества. LogP=2.25. (М+Н)=375.
Пример получения (I)-12: этил N-[(3-бром-4,5-дихлор-2-тиенил)карбонил]-2-метилаланината (соединение I.1062)
Стадия 1: Получение этил N-[(3-амино-4,5-дихлор-2-тиенил)карбонил]-2-метилаланината
Раствор 160 мг (0,94 ммоль) 2-хлор-1,3-диметилимидазолидиния хлорида, растворенного в 2 мл дихлорметана, добавляли к раствору 154 мг (0,72 ммоль) 3-амино-4,5-дихлортиофен-2-карбоновой кислоты и 0,55 мл (3,13 ммоль) N,N-диизопропилэтиламина, растворенных в 5 мл дихлорметана. Через 5 мин перемешивания добавляли 1,0 г (6,66 ммоль) гидрохлорида этил 2-метилаланинат (1:1) и реакционную смесь перемешивали при комнатной температуре в течение 48 часов. Добавляли воду и полученную реакционную смесь дважды экстрагировали дихлорметаном. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент гептан/этилацетат) с получением 205 мкг (чистота 100%, выход 87%) указанного в заголовке соединения в виде белого твердого вещества. LogP=3.09. (М+Н)=325.
Стадия 2: Получение этил N-[(3-бром-4,5-дихлор-2-тиенил)карбонил]-2-метилаланината (соединение I.1062)
К раствору бромида меди(I) (114 мг, 0,79 ммоль) в 7 мл безводного ацетонитрила по каплям добавляли трет-бутилнитрит (105 мкл, 0,79 ммоль) при 0°С. Смеси давали нагреться до комнатной температуры и порциями добавляли 173 мг (0,53 ммоль) этил N-[(3-амино-4,5-дихлор-2-тиенил)карбонил]-2-метилаланината. Реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь разбавляли дихлорметаном и осторожно подкисляли 1 М водным раствором соляной кислоты. Водный слой дважды экстрагировали дихлорметаном. Объединенные органические слои сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 63 мг (чистота 100%, выход 30%) указанного в заголовке соединения в виде белого твердого вещества. LogP=4.24. (М+Н)=388.
Синтез соединений формулы (II)
Пример получения (II)-1: Получение метил 5-хлор-4-циано-3-метилтиофен-2-карбоксилат (соединение II.028)
К раствору хлорида меди(I) (1,89 г, 19,1 ммоль) в 45 мл безводного ацетонитрила по каплям добавляли трет-бутилнитрит (2,27 мл, 19,1 ммоль) при 0°С. Через 5 минут перемешивания при 0°С порциями добавляли 2,50 г (12,7 ммоль) метил 5-амино-4-циано-3-метилтиофен-2-карбоксилата. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 18 часов. Реакционную смесь разбавляли дихлорметаном и осторожно подкисляли 1 М водным раствором соляной кислоты. Водный слой дважды экстрагировали дихлорметаном. Объединенные органические слои сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н -гептан/этилацетат) с выходом 1,15 г (чистота 100%, выход 42%) указанного в заголовке соединения в виде белого твердого вещества. LogP=3.01. (М+Н)=216.
Пример получения (II)-2: Получение 4-бром-5-циано-3-метилтиофен-2-карбоновой кислоты (соединение II.042)
К раствору 150 мг (0,86 ммоль) метил 4-бром-5-циано-3-метилтиофен-2-карбоксилата в 3,9 мл тетрагидрофурана добавляли по каплям 0,7 мл 1,1 М водный раствор гидроксида лития (0,7 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Полученную реакционную смесь осторожно подкисляют 1,0 М водным раствором соляной кислоты при 0°С и экстрагировали этилацетатом. Объединенные органические слои сушили над безводным сульфатом магния, фильтовали и концентрировали при пониженном давлении с получением 142 мг (чистота 97%, выход 97%) указанного в заголовке соединения в виде белого твердого вещества. LogP=2.05. (М+Н)=246.
Пример получения (II)-3: Получение метил 4-хлор-5-цианотиофен-2-карбоксилата (соединение II.046)
В микроволновом флаконе к раствору 100 мг (0,53 ммоль) 4-хлор-5-цианотиофен-2-карбоновой кислоты в 3 мл сухого дихлорметана, добавляли при комнатной температуре 60 мкл (0,69 ммоль) оксалилхлорида и каплю N,N-диметилформамида. Через 2 часа перемешивания добавляли 0,86 мл (21,3 ммоль) метанола и реакционную смесь перемешивали при комнатной температуре в течение 16 часы. Полученную смесь фильтровали через картридж с силикагелем и концентрировали при пониженном давлении. Полученную реакционную смесь перемешивали при комнатной температуре в течение 60 часов, разбавляли водой и осторожно подкисляли 37% (масс./масс.) водным раствором соляной кислоты при 0°С. Образовавшийся осадок отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 86 мг (чистота 99%, выход 79%) целевого соединения в виде белого твердого вещества. LogP=2.52. (М)=201.
Пример получения (II)-4: Получение метил 4,5-дибром-3-(дифторметил)тиофен-2-карбоксилата (соединение II.055)
К раствора 57 г (182 ммоль) метил 4,5-дибром-3-метилтиофен-2-карбоксилата в 500 мл четыреххлористого углерода добавляли 2,7 г (11 ммоль) дибензоилпероксида и 35,7 г (200 ммоль) N-бромсукцинимида порциями при комнатной температуре. Реакционную смесь кипятили с обратным холодильником в течение 18 часов. Осадок отфильтровывали. Органический слой промывали теплой водой, насыщенным водным раствором бикарбоната натрия и солевым раствором, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением 71 г соответствующего бромметилового соединения в виде твердого вещества желтого цвета. К раствору этого соединения (71 г, 181 ммоль) в 500 мл сухого ацетонитрила добавляли порциями 63,4 г (540 ммоль) моногидрата N-оксида 4-метилморфолина при 0°С. После перемешивания при комнатной температуре в течение 16 ч., реакционную смесь по каплям добавляли к 2 л 2 Н водного раствора соляной кислоты и экстрагировали EtOA. Органический слой промывлиа водой, насыщенным водным раствором бикарбоната натрия и солевым раствором, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением 23 г соответствующего альдегида в виде твердого вещества желтого цвета. К раствору 23 г (70 ммоль) последнего в 500 мл дихлорметана по каплям добавляли 12 мл (99 ммоль) трифторида морфолиносеры при 0°С. Реакционную смесь перемешивали при комнатной температуре в течение 18 ч. Затем реакционную смесь осторожно добавляли в смесь льда и воды и дважды экстрагировали дихлорметаном. Органический слой дважды промывали водой, дважды солевым раствором, сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении, получая 8,9 г. г (выход 14%) указанного в заголовке соединения. LogP=3.81. (М)=348.
Пример получения (II)-5: Получение метил 4,5-дихлор-3-цианотиофен-2-карбоксилата (соединение II.085)
К раствору 10 г (44 ммоль) метил 3-амино-4,5-дихлортиофен-2-карбоксилата в 250 мл диэтилового эфира добавляли 11.2 мл (88 ммоль) диэтилэтерата трифторида бора при комнатной температуре. К перемешиваемой смеси добавляли 7,4 мл изопентилнитрита (55 ммоль), что приводит к медленному образованию серого осадка. Затем осадок отфильтровывали и промывали диэтиловым эфиром. Полученное твердое вещество добавляли порциями к перемешиваемому раствору 27,4 г. г (42 ммоль) цианида калия и 8,3 г (93 ммоль) цианида меди (I) в 300 мл воды на 15°С. Реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Этилацетат выливали в перемешиваемую реакционную смесь и отделяли органический слой. Водный слой дважды экстрагировали этилацетатом. Объединенные органические слои промывали водой, сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с выходом 2,24 г (выход 21%) целевого соединения в виде белого твердого вещества. LogP=2.98. (М)=235.
Пример получения (II)-6: Получение этил 4,5-дихлор-3-цианотиофен-2-карбоксилата (соединение II.053)
Стадия 1: Получение этил 4,5-дихлор-3-йодтиофен-2-карбоксилата К раствору 225 мг (1,0 ммоль) этил 4,5-дихлортиофен-2-карбоксилата в 10 мл сухого тетрагидрофурана в атмосфере аргона по каплям добавляли комплекса 2,39 мл (1,3 ммоль) раствора 2,2,6,6-тетраметилпиперидинилмагния хлорида и хлорида лития (17% в тетрагидрофуране) при 0°С. Реакционную смесь перемешивали при комнатной температуре в течение 20 минут. К перемешиваемой смеси по каплям добавляли раствор 508 мг йода (2,0 ммоль) в 5 мл сухого. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную реакционную смесь гасили насыщенным водным раствором тиосульфата натрия и экстрагировали этилацетатом. Объединенные органические слои промывали водой, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением 368 мг (чистота 95%, выход 99%) указанного в заголовке соединения в виде твердого вещества. LogP=4.75. (М)=350.
Стадия 2: Получение этил 4,5-дихлор-3-цианотиофен-2-карбоксилат (соединение II.053)
В микроволновый флакон объемомо 5 мл в инертной атмосфере 200 мг (0,57 ммоль) этил 4,5-дихлор-3-иодтиофен-2-карбоксилата и 61 мг (0,68 ммоль) цианида меди(I) последовательно добавляли, а затем дегазированный N,N-диметилформамид (1,5 мл). Флакон закрывали и реакционную смесь перемешивали при 110°С в течение 5 часов. Полученную реакционную смесь гасили насыщенным водным раствором бикарбоната натрия и экстрагировали дихлорметаном. Объединенные органические слои промывали водой, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) и препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/водный раствор муравьиной кислоты (0,1%)), получая 60 мг (чистота 100%, выход 42%) целевого соединения в виде белого твердого вещества. LogP=3.54. (M+Na)=272.
Пример получения (II)-7: Получение этил 5-бром-4-хлор-3-метилтиофен-2-карбоксилата (соединение II.033)
Стадия 1: Получение этил 5-амино-4-хлор-3-метилтиофен-2-карбоксилата
Раствор 500 мкг (2,25 ммоль) гидрохлорида этил 5-амино-3-метилтиофен-2-карбоксилата (1:1) в водном растворе бикарбоната натрия дважды экстрагировали дихлорметаном. Объединенные органические слои промывали насыщенным водным раствором бикарбоната натрия, фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. К раствору остатка в 4 мл тетрагидрофурана добавляли 331 мг (2,48 ммоль) N-хлорсукцинимида при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную реакционную смесь гасили насыщенным водным раствором бикарбоната натрия и экстрагировали дихлорметаном. Объединенные органические слои фильтровали через картридж Chem ElutФ и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с получением 260 мкг (чистота 99%, выход 52%) указанного в заголовке соединения в виде коричневого твердого вещества. LogP=2.67. (М+Н)=220.
Стадия 2: Получение этил 5-бром-4-хлор-3-метилтиофен-2-карбоксилата (соединение II.033)
К раствору хлорида меди(I) (1,89 г, 19,1 ммоль) в 45 мл безводного ацетонитрила по каплям добавляли трет-бутилнитрит (2,27 мл, 19,1 ммоль) при 0°С. Через 5 минут перемешивания при 0°С порциями добавляли 2,50 г (12,7 ммоль) этил 5-амино-4-хлор-3-метилтиофен-2-карбоксилата. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 18 часов. Реакционную смесь разбавляли дихлорметаном и осторожно подкисляли 1 М водным раствором соляной кислоты. Водный слой дважды экстрагировали дихлорметаном. Объединенные органические слои сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (градиент н-гептан/этилацетат) с выходом 1,15 г (чистота 100%, выход 42%) указанного в заголовке соединения в виде белого твердого вещества. LogP=3.01. (М+Н)=216.
Пример получения (II)-8: Получение 4,5-дихлор-3-цианотиофен-2-карбоновой кислоты (соединение II. 103)
К раствору 500 мг (2,80 ммоль) 4,5-дихлортиофен-3-карбонитрила в 10 мл сухого тетрагидрофурана при -78°С добавляли по каплям 1,40 мл (2,80 ммоль) раствора диизопропиламида лития (2,0 М в тетрагидрофуране). Реакционную смесь выливали в раствор измельченного сухого льда в сухом тетрагидрофуране. Реакционную смесь концентрировали при пониженном давлении. Раствор остатка в воде осторожно подкисляли до рН 1 с помощью 1,0 М водного раствора соляной кислоты при 0°С и трижды экстрагировали этилацетатом. Объединенные органические слои сушили и концентрировали при пониженном давлении. Остаток очищали препаративной высокоэффективной жидкостной хроматографией (градиент ацетонитрил/вода) с получением 327 мг (чистота 95%, выход 50%) указанного в заголовке соединения в виде белого твердого вещества. LogP=1.61.
Иллюстративные соединения
Иллюстативные соединения согласно настоящему изобретению, показанные в таблицах 1а и lb, получали по аналогии с примерами, приведенными выше, и/или в соответствии с общим описанием раскрытых в настоящем документе способов. Следующие таблицы 1.1 и 1.2 иллюстрируют без ограничения примеры соединений согласно формуле (I).
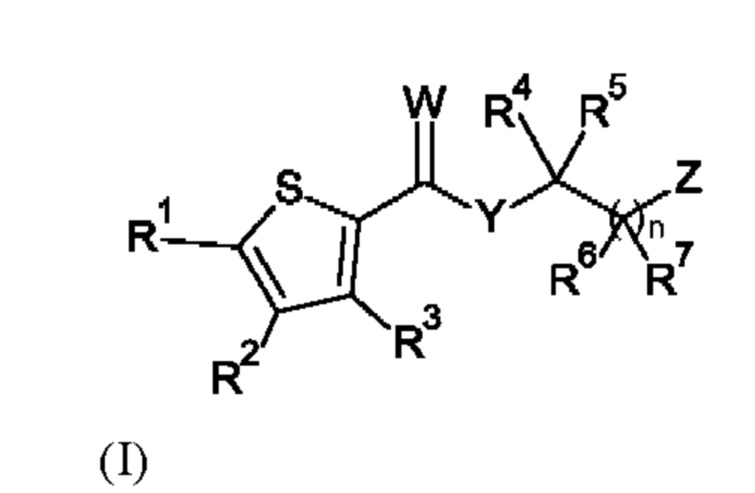
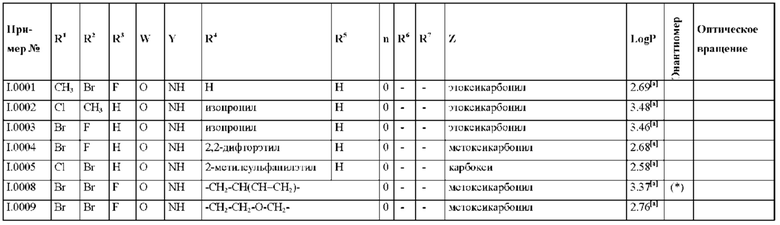
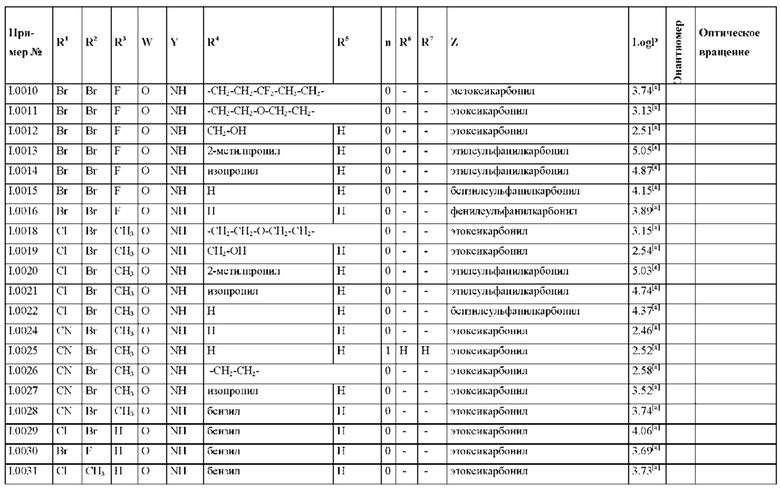
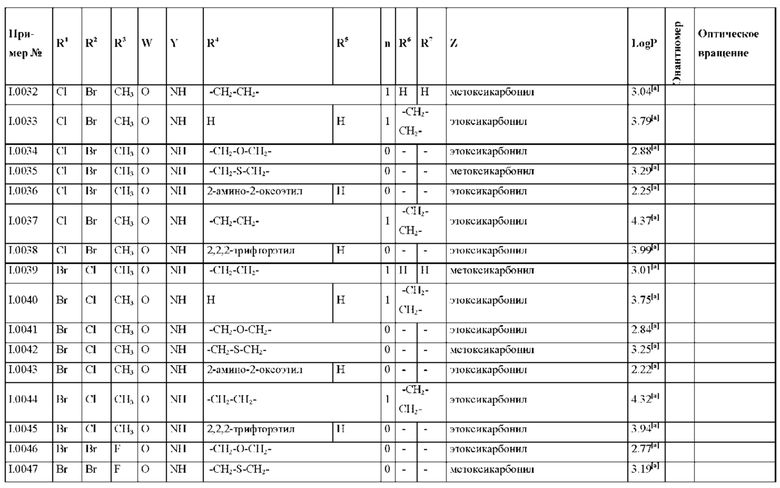
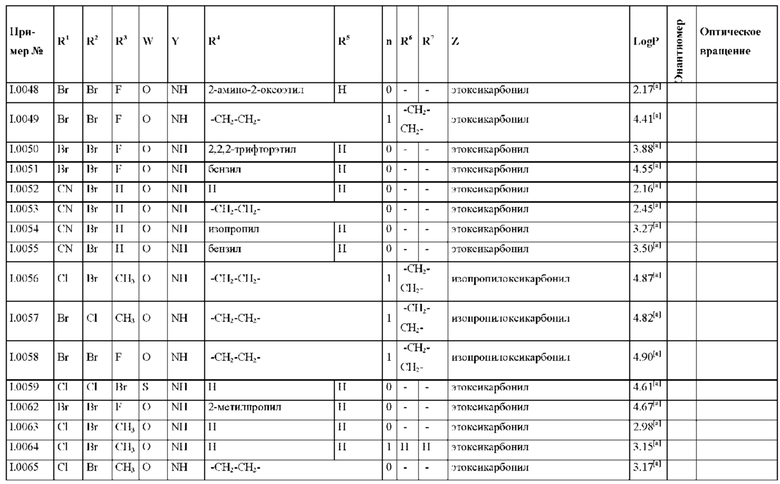
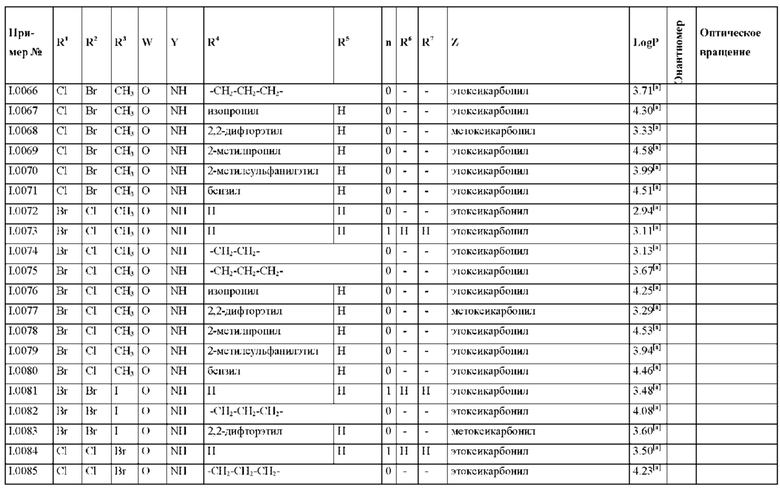
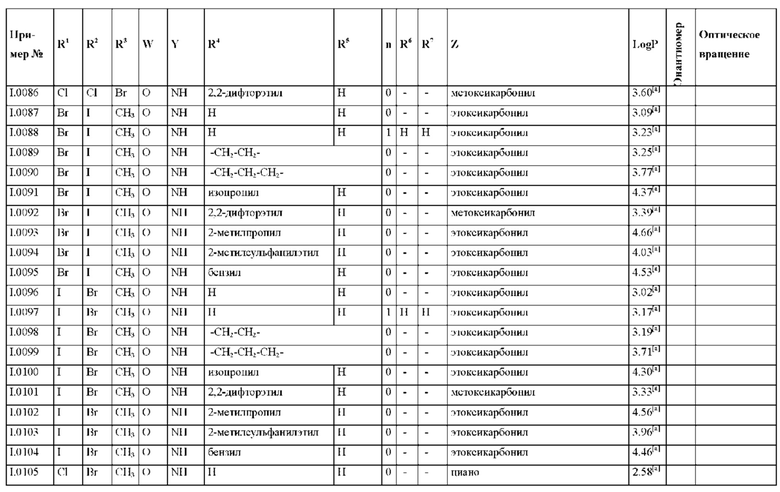
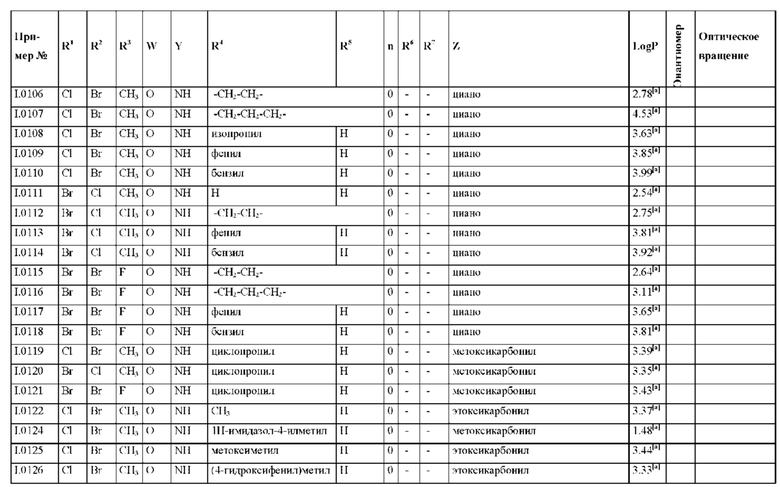
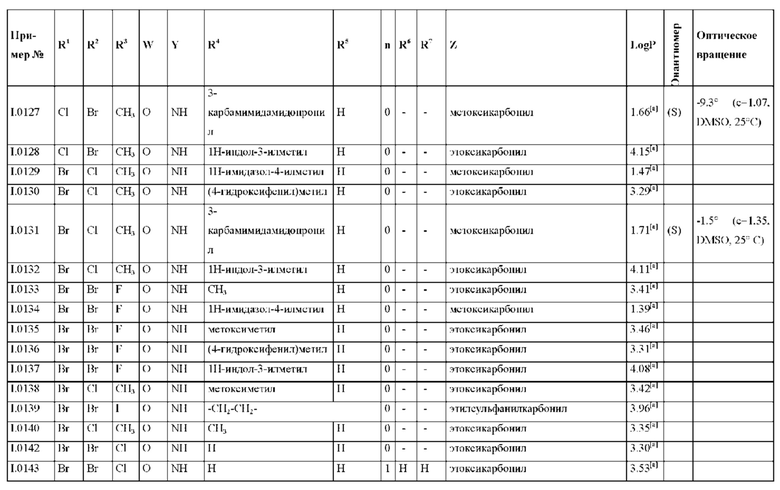
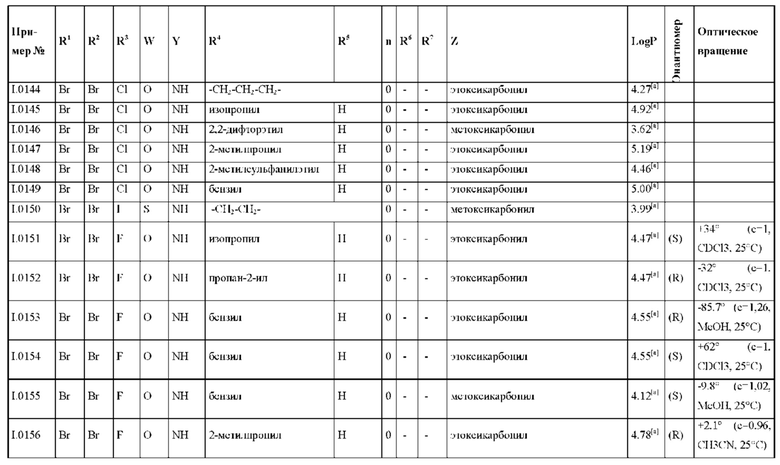
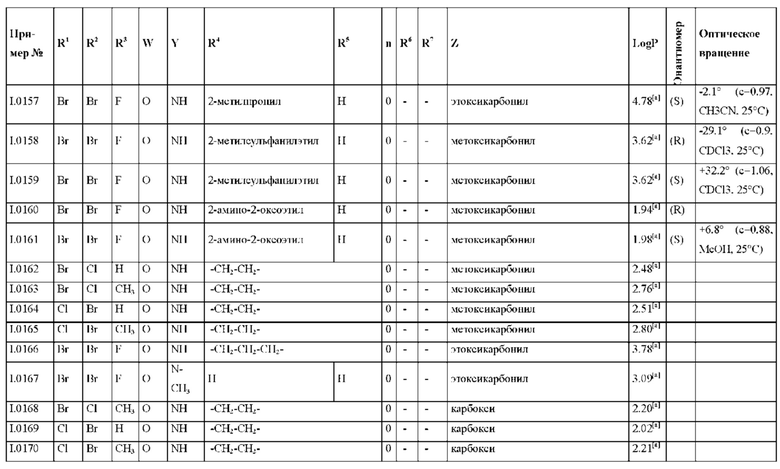
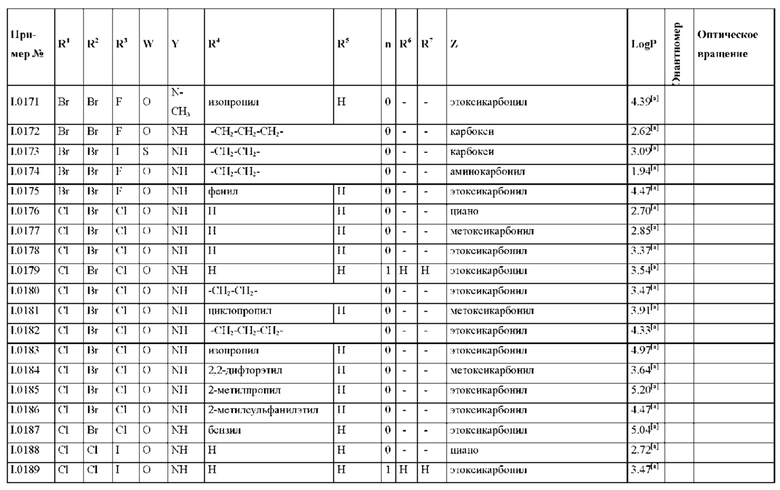
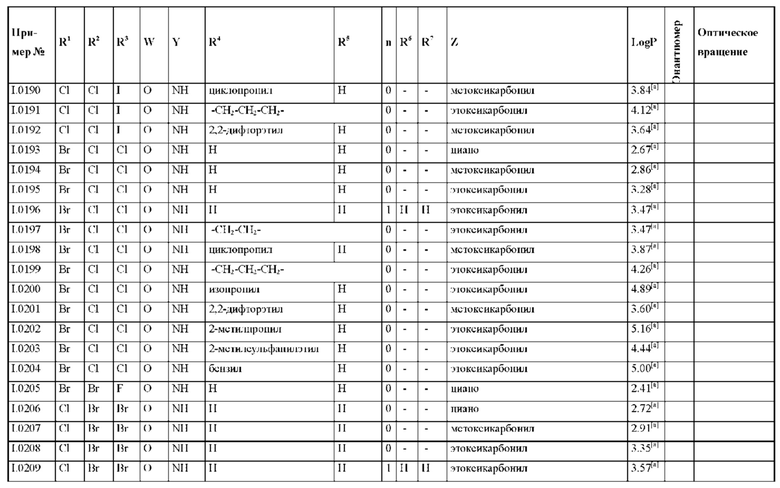
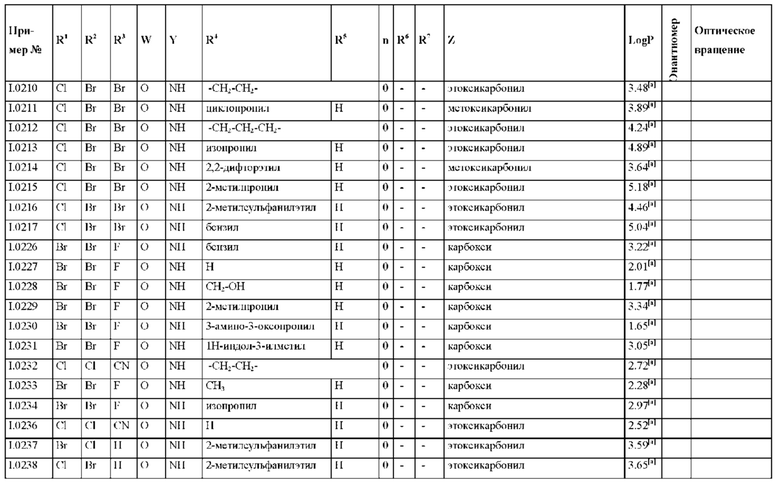
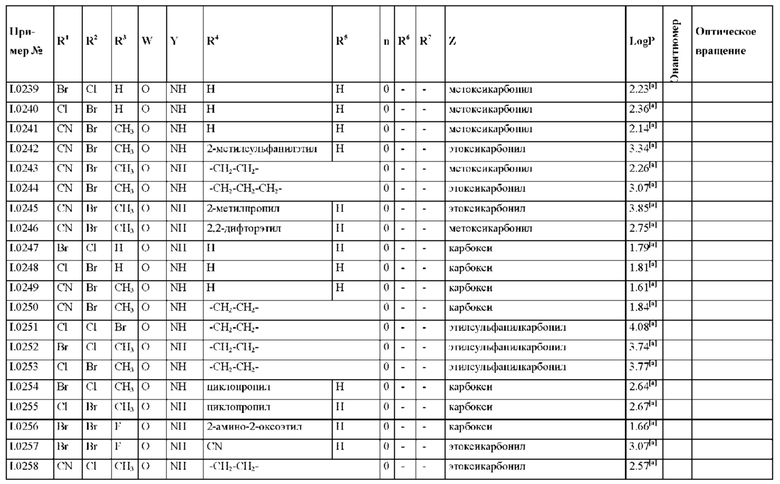
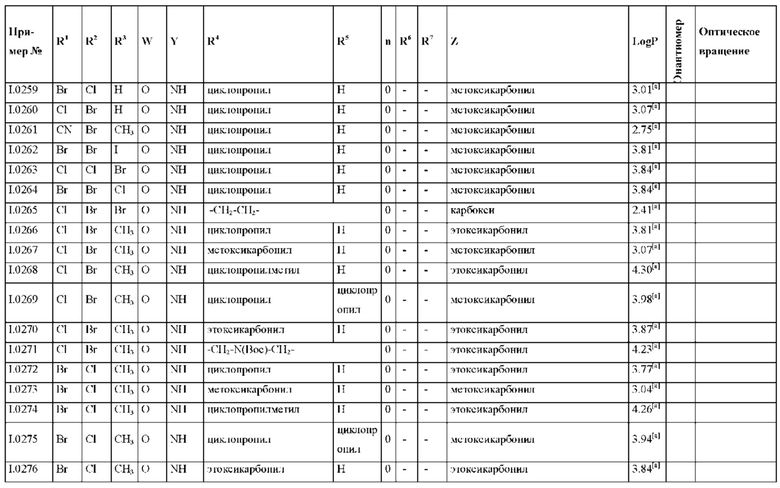
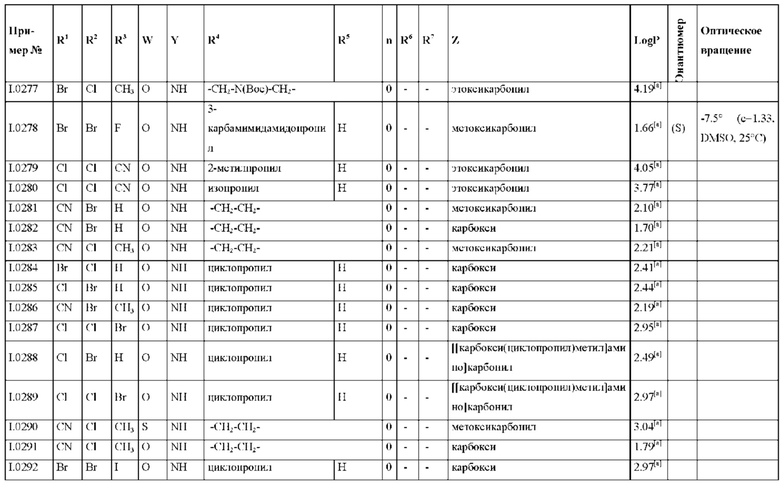
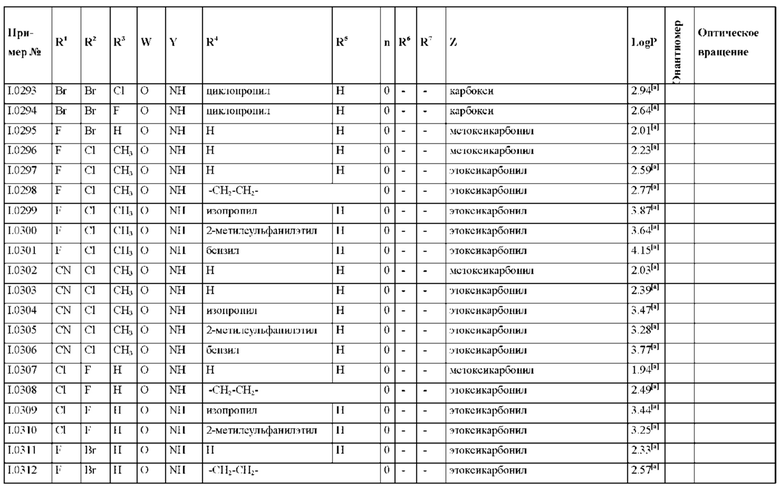
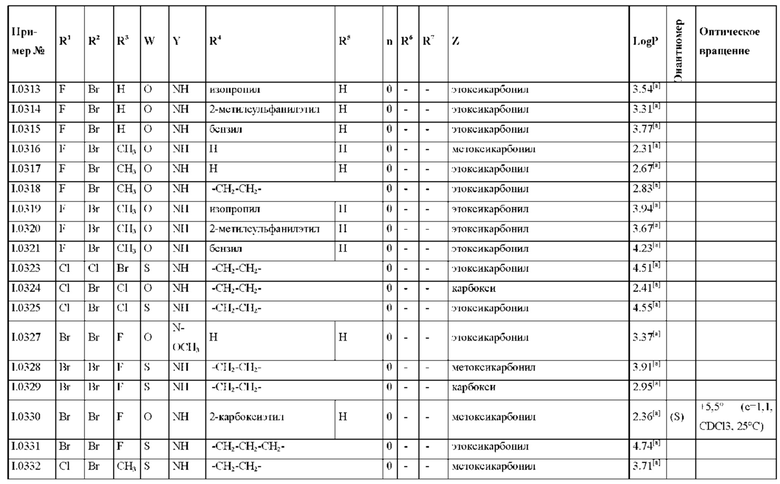
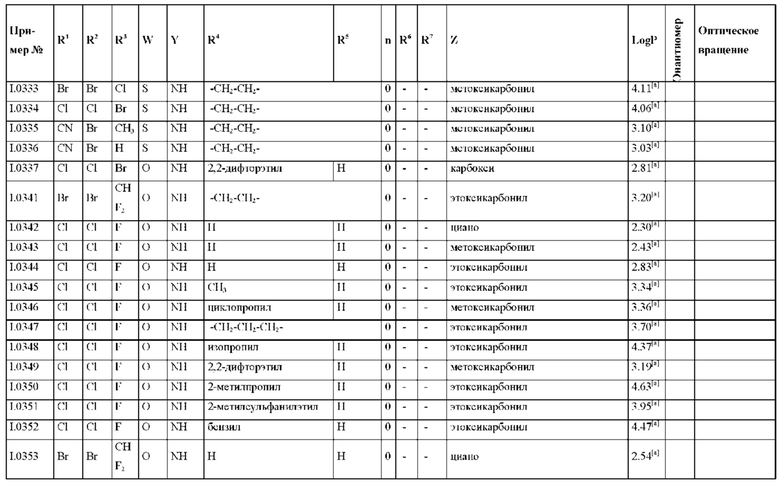
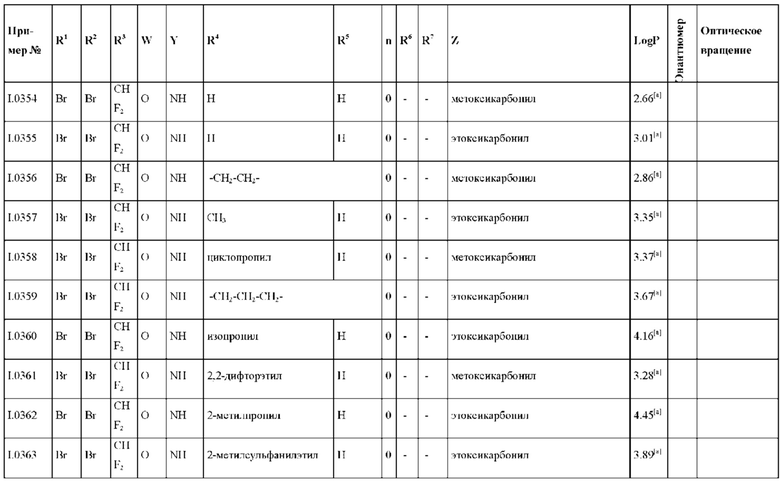
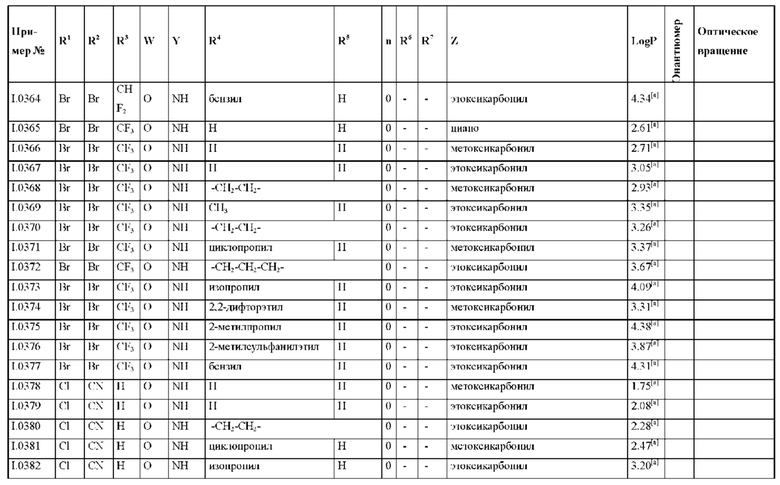
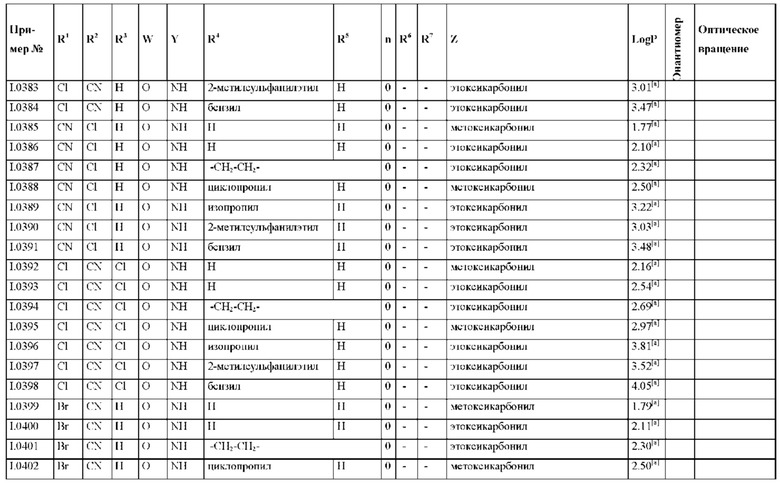
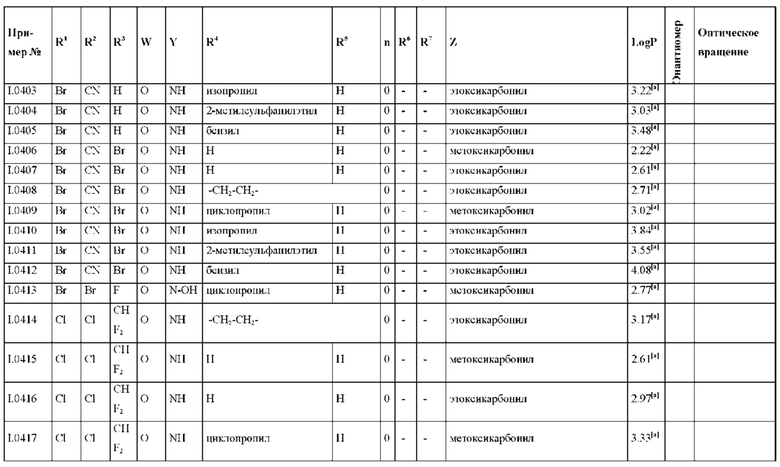
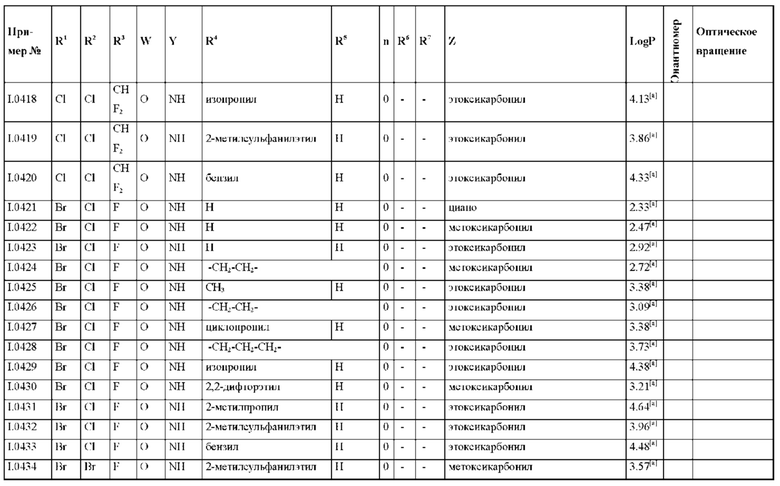
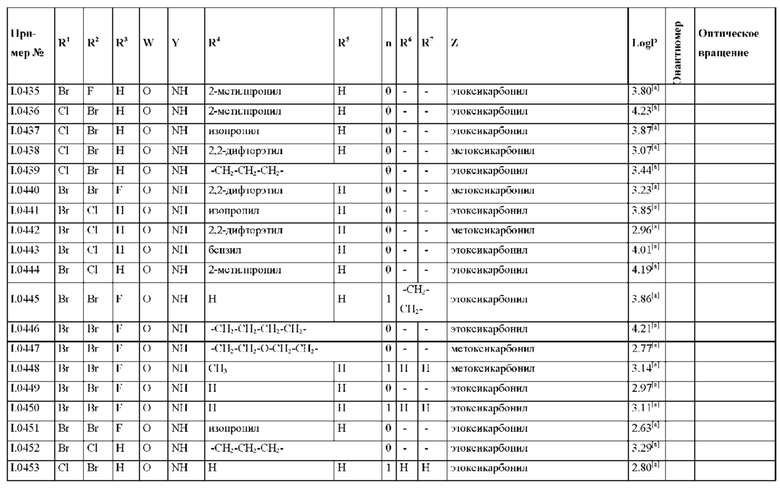
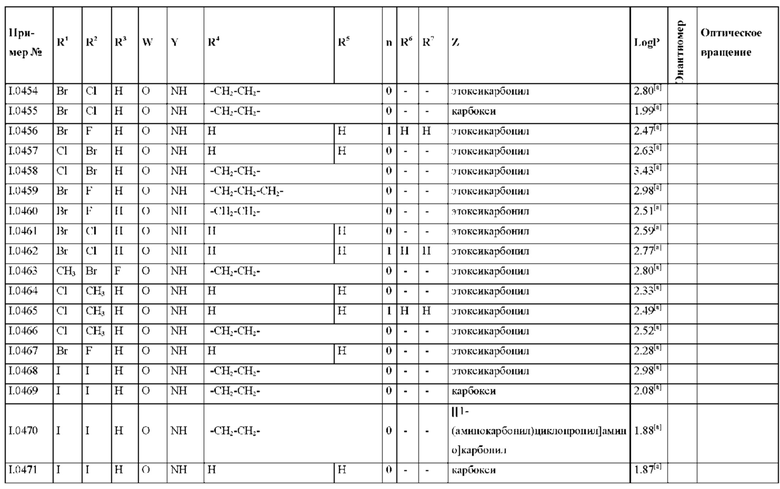
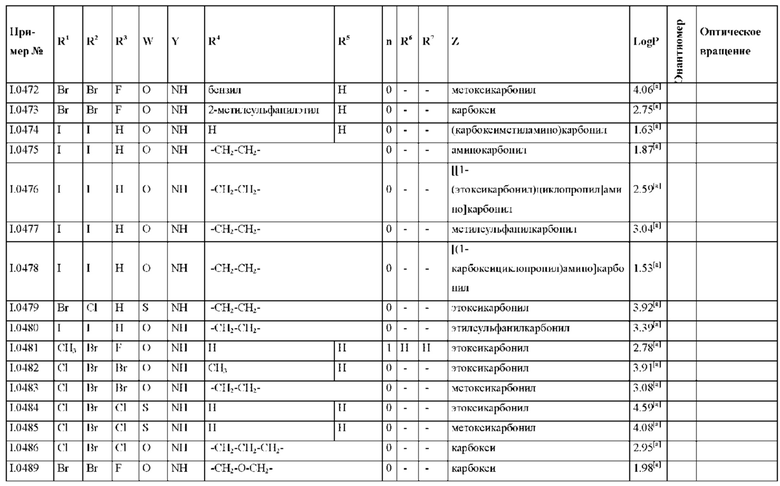
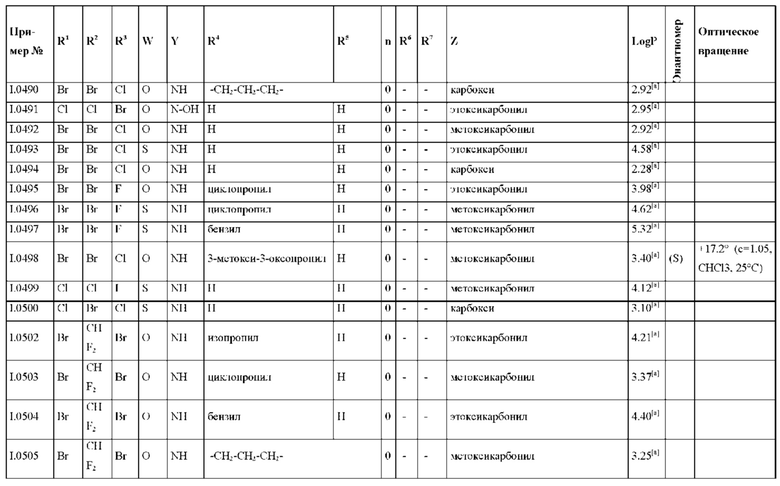
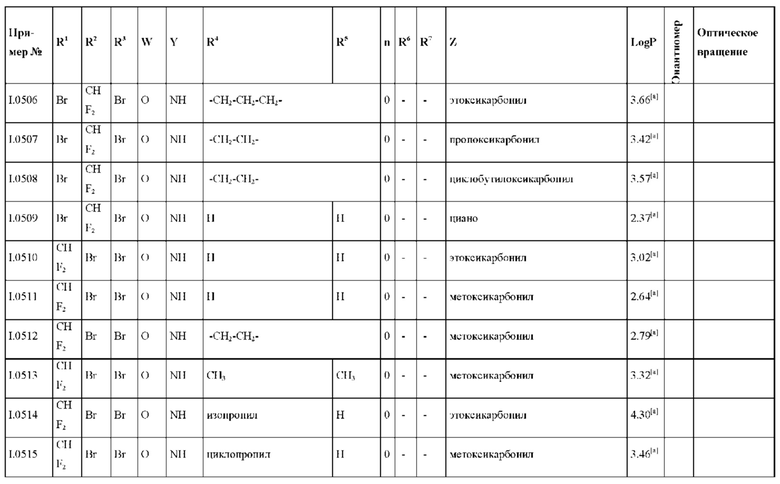
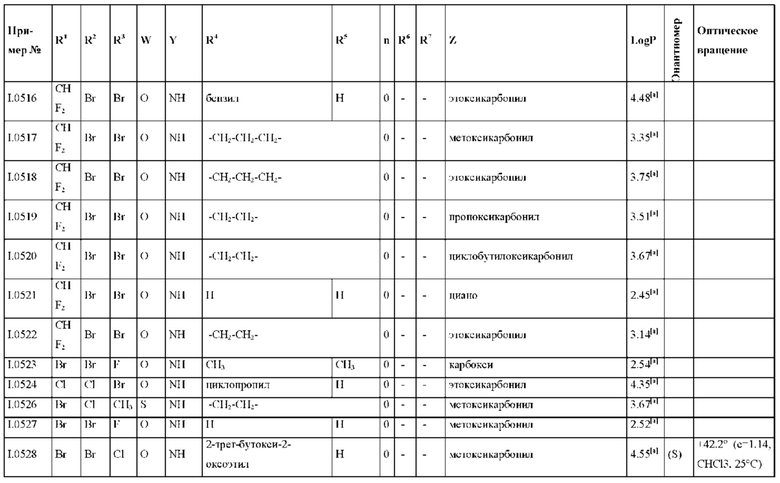
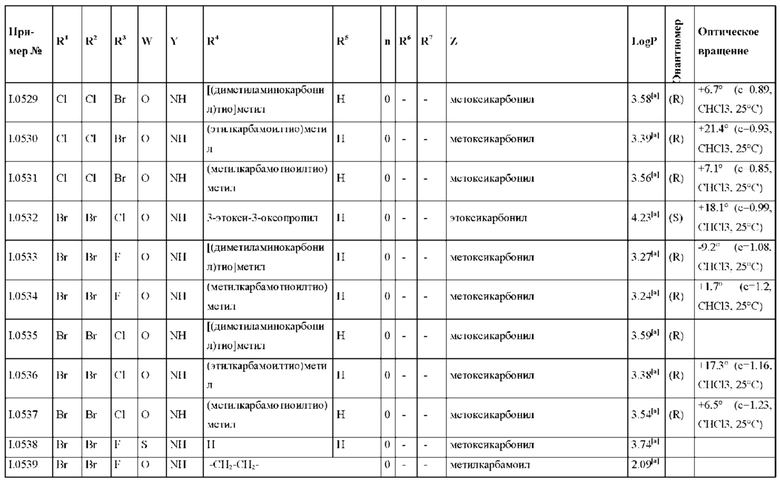
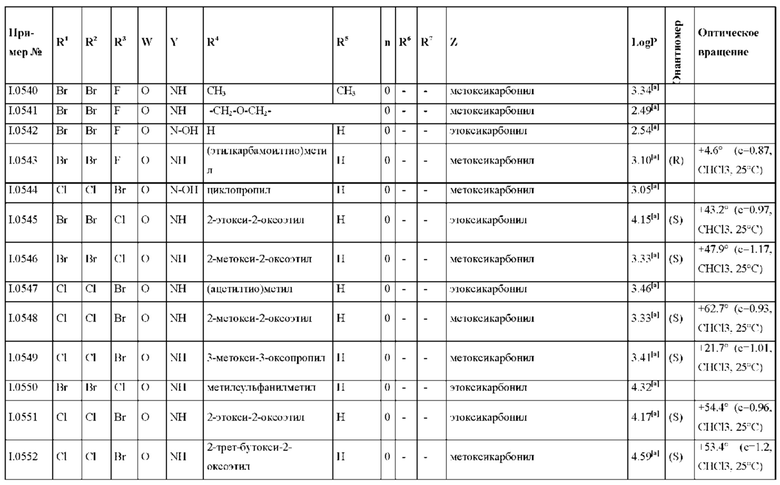
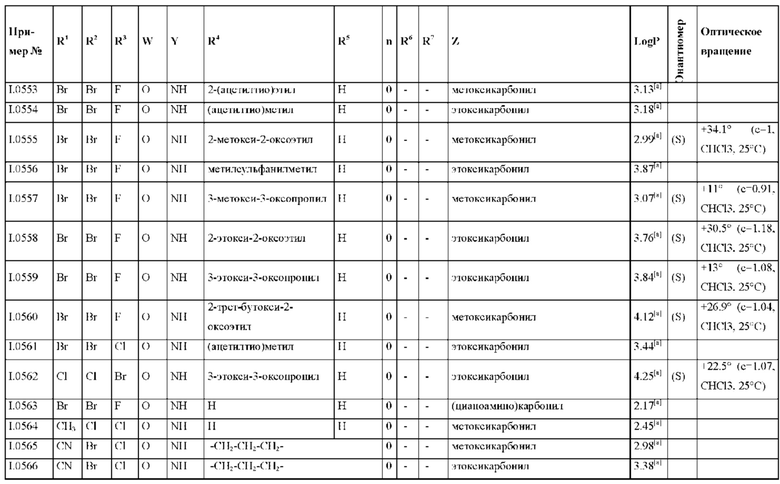
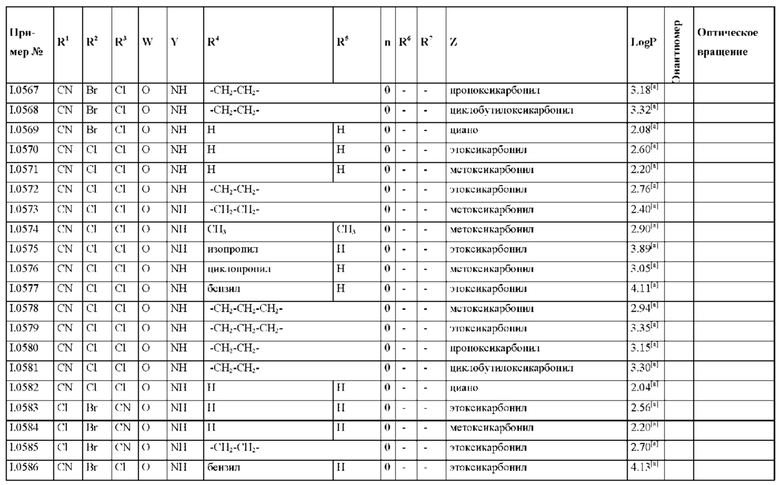
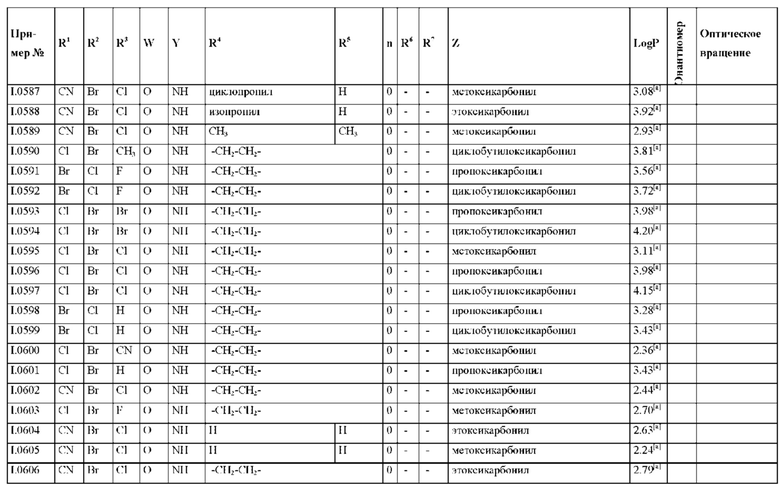
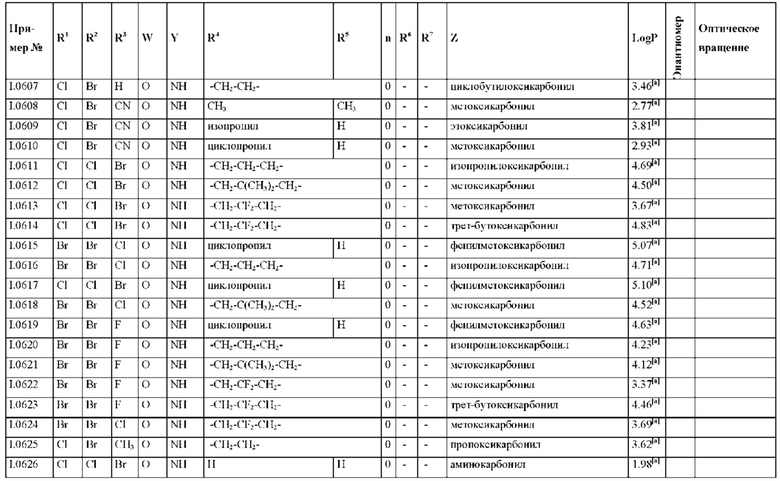
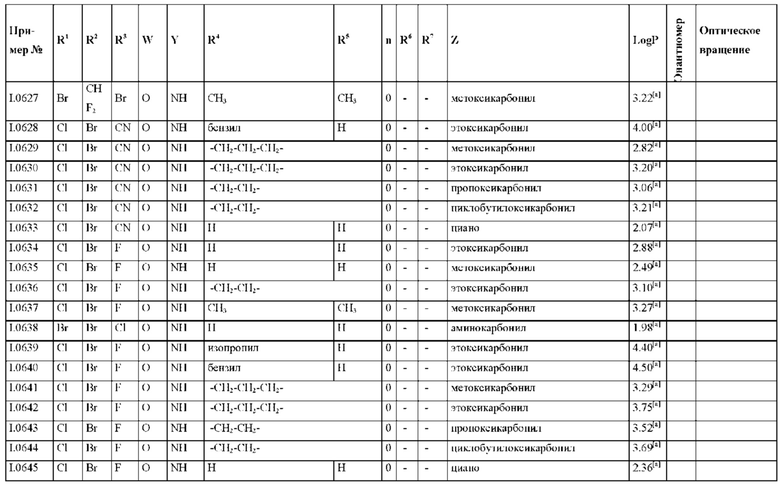
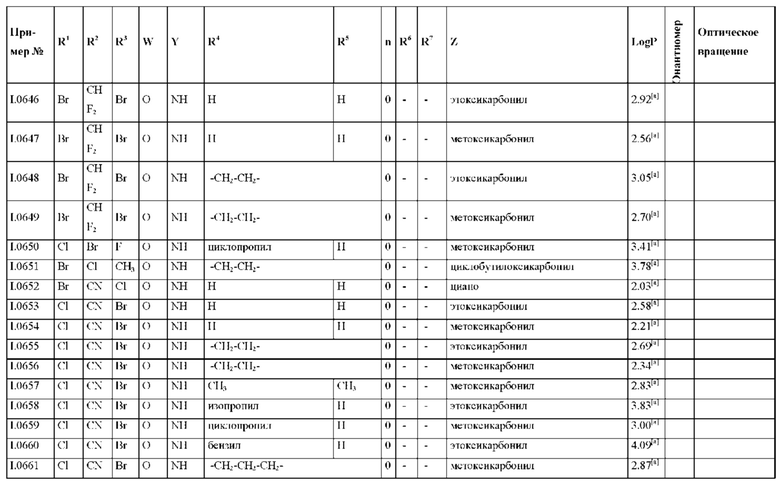
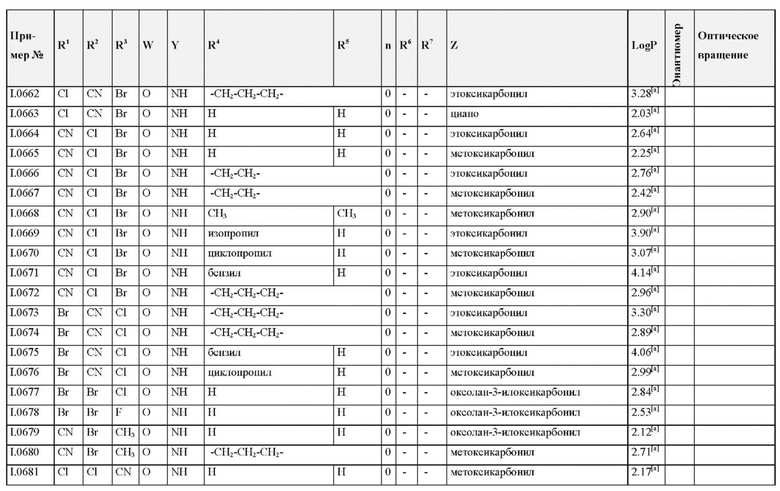
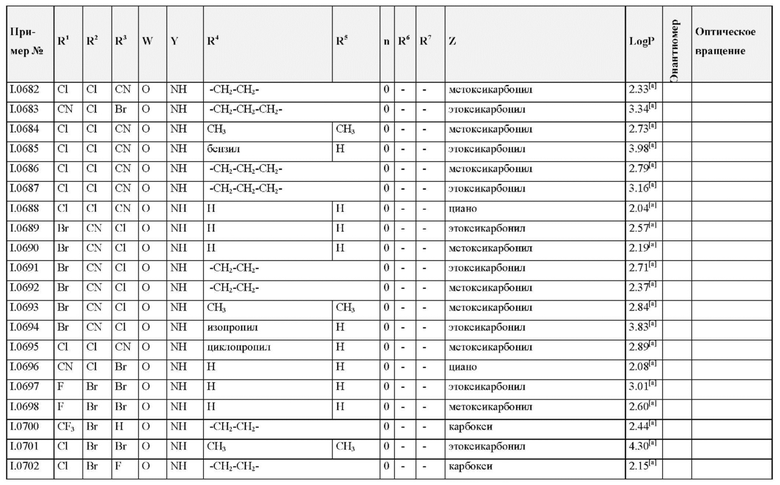
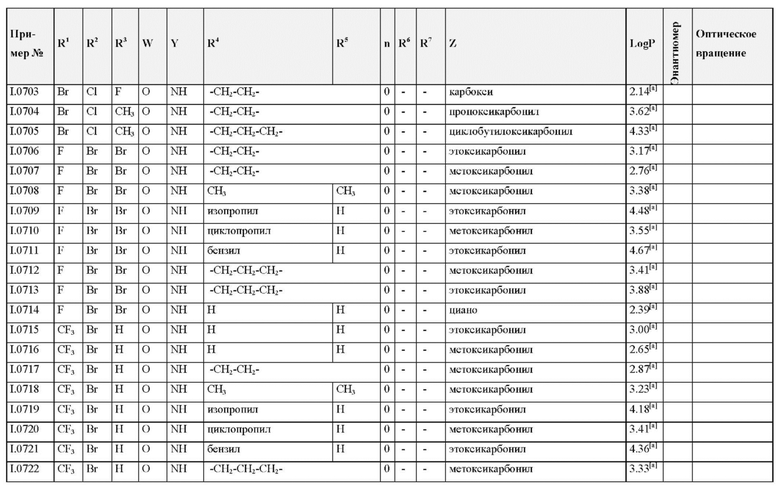
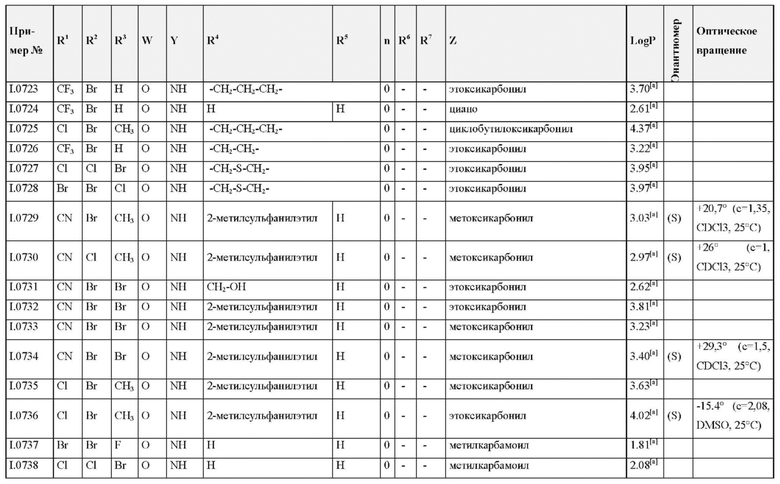
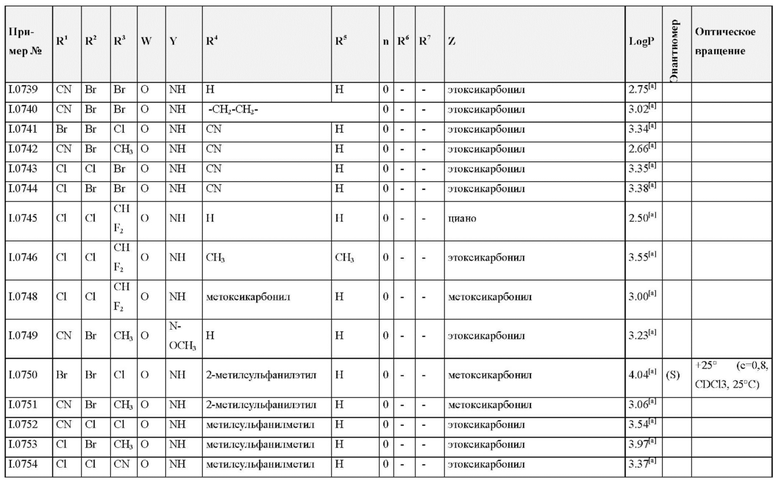
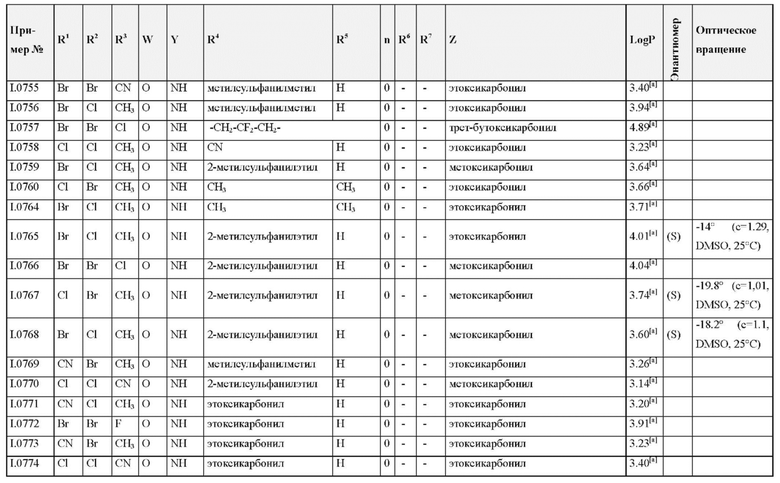
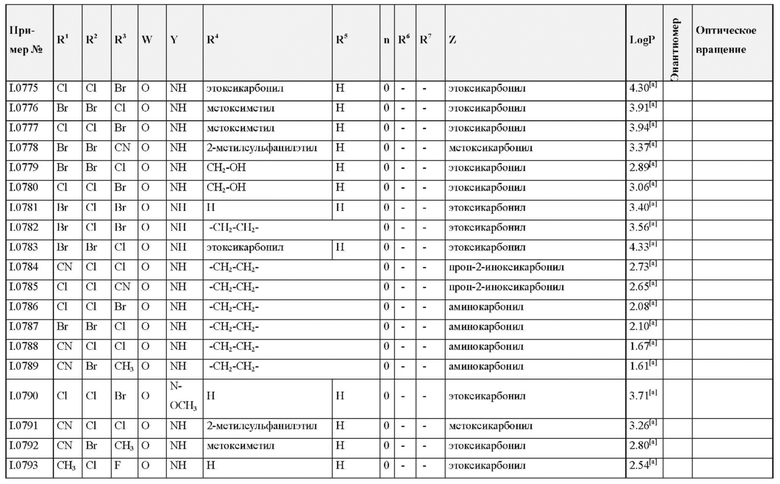
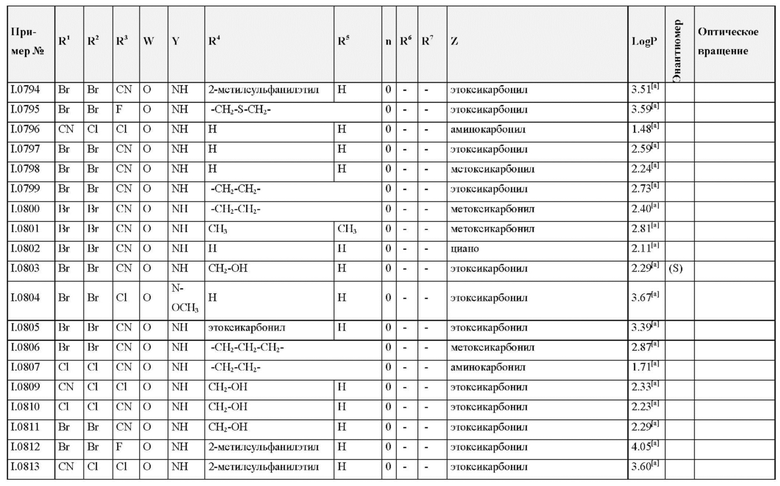
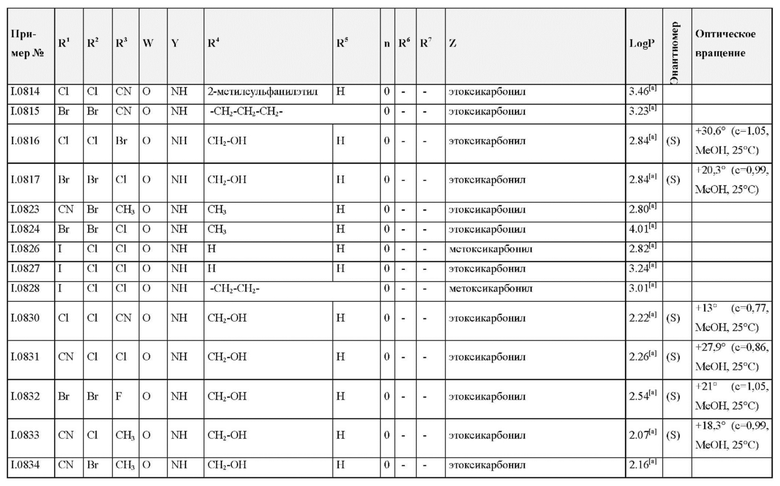
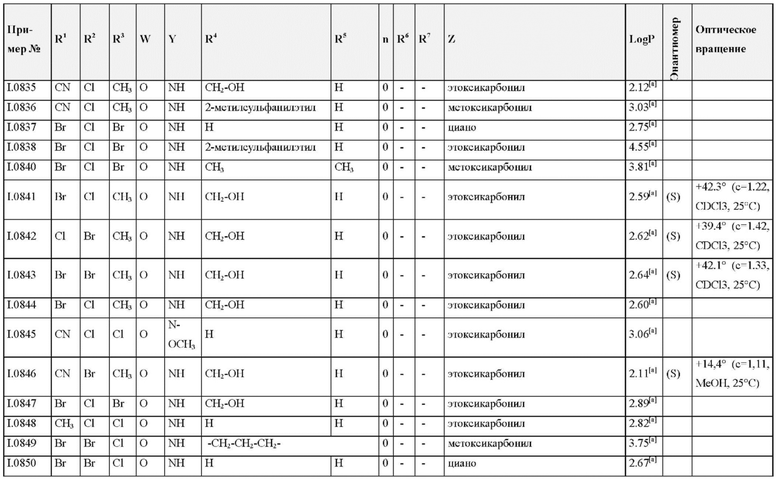
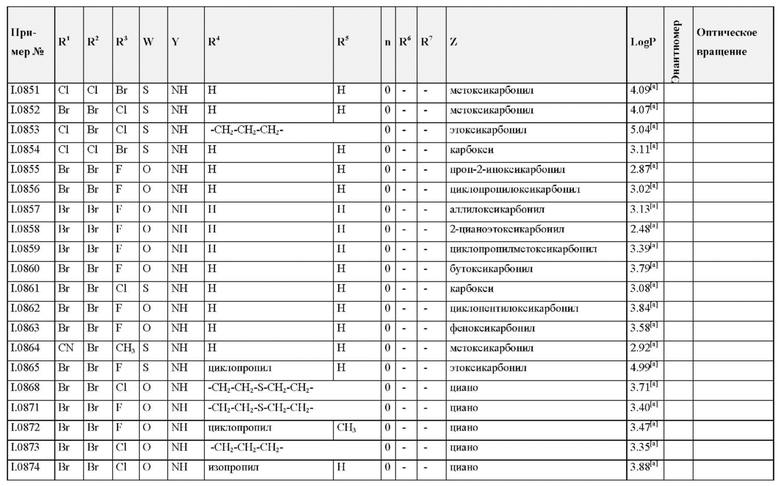
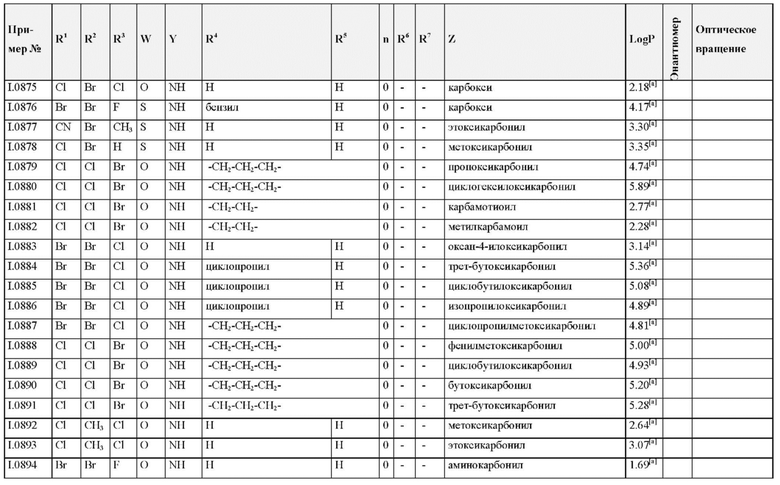
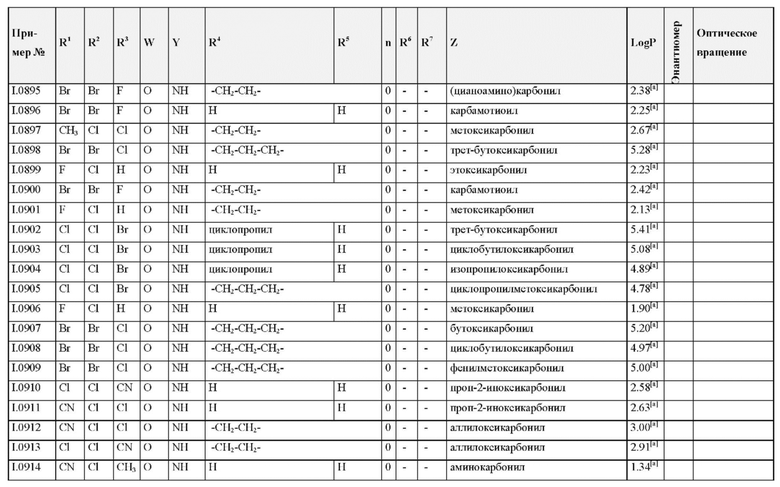
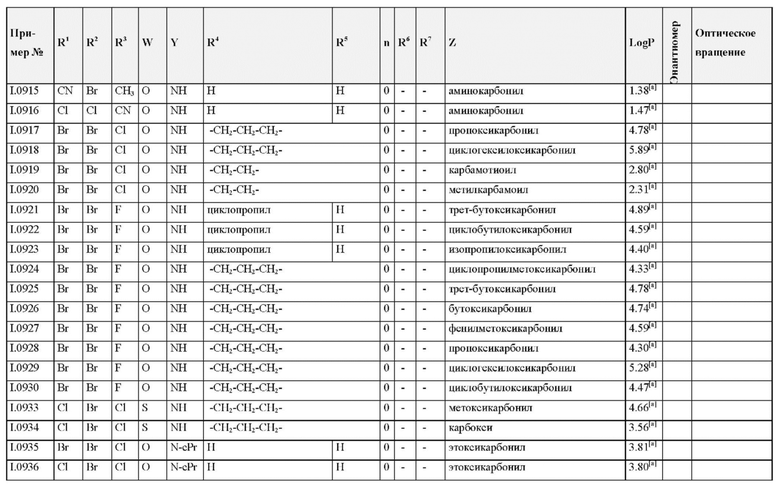
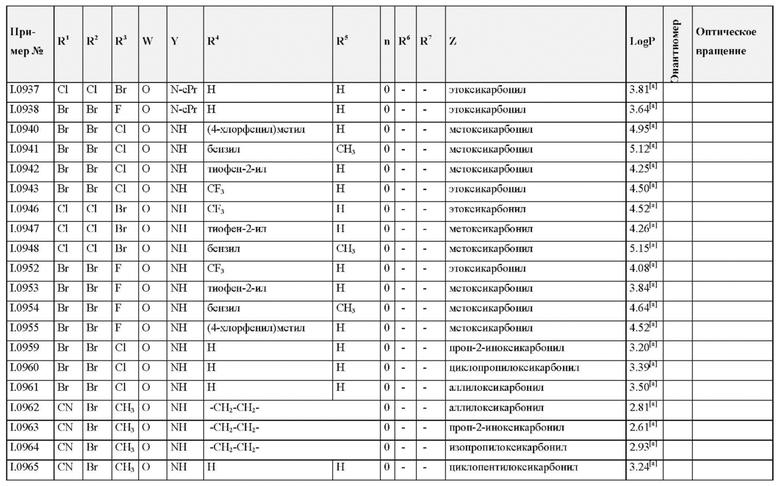
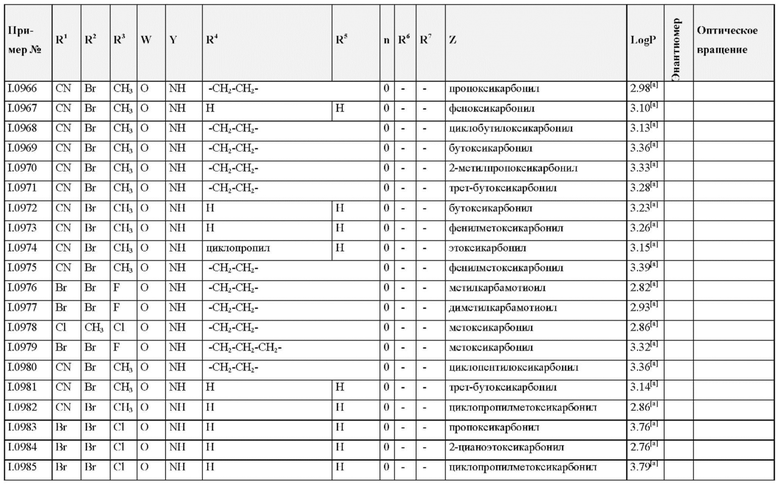
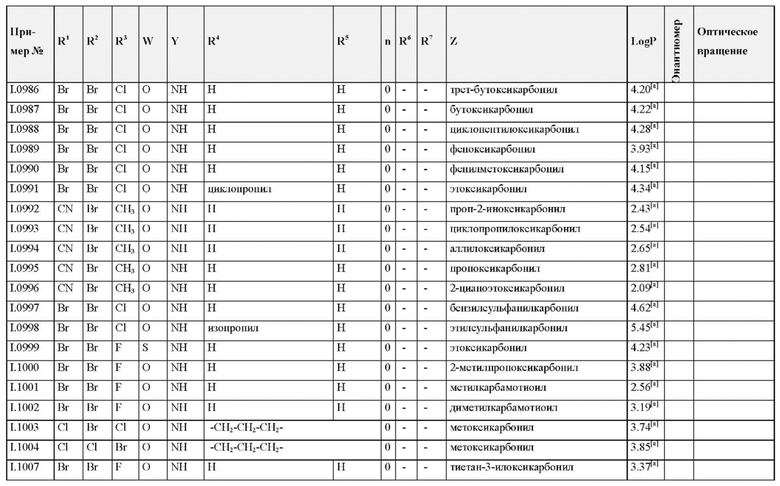
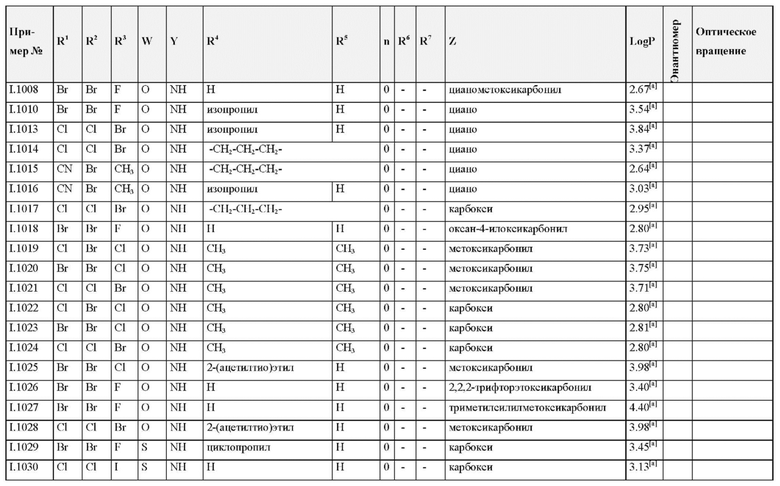
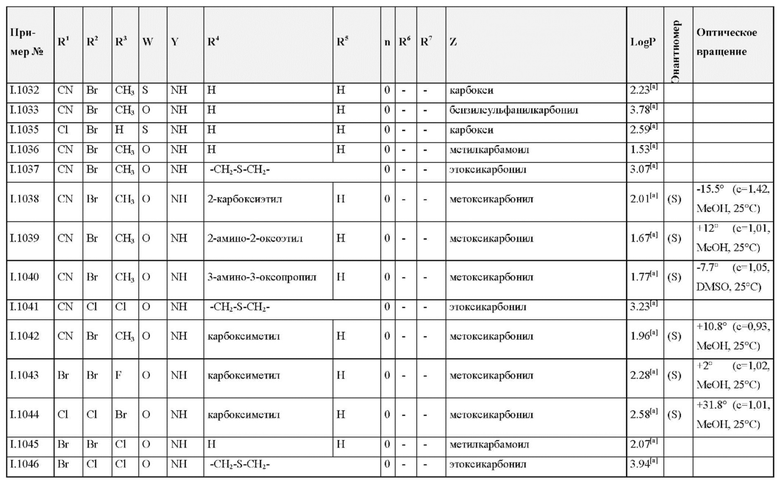
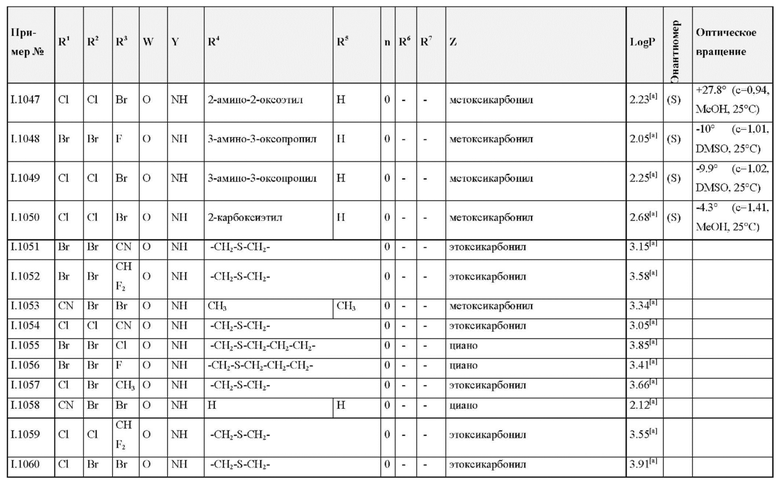
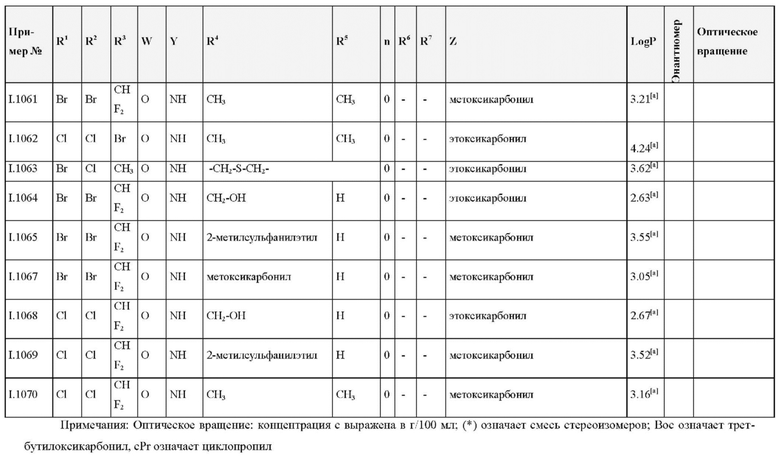
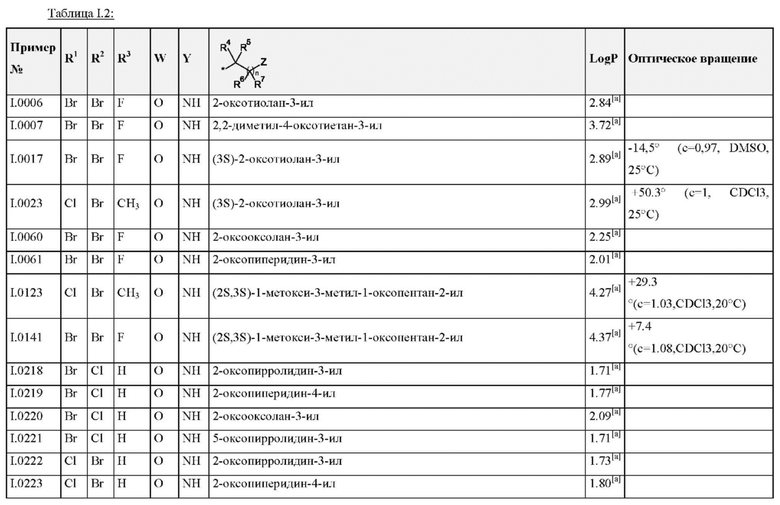
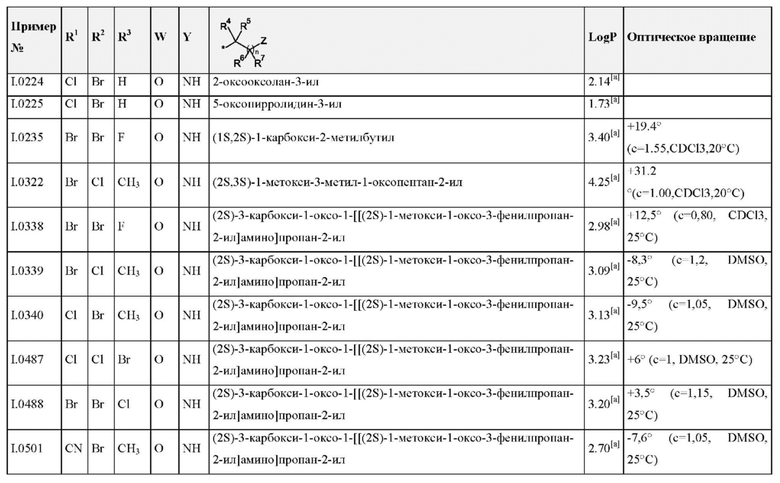
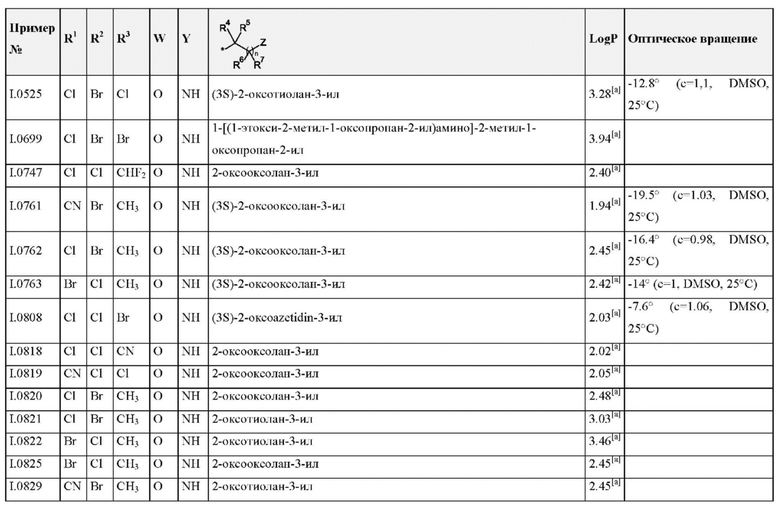
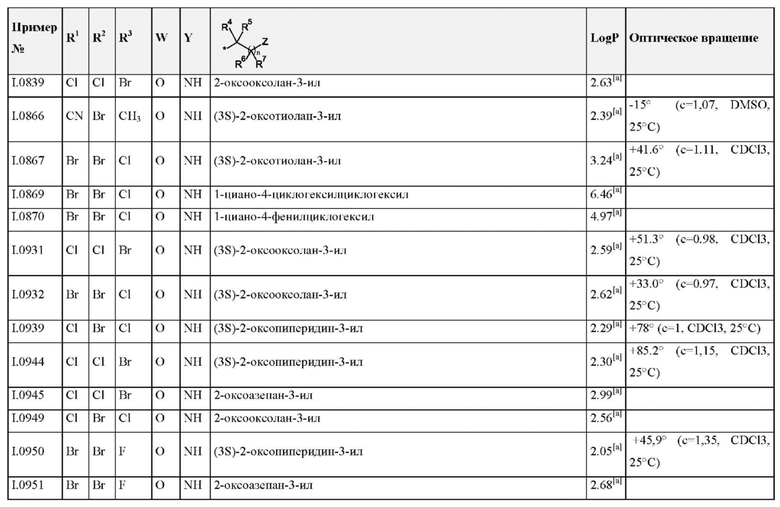
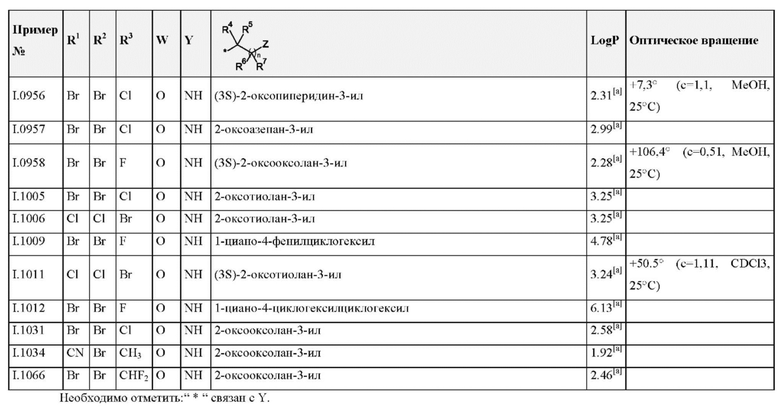
Следующая таблица II. 1 иллюстрирует неограничивающим образом примеры соединений в соответствии с формулой (II).
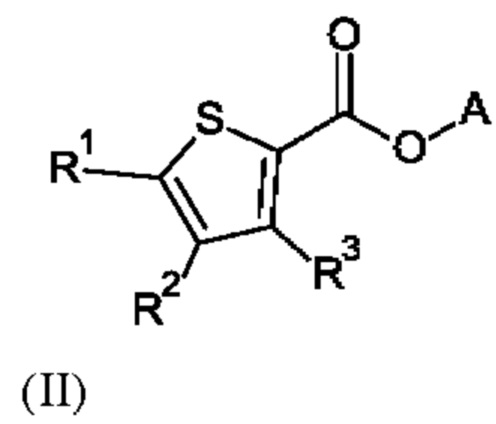
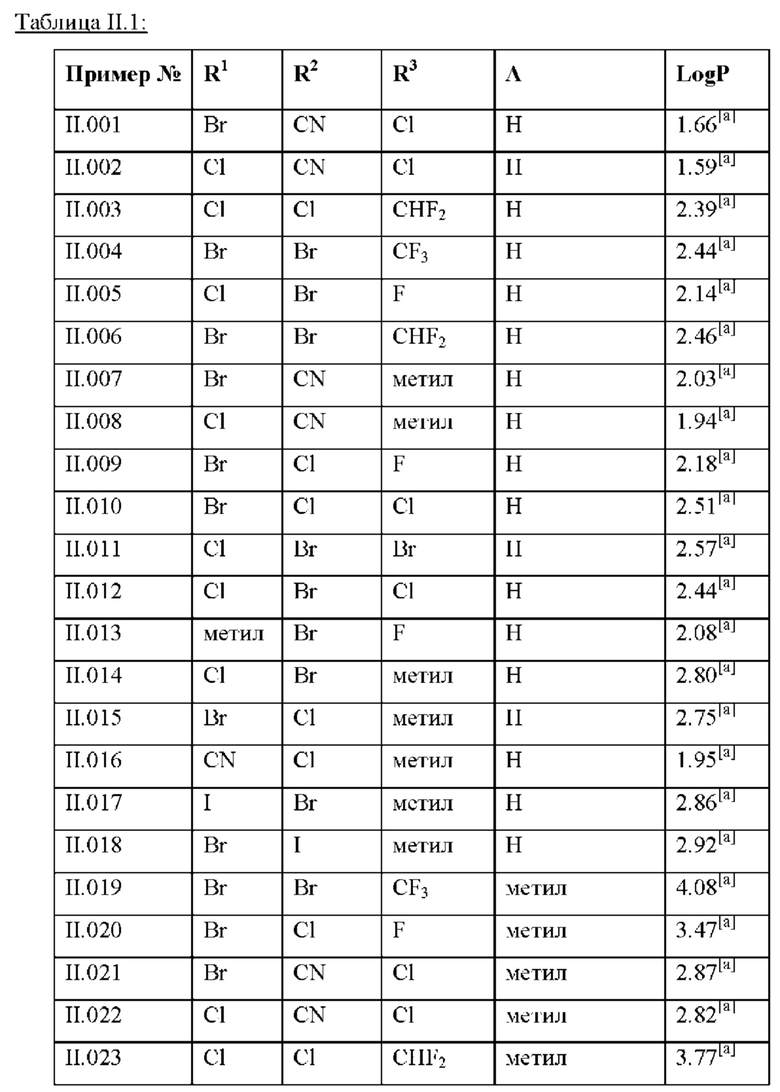
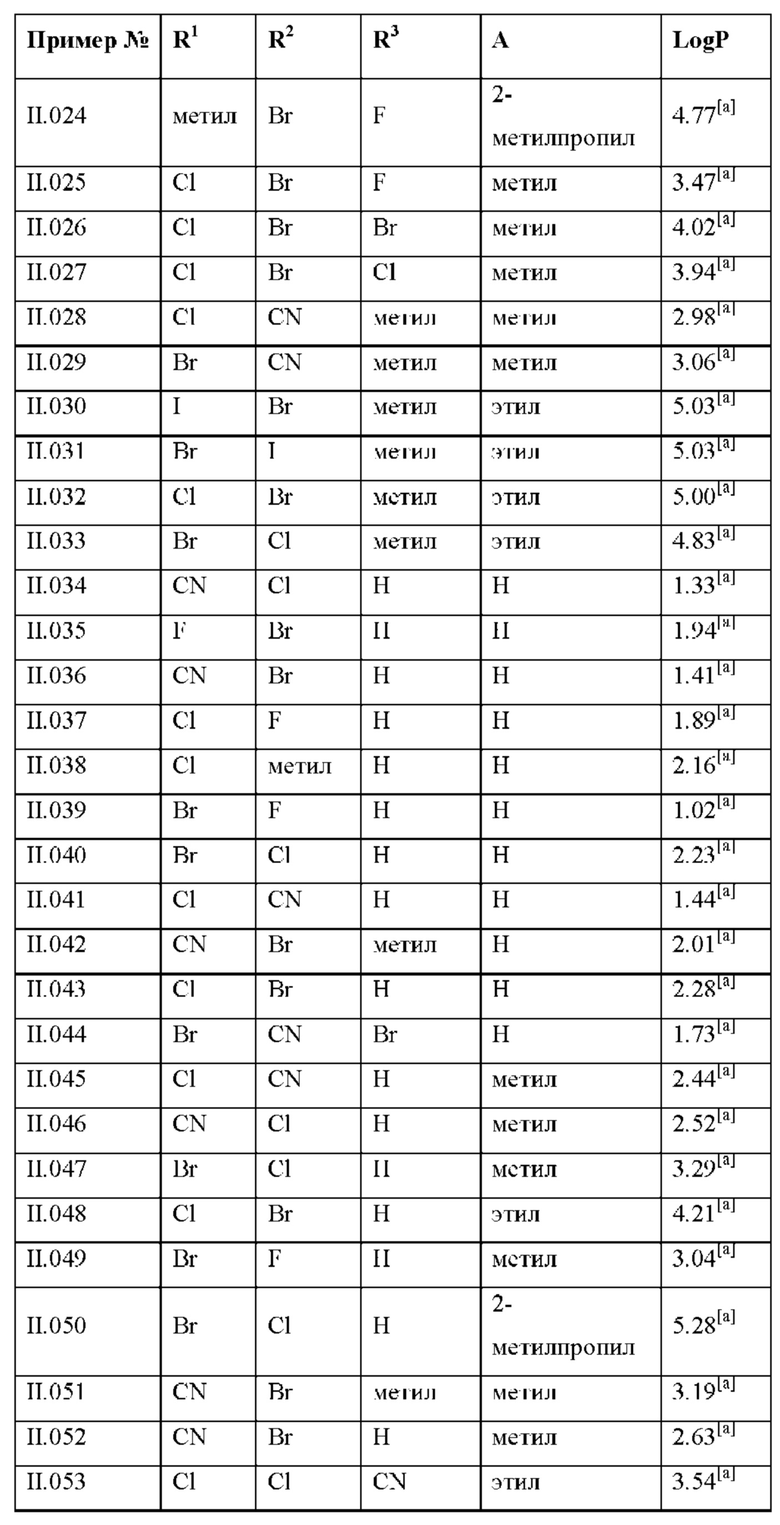
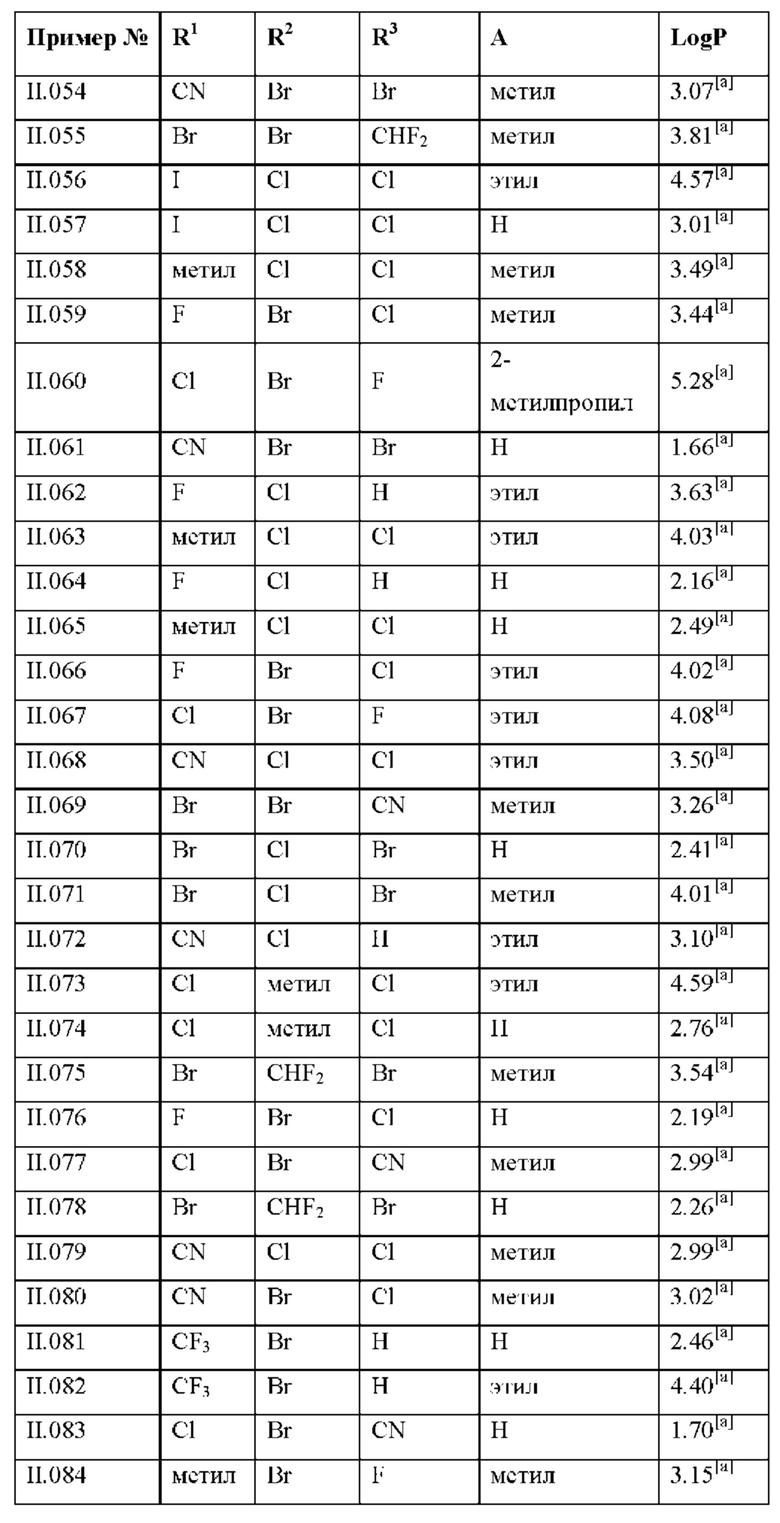
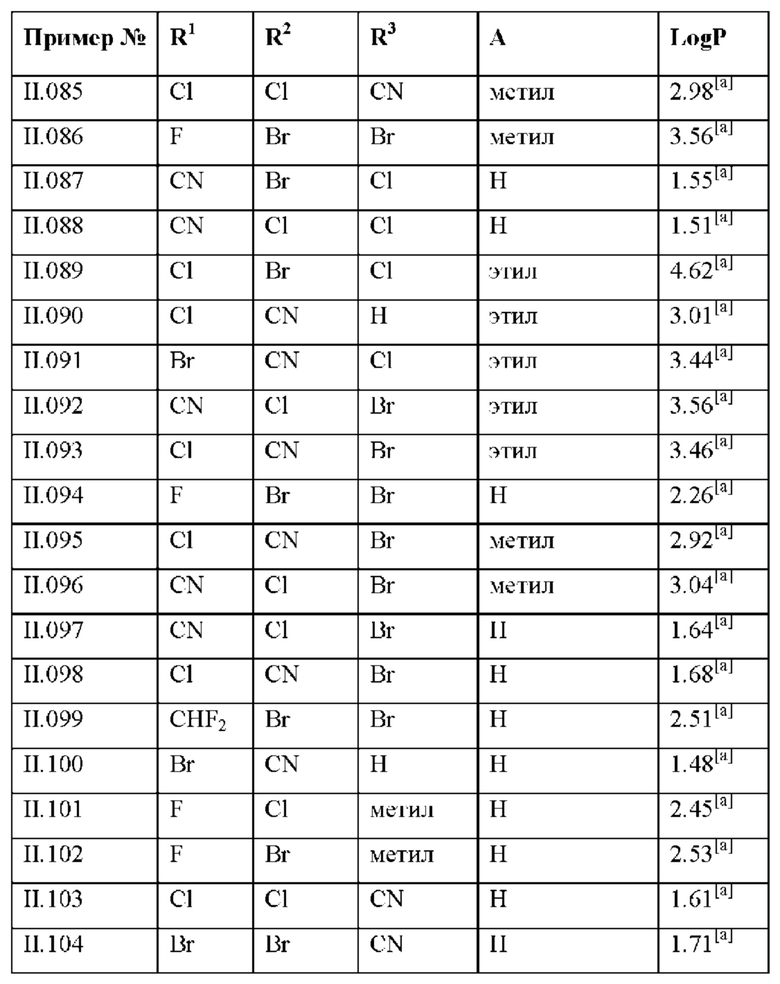
В вышеуказанных таблицах измерение значений LogP проводили в соответствии с директивой EEC 79/831 Annex V.A8 посредством ВЭЖХ (Высоко эффективная жидкостная хроматография) на колонке с обращенной фазой со следующими методами:
[a] значение LogP определяется посредством измерения LC-UV, в кислом диапазоне, с 0,1% муравьиной кислоты в воде и ацетонитриле в качестве элюента (линейный градиент от 10% ацетонитрила до 95% ацетонитрила).
[b] значение LogP определяется посредством измерения LC-UV, в нейтральном диапазоне, с 0.001 молярным раствором ацетата аммония в воде и ацетонитриле в качестве элюента (линейный градиент от 10% ацетонитрила до 95% ацетонитрила).
[c] значение LogP определяется посредством измерения LC-UV, в кислом диапазоне, с 0.1 фосфорной кислотой и ацетонитрилом в качестве элюента (линейный градиент от 10% ацетонитрила до 95% ацетонитрила).
Если в рамках одного и того же метода доступно более одного значения LogP, все значения указываются и разделяются знаком «+».
Калибровку проводили с неразветвленными алкан-2-онами (с 3 до 16 атомами углерода) с известными значениями LogP (измерение значений LogP с использованием времени удерживания с линейной интерполяцией между последовательными алканонами). Максимальные значения лямбда определяли с помощью УФ-спектров от 200 нм до 400 нм и значениями в максимуме хроматографических сигналов.
1H-ЯМР выбранных примеров записывают в виде списков пиков 1Н-ЯМР. Для каждого пика сигнала указано dзначение в ppm и интенсивность сигнала в круглых скобках. Между dпарами -значение интенсивность сигнала стоит точка с запятой в качестве разделителя.
Таким образом, список пиков примера имеет вид:
d1 (интенсивность 1); d2 (интенсивность 2); јјј; di (интенсивность i); јј; dn (интенсивность n)
Интенсивность резких сигналов коррелирует с высотой сигналов в распечатанном примере спектра ЯМР в см и показывает реальные отношения интенсивностей сигналов. Из широких сигналов можно показать несколько пиков или середину сигнала и их относительную интенсивность по сравнению с наиболее интенсивным сигналом в спектре.
Для калибровки химического сдвига для спектров 1 Н мы используем тетраметилсилан и/или химический сдвиг используемого растворителя, особенно в случае спектров, измеренных в ДМСО. Следовательно, в списках пиков ЯМР пик тетраметилсилана может встречаться, но не обязательно.
Списки пиков 1 Н-ЯМР аналогичны классическим отпечаткам 1 Н-ЯМР и поэтому обычно содержат все пики, которые перечислены при классической интерпретации ЯМР.
Кроме того, они могут показывать, как классические отпечатки 1 Н-ЯМР, сигналы растворителей, стереоизомеров целевых соединений, которые также являются объектом изобретения, и/или пики примесей.
Чтобы показать сигналы соединений в дельта-диапазоне растворителей и/или воды, обычные пики растворителей, например, пики ДМСО в ДМСО-D 6 и пик воды показаны в наших списках пиков 1 Н-ЯМР и обычно имеют средняя высокая интенсивность.
Пики стереоизомеров целевых соединений и/или пики примесей обычно в среднем имеют меньшую интенсивность, чем пики целевых соединений (например, с чистотой >90%).
Такие стереоизомеры и/или примеси могут быть типичными для конкретного способа получения. Следовательно, их пики могут помочь распознать воспроизведение нашего процесса приготовления по «отпечаткам побочных продуктов».
Эксперт, вычисляющий пики целевых соединений известными методами (MestreC, ACD-симуляция, а также с эмпирически оцененными математическими ожиданиями), может при необходимости выделить пики целевых соединений, опционально используя дополнительные фильтры интенсивности. Это выделение было бы похоже на выделение соответствующего пика при классической интерпретации 1 Н-ЯМР.
Данные 13С-ЯМР отображаются аналогично данным 1H-ЯМР в виде перечней пиков из широкополосных спектров 13С-ЯМР с развязкой. Сигналы растворителя и тетраметилсилана 13С-ЯМР исключаются из калибровки относительной интенсивности, поскольку эти сигналы могут иметь очень высокую интенсивность.
Более подробную информацию об описании данных ЯМР со списками пиков вы найдете в публикации «Цитирование данных списка пиков ЯМР в патентных заявках» базы данных раскрытия информации исследований №564025.


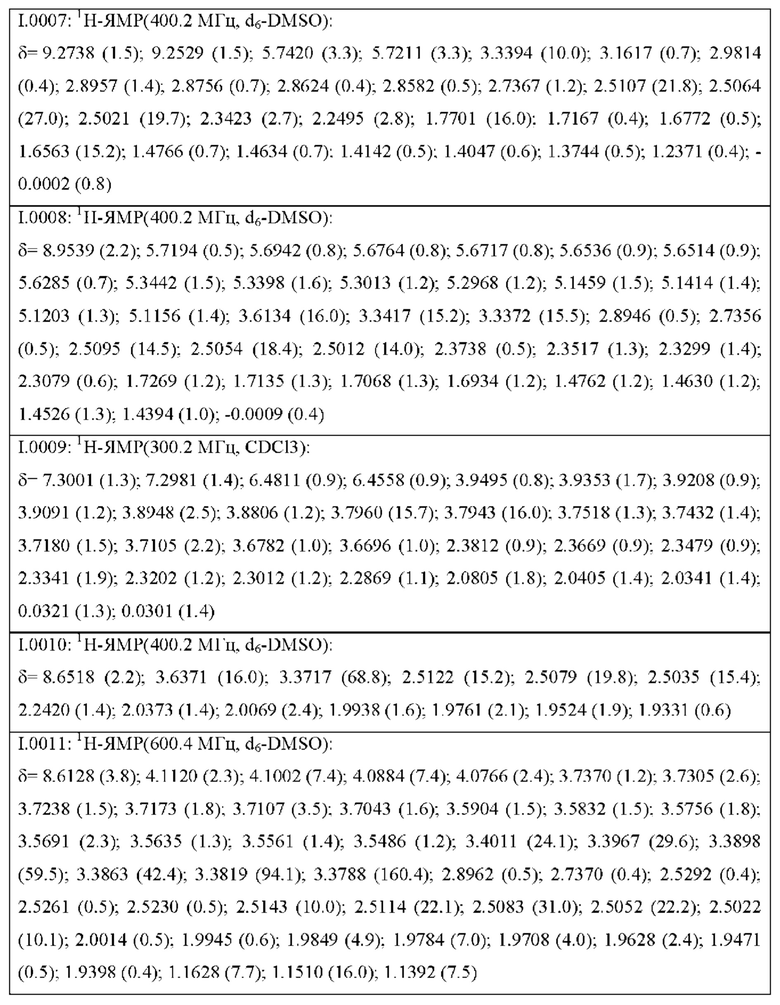
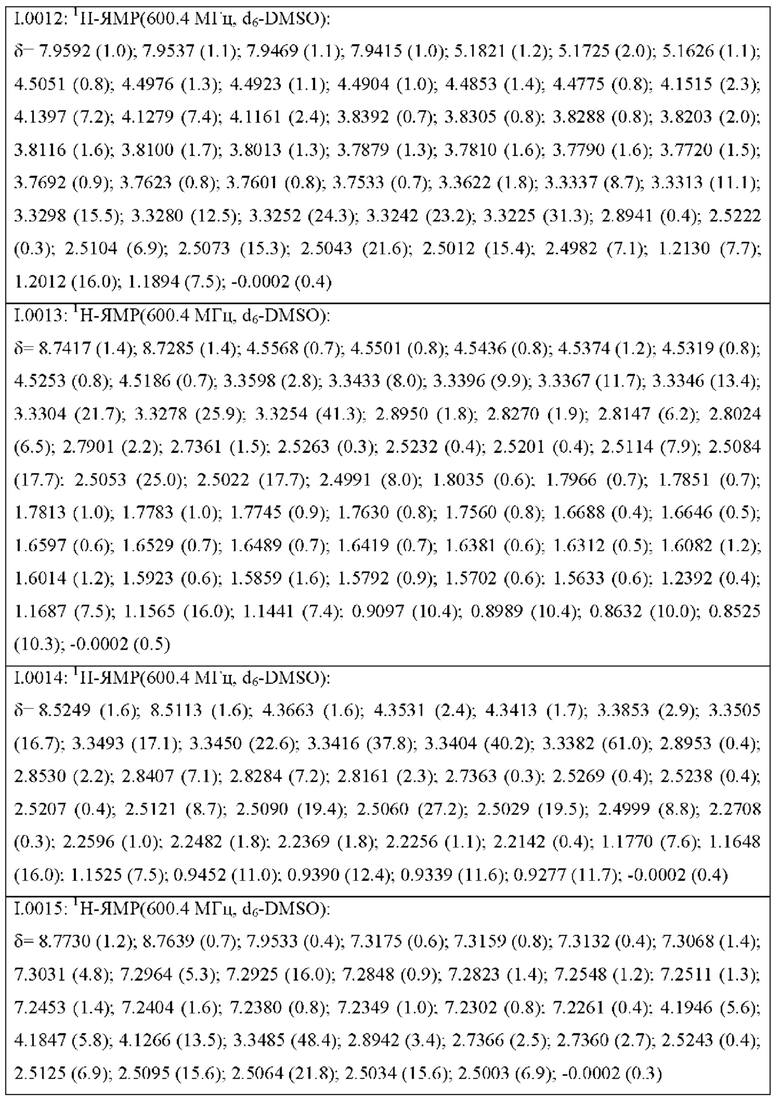

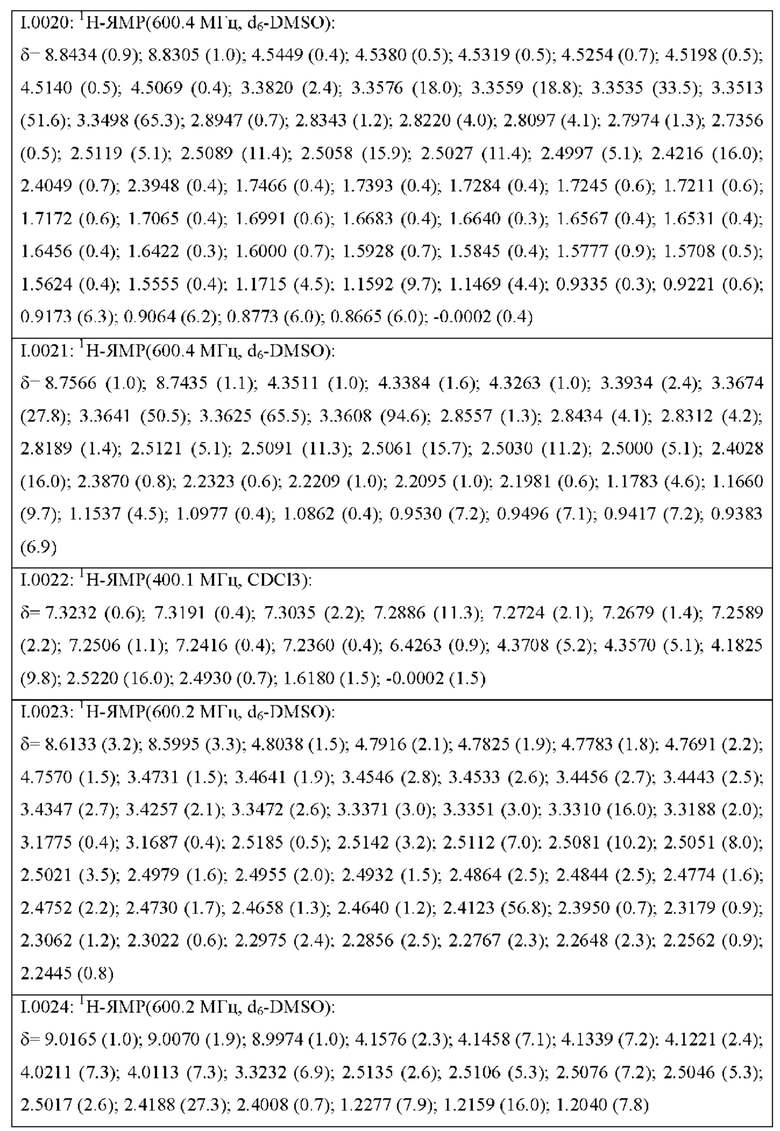
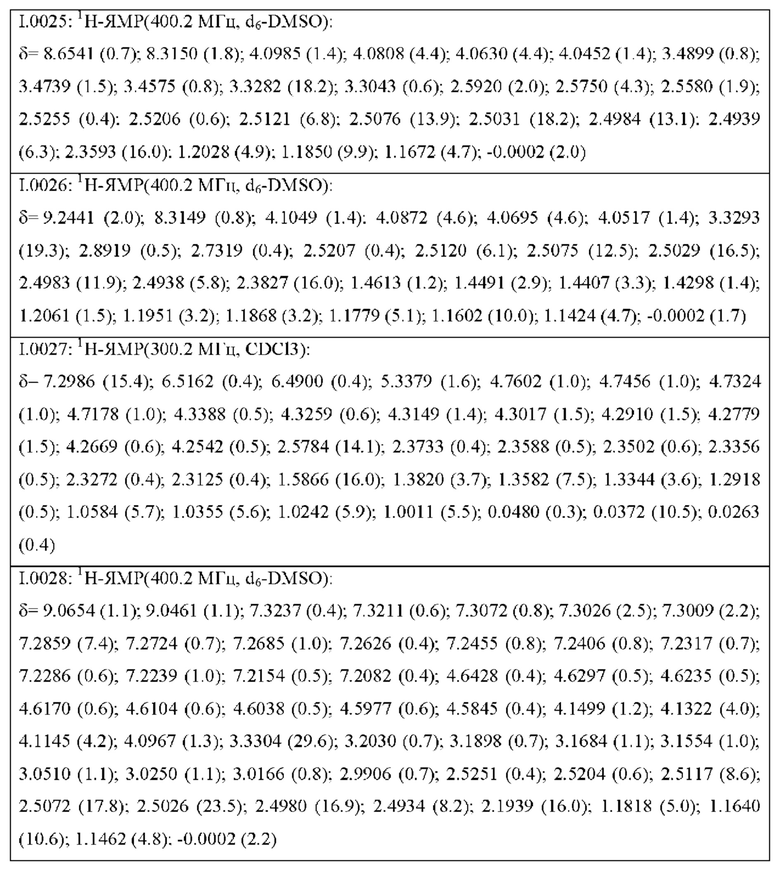
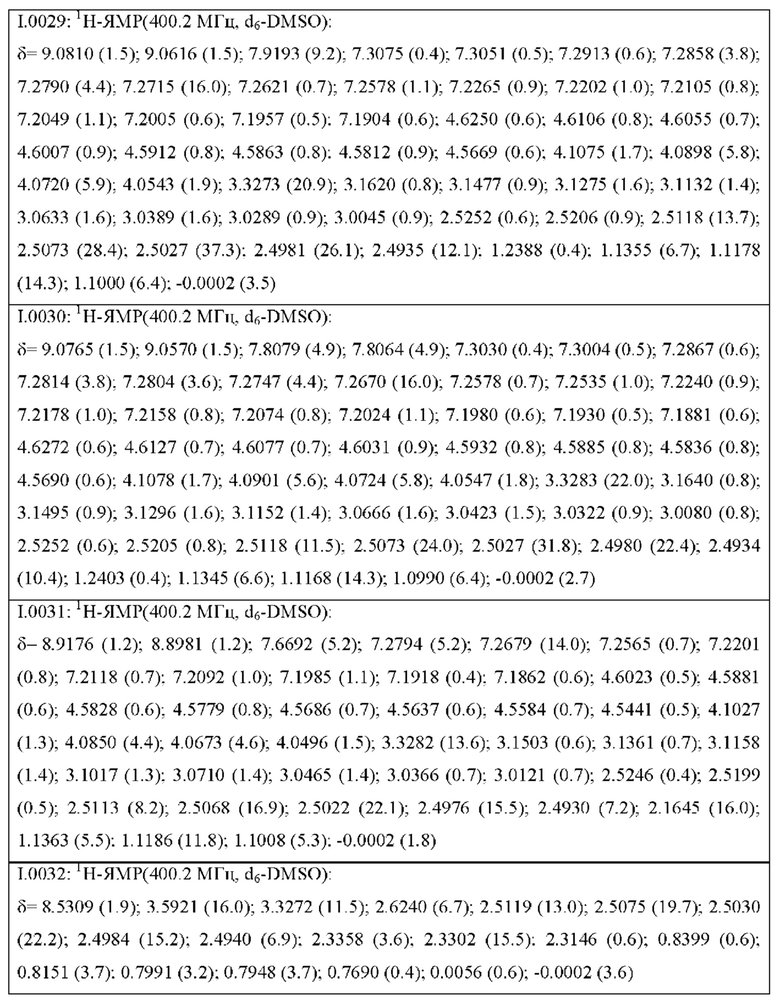
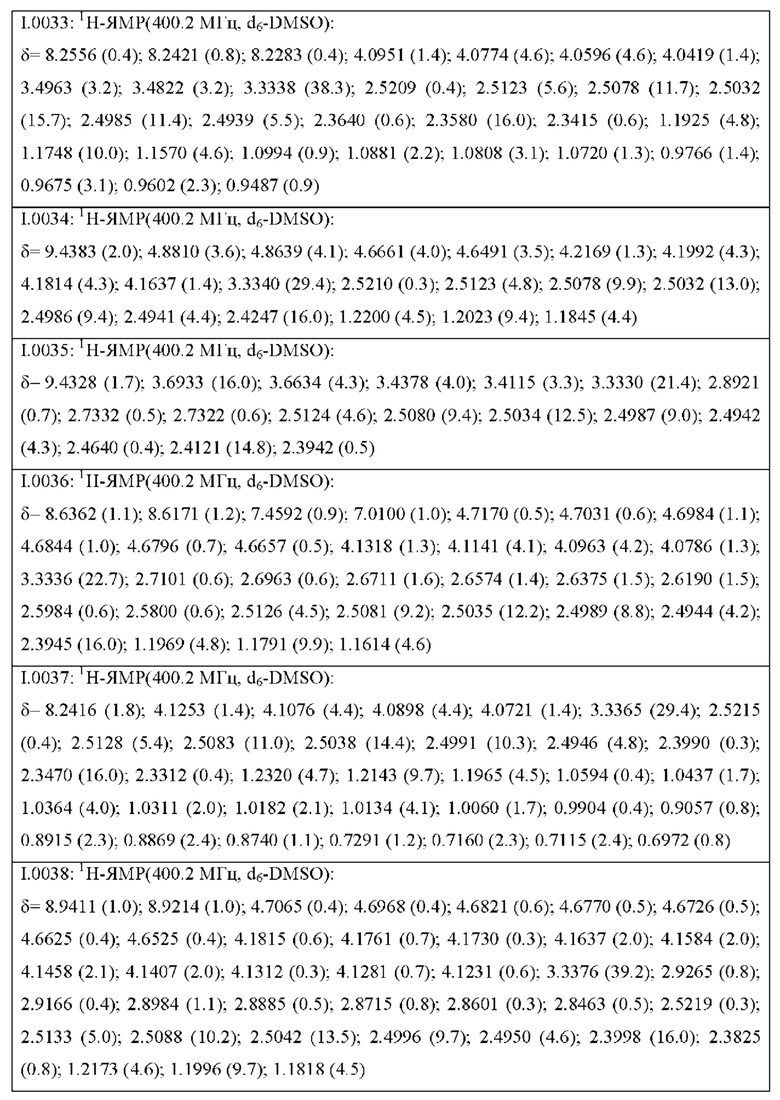
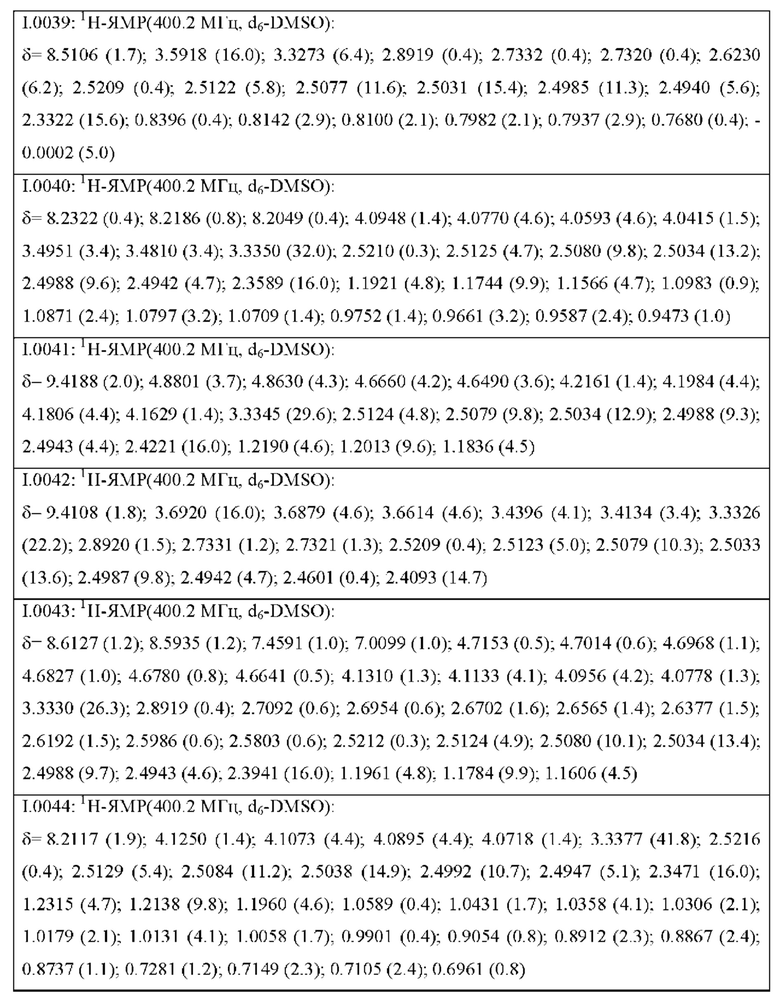
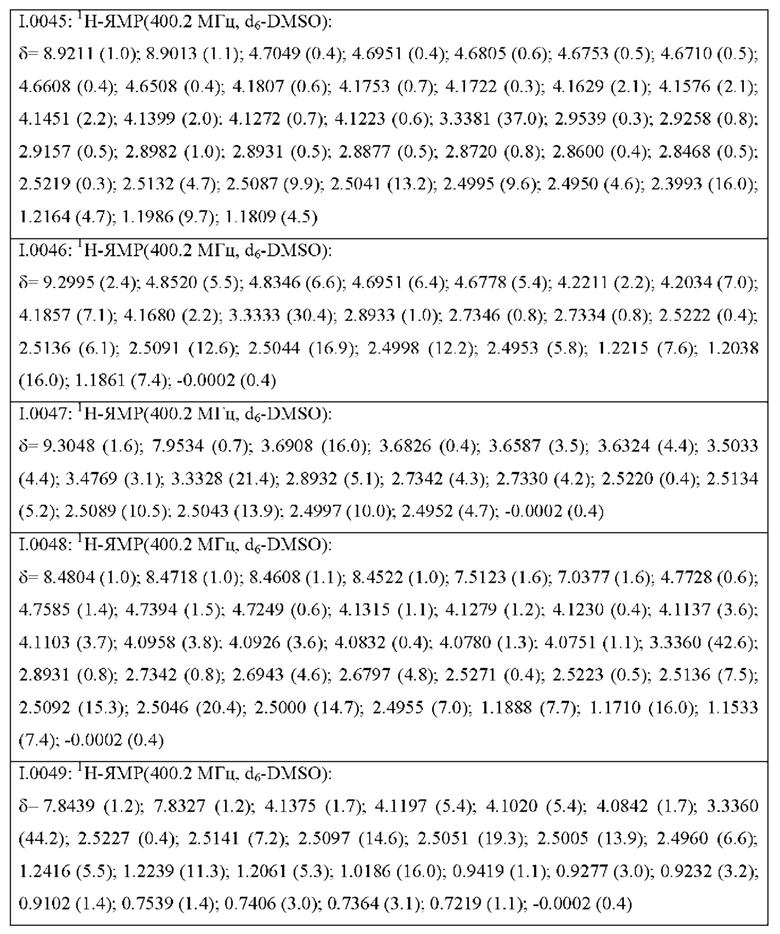
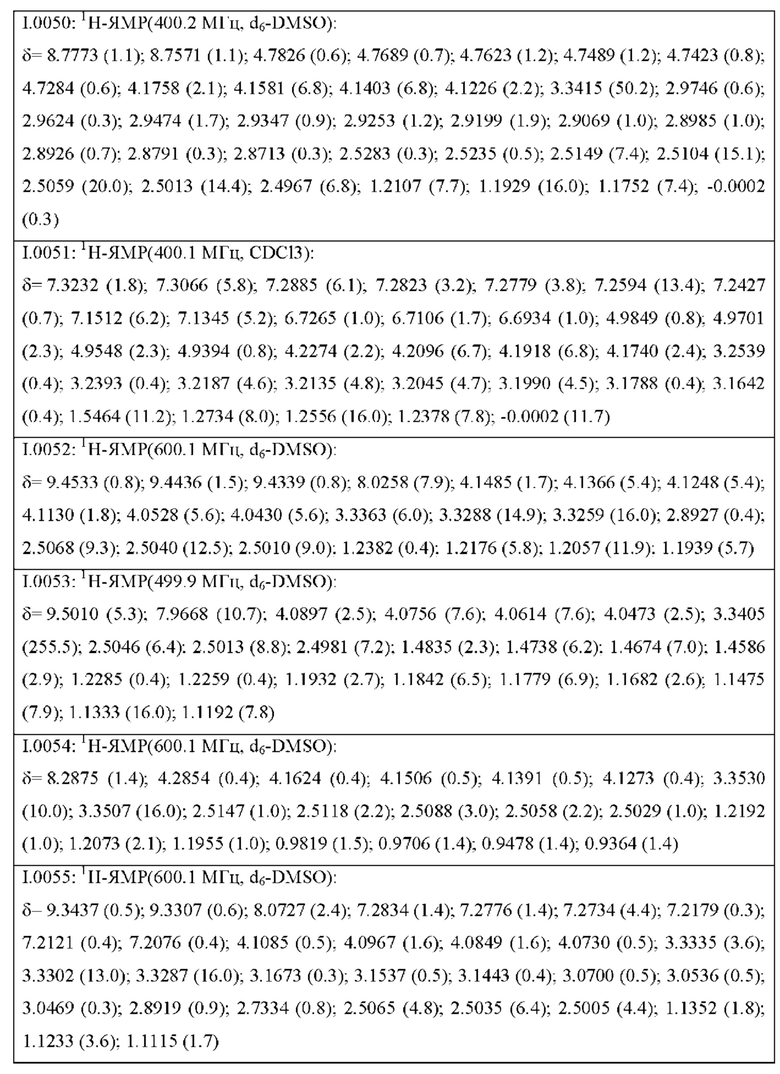

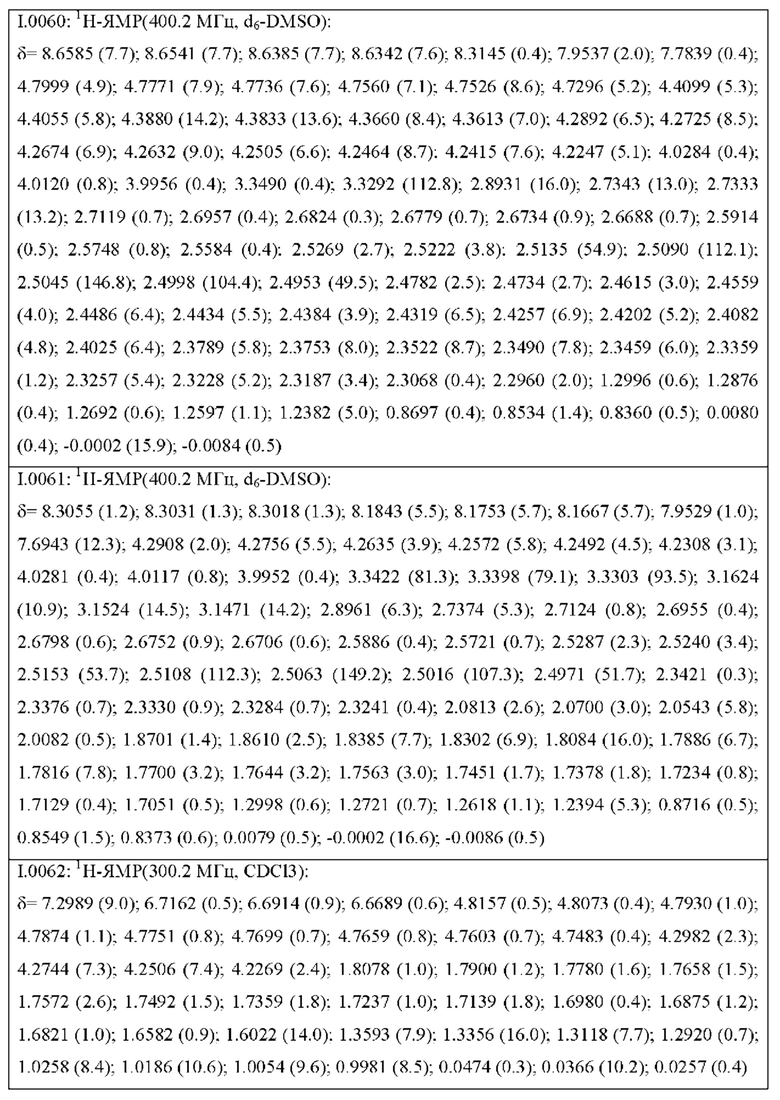




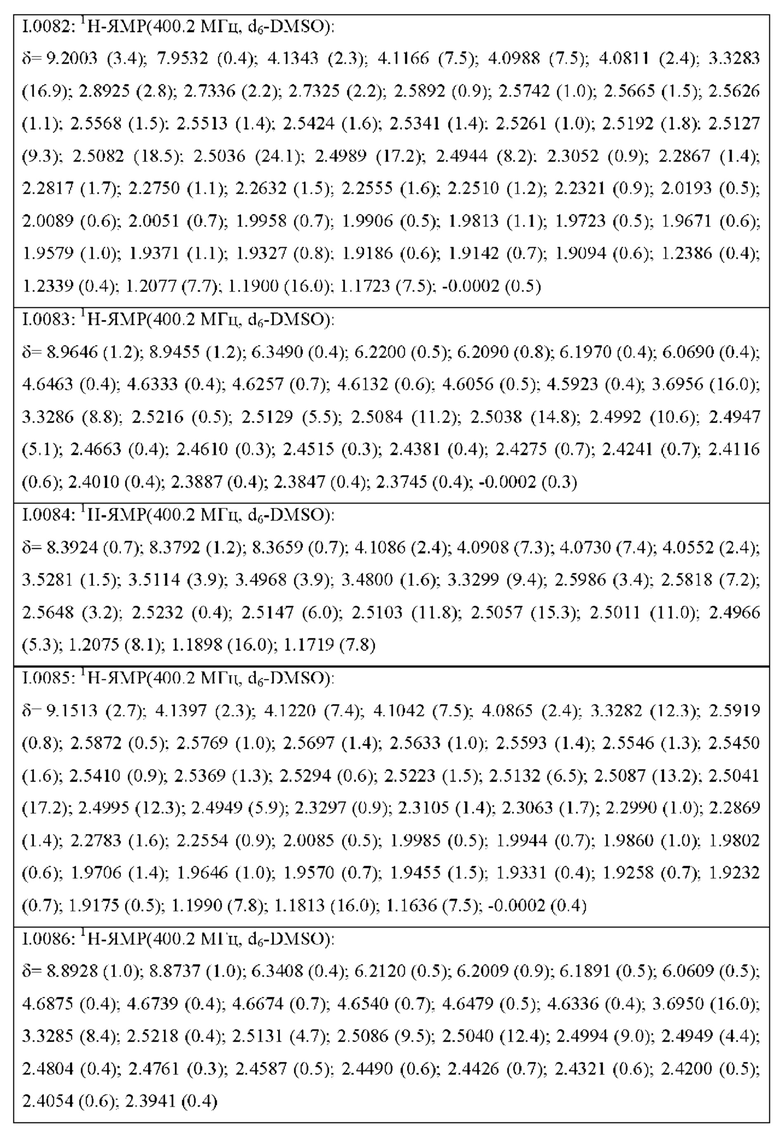

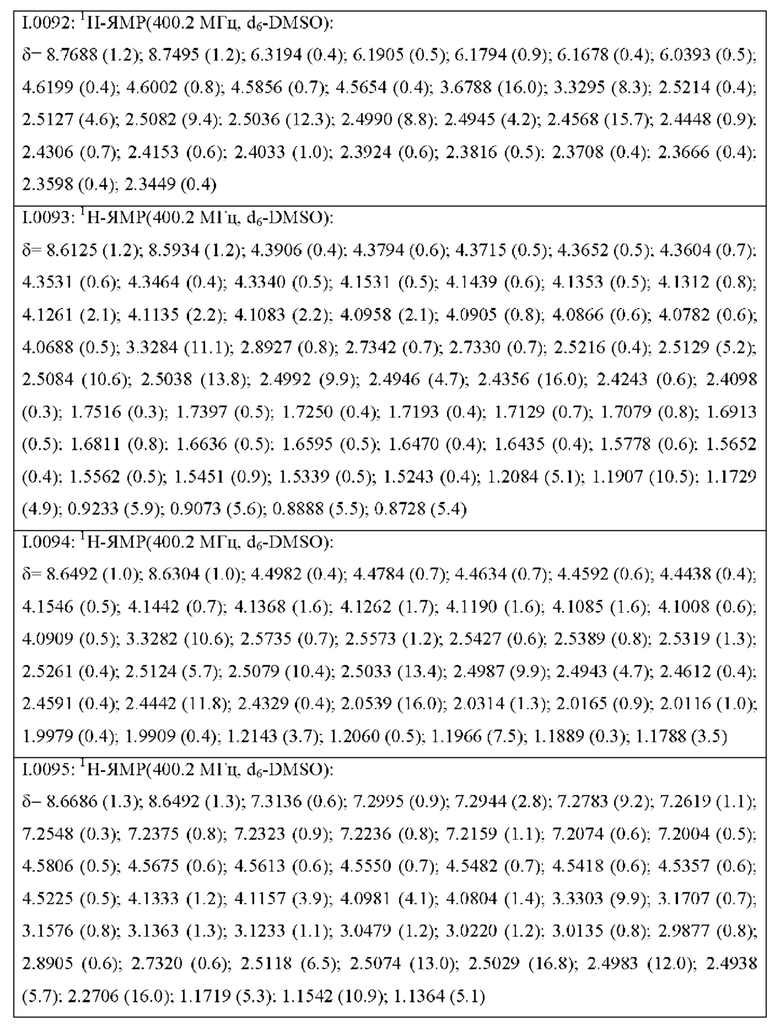

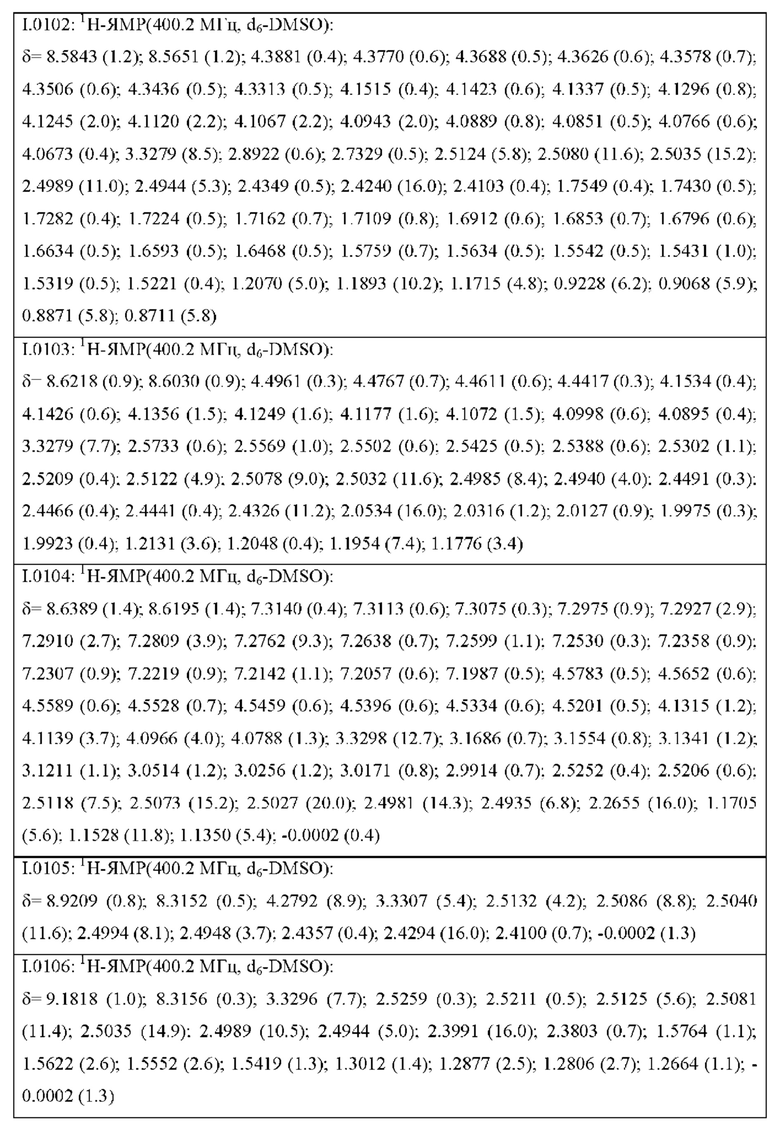
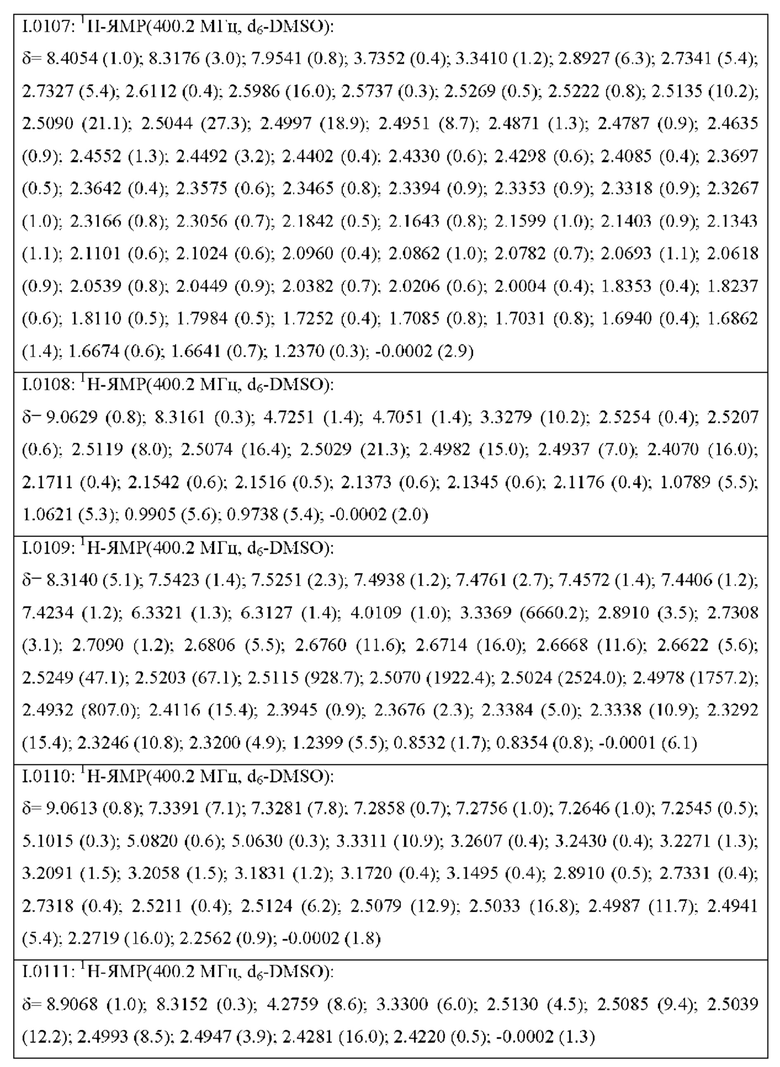


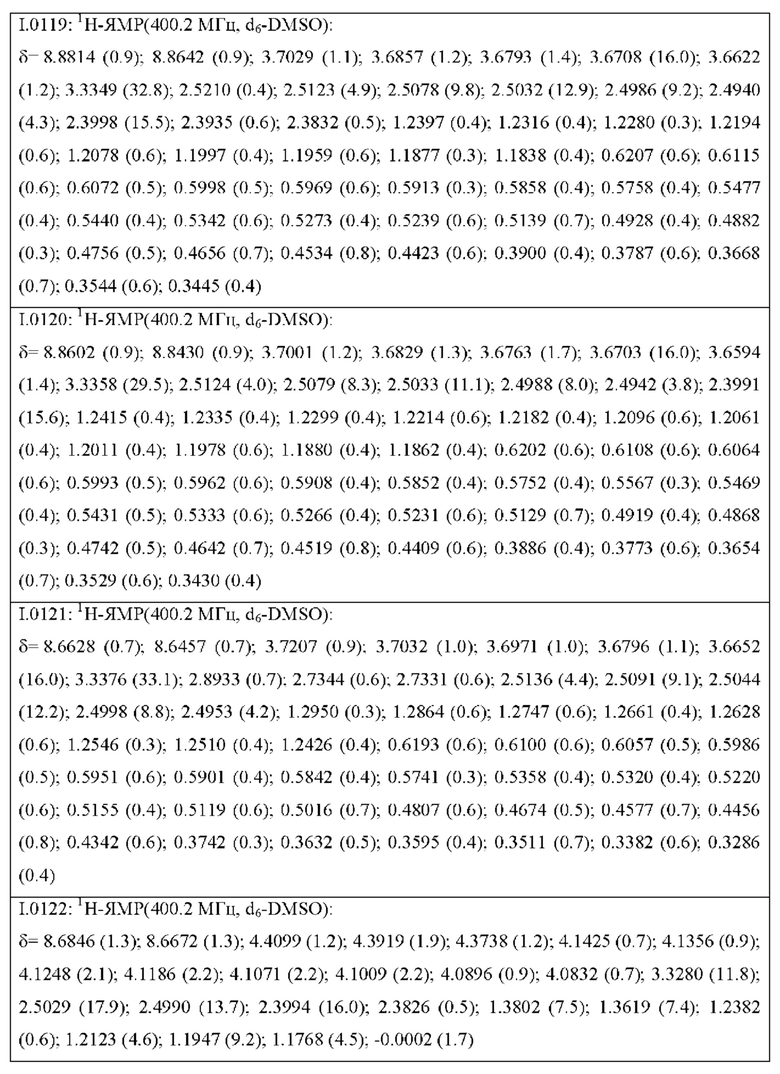
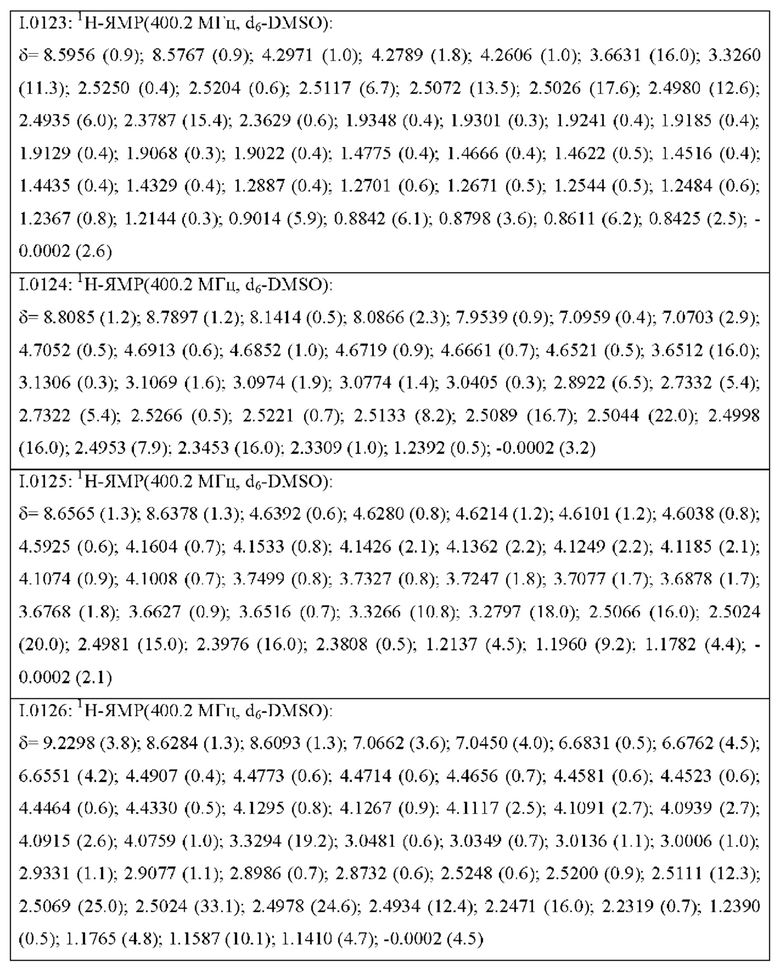
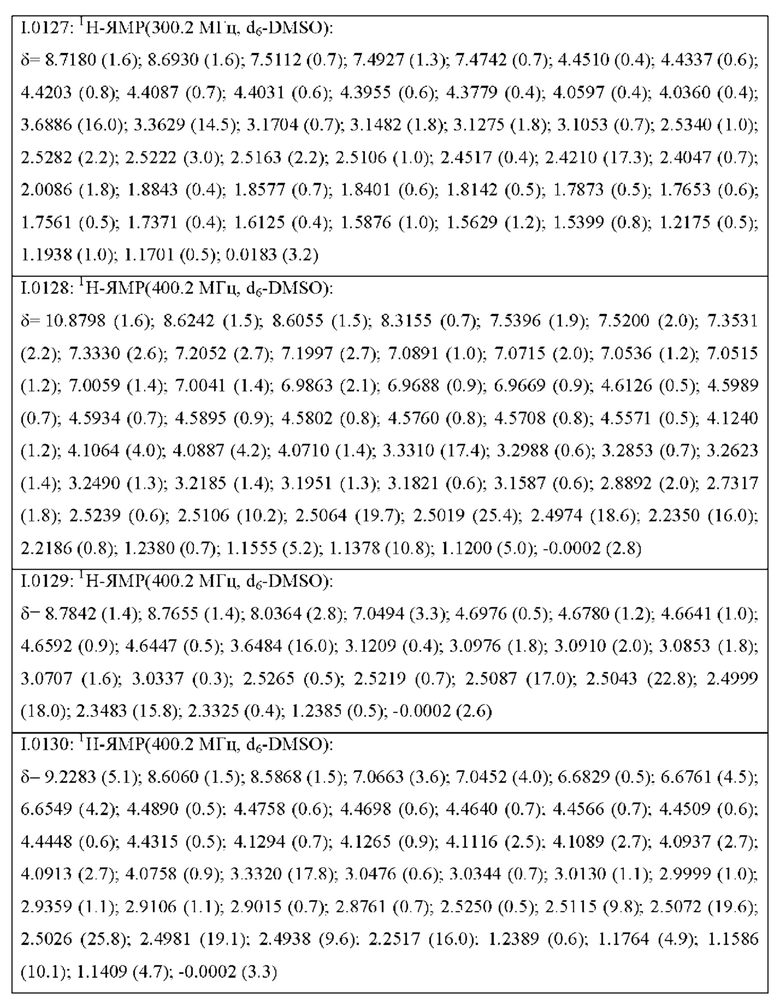
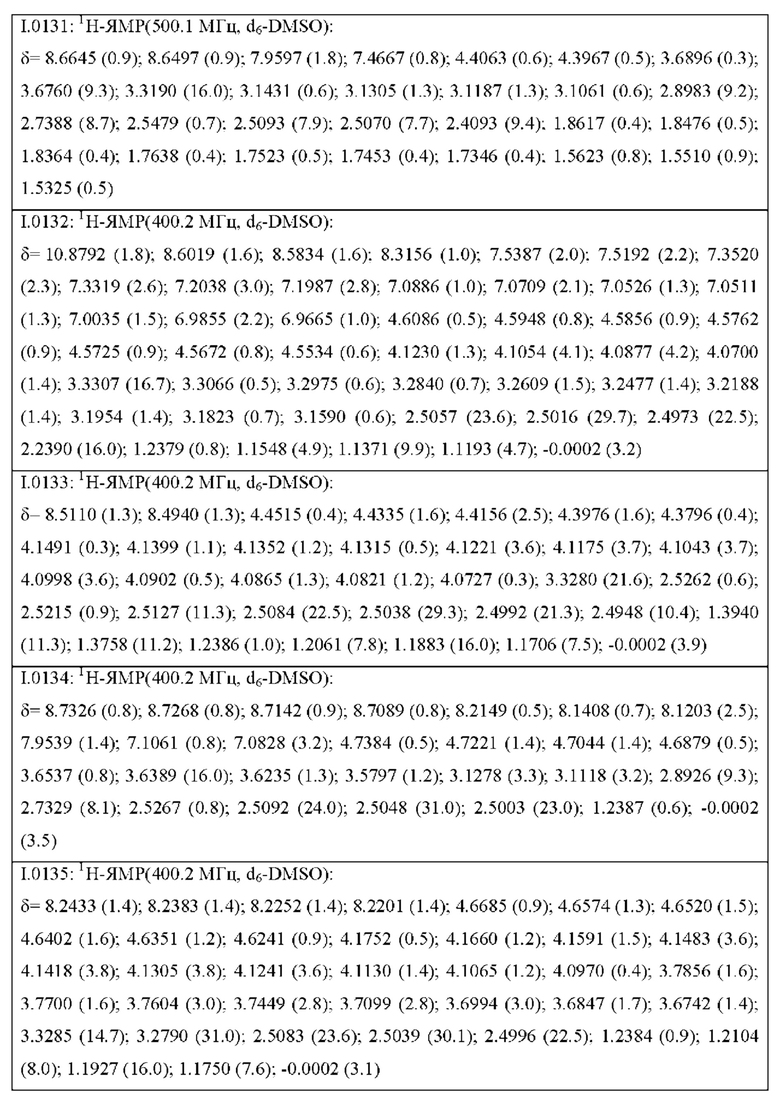


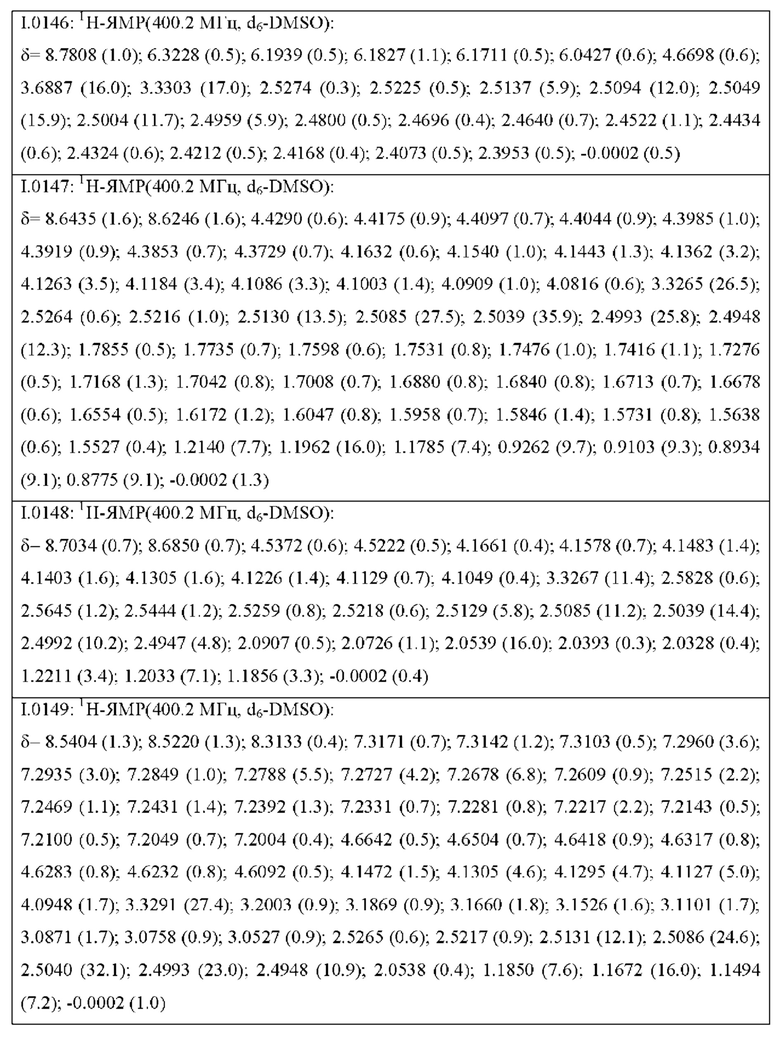
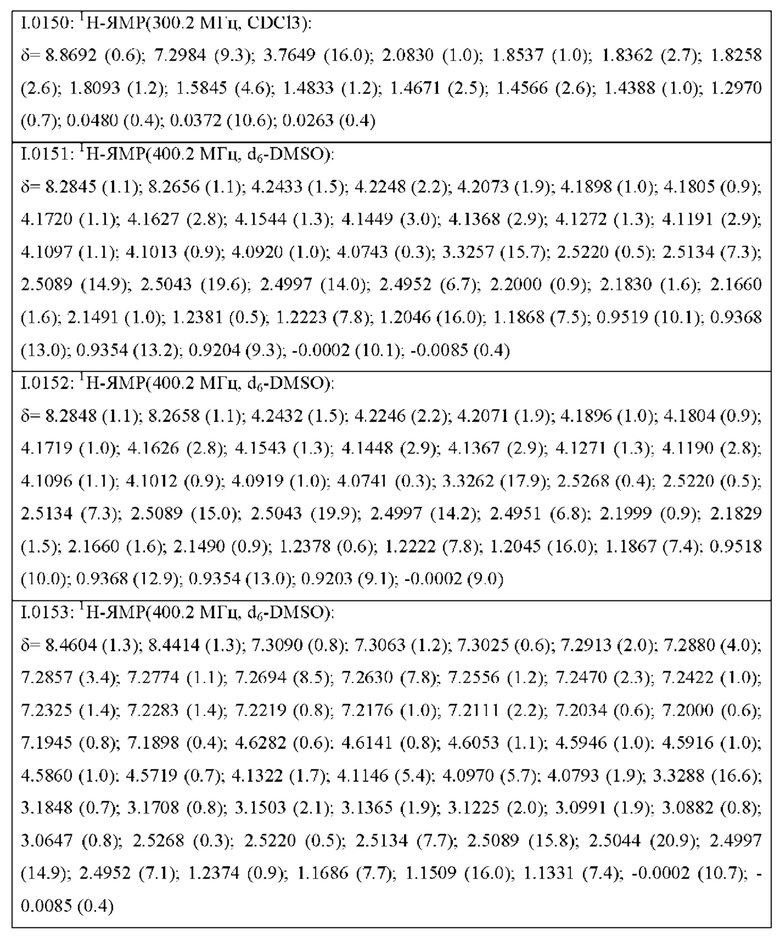

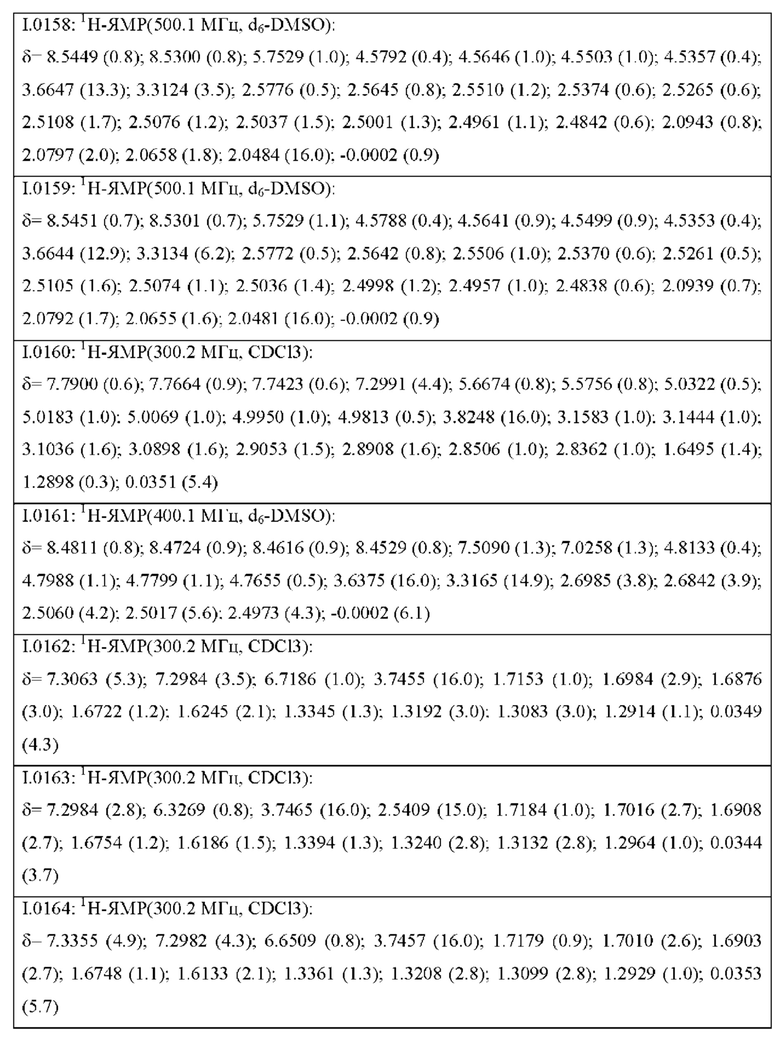
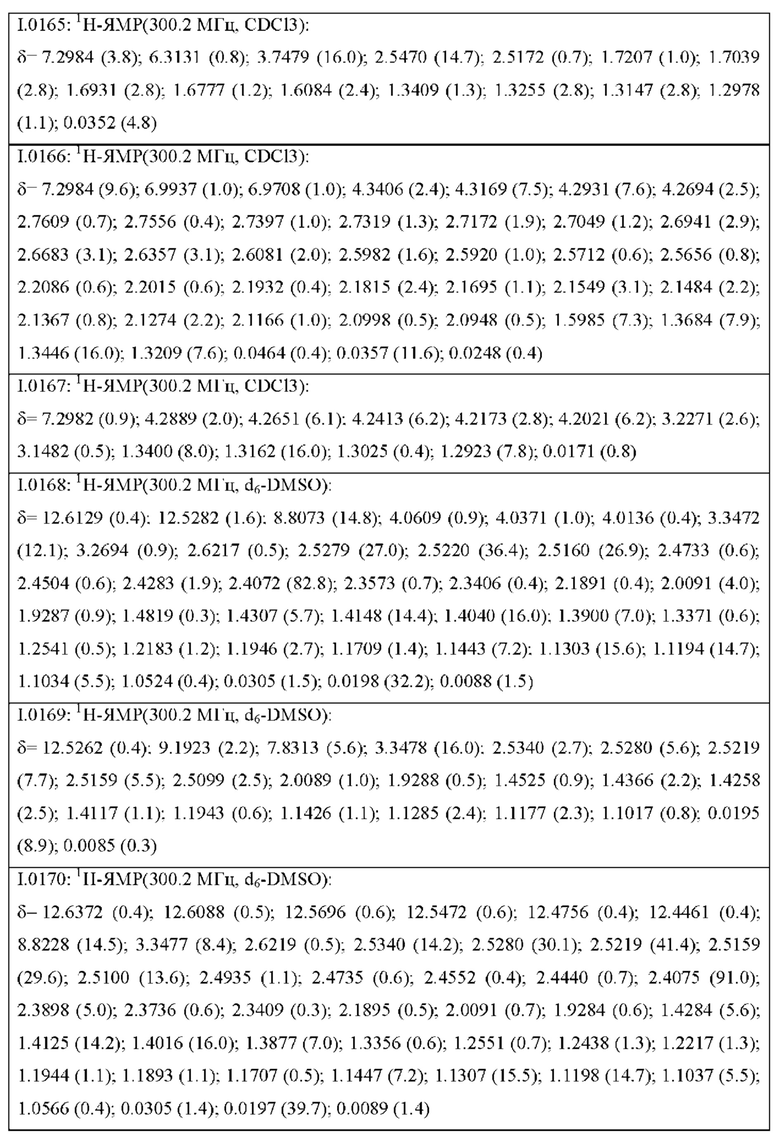

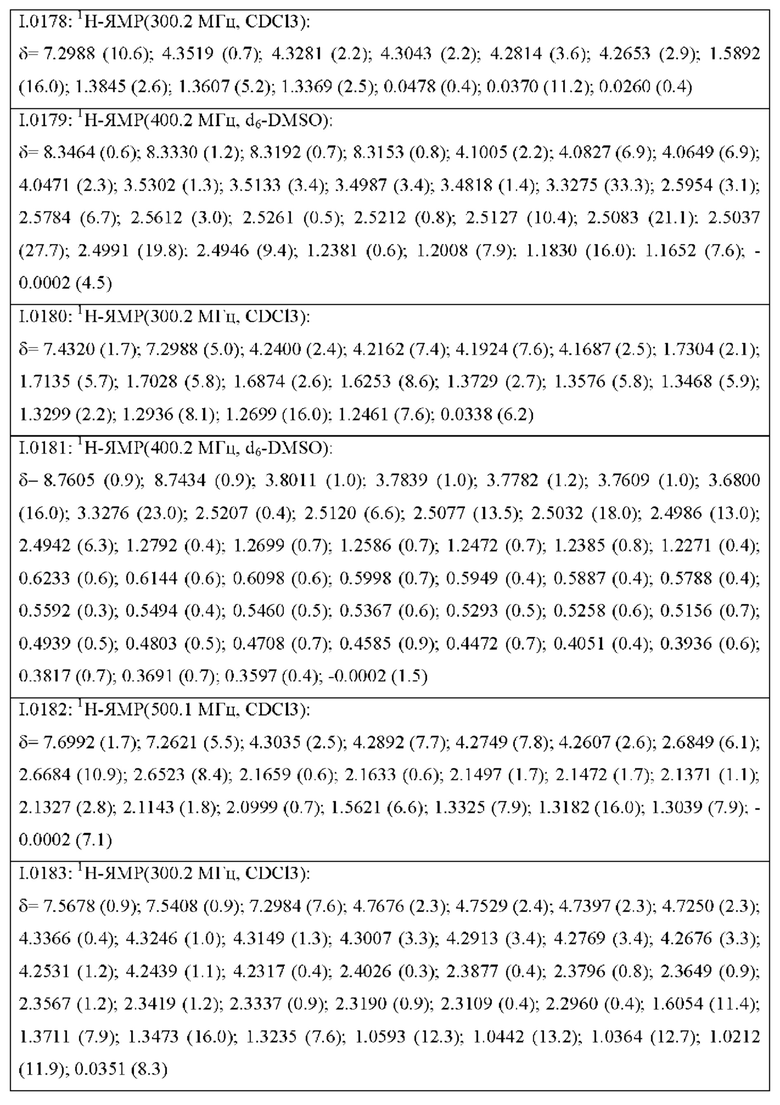
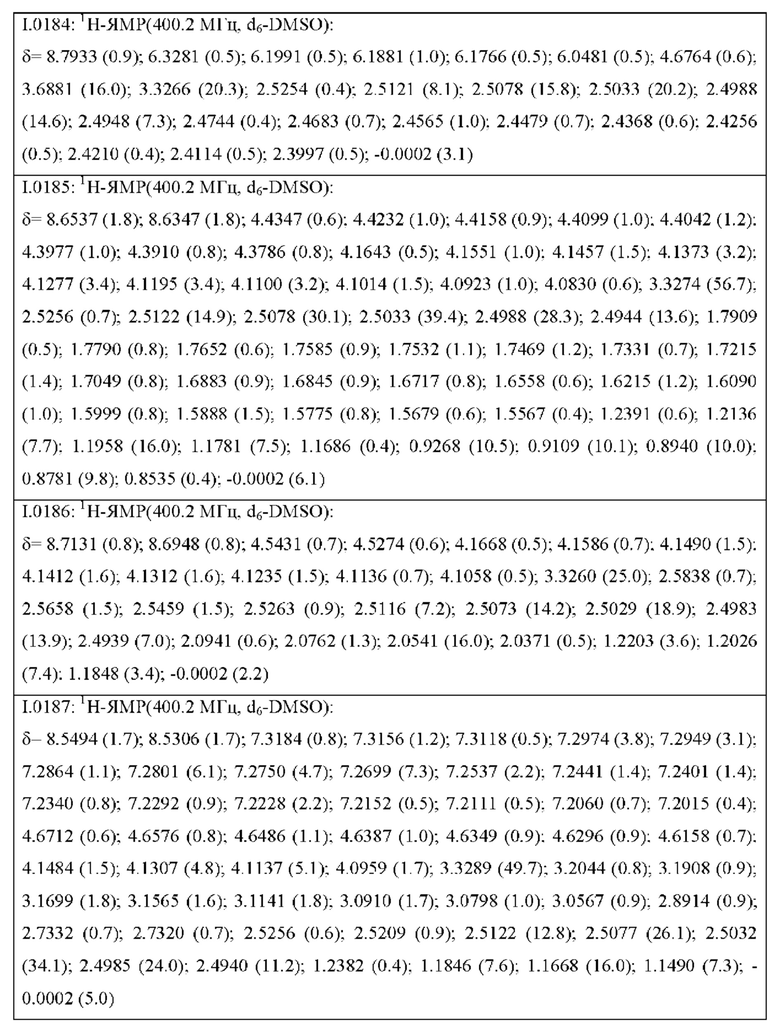
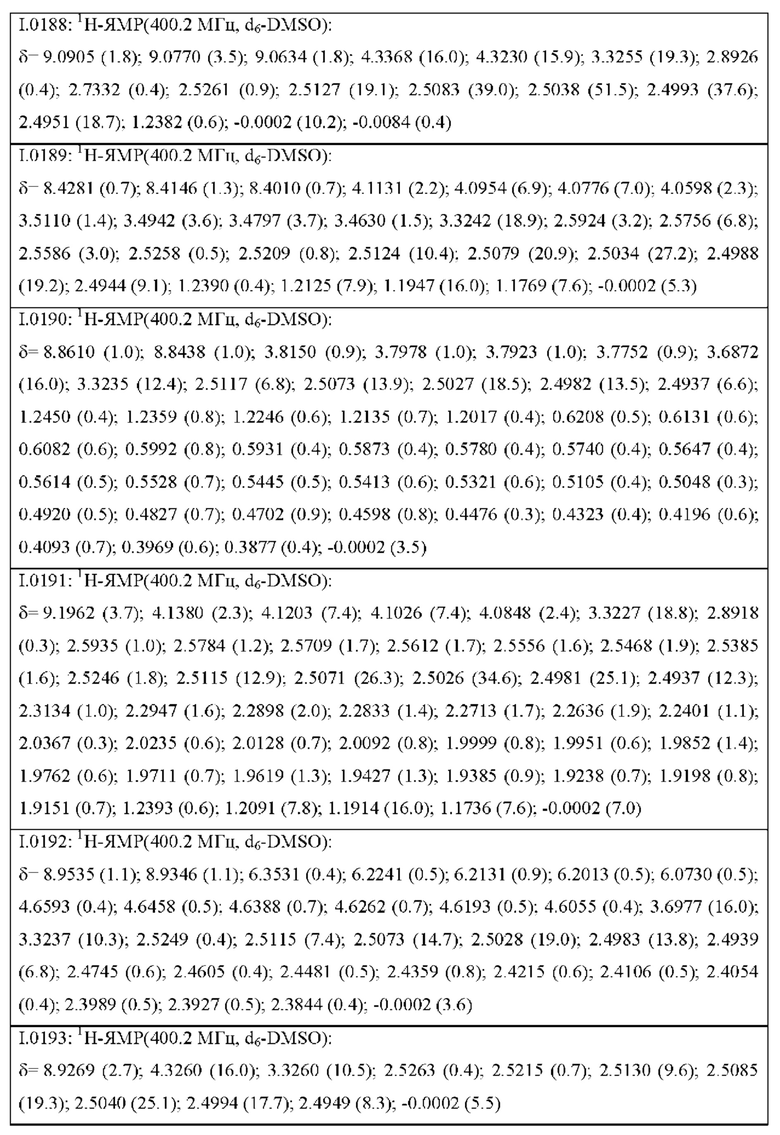
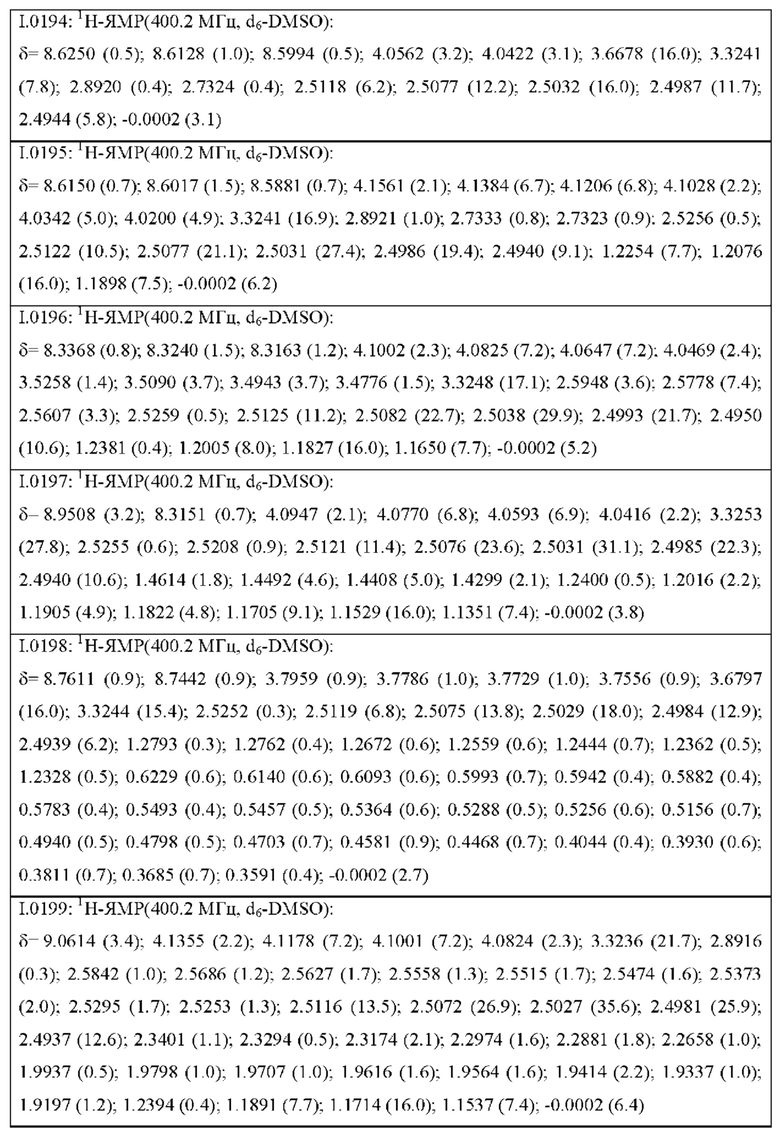

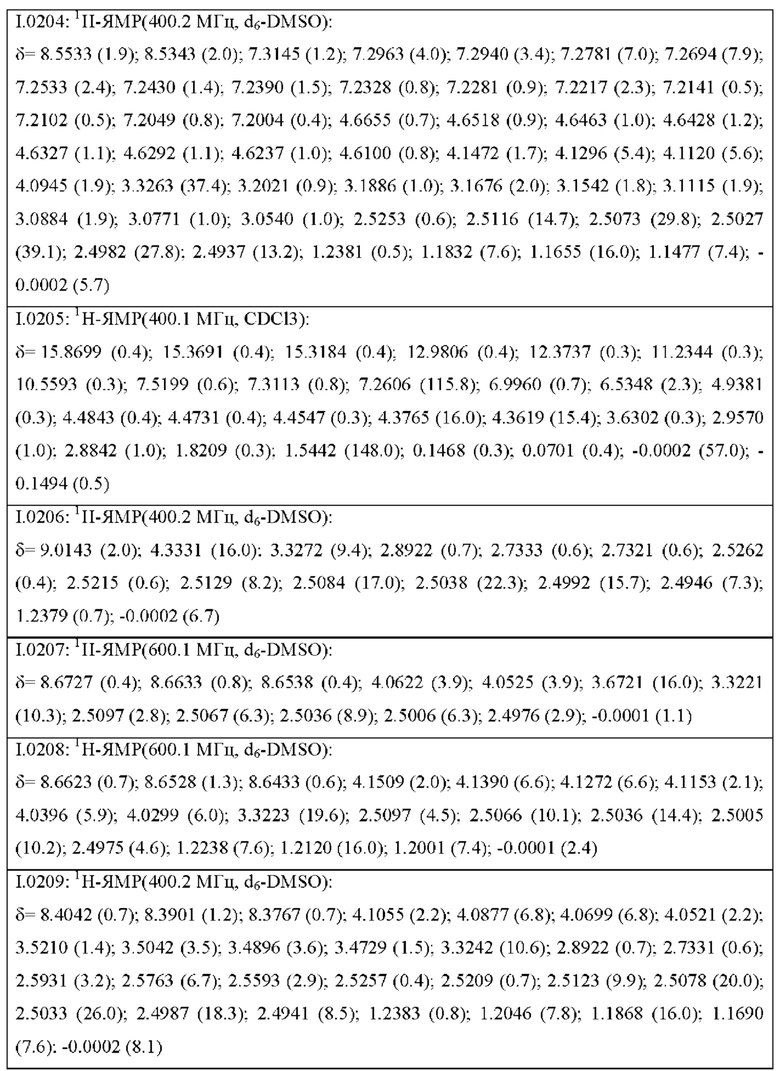

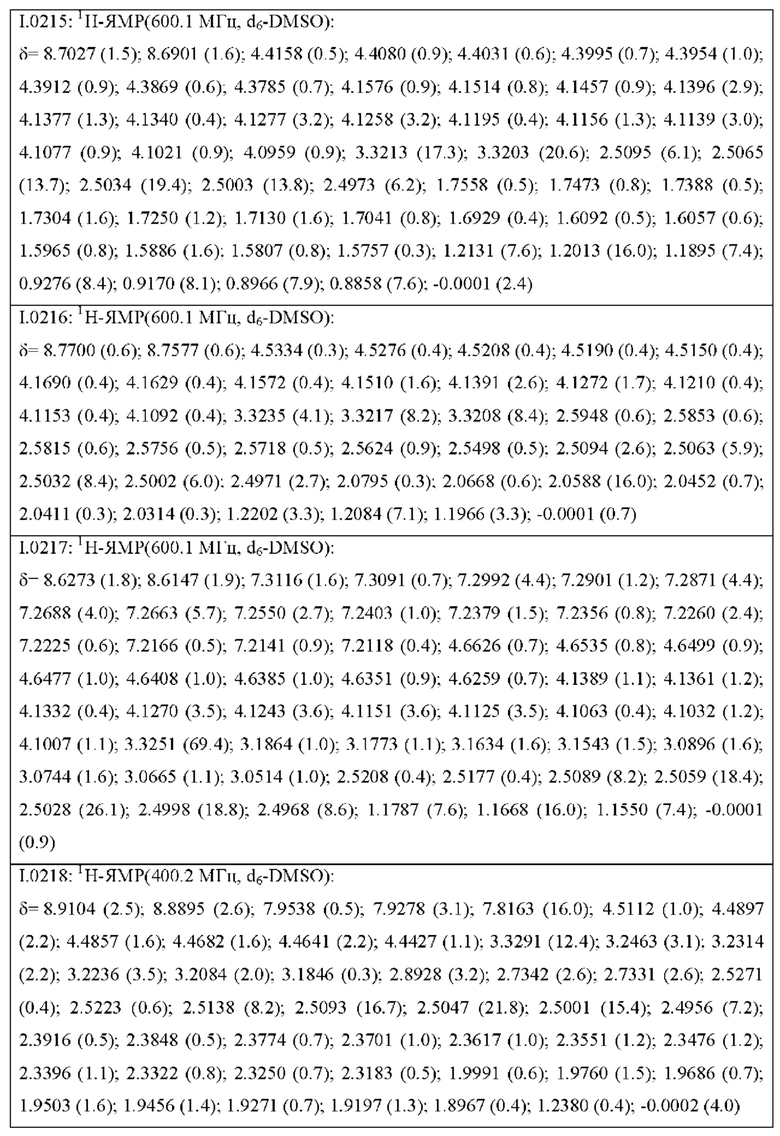
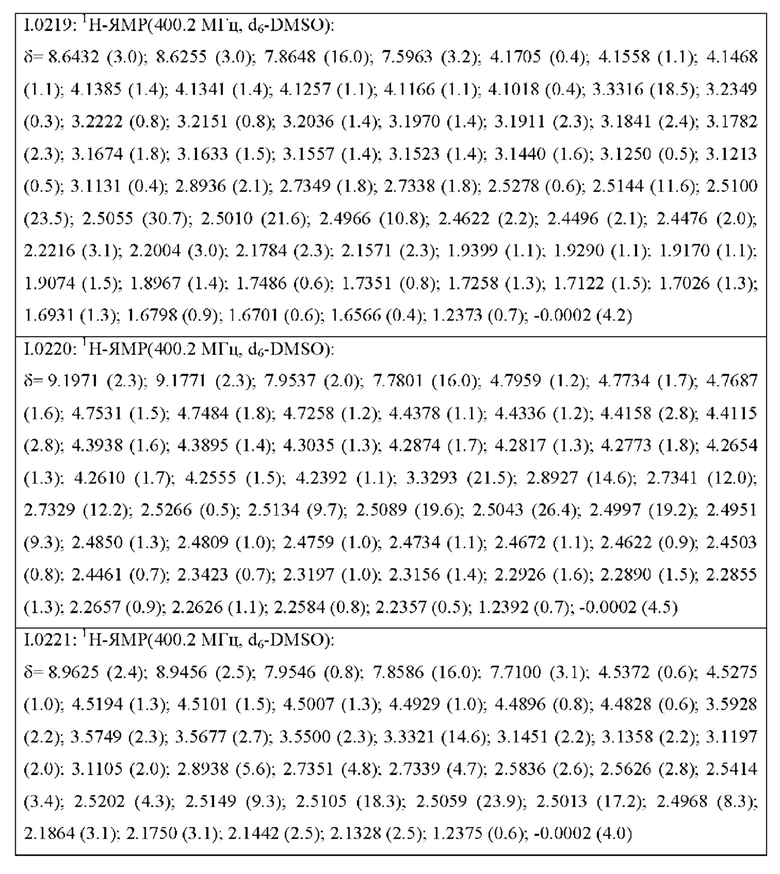


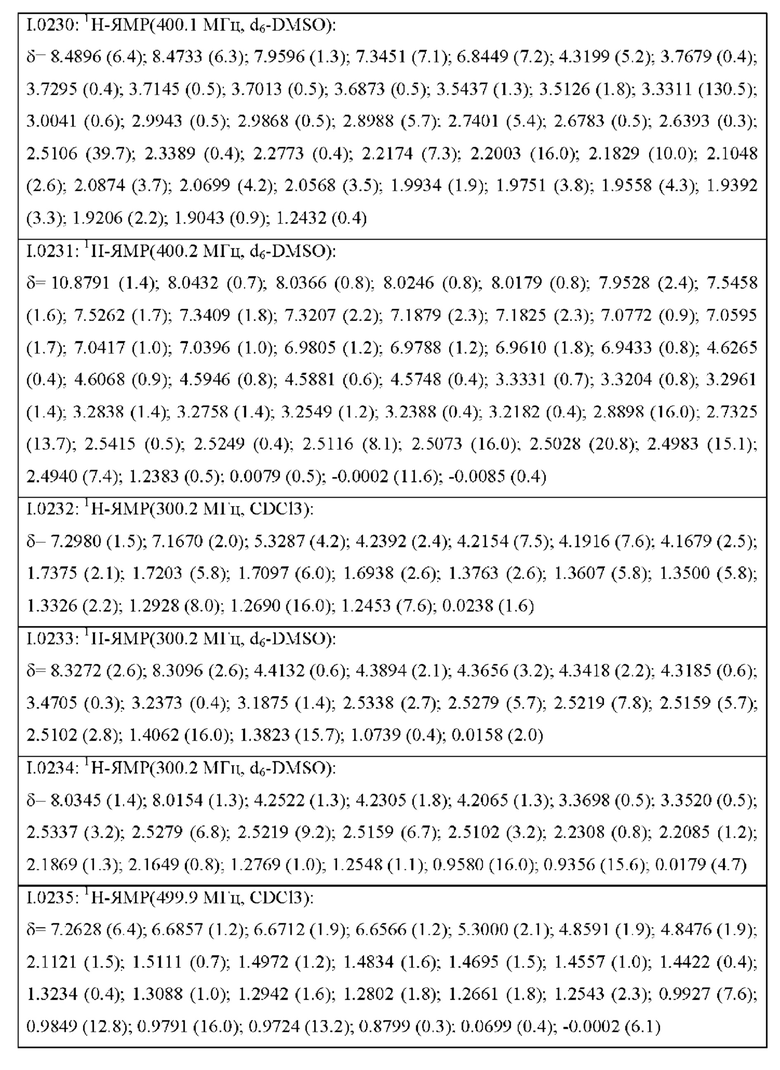
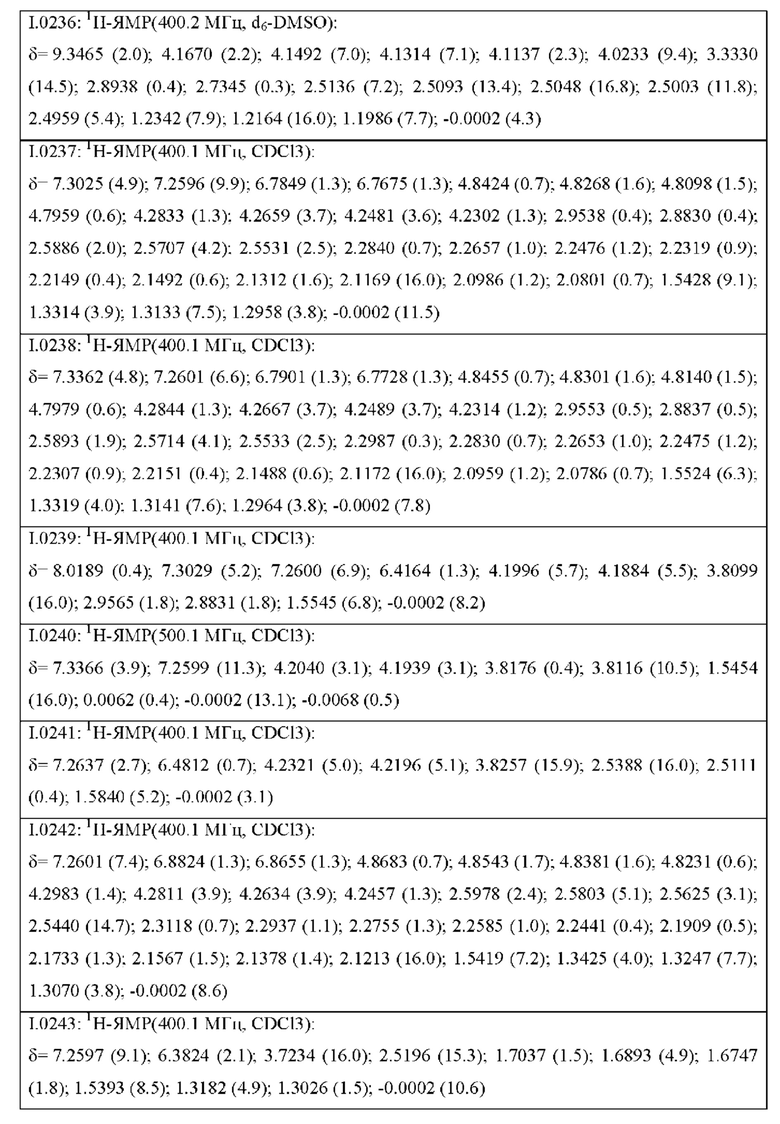

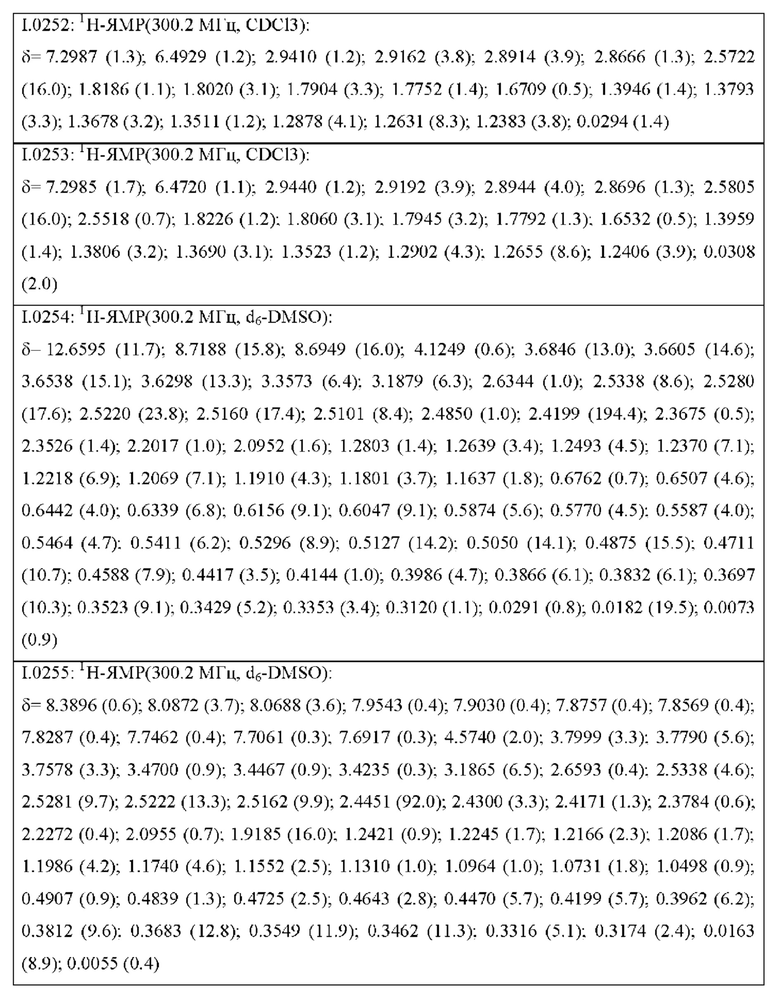
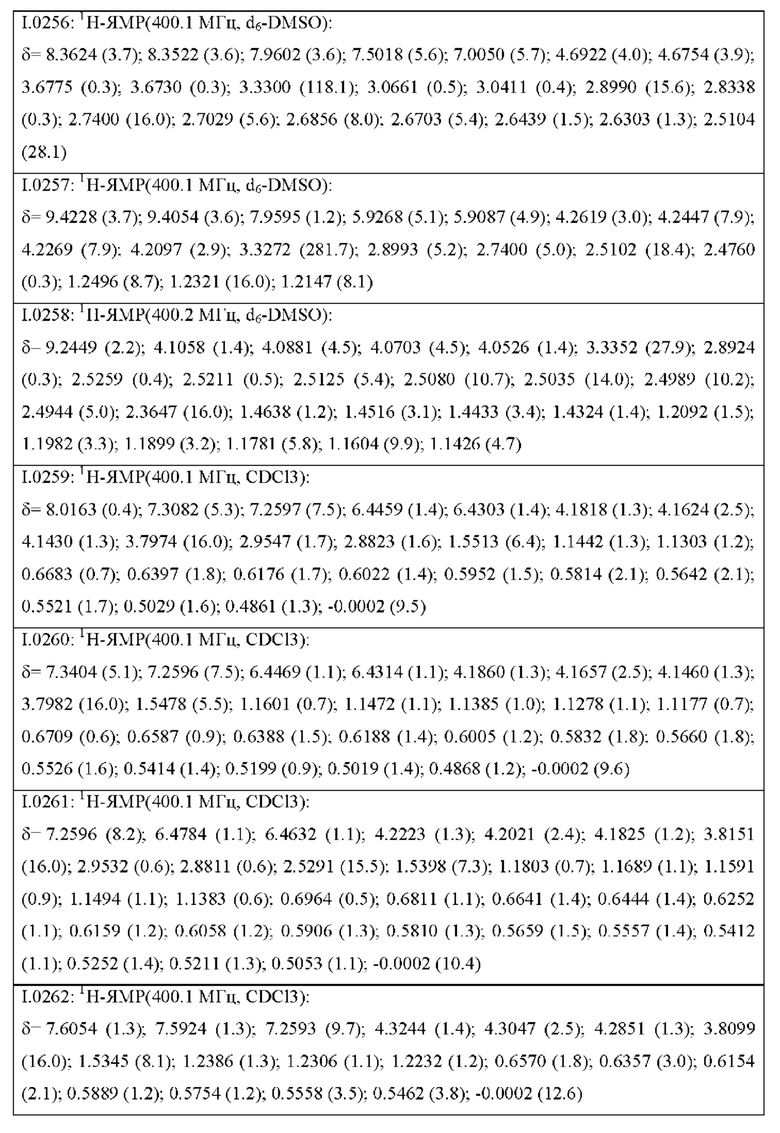
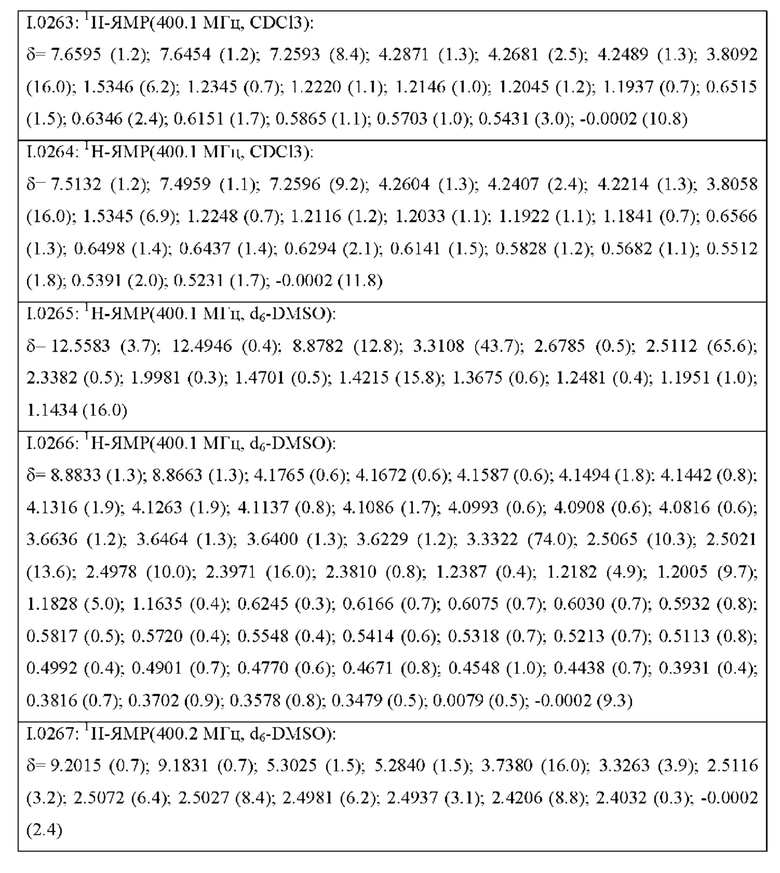
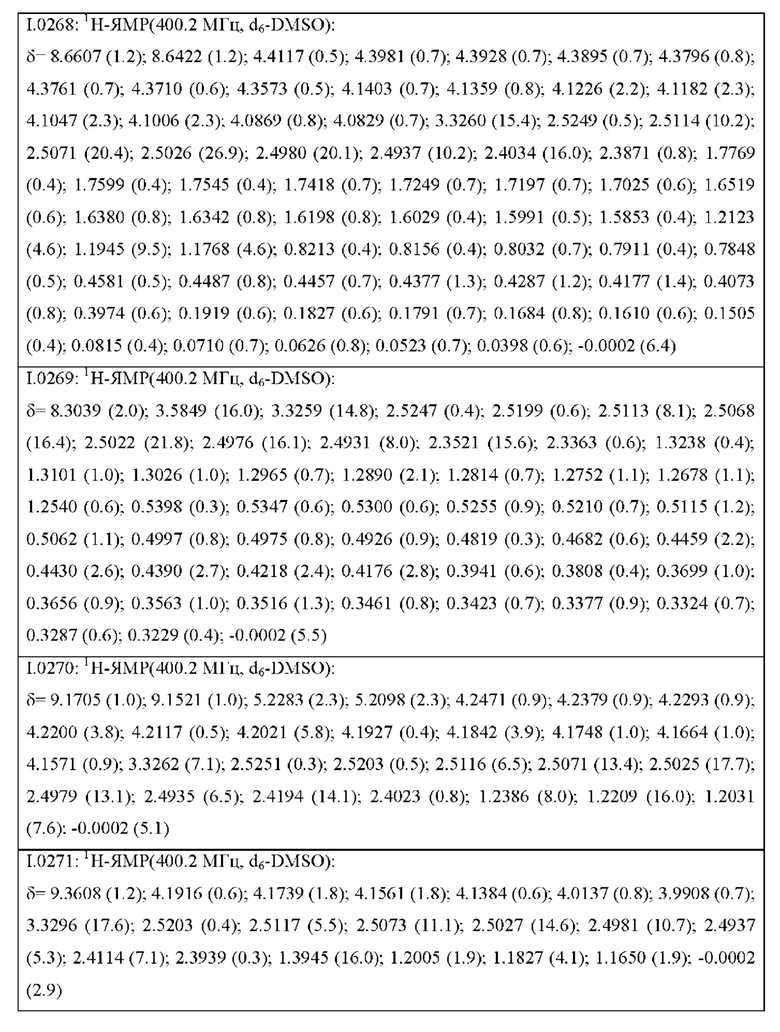
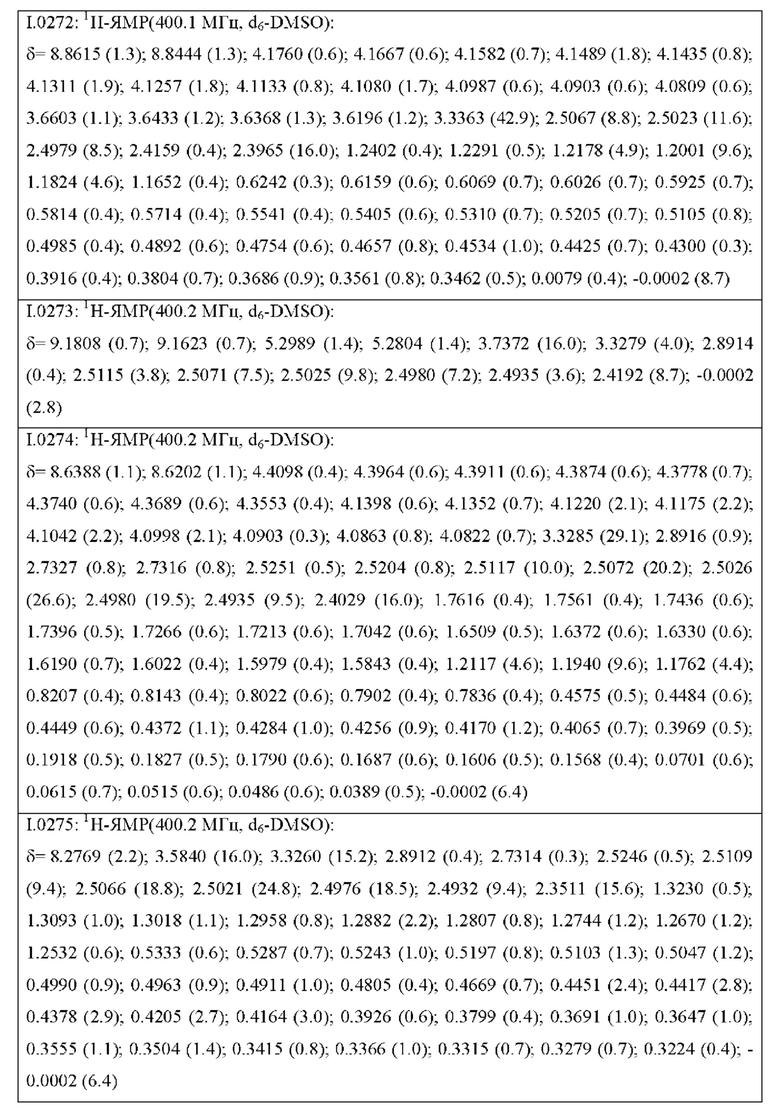
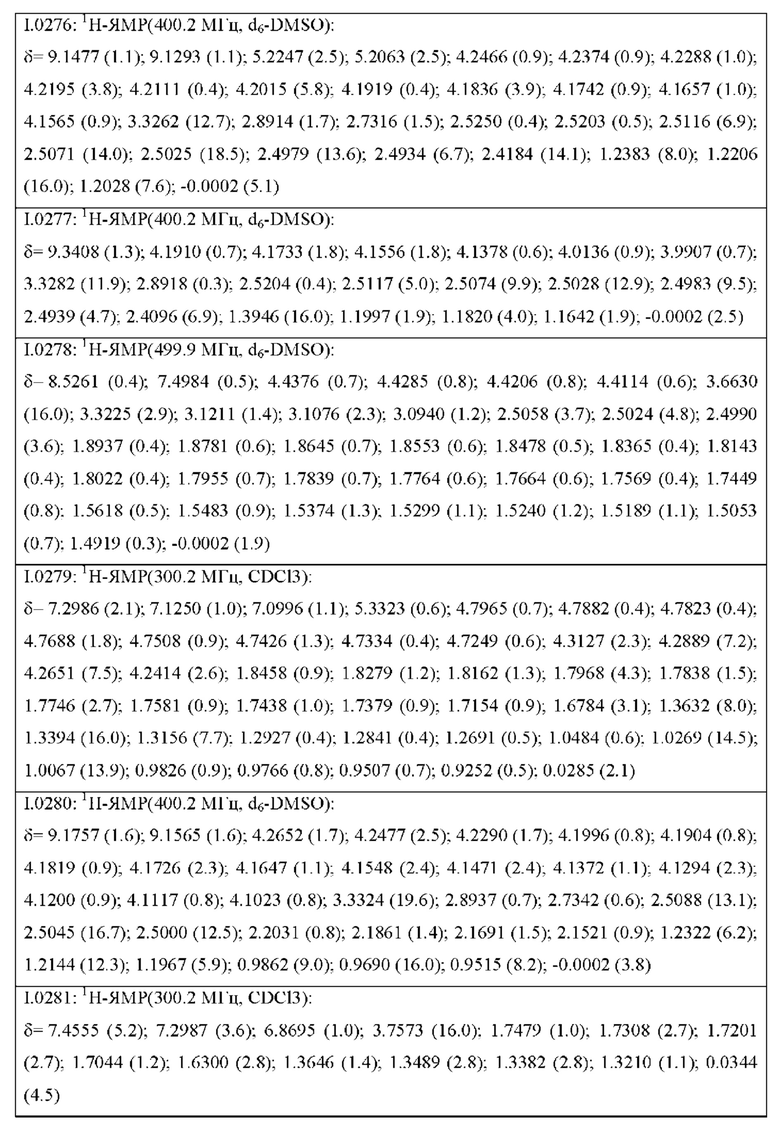
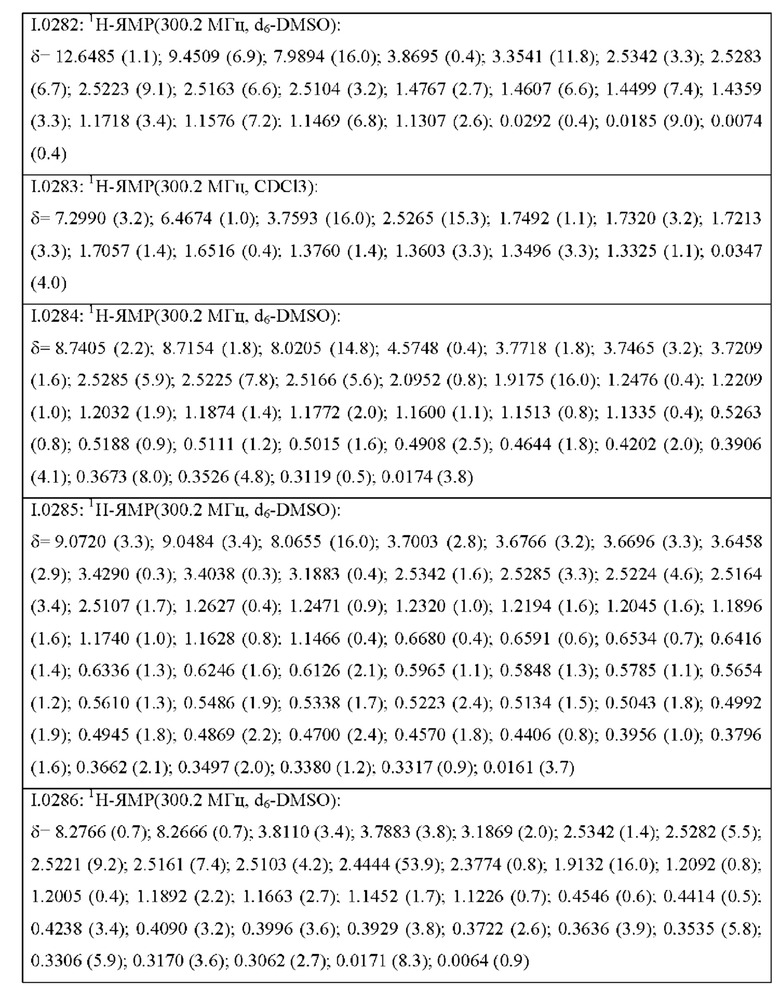
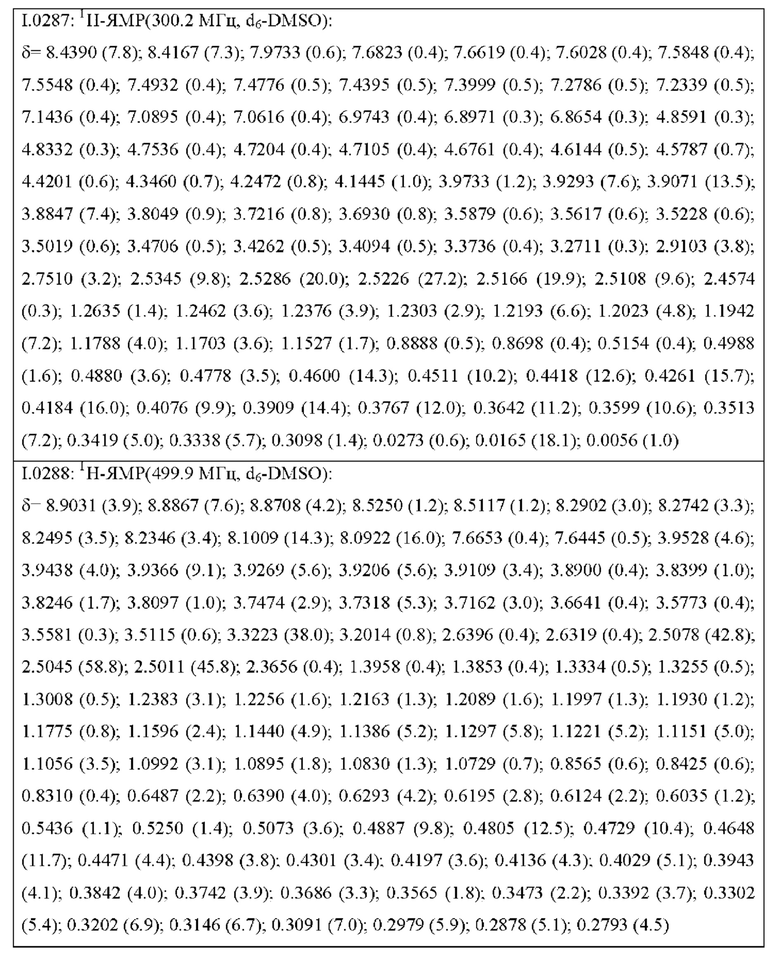
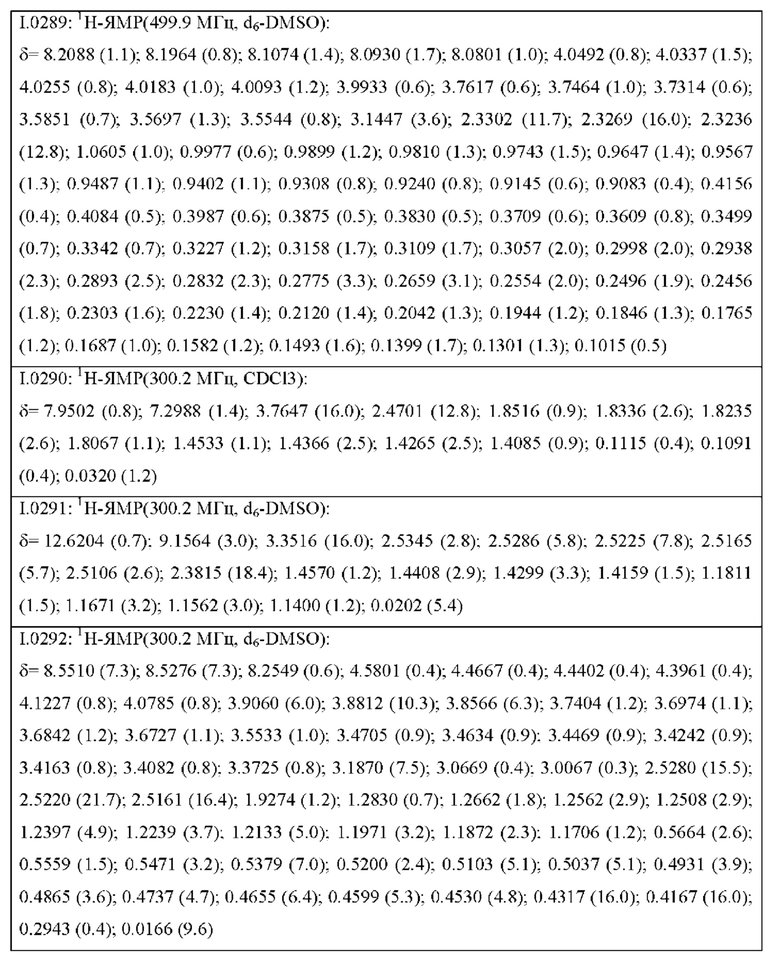


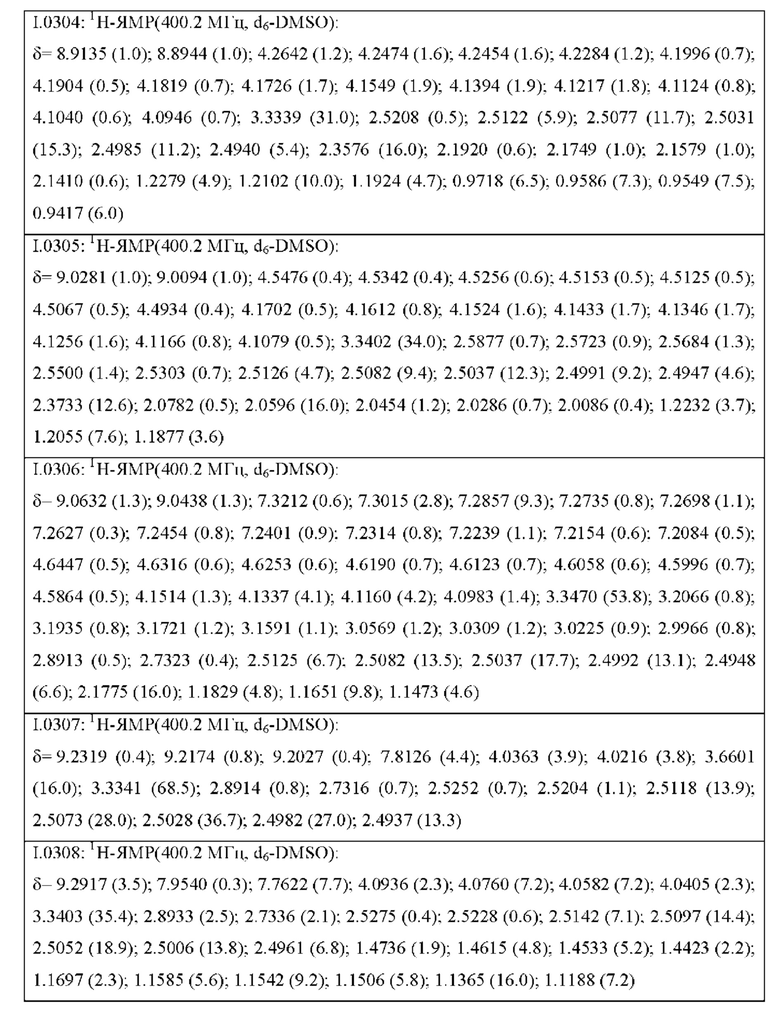
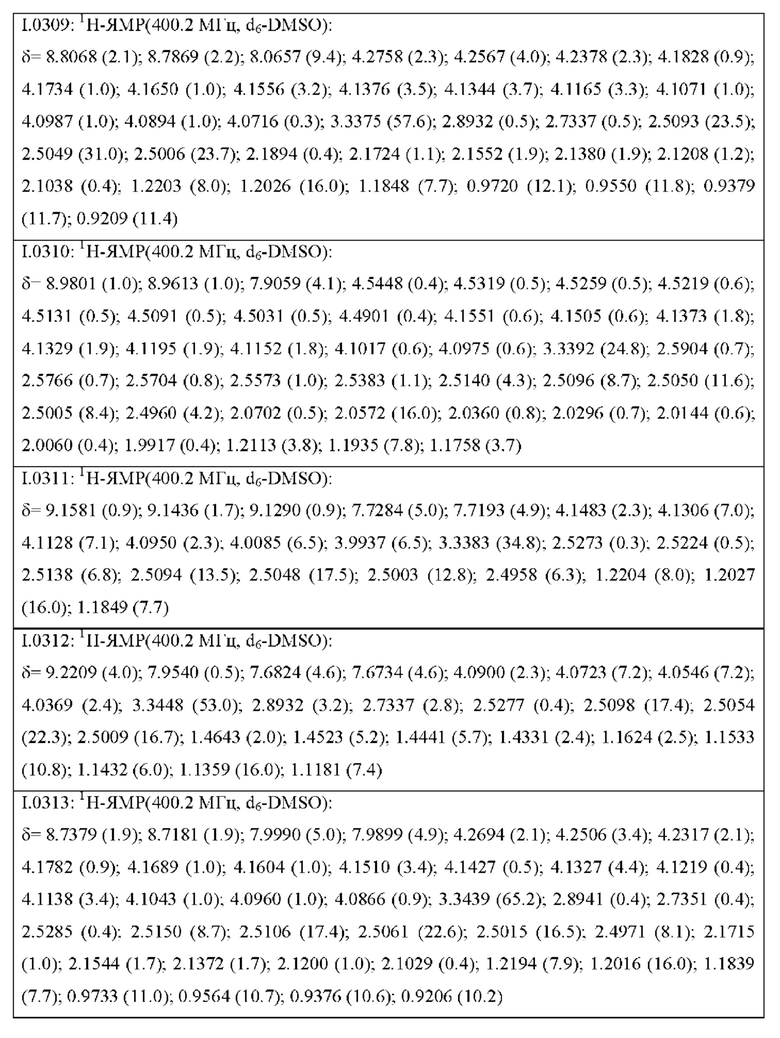

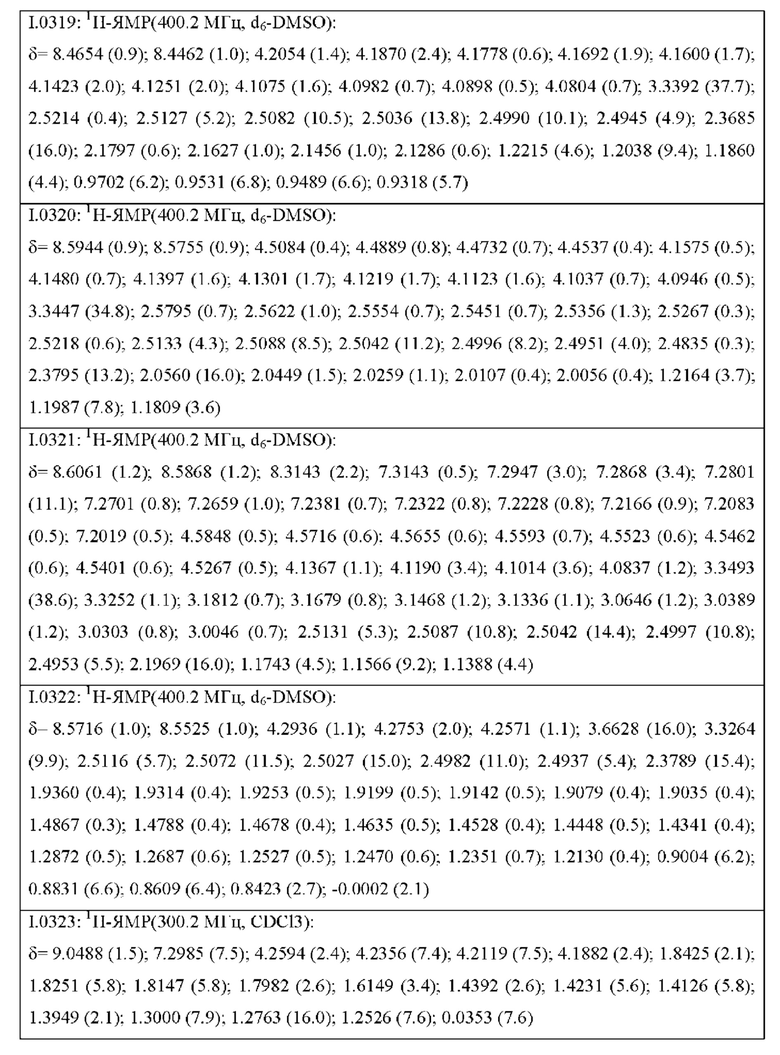
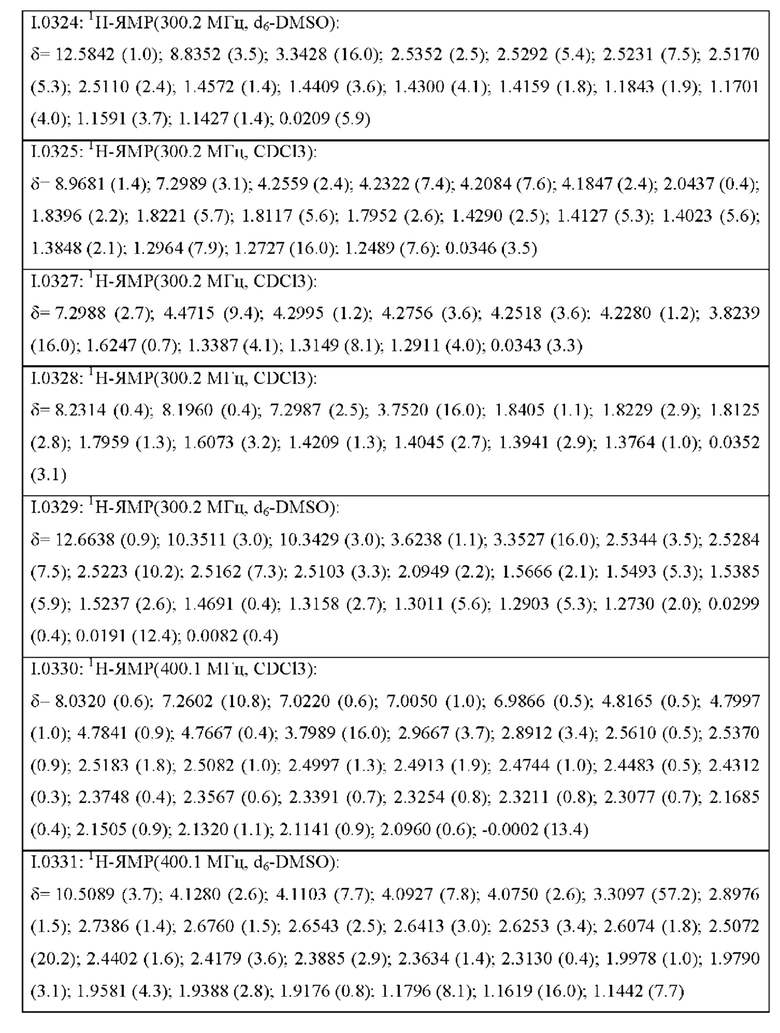

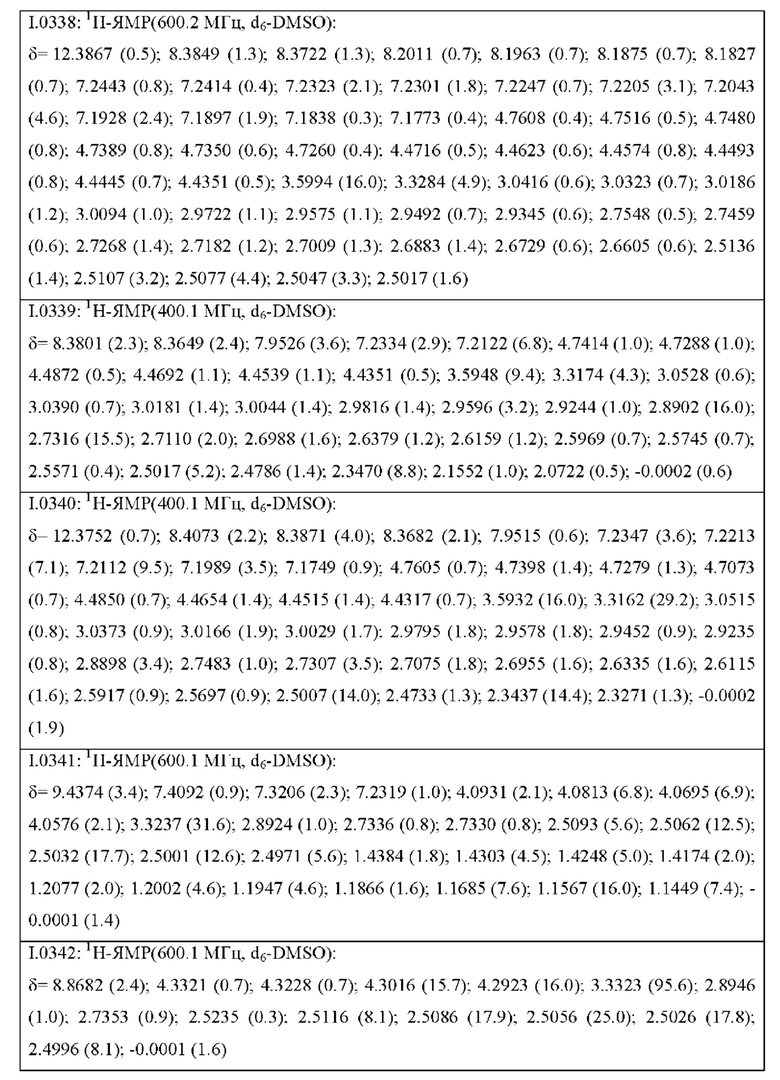
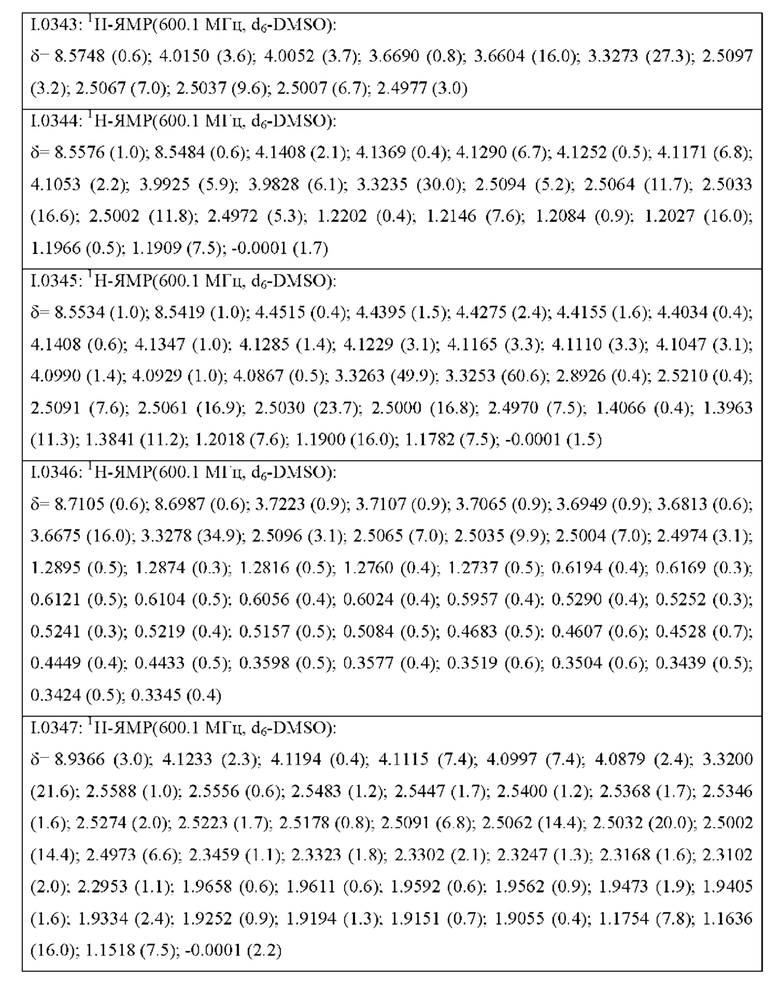

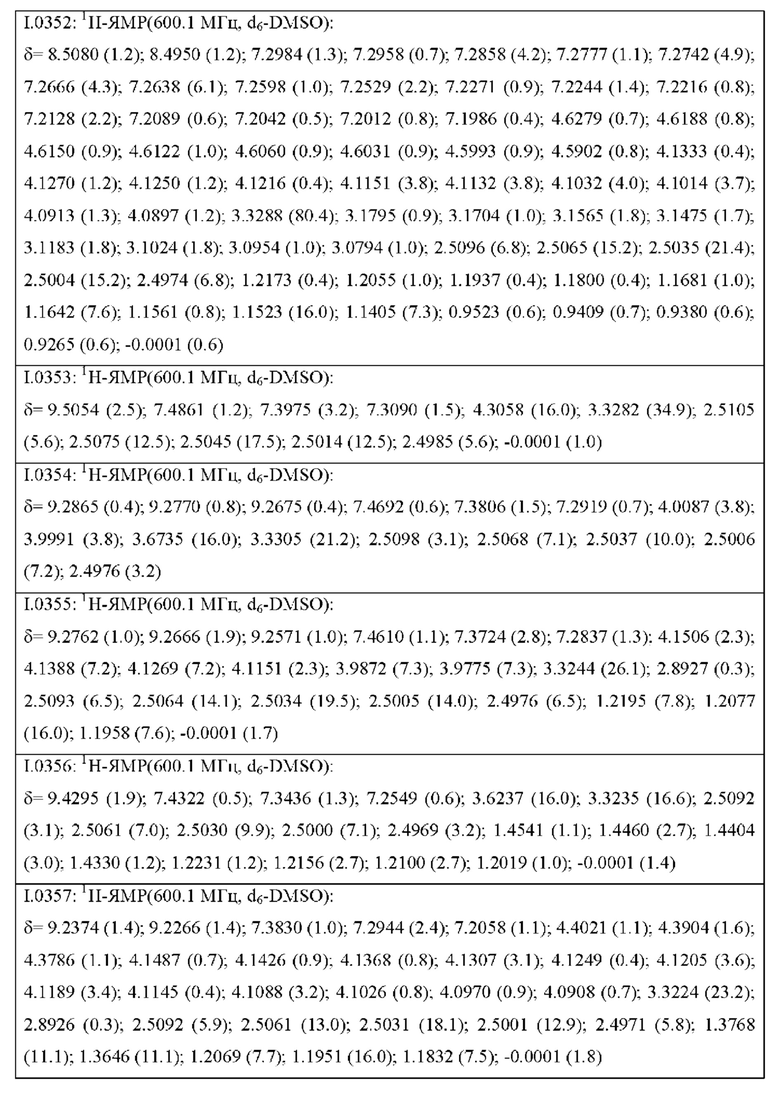

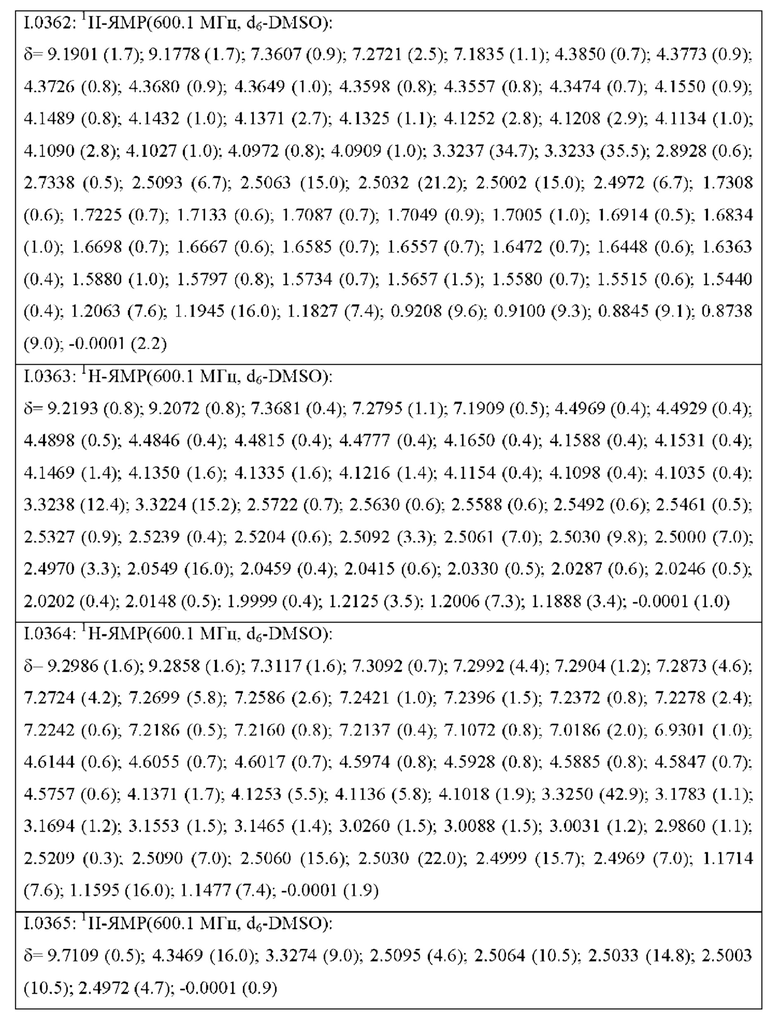
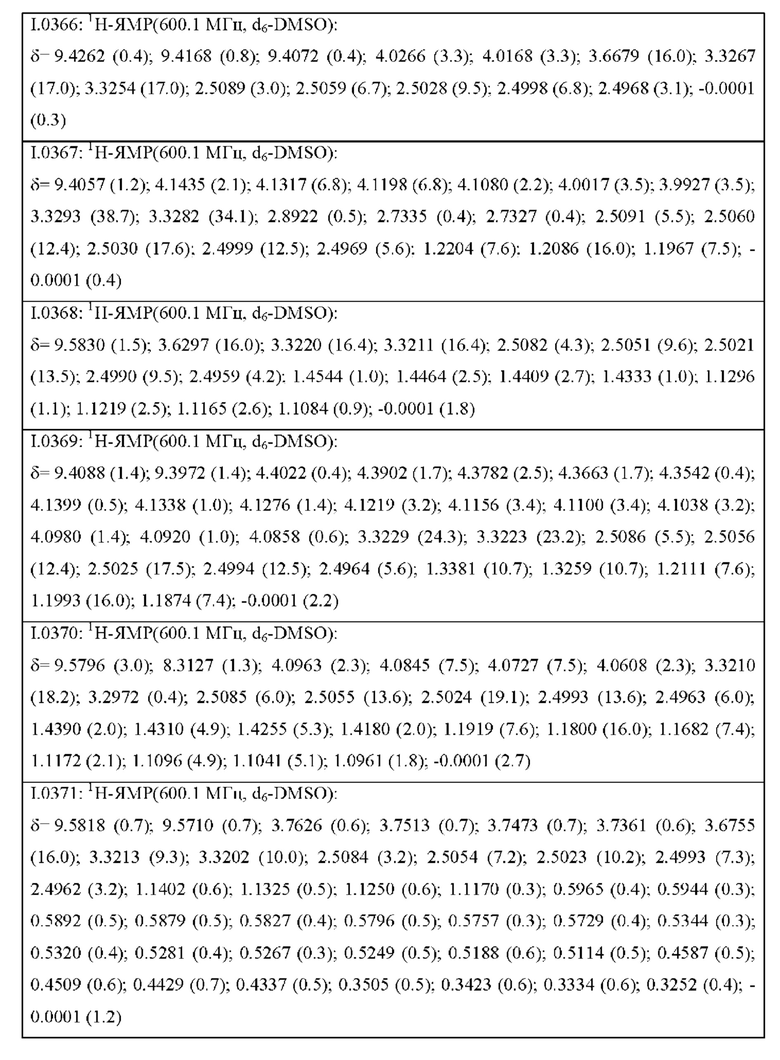
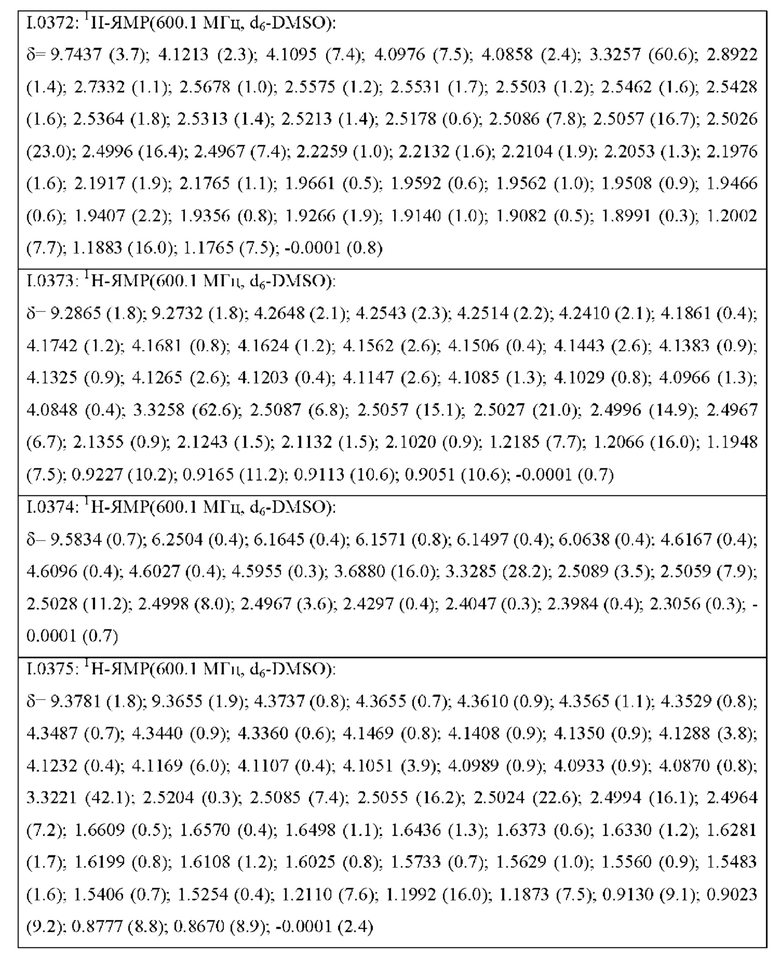

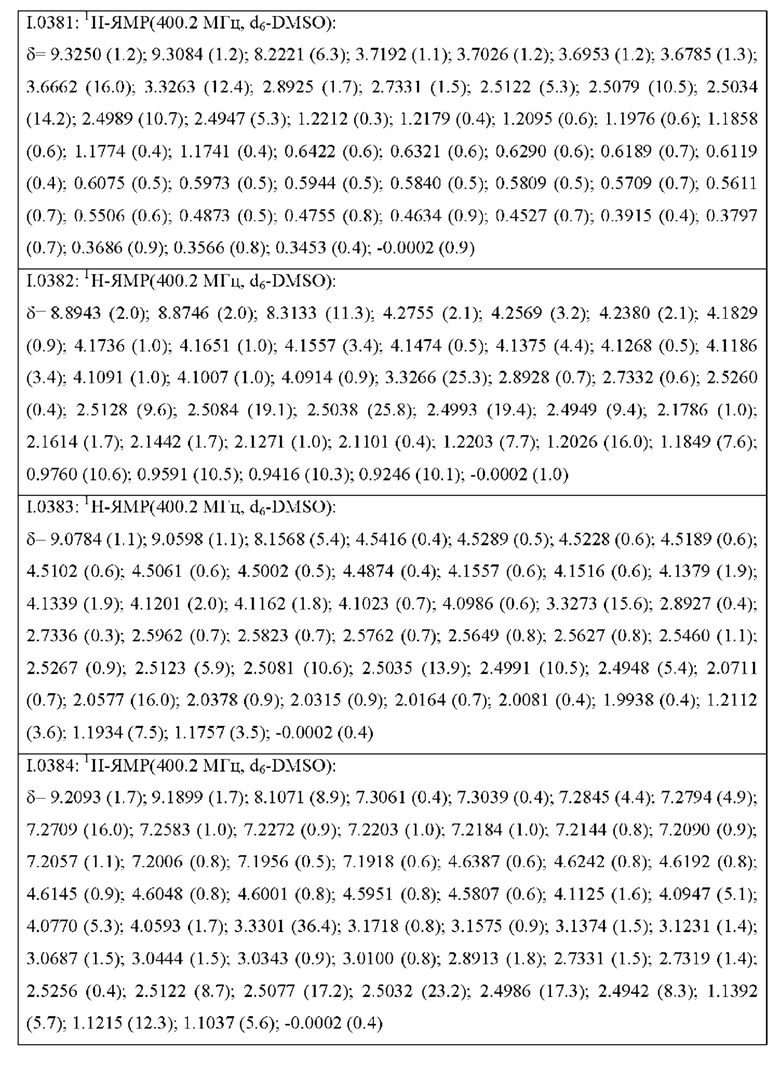

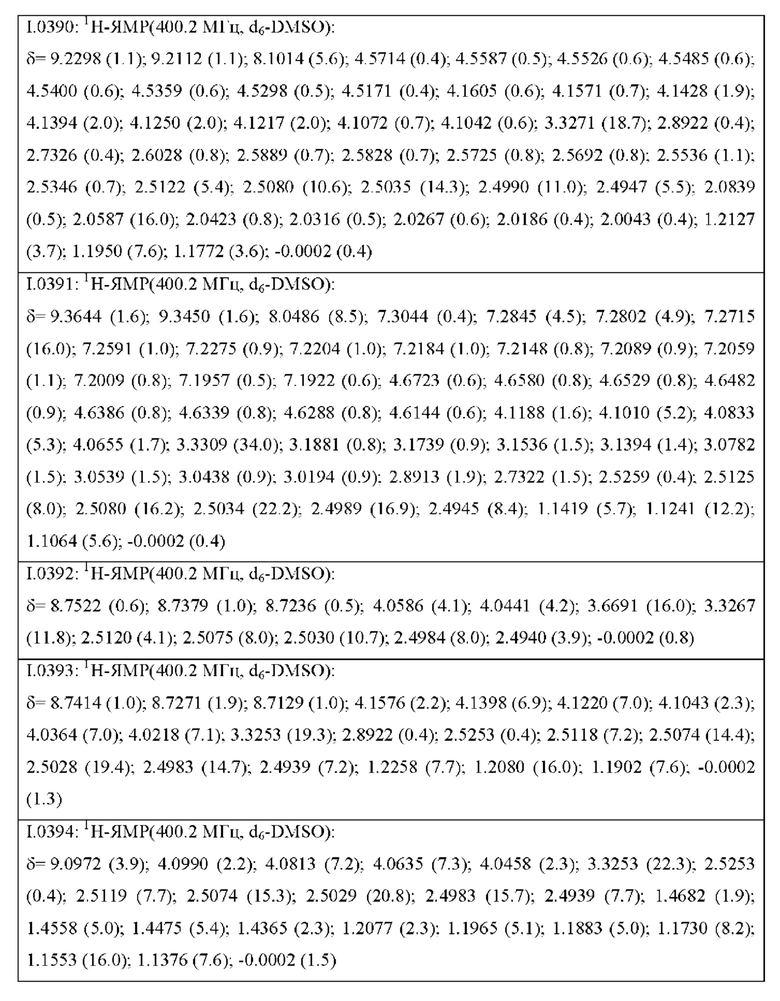
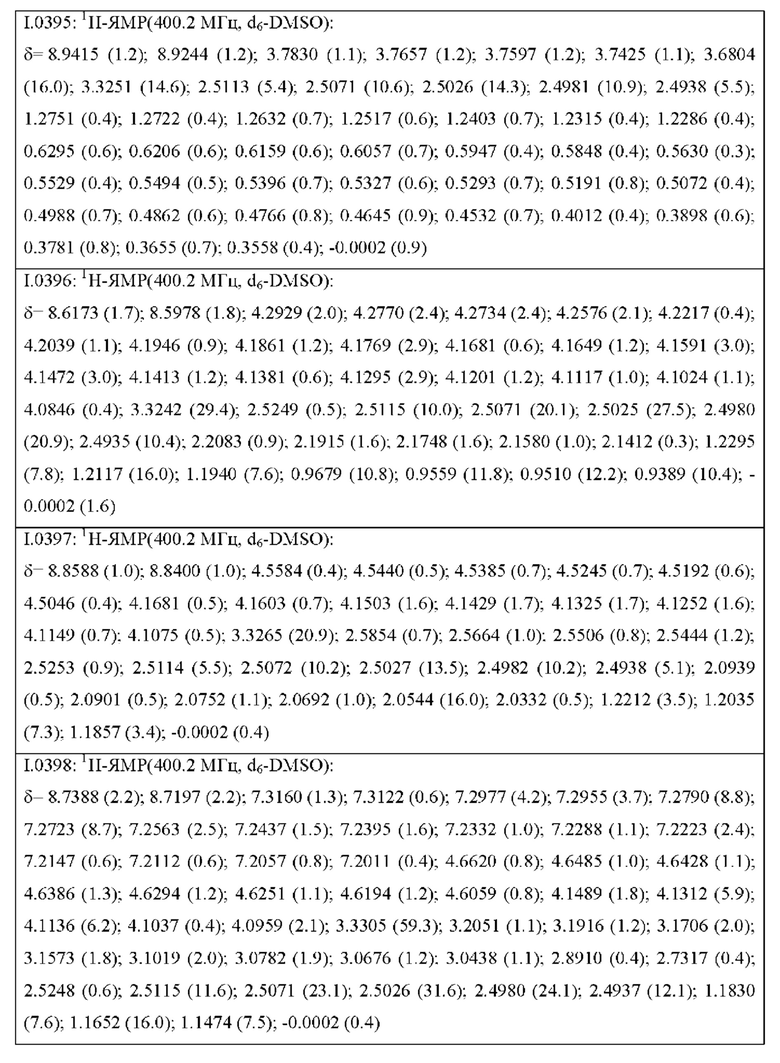
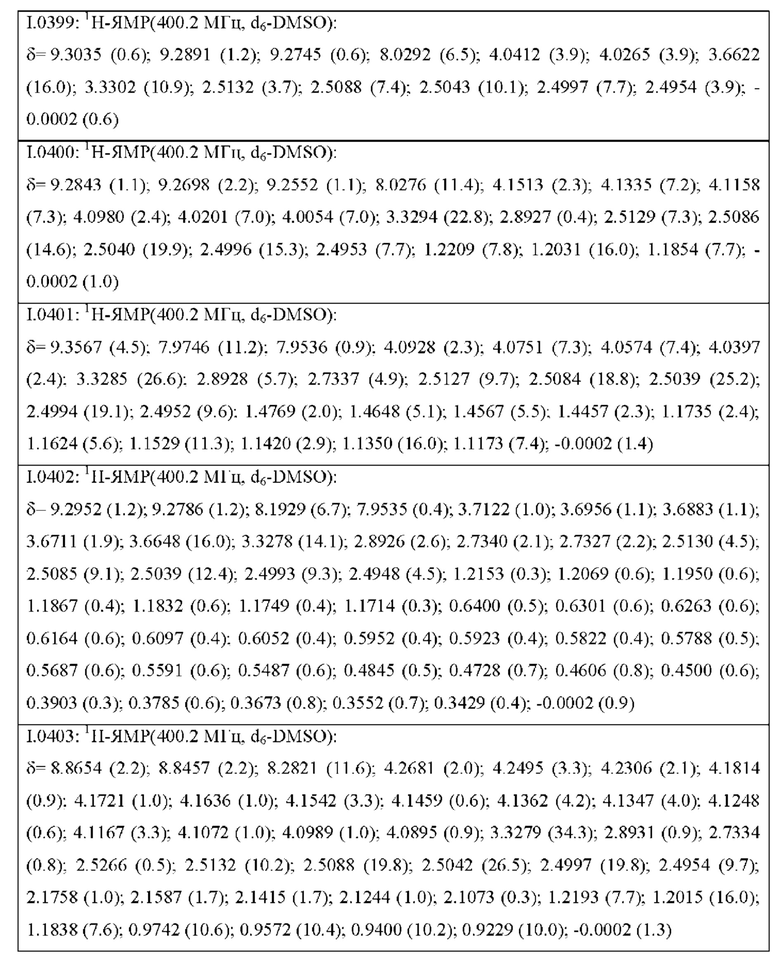

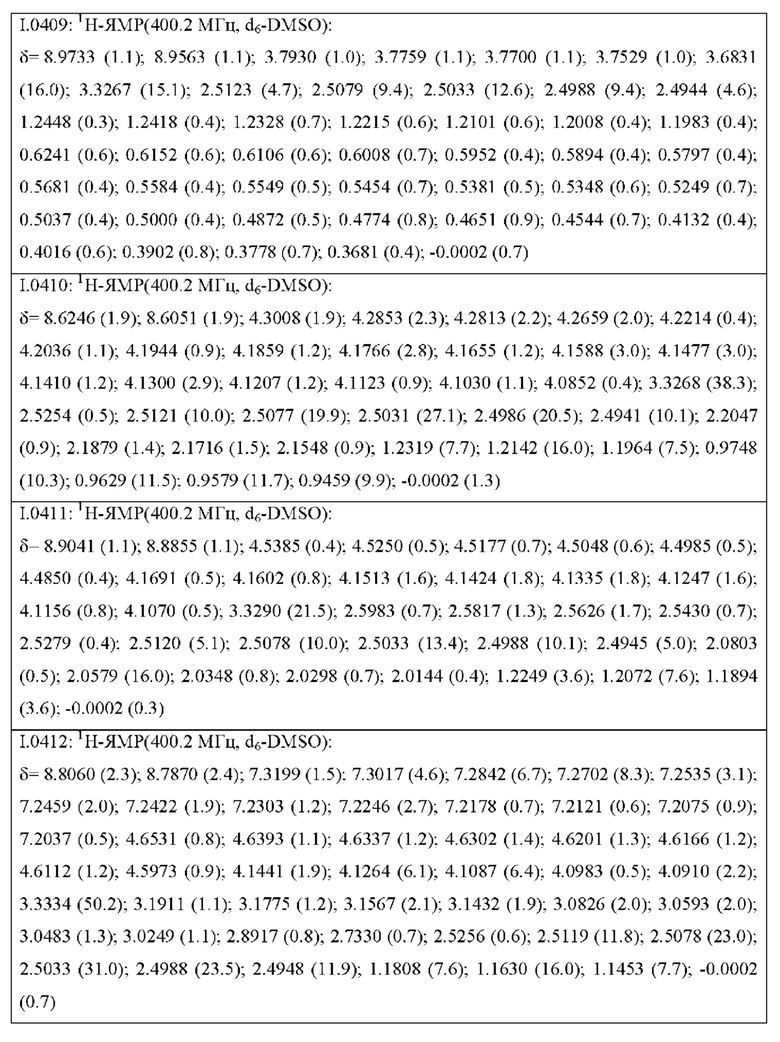
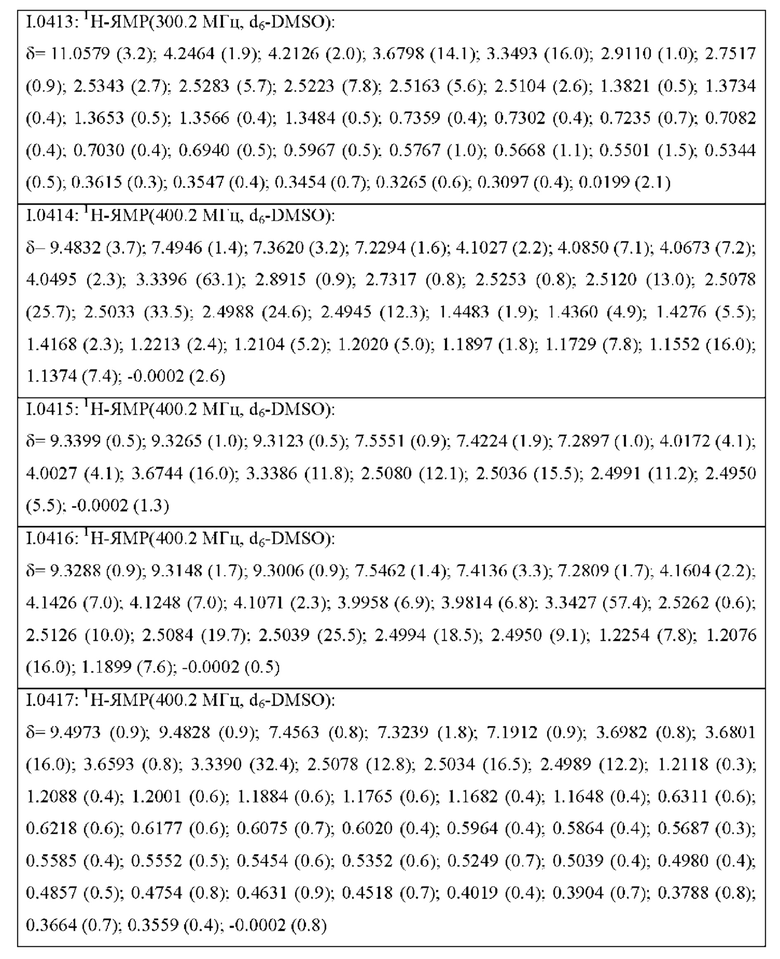

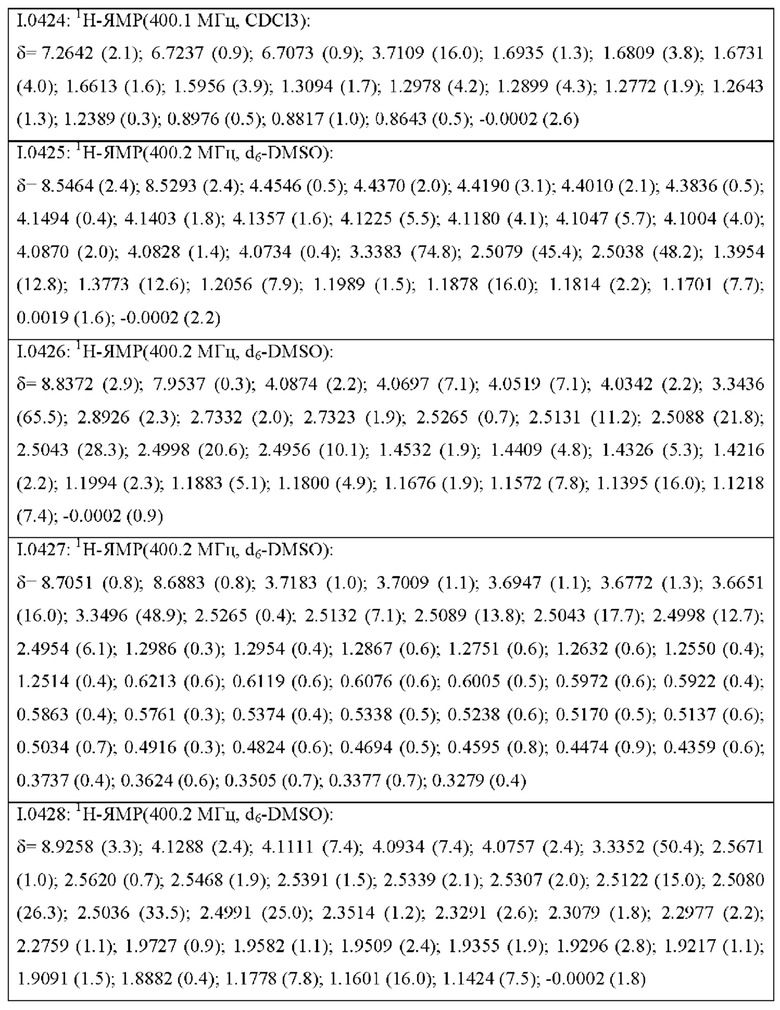


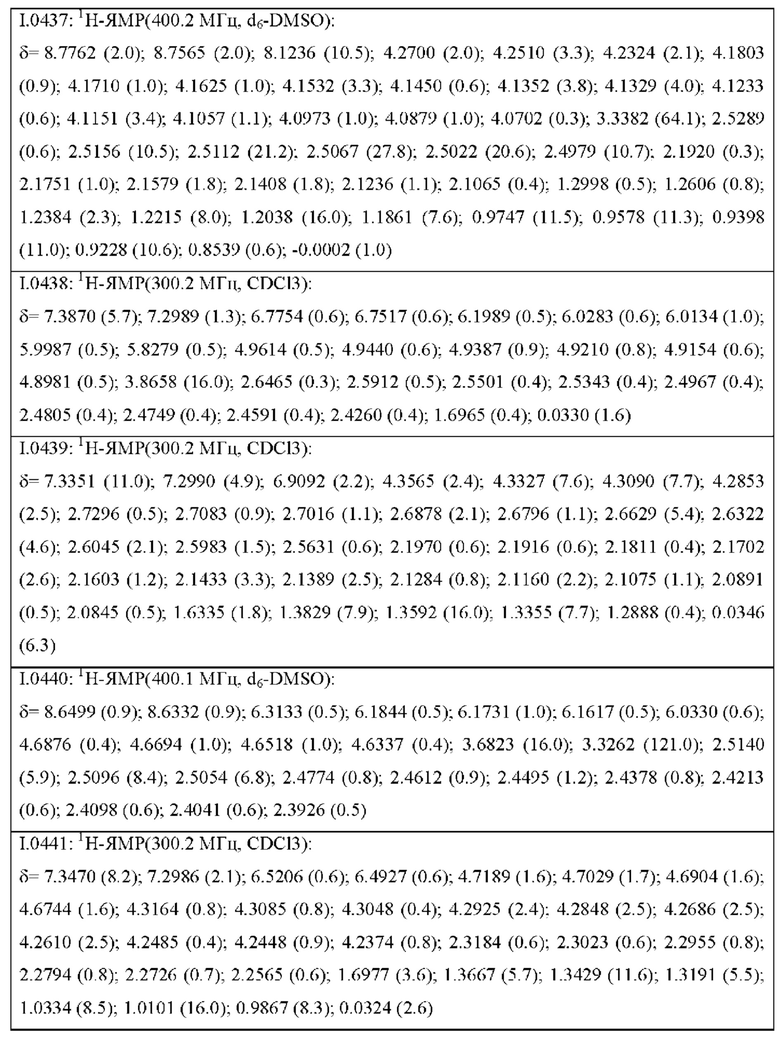
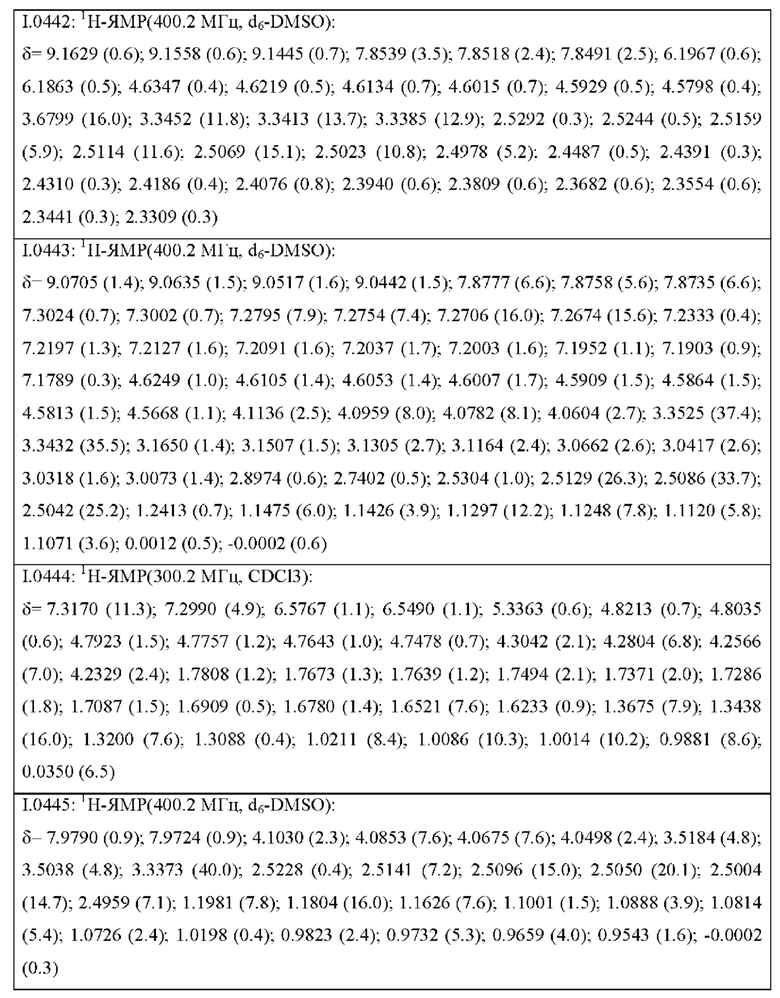
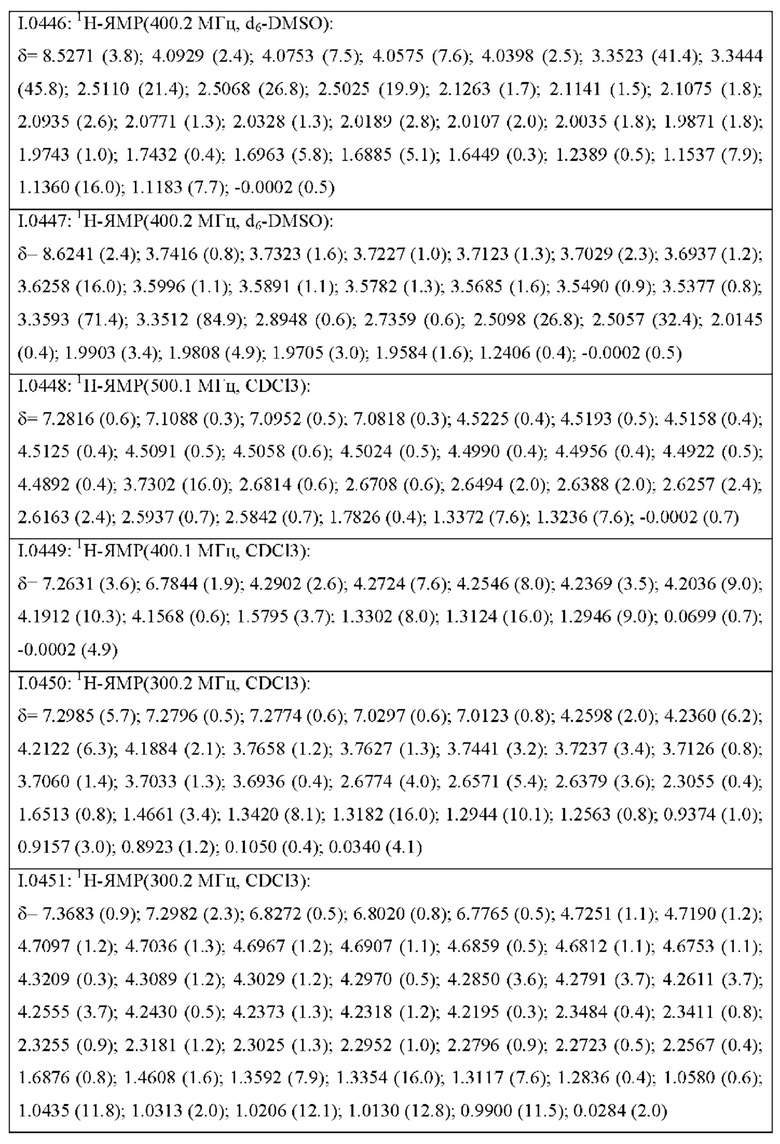
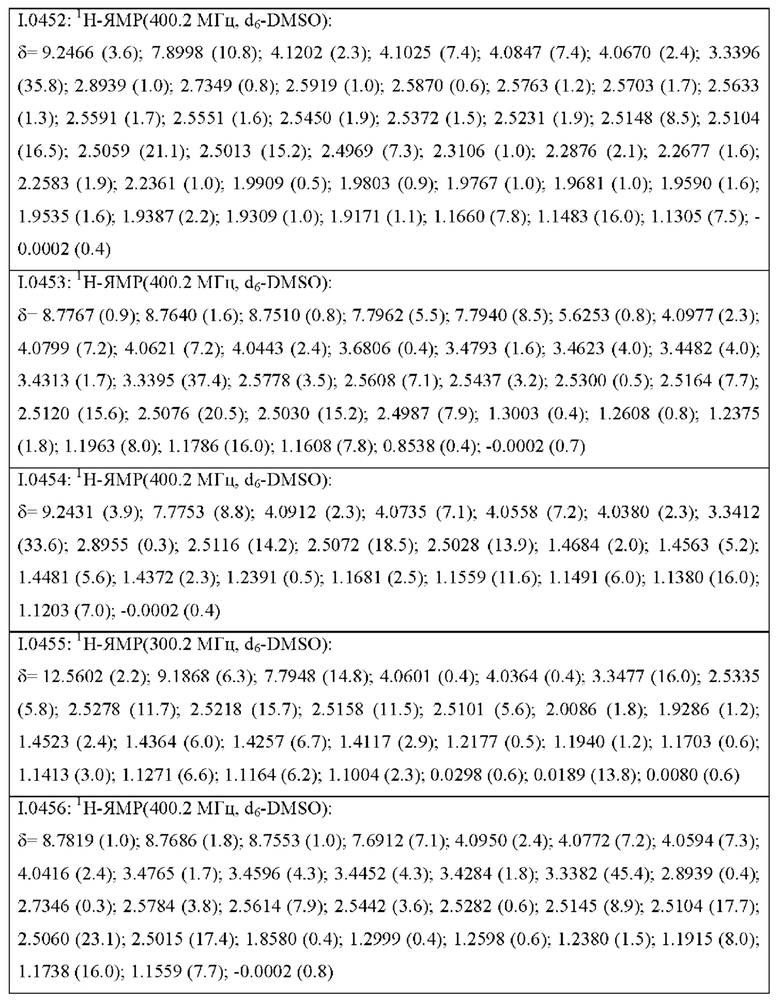
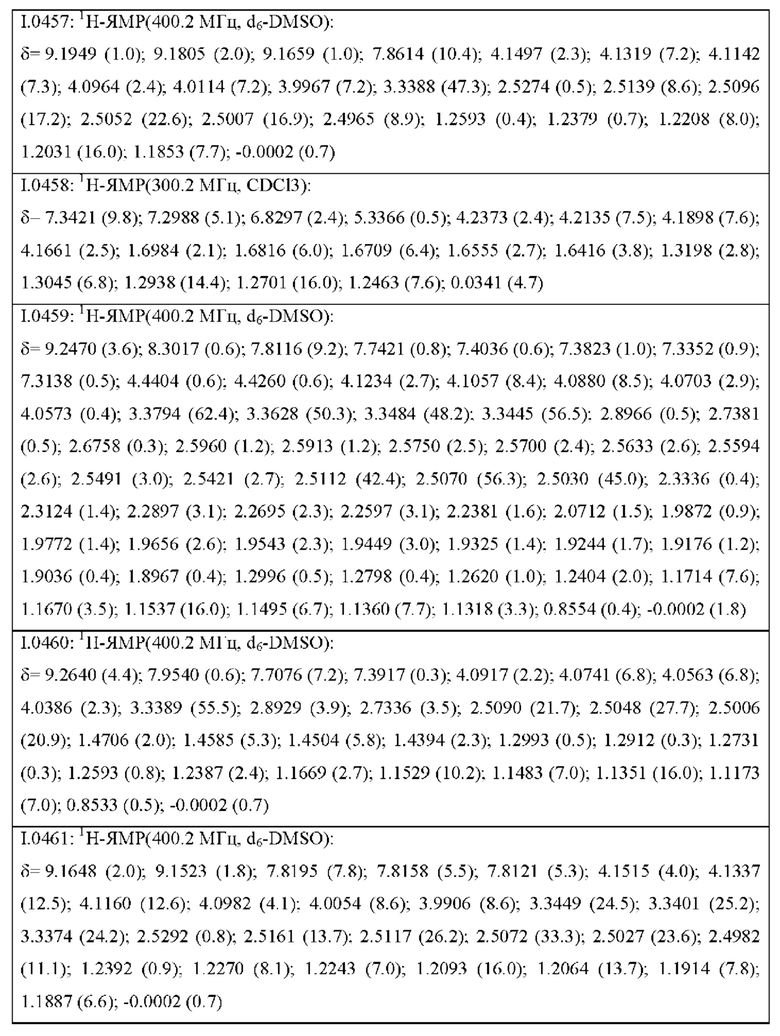
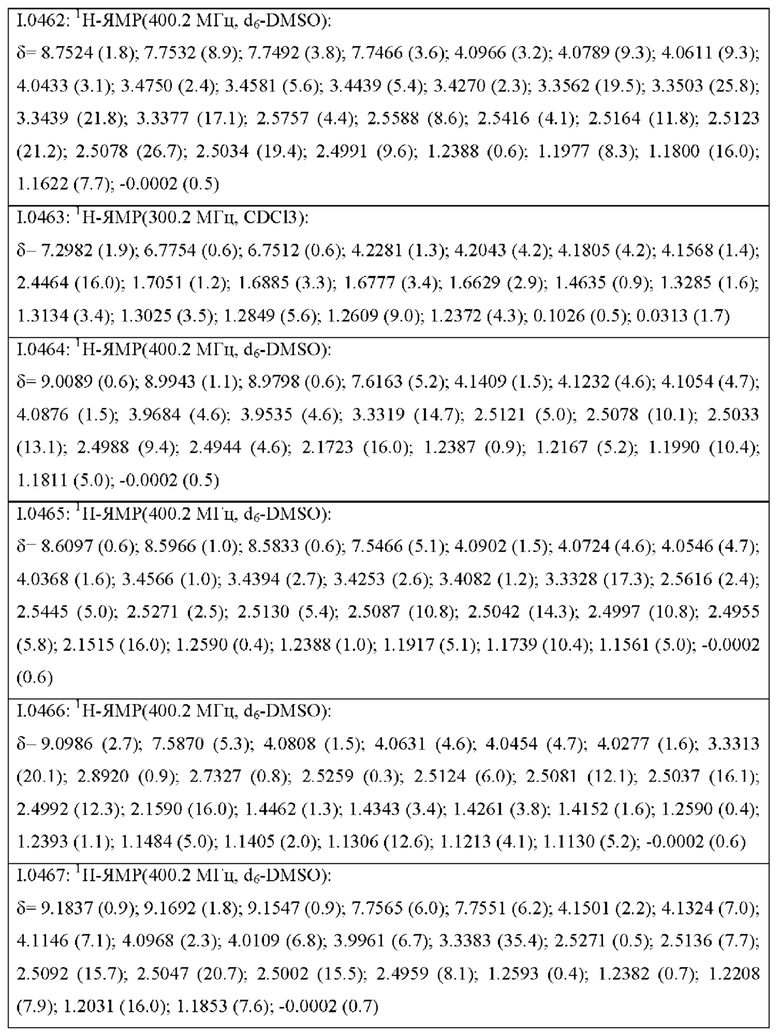
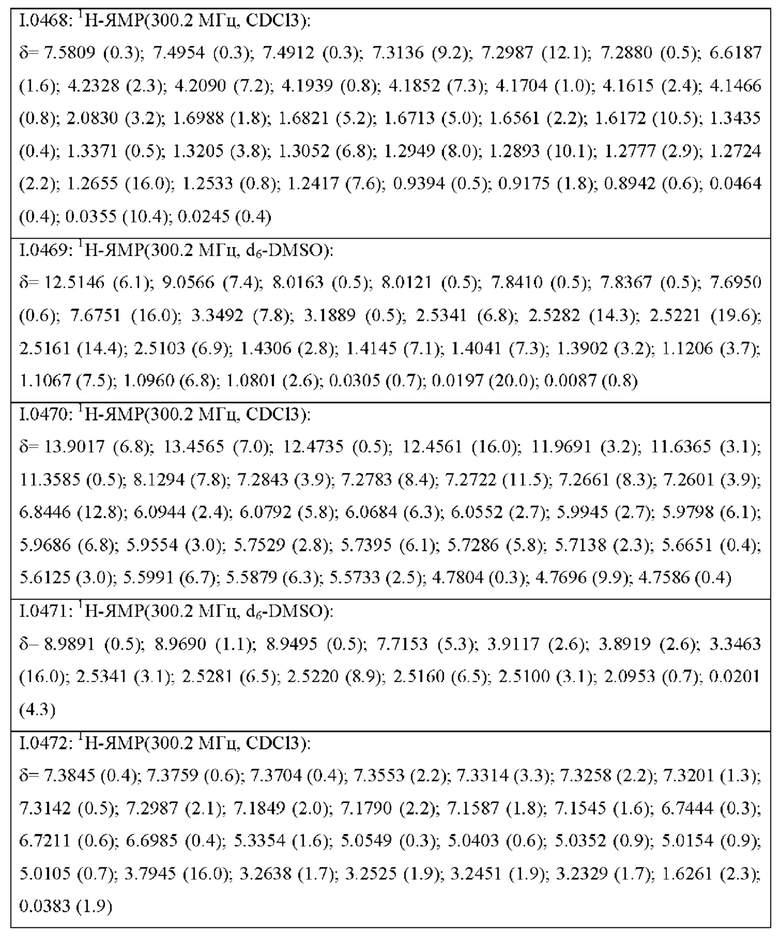
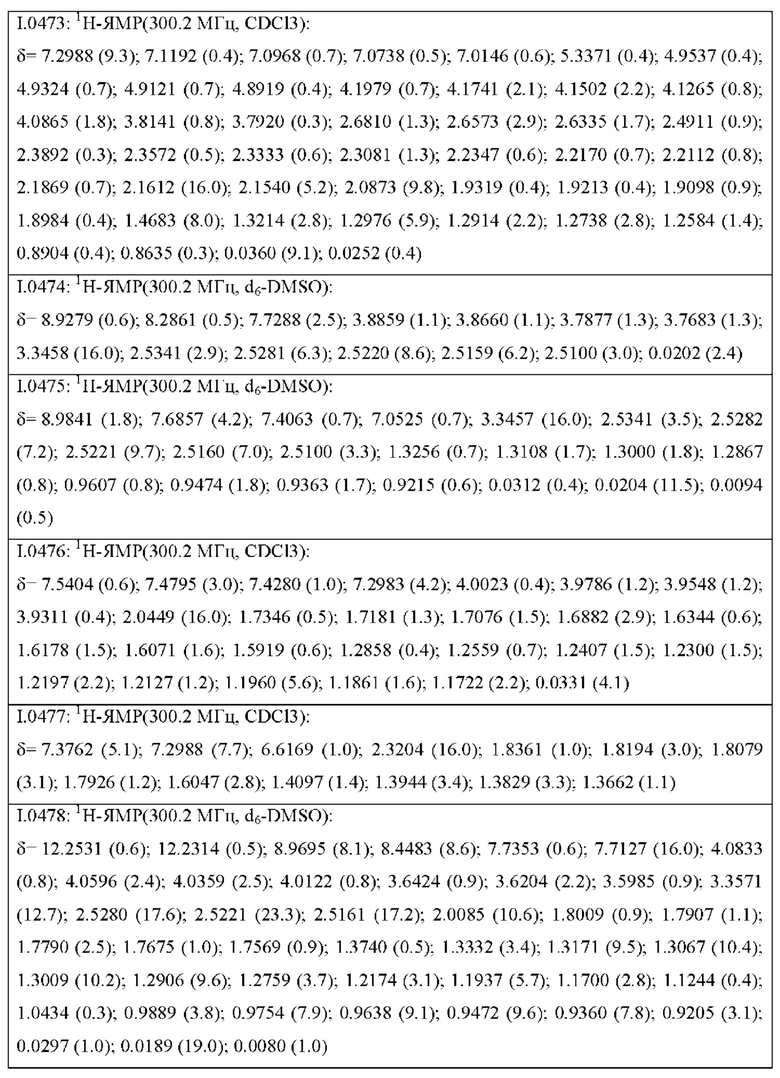
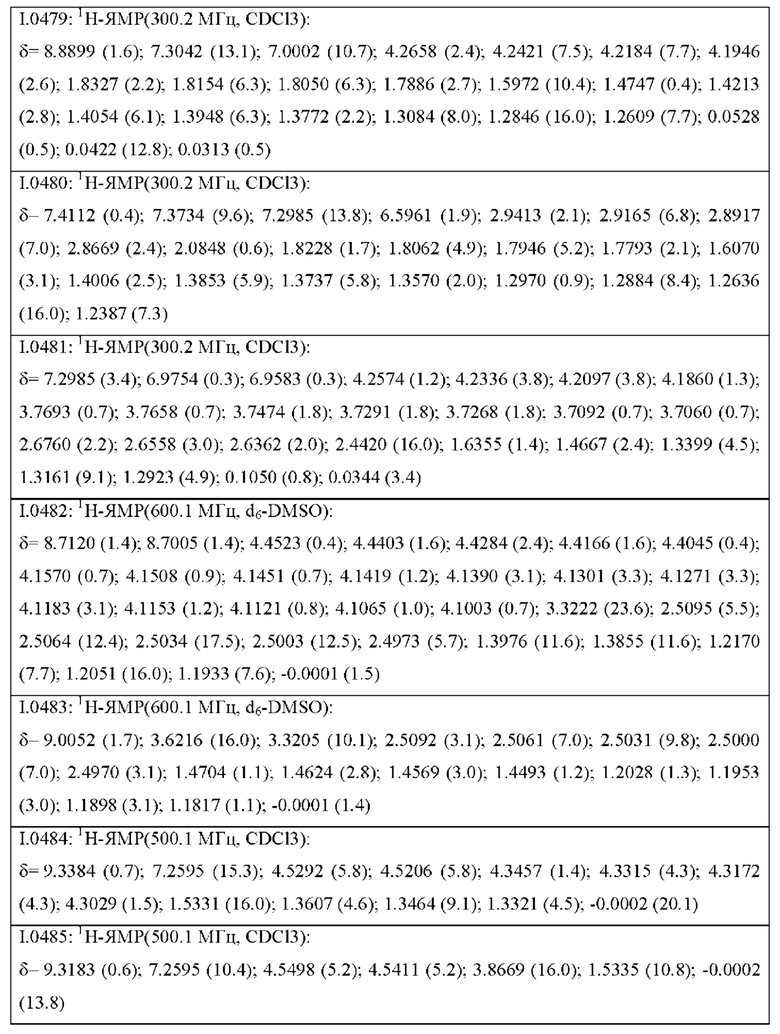

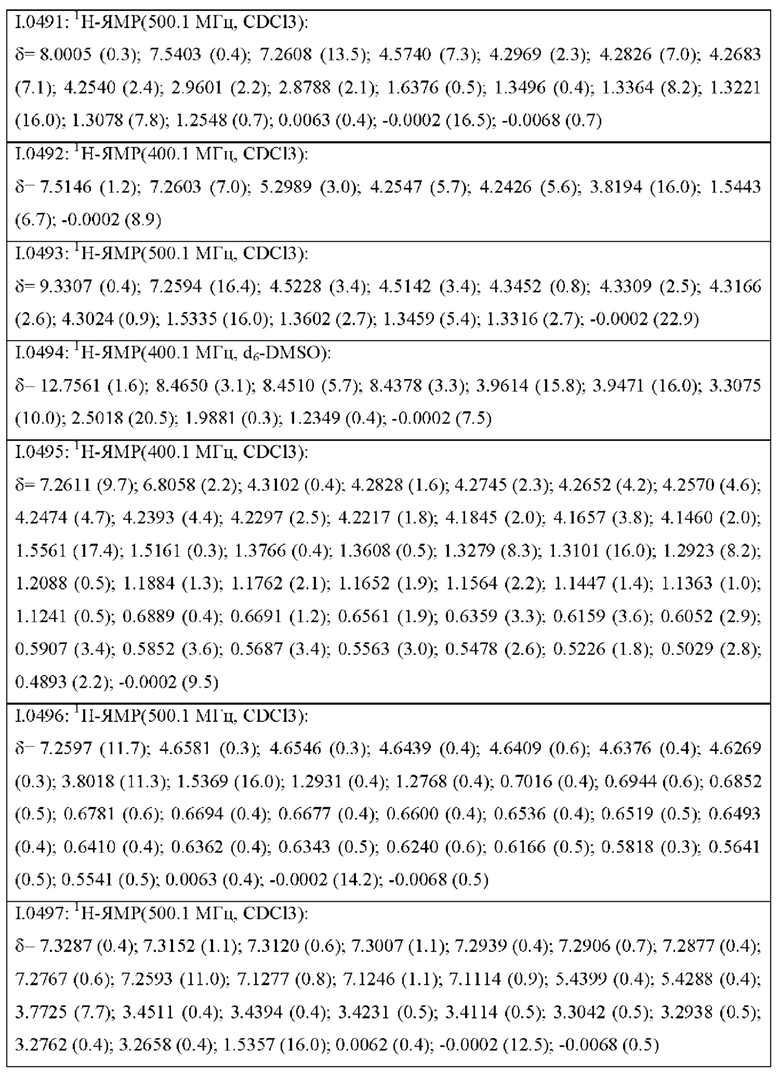
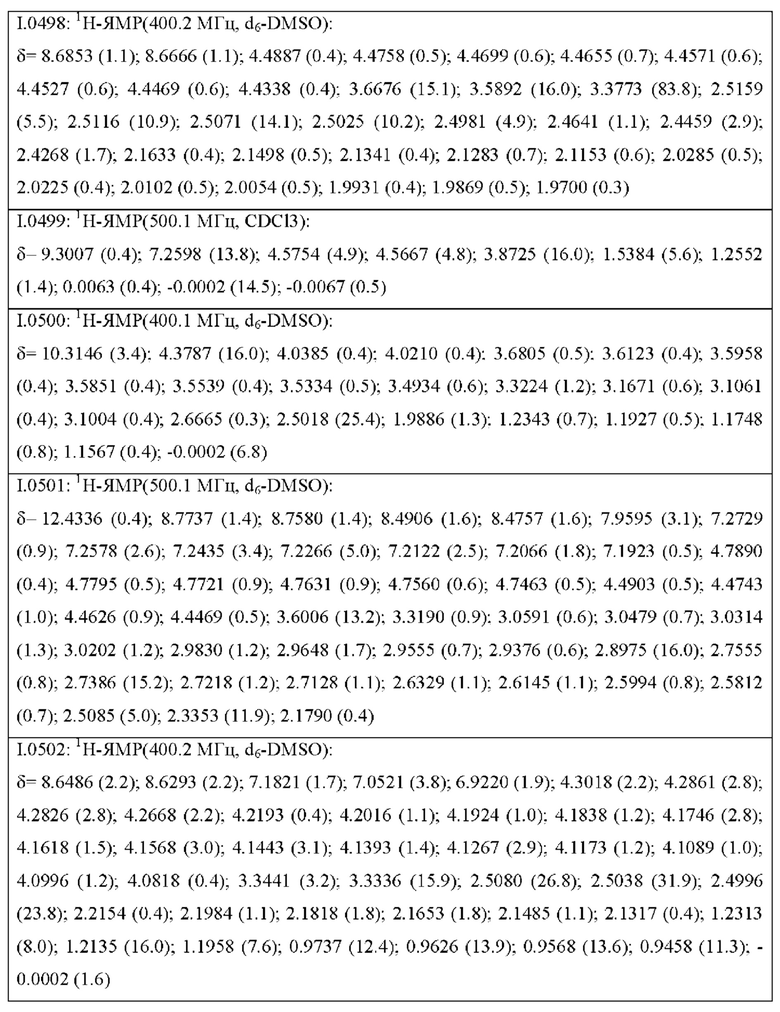
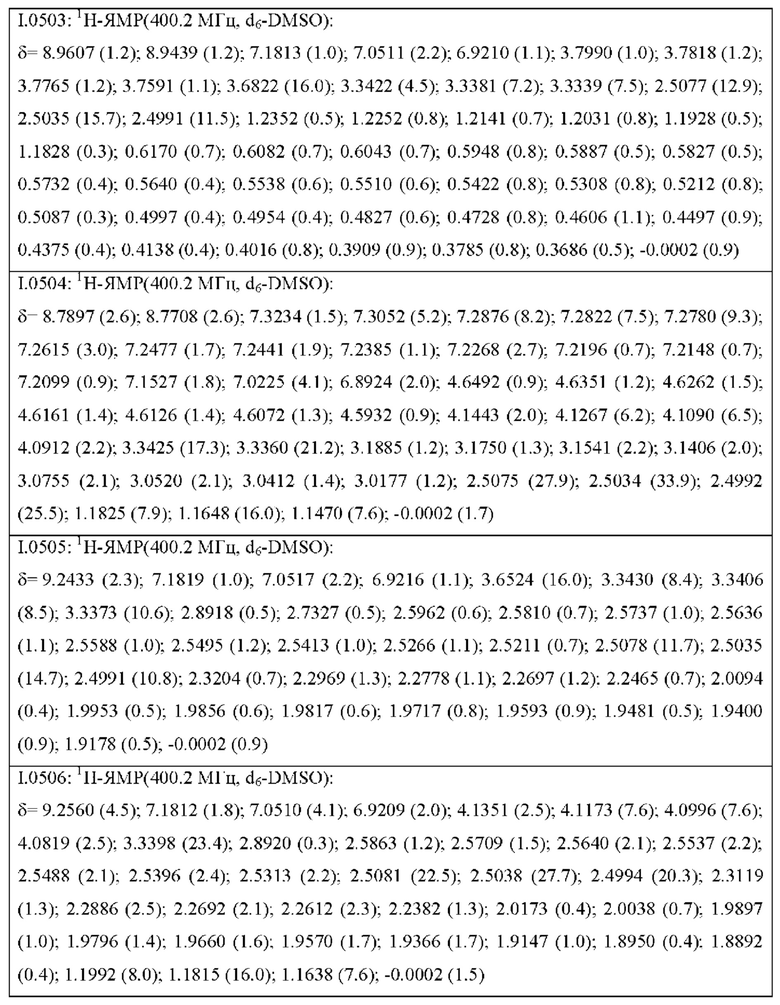

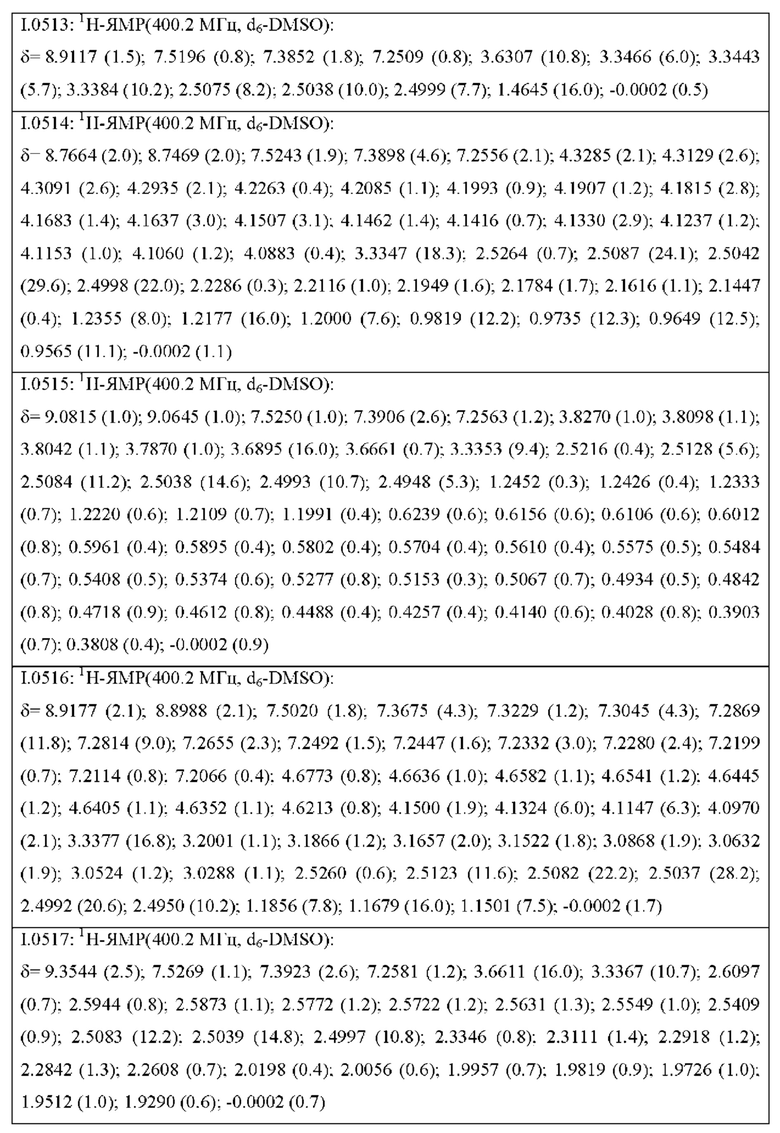

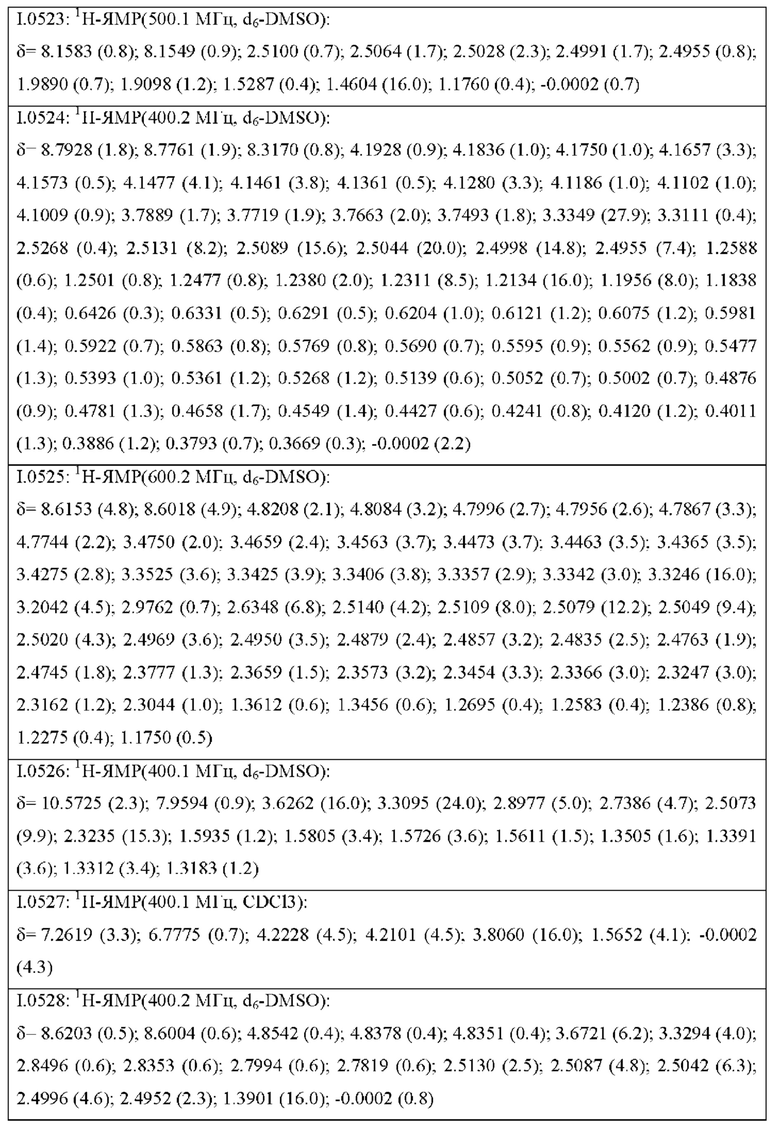
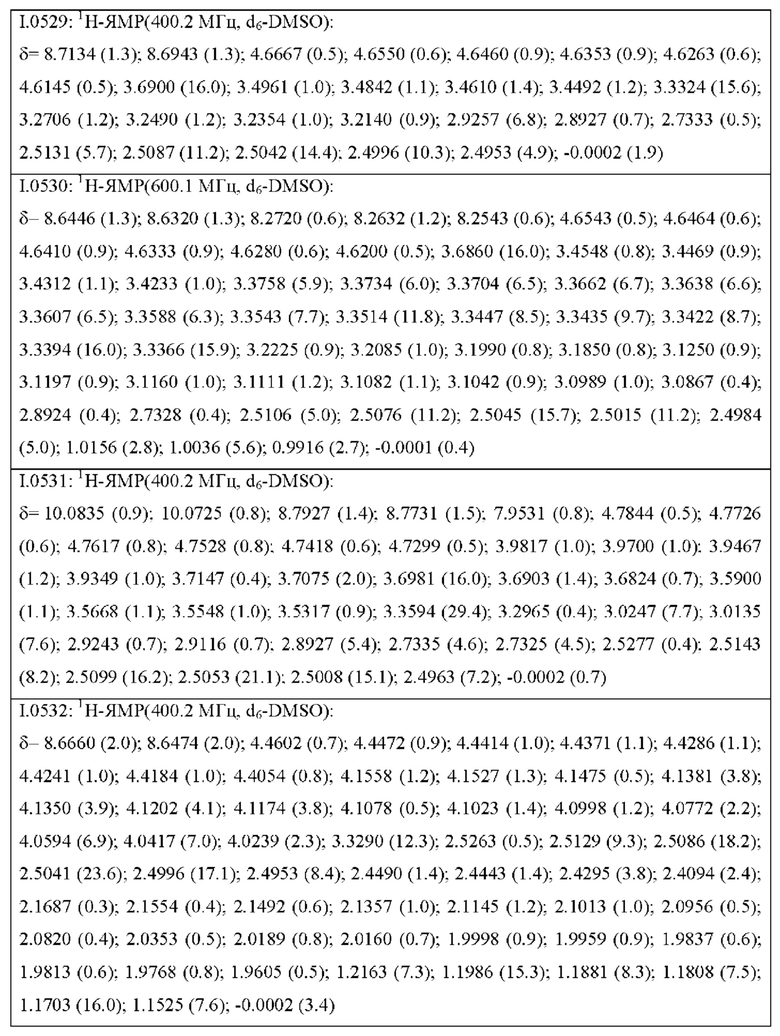

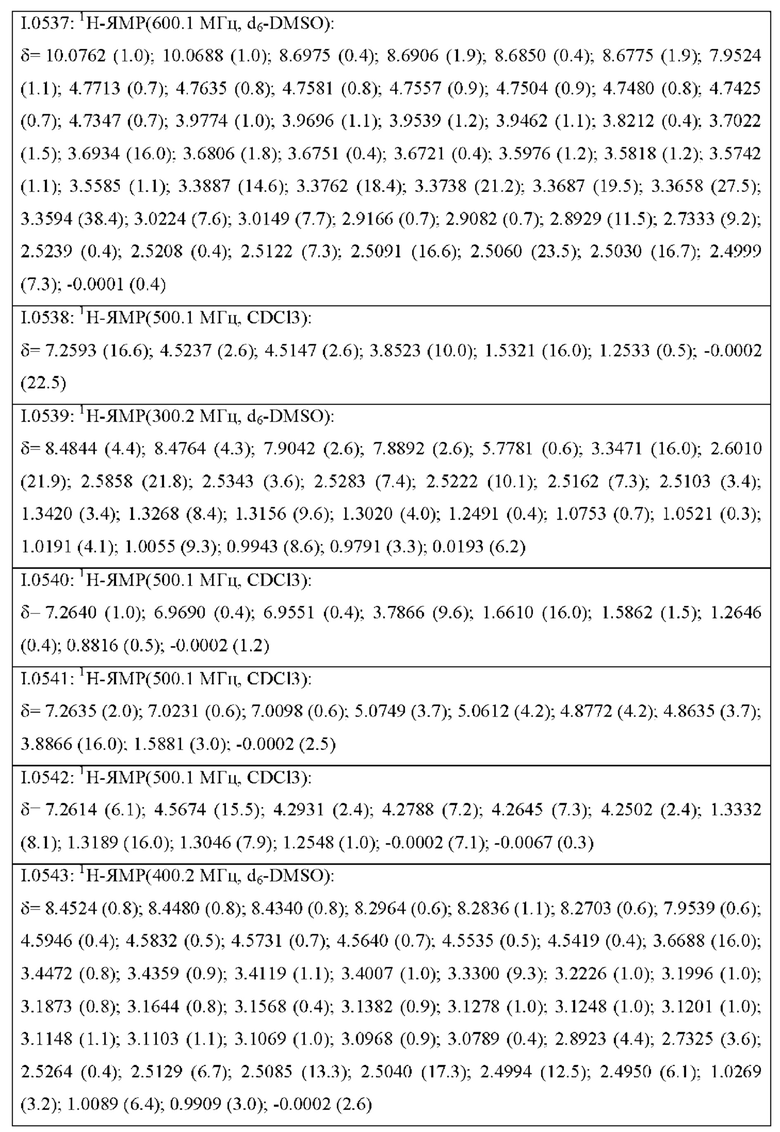
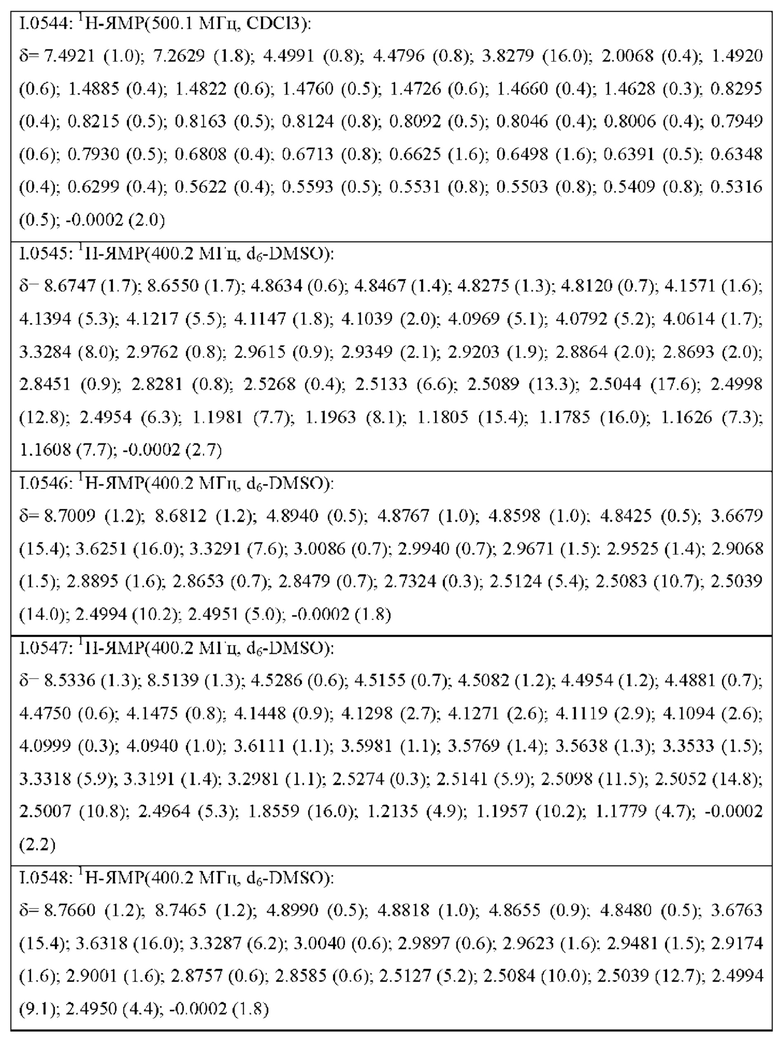

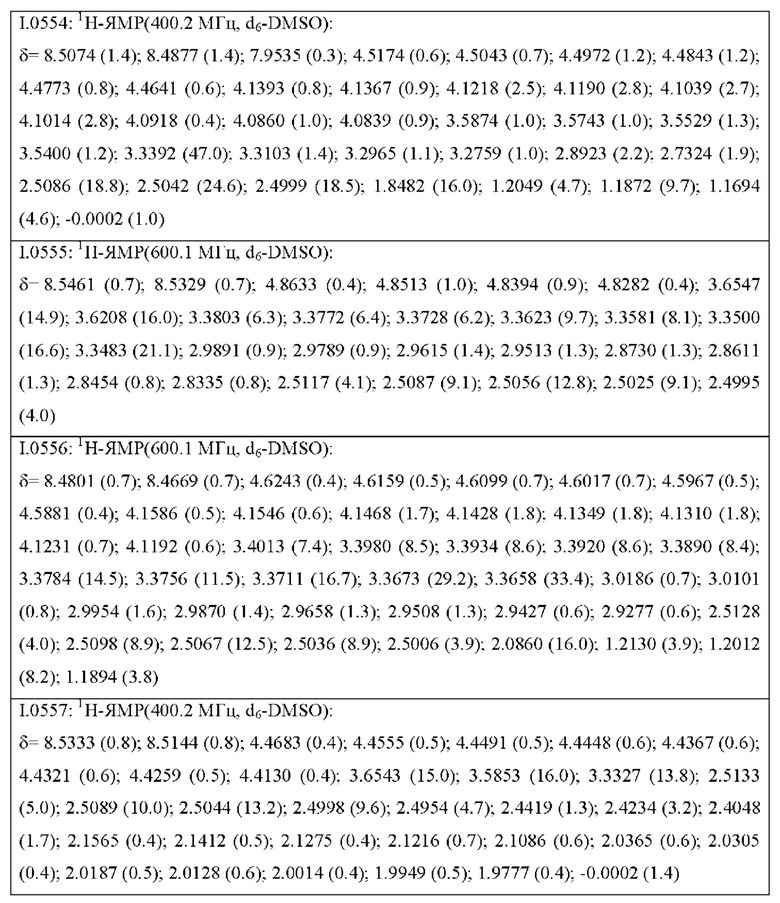

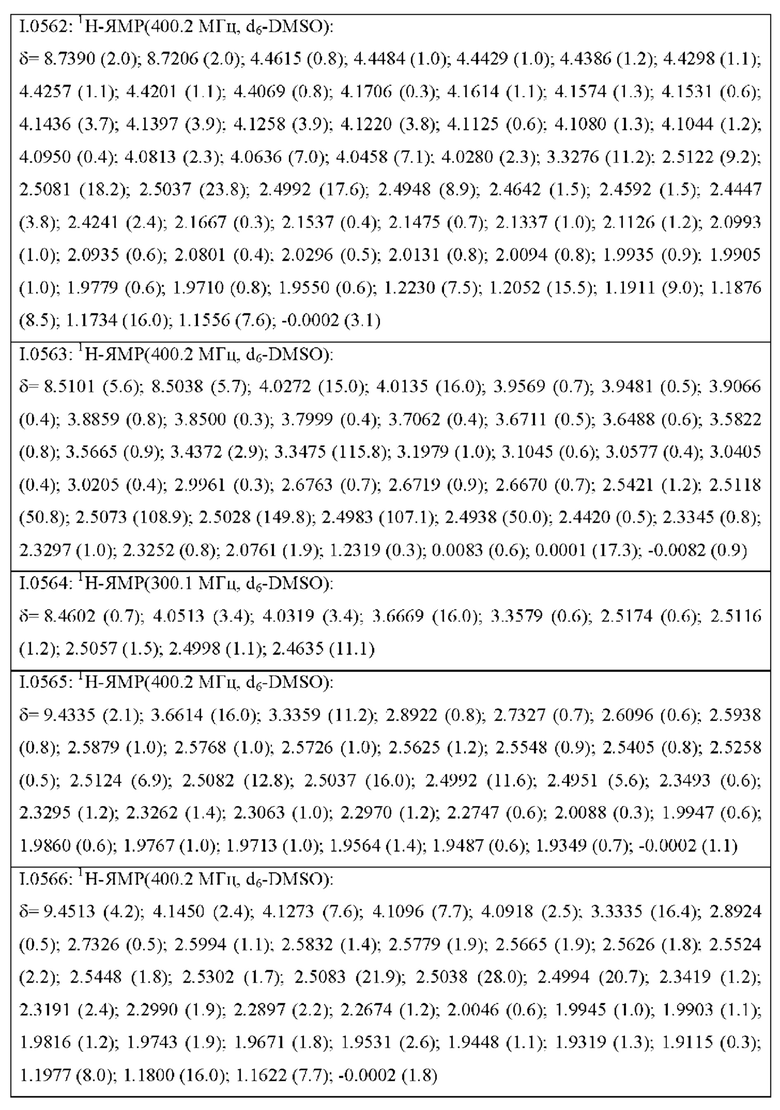
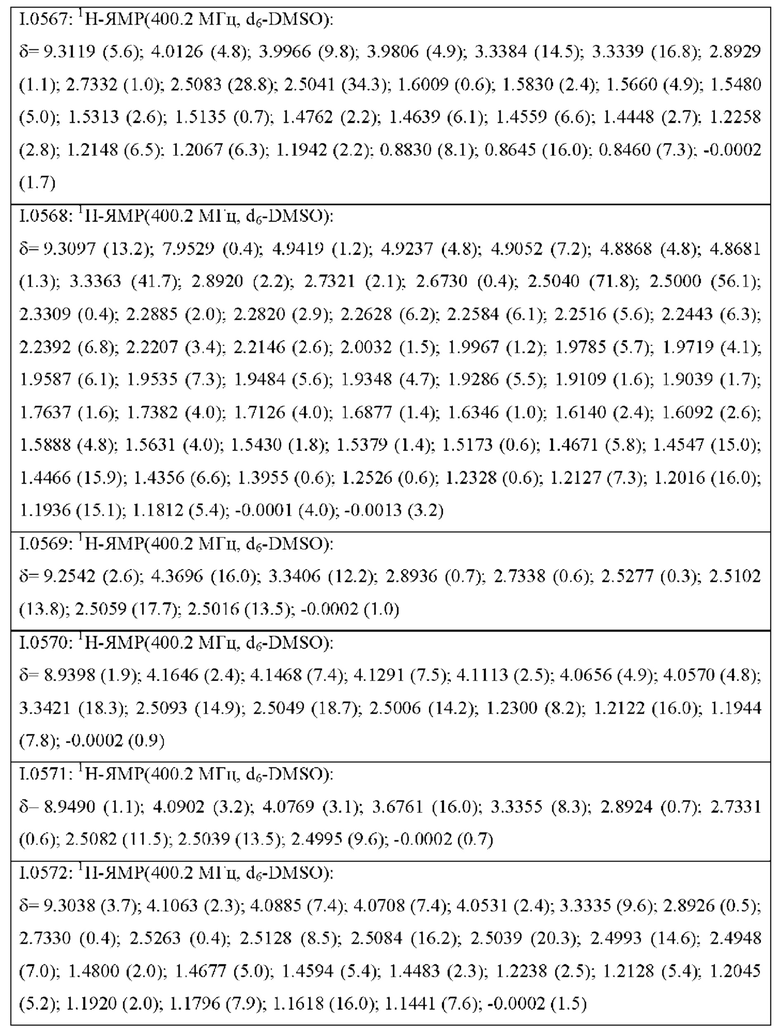
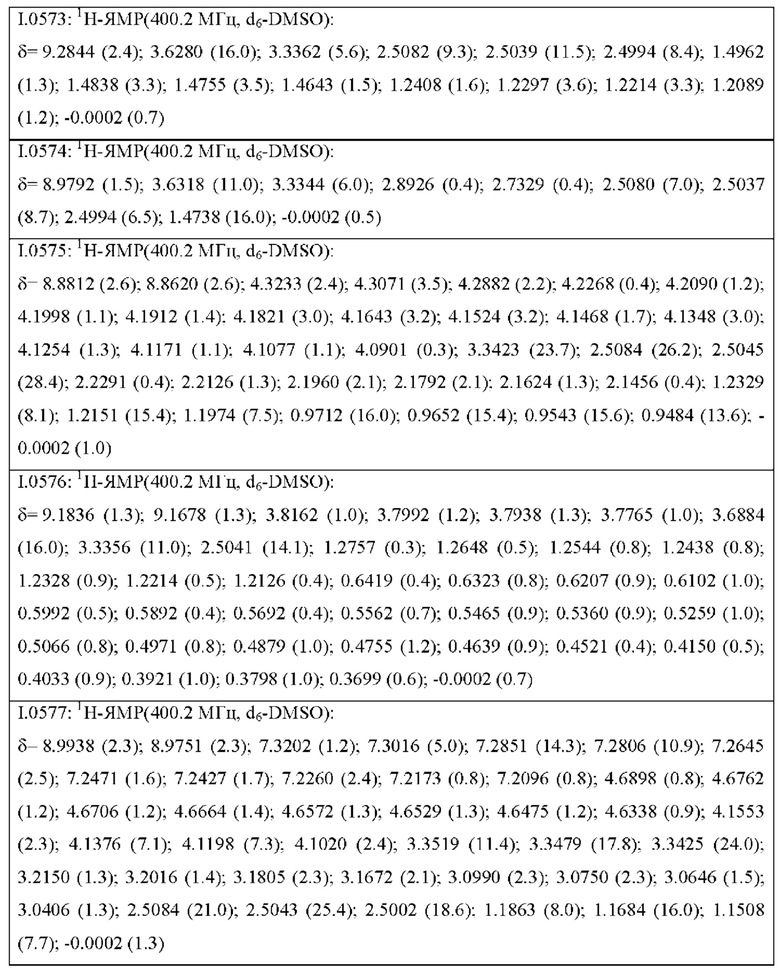
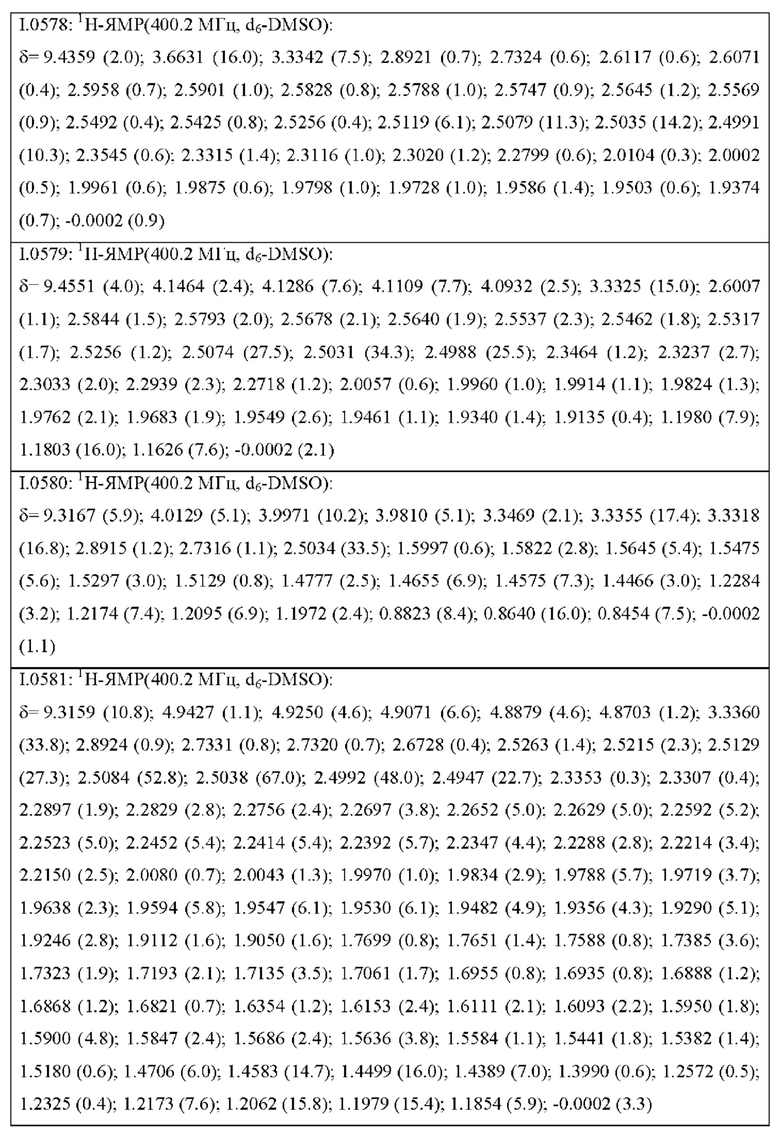
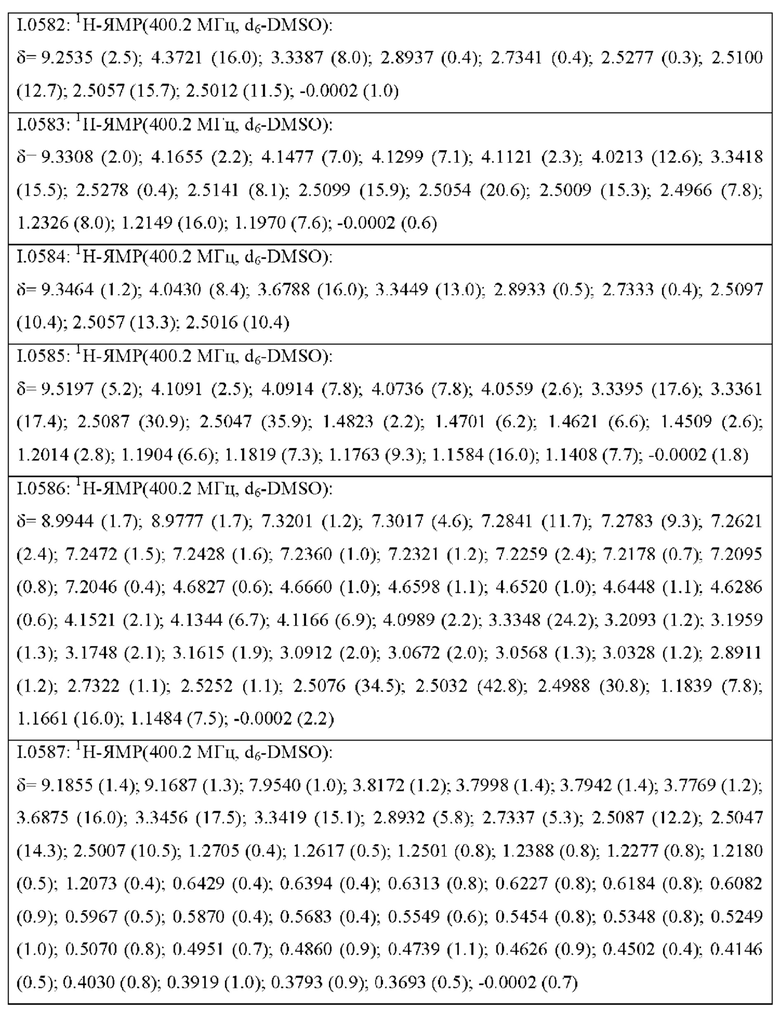
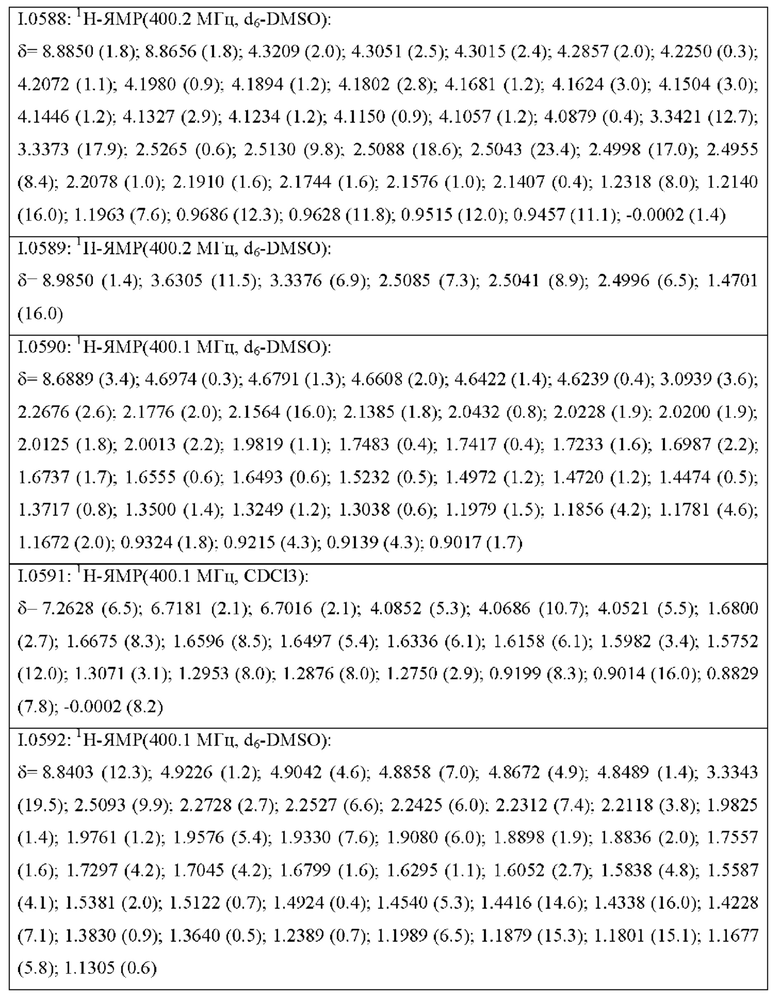
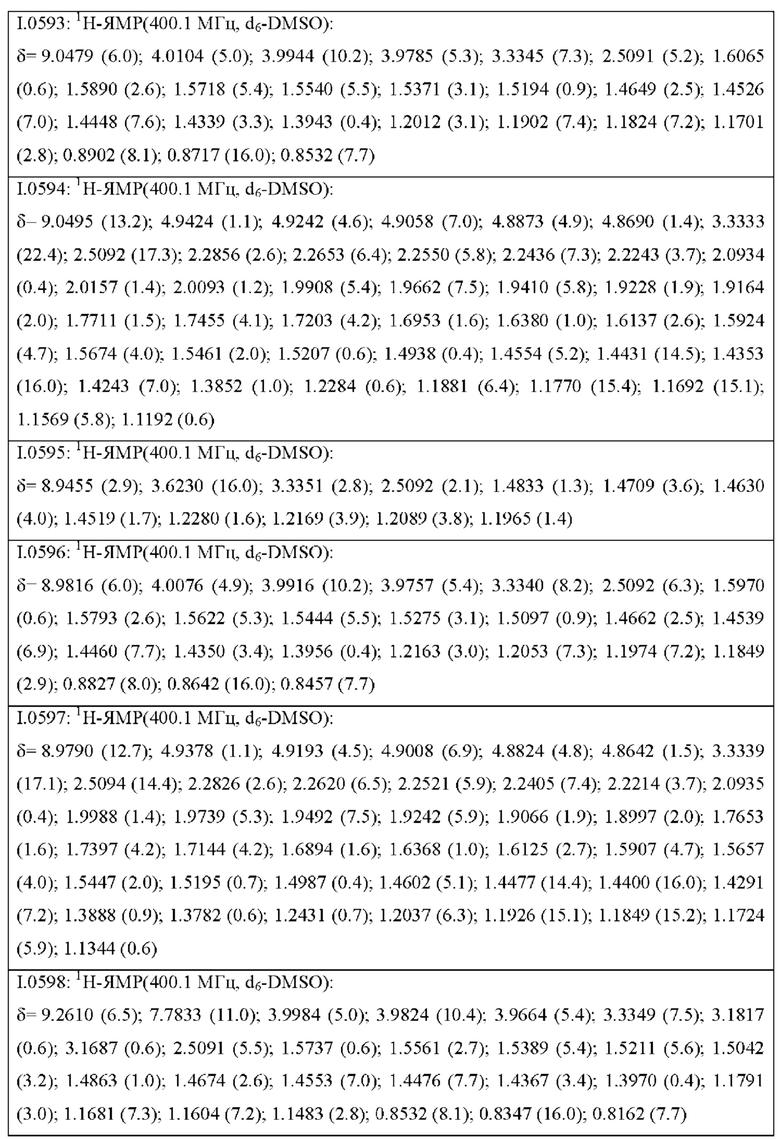
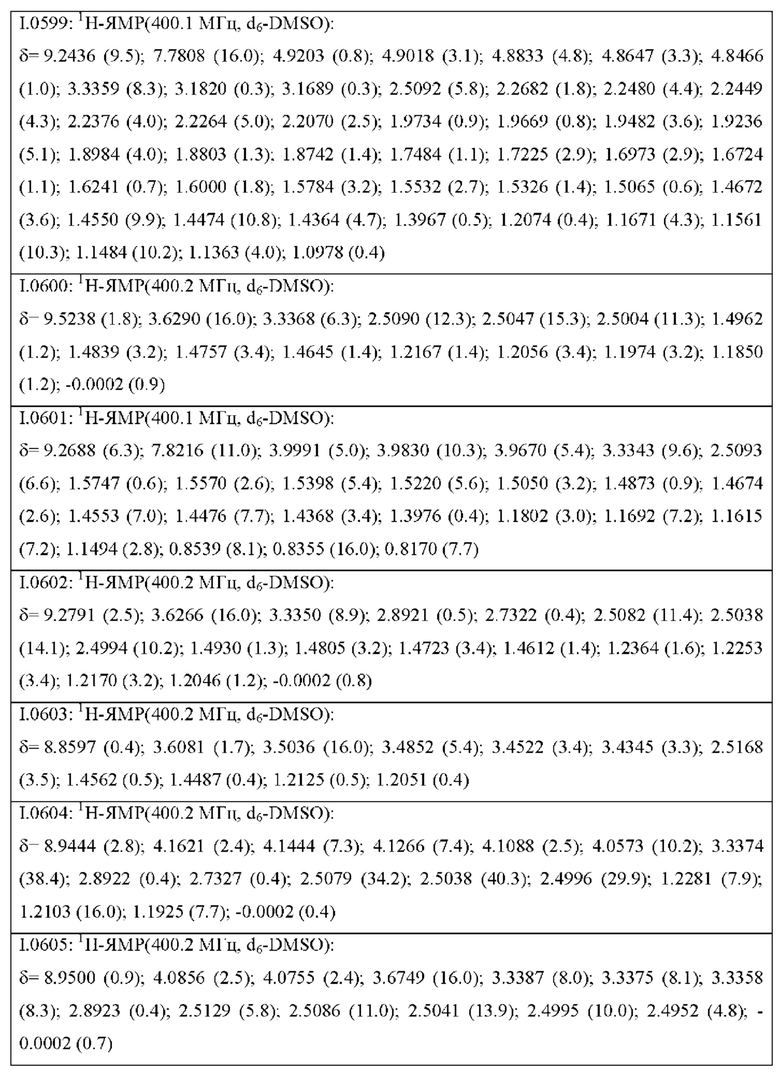


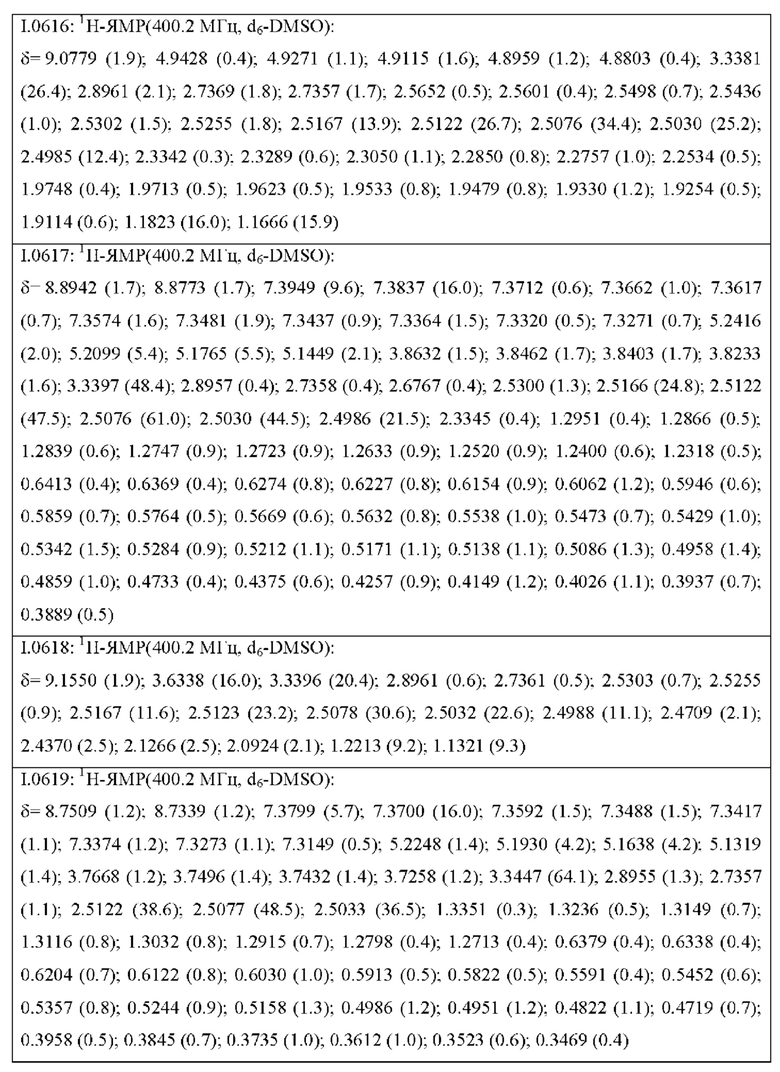
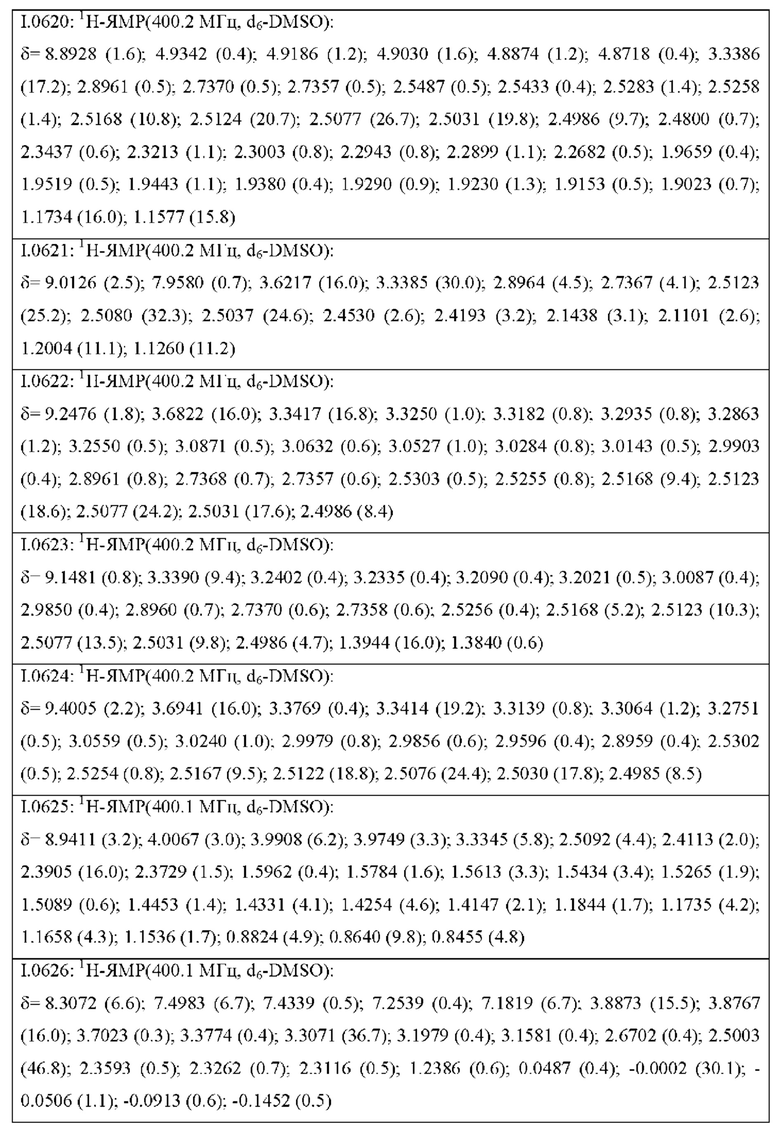
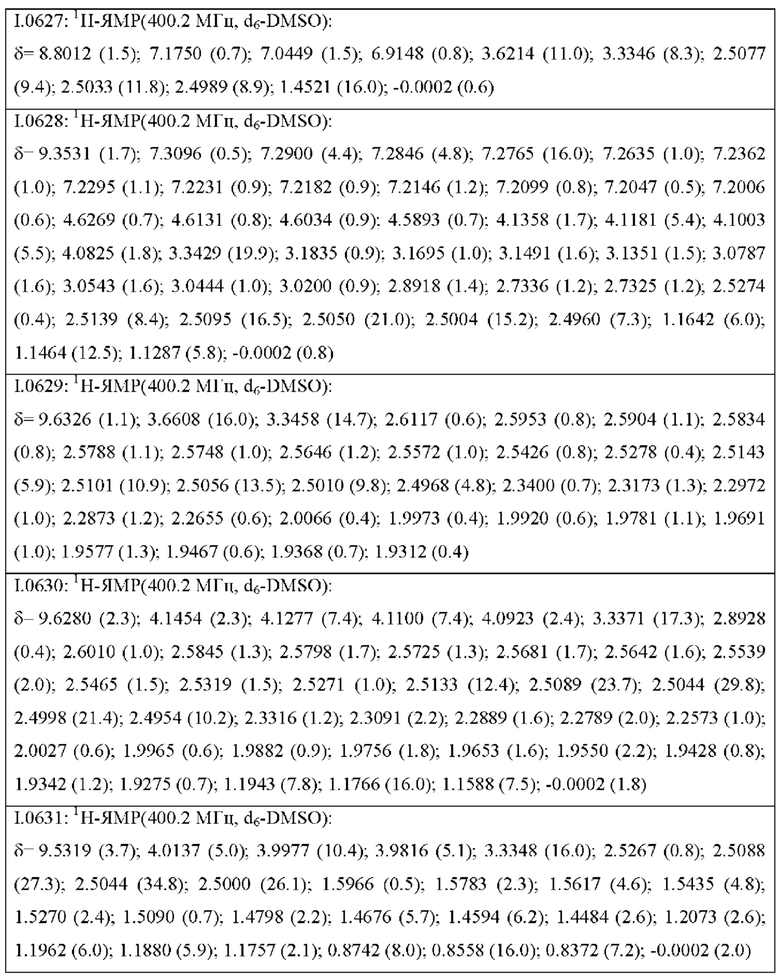
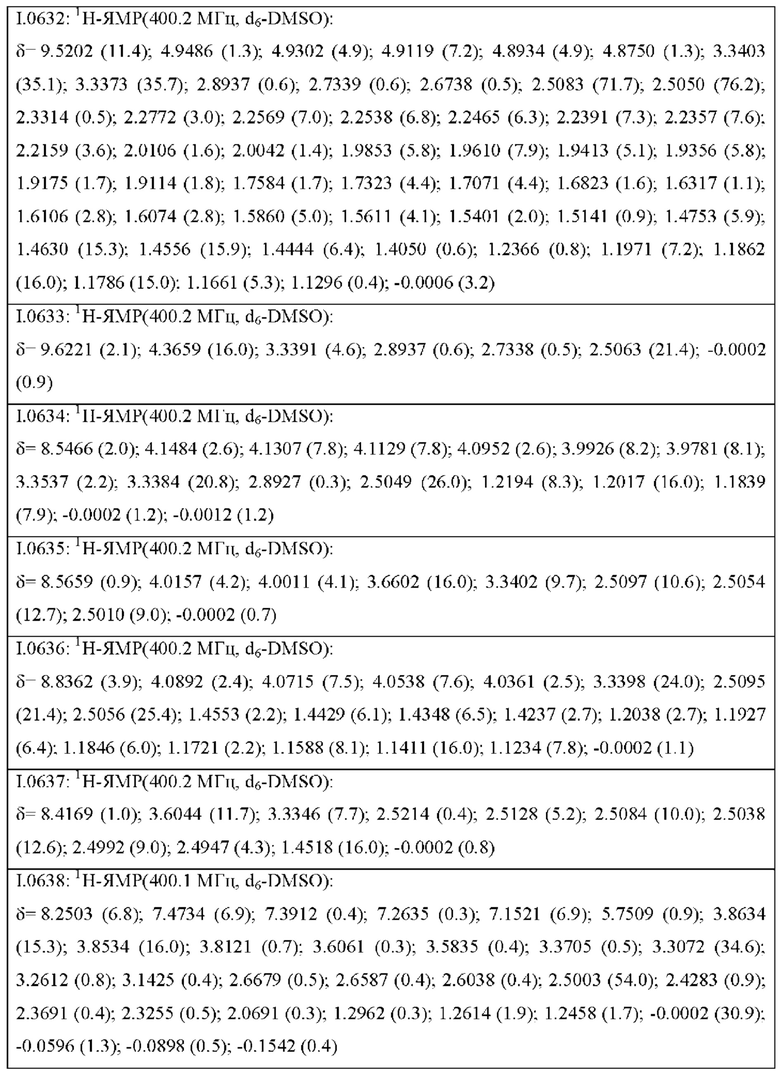
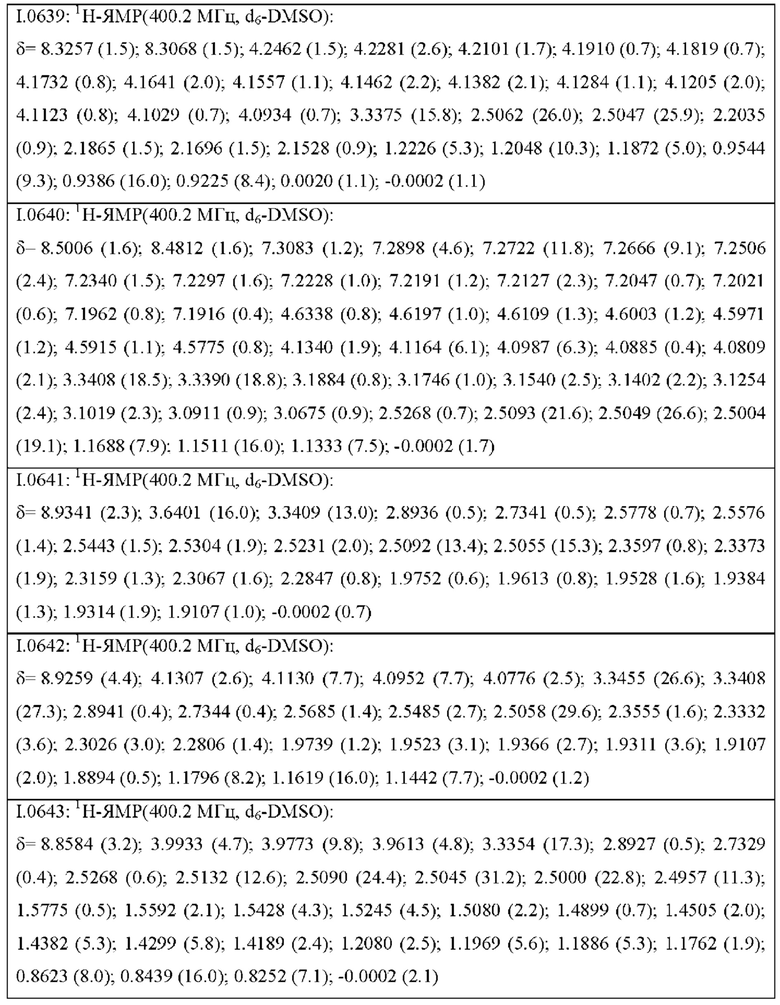
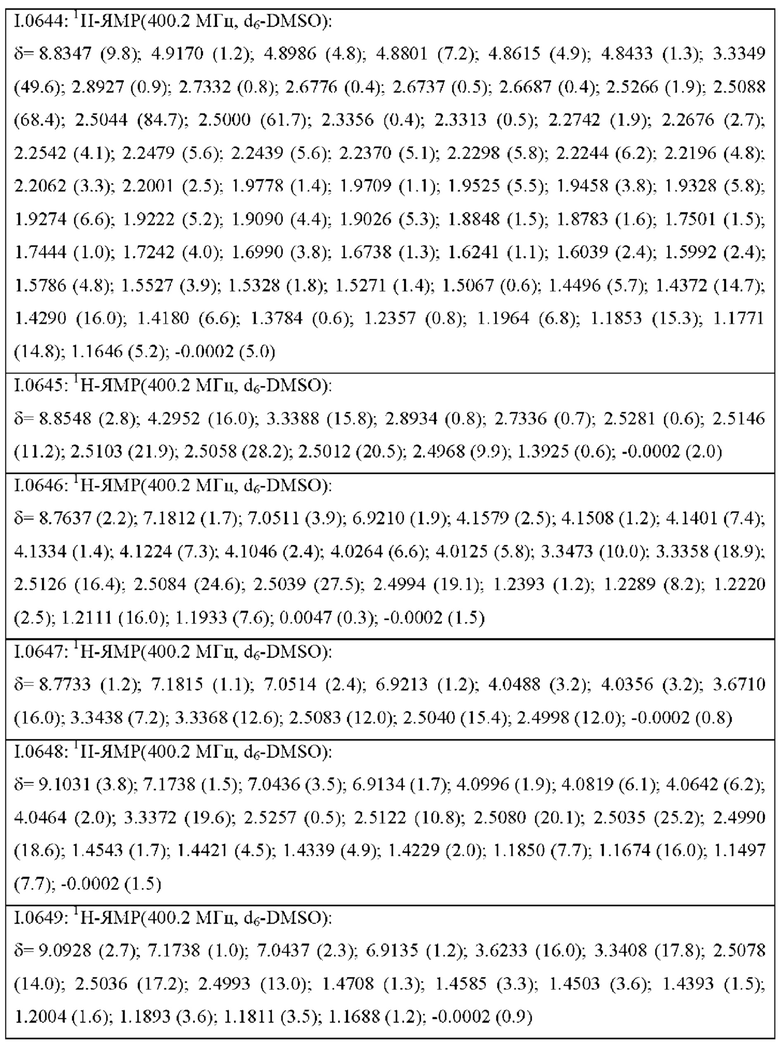

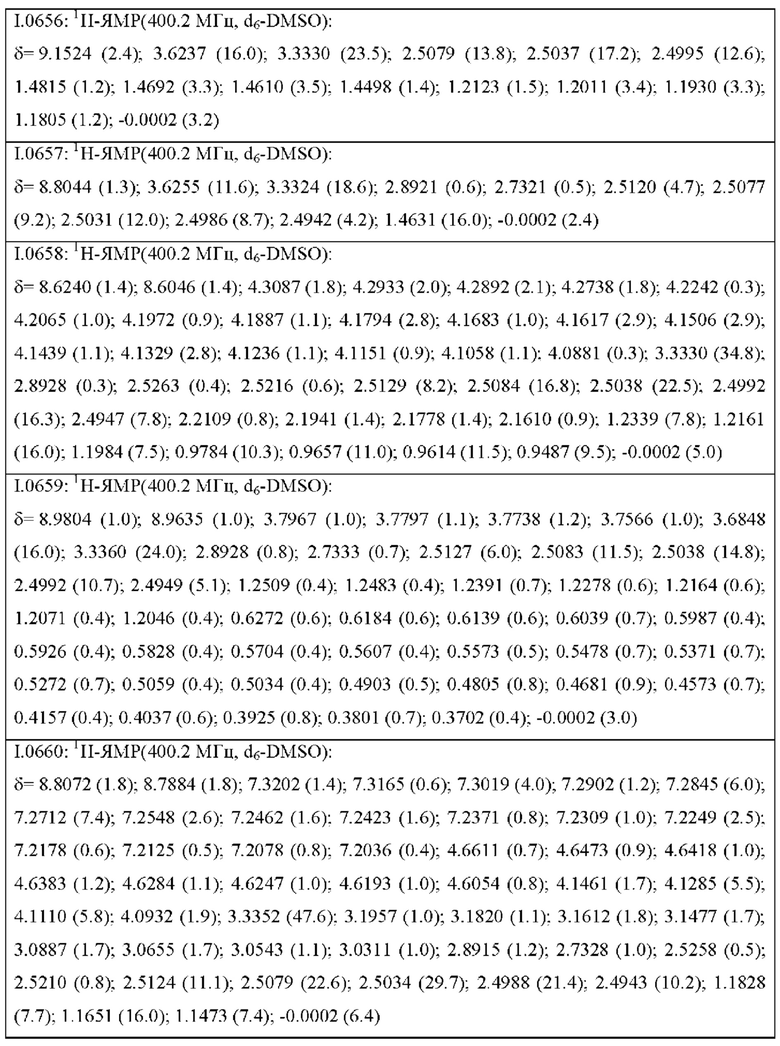

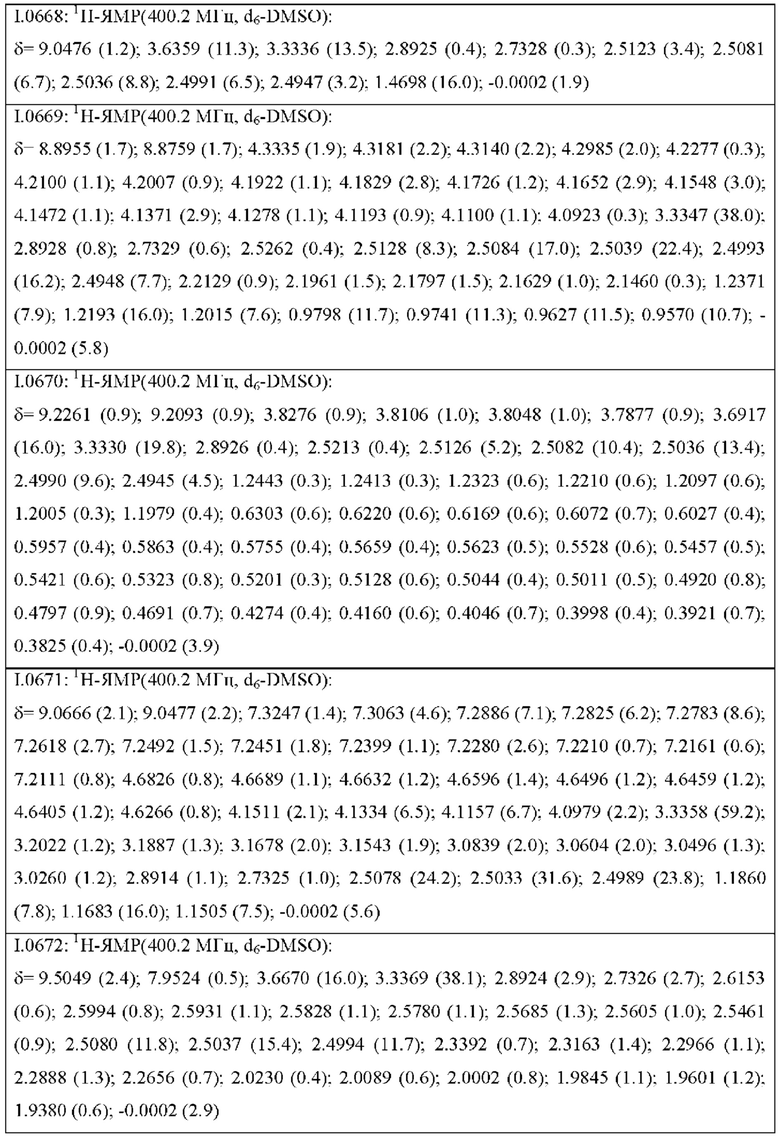
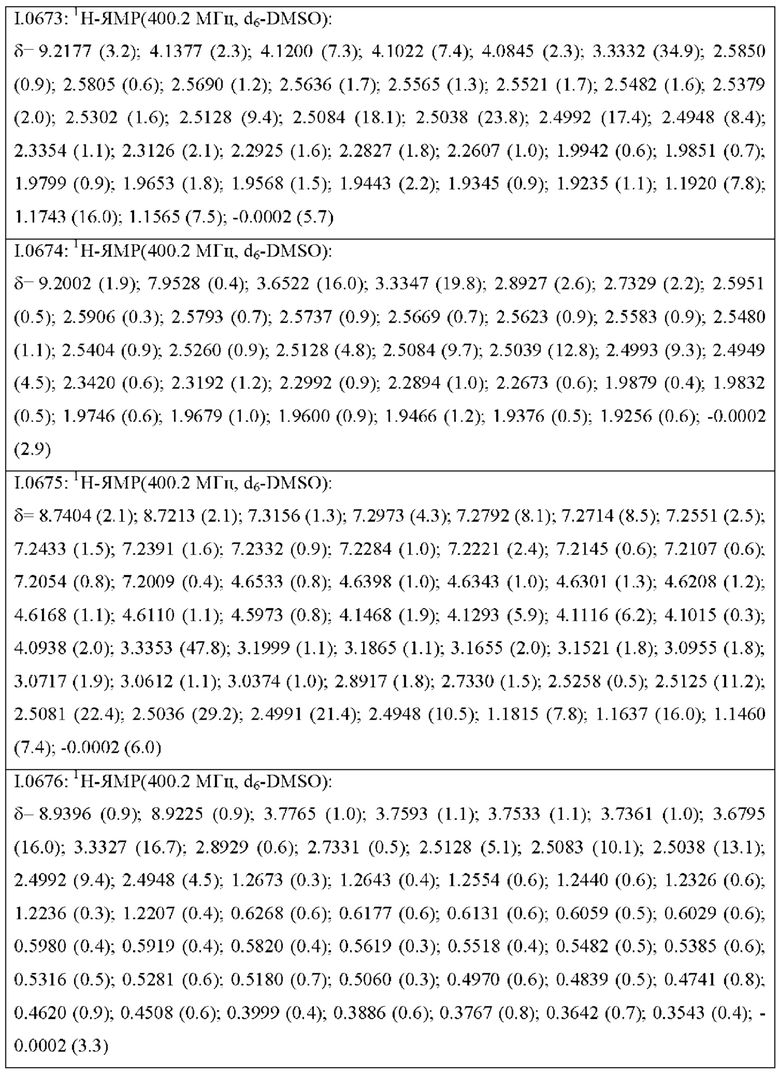
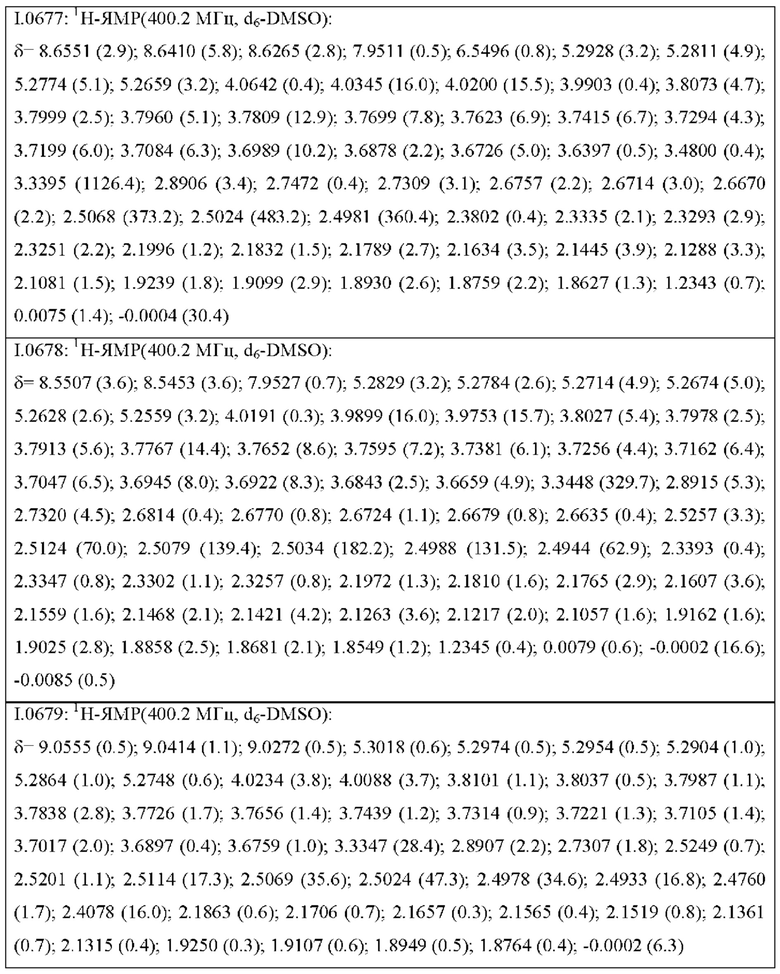


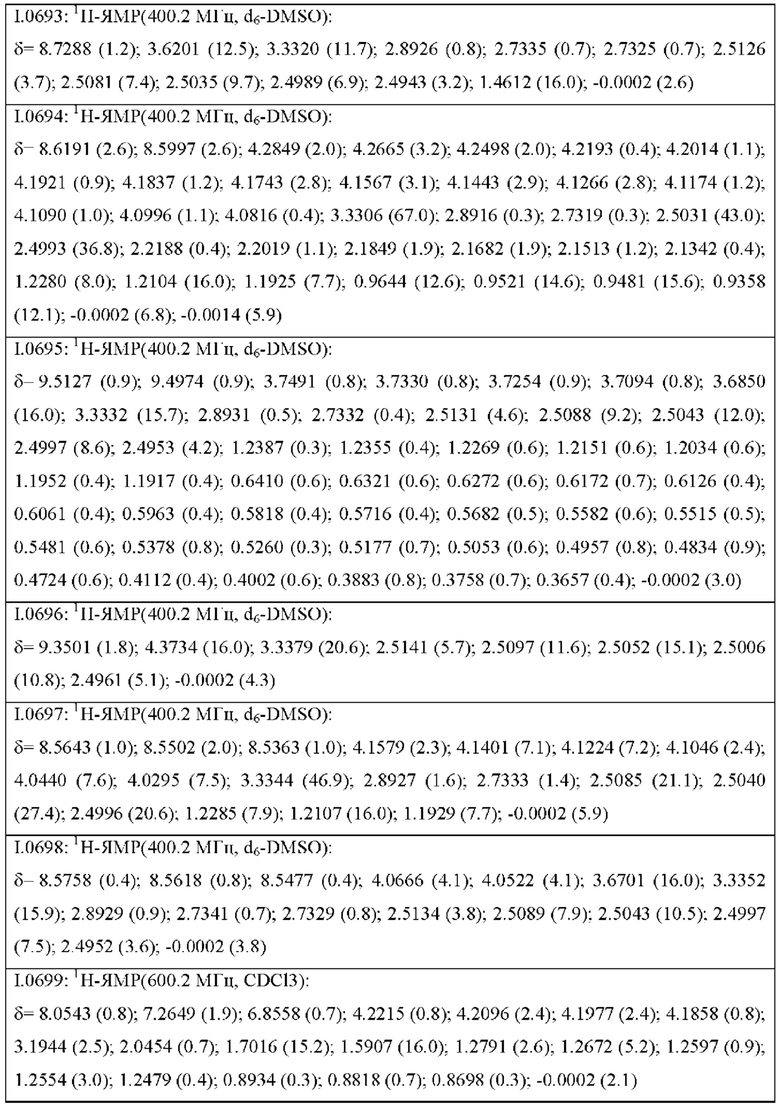

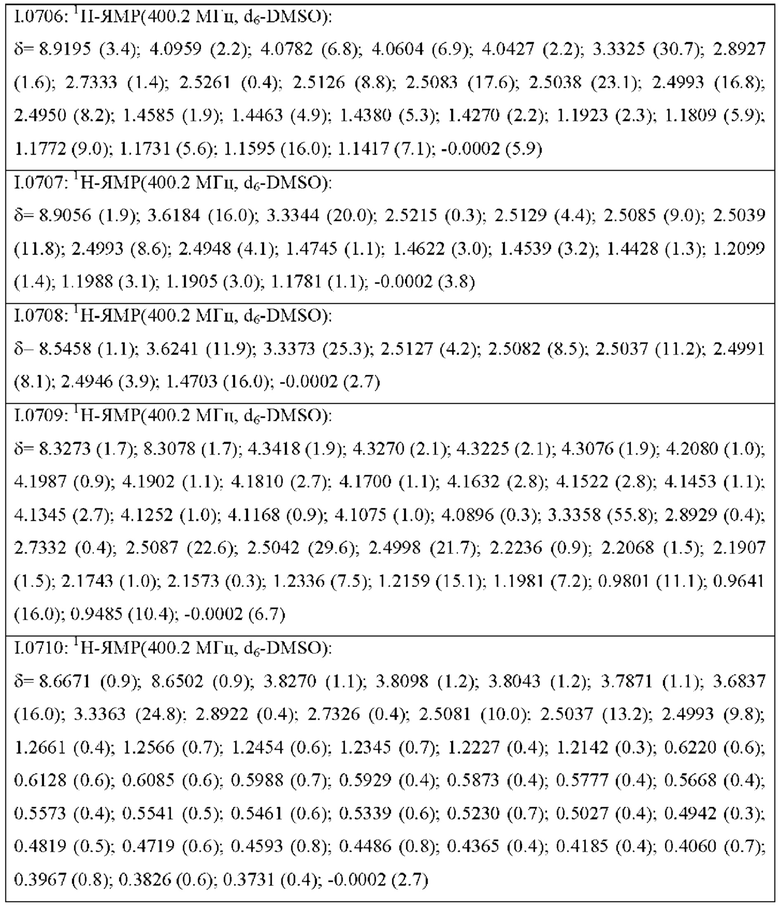
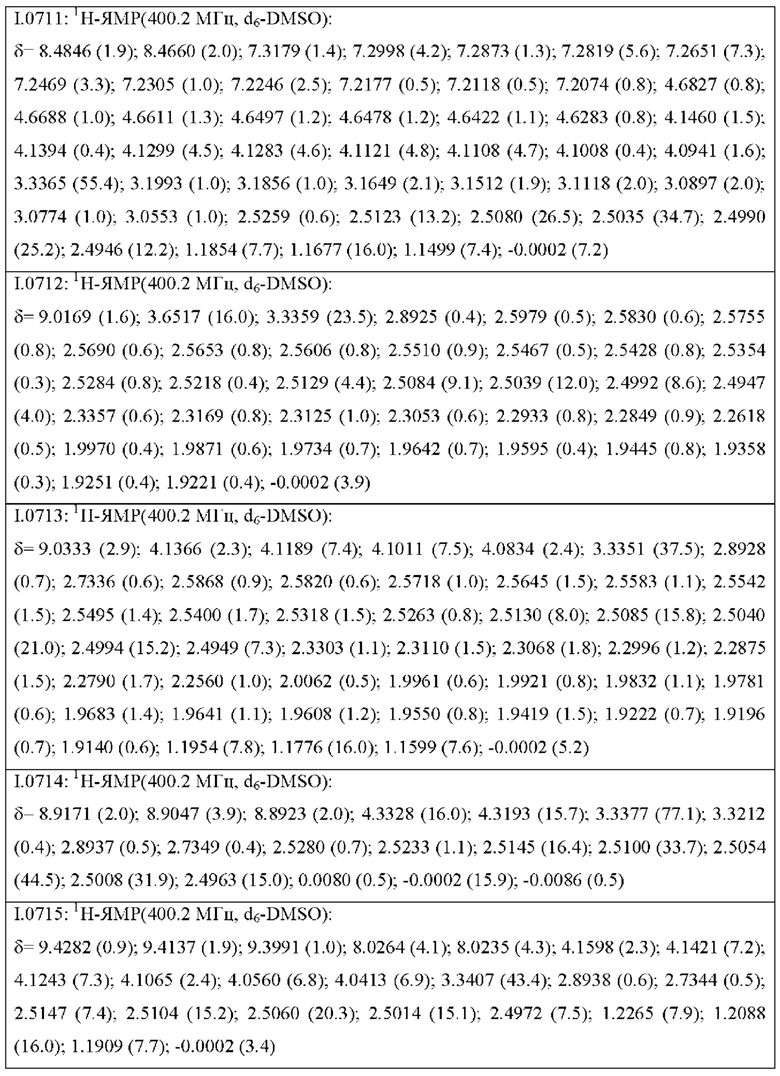


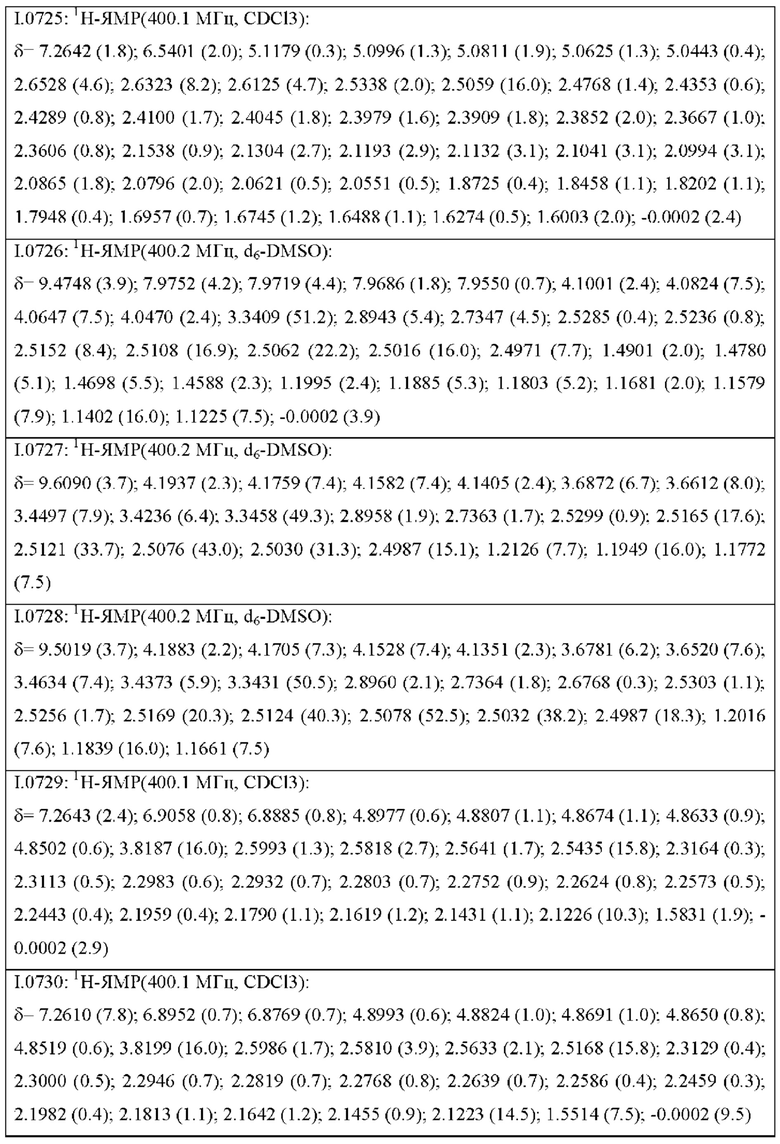
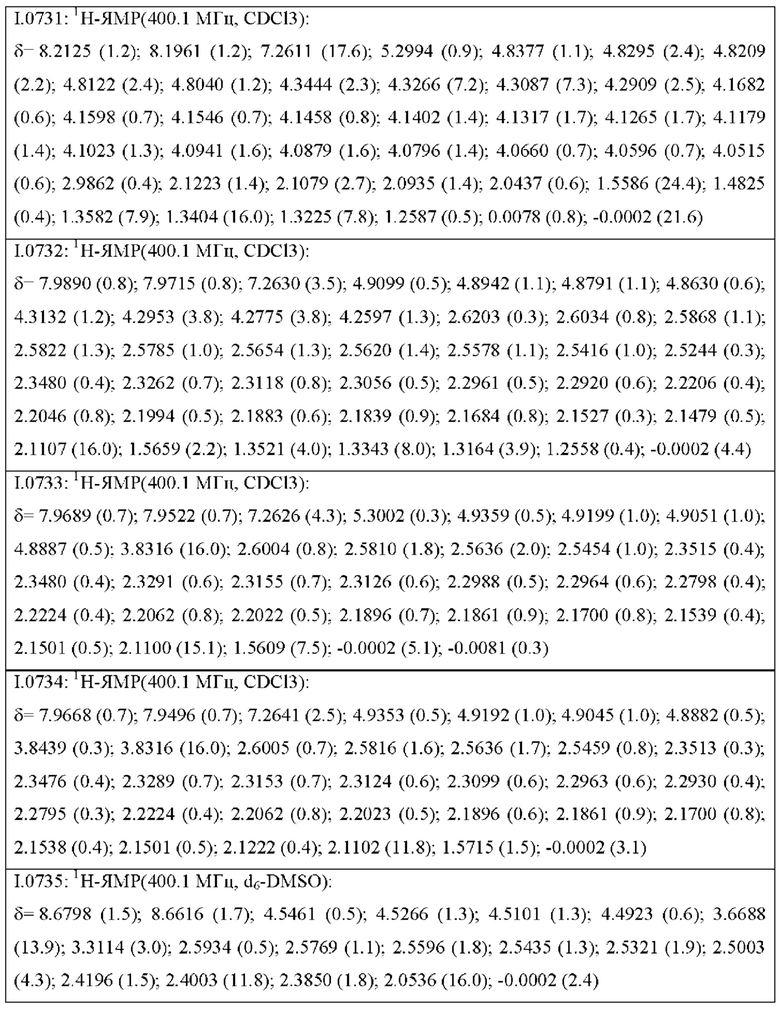
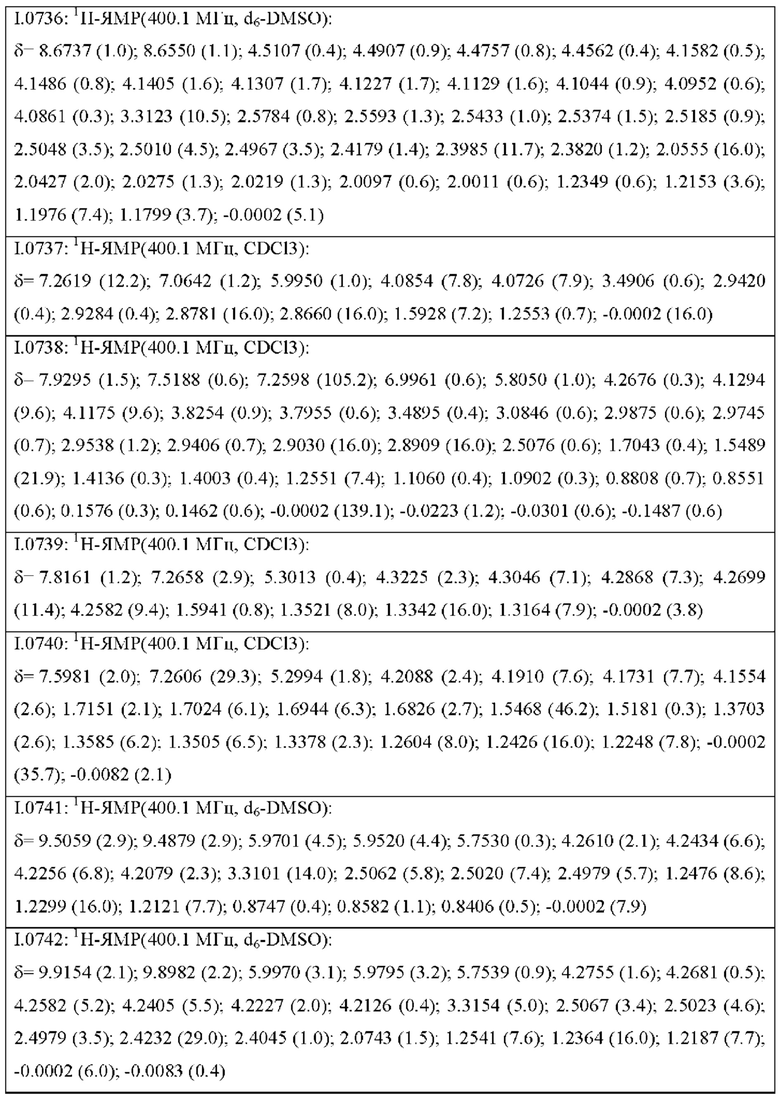
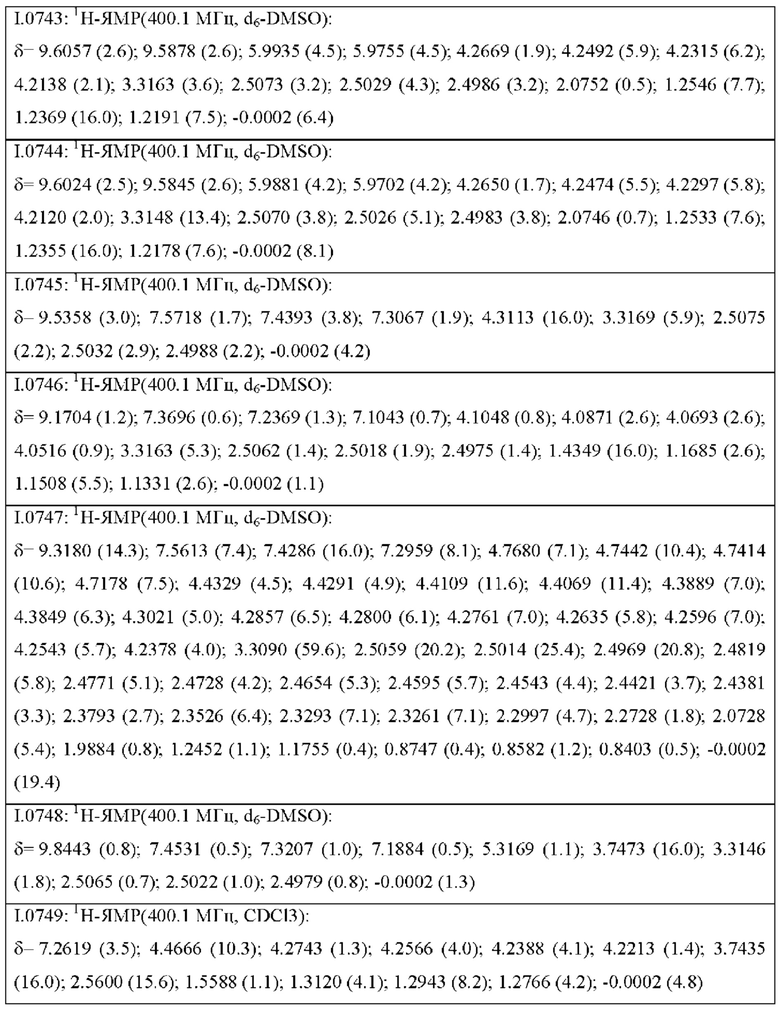
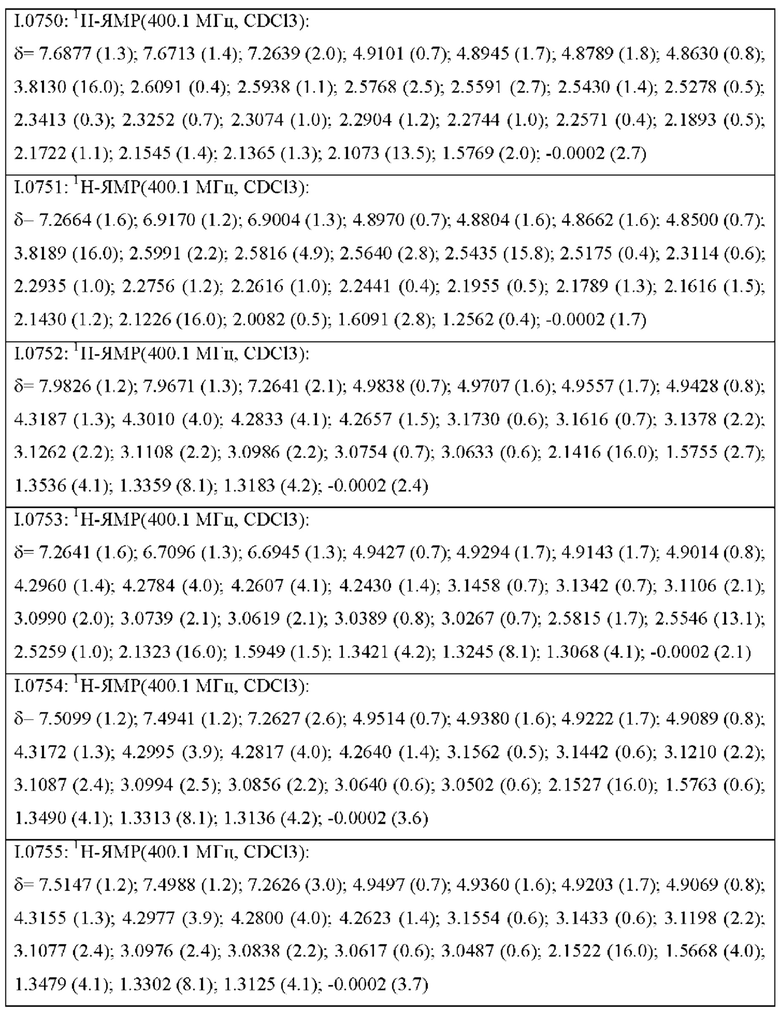
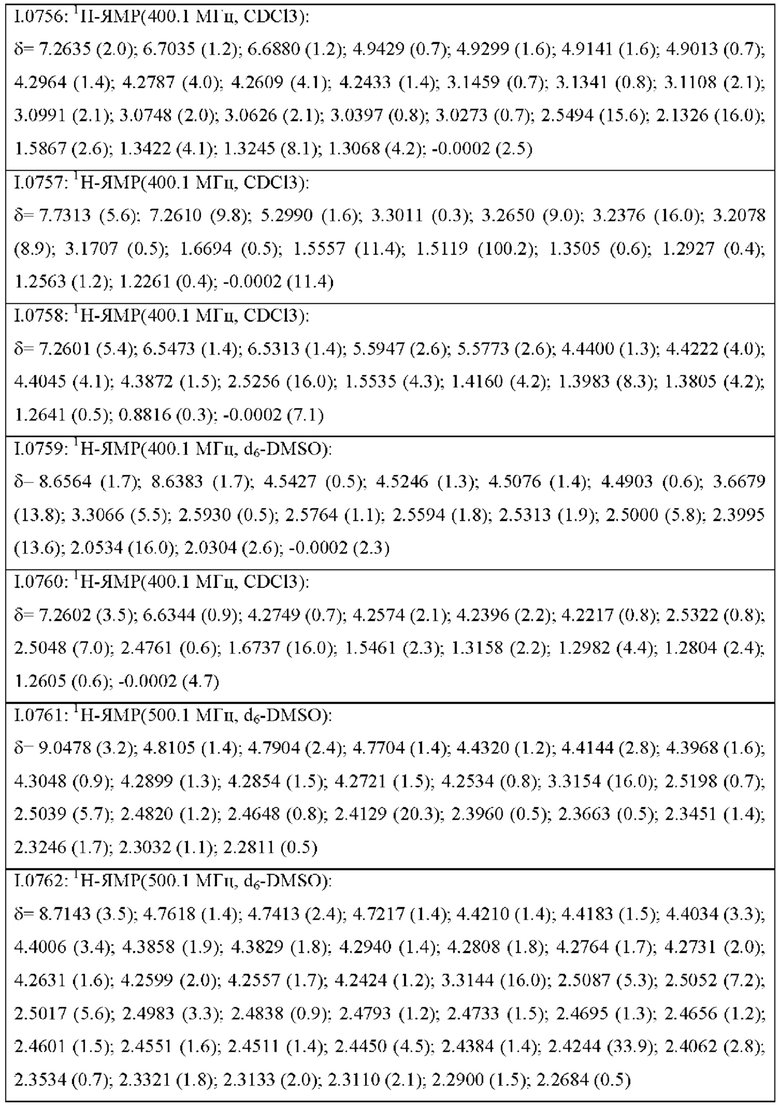
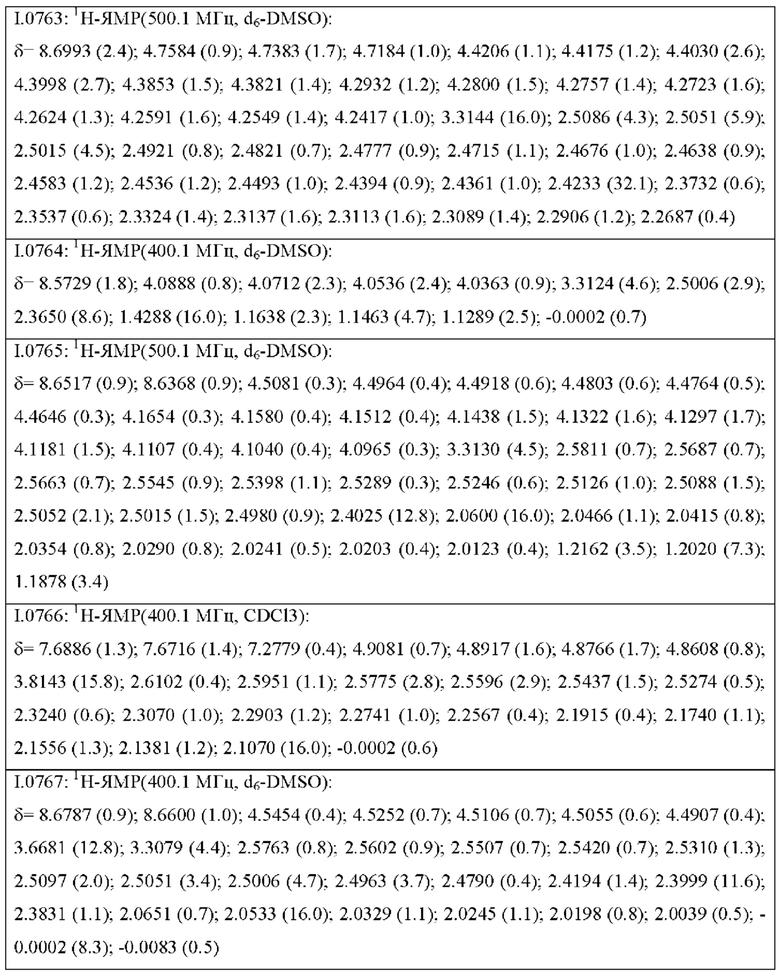
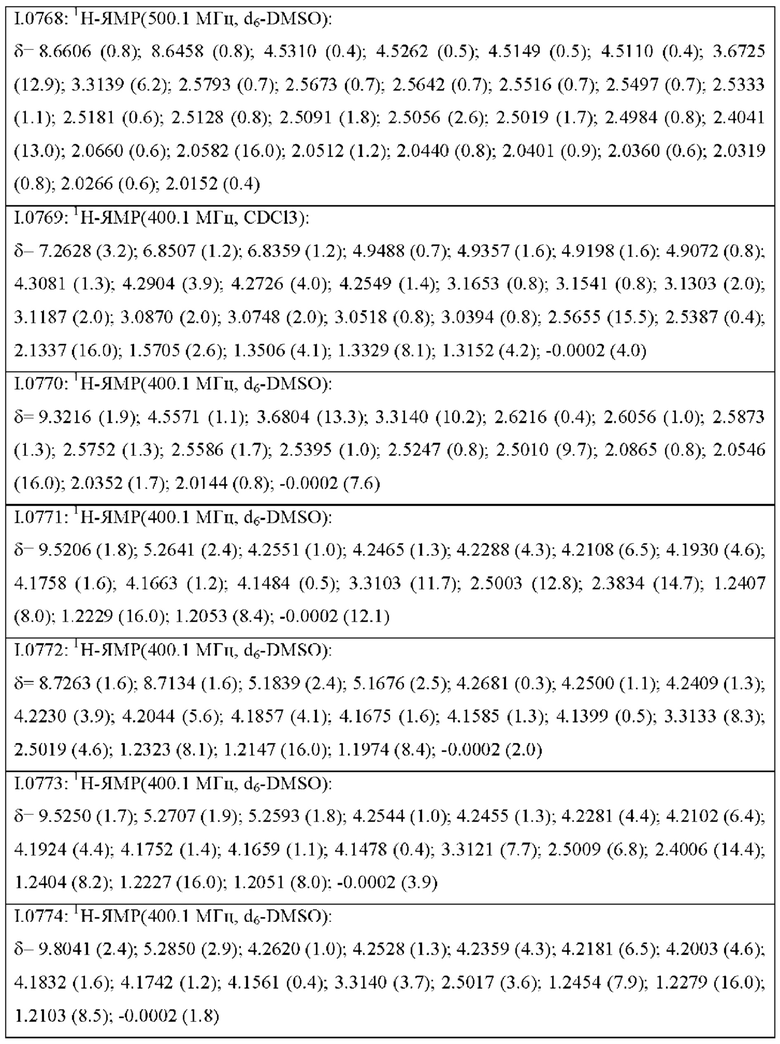
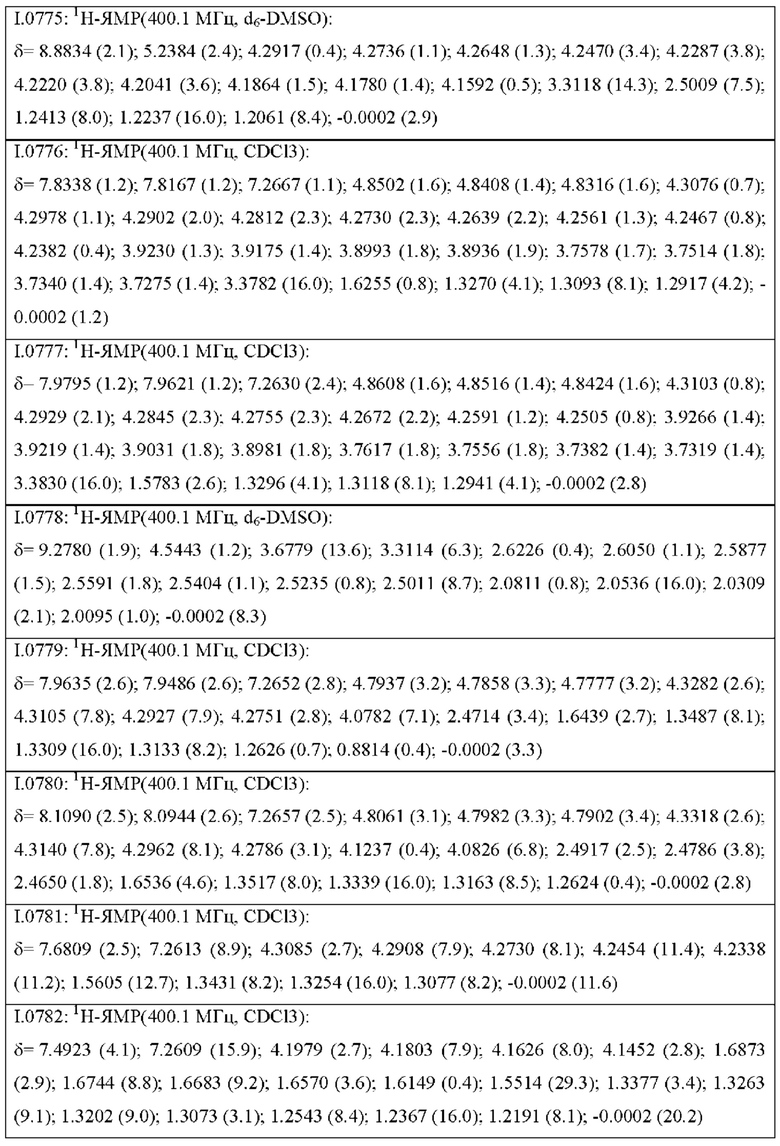
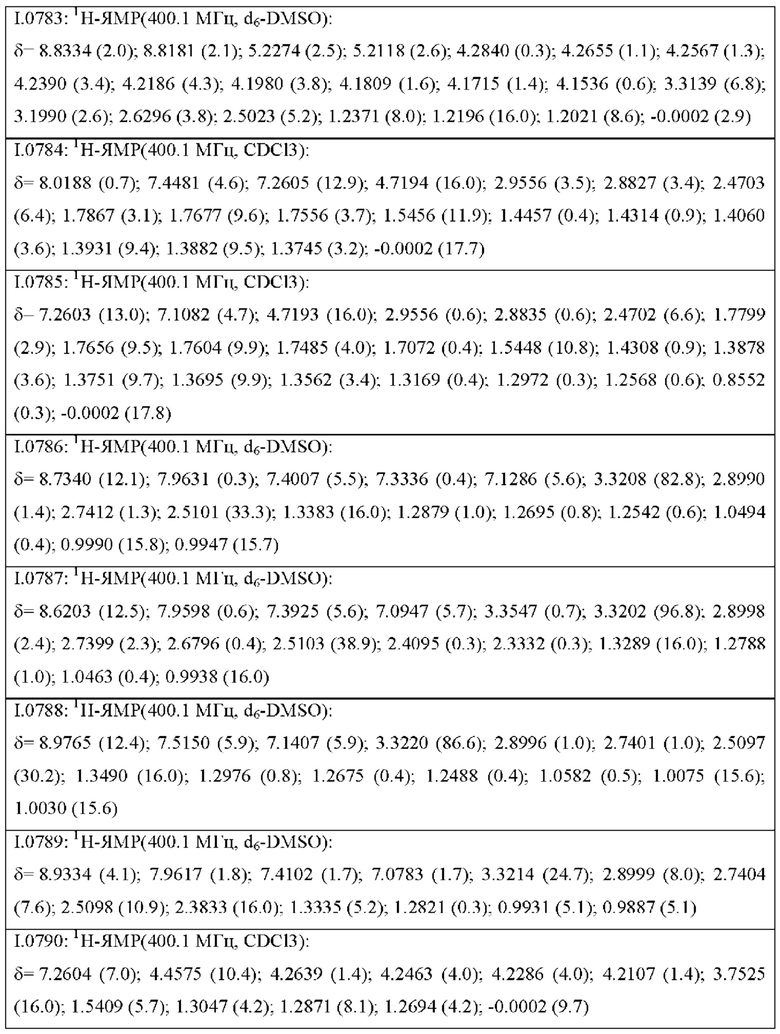
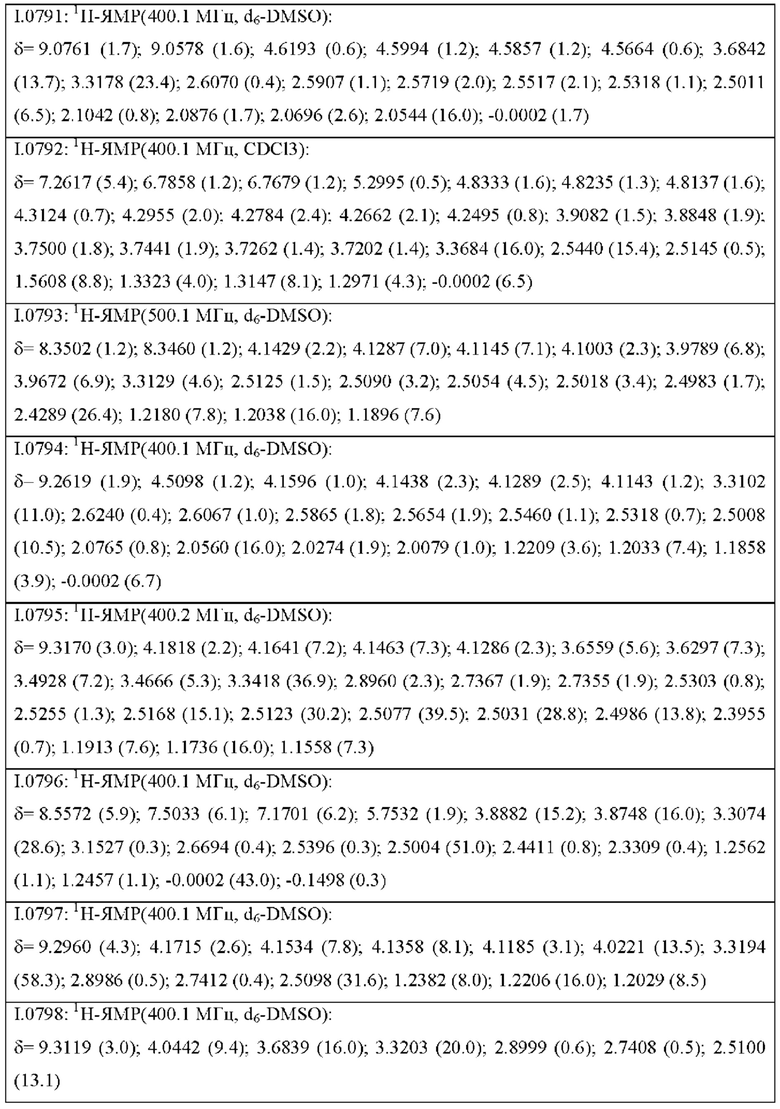
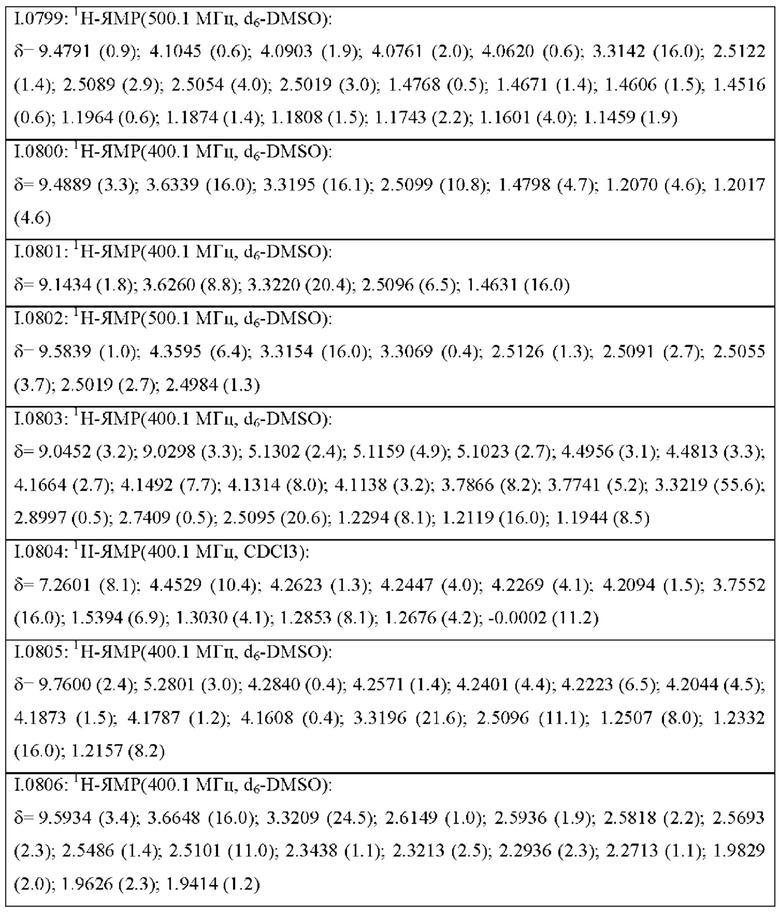
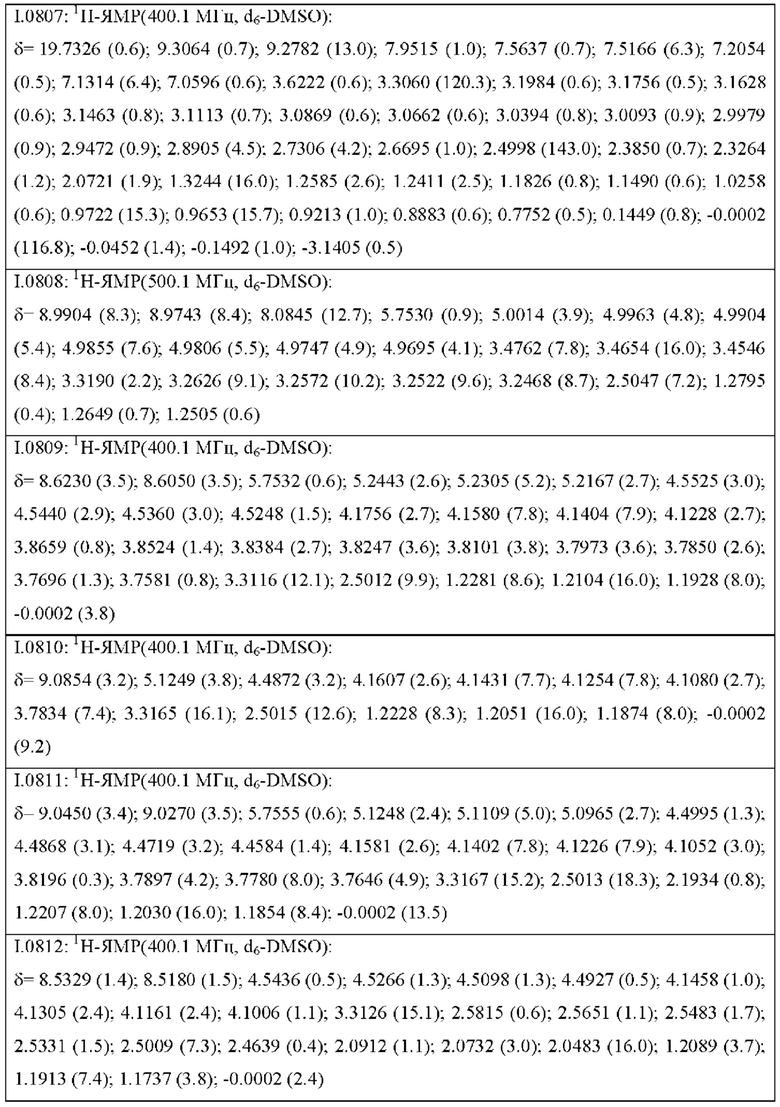
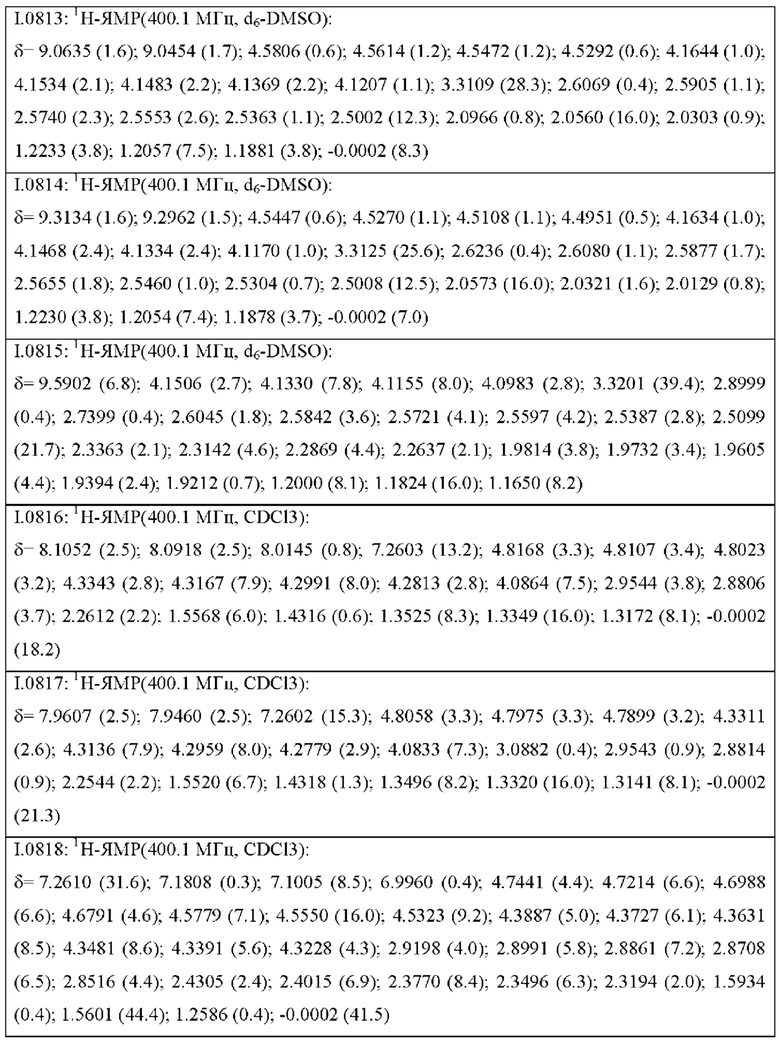
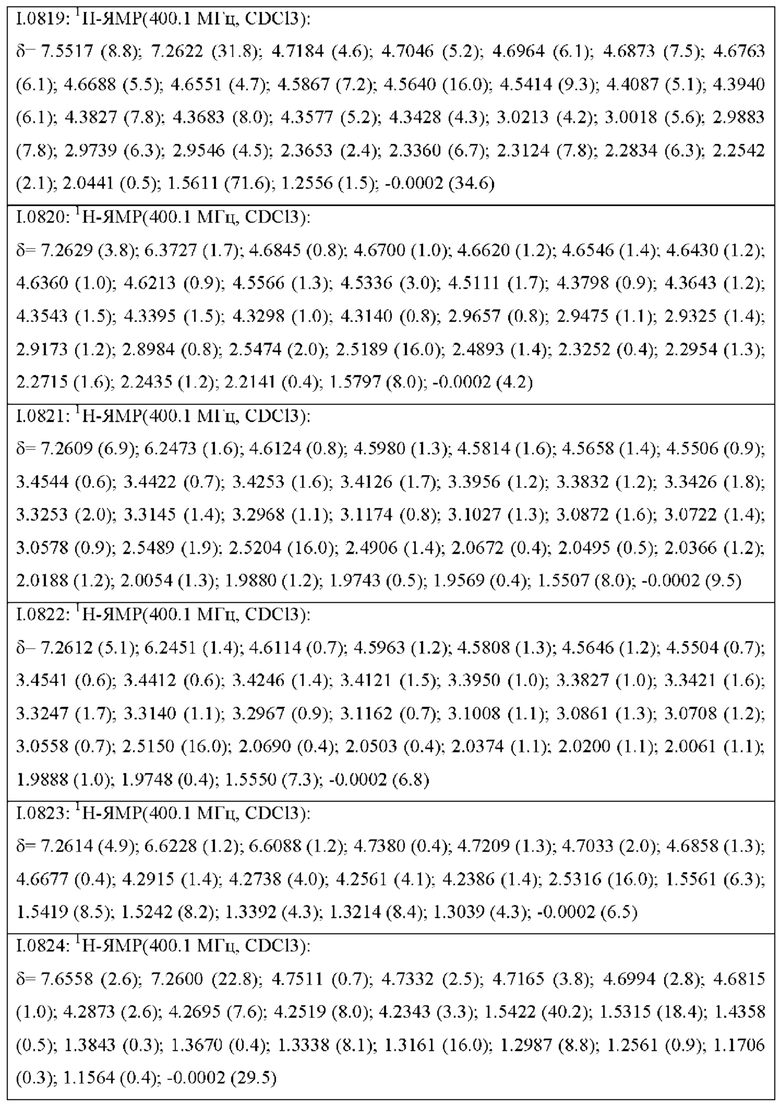


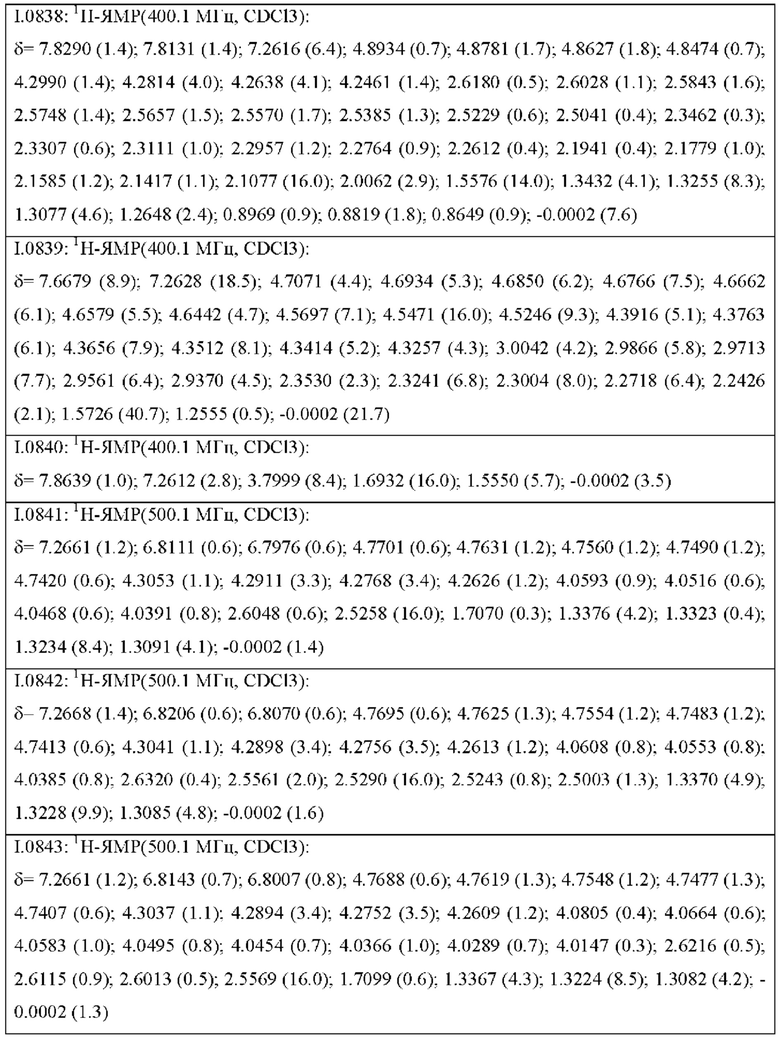
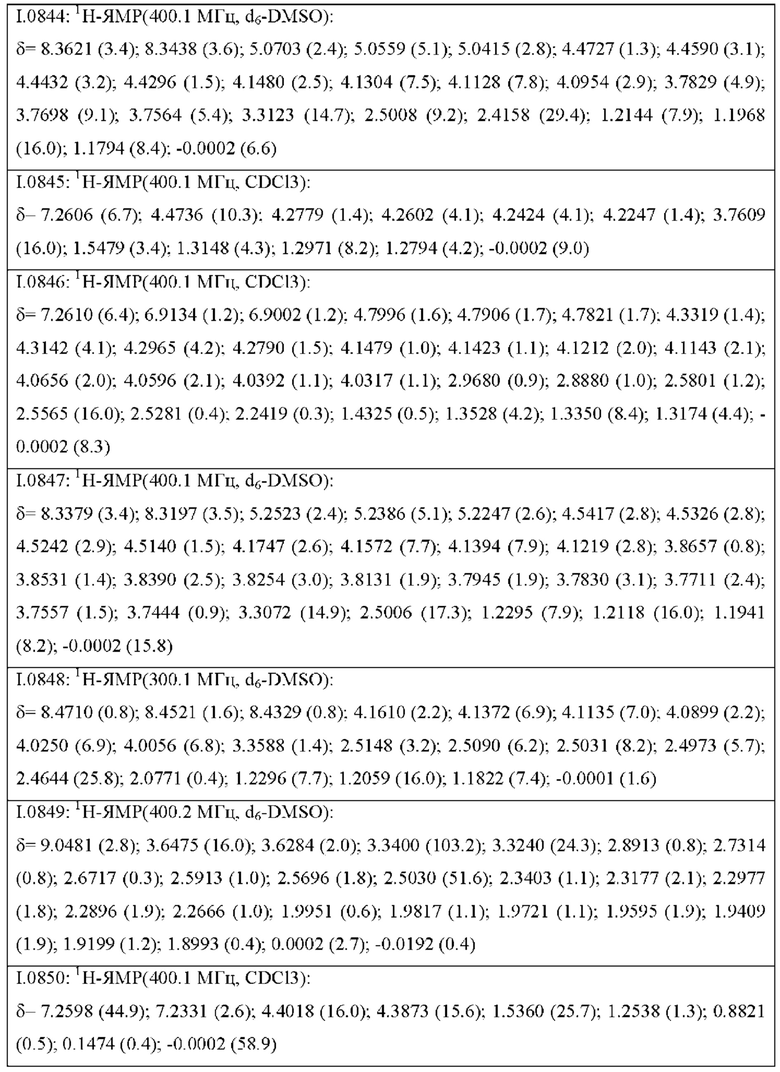
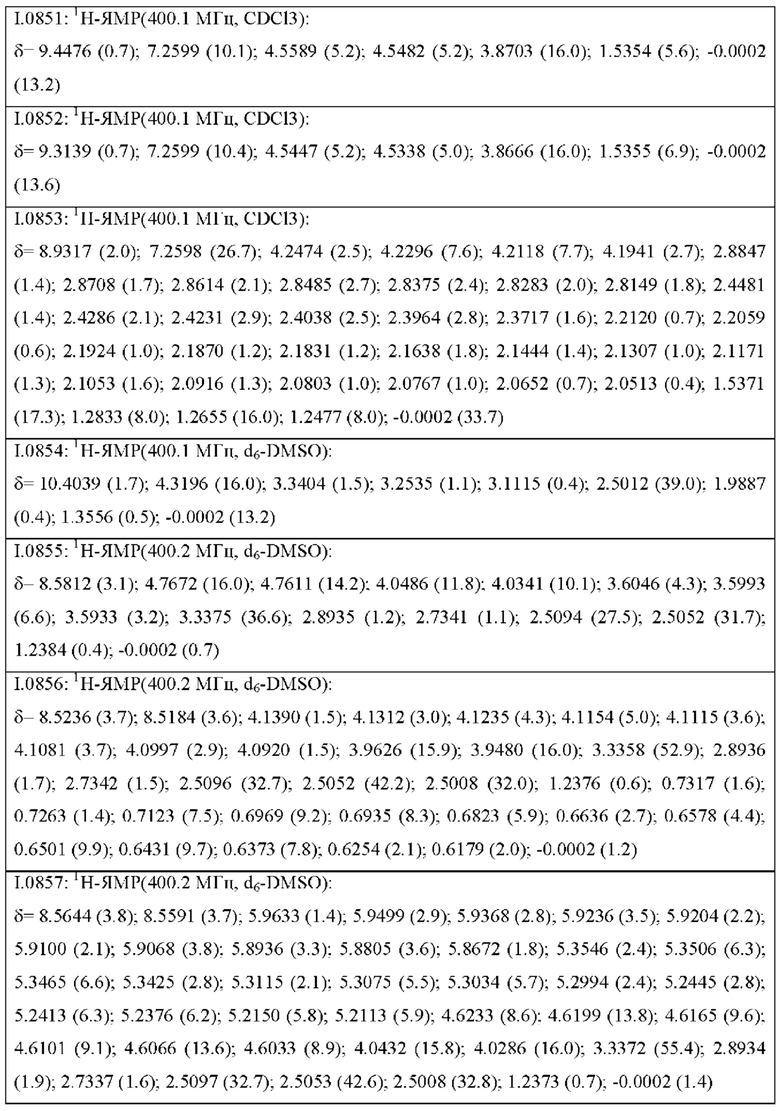
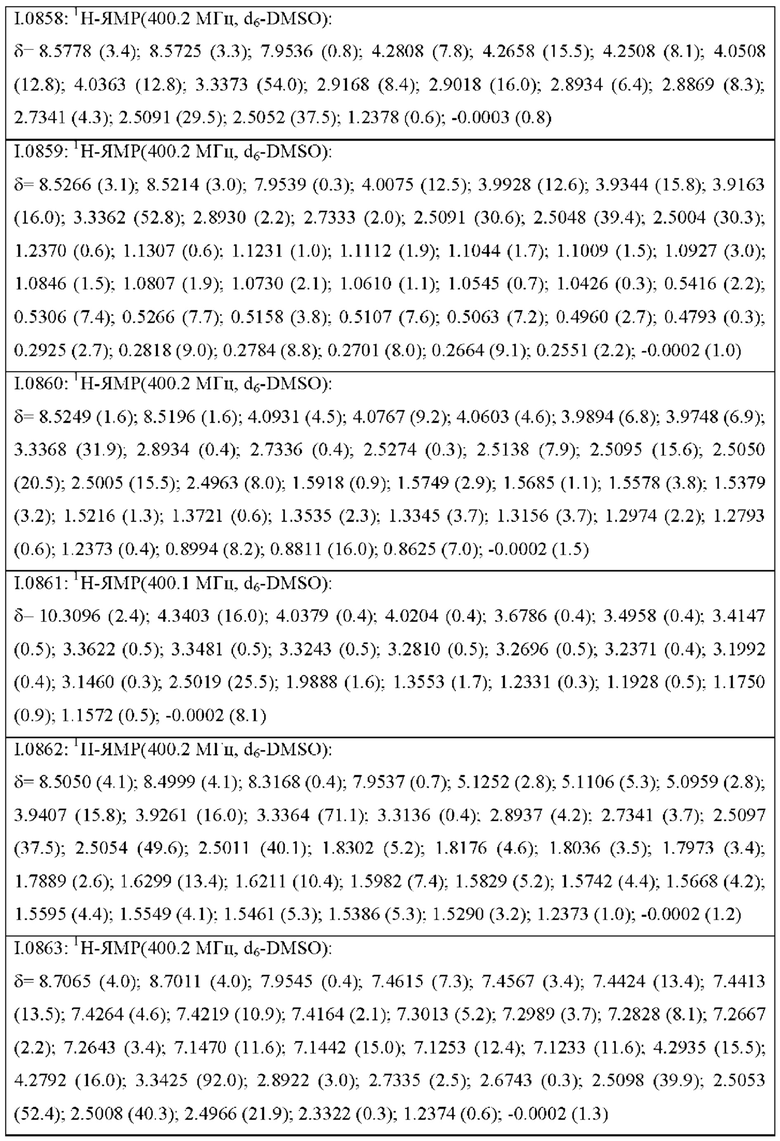


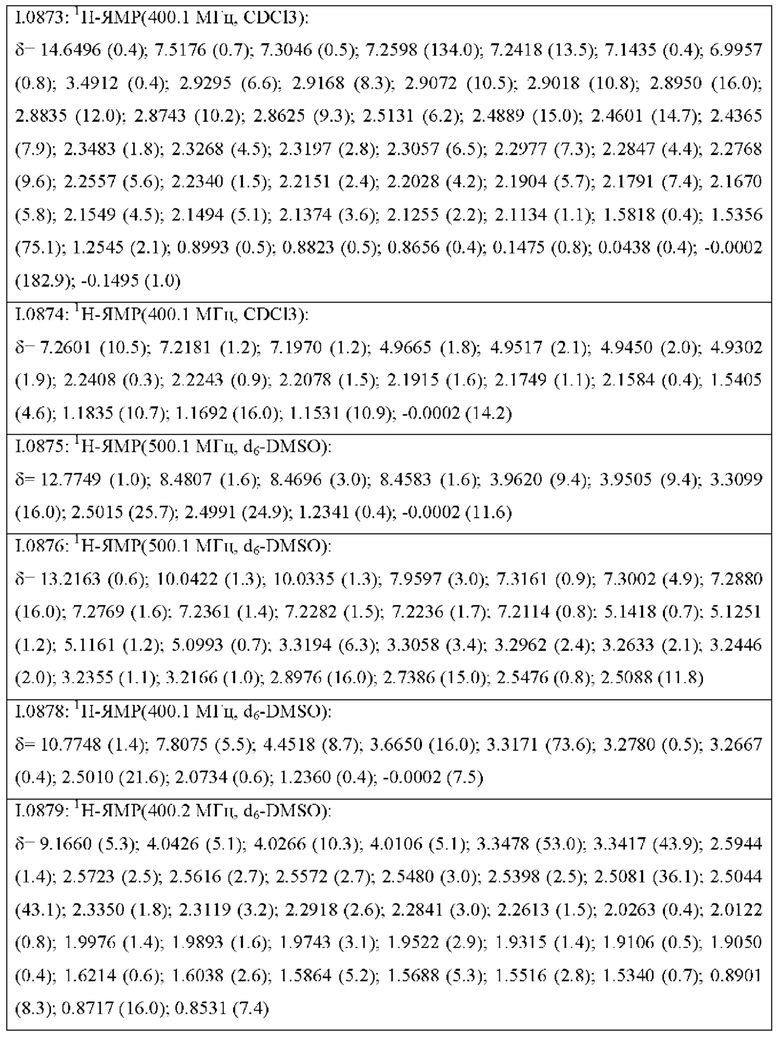
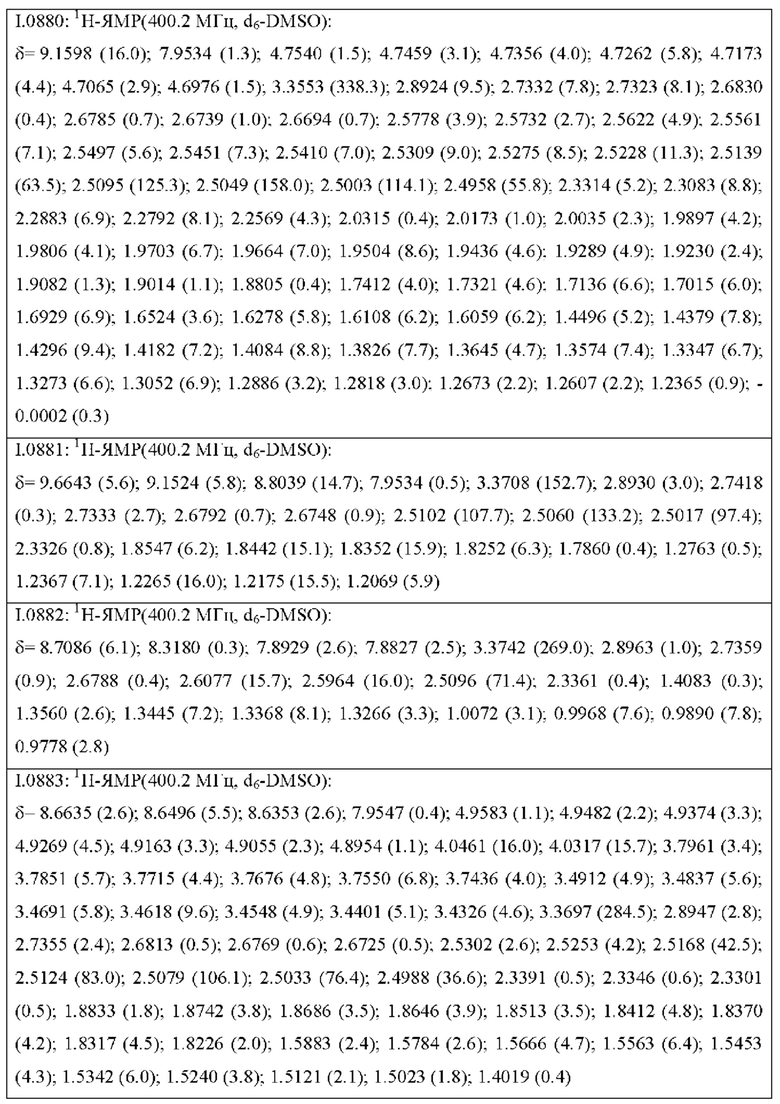

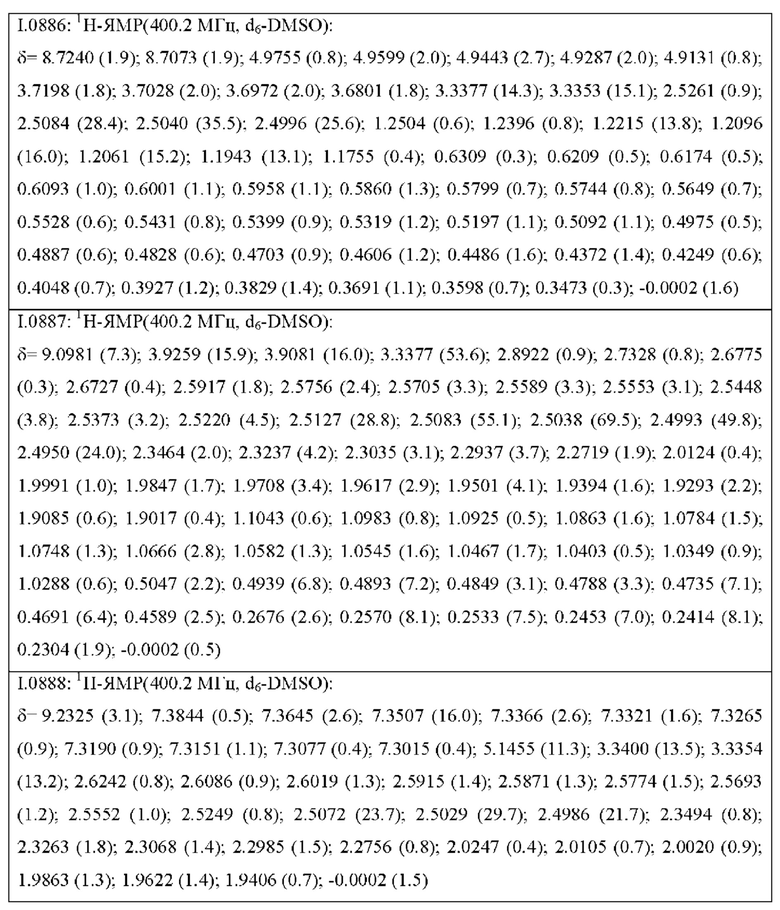
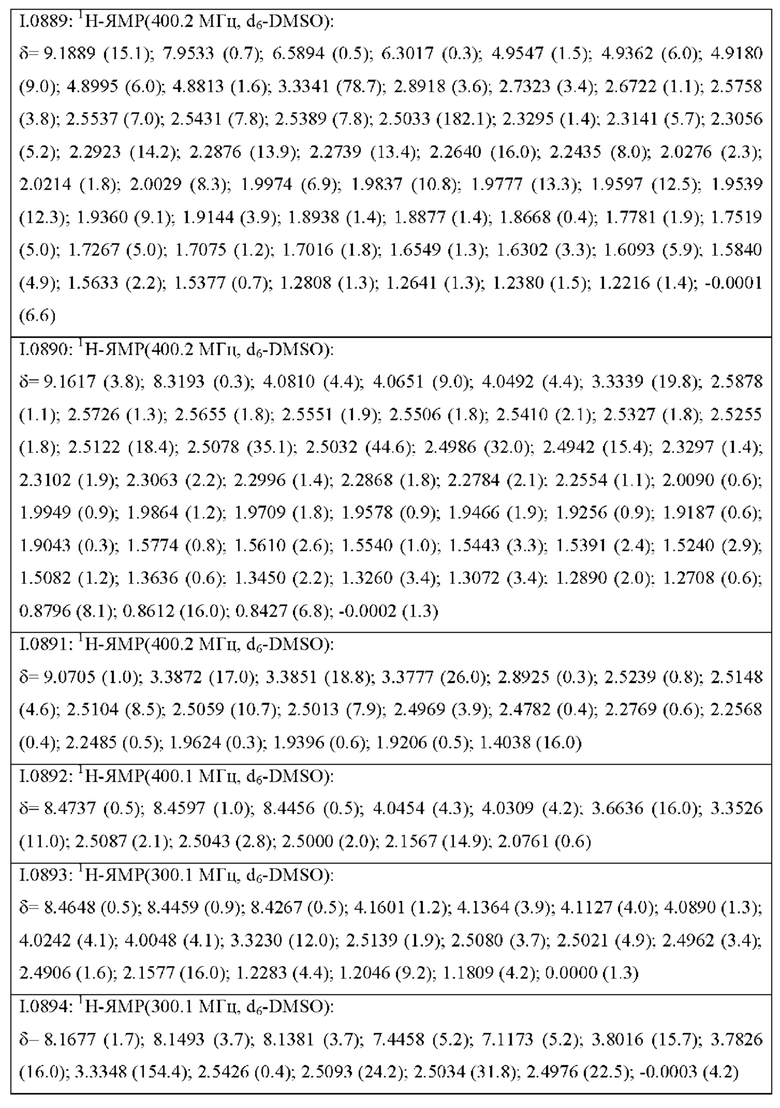
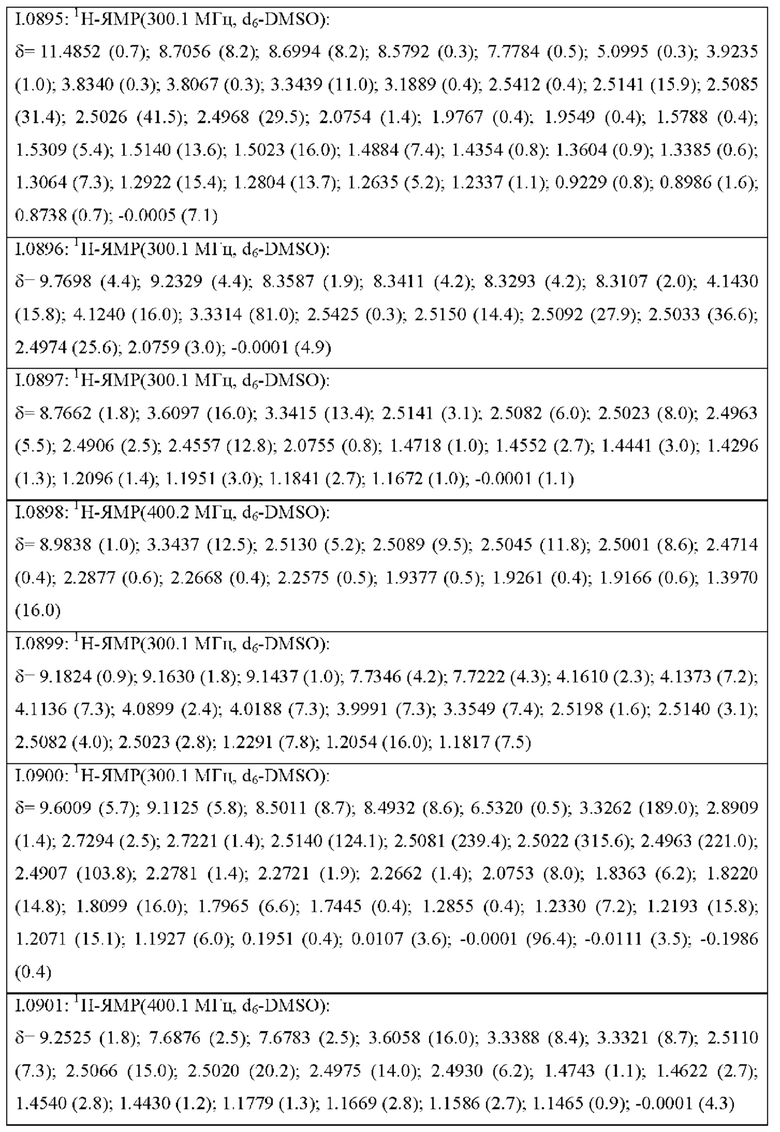
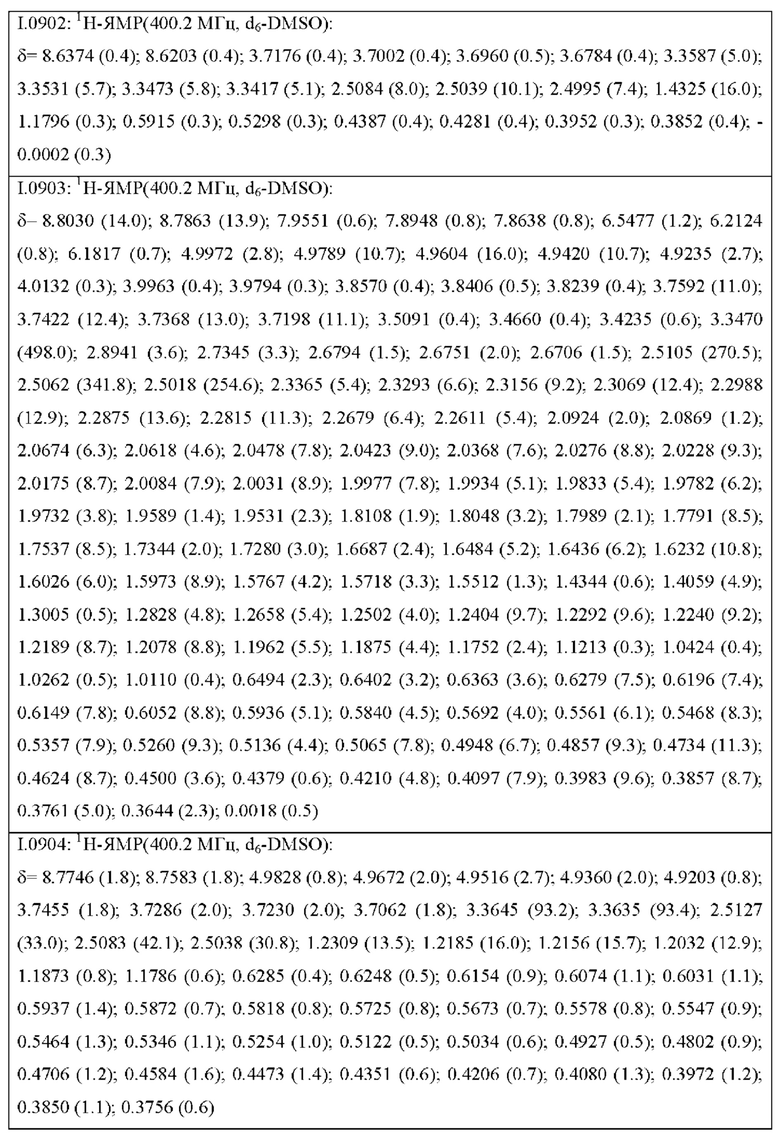



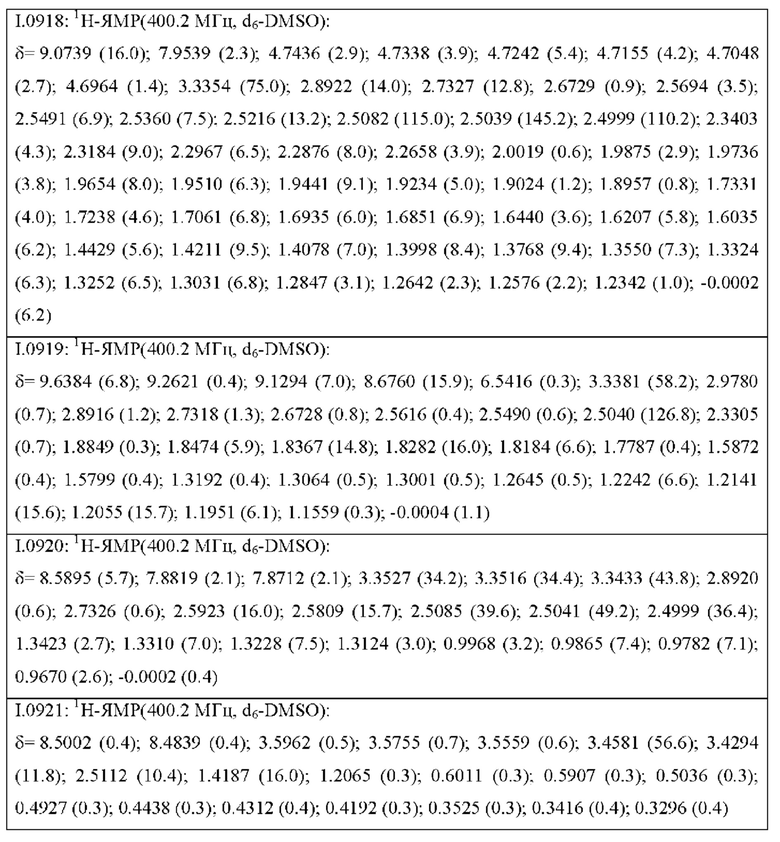
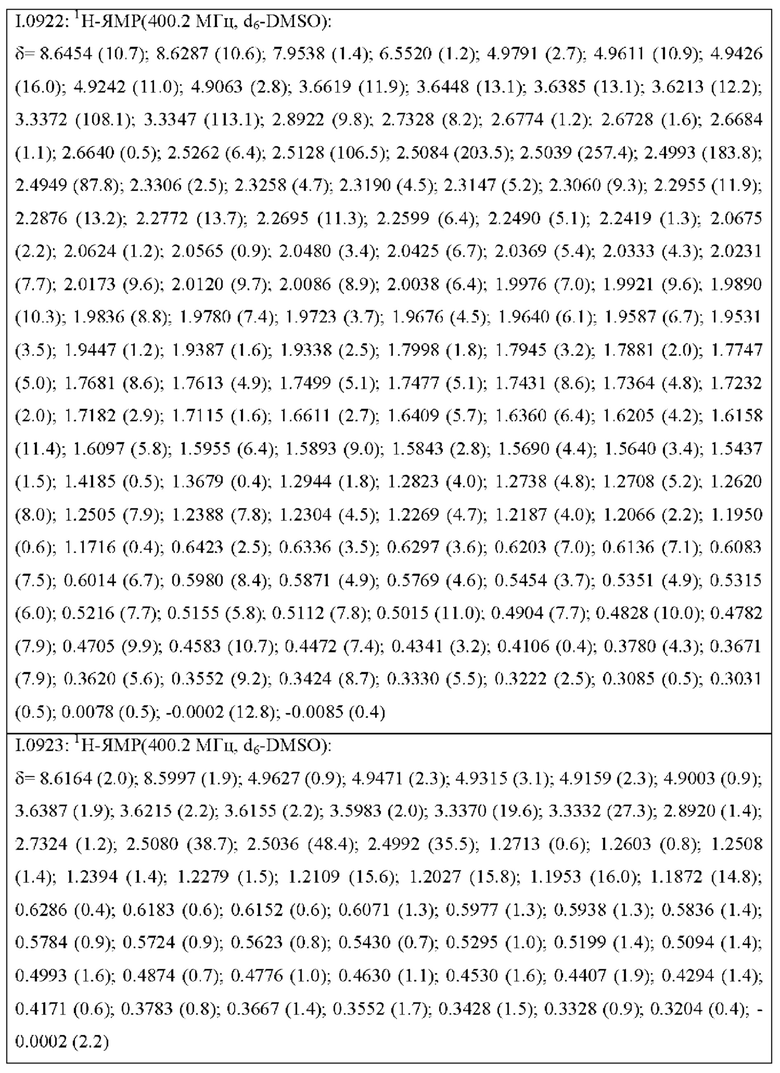


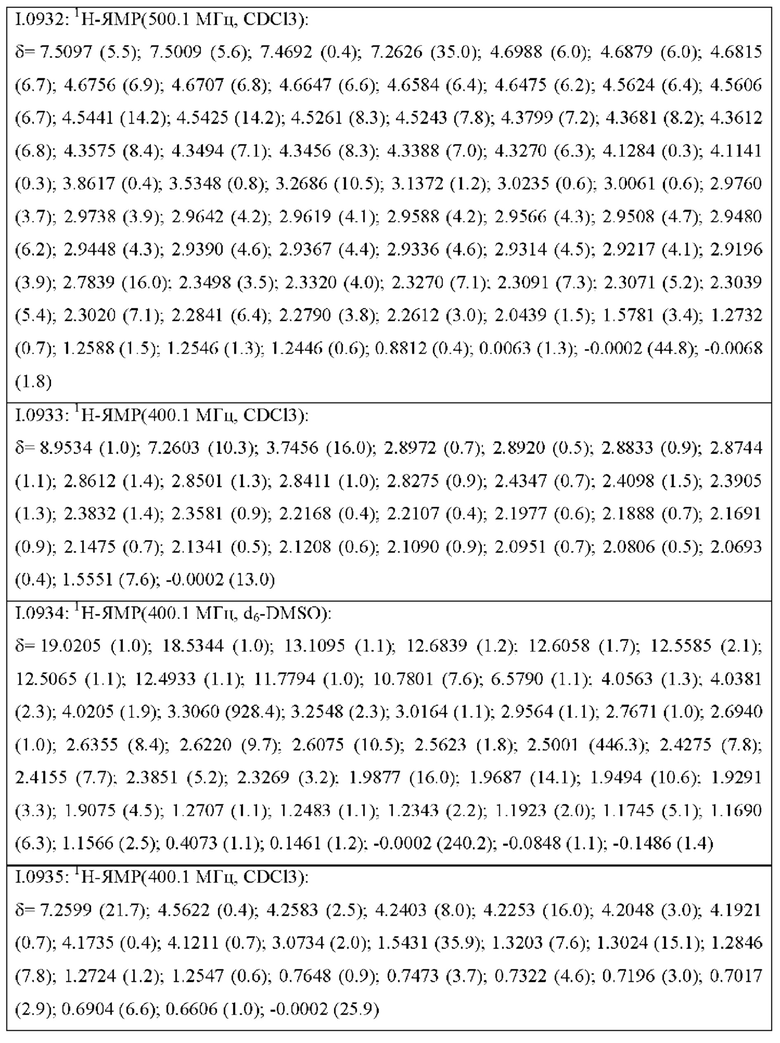
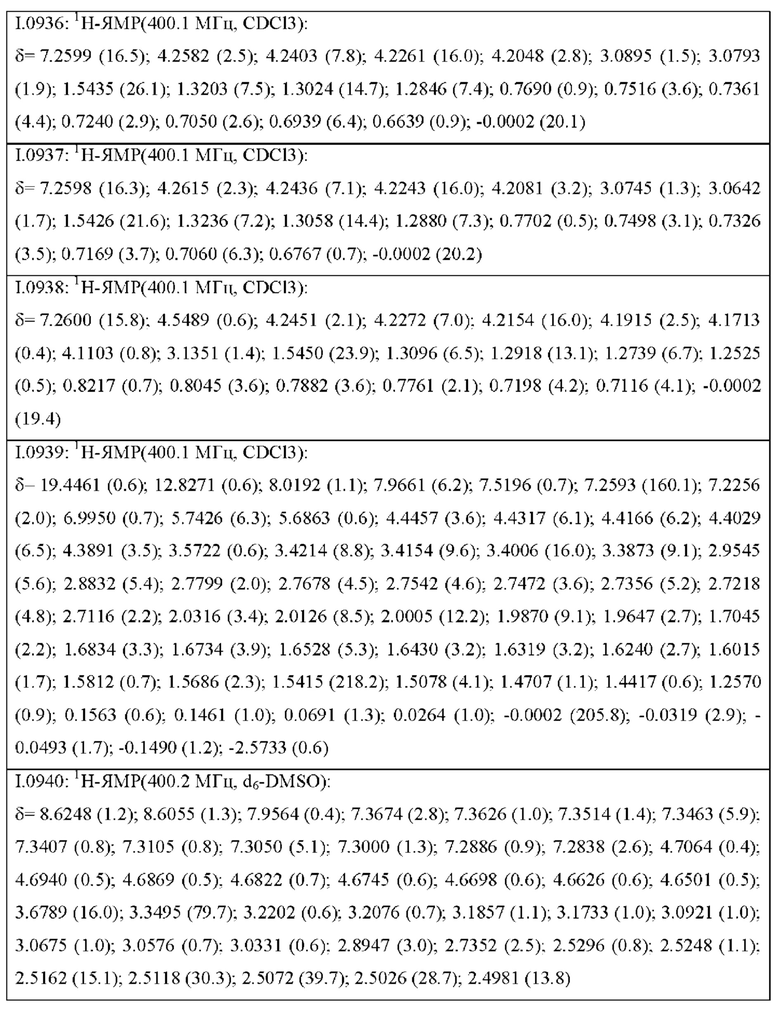
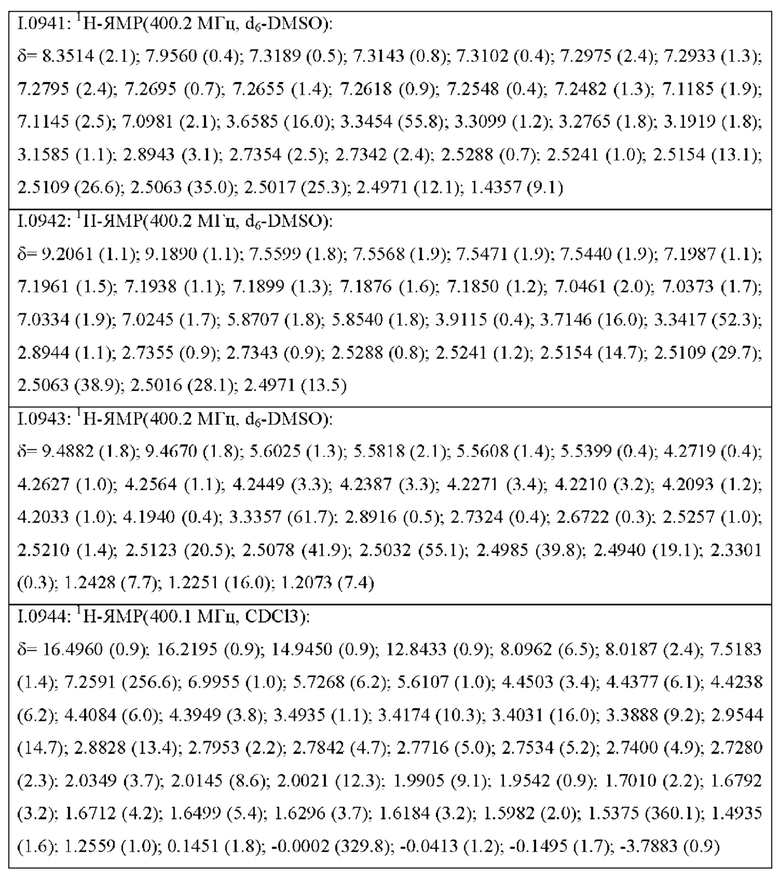
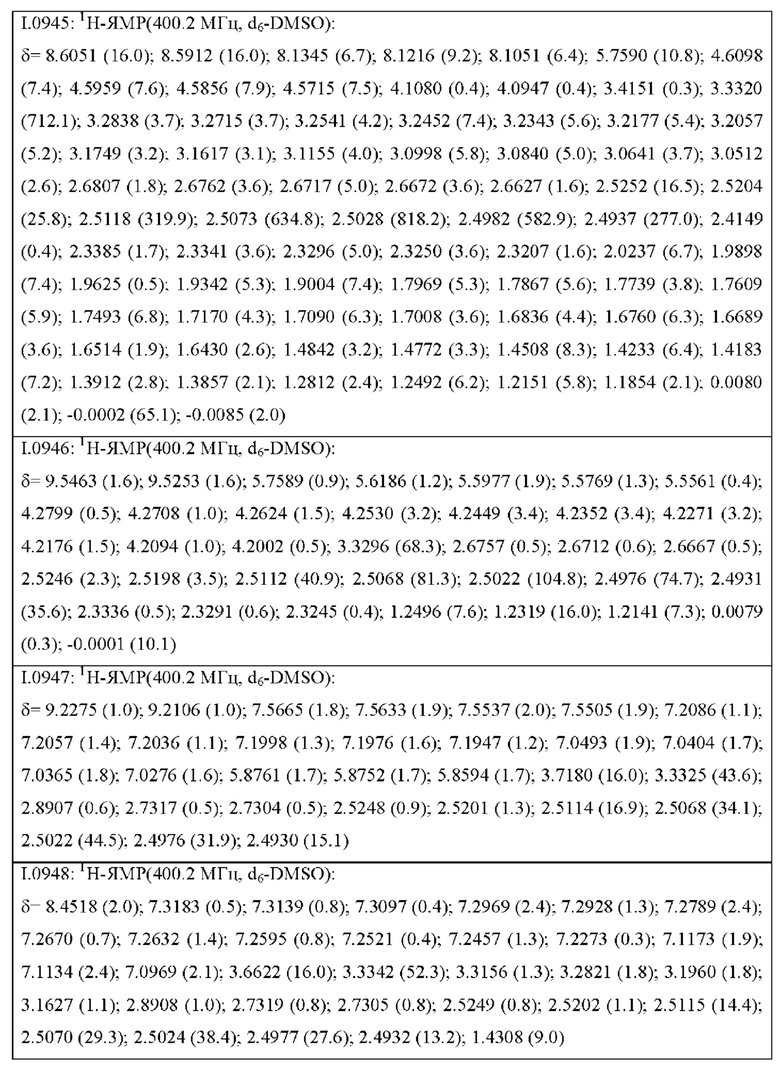
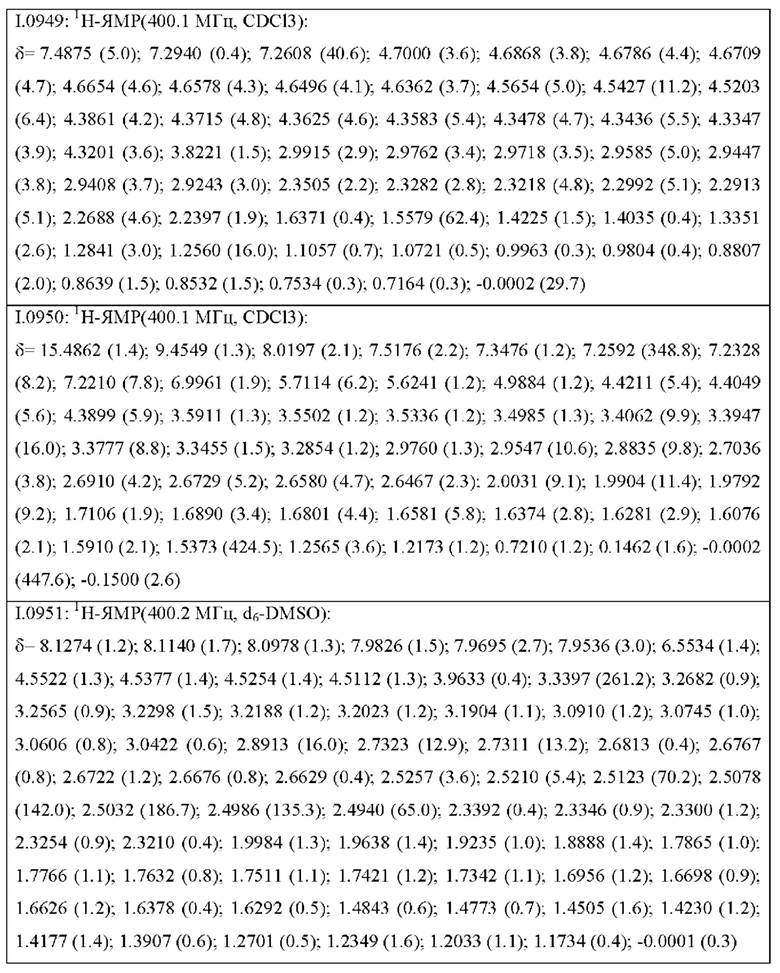
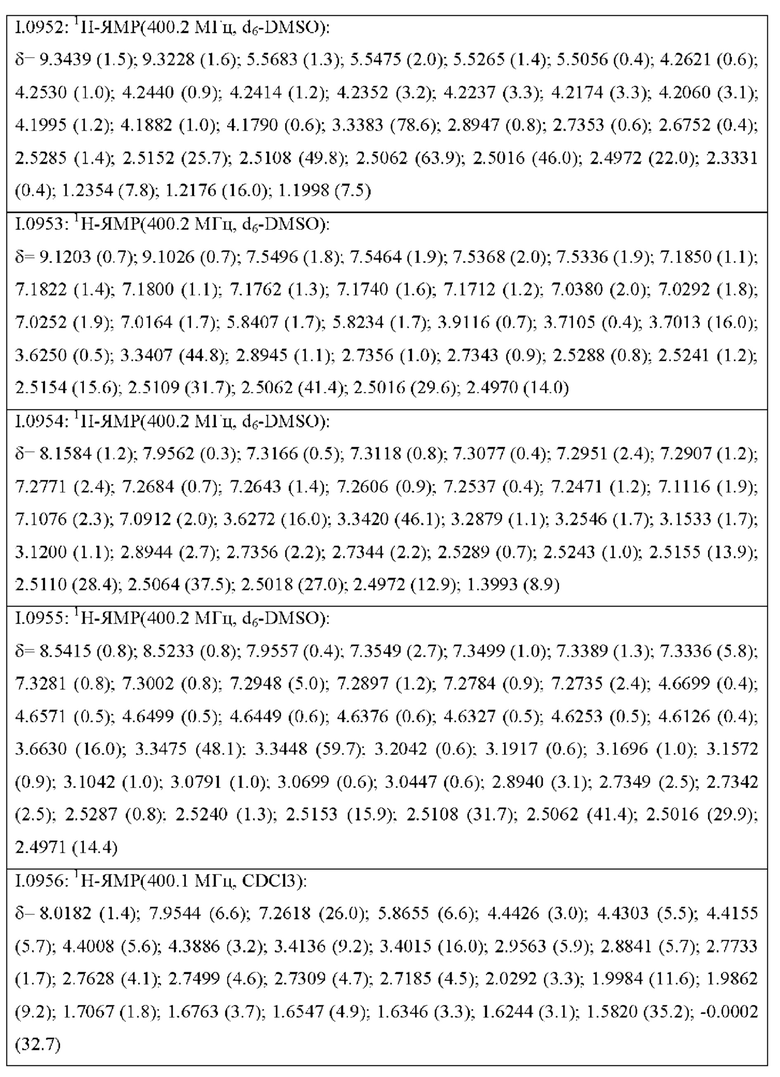
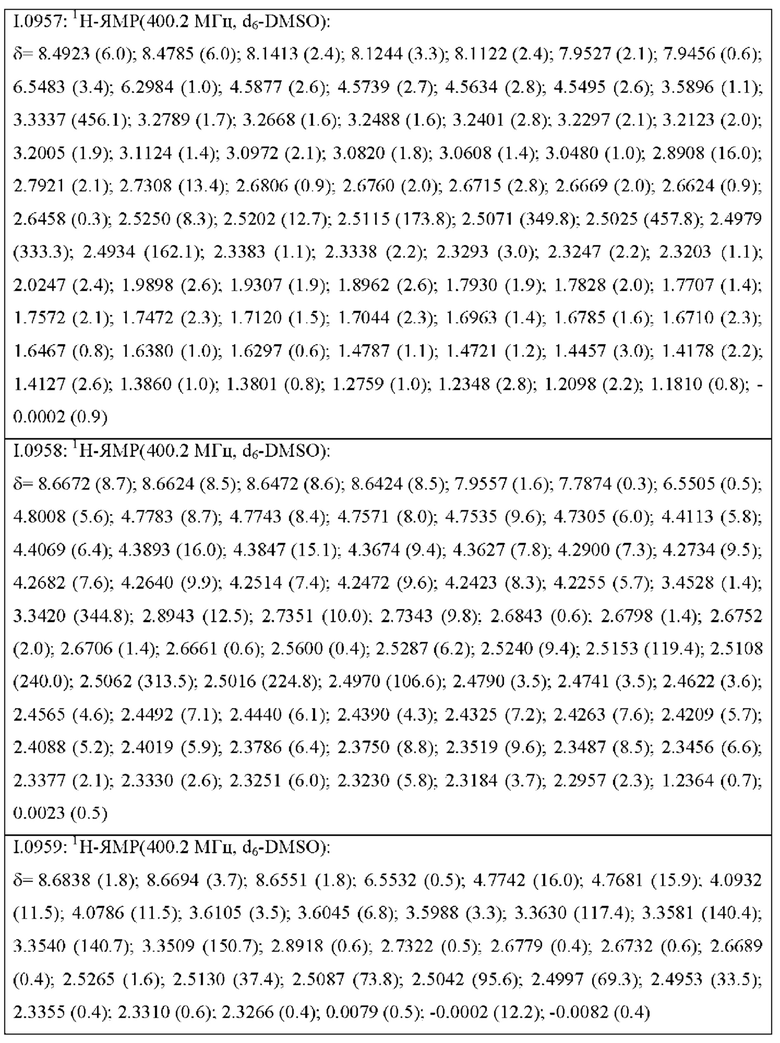
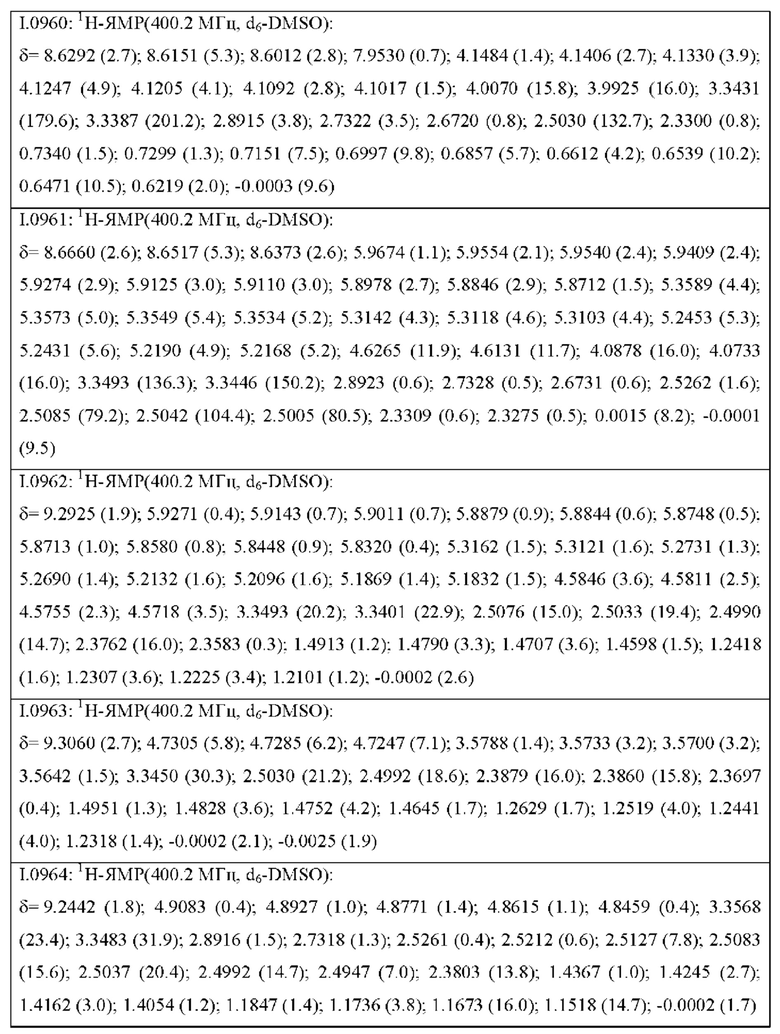
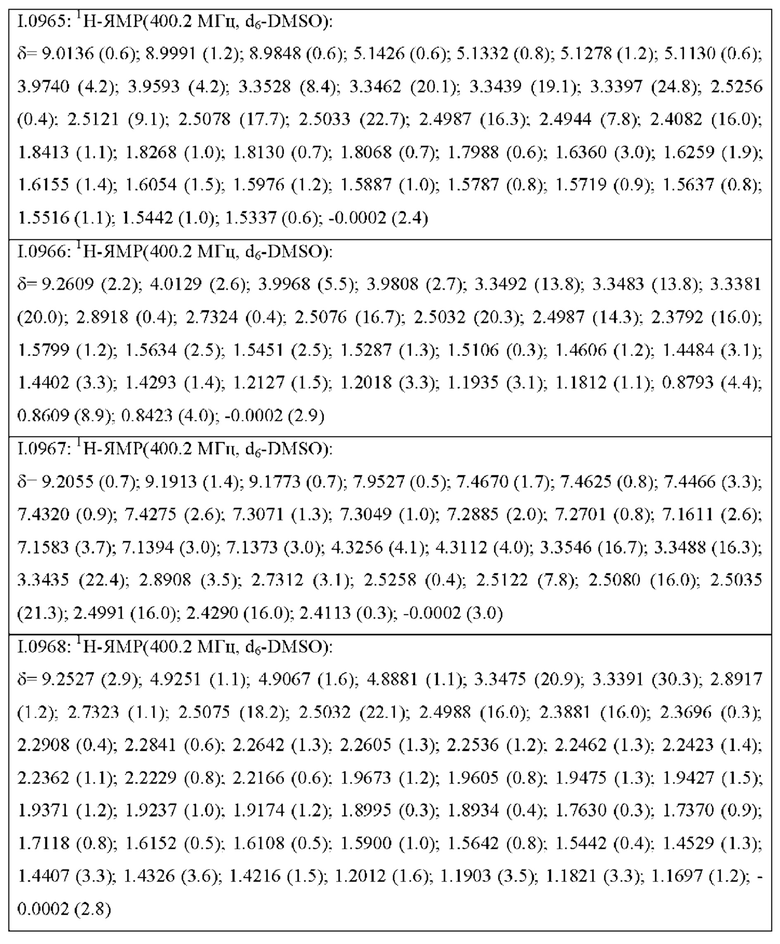

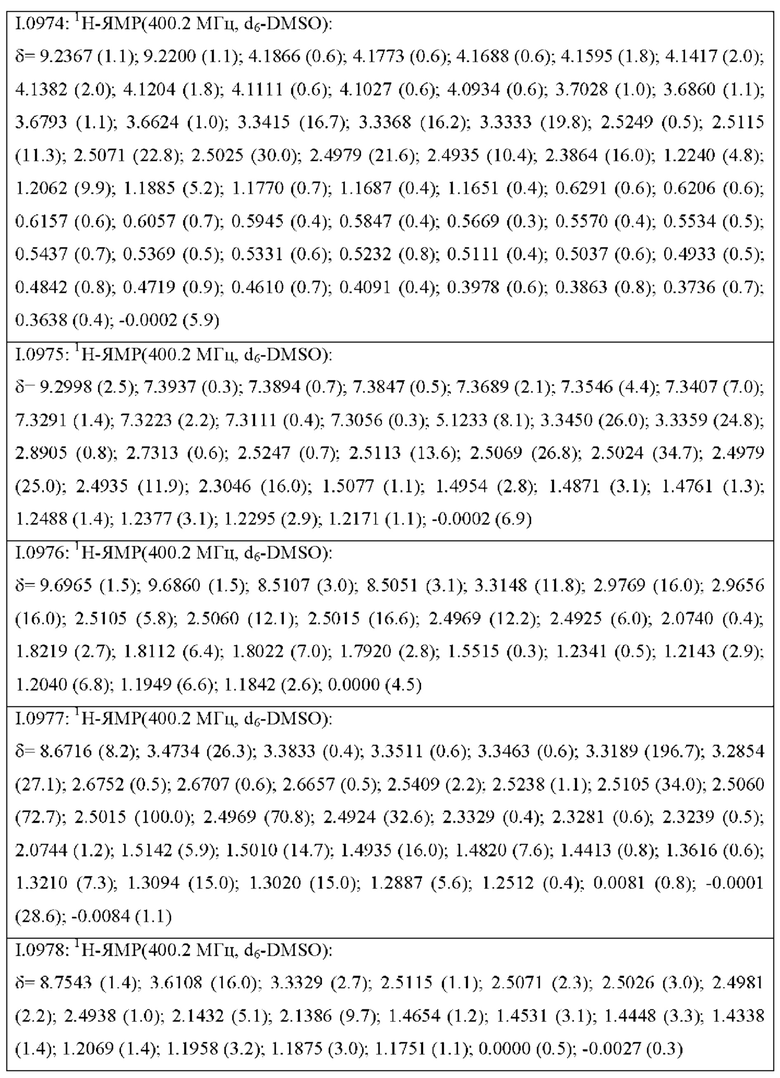


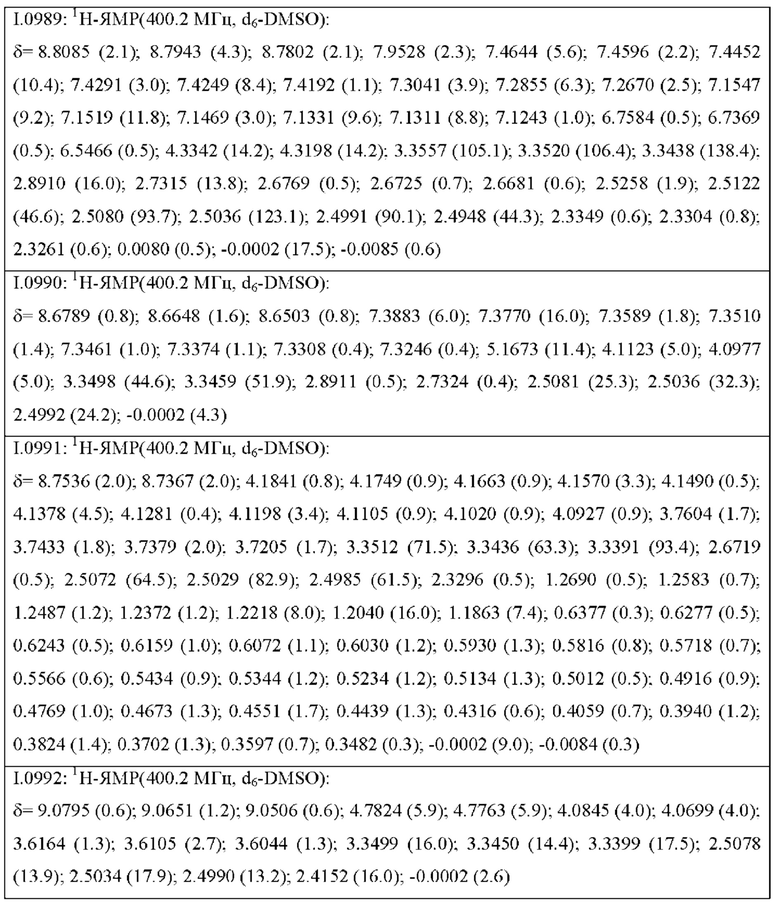
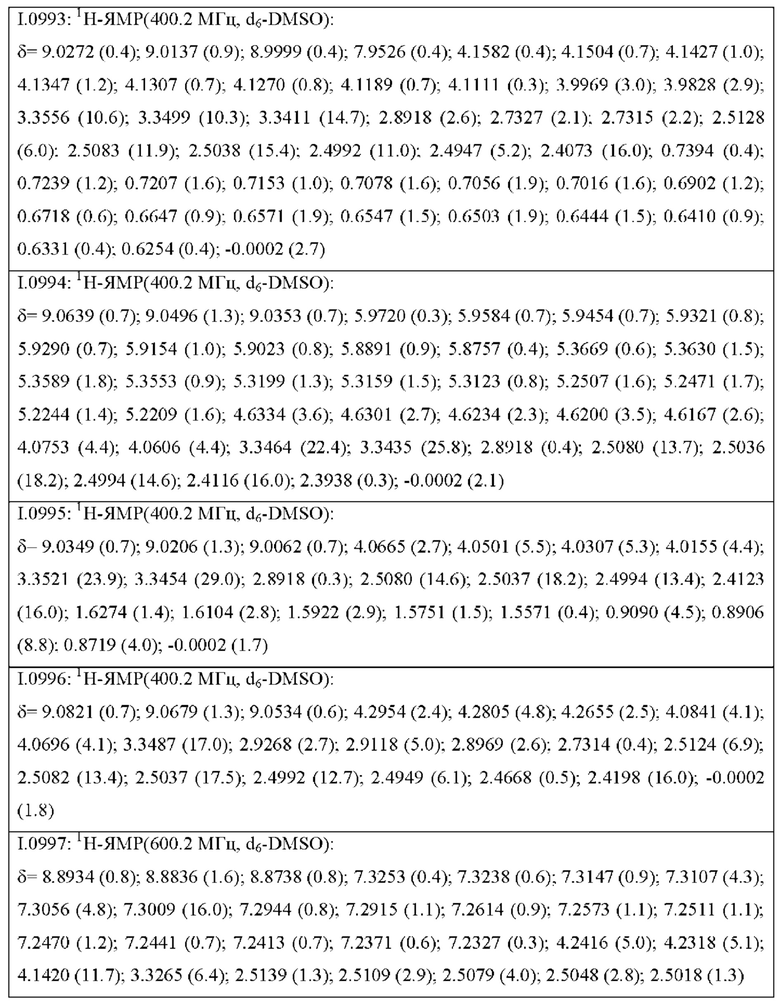

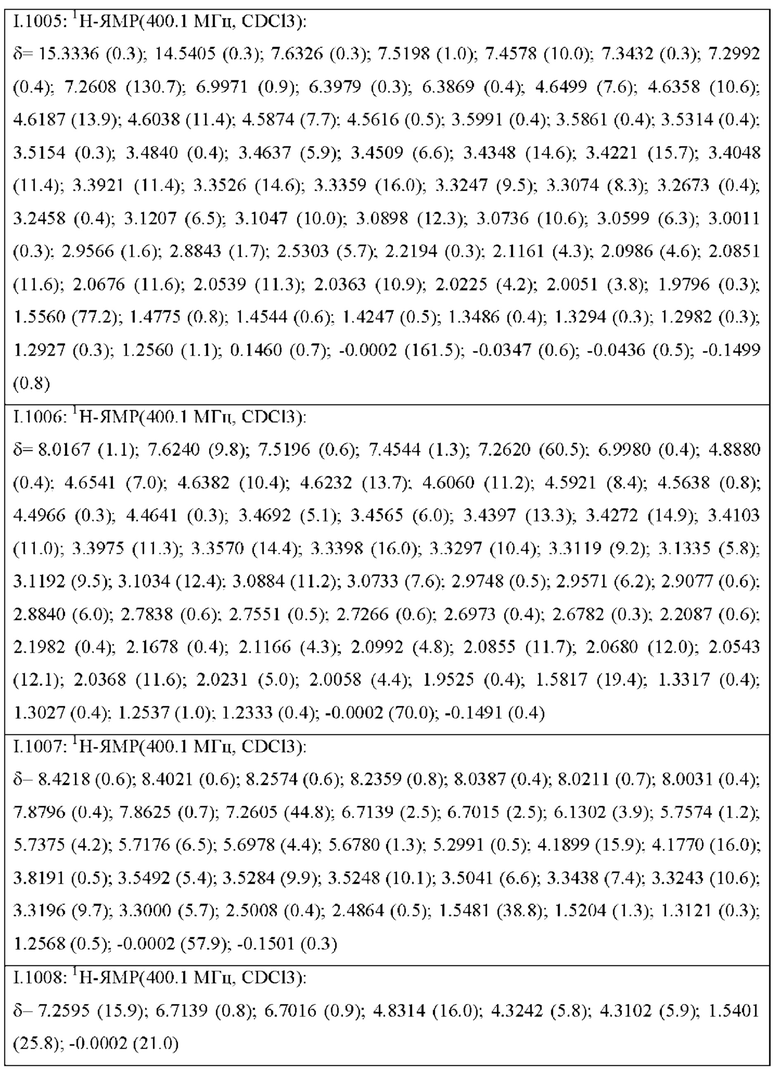
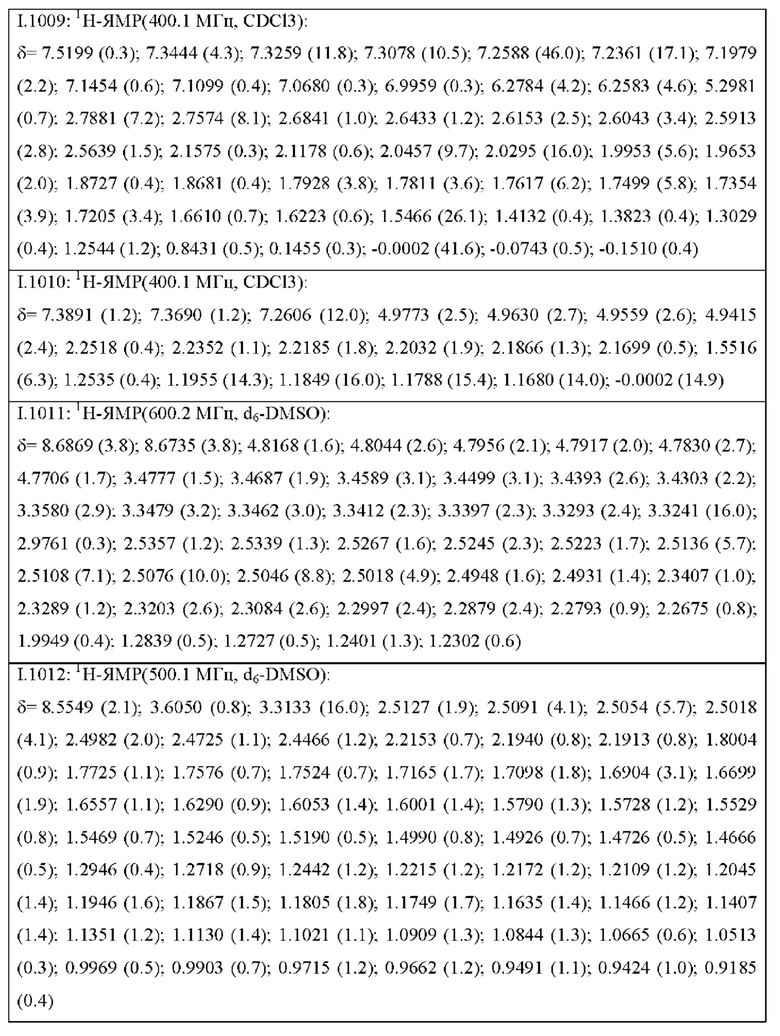

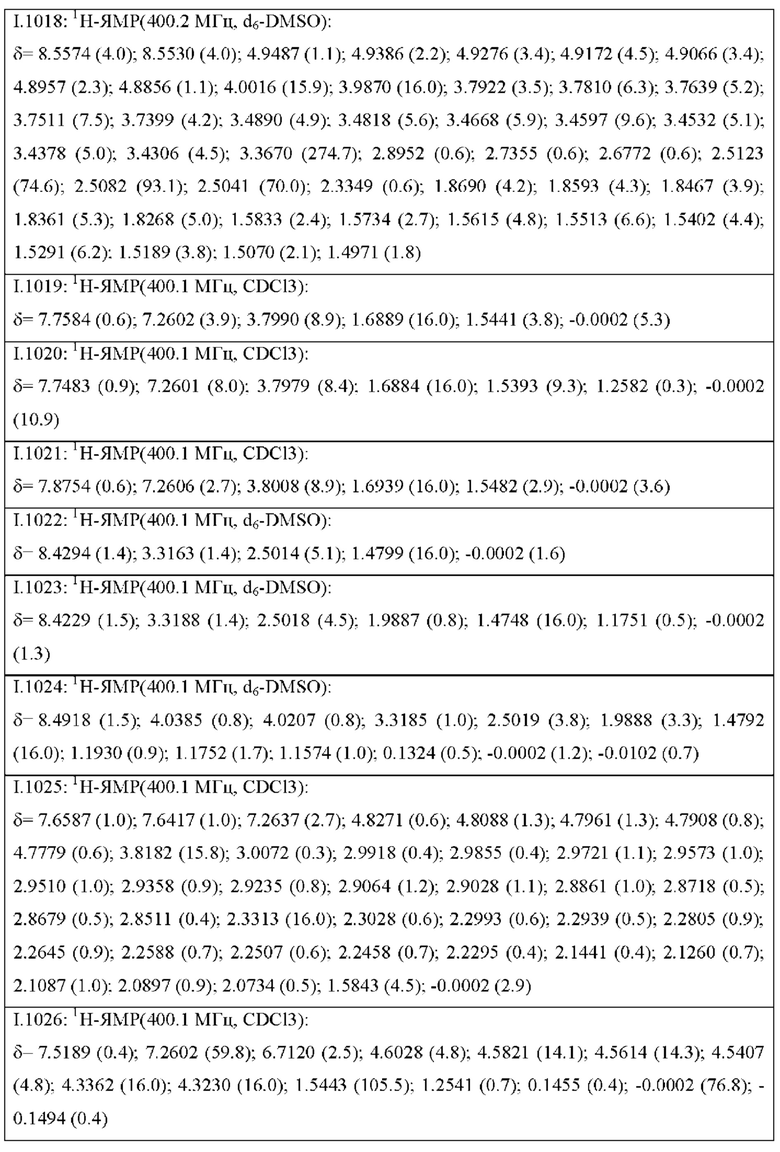
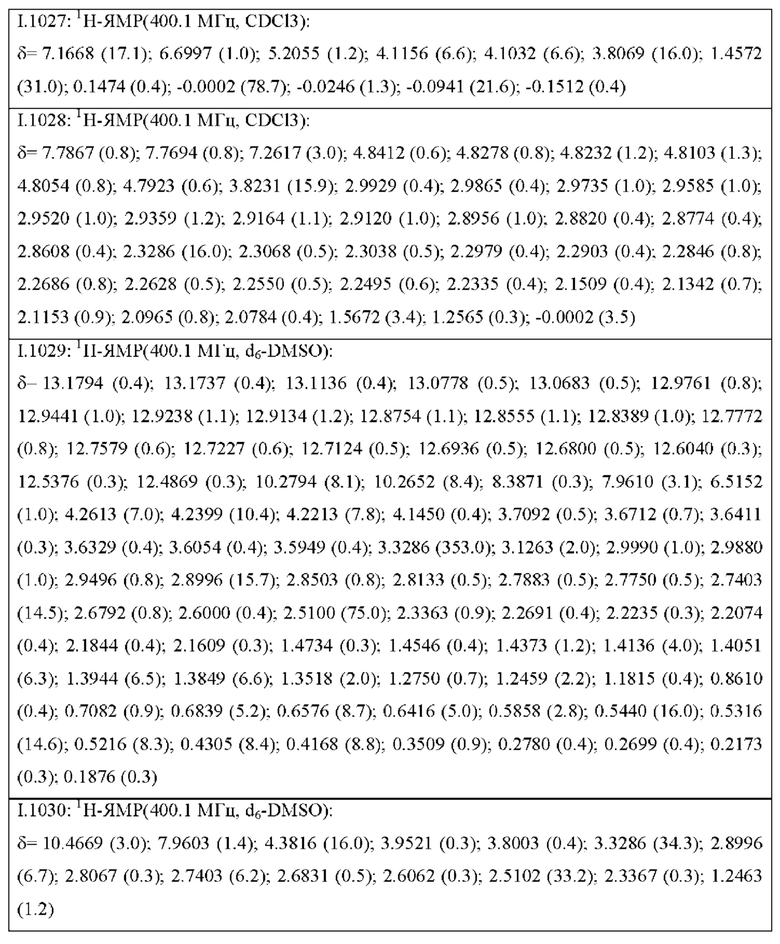

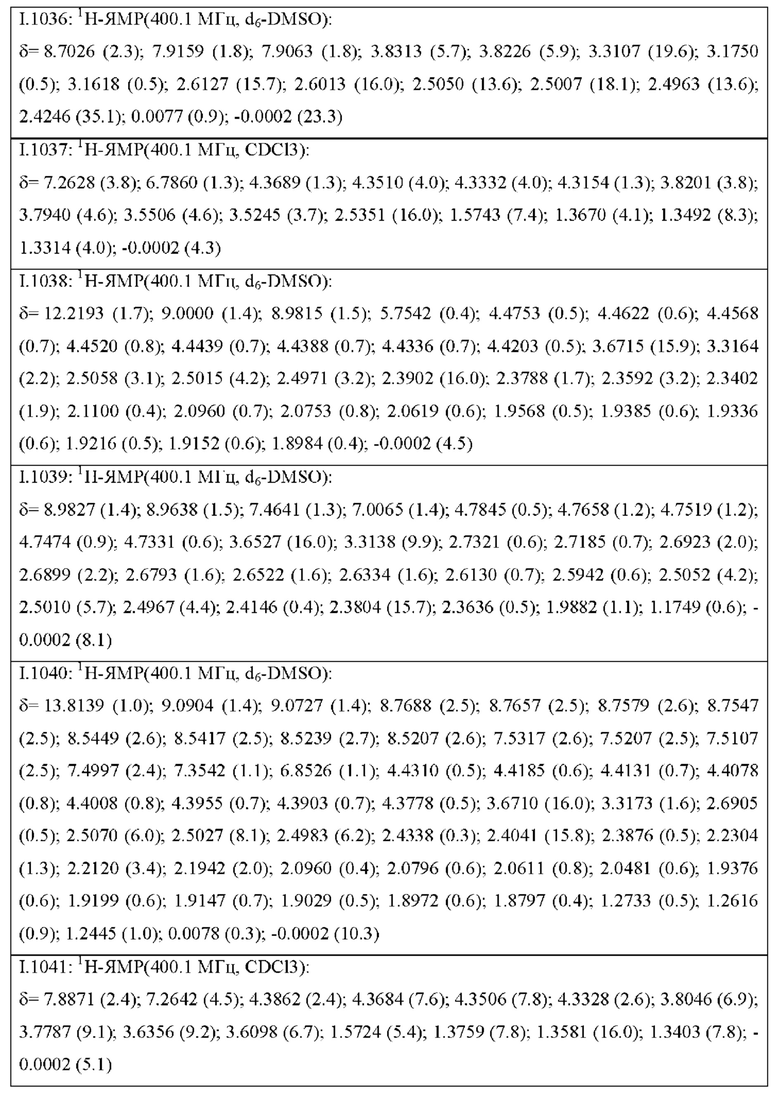

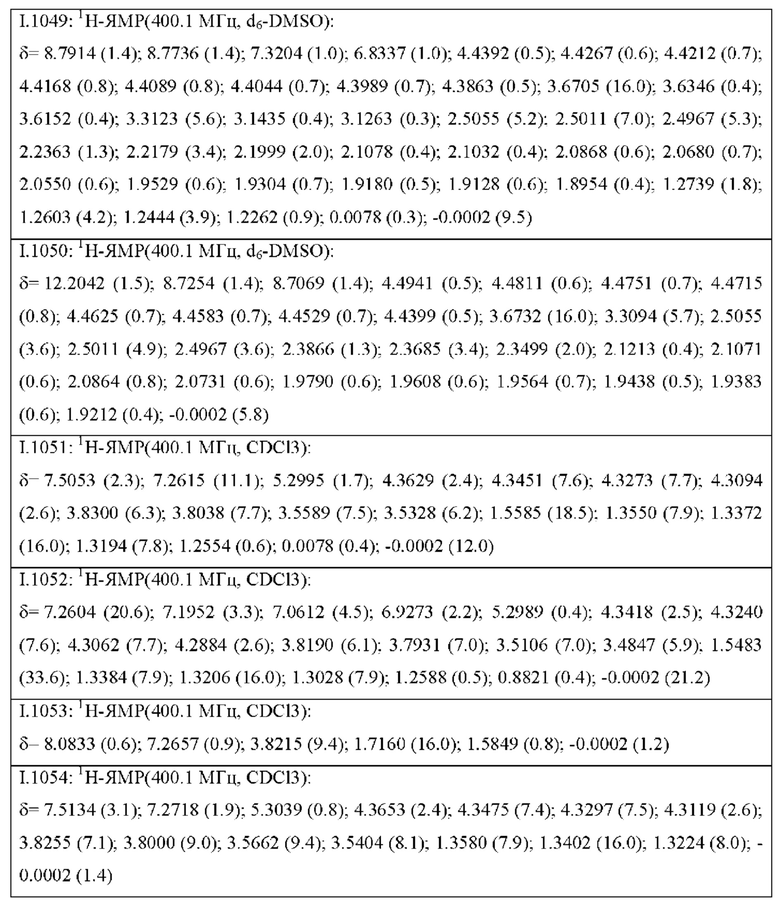
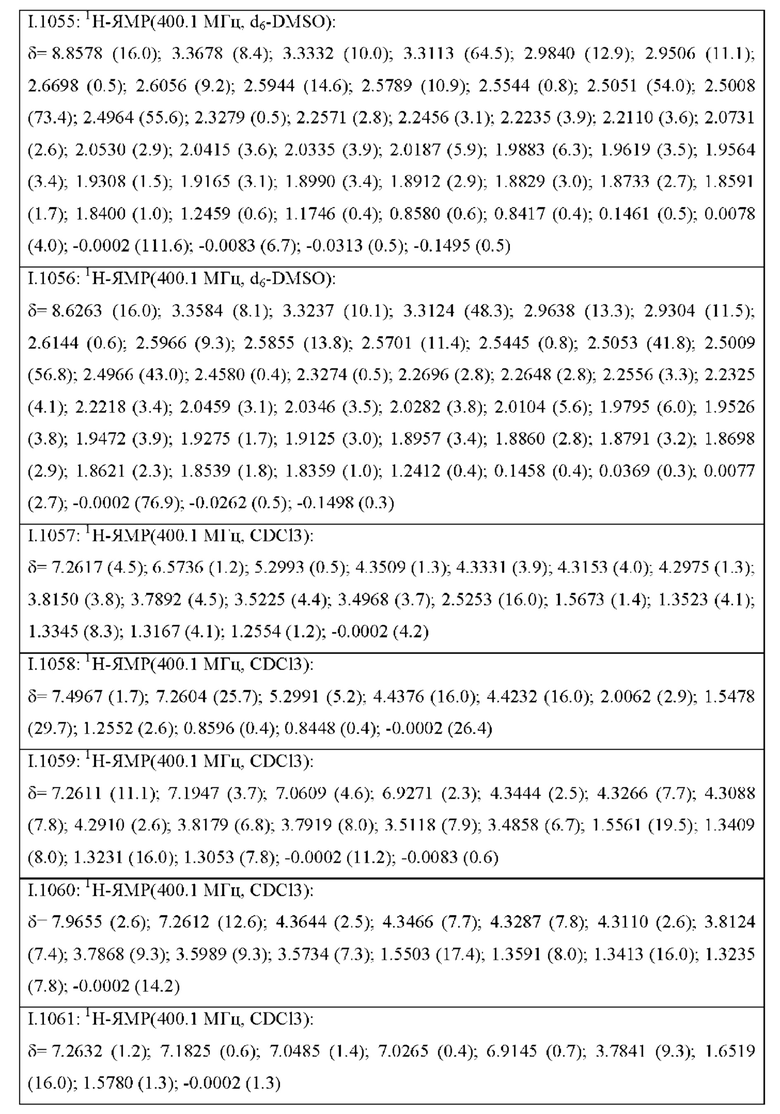
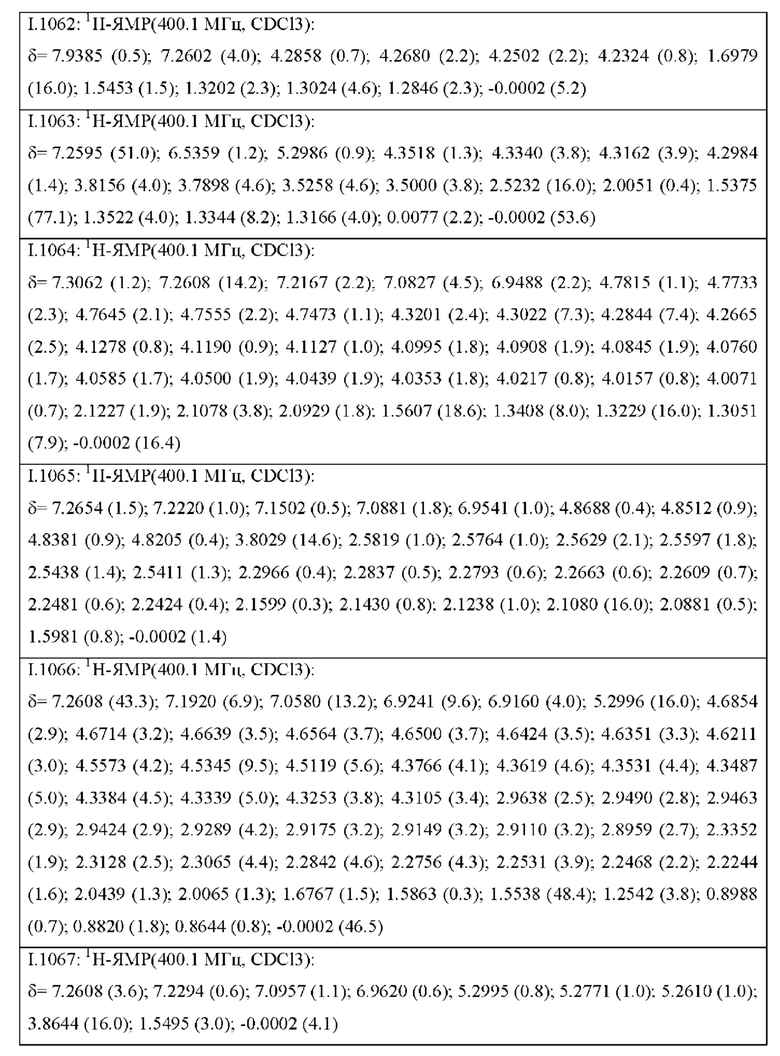


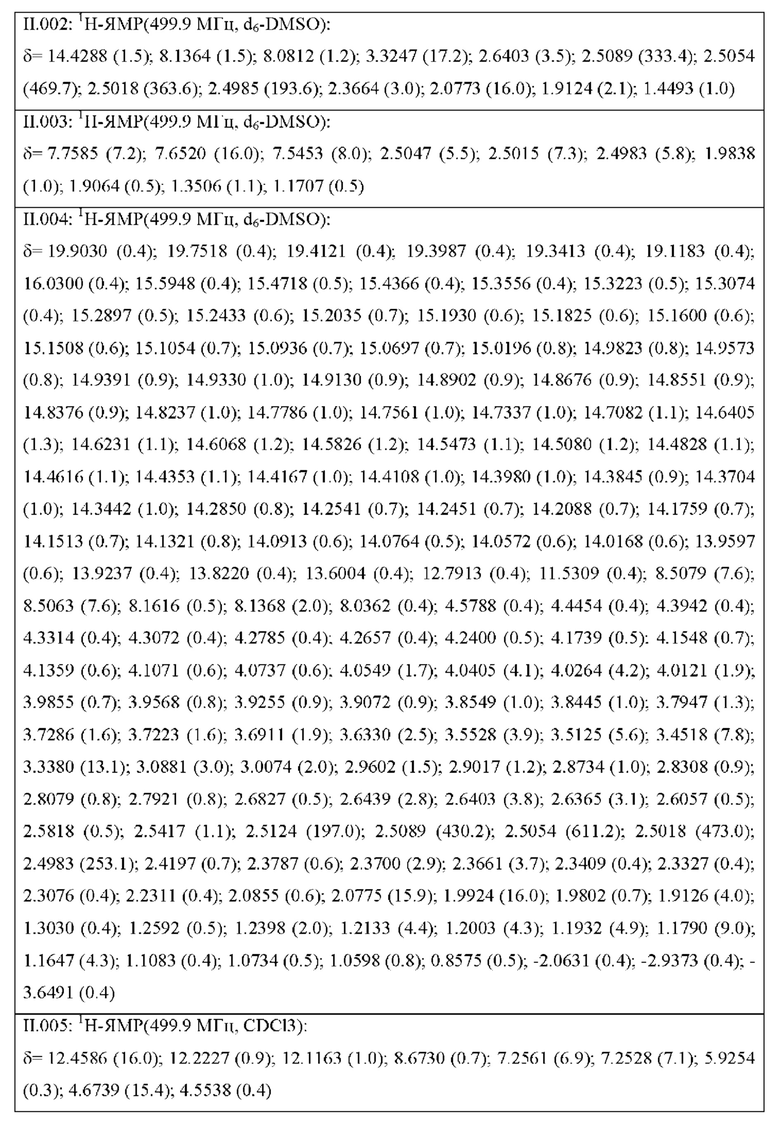
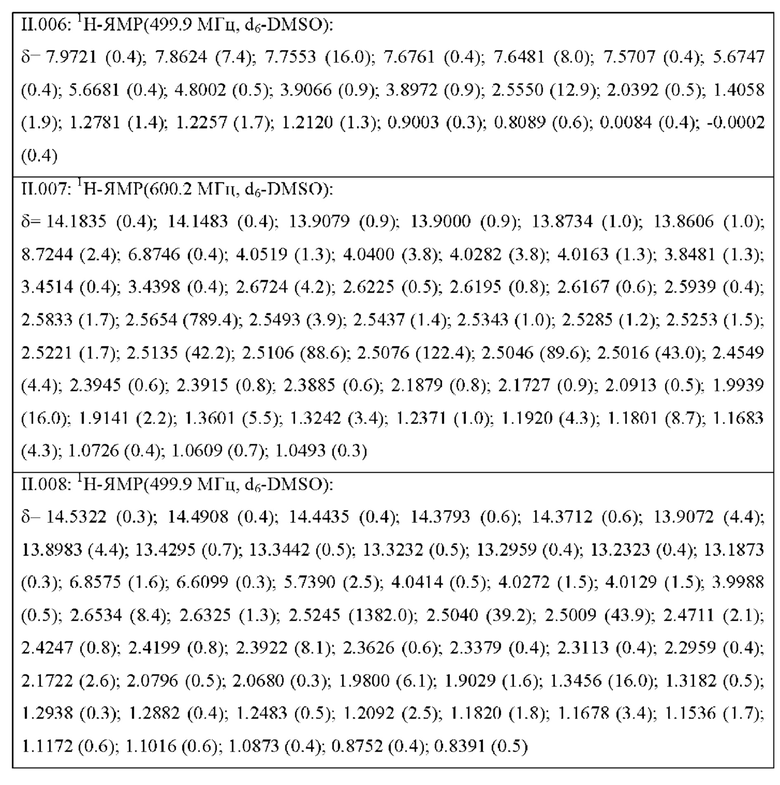
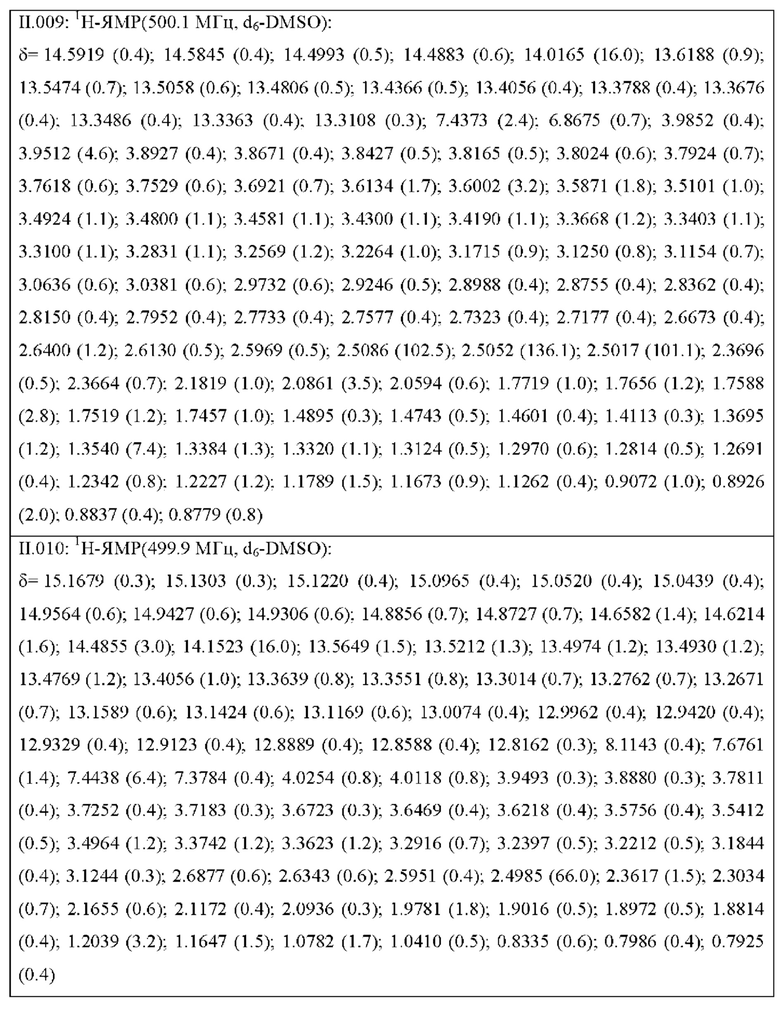
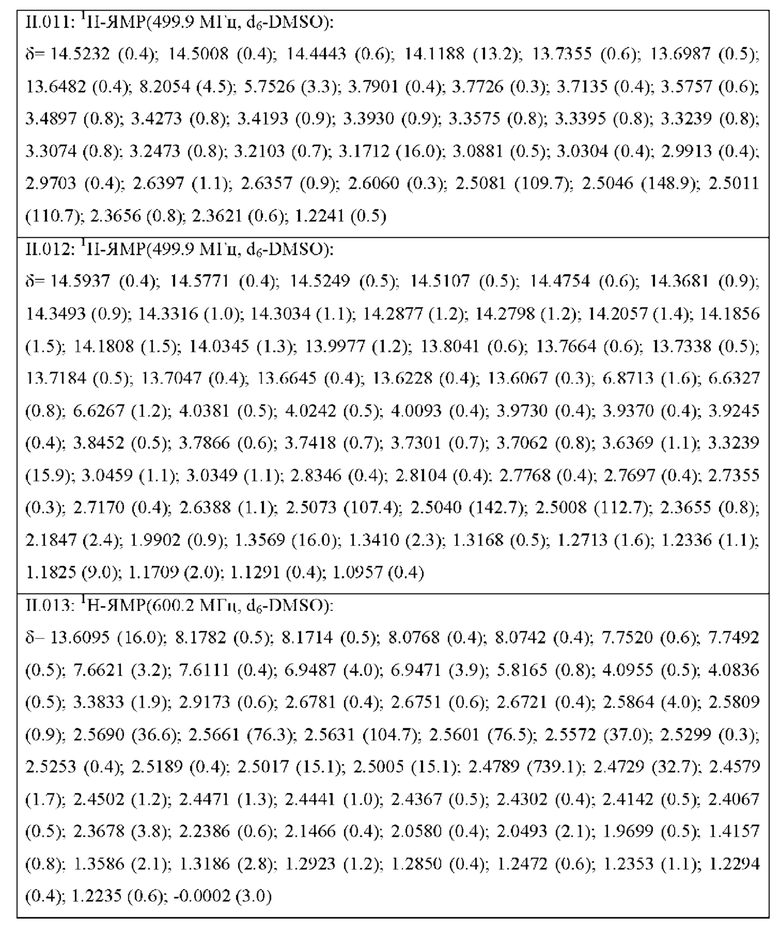
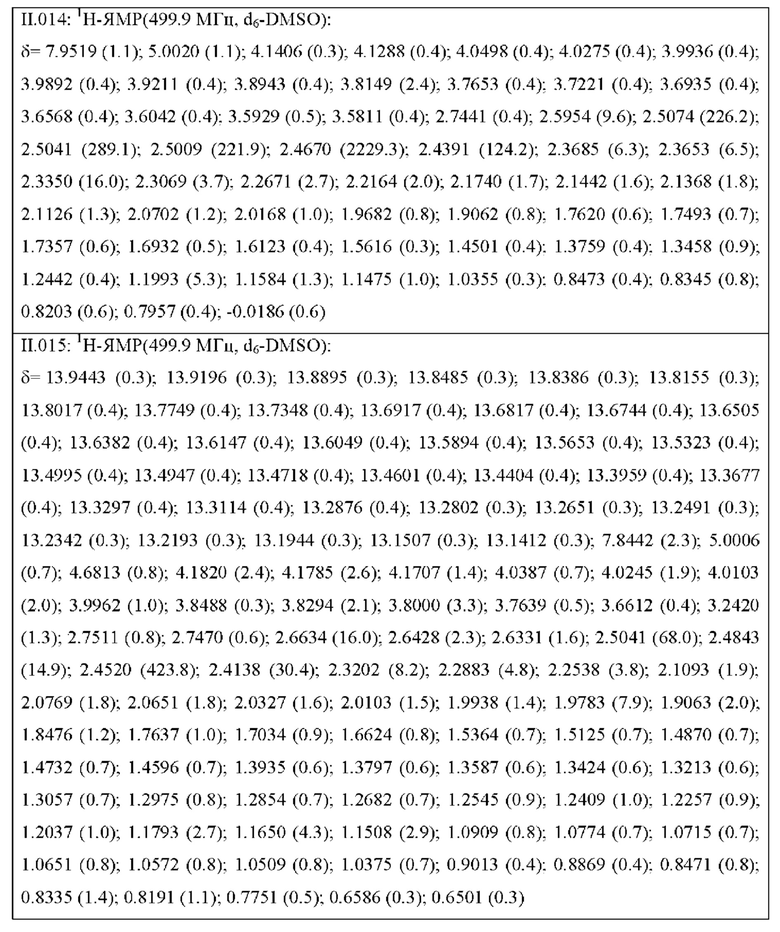
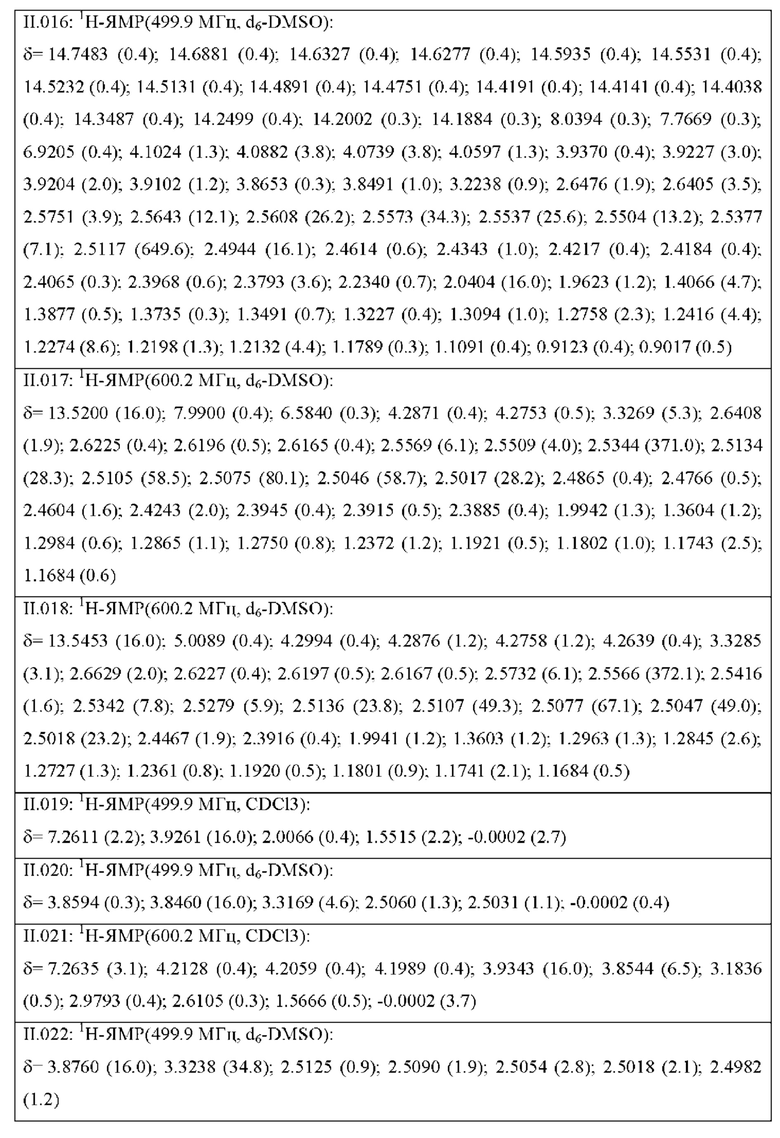
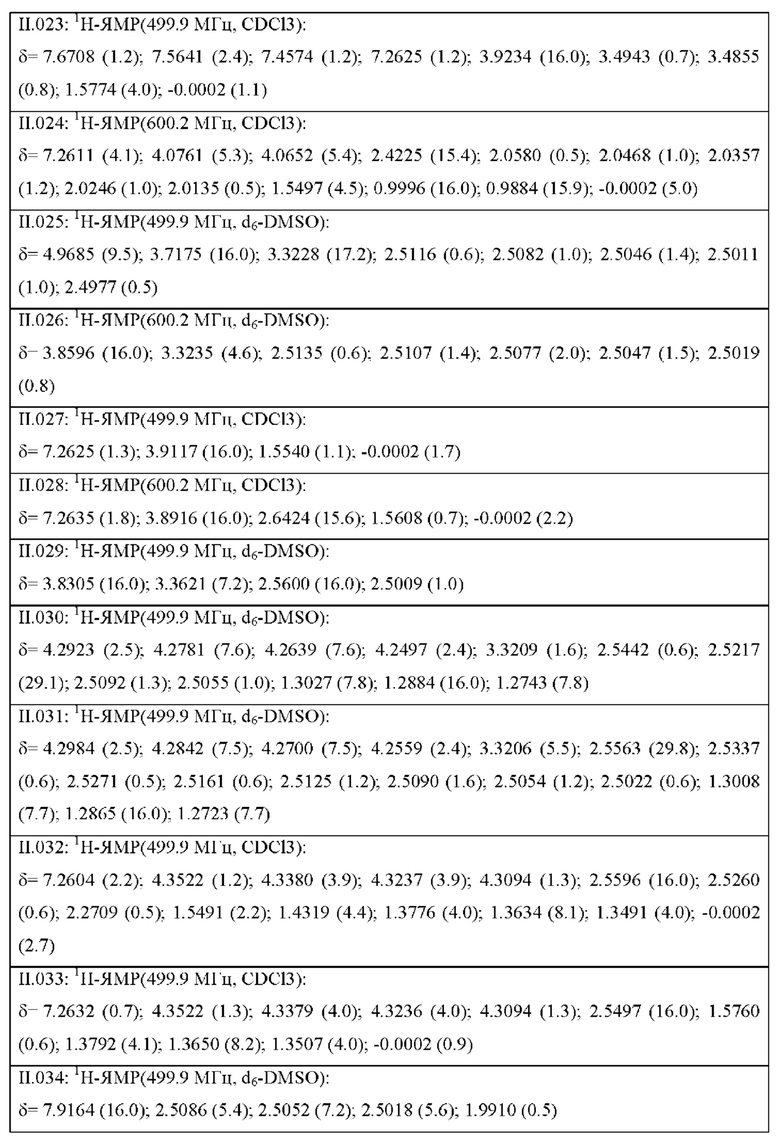







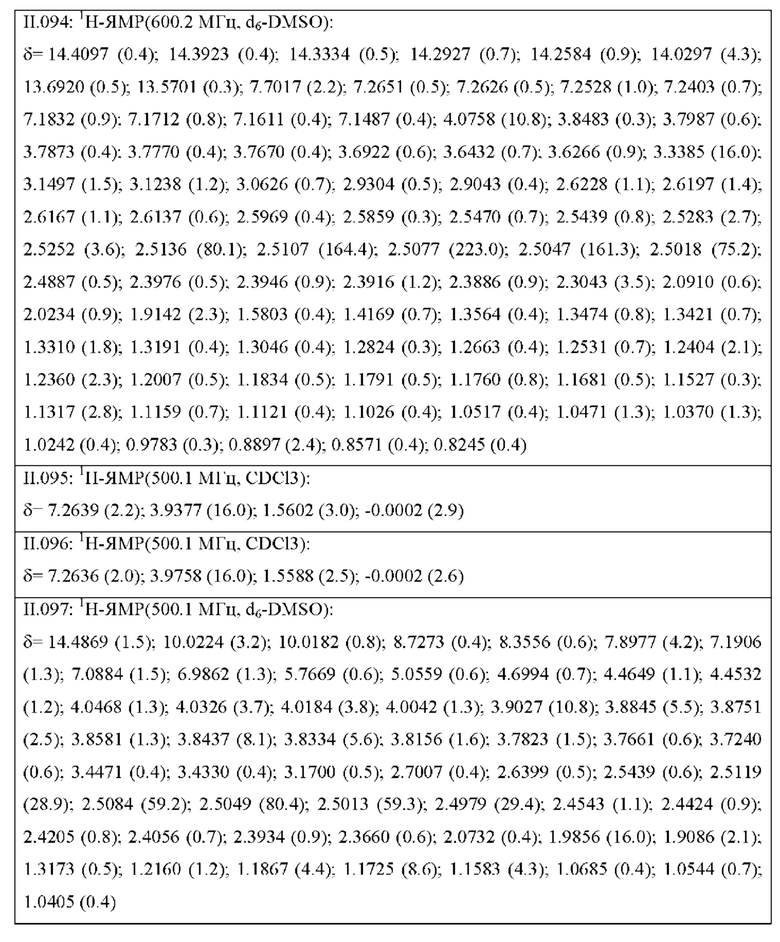
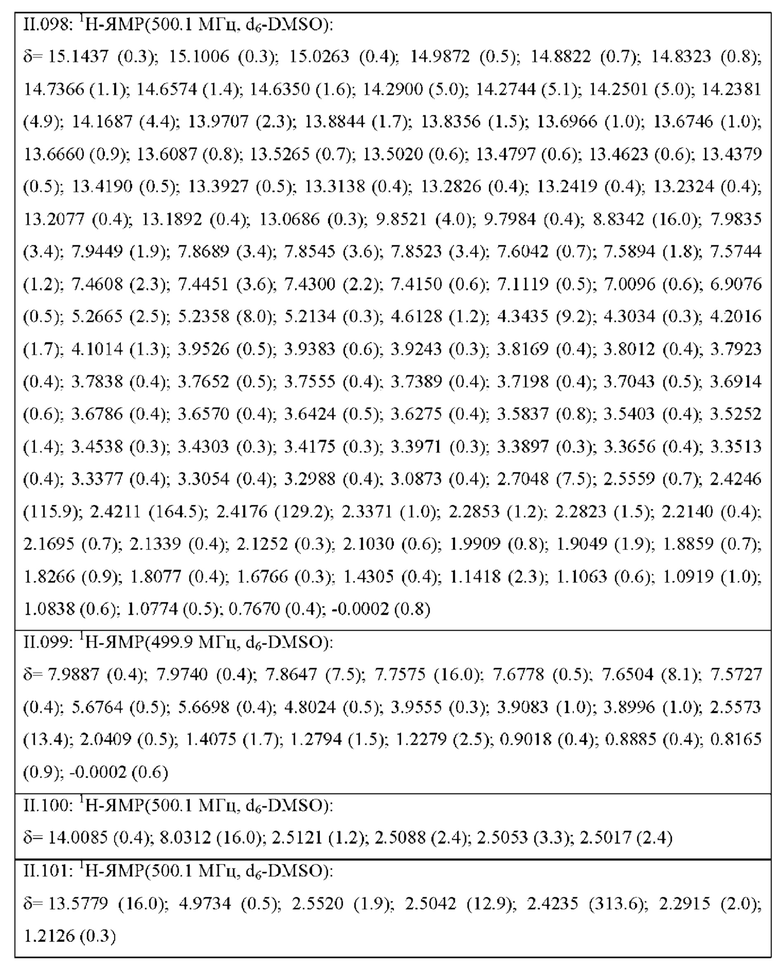


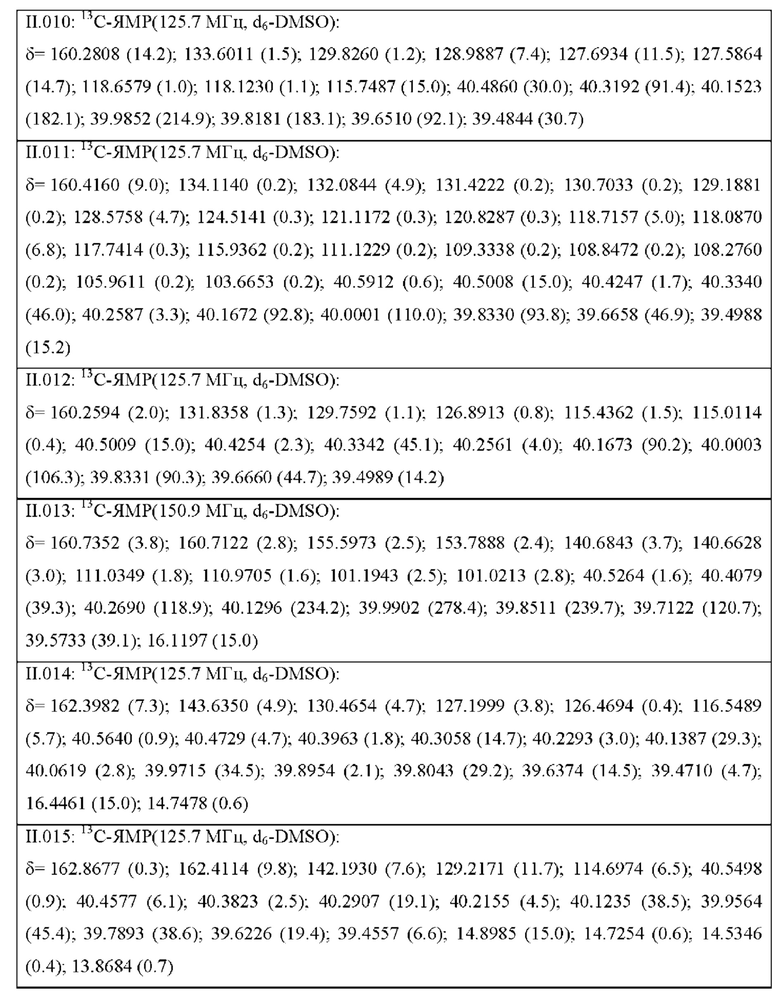
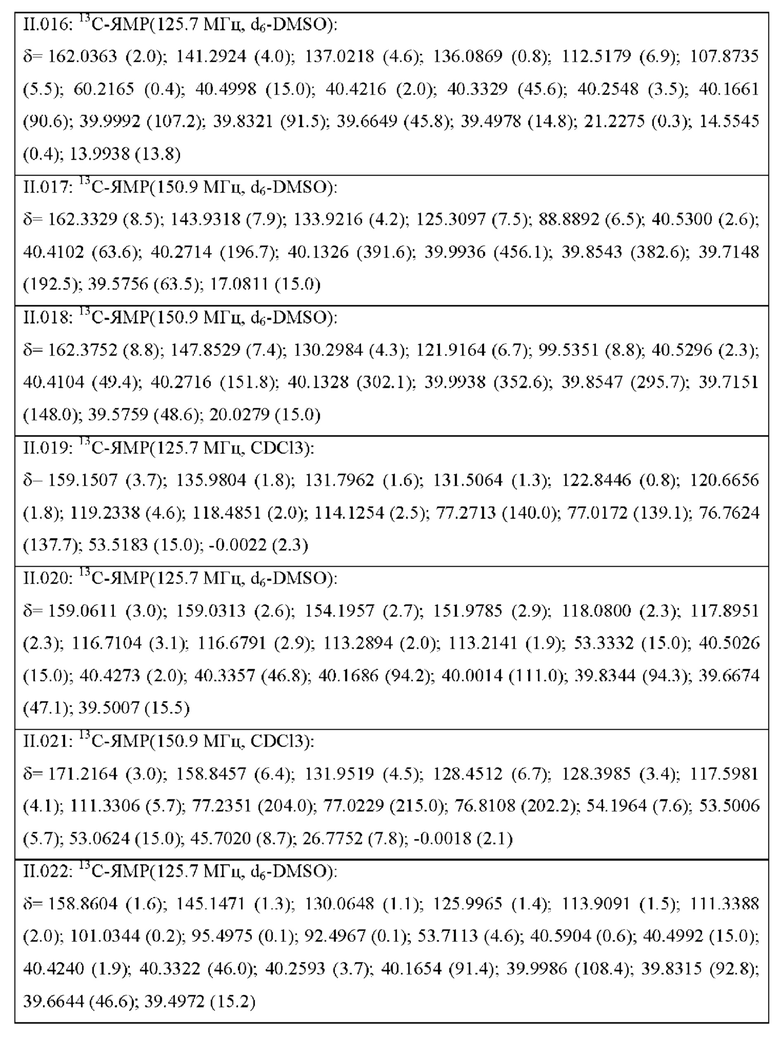
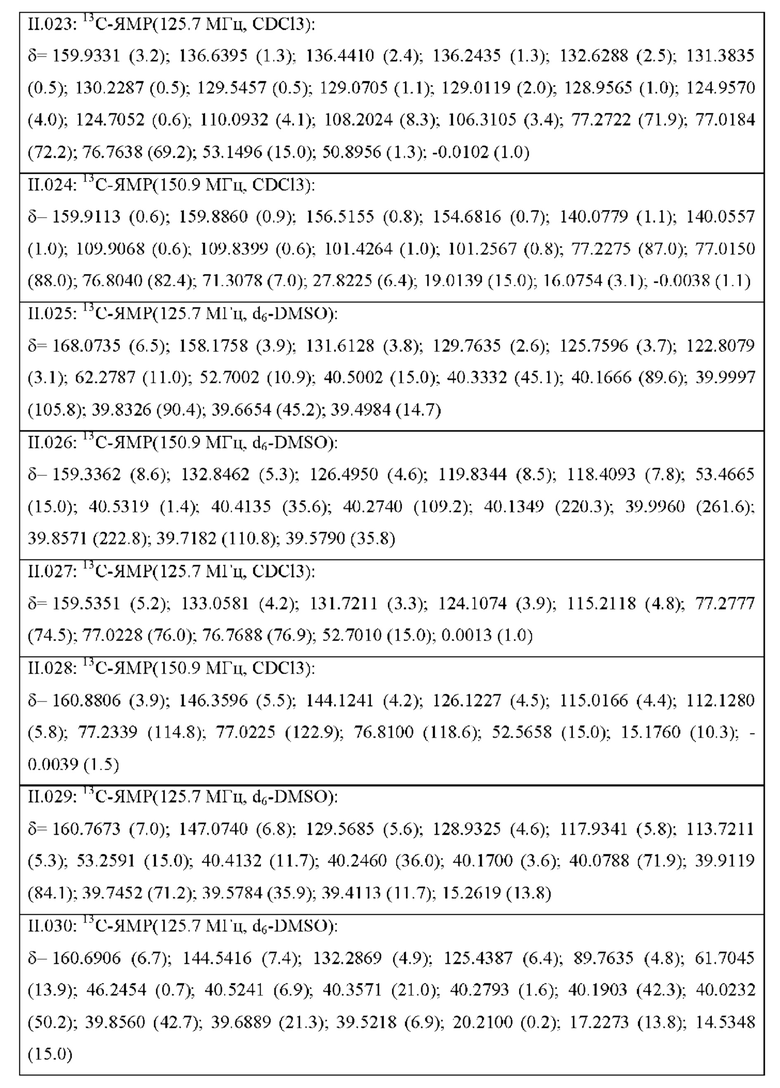

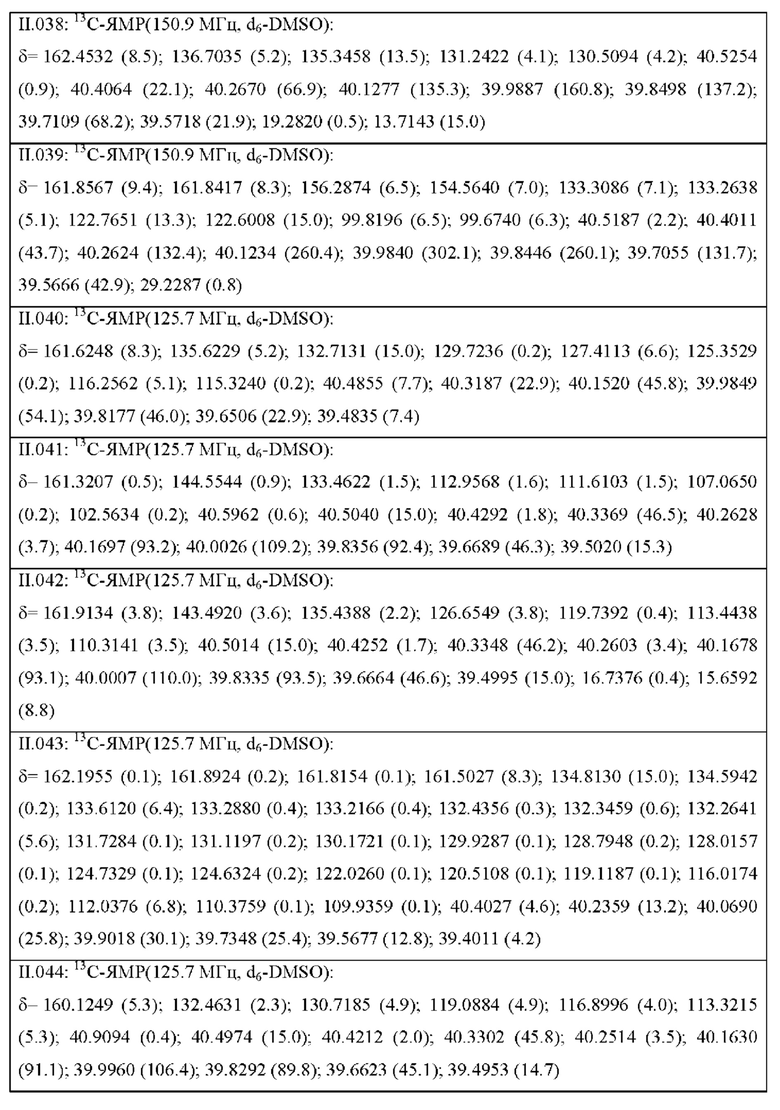
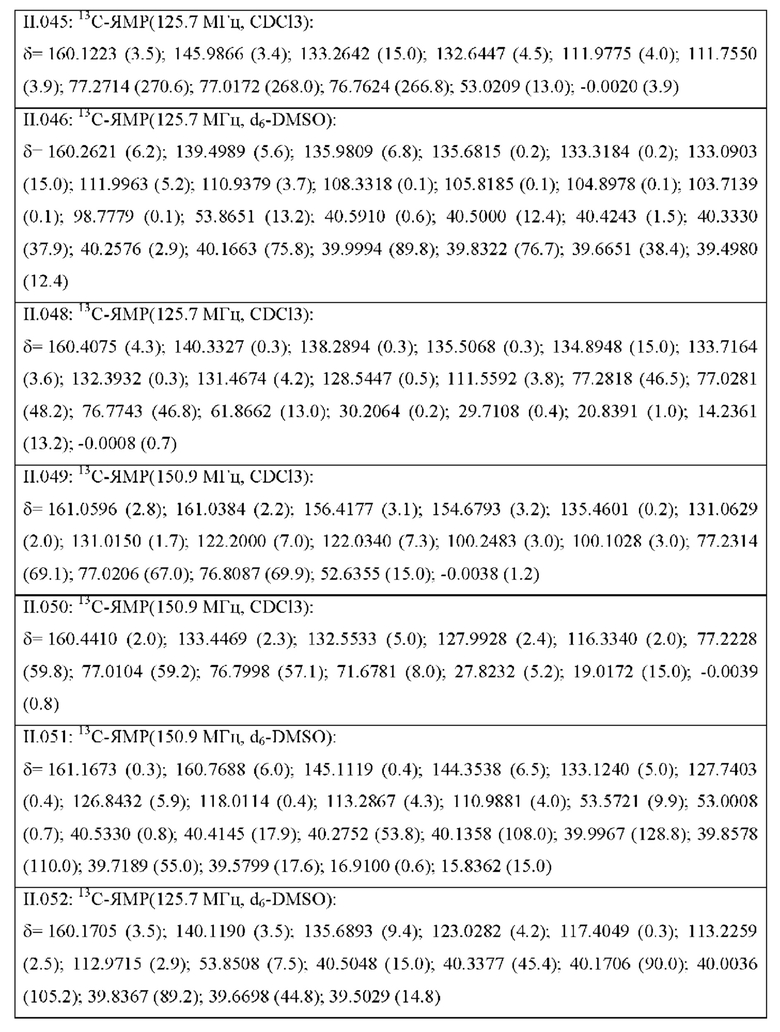
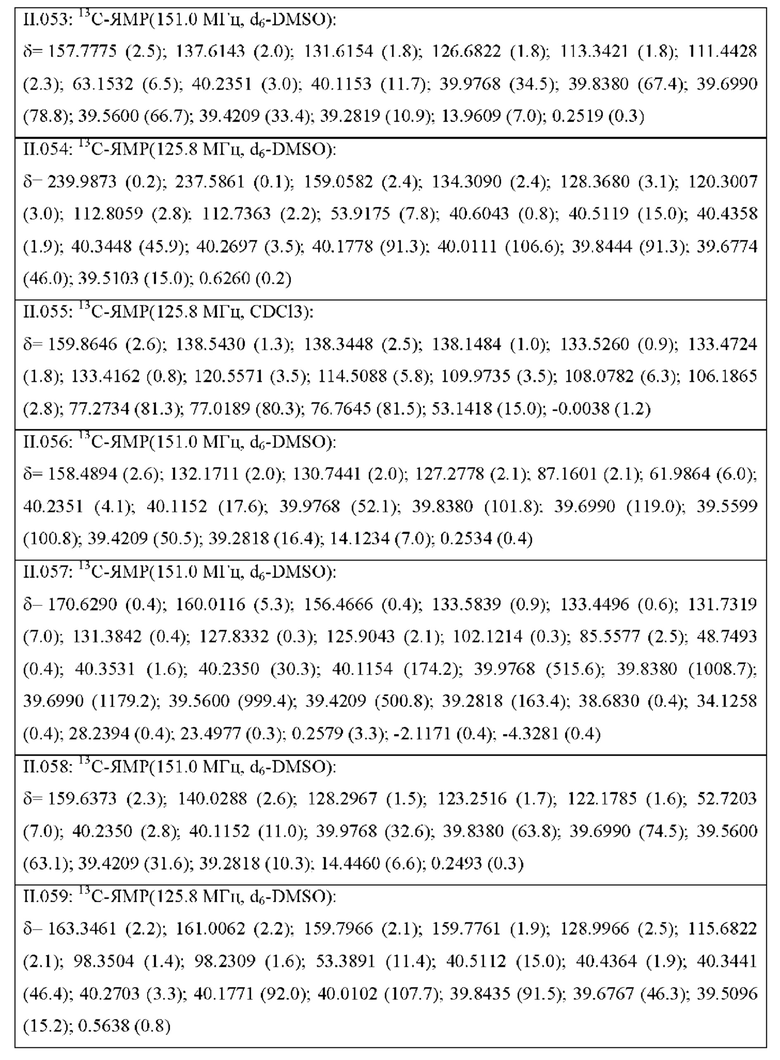
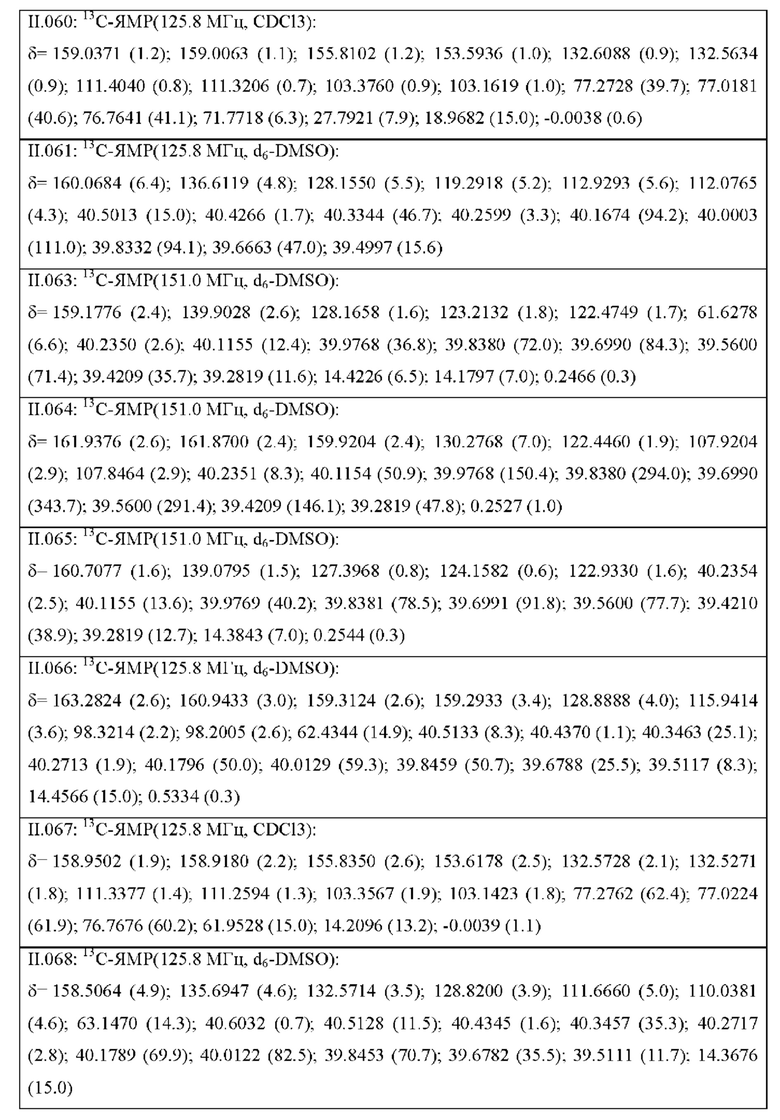
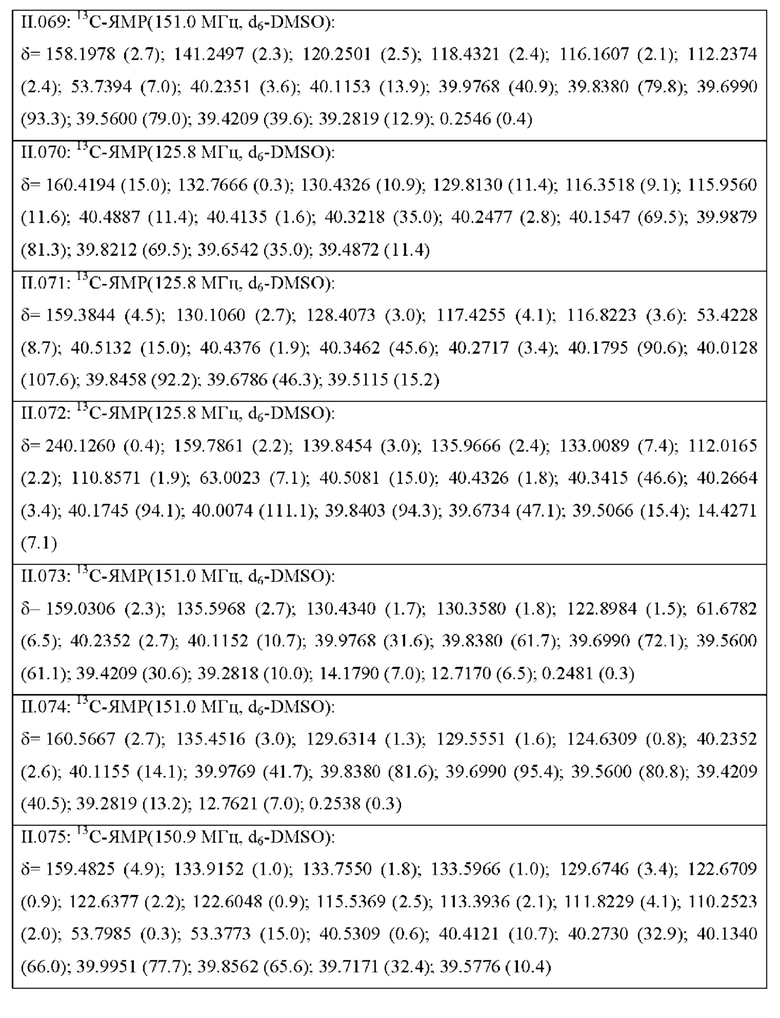
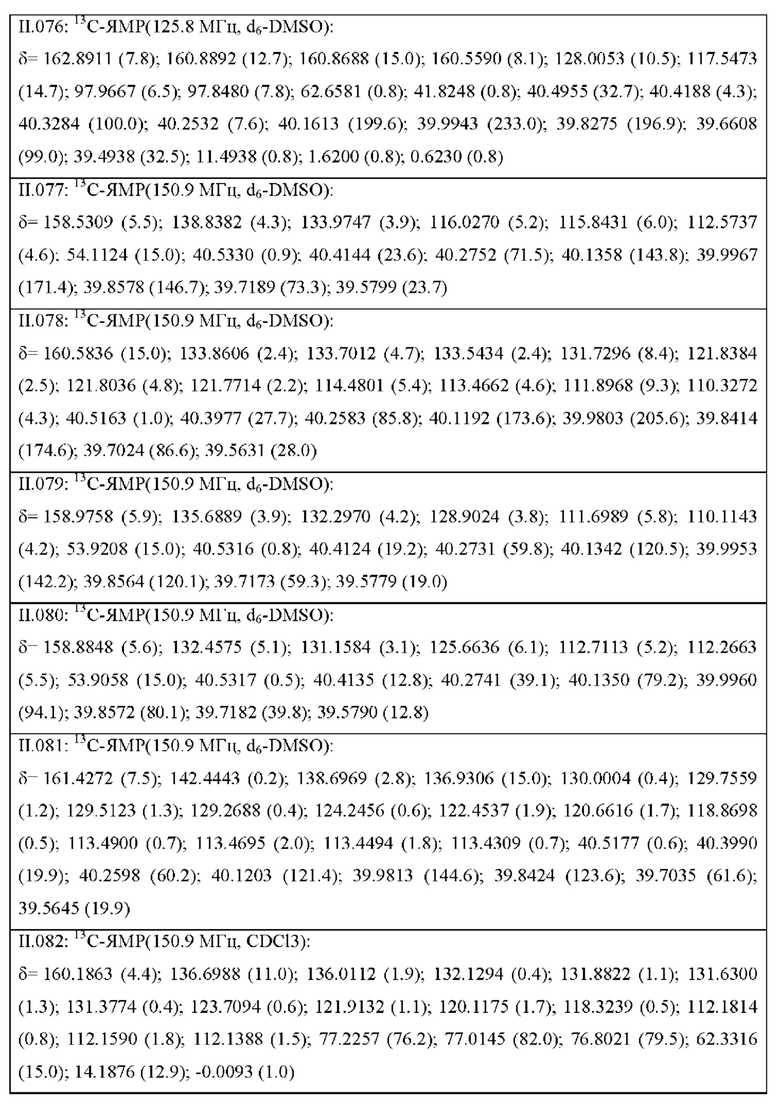
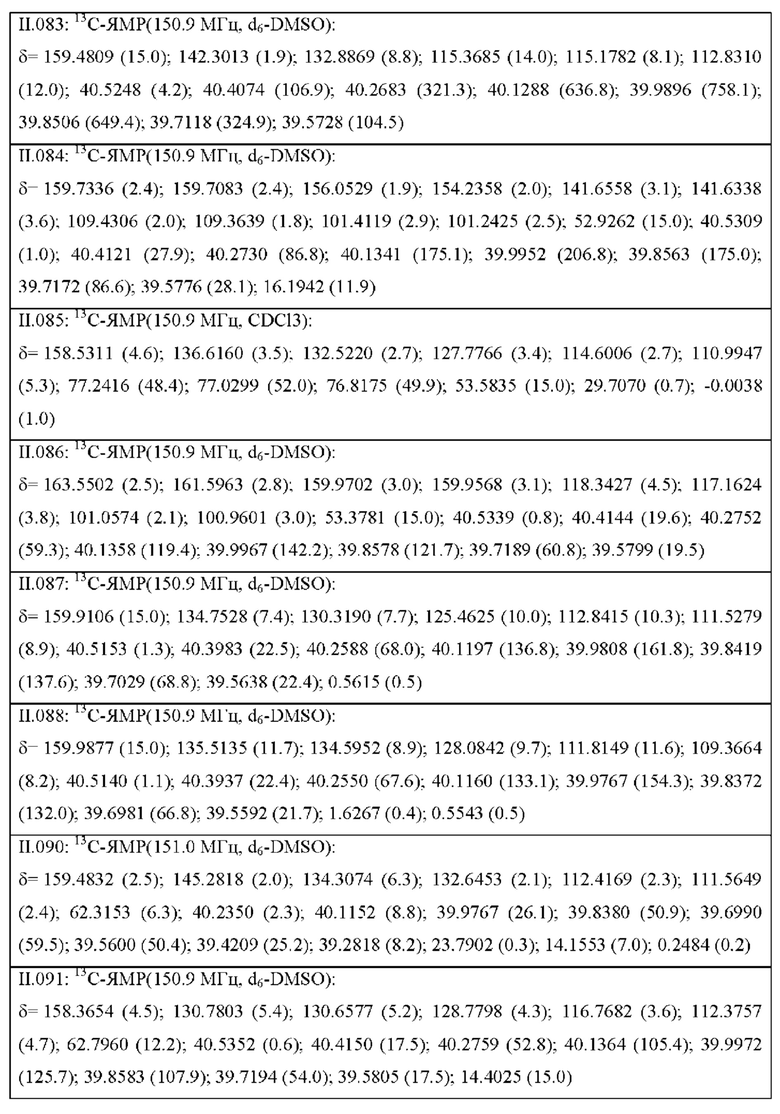
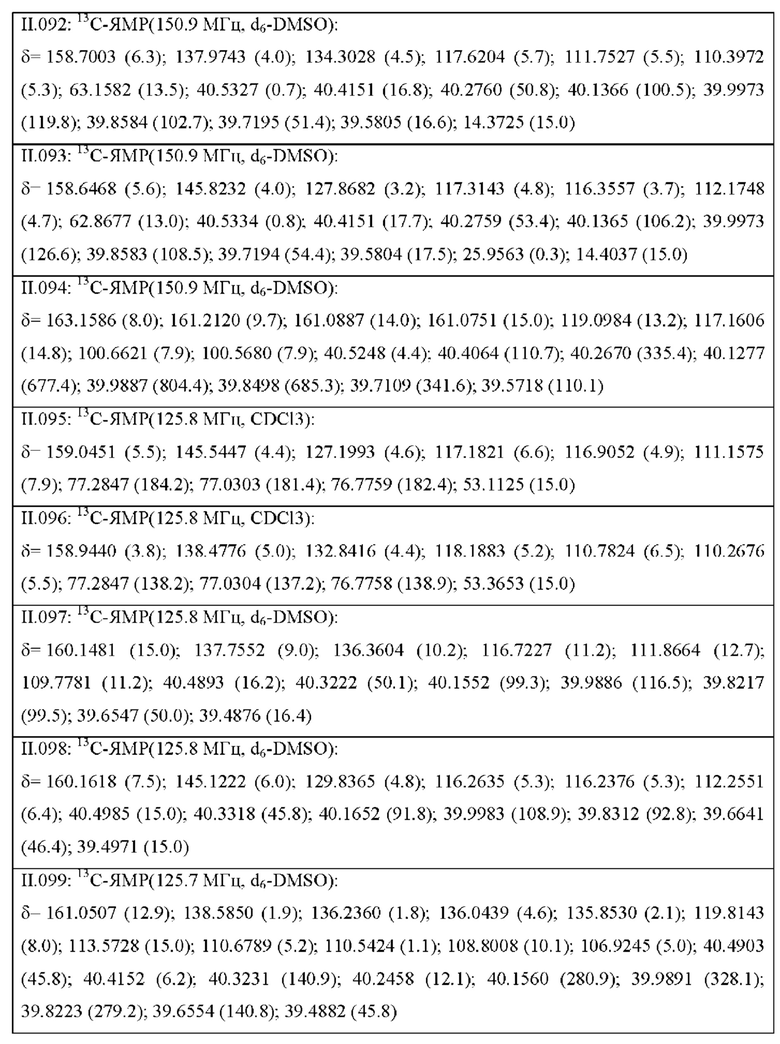

Биологические данные - Соединения формулы (I)
Пример А, описанный ниже, показывает индукцию экспрессии защитных генов у Arabidopsis thaliana с помощью соединения согласно формуле (I), в частности, стимуляцию метаболического пути салициловой кислоты. Следовательно, эти соединения могут индуцировать защитные силы хозяина и, таким образом, защищать растения от широкого спектра патогенов, включая бактерии и грибы.
Примеры В, С, D, Е и F, описанные ниже, показывают активность in vivo соединений согласно формуле (I) in planta путем стимуляции защиты растений от различных патогенов, заражающих растения, включая бактерии и грибки.
Примеры G, Н, I и J, описанные ниже, показывают прямую неактивность в клеточном тесте in vitro соединения формулы (I) против различных патогенов, включая бактерии и грибы, что иллюстрирует способ действия соединений формулы (I) в качестве индукторов защиты растения-хозяина.
Пример А: Индукция экспрессии защитного гена у Arabidopsis thaliana
Репортерные растения Arabidopsis thaliana, содержащие кодирующую последовательность зеленого флуоресцентного белка (GFP), связанную с последовательностью промотора, чувствительной к салицилатам, гена PR1 (белок I, связанный с патогенезом) (AT2G14610), выращивали в течение пяти дней, а затем опрыскивали соединениями. На 3-й день после опрыскивания оценивали флуоресценцию растений с помощью прибора MacroFluo фирмы Leica Microsystems (Wetzlar, Германия). Флуоресценцию количественно определяли с помощью программного обеспечения Meta-Morph Microscopy Automation & Image Analysis (Molecular Devices, Саннивейл, Калифорния, США).
Фоновая флуоресценция в ложно обработанных листьях была принята за 1,00. Обработка салициловой кислотой (300 частей на миллион) привела к относительному значению флуоресценции 2,70, что подтверждает достоверность тест-системы.
В этом тесте следующие соединения согласно изобретению показали относительное значение флуоресценции, по меньшей мере, выше 2 при концентрации соединения 300 частей на миллион: 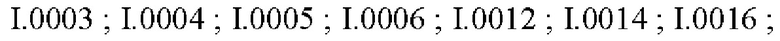



В этом тесте следующие соединения согласно изобретению показали относительное значение флуоресценции, по меньшей мере, выше 2 при концентрации соединения 75 частей на миллион: 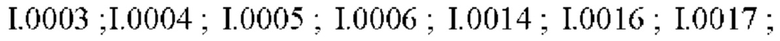


Салицилат является основным защитным гормоном против патогенов растений. Все соединения, описанные выше, стимулируют путь салициловой кислоты и, следовательно, могут защищать растения от широкого спектра патогенов
Пример В: профилактическое испытание in vivo на Peronospora parasitica (ложная мучнистая роса крестоцветных)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения капусты обрабатывали путем опрыскивания активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией спор Peronospora parasitica. Зараженные растения капусты инкубировали в течение 5 дней при 20°С и 100% относительной влажности.
Тест оценивали через 5 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: 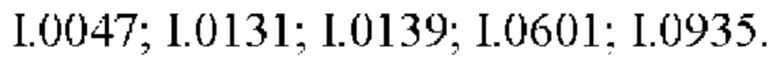
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: 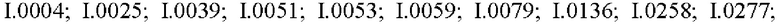
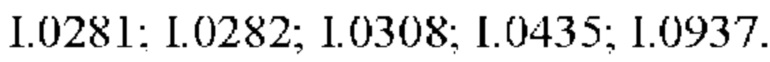
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 31 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 31 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 31 частей на миллион активного ингредиента: 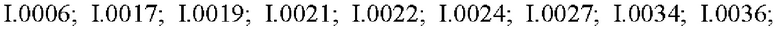

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: 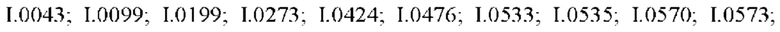
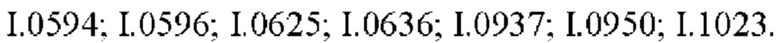
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: 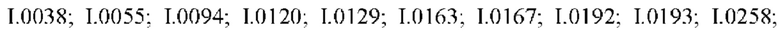
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 
Пример С: профилактическое испытание in vivo на Pseudomonas syringae pv. tomato (бактериальная пятнистость на помидоре)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения томата обрабатывали путем опрыскивания активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией бактерий Pseudomonas syringae pv. tomato. Зараженные растения томатов инкубировали в течение 4 дней в насыщенной атмосфере при 22°С днем / 20°С ночью - 70%HR, а затем в течение 1 или 2 дней при 22°С днем / 20°С ночью при относительной влажности 70-80%..
Тест оценивали через 5 или 6 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: 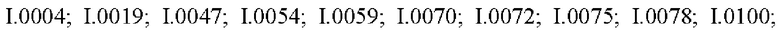
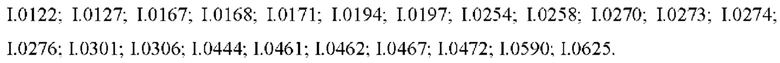
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: 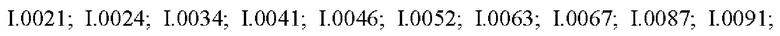

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 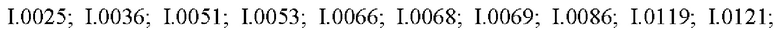

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 31 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 31 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 31 частей на миллион активного ингредиента: 
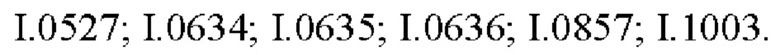
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: 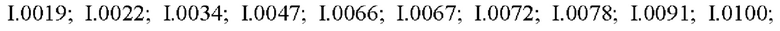

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: 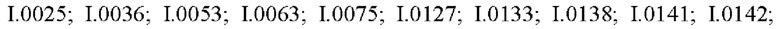

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 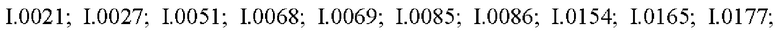

Пример D: профилактическое испытание in vivo на Xanthomonas campestris pv. campestris (черная гниль капусты)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения капусты обрабатывали путем опрыскивания активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией бактерий Xanthomonas campestris pv. campestris. Зараженные растения капусты инкубировали в течение 8 или 10 дней при 27°С и относительной влажности 95%.
Тест оценивали через 8 или 10 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: 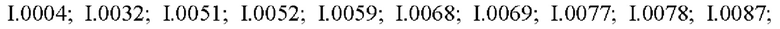
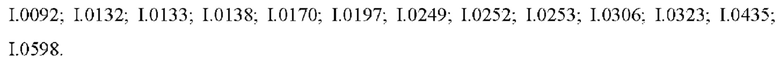
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: 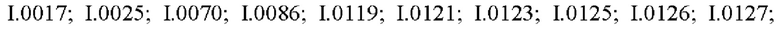
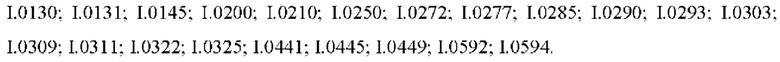
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 31 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 31 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 31 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 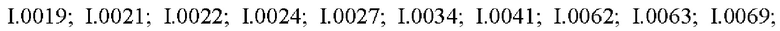

Пример Е: Профилактическое испытание in vivo на Colletotrichum lindemuthianum (антракноз фасоли)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения фасоли обрабатывали опрыскиванием активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией спор Colletotrichum lindemuthianum. Зараженные растения фасоли инкубировали в течение 24 часов при 20°С и относительной влажности 100%, а затем в течение 5 дней при 20°С и относительной влажности 90%.
Тест оценивали через 6 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: 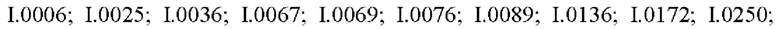
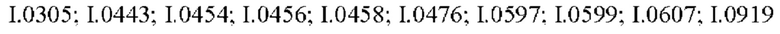
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: 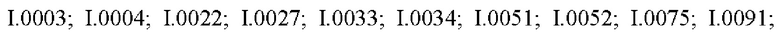

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 31 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 31 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 31 частей на миллион активного ингредиента: 
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 

Пример F: профилактическое испытание in vivo на Uromyces appendiculatus (бобовая ржавчина)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения фасоли обрабатывали опрыскиванием активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали опрыскиванием листьев водной суспензией спор Uromyces appendiculatus. Зараженные растения фасоли инкубировали в течение 24 часов при 20°С и относительной влажности 100%, а затем в течение 9 дней при 20°С и относительной влажности 70-80%.
Тест оценивали через 10 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: 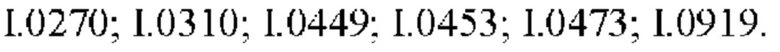
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: 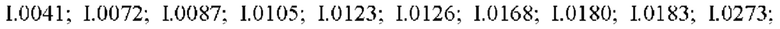
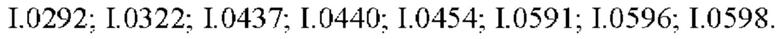
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 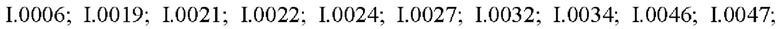

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 31 частей на миллион активного ингредиента: 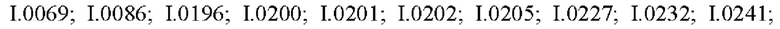
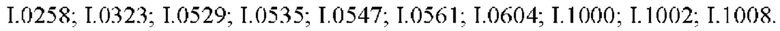
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 31 частей на миллион активного ингредиента: 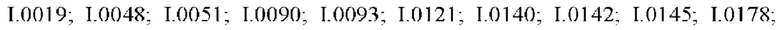
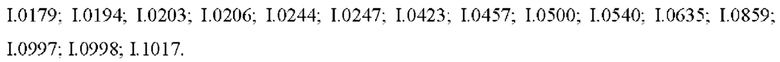
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 31 частей на миллион активного ингредиента: 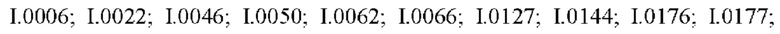

В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: 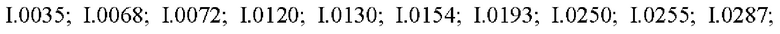
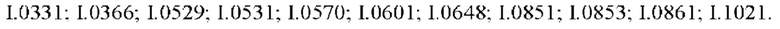
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: 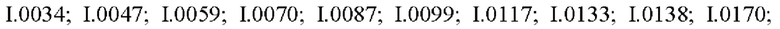
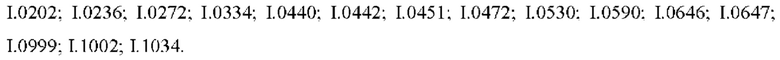
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 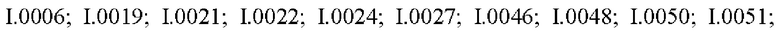

Пример G: Alternaria alternate клеточный тест in vitro
Фунгициды солюбилизировали в ДМСО и из раствора готовили необходимый диапазон концентраций. Конечная концентрация ДМСО, использованного в анализе, составляла Ј1%.
Суспензию спор A. alternata готовили и разбавляли до желаемой плотности спор.
Фунгициды оценивали по их способности ингибировать прорастание спор и рост мицелия в анализе жидкой культуры. Соединения добавляли в нужной концентрации в культуральную среду со спорами. После 5 дней инкубации фунгицидную токсичность соединений определяли спектрометрическим измерением роста мицелия. Ингибирование роста грибов определяли путем сравнения значений оптической плотности в лунках, содержащих фунгициды, с оптической плотностью в контрольных лунках без фунгицидов.
В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 20 частей на миллион: 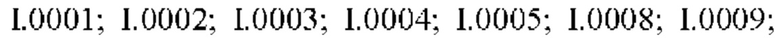


В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 10 частей на миллион: 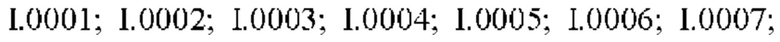


Пример H: in vitro исследование на клетке Colletotrichum lindemuthianum
Активные ингредиенты суспендировали в DMSO, и раствор применяли для получения требуемого диапазона концентраций. Конечная концентрация в DMSO, применяемая для анализа, составляла Ј1%.
Суспензию спор С. lindemuthianum получали и разбавляли до желаемой плотности спор.
Активные ингредиенты оценивали по их способности подавлять прорастание спор и рост мицелия в анализе жидких культур. Соединения добавляли в желаемой концентрации в культуральную среду со спорами. После 6 дней инкубации токсичность соединений в отношении грибков определяли спектрометрическим измерением роста мицелия. Ингибирование роста грибков определяли путем сравнения значений поглощения в лунках, содержащих активные ингредиенты, с поглощением в контрольных лунках без активных ингредиентов.
В этом тесте следующие соединения согласно настоящему изобретению не показали прямую активность (эффективность ниже или равную 30%) при концентрации 20 частей на миллион активного ингредиента: 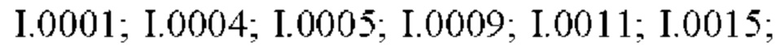


В этом тесте следующие соединения согласно настоящему изобретению не показали прямую активность (эффективность ниже или равную 30%) при концентрации 10 частей на миллион активного ингредиента: 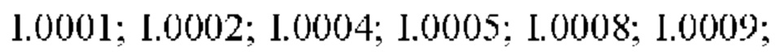



Пример I: Xanthomonas campestris pv. Campestris клеточный тест in vitro
Соединения солюбилизировали в ДМСО и раствор использовали для приготовления необходимого диапазона концентраций. Конечная концентрация ДМСО, использованного в анализе, составляла Ј1%.
Инокулят готовили из предварительной культуры бактерий, выращенных в жидкой среде и разбавленных до нужной оптической плотности (ОП).
Соединения оценивали на их способность ингибировать рост бактерий в анализе жидкой культуры. Соединения добавляли в нужных концентрациях в культуральную среду, содержащую суспензию бактерий. Через 24 ч инкубации эффективность соединений определяли спектрометрическим измерением роста бактерий. Ингибирование определяли путем сравнения значений поглощения в лунках, содержащих соединения, с показателями поглощения в контрольных лунках без активных ингредиентов.
В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 20 частей на миллион: 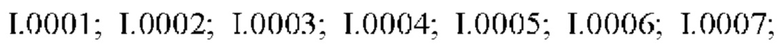



В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 10 частей на миллион: 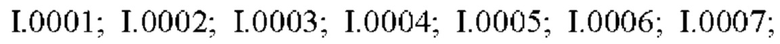



Пример J: Pseudomonas syringae pv. tomato клеточный тест in vitro
Соединения солюбилизировали в ДМСО и раствор использовали для приготовления необходимого диапазона концентраций. Конечная концентрация ДМСО, использованного в анализе, составляла Ј1%.
Инокулят готовили из предварительной культуры бактерий, выращенных в жидкой среде и разбавленных до нужной оптической плотности (ОП).
Соединения оценивали на их способность ингибировать рост бактерий в анализе жидкой культуры. Соединения добавляли в нужных концентрациях в культуральную среду, содержащую суспензию бактерий. Через 24 ч инкубации эффективность соединений определяли спектрометрическим измерением роста бактерий. Ингибирование определяли путем сравнения значений поглощения в лунках, содержащих соединения, с показателями поглощения в контрольных лунках без активных ингредиентов.
В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 20 частей на миллион: 



В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 10 частей на миллион: 


Биологические данные - Соединения формулы (II)
Пример К, описанный ниже, показывает индукцию экспрессии защитных генов у Arabidopsis thaliana с помощью соединения согласно формуле (II), в частности, стимуляцию метаболического пути салициловой кислоты. Следовательно, эти соединения могут индуцировать защитные силы хозяина и, таким образом, защищать растения от широкого спектра патогенов, включая бактерии и грибы.
Примеры L, М и N, описанные ниже, показывают активность in vivo соединений согласно формуле (II) in planta путем стимуляции защиты растений от различных патогенов, заражающих растения, включая бактерии и грибки.
Примеры О и Р, описанные ниже, показывают прямую неактивность в клеточном тесте in vitro соединения формулы (II) против различных патогенов, включая бактерии и грибы, что иллюстрирует способ действия соединений формулы (II) в качестве индукторов защиты растения-хозяина.
Пример К: Индукция экспрессии защитного гена у Arabidopsis thaliana
Репортерные растения Arabidopsis thaliana, содержащие кодирующую последовательность зеленого флуоресцентного белка (GFP), связанную с последовательностью промотора, чувствительной к салицилатам, гена PR1 (белок I, связанный с патогенезом) (AT2G14610), выращивали в течение пяти дней, а затем опрыскивали соединениями. На 3-й день после опрыскивания оценивали флуоресценцию растений с помощью прибора MacroFluo фирмы Leica Microsystems (Wetzlar, Германия). Флуоресценцию количественно определяли с помощью программного обеспечения Meta-Morph Microscopy Automation & Image Analysis (Molecular Devices, Саннивейл, Калифорния, США).
Фоновая флуоресценция в ложно обработанных листьях была принята за 1,00. Обработка салициловой кислотой (300 частей на миллион) привела к относительному значению флуоресценции 2,70, что подтверждает достоверность тест-системы.
В этом тесте следующие соединения согласно изобретению показали относительное значение флуоресценции, по меньшей мере, выше 2 при концентрации соединения 300 частей на миллион: 


В этом тесте следующие соединения согласно изобретению показали относительное значение флуоресценции, по меньшей мере, выше 2 при концентрации соединения 75 частей на миллион: 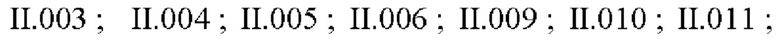

Салицилат является основным защитным гормоном против патогенов растений. Все соединения, описанные выше, стимулируют путь салициловой кислоты и, следовательно, могут защищать растения от широкого спектра патогенов.
Пример L: профилактическое испытание in vivo на Peronosyora parasitica (ложная мучнистая роса крестоцветных)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения капусты обрабатывали путем опрыскивания активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией спор Peronospora parasitica. Зараженные растения капусты инкубировали в течение 5 дней при 20°С и 100% относительной влажности.
Тест оценивали через 5 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: II.083.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: II.032; II.033.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: 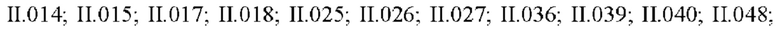
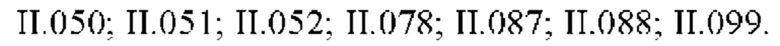
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: II.052; II.083.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: II.017; II.036; II.040.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: 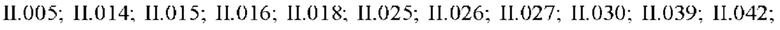
Пример М: профилактическое испытание in vivo на Xanthomonas campestris pv. campestris (черная гниль капусты)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения капусты обрабатывали путем опрыскивания активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали путем опрыскивания листьев водной суспензией бактерий Xanthomonas campestris pv. campestris. Зараженные растения капусты инкубировали в течение 8 или 10 дней при 27°С и относительной влажности 95%.
Тест оценивали через 8 или 10 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 500 частей на миллион активного ингредиента: II.028; II.050; II.083.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 500 частей на миллион активного ингредиента: II.017.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 500 частей на миллион активного ингредиента: II.018; II.025; II.026; II.051.
Пример N: профилактическое испытание in vivo на Uromyces aypendiculatus (бобовая ржавчина)
Тестируемые активные ингредиенты были приготовлены путем гомогенизации в смеси ацетон/диметилсульфоксид/твинТ, а затем разбавлены водой для получения желаемой концентрации активного вещества.
Молодые растения фасоли обрабатывали опрыскиванием активным ингредиентом, приготовленным, как описано выше. Контрольные растения обрабатывали только водным раствором ацетон/диметилсульфоксид/твинТ.
Через 72 часа растения заражали опрыскиванием листьев водной суспензией спор Uromyces appendiculatus. Зараженные растения фасоли инкубировали в течение 24 часов при 20°С и относительной влажности 100%, а затем в течение 9 дней при 20°С и относительной влажности 70-80%.
Тест оценивали через 10 дней после инокуляции. 0% означает эффективность, которая соответствует эффективности контрольных растений, тогда как эффективность 100% означает, что заболевание не наблюдалось.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 70% до 79% при концентрации 125 частей на миллион активного ингредиента: II.077; II.078.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 80% до 89% при концентрации 125 частей на миллион активного ингредиента: II.015; II.037; II.079; II.080; II.088.
В этом тесте следующие соединения согласно настоящему изобретению показали эффективность от 90% до 100% при концентрации 125 частей на миллион активного ингредиента: II.017; II.018; II.027; II.042; II.051; II.075; II.087.
Пример О: in vitro исследование на клетке Colletotrichum tindemuthianum
Активные ингредиенты суспендировали в DMSO, и раствор применяли для получения требуемого диапазона концентраций. Конечная концентрация в DMSO, применяемая для анализа, составляла Ј1%.
Суспензию спор С. lindemuthianum получали и разбавляли до желаемой плотности спор.
Активные ингредиенты оценивали по их способности подавлять прорастание спор и рост мицелия в анализе жидких культур. Соединения добавляли в желаемой концентрации в культуральную среду со спорами. После 6 дней инкубации токсичность соединений в отношении грибков определяли спектрометрическим измерением роста мицелия. Ингибирование роста грибков определяли путем сравнения значений поглощения в лунках, содержащих активные ингредиенты, с поглощением в контрольных лунках без активных ингредиентов.
В этом тесте следующие соединения согласно настоящему изобретению не показали прямую активность (эффективность ниже или равную 30%) при концентрации 20 частей на миллион активного ингредиента: 

В этом тесте следующие соединения согласно настоящему изобретению не показали прямую активность (эффективность ниже или равную 30%) при концентрации 10 частей на миллион активного ингредиента: 

Пример Р: Xanthomonas campestris pv. Campestris клеточный тест in vitro
Соединения солюбилизировали в ДМСО и раствор использовали для приготовления необходимого диапазона концентраций. Конечная концентрация ДМСО, использованного в анализе, составляла Ј1%.
Инокулят готовили из предварительной культуры бактерий, выращенных в жидкой среде и разбавленных до нужной оптической плотности (ОП).
Соединения оценивали на их способность ингибировать рост бактерий в анализе жидкой культуры. Соединения добавляли в нужных концентрациях в культуральную среду, содержащую суспензию бактерий. Через 24 ч инкубации эффективность соединений определяли спектрометрическим измерением роста бактерий. Ингибирование определяли путем сравнения значений поглощения в лунках, содержащих соединения, с показателями поглощения в контрольных лунках без активных ингредиентов.
В этом тесте следующие соединения по изобретению не проявляли прямой активности (эффективность ниже или равна 30%) при концентрации активного ингредиента 20 частей на миллион: 

| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ С НЕМАТОЦИДНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2608217C2 |
| Замещенные тиофенкарбоксамиды и их производные в качестве микробиоцидов | 2020 |
|
RU2832576C1 |
| ТИЕНИЛОКСАЗОЛОНЫ И АНАЛОГИ | 2020 |
|
RU2831013C1 |
| ЗАМЕЩЕННЫЕ ТИОФЕНКАРБОКСАМИДЫ И ИХ ПРОИЗВОДНЫЕ | 2020 |
|
RU2834236C2 |
| ЗАМЕЩЕННЫЕ ТИОФЕНКАРБОКСАМИДЫ И ИХ ПРОИЗВОДНЫЕ | 2020 |
|
RU2837213C1 |
| ПРОИЗВОДНЫЕ ПИРРОЛА, ДИАЗОЛА, ТРИАЗОЛА ИЛИ ТЕТРАЗОЛА, ПОДХОДЯЩИЕ ДЛЯ БОРЬБЫ С ЧЛЕНИСТОНОГИМИ | 2016 |
|
RU2777537C2 |
| N-(2-ФТОР-2-ФЕНЭТИЛ)КАРБОКСАМИДЫ В КАЧЕСТВЕ НЕМАТИЦИДОВ И ЭНДОПАРАЗИТИЦИДОВ | 2014 |
|
RU2667779C2 |
| ПРИМЕНЕНИЕ АРИЛЬНЫХ И ГЕТАРИЛЬНЫХ КАРБОКСАМИДОВ В КАЧЕСТВЕ ЭНДОПАРАЗИТИЦИДОВ | 2012 |
|
RU2638830C2 |
| АЗОЛИНОВЫЕ СОЕДИНЕНИЯ, ЗАМЕЩЕННЫЕ КОНДЕНСИРОВАННОЙ КОЛЬЦЕВОЙ СИСТЕМОЙ | 2015 |
|
RU2742767C2 |
| ПИРАЗОЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ИСПОЛЬЗОВАНИЕ В СПОСОБЕ БОРЬБЫ С БЕСПОЗВОНОЧНЫМИ ВРЕДИТЕЛЯМИ, В СПОСОБЕ ЗАЩИТЫ МАТЕРИАЛА РАЗМНОЖЕНИЯ РАСТЕНИЙ, В СПОСОБЕ ЛЕЧЕНИЯ ИЛИ ЗАЩИТЫ ЖИВОТНЫХ ОТ ИНВАЗИИ ИЛИ ИНФИЦИРОВАНИЯ, В МАТЕРИАЛЕ РАЗМНОЖЕНИЯ РАСТЕНИЙ И СЕЛЬСКОХОЗЯЙСТВЕННЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ПИРАЗОЛЬНЫЕ СОЕДИНЕНИЯ | 2008 |
|
RU2516290C2 |
Настоящее изобретение относится к замещенным тиофенкарбоксамидным производным, а именно к соединению формулы (I), его применению для борьбы с бактериальными и/или грибковыми заболеваниями растений и содержащей его композиции. Также предложено соединение формулы (II-A) и применение соединения формулы (II) для защиты растения от фитопатогенных грибов и/или бактерий. Значение переменных групп в формулах (I), (II) и (IIA) такие, как приведены в формуле изобретения. Предложенные соединения применяются для борьбы с бактериальными и/или грибковыми заболеваниями растений или частей растений. 6 н. и 13 з.п. ф-лы, 4 табл., 36 пр.
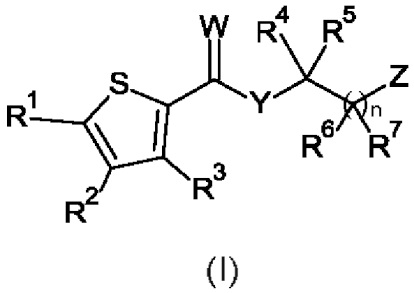
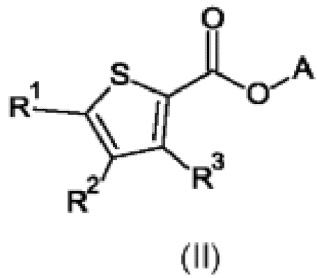
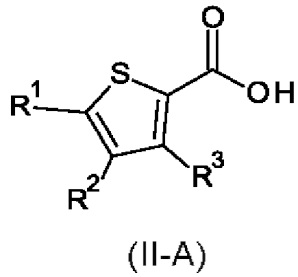
1. Соединение формулы (I)
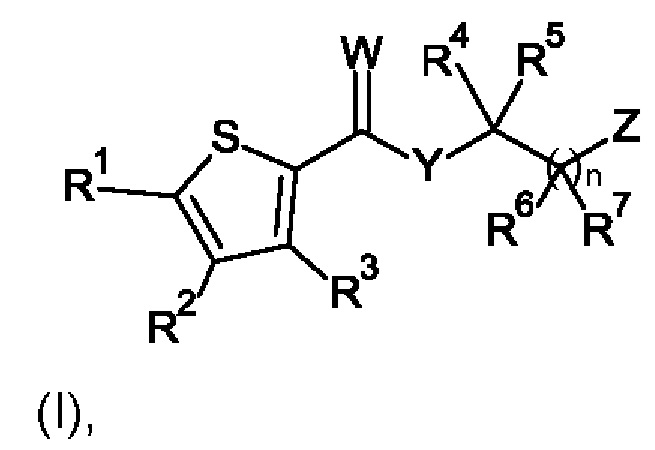
где R1 и R2 независимо выбраны из группы, состоящей из галогена, циано, C1-С6-алкила или С1-С6-галоалкила, где по меньшей мере один из R1 или R2 представляет собой галоген;
R3 выбран из группы, состоящей из водорода, галогена, циано, С1-С6-алкила или С1-С6-галоалкила;
R4 и R5 независимо выбраны из группы, состоящей из водорода, галогена, циано, гидроксила, С1-С6-алкила, С1-С6-гидроксиалкила, С1-С6-алкокси, С1-С6-галоалкила, -O-С(=O)-С1-С6-алкила, С3-С6-карбоцикла, -С(=O)-ОН, -С(=O)-O-С1-С6-алкила, С6-С10-арила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -C1-С6-алкил-гидроксиарила, -С1-С6-алкил-5-9-членного гетероарила, содержащего от 1 до 2 гетероатомов, неависимо выбранных из группы, состоящей из азота и серы, -С1-С6-алкил-S-С1-С6-алкила, -C1-С6-алкил-S-С(=O)-С1-С6-алкила, -С1-С6-алкил-O-(С=O)-С1-С6-алкила, -C1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-С(=O)-N(С1-С6-алкила)2, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-NH-C(=NH)-NH2, -С1-С6-алкил-S-С(=O)-O-С1-С6-алкила, -С1-С6-алкил-S-C(=O)-NH2, -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила), -С1-С6-алкил-S-С(=O)-NH(С1-С6-алкила)2, -C1-C6-алкил-S-C(=S)-NH2, -C1-C6-алкил-S-C(=S)-NH(C1-С6-алкила), -С1-С6-алкил-S-С(=S)-NH(С1-С6-алкила)2, где ациклические R4, R5 радикалы могут быть замещены одним или несколькими Rw заместителями, где циклические R4, R5 радикалы могут быть замещены одним или несколькими Rx заместителями, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл или 3-6-членный гетероцикл, содержащий один гетероатом, выбранный из группы кислорода, азота и серы, где указанный С3-С6-карбоцикл и 3-6-членный гетероцикл могут быть замещены одним или несколькими Rx заместителями, где Rw независимо выбран из группы, состоящей из гидроксила, сульфанила, пентафтор-λ6-сульфанила, С3-С7-циклоалкила, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена, С1-С8-алкокси, С1-С8-галогеноалкокси, имеющего от 1 до 5 атомов галогена, С1-С8-алкилсульфанила, С1-С8-галогеноалкилсульфанила, имеющего от 1 до 5 атомов галогена, где Rx независимо выбран из группы, состоящей из галогена, циано, С1-С8-алкила, С3-С7-циклоалкила, С1-С8-галогеноалкила, имеющего от 1 до 5 атомов галогена, С3-С7-галогеноциклоалкила, имеющего от 1 до 5 атомов галогена;
R6 и R7 независимо выбраны из водорода или R6 и R7 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл;
n представляет собой 0 или 1;
W представляет собой кислород или серу;
Y представляет собой NR8, где R8 выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-галоалкила, С1-С6-цианоалкила, гидрокси, C1-С6-алкокси или С3-С6-карбоцикла;
Z выбран из группы, состоящей из циано, -C(=O)-ORa, -C(=O)-SRa, -С(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, где Ra выбран из группы, состоящей из водорода, С1-С6-алкила, С1-С6-галоалкила, С1-С6-цианоалкила, С2-С6-алкенила, С2-С6-алкинила, С3-С8-циклоалкила, С6-С10-арила, С6-С10-ар-С1-С6-алкила, 4-, 5- или 6-членного неароматического гетероциклила, содержащего 1 гетероатом, выбранный из группы, состоящей из кислорода и серы, -С1-С6-алкил-Si(С1-С6-алкила)3, -С1-С6-алкил-С3-С8-циклоалкила, или Ra может образовывать вместе с R4 и с атомами, к которым они присоединены, 4-7-членный гетероцикл, содержащий один гетероатом, выбранный из группы, состоящей из кислорода и серы, где Rb и Rc независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, циано, С1-С6-цианоалкила, или Rb может образовывать вместе с R4 и с атомами, к которым они присоединены, 4-7-членный гетероцикл, содержащий один гетероатом, выбранный из азота, где Rd и Re независимо выбраны из группы, состоящей из водорода, при условии, что соединения формулы (I) со следующими комбинациями R1, R2 и R3
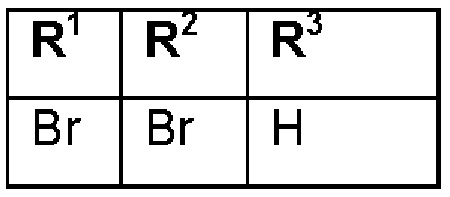
исключены, если R4 и R5 образуют вместе с атомом углерода, к которому они присоединены, С3-карбоцикл, n представляет собой 0, W представляет собой кислород, Y представляет собой NR8, где R8 представляет собой водород.
2. Соединение по п. 1 при условии, что если R1 представляет собой С1-С6-галоалкил или R2 представляет собой С1-С6-галоалкил, и R4 выбран из группы, состоящей из водорода, С1-С6-алкила, и R5 выбран из группы, состоящей из водорода, С1-С6-алкила, и n представляет собой 0, и W представляет собой кислород, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
3. Соединение по п. 1 при условии, что если R4 и R5 независимо выбраны из группы, состоящей из водорода, С1-С6-алкила, С1-С6-гидроксиалкила, С3-С6-карбоцикла, арила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С3-С6-карбоцикла, С1-С6-алкил-O-(С=O)-С1-С6-алкила, -C1-С6-алкил-арила, -С1-С6-алкил-S-С1-С6-алкила, где по меньшей мере один из R4 и R5 представляет собой водород, С1-С6-алкил или С3-С6-карбоцикл, и n представляет собой 0, и W представляет собой кислород, и Y представляет собой NR8, где R8 выбран из группы, состоящей из водорода, C1-С6-алкила, тогда Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa.
4. Соединение по п. 1, где R1 и R2 независимо выбраны из группы, состоящей из F, Cl, Br, I, циано, СН3, и предпочтительно выбраны независимо друг от друга из группы, состоящей из F, Cl, Br, I.
5. Соединение по п. 1, где R3 выбран из группы, состоящей из водорода, F, Cl, Br, I, циано, СН3, CHF2, CF3, и предпочтительно выбран из группы, состоящей из водорода, F, Cl, Br, I, циано, СН3.
6. Соединение по п. 1 со следующими комбинациями R1, R2 и R3
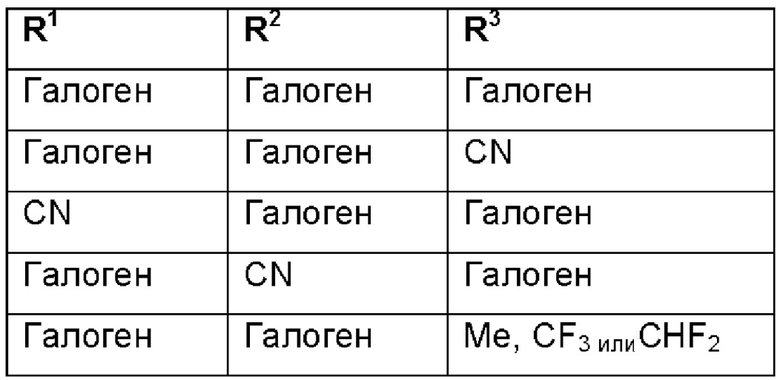
7. Соединение по п. 1, где R4 выбран из группы, состоящей из водорода, C1-С6-алкила, C1-С6-гидроксиалкила, С3-С6-карбоцикла, С(=O)-ОН, -С(=O)-O-С1-С6-алкила, -С1-С6-алкил-С1-С6-алкокси, -С1-С6-алкил-С1-С6-галоалкила, -С1-С6-алкил-С3-С6-карбоцикла, -С1-С6-алкил-арила, -С1-С6-алкил-гидроксиарила, -С1-С6-алкил-S-С1-С6-алкила-, -С1-С6-алкил-С(=O)-NH2, -С1-С6-алкил-С(=O)-O-С1-С6-алкила, R5 выбран из группы, состоящей из водорода, C1-С6-алкила или С3-С6-карбоцикла; или R4 и R5 образуют вместе с атомом водорода, к которому они присоединены, С3-С6-карбоцикл.
8. Соединение по п. 1, где R6 и R7 независимо представляют собой водород.
9. Соединение по п. 1, где n представляет собой 0.
10. Соединение по п. 1, где W представляет собой кислород.
11. Соединение по п. 1, где Y выбран из группы, состоящей из NH, N-OCH3, N-ОН, и предпочтительно NH.
12. Соединение по любому из пп. 1-11, где Z выбран из группы, состоящей из циано, -C(=O)-SRa, -C(=O)-NRbRc, -C(=S)-NRbRc или -C(=O)-NH-CRdRe-C(=O)-ORa, и предпочтительно -C(=O)-ORa.
13. Композиция для борьбы с бактериальными и/или грибковыми заболеваниями растений или частей растений, содержащая по меньшей мере одно соединение формулы (I) по любому из пп. 1-12 и по меньшей мере одно сельскохозяйственно приемлемое вспомогательное вещество.
14. Способ борьбы с бактериальными и/или грибковыми заболеваниями растений, включающий стадию нанесения по меньшей мере одного соединения формулы (I) по любому из пп. 1-12 или композиции по п. 13 на растения, части растения, семена, плоды или в почву, в которой растут растения.
15. Применение соединения по любому из пп. 1-12 или композиции по п. 13 для борьбы с бактериальными и/или грибковыми заболеваниями растений или частей растений.
16. Применение соединения формулы (II) для защиты растения от фитопатогенных грибов и/или бактерий:
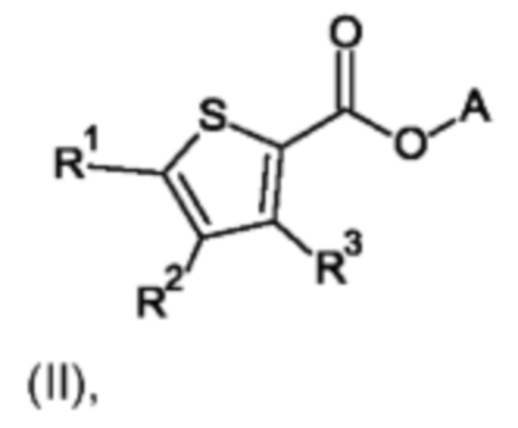
где R1 и R2 независимо друг от друга выбраны из группы, состоящей из галогена, циано, С1-С3-алкила или С1-С3-галоалкила, где по меньшей мере один из R1 или R2 представляет собой галоген;
R3 выбран из группы, состоящей из водорода, галогена, циано, С1-С3-алкила или С1-С3-галоалкила;
А выбран из группы, состоящей из водорода и С1-С6-алкила;
при условии, что соединения формулы (II) со следующими комбинациями R1, R2 и R3
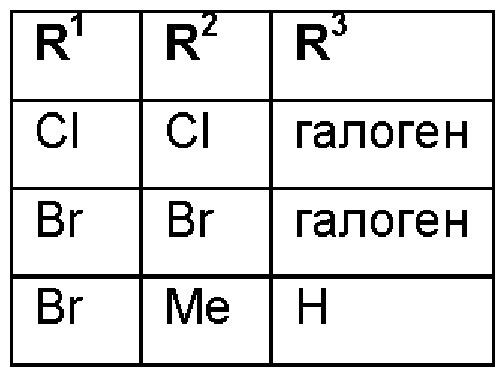
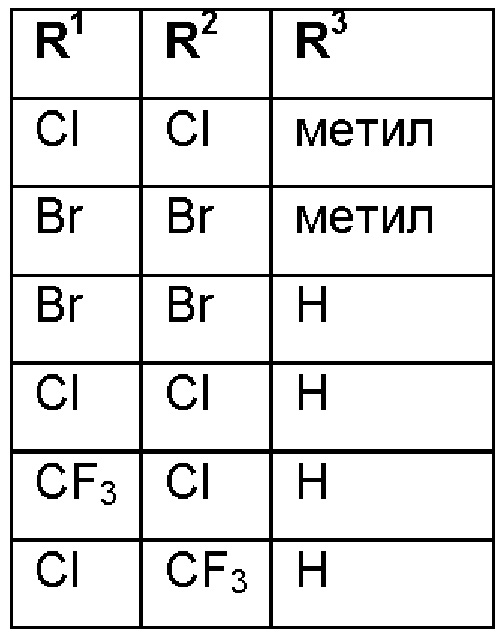
исключены.
17. Применение по п. 16, где R1 и R2 независимо друг от друга выбраны из группы, состоящей из галогена, циано или С1-С3-алкила, где по меньшей мере один из R1 или R2 представляет собой галоген.
18. Применение по любому из пп. 16 или 17, где соединение формулы (II) применяют для борьбы с фитопатогенными грибами и/или бактериями на растениях или частях растения.
19. Соединение формулы (II-А)
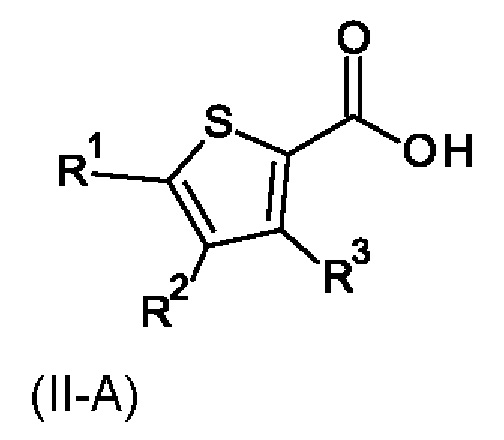 ,
,
где R1 выбран из группы, состоящей из галогена, циано, метила или C1-C2-галоалкила;
R2 выбран из группы, состоящей из галогена, циано или С1-С2-галоалкила;
R3 выбран из группы, состоящей из галогена, циано, метила или С1-С2-галоалкила;
где по меньшей мере два из R1, R2 или R3 представляют собой галоген;
при условии, что соединения формулы (II) со следующими комбинациями R1, R2 и R3
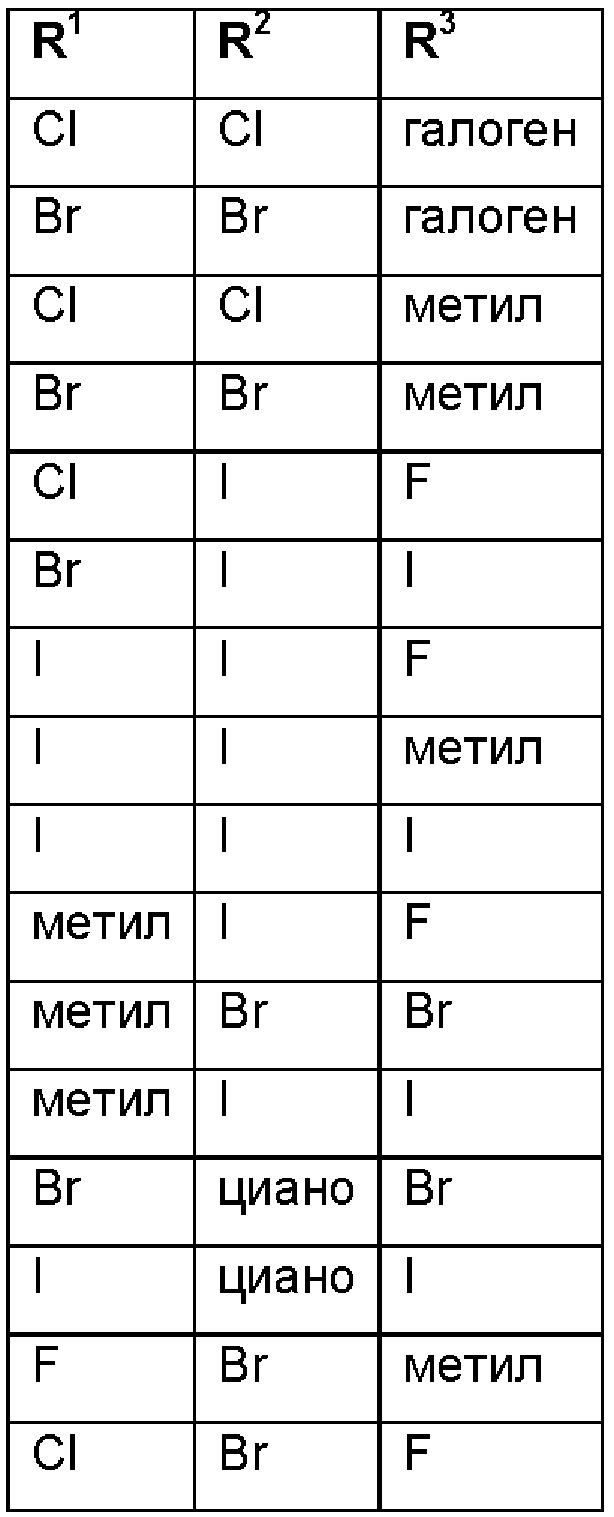
исключены.
| WO 2004024692 A1, 25.03.2004 | |||
| Кольцевой распределитель импульсов | 1972 |
|
SU450355A1 |
| DE 4412333 A1, 12.10.1995 | |||
| HULL J.W | |||
| Jr | |||
| et al, Development of potential manufacturing routes for substituted thiophenes - Preparation of halogenated 2-thiophenecarboxylic acid derivatives as building blocks for a new family of 2,6-dihaloaryl 1,2,4-triazole insecticides, Beilstein Journal of | |||
Авторы
Даты
2025-03-26—Публикация
2020-12-17—Подача