Группа изобретений относится к области аналитической химии и может быть использована для количественного определения антрациклинового препарата доксорубицина в лекарственных препаратах, биологических препаратах и биологических жидкостях человека.
На дату представления заявочных материалов, в мире существует актуальная проблема точного определения концентрации доксорубицина в образцах лекарственных препаратов, биологических препаратах и в биологических жидкостях человека - в плазме крови, моче и желчи, выделяемых человеком при прохождении курса химиотерапевтического лечения онкологических заболеваний с использованием доксорубицина.
Количественное определение доксорубицина обеспечивает возможность решения ряда задач в следующих сферах науки и промышленности:
– медицина: измерение количества доксорубицина в биологических жидкостях человека – в плазме крови, моче и желчи, выделяемых человеком, получающим курс химиотерапевтического лечения онкологических заболеваний, для осуществления контроля влияния препарата на организм и предотвращения нежелательных явлений. При концентрации доксорубицина в плазме крови ниже предполагаемой терапевтической концентрации может быть предположено отсутствие или недостаточность всасывания препарата в кровоток пациента, что говорит о необходимости повышения дозировки доксорубицина или замены на другой лекарственный препарат. В случае концентрации доксорубицина в плазме крови выше предполагаемой терапевтической концентрации, а также при обнаружении концентраций доксорубицина в образцах желчи и мочи выше нормированных, повышается риск возникновения нежелательных явлений, в связи с чем требуется снижение дозировки доксорубицина или замена на другой лекарственный препарат;
– биология и биохимия: измерение количества доксорубицина в рамках изучения свойств и структуры растворов природных образцов ДНК и синтетических ДНК-аптамеров, а также образцов клеток, содержащих ДНК. Доксорубицин взаимодействует с ДНК и ДНК-аптамерами по механизму интеркалирования – встраивания молекулы доксорубицина между основаниями ДНК. Количественное измерение концентрации доксорубицина до и после взаимодействия с ДНК в составе образца молекулы ДНК или ДНК-аптамера или ДНК в составе клетки позволяет получить ряд данных о структуре и биохимических свойствах исследуемого образца;
– фармакология: измерение количества доксорубицина в буферных растворах, модельных образцах искусственных биологических жидкостей и образцах биологических жидкостей, выделяемых человеком (плазма крови, моча, желчь) при проведении рандомизированных контролируемых испытаний новых лекарственных препаратов с активным контролем, в ходе которых доксорубицин используется в качестве сравнительного препарата с доказанной безопасностью и эффективностью. Измерение концентрации доксорубицина в буферных растворах, модельных образцах искусственных биологических жидкостей и образцах биологических жидкостей, выделяемых человеком (плазма крови, моча, желчь) в сравнении с измерением концентрации нового лекарственного препарата в ходе проведения клинических испытаний позволяет выявлять закономерности фармакокинетики и фармакодинамики нового лекарственного препарата, сравнивать их эффективность и безопасность;
– производство лекарственных препаратов: измерение количества доксорубицина в образцах коммерческих препаратов доксорубицина для контроля качества производимых препаратов на предмет наличия в образце заявленной концентрации доксорубицина; проверка отсутствия влияния других компонентов коммерческого препарата на концентрацию доксорубицина в нем – если обнаруженная концентрация доксорубицина окажется меньше заявленной, то это может свидетельствовать о мешающем взаимодействии между другими компонентами препарата и доксорубицином, что требует пересмотра состава лекарственного препарата.
На дату представления заявочных материалов, для количественного определения доксорубицина используется ряд классических инструментальных методов:
– высокоэффективная жидкостная хроматография,
– капиллярный электрофорез,
– УФ-видимая спектрофотометрия,
– флуоресцентная спектрометрия.
Использование данных методов сопряжено с рядом определенных недостатков: трудоёмкость процесса определения, требующего высокой квалификации персонала, высокая стоимость оборудования и расходных материалов.
При этом, в отличие от них, методы электрохимического анализа с использованием электрохимических сенсоров имеют значительные преимущества и характеризуются простотой в эксплуатации, доступностью для использования конечным потребителем, низкой стоимостью оборудования и расходных материалов.
Из исследованного заявителем уровня техники выявлено изобретение по патенту CN107153089B «Способ получения дендроидного нанокомплексного электрохимического сенсора для определения доксорубицина». Сущностью является способ получения дендроидного нанокомплексного электрохимического сенсора для определения доксорубицина, отличающийся тем, что конкретный технологический пакет включает следующие этапы: (1) получение оксида графена посредством использования метода Хаммерса: 1,0 г графита добавляют в 250 мл круглодонную трехгорлую колбу, по каплям добавляют 25 мл карбонизированных графитов в концентрированной серной кислоте, медленно перемешивают для реакции в течение 24 часов, а затем добавляют 1,5 г перманганата калия, трехгорлую колбу переносят на охлаждение в ледяной бане, продолжают перемешивать для реакции в течение 30 минут, затем нагревают до 60°, перемешивают для реакции 45 минут, через каждые 15 минут добавляют 3 мл вторичной дистиллированной воды, после завершения реакции добавляют 180 мл вторичной дистиллированной воды для прекращения реакции, продукт и охлажденный до комнатной температуры раствор фильтруют, из осадка получают путем промывки и сушки оксид графена; (2) лимонную кислоту и гидрокарбонат аммония подвергают термической карбонизации в растворителе для получения углеродных точек: 1,0 грамма лимонной кислоты и 2,0 грамма гидрокарбоната аммония растворяют в 10 миллилитрах диметилсульфоксидов, смешанный раствор переносят в реакционный котел, перемешивают в течение 6 часов, раствор расплавляется при 160°C, после охлаждения жидкости до комнатной температуры добавляют водный раствор гидроксида натрия объемом 20 миллилитров и массовой концентрацией 50 мг/мл, перемешивают до реакции 1 минуту, центрифугируют 10 минут при 16000 об/мин скорости вращения центрифуги, полученный осадок растворяют во вторичной дистиллированной воде, снова центрифугируют, удаляя все кроме осадка соли и щелочи, наконец, при сублимационной сушке получают углеродные точки; (3) углеродные точки, полученные из оксида графена на этапе (1), смешиваются с углеродными точками, полученными на этапе (2), до получения однородной водной дисперсии углеродных точек/оксида графена с массовой концентрацией 1,0–2,0 мг/мл, при этом массовое соотношение углеродных точек и оксида графена составляет 1:5~5:1; (4) В водный раствор нитрата серебра с концентрацией 50 ммоль/л добавляют гидроксид аммония с концентрацией 40 ммоль/л. Водный раствор диамминогидроксида серебра окисляется, водные дисперсии углеродных точек/оксида графена, приготовленные на этапе (3), смешиваются, в результате чего получают однородные водные дисперсии углеродных точек/оксида графена и диамминогидроксида серебра с соотношением массовых концентраций 1:10~10:1; (5) углеродные точки/оксид графена приготовленные на стадии (4) и водные дисперсии диамминогидроксида серебра добавляют в количестве, достаточном для заполнения вещества. 1 ммоль/л буферного раствора из фосфорной кислоты помещают в электрохимическую ячейку, в электрохимическую ячейку помещают стеклоуглеродный электрод, используя метод циклической вольтамперометрии проводят стадию электроосаждения оксида графена и совместного восстановления диамминогидроксида серебра с восстановлением кислорода на границе раздела стеклоуглеродного электрода до графитового алкена и нанозернистого серебра, скорость циклической вольтамперометрии составляет 0 ~ 50 мВ/с и 0 ~ 2,0 В диапазон сканирования потенциала, проводится циклирование в течение 0 ~ 20 циклов с получением трехкомпонентного дендроидного нанометра нанозернистого серебра/углеродных точек/окислительно-восстановительного графена на границе раздела стеклоуглеродный электрод; (6) нанозернистое серебро/углеродные точки/окислительно-восстановительный графен, полученные на этапе (5)/ стеклоуглеродный электрод используются для изготовления сенсора, использующего для измерения сигнала электрохимический профиль дифференциально-импульсной вольтамперометрии, устанавливающей линейную зависимость интенсивность тока окисления Ip (мкА) и концентрации доксорубицина [DOX]: Ip (мкА) = 2,197 + 8,293 [DOX] , где диапазон [DOX] составляет 0~250×10-8 моль/л, то есть получают дендроидный нанокомплексный электрохимический сенсор для определения доксорубицина.
Кратко сущностью является способ изготовления дендроидного нанокомплексного электрохимического сенсора для определения доксорубицина на основе оксида графена, углеродных точек и наночастиц серебра. На поверхность стеклоуглеродного электрода электрохимически (методом циклической вольтамперометрии) осаждают смесь оксида графена, углеродных точек и наночастиц серебра, получая на поверхности стеклоуглеродного электрода дендроидный нанокомплекс. В соответствии со способом изготовления дендроидного нанокомплексного электрохимического сенсора для определения доксорубицина на основе трехкомпонентного дендронизованного нанокомплекса получена конструкция дендроидного нанокомплексного электрохимического сенсора для определения доксорубицина, которая и подвергается анализу. Сенсор представляет собой стеклоуглеродный электрод, на который нанесен слой дендроидного нанокомплекса из оксида графена, углеродных точек и наночастиц серебра. Известный сенсор позволяет проводить определение доксорубицина в растворе в режиме дифференциально-импульсной вольтамперометрии: сенсор демонстрирует линейную зависимость анодного тока от концентрации доксорубицина в диапазоне 1 нМ-5 мкМ с пределом обнаружения 0.3 нМ.
Недостатком известного технического решения в отношении конструкции сенсора. является недостаточно низкий предел обнаружения (0.3 нМ против 1 пМ у заявленного технического решения), узкий диапазон определяемых концентраций (от 1 нМ до 5 мкМ против диапазона определяемых концентраций от 10 мкМ до 1 пМ для заявленного технического решения), сложная процедура создания сенсора за счет использования большого количества реагентов (11 реагентов – графит, карбонизированный графит, серная кислота, перманганат калия, лимонная кислота, гидрокарбонат аммония, диметилсульфоксиды, гидроксид натрия, нитрат серебра, гидроксид аммония, фосфорная кислота против 8 реагентов в заявленном техническом решении – углеродная чернь, ДНК из молок рыбы; калий фосфорнокислый двузамещенный 3-водный, калий хлористый, этанол, пропиленкарбонат, 3,7-бис(фениламино)фенотиазин-5-ия хлорид).
Из исследованного заявителем уровня техники выявлена полезная модель по патенту RU169124 «Амперометрический сенсор для определения антрациклиновых препаратов» для обнаружения и измерения концентрации антрациклиновых препаратов, таких, как доксорубицин в лекарственных препаратах и плазме крови. Сущностью является амперометрический сенсор для определения антрациклиновых препаратов в водном растворе, фармпрепаратах и плазме крови на основе стеклоуглеродного электрода в тефлоновом корпусе, рабочая область которого покрыта слоем электрополимеризованного полианилина, отличающийся тем, что слой электрополимеризованного полианилина включает комплекс ДНК с метиленовым синим.
Известный амперометрический сенсор позволяет проводить определение доксорубицина в растворе в диапазоне определяемых концентраций 5 пМ – 0.1 мМ с пределом обнаружения 5 пМ доксорубицина.
Недостатком известного технического решения является недостаточно низкий предел обнаружения (5 пМ против 1 пМ у заявленного технического решения), недостаточно низкая нижняя граница диапазона определяемых концентраций (5 пМ против 1 пМ у заявленного технического решения).
Из исследованного заявителем уровня техники выявлен источник [Каппо Д., Кузин Ю.И., Шурпик Д.Н., Стойков И.И., Евтюгин Г.А. Вольтамперометрический ДНК-сенсор на основе редокс-активных красителей для определения доксорубицина // Ж. аналит. химии, 2022. – Т.77. - №1. – С. 70-77], в котором описан вольтамперометрический сенсор для определения доксорубицина с использованием вольтамперометрического сенсора. Сущностью прототипа является вольтамперометрический сенсор для определения доксорубицина в водном растворе и синтетической плазме крови на основе стеклоуглеродного электрода в тефлоновом корпусе, рабочая область которого покрыта слоем дисперсии углеродной черни в хитозане, пиллар[5]ареном, электрополимеризованного поли(нейтрального красного) и ДНК, включаемой на стадии электрополимеризации красителя. В буферный раствор для проведения измерений дополнительно вводят метиленовый синий. Полимерная пленка поли(нейтрального красного) выполнена путем электроосаждения из раствора нейтрального красного, содержащего ДНК, в течение 9.5 циклов сканирования потенциала. Для определения доксорубицина электрохимический сенсор устанавливают рабочей поверхностью вверх, наносят раствор доксорубицина на рабочую поверхность для инкубирования. После этого сенсор промывают и погружают в электрохимическую ячейку с буферным раствором. Затем в ячейку добавляют раствор метиленового синего и снимают циклическую вольтамперограмму. Аналитическим сигналом является величина тока пика поли(нейтрального красного). Устройство позволяет проводить определение доксорубицина с пределом обнаружения 3 нМ в диапазоне определяемых концентраций от 10 нМ до 0.1 мМ.
Недостатком известного технического решения является:
1. Недостаточно низкий предел обнаружения – 3 нМ против 1 пМ для заявленного технического решения.
2. Узкий диапазон определяемых концентраций – от 10 нМ до 0.1 мМ против диапазона определяемых концентраций от 10 мкМ до 1 пМ для заявленного технического решения.
3. Сложная конструкция сенсора, включающая большое количество не связанных друг с другом электродов против объединенных в заявленном техническом решении рабочего электрода, электрода сравнения и вспомогательного электрода в единое устройство на основе печатного графитового электрода, выполненного методом трафаретной печати.
4. Сложная процедура создания сенсора за счет использования большого количества реагентов – 13 реагентов – ДНК из молок рыбы, нейтральный красный (n8,n8,3-триметилфеназин-2,8-диамин хлорид), метиленовый синий (3,7-бисдиметиламинофенотиазина хлорид), хитозан, углеродная чернь, пиллар[5]арен, NaH2PO4, NaNO3, Na2SO4, HCl, NaOH, ацетон, дистиллированная вода против 8 реагентов в заявленном техническом решении – углеродная чернь, ДНК из молок рыбы; калий фосфорнокислый двузамещенный 3-водный, калий хлористый, этанол, пропиленкарбонат, 3,7-бис(фениламино)фенотиазин-5-ия хлорид.
5. Высокая продолжительность времени анализа из-за необходимости инкубирования сенсора в растворе аналита перед непосредственным проведением анализа против отсутствия необходимости инкубировать сенсор перед проведением анализа в заявленном техническом решении.
Выявленные аналоги совпадают с заявленным техническим решением по отдельным совпадающим признакам, поэтому прототип не выявлен, и формула изобретения составлена без ограничительной части.
Технической проблемой, решаемой заявленным техническим решением, и его техническим результатом является устранение недостатков аналогов, преимущественно [Каппо Д., Кузин Ю.И., Шурпик Д.Н., Стойков И.И., Евтюгин Г.А. Вольтамперометрический ДНК-сенсор на основе редокс-активных красителей для определения доксорубицина // Ж. аналит. химии, 2022. – Т.77. - №1. – С. 70-77], а именно:
1. Снижение предела обнаружения за счет присутствия в определяемом растворе полиэлектролитного комплекса, состоящего из биокомпонента – ДНК – и 3,7-бис(фениламино)фенотиазин-5-ия хлорида, повышающего чувствительность сенсора к взаимодействию с доксорубицином.
2. Расширение диапазона определяемых концентраций за счет присутствия в определяемом растворе полиэлектролитного комплекса, состоящего из биокомпонента – ДНК – и 3,7-бис(фениламино)фенотиазин-5-ия хлорида, повышающего чувствительность сенсора к взаимодействию с доксорубицином.
3. Упрощение конструкции сенсора за счет объединения рабочего электрода, электрода сравнения и вспомогательного электрода в единое устройство на основе печатного графитового электрода, выполненного методом трафаретной печати;
4. Упрощение процедуры создания сенсора за счет использования малого количества реагентов.
5. Снижение продолжительности времени анализа за счет отсутствия необходимости инкубирования сенсора в растворе аналита.
Сущностью заявленного технического решения является электрохимический сенсор для определения доксорубицина, содержащий планарный графитовый электрод, выполненный на основе из полиэфирной прозрачной пленки неправильной формы, содержащей круглую часть с возможностью нанесения круглой капли и прямоугольную часть с возможностью присоединения к потенциостату-гальваностату; на основу из полиэфирной прозрачной пленки нанесены по всей длине с выступом на 20 мм проводящие серебряные дорожки из полимерной серебряной пасты; в центре круглой части основы из полиэфирной прозрачной пленки выполнен рабочий электрод из углеграфитовой пасты в форме круга диаметром 2.2 мм; по краям круглой части основы из полиэфирной прозрачной пленки выполнены вспомогательный электрод из углеграфитовой пасты в форме полукруга и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl в форме полосы; при этом проводящие серебряные дорожки из полимерной серебряной пасты, рабочий электрод из углеграфитовой пасты, вспомогательный электрод из углеграфитовой пасты и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl закреплены на поверхности основы из полиэфирной прозрачной пленки изоляционным слоем из синей диэлектрической пасты с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты не покрытыми изоляционным слоем из синей диэлектрической пасты для возможности присоединения их к потенциостату-гальваностату; на поверхность рабочего электрода из углеграфитовой пасты нанесена и высушена при 100 °С дисперсия углеродной черни в пропиленкарбонате; поверх дисперсии углеродной черни в пропиленкарбонате нанесена капля объемом 10 мкл, содержащая 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида. Способ изготовления электрохимического сенсора для определения доксорубицина по п.1, заключающийся в том, что берут основу из полиэфирной прозрачной пленки, наносят на нее по всей длине с выступом на 20 мм электропроводящие серебряные дорожки из полимерной серебряной пасты; в центр круглой части основы из полиэфирной прозрачной пленки наносят рабочий электрод из углеграфитовой пасты в форме круга диаметром 2.2 мм; по краям круглой части основы из полиэфирной прозрачной пленки наносят вспомогательный электрод из углеграфитовой пасты, сформированный в форме полукруга; далее наносят псевдоэлектрод сравнения из полимерной пасты Ag/AgCl в форме полосы; далее проводящие серебряные дорожки из полимерной серебряной пасты, рабочий электрод из углеграфитовой пасты, вспомогательный электрод из углеграфитовой пасты и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl закрепляют на поверхности фиг.основы из полиэфирной прозрачной пленки изоляционным слоем, выполненным из синей диэлектрической пасты с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты не покрытыми изоляционным слоем из синей диэлектрической пасты для возможности присоединения их к потенциостату-гальваностату; на поверхность рабочего электрода из углеграфитовой пасты наносят и высушивают при 100 °С дисперсию углеродной черни в пропиленкарбонате, поверх которой наносят каплю объемом 10 мкл, содержащую 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Заявленное техническое решение иллюстрируется Фиг.1, Фиг.2.
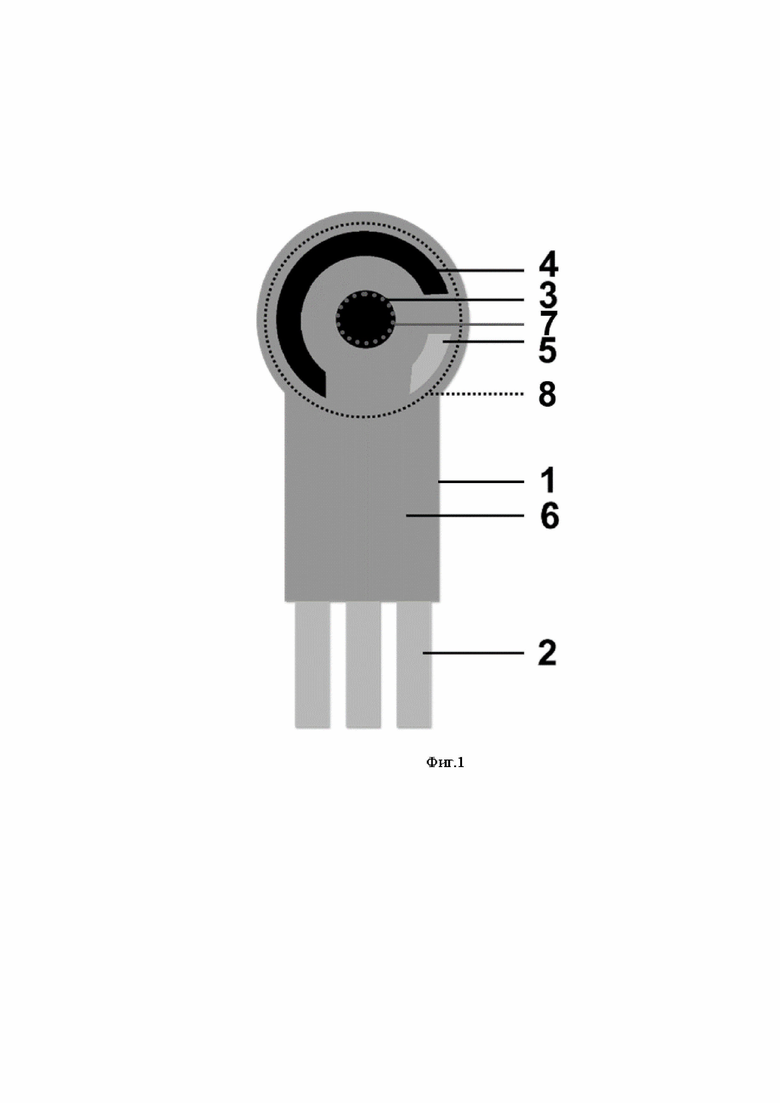
На Фиг.1 приведена конструкция заявленного электрохимического сенсора, где:
1 – основа из полиэфирной прозрачной пленки,
2 – проводящие серебряные дорожки из полимерной серебряной пасты,
3 – рабочий электрод из углеграфитовой пасты,
4 – вспомогательный электрод из углеграфитовой пасты,
5 – псевдоэлектрод сравнения из полимерной пасты Ag/AgCl,
6 – изоляционный слой из синей диэлектрической пасты,
7 – дисперсия углеродной черни в пропиленкарбонате,
8 – капля объемом 10 мкл, содержащая 0.01 м фосфатного буферного раствора, состоящем из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
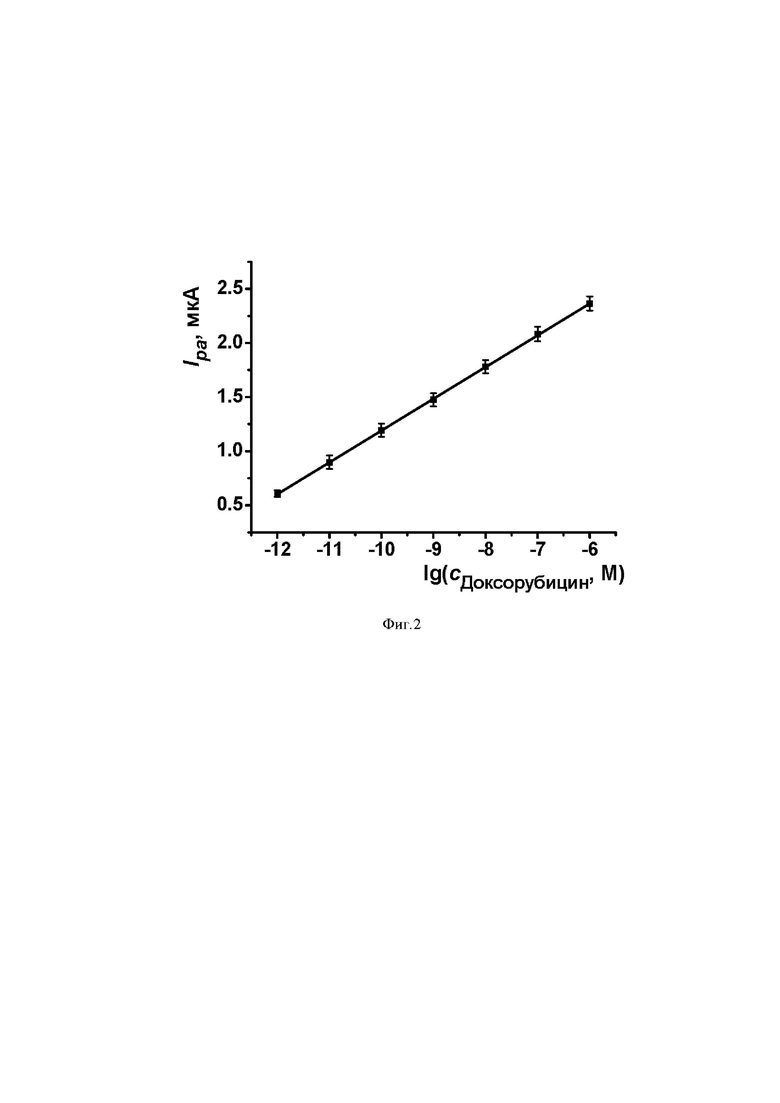
На Фиг.2 приведена градуировочная зависимость определения доксорубицина в водном растворе на заявленном электрохимическом сенсоре.
Далее заявителем приведено описание заявленного технического решения.
Заявленный электрохимический сенсор предназначен для определения концентрации доксорубицина после проведения измерения в анализируемом объекте: для полученного значения тока пика окисления находят соответствующее значение логарифма концентрации доксорубицина, из которого рассчитывают значение концентрации доксорубицина, которую необходимо определять, например, в следующих сферах науки и промышленности: в медицине при измерении количества доксорубицина в биологических жидкостях человека – в плазме крови, моче и желчи, выделяемых человеком, получающим курс химиотерапевтического лечения онкологических заболеваний, для осуществления контроля влияния препарата на организм и предотвращения нежелательных явлений; в биологии и биохимии в рамках изучения свойств и структуры растворов природных образцов ДНК и синтетических ДНК-аптамеров, а также образцов клеток, содержащих ДНК; в фармакологии при измерении количества доксорубицина в буферных растворах, модельных образцах искусственных биологических жидкостей и образцах биологических жидкостей, выделяемых человеком (плазма крови, моча, желчь) при проведении рандомизированных контролируемых испытаний новых лекарственных препаратов с активным контролем, в ходе которых доксорубицин используется в качестве сравнительного препарата с доказанной безопасностью и эффективностью; в производстве лекарственных препаратов при измерении количества доксорубицина в образцах коммерческих препаратов доксорубицина для контроля качества производимых препаратов на предмет наличия в образце заявленной концентрации доксорубицина и при проверке отсутствия влияния других компонентов коммерческого препарата на концентрацию доксорубицина в нем.
Заявителем использованы следующие реагенты:
- дистиллированная вода по ГОСТ Р 58144–2018;
- углеродная чернь «ENSACO® 250G CARBON BLACK» марки «IMERYS S.A.», Франция, с зернистостью 0.6 ppm, площадью поверхности 66 м2/г, проводимостью 1.0 мкСм/см по ГОСТ 7885-86;
- ДНК из молок рыбы марки «Sigma Aldrich» по ГОСТ 21571–2014;
- калий фосфорнокислый двузамещенный 3-водный по ГОСТ 2493–75;
- калий хлористый по ГОСТ 4568–95;
- этанол по ГОСТ 5962–2013;
- пропиленкарбонат по стандарту Фармакопеи США 1576504;
- 3,7-бис(фениламино)фенотиазин-5-ия хлорид получают по методике [A.I. Khadieva, V.V. Gorbachuk, I.I. Stoikov. Synthesis and supramolecular self-assembly of phenothiazine functionalized by carboxyphenyl fragments. / Russian Chemical Bulletin, 2020 г., Т. 69, №1, с. 333-338.]:
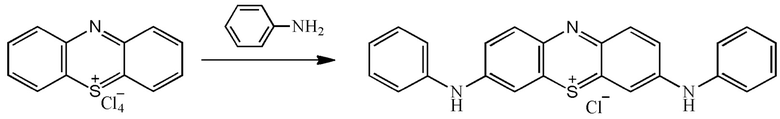
Заявителем использованы следующие материалы и оборудование:
- потенциостат-гальваностат «PGSTAT AutoLab 320N», «Metrohm AG», Швейцария;
- полуавтомат трафаретной печати «DEK 248», «DEK», Великобритания;
- рН-метр-иономер «Эксперт-001» со стеклянным рН-метрическим электродом «ЭВЛ-1М3.1», ЗАО НПП «Эконикс-Эксперт», Россия;
- дозаторы «ThermoFischer», ЗАО «Ленпипет», Россия;
- полиэфирная прозрачная пленка «Lomond PE DS Laser Film» (толщина 125 мкм), «Lomond Trading Ltd», остров Мэн;
- полимерная серебряная паста PSP-2, ООО "НПП ДЕЛЬТА-ПАСТЫ", Россия;
- полимерная паста Ag/AgCl PSCP-1, ООО "НПП ДЕЛЬТА-ПАСТЫ", Россия;
- углеграфитовая паста C2030519P4, «Gwent Group», Великобритания;
- синяя диэлектрическая паста D21440114D5, «Gwent Group», Великобритания.
Заявленный технический результат достигается разработкой электрохимического сенсора для определения доксорубицина и способа его изготовления.
Заявленный электрохимический сенсор содержит планарный графитовый электрод, выполненный методом трафаретной печати на основе из полиэфирной прозрачной пленки 1 неправильной формы, содержащей круглую часть с возможностью нанесения круглой капли и прямоугольную часть с возможностью присоединения к потенциостату-гальваностату.
На основу из полиэфирной прозрачной пленки 1 нанесены по всей длине с выступом на 20 мм проводящие серебряные дорожки из полимерной серебряной пасты 2.
В центре круглой части основы из полиэфирной прозрачной пленки 1 выполнен рабочий электрод из углеграфитовой пасты 3 в форме круга диаметром 2.2 мм.
По краям круглой части основы из полиэфирной прозрачной пленки 1 выполнены вспомогательный электрод из углеграфитовой пасты 4 в форме полукруга и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl 5 в форме полосы.
При этом проводящие серебряные дорожки из полимерной серебряной пасты 2, рабочий электрод из углеграфитовой пасты 3, вспомогательный электрод из углеграфитовой пасты 4 и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl 5 закреплены на поверхности основы из полиэфирной прозрачной пленки 1 изоляционным слоем из синей диэлектрической пасты 6 с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты 2 не покрытыми изоляционным слоем из синей диэлектрической пасты 6 для возможности присоединения их к любому коммерчески доступному потенциостату-гальваностату.
На поверхность рабочего электрода из углеграфитовой пасты 3 нанесена и высушена при 100 °С дисперсия углеродной черни в пропиленкарбонате 7.
Поверх дисперсии углеродной черни в пропиленкарбонате 7 нанесена капля 8, объемом 10 мкл, содержащая 0.01 М фосфатного буферного раствора состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Заявленный способ изготовления заявленного электрохимического сенсора заключается в том, что;
– берут основу из полиэфирной прозрачной пленки 1,
– наносят на нее (например, с помощью полуавтомата трафаретной печати «DEK 248», «DEK», Великобритания) по всей длине с выступом на 20 мм электропроводящие серебряные дорожки, выполненные из полимерной серебряной пасты 2;
– в центр круглой части основы из полиэфирной прозрачной пленки 1 наносят (например, с помощью полуавтомата трафаретной печати «DEK 248», «DEK», Великобритания) рабочий электрод из углеграфитовой пасты 3 в форме круга диаметром 2.2 мм;
– по краям круглой части основы из полиэфирной прозрачной пленки 1 наносят, (например, с помощью полуавтомата трафаретной печати «DEK 248», «DEK», Великобритания) вспомогательный электрод из углеграфитовой пасты 4, сформированный в форме полукруга, далее наносят (например, с помощью полуавтомата трафаретной печати «DEK 248», «DEK», Великобритания) псевдоэлектрод сравнения из полимерной пасты Ag/AgCl 5 в форме полосы;
– далее проводящие серебряные дорожки из полимерной серебряной пасты 2, рабочий электрод из углеграфитовой пасты 3, вспомогательный электрод из углеграфитовой пасты 4 и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl 5 закрепляют (например, с помощью полуавтомата трафаретной печати «DEK 248», «DEK», Великобритания) на поверхности основы из полиэфирной прозрачной пленки 1 изоляционным слоем, выполненным из синей диэлектрической пасты 6 с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты 2 не покрытыми изоляционным слоем из синей диэлектрической пасты 6 для возможности присоединения их к любому коммерчески доступному потенциостату-гальваностату (например, потенциостату-гальваностату «PGSTAT AutoLab 320N», «Metrohm AG», Швейцария);
– на поверхность рабочего электрода из углеграфитовой пасты 3 наносят дозатором (например, дозатором «ThermoFischer», ЗАО «Ленпипет», Россия) и высушивают при 100 °С дисперсию углеродной черни в пропиленкарбонате 7, поверх которой наносят дозатором (например, дозатором «ThermoFischer», ЗАО «Ленпипет», Россия) каплю 8 объемом 10 мкл, содержащую 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида, при этом рН определяют, например рН-метром-иономером «Эксперт-001» со стеклянным рН-метрическим электродом «ЭВЛ-1М3.1», ЗАО НПП «Эконикс-Эксперт», Россия.
Далее заявителем приведены примеры осуществления заявленного технического решения.
Пример 1. Использование заявленного электрохимического сенсора, изготовленного по заявленному способу, содержащего 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 1 мг/мл ДНК из молок рыбы, 0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Заявленный электрохимический сенсор изготавливают по описанному выше заявленному способу, при этом капля 8 объемом 10 мкл (объем капли определяют, исходя из геометрических характеристик планарного графитового электрода) содержит 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 1 мг/мл ДНК из молок рыбы и 0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Для определения концентрации доксорубуцина вначале строят градуировочную зависимость в координатах «ток пика окисления, мкА – логарифм концентрации доксорубицина, М».
Для этого на поверхность электрохимического сенсора наносят дозатором каплю 8 и аликвоту раствора доксорубицина, например, концентрации 1 пМ, и регистрируют с помощью любого коммерчески доступного потенциостата-гальваностата, например, потенциостата-гальваностата «PGSTAT AutoLab 320N», «Metrohm AG», Швейцария, дифференциально-импульсную вольтамперограмму в диапазоне потенциалов от минус 800 до 0 мВ при шаге потенциала 4 мВ, амплитуде 50 мВ, ширине импульса 0.06 с, интервале импульса 0.5 с.
Затем повторяют последовательность действий по предыдущему абзацу, изменяя последовательно концентрацию раствора доксорубицина в аликвоте, например, до 1 мкМ. Вольтамперометрические измерения проводят после каждого добавления доксорубицина различной концентрации в каплю. Измеряют ток пика окисления 3,7-бис(фениламино)фенотиазин-5-ия хлорида. Аналитическим сигналом является величина тока пика окисления 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Строят градуировочную зависимость в координатах «ток пика окисления, мкА – логарифм концентрации доксорубицина, М» (см. Фиг.2).
Далее проводят определение доксорубицина в рабочей пробе.
Для этого на поверхность электрохимического сенсора наносят дозатором каплю 8 и аликвоту определяемой пробы раствора доксорубицина, и регистрируют с помощью любого коммерчески доступного потенциостата-гальваностата, например, потенциостата-гальваностата «PGSTAT AutoLab 320N», «Metrohm AG», Швейцария, дифференциально-импульсную вольтамперограмму в диапазоне потенциалов от минус 800 до 0 мВ при шаге потенциала 4 мВ, амплитуде 50 мВ, ширине импульса 0.06 с, интервале импульса 0.5 с.
Определяют ток пика окисления 3,7-бис(фениламино)фенотиазин-5-ия хлорида. Для полученного значения тока пика окисления 3,7-бис(фениламино)фенотиазин-5-ия хлорида по градуировочной зависимости находят соответствующее значение логарифма концентрации доксорубицина, из которого рассчитывают значение концентрации доксорубицина.
Воспроизводимость сигнала составляет 2.3±0.5%. Устройство позволяет проводить определение доксорубицина с пределом обнаружения 1 пМ доксорубицина с интервалом определяемых концентраций от 1 мкМ до 1 пМ.
Пример 2. Использование заявленного электрохимического сенсора, содержащего 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5 мг/мл ДНК из молок рыбы, 0.07 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Заявленный электрохимический сенсор изготавливают по описанному выше заявленному способу, отличающийся тем, что берут каплю 8, содержащую 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0,5 мг/мл ДНК из молок рыбы и 0.07 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
Проводят последовательность действий по Примеру 1.
Воспроизводимость сигнала составляет 3.5±0.5%. Устройство позволяет проводить определение доксорубицина с пределом обнаружения 1 пМ доксорубицина с интервалом определяемых концентраций от 1 мкМ до 1 пМ.
Таким образом, заявителем решена выявленная техническая проблема и достигнут заявленный технический результат, а именно:
1. Снижен предел обнаружения за счет присутствия в определяемом растворе полиэлектролитного комплекса (состоящего из биокомпонента – ДНК, и 3,7-бис(фениламино)фенотиазин-5-ия хлорида), образованного за счет множественных взаимодействий заряженных групп, что повышает чувствительность сенсора к взаимодействию с доксорубицином – предел обнаружения снизился от 3 нМ до 1 пМ по Примерам 1 и 2.
2. Расширен диапазон определяемых концентраций за счет присутствия в определяемом растворе полиэлектролитного комплекса (состоящего из биокомпонента – ДНК, и 3,7-бис(фениламино)фенотиазин-5-ия хлорида), образованного за счет множественных взаимодействий заряженных групп, что повышает чувствительность сенсора к взаимодействию с доксорубицином – от диапазона определяемых концентраций 10 нМ до 0.1 мМ к диапазону определяемых концентраций от 10 мкМ до 1 пМ по Примерам 1 и 2;
3. Упрощена конструкция сенсора за счет объединения рабочего электрода, электрода сравнения и вспомогательного электрода в единое устройство на основе печатного графитового электрода, выполненного методом трафаретной печати;
4. Упрощена процедура создания сенсора за счет использования малого количества реагентов – от 13 до 8 реагентов – углеродная чернь, ДНК из молок рыбы; калий фосфорнокислый двузамещенный 3-водный, калий хлористый, этанол, пропиленкарбонат, 3,7-бис(фениламино)фенотиазин-5-ия хлорид.
5. Снижена продолжительность времени анализа за счет отсутствия необходимости инкубирования сенсора в растворе аналита и проведения анализа непосредственно после добавления аликвоты доксорубицина в каплю.
Заявленное техническое решение соответствует условию патентоспособности «новизна», предъявляемому к изобретениям, т.к. заявленная совокупность признаков не выявлена из исследованного уровня техники и не известны технические результаты, которые реализованы в заявленном техническом решении.
Заявленное техническое решение соответствует условию патентоспособности «изобретательский уровень», предъявляемому к изобретениям, поскольку не выявлены технические решения, имеющие признаки, совпадающие с отличительными признаками данного изобретения, и не установлена известность влияния отличительных признаков на полученные технические результаты.
Заявленное техническое решение соответствует условию патентоспособности «промышленная применимость», предъявляемому изобретениям, так как может быть реализовано с помощью известных приемов на известном оборудовании.
| название | год | авторы | номер документа |
|---|---|---|---|
| Универсальное устройство для проточного электрохимического анализа для твердотельных и планарных электродов и способ его изготовления (варианты) | 2025 |
|
RU2839556C1 |
| Тест-полоска для определения содержания этилового спирта в крови электрохимическим способом с помощью портативной амперометрической ячейки | 2019 |
|
RU2713111C1 |
| Вольтамперометрический способ качественного анализа меда | 2023 |
|
RU2829902C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОХИМИЧЕСКОГО КАТАЛИЗАТОРА НА ОСНОВЕ ВОССТАНОВЛЕННОГО ЗОЛОТА | 2021 |
|
RU2784199C1 |
| ГИДРОЗОЛЬ ДЛЯ ФОРМИРОВАНИЯ ПОКРЫТИЙ ЭЛЕКТРОХИМИЧЕСКИХ ПЕРОКСИДЧУВСТВИТЕЛЬНЫХ СЕНСОРОВ И БИОСЕНСОРОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЭЛЕКТРОХИМИЧЕСКИЙ СЕНСОР И БИОСЕНСОР, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2419785C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ИНДИКАЦИИ ИММУНОХИМИЧЕСКИ АКТИВНЫХ МАКРОМОЛЕКУЛ В ИССЛЕДУЕМЫХ РАСТВОРАХ | 1997 |
|
RU2107296C1 |
| МОДИФИЦИРОВАННОЕ ГАЛЬВАНИЧЕСКОЕ СЕРЕБРЯНОЕ ПОКРЫТИЕ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2551327C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СЕНСОРОВ ДЛЯ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ САХАРОВ И ГИДРОКСИКИСЛОТ | 2016 |
|
RU2639494C1 |
| Способ изготовления газового мультисенсора кондуктометрического типа на основе оксида олова | 2016 |
|
RU2626741C1 |
| СПОСОБ ОЦЕНКИ МЕТАБОЛИЧЕСКОЙ АКТИВНОСТИ КЛЕТОК И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2011 |
|
RU2460767C1 |
Изобретение относится к области аналитической химии и может быть использовано для количественного определения антрациклинового препарата доксорубицина в лекарственных препаратах, биологических препаратах и биологических жидкостях человека. Электрохимический сенсор для определения доксорубицина содержит планарный графитовый электрод, выполненный на основе из полиэфирной прозрачной пленки неправильной формы, содержащей круглую часть с возможностью нанесения круглой капли и прямоугольную часть с возможностью присоединения к потенциостату-гальваностату. На основу из полиэфирной прозрачной пленки нанесены по всей длине с выступом на 20 мм проводящие серебряные дорожки из полимерной серебряной пасты. В центре круглой части основы из полиэфирной прозрачной пленки выполнен рабочий электрод из углеграфитовой пасты в форме круга диаметром 2.2 мм. По краям круглой части основы из полиэфирной прозрачной пленки выполнены вспомогательный электрод из углеграфитовой пасты в форме полукруга и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl в форме полосы. При этом проводящие серебряные дорожки из полимерной серебряной пасты, рабочий электрод из углеграфитовой пасты, вспомогательный электрод из углеграфитовой пасты и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl закреплены на поверхности основы из полиэфирной прозрачной пленки изоляционным слоем из синей диэлектрической пасты с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты не покрытыми изоляционным слоем из синей диэлектрической пасты для возможности присоединения их к потенциостату-гальваностату. На поверхность рабочего электрода из углеграфитовой пасты нанесена и высушена при 100°С дисперсия углеродной черни в пропиленкарбонате. Поверх дисперсии углеродной черни в пропиленкарбонате нанесена капля объемом 10 мкл, содержащая 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида. Техническим результатом является снижение предела обнаружения и продолжительности времени анализа, расширение диапазона определяемых концентраций, упрощение конструкции сенсора и процедуры изготовления сенсора. 2 н.п. ф-лы, 2 ил.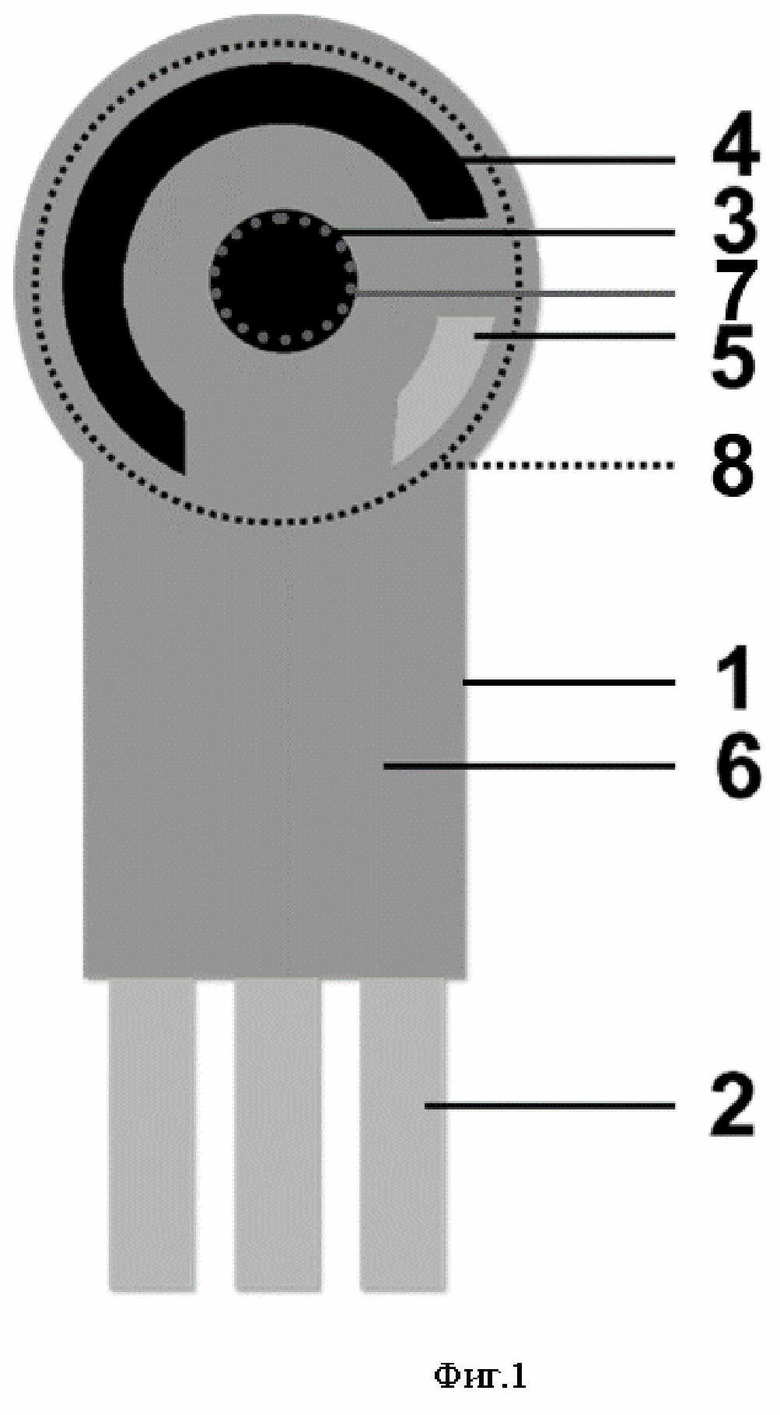
1. Электрохимический сенсор для определения доксорубицина, содержащий планарный графитовый электрод, выполненный на основе из полиэфирной прозрачной пленки неправильной формы, содержащей круглую часть с возможностью нанесения круглой капли и прямоугольную часть с возможностью присоединения к потенциостату-гальваностату;
на основу из полиэфирной прозрачной пленки нанесены по всей длине с выступом на 20 мм проводящие серебряные дорожки из полимерной серебряной пасты;
в центре круглой части основы из полиэфирной прозрачной пленки выполнен рабочий электрод из углеграфитовой пасты в форме круга диаметром 2.2 мм;
по краям круглой части основы из полиэфирной прозрачной пленки выполнены вспомогательный электрод из углеграфитовой пасты в форме полукруга и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl в форме полосы;
при этом проводящие серебряные дорожки из полимерной серебряной пасты, рабочий электрод из углеграфитовой пасты, вспомогательный электрод из углеграфитовой пасты и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl закреплены на поверхности основы из полиэфирной прозрачной пленки изоляционным слоем из синей диэлектрической пасты с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты не покрытыми изоляционным слоем из синей диэлектрической пасты для возможности присоединения их к потенциостату-гальваностату;
на поверхность рабочего электрода из углеграфитовой пасты нанесена и высушена при 100°С дисперсия углеродной черни в пропиленкарбонате;
поверх дисперсии углеродной черни в пропиленкарбонате нанесена капля объемом 10 мкл, содержащая 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
2. Способ изготовления электрохимического сенсора для определения доксорубицина по п.1, заключающийся в том, что
берут основу из полиэфирной прозрачной пленки, наносят на нее по всей длине с выступом на 20 мм электропроводящие серебряные дорожки из полимерной серебряной пасты;
в центр круглой части основы из полиэфирной прозрачной пленки наносят рабочий электрод из углеграфитовой пасты в форме круга диаметром 2.2 мм;
по краям круглой части основы из полиэфирной прозрачной пленки наносят вспомогательный электрод из углеграфитовой пасты, сформированный в форме полукруга;
далее наносят псевдоэлектрод сравнения из полимерной пасты Ag/AgCl в форме полосы;
далее проводящие серебряные дорожки из полимерной серебряной пасты, рабочий электрод из углеграфитовой пасты, вспомогательный электрод из углеграфитовой пасты и псевдоэлектрод сравнения из полимерной пасты Ag/AgCl закрепляют на поверхности основы из полиэфирной прозрачной пленки изоляционным слоем, выполненным из синей диэлектрической пасты с оставлением части проводящих серебряных дорожек из полимерной серебряной пасты не покрытыми изоляционным слоем из синей диэлектрической пасты для возможности присоединения их к потенциостату-гальваностату;
на поверхность рабочего электрода из углеграфитовой пасты наносят и высушивают при 100°С дисперсию углеродной черни в пропиленкарбонате, поверх которой наносят каплю объемом 10 мкл, содержащую 0.01 М фосфатного буферного раствора, состоящего из 0.01 М калия фосфорнокислого двузамещенного 3-водного, 0.1 М калия хлористого и 50 об.% этанола, рН=7.0, 0.5-1 мг/мл ДНК из молок рыбы и 0.07-0.15 мМ 3,7-бис(фениламино)фенотиазин-5-ия хлорида.
| КАППО Д | |||
| И ДР | |||
| "ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ ДНК-СЕНСОР НА ОСНОВЕ РЕДОКС-АКТИВНЫХ КРАСИТЕЛЕЙ ДЛЯ ОПРЕДЕЛЕНИЯ ДОКСОРУБИЦИНА", ЖУРНАЛ АНАЛИТИЧЕСКОЙ ХИМИИ, Т.77, N1, С | |||
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРОЦЕЛЛЮЛОЗНЫХ ЛАКОВ ДЛЯ ЭМАЛЕЙ И ПОКРЫТИЙ НА ИХ ОСНОВЕ | 0 |
|
SU169124A1 |
| CN 107153089 B, 08.03.2019 | |||
| Прибор для экспериментального контактирования насекомых с обработанной инсектицидами поверхностью | 1949 |
|
SU82336A1 |
Авторы
Даты
2025-04-14—Публикация
2024-11-05—Подача