ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] В данной заявке заявлен приоритет предварительной заявки на патент США № 62/942624, поданной 2 декабря 2019 года, полное содержание которой включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Данное описание относится к области высокомолекулярных косметологических композиций, таких как гидрогели, содержащие поперечно-сшитые полисахариды, а также к применению таких гидрогелей в медицинских и/или косметических областях применения, таких как имплантаты для подкожной или внутрикожной инъекции, которые можно использовать для людей в реконструктивной или пластической хирургии и в косметической дерматологии. Более конкретно, данное описание относится к гидрогелям, содержащим поперечно-сшитые высокомолекулярные гликозаминогликаны (ГАГ), в частности, поперечно-сшитую гиалуроновую кислоту, хондроитин или сульфат хондроитина.
УРОВЕНЬ ТЕХНИКИ
[0003] Гидрогели широко используют в медицине, их получают посредством химического сшивания полимеров с образованием больших полимерных сетей. Тогда как и мономерные, и минимально полимеризованные полисахариды абсорбируют воду до точки насыщения, полисахариды растворяются в точке насыщения, а гидрогели, содержащие те же полисахариды, будучи поперечно-сшитыми, обычно могут абсорбировать воду без растворения, что приводит к набуханию гидрогеля.
[0004] Все гликозаминогликаны (ГАГ) представляют собой отрицательно заряженные длинные линейные гетерополисахариды, которые обладают способностью абсорбировать большое количество воды. Гиалуроновая кислота, хондроитин и сульфат хондроитина являются известными биосовместимыми ГАГ, используемыми в медицинской и косметической областях применения. Одним из наиболее широко применяемых биосовместимых полимеров для медицинского применения является гиалуроновая кислота и ее производные. Модификация молекул гиалуроновой кислоты посредством поперечного сшивания и другими способами необходима для увеличения продолжительности сохранения гиалуроновой кислоты in vivo, например, посредством поперечного сшивания гиалуроновой кислоты с образованием гидрогеля гиалуроновой кислоты.
[0005] Получение гидрогелей из высокомолекулярных ГАГ, таких как гиалуроновая кислота, обеспечивает подходящий наполнитель для многих типов медицинского или косметического применения; однако указанные гидрогели могут разлагаться или гидролизоваться при хранении или в условиях, вызывающих разложение, таких как тепловая стерилизация или ускоренные испытания стабильности. Способы увеличения стабильности гидрогелей включают увеличение количества поперечных связей в гидрогелях, но увеличение количества поперечных связей высокомолекулярных ГАГ может приводить к образованию гидрогелей, которые стабильны в условиях, вызывающих разложение, но приводят к разделению фаз гидрогеля. В результате возникает проблема дальнейшего разбавления гидрогелей без разделения фаз.
[0006] Задача данного описания заключается в преодолении проблем, связанных с получением гидрогелей из высокомолекулярных ГАГ, которые демонстрируют повышенную стабильность и способны сохранять целостность гидрогеля в условиях, вызывающих разложение, таких как тепловая стерилизация, при сохранении возможности разбавления гидрогелей до требуемой концентрации ГАГ для таких применений как наполнение шприцов гидрогелями.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] Данное описание, в целом, относится к способам получения гидрогеля из поперечно-сшитых высокомолекулярных гликозаминогликанов (ГАГ), способного сохранять структурную целостность в таких условиях, которые в противном случае приводят к гидролизу гидрогеля или разделению фаз гидрогеля. Данное описание дополнительно относится к композициям гидрогеля, полученным предложенными способами.
[0008] В некоторых аспектах данное описание, в целом, относится к способу получения гидрогеля, содержащего поперечно-сшитые молекулы гликозаминогликана (ГАГ), указанный способ включает (a) поперечное сшивание ГАГ, имеющего молекулярную массу по меньшей мере 1,5 МДа, сшивающим агентом, причем концентрация ГАГ составляет от 2% до 10% (мас./мас.), и молярное отношение сшивающего агента к ГАГ составляет менее или ровно 2%, с получением гликозаминогликанового гидрогеля, поперечно-сшитого амидными связями.
[0009] В некоторых аспектах, если концентрация ГАГ на стадии (a) составляет от 1% до 4,5% (мас./мас.), то концентрация сшивающего агента составляет от 0,8 до 2% мол. относительно дисахарида ГАГ; и если концентрация ГАГ на стадии (a) составляет от 4,6% до 5,9% (мас./мас.), то концентрация сшивающего агента составляет от 0,5 до 0,8% мол. относительно дисахарида ГАГ; и если концентрация ГАГ на стадии (a) составляет от 6% до 12% (мас./мас.), то концентрация сшивающего агента составляет от 0,3 до 0,5% мол. относительно дисахарида ГАГ.
[0010] В некоторых аспектах сшивающий агент на стадии (a) представляет собой ди- или полинуклеофильный функциональный сшивающий агент. В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент представляет собой алифатическое или ароматическое диамино-производное, пептид или пептидную последовательность. В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент содержит спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов. В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент представляет собой диаминотрегалозу (DATH).
[0011] В некоторых аспектах поперечное сшивание на стадии (a) включает: a1) обеспечение или получение раствора молекул гликозаминогликана (ГАГ); a2) активацию карбоксильных групп в молекулах гликозаминогликана с помощью связующего агента с получением активированных молекул гликозаминогликана; и a3) поперечное сшивание активированных молекул гликозаминогликана (ГАГ) через их активированные карбоксильные группы с использованием ди- или полинуклеофильного функционального сшивающего агента с получением гликозаминогликанового гидрогеля, поперечно-сшитого амидными связями. В некоторых аспектах связующий агент, используемый на стадии a2), представляет собой связующий агент на основе триазина, такой как хлорид 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния (DMTMM).
[0012] В некоторых аспектах сшивающий агент на стадии (a) представлен при рН 5,0-9,0, предпочтительно при рН 6,0-8,0. В некоторых аспектах предложенные способы дополнительно включают составление композиции поперечно-сшитого гидрогеля, полученного на стадии (a), с конечной концентрацией гликозаминогликана (ГАГ) 10-30 мг/мл. В некоторых аспектах предложенные способы дополнительно включают (b) стерилизацию поперечно-сшитого гидрогеля, полученного на стадии (a).
[0013] В некоторых аспектах гликозаминогликан (ГАГ) представляет собой гиалуроновую кислоту (ГК). В некоторых аспектах ГАГ на стадии (a) имеет молекулярную массу 2,0-10 МДа, предпочтительно 2,5-3,5 МДа. В некоторых аспектах концентрация ГАГ составляет 3-5% (мас./мас.). В некоторых аспектах молярное отношение сшивающего агента к ГАГ составляет 0,9-1,1%. В некоторых аспектах ГАГ представляет собой гиалуроновую кислоту (ГК), имеющую молекулярную массу 2,5-3,5 МДа, а сшивающий агент представляет собой диаминотрегалозу (DATH), и при этом концентрация ГК составляет 3-5% (мас./мас.), а молярное отношение DATH к ГК составляет 0,9-1,1%.
[0014] В некоторых аспектах данное описание, в целом, относится к гидрогелевому продукту, полученному любым из способов, описанных в данном документе. В некоторых аспектах данное описание, в целом, относится к гидрогелевому продукту, содержащему молекулы гликозаминогликана (ГАГ) в качестве способного к набуханию полимера, причем молекулы гликозаминогликана поперечно-сшиты амидными связями, и при этом кажущаяся молекулярная масса (ММкаж.) поперечно-сшитых молекул гликозаминогликана составляет более 1,0 МДа; и при этом термостабильность способного к набуханию полимера (норм. Cгеля) составляет более 80% через 24 часа.
[0015] В некоторых аспектах молекулы гликозаминогликана ковалентно сшиты поперечными связями, содержащими спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов. В некоторых аспектах спейсерная группа представляет собой трегалозу. В некоторых аспектах гликозаминогликан (ГАГ) представляет собой гиалуроновую кислоту (ГК). В некоторых аспектах гидрогелевый продукт является стерилизованным.
[0016] В соответствии с одним или более из любых предшествующих аспектов, ГАГ не имеет молекулярную массу менее 1,5 МДа или необязательно менее 1,4 МДа, 1,3 МДа, 1,2 МДа, 1,1 МДа, 1,0 МДа, 0,9 МДа, 0,8 МДа или 0,7 МДа.
[0017] В соответствии с одним или более из любых предшествующих аспектов, гидрогель не подвержен разложению гликозаминогликана после поперечного сшивания. В соответствии с одним или более из любых предшествующих аспектов, гидрогель подвержен разложению в условиях окружающей среды после поперечного сшивания; однако гидрогель не демонстрирует значение Cmin менее Cкон./2. В соответствии с одним или более из любых предшествующих аспектов, гидрогель демонстрирует значение Cmin более Cкон./2 данного гидрогеля.
[0018] В некоторых аспектах стадии (a) и (b) осуществляют поэтапно, от (a) к (b). В некоторых аспектах a1), a2) и a3) осуществляют поэтапно, от a1) к a2) к a3). В некоторых аспектах стадии (a) и (b) не осуществляют поэтапно от (a) к (b). В некоторых аспектах a1), a2) и a3) не осуществляют поэтапно от a1) к a2) к a3).
[0019] В некоторых аспектах данное описание, в целом, относится к способу косметического лечения кожи, который включает введение в кожу гидрогелевого продукта в соответствии с одной из любых гидрогелевых композиций, описанных в данном документе.
[0020] Следующее подробное описание является иллюстративным и пояснительным, и оно предназначено для дополнительного объяснения данного изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
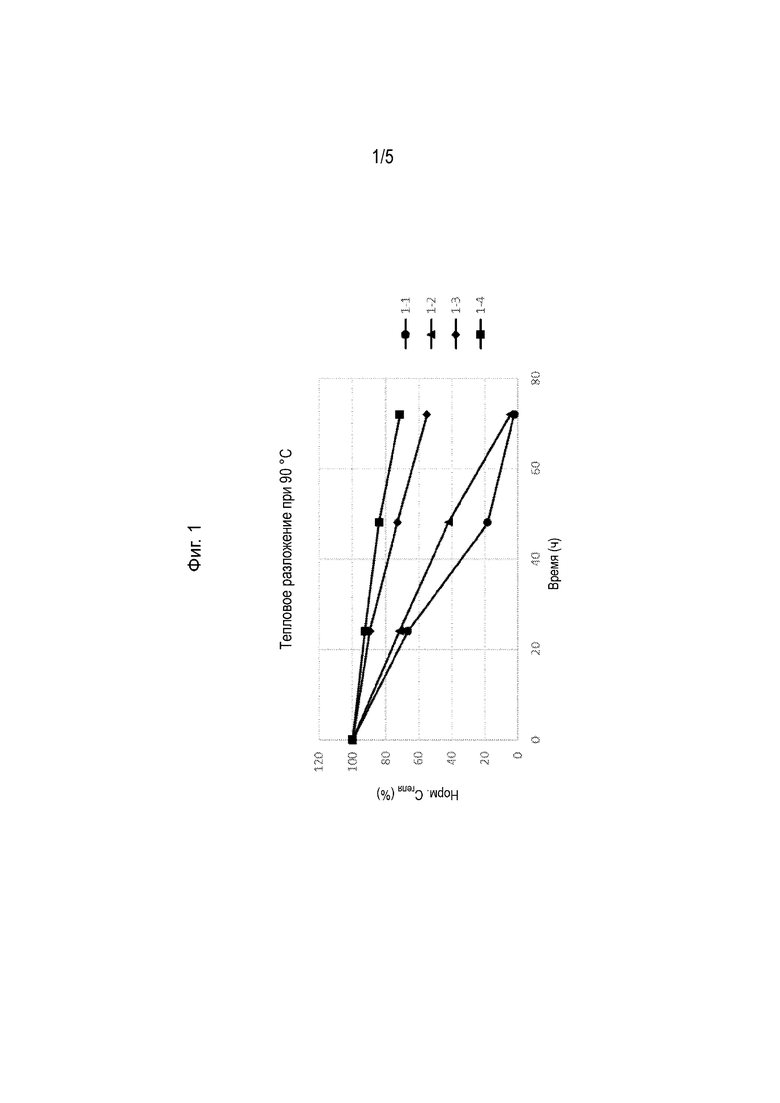
[0021] На Фиг. 1 представлено нормализованное содержание геля (норм. Cгеля (%)) для четырех образцов геля, содержащих различные ГК (ММ) и имеющих различное поперечное сшивание ГК в течение приблизительно 70 часов при 90 °С.
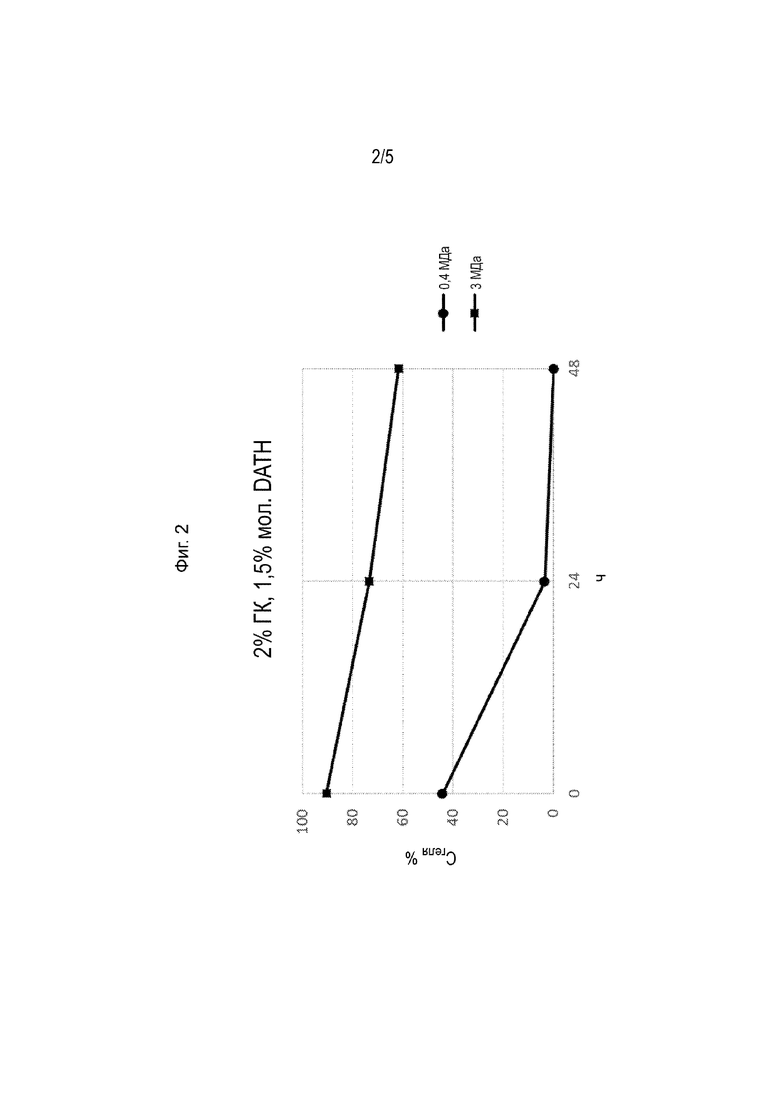
[0022] На Фиг. 2 показано содержание геля (Cгеля %), соответствующее образцам 1 и 2 в таблице 2, после инкубации гелей при 90 °С в течение 24 или 48 часов.
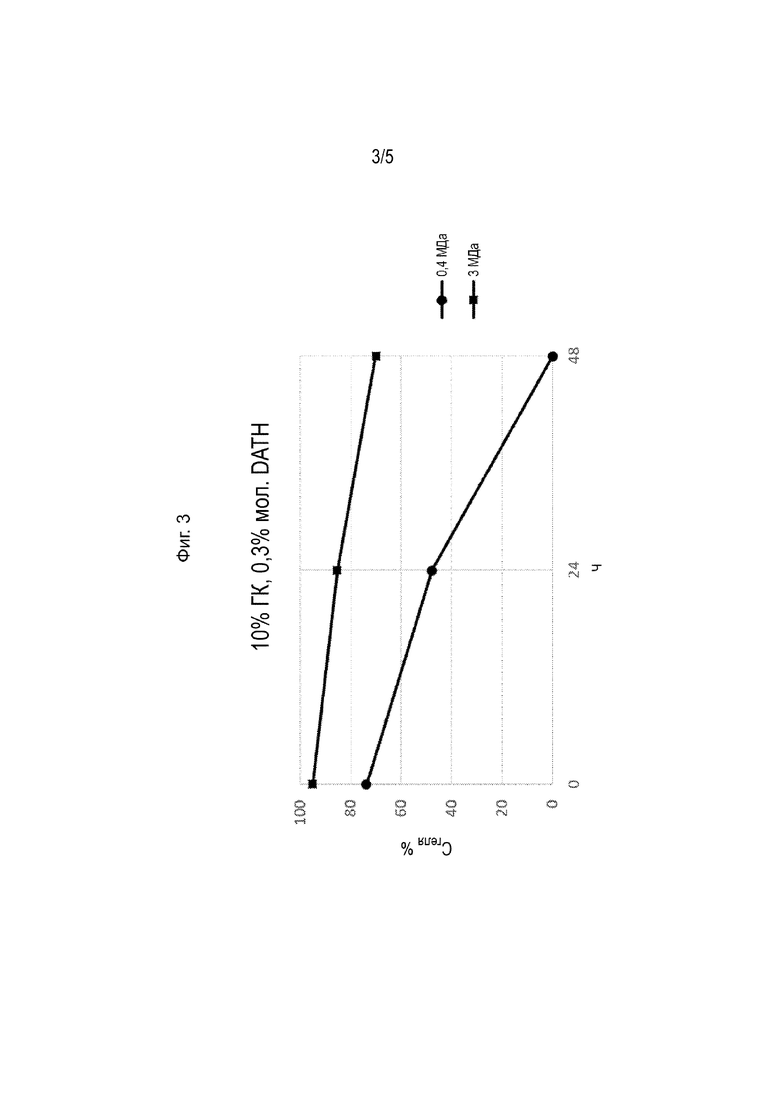
[0023] На Фиг. 3 показано содержание геля (Cгеля %), соответствующее образцам 3 и 4 в таблице 2, после инкубации гелей при 90 °С в течение 24 или 48 часов.
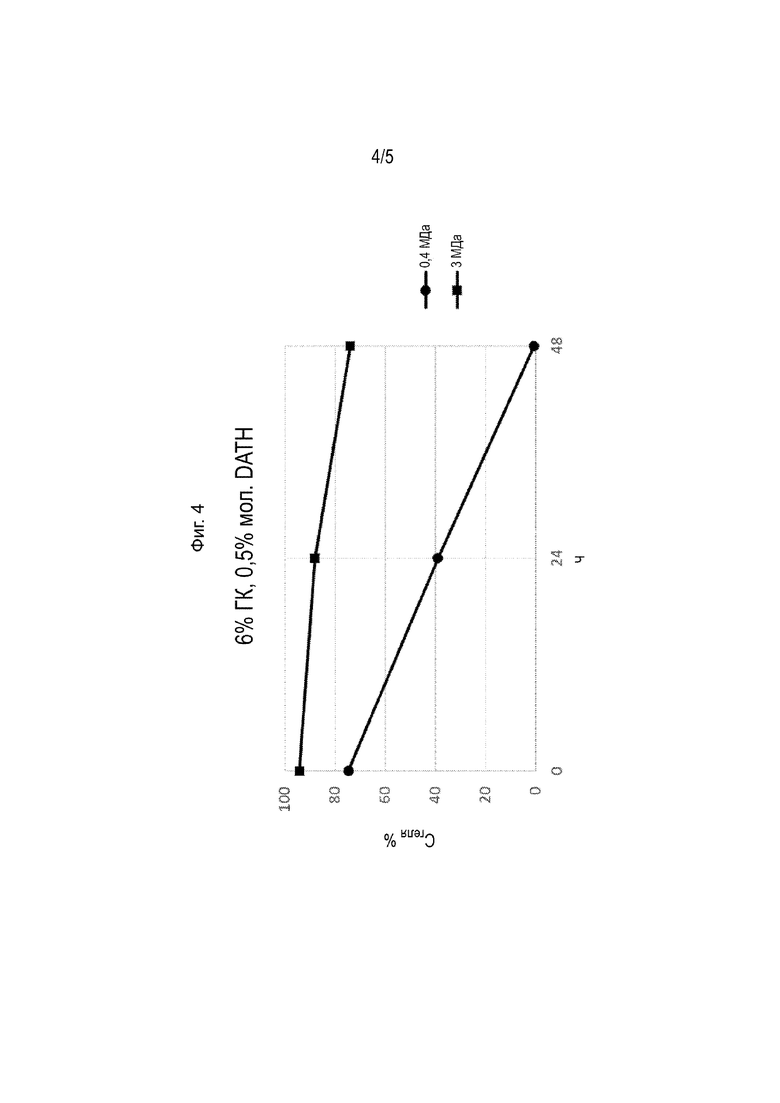
[0024] На Фиг. 4 показано содержание геля (Cгеля %), соответствующее образцам 5 и 6 в таблице 2, после инкубации гелей при 90 °С в течение 24 или 48 часов.
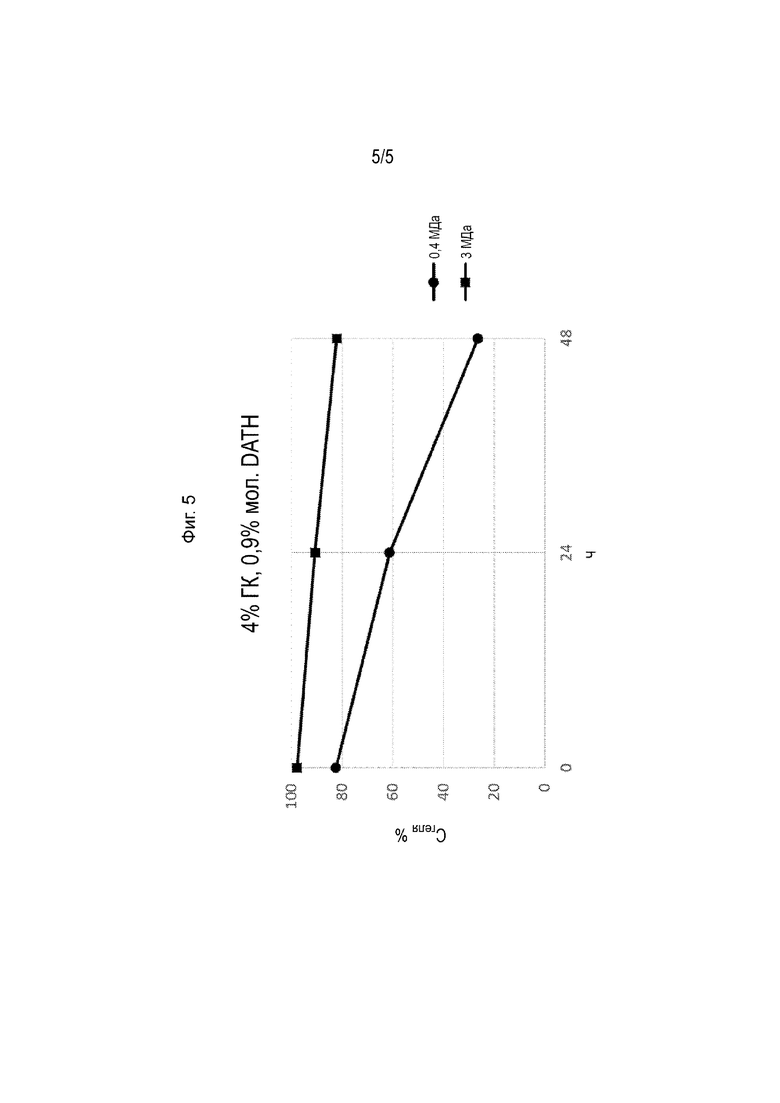
[0025] На Фиг. 5 показано содержание геля (Cгеля %), соответствующее образцам 7 и 8 в таблице 2, после инкубации гелей при 90 °С в течение 24 или 48 часов.
Подробное описание изобретения
Определения
[0026] Несмотря на то, что следующие термины предположительно хорошо известны специалистам в данной области техники, представленные ниже определения приведены для облегчения пояснения описанного объекта данного изобретения.
[0027] Термины в форме единственного числа могут относиться к одному или более указанным элементам, т.е. могут относиться к форме множественного числа. Таким образом, термины в единственном числе, «один или более» и «по меньшей мере один» использованы в данном контексте взаимозаменяемо. Кроме того, ссылка на «элемент» в единственном числе не исключает возможность присутствия более чем одного из указанных элементов, если в контексте очевидно не предусмотрено наличие одного и только одного из элементов.
[0028] Упоминание в тексте данного описания «одного варианта реализации», «варианта реализации», «одного аспекта» или «аспекта» означает, что конкретный признак, структура или характеристика, описанная в отношении указанного варианта реализации, включена в по меньшей мере один вариант реализации данного описания. Таким образом, появление выражений «в одном варианте реализации» или «в варианте реализации» в различных местах данного описания не обязательно относится к одному и тому же варианту реализации. Кроме того, конкретные признаки, структуры или характеристики могут быть объединены любым подходящим образом в одном или более вариантах реализации.
[0029] В данном контексте термины «около» или «приблизительно», предшествующие числовому значению, обозначают указанное значение плюс или минус диапазон 10% от указанного значения.
[0030] Специалистам в данной области техники для любых и всех целей, в частности, в отношении обеспечения письменного описания, понятно, что все диапазоны, описанные в данном документе, охватывают также любые и все возможные поддиапазоны и комбинации поддиапазонов. Любой перечисленный диапазон может быть легко распознан как в достаточной степени описывающий и дающий возможность разделения некоторых диапазонов на по меньшей мере равные половины, трети, четверти, пятые доли, десятые доли и т.д. В качестве неограничивающего примера, каждый диапазон, описанный в данном документе, может быть легко разделен на нижнюю треть, среднюю треть и верхнюю треть и т.д. Специалистам в данной области техники понятно также, что выражения типа «до», «по меньшей мере», «более чем», «менее чем» и т.п. включают указанное значение и относятся к диапазонам, которые могут быть затем разбиты на поддиапазоны, как описано выше. Наконец, специалистам в данной области техники понятно, что диапазон включает каждый отдельный элемент. Так, например, группа, содержащая 1-3 клетки, относится к группам, содержащим 1, 2 или 3 клетки. Аналогично, группа, содержащая 1-5 клеток, относится к группам, содержащим 1, 2, 3, 4 или 5 клеток, и т.д.
[0031] В данном контексте «контроль» представляет собой альтернативный образец, использованный в эксперименте в целях сравнения. Контроль может быть «положительным» или «отрицательным». «Контрольный образец» или «эталонный образец» в данном контексте относится к образцу или эталону, который действует как контроль для сравнения с экспериментальным образцом. Например, экспериментальный образец содержит соединение A, B и C во флаконе, а контроль может быть образцом такого же типа, обработанным так же, как экспериментальный образец, но без одного или более из соединений A, B или C.
[0032] В данном контексте термин «эффективное количество» относится к количеству, достаточному для достижения требуемого терапевтического и/или профилактического эффекта, например, к количеству, которое приводит к предотвращению одного или более исходов или к усилению одного или более исходов.
[0033] В данном контексте термины «индивидуум», «пациент» или «субъект» могут представлять собой отдельный организм, позвоночное, млекопитающее или человека. В предпочтительном аспекте индивидуумом, пациентом или субъектом является человек.
[0034] В данном контексте термин «мягкая ткань» относится к тканям, которые соединяют, поддерживают или окружают другие структуры и органы тела. Мягкая ткань включает мышцы, фиброзные ткани и жир.
[0035] В данном контексте выражение «наращивание мягкой ткани» относится к любому типу объемного наращивания мягких тканей, включая, но не ограничиваясь ими, пластику контура лица (например, более выраженные щеки, подбородок или губы), коррекцию вогнутых деформаций (например, посттравматических или липоатрофии на фоне ВИЧ) и коррекцию глубоких возрастных морщин лица. Таким образом, наращивание мягкой ткани может быть использовано в косметических целях или в медицинских целях, например, вследствие травмы или дегенеративного заболевания. Наращивание мягкой ткани дополнительно относится к дермальному филлингу, пластике контуров тела и гингивальному филлингу.
[0036] В данном контексте выражение «неживотного происхождения» относится к источнику, исключающему животных, но включает такие источники как дрожжи, бактерии или синтетический способ получения.
[0037] В данном контексте термин «биорассасывающийся» относится к явлению или явлениям разрушения: биорассасывающиеся вещества могут растворяться, подвергаться фагоцитозу или могут просто распадаться в течение какого-либо времени, в результате чего такие вещества выводятся из организма, органа, ткани, области или клетки в течение определенного периода времени. Такие вещества или продукты их разложения могут метаболизироваться, встраиваться в другие молекулы или соединения или экскретироваться.
[0038] В данном контексте термин «асептический» относится к чему-либо, не содержащему патогенных микроорганизмов или освобожденному от них.
[0039] В данном контексте термин «стерильный» относится к чему-либо, не содержащему живых организмов, обычно не содержащему живых микроорганизмов.
[0040] В данном контексте термин «пригодный для инъекций» относится к возможности инъекции композиции по данному описанию через иглу.
[0041] В данном контексте термины «ММ» или «Mw» относится к средневесовой молекулярной массе.
[0042] В данном контексте термин «ММкаж.» относится к кажущейся ММ, которая представляет собой смоделированное значение для молекулярной массы ГАГ в гидрогелях.
[0043] В данном контексте термин «SwF» относится к анализу набухаемости в солевом растворе, которая представляет собой объем солевого раствора на 1 грамм геля, набухшего до своего максимума, обычно выражаемый в мл/г.
[0044] В данном контексте «содержание геля» или «Cгеля» относится к проценту в содержании общей ГК, которая связана в форму геля - дополнительно описывается как количество ГК в образце, которая не проходит через фильтр с размером пор 0,22 мкм. Cгеля рассчитывают по количеству ГК, собранной в фильтрате, и записывают в процентах от общего количества ГК в образце геля.
[0045] В данном контексте «SwD» относится к степени набухания, которая является обратной концентрацией гелеобразной формы ГАГ в геле, полностью набухшем в 0,9% солевом растворе, т.е. представляет собой объем или массу полностью набухшего геля, который может быть получен из одного грамма сухого поперечно-сшитого ГАГ. Обычно SwD описывает максимальную способность продукта к абсорбции жидкости (0,9% солевого раствора). Предпочтительно, SwD выражают в г/г, мл/г или как безразмерное значение.
SwD=масса (полностью набухшего геля)
масса (гелеобразной формы ГАГ в полностью набухшем геле)
[0046] SwD также может быть выражен как
SwD=[ГАГ] * Cгеля
SwF
[0047] В данном контексте «CrRDATH» относится к эффективной степени поперечного сшивания, измеренную с помощью анализа ЖХ-ГПХ-МС, более конкретно, определенную как
CrR=моль сшитого сшивающего агента с амидными связями
моль связанного сшивающего агента с амидными связями
[0048] Значение CrR 1,0 означает, что весь сшивающий агент является поперечно-сшитым.
[0049] В данном контексте «Cmin» представляет собой минимальную теоретическую концентрацию ГАГ, концентрацию гелеобразной формы ГАГ в геле, полностью набухшем в 0,9% солевом растворе, обычно выраженную в мг/г или мг/мл.
Cmin-1=SwD
[0050] В данном контексте «Cкон.» представляет собой предполагаемую концентрацию ГАГ в конечном гидрогелевом продукте. В некоторых аспектах Cкон. составляет более 2 x Cmin.
[0051] Предложенная технология также не ограничена конкретными аспектами, описанными в данной заявке, которые предназначены в качестве отдельных иллюстраций некоторых аспектов предложенной технологии. Многочисленные модификации и вариации предложенной технологии могут быть сделаны без отклонения от сущности и объема изобретения, как понятно специалистам в данной области техники. Функционально эквивалентные способы и устройства, входящие в объем предложенной технологии, помимо тех, которые перечислены в настоящем документе, очевидны для специалистов в данной области техники из изложенного выше описания. Предусмотрено, что такие модификации и варианты входят в границы объема предложенной технологии. Следует понимать, что предложенная технология не ограничена конкретными способами, реагентами, соединениями, композициями или биологическими системами, которые, безусловно, могут варьироваться. Следует также понимать, что используемая в данном документе терминология предназначена лишь для описания конкретных вариантов реализации, и ее не следует толковать как ограничивающую.
II. Гидрогели и способы получения гидрогелей
[0052] Филлеры, такие как дермальные филлеры, используют для восстановления, реконструкции или наращивания дефектов контура твердой или мягкой ткани тела вследствие старения, травмы или приобретенных или врожденных деформаций лица, тела и внутренних органов. Филлеры могут представлять собой природные или синтетические вещества, которые используют для уменьшения морщин и/или тонких морщин, восстановления утраченного объема, увлажнения кожи, смягчения носогубных складок, наращивания и пластики контура губ, улучшения состояния рубцов (атрофических, гипертрофических и келоидных рубцов), укрепления ослабленных голосовых связок и обеспечения других улучшений мягких тканей. Используемые вещества включают жир, парафин, человеческий коллаген, бычий коллаген, кремнийорганические соединения, гиалуроновые кислоты, молочные кислоты и гликолевые кислоты. В 1981 году после одобрения FDA бычьего коллагена началась новая эра филлеров для мягких тканей. С тех пор появилось много филлеров для мягких тканей. Значительное увеличение количества известных и экспериментальных филлеров было вызвано многими факторами, включая достижения в области биотехнологии и акцент на внешнюю привлекательность в обществе. С появлением новых филлеров появилась постоянная потребность в оценке их профилей риск/польза и в определении их ограничений с целью максимизации косметического результата и безопасности для пациента. Обычные композиции филлеров/гидрогелей содержат ГАГ, такие как гиалуроновая кислота.
[0053] Способы получения гидрогелей ГАГ описаны в публикациях PCT с номерами WO2017/114867, WO2017/114861, WO2017/114864 и WO2017/114865; в предварительных публикациях США с номерами US20190023812A1, US20190016830A1, US20190023855A1 и US20070066816A1; и в заявках на патент США с номерами 8858999, 6831172, 8887243 и 6703444.
[0054] Обычным способом поперечного сшивания гиалуроновой кислоты является использование диглицидилового эфира, например, диглицидилового эфира бутандиола (BDDE). В качестве альтернативы, перспективным способом получения поперечно-сшитых молекул гиалуроновой кислоты, подходящих для гидрогелевых продуктов, является амидное связывание с использованием ди- или полиаминного функционального сшивающего агента вместе со связующим агентом. Например, показано, что использование хлорида 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния (DMTMM) для активации карбоксилата и последующей конденсации с диамино-структурой, например, диаминотрегалозой (DATH), является эффективным способом получения гидрогелей, состоящий из поперечно-сшитой гиалуроновой кислоты с незначительным разложением биополимера.
[0055] В некоторых аспектах поперечное сшивание осуществляют с помощью сшивающих агентов, содержащих спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов. В результате получают гидрогелевый продукт, полностью основанный на углеводных структурах или их производных, что минимизирует нарушение нативных свойств ГАГ, используемых для получения гидрогеля, вследствие поперечного сшивания.
[0056] В некоторых аспектах сам сшивающий агент способствует сохранению или усилению свойств гидрогеля, например, при поперечном сшивании с использованием структуры, коррелирующей с гиалуроновой кислотой (например, тетрасахарида диаминогиалуроновой кислоты), или при поперечном сшивании с использованием структуры с высокими водоудерживающими свойствами (например, трегалозы).
[0057] В некоторых аспектах ГАГ представляет собой сульфатированный или несульфатированный ГАГ, такой как гиалуронан, сульфат хондроитина, сульфат гепарана, гепарозан, гепарин, сульфат дерматана и сульфат кератана. В некоторых аспектах ГАГ представляет собой гиалуроновую кислоту, хондроитин или сульфат хондроитина. В одном аспекте ГАГ представляет собой гиалуроновую кислоту. В некоторых аспектах ГАГ представляет собой нативный ГАГ. В некоторых аспектах ГАГ представляет собой природный ГАГ. В некоторых аспектах ГАГ используют в его нативном состоянии (т.е. химическая структура ГАГ не изменена или не модифицирована посредством присоединения функциональных групп или т.п.). Использование ГАГ в его нативном состоянии является предпочтительным, поскольку это обеспечивает возможность получения поперечно-сшитой структуры, больше похожей на природные молекулы, которая сохраняет нативные свойства и эффекты самого ГАГ, и может минимизировать иммунный ответ при введении поперечно-сшитого ГАГ в организм.
[0058] В некоторых аспектах ГАГ являются ковалентно поперечно-сшитыми. В некоторых аспектах ковалентно поперечно-сшитые молекулы ГАГ состоят или по существу состоят из структур углеводного типа или их производных. В некоторых аспектах поперечно-сшитые ГАГ или гидрогели не содержат или по существу не содержат синтетические неуглеводные структуры или линкеры. Это может быть достигнуто посредством применения ГАГ в его нативном состоянии вместе со сшивающим агентом, который содержит, состоит или по существу состоит из структур углеводного типа или их производных. В некоторых аспектах функциональные группы сшивающего агента ковалентно связаны непосредственно с карбоксильными группами ГАГ. В некоторых аспектах поперечные связи ковалентно поперечно-сшитых ГАГ содержат, состоят или по существу состоят из ди-, три-, тетра- и олигосахаридных спейсерных групп.
[0059] В некоторых аспектах поперечно-сшитый ГАГ содержит поперечные связи между цепями молекул ГАГ, которые создают непрерывную сеть молекул ГАГ, удерживаемых вместе ковалентными поперечными связями.
[0060] В некоторых аспектах поперечно-сшитые ГАГ под действием жидкости, обычно водной жидкости, образуют гель или гидрогель - не растворимую в воде, но существенно разбавленную поперечно-сшитую систему ГАГ.
[0061] В некоторых аспектах способ получения гидрогелевого продукта, содержащего поперечно-сшитые молекулы гликозаминогликана, включает, состоит или по существу состоит из: (a) обеспечения раствора молекул гликозаминогликана; (b) активации карбоксильных групп в молекулах гликозаминогликана с помощью сшивающего агента с получением активированных молекул гликозаминогликана; и (c) поперечного сшивания активированных молекул гликозаминогликана через их активированные карбоксильные группы с использованием ди- или полинуклеофильного функционального сшивающего агента, содержащего спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов, с получением поперечно-сшитых молекул гликозаминогликана.
[0062] В некоторых аспектах ГАГ поперечно-сшиты ковалентными связями, такими как амидные связи, обычно с использованием активирующего агента для карбоксильных групп в скелете молекулы ГАГ и ди- или полинуклеофильного функционального сшивающего агента, содержащего спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов. В некоторых аспектах поперечное сшивание ГАГ может быть достигнуто с использованием мягких и эффективных способов, обеспечивающих высокий выход с минимальным разложением молекул ГАГ.
[0063] В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент содержит спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов, которая сохраняется в поперечных связях между молекулами ГАГ. В некоторых аспектах ди- или полинуклеофильные функциональные ди-, три-, тетра- и олигосахариды содержат по меньшей мере две нуклеофильные функциональные группы, присоединенные к ним. В некоторых аспектах по меньшей мере две нуклеофильные функциональные группы разделены спейсерной группой, выбранной из группы, состоящей из ди-, три-, тетра- и олигосахаридов.
[0064] В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент содержит две или более функциональных групп, способных взаимодействовать с функциональными карбоксильными группами ГАГ, что приводит к образованию ковалентных связей, таких как амидные связи. В некоторых аспектах нуклеофильные функциональные группы способны взаимодействовать с карбоксильными группами с молекуле гликозаминогликана с образованием амидных связей. В некоторых аспектах нуклеофильные функциональные группы ди-, три-, тетра- и олигосахаридов выбраны из группы, состоящей из первичного амина, гидразина, гидразида, карбазата, семикарбазида, тиосемикарбазида, тиокарбазата и аминокси. В некоторых аспектах ди- или полинуклеофильные функциональные ди-, три-, тетра- и олигосахариды могут быть получены из нуклеофильных функциональных полисахаридов, таких как хитобиоза, полученная из хитина. В некоторых аспектах ди- или полинуклеофильные функциональные ди-, три-, тетра- и олигосахариды также могут представлять собой ди-, три-, тетра- и олигосахариды, которые модифицированы посредством внедрение двух или более нуклеофильных функциональных групп.
[0065] В некоторых аспектах ди- или полинуклеофильный функциональный сшивающий агент включает гомо- или гетеробифункциональные первичные амины, гидразины, гидразиды, карбазаты, семикарбазиды, тиосемикарбазиды, тиокарбазаты и аминокси.
[0066] В некоторых аспектах сшивающий агент выбран из группы, состоящей из тетрасахарида диаминогиалуроновой кислоты, гексасахарида диаминогиалуроновой кислоты, диаминотрегалозы (DATH), диаминолактозы, диаминомальтозы, диаминосахарозы, диаминохитобиозы, хитобиозы или диаминораффинозы.
[0067] В некоторых аспектах стадию активации и стадию поперечного сшивания проводят одновременно. В некоторых аспектах стадию активации проводят до и отдельно от стадии поперечного сшивания.
[0068] В некоторых аспектах стадия, следующая за поперечным сшиванием, включает обеспечение частиц поперечно-сшитых молекул ГАГ, имеющих средний размер в диапазоне 0,01 5 мм, предпочтительно 0,1-0,8 мм.
[0069] В некоторых аспектах указанные частицы имеют размер от 20 до 800 мкм. В некоторых аспектах указанные частицы имеют размер от около 100 до около 500 мкм. В некоторых аспектах указанный размер может быть длиной, диаметром или шириной. В общем случае он относится к диаметру. В некоторых аспектах указанные частицы имеют размер от 20 до 800 мкм, от 20 до 700 мкм, от 20 до 600 мкм, от 20 до 500 мкм, от 20 до 400 мкм, от 20 до 300 мкм, от 20 до 200 мкм, от 100 до 800 мкм, от 100 до 700 мкм или от 100 до 300 мкм.
[0070] В некоторых аспектах связующий агент представляет собой пептидный связующий реагент. В некоторых аспектах связующий реагент выбран из хлорида 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния (DMTMM) и 2-хлор-4,6-диметокси-1,3,5-триазина (CDMT). Предпочтительный пептидный связующий реагент на основе триазина представляет собой DMTMM. Другие предпочтительные пептидные связующие реагенты представляют собой карбодиимидные связующие реагенты, предпочтительно N-(3-диметиламинопропил)-N'-этилкарбодиимид (EDC) в комбинации с N-гидроксисукцинимидом (NHS).
[0071] В некоторых аспектах поперечное сшивание активированных молекул ГАГ происходит через их карбоксильные группы с использованием сшивающего агента. В некоторых аспектах сшивающий агент представляет собой ди- или полинуклеофильный функциональный сшивающий агент, содержащий спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов. В некоторых аспектах сшивающий агент соединяет цепи ГАГ друг с другом через карбоксильные группы в скелете ГАГ. В некоторых аспектах спейсерная группа может представлять собой остаток тетрасахарида гиалуроновой кислоты, гексасахарида гиалуроновой кислоты, трегалозы, лактозы, мальтозы, сахарозы, целлобиозы или раффинозы. Термин «остаток» в данном контексте означает, что структура соединения подобна, но не идентична исходным соединениям, тетрасахариду гиалуроновой кислоты, гексасахариду гиалуроновой кислоты, трегалозе, лактозе, мальтозе, сахарозе, целлобиозе или раффинозе, соответственно. Структура остатка может отличаться от структуры исходного соединения в том отношении, что она снабжена двумя или более нуклеофильными функциональными группами и необязательно ковалентно связана через указанные нуклеофильные функциональные карбоксильные группы в скелете ГАГ.
[0072] В соответствии с родственным аспектом, в данном изобретении также предложено применение гидрогелевого продукта в качестве лекарственного средства, например, для лечения нарушений мягких тканей. Предложен способ лечения пациента, страдающего от нарушения мягких тканей, посредством введения пациенту терапевтически эффективного количества гидрогелевого продукта. Также предложен способ обеспечения корректирующего или эстетического лечения пациента посредством введения пациенту терапевтически эффективного количества гидрогелевого продукта.
[0073] В некоторых аспектах гидрогель, по большей части, является жидкостью по своей массе и может содержать 90-99,9% воды, но имеет свойства, характерные для твердого вещества, благодаря трехмерной поперечно-сшитой сети молекул ГАГ в указанной жидкости. Вследствие существенного содержания жидкости, гидрогель является структурно эластичным и подобен натуральным тканям, что обусловливает его высокую применимость в качестве каркаса для конструирования тканей и для наращивания тканей. Он также пригоден для лечения нарушений мягких тканей и для корректирующего или эстетического лечения. В некоторых аспектах гидрогель используют в качестве лекарственной формы, пригодной для инъекций.
[0074] Способы, описанные в данном документе, представляют собой способы применения инъекционных композиций для реконструктивной или пластической хирургии, в косметической дерматологии, для контурной пластики лица, контурной пластики тела и наращивания десен. В некоторых аспектах предложенные композиции высушены замораживанием или лиофилизированы. В некоторых аспектах предложенные композиции содержат гидрогель, содержащий водный раствор.
[0075] В некоторых аспектах поперечно-сшитый гликозаминогликановый продукт, такой как продукт на основе гиалуроновой кислоты, получают из высокомолекулярного (ВММ) гликозаминогликана с помощью амидного связывания.
[0076] В некоторых аспектах поперечно-сшитый продукт на основе гиалуроновой кислоты, полученный из ВММ гиалуроновой кислоты с использованием химического механизма DATH/DMTMM, составлен в композицию, обеспечивающую получение концентрации ГАГ, подходящей для применения (Cкон. 10-45 мг/мл). В некоторых аспектах ГАГ представляет собой гиалуроновую кислоту. В некоторых аспектах подходящая концентрация ГАГ предназначена для дерматологического применения, применения в стоматологии, медицинского применения или реконструктивного хирургического применения.
[0077] В некоторых аспектах подходящая концентрация ГАГ составляет от 10 до 50 мг/мл, от 10 до 45 мг/мл, от 10 до 40 мг/мл, от 10 до 35 мг/мл, от 10 до 30 мг/мл, от 10 до 25 мг/мл, от 10 до 20 мг/мл, от 10 до 15 мг/мл, от 15 до 40 мг/мл, от 15 до 40 мг/мл, от 15 до 35 мг/мл, от 15 до 30 мг/мл, от 15 до 25 мг/мл, от 15 до 20 мг/мл, от 20 до 50 мг/мл, от 20 до 45 мг/мл, от 20 до 40 мг/мл, от 20 до 35 мг/мл, от 20 до 30 мг/мл, от 20 до 25 мг/мл, от 25 до 50 мг/мл, от 25 до 45 мг/мл, от 25 до 40 мг/мл, от 25 до 35 мг/мл, от 25 до 30 мг/мл, от 30 до 50 мг/мл, от 30 до 45 мг/мл, от 30 до 40 мг/мл, от 30 до 35 мг/мл, от 35 до 50 мг/мл, от 35 до 45 мг/мл, от 35 до 40 мг/мл, от 40 до 50 мг/мл или от 40 до 45 мг/мл.
[0078] В некоторых аспектах подходящая концентрация ГАГ составляет от окoло 10 до окoло 50 мг/мл, от окoло 10 до окoло 45 мг/мл, от окoло 10 до окoло 40 мг/мл, от окoло 10 до окoло 35 мг/мл, от окoло 10 до окoло 30 мг/мл, от окoло 10 до окoло 25 мг/мл, от окoло 10 до окoло 20 мг/мл, от окoло 10 до окoло 15 мг/мл, от окoло 15 до окoло 40 мг/мл, от окoло 15 до окoло 40 мг/мл, от окoло 15 до окoло 35 мг/мл, от окoло 15 до окoло 30 мг/мл, от окoло 15 до окoло 25 мг/мл, от окoло 15 до окoло 20 мг/мл, от окoло 20 до окoло 50 мг/мл, от окoло 20 до окoло 45 мг/мл, от окoло 20 до окoло 40 мг/мл, от окoло 20 до окoло 35 мг/мл, от окoло 20 до окoло 30 мг/мл, от окoло 20 до окoло 25 мг/мл, от окoло 25 до окoло 50 мг/мл, от окoло 25 до окoло 45 мг/мл, от окoло 25 до окoло 40 мг/мл, от окoло 25 до окoло 35 мг/мл, от окoло 25 до окoло 30 мг/мл, от окoло 30 до окoло 50 мг/мл, от окoло 30 до окoло 45 мг/мл, от окoло 30 до окoло 40 мг/мл, от окoло 30 до окoло 35 мг/мл, от окoло 35 до окoло 50 мг/мл, от окoло 35 до окoло 45 мг/мл, от окoло 35 до окoло 40 мг/мл, от окoло 40 до окoло 50 мг/мл или от окoло 40 до окoло 45 мг/мл.
[0079] В некоторых аспектах гиалуроновая кислота включает все варианты и комбинации вариантов гиалуроновой кислоты, гиалуроната или гиалуронана - различной длины цепи и состояния заряда, а также с различными химическими модификациями, включая поперечное сшивание.
[0080] В некоторых аспектах гиалуроновая кислота включает различные гиалуронатные соли гиалуроновой кислоты с различными противоионами, такие как гиалуронат натрия. В некоторых аспектах при упоминании гиалуроновой кислоты предусмотрены также различные модификации гиалуроновой кислоты, такие как окисление, например, окисление групп -CH2OH до -CHO и/или -COOH; периодатное окисление вицинальных гидроксильных групп, после которого может быть осуществлено восстановление, например, восстановление -CHO до -CH2OH, или связывание с аминами с образованием иминов с последующим восстановлением до вторичных аминов; сульфирование; дезамидирование, после которого может быть осуществлено дезаминирование или образование амида с новыми кислотами; эстерификация; поперечное сшивание; замещения с различными соединениями, например, с использованием поперечно-сшивающего агента или связывания с помощью карбодиимидов; включая связывание различных молекул, таких как белки, пептиды и активные лекарственные компоненты, с гиалуроновой кислотой; и деацетилирование. В некоторых аспектах гиалуроновая кислоты может быть дополнительно модифицирована посредством связывания с изомочевиной, гидразидом, бромцианом, моноэпоксидом и моносульфоном.
[0081] В некоторых аспектах гиалуроновая кислота может быть получена из различных источников животного и неживотного происхождения. В некоторых аспектах источники неживотного происхождения включают дрожжи или бактерии. В некоторых аспектах молекулярная масса одной молекулы гиалуроновой кислоты обычно составляет от 0,1 до 10 МДа, но возможны и другие молекулярные массы.
[0082] В некоторых аспектах данное описание относится к по меньшей мере частичному деацетилированию биополимера/гидрогеля, содержащего ацетильные группы, включающему: a) обеспечение биополимера, содержащего ацетильные группы; b) взаимодействие биополимера, содержащего ацетильные группы, с гидроксиламином или его солью при температуре 100 °С или менее в течение от 2 до 200 часов с получением по меньшей мере частично деацетилированного биополимера, и c) выделение по меньшей мере частично деацетилированного биополимера. В некоторых аспектах гидрогель получают из ВММ ГАГ способами, описанными в данном документе.
[0083] В некоторых аспектах данное описание относится к способу получения гидрогелевого продукта, содержащего поперечно-сшитые ГАГ, включающему: a) обеспечение ГАГ, поперечно-сшитого амидными связями, причем поперечно-сшитые ГАГ содержат остаточные аминные группы, и b) ацилирование остаточных аминных групп поперечно-сшитых ГАГ, полученных на стадии a), с получением ацилированных поперечно-сшитых ГАГ. В некоторых аспектах гидрогель получают из ВММ ГАГ способами, описанными в данном документе.
[0084] В некоторых аспектах данное описание относится к способу получения гидрогелевого продукта, содержащего поперечно-сшитые ГАГ, включающему: a) обеспечение ГАГ, поперечно-сшитого амидными связями, причем поперечно-сшитые ГАГ содержат сложноэфирные поперечные связи, образованные в качестве побочных продуктов во время амидного сшивания; и b) щелочную обработку поперечно-сшитых ГАГ для гидролиза сложноэфирных поперечных связей, образованных в качестве побочных продуктов во время амидного сшивания. В некоторых аспектах гидрогель получают из ВММ ГАГ способами, описанными в данном документе.
[0085] При получении гидрогелей из высокомолекулярного (ВММ) гликозаминогликана, такого как гиалуроновая кислота, в системе DATH/DMTMM с использованием низкого содержания DATH, первоначально образуется гель, подходящий для филлерной композиции, но такой гидрогель может гидролизоваться при хранении или под действием условий, вызывающих разложение (например, тепловая стерилизация, ускоренные испытания стабильности). Это означает, что необходимо большее количество поперечных связей для сохранения целостности геля и его защиты от гидролиза. Однако увеличение количества DATH/DMTMM для увеличения количества поперечных связей в геле может приводить к получению гелей с высоким значением Cmin, которые подвергаются разделению фаз при соответствующих концентрациях ГАГ. Другими словами, при получении гелей из ВММ ГАГ с достаточным количеством поперечных связей для обеспечения их стабильности при автоклавировании невозможно разбавить полученные гели до 20 мг/мл (10-45 мг/мл) без разделения фаз. В свою очередь, это усложняет процесс, например, наполнения гелем шприцов. В некоторых аспектах предложенный гидрогель является однородным. Однородный продукт не подвержен разделению фаз. В некоторых аспектах гидрогель составляют в композицию с концентрацией, подходящей для дерматологического применения (такой как 10-45 мг/мл), но он сохраняет способность к набуханию в присутствии избытка солевого раствора.
[0086] В некоторых аспектах предложенный способ получения гидрогеля не приводит к разделению фаз гидрогеля. В некоторых аспектах гидрогель, полученный или выделенный способами, описанными в данном документе, не подвержен разделению фаз. В некоторых аспектах предложенный способ разбавления гидрогеля после тепловой стерилизации не приводит к разделению фаз гидрогеля.
[0087] В некоторых аспектах гидрогель разбавлен в буфере PBS. В некоторых аспектах гидрогель разбавлен в 1 мМ, 2 мМ, 3 мМ, 4 мМ, 5 мМ, 6 мМ, 7 мМ, 8 мМ, 9 мМ, 10 мМ, 11 мМ, 12 мМ, 13 мМ, 14 мМ, 15 мМ, 16 мМ, 17 мМ, 18 мМ, 19 мМ или 20 мМ фосфатном буфере. В некоторых аспектах гидрогель разбавлен в фосфатном буфере с концентрацией около 1 мМ, окoло 2 мМ, окoло 3 мМ, окoло 4 мМ, окoло 5 мМ, окoло 6 мМ, окoло 7 мМ, окoло 8 мМ, окoло 9 мМ, окoло 10 мМ, окoло 11 мМ, окoло 12 мМ, окoло 13 мМ, окoло 14 мМ, окoло 15 мМ, окoло 16 мМ, окoло 17 мМ, окoло 18 мМ, окoло 19 мМ или окoло 20 мМ. В некоторых аспектах гидрогель разбавлен в фосфатном буфере до концентрации от 1 мМ до 20 мМ, от 1 мМ до 15 мМ, от 1 мМ до 10 мМ, от 1 мМ до 5 мМ, от 5 мМ до 20 мМ, от 5 мМ до 15 мМ, от 5 мМ до 10 мМ, от 10 мМ до 20 мМ, от 10 мМ до 15 мМ или от 15 мМ до 20 мМ. В некоторых аспектах гидрогель разбавлен в фосфатном буфере до концентрации от окoло 1 мМ до окoло 20 мМ, от окoло до 1 мМ до окoло 15 мМ, от окoло 1 мМ до окoло 10 мМ, от окoло 1 мМ до окoло 5 мМ, от окoло 5 мМ до окoло 20 мМ, от окoло 5 мМ до окoло 15 мМ, от окoло 5 мМ до окoло 10 мМ, от окoло 10 мМ до окoло 20 мМ, от окoло 10 мМ до окoло 15 мМ или от окoло 15 мМ до окoло 20 мМ.
[0088] В некоторых аспектах гидрогель разбавлен в растворе при рН окoло 6,0, окoло 6,2, окoло 6,4, окoло 6,6, окoло 6,8, окoло 7,0, окoло 7,2, окoло 7,4, окoло 7,6, окoло 7,8 или окoло 8,0. В некоторых аспектах гидрогель разбавлен в растворе при рН 6,0 6,2, 6,4, 6,6, 6,8, 7,0, 7,2, 7,4, 7,6, 7,8 или 8,0. В некоторых аспектах гидрогель разбавлен в растворе при рН от 6,0 до 8,0, от 6,0 до 7,0, от 7,0 до 8,0, от 6 до 7,5, от 7,0 до 7,5 или от 6,5 до 7,5.
[0089] В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет окoло 1%, окoло 1,5%, окoло 2%, окoло 2,5%, окoло 3%, окoло 3,5%, окoло 4%, окoло 4,5%, окoло 5%, окoло 5,5%, окoло 6%, окoло 6,5%, окoло 7%, окoло 7,5%, окoло 8%, окoло 8,5%, окoло 9%, окoло 9,5%, окoло 10%, окoло 11%, окoло 12%, окoло 13%, окoло 14%, окoло 15%, окoло 16%, окoло 17%, окoло 18%, окoло 19% или окoло 20%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет 1%, 1,5%, 2%, 2,5%, 3%, 3,5%, 4%, 4,5%, 5%, 5,5%, 6%, 6,5%, 7%, 7,5%, 8%, 8,5%, 9%, 9,5%, 10% 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19% или 20%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет от 1% до 3%, от 2% до 5%, от 3% до 5%, от 4% до 5%, от 2% до 3%, от 2% до 4%, от 3% до 5%, от 3% до 4%, от 1% до 20%, от 1% до 15%, от 1% до 10%, от 1% до 5%, от 1% до 2%, от 2% до 5%, от 2% до 10%, от 2% до 15%, от 2% до 20%, от 5% до 20%, от 5% до 15%, от 5% до 10%, от 10% до 20%, от 10% до 15% или от 15% до 20%.
[0090] В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 10%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 9%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 8%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 7%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 6%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 5%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 4%. В некоторых аспектах концентрация ГК в реакции поперечного сшивания составляет не более 3%.
[0091] В некоторых аспектах содержание DATH в реакции поперечного сшивания, выраженное в % мол., составляет 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 1,1%, 1,2%, 1,3%, 1,4%, 1,5%, 1,6%, 1,7%, 1,8%, 1,9% или 2%. В некоторых аспектах содержание DATH в реакции поперечного сшивания, выраженное в % мол., составляет окoло 0,1%, окoло 0,2%, окoло 0,3%, окoло 0,4%, окoло 0,5%, окoло 0,6%, окoло 0,7%, окoло 0,8%, окoло 0,9%, окoло 1%, окoло 1,1%, окoло 1,2%, окoло 1,3%, окoло 1,4%, окoло 1,5%, окoло 1,6%, окoло 1,7%, окoло 1,8%, окoло 1,9% или окoло 2%. В некоторых аспектах содержание DATH в реакции поперечного сшивания, выраженное в % мол., составляет от 0,1% до 2%, от 0,1% до 1,5%, от 0,1% до 1%, от 0,1% до 0,5%, от 0,2% до 1%, от 0,2% до 0,5%, от 0,2% до 0,3%, от 0,5% до 1%, от 0,5% до 1,5%, от 0,5% до 2%, от 1% до 2% или от 1% до 1,5%.
[0092] В некоторых аспектах ГАГ имеет молекулярную массу около 700 кДа, 800 кДа, 900 кДа, 1000 кДа, 1100 кДа, 1200 кДа, 1300 кДа, 1400 кДа, 1500 кДа, 1600 кДа, 1700 кДа, 1800 кДа, 1900 кДа, 2000 кДа, 2500 кДа, 3000 кДа, 3500 кДа, 4000 кДа, 4500 кДа, 5000 кДа, 5500 кДа, 6000 кДа, 6500 кДа, 7000 кДа, 7500 кДа, 8000 кДа, 8500 кДа, 9000 кДа, 9500 кДа или 10000 кДа.
[0093] В некоторых аспектах Гаг имеет молекулярную массу более чем около 700 кДа, окoло 800 кДа, окoло 900 кДа, окoло 1000 кДа, окoло 1100 кДа, окoло 1200 кДа, окoло 1300 кДа, окoло 1400 кДа, окoло 1500 кДа, окoло 1600 кДа, окoло 1700 кДа, окoло 1800 кДа, окoло 1900 кДа, окoло 2000 кДа, окoло 2500 кДа, окoло 3000 кДа, окoло 3500 кДа, окoло 4000 кДа, окoло 4500 кДа, окoло 5000 кДа, окoло 5500 кДа, окoло 6000 кДа, окoло 6500 кДа, окoло 7000 кДа, окoло 7500 кДа, окoло 8000 кДа, окoло 8500 кДа, окoло 9000 кДа, окoло 9500 кДа или окoло 10000 кДа.
[0094] В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 80% через 24 часа. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 80% через 48 часов. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 80% через 24 часа при температуре около 90 °С. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 80% через 24 часа или 48 часов при температуре по меньшей мере 70 °С. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 80% через 24 часа или 48 часов при температуре по меньшей мере 90 °С.
[0095] В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 70%, 75%, 80%, 85%, 90% или 95% через 24 часа или 48 часов. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 70%, 75%, 80%, 85%, 90% или 95% через 24 часа или 48 часов при температуре по меньшей мере 70 °С или по меньшей мере 90 °С.
[0096] В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере окoло 70%, окoло 75%, окoло 80%, окoло 85%, окoло 90% или окoло 95% через 24 часа или 48 часов. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля составляет по меньшей мере 70%, 75%, 80%, 85%, 90% или 95% через 24 часа или 48 часов при температуре по меньшей мере 70 °С или по меньшей мере 90 °С.
[0097] В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля снижается менее чем на 5%, 10%, 15%, 20%, 25% или 30% через 24 часа или 48 часов при температуре по меньшей мере 70 °С или по меньшей мере 90 °С. В некоторых аспектах термостабильность (норм. Cгеля или Cгеля) гидрогеля снижается менее чем на окoло 5%, окoло 10%, окoло 15%, окoло 20%, окoло 25% или окoло 30% через 24 часа или 48 часов при температуре по меньшей мере 70 °С или по меньшей мере 90 °С.
[0098] В некоторых аспектах температура, при которой определяют термостабильность, составляет по меньшей мере 70 °С, 72 °С, 74 °С, 76 °С, 78 °С, 80 °С, 82 °С, 84 °С, 86 °С, 88 °С, 90 °С, 92 °С, 94 °С, 96 °С, 98 °С, 100 °С, 102 °С, 104 °С, 106 °С, 108 °С или 110 °С. В некоторых аспектах температура, при которой определяют термостабильность, составляет по меньшей мере окoло 70 °С, окoло 72 °С, окoло 74 °С, окoло 76 °С, окoло 78 °С, окoло 80 °С, окoло 82 °С, окoло 84 °С, окoло 86 °С, окoло 88 °С, окoло 90 °С, окoло 92 °С, окoло 94 °С, окoло 96 °С, окoло 98 °С, окoло 100 °С, окoло 102 °С, окoло 104 °С, окoло 106 °С, окoло 108 °С или окoло 110 °С.
[0099] В некоторых аспектах период времени после производства, по истечении которого определяют термостабильность, составляет по меньшей мере 24 часа, 26 часов, 28 часов, 30 часов, 32 часа, 34 часа, 36 часов, 38 часов, 40 часов, 42 часа, 44 часа, 46 часов, 48 часов, 50 часов, 52 часа, 54 часа, 56 часов, 58 часов, 60 часов, 62 часа, 64 часа, 66 часов, 68 часов, 70 часов, 72 часа, 74 часа, 76 часов, 78 часов или 80 часов. В некоторых аспектах период времени после производства, по истечении которого определяют термостабильность, составляет по меньшей мере окoло 24 часа, окoло 26 часов, окoло 28 часов, окoло 30 часов, окoло 32 часа, окoло 34 часа, окoло 36 часов, окoло 38 часов, окoло 40 часов, окoло 42 часа, окoло 44 часа, окoло 46 часов, окoло 48 часов, окoло 50 часов, окoло 52 часа, окoло 54 часа, окoло 56 часов, окoло 58 часов, окoло 60 часов, окoло 62 часа, окoло 64 часа, окoло 66 часов, окoло 68 часов, окoло 70 часов, окoло 72 часа, окoло 74 часа, окoло 76 часов, окoло 78 часов или около 80 часов.
[00100] В некоторых аспектах предложенная композиция является биорассасывающейся. В некоторых аспектах предложенный гидрогель является биорассасывающимся. В некоторых аспектах композиция подвергается биорассасыванию в течение от около 1 года до около 3 лет. В некоторых аспектах композиция подвергается биорассасыванию в течение от 1 года до 3 лет. В некоторых аспектах гидрогель подвергается биорассасыванию в течение от около 1 года до около 3 лет. В некоторых аспектах гидрогель подвергается биорассасыванию в течение от 1 года до 3 лет.
[00101] В некоторых аспектах композиция дополнительно содержит местный анестетик. В некоторых аспектах композиция содержит по меньшей мере один местный анестетик. В некоторых аспектах местный анестетик представляет собой местный анестетик амидного типа. В некоторых аспектах местный анестетик представляет собой местный анестетик сложноэфирного типа.
[00102] В некоторых аспектах местный анестетик выбран из группы, состоящей из: бупивакаина, бутаниликаина, картикаина, цинхокаина (дибукаина), клибукаина, этилпарапиперидиноацетиламинобензоата, этидокаина, лигнокаина (лидокаина), мепивакаина, оксетазаина, прилокаина, ропивакаина, толикаина, тримекаина, вадокаина, артикаина, левобупивакаина, амилокаина, кокаина, пропанокаина, клормекаина, циклометикаина, проксиметакаина, аметокаина (тетракаина), бензокаина, бутакаина, бутоксикаина, бутиламинобензоата, хлорпрокаина, диметокаина (ларокаина), оксибупрокаина, пиперокаина, паретоксикаина, прокаина (новокаина), пропоксикаина и трикаина; или их комбинации.
[00103] В некоторых аспектах концентрация местного анестетика в композиции составляет от 1 до 5 мг/мл. В некоторых аспектах концентрация местного анестетика в композиции составляет от около 1 до около 5 мг/мл. В некоторых аспектах концентрация местного анестетика в композиции составляет от 2 до 4 мг/мл. В некоторых аспектах концентрация местного анестетика в композиции составляет от около 2 до около 4 мг/мл. В некоторых аспектах концентрация местного анестетика в композиции составляет 0,5 мг/мл, 1 мг/мл, 1,5 мг/мл, 2 мг/мл, 2,5 мг/мл, 3 мг/мл, 3,5 мг/мл, 4 мг/мл, 4,5 мг/мл или 5 мг/мл. В некоторых аспектах концентрация местного анестетика в композиции составляет окoло 0,5 мг/мл, окoло 1 мг/мл, окoло 1,5 мг/мл, окoло 2 мг/мл, окoло 2,5 мг/мл, окoло 3 мг/мл, окoло 3,5 мг/мл, окoло 4 мг/мл, окoло 4,5 мг/мл или окoло 5 мг/мл.
[00104] В некоторых аспектах предложенная композиция пригодна для инъекций. В некоторых аспектах композиция для инъекций представляет собой инъекционный имплантат. В некоторых аспектах данное описание относится к инъекционному имплантату, содержащему любую из композиций, описанных в данном документе. В некоторых аспектах инъекционный имплантат пригоден для субдермальной, внутрикожной, подкожной, внутримышечной, подмышечной, интрагингивальной инъекции.
[00105] В некоторых аспектах данное описание относится к предварительно наполненному шприцу, содержащему любую из композиций, описанных в данном документе. В некоторых аспектах данное описание относится к предварительно наполненному флакону, содержащему любую из композиций, описанных в данном документе.
[00106] В некоторых аспектах набор содержит предварительно наполненный шприц, содержащий любую из композиций, описанных в данном документе. В некоторых аспектах набор содержит предварительно наполненный флакон, содержащий любую из композиций, описанных в данном документе, шприц и одну или более игл для подкожных инъекций. В некоторых случаях набор содержит противомикробную композицию для введения в место инъекции.
[00107] В некоторых аспектах предусмотрены наборы для применения при практическом осуществлении способов, описанных в данном документе. В некоторых аспектах наборы содержат все растворы, буферы, соединения, емкости и/или инструкции, достаточные для осуществления способов, описанных в данном документе.
[00108] В некоторых аспектах композиция дополнительно содержит хлорид натрия. В некоторых аспектах композиция имеет концентрацию хлорида натрия 0,9% мас./об. В некоторых аспектах композиция дополнительно содержит фосфатный буфер. В некоторых аспектах композиция дополнительно содержит фармацевтически приемлемый носитель. В некоторых аспектах композиция дополнительно содержит хлорид натрия, фосфатный буфер и фармацевтически приемлемый носитель.
[00109] В некоторых аспектах композиция содержит один или более агентов для увеличения плотности. В некоторых аспектах агенты для увеличения плотности могут быть выбраны из сорбита, маннита и фруктозы.
[00110] В некоторых аспектах композиция содержит буферный агент. Буферный агент представляет собой химическое соединение или соединения, которое или которые добавляют в раствор для того, чтобы рН раствора не изменялся при разбавлении или при добавлении небольшого количества кислот или оснований. В эффективных буферных системах используют растворы, которые содержат высокие и приблизительно равные концентрации сопряженной пары кислоты-основания (или буферных агентов). Буферный агент, используемый в данном описании, может представлять собой любое такое химическое соединение(я), которое является фармацевтически приемлемым, включая, но не ограничиваясь ими, соли (сопряженные кислоты и/или основания), представляющие собой фосфаты и цитраты. В некоторых аспектах буферный агент содержит фосфатно-солевой буферный раствор (PBS) или альтернативный фосфатный буфер.
[00111] В некоторых аспектах предложенная композиция является асептической. В некоторых аспектах предложенная композиция является стерильной. В некоторых аспектах композицию стерилизуют методом стерилизации фильтрованием, тепловой стерилизации или стерилизации облучением. В некоторых аспектах компоненты композиции стерилизуют до смешивания или получения общей композиции, с получением композиции, которая содержит два или более компонентов, стерилизованных до получения композиции.
[00112] В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,5 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,4 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,3 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,2 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,1 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 1,0 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 0,9 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 0,8 МДа. В некоторых аспектах ГАГ не имеет молекулярную массу менее 0,7 МДа.
[00113] В некоторых аспектах не подвержен разложению гликозаминогликана после поперечного сшивания. В некоторых аспектах гидрогель подвержен разложению после поперечного сшивания в условиях окружающей среды; однако гидрогель не демонстрирует значение Cmin менее Cкон./2. В некоторых аспектах гидрогель демонстрирует значение Cmin более Cкон./2 данного гидрогеля.
[00114] Другие аспекты и предпочтительные варианты реализации данного изобретения станут понятны из следующего подробного описания данного изобретения и прилагаемой формулы изобретения.
Способы применения гидрогелей
[00115] В некоторых аспектах данное описание включает способы осуществления реконструктивного или эстетического дерматологического лечения. В некоторых аспектах реконструктивное или эстетическое дерматологическое лечение включает инъекцию субъекту композиции, описанной в данном документе. В некоторых аспектах инъекция является субдермальной, внутрикожной, подкожной, внутримышечной, подмышечной или интрагингивальной инъекцией.
[00116] В некоторых аспектах способы по данному описанию относятся к интрагингивальной инъекции для заполнения десен в результате рецессии десен. В некоторых аспектах способы относятся к инъекции композиции в одну или более тканей полости рта.
[00117] В некоторых аспектах инъекция пригодна для дермального филлинга, контурной пластики тела, контурной пластики лица и гингивального филлинга.
[00118] В некоторых аспектах инъекция композиции, описанной в данном документе, пригодна для дермального филлинга. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения трещин кожи. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения тонких морщин на лице, шее, кистях рук, стопах, коленях и локтях. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения мелких морщин на лице, шее, кистях рук, стопах, коленях и локтях. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения тонких морщин на лице, шее, кистях рук, стопах, коленях и локтях.
[00119] В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения рубцов. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения атрофических рубцов. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения гипертрофических рубцов. В некоторых аспектах способы дермального филлинга включают инъекцию композиции для заполнения келоидных рубцов.
[00120] В некоторых аспектах способы дермального филлинга включают инъекцию композиции для восстановления и/или коррекции признаков утраты лицевого жира (липоатрофии) у людей с вирусом иммунодефицита человека (ВИЧ).
[00121] В некоторых аспектах способы дермального филлинга включают инъекцию композиции в тыльную сторону кистей рук или в верхнюю часть стопы.
[00122] В некоторых аспектах способы дермального филлинга включают инъекцию композиции для укрепления ослабленных голосовых связок.
[00123] В некоторых аспектах способы дермального филлинга включают инъекцию композиции для восстановления утраченного объема какой-либо части тела в результате старения, болезни или травмы.
[00124] В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения контура лица. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в губы для наращивания размера и/или формы губ.
[00125] В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для улучшения симметрии лица. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции для изменения формы лица на овальную форму, круглую форму, квадратную форму, треугольную форму, форму перевернутого треугольника, прямоугольную форму или продолговатую форму. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции для увеличения общей ширины лица. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции для увеличения общей длины лица.
[00126] В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для увеличения ширины лба и/или скул. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для увеличения длины линии подбородка.
[00127] В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения размера и/или формы подбородка. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения размера и/или формы лба. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения размера и/или формы щек. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения размера и/или формы бровей.
[00128] В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения внешнего вида, связанного с ретрогнатией. В некоторых аспектах способы контурной пластики лица включают инъекцию композиции в лицо для изменения внешнего вида, связанного с прогнатией.
[00129] В некоторых аспектах способы контурной пластики тела включают инъекцию композиции в тело для изменения размера и формы различных аспектов тела. В некоторых аспектах способы контурной пластики тела включают инъекцию композиции в тело для изменения размера и формы каких-либо аспектов тела для улучшения симметрии.
[00130] В некоторых аспектах способы контурной пластики тела включают инъекцию композиции в тело для изменения размера и формы молочных желез, ягодиц, крестца, паха, бедер, области живота, грудной клетки, стоп, ног, коленей, подколенной области, голеней, кистей рук, рук, локтей и/или передней части локтя.
[00131] В некоторых аспектах способы контурной пластики тела включают инъекцию композиции в тело для заполнения вогнутой деформации. В некоторых аспектах вогнутая деформация является результатом старения, болезни, травмы или предрасположенности. В некоторых аспектах способы контурной пластики тела включают инъекцию композиции в тело для уменьшения проявлений целлюлита.
ПРИМЕРЫ
Пример 1
Получение высокомолекулярного гидрогеля
[00132] В примере 1 предложен общий способ получения высокомолекулярных гидрогелей ГАГ, описанных в данном документе.
[00133] Гиалуроновую кислоту (ГК) и растворы диаминотрегалозы (DATH) и хлорида 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния (DMTMM) смешивали для поперечного сшивания. После поперечного сшивания разделяли гель и разбавляли с получением набора концентраций. Затем нагревали гель до приблизительно 70 °С в течение приблизительно 24 часов. Затем подвергали гель измельчению частиц (particle size reduction, PSR) и осаждению, и затем промывали и сушили с получением порошка. Затем смешивали порошок геля с соответствующим буфером, и гель набухал; затем автоклавировали гель.
[00134] Таблица 1: Композиции гидрогеля, соответствующие Фиг. 1.
НО=не определяли
[00135] Содержание геля анализировали у условиях теплового разложения при 90 °С и оценивали в течение чуть более 70 часов (Фиг. 1). Значения содержания геля нормализовали для простоты сравнения, и отображали как «норм. Cгеля (%)» по оси y на Фиг. 1. Полученные данные свидетельствуют о том, что высокомолекулярная ГК обеспечивает получение гелей, которые сохраняют более высокую степень содержания геля в условиях теплового разложения, по сравнению с гелями, полученными из более низкомолекулярной ГК.
Пример 2
Получение и оценка гидрогелей, полученных из высокомолекулярной (ВММ) и низкомолекулярной (НММ) гиалуроновой кислоты (ГК)
Общий способ поперечного сшивания ВММ и НММ ГК
[00136] Получали свежие исходные растворы каждого из сшивающих агентов, DMTMM и DATH, в воде. Реакционный раствор получали посредством добавления в воду требуемых объемов исходных растворов DMTMM (% мол. DATH х 8,5) и DATH (см. таблицу 1), соответственно. Реакционный раствор смешивали и напрямую добавляли в предварительно взвешенную ГК (0,4 МДа или 2,1 МДа) в реакционной емкости. Затем смесь энергично перемешивали в течение 3 минут и инкубировали. Через 24 ± 2 часа продавливали полученный материал через 1 мм стальную сетку. Гомогенизировали материал в течение 24 ± 2 часа при 70 °С, затем подвергали гель измельчению частиц (PSR) с помощью 3х315 мкм фильтра и затем осаждали посредством добавления EtOH. Полученный порошок сушили под вакуумом в течение ночи и разбавляли в 7 мМ фосфатном растворе с 0,7% NaCl и 3 мг/г Lido-HCl при нейтральном рН. Наполняли полученным гелем шприцы и затем автоклавировали.
[00137] Таблица 2: Условия реакции и свойства полученных гелей.
[00138] Полученные гели инкубировали в герметично закрытых стеклянных флаконах при 90 °С на водяной бане в течение 24 часов или 48 часов. В указанное время охлаждали образцы до комнатной температуры и анализировали гели. См. Фиг. 2-4.
[00139] На Фиг. 2 показано содержание геля (Cгеля %), соответствующее образцам 2-1 и 2-2 в таблице 2. На Фиг. 3 показано содержание геля (Cгеля %), соответствующее образцам 2-3 и 2-4 в таблице 2. На Фиг. 4 показано содержание геля (Cгеля %), соответствующее образцам 2-5 и 2-6 в таблице 2. На Фиг. 5 показано содержание геля (Cгеля %), соответствующее образцам 2-7 и 2-8 в таблице 2.
Общий способ определения ММкаж. в ВММ гелях
[00140] В реакционной емкости смешивали навеску ГК (2,1 МДа) с водой. Смесь энергично перемешивали в течение 3 минут и инкубировали при комнатной температуре. Через 24 часа разбавляли раствор водой, добавляли NaCl (тв.) (конечная концентрация 0,9%) и инкубировали полученный материал при 70 °С. После инкубации в течение 24 часов наполняли полученным раствором шприцы. Затем автоклавировали шприцы для образца 2-10, а шприцы для образца 2-9 не автоклавировали. ММ растворов определяли методом эксклюзионной хроматографии с детектированием рассеивания лазерного излучения с кратными углами (SEC-MALLS).
[00141] Таблица 3: Условия реакции и свойства полученных гелей.
* * * * *
[00142] Способы, иллюстративно описанные в данном документе, могут быть соответствующим образом осуществлены на практике в отсутствие любого элемента или элементов, ограничения или ограничений, специально не описанных в данном документе. Так, например, термины «содержащий», «включающий», «который содержит» и т.д. следует толковать расширительно и без ограничения. Кроме того термины и выражения, использованные в данном документе, использованы в качестве описания, а не ограничения, и при использовании таких терминов и выражений не предусмотрено исключение любых эквивалентов представленных и описанных признаков или их частей. Следует понимать, что в пределах объема заявленного изобретения возможны различные модификации. Таким образом, следует понимать, что хотя настоящее изобретение описано, в частности, с помощью предпочтительных вариантов реализации и необязательных признаков, специалисты в данной области техники могут осуществлять модификации и вариации различных вариантов реализации изобретения, описанных в настоящем документе, и что такие модификации и вариации входят в объем настоящего изобретения.
[00143] В данном документе изобретение описано в широком смысле и обобщенно. Каждая из более узких групп элементов и субгенерических групп, входящих в общее описание, также образует часть предложенных способов. Они включают общее описание предложенных способов при условии или отрицательном ограничении исключения любого рассматриваемого объекта из данного класса, не зависимо от явного указания в настоящем документе исключаемого материала. Предложенная технология также не ограничена конкретными вариантами реализации, описанными в данной заявке, которые предназначены в качестве отдельных иллюстраций некоторых аспектов предложенной технологии. Многочисленные модификации и вариации предложенной технологии могут быть сделаны без отклонения от сущности и объема изобретения, как понятно специалистам в данной области техники. Функционально эквивалентные способы и устройства, входящие в объем предложенной технологии, помимо тех, которые перечислены в настоящем документе, очевидны для специалистов в данной области техники из изложенного выше описания. Предусмотрено, что такие модификации и варианты входят в границы объема предложенной технологии. Следует понимать, что предложенная технология не ограничена конкретными способами, реагентами, соединениями, композициями или биологическими системами, которые, безусловно, могут варьироваться. Следует также понимать, что используемая в данном документе терминология предназначена лишь для описания конкретных вариантов реализации, и ее не следует толковать как ограничивающую.
[00144] Специалистам в данной области техники понятно, что данное изобретение может быть без труда адаптировано для выполнения указанных задач и достижения упомянутых целей и преимуществ, а также присущих ему. Возможность их модификации и другого применения понятна специалистам в данной области техники. Такие модификации входят в сущность данного изобретения и определены объемом формулы изобретения, в которой представлены неограничивающие варианты реализации настоящего изобретения.
[00145] Кроме того, если особенности или аспекты настоящего изобретения описаны с помощью групп Маркуша, то специалистам в данной области техники понятно, что настоящее изобретение тем самым изложено также в отношении любого отдельного члена или подгруппы членов указанной группы Маркуша.
[00146] Все ссылки, статьи, публикации, патенты, публикации патентов и патентные заявки, цитируемые в данном документе, полностью включены в данный документ посредством ссылки во всех отношениях.
[00147] Однако упоминание любой ссылки, статьи, публикации, патента, публикации патента и патентной заявки, цитируемой в данном документе, не является и не должна рассматриваться как признание или любая форма предположения того, то они составляют достоверный уровень техники или образуют часть общедоступных известных знаний в любой стране мира.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНЪЕКЦИОННЫЙ ГЕЛЕВЫЙ ПРОДУКТ | 2018 |
|
RU2783125C2 |
| СПОСОБ ДЕАЦЕТИЛИРОВАНИЯ БИОПОЛИМЕРОВ | 2016 |
|
RU2748235C2 |
| КОМПОЗИЦИЯ КОЖНОГО НАПОЛНИТЕЛЯ И СПОСОБ ЛЕЧЕНИЯ | 2012 |
|
RU2679317C1 |
| УГЛЕВОДНЫЙ СШИВАЮЩИЙ АГЕНТ | 2016 |
|
RU2733145C2 |
| КОМПОЗИЦИИ КОЖНЫХ НАПОЛНИТЕЛЕЙ | 2012 |
|
RU2638713C2 |
| ИМПЛАНТАТЫ ДЛЯ МОДЕЛИРОВАНИЯ, УВЕЛИЧЕНИЯ ИЛИ КОРРЕКЦИИ ЧАСТЕЙ ЛИЦА, НАПРИМЕР ПОДБОРОДКА | 2016 |
|
RU2715234C2 |
| СТАБИЛИЗИРОВАННАЯ ГИАЛУРОНОВАЯ КИСЛОТА | 2019 |
|
RU2805502C2 |
| СПОСОБ ПРОИЗВОДСТВА ФОРМОВАННОГО ПРОДУКТА ИЗ ПОПЕРЕЧНО-СШИТОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2013 |
|
RU2640865C2 |
| КОМПОЗИЦИИ КОЖНОГО НАПОЛНИТЕЛЯ ДЛЯ ЛЕЧЕНИЯ МЕЛКИХ МОРЩИН | 2012 |
|
RU2626513C2 |
| ГЕЛЬ ГИАЛУРОНОВОЙ КИСЛОТЫ ДЛЯ ВНУТРИКОЖНОЙ ИНЪЕКЦИИ | 2007 |
|
RU2448740C2 |
Группа изобретений относится к гидрогелю высокомолекулярного гликозаминогликана. Способ получения гидрогеля включает поперечное сшивание гликозаминогликана (ГАГ), имеющего молекулярную массу 2,1-3,5 МДа, сшивающим агентом с получением гликозаминогликанового гидрогеля, поперечно-сшитого амидными связями, где сшивающий агент представляет собой ди- или полинуклеофильный функциональный сшивающий агент, содержащий спейсерную группу, выбранную из ди-, три-, тетра- и олигосахаридов; причем концентрация ГАГ составляет от 2% до 10% (мас./мас.), молярное отношение сшивающего агента к ГАГ составляет менее или равно 2% мол. на дисахарид ГАГ. Также раскрыты гидрогелевый продукт и способ восстановления, реконструкции или наращивания твердой или мягкой ткани. Группа изобретений обеспечивает устойчивость к деградации геля. 4 н. и 15 з.п. ф-лы, 5 ил., 3 табл., 2 пр.
1. Способ получения гидрогеля, содержащего поперечно-сшитые молекулы гликозаминогликана (ГАГ), включающий поперечное сшивание ГАГ, имеющего молекулярную массу 2,1-3,5 МДа, сшивающим агентом с получением гликозаминогликанового гидрогеля, поперечно-сшитого амидными связями,
где сшивающий агент представляет собой ди- или полинуклеофильный функциональный сшивающий агент, содержащий спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов;
причем концентрация ГАГ составляет от 2% до 10% (мас./мас.), и
молярное отношение сшивающего агента к ГАГ составляет менее или равно 2% мол. на дисахарид ГАГ.
2. Способ получения гидрогеля по п. 1, отличающийся тем, что
если концентрация ГАГ составляет от 2% до 4,5% (мас./мас.), то концентрация сшивающего агента составляет от 0,8 до 2% мол. относительно дисахарида ГАГ; и
если концентрация ГАГ составляет от 4,6% до 5,9% (мас./мас.), то концентрация сшивающего агента составляет от 0,5 до 0,8% мол. относительно дисахарида ГАГ; и
если концентрация ГАГ составляет от 6% до 10% (мас./мас.), то концентрация сшивающего агента составляет от 0,3 до 0,5% мол. относительно дисахарида ГАГ.
3. Способ по п. 1, отличающийся тем, что ди- или полинуклеофильный функциональный сшивающий агент представляет собой диаминотрегалозу (DATH).
4. Способ по любому из пп. 1-3, отличающийся тем, что поперечное сшивание включает:
(1) обеспечение раствора молекул гликозаминогликана (ГАГ);
(2) активацию карбоксильных групп в молекулах гликозаминогликана с помощью связующего агента с получением активированных молекул гликозаминогликана;
(3) поперечное сшивание активированных молекул гликозаминогликана (ГАГ) через их активированные карбоксильные группы с использованием ди- или полинуклеофильного функционального сшивающего агента с получением гликозаминогликанового гидрогеля, поперечно-сшитого амидными связями.
5. Способ по п. 4, отличающийся тем, что связующий агент представляет собой связующий агент на основе триазина, такой как хлорид 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния (DMTMM).
6. Способ по любому из пп. 1-5, отличающийся тем, что поперечное сшивание осуществляют при рН 5,0-9,0, предпочтительно при рН 6,0-8,0.
7. Способ по любому из пп. 1-6, дополнительно включающий составление в композицию поперечно-сшитого гидрогеля с конечной концентрацией гликозаминогликана (ГАГ) 10-45 мг/мл.
8. Способ по любому из пп. 1-7, дополнительно включающий стерилизацию поперечно-сшитого гидрогеля.
9. Способ по любому из пп. 1-8, отличающийся тем, что гликозаминогликан (ГАГ) представляет собой гиалуроновую кислоту (ГК).
10. Способ по любому из пп. 1-9, отличающийся тем, что ГАГ имеет молекулярную массу 2,5-3,5 МДа.
11. Способ по любому из пп. 1-10, отличающийся тем, что концентрация ГАГ составляет 3-5% (мас./мас.).
12. Способ по любому из пп. 1-11, отличающийся тем, что молярное отношение сшивающего агента к ГАГ составляет 0,9-1,1% мол. на дисахарид ГАГ.
13. Способ по любому из пп. 1-12, отличающийся тем, что ГАГ представляет собой гиалуроновую кислоту (ГК), имеющую молекулярную массу 2,1-3,5 МДа, а сшивающий агент представляет собой диаминотрегалозу (DATH), и при этом концентрация ГК составляет 3-5% (мас./мас.), а молярное отношение DATH к ГК составляет 0,9-1,1% мол. на дисахарид ГАГ.
14. Гидрогелевый продукт для восстановления, реконструкции или наращивания твердой или мягкой ткани, полученный способом по любому из пп. 1-13.
15. Гидрогелевый продукт для восстановления, реконструкции или наращивания твердой или мягкой ткани, содержащий молекулы гликозаминогликана (ГАГ) в качестве способного к набуханию полимера, причем молекулы гликозаминогликана поперечно сшиты амидными связями между сшивающим агентом и молекулами ГАГ,
где молекулы гликозаминогликана ковалентно сшиты поперечными связями, содержащими спейсерную группу, выбранную из группы, состоящей из ди-, три-, тетра- и олигосахаридов, и
при этом кажущаяся молекулярная масса (MМкаж.) поперечно-сшитых молекул гликозаминогликана составляет более 1,0 МДа и при этом термостабильность способного к набуханию полимера (норм. Cгеля) составляет более 80% через 24 часа.
16. Гидрогелевый продукт по п. 15, отличающийся тем, что спейсерная группа представляет собой трегалозу.
17. Гидрогелевый продукт по п. 15 или 16, отличающийся тем, что гликозаминогликан (ГАГ) представляет собой гиалуроновую кислоту (ГК).
18. Гидрогелевый продукт по любому из пп. 15-17, отличающийся тем, что гидрогелевый продукт является стерилизованным.
19. Способ восстановления, реконструкции или наращивания твердой или мягкой ткани, включающий инъекцию в кожу гидрогелевого продукта по любому из пп. 15-18.
| WO 2017114867 A1, 06.07.2017 | |||
| ДЕРМАЛЬНАЯ ИНЪЕЦИРУЕМАЯ СТЕРИЛЬНАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2653729C2 |
| WO 2019002368 A1, 03.01.2019 | |||
| ГЕЛЬ ГИАЛУРОНОВОЙ КИСЛОТЫ ДЛЯ ВНУТРИКОЖНОЙ ИНЪЕКЦИИ | 2007 |
|
RU2448740C2 |
| Большая Медицинская Энциклопедия // под редакцией Петровского Б.В., 3-е издание, 1989, онлайн версия, Электронный ресурс, URL: | |||
Авторы
Даты
2025-04-29—Публикация
2020-12-01—Подача