(21)4166882/24-25
(22)25.12.86
(46) 30.09.88. Бюл. № 36
(71)Всесоюзный научно-исследовательский институт по охране вод .
(72)Д.В.Савенко, Я.Г.Подоба, Ю .П.Беличенко, Н.П.Якименко
и С.Е.Лебедев
(53)543.25.543.4 (088.8)
(56) Авторское свидетельство СССР . .1165988, кл, G 01 N 33/18, 1986.
Авторское свидетельство СССР № 855497, кл. G 01 N 33/18, 197-9.
(54)ФОТОАКТИВНЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ ДАТЧИК ДЛЯ ОЦЕНКИ ТОКСИЧНОСТИ ЖИДКОСТЕЙ
(57)- Изобретение относится к устройствам для исследования химических свойств веществ, а точнее к анализу воды методом биотестирования с использованием микроводорослей. Изобретение позволяет повысить точность, экспрессность и автоматизацию контроля путем обеспечения оптимальных условий взаимодействия биологического тест-объекта и токсических веществ контролируемой жидкости, получить максимально достоверное значение
функции отклика детектирующим злект- родом за счет повышения динамических характеристик электрохимического датчика и возможности оценки непосредственно в точке контроля. Фотоактивный электрохимический датчик содержит три блока - детектирующий электрод, биологический индикатор и блок подвода света - и состоит из составного корпуса, в верхней части которого установлен термистор и имеется полость для контактов. Детектирующий элект- род включает диэлектрический стеклянный, стержень с полостью, анод, индикаторный электрод и камеру электролита. Биологический индикатор крепится и детектирующему электроду. Для определения токсичности жидкостей первоначально подготавливают биологический индикатор, который устанавливают газопроницаемой пленкой непо-г- средственно на воспринимающую поверхность детектирующего электрода и погружают его в контролируемую жидкость, В зависимости от степени поражения токсическими веществами клеток микроводорослей в энзимном слое они будут по разному фотосинтезировать, что будет выражено в зависимости изменения кислорода во времени. 4 ил.
С/:
с
4
Э
ОС
Изобретение относится к устройствам для исследования химических свойств веществ, а точнее к анализу воды методом биотестирования с ис- . пользованием микроводорослей для оценки токсичности сточных вод, поступающих на очистные сооружения, сбрасывае мьк в водные объекты гидрологической сети или используемых в оборотном водоснабжении предприятий химической, фармацевтической и других отраслей промышленности, а также поверхност- ного стока, поступающего с городских территорий и сельхозугодий в водоемы.
Цель изобретения - повьшение точности, экспрессности и автоматизации контроля путем, обеспечения оптимальных условий взаимодействия биологического тест-объекта и токсических ве- ществ контролируемой жидкости и получение максимального достоверного значения функции отклика детектирующим электродом за счет повышения динамических характеристик электро- химического датчика и возможности оценки непосредственно в точке контроля in situ.
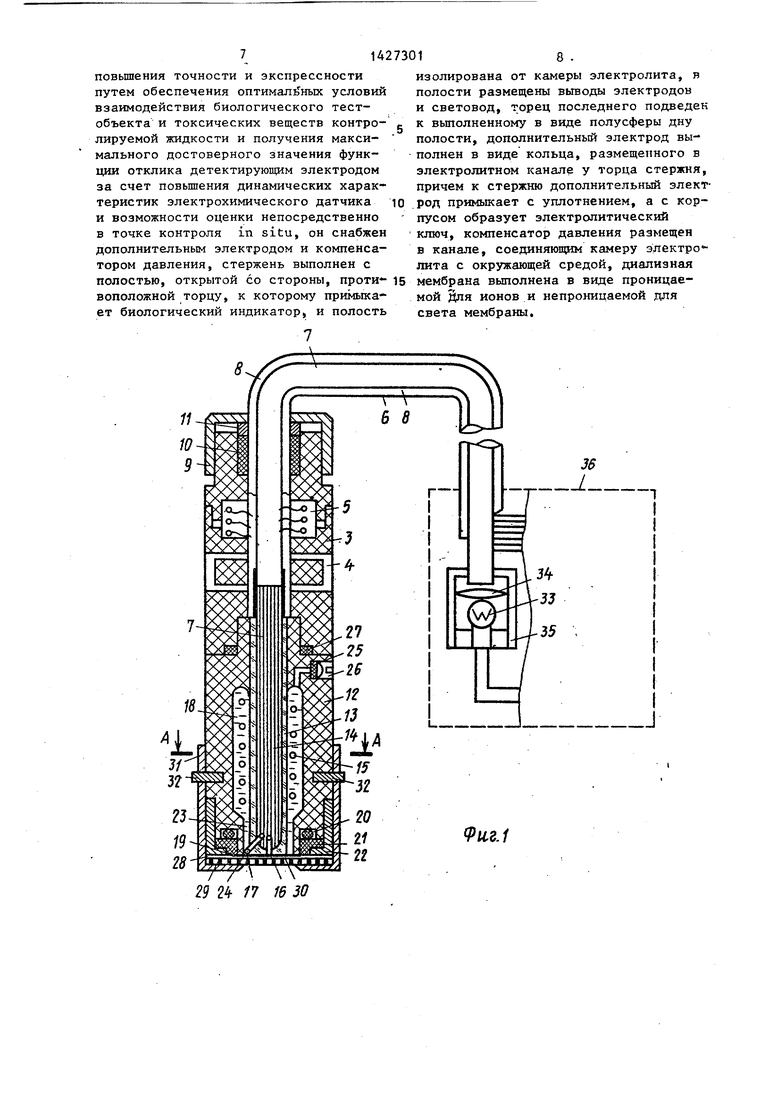
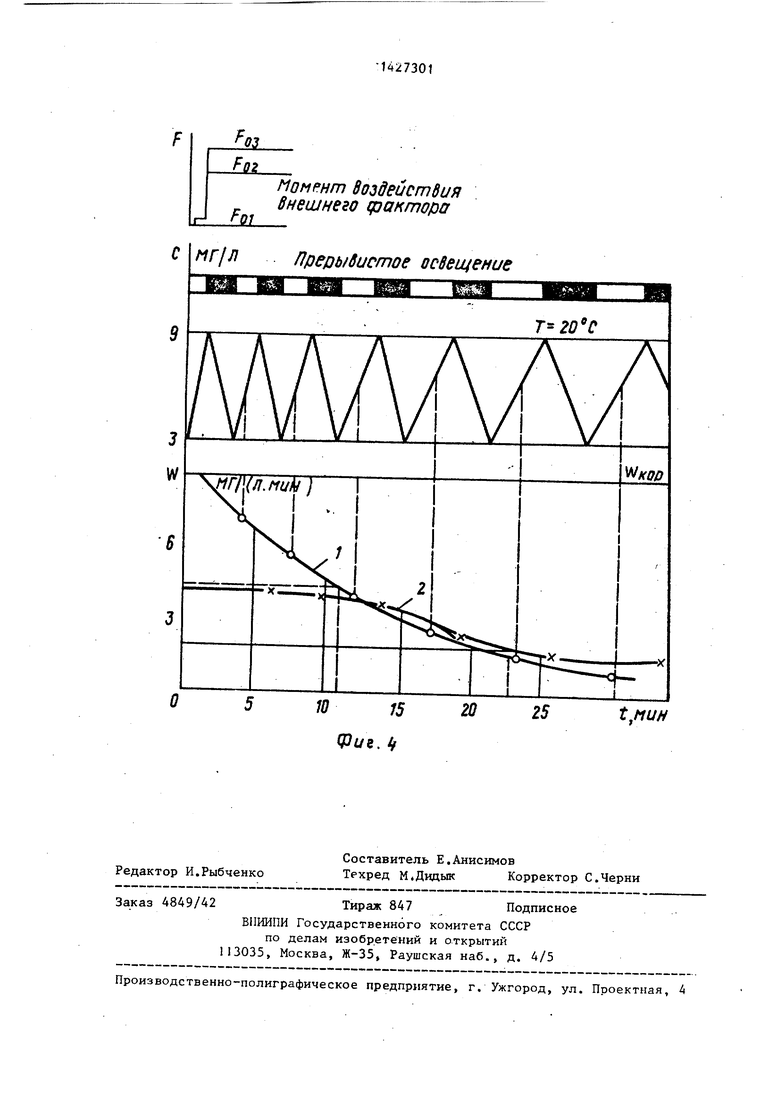
На фиг. 1 изображен фотоактивный электрохимический датчик для оценки токсичности жидкостей, общий вид; на фиг. 2 - разрез А-А на фиг. 1; на фиг. 3 - фотоактивный электрохимический датчик в области биологического индикатора; на фиг, 4 - форма по-, лучения и обработка результатов измерения (кривая 1 - зависимость активности фотосинтеза во времени при воздействии токсических веществ; кривая 2 - зависимость активности дыхания во времени при аналогичных условиях).
Фотоактивный электрохимический датчик для оценки токсичности жидкостей включает в себя Три блока (детек- тирующий блок, биологический индикатор и блок подвода света).и состоит из составного корпуса 3, в верхней части которого установлен термистор 4 и имеется полость 5 для контактов. Герметизированный ввод кабеля 6 выполненного в виде световода 7 и расположенных по диаметру электрических проводов 8, выполнен посредством гайки 9, резиновой втулки 10 и кольца 11
Детектирующий блок 12, в качестве которого можно использовать, например электрохимический датчик растворенного кислорода, расположен в нижней части корпуса 3 и включает в себя диэлектрический стеклянный стержень 13 с полостью 14, анод 15, индикаторный электрод (катод) 16 с выводом, дополнительный электрод 17 с выводом и камеру 18 электролита. Камера 18 образована внутренней стенкой полости детектирующего блока 12 и стержнем 13 снизу закрыта полимерной мембраной 19. Мембрана 19 посредством
резиновой прокладки 20, шайбы 21 и гайки 22 плотно прижимается к торцу стержня 13 и равномерно натягивается по торцовой части датчика. Анод
15выполнен из серебряной проволоки диаметром 0,5 мм и пробой не ниже 99,99 в виде намотки на стержень 13, Индикаторньш электрод (катод)
16вварен в торец стержня 13. Камера 18 в нижней части соединена с электролитным каналом 23, раз- мещеннем у приторцовой части стержня 13. В электролитном канапе 23 установлен дополнительный электрод 17, выполненный в виде кольца, размещенного у торца стержня 13., К стержню 13 дополнительный электрод
17примыкает с уплотнением, а со стенкой корпуса детектирующего блока 12 образует электролитический ключ 24. Электрический вывод дополнительного электрода 17 выполнен через боковую стенку стержня 13 и введен в полость 14 и далее в кабель 6.
Полость 14 стержня 13 открыта со стороны, противоположной торцу, в которьм вварен индикаторный электрод 16. Полость 14 изолирована от камеры 18 электролита, а дно вьшолнено в виде полусферы. В полость 14 введен конец световода 7, .который своей торцовой частью соприкасается с дном полости 14.
Б верхней части детектирующего блока расположен компенсатор гидростатического давления, выполненный в виде эластичной, например резиновой, мембраны 25, которая закрепле- на по периферии пробкой 26 со сферическим дном. Детектирующий блок 12 герметично крепится к корпусу 3 посредством резиновой прокладки 27. Непосредственно на полимерную мембрану 19 детектирующего блока 12 установлен биологический индикатор, выполненный в виде двух слоев, из
J1427301
которых один слой со стороны торца цаемой пленкой 28 непосредственно стержня 13 представляет собой газо- на воспринимающую поверхность детекти- проницаемую пленку 28, а другой слой- рующего блока 12 и закрепляют гайкой


| название | год | авторы | номер документа |
|---|---|---|---|
| Фотоактивный электрохимический датчик для оценки токсичности жидкости | 1983 |
|
SU1165988A1 |
| Устройство фотоактивное электрохи-МичЕСКОЕ для ОцЕНКи ТОКСичНОСТи жид-КОСТЕй | 1979 |
|
SU840738A1 |
| Фотоактивное электрохимическое устройство для оценки токсичности жидкости | 1981 |
|
SU1029077A1 |
| Датчик для оценки токсичности жидкости | 1979 |
|
SU855497A1 |
| Способ определения токсичности жидкостей и устройство для его осуществления | 1981 |
|
SU1010557A1 |
| Устройство фотоэлектрохимическое для оценки токсичности жидкости | 1980 |
|
SU957104A1 |
| Способ определения токсичности жидкостей | 1986 |
|
SU1399673A1 |
| Устройство для оценки токсичности жидкостей под давлением | 1981 |
|
SU945793A1 |
| Способ оценки токсичности водной среды | 1990 |
|
SU1784914A1 |
| БИОТЕРМОФОТОЭЛЕКТРОКАТАЛИТИЧЕСКАЯ КОГЕНЕРАЦИОННАЯ УСТАНОВКА ДЛЯ ЭКОЛОГИЧЕСКИ БЕЗОПАСНОЙ УТИЛИЗАЦИИ СВАЛОЧНОГО БИОГАЗА | 2007 |
|
RU2362636C2 |
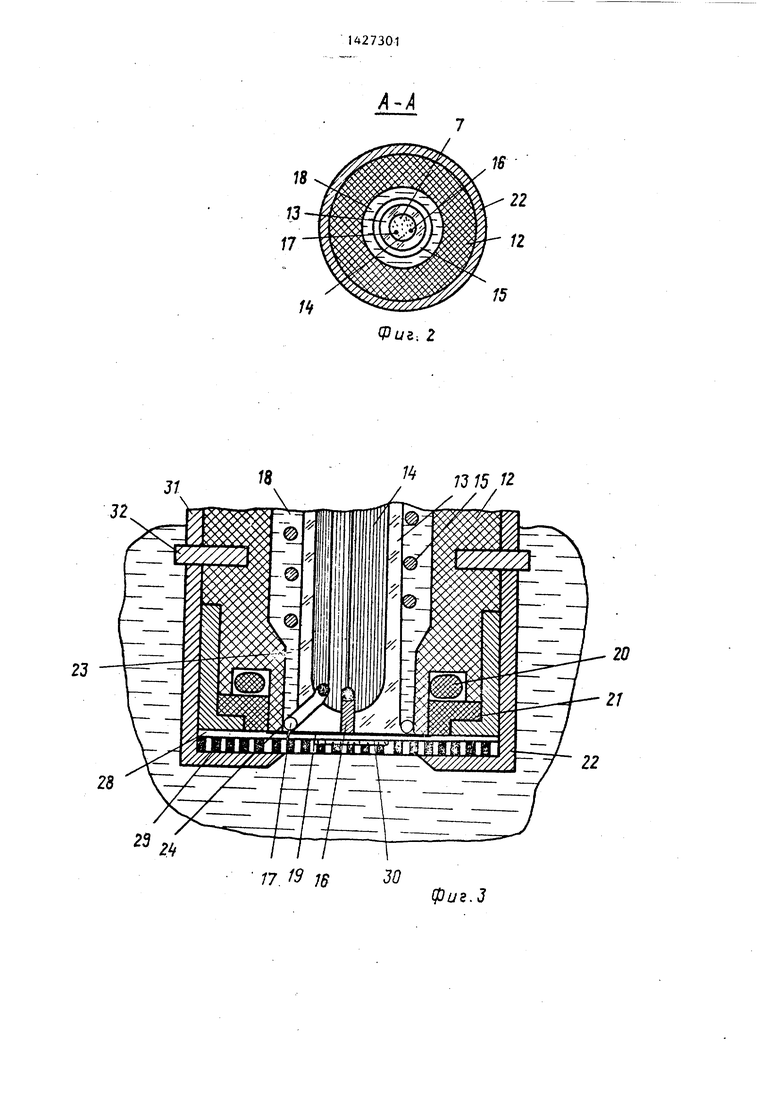

диализную мембрану 29, содержащую цилиндрическую полость для слоя 30 энзима. Биологический индикатор крепится к детектирующему блоку 12 посредством гайки 31 и штифтов 32 байо- нетным креплением.
Внутренний диаметр корпуса детектирующего блока 12 в электролитном канале 23, т.е. наружный диаметр этого канала, и диаметр стержня 13
определяют по соотношению
D.
(1,1 - 1,2) D,,
где DH - внутренний диаметр корпуса в электролитном канале, мм; D - диаметр стержня, мм.
с 31. Детектирующий блок 12 погружают в контролируемую жидкость и выдерживают в течение 10 мин. Так как биологический индикатор затемнен, то клетки микроводорослей в этот период 10 поглощают кислород (процесс дыхания) в иммобилизованном энзимном слое 30, а также кислород контролируемой жидкости, экранируя при этом воспринимающую поверхность детектирующего 15 блока 12 от проникновения кислорода на его поверхность. Примерно через 2-3 мин показание детектирующего блока 12 равно нулю (концентрация кислорода на его воспринимающей поверхИсточник 33 и линза 34 уста-20 ности равна нулю) . Нулевое содержа- новлены в корпусе 35 измерительного кислорода используется для кали- блока 36. бровки и проверки работоспособности
Измерительный блок 36 включает в . детектирующего блока 12, Очевидно, себя усилитель и несколько блоков, что киспород, индуцируемой клетками которые позволяют усиливать выходной ыикроводорослей, благодаря наличию ток фотоактивного датчика и фиксировать соответствующие значения на цифровом индикаторе. Одновременно измерительный блок 36 по заданной программе обрабатывает на микрокалькуля-30 ном электроде. Кроме того, кислород торе результаты измерения при оценке энзимного слоя 30 может диффундиро- токсичности жидкостей и конечный результат фиксирует на цифровом индикаторе. Измерительный блок 36 выполнен переносным массой 3,5 кг и снабжен 35 контролируемой жидкостью и иммобили- кожухом с ремнем для переноса и удоб- зованным слоем всегда значительно ства в работе непосредственно у водоема.
Оценка токсичности жидкостей фотоактивным электрохимическим датчиком 40
краевых эффектов диффундирует и к электролиту детектирующего блока 12. Однако в камеру 18 он не проникает и восстанавливается на дополнительвать в контролируемую жидкость. Однако этого практически не происходит, так как градиент концентраций между
меньше или равен нулю. В то же время между слоем и воспринимающей поверхностью детектирующего блока 12 он имеет максимальное значение за счет потребления кислорода индикаторным Т6 и дополнительным 17 электродами.
осуществляется следующим образом.
Первоначально подготавливают биологический индикатор. Изготовление биологического индикатора может быть осуществлено следующим образом. В центре диализной мембраны 29 диаметром 11 мм, изготовленной, например, из черного капрона с ячейкой 1-2 мкм и толщиной 20 мкм, выбирается полость диаметром 2 мм и глубиной 10 мкм, в которую методом фильтрации наносится тонкий слой 30 микроводорослей хлорелла или сценедесмумс. Сверху диализная
За период световой экспозиции центрация кислорода изменяется от нулевого значения до установившей концентрации. В начальный момент к матическая кривая этого процесса носит практически линейный характ
мембрана 29 закрывается газопронизае- мой пленкой 28, изготовленной из поли-55 затем постепенно отклоняется от этилена диаметром 11 мм и толщиной линейного. Поэтому для сокращения 5 мкм.
Подготовленный заранее биологический индикатор устанавливают газопронйвремени измерения и более достове ного определения характеристики с рости предпочтительно в расчетах
детектирующего блока 12, Очевидно, что киспород, индуцируемой клетками ыикроводорослей, благодаря наличию ном электроде. Кроме того, кислород энзимного слоя 30 может диффундиро- контролируемой жидкостью и иммобили- зованным слоем всегда значительно
краевых эффектов диффундирует и к электролиту детектирующего блока 12. Однако в камеру 18 он не проникает и восстанавливается на дополнительетектирующего блока 12, Очевидно, что киспород, индуцируемой клетками икроводорослей, благодаря наличию ном электроде. Кроме того, кислород энзимного слоя 30 может диффундиро- контролируемой жидкостью и иммобили- зованным слоем всегда значительно
вать в контролируемую жидкость. Однако этого практически не происходит, так как градиент концентраций между
етектирующего блока 12, Очевидно, что киспород, индуцируемой клетками ыикроводорослей, благодаря наличию ном электроде. Кроме того, кислород энзимного слоя 30 может диффундиро- контролируемой жидкостью и иммобили- зованным слоем всегда значительно
меньше или равен нулю. В то же время между слоем и воспринимающей поверхностью детектирующего блока 12 он имеет максимальное значение за счет потребления кислорода индикаторным Т6 и дополнительным 17 электродами.
В зависимости от степени поражения токсическими веществами клеток микро- водорослей в энзимном слое 30 они по разному фотосинтезируют, что выражается в наклоне кривой зависимости изменения кислорода во времени.
За период световой экспозиции концентрация кислорода изменяется от нулевого значения до установившейся концентрации. В начальный момент кинематическая кривая этого процесса носит практически линейный характер.
затем постепенно отклоняется от линейного. Поэтому для сокращения
затем постепенно отклоняется от линейного. Поэтому для сокращения
времени измерения и более достоверного определения характеристики скорости предпочтительно в расчетах использовать линейный участок кинематической кривой на протяжении первых 1-2 мин освещения, ограниченный кон- центра1щями кислорода 3-9 мг/л.
При достижении концентрации кислорода в иммобилизированном слое 30, например5 9,0 мг/л источник 33 света выключается (фиг. 4) и происходит последующее потребление кислорода в иммобилизованном слое 30, которое определяется дете ктирующим блоком 12, При достижении концентрации кисло рода, например, 3,0 мг/л источника 33 света снова включается и начинаетг ся очередное выделение кислорода и его измерение детектирующим блоком 12,, Далее цикл повторяется. Таким образом можно получить серию кривых зависимости активности фотосинтеза и дыхания во времени при воздействии токсических веществ контролируемой жидкостис Оценку токсичности производят например, по уменьшению на 50% активности фотосинтеза или дыхания по сравнению с первоначальными калибровочными значениями или по определению времени достижения заданного значения з еньшения активности фотосинтеза. дыхания.
Первоначальные калибровочные знача ния периодически получают, погружая датчик в калибровочную жидкость, например водопроводную воду или среду питанияJ и определяя указанным методом скорость фотосинтеза и дыхания. Выбор скорости для фотосинтеза может регулироваться интенсивностью осе- вещенности иммобилизованного энзимного слоя 30 Периодичность получения калибровочных значений определяется состоянием биологического индикатора и составляет примерно один раз для 30--40 измерений. Невозможность получения первоначальных значений скорое- 45 корпуса образует камер электролита тей фотосинтеза и дыхания свидетельст- и соединенный с ней электролитный
вует о непригодности использования биологического индикатора для оценки токсичности жидкостей и требует его замены.
Контролируемая жидкость может иметь различную температуру Поэтому в датчике предусмотрен термистор 4, выполненный .в виде белкорпусного
транзистора. Измеряя температуру конт-дц мембрану, содержащую цилиндрическую
ролируемой жидкости, вводят соответствующие поправки в измерительном блоке 36 на изменение выходного сигнала детектирующего электрода, йзмененке
температуры учитывается также при определении процессов фотосинтеза и дыхания.
. Датчик без биологического индикатора работает как электрохимический датчик дпя измерения концентрации растворенного кислорода 0-25 мг/л и температуры 0-40°С. Высокие динамические характеристики, обусловленные принятыми техническими решениями, позволяют также с высокой точностью определять концентрацию растворенного кислорода в прир одных и сточных водах.
Погрешность измерения для данной
конструкции достигается +1% ,(сов5)е- менные кислородомеры имеют погрешность измерения +5%), нижний предел обнаружения кислорода 0,05 мг/л.
Электрохимический датчик работает совместно с комбинированными приборами и -сигнализаторами для определения концентрации растворенного кислорода, температуры и. оценки токсичности
жидкостей (окситоксиметрами), Датчик прост в изготовлении, не требует высококвалифицированного персонала для обслуживания. Он может быть ис- .пользован в автоматических промьшшен-
ных, лабораторных и переносных приборах и сигнализаторах прИ контроле состава природных и сточных вод
35
40
Формула изобретения
Фотоактивньй. электрохимический датчик для оце«ки токсичности идкос- тей, содержащий детектирующий электрод, биологический индикатор и блок подвода света, при этом детектирующий электрод включает корпус с раз- мещенным в нем анодом и диэлектрическим стержнем, в торце последнего закреплен катод, стержень со стенкой
канал, рамещенный у приторцовой части стержня, к торцу последнего непосредственно на полимерную мембрану уста- 50 новлен биологический индикатор, выполненный в виде двух слоев, из которых один слой со стороны торца стержня представляет собой газопроницаемую пленку, а другой слой - диализную
полость для энзима, а блок подвода
виде соединенных с
световодов, о т л и- f.
тем, что, с целью
17 1630
1I
911Z.1
31
32
23
29
2
п. 1д 1В
15
Фиг, 2
22
30
физ.З
MoMf Hm боздейстдия Внешнего дзакторо
мг1л прерывистое освещение
t,nuH

Авторы
Даты
1988-09-30—Публикация
1986-12-25—Подача