(21)4202512/04
(22)29.04.37 (31)8610532
(32)30.04.86 (33) GB
(46) 23.04.91. Бнот. 15
(71)Иеринг Агрокемикалз Лимитед (GB)
(72)Дэвид Эрик Грин (GB)
(53)547.892.07(088.8) (56) Патент ФРГ № 3001424, кл. С 07 D 487/04, 1980.
Патент СССР Р 1347865, кл. С 07 D 487/04, 1984.
Патент СССР № 1468423, кл. С 07.D 487/04, 1985.
(54)СПОСОБ ПОЛУЧЕНИЯ ТРИАЗОЛСУЛЬФОН- АМИДОВ
(57) Изобретение относится к гетероциклическим соединениям, в частности к получению триазолсульфонамидов
ф-лы I R (R,)(Ro)-N-C
Ј7 .,.,.... .. ,,,
N-C(S02NHR4), где R , - Н, СН3, С1
или Br; R2 -Н, С1Ц или этил; Р-j Н, СН3 или фенил; Rq -фенил, замещенный от 1 до 4 атомами Cl, F илиСН3, метокси, нит- ро, цианоили карбоксиметильными группами, обладающихгербипидными свойствами. Цель - разработка способа получения более активных соединений. Получение ведут реакцией соединения ф-лы I, где R/j-R - указано выше,.а группа NHR -галоид с амином ф-лы , где R,, - указано выше, в присутствии органического основания. 3 табл.
о 


| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2062576C1 |
| Способ получения сульфоанилидов или их солей с основаниями | 1989 |
|
SU1750428A3 |
| ГЕРБИЦИДНОЕ СРЕДСТВО НА ОСНОВЕ АРИЛСУЛЬФОНИЛАМИНОКАРБОНИЛТРИАЗОЛИНОНОВ | 1997 |
|
RU2240691C2 |
| СЕЛЕКТИВНЫЕ ГЕРБИЦИДЫ НА ОСНОВЕ АРИЛСУЛЬФОНИЛАМИНОКАРБОНИЛТРИАЗОЛИНОНОВ | 2001 |
|
RU2277335C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ N-(АРИЛ)-1,2,4-ТРИАЗОЛОПИРИМИДИН-2-СУЛЬФАМИДОВ | 1992 |
|
RU2061692C1 |
| ГЕРБИЦИДНОЕ СРЕДСТВО | 2002 |
|
RU2303872C9 |
| ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ НА ОСНОВЕ КАРБАМОИЛТРИАЗОЛИНОНА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2539210C2 |
| N-ПИРАЗОЛИЛ-1,2,4-ТРИАЗОЛО-[1,5-С]-ПИРИМИДИН-2-СУЛЬФОНАМИДНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ | 1992 |
|
RU2065861C1 |
| ГЕРБИЦИДНОЕ СРЕДСТВО В ВИДЕ СУСПЕНЗИИ | 2001 |
|
RU2302111C2 |
| АРИЛСУЛЬФОНИЛМОЧЕВИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 1992 |
|
RU2314291C2 |

Изобретение относится к способу получения новых триазолсульфонамидов общей формулы
S00NHR,
где R. - водород, метил, бром;
(I) хлор или
R2 - водород, метил или этил;
RJ - водород, метил или фенил;
R4 - фенил, замещенный от 1 до 4 атомами хлора, фтора или метил, метокси, нитро, циано
или карбоксиметильными группами, обладающих гербицидными свойствами.
Цель изобретения - получение новых производных триазолсульфонамида, обладающих иным спектром биологических свойств, чем известный структурный аналог - прометрин.
Пример 1. М-(2-хлорфенил)- ; 5,7-диметил(1,2,4)триазоло(1,5-с)пиг римидин-2-сульфонамид.
а) 5,7-Диметил-(1,2,4)триазоло (1,5.-с)пиримидин-.-сульфонилхлорид.
Газообразный хлор пропускают через суспензию 5,7-диметил(1,2,4)три- азоло(1,5-с)пиримидин-2-тиола (5,4 г) в воде (50 мл) при 5-10°С и интенсивном перемешивании 30 мин.Твердое сое-динение отфильтровывают и растворяют в дихлорметане (80 мл). Органический раствор промывают водой (10 мл), сушат над сульфатом магния, концентрируют под вакуумом и получают желтое смолистое соединение (2,7 г) которое, как было установлено спектроскопически, является целевым продуктом. 1 Ъ) №-(2-хлорфенил)-5,7-днметил (1,2,,4)триазоло(1,5-с)пиримидин-2- супьфонамид.
Раствор полученного выше сульфонил- „елорида (2,7 г) в дихпорметане (10 мл)
.медленно при 10-15 С прибавляют к перемешиваемому раствору 2-хлоранили- на (1,54 г) в пиридине (20 мл). Температуру поддерживают ниже 15°С. После завершения прибавления смесь оставля™
ют нагреваться до комнатной температуры и перемешивают в течение ночи. Затем ее концентрируют под вакуумом
и к остатку прибавляют 5%-ную хлористоводородную кислоту (15 мл) и эфир (10 мл). Образующееся твердое соединение отфильтровывают и хроматографи- руют одной дозой на силикагеле с помоЩью смеси петролейиого эфира (т.кип. 60т80°С) с этилацетатом (1:1) в качестве элюента. Целевой сульфонамид (1 г) получают в виде твердого соединения кремового цвета (т.шт. 190- 192°С).
I
Примеры 2-38. По методике, описанной в примере 1, получают следующие соединения указанной формулы 1Т а б л и ц а 1
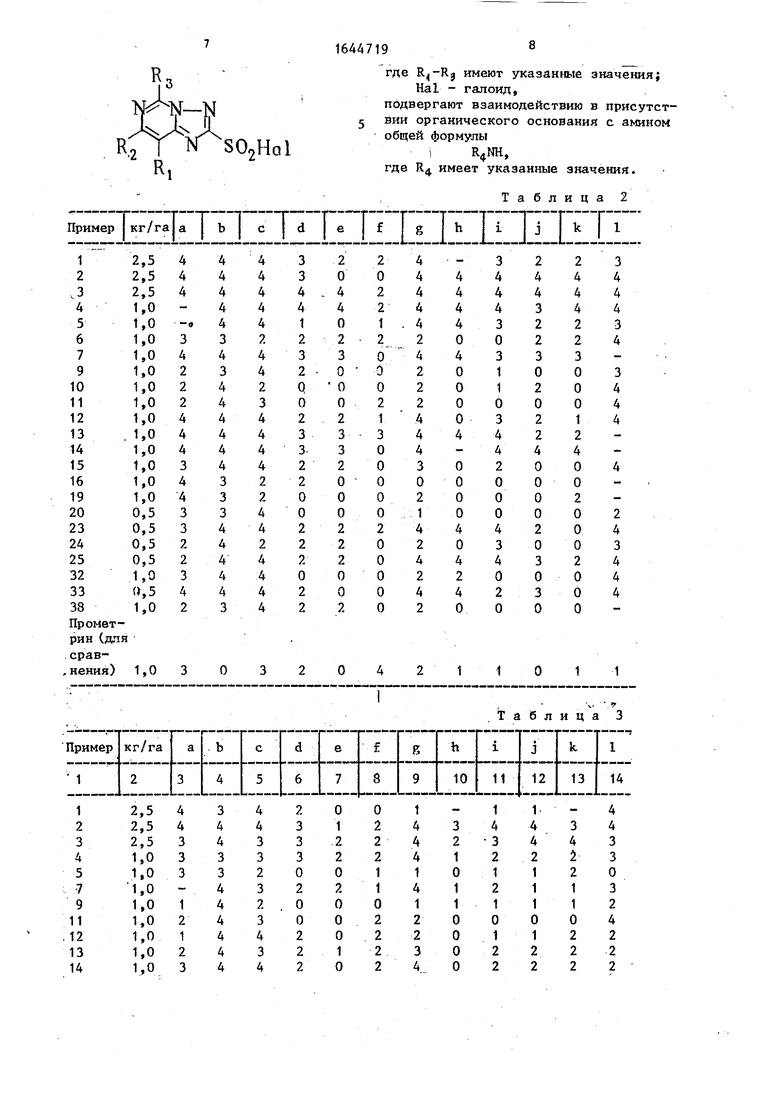
В табл. 2 приведены данные пред- всходовой гербицидной активности.
В табл. 3 приведены данные по ак- тивности при испытании после появле- ния всходов.
Оценка активности произведена по следующей шкале: 0 отсутствие эфа - Polygonum lapathifoliu
b - Galium aparine
с - Chrysanthemum segetum
d - Alopecurus myosuroides
e - Elymus repeus
f - Avena fatua
g - Abutilon theophrasti
h - Cyperus rotundus
i - Pharbitis purpurea
j - Echinochloa crus-galli
k - Setaria viridis
1 - Solanum nigrum
Как видно из приведенных таблиц, соединения указанной формулы являютс гербицидно-активными по отношению к широкому набору широколиственных и травянистых сорняков, но они относительно безопасны для некоторых видов полезных культур. Поэтому их можно использовать как селективные гербициды, в частности, при борьбе с рядом сорняков в злаковых и других культурах, например в пшенице, ячмене, маисе, сое, капусте, хлопке и сахарной свекле.
Формула изобретения
Способ получения триаэолсульфон- амидов общей формулы
Продолжение табл. 1
фекта, 1 эффект 1-24%, 2 эффект 25 - 69%, 3 эффект 70-89% и 4 эффект 90-100%.
5 В таблицах для обозначения видов , растений используют следующие буквенные обозначения:
I
(горец шероховатый);
(подмаренник цепкий);
(златоцвет);
(лисохвост мышехвостниковый);
(пырей);
(овсюг);
(канатник Теофраста);
(сыть пурпурная);
(ипомея);
(просо петушье);
(щетинник зеленый);
(сыть черная).
45
SOoNHR,
где R
- водород, бром;
метил, хлор или
R4 - водород, метил или этил; | R3 - водород, метил или фенил; R, - фенил, замещенный 1-4 атомами хлора, фтора или метил, метокси, нитро, циано или карбоксиметильными группами, отличающийся тем, что сульфонил галогенид общей формулы
Авторы
Даты
1991-04-23—Публикация
1987-04-29—Подача