Изобретение относится к молочной промышленности, а именно к получению очищенных гидролизатов молочных белков (ОГМБ) с высокой биологической ценностью, обладающих гипоаллергенными свой- ,ствами, используемых при производстве широкого ассортимента продуктов лечебного питания, в т.ч. для детей и взрЪслых, страдающих пищевой аллергией.
Известен способ получения гидролиза- таказеина пищевого(1). Гидролизатказеина вьфабатывают из обезжиренного молока путем его осаждения молочно-кислотным способом с последующим ферментативным гидролизом и сушкой. Продукт предложен для детского и диетического питания в качестве белковой основы..
Существенными недостатками способа являются: поверхностный гидро лиз, который не снижает гипоаллергенных свойств гидролизата, а также наличие в его составе остаточных количеств сывороточных белков; большие энергетические затраты и потери сырья по всему технологическому циклу; несбалансирован- ность по аминокислотному скору конечного продукта.
Наиболее близким к предлагаемому являются способ получения гидролизатов молочныхбелков, обладающих гипоаллергенными свойствами. Согласно этому способу, который предусматривает получение белкового концентрата из обезжиренного молока, сыворотки или их смеси в требуемой пропорции с применением про- цессрв ультра- и диафильтрации, приготовление и пастеризацию белкового раствора, ферментативный гидролиз,, инактивацию фермента. УФ-разделение и получение ОГМБ с различной молекулярной массой пептидов. дополнительную УФ обработку, причём кратность пропускания ОГМБ зависит от массовой доли сывороточных белков в исходном сырье и равна соответственно:
п - 0.5 + 0,025 Бс,(1) где п - кратность повторного пропускания ОГМБ, крат.;
0,5; 0,025 - пересчетные коэффициенты,
Бс - массовая доля сывороточных белков. %.
Особое внимание при этом уделяется сывороточным белкам, в частности, / -лак- тоглрбулину (БЛГ). как наиболее опасному источнику гипоаллергенных свойств белкового гидролизата. Кратность повторного пропускания была выбрана с учетом массовой доли БЛГ в 20%-ном растворе ОГМБ, которая при проведении иммунохимиче- ских исследований не должна обнаруживаться. Гидролизаты, выработанные по
данной технологии, имеют сниженные аллергенные свойства в сравнении с натив- ным белком молока.
Существенными недостатками способа- прототипа являются: низкая экономическая эффективность процесса, т.к. способ предусматривает до 3-х дополнительных УФ- обработок (в случае сывороточных белков); процесс направлен; на очистку ОГМБ от на- тивных сывороточных белков, в частности от БЛГ, что является явно недостаточным, т.к. в данном случае получаются препараты с широким диапазоном изменений молекулярных масс пептидов. а также соотношений между ними; получаемые по данной технологии ОКМБ не могут использоваться в лечебных целях при острых формах пищевой аллергии, т.к. обладают довольно высокими показателями тяжести пищевой анафилакции, в т.ч. летальность (29,4- 33,3%), судороги (33,3-47,1%), анафилактический индекс (60,7-63.9).
В связи с этим диапазон их использования сужен до использования в профилактических целях.
Целью изобретения является снижение гипоаллергенных свойств гидролизата и повышение производительности процесса, расширение ассортимента продуктов лечебного питания на основе ОГМБ.
Поставленная цель достигается тем, что в известном способе получения гидролизата молочных белков, предусматривающем пастеризацию исходного белкового pacfeo- ра, его ферментативный гидролиз, основнуюи дополнительную ультрафильтрационную обработку и получение очищенного гидролизата молочных белков различной молекулярной массой пептидов, полученный после основной уль- трафильтрационной обработки гидролизат в виде фильтрата подвергают дополнительному ферментативному гидролизу с последующей дополнительной ультрафильтрационной обработкой на мембранах с пропускной способностью по молекулярной массе от 500 до 1000 дальтон при кратности концентрирования от 2 до 10 и давлении от 0,75 до 2,5 МПа.
Существенными отличиями предлагаемого способа от прототипного являются:
использование после основной УФ-об- работки процесса ферментативного гидролиза, что существенно изменяет пептидный профиль белкового гидролизата в сторону увеличения квоты пептидов с молекулярной массой пептидов 1000 дальтон до 90% и тем самым увеличить выход продукта;
использование в процессе дополнительной УФ-обработки мембран с пропуской способностью оо молекулярной массе т 500 до 1000 дальтон, позволяет получать ГМБ требуемого пептидного профиля, а акже исключить УФ-обработку с кратно- ью пропускания 2;,
кратность концентрирования от 2 до 10, оторая позволяет снизить массовую долю ысокомолекулярных пептидов в 10-100 аз:
давление при дополнительной УФ-об- аботкеотО,75до2,5 МПа повышает эффектность разделения от 2-х до 5-ти раз.
Предлагаемый способ предусматривает спользование после основной УФ-обра- отки процесса ферментативного гидроли- а. Введение данной технологической перации обусловлено несколькими причи- ами.
Во-первых, в процессе ферментативно- гидролиза перед основной УФ-обработ- ой при массовой доле сухих веществ в астворе дол 10% образуется дополнительное количество пептидов (дол 85%) в широ- к эм диапазоне изменения молекулярных, асе (до 10000 дальтон), которые выступают нгибиторами в процессе гидролиза, тем с 1мым резко снижая его эффективность, аиболее ценной является пептидная фрак- /1я с-молёкулярной массой пептидов 1000 льтоц, которая занимает незначительную лю (до 30%) в общей массе пептидов. До- п элнительная операция ферментативного ri дролиоза, но уже только с использованием ферментов, гидролизующих пептиды (пептидаз), приводит к увеличению выше- уг омянутой квоты до 90%,
Впервые предложены для получения О МБ УФ-мембраны с диапазоном пропускной способности по молекулярной массе от 500 дол 1000 дальтон.
Использоавние УФ-мембран с пропуск- нс и .способностью, по молекулярной-массе 5С 0 дальтон становится нецелесообразным в :вязи с тем, что:
: падает эффективность процесса из-за резкого повышения селективности мемб- ра|н, в т.ч. по пептидам с мол. массой 1000 дальтон до 70%; баромембранный процесс входит в об- ла ;ть обратного осмоса, что требует исполь- зо зания высоких давлений 3,0 МПа. При этим процесс обратного осмоса всегда ис- потьзовэлся для концентрирования и ни- ко да. не использовался для разделения пищевых веществ.
Использование УФ-мембран с пропуск- 1 способностью 1000 дальтон также нецено
ле
ообразно ввиду того, что в готовом парате булуг пептнды с молекулярной
массой 1000 дальтон, которые резко снижают его гипоаллергенные свойства.
Использование данных УФ-мембран позволит получать ОГМБ требуемого пеп- 5 тидного профиля, а также исключить дополнительные УФ-обработки, тем самым резко повысить эффективность процесса. Очень важным показателем при УФ-обработке препаратов с целью очистки от высокомоле- 10 кулярных соединений (ВМС) является кратность концентрирования. Массовая доля ВМС в фильтрате повышается и находится в прямой зависимости от кратности концент- риро§ания.
15 Предложенный диапазон кратности концентрирования ультрафильтрацией от 2 до 10 вполне объясним, т.к. позволяет соответственно снижать массовую долю ВМС в среднем от 100 до. 10 раз.
0 При кратности концентрирования 2 эффективность процесса резко падает,. Это объясняется тем, что на фоне незначительного изменения массовой доли ВМС в.филь- трате (сотые доли процесса) значительно
5 уменьшаются объемы получаемого препарата. При кратности концентрирования 10 эффективность процесса также резко падает. Однако в. данном случае можно наблюдать обратную ситуацию: на фоне
0 незначительного изменения получаемых объемов препарата (от 1 до 10%) значительно изменяется в сторону увеличения массо- оваядоля ВМС в фильтрате (от 10-99%). что ухудшает качество продукта.
5 На эффективность процесса дополнительной УФ-обработки влияет диапазон давлений, который ранее при УФ-обработке пищевого сырья не применялся.
Предложенный диапазон давлений, в
0 котором проходит процесс, находится на стыке ультрафильтрации (диапазон давлений 0,1-0,7 МПа) и обратного осмоса (диапазон давлений 3,0-6,0 МПа).
Проведенными исследованиями в Инс5 титуте питания АМН СССР установлено изменение селективности УФ-мембран по ВМС (до 99,9%) при увеличении давлений фильтрации.
Применение давлений 0,75 МПэ приве0 дет к неоправданному снижению эффективности процесса (в 5 раз), а применение давлений 2,5 МПа приведет к резкому уплотнению УФ-мембраны, и как следствие этого к резкому снижению производительности, а также к резкому повышению селективности, в т.ч. к пептидам с молекулярной массой 1000 дальтон.
Предлагаемый способ получения О КМ Б заключается в следующем.
Подсырную сыворотку по ОСТ 49 92-75 очищают на сепараторах-очистителях непрерывного действия марки А1-ОХ2-С от жира и казеиновой пыли, пастеризуют при 70-74°С и выдержке 17-19 с, охлаждают до температуры УФ и подают в ультрафильтра- ционную установку (отечественного производства марки А1-ОУВ или фирмы OPS) с диаметром пор ультрафильтрационных мембран 50 ± 10 нм.
Концентрирование осуществляют при давлении 0,05-0.7 МЛа .и температуре 5- 55°С до массовой доли сухих веществ в концентрате 8-27%. В концентрате сыворотки добавляют обезжиренное молоко, полученное при сепарировании цельного молока (заготовленного по ГОСТ 13264-70) и затем пастеризованного при температуре 70- 74°С и выдержке 17-19 с, в зависимости от требуемого соотношения казеина к сыворо- белкам от 1/99 до 80/20. Расчет массы обезжиренного молока или сыворотки производят по следующим формулам:
M80JQ БК/20 (О.в - 0.2К)
К Б/99 К Bvgg MVgg
Ml/991
.(2)
МвО/20
(3)
.)1 где М 1/9.9 - масса сыворотки ультра- или диафмльтрационногсг концентрата сыворотки, кг;
Мао/20 - масса обезжиренного молока, ультра- и диафильтрационного концентрата обезжиренного молока, кг;
Б1/99 - массовая доля белка в соответствующей М1 /99. %;
Бво/20 - массовая доля белка в соответствующей Мво/20. %;
К - коэффициент, равный требуемого К/С. .
Формулы (2) и (3) были получены с учетом средних данных по содержанию сывороточных белков и казеина в обезжиренном молоке и сыворотке. Они носят универсальный характер, т.к. позволяют производить необходимые расчеты независимо от вида исходного сырья (обезжиренное молоко или сыворотка, их УФ- или ДФ-концентрат).
Для получения гидролизатов с соотношением К/С 80/20 используют только обезжиренное молоко, а для гидролизатов сывороточных белков (К/С 1/99) только сыворотку. Операция нормализации Для этих двух видов гидролизатов отсутствует.
Далее осуществляют концентрирова- ние смеси до массовой доли сухих веществ в концентрате 22-27% с последующей диа- фильтрэцией промывной водой с рН 4,7-7.0. Промывку УФ-концентрата осуществляют до содержания сухих веществ в уходящем
фильтрате 0,2-0,3%. Получают безлактоз- ный диафильтрационный концентрат с требуемым соотношением К/С. Концентрат пастеризуют при 70-74°С с выдержкой 1719 с, и охлаждают до 40-50°С.
Затем проводят разбавление полученного концентрата пастеризованной и охлажденной до 40-50°С питьевой водой (ГОСТ 2874-82) до массовой доли сухих ве0 ществ 8,0-10,0%. вносят лимоннокислую соль калия или натрия в количестве 1,0- 5,0% к сухим веществам концентрата. При необходимости интенсификации процесса гидролиза температурную обработку прово5 дят после процессов разбавления и внесения солей, при этом используют следующие , тепловые режимы: температура 100-140°С с выдержкой от 10с до 4 мин или температура 75-100°С с выдержкой от 2 до 60 мин с
0 последующим охлаждением до 40-50°С.
В концентрате устанавливают рН 6,7- 7,5 добавлением 10%-ного раствора едкого калия или гидроокиси кальция. Вносят фермент панкреатин медицинский по ГФ IX
5 изд. 1961, ст. 362 активностью 25-30 единиц в количестве 0,1-1,0% от массовой доли сухих веществ концентрата. Гидролиз проводят в течение 10 мин - 4 ч до массовой доли , аминного азота 5-16%. Процесс гидролиза
0 контролируют по нарастанию аминного азота, массовую долю которого определяют по ТУ 49 1034-83. После гидролиза измеряют рН и устанавливают его равным 6,7-7,2. Полученный гидролоизат направляют или
5 на инактивацию или сразу на УФ-разделе- ние. В первом случае гидролизат направляют на пластинчатую пастеризационную , установку для инактивации фермента, которую осуществляют при 78-90°С в течение 10
0 мин - 1 ч. Гидролизат подают на УФ-уста- нрвку, которая укомплектована мембранами с пропускной способностью по молекулярной массе, равной 1000-10000 дальтон. Концентрирование осуществляют
5 при давлении 0,05-0,7 МПа и температуре 5-55°С до массовой доли сухих веществ в концентрате 22-27%. Промывку УФ-концентрата осуществляютЪастеризованной и охлажденной до 5-55°С питьевой водой до
0 содержания сухих веществ в уходящем фильтрате 0,2-0,9%. Фильтрат(ОГМБ) собирают в отдельную емкость, причем сбор фильтрата прекращают по достижению массовой доли сухих веществ в нем. равной 15 3%. что обусловлено высоким содержанием ВМС в пересчете на сухое вещество ОГМБ. Собранный в отдельной емкости ОГМБ направляют на повторный ферментативный гидролиз. Для этого используют протеазу (из Bacillus subtilis), иммобилизованную на
.илохроме, которую готовят по ТУ 6-09-10- 1627-84 (оптимум действия рН от 8,0 до 8,1,
емпература от 30 до 40°С).
Перед повторным гидролизом измеряет рН ОГМБ и устанавливают его равным
5,0-8,1. Температуру устанавливают равной $0-40°С. Затем проводят гидролиз, прокачивая ОГМБ через колонку с иммобилизо- панным ферментом (до достижения массовой доли аминного азота от 15 до ( 0%). Собранный после повторного гидро- / иза в отдельную емкость ОГМБ направля- i JT на дополнительную УФ-обработку, i оторую проводят На УФ-установке, укомп- /ектованной мембранами с пропускной способностью по молекулярной массе от Ј00 до 1000 дачьтон. Кратность концентри- р ования при УФ-обработке составляет от 2 f.o 10 крат; давление от 0,75 до 2,5 МПа, т эмпература от 5 до 75°С.
i После дополнительной УФ-обработки в С ГМБ измеряют рН, устанавливают его рав- н от 6,65 до 6,85 и направляют его на д )льнейшее использование, которое может з 1ключаться в следующем:г либо препарат сразу используют (в каЧ1г
Bi
cvxoro ОГМБ.
Оставшуюся часть ОГМБ (концентрат) пс еле дополнительной УФ-обработки снова правляют на повторный ферментативный ролиз с использованием протеаз, Пример Для получения ОГМБ с К/С 80/20 используют обезжиренное молоко в количестве 63460 кг с массовой долей белка З1,, полученное при сепарировании цельно
стве полуфабриката) при производстве поаллергенных продуктов;
либо его направляют на вакуум-выпари- ние с последующей сушкой и получением
и затем пастеризованного при темпера- 70°С
го
ту е 70°С и выдержке 17 с, подают в
Ус «-установку. Концентрирование осуществл ;ют при давлении 0,05 МПа, температуре
5° и рН 4,7, которое достигают подкислением 0.1 н раствором HCI до м.д. с.в, в
концентрате 22% с последующей диафильтр
со/
за
M.f.
жн
кг 20%-ного раствора белка обезжиренного моАока, который пастеризуют при 70°С.с выдержкой 17 с, охлаждают до 40°С. Затем npq водят разбавление полученного концен- трата пастеризованной и охлажденной до 40°С питьевой водой в количестве 13298 кг до л.д.с.в. 8,1 %, вносят лимоннокислый кз- ли|/ в количестве 19,8 кг (1% к сухим веще- стввм концентрата), устанавливают рН 6.7
цией подкисленной до рН 4,7 0,1 н и яной кислотой питьевой водой. Контроль окончанием процесса осуществляют до .с.в. в уходящем фильтрате, которая дол- з быть 0,2%. Получают после ДФ 10000
10
5
0
5
0
5
0
5
5
0
добавлением 10%-ного раствора едкого калия или гидроокиси кальция. Вносят, фермент панкреатин медицинский в количестве 0,99 кг (0,1 % отм.д.с.в. концентрата). Гидролиз проводят в течение 10 мин до массовой доли аминного азота 5%. После гидролиза потенциометрически определяют рН и устанавливают его равным 6,7. Инактивируют фермент пастеризацией при 78°С в течение 1 ч, а затем охлаждают до 5°С. Гидролизо- ванный инактивированный охлажденный концентрат подают в УФ-установку, которая укомплектована мембранами с пропускной способностью по молекулярной массе, равной 10000 дальтон. Концентрирование осуществляют при давлении 0,05 МПа и температуре 5РС до м.д.с.в. в концентрате 22%. Диафильтрацию осуществляют пастеризованной и охлажденной дло 5°С питьевой водой до содержания сухих веществ в уходящем растворе - фильтрате 0,2%. ОГМБ (фильтрат) в количестве 20000 кг с м.д.с.в. 1,5% в растворе собирают в отдельную емкость и направляют на повторную УФ-обработку на УФ-мембранах с тем же диаметром пор. Кратность пропускания ОГМБ определяют по формуле (1), откуда
п 0,5 + 0.25- 20 1.
Таким образом, после определения ОГМБ еще раз пропускают через мембраны с пропускной способностью 10000 дальтон. Очищенный от остаточных концентраций БЛГ ОГМБ в количестве 20000 кг м.д.с.в. 1,5% направляют в отдельную емкость. Затем его используют по назначению. Полученный в процессе УФ-разделении 20%-ный концентрат ВМС в количестве 8500 кг направляют на повторное использование ОГМБ, полученный по технологиие- ским параметрам в приведённом примере, характеризуется следующими свойствами:
высокой биологической ценностью (скор. 0,86),
ОГМБ содержит в своем составе большое количество крупных пептидов с размерами 8000-10000 дальтон (20%), 50-8t) дальтон (80%), полностью очищен от БЛГ, обладает сниженной на 30% алергенно- стью. а также гипоаллергенными свойствами, которые являются недостаточными для его использования в качестве белкового компонента при производстве продуктов, обладающих гипоаллергенным действием.
Пример 2. Для получения ОГМБ с К/С 80/2Р используют обезжиренное молоко в количестве 63460 кг с массовой долей белка 3%. полученное при сепарировании цельного и затем пастеризованного при 70°Си выдержке 17с. подают в УФ-установку. „Концентрирование осуществляют при
давлении 0,05 МПа. температуре 5°С и рН 4,7. которое достигают подкислением 0,1 н, раствором HCI до м.д.с.в. в концентрате 22% с последующей диафильтрацией подкисленной до рН 4,70,1 н. соляной кислотой питьевой водой. Контроль за окончанием процесса осуществляют по м.д.с.в. в уходящем фильтрате, которая должна быть 0,2%. Получают после диафильтрации 10000 кг 20%-ного раствора нативного белка обезжиренного молока, который пастеризуют при 70°С с выдержкой 17 с, охлаждают до 40°С. Затем проводят разбавление полученного концентрата пастеризованной и охлажденной до 40°С питьевой водой в количестве 13298 кг до м.д.с.в. 8,1 %, вносят лимоннокислый калий в количестве 19,8 кг (1 % к сухим веществам концентрата), устанавливают рН 6,7 добавлением 10%-ного раствора КОН или Са(ОН)2. Вносят фермент панкреатин медицинский в количестве 0,99 кг (0,1% м.д.с.в. концентрата). Гидролиз проводят в течение 10 мин до массовой доли аминного азота 5%. После гидролиза потен- циометрически определяют рН и устанавливают его равным 6,7, а затем охлаждают ОГМБ до 5°С и направляют на УФ-обработ- ку. В случае периодичности процесса фер- инактивируют пастеризацией при 78°С в течение 1 ч, а затем охлаждают до 5°G. Гидролиз подают в установку которая укомплектована мембранами с пропускной способностью по молекулярной массе, равной 10000 дальтон. Концентрирование осуществляют при давлении 0,05 МПа и температуре 5°С до м.д.с.в. в концентрате 22%. Диафильтрацию осуществляют пастеризованной и охлажденной до 5°С питьевой водой до содержания сухих веществ в уходящем фильтрате 0,2%. ОГМБ (фильтрат) в количестве 20000 кг с м.д.с.в. в 1,5%, в растворе собирают в отдельную емкость, откуда направляют его на повторный ферментативный гидролиз с использованием иммобилизованной протеазы.
Перед гидролизом измеряют рН и устанавливают его равным 0,8, добавлением 0,1 н. раствора КОН или Са(ОН)г. Температуру устанавливают, равной 30°С. Затем проводят гидролиз, прокачивая ОГМБ до массовой доли амминного азота в ОГМБ 15%. Собранный после повторного гидролиза в отдельную емкость ОГМБ в количестве 20000 кг с м.д.с.в. 1,5 направляют на дополнительную УФ-обработку, которую проводит на УФ-установке. укомплектованной УФ-мембранами с пропускной способностью 1000 дальтон. Процесс ведут при 50°С и давлении 0,75 МПа до кратности концентрированна, равной 2. Полученный ОГМБ в
количестве 10000 кг и с массовой долей сухих веществ 1,4% собирают в отдельную емкость, устанавливают рН 6,65 и используют по назначению. Оставшуюся часть ОГМБ (концентрат) в количестве 10000 кн с м.д.с.в. 1,6% снова направляют на повторный ферментативный гидролиз с использованием пептидаз.
ОГМБ, полученный по технологическим 0 параметрам в приведенном примере, характеризуется следующими свойствами:
высокой биологической ценностью
(СКОР; 0,86)
ОГМБ - максимально деминерализован
5 ( 70%),
ОГМБ содержит в своем составе до 98% т пептидов с молекулярной массой до 1000 дальтон, что позволяет с успехом использовать его в качестве белковой основы при
0 производстве продуктов, обладающих гипо- аллергенными свойствами,
ОГМБ в сухом виде представляет собой однородный мелкодисперсный порошок белого цвета, с легкой горечью, полностью
5 растворим, в растворе имеет зеленый оттенок.
Пример 3. Получают ОГМБ с К/С 40/60.
Подсырную сыворотку с м.д. белка 0,6%
0 в количестве 158600 кг очищают от жира и казеиновой пыли, пастеризуют при 72°С с выдержкой 18 с, охлаждают до 45°С, подкисляют до рН 3,8 0,1 н соляной кислотой, подают в УФ-установку. Затем ее концент5 рируют при давлении 0,325 МПа и раскисляют до рН 5,8 с помощью буферной смеси 0,2 н и NaHPO и 0,1 н лимонной кислотой при соотношении компонентов 1:3,87 соответственно. Далее в концентрат сыворотки с
0 м.д.с.в. 8% вносят расчетную массу обезжиренного молока с м.д. белка 3%, которую определяют по формуле (3) 0,66 159600 0,6 о..,-.,- М80/20 3.0 -(0.8 -0.2 0.66) 31537кг5 где 0,66 - значение К для соотношения К/О 40/60..
Осуществляют концентрированно смеси до м.д.с.в. 24,5% с Последующей диафильтрацией промывной водой,
0 подкисленной 0,1 н соляной кислотой до рН 5,8. Промывку УФ-концентрата проводят до содержания с.в. в уходящем фильтрате 0.25%. Получают безлактозный диафильтра- ционный концентрат с м.д.с.в. 20% в коли5 честве 10000 кг с соотношением К/С 40/60, который пастеризуют при 72°С и выдержке 18 с, а затем охлаждают до 45°С. Разбавляют полученный концентрат пастеризованной охлажденной до 45°С питьевой водой в количестве 6575 кг до м.д.с.в. 9%.
вносят лимоннокислый калий в количестве 5
ю
ГС
ф
,4 кг(3% к с.в. концентрата), устанавлива- рН 7,1, добавляя 10%-ный раствор едко- калия или гидроокиси кальция. Вносят
рмент панкреатин медицинский в количестве 5.94 кг (0,6% к м.д.с.в, концентрата). (Чдролиз проводят в течение 1 ч по м.д. аминного азота 10%. После гидролиза уста- HJ вливают рН 7,0. Гидролизат пастеризуют д/ я инактивации фермента при 80°С в тече- Hi e 20 мин, а затем охлаждают до 45°С. Rдролизованный инактивированный, охлажденный концентрат подают в УФ-уста- н вку, которая укомплектована м( мбранами с пропускной способностью по мс пекулярной массе 5000 дальтон. Концентр чрование осуществляют при давлении О,; 25 МПа и температуре 45°С до м.д.с.в. в ко «центрате 24.5%. Диафильтрацию осуще- ст ляют пастеризованной и охлажденной до 45°С питьевой водой до содержания сухи с веществ в уходящем фильтрате 0,25%. ОПМБ в количестве 16666,66 кг .д.с.в. 3% в шастворе собирают в отдельную емкость ил 1 сразу направляют на повторный фер- ме дативный гидролиз. Перед гидролизом ус- анавливают рН 8,05, добавляя 0,1 н КОН лп i Са(ОН)2, а температуру 35°С. Затем проводят гидролиз, прокачивая ОГМБ через ко- ло жу.с иммобилизованным ферментом. Гидролиз ведут до массовой доли аминного азе та в ОГМБ - 22,5%. Собранный после noi (торного гидролиза в отдельную емкость ОГ ИБ в количестве 16666,66 кг с м.д.с.в. 3% наг равляют на дополнительную УФ-обра601
ку, которую, проводят на УФ-установке.
укомплектованной УФ-мембранами с про- пу кной способностью 750 дальтон. Про- це с ведут при 40°С и давлении 1,625 МПа до сратности концентрированна, равной 6. По; ученный ОГМБ в количестве 13888,88 с м.д.с.в. 2,8% собирают в отдельную емкое гь, устанавливают рН 6,75 и используют по назначению. Оставшуюся часть ОГМБ (ко щентрат) в количестве 2777,78 кг с м.дс.в. 3,4% снова направляют на повтор- ныЈ ферментативный гидролиз с использован
лем пиптидаз.
40/
ОГМБ, выработанный в соответствии с технологическими параметрами, приведен- ныь и в данном примере, характеризуются следующими свойствами:
он обладает максимальной биологическом ценностью, т.к. соотношение К/С
О является оптимальным (скор. 1),
ЮГМБ содержит в своем составе до 99% пеп -идов с молекулярной массой до 1000 дальтон. Средняя молекулярная масса пеп- - 750 дэльтон. В связи с этим данный
препарат обладает четко выраженными ги- поаллергенными свойствами,
ОГМБ доминерализован на 30-40%, что позволяет использовать его в качестве бел- 5 ковой основы в специализированных заменителях женского молока для питания детей 1-го года жизни, страдающих пищевой аллергией,
ОГМБ в сухом виде представляет собой 10 однородный мелкодисперсный порошок белого цвета, с едва уловимой горечью, полностью растворим, в растворе имеет желто-зеленый оттенок.
ГГр и м е р 4. Получают ОГМБ сыворо5 точных белков с К/С - 1/99.
Лодсырную сыворотку с м.д. белка 0.6% в количестве 333333 кг очищают от жира и казеиновой пыли, пастеризуют при 74°С и выдержке 19с, подают в УФ-установку. Кон- 0 центрирование осуществляют при давлении 0,7 МПа и температуре 55°С. УФ ведут до м.д.с.в. в концентрате,27% с последующей диафильтрацией промывной водой. Про- мывку УФ-концентрата осуществляют до со5 держания сухих веществ в уходящем фильтрате 0,3%. Получают безлактозный диэфильтрационный концентрат с м.д.с.в. 20% в количестве 10000 кг/
ДФ-концентрат пастеризуют при 74°С с
0 выдержкой 19 с, а затем разбавляют водой (температура 50°С) в количестве 10000 кг. После этого в полученный раствор вносят лимоннокислый калий в количестве 100 кг (5% к с.в. концентрата), устанавливают рН
5 7,5 с добавлением 10 %-ного раствора гидроокиси кальция или едкого натра. Вносят при перемешивании фермент панкреатин медицинский в количестве 20 кг (1% к с.в. концентрата). Гидролиз проводят в течение
0 4 ч до массовой доли аминного азота 15%, измеряют величину рН и устанавливают ее равной 7,2. Инактивируют фермент пастеризацией при 90°С в течение 10 мин, затем охлаждают до 55°С и направляют в УФ-ус5 тановку, которая укомплектована УФ-мембранами с пропускной способностью по молекулярной массе, равной 1000 дальтон. Концентрирование осуществляют при давлении 0,7 МПа и температуре 55°С до
0 м.д.с.в. в концентрате27%. Диафильтрацию осуществляют пастеризованной и охлажденной до 55°С питьевой водой до содержания сухих веществ в уходящем фильтрате 0,9%. ОГМБ в количестве 15385 кг с м.д.е.в.
5 6,5% собирают в отдельную емкость или сразу направляют надповторный ферментативный гидролиз. Перед гидролизом устанавливают рН 8,1, добавляя 0,1 н КОН или Са(ОН)2, а температуру 40°С. Затем прово- гидролиз, прокачивая ОГМБ через коломку с иммобилизованным ферментом. Гидролиз ведут до массовой доли аминного азота в ОГМБ - 30%. Собранный после повторного гидролиза в отдельную емкость ОГМБ в количестве 15385 кг см. д. с. в. 6,5% направляют на дополнительную УФ-обра- ботку, которую проводят на УФ-установке, укомплектованной УФ-мембранами с пропускной способностью 500 дальтон. Процесс ведут при 75°С и давлении 2,5 МПа до кратности концентрирования 10. Полученный ОГМБ в количестве 13847 кг с м.д.с.в. 6.0% собирают в отдельную емкость, устанавливают рН 6,85 и используют по назначению. Оставшуюся часть ОГМБ (концентрат) в количестве 1538,5 кг с м.д.с.в. 7,8% снова направляют на повторный ферментативный гидролиз с использованием пептилаз.
ОГМБ, выработанный в соответствии с технологическими параметрами, приведенными в данном примере, характеризуются следующими свойствами:
максимальной усвояемостью (98%), а также высокими показателями биологической ценности (96,4%) и коэффициента чистой утилизации (94,5%).
ОГМБ содержит в своем составе 99,9% лептидов с молекулярной массой до 1000 дальтон. Средняя молекулярная масса пептидов дальтон.
Препарат обладает выраженными гипо- аллергенными свойствами, а также в жидком виде может быть использован в качестве белкового препарата для пэрэнте- рального питания. В.ОГМБ имеется значительное количествосвободных аминокислот -до 50%,
ОГМБ в сухом виде представляет собой мелкодисперсный порошрк желтоватого цвета, легко растворим в воде. ОГМБ имеет привкус горечи, без запаха, в растворе - жидкость с желтым оттенком.
Пример 5. Приведенные компоненты и параметры процесса примера 2 использованы для получения гидролизата с К/С 80/20. Однако дополнительную ультра- фильтрационную обработку ведут на мембранах с пропускной способностью по молекулярной массе 1500 дальтон. В этом препарате берут от 3 до 10% пептидов с молекулярной массой от 1000 до 15000 даль- тон. Наличие этих пептидов приведет к резкому снижению (на 30%) гипоаллергенных свойств.
Пример 6. Приведенные компоненты и параметры процесса примера 2 использованы для получения гидролизагэ с К/С - 80/20. Однако дополнительную ультра- фипьтряционную обработку ведут при кратности концентрирования, равной 1,5. Эффективность процесса падает в 2 раза за счет небольшого получаемого объема готового продукта (1/3 исходного объема).
Пример 7. Приведенные компоненты и параметры процесса примера 2 использованы для получения гидролизата с К/С - 80/20. Однако дополнительную ультрафиль- трационную обработку ведут при давлении
0 0,5 МПа. Использование данного давления приведет к неоправданному снижению производительности процесса (примерно в 3 раза), т.к. оптимум давлений для УФ-мемб- ран с пропускной способностью 500-1000
5 дальтон находится в диапазоне 0,8-0,5 МПа.
Пример 8. Приведенные компоненты и параметры процесса примера 4 использованы для получения гидролизата с К/С 0 1/99. Однако, дополнительно ультрафильт- рационную обработку ведут на мембранах с пропускной способностью 250 дальтон. В этом случае резко упадет эффективность процесса(на50%)ввидуследующхи причин:
5 повысится селективность по пептидам с молекулярной массой 1000 дальтон до 70%; производительность мембран снизится на 50% .за счет уплотнения мембран.
П р и м е р 9, Приведенные компоненты
0 и параметры процесса примера 4 использо- ванны для получения гидролизата с К/С - 1 /99. Однако дополнительную ультрафильт- рационмую обработку ведут при кратности концентрирования, равной 12. Эффектив5 ность процесса падает за счет увеличения на 10% концентрации ВМС в фильтрате. В связи с этим фильтрат имеет в своем составе концентрацию ВМС, аналогичную исходному препарату.
0 Пример 10. Приведенные компоненты и параметры процесса примера 4 использованы для получения гидролизата с К/С - 1/99. Однако дополнительную ультрафильт- рационную обработку ведут при давлении
5 3,0 МПа. Данное давление приведет к резкому увеличению селективности (до 90 %) по пептидам с молекулярной массой 1000 даль- тон, а также к резкому падению производительности процесса (на 50%) за счет
0 уплотнения мембраны.Гидролизаты примеров 1 (ОГМБ-1- 80/20-прототип) и 2 (ОГМБ-2-80/20-пред- лагаемый способ) были получены в полупроизводственных условиях экспери5 ментального цеха ВНИИДП. Для оценки аллергенных свойств этих гидролизатов использовали критерий тяжести экспериментальной пищевой анафилаксии. Работа выполнялась на беспородных морских СРИН- ках-самцах с исходной массой 250-300 г.
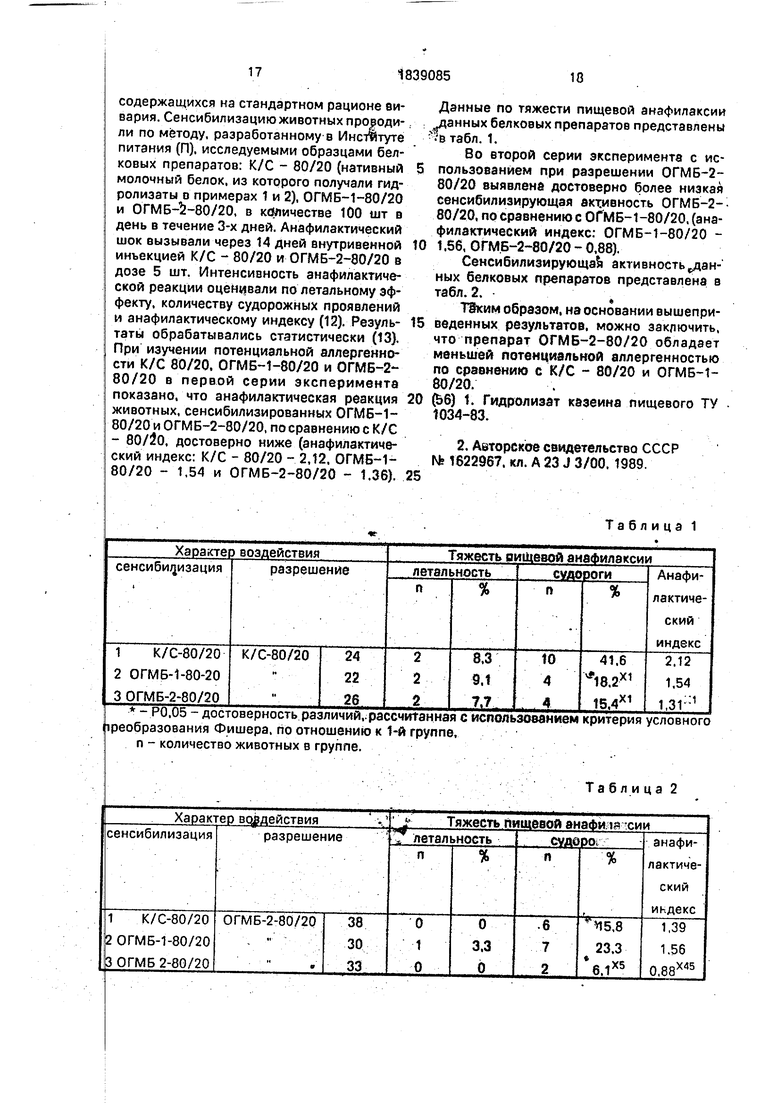
содержащихся на стандартном рационе вивария. Сенсибилизацию животных проводили по методу, разработанному в Институте питания (П). исследуемыми образцами белковых препаратов: К/С - 80/20 (нативный молочный белок, из которого получали гид- ролизаты в примерах 1 и 2), ОГМБ-1-80/20 и ОГМБ-5-80/20, в количестве 100 шт в день в течение 3-х дней, Анафилактический шок вызывали через 14 дней внутривенной инъекцией К/С - 80/20 и ОГМБ-2-80/20 в дозе 5 шт. Интенсивность анафилактической реакции оценивали по летальному эффекту, количеству судорожных проявлений и анафилактическому индексу (12). Результаты обрабатывались статистически (13), При изучении потенциальной аллергенно- сти К/С 80/20. ОГМБ-1-80/20 и ОГМБ-2- 80/20 в первой серии эксперименте показано, что анафилактическая реакция животных, сенсибилизированных ОГМБ-1- 80/20 и ОГМБ-2-80/20, по сравнению с К/С - 80/2о, достоверно ниже (анафилактический индекс: К/С - 80/20 - 2,12. ОГМБ-1- 80/20 - 1,54 и ОГМБ-2-80/20 - 1.36).
Данные по тяжести пищевой анафилаксии данных белковых препаратов представлены втабл. 1.
Во второй серии эксперимента с ис- пользованием при разрешении ОГМБ-2- 80/20 выявлена достоверно более низкая сенсибилизирующая активность ОГМБ-2-- 80/20, по сравнению с ОГМБ-1-80/20. (анафилактический индекс: ОГМБ-1-80/20 - 1.56, ОГМ.Б-2-80/20 - 0,88).
Сенсибилизирующая активность данных белковых препаратов представлена в табл.2.t
ТЗким образом, на основании еышепри- веденных результатов, можно заключить, что препарат ОГМБ-2-80/20 обладает меньшей потенциальной аллергенностью по сравнению с К/С - 80/20 и ОГМБ-1- 80/20.
(Ь6) 1. Гидролизат казеина пищевого ТУ 1034-83.
2. Авторское свидетельство СССР № 1622967. кл. А 23 J 3/00. 1989.
25






| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОЛИЗАТА СЫВОРОТОЧНЫХ БЕЛКОВ С ВЫСОКОЙ СТЕПЕНЬЮ ГИДРОЛИЗА И ГИДРОЛИЗАТ СЫВОРОТОЧНЫХ БЕЛКОВ С ВЫСОКОЙ СТЕПЕНЬЮ ГИДРОЛИЗА | 2010 |
|
RU2428047C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО ГИДРОЛИЗАТА СЫВОРОТОЧНЫХ БЕЛКОВ СО СРЕДНЕЙ СТЕПЕНЬЮ ГИДРОЛИЗА | 2008 |
|
RU2375910C1 |
| СПОСОБ ПРОИЗВОДСТВА ГИДРОЛИЗАТА СЫВОРОТОЧНЫХ БЕЛКОВ | 2015 |
|
RU2663583C2 |
| СПОСОБ ПРОИЗВОДСТВА ГИДРОЛИЗАТА СЫВОРОТОЧНЫХ БЕЛКОВ С ВЫСОКОЙ СТЕПЕНЬЮ ГИДРОЛИЗА И НИЗКОЙ ОСТАТОЧНОЙ АНТИГЕННОСТЬЮ | 2012 |
|
RU2529707C2 |
| Способ получения молокосодержащего напитка с гидролизатом сывороточных белков | 2021 |
|
RU2792437C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО СЫВОРОТОЧНЫХ БЕЛКОВ | 2013 |
|
RU2528068C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОГИДРОЛИЗОВАННОЙ ПЕПТИДНОЙ КОМПОЗИЦИИ ИЗ БЕЛКОВ МОЛОЧНОЙ СЫВОРОТКИ | 2013 |
|
RU2531164C1 |
| ПОЛУЧЕНИЕ РАСТВОРИМЫХ В КИСЛОЙ СРЕДЕ ГИДРОЛИЗАТОВ БОБОВОГО БЕЛКА С НИЗКОЙ ТЕРПКОСТЬЮ ИЛИ БЕЗ ТЕРПКОСТИ И ГИДРОЛИЗАТОВ БОБОВОГО БЕЛКА С УЛУЧШЕННЫМ АМИНОКИСЛОТНЫМ СКОРОМ | 2018 |
|
RU2781778C2 |
| СПОСОБ ПРОИЗВОДСТВА БЕЗЛАКТОЗНОГО МОЛОКА | 2017 |
|
RU2766351C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЙОГУРТА СО СНИЖЕННОЙ АЛЛЕРГЕННОСТЬЮ СЫВОРОТОЧНЫХ БЕЛКОВ | 2015 |
|
RU2595393C1 |

- Р0.05 - достоверность различий, рассчитанная с использованием критерия условного |реобразования Фишера, по отношению к 1-й группе, п - количество животных в группе.
Таблица 1
Таблица 2
Формула изобретения
СПОСОБ ПОЛУЧЕНИЯ ГИДРОЛИЗАТА МОЛОЧНЫХ БЕЛКОВ с проведением процессов пастеризации белкового раствора, ультрафильтрации, диафильтрации, ферментативного гидролиза панкреатином, инактивации фермента, ультрафильтрации полученного гидролизата, диафильтрации его, отличающийся тем, что, с целью снижения гипоаллергенных свойств гидролизата и повышения производительности процесса, ультрафильтрацию и диафильт5 рацию полученного гидролизата осуществляют на мембранах с пропускной способностью по мол.м. 500 - 1000 Дальтон при кратности концентрирования 2 - 10 и давлении 0,75 - 2,5 МПа, а после диаЮ фильтрации полученный гидролизат подвергают ферментативному гидролизу.
Авторы
Даты
1993-12-30—Публикация
1990-07-06—Подача