До сих пор получение алюминия происходит электролизом алюминия в расплавленном криолите. Электролиз в водной среде не может быть осуществлен, так как алюминий при своем сродстве к кислороду не может быть выделен из водного раствора; вместо алюминия на катоде будет выделяться окись алюминия Al2O3, так как алюминий в момент выделения отнимает из воды кислород и садится на катоде в виде окиси алюминия. По предлагаемому способу электролиз производят в водном растворе одной из алюминиевых солей, причем катод защищен от проникновения растворителя (воды) диафрагмой, пропускающей ток, но не пропускающей воду. В качестве диафрагмы применяются нерастворимые в воде и не смешивающиеся с ней органические вещества большего удельного веса, чем вода. Жидкость эта покрывает катод слоем от 1 до 3 см. В качестве диафрагменных жидкостей применяется йодистый метил CH3I, имеющий удельный вес 2,3346, или хлороформ CHCl3, обладающий удельным весом 1,5. Обе эти жидкости с водой не смешиваются и хорошо проводят ток. Напряжение на электродах 4V; так как ампер-час выделяет 0,337 г Al, то kW выделит из раствора:
0,337×250=84,150 г Al.
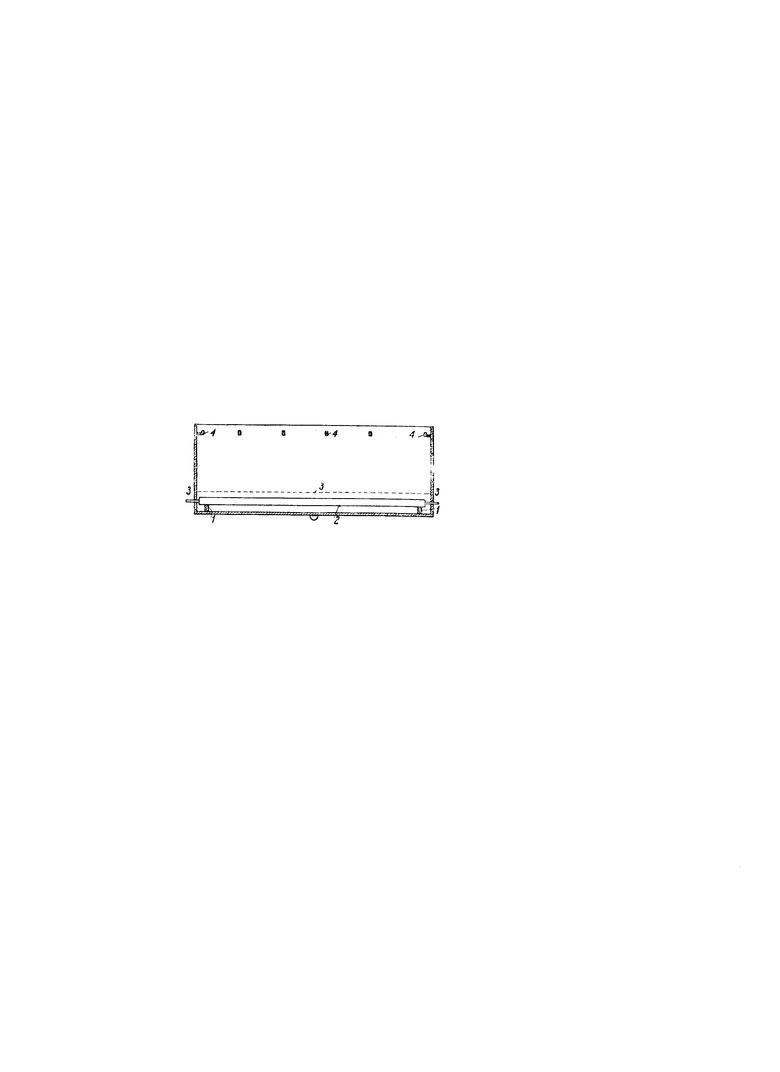
Изображенная на чертеже в схематическом виде, предназначенная для проведения предлагаемого способа электролитического получения алюминия, ванна состоит из железного прямоугольного бака, на дне которого на изоляторах 1,1 помещен катод 2. Ванна до уровня 3 наполнена иодистым метилом или хлороформом; выше ванна наполнена электролитом, состоящим из насыщенного раствора сернокислого алюминия Al2(SO4)3: на крючках 4 подвешивается сетчатый анод. При электролизе осаждается на катоде металлический алюминий, где он защищен от воды слоем органического соединения и потому не разлагается; образующийся анион SO4, на катоде с водой дает серную кислоту
2Al2(SO4)3+6H2O→4Al+6H4SO4+3O2.
Применение жидких диафрагм позволяет вести электролиз с более дешевым сырьем, чем Al2O3 и уменьшает расход энергии.
По наблюдениям изобретателя, когда в качестве электролита брался раствор сернокислого алюминия, а катодной диафрагмой служил слой анилина, последний частично растворялся в электролите, а избыток анилина образовал слой, не смешивающийся с водой. В слое анилина помещается катод. Во время электролиза на катоде выделяется водород и алюминий (при опытах алюминий полностью покрыл ровным слоем катодную пластину).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения алюминия из глин, боксита и т.п. | 1928 |
|
SU28482A1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ СЕРНОКИСЛОГО ОКИСНОГО | 1973 |
|
SU381610A1 |
| СПОСОБ ЭЛЕКТРОЛИТИЧЕСКОГО ПОЛУЧЕНИЯ МЕТАЛЛОВ | 1933 |
|
SU39979A1 |
| СПОСОБ УДАЛЕНИЯ СОЛЕЙ ИЗ ВОДЫ | 1926 |
|
SU5935A1 |
| Способ электроэкстракции меди из сульфатных электролитов | 2018 |
|
RU2690329C1 |
| Способ получения галлия из щелочно-алюминатных растворов глиноземного производства | 2016 |
|
RU2636337C2 |
| СПОСОБ ЗАЩИТЫ КАТОДНОГО УСТРОЙСТВА АЛЮМИНИЕВОГО ЭЛЕКТРОЛИЗЕРА | 2009 |
|
RU2401886C1 |
| Способ получения , -диалкил -с1 -с3-тетрагидро-4,4-бипиридила | 1978 |
|
SU843741A3 |
| СОСТАВ ЭЛЕКТРОЛИТА АНТИФРИКЦИОННОГО ЭЛЕКТРОЛИТИЧЕСКОГО СПЛАВА "ЦИНК-ЖЕЛЕЗО" ДЛЯ ОСАЖДЕНИЯ В УСЛОВИЯХ ГИДРОМЕХАНИЧЕСКОГО АКТИВИРОВАНИЯ | 2015 |
|
RU2633866C2 |
| Способ получения -метил -2пирролидона | 1976 |
|
SU619484A1 |
Способ электролитического получения алюминия из водных растворов его солей, отличающийся тем, что, с целью воспрепятствования обратному, растворению осаждаемого алюминия, горизонтально на дне ванны расположенный катод диафрагмируют не смешивающимся с водой слоем электропроводной органической жидкости, напр. анилина, хлороформа и т.п.
Авторы
Даты
1934-08-31—Публикация
1932-06-16—Подача