(54) СПОСОБ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИК ЭЛЕКТРОПЕРЕНОСА РАСТВОРОВ ЭЛЕКТРОЛИТОВ Изобретение относится к области электрохимии, занимающейся изучением явлений переноса в растворах электролитов, и предназначено для определения подвижности ионов и электроперено са нейтрального растворителя при пропускании через раствор постоянного электрического тока. Известно применение изотопов для измерения электропереноса нейтрального растворителя 1. Устройство для измерения содержит электролитическую ячейку, разделенную на 4 части диафрагмами из пергамента две соседние камеры, одна из которых является приэлектродной, заполнены раствором, в котором растйорителём является вода, обогащенная . После пропускания тока производят анализ изотопного состава воды во всех 4 час тях прибора. Принципиальным недостатком указанного способа определения электропереноса растворителя является несбходимость применения мембран, - Наблюдавмый эффект определяется наличием мембран, поэтому полученные в этих опыта чрезвычайно высокие значения кннетических чисел гидратгщии ионов весьма сомнительны. Применение изотопов при опр.еделении чисел переноса ионов в растворах электролитов ограничивается, в основном, целями регистрации ионных границ. Для этого в ряде экспериментальных офор-шений метода движущейся границы в исследуекале растворы (или в один из них) вводятся небольшие количества Р)- или т-активных добавок. В модификации метода движущейся границы, известнсмл под названием метода идентичных растворов, ведущий и следящий растворы имеют одинаковый химический состав, небольшая часть ионного компонента одного из растворов радиоактивна (2 . Наиболее близким техническим решением является определение чисел переноса (а, следовательно, и подвижности) ионов по способу подвижной границы 13. В измерительной трубке с известнь вну ренним сечением создают два слоя различных растворов, имеющих общий катион или анион, так, чтобы граница между ними была отчет.пивой. При прохождении тока граница перемещается относительно измерительной трубки со скоростью, равной скорости движения ионов. Для учета перемещения растворителя относительноизмерительной трубки в процессе прохождения тока ибполь эуется прибор с одним закрмтым электтродным пространством (анодным или катодным), в котором возможен учет объемных изменений раствора, вызванных электродными процессами, Упомянутый прибор с закрытым электродным объемом позволяет также исключить общее движение раствора, вызванное электроосмосом, при малых концентрациях электролита. Числа переноса относительно растворителя получают из скорости перемещения границы по соотношению, учитывающему влияние на перемещение границы объемных изменений раствора у электрода, которые зайисят от свойств изучаемых растворов, электродных процессов и условий измерения Недостатком упомянутых выше способ определения чисел переноса ионов является необходимость учитывать переме щение растворителя за счет гидратаци- онного переноса и изменения объема раствора в закрытом приэлектродном пространстве. Для расчета перемещения растворителя необходимо знать распределение концентрации раствора в приэлектродном пространстве, зависимость плотности раствора, образующегося в приэлектродном пространстве, от концентрации. Величина поправки увеличивается с увеличением концентрации раствора, к тому же она в принципе зависит от конструкции ячейки, так как упомянутое изменение объема зависит от перемешивания, а оно в условиях выделения джоулева тепла определяется термостатировани ем прибора и осу ществляется посредством конвекции и диффузии. Принципиальным ограничением измерения чисел переноса методом движущейся границы является необходимость подбора индикаторного электролита, имеющего один ион, с исследуемым, и число переноса необщего иона меньшее, чем у исследуемого. Описываемый способ может применят ся только дня тех растворов электролитов, для которых возможно подобрат обратимые электроды, в случае применения необратимых электродов для вве дения поправок необходимо иметь точные сведения обо всех электродных реакциях и физическом состоянии продуктов электролиза. Способ движущейс границы в рассматриваемом оформлении не позволяет измерять величину элект ропереноса растворителя. Цель изобретения - повышение точности измерений в области высоких ко центраций растворов, расширение диап зона изучаемых веществ, измерение ве личины электропёреноса нейтрального растворителя и значений подвижности ионов в растворах электролитов (без ограничения их концентрации) относительно растворителя. Указанная цель достигается тем, что в известном способе определения характеристик длектрюпереноса раст воров электролитов путем приведения в электролитической ячейке в контакт двух растворов, создания границы раздела компонентов растворов и измерения перемещения границ раздела компонентов в постоянном электрическом поле, исходные растворы, приводимые в контакт, берут одинаковы по химическому составу, но различными по изотопному составу элементов изучаемых ионов и растворителя, либо берут исходные растворы, различные по химическому составу, имеющие общий катион или анион и концентрации, соответствующие регулирующему соотношению Кольрауша, и различающиеся по изотопному составу растворителя, пропускают электрический ток, проводят анализ изотопного состава компонентов и растворителя по длине измерительной ячейки, строят по зависимостям f(x), - относительная концентрация изотопов в изучаег их компонентах раствора; X - расстояние по длине измерительной ячейки; i - номер компонента раствора, и по полученным зависимостям определяют искомые величины. Различие изотопного состава растворителя и катионов и анионов в приводимых в контакт растворах позволяет проводить прямое измерение перемещения в электрическом поле растворителя и измерение перемещения катионов и анионов относительно растворителя в целом. Измерение тгеремеиения ионов относительно растворителя в целом не требует поправок на перемещение раствора, вызванное разного рода причинами (например, электродными процессами, электроосмотическим течением раствора и т. р., что приводит к повышению точности измерений, особенно в области высоких концентраций растворов электролитов, и позволяет производить измерения в растворах, для которых трудно подобрать электроды с известными данными обо всех электродных реакциях и физическом состоянии продуктов электролиза. Таким образом, предлагается два несколько отличных варианта способа определения. 1. Допустим, необходимо измерить подвижность катионов М, анионов А и перенос растворителя в растворе определенной концентрации С . .Дополнительно к исследуемому раствору готовят растворы того же химического вещества КцА, той же химической концейтрации С-, , но с другой изотопной концентрацией элементов катионов, анионов и растворителя. Указанные два раствора приводят в контакт в определенном месте измерительной электролитической ячейки, принимая меры к тому, чтобы растворы в минимальной степени перемешивались при проведении этой процедуры. Затем через растворы определенное время пропускают постоянный электрический ток известной величины. В процессе пропускания тока фронты изотопной концентрации катионов, анионов и растворителя, первоначально совпадающие в месте контакта растворов, разделяются по длине измерительной трубки, так как подвижности всех этих компонентов различные. После выключения тока из измерительной трубки последо вательно отбирают пробы раствора (удобнее одинаковые). В каждой пробе определяют изотопный состав в.сех исследуемых компонентов раствора и растворителя. Полученные данные наносят на график и получают распределение изотопной концентрации исследуемых компонентов по длине измерительной трубки. В области контакта растворов молекулярная диффузия и конвективные процессы изменяют крутизну фрон.тов ИЗОТОПНОЙ концентрации компонентов, однако центры распределения концентраций эти процессы не смешают. Перемещение центров фронтов распределения изотопных концентраций изучаемых компонентов характеризует скорость их перемещения в постоянном электрическом поле. Смещение фронта растворителя относительно его первоначального положения (при отсутствии конвективного перемещения, т. е. течение всего раствора относительно из мерительной трубки) характеризует величину электропереноса растворителя относительно измерительной трубки а смещение изотопных фронтов катионов и анионов от носительно найденного после пропускания тока центра рас пределения изотопной концентрации ра створителя характеризует величину их подвижности относительно растворител в целом. Очевидно, что на величине смещения ионов относительно раствори теля не сказывается общее течение ра створа. 2. К исследуемому раствору го товят дополнительный раствор иного химического вещества M2. имеющего иной катион и общий с первым анион (если исследуется подвижность катиола М ) . Число переноса катиона Mj в tiacTBOpe MjA должно быть меньше, чем число переноса катиона М в растворе . Концентрация этого вспомогательного раствора должна удовлетворять регулирующему соотношению Кольр уша и должна быть определена в предварительных опытах. Растворитель для одного из растворов имеет отличный изотопный состав, по крайней мере, по одному из входящих в него элемен тов по сравнению с изотопным составом растворителя другого раствора. казанные два раствора приводят в контакт так, что между ними сразу обазуется стабильная катионнйя граниа при пропус ка,нии тока нужного направления (чтобы М находился впереди по направлению движения границы). бычно вспомогательный растрор электролита выбирают так, чтобы он отличался от исследуемого по цвету, тогда скорость перемещения границы наблюдают в микроскоп визуально. Положение бесцветных ионных границ наблюдают по рефракционной картине в плоском пучке видимого света или с помощью термопары, фиксирующей изменение температуры растворов в районе границы. После пропускания определенного количества электричества, когда скорость движения границы в лабораторной системе к766рдинЖТ 6г 1ределёнау выключают ток и из измерительной трубки отбирают пробы растворов. В каждой пробе определяют изотопный состав растворИтёлк. Смещение центра распределения изотопной концентрации раство рителя Относительно первоначального положения ионной границы характеризует величину электропереноса растворителя в том растворе, в котором изотопный фронт находится, а смещение ионной границы относительно фронта изотопной концентрации растворителя - подвижность ионов относительно растворителя в целом. Задаваемое первоначально различие ИЗОТОПНОЙ концентрации ионов, подвижность которых исследуется, и растворителя в исследуемых растворах зависит от точности анализа изотопной .концентрации и выбирается таким, чтобы с необходимой для определения подвижностей. компонентов точностью регистрировать положения центров распределения фронтов изотопных концентраций. Некоторая, хотя и слабая, зависимость подвижностей ионов и растворителя от изотопного состава позволяет изменять изотопный состав компонентов в приводимых в контакт растворах на небольшую величину, чтобы иметь основание относить измеренные значения подвижности к раствору определенного изотопного состава. Точность предлагаемого методаограничена тем, что ионы изотопов обладают несколько отличающейся подвижностью. Изотопный эффект подвижностей искажает фронт распределения изотопной концентрации . Величина разницы подвижностей изотопов для известных ионов (кроме и ) непревосходит нескольких десятых долей процента и, соответственно,, такая величина является принципиальным пределом относительной точности измерения
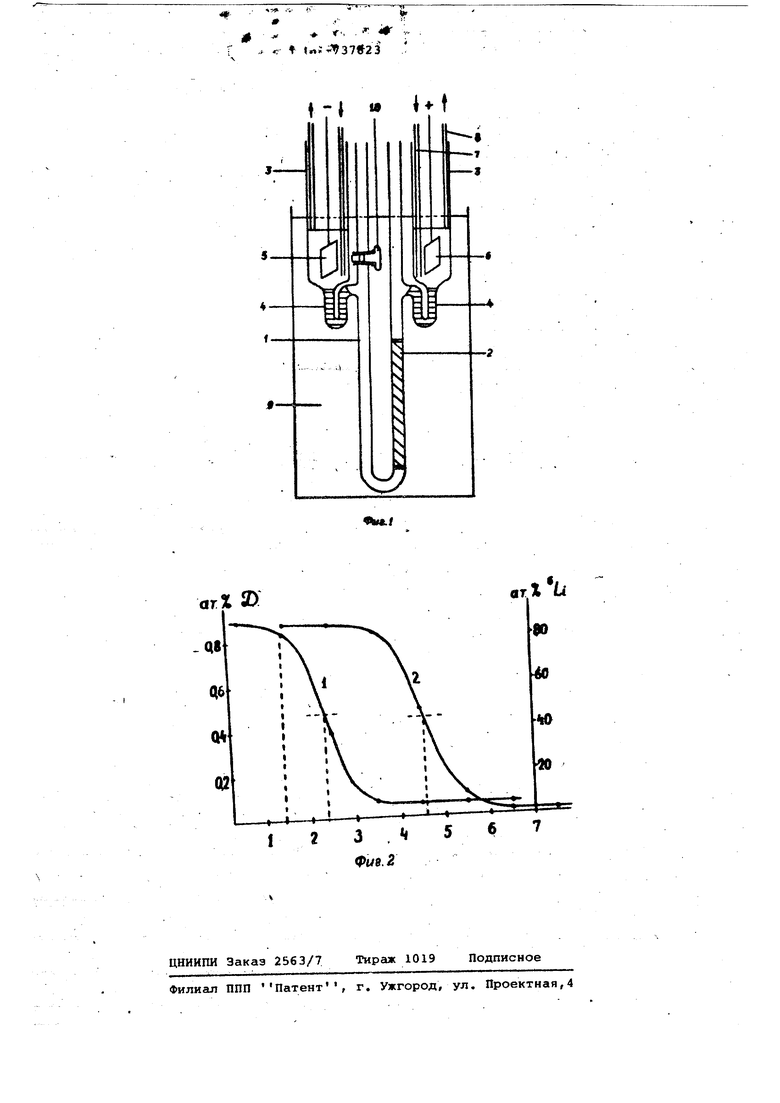
7 подвижностей ионов и растворителя предлагаемым методом. Предлагаемый спосоЬ применяют для определения величина электроПёреноса воды в растворе LlCC и измерения подвйжнвсти лития относительно растворителя в целом и относительно растBOpia. . . . На фиг. 1 изображен прибор для определения характеристик электропереHbda растворов электролитов; на фиг. 2 - график распределения концен рацйй изотопов Лития и вЬДброда по длине измерительной трубки. У-образная измерительная трубка сострит из двух прям6линёйных участков 1 и 2, имеющих одинаковую и постоянную по длине площадь внутреннего поперечного сечения, внутренний ди аметр трубок 6,5 мм. Трубка 2 заполнена в ч нижней части лварцевам ПесКом с размером зерен 20-40 мкм, высота засыпки 8 см. Песок насыпан на закреп ленный диск из стеклянного фильтра № 1, тщательно отмыт, утрамбован и накрыт сверху таким же фильтром. Во опыта по электропереносу в песке находилось место контакта растворов . Песок уменьшает конвективное перемешивание растворов. Кроме того, при заливке ячейки растворами и отборе пробПОСНепропускания тока верхняя граница фильтра является опорной точкой для отсчета координаты места Контакта растворов и распределения концентрации изотопов по длине измерительной трубки. Измерительная трубка соединена с электродными сосудами 3 трубками 4, которые заполнены 3%-ны раствором агар-агара в исследуемом ра створе. Агаровые пробки в застывшем состоянии обладают малой пронида йостыо и позволяет в процессе опыта создать в измерительной трубке требуемое механическое равновесие. Электро дами 5, б служат обратимые хлорсеребряные электроды: серебряный анод и хлорсеребряный катод. Раствор электро лита в электродных сосудах непрерывно обновляется. Свежий раствор с концентрацией, равной концентрации иссле дуемого раствора, noctynaei- по трубке 7, трубка 8 отсасывает раствор. Прибор помещают в водяной термостат 9 с прозрачными стенками, в котором под держивается температура с точностью ± 0,002°С. Стабилизированный выпрямйтель служит источником постоянного электрического тока. Приготавливают исследуемый 4,3 и раствор Lice (первый раствор) с концентрацией изотопа Ы, равной 6,0 ат. Рас вори тбяем для этого раствора )ад1Ш ГТ1зЪ1чШ1йЩ8 вом. Второй раствор - также 4,3 н раствор псе, но с изотопным составом лития 88,0 ат.%, растворителе1М для не го служит вода с,содержаннем дейтерия
8 0,87 ат.%. В обоих растворах хлор не имеет изотопной метки. Заполнение электролитической ячейки первым и вторим растворами с точной фиксацией относительно трубки положения места контакта растворов проводят следующим образом. В измерительную трубку з пивгиот первый раствор выше крана Ю. Кран 10 перекрываиот, из трубки 2 отбирают раствор до уровня верхнего фильтра. В трубку 2 на первый раствор, находящийся в песке, в два приема зг ивают второй раствор. При первой заливке длина столба раствора (над песком) составляет .примерно 2 см. В трубке 1 над краном 10 создают разрежение (около 10 см вод.ст.), кран 10 открывают, после чего второй раствор затекает в песок, вытесняя первый раствор, в микроскоп Мир с увеличением около 10, закрепленный на вертикальной измерительной линейке, наблюдают за изменением уровня раствора и по этим ;аанным определяют длину столба раствора, зашедшего в кварцевый песок, измеренного для трубки, свободной от песка. (При отборе Проб длина столба Пробы также определяется для свободной от песка трубки. Такое определение исключает необходимость измерения пористости песка для обработки данных опыта. Важно только, чтобы концентрационные профили в процессе опыта по электропереносу оставались в песке). Введя место контакта растворов на некоторую определенную глубину в песок, уровни растворов в обоих коленах измерительной трубки поднимают, долива.я соответствующие растворы, до уровней растворов в электродных сосудах. Проведя заливку растворов , через электролитическую ячейку пропускают постоянный ток силой 40 мА в течение 5 ч, 10 мин. В процессе пропускания тока ведут наблюдение за уровнями растворов в трубках 1 и 2, смещение уровней не прейыаает 0,2- 0,3 мм. После выключения,тока из трубки 2 при закрытом кране 10 раствор до уровня верхней поверхности фильтра, над песком. Из песка вытесняют раствор (открывая и закрывая кран 10) и производят отбор проЛ. Дпк на столба отдельной пробы (для трубки 2 в области над песком) составляет 5,75 мм. Последовательно отбирают около 1U проб. Из каждой пробы в вакууме отгоняют воду и ее изотопный состав определяют по плотности воды по плавковым методом. Изотопный состав лития в пробах определяют на масспектрометре МИ-1101. На фиг. 2 представлены результаты .исследований. По горизонтальной оси Отложен номер пробы, по вертикальной - изотопный состав лития и воды « пробе. На графике вертикгшьной штрих-пунктирной линией показано положение центров распределения изотопных концентраций лития и водорода до включения тока (место контакта первого и второго раств.оров) . После пропускания тока центры распределения концентрации изотопов лития и водорода разделяются. Кривые показывают конечное распределение концентрации водорода (1) и лития (2) по длине измерительной трубки. Из графика получают для смещения воды величину, равную 5,22 мм, для смешения ионов лития - величину 17,87 мм, соответственно, смещение ионов лития относительно воды равно 12,65 мм. Величина 5,22 мм и 17,87 мм представляют собой электроперенос воды и лития относительно раствора. Напряженность электрического поля При токе 40 мА и электропроводности 4,3 н раствора Lice при 20,00°С,равной Эе 0,166 , в трубке диаметром 6,5 мм имеет величину Е -0,726 В/ Тогда подвижность ионов лития относительно раствора иводы (растворителя в целом) равна соответственно 1,32 х X см/В и 0,94 см/ Зти значения согласуются с данными по подвижности ионов лития, приводимыми в справочной литературе. Предлагаемый способ позволяет непосредственно экспериментально измерять величину электропереноса нейтра льного растворителя и значения подвижностей ионов относительно растворителя в целом, т. е, в строго фиксированной системе координат. Указанные величины входят в ряд фундаментальных величин, знание которых необходимо для построения теории кинетических свойств растворов электро литов. Предлагаемый метод одинаково хорошо может применяться для растворо низких и высоких концентраций, позво ляет исключить влияние приэлектродны процессов, не требует введения трудно определимых поправок, как болы11инств известных методов. Электроперенос не трального растворителя в описанной выше простой постановке опытов неотделим от его перемещения вместе со всем раствором при возникновении эле трбосмотического движения в растворах малых концентраций, (Подобное осложнение имеет место и во всех иных при меняемых в практике способах), Однак предлагаемый способ позволяет опреде лять числа переноса относительно растворителя и при наличии электроосмо тического движения раствора. Действительно, электроосмотическое движение раствора дает одинаковыми вклад как в перенос растворителя, так и в перемещение ионов. Предлагаемый способ позволяет опеделить аномальную чарть подвижноси при электромиграции протона и гидоксила в растворах. Измерения чисел переноса и подвижое тей ионов -в строго фиксированной истеме координат-растворитель в цеом имеют практическое значение, в астности для выбора условий разделеия неорганических и органических онов по подвйжностям методом изотаофрреза, - ..---,. ... ,... Формула изобретения Способ определения характеристик электропереноса растворов электролитов путем приведения в контакт двух растворов, создания границы раздела компонентов растворов в электролитической ячейке и измерения перемещения границ компонентов в постоянном электрическом поле, отличающийс я тем, что, с целью повышения точности определения в области высоких концентраций растворов, расширения диапазона изучаемых веществ и определения величины электропереноса нейтрального растворителя и значений подвижности ионов относительно раствбрителя, исходные раств.оры берут отличными по изотопному составу изучаемых компонентов й изотопному составу растворителя, но одинаковыми.по химическому составу, и химической концентрации, или отличными по химическому составу и по изотопному Составу растворителя, но имеющими общий катион или анион и химически..; .концентрации, соответствующие регулирующему соотношению Кольрауша, пропускают электрическийток,проводят анализ изотопного состава исследуемых компонентов и растворителя по длине измерительной ячейки, и по зависимостям C.J f(x), где X - расстояние по длине измерительной ячейки; С - относительная концентрация изотопов в изучаемых компонентах раствора; 1 - номер компонента раствора, опредеттяшт -искомые величины. Источники информации, принятые во внимание при экспер;тизе 1,Rutgers, А. 3- Hendrikx Y, Trans Faraday Society, 58, 1962, с. 2184, 2,Методы измерения в электроэлемент. Под ред, Э, Егери А. Залкинд. М,, мир, 19V7i 3,MiCios Р, Newman Y, Y, Phys. Chem, 75, 1969, c, 298
5 ,V If 4, -.,. .
, t 





f-l
ut
Авторы
Даты
1980-05-30—Публикация
1977-12-12—Подача