(54) ПРОИЗВОДНЫЕ АЛЛИЛАМИДОВ КИСЛОТ ФОСФОРА, ОБЛАДАЮЩИЕ ХЕМОСТЕРИЛИЗУЮЩЕЙ АКТИВНОСТЬЮ




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ разведения трихограммы | 1980 |
|
SU865243A1 |
| СПОСОБ ПОЛОВОЙ СТЕРИЛИЗАЦИИ НАСЕКОМЫХ, В ЧАСТНОСТИ, ЯБЛОННОЙ ПЛОДОЖОРКИ | 1971 |
|
SU294593A1 |
| СПОСОБ ПОЛУЧЕНИЯ, СОДЕРЖАНИЯ И ХРАНЕНИЯ ЖИВОГО КОРМА ДЛЯ БИОЛОГИЧЕСКИХ ОБЪЕКТОВ ПТИЦ И РЫБ | 1999 |
|
RU2154940C1 |
| ПРЕПАРАТ ДЛЯ ПОЛОВОЙ СТЕРИЛИЗАЦИИ ВРЕДИТЕЛЕЙ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР | 1965 |
|
SU169940A1 |
| Добавка в питательную среду для разведения насекомых | 1989 |
|
SU1629009A1 |
| Аллиламиды диалкилфосфорных кислот, обладающие свойствами хемостерилянтов вредных насекомых | 1978 |
|
SU701627A1 |
| БАКТЕРИАЛЬНЫЙ ИНСЕКТИЦИД ДЛЯ БОРЬБЫ С ЧЕШУЕКРЫЛЫМИ | 1993 |
|
RU2080065C1 |
| Способ выращивания полезных насекомых | 1987 |
|
SU1505487A1 |
| СПОСОБЫ ПРОФИЛАКТИКИ БОЛЕЗНЕЙ РАСТЕНИЙ И ПОВРЕЖДЕНИЙ РАСТЕНИЙ НАСЕКОМЫМИ (ВАРИАНТЫ) | 2007 |
|
RU2409030C1 |
| СПОСОБ ЗАЩИТЫ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР ОТ ВРЕДНЫХ НАСЕКОМЫХ | 2010 |
|
RU2424658C1 |

Изобретение относится к химии фосфорорганических соединений, а именно к новым производным аллилами дов кислот фосфора общей формулы Р-МНСН„СН-СН„ (1) где R - метокси-, бутоксигруппа, гексил или гептил; R - гексил, аллиламино-или эти ленаминогруппа. обладающим хемостерилизующей активностью, которые могут найти применение в сельском хозяйстве для половой химической стерилизации вреди телей сельскохозяйственных культур Известны органические соединения фосфора, проявляющие хемостерилирую щую активность, например производные этиленамидофосфата (препараты тэфа, метэфа, тиотэфа, метиотэфа), причем некоторые из этих соединений являются очень эффективными хемосте рилизаторами насекомых, например тиотэфа 1 и 2. Однако он нестоек при хранении, быстро теряет стерилизующую активность в водных растворах и обладает довольно высокой токсичностью для теплокровных и насекомых. Цель изобретения - расширение арсенала средств воздействия на живой организм. Поставленная цель достигается описываемыми производныг.чи аллиламидов кислот фосфора формулы (I), обладающими хемостерилизующей активностью. Способ получения соединений формулы (I) основан на взаимодействии фосфор со дер.жащих моно- или дих-поридов с аллиламином в органическом растворителе в присутствии акцептора хлористого водорода. В качестве фосфорсодержащих моно- или .цихлоридов применяют хлоранги.приды фосфиновых кислот, дихлорангидриды фосфоновых или фосфорных кислот. Акцептором хлористого водорода служит триэтиламин. Реакцию ведут при охлал;дении от -20 до +5°С в диэтиловом эфире или бензоле. Пример 1. Получение диаллила№1да гексилфосфоновой кислоты (Кох 05.03),К раствору 6 МП (0,08 моль) сухого аллиламина, 11,2 .ш (0,08 моль) сухого триэтиламина в 50 мл абсолют кого бензола при в течение 20 минут при интенсивного перемешива нии добавляют раствор г (0,04 моль) дихлорангидрида гексилфосфоновой кислоты в 25 MJI абсолютиого бензола. Выделяется бесдветный осадок хлоргидрата тризтилаг- ина. Массу перемешивают 2 ч ripis когднатной температуре. На следующ| й день выпавший осадок отфнльтрозываштр пр вают на фильтре абсолютны. бензолом Бензол отгоняют на роторном испари;геле, остаток выдерживают в вакууме масляного насоса. Масло кристаллизуется. Т.пл. . Выход 8,8 г (90%), R на оксиде в ацетоне 0,бб/в системе беЕ- зол-яиоксан (1:3) 0,32. Найдено,%: С Н 10,24Г Р 12,34. . Е ычислено, %: С 59,01; Н 10,25; Р 12,70. В ИК-спектрах полоса валентньзх колебаний связи находится в области 1160 СН СН2-Группы в области 1642 см, ЯЫ-связи - 3160 Пример 2, Получение аллил амида дигептилфосфиновой кислоты {Кох 05.05) . К раствору 3 мл (0,04 моль) сухо го аллиламина, 5/6 мл (0,04. моль) сухого триэтиламина в 50 w; абсолю ного бензола при охлаждении до в течение 15 мин добавляют Р а ст вор 11,2 г (О f О 4 моль) x.riop ан ги рида дигептил(|)осфиновой кислоты в 25 мл абсолютного бензола. Массу п ременив ают 3 ч при комнатной темпе .ратуре. Хлоргидрат триэтиламина отфильтровывают, про лывают на филь абсолютным бензолом. Бензол упари.вают на роторном испарителе, остат вакуумируют с масляным насосом.,Мас бледно-желтого цвета при охлаждени в холодильнике закристгшлизовывает .Т.пл, . Выход 11,5 г (95,5% Rp на оксиде алюминия в ацетоне 0,67, в системе бензол-диоксан (1: 0,57, Найдено,%: С 66,91; Н 12,40; Р 10,12. С Н,,ЫОР, Вычислено,%: С 67,77; Н 11,96; Р 10,29. В ИК-спектрах полоса валентных колебаний группы находится в области 1160 см , Cll-CHy-ipyimroi - облао;ги 1645 см, ЯН - группы - в области 3170 см. Пример 3. Получение этиле a Ф дoaллилaмидa метил фосфорной кис лоты (Кох 05.01). К раствору 7,45 г (0,05 моль) дихлорангидрида метилфосфорной кис ты в 50 мл абсолютного эфира при охлаждении до добавляют в т-е чеяие 20 мин раствор 3,75 мл (0,05 моль) сухого аллиламина и 7 мл (0,05 моль) сухого триэтиламина в 5 мл абсолютного эфира. Образуется есцветный осадок. Температура еакционной массы в течение 20-30 мин овышается до . При температура т -5 до в течение 15 мин добавяют раствор 2;б глл (0,05 моль) этиенимина и 7 мл (0,05 моль) сухого риэтиламина в 25 мл абсолютного фира. Реакционную массу перемешиают 2 ч при комнатной температуре. На следующий день хлоргидрат триэтиламина отфильтровывают, прог/ы вают абсолютным эфиром, эфир упаривают на роторном испарителе, остаток перегоняют в глубоком вакууме,. Т.кип. (в бане).д рт.ст, п 1,4780. Выход 6,5 г (74%), Кг на оксиде алюминия в ацетоне 0,51 в системе бензол-д;юксан (1:3) 0,59. Найдено,%: С 40,73; Н 7,17; Р 17,54. .,0. Вычислено,%: С 40,91; Н 7,39; Р ,17,61. В ИК-спектрах полоса валентных колебаний группы находится в области 1210 см и 1270 СИ СН2-группы - 1643 см , NH rpynпы - 3240 Пример 4. Получение этилен амидоалли л амида бутилфосёорной кислоты (Кох 05,02). Этиленамидоаллилагдад бутилФосфорной кислоты получают аналогично примеру 3 из 19,1 г (0,1 моль) ди- . хлорангидрида бутилфосфорной кислоты, 7,5 лш (0,1 гжэль) сухого аллилагжна, 5,2 мл (0,1 моль) сухого этиленимина и 28 мл (0,2 моль) сухого триэтилаьтана. Выход 17,5 г (80,5%), Т.кип. 90-100 С (в 6aHe)/lOt-tviM рт , ст . 1,4690, RjHa оксиде азшминия в ацетоне 0,67, в системе бензолдиоксан (1:3) 0,63, Найдено,%: С 49,65; Н 9,16; F 13,90. .,, Вычислено, %: С 49,54: Н 8,71; Р 14,22. В ИК-спектрах полоса валентных колебаний . группы находится в области 1211 см- и 1268 группы - в области 1642 см ,. NHгруппы - в области 3240 см , Описывае Ф1е соединения исследуют в качестве хемостерилизаторов на 5 биообъектах: виноградной пестрянке (Teresia ampeEophaga BayiLt) , яблонной плодожорке (Carpocapsa ротопеСЕа L,), непарном шелкопряде (Oscheria dispar L,),, мельничной огневке (Epestia kuhnie ЕЕа LebP..), зерновой 11ЮЛИ (Sitotroga ceraneEEa OpiC) . Для половой стерилизации этихбабочек испытывают препараты в концентрациях 0,5%, 1%, 2%, 3% методом контакта
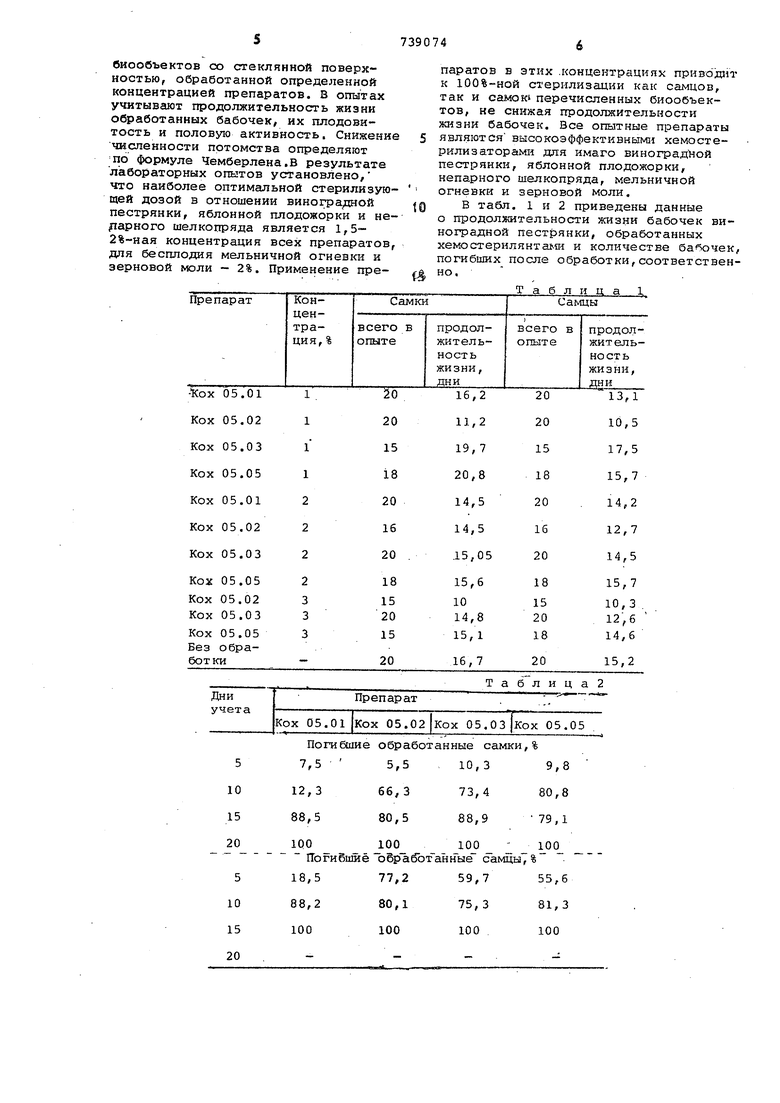
биообъектов со стеклянной поверхностью, обработанной определенной концентрацией препаратов. В опытах учитывают продолжительность жизни обработанных бабочек, их плодовитость и половую активность. Снижение численности потомства определяют по формуле Чемберлена.В результате лабораторных опытов установлено, что наиболее оптимальной стерилизующей дозой в отношении виноградной пестрянки, яблонной плодожорки и не lapHoro шелкопряда является 1,52%-ная концентрация всех препаратов, для бесплодия мельничной огневки и зерновой моли - 2%, Применение преПогибшие обработанные самки,%
18,5 77,2 59,7 55,6 88,2 80,1 75,3 81,3 100 100 100 100
паратов в этих .концентрациях приводит к 100%-ной стерилизации как самцов, так и самок перечисленных биообъектов, не снижая продолжительности жизни бабочек. Все опытные препараты являются высокоэффективными хемостерилизаторамн для имаго виноградной пестрянки, яблонной плодожорки, непарного шелкопряда, мельничной огневки и зерновой моли.
В табл. 1 и 2 приведены данные о продолжительности жизни бабочек виноградной пестрянки, обработанных хемостеридянтаьт и количестве бабочек, погибших после обработки,соответственно.
-Т а б л и U а I
Таблица2
В опытах по стерилизации виногадной пестрянки гибель самок и сгшов наблюдается при 3%-ной концентраии препаратов. Количество погибших Б исследованных вариантах достигает 17%. Продолжительность жизни обра(5отанных особей в большинстве случаев немного уменьшается (табл.1). Наименьшая продолжительность жизни обработанных самок (10 дней) отмечается при испытании 3%-ной концентрации Кох05.02. В других вариантах; обработанные бабочки живут 10-18,7 дня, в контроле - 16,7-15,2 дня. Обработанные самцы более чувствительны к испытываемым соединениям, чем самки, и живут в среднем на 1-4 дня меньше.
Из табл.2 следует, что наиболее значительная смертность самок отмечается в вариантах с препаратами .Кох 05.03 и Кох 135.05, когда в возрасте до 10 дней погибает 73,4- 80,8% самок в контроле. 100%-ная гибель самцов на 15-тый день отмечается во всех вариантах. 5 Разработан эффективный способ половой химической стерилизации, ОснованнЬй на 6-часовом контакте бабочек со стеклянной поверхностью, обработанной препаратами определен0 ной концентрации, при этом учитывается продолжительность жизни обработанных бабочек, их плодовитость и половая активность.
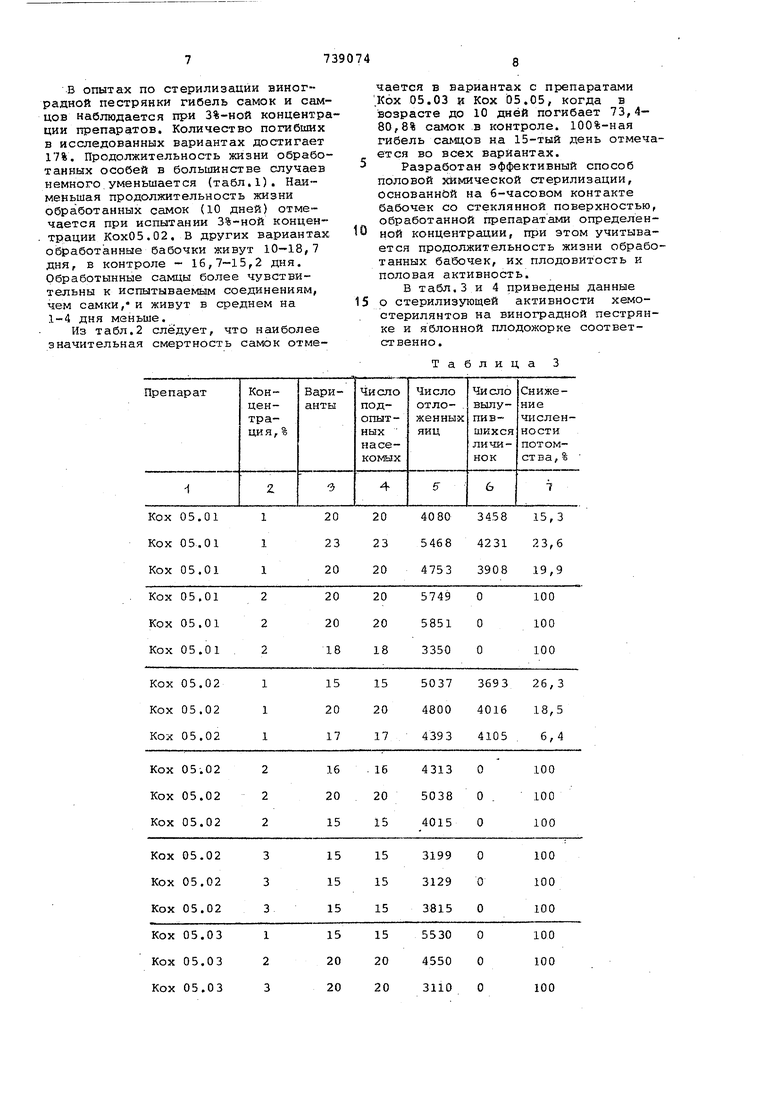
В табл.3 и 4 приведены данные
5 о стерилизующей активности хемостерилянтов на виноградной пестрянке и яблонной плодожорке соответственно.
Т а
лица
Продолжение табл. 3
Таблица
Первичная оценка препаратов ох 15.01, 05.02, 05.03 и 05.05 для терилизации виноградной пестрянки оказывает, что оптимальной стерилизующей дозой является 1,5-2% (табл.-З). Эти концентрации вызывают 100%-ную стерилизацию бабочек. Во всех вариантах обработанные бабочки ткладывают яйца, но зигота не развивается.
Повышение коицентрации от 2 до 3% казывает существенное влияние на снижение количества откладываемых яиц и на продолжительность бабочек, несмотря на то, что во всез вариантах получено полное беспло,цие бабочек.
При спаривании нормальных самок с обработанными 3%-ными препаратамй самцами не кахсдая самка откладывает яйца, однако этого не наблюдается при спаривании самок с самцами, стерилизованными препаратaJ«J l,5-2%i ной концентрации.
При испытании 0,5-1%-ной концентрации Кох 05.01 получен низкий эффект стерилизации бабочек.
Изучена также конкурентная способность стерилизованных самцов виноградной пестрянки в соотношениях полов 1:1:1, 5:1:5, 8:1:10, 10:1:10, 15:1:15, 20:1:20. Самки сохраняют свою конкурентоспособность и нормаль ное поведение, В этой серии опытов гусеницы не отраждались при соотношении. 20:1:20 .
На основании полученных данных можно заключить, что наиболее оптимальной стерилизующей дозой в отношении виноградной пестрянки является 1,5-2%-ная концентрация
всех опытных препаратов Кох 05,01, 05.02, 05,03, 05.05.
В этих концентрациях используе ле препараты стерилизуют как самцов, так и самок, не снижая значительно продолжительности жизни бабочек. Для стерилизации имагинальной стадии яблонной плодожорки контактны способом испытаны Кох 05.01 и Кох 05.02. Первое соединение растворяют в этиловом спирте. Бабочки обрабатывают 4 часовой экспозицией.
Анализ данных табл, 4 показывает, что 3%-ные Кох 05.01 и 05.02 при длительном контакте вызывают 50-100%yso гибель насекомых. У вызкивших бабочек значительно уменьшается жизнеспособность и половая активность. Оптимальной концентрацией для стерилизации бабочек аблонной плодожорки является 2%-ный Кох О5,.01 и 05.02. Снижение численности потомства после 4-х часового контакта достигает 100% у бабочек обоих полов. При этом половая активность и жизнеспособность стерилизованных особей не снижается. Анализ яйцевых трубок показывает, что после контакта со стерилянтом процесс формирования ооцитов прекращается и незрелые ооциты рассасываются.
Во всех вариантах с 1%-ными препаратами получена неполная стерилизация бабочек.
С целью определения конкурентоспособности стерилизованных самцов с нормальными в опытах стерильные и фертильные самцы и девственные самки подобраны в соотношениях I:ls5, 5:1:6 8:1:10, 10:1:8; 10:1:10; 20:1:10. Результаты эксперимента приведены в табл.5.
Таблица 5
В опытах нормальным бабочкам предоставлена возможность выбора между нормальными и стерилизованными самками. Они оплодотворяют последних почти в одинаковой степени, несколь-ко предпочитая нормальных . Стерилизованные самцы одинаково спариваются .с но мальными и стерилизованными самками. Таким образом, Кох 05.01 и Кох 05.02 в 2%-ной концентрации при контактном способе применения лишь незначительно снижает половую активность самцов и половую привлекаемость самок.
Конкуренция стерилизованных самцов с нормальными выявляется в активности поиска самок, способности к
Продолжение табл. 5
копуляции, а также способности спер2/% Nffii стерилизованных самцов участвовать в оплодотворении ооцитов наравне со спермой нормальных.
Таким образом высокий эффект стерилизации достигается при соотношении 15:1; 20:1 (эмбрион не разви- 25 вается в 73-91,7% случаев.Спаривание в опыте и в контроле незначительно отличается (в опыте 1-1,25, в контроле - 1,45).
Таким образом, конкурентная спо30 собиость стерилизованных самцов значительно не уменьшается.
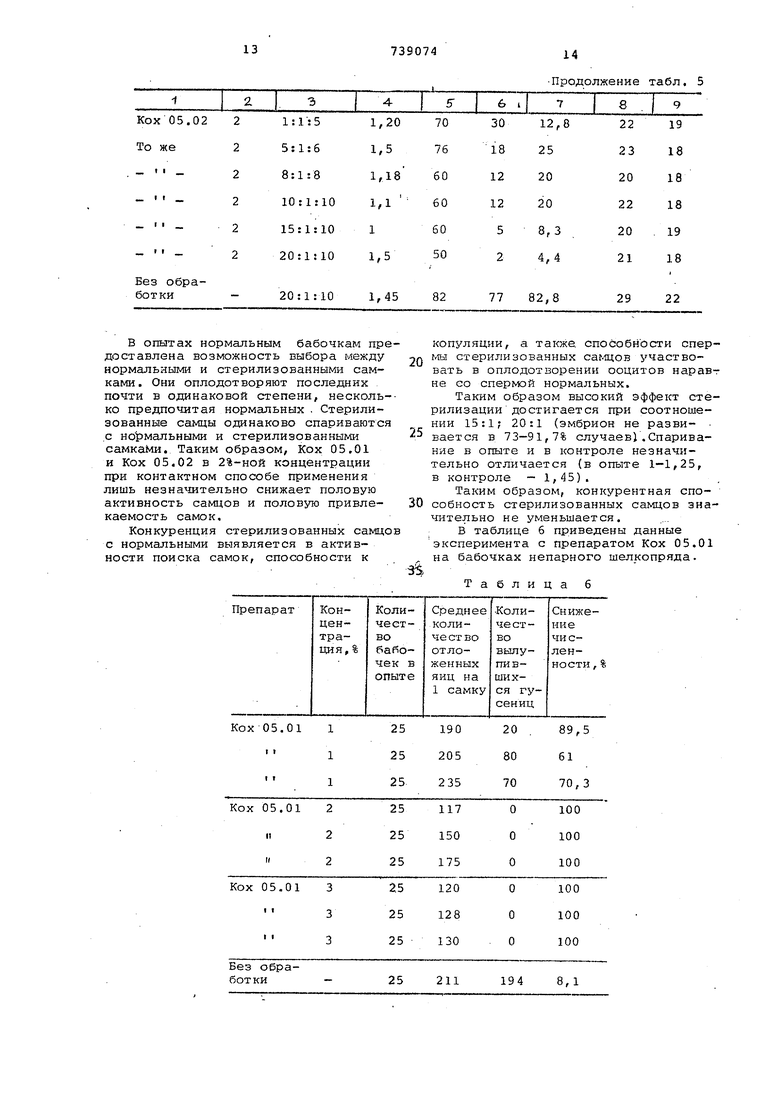
В таблице б приведены данные эксперимента с препаратом Кох 05.01 на бабочках непарного шелкопряда.
3i
Таблица 6
Как видно из табл. б, Кох 05.01, 2 3%-ой концентрации вызывает полную неплодовитость непарного шелкопряда. Во всех вариантах обработанные бабочки откладывают яйца, но зигота не развивается. Анализ яйцевых трубок показывает, что после контакта со стерилянтом (6 ч) процесс формирования ооцитов приостанавливается и незрелые ооциты рассасываются. Продолжительность жизни обработанных бабочек составляет 8-16 дней, что оказывается немного мэньше продолжительности жизни контрольных особей. Во всех варианта количество оплодотворенных самок ниже, чем в контроле. Особенно значительное снижение количества cnsi рившихся самок отмечается в том случае, если оба пола стерилизованы 2%-ным Кох 05 „01.
Аналогичные результаты полу;1ены при стерилизации мельничной огневки и зерновой моли.
Таким образом, наиболее оптимальной стерилизующей дозой для яблонно плодожорки и непарного шелкопряда является 1,5-2%-ная концентрация всех препаратов, мельничной огневки и зерновой моли - 2%. Препараты так концентрации стерилизуют как самцов так и самок исследованных биообъектов, не снижая продолжительности жизни бабочек.
Предложенные препараты являются высо коэ ффекти вными хемостерилянт ами для имаго виноградной пестрянки, яблонной плодожорки, непарного шелкопряда, мельничной огневки и зерновой моли.
Формула изобретения
Производные аллиламидов кислот фосфора общей
9
R
„ Р-мнение и-СИ 2.
где R
- метокси-, бутокоигруппа, гексил или гептил;
R
- гексил, аллиламино- или
этиленаминогруппа,
обладающие хемостерилизующей активностью.
Источники информации, принятые во внимание при экспертизе
с вpeдны vtи насекомыми. М., Колос, 1971.
с. 192-199.
Авторы
Даты
1980-06-05—Публикация
1978-01-23—Подача