Изобретение касается 3-(1,2-бензилоксазол-3-ил)-4-пиридаминов общей формулы I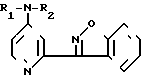 где R1 - водород или низший алкил; R2 - водород или низший алкил, обладающих анальгетической, антихолинэстеразной и дерматологической активностью.
где R1 - водород или низший алкил; R2 - водород или низший алкил, обладающих анальгетической, антихолинэстеразной и дерматологической активностью.
Соединения этого изобретения полезны в качестве анальгетиков для облегчения различных дисфункций памяти, характеризующихся снижением холинрегической функции, в качестве диагностических генов-усилителей в лечении старческого слабоумия, такого как болезнь Альцгеймера, и в качестве локальных противовоспалительных агентов для лечения различных дерматозов, включая, например, экзогенные дерматиты (например, солнечную эритему, фотоаллергический дерматит, крапивницу, контактный дерматит, аллергический дерматит), эндогенные дерматиты (например, атонический дерматит, себорейный дерматит, склеивающий дерматит), дерматиты неизвестной этиологии (например, распространенный шелушащийся дерматит), заболевания кожи с воспалительным компонентом (например, псориаз).
В описании и приложенной формуле изобретения данные химические формулы и названия обозначают все стерео-, оптические и геометрические изомеры и рацемические смеси, где такие изомеры и смеси существуют.
Если по другому не обозначено или не указано, применяют следующие определения в описании и приложенной формуле изобретения.
Термин "низший алкил" относится к линейному или разветвленному углеводороду с 1-6 углеродными атомами, не содержащему ненасыщенности, например, метил, этил, пропил, изопропил, 2-бутил, неопентил, н-гексил и т. д.
Соединения настоящего изобретения получают следующим образом. Заместители R1 и R2 являются такими, как определено выше. Оксид формулы II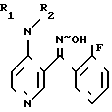 циклизуют в присутствии основания, получая соединение формулы I. Эта реакция обычно происходит в присутствии сильного основания, такого, как гидроокись натрия, гидроокись калия, трет-бутилат калия и др. , в низшем спирте в качестве растворителя, таком, как метанол, этанол и др. , при температуре приблизительно от 0 до 100оС (или при нагревании с обратным холодильником) в течение 1-24 ч.
циклизуют в присутствии основания, получая соединение формулы I. Эта реакция обычно происходит в присутствии сильного основания, такого, как гидроокись натрия, гидроокись калия, трет-бутилат калия и др. , в низшем спирте в качестве растворителя, таком, как метанол, этанол и др. , при температуре приблизительно от 0 до 100оС (или при нагревании с обратным холодильником) в течение 1-24 ч.
Соединение II получают по реакции соединения формулы III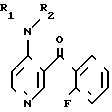 c хлоргидратом гидроксиламина в подходящем растворителе, таком, как пиридин или этанол, в присутствии подходящего основания, такого, как ацетат натрия, при 25оС с обратным холодильником.
c хлоргидратом гидроксиламина в подходящем растворителе, таком, как пиридин или этанол, в присутствии подходящего основания, такого, как ацетат натрия, при 25оС с обратным холодильником.
Соединение формулы III получают из соединения формулы IV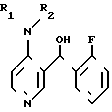 путем окисления бихроматом пиридина или другим подходящим агентом в подходящем растворителе, таком, как диметилформамид.
путем окисления бихроматом пиридина или другим подходящим агентом в подходящем растворителе, таком, как диметилформамид.
Соединение IV можно получить следующим образом: 2,2-диметил-N-(4-пиридинил)-пропанамиду формулы дают прореагировать с н-бутиллитием и полученному дианиону дают прореагировать с орто-фторбензальдегидом формулы
дают прореагировать с н-бутиллитием и полученному дианиону дают прореагировать с орто-фторбензальдегидом формулы 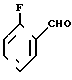 получая соединение IV. Обычно первую реакцию проводят в подходящем растворителе, таком, как тетрагидрофуран, при температуре около - 78-25оС. Вторую фракцию также проводят в подходящем растворителе, таком, как тетрагидрофуран.
получая соединение IV. Обычно первую реакцию проводят в подходящем растворителе, таком, как тетрагидрофуран, при температуре около - 78-25оС. Вторую фракцию также проводят в подходящем растворителе, таком, как тетрагидрофуран.
Соединения настоящего изобретения полезны в качестве анальгетиков. Это применение показано при испытании на мышах с судорогами от фенил-пара-хинона, стандартных испытаниях для анальгетиков Рroc. Soc. Exptl. Biol. Med. 95, 729 (1957). Обезболивающее действие соединений изобретения выраженное в % ингибирования судорог, приведено в табл. 1.
Облегчения боли достигают, когда вводят соединения изобретения животному, подвергаемому испытанию, орально, парентерально или внутривенно в эффективной дозе от 0,1 до 25 мг/кг веса тела в день, в частности, эффективным количеством является приблизительно 5 мг/кг веса тела в день. Понятно, что для любого отдельного субъекта необходимо подобрать схему приема лекарства в соответствии с индивидуальной потребностью и профессиональным заключением типа, назначающего или наблюдающего за приемом вышеупомянутого соединения. Необходимо также понимать, что приведенная здесь далее дозировка только иллюстративна и не обеспечивает область применения изобретения.
Соединения настоящего изобретения можно также использовать для лечения различных дисфункций памяти, характеризующихся снижением различных дисфункций памяти, характеризующихся снижением холиэргической функции, такие, как болезнь Альцгеймера. Это применение продемонстрировано в испытаниях по избеганию темноты.
Испытание по избеганию темноты.
В этом испытании мышей проверяют на их способность помнить неприятный раздражитель в течение 24 ч. Мышь помещают в камеру, которая имеет темный отсек; яркий свет от лампы накаливания загоняет мышь в темный отсек, где на нее воздействуют электрическим током через металлические пластины на полу. Животное вынимают из тестового прибора и проверяют снова через 24 ч на способность помнить электрошок.
Если животному перед первым помещением в тестовую камеру ввести скополамин, антихолэнергическое средство, известное, как ослабляющее память, то животное возвращается в темный отсек вскоре после помещения в тестовую камеру через 24 ч. Действие скополамина блокируют тестовым активным соединением, в результате чего увеличивается интервал перед возвращением животного в темный отсек.
Результаты исследования активного соединения выражают в процентах от группы животных, у которых блокировано действие скополамина, что показывает увеличение интервала между помещением животного в тестовую камеру и его возвращением в темный отсек.
Результаты по некоторым тестовым соединениям этого изобретения и веществу сравнения представлены в табл. 2.
Соединения этого изобретения также полезны в качестве локальных противовоспалительных агентов для лечения различных дерматозов, как упомянуто раньше. Дерматологическую активность соединений этого изобретения определяли со ссылкой на следующие методы.
Дерматологические тестовые методы.
Отек уха, вызванный ТРА (ТРАЕЕ). Цель этого исследования определить способность соединения, нанесенного локально, предупреждать отек уха, вызванный местным применением ТРА (форбол-12-миристатацетат). Самки Швейцарских Webster мышей получают локально ТРА (10 μг/ухо) на правое ухо и наполнитель на левое ухо. Тестовое соединение (10 μг/ухо) наносят на оба уха. Через 5 ч животных умерщвляют и с каждого уха берут пробу (4 мм). Определяют разницу веса проб с правого и левого уха для каждого животного, чтобы оценить активность (Стандарт: гидрокортизон ЭД50 = 47 μг/ухо). Смотри Joung J. M. et al. J. Invest Dermatol. , 80 (1983), с. 48-52.
Дерматологическая активность для соединения настоящего изобретения представлена в табл. 3.
Эффективные количества соединений настоящего изобретения можно вводить субъекту различными методами, например, орально в капсулах или таблетках, парентерально в виде стерильных растворов или суспензий и в некоторых случаях внутривенно в виде стерильных растворов. Соединения настоящего изобретения, эффективные сами по себе, можно приписывать и принимать в виде их фармацевтически пригодных солей присоединения для стабильности, удобства кристаллизации, повышения растворимости и прочее.
Предпочтительные фармацевтически пригодные соли присоединения включают соли неорганических кислот, таких, как соляная, бромистоводородная, серная, азотная, фосфорная и хлорная кислоты; также и органических кислот, таких, как винная, лимонная, уксусная, янтарная, малеиновая, фумаровая и щавелевая кислоты.
Активные соединения этого изобретения можно принимать орально, например, с инертным разбавителем или годным в пищу носителем. Их можно включать в желатиновые капсулы или прессовать в таблетки. Для орального фармацевтического применения соединения можно объединять с наполнителем и использовать в виде таблеток, лепешек, капсул, эликсиров, суспензий, сиропов, облаток, жевательных резинок и тому подобного. Препараты должны содержать по крайней мере 0,5% активного вещества, но количество можно варьировать в зависимости от конкретной формы, удобным может быть содержание от 4% до приблизительно 75% по массе. Количество соединения такой композиции таково, что получают удобную дозу. Предпочтительные композиции и препараты в соответствии с настоящим изобретением готовят таким образом, что доза для орального приема содержит от 1,0 до 300 мг активного соединения.
Таблетки, пилюли, капсулы, облатки и подобное могут содержать следующие ингредиенты: связующее вещество, такое, как микрокристаллическая целлюлоза, трагакант или желатин; наполнитель, такой, как крахмал или лактоза; дезинтегратор, такой, как альгиновая кислота, PrimogelTM, зернистый крахмал и тому подобное, смазочный материал, такой, как стеарат магния или Sterotex , агент для скольжения, такой, как коллоидная двуокись кремния, подслащающий агент, такой, как сахароза или сахарин или агент для вкуса и запаха, такой, как мята, метилсалицилат, или можно добавить апельсиновую отдушку. Когда дозированная единица является капсулой, она может содержать вдобавок к материалам, упомянутым выше, жидкий носитель, такой, как жирное масло. Другая дозированная единица может содержать другие различные материалы, которые модифицируют физическую форму дозированной единицы, например, покрытия. Таким образом, таблетки или пилюли могут быть покрыты сахаром, шеллаком или другими энтеросолюбильными оболочками. Сиропы могут содержать в добавок к активному компоненту сахарозу в качестве подслащивающего агента и определенные консерванты, красители, краски и корригенты. Материалы, используемые в приготовлениях этих различных композиций, должны быть фармацевтически чистыми и нетоксичными в используемых количествах.
, агент для скольжения, такой, как коллоидная двуокись кремния, подслащающий агент, такой, как сахароза или сахарин или агент для вкуса и запаха, такой, как мята, метилсалицилат, или можно добавить апельсиновую отдушку. Когда дозированная единица является капсулой, она может содержать вдобавок к материалам, упомянутым выше, жидкий носитель, такой, как жирное масло. Другая дозированная единица может содержать другие различные материалы, которые модифицируют физическую форму дозированной единицы, например, покрытия. Таким образом, таблетки или пилюли могут быть покрыты сахаром, шеллаком или другими энтеросолюбильными оболочками. Сиропы могут содержать в добавок к активному компоненту сахарозу в качестве подслащивающего агента и определенные консерванты, красители, краски и корригенты. Материалы, используемые в приготовлениях этих различных композиций, должны быть фармацевтически чистыми и нетоксичными в используемых количествах.
Для парентерального терапевтического приема активные соединения изобретения можно включать в растворы и суспензии. Такие препараты должны содержать по крайней мере 0,1% указанного соединения, но его количество можно варьировать от 0,5 до приблизительно 30% по массе. Количество активного соединения в таких композициях таково, что получают подходящую дозу. Предпочтительные композиции и препараты в соответствии с настоящим изобретением получают таким образом, что дозированная единица для парентерального приема содержит от 0,5 до 100 мг активного вещества.
Растворы или суспензии могут также содержать следующие компоненты: стерильный разбавитель, такой, как вода для инъекции, физиологический раствор, определенные масла, полиэтиленгликоль, глицерин, пропиленгликоль или другие синтетические растворители, антибактериальные агенты, такие, как бензиловый спирт или метилпарааминобензойная кислота, антиоксидаты, такие, как аскорбиновая кислота или бисульфит натрия, вещества, вызывающие образование хелатных соединений, такие, как этилендиаминтетрауксусная кислота, буферы, такие, как ацетаты, цитраты или фосфаты, и агенты для регулирования тонуса, такие, как хлорид натрия или декстроза. Препарат для парентерального приема можно помещать в ампулы, наполнять им имеющиеся шприцы или пузырьки из стекла или пластика на много доз. Примерами соединений этого изобретения являются: N-[3-(1,2-бензизоксазол-3-ил)-4-пиридинил] -N-метил-2,2-диметилпропанамид; 3-(1,2-бензизоксазол-3-ил)-N-фенилметил-4-пиридинамин; 3-(5-нитро-1,2-бензизоксазол-3-ил)-4-пиридинамин; 3-(5-амино-1,2-бензизоксазол-3-ил)-4-пиридинамин и 3-(6-фтор-1,2-бензизоксазол-3-ил)-4-пиридинамин. Были проведены испытания на токсичность для каждого соединения примера.
При этом была определена точная летальная доза (АLD50), равная более чем 80 мг/кг i. p.
Это означает, что в контрольной группе из четырех животных доза больше чем 80 мг/кг i. p. не являлась летальной по крайней мере для двух из четырех животных.
П р и м е р. 1. α-(3-Фторфенил)-4-аминопиридин-3-метанолгидрохлорид.
Раствор α-[4-(2,2-диметилпропионамидо)-3-пиридинил] -α-(2-фторфенил-1)-мета- нола (18 г) в 200 мл метанола и 20 мл 10% -ного водного раствора гидроокиси натрия перемешивают при 75-80оС в течение 2 ч, затем охлаждают, испаряют смешивают с водой и экстрагируют смесью этилацетат-эфир. Органический экстракт промывают водой и насыщают хлоридом натрия, затем сушат (безводным MgSO4), фильтруют и испаряют, получая 13 г масла. Его чистят хроматографией с мгновенным испарением (двуокись кремния, 20% метанол в дихлорметане) с выходом 11,5 г продукта в виде твердого вещества с температурой плавления 60-65оС. 3 г переводят в соль соляной кислоты в смеси метанол-эфир с выходом 2,8 г твердого вещества с температурой плавления 210-213оС. Его перекристаллизовывают из метилового эфира с выходом 2,2 г α-(2-фторфенил-4-аминопиридин-3-метанолгидрохлорида, т. пл. 215-216оС.
Элементный анализ.
Вычислено C12H12ClFN2O, % : 56,59 С; 4,75 Н; 11,00 N
Найдено, % : С 56,60; Н 4,75; N 10,94 N.
II. (4-Амино-3-пиридинил)-(2-фторфенил)-метаноксим. Раствор (4-амино-3-пиридинил)-(2-фторфенил)-метанола (19 г) и гидроксиламингидрохлорида (31 г) в 125 мл пиридина перемешивают при нагревании с обратным холодильником в течение 2 ч, затем охлаждают и испаряют. Остаток перемешивают с водой, подщелачивают бикарбонатом натрия и экстрагируют смесью этилацетат-эфир. Органический экстракт промывают водой и насыщают хлоридом натрия, сушат (безводным MgSO4), фильтруют и испаряют, получая 25 г масла. Это масло элюируют 10% -ным метанолом в дихлорметане на двуокиси кремния методом хроматографии с мгновенным испарением с выходом 14,6 г твердого вещества, т. пл. 170-180оС. 3 г перекристаллизовывают из ацетонитрила с выходом 1,7 г (4-амино-3-пиридинил)-(2-фторфенил)-метаноксима в виде твердого вещества с т. пл. 212-214оС.
Элементный анализ.
Вычислено C12H10FN3O, % : 62,33 C; 4,36 H; 18,18 N.
Найдено, % : 62,11 C; 4,41 H; 17,99 N.
III. N-[3-(1,2-Бензизоксазол-3-ил)-4-пиридинил] -2,2-диметилпропанамид. Раствор [4-(2,2-диметилпропионамидо)-3-пириди- нил] -2-фторфенилметаноксима (2,3 г) в 20 мл метанола и 2 мл 10% -ного водного раствора гидроокиси натрия перемешивают при нагревании с обратным холодильником в течение 2 ч, затем охлаждают, перемешивают с водой и экстрагируют дихлорметаном. Высушенный безводным сульфатом магния органический слой фильтруют и испаряют, получая 2,4 г твердого вещества. Его соединяют с 1,5 г продукта, полученного из предыдущей фракции, и элюируют на двуокиси кремния 5% -ным этилацетатом в дихлорметане (ДХМ) методом колоночной хроматографии с мгновенным испарением, получая 2,5 г твердого вещества, т. пл. 133-134оС. Твердое вещество перекристаллизовывают из метанола с выходом 2,3 г N-[3-(1,2-бензилоксазол-3-ил)-4-пиридинил] -2,2-диметилпропанамида, т. пл. 137-138оС.
Элементный анализ.
Вычислено С17Н17N3O2, % : 69,13 C; 5,80 H; 14,23 N.
Найдено, % : 69,11 C; 5,82 H; 14,19 N.
П р и м е р 2. 3-(1,2-Бензизоксазол-3-ил)-4-пиридинамин-малеат.
Раствор [4-(2,2-диметилпропионамидо)-3-пиридинил] -2-фторфенил-метаноксима (5,2 г) в 60 мл метанола и 10 мл 10% -ного водного раствора гидроокиси натрия перемешивают при нагревании с обратным холодильником в течение 4 ч затем охлаждают, смешивают с водой и экстрагируют ДМХ. Высушенный безводным сульфатом магния органический слой фильтруют и испаряют, получая 3,7 г масла. Это масло элюируют на двуокиси кремния 20% -ным этилацетатом в ДХМ, потом этилацетатом методом колоночной хроматографии с мгновенным испарением с выходом 2,2 г продукта в виде твердого вещества, т. пл. 146-148оС. Этот твердый продукт переводят в соль малеиновой кислоты в метаноле, затем перекристаллизовывают из метанола с выходом 3,3 г 3-(1,2-бензизоксазол-3-ил)-4-пиридинаминмалеата, плавится с разложением при 188-190оС.
Элементный анализ.
Вычислено С16Н13N3O5, % : 58,71 C; 4,00 H 12,84 N
Найдено, % : 58,66 C 3,99 H 12,84 N.


Использование: в медицине в качестве веществ, проявляющих анальгетическую антихолинэстеразную и дерматологическую активность. Сущность изобретения: продукт 3-(1,2-бензизоксазол-3-ил)-4-пиридамины формулы I, где R1 и R2 - водород или низший алкил. Соединения формулы 1 получают циклизацией соответствующим образом замещенного о-галогенфенилметаноксима в присутствии основания в среде низшего спирта. 3 табл. Ф-ла 1 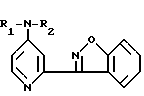
3-(1,2-Бензизоксазол-3-ил)-4-пиридамины общей формулы
1
где R1 - водород или низший алкил;
R2 - водород или низший алкил, проявляющие анальгетическую, антихолинэстеразную и дерматологическую активность.
Авторы
Даты
1994-05-15—Публикация
1991-08-12—Подача